1.9 一般的名称に係る文書 1.9 一般的名称に係る文書 国際一般名 (INN) thrombomodulin alfa(r-inn List54, WHO Drug Information, Vol.19, No.3, 2005) 一般的名称 (JAN) 一般的名称 (J
|
|
|
- ありおき さだい
- 5 years ago
- Views:
Transcription
1 リコモジュリン点滴静注用 トロンボモデュリンアルファ ( 遺伝子組換え ) 第 1 部 1.9 一般的名称に係る文書
2 1.9 一般的名称に係る文書 1.9 一般的名称に係る文書 国際一般名 (INN) thrombomodulin alfa(r-inn List54, WHO Drug Information, Vol.19, No.3, 2005) 一般的名称 (JAN) 一般的名称 (JAN) は 平成 17 年 11 月 11 日に INN 収載品目として医薬品一般的名称の届出を行い 平成年月日の医薬品名称専門協議で確認され 平成 18 年 4 月 5 日薬食審査発第 号において 以下のように通知された 日本名 : トロンボモデュリンアルファ ( 遺伝子組換え ) 英名 :Thrombomodulin Alfa(Genetical Recombination) 1.9-1
3 リコモジュリン点滴静注用 トロンボモデュリンアルファ ( 遺伝子組換え ) 第 1 部 1.10 毒薬 劇薬等の指定審査資料のまとめ
4 1.10 毒薬 劇薬等の指定審査資料のまとめ 化学名 別名 構造式効能 効果用法 用量 劇薬等の指定市販名及び有効成分 分量 毒性 毒薬 劇薬等の指定審査資料のまとめ ヒトトロンボモデュリンの 番目のアミノ酸残基をコードする cdna の発現により チャイニーズハムスター卵巣細胞で産生される 498 個のアミノ酸残基 (C 2230 H 3357 N 633 O 718 S 50 ; 分子量 : 52,124.58) からなる糖タンパク質 ( 分子量 : 約 64,000) アミノ酸配列は別紙のとおり汎発性血管内血液凝固症 (DIC) 通常 成人には トロンボモデュリンアルファとして 1 日 1 回 380U/kg を約 30 分かけて点滴静注する なお 症状に応じ適宜減量する 原体 : トロンボモデュリンアルファ ( 遺伝子組換え ) 製剤 : リコモジュリン点滴静注用 12800(1 バイアル中トロンボモデュリンアルファ ( 遺伝子組換え ) として 12,800U 含有 ) 単回投与毒性動物種投与経路概略致死量ラット静脈内 1,200,000 U/kg/ 日 (180 mg/kg/ 日 ) サル静脈内 1,200,000 U/kg/ 日以上 (180 mg/kg/ 日以上 ) 反復投与毒性動物種投与期間投与経路投与量無毒性量主な所見 U/kg/ 日 (mg/kg/ 日 ) ラット 1 ヶ月間 静脈内 13,000 38, ,000 (2 6 18) サル 2 週間 静脈内 380 1,300 3,800 ( ) サル 1 ヶ月間 静脈内 1,300 3,800 13,000 38,000 ( ) サル 6 ヵ月間 静脈内 1,300 3,800 13,000 ( ) 38,000 (6) 3,800 (0.6) 1,300 (0.2) 1,300 (0.2) 腎臓被膜下 胸腺あるいは卵巣に出血 皮膚の蒼白 自発運動の低下 及び体重減少 貧血 毒性変化はみられなかった 3,800 U/kg から投与部位の紫斑又は腫脹 及び口腔粘膜の蒼白 3,800 U/kg から貧血 3,800 U/kg から投与部位の皮下組織に出血 13,000 U/kg から全身の皮膚及び皮下組織に出血 13,000 U/kg で膀胱の出血 38,000 U/kg で精巣の出血 13,000 U/kg から出血による死亡あるいは切迫屠殺例 13,000 U/kg から口腔粘膜の蒼白 自発運動減少 摂餌量減少 及び体重減少 3,800 U/kg から貧血 3,800 U/kg から採血部位周囲の大腿部出血 卵巣出血 本薬に対する抗体価は 13,000 U/kg の雄 1 例で顕著に上昇したほか 1,300 及び3,800 U/kgでも軽度に上昇する例が散見された
5 1.10 毒薬 劇薬等の指定審査資料のまとめ 副作用 * 副作用 臨床検査異常発現率 36/279=12.9% 副作用 臨床検査異常 * の種類 例数 血清 AST (GOT) 上昇 10 血清 ALT (GPT) 上昇 8 カテーテル留置部位出血 7 尿沈渣赤血球 5 口内出血 4 紫斑 ( 病 ) 4 アルカリフォスファターゼ上昇 4 尿潜血陽性 4 血尿 3 蛋白尿 3 等 *: 本剤との関連性が否定できないもの 会社 原体 : 製造 株式会社富士薬品 製剤 : 製造
6 1.10 毒薬 劇薬等の指定審査資料のまとめ 別紙 Ala-Pro-Ala-Glu-Pro-Gln-Pro-Gly-Gly-Ser-Gln-Cys-Val-Glu-His-Asp-Cys-Phe-Ala-Leu- 20 * Tyr-Pro-Gly-Pro-Ala-Thr-Phe-Leu-Asn-Ala-Ser-Gln-Ile-Cys-Asp-Gly-Leu-Arg-Gly-His- 40 Leu-Met-Thr-Val-Arg-Ser-Ser-Val-Ala-Ala-Asp-Val-Ile-Ser-Leu-Leu-Leu-Asn-Gly-Asp- 60 Gly-Gly-Val-Gly-Arg-Arg-Arg-Leu-Trp-Ile-Gly-Leu-Gln-Leu-Pro-Pro-Gly-Cys-Gly-Asp- 80 * * Pro-Lys-Arg-Leu-Gly-Pro-Leu-Arg-Gly-Phe-Gln-Trp-Val-Thr-Gly-Asp-Asn-Asn-Thr-Ser-100 Tyr-Ser-Arg-Trp-Ala-Arg-Leu-Asp-Leu-Asn-Gly-Ala-Pro-Leu-Cys-Gly-Pro-Leu-Cys-Val- 120 Ala-Val-Ser-Ala-Ala-Glu-Ala-Thr-Val-Pro-Ser-Glu-Pro-Ile-Trp-Glu-Glu-Gln-Gln-Cys- 140 Glu-Val-Lys-Ala-Asp-Gly-Phe-Leu-Cys-Glu-Phe-His-Phe-Pro-Ala-Thr-Cys-Arg-Pro-Leu- 160 Ala-Val-Glu-Pro-Gly-Ala-Ala-Ala-Ala-Ala-Val-Ser-Ile-Thr-Tyr-Gly-Thr-Pro-Phe-Ala- 180 Ala-Arg-Gly-Ala-Asp-Phe-Gln-Ala-Leu-Pro-Val-Gly-Ser-Ser-Ala-Ala-Val-Ala-Pro-Leu- 200 Gly-Leu-Gln-Leu-Met-Cys-Thr-Ala-Pro-Pro-Gly-Ala-Val-Gln-Gly-His-Trp-Ala-Arg-Glu- 220 Ala-Pro-Gly-Ala-Trp-Asp-Cys-Ser-Val-Glu-Asn-Gly-Gly-Cys-Glu-His-Ala-Cys-Asn-Ala- 240 Ile-Pro-Gly-Ala-Pro-Arg-Cys-Gln-Cys-Pro-Ala-Gly-Ala-Ala-Leu-Gln-Ala-Asp-Gly-Arg- 260 Ser-Cys-Thr-Ala-Ser-Ala-Thr-Gln-Ser-Cys-Asn-Asp-Leu-Cys-Glu-His-Phe-Cys-Val-Pro- 280 * Asn-Pro-Asp-Gln-Pro-Gly-Ser-Tyr-Ser-Cys-Met-Cys-Glu-Thr-Gly-Tyr-Arg-Leu-Ala-Ala- 300 Asp-Gln-His-Arg-Cys-Glu-Asp-Val-Asp-Asp-Cys-Ile-Leu-Glu-Pro-Ser-Pro-Cys-Pro-Gln Arg-Cys-Val-Asn-Thr-Gln-Gly-Gly-Phe-Glu-Cys-His-Cys-Tyr-Pro-Asn-Tyr-Asp-Leu-Val- 340 Asp-Gly-Glu-Cys-Val-Glu-Pro-Val-Asp-Pro-Cys-Phe-Arg-Ala-Asn-Cys-Glu-Tyr-Gln-Cys- 360 * Gln-Pro-Leu-Asn-Gln-Thr-Ser-Tyr-Leu-Cys-Val-Cys-Ala-Glu-Gly-Phe-Ala-Pro-Ile-Pro- 380 * His-Glu-Pro-His-Arg-Cys-Gln-Met-Phe-Cys-Asn-Gln-Thr-Ala-Cys-Pro-Ala-Asp-Cys-Asp- 400 Pro-Asn-Thr-Gln-Ala-Ser-Cys-Glu-Cys-Pro-Glu-Gly-Tyr-Ile-Leu-Asp-Asp-Gly-Phe-Ile- 420 Cys-Thr-Asp-Ile-Asp-Glu-Cys-Glu-Asn-Gly-Gly-Phe-Cys-Ser-Gly-Val-Cys-His-Asn-Leu- 440 Pro-Gly-Thr-Phe-Glu-Cys-Ile-Cys-Gly-Pro-Asp-Ser-Ala-Leu-Val-Arg-His-Ile-Gly-Thr- 460 * * Asp-Cys-Asp-Ser-Gly-Lys-Val-Asp-Gly-Gly-Asp-Ser-Gly-Ser-Gly-Glu-Pro-Pro-Pro-Ser- 480 * * * * Pro-Thr-Pro-Gly-Ser-Thr-Leu-Thr-Pro-Pro-Ala-Val-Gly-Leu-Val-His-Ser-Gly 498 図トロンボモデュリンアルファの全アミノ酸配列
7 リコモジュリン点滴静注用 トロンボモデュリンアルファ ( 遺伝子組換え ) 第 1 部 1.12 添付資料一覧
8 第 3 部品質に関する文書 3.2 データ又は報告書 3.2.S 原薬 3.2.S.1 一般情報 3.2.S.1 一般情報 S.2 製造 3.2.S.2.1 製造業者 S.2.2 製造方法及びプロセス コントロール S.2.3 原材料の管理 S.2.4 重要工程及び重要中間体の管理 S.2.5 プロセス バリデーション / プロセス評価 3.2.S.2.6 製造工程の開発の経緯 3.2.S.3 特性 3.2.S.3.1 構造その他の特性の解明 3.2.S.3.2 不純物 S.4 原薬の管理 3.2.S.4.1 規格及び試験方法 S.4.2 試験方法 ( 分析方法 ) S.4.3 試験方法 ( 分析方法 ) のバリデーション 3.2.S.4.4 ロット分析 3.2.S.4.5 規格及び試験方法の妥当性 S.5 標準品又は標準物質 3.2.S.5 標準品又は標準物質 S.6 容器及び施栓系 3.2.S.6 容器及び施栓系 S.7 安定性 3.2.S.7.1 安定性のまとめ及び結論 S.7.2 承認後の安定性試験計画の作成及び実施 S.7.3 安定性データ 20 / ~ 継続中 3.2.P 製剤 3.2.P.1 製剤及び処方 3.2.P.1 製剤及び処方
9 3.2.P.2 製剤開発の経緯 3.2.P.2 製剤開発の経緯 3.2.P.3 製造 3.2.P.3 製造 P.4 添加剤の管理 3.2.P.4 添加剤の管理 P.5 製剤の管理 3.2.P.5.1 規格及び試験方法 P.5.2 試験方法 ( 分析方法 ) P.5.3 試験方法 ( 分析方法 ) のバリデーション 3.2.P.5.4 ロット分析 3.2.P.5.5 不純物の特性 3.2.P.5.6 規格及び試験方法の妥当性 P.6 標準品又は標準物質 3.2.P.6 標準品又は標準物質 P.7 容器及び施栓系 3.2.P.7 容器及び施栓系 P.8 安定性 3.2.P.8.1 安定性のまとめ及び結論 P.8.2 承認後の安定性試験計画の作成及び実施 P.8.3 安定性データ 20 / ~ 継続中 3.2.A その他 3.2.A.1 製造施設及び設備 3.2.A.1 製造施設及び設備 A.2 外来性感染性物質の安全性評価 3.2.A.2 外来性感染性物質の安全性評価 3.2.A.3 添加剤 3.2.A.3 添加剤 R 各極の要求資料 3.3 参考文献
10 3.3 Establishment of a Standard Assay Method for Human Thrombomodulin and Determination of the Activity of the Japanese Reference Standard S. Niimi et al. Biologicals 2002; 30: 第 4 部非臨床試験報告書 4.2 試験報告書 薬理試験 効力を裏付ける試験 Tissue Factor 誘発トロンビン生成に対 する ART-123 及びヘパリンの作用トロンビン凝固時間に対する ART-123 及びヘパリンの作用 ART-123 のプロトロンビナーゼ阻害 におよぼす血漿中プロテイン C の影響 Tissue Factor 誘発ラット DIC モデルにおける ART-123 ダルテパリン メシ ル酸ガベキサート 及びメシル酸ナファモスタットの薬効試験 Tissue Factor 誘発ラット DIC モデルの 出血時間に対する ART-123 及びヘパリンの作用 LPS 誘発ラット DIC モデルの生存率に 対する ART-123 の効果カニクイザルを用いた TF 誘発 DIC モ デルにおける AT-908 の薬効試験カニクイザルを用いた TF 誘発 DIC モ デルにおけるヘパリンの薬効試験公表論文 :The inhibitory effect of recombinant human soluble thrombomodulin on initiation and extension of coagulation A comparison with other anticoagulants 公表論文 : 組換えヒト可溶型トロンボ モジュリン (ART-123) の抗凝固作用公表論文 :Antithrombotic effect of recombinant human soluble thrombomodulin on endotoxin-induced disseminated intravascular coagulation in rats. 公表論文 :Intravenous extended infusion of recombinant human soluble thrombomodulin prevented tissue factor-induced disseminated intravascular coagulation in rats Mitsunobu Mohri 中薗修 旭化成株式会社 Thromb Haemost 1999; 82: Jpn Pharmacol Ther( 薬理と治療 )2006; 34: Yasunori Gonda Thromb Res 1993; 71: Mitsunobu Mohri Am J Hematol 1994; 45:
11 公表論文 :Effects of recombinant human soluble thrombomodulin (rhs-tm) on a rat model of disseminated intravascular coagulation with decreased levels of plasma antithrombin III 公表論文 :The antithrombotic effects of recombinant human soluble thrombomodulin (rhstm) on tissue factor-induced disseminated intravascular coagulation in crab-eating monkeys (Macaca fascicularis) Tissue Factor 誘発トロンビン生成に対 する ART-123 活性化プロテイン C ヒルジン 及びアルガトロバンの作用 ( 追加解析 ) 副次的薬理試験 Tissue Factor 誘発ラット DIC モデルを 用いた血漿中 TAFI 値低下におよぼす ART-123 の作用公表論文 :Heat stability of carboxypeptidase R of experimental animals 公表論文 :Antithrombotic effects of recombinant human soluble thrombomodulin (rhs-tm) on arteriovenous shunt thrombosis in rats 学会要旨 :The effect of recombinant human soluble thrombomodulin on sepsis after severe injury in a murine model 公表論文 : 組換えヒト可溶型トロンボ モジュリン (ART-123) の LPS 誘発 DIC モデルにおける血漿中 IL-1βおよび生存率に対する作用 安全性薬理試験 Yoshikazu Aoki M. Mohri Hidefumi Komura Thromb Haemost 1994; 71: Blood Coagul Fibrinolysis 1997; 8: Microbiol Immunol 2002; 46: Yoshikazu Aoki Am J Hematol 1994; 47: G. Tajima 中薗修 [Available from] 05PosterAbstracts.pdf Jpn Pharmacol Ther( 薬理と治療 )2006; 34: ART-123 の herg 導入 CHO-K1 細胞のカリウム電流に対する作用 ART-123 のラットにおける中枢神経 系に対する安全性薬理試験 ART-123 のカニクイザルにおける心 血管系及び呼吸系に対する安全性薬理試験 AT-908 の一般薬理試験 薬力学的薬物相互作用試験 ART-123 とヘパリンの APTT 延長作用における薬力学的薬物相互作用の検討 ART-123 とダルテパリンの APTT 延長作用における薬力学的薬物相互作用の検討
12 薬物動態試験 ART-123 とメシル酸ガベキサートの APTT 延長作用における薬力学的薬物相互作用の検討 ART-123 とメシル酸ナファモスタットの APTT 延長作用における薬力学的薬物相互作用の検討 ART-123 のトロンビン生成阻害作用に対するヘパリン ダルテパリン メシル酸ガベキサート 及びメシル酸ナファモスタットの作用 分析法及びバリデーション報告書 ラット血漿中 ART-123 濃度測定用 ELISA 法バリデーション サル血漿中及び尿中 ART-123 濃度測定用 ELISA バリデーション試験 サル血漿中 ART-123 活性測定バリデーション試験 I-AT-908 本合成 物性保証試験 吸収 ラット静脈内投与時の ART-123 血漿中濃度推移 AT-908 の体内動態試験 (I) ラットに おける分布 代謝 排泄 ART-123 のカニクイザルにおける薬物動態試験 ( 単回投与 - 用量依存性 ) ART-123 のカニクイザルにおける薬物動態試験 ( 反復静脈内急速投与 ) ART-123 のカニクイザルにおける薬物動態試験 ( 単回投与 - 静脈内持続投与 ) ART-123 体内動態試験ラット血漿中濃度試験 ( 単回投与 - 用量依存性 ) ART-123 血漿中動態の線形性の解析 分布 項に記載 代謝 項に記載 排泄 項に記載 項に記載 項に記載 項に記載
13 薬物動態学的薬物相互作用 ( 非臨床 ) その他の薬物動態試験 ART-123(TM) の体内動態 腎機能障害モデルラットにおける ART-123 の血漿中濃度推移 - ART-123 の薬物動態に対する腎機能 障害による影響について - 追加解析及び考察 毒性試験 単回投与毒性試験 AT-908 のラットにおける静脈内単回 投与毒性試験 AT-908 のカニクイザルにおける単回 静脈内投与毒性試験 反復投与毒性試験 AT-908 のラットにおける静脈内 1 カ月間反復投与毒性試験および回復性試験 ART-123 のトキシコキネティクス試験 : ラットにおける静脈内投与による 28 日間反復投与毒性試験 旭化成株式会社 AT-908 のカニクイザルにおける 2 週間反復静脈内投与毒性試験 ART-123(AT-908) のカニクイザルに おける 4 週間反復静脈内投与毒性試験および 4 週間回復試験 ART-123 のカニクイザルにおける 26 週間反復静脈内投与毒性試験 遺伝毒性試験 In Vitro 試験 AT-908 のほ乳類の培養細胞を用いる 染色体異常試験 In Vivo 試験 東洋醸造株式会社 がん原性試験 生殖発生毒性試験 受胎能及び着床までの初期胚発生に関する試験 ( 妊娠前及び妊娠初期投与試験 ) ART-123 の生殖 発生毒性試験 : ラットにおける静脈内投与による妊娠前及び妊娠初期投与試験 胚 胎児発生に関する試験 ( 胎児の器官形成期投与試験 )
14 ART-123 の生殖 発生毒性試験 : ラットにおける静脈内投与による胎児の器官形成期投与試験 ( 妊娠末期観察試験 ) ART-123 の生殖 発生毒性試験 : ラットにおける静脈内投与による胎児の器官形成期投与試験 ( 妊娠末期観察試験の投与量追加試験 ) ART-123 の生殖 発生毒性試験 : ラットにおける静脈内投与による胎児の器官形成期投与試験 ( 生後観察試験 ) ART-123 のカニクイザルにおける静脈内投与による胚 胎児発生への影響に関する試験 出生前及び出生後の発生並びに母体の機能に関する試験 ( 周産期及び授乳期投与試験 ) ART-123 の生殖 発生毒性試験 : ラットにおける静脈内投与による周産期及び授乳期投与試験 新生児を用いた試験 旭化成株式会社 局所刺激性試験 ART-123 のウサギにおける血管に対 する局所刺激性試験 その他の毒性試験 抗原性試験 AT-908 の抗原性試験モルモット全 身性アナフィラキシー反応 免疫毒性試験 東洋醸造株式会社 毒性試験の機序に関する試験 依存性試験 代謝物の毒性試験 不純物の毒性試験 ART-123 強制劣化品のラットにおける単回静脈内投与毒性試験 ART-123 劣化物の抗原性試験 旭化成株式会社 -モルモットの ASA 反応 - ART-123 劣化物の抗原性試験 旭化成株式会社 -モルモットの PCA 反応 - ART-123 劣化物の抗原性試験 - マウス - ラットの PCA 反応 - 旭化成株式会社
15 その他の試験 4.3 参考文献 第 5 部臨床試験報告書 5.3 試験報告書及び関連情報 生物薬剤学試験報告書 バイオアベイラビリティ (BA) 試験報告書 比較 BA 試験及び生物学的同等性 (BE) 試験報告書 In Vitro-In Vivo の関連を検討した試験報告書 生物学的及び理化学的分析法検討報告 ヒト血漿中及び尿中 ART-123 濃度測定用 ELISA バリデーション試験 ヒト生体試料中 ( 血漿 尿 )ART-123 濃度測定用 ELISA 法追加バリデー ション試験 ( 選択性の確認 ) ヒト血清中抗 ART-123 抗体価測定法 のバリデーション ヒト血清中抗宿主細胞由来タンパク 抗マウス免疫グロブリン G および抗 ウシ血清成分抗体価測定法のバリ デーション ヒト血漿中 ART-123 濃度および血清 中中和抗体ならびに抗体価測定法の バリデーション ART-123 のヒト血漿中での 2 年間安定 性試験 ヒト血清中抗 ART-123 中和抗体価測 定法追加バリデーション試験 ヒト血清中抗 ART-123 抗体価測定法 追加バリデーション試験 静脈内持続投与時間による ART-123 の血漿中濃度値への影響 ヒト生体試料を用いた薬物動態関連の試験報告書 旭化成株式会社 臨床薬物動態 (PK) 試験報告書 健康被験者における PK 及び初期忍容性試験報告書
16 治験総括報告書 :ART-123 第 I 相臨床 試験 ( 静脈内持続投与 ) 治験総括報告書 :ART-123 第 I 相臨床 試験 ( 静脈内急速投与 ) 患者における PK 及び初期忍容性試験報告書 内因性要因を検討した PK 試験報告書 外因性要因を検討した PK 試験報告書 健康被験者における PK 及び初期忍容性試験報告書 ART-123 の population pharmacokinetics 解析 臨床薬力学 (PD) 試験報告書 有効性及び安全性試験報告書 申請する適応症に関する比較対照試験報告書 治験総括報告書 :ART-123 後期第 II 相臨床試験 計 92 施設 他 治験総括報告書 :ART-123 第 3 相臨床試験 他計 113 施設 非対照試験報告書 治験総括報告書 :ART-123 前期第 II 相臨床試験 計 32 施設 他 複数の試験成績を併せて解析した報告書 その他の臨床試験報告書 公表論文 :Phase I study of a novel recombinant human soluble thrombomodulin, ART-123 公表論文 :Dose-response study of recombinant human soluble thrombomodulin(art-123) in the prevention of venous thromboembolism after total hip replacement 市販後の使用経験に関する報告書 S.Moll C.Kearon J Thromb Haemost 2004; 2: J Thromb Haemost 2005; 3: 患者データ一覧表及び症例記録 後期第 2 相臨床試験の症例一覧表 ( 用量設定試験 )
17 第 3 相臨床試験の症例一覧表 全試験の副作用発現症例一覧表 全試験の重篤有害事象症例一覧表 全試験の臨床検査値異常変動症例一覧表 全試験の臨床検査値変動図 参考文献 DIC 診断基準の 診断のための補助的検査成績, 所見 の項の改訂について Efficacy and safety of recombinant human soluble thrombomodulin(art-123) in disseminated intravascular coagulation: results of a phase III, randomized, double-blind clinical trial 青木延雄 他 H. Saito et al. 厚生省特定疾患血液凝固異常症調査研究班, 昭和 62 年度研究報告書. 1988: J Thromb Haemost 2007; 5:
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社
 オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
アミヴィッド静注 CTD 第 2 部 2.1 第 2 部から第 5 部の目次 富士フイルム RI ファーマ株式会社
 CTD 第 2 部 富士フイルム RI ファーマ株式会社 ( 空白ページ ) 2 第 2 部 ( モジュール 2): CTD の概要 ( サマリー ) ---------------------------------------------- 第 2 巻 2.2 緒言 2.3 品質に関する概括資料緒言 2.3.S 原薬 (AV-105, ) 2.3.S 原薬 ( フロルベタピル ( 18 F),
CTD 第 2 部 富士フイルム RI ファーマ株式会社 ( 空白ページ ) 2 第 2 部 ( モジュール 2): CTD の概要 ( サマリー ) ---------------------------------------------- 第 2 巻 2.2 緒言 2.3 品質に関する概括資料緒言 2.3.S 原薬 (AV-105, ) 2.3.S 原薬 ( フロルベタピル ( 18 F),
3. 安全性本治験において治験薬が投与された 48 例中 1 例 (14 件 ) に有害事象が認められた いずれの有害事象も治験薬との関連性は あり と判定されたが いずれも軽度 で処置の必要はなく 追跡検査で回復を確認した また 死亡 その他の重篤な有害事象が認められなか ったことから 安全性に問
 フェキソフェナジン塩酸塩錠 6mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにフェキソフェナジン塩酸塩は 第二世代抗ヒスタミン薬の一つであり 抗原抗体反応に伴って起こる肥満細胞からのヒスタミンなどのケミカルメディエーターの遊離を抑制すると共に ヒスタミンの H1 作用に拮抗することにより アレルギー症状を緩和する 今回 フェキソフェナジン塩酸塩錠 6mg
フェキソフェナジン塩酸塩錠 6mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにフェキソフェナジン塩酸塩は 第二世代抗ヒスタミン薬の一つであり 抗原抗体反応に伴って起こる肥満細胞からのヒスタミンなどのケミカルメディエーターの遊離を抑制すると共に ヒスタミンの H1 作用に拮抗することにより アレルギー症状を緩和する 今回 フェキソフェナジン塩酸塩錠 6mg
kss poi-1-jp
 1.10 毒薬 劇薬等の指定審査資料のまとめ 1.10 毒薬 劇薬等の指定審査資料のまとめ 毒薬 劇薬等の指定審査資料のまとめ < 追加 > 化学名 別名構造式効能 効果シェーグレン症候群患者の口腔乾燥症状の改善用法 用量劇薬等の指定市販名及び有効成分 分量毒性副作用 [ シェーグレン症候群患者の口腔乾燥症状の改善 ] 会社 副作用発現率 282/367 =76.8% 副作用の種類 例数 (%) 多汗
1.10 毒薬 劇薬等の指定審査資料のまとめ 1.10 毒薬 劇薬等の指定審査資料のまとめ 毒薬 劇薬等の指定審査資料のまとめ < 追加 > 化学名 別名構造式効能 効果シェーグレン症候群患者の口腔乾燥症状の改善用法 用量劇薬等の指定市販名及び有効成分 分量毒性副作用 [ シェーグレン症候群患者の口腔乾燥症状の改善 ] 会社 副作用発現率 282/367 =76.8% 副作用の種類 例数 (%) 多汗
<4D F736F F F696E74202D2097D58FB08E8E8CB1838F815B834E F197D58FB E96D8816A66696E616C CF68A4A2E >
 再生医療等製品の非臨床安全性評価の考え方 ex vivo 遺伝子治療を中心に 独立行政法人医薬品医療機器総合機構 (PMDA) 再生医療製品等審査部 真木一茂 様式 1-B 第 24 回日本遺伝子細胞治療学会学術集会 CO I 開示 発表者名 : 真木一茂 演題発表に関連し 開示すべき CO I 関係にある企業などはありません 2 1 本日の話 1.Ex vivo 遺伝子治療について 2. 治験開始に必要な非臨床試験
再生医療等製品の非臨床安全性評価の考え方 ex vivo 遺伝子治療を中心に 独立行政法人医薬品医療機器総合機構 (PMDA) 再生医療製品等審査部 真木一茂 様式 1-B 第 24 回日本遺伝子細胞治療学会学術集会 CO I 開示 発表者名 : 真木一茂 演題発表に関連し 開示すべき CO I 関係にある企業などはありません 2 1 本日の話 1.Ex vivo 遺伝子治療について 2. 治験開始に必要な非臨床試験
添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示され
 添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示されます 検索条件設定時の注意 検索はテキスト文章 (SGML 又は XML) が対象となっており 画像及び
添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示されます 検索条件設定時の注意 検索はテキスト文章 (SGML 又は XML) が対象となっており 画像及び
Microsoft Word _2180AMY10104_K104_1.doc
 アボネックス 筋注用シリンジ ( インターフェロン β-1a) 第 2 部 CTD 概要 ジェンザイム ジャパン株式会社 目次 2.7.6.1 個々の試験の一覧... 1 2.7.6.2 個々の試験の概要 2.7.6.2.1 試験 C90-042 の概要外国人健康志願者における IFNβ-1a(XG90xx) の用量漸増試験 ( 試験報告書 5.3.1.1-1)... 7 2.7.6.2.2 試験
アボネックス 筋注用シリンジ ( インターフェロン β-1a) 第 2 部 CTD 概要 ジェンザイム ジャパン株式会社 目次 2.7.6.1 個々の試験の一覧... 1 2.7.6.2 個々の試験の概要 2.7.6.2.1 試験 C90-042 の概要外国人健康志願者における IFNβ-1a(XG90xx) の用量漸増試験 ( 試験報告書 5.3.1.1-1)... 7 2.7.6.2.2 試験
ータについては Table 3 に示した 両製剤とも投与後血漿中ロスバスタチン濃度が上昇し 試験製剤で 4.7±.7 時間 標準製剤で 4.6±1. 時間に Tmaxに達した また Cmaxは試験製剤で 6.3±3.13 標準製剤で 6.8±2.49 であった AUCt は試験製剤で 62.24±2
 ロスバスタチン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロスバスタチンは HMG-CoA 還元酵素を競合的に阻害することにより HMG-CoA のメバロン酸への変更を減少させ コレステロール生合成における早期の律速段階を抑制する高コレステロール血症治療剤である 今回 ロスバスタチン錠 mg TCK とクレストール 錠 mg の生物学的同等性を検討するため
ロスバスタチン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロスバスタチンは HMG-CoA 還元酵素を競合的に阻害することにより HMG-CoA のメバロン酸への変更を減少させ コレステロール生合成における早期の律速段階を抑制する高コレステロール血症治療剤である 今回 ロスバスタチン錠 mg TCK とクレストール 錠 mg の生物学的同等性を検討するため
リコモジュリン点滴静注用12800
 **2018 年 2 月改訂 ( 第 9 版 ) *2016 年 4 月改訂 日本標準商品分類番号 873339 生物由来製品処方箋医薬品 注意 - 医師等の処方箋により使用すること 血液凝固阻止剤 承認番号 22000AMX00023000 薬価収載 2008 年 4 月 販売開始 2008 年 5 月 ** 再審査結果 2017 年 12 月 ( トロンボモデュリンアルファ ( 遺伝子組換え )
**2018 年 2 月改訂 ( 第 9 版 ) *2016 年 4 月改訂 日本標準商品分類番号 873339 生物由来製品処方箋医薬品 注意 - 医師等の処方箋により使用すること 血液凝固阻止剤 承認番号 22000AMX00023000 薬価収載 2008 年 4 月 販売開始 2008 年 5 月 ** 再審査結果 2017 年 12 月 ( トロンボモデュリンアルファ ( 遺伝子組換え )
(案-1)
 薬食審査発 0930 第 1 号 平成 26 年 9 月 30 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) 医薬品の一般的名称について 標記については 医薬品の一般的名称の取扱いについて ( 平成 18 年 3 月 31 日薬食発第 0331001 号厚生労働省医薬食品局長通知 ) 等により取り扱っているところであるが 今般 我が国における医薬品一般的名称
薬食審査発 0930 第 1 号 平成 26 年 9 月 30 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) 医薬品の一般的名称について 標記については 医薬品の一般的名称の取扱いについて ( 平成 18 年 3 月 31 日薬食発第 0331001 号厚生労働省医薬食品局長通知 ) 等により取り扱っているところであるが 今般 我が国における医薬品一般的名称
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠 50mg 医薬品リスク管理計画書 (RMP) の概要 有効成分 タペンタ 錠 100mg 製造販売業者 ヤンセンファーマ株式会社 薬効分類 821 提出年月 平成 30 年
 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
2.1 目次 アレジオン点眼液 0.05% 第 2 部 ( モジュール 2): CTD の概要 ( サマリー ) 2.1 第 2 部 ( モジュール 2) から第 5 部 ( モジュール 5) の目次 参天製薬株式会社 1
 アレジオン点眼液 0.05% 第 2 部 ( モジュール 2): CTD の概要 ( サマリー ) 2.1 第 2 部 ( モジュール 2) から第 5 部 ( モジュール 5) の目次 参天製薬株式会社 1 第 2 部 ( モジュール 2):CTD の概要 ( サマリー ) 2.1 第 2 部 ( モジュール 2) から第 5 部 ( モジュール 5) の目次 2.2 緒言 2.3 品質に関する概括資料
アレジオン点眼液 0.05% 第 2 部 ( モジュール 2): CTD の概要 ( サマリー ) 2.1 第 2 部 ( モジュール 2) から第 5 部 ( モジュール 5) の目次 参天製薬株式会社 1 第 2 部 ( モジュール 2):CTD の概要 ( サマリー ) 2.1 第 2 部 ( モジュール 2) から第 5 部 ( モジュール 5) の目次 2.2 緒言 2.3 品質に関する概括資料
あった AUCtはで ± ng hr/ml で ± ng hr/ml であった 2. バイオアベイラビリティの比較およびの薬物動態パラメータにおける分散分析の結果を Table 4 に示した また 得られた AUCtおよび Cmaxについてとの対数値
 モンテルカストチュアブル錠 5mg TCK の生物学的同等性試験 ( 口中溶解後 水なし投与 ) バイオアベイラビリティの比較 辰巳化学株式会社 はじめにモンテルカストナトリウムは アレルギーのメディエーターの 1 つであるロイコトリエン (LT) の受容体の内 cyslt1 受容体を遮断する抗アレルギー薬である 今回 モンテルカストチュアブル錠 5mg TCK とキプレス チュアブル錠 5mg の生物学的同等性を検討するため
モンテルカストチュアブル錠 5mg TCK の生物学的同等性試験 ( 口中溶解後 水なし投与 ) バイオアベイラビリティの比較 辰巳化学株式会社 はじめにモンテルカストナトリウムは アレルギーのメディエーターの 1 つであるロイコトリエン (LT) の受容体の内 cyslt1 受容体を遮断する抗アレルギー薬である 今回 モンテルカストチュアブル錠 5mg TCK とキプレス チュアブル錠 5mg の生物学的同等性を検討するため
使用上の注意 1. 慎重投与 ( 次の患者には慎重に投与すること ) 1 2X X 重要な基本的注意 1TNF 2TNF TNF 3 X - CT X 4TNFB HBsHBcHBs B B B B 5 6TNF 7 8dsDNA d
 2015 5 7 201410 28 TNF 阻害薬 TNFFab シムジア 皮下注 200mg シリンジ Cimzia 200mg Syringe for S.C. Injection セルトリズマブペゴル ( 遺伝子組換え ) 製剤 873999 22400AMX01488000 20132 20133 20155 20079 警告 1. 2. 1 2 X - CT 3. TNF 4. 1 禁忌
2015 5 7 201410 28 TNF 阻害薬 TNFFab シムジア 皮下注 200mg シリンジ Cimzia 200mg Syringe for S.C. Injection セルトリズマブペゴル ( 遺伝子組換え ) 製剤 873999 22400AMX01488000 20132 20133 20155 20079 警告 1. 2. 1 2 X - CT 3. TNF 4. 1 禁忌
用法 用量 発作性夜間ヘモグロビン尿症における溶血抑制 mg mg mg mg kg 30kg 40kg 20kg 30kg 10kg 20kg 5kg 10kg 1900mg mg mg mg
 C EculizumabGenetical Recombination AMX 警告 1 2 禁忌 ( 次の患者には投与しないこと ) 1 2 組成 性状 ml mg mg mg mg mg ph ph mgml 効能 効果 発作性夜間ヘモグロビン尿症における溶血抑制 < 効能 効果に関連する使用上の注意 > 共通 1C5 C5b-9 b 発作性夜間ヘモグロビン尿症における溶血抑制 1 2 3 4
C EculizumabGenetical Recombination AMX 警告 1 2 禁忌 ( 次の患者には投与しないこと ) 1 2 組成 性状 ml mg mg mg mg mg ph ph mgml 効能 効果 発作性夜間ヘモグロビン尿症における溶血抑制 < 効能 効果に関連する使用上の注意 > 共通 1C5 C5b-9 b 発作性夜間ヘモグロビン尿症における溶血抑制 1 2 3 4
医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能
 医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 1 2 3 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能 ) ( 医薬品の名称のみで検索する場合 34 の項目は未選択 未入力で可 ) 検索結果で表示したい文書を選択
医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 1 2 3 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能 ) ( 医薬品の名称のみで検索する場合 34 の項目は未選択 未入力で可 ) 検索結果で表示したい文書を選択
ピルシカイニド塩酸塩カプセル 50mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにピルジカイニド塩酸塩水和物は Vaughan Williams らの分類のクラスⅠCに属し 心筋の Na チャンネル抑制作用により抗不整脈作用を示す また 消化管から速やかに
 ピルシカイニド塩酸塩カプセル 50mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにピルジカイニド塩酸塩水和物は Vaughan Williams らの分類のクラスⅠCに属し 心筋の Na チャンネル抑制作用により抗不整脈作用を示す また 消化管から速やかに吸収され 体内でもほとんど代謝を受けない頻脈性不整脈 ( 心室性 ) に優れた有効性をもつ不整脈治療剤である
ピルシカイニド塩酸塩カプセル 50mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにピルジカイニド塩酸塩水和物は Vaughan Williams らの分類のクラスⅠCに属し 心筋の Na チャンネル抑制作用により抗不整脈作用を示す また 消化管から速やかに吸収され 体内でもほとんど代謝を受けない頻脈性不整脈 ( 心室性 ) に優れた有効性をもつ不整脈治療剤である
1_alignment.ppt
 " " " " n " n n " n " n n n " n n n n " n LGPSSKQTGKGW-SRIWDN! + +! LN-ITKSAGKGAIMRLGDA! " n -------TGKG--------!! -------AGKG--------! " n w w w " n w w " " " 11 12 " n w w w " n w w A! M! O! A!
" " " " n " n n " n " n n n " n n n n " n LGPSSKQTGKGW-SRIWDN! + +! LN-ITKSAGKGAIMRLGDA! " n -------TGKG--------!! -------AGKG--------! " n w w w " n w w " " " 11 12 " n w w w " n w w A! M! O! A!
査を実施し 必要に応じ適切な措置を講ずること (2) 本品の警告 効能 効果 性能 用法 用量及び使用方法は以下のとお りであるので 特段の留意をお願いすること なお その他の使用上の注意については 添付文書を参照されたいこと 警告 1 本品投与後に重篤な有害事象の発現が認められていること 及び本品
 薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
Ⅰ. 改訂内容 ( 部変更 ) ペルサンチン 錠 12.5 改 訂 後 改 訂 前 (1) 本剤投与中の患者に本薬の注射剤を追加投与した場合, 本剤の作用が増強され, 副作用が発現するおそれがあるので, 併用しないこと ( 過量投与 の項参照) 本剤投与中の患者に本薬の注射剤を追加投与した場合, 本
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意 改訂のお知らせ 2006 年 1 月日本ベーリンガーインゲルハイム株式会社 注 ) 処方せん医薬品 ( ジピリダモール製剤 ) = 登録商標注 ) 注意 - 医師等の処方せんにより使用すること 謹啓時下ますますご清祥のこととお慶び申し上げます 平素は弊社製品につきましてご愛顧を賜り厚く御礼申し上げます さて, この度, 自主改訂によりペルサンチン
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意 改訂のお知らせ 2006 年 1 月日本ベーリンガーインゲルハイム株式会社 注 ) 処方せん医薬品 ( ジピリダモール製剤 ) = 登録商標注 ) 注意 - 医師等の処方せんにより使用すること 謹啓時下ますますご清祥のこととお慶び申し上げます 平素は弊社製品につきましてご愛顧を賜り厚く御礼申し上げます さて, この度, 自主改訂によりペルサンチン
モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム 製造販売業者 EA ファーマ株式会社 薬効分類 提出年月 平成 30 年 10 月 1.1. 安全
 モビコール配合内用剤 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はEAファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません EA ファーマ株式会社 モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム
モビコール配合内用剤 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はEAファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません EA ファーマ株式会社 モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム
医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など ) 医薬品候補物質のスクリーニン
 特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名要望された医薬品要望内容 CSL ベーリング株式会社要望番号 Ⅱ-175 成分名 (10%) 人免疫グロブリン G ( 一般名 ) プリビジェン (Privigen) 販売名 未承認薬 適応 外薬の分類
 未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名要望された医薬品要望内容 CSL ベーリング株式会社要望番号 Ⅱ-175 成分名 (10%) 人免疫グロブリン G ( 一般名 ) プリビジェン (Privigen) 販売名 未承認薬 適応 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) ( 要望されたについて記載する
未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名要望された医薬品要望内容 CSL ベーリング株式会社要望番号 Ⅱ-175 成分名 (10%) 人免疫グロブリン G ( 一般名 ) プリビジェン (Privigen) 販売名 未承認薬 適応 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) ( 要望されたについて記載する
 一般名 : オファツムマブ ( 遺伝子組換え ) 製剤 はじめに ( 適正使用に関するお願い )4 治療スケジュール6 投与に際しての注意事項 7 7 8 8 9 1 1 11 12 13 14 15 重大な副作用とその対策 18 18 28 32 34 36 4 42 44 45 参考資料 5 付録 55 55 55 64 3 1 はじめに4 はじめ 5 に1 2 治療スケジュール6 対象患者の選択インフォームドコンセント投与準備
一般名 : オファツムマブ ( 遺伝子組換え ) 製剤 はじめに ( 適正使用に関するお願い )4 治療スケジュール6 投与に際しての注意事項 7 7 8 8 9 1 1 11 12 13 14 15 重大な副作用とその対策 18 18 28 32 34 36 4 42 44 45 参考資料 5 付録 55 55 55 64 3 1 はじめに4 はじめ 5 に1 2 治療スケジュール6 対象患者の選択インフォームドコンセント投与準備
ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル
 ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル 1mg は 1 カプセル中ロペラミド塩酸塩 1 mg を含有し消化管から吸収されて作用を発現する このことから
ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル 1mg は 1 カプセル中ロペラミド塩酸塩 1 mg を含有し消化管から吸収されて作用を発現する このことから
™·”õ/sec3_p63_84/fiü“eflÅ
 Section3 64 1 65 Section 3 1 2 3 4 5 6 7 8 9 10 11 12 13 14 1 Babara E. Ainsworth et al. Med. Sci. Sports. Exevc.1993 66 67 Section 3 1 10 9 8 1 2 3 4 7 6 5 6 7 5 1 2 3 4 68 69 Section 3 2 70 Section 3
Section3 64 1 65 Section 3 1 2 3 4 5 6 7 8 9 10 11 12 13 14 1 Babara E. Ainsworth et al. Med. Sci. Sports. Exevc.1993 66 67 Section 3 1 10 9 8 1 2 3 4 7 6 5 6 7 5 1 2 3 4 68 69 Section 3 2 70 Section 3
減量・コース投与期間短縮の基準
 用法 用量 通常 成人には初回投与量 (1 回量 ) を体表面積に合せて次の基準量とし 朝食後および夕食後の 1 日 2 回 28 日間連日経口投与し その後 14 日間休薬する これを 1 クールとして投与を繰り返す ただし 本剤の投与によると判断される臨床検査値異常 ( 血液検査 肝 腎機能検査 ) および消化器症状が発現せず 安全性に問題がない場合には休薬を短縮できるが その場合でも少なくとも
用法 用量 通常 成人には初回投与量 (1 回量 ) を体表面積に合せて次の基準量とし 朝食後および夕食後の 1 日 2 回 28 日間連日経口投与し その後 14 日間休薬する これを 1 クールとして投与を繰り返す ただし 本剤の投与によると判断される臨床検査値異常 ( 血液検査 肝 腎機能検査 ) および消化器症状が発現せず 安全性に問題がない場合には休薬を短縮できるが その場合でも少なくとも
スライド 1
 薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
一般薬理試験及び毒性試験 2. 毒性試験 (1) 単回投与毒性試験 ( マウス イヌ サル ) 33) 動物種 投与経路 投与量 (mg/kg) 概略の致死量 (mg/kg) マウス 経口 2000 雌雄 :>2000 腹腔内 300 雌雄 :300 経口 750 雌雄 :>750 腹腔内 500
 枢神経系影響なし心血管系一般薬理試験及び毒性試験 1. 一般薬理試験 32) 試験項目 動物種 ( 性 動物数 ) 投与経路投与量主な結果 評価中一般状態 体温及び自発運動量に及ぼす作用 (Irwin 法 ) ( 雄 4 ) 30 100 300mg/kg herg 電流に及ぼす作用 ( ホールセルパッチクランプ法 ) herg 発現ヒト胎児腎細胞株 HEK293 in vitro 4 20 100μmol/L
枢神経系影響なし心血管系一般薬理試験及び毒性試験 1. 一般薬理試験 32) 試験項目 動物種 ( 性 動物数 ) 投与経路投与量主な結果 評価中一般状態 体温及び自発運動量に及ぼす作用 (Irwin 法 ) ( 雄 4 ) 30 100 300mg/kg herg 電流に及ぼす作用 ( ホールセルパッチクランプ法 ) herg 発現ヒト胎児腎細胞株 HEK293 in vitro 4 20 100μmol/L
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 <その他分野 ( 消化器官用薬 解毒剤 その他 )> 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号
 資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
審査報告 (1) 別紙 平成 29 年 4 月 3 日 本申請において 申請者が提出した資料及び医薬品医療機器総合機構における審査の概略等は 以下 のとおりである 申請品目 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノ
![審査報告 (1) 別紙 平成 29 年 4 月 3 日 本申請において 申請者が提出した資料及び医薬品医療機器総合機構における審査の概略等は 以下 のとおりである 申請品目 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノ 審査報告 (1) 別紙 平成 29 年 4 月 3 日 本申請において 申請者が提出した資料及び医薬品医療機器総合機構における審査の概略等は 以下 のとおりである 申請品目 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノ](/thumbs/92/110667825.jpg) 審査報告書 平成 29 年 5 月 17 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノバルティスファーマ株式会社 [ 申請年月日 ] 平成 28 年 7 月 28 日 [ 剤形 含量
審査報告書 平成 29 年 5 月 17 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノバルティスファーマ株式会社 [ 申請年月日 ] 平成 28 年 7 月 28 日 [ 剤形 含量
記載データ一覧 品目名 製造販売業者 BE 品質再評価 1 マグミット錠 250mg 協和化学工業 2 酸化マグネシウム錠 250mg TX みらいファーマ 3 酸化マグネシウム錠 250mg モチダ 持田製薬販売 # 4 酸化マグネシウム錠 250mg マイラン マイラン製薬 # 5 酸化マグネシ
 医療用医薬品最新品質情報集 ( ブルーブック ) 2017.7.7 初版 有効成分 酸化マグネシウム 品目名 ( 製造販売業者 ) 1 マグミット錠 250mg 協和化学工業 後発医薬品 2 酸化マグネシウム錠 250mg TX みらいファーマ 3 酸化マグネシウム錠 250mg モチダ 持田製薬販売 4 酸化マグネシウム錠 250mg マイラン マイラン製薬 5 酸化マグネシウム錠 250mg ケンエー
医療用医薬品最新品質情報集 ( ブルーブック ) 2017.7.7 初版 有効成分 酸化マグネシウム 品目名 ( 製造販売業者 ) 1 マグミット錠 250mg 協和化学工業 後発医薬品 2 酸化マグネシウム錠 250mg TX みらいファーマ 3 酸化マグネシウム錠 250mg モチダ 持田製薬販売 4 酸化マグネシウム錠 250mg マイラン マイラン製薬 5 酸化マグネシウム錠 250mg ケンエー
 エムプリシティ点滴静注用 300 mg エムプリシティ点滴静注用 400 mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はブリストル マイヤーズスクイブ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ブリストル マイヤーズスクイブ株式会社 医薬品リスク管理計画書 平成 29 年 10 月 16 日 独立行政法人医薬品医療機器総合機構理事長殿
エムプリシティ点滴静注用 300 mg エムプリシティ点滴静注用 400 mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はブリストル マイヤーズスクイブ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ブリストル マイヤーズスクイブ株式会社 医薬品リスク管理計画書 平成 29 年 10 月 16 日 独立行政法人医薬品医療機器総合機構理事長殿
B0B820DFD845F9DE49256B7D0002B34
 平成 13 年 ( 行ケ ) 第 238 号特許取消決定取消請求事件 ( 平成 13 年 11 月 2 9 日口頭弁論終結 ) 判決原告バイオ-ラッドラボラトリーズ インコーポレイティド ( 旧表示ジェネティックシステムズコーポレイション ) 訴訟代理人弁護士上谷清同宇井正一同笹本摂同弁理士福本積被告特許庁長官及川耕造指定代理人後藤千恵子同森田ひとみ同茂木静代主文特許庁が平成 10 年異議第 73683
平成 13 年 ( 行ケ ) 第 238 号特許取消決定取消請求事件 ( 平成 13 年 11 月 2 9 日口頭弁論終結 ) 判決原告バイオ-ラッドラボラトリーズ インコーポレイティド ( 旧表示ジェネティックシステムズコーポレイション ) 訴訟代理人弁護士上谷清同宇井正一同笹本摂同弁理士福本積被告特許庁長官及川耕造指定代理人後藤千恵子同森田ひとみ同茂木静代主文特許庁が平成 10 年異議第 73683
生殖発生毒性試験の実施時期について
 S5(R3) Informal 医薬品の生殖発生毒性試験法 ( 改訂 ) 日本製薬工業協会 ICH プロジェクト委員会 S5(R3) Informal WG トピックリーダー藤原道夫 1 本日の内容 1. リスボンInformal WG 対面会議開催に至る経緯 2. ミネアポリス会議以後の活動 3. S5(R3) コンセプトペーパーの変遷 4. S5(R3) に向けて検討されるべき事項 5. S5(R3)
S5(R3) Informal 医薬品の生殖発生毒性試験法 ( 改訂 ) 日本製薬工業協会 ICH プロジェクト委員会 S5(R3) Informal WG トピックリーダー藤原道夫 1 本日の内容 1. リスボンInformal WG 対面会議開催に至る経緯 2. ミネアポリス会議以後の活動 3. S5(R3) コンセプトペーパーの変遷 4. S5(R3) に向けて検討されるべき事項 5. S5(R3)
葉酸とビタミンQ&A_201607改訂_ indd
 L FO AT E VI TAMI NB12 医療関係者用 葉酸 とビタミンB ビタミンB12 アリムタ投与に際して 警告 1 本剤を含むがん化学療法に際しては 緊急時に十分対応できる医療施設において がん化学療 法に十分な知識 経験を持つ医師のもとで 本剤の投与が適切と判断される症例についてのみ投 与すること 適応患者の選択にあたっては 各併用薬剤の添付文書を参照して十分注意すること また 治療開始に先立ち
L FO AT E VI TAMI NB12 医療関係者用 葉酸 とビタミンB ビタミンB12 アリムタ投与に際して 警告 1 本剤を含むがん化学療法に際しては 緊急時に十分対応できる医療施設において がん化学療 法に十分な知識 経験を持つ医師のもとで 本剤の投与が適切と判断される症例についてのみ投 与すること 適応患者の選択にあたっては 各併用薬剤の添付文書を参照して十分注意すること また 治療開始に先立ち
D961H は AstraZeneca R&D Mӧlndal( スウェーデン ) において開発された オメプラゾールの一方の光学異性体 (S- 体 ) のみを含有するプロトンポンプ阻害剤である ネキシウム (D961H の日本における販売名 ) 錠 20 mg 及び 40 mg は を対象として
 第 2 部 CTD の概要 一般名 : エソメプラゾールマグネシウム水和物 版番号 : 2.2 緒言 ネキシウム カプセル ネキシウム 懸濁用顆粒分包 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています D961H は AstraZeneca R&D Mӧlndal( スウェーデン ) において開発された オメプラゾールの一方の光学異性体
第 2 部 CTD の概要 一般名 : エソメプラゾールマグネシウム水和物 版番号 : 2.2 緒言 ネキシウム カプセル ネキシウム 懸濁用顆粒分包 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています D961H は AstraZeneca R&D Mӧlndal( スウェーデン ) において開発された オメプラゾールの一方の光学異性体
緒言
 CERA 2.2 緒言 Page 1 ミルセラ注シリンジ25 μg ミルセラ注シリンジ50 μg ミルセラ注シリンジ75 μg ミルセラ注シリンジ100 μg ミルセラ注シリンジ150 μg ミルセラ注シリンジ200 μg ミルセラ注シリンジ250 μg [ 腎性貧血 ] 第 2 部 CTD の概要 ( サマリー ) 2.2 緒言 中外製薬株式会社 CERA 2.2 緒言 Page 2 目次頁 2.2
CERA 2.2 緒言 Page 1 ミルセラ注シリンジ25 μg ミルセラ注シリンジ50 μg ミルセラ注シリンジ75 μg ミルセラ注シリンジ100 μg ミルセラ注シリンジ150 μg ミルセラ注シリンジ200 μg ミルセラ注シリンジ250 μg [ 腎性貧血 ] 第 2 部 CTD の概要 ( サマリー ) 2.2 緒言 中外製薬株式会社 CERA 2.2 緒言 Page 2 目次頁 2.2
シプロフロキサシン錠 100mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを
 シプロフロキサシン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを有し 上気道感染症 尿路感染症 皮膚感染症などに有効なニューキノロン系の合成抗菌剤である シプロキサン 錠
シプロフロキサシン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを有し 上気道感染症 尿路感染症 皮膚感染症などに有効なニューキノロン系の合成抗菌剤である シプロキサン 錠
DRAFT#9 2011
 報道関係各位 2019 年 1 月 8 日 ユーシービージャパン株式会社 抗てんかん剤 ビムパット ドライシロップ 10% 及び ビムパット 点滴静注 200mg 製造販売承認のお知らせ ユーシービージャパン株式会社 ( 本社 : 東京都新宿区 代表取締役社長 : 菊池加奈子 以下 ユーシービージャパン また ユーシービーグループを総称して以下 ユーシービー ) は本日 抗てんかん剤 ビムパット ドライシロップ
報道関係各位 2019 年 1 月 8 日 ユーシービージャパン株式会社 抗てんかん剤 ビムパット ドライシロップ 10% 及び ビムパット 点滴静注 200mg 製造販売承認のお知らせ ユーシービージャパン株式会社 ( 本社 : 東京都新宿区 代表取締役社長 : 菊池加奈子 以下 ユーシービージャパン また ユーシービーグループを総称して以下 ユーシービー ) は本日 抗てんかん剤 ビムパット ドライシロップ
試験デザイン :n=152 試験開始前に第 VIII 因子製剤による出血時止血療法を受けていた患者群を 以下のい ずれかの群に 2:2:1 でランダム化 A 群 (n=36) (n=35) C 群 (n=18) ヘムライブラ 3 mg/kg を週 1 回 4 週間定期投与し その後 1.5 mg/k
 各位 2018 年 5 月 21 日 ヘムライブラ の 2 本の第 III 相国際共同治験の成績を世界血友病連盟 (WFH)2018 世界大会で発表 中外製薬株式会社 ( 本社 : 東京 代表取締役社長 CEO: 小坂達朗 ) は 血友病 A 治療薬ヘムライブラ [ 一般名 : エミシズマブ ( 遺伝子組換え )] について 第 III 相国際共同治験である HAVEN 3 試験 (NCT02847637)
各位 2018 年 5 月 21 日 ヘムライブラ の 2 本の第 III 相国際共同治験の成績を世界血友病連盟 (WFH)2018 世界大会で発表 中外製薬株式会社 ( 本社 : 東京 代表取締役社長 CEO: 小坂達朗 ) は 血友病 A 治療薬ヘムライブラ [ 一般名 : エミシズマブ ( 遺伝子組換え )] について 第 III 相国際共同治験である HAVEN 3 試験 (NCT02847637)
バイオ医薬品は生物を用いて製造されます 通常 細菌や動物細胞などの生体の中で目的とするタンパク質を産生させます バイオ医薬品の特性は製造プロセスの状態に依存するところが大きく しばしば プロセスが製品 と喩えられます 事実 製造プロセスにおける小さな変更でも 最終製品の違いにつながる可能性があります
 バイオ医薬品とバイオシミラー ( バイオ後続品 ) に関する Q&A 1. バイオテクノロジーとは そしてバイオ医薬品の役割とはどのようなものでしょうか? バイオテクノロジーとは 製品やサービスを生み出するために生物やその一部による修飾を用いた一連の方法やプロセスです 1970 年代のいわゆる 組換えDNA 技術 の発展 展開により 分子レベル でのバイオテクノロジーという新たな時代が幕を開け 様々な分野で知識革命を引き起こしました
バイオ医薬品とバイオシミラー ( バイオ後続品 ) に関する Q&A 1. バイオテクノロジーとは そしてバイオ医薬品の役割とはどのようなものでしょうか? バイオテクノロジーとは 製品やサービスを生み出するために生物やその一部による修飾を用いた一連の方法やプロセスです 1970 年代のいわゆる 組換えDNA 技術 の発展 展開により 分子レベル でのバイオテクノロジーという新たな時代が幕を開け 様々な分野で知識革命を引き起こしました
審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果
![審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果 審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果](/thumbs/92/108604766.jpg) 審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
MRS_T_IF_1509_08.indb
 2015 年 9 月改訂 ( 改訂第 8 版 ) 日本標準商品分類番号 871339 医薬品インタビューフォーム IF 2013 めまい 平衡障害治療剤日本薬局方ベタヒスチンメシル酸塩錠 剤形 製剤の規制区分 規格 含量 一般名 製造販売承認年月日薬価基準収載 発売年月日 開発 製造販売 ( 輸入 ) 提携 販売会社名 医薬情報担当者の連絡先 問い合わせ窓口 6mg 1 6mg 12mg 1 12mg
2015 年 9 月改訂 ( 改訂第 8 版 ) 日本標準商品分類番号 871339 医薬品インタビューフォーム IF 2013 めまい 平衡障害治療剤日本薬局方ベタヒスチンメシル酸塩錠 剤形 製剤の規制区分 規格 含量 一般名 製造販売承認年月日薬価基準収載 発売年月日 開発 製造販売 ( 輸入 ) 提携 販売会社名 医薬情報担当者の連絡先 問い合わせ窓口 6mg 1 6mg 12mg 1 12mg
トリアムシノロンアセトニド マキュエイド硝子体内注用 40mg 医薬品製造販売承認事項一部変更承認申請書 添付資料 CTD 第 2 部 ( 資料概要 ) 2.6 非臨床試験の概要文及び概要表 薬物動態試験の概要文 わかもと製薬株式会社 1
 トリアムシノロンアセトニド マキュエイド硝子体内注用 40mg 医薬品製造販売承認事項一部変更承認申請書 添付資料 CTD 第 2 部 ( 資料概要 ) 2.6 非臨床試験の概要文及び概要表 2.6.4 薬物動態試験の概要文 わかもと製薬株式会社 1 2.6.4 薬物動態試験の概要文マキュエイド硝子体内注用 目次 2.6.4 薬物動態試験の概要文... 4 2.6.4.1 まとめ... 4 2.6.4.2
トリアムシノロンアセトニド マキュエイド硝子体内注用 40mg 医薬品製造販売承認事項一部変更承認申請書 添付資料 CTD 第 2 部 ( 資料概要 ) 2.6 非臨床試験の概要文及び概要表 2.6.4 薬物動態試験の概要文 わかもと製薬株式会社 1 2.6.4 薬物動態試験の概要文マキュエイド硝子体内注用 目次 2.6.4 薬物動態試験の概要文... 4 2.6.4.1 まとめ... 4 2.6.4.2
Microsoft PowerPoint 説明資料(きのこを活用してGABA富化素材を作る)林産試験場
 きのこを活用して GABA 富化素材を作る 説明内容 はじめに きのこと GABA のこと 本技術の開発と技術内容 GABA に着目した理由 きのこのGABA 生産能素材の機能性評価素材生産プロセスの効率化 本技術の活用 素材の多様化 用途企業等への期待 課題 展開 施設栽培により生産されているきのこ GABA( ギャバ ) の機能性 血圧上昇抑制精神安定成長ホルモン分泌促進その他記憶学習促進体重低減血中の中性脂肪低減
きのこを活用して GABA 富化素材を作る 説明内容 はじめに きのこと GABA のこと 本技術の開発と技術内容 GABA に着目した理由 きのこのGABA 生産能素材の機能性評価素材生産プロセスの効率化 本技術の活用 素材の多様化 用途企業等への期待 課題 展開 施設栽培により生産されているきのこ GABA( ギャバ ) の機能性 血圧上昇抑制精神安定成長ホルモン分泌促進その他記憶学習促進体重低減血中の中性脂肪低減
グルコースは膵 β 細胞内に糖輸送担体を介して取り込まれて代謝され A T P が産生される その結果 A T P 感受性 K チャンネルの閉鎖 細胞膜の脱分極 電位依存性 Caチャンネルの開口 細胞内 Ca 2+ 濃度の上昇が起こり インスリンが分泌される これをインスリン分泌の惹起経路と呼ぶ イ
 薬効薬理 1. 作用機序 アナグリプチンはジペプチジルペプチダーゼ -4(DPP-4) の競合的かつ可逆的な選択的阻害剤である インクレチンであるグルカゴン様ペプチド-1(GL P-1) 及びグルコース依存性インスリン分泌刺激ポリペプチド (GI P) は グルコース依存的なインスリン分泌促進作用やグルカゴン分泌抑制作用等 ( 主にGLP-1の作用 ) を有するが 24) DPP-4により分解されて活性を失う
薬効薬理 1. 作用機序 アナグリプチンはジペプチジルペプチダーゼ -4(DPP-4) の競合的かつ可逆的な選択的阻害剤である インクレチンであるグルカゴン様ペプチド-1(GL P-1) 及びグルコース依存性インスリン分泌刺激ポリペプチド (GI P) は グルコース依存的なインスリン分泌促進作用やグルカゴン分泌抑制作用等 ( 主にGLP-1の作用 ) を有するが 24) DPP-4により分解されて活性を失う
抗菌薬の殺菌作用抗菌薬の殺菌作用には濃度依存性と時間依存性の 2 種類があり 抗菌薬の効果および用法 用量の設定に大きな影響を与えます 濃度依存性タイプでは 濃度を高めると濃度依存的に殺菌作用を示します 濃度依存性タイプの抗菌薬としては キノロン系薬やアミノ配糖体系薬が挙げられます 一方 時間依存性
 2012 年 1 月 4 日放送 抗菌薬の PK-PD 愛知医科大学大学院感染制御学教授三鴨廣繁抗菌薬の PK-PD とは薬物動態を解析することにより抗菌薬の有効性と安全性を評価する考え方は アミノ配糖体系薬などの副作用を回避するための薬物血中濃度モニタリング (TDM) の分野で発達してきました 近年では 耐性菌の増加 コンプロマイズド ホストの増加 新規抗菌薬の開発の停滞などもあり 現存の抗菌薬をいかに科学的に使用するかが重要な課題となっており
2012 年 1 月 4 日放送 抗菌薬の PK-PD 愛知医科大学大学院感染制御学教授三鴨廣繁抗菌薬の PK-PD とは薬物動態を解析することにより抗菌薬の有効性と安全性を評価する考え方は アミノ配糖体系薬などの副作用を回避するための薬物血中濃度モニタリング (TDM) の分野で発達してきました 近年では 耐性菌の増加 コンプロマイズド ホストの増加 新規抗菌薬の開発の停滞などもあり 現存の抗菌薬をいかに科学的に使用するかが重要な課題となっており
2. 新ガイドラインの要点 ⑴ 新ガイドラインは 旧ガイドラインの内容を第 1 部とし 今般 ICH において合意された内容を第 2 部 ( 補遺 ) としたこと ⑵ 第 1 部については 現時点において標準的に使用される用語等を踏まえ 記載整備を行ったこと ⑶ 第 2 部については 動物実験の 3
 薬食審査発 0323 第 1 号平成 24 年 3 月 23 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 バイオテクノロジー応用医薬品の非臨床における安全性評価 について 医薬品の製造販売承認に際して添付すべき非臨床における安全性試験の資料に関し バイオテクノロジー応用医薬品の非臨床における安全性評価については バイオテクノロジー応用医薬品の非臨床における安全性評価について
薬食審査発 0323 第 1 号平成 24 年 3 月 23 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 バイオテクノロジー応用医薬品の非臨床における安全性評価 について 医薬品の製造販売承認に際して添付すべき非臨床における安全性試験の資料に関し バイオテクノロジー応用医薬品の非臨床における安全性評価については バイオテクノロジー応用医薬品の非臨床における安全性評価について
Perl + α. : DNA, mrna,,
 2009 Perl + α. : DNA, mrna,, DNA .. DNA A C G T DNA 2 A-T, C-G DNA NH 2 NH 2 O - O O N P O - O CH 2 O N N O - O P O CH 2 O N O - O O P O NH 2 O - O - N CH 2 O N O OH OH OH DNA or RNA (U) (A) (G) (C)
2009 Perl + α. : DNA, mrna,, DNA .. DNA A C G T DNA 2 A-T, C-G DNA NH 2 NH 2 O - O O N P O - O CH 2 O N N O - O P O CH 2 O N O - O O P O NH 2 O - O - N CH 2 O N O OH OH OH DNA or RNA (U) (A) (G) (C)
1)~ 2) 3) 近位筋脱力 CK(CPK) 高値 炎症を伴わない筋線維の壊死 抗 HMG-CoA 還元酵素 (HMGCR) 抗体陽性等を特徴とする免疫性壊死性ミオパチーがあらわれ 投与中止後も持続する例が報告されているので 患者の状態を十分に観察すること なお 免疫抑制剤投与により改善がみられた
 適正使用に欠かせない情報です 必ずお読みください 使用上の注意 改訂のお知らせ 注 1) 処方箋医薬品 ATORVASTATIN TABLETS AMALUET COMBINATION TABLETS 注 1) 処方箋医薬品 PRAVASTATIN SODIUM TABLETS 注 1) 注意 - 医師等の処方箋により使用すること PITAVASTATIN CALCIUM TABLETS 2016
適正使用に欠かせない情報です 必ずお読みください 使用上の注意 改訂のお知らせ 注 1) 処方箋医薬品 ATORVASTATIN TABLETS AMALUET COMBINATION TABLETS 注 1) 処方箋医薬品 PRAVASTATIN SODIUM TABLETS 注 1) 注意 - 医師等の処方箋により使用すること PITAVASTATIN CALCIUM TABLETS 2016
<4D F736F F D B A814089FC92F982CC82A8926D82E782B95F E31328C8E5F5F E646F63>
 - 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ 抗悪性腫瘍剤 ( ブルトン型チロシンキナーゼ阻害剤 ) ( 一般名 : イブルチニブ ) 2016 年 12 月 この度 抗悪性腫瘍剤 イムブルビカ カプセル 140 mg ( 以下標記製品 ) につきまして 再発又は難治性のマントル細胞リンパ腫 の効能追加承認を取得したことに伴い
- 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ 抗悪性腫瘍剤 ( ブルトン型チロシンキナーゼ阻害剤 ) ( 一般名 : イブルチニブ ) 2016 年 12 月 この度 抗悪性腫瘍剤 イムブルビカ カプセル 140 mg ( 以下標記製品 ) につきまして 再発又は難治性のマントル細胞リンパ腫 の効能追加承認を取得したことに伴い
3. 生化学的検査 >> 3C. 低分子窒素化合物 >> 3C045. 検体採取 患者の検査前準備 検体採取のタイミング 記号添加物 ( キャップ色等 ) 採取材料採取量測定材料ネ丸底プレイン ( 白 ) 尿 9 ml 注 外 N60 セイカ 検体ラベル ( 単項目オーダー時 ) ホンハ
 3. 生化学的検査 >> 3C. 低分子窒素化合物 >> 3C045. amino acid fractionation 基本情報 3C045 分析物 連絡先 : 3764 JLAC10 診療報酬 識別 材料 001 尿 ( 含むその他 ) 測定法 204 高速液体クラマトグラフィー (HPLC) 結果識別 第 2 章 特掲診療料 D010 5 アミノ酸 第 3 部 検査 D010 5ロ 5 種類以上
3. 生化学的検査 >> 3C. 低分子窒素化合物 >> 3C045. amino acid fractionation 基本情報 3C045 分析物 連絡先 : 3764 JLAC10 診療報酬 識別 材料 001 尿 ( 含むその他 ) 測定法 204 高速液体クラマトグラフィー (HPLC) 結果識別 第 2 章 特掲診療料 D010 5 アミノ酸 第 3 部 検査 D010 5ロ 5 種類以上
Z_O_IF_1409_06.indb
 2014 年 9 月改訂 ( 改訂第 6 版 ) 日本標準商品分類番号 872649 医薬品インタビューフォーム IF 2013 外用ビタミン A 剤 ビタミン A 製剤 剤形 製剤の規制区分 規格 含量 一般名 製造販売承認年月日薬価基準収載 発売年月日 開発 製造販売 ( 輸入 ) 提携 販売会社名 医薬情報担当者の連絡先 問い合わせ窓口 1g A 5mg A 5,000 A A Vitamin
2014 年 9 月改訂 ( 改訂第 6 版 ) 日本標準商品分類番号 872649 医薬品インタビューフォーム IF 2013 外用ビタミン A 剤 ビタミン A 製剤 剤形 製剤の規制区分 規格 含量 一般名 製造販売承認年月日薬価基準収載 発売年月日 開発 製造販売 ( 輸入 ) 提携 販売会社名 医薬情報担当者の連絡先 問い合わせ窓口 1g A 5mg A 5,000 A A Vitamin
トピロリック錠 インタビューフォーム
 Ⅸ. 非臨床試験に関する項目 1. 薬理試験 (1) 薬効薬理試験 ( Ⅵ. 薬効薬理に関する項目 参照 ) (2) 副次的薬理試験 該当資料なし 42) (3) 安全性薬理試験 試験項目 動物種 / 系統投与経路 ( 例数 ) 投与量 特記すべき所見 中枢神経系 一般状態 体温及び自発運動量に及ぼす作用 (Irwin 法 ) ラット / Wistar( 雄 4) herg 電流に及ぼす作用 herg
Ⅸ. 非臨床試験に関する項目 1. 薬理試験 (1) 薬効薬理試験 ( Ⅵ. 薬効薬理に関する項目 参照 ) (2) 副次的薬理試験 該当資料なし 42) (3) 安全性薬理試験 試験項目 動物種 / 系統投与経路 ( 例数 ) 投与量 特記すべき所見 中枢神経系 一般状態 体温及び自発運動量に及ぼす作用 (Irwin 法 ) ラット / Wistar( 雄 4) herg 電流に及ぼす作用 herg
301128_課_薬生薬審発1128第1号_ニボルマブ(遺伝子組換え)製剤の最適使用推進ガイドラインの一部改正について
 薬生薬審発 1128 第 1 号平成 30 年 1 1 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) ニボルマブ ( 遺伝子組換え ) 製剤の最適使用推進ガイドライン ( 非小細胞肺癌 悪性黒色腫 頭頸部癌 腎細胞癌 古典的ホ ジキンリンパ腫 胃癌及び悪性胸膜中皮腫 ) の一部改正について 経済財政運営と改革の基本方針
薬生薬審発 1128 第 1 号平成 30 年 1 1 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) ニボルマブ ( 遺伝子組換え ) 製剤の最適使用推進ガイドライン ( 非小細胞肺癌 悪性黒色腫 頭頸部癌 腎細胞癌 古典的ホ ジキンリンパ腫 胃癌及び悪性胸膜中皮腫 ) の一部改正について 経済財政運営と改革の基本方針
,328 C 6426 H 9900 N 1700 O 2008 S , ,
 2458 13 4 24 1 11 9 17 1,328 C 6426 H 9900 N 1700 O 2008 S 44 145,000 148,000 10 11 27 2 13 4 24 11 9 17 (1) CD20 B CD20 (2) infusion reaction infusion-associated symptom CD20 B 1 375mg/m 2 1 4 3 Heavy
2458 13 4 24 1 11 9 17 1,328 C 6426 H 9900 N 1700 O 2008 S 44 145,000 148,000 10 11 27 2 13 4 24 11 9 17 (1) CD20 B CD20 (2) infusion reaction infusion-associated symptom CD20 B 1 375mg/m 2 1 4 3 Heavy
略語一覧 略語 略していない表現 ( 英 ) 略していない表現 ( 日 ) HPLC high performance liquid chromatography 高速液体クロマトグラフィー LMB Leucomethylene blue ロイコメチレンブルー MAO monoamine oxida
 目次 1. 非臨床試験計画概略...4 2. 薬理試験...5 3. 薬物動態試験...7 4. 毒性試験...8 5. 総括及び結論...10 6. 参考文献一覧...12 1 略語一覧 略語 略していない表現 ( 英 ) 略していない表現 ( 日 ) HPLC high performance liquid chromatography 高速液体クロマトグラフィー LMB Leucomethylene
目次 1. 非臨床試験計画概略...4 2. 薬理試験...5 3. 薬物動態試験...7 4. 毒性試験...8 5. 総括及び結論...10 6. 参考文献一覧...12 1 略語一覧 略語 略していない表現 ( 英 ) 略していない表現 ( 日 ) HPLC high performance liquid chromatography 高速液体クロマトグラフィー LMB Leucomethylene
シダキュアスギ舌下錠 2,000JAU 5,000JAU に係る医薬品リスク管理計画書 (RMP) の概要 販売名 シダキュアスギ舌下錠 2,000JAU,5,000JAU 有効成分 スギ花粉エキス原末 承認取得者名 鳥居薬品株式会社 薬効分類 提出年月 平成 30 年 8 月 1.1.
 シダキュアスギ舌下錠 2,000JAU シダキュアスギ舌下錠 5,000JAU に係る医薬品リスク管理計画書 本資料に記載された情報に関する権利及び内容についての責任は 鳥居薬品株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません 鳥居薬品株式会社 1 シダキュアスギ舌下錠 2,000JAU 5,000JAU に係る医薬品リスク管理計画書 (RMP) の概要 販売名 シダキュアスギ舌下錠
シダキュアスギ舌下錠 2,000JAU シダキュアスギ舌下錠 5,000JAU に係る医薬品リスク管理計画書 本資料に記載された情報に関する権利及び内容についての責任は 鳥居薬品株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません 鳥居薬品株式会社 1 シダキュアスギ舌下錠 2,000JAU 5,000JAU に係る医薬品リスク管理計画書 (RMP) の概要 販売名 シダキュアスギ舌下錠
Microsoft PowerPoint - 新技術説明会配付資料rev提出版(後藤)修正.pp
 食品の抗アレルギー活性評価に利用できる マウスモデルの紹介 農研機構食品総合研究所 食品機能研究領域主任研究員 後藤真生 農研機構 は独立行政法人農業 食品産業技術総合研究機構のコミュニケーションネームです 国民の 1/3 はアレルギー症状を自覚している 1 アレルギー症状なし (59.1%) 皮膚 呼吸器 目鼻いずれかのアレルギー症状あり (35.9%) 医療機関に入院 通院中 (58.2%) (
食品の抗アレルギー活性評価に利用できる マウスモデルの紹介 農研機構食品総合研究所 食品機能研究領域主任研究員 後藤真生 農研機構 は独立行政法人農業 食品産業技術総合研究機構のコミュニケーションネームです 国民の 1/3 はアレルギー症状を自覚している 1 アレルギー症状なし (59.1%) 皮膚 呼吸器 目鼻いずれかのアレルギー症状あり (35.9%) 医療機関に入院 通院中 (58.2%) (
2. 改正の内容 CTD 通知の別紙 5 を この通知の別添のとおり改める 3. 適用期日この通知による取扱いは 平成 30 年 7 月 1 日以降に行われる製造販売承認申請について適用する ただし 本日以降 この改正の内容に従って製造販売承認申請を行っても差し支えない 以上
 薬生薬審発 0202 第 1 号 平成 29 年 2 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) 新医薬品の製造販売の承認申請に際し承認申請書に添付すべき資料の作成要 領について の一部改正について 新医薬品の製造販売の承認申請に際し承認申請書に添付すべき資料は 平成 26 年 11 月 21 日付け薬食発 1121 第 2 号厚生労働省医薬食品局長通知
薬生薬審発 0202 第 1 号 平成 29 年 2 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) 新医薬品の製造販売の承認申請に際し承認申請書に添付すべき資料の作成要 領について の一部改正について 新医薬品の製造販売の承認申請に際し承認申請書に添付すべき資料は 平成 26 年 11 月 21 日付け薬食発 1121 第 2 号厚生労働省医薬食品局長通知
(2) 健康成人の血漿中濃度 ( 反復経口投与 ) 9) 健康成人男子にスイニー 200mgを1 日 2 回 ( 朝夕食直前 ) 7 日間反復経口投与したとき 血漿中アナグリプチン濃度は投与 2 日目には定常状態に達した 投与 7 日目における C max 及びAUC 0-72hの累積係数はそれぞれ
 1. 血漿中濃度 (1) 健康成人の血漿中濃度 ( 単回経口投与 ) 8) 健康成人男子にスイニー 100mg 又は200mgを空腹時に単回経口投与したときの血漿中アナグリプチン濃度は 投与後約 1~ 2 時間で C maxに達した後 二相性の消失を示し t 1/2αは約 2 時間 t 1/2βは約 6 時間であった C max 及びAUC0- は投与量の増加に伴って増加した 血漿中アナグリプチン濃度推移
1. 血漿中濃度 (1) 健康成人の血漿中濃度 ( 単回経口投与 ) 8) 健康成人男子にスイニー 100mg 又は200mgを空腹時に単回経口投与したときの血漿中アナグリプチン濃度は 投与後約 1~ 2 時間で C maxに達した後 二相性の消失を示し t 1/2αは約 2 時間 t 1/2βは約 6 時間であった C max 及びAUC0- は投与量の増加に伴って増加した 血漿中アナグリプチン濃度推移
PowerPoint プレゼンテーション
 2015JSGT 臨床試験トレーニングコース 非臨床安全性試験 GLP 独立行政法人医薬品医療機器総合機構 (PMDA) 再生医療製品等審査部 角田聡 真木一茂 西村拓也 笛木修 1 2015JSGT 臨床試験トレーニングコース COI 開示 発表者名 : 角田聡 演題発表に関連し 開示すべき COI 関係にある企業等はありません 本発表は演者の個人的見解を示すものであり 所属する組織の公式な見解ではないことをご留意ください
2015JSGT 臨床試験トレーニングコース 非臨床安全性試験 GLP 独立行政法人医薬品医療機器総合機構 (PMDA) 再生医療製品等審査部 角田聡 真木一茂 西村拓也 笛木修 1 2015JSGT 臨床試験トレーニングコース COI 開示 発表者名 : 角田聡 演題発表に関連し 開示すべき COI 関係にある企業等はありません 本発表は演者の個人的見解を示すものであり 所属する組織の公式な見解ではないことをご留意ください
胚乳細胞中のタンパク質顆粒 I(PB-I) に改変型 Cry j 1タンパク質 及びCry j 2タンパク質を蓄積させたものです 2 スギ花粉ペプチド含有米( キタアケ ) スギ花粉が有する主要アレルゲンタンパク質 2 種 (Cry j 1 Cry j 2) の7 種類の主要 T 細胞エピトープを連
 別紙 1 平成 30 年 4 月 10 日 スギ花粉米 の外部機関への提供に関する応募要領 1. 趣旨国立研究開発法人農業 食品産業技術総合研究機構 ( 農研機構 ) は 遺伝子組換え (GM) イネにより 農研機構の隔離ほ場で生産した スギ花粉米 ( スギ花粉ポリペプチド含有米 及び スギ花粉ペプチド含有米 ) を活用した用途開発等の実用化を加速するため 一定の条件の下で これらの生物材料を民間企業や大学
別紙 1 平成 30 年 4 月 10 日 スギ花粉米 の外部機関への提供に関する応募要領 1. 趣旨国立研究開発法人農業 食品産業技術総合研究機構 ( 農研機構 ) は 遺伝子組換え (GM) イネにより 農研機構の隔離ほ場で生産した スギ花粉米 ( スギ花粉ポリペプチド含有米 及び スギ花粉ペプチド含有米 ) を活用した用途開発等の実用化を加速するため 一定の条件の下で これらの生物材料を民間企業や大学
ŁRŁ¸•ñŁŁŁ‘
 16 11 5 25mg 14 11 18 1 25mg 1 150,000 934 1 2 : 1-235-tumor necrosis factor receptor (human) fusion protein with 236-467-immunoglobulin G1 (human γ1-chain Fc fragment), dimmer : : 1 235 236 467 G 1 γ1
16 11 5 25mg 14 11 18 1 25mg 1 150,000 934 1 2 : 1-235-tumor necrosis factor receptor (human) fusion protein with 236-467-immunoglobulin G1 (human γ1-chain Fc fragment), dimmer : : 1 235 236 467 G 1 γ1
審査結果 平成 23 年 4 月 5 日 [ 販 売 名 ] ゴナールエフ皮下注用 150 [ 一 般 名 ] ホリトロピンアルファ ( 遺伝子組換え ) [ 申請者名 ] メルクセローノ株式会社 [ 申請年月日 ] 平成 22 年 7 月 21 日 [ 審査結果 ] 提出された資料から 本剤の視床
![審査結果 平成 23 年 4 月 5 日 [ 販 売 名 ] ゴナールエフ皮下注用 150 [ 一 般 名 ] ホリトロピンアルファ ( 遺伝子組換え ) [ 申請者名 ] メルクセローノ株式会社 [ 申請年月日 ] 平成 22 年 7 月 21 日 [ 審査結果 ] 提出された資料から 本剤の視床 審査結果 平成 23 年 4 月 5 日 [ 販 売 名 ] ゴナールエフ皮下注用 150 [ 一 般 名 ] ホリトロピンアルファ ( 遺伝子組換え ) [ 申請者名 ] メルクセローノ株式会社 [ 申請年月日 ] 平成 22 年 7 月 21 日 [ 審査結果 ] 提出された資料から 本剤の視床](/thumbs/92/108897527.jpg) 審査報告書 平成 23 年 4 月 5 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販 売 名 ] ゴナールエフ皮下注用 150 [ 一 般 名 ] ホリトロピンアルファ ( 遺伝子組換え ) [ 申請者名 ] メルクセローノ株式会社 [ 申請年月日 ] 平成 22 年 7 月 21 日 [ 剤形 含量
審査報告書 平成 23 年 4 月 5 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販 売 名 ] ゴナールエフ皮下注用 150 [ 一 般 名 ] ホリトロピンアルファ ( 遺伝子組換え ) [ 申請者名 ] メルクセローノ株式会社 [ 申請年月日 ] 平成 22 年 7 月 21 日 [ 剤形 含量
( 続紙 1 ) 京都大学 博士 ( 薬学 ) 氏名 大西正俊 論文題目 出血性脳障害におけるミクログリアおよびMAPキナーゼ経路の役割に関する研究 ( 論文内容の要旨 ) 脳内出血は 高血圧などの原因により脳血管が破綻し 脳実質へ出血した病態をいう 漏出する血液中の種々の因子の中でも 血液凝固に関
 Title 出血性脳障害におけるミクログリアおよびMAPキナーゼ経路の役割に関する研究 ( Abstract_ 要旨 ) Author(s) 大西, 正俊 Citation Kyoto University ( 京都大学 ) Issue Date 2010-03-23 URL http://hdl.handle.net/2433/120523 Right Type Thesis or Dissertation
Title 出血性脳障害におけるミクログリアおよびMAPキナーゼ経路の役割に関する研究 ( Abstract_ 要旨 ) Author(s) 大西, 正俊 Citation Kyoto University ( 京都大学 ) Issue Date 2010-03-23 URL http://hdl.handle.net/2433/120523 Right Type Thesis or Dissertation
3. 本ガイドラインの実施時期平成 23 年 1 月 1 日以降に申請される医薬品に添付される非臨床安全性試験に関する資料は 今回の改正をふまえたものであること ただし 平成 22 年 3 月 31 日までに実施され または開始されている試験については 当分の間 原則として本ガイドラインに基づいた試
 各都道府県衛生主管部 ( 局 ) 長殿 薬食審査発 0 2 1 9 第 4 号 平成 22 年 2 月 19 日 厚生労働省医薬食品局審査管理課長 医薬品の臨床試験及び製造販売承認申請のための非臨床安全性試験の実施 についてのガイダンス について 医薬品の製造販売承認申請に際して提出すべき資料の収集のために行われる非臨床安全性試験に関し その実施時期等については 平成 10 年 11 月 13 日医薬審第
各都道府県衛生主管部 ( 局 ) 長殿 薬食審査発 0 2 1 9 第 4 号 平成 22 年 2 月 19 日 厚生労働省医薬食品局審査管理課長 医薬品の臨床試験及び製造販売承認申請のための非臨床安全性試験の実施 についてのガイダンス について 医薬品の製造販売承認申請に際して提出すべき資料の収集のために行われる非臨床安全性試験に関し その実施時期等については 平成 10 年 11 月 13 日医薬審第
狂牛病調査第2巻1章,2章.doc
 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 2.1 A LD50/30mg () 10 ND 1 2.8 ND ND ND 11 ND 2.3 1.0 ND ND 11 ND ND 1.3 1.7 ND 13 ND
21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 2.1 A LD50/30mg () 10 ND 1 2.8 ND ND ND 11 ND 2.3 1.0 ND ND 11 ND ND 1.3 1.7 ND 13 ND
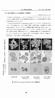 ,...~,.'~ 表 2.6.2.2-26 試験管内 PAE 菌株薬剤 MIC (µg/ml) PAE (h) 1 MIC 4 MIC STFX 0.025 0.92 2.35 S. aureus FDA 209-P LVFX 0.20 0.68 2.68 CPFX 0.20 1.05 1.59 SPFX 0.10 0.35 1.07 STFX 0.025 2.33 1.14 E. coli KL-16
,...~,.'~ 表 2.6.2.2-26 試験管内 PAE 菌株薬剤 MIC (µg/ml) PAE (h) 1 MIC 4 MIC STFX 0.025 0.92 2.35 S. aureus FDA 209-P LVFX 0.20 0.68 2.68 CPFX 0.20 1.05 1.59 SPFX 0.10 0.35 1.07 STFX 0.025 2.33 1.14 E. coli KL-16
2.5.4 有効性の概括評価トロンボモデュリンアルファの DIC に対する有効性の評価は 前期第 2 相臨床試験 ( 添付資料番号 : ) 後期第 2 相臨床試験 ( 添付資料番号 : ) 第 3 相臨床試験 ( 添付資料番号 : ) の 3 試験の成
 2.5.4 有効性の概括評価 2.5.4 有効性の概括評価トロンボモデュリンアルファの DIC に対する有効性の評価は 前期第 2 相臨床試験 ( 添付資料番号 :5.3.5.2-1) 後期第 2 相臨床試験 ( 添付資料番号 :5.3.5.1-1) 第 3 相臨床試験 ( 添付資料番号 :5.3.5.1-2) の 3 試験の成績に基づいて行った 3 試験の概略は表 2.5.4-1 に示した 表 2.5.4-1
2.5.4 有効性の概括評価 2.5.4 有効性の概括評価トロンボモデュリンアルファの DIC に対する有効性の評価は 前期第 2 相臨床試験 ( 添付資料番号 :5.3.5.2-1) 後期第 2 相臨床試験 ( 添付資料番号 :5.3.5.1-1) 第 3 相臨床試験 ( 添付資料番号 :5.3.5.1-2) の 3 試験の成績に基づいて行った 3 試験の概略は表 2.5.4-1 に示した 表 2.5.4-1
審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ]
![審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ] 審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ]](/thumbs/91/105024304.jpg) 審査報告書 平成 26 年 2 月 7 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所
審査報告書 平成 26 年 2 月 7 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所
<4D F736F F D2082A8926D82E782B995B68F E834E838D838A E3132>
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能 効果 用法 用量 使用上の注意 改訂のお知らせ 2013 年 12 月 東和薬品株式会社 このたび 平成 25 年 8 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 25 年 11 月 29 日付にて 下記の内容で承認されました また 使用上の注意 を改訂致しましたので 併せてお知らせ申し上げます
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能 効果 用法 用量 使用上の注意 改訂のお知らせ 2013 年 12 月 東和薬品株式会社 このたび 平成 25 年 8 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 25 年 11 月 29 日付にて 下記の内容で承認されました また 使用上の注意 を改訂致しましたので 併せてお知らせ申し上げます
<4D F736F F F696E74202D FA967B82CC96F28E9690A C982C282A282C42E >
 日本の薬事制度について 厚生労働省 医薬食品局審査管理課中西民二 本日の内容 医薬品の製造販売 外国製造業者の認定と GMP 適合性調査 外国製造業者の認定 承認審査における GMP 適合性調査 原薬等登録原簿 (MF) 医薬品の製造販売 医薬品の製造販売に関する規制 製造販売とは 製造等製造等 ( 他に委託して製造をする場合を含む ) をし 又は輸入をした医薬品 ( 原薬たる医薬品を除く ) を
日本の薬事制度について 厚生労働省 医薬食品局審査管理課中西民二 本日の内容 医薬品の製造販売 外国製造業者の認定と GMP 適合性調査 外国製造業者の認定 承認審査における GMP 適合性調査 原薬等登録原簿 (MF) 医薬品の製造販売 医薬品の製造販売に関する規制 製造販売とは 製造等製造等 ( 他に委託して製造をする場合を含む ) をし 又は輸入をした医薬品 ( 原薬たる医薬品を除く ) を
日本医薬品安全性学会 COI 開示 筆頭発表者 : 加藤祐太 演題発表に関連し 開示すべき COI 関連の企業などはありません
 医薬品副作用データベース (JADER) を用いた市販後の副作用発現状況の検討 加藤祐太 1)2) 岸達生 3) 高松昭司 2) 白石正 4) 1) 山形大学医学部医薬品医療機器評価学講座 2) 医薬品医療機器総合機構安全第二部 3) 医薬品医療機器総合機構信頼性保証部 4) 山形大学医学部附属病院薬剤部 日本医薬品安全性学会 COI 開示 筆頭発表者 : 加藤祐太 演題発表に関連し 開示すべき COI
医薬品副作用データベース (JADER) を用いた市販後の副作用発現状況の検討 加藤祐太 1)2) 岸達生 3) 高松昭司 2) 白石正 4) 1) 山形大学医学部医薬品医療機器評価学講座 2) 医薬品医療機器総合機構安全第二部 3) 医薬品医療機器総合機構信頼性保証部 4) 山形大学医学部附属病院薬剤部 日本医薬品安全性学会 COI 開示 筆頭発表者 : 加藤祐太 演題発表に関連し 開示すべき COI
スライド 1
 3 年次後期専門科目群 Ⅰ ( 必修科目 ) 2 単位 臨床薬理学 5 回目 生物薬剤学講座児玉庸夫 1 臨床薬理学は薬物治療学を支える 基礎として機能する 薬物治療学 臨床薬理学 治療薬や用量などの薬物治療の個別化 臨床薬物動態学 例えば TDM や薬物相互作用 医療薬学 例えば 調剤 製剤 服薬指導 在宅医療における訪問薬剤管理指導 2 臨薬 臨床薬理学は医薬品開発や臨床薬効評価などを行う学問である
3 年次後期専門科目群 Ⅰ ( 必修科目 ) 2 単位 臨床薬理学 5 回目 生物薬剤学講座児玉庸夫 1 臨床薬理学は薬物治療学を支える 基礎として機能する 薬物治療学 臨床薬理学 治療薬や用量などの薬物治療の個別化 臨床薬物動態学 例えば TDM や薬物相互作用 医療薬学 例えば 調剤 製剤 服薬指導 在宅医療における訪問薬剤管理指導 2 臨薬 臨床薬理学は医薬品開発や臨床薬効評価などを行う学問である
販売名 製造販売業者 レフィキシア静注用 500/1000/2000 に係る医薬品リスク管理計画書 (RMP) の概要 レフィキシア静注用 500/1000/2000 ノボノルディスクファーマ株式会社提出年月 ( 別紙様式 ) 有効成分ノナコグベータペゴル ( 遺伝子組換え ) 薬効分類 6343
 レフィキシア静注用 500/1000/2000 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はノボノルディスクファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ノボノルディスクファーマ株式会社 販売名 製造販売業者 レフィキシア静注用 500/1000/2000 に係る医薬品リスク管理計画書 (RMP) の概要 レフィキシア静注用
レフィキシア静注用 500/1000/2000 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はノボノルディスクファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ノボノルディスクファーマ株式会社 販売名 製造販売業者 レフィキシア静注用 500/1000/2000 に係る医薬品リスク管理計画書 (RMP) の概要 レフィキシア静注用
1. 今回の変更に関する整理 効能 効果及び用法 用量 ( 添付文書より転載 ) 従来製剤 ( バイアル製剤 ) と製法変更製剤 ( シリンジ製剤 ) で変更はない 効能 効果 用法 容量 B 型肝炎の予防通常 0.5mL ずつ4 週間隔で2 回 更に 20~24 週を経過した後に1 回 0.5mL
 資料 6 MSD 社の製造する B 型肝炎単抗原ワクチンについて 経緯 1986 年米国メルク社製 B 型肝炎ワクチン ( 酵母由来 ) が米国で承認 1988 年 MSD 社製 B 型肝炎ワクチン ( 酵母由来 ) が日本で承認 2000 年欧州で HEXAVAC( ジフテリア 破傷風 百日咳 B 型肝炎 不活化ポリオ Hib 感染症を予防する 6 種混合ワクチン ) 承認 2001 年欧州で HEXAVAC
資料 6 MSD 社の製造する B 型肝炎単抗原ワクチンについて 経緯 1986 年米国メルク社製 B 型肝炎ワクチン ( 酵母由来 ) が米国で承認 1988 年 MSD 社製 B 型肝炎ワクチン ( 酵母由来 ) が日本で承認 2000 年欧州で HEXAVAC( ジフテリア 破傷風 百日咳 B 型肝炎 不活化ポリオ Hib 感染症を予防する 6 種混合ワクチン ) 承認 2001 年欧州で HEXAVAC
薬食発第 号平成 21 年 3 月 4 日 各都道府県知事殿 厚生労働省医薬食品局長 バイオ後続品の承認申請について 医薬品の製造販売の承認申請の取扱いについては 平成 17 年 3 月 31 日付け薬食発第 号医薬食品局長通知 医薬品の承認申請について ( 以下 局
 薬食発第 0304004 号平成 21 年 3 月 4 日 各都道府県知事殿 厚生労働省医薬食品局長 バイオ後続品の承認申請について 医薬品の製造販売の承認申請の取扱いについては 平成 17 年 3 月 31 日付け薬食発第 0331015 号医薬食品局長通知 医薬品の承認申請について ( 以下 局長通知 という ) により取り扱ってきたところであるが 今般 バイオ後続品の承認申請書に添付すべき資料の範囲に関して
薬食発第 0304004 号平成 21 年 3 月 4 日 各都道府県知事殿 厚生労働省医薬食品局長 バイオ後続品の承認申請について 医薬品の製造販売の承認申請の取扱いについては 平成 17 年 3 月 31 日付け薬食発第 0331015 号医薬食品局長通知 医薬品の承認申請について ( 以下 局長通知 という ) により取り扱ってきたところであるが 今般 バイオ後続品の承認申請書に添付すべき資料の範囲に関して
菌種 報告年 株数 MIC(μg/mL) Range MIC50 MIC > ( 幾何平均 ) C.tropicalis >
 生物学的同等性試験におけるイトリゾール カプセル 50 のロット間での統計学 的有意差が本剤の有効性及び安全性に与える影響について イトリゾール カプセル 50 は,1993 年に内臓真菌症 ( 深在性真菌症 ), 深在性皮膚真菌症及び表在性皮膚真菌症を適応症として承認され, その後,1999 年に爪白癬等の適応を追加,2004 年及び 2006 年にはそれぞれ爪白癬のパルス療法および注射剤からの切り替えとしての新用法
生物学的同等性試験におけるイトリゾール カプセル 50 のロット間での統計学 的有意差が本剤の有効性及び安全性に与える影響について イトリゾール カプセル 50 は,1993 年に内臓真菌症 ( 深在性真菌症 ), 深在性皮膚真菌症及び表在性皮膚真菌症を適応症として承認され, その後,1999 年に爪白癬等の適応を追加,2004 年及び 2006 年にはそれぞれ爪白癬のパルス療法および注射剤からの切り替えとしての新用法
1. Caov-3 細胞株 A2780 細胞株においてシスプラチン単剤 シスプラチンとトポテカン併用添加での殺細胞効果を MTS assay を用い検討した 2. Caov-3 細胞株においてシスプラチンによって誘導される Akt の活性化に対し トポテカンが影響するか否かを調べるために シスプラチ
 ( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 朝日通雄 恒遠啓示 副査副査 瀧内比呂也谷川允彦 副査 勝岡洋治 主論文題名 Topotecan as a molecular targeting agent which blocks the Akt and VEGF cascade in platinum-resistant ovarian cancers ( 白金製剤耐性卵巣癌における
( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 朝日通雄 恒遠啓示 副査副査 瀧内比呂也谷川允彦 副査 勝岡洋治 主論文題名 Topotecan as a molecular targeting agent which blocks the Akt and VEGF cascade in platinum-resistant ovarian cancers ( 白金製剤耐性卵巣癌における
PowerPoint プレゼンテーション
 多能性幹細胞を利用した毒性の判定方法 教授 森田隆 准教授 吉田佳世 ( 大阪市立大学大学院医学研究科遺伝子制御学 ) これまでの問題点 化学物質の人体および環境に及ぼす影響については 迅速にその評価を行うことが社会的に要請されている 一方 マウスやラットなど動物を用いた実験は必要ではあるが 動物愛護や費用 時間的な問題がある そこで 哺乳動物細胞を用いたリスク評価系の開発が望まれる 我々は DNA
多能性幹細胞を利用した毒性の判定方法 教授 森田隆 准教授 吉田佳世 ( 大阪市立大学大学院医学研究科遺伝子制御学 ) これまでの問題点 化学物質の人体および環境に及ぼす影響については 迅速にその評価を行うことが社会的に要請されている 一方 マウスやラットなど動物を用いた実験は必要ではあるが 動物愛護や費用 時間的な問題がある そこで 哺乳動物細胞を用いたリスク評価系の開発が望まれる 我々は DNA
ルグリセロールと脂肪酸に分解され吸収される それらは腸上皮細胞に吸収されたのちに再び中性脂肪へと生合成されカイロミクロンとなる DGAT1 は腸管で脂質の再合成 吸収に関与していることから DGAT1 KO マウスで認められているフェノタイプが腸 DGAT1 欠如に由来していることが考えられる 実際
 学位論文の内容の要旨 論文提出者氏名 津田直人 論文審査担当者 主査下門顕太郎副査吉田雅幸横関博雄 論文題目 Intestine-Targeted DGAT1 Inhibition Improves Obesity and Insulin Resistance without Skin Aberrations in Mice ( 論文内容の要旨 ) < 要旨 > Diacylglycerol O-acyltransferase
学位論文の内容の要旨 論文提出者氏名 津田直人 論文審査担当者 主査下門顕太郎副査吉田雅幸横関博雄 論文題目 Intestine-Targeted DGAT1 Inhibition Improves Obesity and Insulin Resistance without Skin Aberrations in Mice ( 論文内容の要旨 ) < 要旨 > Diacylglycerol O-acyltransferase
目次 ( 用語の定義 ) 背景 ガイドラインの対象 がん治療用ウイルスの選択 初期段階での確認事項 ウイルス選択の理由 腫瘍選択性 ウイルスの分子変異の確認 規格 製造
 実践に基づくウイルス療法開発のガイドライン策定と人材育成 がん治療用ウイルス製造及び非臨床試験に関するガイドライン 総論編 ドラフト 東京大学医科学研究所 1 目次 ( 用語の定義 )... 5 1 背景 ガイドラインの対象... 6 1.1 がん治療用ウイルスの選択 初期段階での確認事項... 7 1.1.1 ウイルス選択の理由... 7 1.1.2 腫瘍選択性.....7 1.1.3 ウイルスの分子変異の確認...
実践に基づくウイルス療法開発のガイドライン策定と人材育成 がん治療用ウイルス製造及び非臨床試験に関するガイドライン 総論編 ドラフト 東京大学医科学研究所 1 目次 ( 用語の定義 )... 5 1 背景 ガイドラインの対象... 6 1.1 がん治療用ウイルスの選択 初期段階での確認事項... 7 1.1.1 ウイルス選択の理由... 7 1.1.2 腫瘍選択性.....7 1.1.3 ウイルスの分子変異の確認...
Microsoft Word - sa_niflec_ doc
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能又は効果 用法及び用量 使用上の注意改訂のお知らせ 経口腸管洗浄剤 発売 2009 年 4 月 製造販売 この度 経口腸管洗浄剤ニフレック 内用において 効能又は効果 用法及び用量 の追加承認を取得したことに伴い 添付文書を以下のとおり改訂致しましたのでご案内申し上げます 今後のご使用につきましては 下記内容をご参照下さいますようお願い申し上げます
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能又は効果 用法及び用量 使用上の注意改訂のお知らせ 経口腸管洗浄剤 発売 2009 年 4 月 製造販売 この度 経口腸管洗浄剤ニフレック 内用において 効能又は効果 用法及び用量 の追加承認を取得したことに伴い 添付文書を以下のとおり改訂致しましたのでご案内申し上げます 今後のご使用につきましては 下記内容をご参照下さいますようお願い申し上げます
DRAFT#9 2011
 報道関係各位 2019 年 3 月 25 日 ユーシービージャパン株式会社 第一三共株式会社 抗てんかん剤 ビムパット 点滴静注 200mg 新発売のお知らせ ユーシービージャパン株式会社 ( 本社 : 東京都新宿区 代表取締役社長 : 菊池加奈子 以下 ユーシービージャパン ユーシービーグループを総称して以下 ユーシービー ) と第一三共株式会社 ( 本社 : 東京都中央区 代表取締役社長 : 眞鍋淳
報道関係各位 2019 年 3 月 25 日 ユーシービージャパン株式会社 第一三共株式会社 抗てんかん剤 ビムパット 点滴静注 200mg 新発売のお知らせ ユーシービージャパン株式会社 ( 本社 : 東京都新宿区 代表取締役社長 : 菊池加奈子 以下 ユーシービージャパン ユーシービーグループを総称して以下 ユーシービー ) と第一三共株式会社 ( 本社 : 東京都中央区 代表取締役社長 : 眞鍋淳
ハイゼントラ20%皮下注1g/5mL・2g/10mL・4g/20mL
 CSL19-158 医薬品の適正使用に欠かせない情報です 必ずお読みください 効能又は効果 用法及び用量 使用上の注意改訂のお知らせ 2019 年 3 月血漿分画製剤 ( 皮下注用人免疫グロブリン製剤 ) この度 標記製品の製造販売承認事項の一部変更が承認されました それに伴い 効能又は効果 用法及び用量 及び 使用上の注意 等を改訂いたしましたので お知らせいたします 改訂添付文書を封入した製品がお手元に届くまでには若干の日時を要しますので
CSL19-158 医薬品の適正使用に欠かせない情報です 必ずお読みください 効能又は効果 用法及び用量 使用上の注意改訂のお知らせ 2019 年 3 月血漿分画製剤 ( 皮下注用人免疫グロブリン製剤 ) この度 標記製品の製造販売承認事項の一部変更が承認されました それに伴い 効能又は効果 用法及び用量 及び 使用上の注意 等を改訂いたしましたので お知らせいたします 改訂添付文書を封入した製品がお手元に届くまでには若干の日時を要しますので
テイカ製薬株式会社 社内資料
 テイカ製薬株式会社社内資料 アレルギー性結膜炎治療剤トラニラスト点眼液.5% TS TRANILAST Ophthalmic Solution.5% TS 生物学的同等性に関する資料 発売元 : 興和株式会社 製造販売元 : テイカ製薬株式会社 9 年 月作成 TSTR5BE9 ラット及びモルモットアレルギー性結膜炎モデルにおける生物学的同等性試験 Ⅰ. 試験の目的トラニラスト点眼液.5% TS および標準製剤の生物学的同等性をラット受動感作アレルギー性結膜炎モデル及びモルモット能動感作アレルギー性結膜炎モデルを用い薬力学的に検討した
テイカ製薬株式会社社内資料 アレルギー性結膜炎治療剤トラニラスト点眼液.5% TS TRANILAST Ophthalmic Solution.5% TS 生物学的同等性に関する資料 発売元 : 興和株式会社 製造販売元 : テイカ製薬株式会社 9 年 月作成 TSTR5BE9 ラット及びモルモットアレルギー性結膜炎モデルにおける生物学的同等性試験 Ⅰ. 試験の目的トラニラスト点眼液.5% TS および標準製剤の生物学的同等性をラット受動感作アレルギー性結膜炎モデル及びモルモット能動感作アレルギー性結膜炎モデルを用い薬力学的に検討した
日本化学療法学会雑誌第57巻第1号
 In vitro Streptococcus pneumoniae Escherichia coli in vitro Streptococcus pneumoniae Escherichia coli µs. pneumoniae E. coli µ Key words in vitrostreptococcus pneumoniae Escherichia coli Escherichia coli
In vitro Streptococcus pneumoniae Escherichia coli in vitro Streptococcus pneumoniae Escherichia coli µs. pneumoniae E. coli µ Key words in vitrostreptococcus pneumoniae Escherichia coli Escherichia coli
ごあいさつ バイオシミラーの課題 バイオ医薬品は 20 世紀後半に開発されて以来 癌や血液疾患 自己免疫疾患等多くの難治性疾患に卓抜した治療効果を示し また一般にベネフィット リスク評価が高いと言われています しかしその一方で しばしば高額となる薬剤費用が 患者の経済的負担や社会保障費の増大に繋がる
 ごあいさつ バイオシミラーの課題 バイオ医薬品は 20 世紀後半に開発されて以来 癌や血液疾患 自己免疫疾患等多くの難治性疾患に卓抜した治療効果を示し また一般にベネフィット リスク評価が高いと言われています しかしその一方で しばしば高額となる薬剤費用が 患者の経済的負担や社会保障費の増大に繋がると指摘されています こうした中 バイオシミラーの普及は 拡大する医療費の抑制に貢献するとともに 経済的な理由でバイオ医薬品による治療を躊躇されている患者に対する治療アクセスの改善を約束します
ごあいさつ バイオシミラーの課題 バイオ医薬品は 20 世紀後半に開発されて以来 癌や血液疾患 自己免疫疾患等多くの難治性疾患に卓抜した治療効果を示し また一般にベネフィット リスク評価が高いと言われています しかしその一方で しばしば高額となる薬剤費用が 患者の経済的負担や社会保障費の増大に繋がると指摘されています こうした中 バイオシミラーの普及は 拡大する医療費の抑制に貢献するとともに 経済的な理由でバイオ医薬品による治療を躊躇されている患者に対する治療アクセスの改善を約束します
23103.indd
 平成 6 年 3 月 輸血用血液製剤の添付文書改訂及び製剤ラベル変更のお知らせ 謹啓時下ますますご清栄のこととお慶び申し上げます 平素より日本赤十字社の血液事業に格別のご高配を賜り厚く御礼申し上げます このたび 日本赤十字社では 平成 5 年 9 月 日付厚生労働省告示第 94 号による生物学的製剤基準の一部改正に基づき 輸血用血液製剤の添付文書の改訂及び製剤ラベルの変更を行うことといたしました また
平成 6 年 3 月 輸血用血液製剤の添付文書改訂及び製剤ラベル変更のお知らせ 謹啓時下ますますご清栄のこととお慶び申し上げます 平素より日本赤十字社の血液事業に格別のご高配を賜り厚く御礼申し上げます このたび 日本赤十字社では 平成 5 年 9 月 日付厚生労働省告示第 94 号による生物学的製剤基準の一部改正に基づき 輸血用血液製剤の添付文書の改訂及び製剤ラベルの変更を行うことといたしました また
検査項目情報 1171 一次サンプル採取マニュアル 4. 内分泌学的検査 >> 4F. 性腺 胎盤ホルモンおよび結合蛋白 >> 4F090. トータル HCG-β ( インタクト HCG+ フリー HCG-β サブユニット ) トータル HCG-β ( インタクト HCG+ フリー HCG-β サブ
 chorionic gonadotropin 連絡先 : 3483 基本情報 4F090 HCGβサブユニット (β-hcg) 分析物 JLAC10 診療報酬 識別 材料 023 血清 測定法 結果識別 第 2 章 特掲診療料 D008 第 3 部 検査 第 1 節 検体検査料 第 1 款 検体検査実施料 ( 生化学的検査 (Ⅱ) ) 18 ヒト絨毛性ゴナドトロピン -β サブユニット (HCG-β)
chorionic gonadotropin 連絡先 : 3483 基本情報 4F090 HCGβサブユニット (β-hcg) 分析物 JLAC10 診療報酬 識別 材料 023 血清 測定法 結果識別 第 2 章 特掲診療料 D008 第 3 部 検査 第 1 節 検体検査料 第 1 款 検体検査実施料 ( 生化学的検査 (Ⅱ) ) 18 ヒト絨毛性ゴナドトロピン -β サブユニット (HCG-β)
< 別紙 1: 検査値等略称 > 略称 名称 A/G 比 アルブミン / グロブリン比 ADI 一日摂取許容量 ALT アラニンアミノトランスフェラーゼ ATPase adenosine triphosphatase アデノシントリフォスファターゼ AUC 血中薬物濃度 時間曲線下面積 Cmax E
 < 別紙 1: 検査値等略称 > 略称 名称 A/G 比 アルブミン / グロブリン比 ADI 一日摂取許容量 ALT アラニンアミノトランスフェラーゼ ATPase adenosine triphosphatase アデノシントリフォスファターゼ AUC 血中薬物濃度 時間曲線下面積 Cmax ECL ELISA EMEA FPIA GC/MS Glu 最高濃度 Enterochromaffin-like
< 別紙 1: 検査値等略称 > 略称 名称 A/G 比 アルブミン / グロブリン比 ADI 一日摂取許容量 ALT アラニンアミノトランスフェラーゼ ATPase adenosine triphosphatase アデノシントリフォスファターゼ AUC 血中薬物濃度 時間曲線下面積 Cmax ECL ELISA EMEA FPIA GC/MS Glu 最高濃度 Enterochromaffin-like
検査項目情報 LDH アイソザイム ( 乳酸脱水素酵素アイソザイム ) Department of Clinical Laboratory, Kyoto University Hospital 一次サンプル採取マニュアル 生化学的検査 >> 3B. 酵素および関連物質 >> 3B05
 lactate dehydrogenase isoenzymes 連絡先 : 3764 基本情報 ( 標準コード (JLAC10) ) 基本情報 ( 診療報酬 ) 標準コード (JLAC10) 診療報酬 3B055 LDHアイソザイム ( 乳酸脱水素酵素アイソザイム ) 特掲診療料 >> 検査 >> 検体検査料 >> 検体検査実施料 >> ( 生化学的検査 (Ⅰ)) 分析物 D007 15 LDアイソザイム
lactate dehydrogenase isoenzymes 連絡先 : 3764 基本情報 ( 標準コード (JLAC10) ) 基本情報 ( 診療報酬 ) 標準コード (JLAC10) 診療報酬 3B055 LDHアイソザイム ( 乳酸脱水素酵素アイソザイム ) 特掲診療料 >> 検査 >> 検体検査料 >> 検体検査実施料 >> ( 生化学的検査 (Ⅰ)) 分析物 D007 15 LDアイソザイム
検査項目情報 トータルHCG-β ( インタクトHCG+ フリー HCG-βサブユニット ) ( 緊急検査室 ) chorionic gonadotropin 連絡先 : 基本情報 ( 標準コード (JLAC10) ) 基本情報 ( 診療報酬 ) 標準コード (JLAC10)
 chorionic gonadotropin 連絡先 : 3479 2-2908 基本情報 ( 標準コード (JLAC10) ) 基本情報 ( 診療報酬 ) 標準コード (JLAC10) 診療報酬 分析物 9186 4. 内分泌学的検査 >> 4F. 性腺 胎盤ホルモンおよび結合蛋白 >> 4F090. Ver.2 4F090 HCGβ サブユニット (β-hcg) 特掲診療料 >> 検査 >> 検体検査料
chorionic gonadotropin 連絡先 : 3479 2-2908 基本情報 ( 標準コード (JLAC10) ) 基本情報 ( 診療報酬 ) 標準コード (JLAC10) 診療報酬 分析物 9186 4. 内分泌学的検査 >> 4F. 性腺 胎盤ホルモンおよび結合蛋白 >> 4F090. Ver.2 4F090 HCGβ サブユニット (β-hcg) 特掲診療料 >> 検査 >> 検体検査料
ICHシンポジウム2013 E14
 ICH 日本シンポジウム 2013 E14 IWG: 非抗不整脈薬における QT/QTc 間隔の延長と催不整脈作用の潜在的可能性に関する臨床的評価 医薬品医療機器総合機構 安藤友紀 本日の内容 これまでの経緯 新たに合意に至った Q&A 今後の活動について 2013/12/10 ICH 日本シンポジウム2013 2 これまでの経緯 (1) 2005 年 5 月 ICH Brussels にて Step4
ICH 日本シンポジウム 2013 E14 IWG: 非抗不整脈薬における QT/QTc 間隔の延長と催不整脈作用の潜在的可能性に関する臨床的評価 医薬品医療機器総合機構 安藤友紀 本日の内容 これまでの経緯 新たに合意に至った Q&A 今後の活動について 2013/12/10 ICH 日本シンポジウム2013 2 これまでの経緯 (1) 2005 年 5 月 ICH Brussels にて Step4
鑑-H リンゼス錠他 留意事項通知の一部改正等について
 日医発第 617 号 ( 保 154) 平成 30 年 8 月 29 日 都道府県医師会長殿 日本医師会長横倉義武 医薬品医療機器等法上の効能 効果等の変更に伴う留意事項の一部改正等について 平成 30 年 8 月 21 日付け保医発 0821 第 1 号厚生労働省保険局医療課長通知により 添付資料の通り保険適用上の取扱いに関する留意事項が一部改正されましたのでお知らせ申し上げます 今回の改正は 同日付けで添付資料の医薬品の効能
日医発第 617 号 ( 保 154) 平成 30 年 8 月 29 日 都道府県医師会長殿 日本医師会長横倉義武 医薬品医療機器等法上の効能 効果等の変更に伴う留意事項の一部改正等について 平成 30 年 8 月 21 日付け保医発 0821 第 1 号厚生労働省保険局医療課長通知により 添付資料の通り保険適用上の取扱いに関する留意事項が一部改正されましたのでお知らせ申し上げます 今回の改正は 同日付けで添付資料の医薬品の効能
の状態により適宜減量する 成人 A 法 : 他の抗悪性腫瘍剤との併用において ブスルファンとして 1 回 0.8 mg/kg を生理食塩液又は 5% ブドウ糖液に混和 調製して 2 時間かけて点滴静注する 本剤は 6 時間毎に 1 日 4 回 4 日間投与する なお 年齢 患者の状態により適宜減量す
 審査報告書 平成 30 年 8 月 2 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販売名 ] ブスルフェクス点滴静注用 60 mg [ 一般名 ] ブスルファン [ 申請者 ] 大塚製薬株式会社 [ 申請年月日 ] 平成 30 年 5 月 28 日 [ 剤形 含量 ] 1 バイアル (10 ml)
審査報告書 平成 30 年 8 月 2 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販売名 ] ブスルフェクス点滴静注用 60 mg [ 一般名 ] ブスルファン [ 申請者 ] 大塚製薬株式会社 [ 申請年月日 ] 平成 30 年 5 月 28 日 [ 剤形 含量 ] 1 バイアル (10 ml)
ルリコナゾールルコナック爪外用液 5% CTD 第 2 部 ( モジュール2): CTDの概要 ( サマリー ) 2.4 非臨床試験の概括評価 佐藤製薬株式会社
 ルコナック爪外用液 5% CTD 第 2 部 ( モジュール2): CTDの概要 ( サマリー ) 佐藤製薬株式会社 略号一覧表 略号 英語 日本語 AUC area under the plasma concentration-time curve 血漿中濃度 - 時間曲線下面積 C. albicans Candida albicans - DMBA 7,12-dimethylbenz[a]anthracene
ルコナック爪外用液 5% CTD 第 2 部 ( モジュール2): CTDの概要 ( サマリー ) 佐藤製薬株式会社 略号一覧表 略号 英語 日本語 AUC area under the plasma concentration-time curve 血漿中濃度 - 時間曲線下面積 C. albicans Candida albicans - DMBA 7,12-dimethylbenz[a]anthracene
新規 P2X4 受容体アンタゴニスト NCP-916 の鎮痛作用と薬物動態に関する検討 ( 分野名 : ライフイノベーション分野 ) ( 学籍番号 )3PS1333S ( 氏名 ) 小川亨 序論 神経障害性疼痛とは, 体性感覚神経系の損傷や疾患によって引き起こされる痛みと定義され, 自発痛やアロディ
 九州大学学術情報リポジトリ Kyushu University Institutional Repository 新規 P2X4 受容体アンタゴニスト NCP-916 の鎮痛作用と薬物動態に関する検討 小川, 亨 http://hdl.handle.net/2324/178378 出版情報 : 九州大学, 216, 博士 ( 創薬科学 ), 課程博士バージョン : 権利関係 : やむを得ない事由により本文ファイル非公開
九州大学学術情報リポジトリ Kyushu University Institutional Repository 新規 P2X4 受容体アンタゴニスト NCP-916 の鎮痛作用と薬物動態に関する検討 小川, 亨 http://hdl.handle.net/2324/178378 出版情報 : 九州大学, 216, 博士 ( 創薬科学 ), 課程博士バージョン : 権利関係 : やむを得ない事由により本文ファイル非公開
