FdData理科3年
|
|
|
- きよたつ こやぎ
- 5 years ago
- Views:
Transcription
1 FdData 中間期末 : 中学理科 3 年 [ 酸 アルカリとイオン ] [ 問題 ](1 学期期末 ) 次の各問いに答えよ (1) 塩酸の中に含まれている 酸 に共通するイオンは何か 1 イオンの名称を答えよ 2 また, このイオンの記号を書け (2) 水酸化ナトリウム水溶液の中に含まれている アルカリ に共通するイオンは何か 1 イオンの名称を答えよ 2 また, このイオンの記号を答えよ [ 解答 ](1)1 水素イオン 2 H + (2)1 水酸化物イオン 2 OH - [ 解説 ]
2 あえん 青色リトマスを赤色に変える, 亜鉛などの金 属をいれると水素が発生する など酸に共通の性質は何が原因なのか また, そもそも酸とは何なえんさんりゅうさんのか 代表的な酸としては, 塩酸 (HCl), 硫酸しょうさんたんさん (H2SO4), 硝酸 (HNO3), 炭酸 (H2CO3) があるが, これらの化学式を見てみると, 共通して水素原子 (H) が含まれていることに気づくはずである 酸はでんかいしつすべて電解質で, 水溶液中では, それぞれ次のよでんりうに電離している 塩酸 :HCl H + +Cl - 硫酸 :H2SO4 2H + +SO4 2 - 硝酸 :HNO3 H + +NO3 - 炭酸 :H2CO3 2H + +CO3 2 - 電離したときに, どの酸でも水素イオン (H + ) が生じるが, この H + こそ酸の正体なのである 青色リトマスを赤色に変える などの酸の性質はH + のはたらきによるものである そして, 酸とは, 水にとかしたとき電離して水素イオン (H + ) を生じる化合物である ということができる では, アルカリはどうか 代表的なアルカリとしすいさんかては, 水酸化ナトリウム水溶液 (NaOH), アンモニア水 (NH3) があるが, 水溶液中では, 次のよう
3 に電離している 水酸化ナトリウム水溶液 :NaOH Na + +OH - アンモニア水 :NH3+H2O NH4 + +OH - 電離したときに, どのアルカリでもOH - ( すいさんかぶつ水酸化物イオン ) が生じるが, このOH - こそアルカリの性質をもたらすものなのである アルカリとは, 水にとかしたとき電離して水酸化物イオン (OH - ) を生じる化合物である ということができる [ 問題 ](1 学期期末 ) 硫酸が水溶液中でイオンに分かれているようすを式で表せ [ 解答 ]H2SO4 2H + +SO4 2- [ 問題 ]( 前期期末 ) アンモニアは水に溶けると水と反応してアルカリ性を示す このときの電離式を化学式とイオン式で表せ [ 解答 ]NH3+H2O NH4 + +OH -
4 [ 問題 ](1 学期中間 ) 図 1,2 のような装置をつくり, 電圧を加えて寒天の色の変化を観察した 次の各問いに答えよ ただし, 電圧を加える前の BTB 溶液の色は中性を示す色である (1) 中性を示す BTB 溶液の色は何色か (2) 図 1 で電圧を加えたときの変化の様子を図 3 のア ~ エから選び, 記号で答えよ (3) (2) のように変化した理由を変化に関係したイオン名を用いて答えよ
5 (4) 図 2 で電圧を加えたときの変化の様子を図 3 のア ~ エから選び, 記号で答えよ (5) (4) のように変化した理由を変化に関係したイオン名を用いて答えよ [ 解答 ](1) 緑色 (2) ア (3) + の電気を帯びた水素イオンが陰極に引かれて移動したから (4) エ (5) - の電気を帯びた水酸化物イオンが陽極に引かれて移動したから [ 解説 ]
6 えんさん (1)~(3) うすい塩酸をしみこませたろ紙の部分では, 塩酸がHCl H + +Cl - でんりのように電離している 電気の+と-は引き合うので, H + いんきょく ( 水素イオン ) は陰極 (- 極 ) に引かれて左側へ 移動する BTB 溶液は酸性では黄色に変化するが, それは H + ( 水素イオン ) のはたらきによるもので ある したがって, 実験の BTB 溶液が入った寒天 えんかぶつ - の左側の部分が黄色に変化していく Cl ( 塩化物 イオン ) は陽極 (+ 極 ) に引かれて右側に移動するが, Cl - はBTB 溶液の色を変化させることはない すいさんか (4)(5) うすい水酸化ナトリウム水溶液をしみこま せたろ紙の部分では, 水酸化ナトリウムが, NaOH Na + +OH - のように電離している OH ようきょく - ( 水酸化物イオン ) は陽極 (+ 極 ) に引かれて右側 に移動する BTB 溶液はアルカリ性では青色に変 化するが, それは OH - ( 水酸化物イオン ) のはたら きによるものである したがって, 実験の BTB 溶 液が入った寒天の右側の部分が青色に変化してい + く Na ( ナトリウムイオン ) は陰極 (- 極 ) に引かれ + て左側に移動するが,Na はBTB 溶液の色を変化 させることはない
7 [ 問題 ](1 学期期末 ) ストローに寒天溶液 (BTB 溶液を入れて緑色にしたもの ) を入れ, ストローの中心に切り込みを入れてそこに塩酸をしみこませたろ紙をはさんだ ストローの両側から炭素棒を入れて電源装置とつないで電圧を加えた 10 分後に変化が起こった どちらの極でどんな変化が起こったか 理由も書いて説明せよ [ 解答 ] 水素イオンが陰極の方向に移動したため, 陰極側の寒天溶液が黄色になった
8 [ 問題 ](2 学期中間 ) 図のように食塩水をしみこませたろ紙と青色リトマス紙を置き, 中心にうすい塩酸をつけて電圧をかけた (1) 青色リトマス紙に塩酸をつけた部分はどのような色になるか (2) 電圧をかけると,(1) の部分は陽極, 陰極のどちらに向かって移動するか (3) 水溶液中で電圧をかけると (2) の極の方に移動するのは陽イオン, 陰イオンのどちらか (4) 酸とは水に溶けて何というイオンを生じる物質か イオン記号で答えよ (5) アルカリとは水に溶けて何というイオンを生じる物質か イオン記号で答えよ
9 [ 解答 ](1) 赤色 (2) 陰極 (3) 陽イオン (4) H + (5) OH - [ 解説 ] 酸は青色リトマスを赤色に変えるが, それは酸の中の水素イオン (H + ) の働きによるものである 塩酸は, HCl H + +Cl - のように電離しているが, 電圧をかけると,H + ( 水素イオン / 陽イオン ) は陰極 (- 極 ) に引かれて左側に移動する これにともなって, 青色リトマス紙の中央より左側の部分が H + によって赤色に変化していく なお,Cl - ( 塩化物イオン ) は陽極 (+ 極 ) に引かれて右側へ移動するが,Cl - はリトマス紙の色の変化をもたらすことはない
10 [ 問題 ](1 学期期末 ) 図のような装置をつくり, リトマス紙の中央に塩酸をしみこませたろ紙を置き, 電圧をかけた (1) 塩酸は何という物質の水溶液か (2) 塩酸にふくまれているイオンを, イオン式を用いてすべて示せ (3) リトマス紙の色が変わるのはア ~ エのどれか (4) (3) でリトマス紙の色を変えたイオンは +,- のどちらの電気を帯びているか (5) 塩酸のかわりに水酸化ナトリウム水溶液をしみこませたろ紙を置き, 電圧をかけると, リトマス紙の色が変わるのはア ~ エのどれか (6) (5) で, リトマス紙の色を変えるはたらきをしたイオンは何イオンか その名称とイオン式を答えよ
11 [ 解答 ](1) 塩化水素 (2) H +,Cl - (3) エ (4) + (5) ア (6) 水酸化物イオン,OH - [ 解説 ] えんさんさんせいすいようえき塩酸のような酸性の水溶液は, 青色のリトマス紙を赤色に変える これはH + ( 水素イオン ) のはたらきによるものである H + は+の電気を帯びているいんきょくため, 水溶液に電圧を加えると陰極 (- 極 ) 側に移動する H + つうかが青色リトマスを通過するとき, 青色リトマスが赤色に変化するので, 図のエのリトマス紙が変化する
12 すいさんか次に, 水酸化ナトリウム水溶液を使った場合を考える アルカリの水溶液は赤色リトマス紙を青色に変えるが, これはOH - すいさんかぶつ ( 水酸化物イオン ) のはたらきによるものである OH - ようきょくは陽極 (+ 極 ) に引かれて左側に移動する OH - が赤色リトマスを通過するとき, 赤色リトマスが青色に変化するので, 図のアのリトマス紙が変化する
13 [ 問題 ]( 前期期末 ) 図のような装置をつくり, ろ紙に塩酸をしみこませて両端から電圧を加えた (1) 電圧を加えたとき, 色が変わるリトマス紙は, 図の a~d のうちのどれか (2) 次の文は,(1) のリトマス紙の色が変わる理由を説明したものである ( ) に適する語句を答えよ 塩酸のような酸性の水溶液は,( 1 ) 色のリトマス紙を ( 2 ) 色に変える これは ( 3 ) イオンのはたらきによるものである (3) イオンは ( 4 ) の電気を帯びているため, 水溶液に電圧を加えると ( 5 ) 極側に移動する したがって,(1) のリトマス紙の色が変わる
14 (3) 塩酸のかわりに水酸化ナトリウム水溶液を使って電圧を加えたとき, 色が変わるリトマス紙は図の a~d のうちどれか (4) (3) のリトマス紙の色が変わる理由を, 水溶液中のイオンの移動に着目して, 説明せよ (5) 塩酸のかわりに次の [ ] の水溶液を使ったとき,(1) と同じリトマス紙の色を変えるものを選べ [ アンモニア水食塩水砂糖水食酢 ] [ 解答 ](1) d (2)1 青 2 赤 3 水素 4 プラス (+) 5 陰 (3) a (4) - の電気を帯びた水酸化物イオンが陽極側に移動し, 赤色のリトマス紙を青色に変えるため (5) 食酢
15 理科 3 年の各ファイルへのリンク FdData 中間期末の特徴 (QandA 方式 ) 製品版 ( パソコン Word 文書 : 印刷 編集用 ) の価格 購入方法 iphone でリンク先が開かない場合は, ibooks で開いてリンクをタップください Fd 教材開発 Mail: info2@fdtext.com
FdData理科3年
 FdData 中間期末 : 中学理科 3 年 : 中和 [ 中和とイオン数の変化 ] [ 問題 ](2 学期中間 ) 次の図は A 液に B 液を加えたときのようすを示している A 液は塩酸,B 液は水酸化ナトリウム水溶液である (1) 1~4 の水溶液はそれぞれ何性か (2) 4 の水溶液にフェノールフタレイン溶液を加えると何色になるか (3) 塩酸 (A 液 ) に水酸化ナトリウム水溶液 (B
FdData 中間期末 : 中学理科 3 年 : 中和 [ 中和とイオン数の変化 ] [ 問題 ](2 学期中間 ) 次の図は A 液に B 液を加えたときのようすを示している A 液は塩酸,B 液は水酸化ナトリウム水溶液である (1) 1~4 の水溶液はそれぞれ何性か (2) 4 の水溶液にフェノールフタレイン溶液を加えると何色になるか (3) 塩酸 (A 液 ) に水酸化ナトリウム水溶液 (B
FdText理科1年
 中学理科 3 年 : 酸とアルカリ [ http://www.fdtext.com/dat/ ] [ 要点 ] 酸の性質 青色リトマスを赤に変える BTB 溶液を黄色に変える あえん金属 ( 亜鉛, マグネシウム, 鉄など ) と反応して水素を発生させる アルカリの性質 赤色リトマスを青色に変える BTB 溶液を青色に変える フェノールフタレイン溶液を赤色に変える ひふタンパク質をとかす ( 皮膚につけるとぬるぬるする
中学理科 3 年 : 酸とアルカリ [ http://www.fdtext.com/dat/ ] [ 要点 ] 酸の性質 青色リトマスを赤に変える BTB 溶液を黄色に変える あえん金属 ( 亜鉛, マグネシウム, 鉄など ) と反応して水素を発生させる アルカリの性質 赤色リトマスを青色に変える BTB 溶液を青色に変える フェノールフタレイン溶液を赤色に変える ひふタンパク質をとかす ( 皮膚につけるとぬるぬるする
< イオン 電離練習問題 > No. 1 次のイオンの名称を書きなさい (1) H + ( ) (2) Na + ( ) (3) K + ( ) (4) Mg 2+ ( ) (5) Cu 2+ ( ) (6) Zn 2+ ( ) (7) NH4 + ( ) (8) Cl - ( ) (9) OH -
 < イオン 電離練習問題 > No. 1 次のイオンの名称を書きなさい (1) + (2) Na + (3) K + (4) Mg 2+ (5) Cu 2+ (6) Zn 2+ (7) N4 + (8) Cl - (9) - (10) SO4 2- (11) NO3 - (12) CO3 2- 次の文中の ( ) に当てはまる語句を 下の選択肢から選んで書きなさい 物質の原子は (1 ) を失ったり
< イオン 電離練習問題 > No. 1 次のイオンの名称を書きなさい (1) + (2) Na + (3) K + (4) Mg 2+ (5) Cu 2+ (6) Zn 2+ (7) N4 + (8) Cl - (9) - (10) SO4 2- (11) NO3 - (12) CO3 2- 次の文中の ( ) に当てはまる語句を 下の選択肢から選んで書きなさい 物質の原子は (1 ) を失ったり
FdData理科3年
 FdData 中間期末 : 中学理科 1 年 : 化学 [ 溶解度 飽和水溶液 ] [ 問題 ](2 学期期末 ) 以下の各問いに答えよ (1) 一定量の水にとける物質の量は水の何によって変化するか (2) 物質がそれ以上とけることのできない水溶液を何というか (3) 固体の物質を水にとかしたのち, 再び固体として取り出すことを何というか [ 解答 ](1) 温度 (2) 飽和水溶液 (3) 再結晶
FdData 中間期末 : 中学理科 1 年 : 化学 [ 溶解度 飽和水溶液 ] [ 問題 ](2 学期期末 ) 以下の各問いに答えよ (1) 一定量の水にとける物質の量は水の何によって変化するか (2) 物質がそれ以上とけることのできない水溶液を何というか (3) 固体の物質を水にとかしたのち, 再び固体として取り出すことを何というか [ 解答 ](1) 温度 (2) 飽和水溶液 (3) 再結晶
FdData理科3年
 FdData 中間期末 : 中学理科 1 年化学 [ 気体総合 ] パソコン タブレット版へ移動 [ 各気体の製法 ] [ 問題 ](3 学期 ) 次の各問いに答えよ (1) 二酸化マンガンにオキシドールを加えると発生する気体は何か (2) 亜鉛にうすい塩酸を加えると発生する気体は何か (3) 発泡入浴剤に湯を加えて発生した気体を石灰水に通したら, 石灰水が白くにごった 発生した気体は何か (4)
FdData 中間期末 : 中学理科 1 年化学 [ 気体総合 ] パソコン タブレット版へ移動 [ 各気体の製法 ] [ 問題 ](3 学期 ) 次の各問いに答えよ (1) 二酸化マンガンにオキシドールを加えると発生する気体は何か (2) 亜鉛にうすい塩酸を加えると発生する気体は何か (3) 発泡入浴剤に湯を加えて発生した気体を石灰水に通したら, 石灰水が白くにごった 発生した気体は何か (4)
【FdData中間期末過去問題】中学理科3年(酸とアルカリ/イオンの移動/中和/塩)
 FdData 中間期末 : 中学理科 3 年 : 酸 アルカリ [ 酸性やアルカリ性の水溶液 / 指示薬 ph 金属との反応 / いろいろな水溶液水素イオンと水酸化物イオン / イオンの移動を調べる実験 / 中和 塩 / 中和の実験イオン数の変化 / 中和の計算問題 / 中和全般 /FdData 中間期末製品版のご案内 ] [FdData 中間期末ホームページ ] 掲載の pdf ファイル ( サンプル
FdData 中間期末 : 中学理科 3 年 : 酸 アルカリ [ 酸性やアルカリ性の水溶液 / 指示薬 ph 金属との反応 / いろいろな水溶液水素イオンと水酸化物イオン / イオンの移動を調べる実験 / 中和 塩 / 中和の実験イオン数の変化 / 中和の計算問題 / 中和全般 /FdData 中間期末製品版のご案内 ] [FdData 中間期末ホームページ ] 掲載の pdf ファイル ( サンプル
2011年度 化学1(物理学科)
 014 年度スペシャルプログラム (1/17) 酸 塩基 : 酸 塩基の定義を確認する No.1 1 酸と塩基の定義に関する以下の文章の正を答えよ 場合は 間違いを指摘せよ 文章正指摘 1 酸と塩基の定義はアレニウスとブレンステッド ローリーの 種類である ルイスの定義もある アレニウスの定義によれば 酸とは H を含むものである 水に溶けて 電離して H+ を出すものである 3 アレニウスの定義によれば
014 年度スペシャルプログラム (1/17) 酸 塩基 : 酸 塩基の定義を確認する No.1 1 酸と塩基の定義に関する以下の文章の正を答えよ 場合は 間違いを指摘せよ 文章正指摘 1 酸と塩基の定義はアレニウスとブレンステッド ローリーの 種類である ルイスの定義もある アレニウスの定義によれば 酸とは H を含むものである 水に溶けて 電離して H+ を出すものである 3 アレニウスの定義によれば
FdData高校入試過去問題】中学理科3年(酸の性質/アルカリの性質/中和とイオン)
 FdData 高校入試 : 中学理科 3 年 : 酸 アルカリ [ 指示薬など /ph/ 水素イオンと水酸化物イオン / イオンの移動の実験 / 中和 / 塩 / 中和の実験 / イオン数の変化 / 中和の計算問題 / 中和全般 /FdData 入試製品版のご案内 ] [FdData 入試ホームページ ] 掲載の pdf ファイル ( サンプル ) 一覧 ] 次のリンクは [Shift] キーをおしながら左クリックすると,
FdData 高校入試 : 中学理科 3 年 : 酸 アルカリ [ 指示薬など /ph/ 水素イオンと水酸化物イオン / イオンの移動の実験 / 中和 / 塩 / 中和の実験 / イオン数の変化 / 中和の計算問題 / 中和全般 /FdData 入試製品版のご案内 ] [FdData 入試ホームページ ] 掲載の pdf ファイル ( サンプル ) 一覧 ] 次のリンクは [Shift] キーをおしながら左クリックすると,
jhs-science1_05-02ans
 気体の発生と性質 (1 1 次の文章の ( に当てはまる言葉を書くか 〇でかこみなさい (1 気体には 水にとけやすいものと ものがある また 空気より (1 密度 が大きい ( 重い ものと 小さい ( 軽い ものがある (2 水に ( とけやすい 気体は水上で集められる 空気より 1 が ( 大きい 小さい 気体は下方 ( 大きい 小さい 気体は上方で それぞれ集められる (3 酸素の中に火のついた線香を入れると
気体の発生と性質 (1 1 次の文章の ( に当てはまる言葉を書くか 〇でかこみなさい (1 気体には 水にとけやすいものと ものがある また 空気より (1 密度 が大きい ( 重い ものと 小さい ( 軽い ものがある (2 水に ( とけやすい 気体は水上で集められる 空気より 1 が ( 大きい 小さい 気体は下方 ( 大きい 小さい 気体は上方で それぞれ集められる (3 酸素の中に火のついた線香を入れると
指導計画 評価の具体例 単元の目標 単元 1 化学変化とイオン 化学変化についての観察, 実験を通して, 水溶液の電気伝導性や中和反応について理解するとともに, これらの事物 現象をイオンのモデルと関連づけて見る見方や考え方を養い, 物質や化学変化に対する興味 関心を高め, 身のまわりの物質や事象を
 指導計画 評価の具体例 単元の目標 単元 化学変化とイオン 化学変化についての観察, 実験を通して, 水溶液の電気伝導性や中和反応について理解するとともに, これらの事物 現象をイオンのモデルと関連づけて見る見方や考え方を養い, 物質や化学変化に対する興味 関心を高め, 身のまわりの物質や事象を新たな見方や考え方でとらえさせる 教科書 P.0 7 (7) 時間 章水溶液とイオン 章の目標 水溶液に電流を流す実験を行い,
指導計画 評価の具体例 単元の目標 単元 化学変化とイオン 化学変化についての観察, 実験を通して, 水溶液の電気伝導性や中和反応について理解するとともに, これらの事物 現象をイオンのモデルと関連づけて見る見方や考え方を養い, 物質や化学変化に対する興味 関心を高め, 身のまわりの物質や事象を新たな見方や考え方でとらえさせる 教科書 P.0 7 (7) 時間 章水溶液とイオン 章の目標 水溶液に電流を流す実験を行い,
<連載講座>アルマイト従事者のためのやさしい化学(XVII)--まとめと問題 (1)
 アルマイト従事者のためのやさしい化学 (ⅩⅦ) - まとめと問題 1- 野口駿雄 Ⅰ. はじめに前号までに化学の基礎 アルミニウム表面処理に使用されている前処理液 ( 特にアルカリ溶液 ) 及び硫酸電解液や蓚酸電解液の分析方法について その手順を 使用する分析用器具を図示し また簡単な使用方法を付け加えながら示し 初心者でもその図を見ながら順を追って操作を行えば それぞれの分析が出来るように心がけ
アルマイト従事者のためのやさしい化学 (ⅩⅦ) - まとめと問題 1- 野口駿雄 Ⅰ. はじめに前号までに化学の基礎 アルミニウム表面処理に使用されている前処理液 ( 特にアルカリ溶液 ) 及び硫酸電解液や蓚酸電解液の分析方法について その手順を 使用する分析用器具を図示し また簡単な使用方法を付け加えながら示し 初心者でもその図を見ながら順を追って操作を行えば それぞれの分析が出来るように心がけ
補足 中学校では塩基性ではなくアルカリ性という表現を使って学習する アルカリはアラビア語 (al qily) で, アル (al) は定冠詞, カリ (qily) はオカヒジキ属の植物を焼いた灰の意味 植物の灰には Na,K,Ca などの金属元素が含まれており, それに水を加えて溶かすと, NaOH
 酸 塩基の定義のいろいろ 酸と塩基の性質酸の水溶液の性質 1 すっぱい味がする 2 青色リトマス紙を赤色に変える 3 BTB( ブロムチモールブルー ) 溶液を黄色に変える 4 多くの金属 (Mg: マグネシウム,Zn: 亜鉛,Fe: 鉄など ) と反応し, 水素を発生 Zn2HCl ZnCl 2 H 2 ( イオン反応式で表すと,Zn2H Zn 2 H 2 ) 酸の水溶液が以上の性質をもつのは,
酸 塩基の定義のいろいろ 酸と塩基の性質酸の水溶液の性質 1 すっぱい味がする 2 青色リトマス紙を赤色に変える 3 BTB( ブロムチモールブルー ) 溶液を黄色に変える 4 多くの金属 (Mg: マグネシウム,Zn: 亜鉛,Fe: 鉄など ) と反応し, 水素を発生 Zn2HCl ZnCl 2 H 2 ( イオン反応式で表すと,Zn2H Zn 2 H 2 ) 酸の水溶液が以上の性質をもつのは,
<4D F736F F F696E74202D A E90B6979D89C8816B91E63195AA96EC816C82DC82C682DF8D758DC03189BB8A7795CF89BB82C68CB48E AA8E E9197BF2E >
 中学 2 年理科まとめ講座 第 1 分野 1. 化学変化と原子 分子 物質の成り立ち 化学変化 化学変化と物質の質量 基本の解説と問題 講師 : 仲谷のぼる 1 物質の成り立ち 物質のつくり 物質をつくる それ以上分けることができない粒を原子という いくつかの原子が結びついてできたものを分子という いろいろな物質のうち 1 種類の原子からできている物質を単体 2 種類以上の原子からできている物質を化合物という
中学 2 年理科まとめ講座 第 1 分野 1. 化学変化と原子 分子 物質の成り立ち 化学変化 化学変化と物質の質量 基本の解説と問題 講師 : 仲谷のぼる 1 物質の成り立ち 物質のつくり 物質をつくる それ以上分けることができない粒を原子という いくつかの原子が結びついてできたものを分子という いろいろな物質のうち 1 種類の原子からできている物質を単体 2 種類以上の原子からできている物質を化合物という
Taro-化学3 酸塩基 最新版
 11 酸 塩基の反応 P oint.29 酸 塩基 ブレンステッドの酸 塩基 酸 水素イオンを 物質 塩基 水素イオンを 物質 NH3 + H2O NH4 + + OH - 酸 塩基の性質 1 リトマス紙 2 フェノールフタレイン溶液 3BTB 液 4 メチルオレンジ 5 金属と反応 6 味 7 水溶液中に存在するイオン 酸 塩基 酸 塩基の分類 1 価数による分類 1 価 2 価 3 価 酸 塩基
11 酸 塩基の反応 P oint.29 酸 塩基 ブレンステッドの酸 塩基 酸 水素イオンを 物質 塩基 水素イオンを 物質 NH3 + H2O NH4 + + OH - 酸 塩基の性質 1 リトマス紙 2 フェノールフタレイン溶液 3BTB 液 4 メチルオレンジ 5 金属と反応 6 味 7 水溶液中に存在するイオン 酸 塩基 酸 塩基の分類 1 価数による分類 1 価 2 価 3 価 酸 塩基
FdData理科3年
 FdData 中間期末 : 中学理科 2 年 : 放電と電流 [ 真空放電 ] [ 問題 ](1 学期中間 ) 次の各問いに答えよ (1) 空気中に電流が流れる現象をとくに何放電というか (2) 放電管の内部の空気を真空ポンプで抜いて大きな電圧をかけると, 電流が流れて放電管が光る この現象を何というか [ 解答 ](1) 空中放電 (2) 真空放電 [ 解説 ] 電気は空気中を流れにくいが, 非常に高い電圧のくうちゅうほうでんときには空中放電がおこる
FdData 中間期末 : 中学理科 2 年 : 放電と電流 [ 真空放電 ] [ 問題 ](1 学期中間 ) 次の各問いに答えよ (1) 空気中に電流が流れる現象をとくに何放電というか (2) 放電管の内部の空気を真空ポンプで抜いて大きな電圧をかけると, 電流が流れて放電管が光る この現象を何というか [ 解答 ](1) 空中放電 (2) 真空放電 [ 解説 ] 電気は空気中を流れにくいが, 非常に高い電圧のくうちゅうほうでんときには空中放電がおこる
FdData理科3年
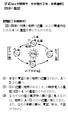 FdData 中間期末 : 中学理科 3 年 : 年周運動 [ 四季の星座 ] [ 問題 ](2 学期期末 ) 図は四季の太陽と地球の位置, および黄道付近にある 4 つの星座を示したものである (1) 日本の夏至の日の地球の位置はどれか A~ D から選べ (2) (1) の位置に地球があるとき, 一晩中見える星座は図の 4 つの星座のうちのどれか (3) 1 みずがめ座が真夜中に南の空に見えるのは,
FdData 中間期末 : 中学理科 3 年 : 年周運動 [ 四季の星座 ] [ 問題 ](2 学期期末 ) 図は四季の太陽と地球の位置, および黄道付近にある 4 つの星座を示したものである (1) 日本の夏至の日の地球の位置はどれか A~ D から選べ (2) (1) の位置に地球があるとき, 一晩中見える星座は図の 4 つの星座のうちのどれか (3) 1 みずがめ座が真夜中に南の空に見えるのは,
FdData理科3年
 FdData 中間期末 : 中学理科 3 年 : 仕事 [ 仕事の原理 : 斜面 ] [ 仕事の原理 引く力 ] [ 問題 ](2 学期期末 ) 図のような斜面を使って質量 35kg の物体を 3m の高さまで引き上げた ただし, ひもの重さ, 斜面や滑車の摩擦はないものとする また,100g の物体を引き上げるのに必要な力を 1N とする (1) このとき, 物体がされた仕事はいくらか (2) 図のとき,
FdData 中間期末 : 中学理科 3 年 : 仕事 [ 仕事の原理 : 斜面 ] [ 仕事の原理 引く力 ] [ 問題 ](2 学期期末 ) 図のような斜面を使って質量 35kg の物体を 3m の高さまで引き上げた ただし, ひもの重さ, 斜面や滑車の摩擦はないものとする また,100g の物体を引き上げるのに必要な力を 1N とする (1) このとき, 物体がされた仕事はいくらか (2) 図のとき,
Word Pro - matome_7_酸と塩基.lwp
 酸と 酸と 酸 acid 亜硫酸 pka =.6 pka =.9 酸 acid ( : 酸, すっぱいもの a : 酸の, すっぱい ) 酸性 p( ) 以下 酸っぱい味 ( 酸味 ) を持つ リトマス ( ) BTB( ) 金属と反応して ( ) を発生 ( 例 )Z l Zl リン酸 P pka =.5 pka =. pka =.8 P P P P P P P 酸性のもと 水素イオン 塩化水素
酸と 酸と 酸 acid 亜硫酸 pka =.6 pka =.9 酸 acid ( : 酸, すっぱいもの a : 酸の, すっぱい ) 酸性 p( ) 以下 酸っぱい味 ( 酸味 ) を持つ リトマス ( ) BTB( ) 金属と反応して ( ) を発生 ( 例 )Z l Zl リン酸 P pka =.5 pka =. pka =.8 P P P P P P P 酸性のもと 水素イオン 塩化水素
現行の学習指導要領(1998年公示,2002年実施)は,教育の総合化をキーワードに,「生きる力の育成」と「ゆとりある教育」をねらいとしている
 マイクロスケール実験によるイオンの移動 坂東舞 1), 芝原寛泰 2) 1) 大山崎町立大山崎中学校 clockwork@y9.dion.ne.jp 2) 京都教育大学理学科 shiba@kyokyo-u.ac.jp キーワード : マイクロスケール実験, イオンの移動, 中学校理科 ( 受付 :2007 年 12 月 16 日 ) Ⅰ. はじめに平成 14 年 (2002 年 ) 度施行の中学校理科学習指導要領
マイクロスケール実験によるイオンの移動 坂東舞 1), 芝原寛泰 2) 1) 大山崎町立大山崎中学校 clockwork@y9.dion.ne.jp 2) 京都教育大学理学科 shiba@kyokyo-u.ac.jp キーワード : マイクロスケール実験, イオンの移動, 中学校理科 ( 受付 :2007 年 12 月 16 日 ) Ⅰ. はじめに平成 14 年 (2002 年 ) 度施行の中学校理科学習指導要領
FdText理科1年
 中学理科 2 年 : 酸化 燃焼 [ http://www.fdtext.com/dat/ ] [ 要点 ] さんか (1) マグネシウムの酸化 物質が酸素と化合する反応を酸化という 熱や光を出しながらはげしく進む酸化を燃焼という 激しく熱と光を出し, 酸化マグネシウム ( 白色の酸化物 ) ができる マグネシウム+ 酸素 酸化マグネシウム,2Mg+O2 2MgO マグネシウム( 燃焼前 ) と酸化マグネシウム
中学理科 2 年 : 酸化 燃焼 [ http://www.fdtext.com/dat/ ] [ 要点 ] さんか (1) マグネシウムの酸化 物質が酸素と化合する反応を酸化という 熱や光を出しながらはげしく進む酸化を燃焼という 激しく熱と光を出し, 酸化マグネシウム ( 白色の酸化物 ) ができる マグネシウム+ 酸素 酸化マグネシウム,2Mg+O2 2MgO マグネシウム( 燃焼前 ) と酸化マグネシウム
がお互いの性質を打ち消しあう また, その際, その他のイオンから塩が生じる パフォーマンス課題 硫酸に電極をさし, 電源装置で電圧を加えると電流が流れ, 電球が点灯する これに水酸化バリウム水溶液を少しずつ加えていくと水溶液は白く濁り, 電球は次第に暗くなり, やがて消える しかし, さらに加え続
 理科第 3 学年東広島市立八本松中学校指導者湯口浩臣 単元名 酸, アルカリとイオン 本単元で育成する資質 能力 課題解決力 単元について (1) 単元観小学校では, 第 6 学年で 水溶液の性質 について学習している また, 中学校では, 第 1 学年で (2) 身の回りの物質, 第 2 学年で (3) 電流とその性質 と (4) 化学変化と原子 分子 について学習している 本単元では, 水溶液の電気伝導性や中和反応について理解させ,
理科第 3 学年東広島市立八本松中学校指導者湯口浩臣 単元名 酸, アルカリとイオン 本単元で育成する資質 能力 課題解決力 単元について (1) 単元観小学校では, 第 6 学年で 水溶液の性質 について学習している また, 中学校では, 第 1 学年で (2) 身の回りの物質, 第 2 学年で (3) 電流とその性質 と (4) 化学変化と原子 分子 について学習している 本単元では, 水溶液の電気伝導性や中和反応について理解させ,
FdText理科1年
 中学理科 1 年 : 気体 [ http://www.fdtext.com/dat/ ] 気体の性質 [ 要点 ] 気体の集め方 すいじょうちかん 水にとけない気体 水上置換 かほうちかん 水にとけて空気より重い気体 下方置換 じょうほうちかん 水にとけて空気より軽い気体 上方置換 酸素 水素 二酸化炭素 アンモニア かさんかすいそすいあえんかいがらえんか製法過酸化水素水亜鉛などの金石灰石 ( 貝殻
中学理科 1 年 : 気体 [ http://www.fdtext.com/dat/ ] 気体の性質 [ 要点 ] 気体の集め方 すいじょうちかん 水にとけない気体 水上置換 かほうちかん 水にとけて空気より重い気体 下方置換 じょうほうちかん 水にとけて空気より軽い気体 上方置換 酸素 水素 二酸化炭素 アンモニア かさんかすいそすいあえんかいがらえんか製法過酸化水素水亜鉛などの金石灰石 ( 貝殻
高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ
![高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ 高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ](/thumbs/94/118405200.jpg) 高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ溶質の20% 溶液 100gと30% 溶液 200gを混ぜると質量 % はいくらになるか ( 有効数字
高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ溶質の20% 溶液 100gと30% 溶液 200gを混ぜると質量 % はいくらになるか ( 有効数字
2 単元の評価規準関心 意欲 態度 科学的な思考 表現 観察 実験の技能 知識 理解 酸 アルカリ, 中和と塩に関する事物 現象に興味 関心を持ち, それを科学的に探究しようとするとともに, 事象を日常生活との関わりで捉えようとする 酸 アルカリ, 中和と塩に関する事象 現象の中に問題を見いだし,
 1 単元の概要 課題を解決するために必要な資質 能力を育成する授業に関する研究 - 第 3 学年 酸 アルカリとイオン ( 中和反応 ) の実践を通して - 鹿屋市立第一鹿屋中学校 教諭安田泉香 (1) 単元名 酸, アルカリとイオン ( 大単元化学変化とイオン ) (2) 単元について本単元のねらいは, 水溶液の電気的な性質や酸とアルカリの性質についての観察, 実験を行い, 結果を分析して解釈し,
1 単元の概要 課題を解決するために必要な資質 能力を育成する授業に関する研究 - 第 3 学年 酸 アルカリとイオン ( 中和反応 ) の実践を通して - 鹿屋市立第一鹿屋中学校 教諭安田泉香 (1) 単元名 酸, アルカリとイオン ( 大単元化学変化とイオン ) (2) 単元について本単元のねらいは, 水溶液の電気的な性質や酸とアルカリの性質についての観察, 実験を行い, 結果を分析して解釈し,
理科科学習指導案
 第 3 学年理科学習指導案 日時平成 27 年 月 日 ( ) 第 校時対象第 3 学年 組 名学校名 立 中学校 1 単元名 化学変化とイオン第 2 章酸 アルカリとイオン 中学校科学 3 ( 学校図書 ) 2 単元の目標 酸性とアルカリ性の水溶液の性質を調べ 酸とアルカリのそれぞれの特性が水素イオンと水酸化物イオ ンによることや 酸とアルカリを混ぜると 水と塩が生成することを理解する 3 単元の評価規準
第 3 学年理科学習指導案 日時平成 27 年 月 日 ( ) 第 校時対象第 3 学年 組 名学校名 立 中学校 1 単元名 化学変化とイオン第 2 章酸 アルカリとイオン 中学校科学 3 ( 学校図書 ) 2 単元の目標 酸性とアルカリ性の水溶液の性質を調べ 酸とアルカリのそれぞれの特性が水素イオンと水酸化物イオ ンによることや 酸とアルカリを混ぜると 水と塩が生成することを理解する 3 単元の評価規準
決するための学習の見通しをもたせ, 単元を貫く課題を意識させ, 目的意識をもたせた授業を展開していきたい 本単元では, 理科での学習内容が日常生活で見られる事象に関連することに気付かせたい 日常生活の事象から酸とアルカリの性質を粒子で考え中和反応をイオンのモデルと関連付けて理解させたい それを通して
 理科第 3 学年熊野町立熊野東中学校指導者磯方源太 単元名 酸とアルカリ 本単元で育成する資質 能力 高い志, 先を見通す力, チャレンジ精神, 他者理解 単元について 本単元は, 中学校学習指導要領の理科第 1 分野の内容 (6) 化学変化とイオンイ酸 アルカリとイオン を受けて設定した ここでは, 酸とアルカリの性質を調べる実験や中和反応の実験を行い, 結果を分析して解釈し, 酸とアルカリの特性や中和反応をイオンのモデルと関連付けて理解させることが主なねらいである
理科第 3 学年熊野町立熊野東中学校指導者磯方源太 単元名 酸とアルカリ 本単元で育成する資質 能力 高い志, 先を見通す力, チャレンジ精神, 他者理解 単元について 本単元は, 中学校学習指導要領の理科第 1 分野の内容 (6) 化学変化とイオンイ酸 アルカリとイオン を受けて設定した ここでは, 酸とアルカリの性質を調べる実験や中和反応の実験を行い, 結果を分析して解釈し, 酸とアルカリの特性や中和反応をイオンのモデルと関連付けて理解させることが主なねらいである
【FdData中間期末過去問題】中学数学1年(負の数/数直線/絶対値/数の大小)
 FdData 中間期末 : 中学数学 年 : 正負の数 [ 正の数 負の数 / 数直線 / 正の数 負の数で量を表す / 絶対値 / 数の大小 / 数直線を使って ] [ 数学 年 pdf ファイル一覧 ] 正の数 負の数 [ 負の数 ] 次の文章中の ( ) に適語を入れよ () +5 や+8 のような 0 より大きい数を ( ) という () - や-7 のような 0 より小さい数を ( ) という
FdData 中間期末 : 中学数学 年 : 正負の数 [ 正の数 負の数 / 数直線 / 正の数 負の数で量を表す / 絶対値 / 数の大小 / 数直線を使って ] [ 数学 年 pdf ファイル一覧 ] 正の数 負の数 [ 負の数 ] 次の文章中の ( ) に適語を入れよ () +5 や+8 のような 0 より大きい数を ( ) という () - や-7 のような 0 より小さい数を ( ) という
Taro-bussitu_T1
 P 気体の性質 ~ 気体の発生 次の表の ~4 にあてはまる言葉を後のア ~ シから選び, それぞれ記号で答えなさい 酸素二酸化炭素水素アンモニア窒素 空気より 4 少し軽い 水に 5 6 7 8 9 その他 0 4 ~4の選択肢 ア. もっとも軽いイ. 軽いウ. 少し重いエ. 重い 5~9の選択肢 オ. 溶けにくいカ. 少し溶けるキ. 溶けやすい 0~4の選択肢 ク. 他の物が燃えるのを助けるケ.
P 気体の性質 ~ 気体の発生 次の表の ~4 にあてはまる言葉を後のア ~ シから選び, それぞれ記号で答えなさい 酸素二酸化炭素水素アンモニア窒素 空気より 4 少し軽い 水に 5 6 7 8 9 その他 0 4 ~4の選択肢 ア. もっとも軽いイ. 軽いウ. 少し重いエ. 重い 5~9の選択肢 オ. 溶けにくいカ. 少し溶けるキ. 溶けやすい 0~4の選択肢 ク. 他の物が燃えるのを助けるケ.
とである そこで, 紫キャベツを使った料理にレモンをかけると色が変わることを取り上げたり, 湖沼の水質の中和やあくとりなどの例を用いたりして, 興味 関心を高めるようにしたい なお,1 学年の いろいろな気体の性質,2 学年の 化学変化と原子 分子 ( 化学式と化学反応式 ),3 学年の 酸 アルカ
 元名理科第 3 学年三次市立塩町中学校指導者大内信之介単化学変化とイオン ( 酸 アルカリと塩 ) 白い煙の正体をあばけ 本単元で育成する資質 能力 情報活用能力 思考力 表現力 人間関係形成能力 1 日時平成 29 年 9 月 19 日 ( 火 )5 校時 2 学年 学級 3 年 B 組 ( 男子 14 人女子 16 人計 30 人 ) 3 単元名酸 アルカリとイオン (1 分野粒子領域化学変化とイオンより
元名理科第 3 学年三次市立塩町中学校指導者大内信之介単化学変化とイオン ( 酸 アルカリと塩 ) 白い煙の正体をあばけ 本単元で育成する資質 能力 情報活用能力 思考力 表現力 人間関係形成能力 1 日時平成 29 年 9 月 19 日 ( 火 )5 校時 2 学年 学級 3 年 B 組 ( 男子 14 人女子 16 人計 30 人 ) 3 単元名酸 アルカリとイオン (1 分野粒子領域化学変化とイオンより
第 11 回化学概論 酸化と還元 P63 酸化還元反応 酸化数 酸化剤 還元剤 金属のイオン化傾向 酸化される = 酸素と化合する = 水素を奪われる = 電子を失う = 酸化数が増加する 還元される = 水素と化合する = 酸素を奪われる = 電子を得る = 酸化数が減少する 銅の酸化酸化銅の還元
 第 11 回化学概論 酸化と還元 P63 酸化還元反応 酸化数 酸化剤 還元剤 金属のイオン化傾向 酸化される = 酸素と化合する = 水素を奪われる = 電子を失う = 酸化数が増加する 還元される = 水素と化合する = 酸素を奪われる = 電子を得る = 酸化数が減少する 銅の酸化酸化銅の還元 2Cu + O 2 2CuO CuO + H 2 Cu + H 2 O Cu Cu 2+ + 2e
第 11 回化学概論 酸化と還元 P63 酸化還元反応 酸化数 酸化剤 還元剤 金属のイオン化傾向 酸化される = 酸素と化合する = 水素を奪われる = 電子を失う = 酸化数が増加する 還元される = 水素と化合する = 酸素を奪われる = 電子を得る = 酸化数が減少する 銅の酸化酸化銅の還元 2Cu + O 2 2CuO CuO + H 2 Cu + H 2 O Cu Cu 2+ + 2e
FdData理科3年
 FdData 中間期末 : 中学理科 3 年 [ 仕事の原理 : 斜面 ] パソコン タブレット版へ移動 [ 仕事の原理 引く力 ] [ 問題 ](2 学期期末 ) 次の図のような斜面を使って質量 35kg の物体を 3m の高さまで引き上げた ただし, ひもの重さ, 斜面や滑車の摩擦はないものとする また,100g の物体にはたらく重力を 1N とする (1) このとき, 物体がされた仕事はいくらか
FdData 中間期末 : 中学理科 3 年 [ 仕事の原理 : 斜面 ] パソコン タブレット版へ移動 [ 仕事の原理 引く力 ] [ 問題 ](2 学期期末 ) 次の図のような斜面を使って質量 35kg の物体を 3m の高さまで引き上げた ただし, ひもの重さ, 斜面や滑車の摩擦はないものとする また,100g の物体にはたらく重力を 1N とする (1) このとき, 物体がされた仕事はいくらか
岐阜大学教育学部教師教育研究 中学校理科における寒天を用いた電気分解実験の一工夫 岐阜大学教育学部附属中学校 土田慎治 岐阜大学教育学部理科教育講座 ( 物理学 ) 澤田諒太 岐阜大学教育学部理科教育講座 ( 物理学 ) 仲澤和馬 1 はじめに学習指導要領解説 ( 平成 20 年 9
 岐阜大学教育学部教師教育研究 7 2011 中学校理科における寒天を用いた電気分解実験の一工夫 岐阜大学教育学部附属中学校 土田慎治 岐阜大学教育学部理科教育講座 ( 物理学 ) 澤田諒太 岐阜大学教育学部理科教育講座 ( 物理学 ) 仲澤和馬 1 はじめに学習指導要領解説 ( 平成 20 年 9 月 ) によると 中学校理科 1 分野下の第 6 単元 化学変化とイオン における目標は 化学変化についての観察
岐阜大学教育学部教師教育研究 7 2011 中学校理科における寒天を用いた電気分解実験の一工夫 岐阜大学教育学部附属中学校 土田慎治 岐阜大学教育学部理科教育講座 ( 物理学 ) 澤田諒太 岐阜大学教育学部理科教育講座 ( 物理学 ) 仲澤和馬 1 はじめに学習指導要領解説 ( 平成 20 年 9 月 ) によると 中学校理科 1 分野下の第 6 単元 化学変化とイオン における目標は 化学変化についての観察
2004 年度センター化学 ⅠB p1 第 1 問問 1 a 水素結合 X HLY X,Y= F,O,N ( ) この形をもつ分子は 5 NH 3 である 1 5 b 昇華性の物質 ドライアイス CO 2, ヨウ素 I 2, ナフタレン 2 3 c 総電子数 = ( 原子番号 ) d CH 4 :6
 004 年度センター化学 ⅠB p 第 問問 a 水素結合 X HLY X,Y= F,O,N ( ) この形をもつ分子は 5 NH である 5 b 昇華性の物質 ドライアイス CO, ヨウ素 I, ナフタレン c 総電子数 = ( 原子番号 ) d CH 4 :6+ 4 = 0個 6+ 8= 4個 7+ 8= 5個 + 7= 8個 4 + 8= 0個 5 8= 6個 4 構造式からアプローチして電子式を書くと次のようになる
004 年度センター化学 ⅠB p 第 問問 a 水素結合 X HLY X,Y= F,O,N ( ) この形をもつ分子は 5 NH である 5 b 昇華性の物質 ドライアイス CO, ヨウ素 I, ナフタレン c 総電子数 = ( 原子番号 ) d CH 4 :6+ 4 = 0個 6+ 8= 4個 7+ 8= 5個 + 7= 8個 4 + 8= 0個 5 8= 6個 4 構造式からアプローチして電子式を書くと次のようになる
電子配置と価電子 P H 2He 第 4 回化学概論 3Li 4Be 5B 6C 7N 8O 9F 10Ne 周期表と元素イオン 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar 価電子数 陽
 電子配置と価電子 P11 1 2 13 14 15 16 17 18 1H 2He 第 4 回化学概論 3Li 4Be 5B 6C 7N 8O 9F 10Ne 周期表と元素イオン 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar 1 2 3 4 5 6 7 0 陽性元素陰性元素安定電子を失いやすい電子を受け取りやすい 原子番号と価電子の数 P16 元素の周期表 P17 最外殻の電子配置と周期表
電子配置と価電子 P11 1 2 13 14 15 16 17 18 1H 2He 第 4 回化学概論 3Li 4Be 5B 6C 7N 8O 9F 10Ne 周期表と元素イオン 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar 1 2 3 4 5 6 7 0 陽性元素陰性元素安定電子を失いやすい電子を受け取りやすい 原子番号と価電子の数 P16 元素の周期表 P17 最外殻の電子配置と周期表
Microsoft PowerPoint - D.酸塩基(2)
 D. 酸塩基 (2) 1. 多塩基酸の ph 2. 塩の濃度と ph 3. 緩衝溶液と ph 4. 溶解度積と ph 5. 酸塩基指示薬 D. 酸塩基 (2) 1. 多塩基酸の ph 1. 多塩基酸の ph (1) 硫酸 H 2 SO 4 ( 濃度 C) 硫酸 H 2 SO 4 は2 段階で電離する K (C) (C) K a1 [H+ ][HSO 4 ] [H 2 SO 4 ] 10 5 第 1
D. 酸塩基 (2) 1. 多塩基酸の ph 2. 塩の濃度と ph 3. 緩衝溶液と ph 4. 溶解度積と ph 5. 酸塩基指示薬 D. 酸塩基 (2) 1. 多塩基酸の ph 1. 多塩基酸の ph (1) 硫酸 H 2 SO 4 ( 濃度 C) 硫酸 H 2 SO 4 は2 段階で電離する K (C) (C) K a1 [H+ ][HSO 4 ] [H 2 SO 4 ] 10 5 第 1
イオン化傾向 イオン化傾向 1 金属の単体はいずれも酸化されて陽イオンになりうる 金属のイオンのなりやすさを表したものをイオン化傾向という イオン化傾向 K Ca Na Mg Al Zn Fe Ni Sn Pb (H) Cu Hg Ag Pt Au e- を出してイオンになりやすい酸化されやすい イ
 イオン化傾向 イオン化傾向 金属の単体はいずれも酸化されて陽イオンになりうる 金属のイオンのなりやすさを表したものをイオン化傾向という イオン化傾向 K Ca Na Mg Al Zn Fe Ni Sn Pb (H) Cu Hg Ag Pt Au e- を出してイオンになりやすい酸化されやすい イオンになりにくい酸化されにくい イオン化傾向の覚え方 K かそう Ca か Na な Mg ま Al あ
イオン化傾向 イオン化傾向 金属の単体はいずれも酸化されて陽イオンになりうる 金属のイオンのなりやすさを表したものをイオン化傾向という イオン化傾向 K Ca Na Mg Al Zn Fe Ni Sn Pb (H) Cu Hg Ag Pt Au e- を出してイオンになりやすい酸化されやすい イオンになりにくい酸化されにくい イオン化傾向の覚え方 K かそう Ca か Na な Mg ま Al あ
でんかいしつすいよう電解質の水溶 教科書 p 第 2 章化学変化と電池 電流をとり出す 実験 えき液の中の金属板と電流 2 枚の金属板を水溶液に入れ, 電子オルゴールや光電池用モーターをつないでみる 電圧計で電圧をはかり, どちらが プラス極, マイナス極かを見る こと
 6 でんかいしつすいよう電解質の水溶 教科書 p.7 7 第 章化学変化と電池 電流をとり出す 実験 えき液の中の金属板と電流 枚の金属板を水溶液に入れ, 電子オルゴールや光電池用モーターをつないでみる 電圧計で電圧をはかり, どちらが プラス極, マイナス極かを見る こと 結果 電解質の水溶液と, 異なる種類の金属板を用いたとき, 電流が流れた ( 電子オルゴールが鳴り, 光でんち電池用モーターが回った
6 でんかいしつすいよう電解質の水溶 教科書 p.7 7 第 章化学変化と電池 電流をとり出す 実験 えき液の中の金属板と電流 枚の金属板を水溶液に入れ, 電子オルゴールや光電池用モーターをつないでみる 電圧計で電圧をはかり, どちらが プラス極, マイナス極かを見る こと 結果 電解質の水溶液と, 異なる種類の金属板を用いたとき, 電流が流れた ( 電子オルゴールが鳴り, 光でんち電池用モーターが回った
Taro-(HP)指導案(改訂).jtd
 第 3 学年理科学習指導案 日 時 平成 2 4 年 1 0 月 2 4 日 ( 水 ) 第 5 校時 場 所 理科室 1 単元名化学変化とイオン 2 単元について ( 1 ) 生徒の実態イオンの学習に入る前に下記のようなアンケートを実施した ( 生徒アンケートについては http://www.nipec.nein.ed.jp/sc/rika/teiken/ を参考に作成 ) アンケートの内容 イオン
第 3 学年理科学習指導案 日 時 平成 2 4 年 1 0 月 2 4 日 ( 水 ) 第 5 校時 場 所 理科室 1 単元名化学変化とイオン 2 単元について ( 1 ) 生徒の実態イオンの学習に入る前に下記のようなアンケートを実施した ( 生徒アンケートについては http://www.nipec.nein.ed.jp/sc/rika/teiken/ を参考に作成 ) アンケートの内容 イオン
(2) 本単元に関わる生徒の実態及び指導方針 1 既習の学習内容 水溶液には酸性 中性 アルカリ性のものがあること 金属を変化させる水溶液があること( 小 6) 気体の発生と性質 物質への水への溶解について( 第 1 学年 ) 物質が原子や分子でできていること( 第 2 学年 ) 電流が電子の流れで
 理科学習指導案 (3 年 ) 平成 28 年 6 月 9 日 ( 木 ) 第 5 校時化学室指導者加藤絵美子 授業の視点 課題解決をする場面で ジグソー学習を取り入れたことは 生徒の科学的な思考力や表現力を互いに伸ばすのに有効であったか 1 単元名 酸 アルカリとイオン 2 考察 (1) 教材観 1 学習内容 : 学習指導要領上の位置付け (6) 化学変化とイオンイ酸 アルカリとイオン ( イ )
理科学習指導案 (3 年 ) 平成 28 年 6 月 9 日 ( 木 ) 第 5 校時化学室指導者加藤絵美子 授業の視点 課題解決をする場面で ジグソー学習を取り入れたことは 生徒の科学的な思考力や表現力を互いに伸ばすのに有効であったか 1 単元名 酸 アルカリとイオン 2 考察 (1) 教材観 1 学習内容 : 学習指導要領上の位置付け (6) 化学変化とイオンイ酸 アルカリとイオン ( イ )
FdData理科3年
 FdData 中間期末 : 中学理科 3 年 : 食物連鎖 [ 分解者のはたらきを調べる実験 1] [ 問題 ](1 学期期末 ) 下の図のように, ビーカーの中で布を広げて水を入れ, そこに落ち葉や土を入れてよくかき回し布でこした こした水をビーカー A に入れ,B には A と同量の水を入れた A と B に同量のデンプン溶液を加え, ラップシートでビーカーにふたをして 2~3 日間, 置いた
FdData 中間期末 : 中学理科 3 年 : 食物連鎖 [ 分解者のはたらきを調べる実験 1] [ 問題 ](1 学期期末 ) 下の図のように, ビーカーの中で布を広げて水を入れ, そこに落ち葉や土を入れてよくかき回し布でこした こした水をビーカー A に入れ,B には A と同量の水を入れた A と B に同量のデンプン溶液を加え, ラップシートでビーカーにふたをして 2~3 日間, 置いた
群教セ G04-03 平 集 理科 - 中 生徒が解決の見通しを持って実験方法を立案する理科授業 モデル図やグラフを使った予想の共有と タブレット端末の活用を通して 特別研修員奈良達也 Ⅰ 研究テーマ設定の理由 平成 29 年 3 月公示の新学習指導要領では 内容のイとして思考 判断
 群教セ G04-03 平 29.265 集 理科 - 中 生徒が解決の見通しを持って実験方法を立案する理科授業 モデル図やグラフを使った予想の共有と タブレット端末の活用を通して 特別研修員奈良達也 Ⅰ 研究テーマ設定の理由 平成 29 年 3 月公示の新学習指導要領では 内容のイとして思考 判断 表現の資質 能力が示された 全学年に共通して規則性や関係性を見いだして表現するといった表記がなされているほか
群教セ G04-03 平 29.265 集 理科 - 中 生徒が解決の見通しを持って実験方法を立案する理科授業 モデル図やグラフを使った予想の共有と タブレット端末の活用を通して 特別研修員奈良達也 Ⅰ 研究テーマ設定の理由 平成 29 年 3 月公示の新学習指導要領では 内容のイとして思考 判断 表現の資質 能力が示された 全学年に共通して規則性や関係性を見いだして表現するといった表記がなされているほか
英語科学習指導案
 理科第 3 学年三次市立甲奴中学校指導者熊谷民夫 単元名 化学変化とイオン ( 酸 アルカリと塩 ) 本単元で育成する資質 能力 対話力 課題解決力 学びを振り返る力 1 日時平成 28 年 9 月 26 日 ( 月 )5 校時 2 学年第 3 学年 ( 男子 9 人女子 12 人計 21 人 ) 3 場所理科室 4 単元名化学変化とイオン ( 酸 アルカリと塩 ) 5 本単元を指導するにあたって
理科第 3 学年三次市立甲奴中学校指導者熊谷民夫 単元名 化学変化とイオン ( 酸 アルカリと塩 ) 本単元で育成する資質 能力 対話力 課題解決力 学びを振り返る力 1 日時平成 28 年 9 月 26 日 ( 月 )5 校時 2 学年第 3 学年 ( 男子 9 人女子 12 人計 21 人 ) 3 場所理科室 4 単元名化学変化とイオン ( 酸 アルカリと塩 ) 5 本単元を指導するにあたって
<576F F202D F94BD899E8EAE82CC8DEC82E895FB5F31325F352E6C7770>
 1 ( 問 ) 金属が溶けて H 2 を発生する場合 ( 例 ) 1. 金属と H で考える Na H 2O H 2 Fe H 2 H 2 2Na 2H 2Na H 2 Fe 2H Fe 2 H 2 2. 水の場合は OH を両辺に加える 2'. 酸の場合は 酸の陰イオンを両辺に加える 3. たし算をする Na H 2O K H 2O Ca H 2O Mg H 2O Zn H 2 Fe H 2 Al
1 ( 問 ) 金属が溶けて H 2 を発生する場合 ( 例 ) 1. 金属と H で考える Na H 2O H 2 Fe H 2 H 2 2Na 2H 2Na H 2 Fe 2H Fe 2 H 2 2. 水の場合は OH を両辺に加える 2'. 酸の場合は 酸の陰イオンを両辺に加える 3. たし算をする Na H 2O K H 2O Ca H 2O Mg H 2O Zn H 2 Fe H 2 Al
Taro-22 No19 大網中(中和と塩
 中和と塩 Ⅰ 視覚的に確認でき, イオンなどの粒子概念の形成に役立つ中和反応の観察 実験例 1 観察 実験のあらまし中和反応の実験は, 塩酸と水酸化ナトリウムで行うことが多い ところが, この反応では生成する塩は塩化ナトリウム ( 食塩 ) という水に溶ける塩であるため, 混ぜた瞬間に中和反応が起きていることがわからない そこで, 硫酸と水酸化バリウムの組み合わせで行うことで硫酸バリウムという水に溶けない塩が生成するので,1
中和と塩 Ⅰ 視覚的に確認でき, イオンなどの粒子概念の形成に役立つ中和反応の観察 実験例 1 観察 実験のあらまし中和反応の実験は, 塩酸と水酸化ナトリウムで行うことが多い ところが, この反応では生成する塩は塩化ナトリウム ( 食塩 ) という水に溶ける塩であるため, 混ぜた瞬間に中和反応が起きていることがわからない そこで, 硫酸と水酸化バリウムの組み合わせで行うことで硫酸バリウムという水に溶けない塩が生成するので,1
▲ 電離平衡
 電離平衡演習その 1 [04 金沢 ] 電離平衡 1 1 酢酸の濃度 C mol/l の水溶液がある 酢酸の電離度を とすると, 平衡状態で溶液中に存在する酢酸イオンの濃度は Ⅰ mol/l, 電離していない酢酸の濃度は Ⅱ mol/l, 水素イオンの濃度は Ⅲ mol/l と表される ここで, 電離度が 1より非常に小さく,1 1と近似すると, 電離定数は Ⅳ mol/l と表される いま,3.0
電離平衡演習その 1 [04 金沢 ] 電離平衡 1 1 酢酸の濃度 C mol/l の水溶液がある 酢酸の電離度を とすると, 平衡状態で溶液中に存在する酢酸イオンの濃度は Ⅰ mol/l, 電離していない酢酸の濃度は Ⅱ mol/l, 水素イオンの濃度は Ⅲ mol/l と表される ここで, 電離度が 1より非常に小さく,1 1と近似すると, 電離定数は Ⅳ mol/l と表される いま,3.0
Microsoft Word - 酸塩基
 化学基礎実験 : 酸 塩基と (1) 酸と塩基 の基本を学び の実験を通してこれらの事柄に関する認識を深めます さらに 緩衝液の性質に ついて学び 緩衝液の 変化に対する緩衝力を実験で確かめます 化学基礎実験 : 酸 塩基と 酸と塩基 水の解離 HCl H Cl - 塩酸 塩素イオン 酸 強酸 ヒドロニウムイオン H 3 O H O H OH - OH ー [H ] = [OH - ]= 1-7 M
化学基礎実験 : 酸 塩基と (1) 酸と塩基 の基本を学び の実験を通してこれらの事柄に関する認識を深めます さらに 緩衝液の性質に ついて学び 緩衝液の 変化に対する緩衝力を実験で確かめます 化学基礎実験 : 酸 塩基と 酸と塩基 水の解離 HCl H Cl - 塩酸 塩素イオン 酸 強酸 ヒドロニウムイオン H 3 O H O H OH - OH ー [H ] = [OH - ]= 1-7 M
2 原子やイオンのつ 3 原子が電気的に中性 3 原子の構造について くりに関心をもっ になる理由を 原子 説明している て説明を聞こうと の構造から指摘して 4 陽イオンや陰イオン する いる の違いを説明でき 4 イオンは原子が電子 イオンをイオン式で を失ったり 受け取っ 表している たりして
 中学校第 3 学年理科学習指導案 日時平成 25 年 月 日第 校時対象第 3 学年 組 名学校名 立 中学校授業者 1 単元名 化学変化とイオン 2 単元の目標化学変化についての観察 実験をとおして 水溶液の電気伝導性や中和反応について理解するとともに これらの事物 現象をイオンのモデルと関連付けてみる見方や考え方を身に付け 物質や化学変化に対する興味 関心を高め 身の回りの物質や事象を新たな見方や考え方で捉える
中学校第 3 学年理科学習指導案 日時平成 25 年 月 日第 校時対象第 3 学年 組 名学校名 立 中学校授業者 1 単元名 化学変化とイオン 2 単元の目標化学変化についての観察 実験をとおして 水溶液の電気伝導性や中和反応について理解するとともに これらの事物 現象をイオンのモデルと関連付けてみる見方や考え方を身に付け 物質や化学変化に対する興味 関心を高め 身の回りの物質や事象を新たな見方や考え方で捉える
<4D F736F F D2093FA D95BD90E690B68EF68BC681458E7793B188C42E646F63>
 第 1 学年 2 組理科学習指導案 平成 17 年 12 月 13 日 ( 火 ) 第 5 校時 男子 17(1) 名女子 21 名計 38 名 指導者日置洋平 1. 単元酸性やアルカリ性を示す水溶液 2. 目標 日常生活に見られる酸 アルカリの水溶液の性質について関心を持ち, 積極的に調べようとする 酸とアルカリの両性質が打ち消しあう反応過程を, 中和の実験の現象より見出すことができる 酸とアルカリを混ぜる中和の実験を正確に,
第 1 学年 2 組理科学習指導案 平成 17 年 12 月 13 日 ( 火 ) 第 5 校時 男子 17(1) 名女子 21 名計 38 名 指導者日置洋平 1. 単元酸性やアルカリ性を示す水溶液 2. 目標 日常生活に見られる酸 アルカリの水溶液の性質について関心を持ち, 積極的に調べようとする 酸とアルカリの両性質が打ち消しあう反応過程を, 中和の実験の現象より見出すことができる 酸とアルカリを混ぜる中和の実験を正確に,
平成27年度 前期日程 化学 解答例
 受験番号 平成 27 年度前期日程 化学 ( その 1) 解答用紙 工学部 応用化学科 志願者は第 1 問 ~ 第 4 問を解答せよ 農学部 生物資源科学科, 森林科学科 志願者は第 1 問と第 2 問を解答せよ 第 1 問 [ 二酸化炭素が発生する反応の化学反応式 ] 点 NaHCO 3 + HCl NaCl + H 2 O + CO 2 CO 2 の物質量を x mol とすると, 気体の状態方程式より,
受験番号 平成 27 年度前期日程 化学 ( その 1) 解答用紙 工学部 応用化学科 志願者は第 1 問 ~ 第 4 問を解答せよ 農学部 生物資源科学科, 森林科学科 志願者は第 1 問と第 2 問を解答せよ 第 1 問 [ 二酸化炭素が発生する反応の化学反応式 ] 点 NaHCO 3 + HCl NaCl + H 2 O + CO 2 CO 2 の物質量を x mol とすると, 気体の状態方程式より,
調査研究「教科等で考える異校種間の連携の工夫」〔理科〕
 事例 6 高等学校 化学 Ⅰ 学習指導案 平成 年 月 日 () 第 校時指導者教諭 学年第 1 学年生徒数 名 ( 男子 名女子 名 ) 1 単元名酸と塩基の反応 2 単元について (1) 単元観生徒は教科書の第 1 章で, 原子の構造が物質の性質を理解するうえで重要であること, さらに, 原子の電子配置モデルを用いたイオンを学習している また, 第 2 章では, 物質の量を表す概念として物質量とその単位のモルを,
事例 6 高等学校 化学 Ⅰ 学習指導案 平成 年 月 日 () 第 校時指導者教諭 学年第 1 学年生徒数 名 ( 男子 名女子 名 ) 1 単元名酸と塩基の反応 2 単元について (1) 単元観生徒は教科書の第 1 章で, 原子の構造が物質の性質を理解するうえで重要であること, さらに, 原子の電子配置モデルを用いたイオンを学習している また, 第 2 章では, 物質の量を表す概念として物質量とその単位のモルを,
Ⅲ 化学変化とイオン 単元における観察 実験の位置付け 学習活動備考 課題 どのような水溶液が電流を通すのだろうか 実験 1 電解質や非電解質の水溶液について電流を通すか調べる実験 様々な水溶液を用意するが この後に 塩化銅水溶液や塩酸の電気分解に触れるため この 2 つの水溶液は用意しておくとよい
 化学変化とイオン 単元のねらい 水溶液の電気的な性質や酸とアルカリの性質についての観察 実験を行い 結果を分析して解釈し 水溶液の電 気伝導性や中和反応について理解させ イオンのモデルと関連付けてみる微視的な見方や考え方を養う 単元の内容 化学変化についての観察 実験を通して 水溶液の電気伝導性や中和反応について理解させるとともに これらの事物 現象をイオンのモデルと関連付けてみる見方や考え方を養う
化学変化とイオン 単元のねらい 水溶液の電気的な性質や酸とアルカリの性質についての観察 実験を行い 結果を分析して解釈し 水溶液の電 気伝導性や中和反応について理解させ イオンのモデルと関連付けてみる微視的な見方や考え方を養う 単元の内容 化学変化についての観察 実験を通して 水溶液の電気伝導性や中和反応について理解させるとともに これらの事物 現象をイオンのモデルと関連付けてみる見方や考え方を養う
見いださせる 3 章 化学変化と電池 本章では電解質水溶液と2 種類の金属を用いて電池をつくる実験を行い 電流が取り出せることを見いださせる このとき化学エネルギーが電気エネルギーに変換されていることを理解させる また 電極での電子の授受をイオンのモデルで表し 電池のしくみを微視的視点でとらえさせる
 3 理科学習指導案平成 27 年 11 月 27 日 ( 金 ) 授業者 教諭 1 単元名化学変化とイオン ( 本時 電圧の大きい電池をつくろう ( 課題選択学習 ) ) 2 単元について ⑴ 教材観 1 単元の目標化学変化の学習を通して これまで身に付けてきた物質についての微視的な見方や考え方と電気的な性質についての知識の統合を図る 水溶液の電気的な性質や酸とアルカリの性質についての観察 実験を行い
3 理科学習指導案平成 27 年 11 月 27 日 ( 金 ) 授業者 教諭 1 単元名化学変化とイオン ( 本時 電圧の大きい電池をつくろう ( 課題選択学習 ) ) 2 単元について ⑴ 教材観 1 単元の目標化学変化の学習を通して これまで身に付けてきた物質についての微視的な見方や考え方と電気的な性質についての知識の統合を図る 水溶液の電気的な性質や酸とアルカリの性質についての観察 実験を行い
木村の理論化学小ネタ 熱化学方程式と反応熱の分類発熱反応と吸熱反応化学反応は, 反応の前後の物質のエネルギーが異なるため, エネルギーの出入りを伴い, それが, 熱 光 電気などのエネルギーの形で現れる とくに, 化学変化と熱エネルギーの関
 熱化学方程式と反応熱の分類発熱反応と吸熱反応化学反応は, 反応の前後の物質のエネルギーが異なるため, エネルギーの出入りを伴い, それが, 熱 光 電気などのエネルギーの形で現れる とくに, 化学変化と熱エネルギーの関係を扱う化学の一部門を熱化学という 発熱反応反応前の物質のエネルギー 大ネルギ熱エネルギーー小エ反応後の物質のエネルギー 吸熱反応 反応後の物質のエネルギー 大ネルギー熱エネルギー小エ反応前の物質のエネルギー
熱化学方程式と反応熱の分類発熱反応と吸熱反応化学反応は, 反応の前後の物質のエネルギーが異なるため, エネルギーの出入りを伴い, それが, 熱 光 電気などのエネルギーの形で現れる とくに, 化学変化と熱エネルギーの関係を扱う化学の一部門を熱化学という 発熱反応反応前の物質のエネルギー 大ネルギ熱エネルギーー小エ反応後の物質のエネルギー 吸熱反応 反応後の物質のエネルギー 大ネルギー熱エネルギー小エ反応前の物質のエネルギー
後期化学
 問 1~ 問 36 の解答を, 指定された解答欄にマークせよ 必要があれば, 次の数値を用いよ 原子量 :H = 1.0,C = 12,O = 16,Mg = 24,Cl = 35.5,Ca = 40,Cu = 64 アボガドロ定数 :6.02 10 23 / mol 気体定数 :8.3 10 3 Pa L / (K mol) または 8.2 10 2 atm L / (K mol) ファラデー定数
問 1~ 問 36 の解答を, 指定された解答欄にマークせよ 必要があれば, 次の数値を用いよ 原子量 :H = 1.0,C = 12,O = 16,Mg = 24,Cl = 35.5,Ca = 40,Cu = 64 アボガドロ定数 :6.02 10 23 / mol 気体定数 :8.3 10 3 Pa L / (K mol) または 8.2 10 2 atm L / (K mol) ファラデー定数
i ( 23 ) ) SPP Science Partnership Project ( (1) (2) 2010 SSH
 i 1982 2012 ( 23 ) 30 1998 ) 2002 2006 2009 1999 2009 10 2004 SPP Science Partnership Project 2004 2005 2009 ( 29 2010 (1) (2) 2010 SSH ii ph 21 2006 10 B5 A5 2014 2 2014 2 iii 21 1962 1969 1987 1992 2005
i 1982 2012 ( 23 ) 30 1998 ) 2002 2006 2009 1999 2009 10 2004 SPP Science Partnership Project 2004 2005 2009 ( 29 2010 (1) (2) 2010 SSH ii ph 21 2006 10 B5 A5 2014 2 2014 2 iii 21 1962 1969 1987 1992 2005
FdData中間期末数学1年
 中学中間 期末試験問題集 ( 過去問 ): 数学 年 四則をふくむ式の計算 http://www.fdtext.com/dat/ [ 加減と乗除が混じった計算 ] [ 問題 ]( 前期中間 ) 9+8 (-) [ 解答 ]-7 加減と乗除が混じった式では, 乗除を先に計算する ( +-の順で計算) 9+8 (-) では,8 (-) の部分を先に計算 9+8 (-)9--7 [ 問題 ]( 学期期末
中学中間 期末試験問題集 ( 過去問 ): 数学 年 四則をふくむ式の計算 http://www.fdtext.com/dat/ [ 加減と乗除が混じった計算 ] [ 問題 ]( 前期中間 ) 9+8 (-) [ 解答 ]-7 加減と乗除が混じった式では, 乗除を先に計算する ( +-の順で計算) 9+8 (-) では,8 (-) の部分を先に計算 9+8 (-)9--7 [ 問題 ]( 学期期末
化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イ
 化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イオンと陰イオンの静電気的な引力による結合を 1 1 という ⑵ 2 個の水素原子は, それぞれ1 個の価電子を出し合い,
化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イオンと陰イオンの静電気的な引力による結合を 1 1 という ⑵ 2 個の水素原子は, それぞれ1 個の価電子を出し合い,
【FdData中間期末過去問題】中学数学1年(項と係数/加法と減法/乗法と除法)
 FdDt 中間期末 : 中学数学 年 : 文字式計算 [ 項と係数 / 加法と減法 / 乗法と除法 / 加減乗除全般 /FdDt 中間期末製品版のご案内 ] [FdDt 中間期末 pdf ファイル ( サンプル ) 一覧 ] [Shift] 左クリック 新規ウィンドウが開きます数学 :[ 数学 年 ],[ 数学 年 ],[ 数学 年 ] 理科 :[ 理科 年 ],[ 理科 年 ],[ 理科 年 ]
FdDt 中間期末 : 中学数学 年 : 文字式計算 [ 項と係数 / 加法と減法 / 乗法と除法 / 加減乗除全般 /FdDt 中間期末製品版のご案内 ] [FdDt 中間期末 pdf ファイル ( サンプル ) 一覧 ] [Shift] 左クリック 新規ウィンドウが開きます数学 :[ 数学 年 ],[ 数学 年 ],[ 数学 年 ] 理科 :[ 理科 年 ],[ 理科 年 ],[ 理科 年 ]
<4D F736F F F696E74202D208D918E8E91CE8DF481698E5F89968AEE816A F38DFC97702E707074>
 国試対策 酸塩基 酸 塩基 ( アルカリ ) って何? H 2 SO 4 水酸化カルシウムアンモニア CH HNO 3 4 HCl 硫酸ナトリウム 新垣 知輝 どれが酸? どれが塩基? 酸 酸と塩基の定義 塩基 H + を出すもの OH を出すもの by アレニウス H + を渡すもの H + を受け取るもの by ブレンステッド ローリー電子対を受け取る電子対を渡すものもの by ルイス 水素イオン
国試対策 酸塩基 酸 塩基 ( アルカリ ) って何? H 2 SO 4 水酸化カルシウムアンモニア CH HNO 3 4 HCl 硫酸ナトリウム 新垣 知輝 どれが酸? どれが塩基? 酸 酸と塩基の定義 塩基 H + を出すもの OH を出すもの by アレニウス H + を渡すもの H + を受け取るもの by ブレンステッド ローリー電子対を受け取る電子対を渡すものもの by ルイス 水素イオン
CERT化学2013前期_問題
 [1] から [6] のうち 5 問を選んで解答用紙に解答せよ. いずれも 20 点の配点である.5 問を超えて解答した場合, 正答していれば成績評価に加算する. 有効数字を適切に処理せよ. 断りのない限り大気圧は 1013 hpa とする. 0 C = 273 K,1 cal = 4.184 J,1 atm = 1013 hpa = 760 mmhg, 重力加速度は 9.806 m s 2, 気体
[1] から [6] のうち 5 問を選んで解答用紙に解答せよ. いずれも 20 点の配点である.5 問を超えて解答した場合, 正答していれば成績評価に加算する. 有効数字を適切に処理せよ. 断りのない限り大気圧は 1013 hpa とする. 0 C = 273 K,1 cal = 4.184 J,1 atm = 1013 hpa = 760 mmhg, 重力加速度は 9.806 m s 2, 気体
必要があれば, 次の数値を使いなさい 原子量 O= 標準状態で mol の気体が占める体積. L 問題文中の体積の単位記号 L は, リットルを表す Ⅰ 次の問いに答えなさい 問 飲料水の容器であるペットボトルに使われているプラスチックを, 次の中から つ選び, 番号をマークしなさい ポリエチレン
 0 年度一般入試前期 A 日程 ( 月 日実施 ) 化学問題 (7 ページ 7 ページ ) 問題は大問 Ⅰ Ⅳ までありますが 一部 他科目との共通問題となっています 大問 Ⅰ は 化学基礎 + 生物基礎 の大問 Ⅰ と共通の問題です 大問 Ⅱ は 化学基礎 + 生物基礎 の大問 Ⅱ と共通の問題です 7 必要があれば, 次の数値を使いなさい 原子量 O= 標準状態で mol の気体が占める体積.
0 年度一般入試前期 A 日程 ( 月 日実施 ) 化学問題 (7 ページ 7 ページ ) 問題は大問 Ⅰ Ⅳ までありますが 一部 他科目との共通問題となっています 大問 Ⅰ は 化学基礎 + 生物基礎 の大問 Ⅰ と共通の問題です 大問 Ⅱ は 化学基礎 + 生物基礎 の大問 Ⅱ と共通の問題です 7 必要があれば, 次の数値を使いなさい 原子量 O= 標準状態で mol の気体が占める体積.
<4D F736F F D2089BB8A778AEE E631358D E5F89BB8AD28CB3>
 第 15 講 酸化と還元 酸化 還元とは切ったリンゴをそのまま放置すると, 時間が経つにつれて断面が変色します これはリンゴの断面が酸化した現象を示しています ピカピカの10 円玉も, しばらくすると黒く, くすんでいきます これも酸化です この10 円玉を水素ガスのなかに入れると, 元のきれいな10 円玉に戻ります これが還元です 1 酸化還元の定義 2 酸化数とは? 3 酸化剤 還元剤についての理解
第 15 講 酸化と還元 酸化 還元とは切ったリンゴをそのまま放置すると, 時間が経つにつれて断面が変色します これはリンゴの断面が酸化した現象を示しています ピカピカの10 円玉も, しばらくすると黒く, くすんでいきます これも酸化です この10 円玉を水素ガスのなかに入れると, 元のきれいな10 円玉に戻ります これが還元です 1 酸化還元の定義 2 酸化数とは? 3 酸化剤 還元剤についての理解
授業では, 課題を解決するための情報を集める前に, どのような方法だと必要な情報を集めることができるのかを考えています 58.8% 41.2% 授業では, 調べたことなどを, 図, グラフ, 表などにまとめています 73.5% 26.5% 授業では, 情報を比べたり ( 比較 ), 仲間分けしたり
 理科第 3 学年三原市立第三中学校指導者多久和勇貴 単元名 ~ 化学変化とイオン 2 章酸 アルカリと塩 ~ 本単元で育成する資質 能力 課題発見 解決力 1 日時 : 平成 29 年 7 月 6 日 ( 木 ) 2 場所 : 理科室 1 3 学年 学級 : 3 年 3 組 36 人 ( 男子 20 人女子 16 人 ) 4 単元名 : 化学変化とイオン 2 章酸 アルカリと塩 (1) 単元観本単元では,
理科第 3 学年三原市立第三中学校指導者多久和勇貴 単元名 ~ 化学変化とイオン 2 章酸 アルカリと塩 ~ 本単元で育成する資質 能力 課題発見 解決力 1 日時 : 平成 29 年 7 月 6 日 ( 木 ) 2 場所 : 理科室 1 3 学年 学級 : 3 年 3 組 36 人 ( 男子 20 人女子 16 人 ) 4 単元名 : 化学変化とイオン 2 章酸 アルカリと塩 (1) 単元観本単元では,
フォルハルト法 NH SCN の標準液または KSCN の標準液を用い,Ag または Hg を直接沈殿滴定する方法 および Cl, Br, I, CN, 試料溶液に Fe SCN, S 2 を指示薬として加える 例 : Cl の逆滴定による定量 などを逆滴定する方法をいう Fe を加えた試料液に硝酸
 沈殿滴定とモール法 沈殿滴定沈殿とは溶液に試薬を加えたり加熱や冷却をしたとき, 溶液から不溶性固体が分離する現象, またはその不溶性固体を沈殿という 不溶性固体は, 液底に沈んでいいても微粒子 ( コロイド ) として液中を浮遊していても沈殿と呼ばれる 沈殿滴定とは沈殿が生成あるいは消失する反応を利用した滴定のことをいう 沈殿が生成し始めた点, 沈殿の生成が完了した点, または沈殿が消失した点が滴定の終点となる
沈殿滴定とモール法 沈殿滴定沈殿とは溶液に試薬を加えたり加熱や冷却をしたとき, 溶液から不溶性固体が分離する現象, またはその不溶性固体を沈殿という 不溶性固体は, 液底に沈んでいいても微粒子 ( コロイド ) として液中を浮遊していても沈殿と呼ばれる 沈殿滴定とは沈殿が生成あるいは消失する反応を利用した滴定のことをいう 沈殿が生成し始めた点, 沈殿の生成が完了した点, または沈殿が消失した点が滴定の終点となる
Microsoft Word - dainityu.doc
 第 3 学年理科学習指導案 指導者三原市立第二中学校笹岡嘉郎 1 日平成 23 年 11 月 18 日 ( 金 )9:40~10:30 2 学年 学級 3 年 1 組 ( 男子 17 名, 女子 15 名計 32 名 ) 3 場所第 1 理科室 (1F) 4 単元名化学変化とイオン ( 酸 アルカリとイオン ) 5 単元について (1) 単元観学習指導要領 1 分野の内容 (6) に位置づけられている本単元は,
第 3 学年理科学習指導案 指導者三原市立第二中学校笹岡嘉郎 1 日平成 23 年 11 月 18 日 ( 金 )9:40~10:30 2 学年 学級 3 年 1 組 ( 男子 17 名, 女子 15 名計 32 名 ) 3 場所第 1 理科室 (1F) 4 単元名化学変化とイオン ( 酸 アルカリとイオン ) 5 単元について (1) 単元観学習指導要領 1 分野の内容 (6) に位置づけられている本単元は,
事例 2-2
 事例 5 中学校第 1 学年 組理科学習活動案 平成 20 年 月 日 () 第 校時指導者教諭 在籍生徒数男子 名女子 名 1 単元名身のまわりの物質第 2 章水溶液の性質 2 単元について (1) 教材観本単元は, 身のまわりの物質についての観察 実験を通して, 固体や液体, 気体の性質, 物質の状態変化について理解させるとともに, 物質の性質や変化の調べ方の基礎を身に付けさせる内容である ここでは,
事例 5 中学校第 1 学年 組理科学習活動案 平成 20 年 月 日 () 第 校時指導者教諭 在籍生徒数男子 名女子 名 1 単元名身のまわりの物質第 2 章水溶液の性質 2 単元について (1) 教材観本単元は, 身のまわりの物質についての観察 実験を通して, 固体や液体, 気体の性質, 物質の状態変化について理解させるとともに, 物質の性質や変化の調べ方の基礎を身に付けさせる内容である ここでは,
Taro-化学5 無機化学 最新版
 18 典型元素とその化合物 Ⅰ P oint.43 アルカリ金属元素 1 価電子価のイオン 2 常温で水と激しく反応する強いアルカリ性を示す Na + H2O に保存 3すべての塩は水に溶ける 4 炎色反応を示す Sr Li Ca Na Ba Cu K 5 イオン化傾向が大きい酸化されやすい 力 6 単体 Na は 7 アンモニアソーダ法 で得る ソルベー法 (1) (5) NaCl NaHCO3
18 典型元素とその化合物 Ⅰ P oint.43 アルカリ金属元素 1 価電子価のイオン 2 常温で水と激しく反応する強いアルカリ性を示す Na + H2O に保存 3すべての塩は水に溶ける 4 炎色反応を示す Sr Li Ca Na Ba Cu K 5 イオン化傾向が大きい酸化されやすい 力 6 単体 Na は 7 アンモニアソーダ法 で得る ソルベー法 (1) (5) NaCl NaHCO3
SO の場合 Leis の酸塩基説 ( 非プロトン性溶媒までも摘要可 一般化 ) B + B の化学反応の酸と塩基 SO + + SO SO + + SO 酸 塩基 酸 塩基 SO は酸にも塩基にもなっている 酸の強さ 酸が強い = 塩基へプロトンを供与する能力が大きい 強酸 ( 優れたプロトン供与
 溶液溶媒 + 溶質 均一な相 溶質を溶かしている物質 溶けている物質 固体 + 液体液体 + 固体 溶質 (solute) イオンの形に解離して溶けているもの ( 電解質 ) 酸と塩基 Copyrigt: A.Asno 1 水素イオン濃度 (ydrogenion concentrtion) 水素イオン指数 (ydrogenion exponent; p) 水の電離 O + O O + + O O +
溶液溶媒 + 溶質 均一な相 溶質を溶かしている物質 溶けている物質 固体 + 液体液体 + 固体 溶質 (solute) イオンの形に解離して溶けているもの ( 電解質 ) 酸と塩基 Copyrigt: A.Asno 1 水素イオン濃度 (ydrogenion concentrtion) 水素イオン指数 (ydrogenion exponent; p) 水の電離 O + O O + + O O +
理科学習指導案
 第 3 学年理科学習指導案 久慈市立久慈中学校 指導者 岩崎幸彦 1 日時平成 23 年 9 月 22 日 ( 木 ) 5 校時 2 学級 3 年 A 組男子 18 名女子 18 名計 36 名 3 単元名 化学変化とイオン 4 単元について 1 野単元 6 エネルギー第 2 章化学変化とエネルギー 第節化学変化とイオン ( 東京書籍プラス 23 P ) (1) 教材について化学変化についての観察
第 3 学年理科学習指導案 久慈市立久慈中学校 指導者 岩崎幸彦 1 日時平成 23 年 9 月 22 日 ( 木 ) 5 校時 2 学級 3 年 A 組男子 18 名女子 18 名計 36 名 3 単元名 化学変化とイオン 4 単元について 1 野単元 6 エネルギー第 2 章化学変化とエネルギー 第節化学変化とイオン ( 東京書籍プラス 23 P ) (1) 教材について化学変化についての観察
FdText理科1年
 中学理科 2 年 : 消化 [ http://www.fdtext.com/dat/ ] [ 要点 ] (1) だ液の実験 だ液にはデンプンを糖に変えるアミラーゼとこうそいう消化酵素が含まれている しょうかこうそ 消化酵素は体温近くでもっともよくはたらく ヨウ素液: デンプンがあると青紫色に変化 ( 図の A,B,D が青紫色に変化 ) しゃふつせきかっしょくとっぷつ ベネジクト液: 糖に加えて煮沸
中学理科 2 年 : 消化 [ http://www.fdtext.com/dat/ ] [ 要点 ] (1) だ液の実験 だ液にはデンプンを糖に変えるアミラーゼとこうそいう消化酵素が含まれている しょうかこうそ 消化酵素は体温近くでもっともよくはたらく ヨウ素液: デンプンがあると青紫色に変化 ( 図の A,B,D が青紫色に変化 ) しゃふつせきかっしょくとっぷつ ベネジクト液: 糖に加えて煮沸
FdText理科1年
 中学理科 2 年 : オームの法則 [ http://www.fdtext.com/dat/ ] オームの法則 [ 要点 ] 電流: 電圧に比例 ( 電圧を 2 倍にすると電流は 2 倍になる ) ていこう : 抵抗の大きさに反比例 ( 抵抗を 2 倍にすると電流は半分になる ) 公式: 電流 (A)= 電圧 (V) 抵抗 (Ω) 抵抗 (Ω)= 電圧 (V) 電流 (A) 電圧 (V)= 抵抗 (Ω)
中学理科 2 年 : オームの法則 [ http://www.fdtext.com/dat/ ] オームの法則 [ 要点 ] 電流: 電圧に比例 ( 電圧を 2 倍にすると電流は 2 倍になる ) ていこう : 抵抗の大きさに反比例 ( 抵抗を 2 倍にすると電流は半分になる ) 公式: 電流 (A)= 電圧 (V) 抵抗 (Ω) 抵抗 (Ω)= 電圧 (V) 電流 (A) 電圧 (V)= 抵抗 (Ω)
木村の化学重要問題集 01 解答編解説補充 H S H HS ( 第 1 電離平衡 ) HS H S ( 第 電離平衡 ) そこで溶液を中性または塩基性にすることにより, つまり [ H ] を小さくすることにより, 上の電離平衡を右に片寄らせ,[ S ] を大きくする 193. 陽イオン分析 配位
![木村の化学重要問題集 01 解答編解説補充 H S H HS ( 第 1 電離平衡 ) HS H S ( 第 電離平衡 ) そこで溶液を中性または塩基性にすることにより, つまり [ H ] を小さくすることにより, 上の電離平衡を右に片寄らせ,[ S ] を大きくする 193. 陽イオン分析 配位 木村の化学重要問題集 01 解答編解説補充 H S H HS ( 第 1 電離平衡 ) HS H S ( 第 電離平衡 ) そこで溶液を中性または塩基性にすることにより, つまり [ H ] を小さくすることにより, 上の電離平衡を右に片寄らせ,[ S ] を大きくする 193. 陽イオン分析 配位](/thumbs/91/107310906.jpg) 木村の化学重要問題集 01 解答編解説補充 1. 無機物質の性質 反応 187. 気体の製法と性質補足ネスラー試薬とアンモニアの反応 1.. ネスラー試薬 [ HgI ] の調製 KI KI Hg ¾¾ HgI ¾¾ [ HgI ] 赤色沈殿. ネスラー試薬とアンモニアの反応 [ HgI ] ( NH ) [ ] NH HgI ( 微量 : 黄色, 多量 : 赤褐色 ) 190. 陽イオンの分離と性質
木村の化学重要問題集 01 解答編解説補充 1. 無機物質の性質 反応 187. 気体の製法と性質補足ネスラー試薬とアンモニアの反応 1.. ネスラー試薬 [ HgI ] の調製 KI KI Hg ¾¾ HgI ¾¾ [ HgI ] 赤色沈殿. ネスラー試薬とアンモニアの反応 [ HgI ] ( NH ) [ ] NH HgI ( 微量 : 黄色, 多量 : 赤褐色 ) 190. 陽イオンの分離と性質
FdData理科3年
 FdData 中間期末 : 中学理科 3 年天体 [ 日食 月食 ] パソコン タブレット版へ移動 [ 太陽と月の見かけの大きさ ] [ 問題 ](1 学期期末 ) 太陽と月を地球から見たとき, 見かけ上の大きさを比較するとどうなるか 次の [ ] から 1 つ選べ [ 太陽が大きい月が大きいほぼ同じである ] [ 解答 ] ほぼ同じである [ 解説 ] 太陽の直径は月の約 400 倍である また,
FdData 中間期末 : 中学理科 3 年天体 [ 日食 月食 ] パソコン タブレット版へ移動 [ 太陽と月の見かけの大きさ ] [ 問題 ](1 学期期末 ) 太陽と月を地球から見たとき, 見かけ上の大きさを比較するとどうなるか 次の [ ] から 1 つ選べ [ 太陽が大きい月が大きいほぼ同じである ] [ 解答 ] ほぼ同じである [ 解説 ] 太陽の直径は月の約 400 倍である また,
2019 年度大学入試センター試験解説 化学 第 1 問問 1 a 塩化カリウムは, カリウムイオン K + と塩化物イオン Cl - のイオン結合のみを含む物質であり, 共有結合を含まない ( 答 ) 1 1 b 黒鉛の結晶中では, 各炭素原子の 4 つの価電子のうち 3 つが隣り合う他の原子との
 219 年度大学入試センター試験解説 化学 第 1 問問 1 a 塩化カリウムは, カリウムイオン K + と塩化物イオン Cl - のイオン結合のみを含む物質であり, 共有結合を含まない ( 答 ) 1 1 b 黒鉛の結晶中では, 各炭素原子の 4 つの価電子のうち 3 つが隣り合う他の原子との共有結合に使われ, 残りの 1 つは結晶を構成する層上を自由に移動している そのため, 黒鉛は固体の状態で電気をよく通す
219 年度大学入試センター試験解説 化学 第 1 問問 1 a 塩化カリウムは, カリウムイオン K + と塩化物イオン Cl - のイオン結合のみを含む物質であり, 共有結合を含まない ( 答 ) 1 1 b 黒鉛の結晶中では, 各炭素原子の 4 つの価電子のうち 3 つが隣り合う他の原子との共有結合に使われ, 残りの 1 つは結晶を構成する層上を自由に移動している そのため, 黒鉛は固体の状態で電気をよく通す
CPT2L1Z1J154.indd
 要点学習化学変化と原子分子 1 1 30 分分解, 物質のしくみ CPT2L1-Z1J1-01 要点 要点を読んで重要なポイントを確認しましょう 分解 1 分解 物質そのものが 性質が異なる別の物質に変わる変化を() といいます 1 種類の物質が2 種類以上の別の物質に分かれる化学変化をといいます 加熱により起こる分解をとくにといい 電流を流すことにより起こる分解をとくに といいます 2 炭酸水素ナトリウムを熱分解する実験
要点学習化学変化と原子分子 1 1 30 分分解, 物質のしくみ CPT2L1-Z1J1-01 要点 要点を読んで重要なポイントを確認しましょう 分解 1 分解 物質そのものが 性質が異なる別の物質に変わる変化を() といいます 1 種類の物質が2 種類以上の別の物質に分かれる化学変化をといいます 加熱により起こる分解をとくにといい 電流を流すことにより起こる分解をとくに といいます 2 炭酸水素ナトリウムを熱分解する実験
Microsoft Word - 小学校第6学年理科指導案「水溶液の性質」
 第 6 学年 理科学習指導案 単元名 水溶液の性質 単元目標いろいろな水溶液を使い, その性質や金属を変化させる様子を推論しながら調べ, 見いだした問題を計画的に追求する活動を通して, 水溶液の性質や働きについての見方や考え方をもつことができるようにする 単元の評価規準 < 自然象への関心 意欲 態度 > いろいろな水溶液の液生や溶けている物及び金属を変化させる様子に興味 関心をもち, 自ら水溶液の性質や働きを調べようとしている
第 6 学年 理科学習指導案 単元名 水溶液の性質 単元目標いろいろな水溶液を使い, その性質や金属を変化させる様子を推論しながら調べ, 見いだした問題を計画的に追求する活動を通して, 水溶液の性質や働きについての見方や考え方をもつことができるようにする 単元の評価規準 < 自然象への関心 意欲 態度 > いろいろな水溶液の液生や溶けている物及び金属を変化させる様子に興味 関心をもち, 自ら水溶液の性質や働きを調べようとしている
木村の有機化学小ネタ セルロース系再生繊維 再生繊維セルロースなど天然高分子物質を化学的処理により溶解後, 細孔から押し出し ( 紡糸 という), 再凝固させて繊維としたもの セルロース系の再生繊維には, ビスコースレーヨン, 銅アンモニア
 セルロース系再生繊維 再生繊維セルロースなど天然高分子物質を化学的処理により溶解後, 細孔から押し出し ( 紡糸 という), 再凝固させて繊維としたもの セルロース系の再生繊維には, ビスコースレーヨン, 銅アンモニアレーヨンがあり, タンパク質系では, カゼイン, 大豆タンパク質, 絹の糸くず, くず繭などからの再生繊維がある これに対し, セルロースなど天然の高分子物質の誘導体を紡糸して繊維としたものを半合成繊維と呼び,
セルロース系再生繊維 再生繊維セルロースなど天然高分子物質を化学的処理により溶解後, 細孔から押し出し ( 紡糸 という), 再凝固させて繊維としたもの セルロース系の再生繊維には, ビスコースレーヨン, 銅アンモニアレーヨンがあり, タンパク質系では, カゼイン, 大豆タンパク質, 絹の糸くず, くず繭などからの再生繊維がある これに対し, セルロースなど天然の高分子物質の誘導体を紡糸して繊維としたものを半合成繊維と呼び,
ア 単元の指導内容と身に付けさせたい力 この単元では, いろいろな水溶液を使い その性質や金属を変化させる様子を調べ, 水溶液に は 1 酸性 アルカリ性及び中性のものがあること 2 気体が溶けているものがあること 3 金 属を変化させるものがあることなど 水溶液の性質や働きについての考えを児童がも
 科学的な見方や考え方を高める指導と評価 - 小学校第 6 学年理科 水よう液の性質 の学習を通して - 斑鳩町立斑鳩小学校教諭梅本利政 Umemoto Toshimasa 要旨児童自らが課題づくりを行ったり 自由試行を行ったりする学習において 児童が作成したコンセプトマップ 能動的な自己評価及びノートを用いて 児童の科学的な見方や考え方が高まっているかどうかを評価した その結果 それらによる評価が
科学的な見方や考え方を高める指導と評価 - 小学校第 6 学年理科 水よう液の性質 の学習を通して - 斑鳩町立斑鳩小学校教諭梅本利政 Umemoto Toshimasa 要旨児童自らが課題づくりを行ったり 自由試行を行ったりする学習において 児童が作成したコンセプトマップ 能動的な自己評価及びノートを用いて 児童の科学的な見方や考え方が高まっているかどうかを評価した その結果 それらによる評価が
Taro-09 寒天を用いた電気泳動の
 村田一平 寒天を用いた電気泳動の実験条件に関する検討 村田 一平 中学校理科の学習指導要領では, 化学的領域で, 原子の成り立ちとイオン において電解質の水溶液中に電気を帯びた粒子が存在することに気付かせること, 酸 アルカリ において酸とアルカリの性質が水素イオンと水酸化物イオンによることを理解させることが示されており, そのための実験としては, 塩化銅や塩酸などの電気泳動を行いイオンの移動を観察させることが考えられる
村田一平 寒天を用いた電気泳動の実験条件に関する検討 村田 一平 中学校理科の学習指導要領では, 化学的領域で, 原子の成り立ちとイオン において電解質の水溶液中に電気を帯びた粒子が存在することに気付かせること, 酸 アルカリ において酸とアルカリの性質が水素イオンと水酸化物イオンによることを理解させることが示されており, そのための実験としては, 塩化銅や塩酸などの電気泳動を行いイオンの移動を観察させることが考えられる
後期化学_04_酸塩基pH
 2011 ( ) ph H3O + H + H3O + HCl H3O + HCl + H2O H3O + + Cl HCl H + + Cl OH OH NaOH OH NaOH Na + + OH NH3 OH NH3 + H2O NH4 + + OH 1 H + OH H + H + * 1 NH3 HCl NH4Cl NH4Cl NH3 + Cl NH3 + HCl NH4 + + Cl.
2011 ( ) ph H3O + H + H3O + HCl H3O + HCl + H2O H3O + + Cl HCl H + + Cl OH OH NaOH OH NaOH Na + + OH NH3 OH NH3 + H2O NH4 + + OH 1 H + OH H + H + * 1 NH3 HCl NH4Cl NH4Cl NH3 + Cl NH3 + HCl NH4 + + Cl.
【FdData中間期末過去問題】中学数学2年(連立方程式計算/加減法/代入法/係数決定)
 FdData 中間期末 : 中学数学 年 : 連立方程式計算 [ 元 1 次方程式 / 加減法 / 代入法 / 加減法と代入法 / 分数などのある連立方程式 / A=B=C, 元連立方程式 / 係数の決定 ] [ 数学 年 pdf ファイル一覧 ] 元 1 次方程式 次の方程式ア~カの中から, 元 1 次方程式をすべて選べ ア y = 6 イ x y = 5 ウ xy = 1 エ x + 5 = 9
FdData 中間期末 : 中学数学 年 : 連立方程式計算 [ 元 1 次方程式 / 加減法 / 代入法 / 加減法と代入法 / 分数などのある連立方程式 / A=B=C, 元連立方程式 / 係数の決定 ] [ 数学 年 pdf ファイル一覧 ] 元 1 次方程式 次の方程式ア~カの中から, 元 1 次方程式をすべて選べ ア y = 6 イ x y = 5 ウ xy = 1 エ x + 5 = 9
キレート滴定
 4. キレート滴定 4.1 0.01MEDTA 標準溶液の調製 キレート滴定において標準溶液として用いられる EDTA は 普通 EDTA の2ナトリウム塩 H 2 Na 2 Y 2H 2 O で ETA と表示されている この試薬は結晶水以外に多少の水分を含んでいるので 通常は約 80 で数時間乾燥して使用するが 本実験では精密な分析を行うために 調製した EDTA 溶液をZnの一次標準溶液で標定して
4. キレート滴定 4.1 0.01MEDTA 標準溶液の調製 キレート滴定において標準溶液として用いられる EDTA は 普通 EDTA の2ナトリウム塩 H 2 Na 2 Y 2H 2 O で ETA と表示されている この試薬は結晶水以外に多少の水分を含んでいるので 通常は約 80 で数時間乾燥して使用するが 本実験では精密な分析を行うために 調製した EDTA 溶液をZnの一次標準溶液で標定して
1 次の問い ( 問 1~ 問 5) に答えよ (23 点 ) 問 1 次の単位変換のうち, 正しいもののみをすべて含む組み合わせは どれか マーク式解答欄 1 (a) 1.0 kg = mg (b) 1.0 dl = ml (c) 1.0 g/cm 3 = 1.
 問 1~ 問 25 の解答を, 指定された解答欄にマークせよ 必要があれば, 次の数値を用いよ 原子量 : H = 1.0, C = 12, N = 14, O = 16, Na = 23, S = 32, Cl = 35.5, Ca = 40, Cu = 64, Zn = 65 気体定数 :8.3 10 3 Pa L/(K mol) ファラデー定数 :9.65 10 4 C/mol セルシウス温度目盛りのゼロ点
問 1~ 問 25 の解答を, 指定された解答欄にマークせよ 必要があれば, 次の数値を用いよ 原子量 : H = 1.0, C = 12, N = 14, O = 16, Na = 23, S = 32, Cl = 35.5, Ca = 40, Cu = 64, Zn = 65 気体定数 :8.3 10 3 Pa L/(K mol) ファラデー定数 :9.65 10 4 C/mol セルシウス温度目盛りのゼロ点
【FdData高校入試過去問題】中学理科2年(化合/硫化鉄/硫化銅/その他)
 FdData 高校入試過去問題 中学理科 2 年 ( 化合 / 硫化鉄 / 硫化銅 / その他 ) http://www.fdtext.com/dan/ 化合 化合 2 種類以上の物質が結びついて別の新しい物質ができる化学変化を ( ) という ( 岐阜県 ) [ 解答 ] 化合 かごう 2 種類の物質が結びついて, 別の 1 種類の物質ができる化学変化を化合という 例えば, 銅さんかどうを加熱すると,
FdData 高校入試過去問題 中学理科 2 年 ( 化合 / 硫化鉄 / 硫化銅 / その他 ) http://www.fdtext.com/dan/ 化合 化合 2 種類以上の物質が結びついて別の新しい物質ができる化学変化を ( ) という ( 岐阜県 ) [ 解答 ] 化合 かごう 2 種類の物質が結びついて, 別の 1 種類の物質ができる化学変化を化合という 例えば, 銅さんかどうを加熱すると,
FdText理科1年
 中学理科 1 年 : 有機物と無機物 [ http://www.fdtext.com/dat/ ] 有機物と無機物 [ 要点 ] (1) ガスバーナーの操作 火のつけ方: ガス調節ねじと空気調節ねじが閉じていることを確認する 元せんを開く マッチに火をつけてからガス調節ねじをゆるめ, 火をななめ下から近づける 炎の大きさを調整する 炎は最初赤色 ( 空気が少ないから ) 空気調節ねじで炎を青色の三角形にする
中学理科 1 年 : 有機物と無機物 [ http://www.fdtext.com/dat/ ] 有機物と無機物 [ 要点 ] (1) ガスバーナーの操作 火のつけ方: ガス調節ねじと空気調節ねじが閉じていることを確認する 元せんを開く マッチに火をつけてからガス調節ねじをゆるめ, 火をななめ下から近づける 炎の大きさを調整する 炎は最初赤色 ( 空気が少ないから ) 空気調節ねじで炎を青色の三角形にする
本時の評価規準 ( 観点 / 方法 ) 1. 今まで学習したことをもとに, 実験を適切な操作で行い, 各極で発生した物質を同定 することができる ( 観察 実験の技能 / ワークシートへの記述 ) 2. 食塩水に電流を通したときの陽極および陰極での変化の様子を粒子モデルを使って図 示し, そのモデル
 中学校理科 ( 第 1 分野 ) 学習指導案 指導者岸本享子 日 時 平成 29 年 10 月 14 日 ( 土 ) 第 2 限 10:35~11:25 場 所 第 1 化学教室 学年 組 中学校 2 年 B 組 42 人 ( 男子 21 人女子 21 人 ) 単 元 化学変化とイオン 目 標 1. 化学変化についての観察, 実験を通して, 水溶液の電気伝導性や中和反応ついて理解する 2. 水溶液の電気伝導性や中和反応に関する事物
中学校理科 ( 第 1 分野 ) 学習指導案 指導者岸本享子 日 時 平成 29 年 10 月 14 日 ( 土 ) 第 2 限 10:35~11:25 場 所 第 1 化学教室 学年 組 中学校 2 年 B 組 42 人 ( 男子 21 人女子 21 人 ) 単 元 化学変化とイオン 目 標 1. 化学変化についての観察, 実験を通して, 水溶液の電気伝導性や中和反応ついて理解する 2. 水溶液の電気伝導性や中和反応に関する事物
( 高等部 )( 自立活動 )学習指導案
 理科 ( 化学基礎 ) 学習指導案 指導者広島特別支援学校 教諭木村友泰 1 日時 場所平成 28 年 12 月 22 日 ( 木 ) 13:00~13:50 理科室 2 学部 学年 学級高等部第 2 学年 1 組 (Ⅰ 類型男子 3 名 ) 3 単元名酸と塩基 4 単元設定の理由 単元観本単元の目標は, 酸と塩基の性質及び中和反応に関与する物質の量的関係を理解することである 中学校では, 酸 アルカリとイオン
理科 ( 化学基礎 ) 学習指導案 指導者広島特別支援学校 教諭木村友泰 1 日時 場所平成 28 年 12 月 22 日 ( 木 ) 13:00~13:50 理科室 2 学部 学年 学級高等部第 2 学年 1 組 (Ⅰ 類型男子 3 名 ) 3 単元名酸と塩基 4 単元設定の理由 単元観本単元の目標は, 酸と塩基の性質及び中和反応に関与する物質の量的関係を理解することである 中学校では, 酸 アルカリとイオン
< F31312D B C82C E837E>
 11 ヨードチンキとビタミン C で金メッキ 1 目的ヨードチンキを用いて金箔を溶解し金のコロイドを生成する そして実際に金属板に金メッキを行いその反応条件等を検討する 2 原理 金は王水にテトラクロロ金 (Ⅲ) 酸イオン [AuC ç4 ] となって溶けるが ヨードチンキにも テトラヨート 金 (Ⅲ) 酸イオン [AuI] 4 となって溶ける 金箔が次第に細かい粒子となり溶解 して均一な溶液になる
11 ヨードチンキとビタミン C で金メッキ 1 目的ヨードチンキを用いて金箔を溶解し金のコロイドを生成する そして実際に金属板に金メッキを行いその反応条件等を検討する 2 原理 金は王水にテトラクロロ金 (Ⅲ) 酸イオン [AuC ç4 ] となって溶けるが ヨードチンキにも テトラヨート 金 (Ⅲ) 酸イオン [AuI] 4 となって溶ける 金箔が次第に細かい粒子となり溶解 して均一な溶液になる
PowerPoint プレゼンテーション
 薬品分析化学第 8 回 HendersonHasselbalch の式 ( 復習 ) ph 緩衝液 (p 55 ~) 溶液中に共役酸 塩基対が存在しているとき ph p 共役酸 塩基の濃度関係を表す 8 弱酸 HA の平衡式 O H O A において HA H A = mol/l, [A= mol/l とすると O [A より O A A [A となり ph p が導かれる 〇弱酸 HA ( mol/l)
薬品分析化学第 8 回 HendersonHasselbalch の式 ( 復習 ) ph 緩衝液 (p 55 ~) 溶液中に共役酸 塩基対が存在しているとき ph p 共役酸 塩基の濃度関係を表す 8 弱酸 HA の平衡式 O H O A において HA H A = mol/l, [A= mol/l とすると O [A より O A A [A となり ph p が導かれる 〇弱酸 HA ( mol/l)
6年 ゆで卵を取り出そう
 単元計画例 単元計画例は, 東京書籍株式会社 平成 7 年度用新編新しい理科年間指導計画作成 資料 を基に作成した を取り出そう 本授業は, 第 6 学年 溶液の性質とはたらき の単元に位置付け, 溶液には金属を変化さ せるはたらきがあるかを予想し, 金属に塩酸や炭酸を注ぐとどうなるかを調べ, まとめる 時間 に設定されている予備時数を利用し, 更に 時間を加え設定する ( 時間扱い ) 東京書籍
単元計画例 単元計画例は, 東京書籍株式会社 平成 7 年度用新編新しい理科年間指導計画作成 資料 を基に作成した を取り出そう 本授業は, 第 6 学年 溶液の性質とはたらき の単元に位置付け, 溶液には金属を変化さ せるはたらきがあるかを予想し, 金属に塩酸や炭酸を注ぐとどうなるかを調べ, まとめる 時間 に設定されている予備時数を利用し, 更に 時間を加え設定する ( 時間扱い ) 東京書籍
Taro-renshu1
 1 覚えたい元素記号と化学式何度も繰り返して覚えよう! 元素記号 [ ] は原子番号を示す 44! これだけ覚えれば, 大学入試も完璧です [1] 水素 H [16] 硫黄 ( イオウ ) S 臭素 Br [2] ヘリウム He [17] 塩素 Cl クリプトン Kr [3] リチウム Li [18] アルゴン Ar ストロンチウム Sr [4] ベリリウム Be [19] カリウム K 銀 Ag
1 覚えたい元素記号と化学式何度も繰り返して覚えよう! 元素記号 [ ] は原子番号を示す 44! これだけ覚えれば, 大学入試も完璧です [1] 水素 H [16] 硫黄 ( イオウ ) S 臭素 Br [2] ヘリウム He [17] 塩素 Cl クリプトン Kr [3] リチウム Li [18] アルゴン Ar ストロンチウム Sr [4] ベリリウム Be [19] カリウム K 銀 Ag
【FdData中間期末過去問題】中学数学1年(比例と反比例の応用/点の移動/速さ)
 FdDt 中間期末過去問題 中学数学 1 年 ( 比例と反比例の応用 / 点の移動 / 速さ ) http://www.fdtet.com/dt/ 水そうの問題 [ 問題 ](2 学期期末 ) 水が 200 l 入る水そうに, 毎分 8 l の割合で水を入れていく 水を入れはじめてから 分後の水の量を y l とするとき, 次の各問いに答えよ (1), y の関係を式に表せ (2) の変域を求めよ
FdDt 中間期末過去問題 中学数学 1 年 ( 比例と反比例の応用 / 点の移動 / 速さ ) http://www.fdtet.com/dt/ 水そうの問題 [ 問題 ](2 学期期末 ) 水が 200 l 入る水そうに, 毎分 8 l の割合で水を入れていく 水を入れはじめてから 分後の水の量を y l とするとき, 次の各問いに答えよ (1), y の関係を式に表せ (2) の変域を求めよ
_nyusi-rika6geYU_KSK_03.indd
 有名校対策 第 2 回 物質の変化 解答と解説は 149 ページ 1 気体 A~C について, あとの問いに答えなさい ただし, それぞれの気体は水素, 酸素, 窒素, 二 酸化炭素, アンモニアのいずれかです 世田谷学園 気体 Aについて 強いにおいがあるので, においをかぐときは注意しなければならない 水でぬらした 1 リトマス試験紙を近づけると色が変わる 2 下方置換法や 3 水上置換法で集めることはできない
有名校対策 第 2 回 物質の変化 解答と解説は 149 ページ 1 気体 A~C について, あとの問いに答えなさい ただし, それぞれの気体は水素, 酸素, 窒素, 二 酸化炭素, アンモニアのいずれかです 世田谷学園 気体 Aについて 強いにおいがあるので, においをかぐときは注意しなければならない 水でぬらした 1 リトマス試験紙を近づけると色が変わる 2 下方置換法や 3 水上置換法で集めることはできない
質問 2 1イオンには大きさがあると思いますか あると思う人は どれくらいの大きさだと思いますか ある 35 人 ない 5 人 すごく小さい 12 人 原子サイズ 6 人 目に見えない大きさ 5 人 原子より小さい 2 人 種類によってちがう 2 人 分子サイズ 1 人 分子の 10 分の1 1 人
 理科学習指導案 日時 : 平成 25 年 5 月 31 日 ( 金 ) 公開授業 Ⅰ 学級 : 岩手大学教育学部附属中学校 3 年 B 組 40 名会場 : 第 1 理科室授業者 : 佐々木俊 1 単元名 化学変化とイオン 2 単元について (1) 生徒観本単元で扱うイオンを普段の生活の中で経験する機会は少ないと考える 事前調査によると 生活の中においてはドライヤーや空気清浄機などで使用されているマイナスイオン発生装置や
理科学習指導案 日時 : 平成 25 年 5 月 31 日 ( 金 ) 公開授業 Ⅰ 学級 : 岩手大学教育学部附属中学校 3 年 B 組 40 名会場 : 第 1 理科室授業者 : 佐々木俊 1 単元名 化学変化とイオン 2 単元について (1) 生徒観本単元で扱うイオンを普段の生活の中で経験する機会は少ないと考える 事前調査によると 生活の中においてはドライヤーや空気清浄機などで使用されているマイナスイオン発生装置や
【FdData中間期末過去問題】中学理科2年(質量保存/質量の割合/発熱反応/吸熱反応)
 FdData 中間期末 : 中学理科 2 年 : 化学 [ 質量保存の法則 ( 硫酸 + 塩化バリウム )/ 炭酸水素ナトリウム + 塩酸 銅 マグネシウムの加熱 / その他の反応 / 発熱反応 / 吸熱反応 / 化学変化と熱全般 ] [ 理科 2 年 pdf ファイル一覧 ] 質量保存の法則 硫酸 + 塩化バリウム [ 問題 ]( 後期中間改 ) 右の図で, うすい硫酸にうすい塩化バリウム水溶液を混ぜ合わせると,
FdData 中間期末 : 中学理科 2 年 : 化学 [ 質量保存の法則 ( 硫酸 + 塩化バリウム )/ 炭酸水素ナトリウム + 塩酸 銅 マグネシウムの加熱 / その他の反応 / 発熱反応 / 吸熱反応 / 化学変化と熱全般 ] [ 理科 2 年 pdf ファイル一覧 ] 質量保存の法則 硫酸 + 塩化バリウム [ 問題 ]( 後期中間改 ) 右の図で, うすい硫酸にうすい塩化バリウム水溶液を混ぜ合わせると,
10 酸 塩基 クロム酸銅 (Ⅱ) の電気泳動 ~ 陽イオンと陰イオン ~ 難易度教材の入手日数準備時間実施時間 1 カ月 2 時間 50 分 目的と内容 イオン結合でできた物質の電気泳動を行い, 陽イオンと陰イオンの移動から, 静電気的な引力による結合であることを理解する イオンの生成を電子配置と
 10 酸 塩基 クロム酸銅 (Ⅱ) の電気泳動 ~ 陽イオンと陰イオン ~ 難易度教材の入手日数準備時間実施時間 1 カ月 2 時間 50 分 目的と内容 イオン結合でできた物質の電気泳動を行い, 陽イオンと陰イオンの移動から, 静電気的な引力による結合であることを理解する イオンの生成を電子配置と関連付けて理解させるととも に, イオン結合がイオン間の静電気的な引力による結合である ことや, イオン結合でできた物質の性質を理解させること
10 酸 塩基 クロム酸銅 (Ⅱ) の電気泳動 ~ 陽イオンと陰イオン ~ 難易度教材の入手日数準備時間実施時間 1 カ月 2 時間 50 分 目的と内容 イオン結合でできた物質の電気泳動を行い, 陽イオンと陰イオンの移動から, 静電気的な引力による結合であることを理解する イオンの生成を電子配置と関連付けて理解させるととも に, イオン結合がイオン間の静電気的な引力による結合である ことや, イオン結合でできた物質の性質を理解させること
Microsoft PowerPoint - presentation2007_03_acid-base.ppt
 酸塩基平衡と中和滴定 ー復習ー酸塩基の定義 酸 (cid, ラテン語の cetum から と塩基 (se, [likli, アラビア語 lklj ( 植物の灰 J.R. Gluer ( アルカリは酸と相反するもので 塩はこれら つから構成される R. Boyle (79 青色リトマスが酸により赤変することを発見 J.L. GyLussc (775 酸には酸素酸と水素酸の 種類があると考える J. Lieig
酸塩基平衡と中和滴定 ー復習ー酸塩基の定義 酸 (cid, ラテン語の cetum から と塩基 (se, [likli, アラビア語 lklj ( 植物の灰 J.R. Gluer ( アルカリは酸と相反するもので 塩はこれら つから構成される R. Boyle (79 青色リトマスが酸により赤変することを発見 J.L. GyLussc (775 酸には酸素酸と水素酸の 種類があると考える J. Lieig
化学基礎 化学 化学基礎 化学 ( 全問必答 ) 第 1 問次の各問い ( 問 1~ 6 ) に答えよ 解答番号 1 ~ 8 ( 配点 25) 問 1 次の a ~ c に当てはまるものを, それぞれの解答群 1~4 のうちから一つずつ 選べ a Al 3+ と物質量の比 2 :3 で化合物をつくる
 ( 全問必答 ) 第 1 問次の各問い ( 問 1~ 6 ) に答えよ 解答番号 1 ~ 8 ( 配点 5) 問 1 次の a ~ c に当てはまるものを, それぞれの解答群 1~4 のうちから一つずつ 選べ a Al + と物質量の比 : で化合物をつくる多原子イオン 1 1 塩化物イオン 酸化物イオン 硫酸イオン 4 リン酸イオン b 水溶液を白金線につけ, ガスバーナーの外炎に入れると, 黄色の炎が見ら
( 全問必答 ) 第 1 問次の各問い ( 問 1~ 6 ) に答えよ 解答番号 1 ~ 8 ( 配点 5) 問 1 次の a ~ c に当てはまるものを, それぞれの解答群 1~4 のうちから一つずつ 選べ a Al + と物質量の比 : で化合物をつくる多原子イオン 1 1 塩化物イオン 酸化物イオン 硫酸イオン 4 リン酸イオン b 水溶液を白金線につけ, ガスバーナーの外炎に入れると, 黄色の炎が見ら
【】 1次関数の意味
 FdText 数学 1 年 : 中学 塾用教材 http://www.fdtext.com/txt/ 直線と角 解答欄に次のものを書き入れよ 1 直線 AB 2 線分 AB 1 2 1 2 右図のように,3 点 A,B,Cがあるとき, 次の図形を書き入れよ 1 直線 AC 2 線分 BC - 1 - 次の図で a, b, c で示された角を A,B,C,D の文字を使って表せ a : b : c :
FdText 数学 1 年 : 中学 塾用教材 http://www.fdtext.com/txt/ 直線と角 解答欄に次のものを書き入れよ 1 直線 AB 2 線分 AB 1 2 1 2 右図のように,3 点 A,B,Cがあるとき, 次の図形を書き入れよ 1 直線 AC 2 線分 BC - 1 - 次の図で a, b, c で示された角を A,B,C,D の文字を使って表せ a : b : c :

