有機化合物の反応9(2018)講義用.ppt
|
|
|
- あつとし さどひら
- 5 years ago
- Views:
Transcription
1 有機化合物の反応 ( 第 9 回 ) 創薬分子薬学講座薬化学部門 金光卓也
2 ハロゲン化アルキルの反応性 l S N 1 と S N 2 の特徴の復習 l S N 1=Unimolecular Nucleophilic Substitution 単分子求核置換反応 l S N 2=Bimolecular Nucleophilic Substitution 二分子求核置換反応
3 1 反応速度 l S N 1 反応 = 一次反応反応速度はハロゲン化アルキル ( 基質 ) の濃度にのみ比例 l S N 2 反応 = 二次反応反応速度はハロゲン化アルキルと求核試薬両方の濃度に比例 ( 両方の濃度の積に比例 )
4 2 立体化学 l S N 1 反応 =ラセミ体が生成キラルな化合物を反応させるとラセミ体が生成する ( 一部立体反転 ) 立体保持した生成物は 50% 以下 l S N 2 反応 = 立体反転求核試薬が脱離基の反対側から反応するため立体配置が逆になる 100% 立体反転する
5 3 反応の中身 l S N 1 反応中間体を経由する ( カルボカチオン ) 二段階反応 ( 一次反応で 2 段階反応 に注意 ) l S N 2 反応 = 立体反転 中間体が存在しない 一段階反応 ( 二次反応で 1 段階反応 に注意 )
6 4 基質による反応性の変化 l S N 1 反応ハロゲン化アルキルの反応性三級 > 二級 > 一級 >メチル 置換基の多い基質が反応しやすい l S N 2 反応ハロゲン化アルキルの反応性メチル> 一級 > 二級 > 三級 立体障害の小さい基質が反応しやすい
7 求核試薬の反応性 S N 2 反応の場合のみ影響 B r + N u - N u + B r - 求核剤 相対反応性 求核剤 相対反応性 2 O 1 - O N l - 1, 000 O - 16, O 1 O - 25, 000 I - 100, 000 N - 125, 000 S - 125, 000
8 求核試薬の反応性に関する大まかな法則 l 反応する原子の種類が同じものである場合 求核性は塩基性の強さと対応している O - > O - > O O l 同族元素の場合 周期表で下のものほど求核反応性は高い S - > O - I - > B r - > l - l 負に荷電した求核種の方が中性の試薬より反応性が高い O - > 2 O
9 脱離基の反応性 (S N 1 と S N 2 に共通 ) l 負電荷を持っていても安定なものが良い脱離基 負電荷を安定化する因子を持っている X + N u - N u + X - 脱離基 X 相対反応性 脱離基 X 相対反応性 O - < < 1 - N 2 < < 1 O < < 1 F - 1 l B r - 10, 000 I - 30, 000 T s O - 6 0, 0 0 0
10 TsO - とは何か p - トルエンスルホン酸 T s O p - t o l u e n e s u l f o n i c a c i d T s O - t o s y l a t e i o n トシラートイオン + 3 S O 3 3 S O 3 O O O 3 S O 3 S O 3 S O O O O p- トルエンスルホン酸の解離により生成するトシラートイオンは 3 つの等価な共鳴構造式が書けるため極めて安定なイオンである
11 問題 1 (R)-2- ブロモブタンと O - の S N 2 反応でどんな生成物が得られるか
12 解答 1 (R)-2- ブロモブタンと O - の S N 2 反応でどんな生成物が得られるか 解法 1) 基質の構造を正確に書く 2) 脱離基の反対側から O - を接近させる O B r O 2 2 ( R ) b r o m o b u t a n e ( S ) b u t a n o l
13 ハロゲン化アルキル alkyl halide の到達目標 l 有機ハロゲン化合物の代表的な性質と反応を列挙し 説明できる l S N 1 および S N 2 反応の機構について 立体化学を含めて説明できる l 脱ハロゲン化水素の機構を図示し 反応の位置選択性を説明できる
14 脱離反応と置換反応 同じ試薬でも 反応位置の違いにより生成物が異なる O 赤矢印 置換反応青矢印 脱離反応 ハロゲンが結合した隣の水素 ( β 位水素 ) に反応 脱離反応 B r ハロゲンが結合した炭素に反応 O 置換反応
15 脱離反応とは 付加反応の逆反応 一つの出発物質が二つの生成物に分かれるときに起こる l + l 単結合から不飽和結合が生成する
16 この反応は β 脱離と呼ばれる β 水素は β 炭素に結合している β- 炭素 l α- 炭素 ハロゲンは α 炭素に結合している α 位のハロゲンと β 位の水素が脱離するため β 脱離と呼ばれる 官能基が結合している位置を α 位と名付け その隣から順に β( ベータ ) γ( ガンマ ) δ( デルタ ) と呼ぶ
17 参考 )α 脱離も存在する ( 第 8 章 ) クロロホルムと塩基からのジクロロカルベンの生成 ジクロロカルベン α 位のハロゲンと α 位の水素が脱離するため α 脱離と呼ばれる
18 β 位に異なる水素が存在する場合 l 位置選択的な脱離反応が進行する β β 2 B r 主生成物 81% 2-butene 2 2 副生成物 19% 1-butene
19 ザイツェフ則 (Zaitsev 則 ) ハロゲン化アルキルから X が脱離する場合 より多く置換されたアルケンが主生成物となる B r b r o m o b u t a n e E t O N a E t O b u t e n e 8 1 % 1 - b u t e n e 1 9 % 二置換一置換 B r E t O N a 2 E t O b r o m o m e t h y l b u t a n e m e t h y l b u t e n e 7 0 % 三置換 2 - m e t h y l b u t e n e 3 0 % 二置換
20 選択性の出る理由 Δ 安定なアルケンが生成する方向に反応している 置換基の多いアルケン 1-ブテン cis-2-ブテン trans-2-ブテン 還元すると何れもブタンになる kcal / mole butane
21 アルケンの安定性の序列 エネルギーの低下 ( 安定性の上昇 ) R R 1,1- R R R R cis trans R 1,2-1,2- R R R 三置換 R R R R 四置換 二置換
22 問題 2 1- クロロ -1- メチルシクロヘキサンとエタノール中の KO との反応で どんな生成物が期待されるか 問題 3 次のアルケンはどんなハロゲン化アルキルからつくったらよいか
23 解答 2 二置換 三置換 脱離基 lのβ 位には二種類の水素 ( と ) がある 反応が左に進行する場合 が脱離する 二置換アルケン反応が右に進行する場合 が脱離する 三置換アルケン反応は右方向に進行し 1-メチルシクロヘキセンが得られる
24 解答 3a) 二重結合に Br を付加させた構造を考えると 2 つの化合物 (A) と (B) ができる しかし (A) を原料にして脱離を行うと 目的の生成物は得られない 従って (B) が正解 より安定な三置換アルケン
25 解答 3b) 前問と同じように (A) と (B) が考えられる 三置換 : 主生成物 二置換 : 少量 (A) を原料とすると三置換アルケンが主に得られ 目的物は少量 従って (B) が正解
26 E2 反応 (Elimination Bimolecular) l 塩基性の強い求核剤と反応させると 基質と求核剤の両方の濃度に比例して反応が起こる ( ) 3 l + N a O 2 k + N a l + 2 O k [ ( ) 3 l ] [ O ] m o l L - 1 s - 1 反応速度がハロゲン化アルキルと水酸化物イオンの両方の濃度に比例 E2 反応
27 反応機構 O A B D B r E A B E D v=k[alkyl halide][o - ] 2 つの脱離基 とハロゲンは アンチの位置にあるとき ( アンチペリプラナー ) 脱離できる トランス脱離 トランス脱離の結果 反応は立体選択的に進行する 幾何異性体の E 体と Z 体が異なる立体異性体から得られる
28 脱離する置換基間の相互作用 アンチペリプラナー形 Anti periplanar ねじれ形最もエネルギーが低い こちらを経由して反応が進む シンペリプラナー形 Syn periplanar かさなり形最もエネルギーが高い
29 E2 反応の遷移状態 塩基 アンチペリプラナー形の出発物質 遷移状態 と X が同時に遠ざかる Π 結合が生成してアルケンとなる 遷移状態では sp 3 混成軌道から p 軌道への変化が進んでいる 生成する p 軌道が結合性の π 結合になるためには アンチペリプラナーから出発する必要がある
30 .. 3 O :.. 結合ができはじめている sp 3.. 遷移状態 結合が切れ始めている R 二重結合が でき始めている R 結合が切れ始めている sp 3.. : Br.. :
31 E2 反応は 1 段階反応である 遷移状態 TS E N E R G Y 出発物質 活性化エネルギー Ea 反応熱 Δ 生成物
32 2- ブロモ -3- フェニルブタン B r 2 O N a 2 O 主生成物 副生成物 主生成物には シス トランスの異性体が考えられる 作り分けることは可能か? + 2
33 2S,3R 異性体からの主生成物 R S P h B r P h B r 回転 アンチペリプラナー Anti periplanar NaOMe MeO P h 生成しない P h 主生成物 trans (Z) (Z)-2-phenyl-2-butene
34 2S,3S 異性体からの主生成物 S S P h 3 B r P h 回転 生成しない P h B r アンチペリプラナー Anti periplanar NaOMe MeO P h 主生成物 cis (E)
35 環状ハロゲン化アルキルの反応性 1-Bromo-2-methylcyclohexane 予想される主生成物は 2 O N a + B r 2 O 主生成物 副生成物 ザイツェフ則に従い 置換基のより多いアルケンが優先して生成する?
36 cis-1- ブロモ -2- メチルシクロヘキサン 脱離が進行するためには と Br がアンチペリプラナーに位置する必要がある cis 3 Br とBrがいずれもアキシアル となったときに反応が起こる 主生成物 ( ザイツェフ則 ) 3 少量の 3 Br 3 黒い点は が上向きに結合していることを表す trans については次の ppt
37 trans-1- ブロモ -2- メチルシクロヘキサン ザイツェフ則に従う生成物は全く得られない 3 Br trans 3 単一の生成物 3 3 は全く得られない Br
38 trans 体が反応するためには環が反転する必要がある l 塩素はどの水素に対してもアンチペリプラナーの位置をとれない 環反転 KO / EtO l
39 ハロゲンはアキシアルの位置をとれないと脱離できない cis と trans で全く反応性が異なる例 B r N a O E t E t O 反応しない B r N a O E t E t O 3 反応速い t- ブチル基は大きいため エクアトリアルにしか入れない
40 まとめると メチル基とハロゲンが シスの場合とトランスの場合で生成物が異なる重要な反応例 t- ブチル基に対して Br がトランスに位置していると脱離が起こらない シスの場合には反応する
41 E1 反応 l カルボカチオンを経由する反応 生成物は S N 1 由来のものだけではない ( ) 3 X 2 O 3 + X 2 O S N 1 ( ) 3 O % 5 % 上記の反応は ハロゲンXの種類がl Br Iのいずれでも同じ比率で生成物が生じる E 1 2 脱離基がとれた後 生成比が決まる = 反応中間体は共通のカルボカチオン +
42 E1 反応は 2 段階反応である 弱塩基 B : カルボカチオン X slow 第一段階 + + :X 3 o > 2 o > 1 o 単分子反応速度 = k [RX] 第二段階 fast
43 E1 反応におけるエネルギー変化図 カルボカチオン中間体 E N E R G Y TS 1 Ea 1 Ea 2 TS 2 出発物質 step 1 step 2 slow Δ 生成物
44 E2 と E1 の比較 :E1 は立体選択性を示さない syn Br NaOEt EtO / Δ E2 3 3 anti EtO / Δ E1 E1 では 脱離基がアンチペリプラナーをとる必要がなく 安定な生成物を与えるザイツェフ則に従って進行する 3
45 問題 4 (1R,2R)-1,2- ジブロモ -1,2- ジフェニルエタンの E2 脱離で得られるアルケンは どのような立体化学を有しているか
46 解答 4 書き直す ポイント脱離する と Br がアンチペリプラナーの位置にくるような立体構造を書く
Microsoft Word - 化学系演習 aG.docx
 有機化学反応の基礎 (4) 脱離反応 (1) 脱離反応 (E1 と E2 反応 )--- ハロゲン化アルキルの例脱離生成物と安定性原子上のプロトン () と電気陰性度の大きな原子を含む脱離基が脱離し π 結合を形成する 脱離基 Xの結合している炭素 (α 位 ) とその隣の炭素 (β 位 ) からXが脱離するので β 脱離とも呼ばれる ザイツェフ則 ( セイチェフ則 ): 多置換アルケン ( 安定性が高い
有機化学反応の基礎 (4) 脱離反応 (1) 脱離反応 (E1 と E2 反応 )--- ハロゲン化アルキルの例脱離生成物と安定性原子上のプロトン () と電気陰性度の大きな原子を含む脱離基が脱離し π 結合を形成する 脱離基 Xの結合している炭素 (α 位 ) とその隣の炭素 (β 位 ) からXが脱離するので β 脱離とも呼ばれる ザイツェフ則 ( セイチェフ則 ): 多置換アルケン ( 安定性が高い
スライド 1
 ハロゲン化アルキル (alkyl halide) ハロゲン化アルキルの命名法 ハロゲン化アルキルの合成 アルコールからの合成 ハロゲン化アルキルの反応 Grignard( グリニャール ) 試薬求核置換反応 (SN2 反応,SN1 反応 ) 脱離反応 (E2 反応,E1 反応 ) ハロゲン化アルキルの命名法 (1) 段階 1: 最も長い炭素鎖を見つけて, 母体を決める. 多重結合がある場合には, 母体の炭素鎖はそれを含むものでなければならない.
ハロゲン化アルキル (alkyl halide) ハロゲン化アルキルの命名法 ハロゲン化アルキルの合成 アルコールからの合成 ハロゲン化アルキルの反応 Grignard( グリニャール ) 試薬求核置換反応 (SN2 反応,SN1 反応 ) 脱離反応 (E2 反応,E1 反応 ) ハロゲン化アルキルの命名法 (1) 段階 1: 最も長い炭素鎖を見つけて, 母体を決める. 多重結合がある場合には, 母体の炭素鎖はそれを含むものでなければならない.
官能基の酸化レベルと官能基相互変換 還元 酸化 炭化水素 アルコール アルデヒド, ケトン カルボン酸 炭酸 H R R' H H R' R OH H R' R OR'' H R' R Br H R' R NH 2 H R' R SR' R" O R R' RO OR R R' アセタール RS S
 官能基の酸化レベルと官能基相互変換 還元 酸化 炭化水素 アルコール アルデヒド, ケトン カルボン酸 炭酸 ' ' ' '' ' ' 2 ' ' " ' ' アセタール ' チオアセタール -'' ' イミン '' '' 2 C Cl C 二酸化炭素 2 2 尿素 脱水 加水分解 ' 薬品合成化学 小問題 1 1) Al 4 は次のような構造であり, ( ハイドライドイオン ) の求核剤攻撃で還元をおこなう
官能基の酸化レベルと官能基相互変換 還元 酸化 炭化水素 アルコール アルデヒド, ケトン カルボン酸 炭酸 ' ' ' '' ' ' 2 ' ' " ' ' アセタール ' チオアセタール -'' ' イミン '' '' 2 C Cl C 二酸化炭素 2 2 尿素 脱水 加水分解 ' 薬品合成化学 小問題 1 1) Al 4 は次のような構造であり, ( ハイドライドイオン ) の求核剤攻撃で還元をおこなう
Microsoft Word - 化学系演習 aG.docx
 有機化学反応の基礎 () 芳香族化合物 ) 芳香族化合物の性質 ベンゼンに代表される芳香族化合物は 環構造を構成する原子すべてが p 軌道をもち 隣同士の原子間で p 軌道が重なり合うことができるので 電子が非局在化 ( 共鳴安定化 ) している 芳香族性をもつため 求電子付加反応ではなく求電子置換反応を起こしやすい 全ての炭素が sp ² 混成 π 結合 p 軌道 π 電子がドーナツ状に分布し 極めて安定
有機化学反応の基礎 () 芳香族化合物 ) 芳香族化合物の性質 ベンゼンに代表される芳香族化合物は 環構造を構成する原子すべてが p 軌道をもち 隣同士の原子間で p 軌道が重なり合うことができるので 電子が非局在化 ( 共鳴安定化 ) している 芳香族性をもつため 求電子付加反応ではなく求電子置換反応を起こしやすい 全ての炭素が sp ² 混成 π 結合 p 軌道 π 電子がドーナツ状に分布し 極めて安定
練習問題
 生物有機化学 練習問題 ( はじめに ) 1 以下の各問題中で 反応機構を書け ということは 電子の流れを曲がった矢印を用いて説明せよ ということである 単純に生成物を書くだけでは正答とはならない 2 で表される結合は 立体異性体の混合物であることを表す 3 反応式を表す矢印 ( ) に書かれている試薬に番号が付いている場合 1. の試薬 を十分に反応させた後に 2. の試薬を加えることを表す 例えば
生物有機化学 練習問題 ( はじめに ) 1 以下の各問題中で 反応機構を書け ということは 電子の流れを曲がった矢印を用いて説明せよ ということである 単純に生成物を書くだけでは正答とはならない 2 で表される結合は 立体異性体の混合物であることを表す 3 反応式を表す矢印 ( ) に書かれている試薬に番号が付いている場合 1. の試薬 を十分に反応させた後に 2. の試薬を加えることを表す 例えば
02 配付資料(原子と分子・アルカンとアルケンとアルキン).key
 1 4 20 4 23 18:45~ 13 1322 18:45~ 1 113 TEL: 03-5841-4321 E-mail kagaku@chem.s.u-tokyo.ac.jp 2 / 3 / 1s/2s 2s 1s 2s 1s Wikipedia 1s 2s 4 / s, p, d 1, 3, 5 5 / 50 2 2 2 2 6 6 メチルアニオン 陽子 6 個 = 正電荷 6 1s 電子
1 4 20 4 23 18:45~ 13 1322 18:45~ 1 113 TEL: 03-5841-4321 E-mail kagaku@chem.s.u-tokyo.ac.jp 2 / 3 / 1s/2s 2s 1s 2s 1s Wikipedia 1s 2s 4 / s, p, d 1, 3, 5 5 / 50 2 2 2 2 6 6 メチルアニオン 陽子 6 個 = 正電荷 6 1s 電子
スライド 1
 立体構造の表し方 眼 こちらから見ると 破線 - くさび型表示 実線 破線 くさび型線の 種類で官能基の立体的な配置を示す ( 最もよく使われる ) sp 混成は 正四面体 構造であることを思い出す! 破線 -くさび型表示 ニューマン投影式 フィッシャー投影式 実線 ( 結合は紙面上 ) 破線 ( 結合は紙面よりも奥側 ) くさび型線 ( 結合は紙面よりも手前側 ) こちらから見たものを押しつぶして書くと
立体構造の表し方 眼 こちらから見ると 破線 - くさび型表示 実線 破線 くさび型線の 種類で官能基の立体的な配置を示す ( 最もよく使われる ) sp 混成は 正四面体 構造であることを思い出す! 破線 -くさび型表示 ニューマン投影式 フィッシャー投影式 実線 ( 結合は紙面上 ) 破線 ( 結合は紙面よりも奥側 ) くさび型線 ( 結合は紙面よりも手前側 ) こちらから見たものを押しつぶして書くと
有機化合物の反応10(2018)講義用.ppt
 有機化合物の反応 ( 第 10 回 ) 創薬分子薬学講座薬化学部門 金光卓也 第 14 章 到達目標 l 共役ジエンの性質及びアルケンとの相違点について説明できる l 化学反応で用いられる 速度支配 熱力学支配 という用語の意味を説明できる l Diels-Alder 反応の特徴を具体例を用いて説明できる l 共役と有機化合物の色の関係について説明できる 14.1 共役化合物 共役 conjugation
有機化合物の反応 ( 第 10 回 ) 創薬分子薬学講座薬化学部門 金光卓也 第 14 章 到達目標 l 共役ジエンの性質及びアルケンとの相違点について説明できる l 化学反応で用いられる 速度支配 熱力学支配 という用語の意味を説明できる l Diels-Alder 反応の特徴を具体例を用いて説明できる l 共役と有機化合物の色の関係について説明できる 14.1 共役化合物 共役 conjugation
スライド 1
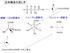 立体構造の表し方 O O 眼 こちらから見ると O 破線 - くさび型表示ニューマン投影式フィッシャー投影式 OO OO OO O 23 O 3 O 2 3 こちらから見たものを押しつぶして書くと 破線 - くさび型表示 実線 破線 くさび型線の 3 種類で官能基の立体的な配置を示す ( 最もよく使われる ) sp 3 混成は 正四面体 構造であることを思い出す! 実線 ( 結合は紙面上 ) O OO
立体構造の表し方 O O 眼 こちらから見ると O 破線 - くさび型表示ニューマン投影式フィッシャー投影式 OO OO OO O 23 O 3 O 2 3 こちらから見たものを押しつぶして書くと 破線 - くさび型表示 実線 破線 くさび型線の 3 種類で官能基の立体的な配置を示す ( 最もよく使われる ) sp 3 混成は 正四面体 構造であることを思い出す! 実線 ( 結合は紙面上 ) O OO
有機化学I 小テスト4 回答 担当:石川勇人
 有機化学 I 小テスト 担当 : 石川勇人 問題 1: 次に示す化合物を IUPAC 命名法にしたがって命名せよ C 2 C 2 CC 2 CC C 2 CC 2 C 2 C 2 C 回答の指針 : 有機化合物の命名法である IUPAC の命名法に従う 以下解説する 7 8 9 C 2 9 8 7 6 5 3 2 1 C 2 CC 2 CC 1 2 3 5 6 上記の化合物について命名する際は まず
有機化学 I 小テスト 担当 : 石川勇人 問題 1: 次に示す化合物を IUPAC 命名法にしたがって命名せよ C 2 C 2 CC 2 CC C 2 CC 2 C 2 C 2 C 回答の指針 : 有機化合物の命名法である IUPAC の命名法に従う 以下解説する 7 8 9 C 2 9 8 7 6 5 3 2 1 C 2 CC 2 CC 1 2 3 5 6 上記の化合物について命名する際は まず
Problem P5
 問題 P5 メンシュトキン反応 三級アミンとハロゲン化アルキルの間の求核置換反応はメンシュトキン反応として知られている この実験では DABCO(1,4 ジアザビシクロ [2.2.2] オクタン というアミンと臭化ベンジルの間の反応速度式を調べる N N Ph Br N N Br DABCO Ph DABCO 分子に含まれるもう片方の窒素も さらに他の臭化ベンジルと反応する可能性がある しかし この実験では
問題 P5 メンシュトキン反応 三級アミンとハロゲン化アルキルの間の求核置換反応はメンシュトキン反応として知られている この実験では DABCO(1,4 ジアザビシクロ [2.2.2] オクタン というアミンと臭化ベンジルの間の反応速度式を調べる N N Ph Br N N Br DABCO Ph DABCO 分子に含まれるもう片方の窒素も さらに他の臭化ベンジルと反応する可能性がある しかし この実験では
B. モル濃度 速度定数と化学反応の速さ 1.1 段階反応 ( 単純反応 ): + I HI を例に H ヨウ化水素 HI が生成する速さ は,H と I のモル濃度をそれぞれ [ ], [ I ] [ H ] [ I ] に比例することが, 実験により, わかっている したがって, 比例定数を k
![B. モル濃度 速度定数と化学反応の速さ 1.1 段階反応 ( 単純反応 ): + I HI を例に H ヨウ化水素 HI が生成する速さ は,H と I のモル濃度をそれぞれ [ ], [ I ] [ H ] [ I ] に比例することが, 実験により, わかっている したがって, 比例定数を k B. モル濃度 速度定数と化学反応の速さ 1.1 段階反応 ( 単純反応 ): + I HI を例に H ヨウ化水素 HI が生成する速さ は,H と I のモル濃度をそれぞれ [ ], [ I ] [ H ] [ I ] に比例することが, 実験により, わかっている したがって, 比例定数を k](/thumbs/81/83835231.jpg) 反応速度 触媒 速度定数 反応次数について. 化学反応の速さの表し方 速さとは単位時間あたりの変化の大きさである 大きさの値は 0 以上ですから, 速さは 0 以上の値をとる 化学反応の速さは単位時間あたりの物質のモル濃度変化の大きさで表すのが一般的 たとえば, a + bb c (, B, は物質, a, b, c は係数 ) という反応において,, B, それぞれの反応の速さを, B, とし,
反応速度 触媒 速度定数 反応次数について. 化学反応の速さの表し方 速さとは単位時間あたりの変化の大きさである 大きさの値は 0 以上ですから, 速さは 0 以上の値をとる 化学反応の速さは単位時間あたりの物質のモル濃度変化の大きさで表すのが一般的 たとえば, a + bb c (, B, は物質, a, b, c は係数 ) という反応において,, B, それぞれの反応の速さを, B, とし,
第11回配布用
 07 年度有機化学 および演習第 回 (07.07.06) (06 年度以前入学者は有機化学序論 ) 担当山下誠居室 号館 0 階 03 号室 e-mail makoto@oec.chembio.nagoya-u.ac.jp 7/3( 木 ) 休講 7/5( 土 ) 限補講 @ 演習で解説してほしい問題は田浦先生 (taura@chembio.nagoya-u.ac.jp) と荒巻先生 (aramaki@chembio.nagoya-u.ac.jp)
07 年度有機化学 および演習第 回 (07.07.06) (06 年度以前入学者は有機化学序論 ) 担当山下誠居室 号館 0 階 03 号室 e-mail makoto@oec.chembio.nagoya-u.ac.jp 7/3( 木 ) 休講 7/5( 土 ) 限補講 @ 演習で解説してほしい問題は田浦先生 (taura@chembio.nagoya-u.ac.jp) と荒巻先生 (aramaki@chembio.nagoya-u.ac.jp)
木村の有機化学小ネタ 糖の構造 単糖類の鎖状構造と環状構造 1.D と L について D-グルコースとか L-アラニンの D,L の意味について説明する 1953 年右旋性 ( 偏光面を右に曲げる ) をもつグリセルアルデヒドの立体配置が
 糖の構造 単糖類の鎖状構造と環状構造.D と L について D-グルコースとか L-アラニンの D,L の意味について説明する 9 年右旋性 ( 偏光面を右に曲げる ) をもつグリセルアルデヒドの立体配置が X 線回折実験により決定され, 次の約束に従い, 構造式が示された 最も酸化された基を上端にする 上下の原子または原子団は中心原子より紙面奥に位置する 左右の原子または原子団は中心原子より紙面手前に位置する
糖の構造 単糖類の鎖状構造と環状構造.D と L について D-グルコースとか L-アラニンの D,L の意味について説明する 9 年右旋性 ( 偏光面を右に曲げる ) をもつグリセルアルデヒドの立体配置が X 線回折実験により決定され, 次の約束に従い, 構造式が示された 最も酸化された基を上端にする 上下の原子または原子団は中心原子より紙面奥に位置する 左右の原子または原子団は中心原子より紙面手前に位置する
酸化的付加 (oxidative addition)
 酸化的付加 酸化的付加 oxidative addition 有機反応との類似点 Grignard 試薬の生成カルベン挿入反応 二核錯体上での酸化的付加 金属の酸化数 :+1 d 電子数 :-1 酸化的配位 求電子剤の配位により形式的に金属が酸化される ( 結合の切断が進行しない点で 酸化的付加と区別 ) 傾向 1. 電子豊富な金属中心の方が有利 2. 立体的に空いている金属中心の方が有利 3. 非極性結合の酸化的付加では
酸化的付加 酸化的付加 oxidative addition 有機反応との類似点 Grignard 試薬の生成カルベン挿入反応 二核錯体上での酸化的付加 金属の酸化数 :+1 d 電子数 :-1 酸化的配位 求電子剤の配位により形式的に金属が酸化される ( 結合の切断が進行しない点で 酸化的付加と区別 ) 傾向 1. 電子豊富な金属中心の方が有利 2. 立体的に空いている金属中心の方が有利 3. 非極性結合の酸化的付加では
PowerPoint プレゼンテーション
 酵素 : タンパク質の触媒 タンパク質 Protein 酵素 Enzyme 触媒 Catalyst 触媒 Cataylst: 特定の化学反応の反応速度を速める物質 自身は反応の前後で変化しない 酵素 Enzyme: タンパク質の触媒 触媒作用を持つタンパク質 第 3 回 : タンパク質はアミノ酸からなるポリペプチドである 第 4 回 : タンパク質は様々な立体構造を持つ 第 5 回 : タンパク質の立体構造と酵素活性の関係
酵素 : タンパク質の触媒 タンパク質 Protein 酵素 Enzyme 触媒 Catalyst 触媒 Cataylst: 特定の化学反応の反応速度を速める物質 自身は反応の前後で変化しない 酵素 Enzyme: タンパク質の触媒 触媒作用を持つタンパク質 第 3 回 : タンパク質はアミノ酸からなるポリペプチドである 第 4 回 : タンパク質は様々な立体構造を持つ 第 5 回 : タンパク質の立体構造と酵素活性の関係
Microsoft Word - 問題解答.doc
 第 15 章例題 1 以下に示す化合物に正しい IUPAC 名を付けなさい 3) 4) C 3 N C3 2 5) 3 C m- ブロモクロロベンゼン p- ブロモアニリン 3)2,6- ジブロモフェノール 4)1,2,3,5- テトラメチルベンゼン 5)3- メチルブチルベンゼン 例題 2 次の名前に相当する構造を書きなさい (a) 3-メチル 1,2-ベンゼンジアミン (b) 1,3,5-ベンゼントリオール
第 15 章例題 1 以下に示す化合物に正しい IUPAC 名を付けなさい 3) 4) C 3 N C3 2 5) 3 C m- ブロモクロロベンゼン p- ブロモアニリン 3)2,6- ジブロモフェノール 4)1,2,3,5- テトラメチルベンゼン 5)3- メチルブチルベンゼン 例題 2 次の名前に相当する構造を書きなさい (a) 3-メチル 1,2-ベンゼンジアミン (b) 1,3,5-ベンゼントリオール
Microsoft Word - answer2013.doc
 ビギナーズ有機化学第二版 練習問題解答例 2013.3.20 作成 第 2 章 2.1 s 軌道電子 :1 種類のみで 対称な球形の電子分布をもつ p 軌道電子 :3 種類あり 互いに直交する方向性をもった電子分布をもつ 2.2 Li + B Mg Al 3+ S 2- l - a 陽子数 : 3 5 12 13 16 17 20 電子数 : 2 5 12 10 18 18 20 2.3 水素化物イオンは最外殻
ビギナーズ有機化学第二版 練習問題解答例 2013.3.20 作成 第 2 章 2.1 s 軌道電子 :1 種類のみで 対称な球形の電子分布をもつ p 軌道電子 :3 種類あり 互いに直交する方向性をもった電子分布をもつ 2.2 Li + B Mg Al 3+ S 2- l - a 陽子数 : 3 5 12 13 16 17 20 電子数 : 2 5 12 10 18 18 20 2.3 水素化物イオンは最外殻
4. 炭素 炭素多重結合 不飽和炭化水素 4.1. C=C 結合 2p 2p z 4-1 2p z 2s 2p z 混成 sp 2 混成軌道 σ 結合を作る C σ π Trigonal 正三角形 + C C π 軌道 2p z 2p z C: sp 2 sp 2 : C π 電子の非局在化 安定化
 4. 炭素 炭素多重結合 不飽和炭化水素 4.1. = 結合 2p 4-1 2s 混成 2 混成軌道 σ 結合を作る σ Trigonal 正三角形 + 軌道 : 2 2 : 電子の非局在化 安定化 (σ 軌道より小さい ) σ σ 結合 結合 例 )ethylene (ethene) 120 回転は困難 4.2. 結合 2s 2p 混成 混成軌道 σ 結合を作る Linear 直線 安定化 非局在化
4. 炭素 炭素多重結合 不飽和炭化水素 4.1. = 結合 2p 4-1 2s 混成 2 混成軌道 σ 結合を作る σ Trigonal 正三角形 + 軌道 : 2 2 : 電子の非局在化 安定化 (σ 軌道より小さい ) σ σ 結合 結合 例 )ethylene (ethene) 120 回転は困難 4.2. 結合 2s 2p 混成 混成軌道 σ 結合を作る Linear 直線 安定化 非局在化
2014 年度大学入試センター試験解説 化学 Ⅰ 第 1 問物質の構成 1 問 1 a 1 g に含まれる分子 ( 分子量 M) の数は, アボガドロ定数を N A /mol とすると M N A 個 と表すことができる よって, 分子量 M が最も小さい分子の分子数が最も多い 分 子量は, 1 H
 01 年度大学入試センター試験解説 化学 Ⅰ 第 1 問物質の構成 1 問 1 a 1 g に含まれる分子 ( 分子量 M) の数は, アボガドロ定数を N A /mol とすると M N A 個 と表すことができる よって, 分子量 M が最も小さい分子の分子数が最も多い 分 子量は, 1 = 18 N = 8 3 6 = 30 Ne = 0 5 = 3 6 l = 71 となり,1 が解答 (
01 年度大学入試センター試験解説 化学 Ⅰ 第 1 問物質の構成 1 問 1 a 1 g に含まれる分子 ( 分子量 M) の数は, アボガドロ定数を N A /mol とすると M N A 個 と表すことができる よって, 分子量 M が最も小さい分子の分子数が最も多い 分 子量は, 1 = 18 N = 8 3 6 = 30 Ne = 0 5 = 3 6 l = 71 となり,1 が解答 (
木村の理論化学小ネタ 熱化学方程式と反応熱の分類発熱反応と吸熱反応化学反応は, 反応の前後の物質のエネルギーが異なるため, エネルギーの出入りを伴い, それが, 熱 光 電気などのエネルギーの形で現れる とくに, 化学変化と熱エネルギーの関
 熱化学方程式と反応熱の分類発熱反応と吸熱反応化学反応は, 反応の前後の物質のエネルギーが異なるため, エネルギーの出入りを伴い, それが, 熱 光 電気などのエネルギーの形で現れる とくに, 化学変化と熱エネルギーの関係を扱う化学の一部門を熱化学という 発熱反応反応前の物質のエネルギー 大ネルギ熱エネルギーー小エ反応後の物質のエネルギー 吸熱反応 反応後の物質のエネルギー 大ネルギー熱エネルギー小エ反応前の物質のエネルギー
熱化学方程式と反応熱の分類発熱反応と吸熱反応化学反応は, 反応の前後の物質のエネルギーが異なるため, エネルギーの出入りを伴い, それが, 熱 光 電気などのエネルギーの形で現れる とくに, 化学変化と熱エネルギーの関係を扱う化学の一部門を熱化学という 発熱反応反応前の物質のエネルギー 大ネルギ熱エネルギーー小エ反応後の物質のエネルギー 吸熱反応 反応後の物質のエネルギー 大ネルギー熱エネルギー小エ反応前の物質のエネルギー
2004 年度センター化学 ⅠB p1 第 1 問問 1 a 水素結合 X HLY X,Y= F,O,N ( ) この形をもつ分子は 5 NH 3 である 1 5 b 昇華性の物質 ドライアイス CO 2, ヨウ素 I 2, ナフタレン 2 3 c 総電子数 = ( 原子番号 ) d CH 4 :6
 004 年度センター化学 ⅠB p 第 問問 a 水素結合 X HLY X,Y= F,O,N ( ) この形をもつ分子は 5 NH である 5 b 昇華性の物質 ドライアイス CO, ヨウ素 I, ナフタレン c 総電子数 = ( 原子番号 ) d CH 4 :6+ 4 = 0個 6+ 8= 4個 7+ 8= 5個 + 7= 8個 4 + 8= 0個 5 8= 6個 4 構造式からアプローチして電子式を書くと次のようになる
004 年度センター化学 ⅠB p 第 問問 a 水素結合 X HLY X,Y= F,O,N ( ) この形をもつ分子は 5 NH である 5 b 昇華性の物質 ドライアイス CO, ヨウ素 I, ナフタレン c 総電子数 = ( 原子番号 ) d CH 4 :6+ 4 = 0個 6+ 8= 4個 7+ 8= 5個 + 7= 8個 4 + 8= 0個 5 8= 6個 4 構造式からアプローチして電子式を書くと次のようになる
三重大学工学部
 反応理論化学 ( その5 6 ポテンシャルエネルギー面と反応経路最も簡単な反応 X + Y X + Y 反応物 ( 生成物 (P X 結合が切断反応系全体のエネルギーは X と Y の Y 結合が形成原子間距離によって変化 r(x と r( Y に対してエネルギーを等高線で表す赤矢印 P:X 結合の切断と Y 結合の形成が同時進行青矢印 P: まず X 結合が切断し次いで Y 結合が形成 谷 X +
反応理論化学 ( その5 6 ポテンシャルエネルギー面と反応経路最も簡単な反応 X + Y X + Y 反応物 ( 生成物 (P X 結合が切断反応系全体のエネルギーは X と Y の Y 結合が形成原子間距離によって変化 r(x と r( Y に対してエネルギーを等高線で表す赤矢印 P:X 結合の切断と Y 結合の形成が同時進行青矢印 P: まず X 結合が切断し次いで Y 結合が形成 谷 X +
三重大学工学部
 反応理論化学 ( その 軌道相互作用 複数の原子が相互作用して分子が形成される複数の原子軌道 ( または混成軌道 が混合して分子軌道が形成される原子軌道 ( または混成軌道 が混合して分子軌道に変化すると軌道エネルギーも変化する. 原子軌道 原子軌道は3つの量子数 ( nlm,, の組合せにより指定される量子数の取り得る値の範囲 n の値が定まる l の範囲は n の値に依存して定まる m の範囲は
反応理論化学 ( その 軌道相互作用 複数の原子が相互作用して分子が形成される複数の原子軌道 ( または混成軌道 が混合して分子軌道が形成される原子軌道 ( または混成軌道 が混合して分子軌道に変化すると軌道エネルギーも変化する. 原子軌道 原子軌道は3つの量子数 ( nlm,, の組合せにより指定される量子数の取り得る値の範囲 n の値が定まる l の範囲は n の値に依存して定まる m の範囲は
Microsoft PowerPoint - 有機元素化学特論11回配布用.pptx
 フッ素化合物の沸点比較 80 80.5 323 フッ素の異常性 ハロゲン - リチウム交換 n-buli R 3 C X R 3 C Li X =, Br, I n-buli R 3 C R 3 C Li フッ素化学入門日本学術振興会フッ素化学第 155 委員会三共出版 2010 ISB 4782706286 フッ素の異常性の原因となる性質 含フッ素生理活性物質 創薬科学入門久能祐子監修佐藤健太郎著オーム社
フッ素化合物の沸点比較 80 80.5 323 フッ素の異常性 ハロゲン - リチウム交換 n-buli R 3 C X R 3 C Li X =, Br, I n-buli R 3 C R 3 C Li フッ素化学入門日本学術振興会フッ素化学第 155 委員会三共出版 2010 ISB 4782706286 フッ素の異常性の原因となる性質 含フッ素生理活性物質 創薬科学入門久能祐子監修佐藤健太郎著オーム社
平成20年度 神戸大学 大学院理学研究科 化学専攻 入学試験問題
 化学 Ⅰ- 表紙 平成 31 年度神戸大学大学院理学研究科化学専攻入学試験 化学 Ⅰ 試験時間 10:30-11:30(60 分 ) 表紙を除いて 7 ページあります 問題 [Ⅰ]~ 問題 [Ⅵ] の中から 4 題を選択して 解答しなさい 各ページ下端にある 選択する 選択しない のうち 該当する方を丸で囲みなさい 各ページに ( 用紙上端 ) と ( 用紙下端 ) を記入しなさい を誤って記入すると採点の対象とならないことがあります
化学 Ⅰ- 表紙 平成 31 年度神戸大学大学院理学研究科化学専攻入学試験 化学 Ⅰ 試験時間 10:30-11:30(60 分 ) 表紙を除いて 7 ページあります 問題 [Ⅰ]~ 問題 [Ⅵ] の中から 4 題を選択して 解答しなさい 各ページ下端にある 選択する 選択しない のうち 該当する方を丸で囲みなさい 各ページに ( 用紙上端 ) と ( 用紙下端 ) を記入しなさい を誤って記入すると採点の対象とならないことがあります
鎖状立体制御概論 ここでは鎖状立体制御の考え方の基本をざっくりとまとめておきます 有機化学では 考え方の習得 は 図を書いて他人に説明できる ことを意味しますので 図を何回も書くことが習得の近道となります 習得 はつまるところ 体得 です 有機化学が 好き なだけではなく 上達する ことや 研究でき
 鎖状立体制御概論 ここでは鎖状立体制御の考え方の基本をざっくりとまとめておきます 有機化学では 考え方の習得 は 図を書いて他人に説明できる ことを意味しますので 図を何回も書くことが習得の近道となります 習得 はつまるところ 体得 です 有機化学が 好き なだけではなく 上達する ことや 研究できるようになる ためには 遷移状態の考え方を体得しけなければなりません これ無しでは いつまでたっても空論を語ることしかできなくなってしまいます
鎖状立体制御概論 ここでは鎖状立体制御の考え方の基本をざっくりとまとめておきます 有機化学では 考え方の習得 は 図を書いて他人に説明できる ことを意味しますので 図を何回も書くことが習得の近道となります 習得 はつまるところ 体得 です 有機化学が 好き なだけではなく 上達する ことや 研究できるようになる ためには 遷移状態の考え方を体得しけなければなりません これ無しでは いつまでたっても空論を語ることしかできなくなってしまいます
改訂履歴 2018/7/30 Ver.1.0 公開 2018/10/02 Ver.1.1 公開 ( 図表 1.1 Marvin JS のダウンロード 利用先 URL を追記 )
 少量新規化学物質の構造式ファイル作成に 係る事業者ガイダンス 第 1.1 版 平成 30 年 7 月 30 日 経済産業省製造産業局 化学物質管理課化学物質安全室 改訂履歴 2018/7/30 Ver.1.0 公開 2018/10/02 Ver.1.1 公開 ( 図表 1.1 Marvin JS のダウンロード 利用先 URL を追記 ) 目次 目次 1. 本ガイダンスの位置付け... 1 2. 構造情報を作成する対象の選択方法...
少量新規化学物質の構造式ファイル作成に 係る事業者ガイダンス 第 1.1 版 平成 30 年 7 月 30 日 経済産業省製造産業局 化学物質管理課化学物質安全室 改訂履歴 2018/7/30 Ver.1.0 公開 2018/10/02 Ver.1.1 公開 ( 図表 1.1 Marvin JS のダウンロード 利用先 URL を追記 ) 目次 目次 1. 本ガイダンスの位置付け... 1 2. 構造情報を作成する対象の選択方法...
<4D F736F F D20914F8AFA8AFA96968E8E8CB15F89F0939A97E12E646F6378>
 平成 23 年度無機化学 2 期末試験 (7/27 実施 ) 解答例 担当榎本真哉 問題間の平均得点には差が生じていますが 全員がどれも自由に選択できる形式ですので 得点調整は行いません 母数には問題番号だけ書いて解答しなかった人も含まれます 参考までに問 1 問 2 問 3 問 4 問 5 問 6 問 7 問 8 問 9 計平均点 9.3 8.7 9.2 5.7 8.4 10.3 15.1 7.1
平成 23 年度無機化学 2 期末試験 (7/27 実施 ) 解答例 担当榎本真哉 問題間の平均得点には差が生じていますが 全員がどれも自由に選択できる形式ですので 得点調整は行いません 母数には問題番号だけ書いて解答しなかった人も含まれます 参考までに問 1 問 2 問 3 問 4 問 5 問 6 問 7 問 8 問 9 計平均点 9.3 8.7 9.2 5.7 8.4 10.3 15.1 7.1
(Microsoft Word - 01\203\213\203C\203X\216\256\202\306\213\244\226\302.doc)
 1. ルイス構造式 学習内容と目標 ルイス構造式の書き方 中心原子と周辺原子 形式電荷の求め方 ルイス構造式とケクレ構造式の相互の書き換え 省略された非共有電子対が表記できるようになること 2.1 はじめに ルイス構造式はアメリカ物理化学者のルイス (G..Lewis, 1916 年 ) によって考案された表記法である 化学結合の性 質や分子の形あるいは反応機構の記述をするために, きわめ て有用な表記法である
1. ルイス構造式 学習内容と目標 ルイス構造式の書き方 中心原子と周辺原子 形式電荷の求め方 ルイス構造式とケクレ構造式の相互の書き換え 省略された非共有電子対が表記できるようになること 2.1 はじめに ルイス構造式はアメリカ物理化学者のルイス (G..Lewis, 1916 年 ) によって考案された表記法である 化学結合の性 質や分子の形あるいは反応機構の記述をするために, きわめ て有用な表記法である
スライド 1
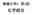 無機化学 II 第 3 回 化学結合 本日のポイント 分子軌道 原子が近づく 原子軌道が重なる 軌道が重なると, 原子軌道が組み合わさって 分子軌道 というものに変化 ( 分子に広がる ) 結合性軌道と反結合性軌道 軌道の重なりが大きい = エネルギー変化が大 分子軌道に電子が詰まった時に, 元の原子よりエネルギーが下がるなら結合を作る. 混成軌道と原子価結合法 ( もっと単純な考え方 ) わかりやすく,
無機化学 II 第 3 回 化学結合 本日のポイント 分子軌道 原子が近づく 原子軌道が重なる 軌道が重なると, 原子軌道が組み合わさって 分子軌道 というものに変化 ( 分子に広がる ) 結合性軌道と反結合性軌道 軌道の重なりが大きい = エネルギー変化が大 分子軌道に電子が詰まった時に, 元の原子よりエネルギーが下がるなら結合を作る. 混成軌道と原子価結合法 ( もっと単純な考え方 ) わかりやすく,
Microsoft Word - t30_西_修正__ doc
 反応速度と化学平衡 金沢工業大学基礎教育部西誠 ねらい 化学反応とは分子を構成している原子が組み換り 新しい分子構造を持つことといえます この化学反応がどのように起こるのか どのような速さでどの程度の分子が組み換るのかは 反応の種類や 濃度 温度などの条件で決まってきます そして このような反応の進行方向や速度を正確に予測するために いろいろな数学 物理的な考え方を取り入れて化学反応の理論体系が作られています
反応速度と化学平衡 金沢工業大学基礎教育部西誠 ねらい 化学反応とは分子を構成している原子が組み換り 新しい分子構造を持つことといえます この化学反応がどのように起こるのか どのような速さでどの程度の分子が組み換るのかは 反応の種類や 濃度 温度などの条件で決まってきます そして このような反応の進行方向や速度を正確に予測するために いろいろな数学 物理的な考え方を取り入れて化学反応の理論体系が作られています
Microsoft PowerPoint - D.酸塩基(2)
 D. 酸塩基 (2) 1. 多塩基酸の ph 2. 塩の濃度と ph 3. 緩衝溶液と ph 4. 溶解度積と ph 5. 酸塩基指示薬 D. 酸塩基 (2) 1. 多塩基酸の ph 1. 多塩基酸の ph (1) 硫酸 H 2 SO 4 ( 濃度 C) 硫酸 H 2 SO 4 は2 段階で電離する K (C) (C) K a1 [H+ ][HSO 4 ] [H 2 SO 4 ] 10 5 第 1
D. 酸塩基 (2) 1. 多塩基酸の ph 2. 塩の濃度と ph 3. 緩衝溶液と ph 4. 溶解度積と ph 5. 酸塩基指示薬 D. 酸塩基 (2) 1. 多塩基酸の ph 1. 多塩基酸の ph (1) 硫酸 H 2 SO 4 ( 濃度 C) 硫酸 H 2 SO 4 は2 段階で電離する K (C) (C) K a1 [H+ ][HSO 4 ] [H 2 SO 4 ] 10 5 第 1
7-7.. 偏光 Polarized Light に対する性質 a) 光学活性 ptical Activity 鏡像異性体 : 偏光 Polarized Light に対する挙動が違う 光 偏光子 Polarizer 1 偏光 偏光子 ( 検光子 ) Not transmitted 偏光子 1 セル
 7. 立体化学 Stereochemistry B. 立体配置 onfiguration と立体異性体 Stereoisomers 7.1. 不斉 Asymmetry と鏡像異性体 Enantiomers 対称面 A Plane of Symmetry が存在 アキラル Achiral 7-1 ex.) -butanol * * * 不斉炭素原子 Asymmetric arbon 対称面 A Plane
7. 立体化学 Stereochemistry B. 立体配置 onfiguration と立体異性体 Stereoisomers 7.1. 不斉 Asymmetry と鏡像異性体 Enantiomers 対称面 A Plane of Symmetry が存在 アキラル Achiral 7-1 ex.) -butanol * * * 不斉炭素原子 Asymmetric arbon 対称面 A Plane
Chap. 1 NMR
 β α β α ν γ π ν γ ν 23,500 47,000 ν = 100 Mz ν = 200 Mz ν δ δ 10 8 6 4 2 0 δ ppm) Br C C Br C C Cl Br C C Cl Br C C Br C 2 2 C C3 3 C 2 C C3 C C C C C δ δ 10 8 6 4 δ ppm) 2 0 ν 10 8 6 4 δ ppm) 2 0 (4)
β α β α ν γ π ν γ ν 23,500 47,000 ν = 100 Mz ν = 200 Mz ν δ δ 10 8 6 4 2 0 δ ppm) Br C C Br C C Cl Br C C Cl Br C C Br C 2 2 C C3 3 C 2 C C3 C C C C C δ δ 10 8 6 4 δ ppm) 2 0 ν 10 8 6 4 δ ppm) 2 0 (4)
有機物質 V 演習問題 以下の化合物 A O の化合物名を書きなさい Ph NH 2 A HO Ph NH 2 B HO C O NH 2 HO HN D O HO HN E N O O O Br Br N H H 2 N N OH F G H I OH O 1 OH J O O O O
 有機物質 V 演習問題 12 1. 以下の化合物 の化合物名を書きなさい r r 2 F G I 1 J K L M : (2R,3)-3-phenylbutan-2-amine : (2R,3)-2-amino-3-phenylbutanol : (3R)-3-amino-4-hydroxylbutan-2-one : (2R)-2-hydroxymethyl-1-azacyclopentan-3-one
有機物質 V 演習問題 12 1. 以下の化合物 の化合物名を書きなさい r r 2 F G I 1 J K L M : (2R,3)-3-phenylbutan-2-amine : (2R,3)-2-amino-3-phenylbutanol : (3R)-3-amino-4-hydroxylbutan-2-one : (2R)-2-hydroxymethyl-1-azacyclopentan-3-one
スライド 1
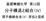 基礎無機化学第 回 分子構造と結合 (IV) 原子価結合法 (II): 昇位と混成 本日のポイント 昇位と混成 s 軌道と p 軌道を混ぜて, 新しい軌道を作る sp 3 混成 : 正四面体型 sp 混成 : 三角形 (p 軌道が つ残る ) sp 混成 : 直線形 (p 軌道が つ残る ) 多重結合との関係炭素などでは以下が基本 ( たまに違う ) 二重結合 sp 混成三重結合 sp 混成 逆に,
基礎無機化学第 回 分子構造と結合 (IV) 原子価結合法 (II): 昇位と混成 本日のポイント 昇位と混成 s 軌道と p 軌道を混ぜて, 新しい軌道を作る sp 3 混成 : 正四面体型 sp 混成 : 三角形 (p 軌道が つ残る ) sp 混成 : 直線形 (p 軌道が つ残る ) 多重結合との関係炭素などでは以下が基本 ( たまに違う ) 二重結合 sp 混成三重結合 sp 混成 逆に,
<4D F736F F F696E74202D20974C8B4089BB8D8795A882CC97A791CC8D5C91A24850>
 章での重要事項 有機化合物の立体構造 P.7. 立体構造の表記方法破線 - くさび型表記法 Newman 投影法 Fischer 投影法. 異性体構造異性体と立体異性体光学異性体 DL 表示法,S 表示法ジアステレオ異性体シス - トランス異性体配座異性体アルカンとシクロヘキサン 異なる 異性体の分類 異性体 結合様式 同じ分子式を持つ 同じ 三次元的配置が異なる 鏡像異性体 chirality chiral
章での重要事項 有機化合物の立体構造 P.7. 立体構造の表記方法破線 - くさび型表記法 Newman 投影法 Fischer 投影法. 異性体構造異性体と立体異性体光学異性体 DL 表示法,S 表示法ジアステレオ異性体シス - トランス異性体配座異性体アルカンとシクロヘキサン 異なる 異性体の分類 異性体 結合様式 同じ分子式を持つ 同じ 三次元的配置が異なる 鏡像異性体 chirality chiral
Microsoft PowerPoint - siryo7
 . 化学反応と溶液 - 遷移状態理論と溶液論 -.. 遷移状態理論 と溶液論 7 年 5 月 5 日 衝突論と遷移状態理論の比較 + 生成物 原子どうしの反応 活性錯体 ( 遷移状態 ) は 3つの並進 つの回転の自由度をもつ (1つの振動モードは分解に相当 ) 3/ [ ( m m) T] 8 IT q q π + π tansqot 3 h h との並進分配関数 [ πmt] 3/ [ ] 3/
. 化学反応と溶液 - 遷移状態理論と溶液論 -.. 遷移状態理論 と溶液論 7 年 5 月 5 日 衝突論と遷移状態理論の比較 + 生成物 原子どうしの反応 活性錯体 ( 遷移状態 ) は 3つの並進 つの回転の自由度をもつ (1つの振動モードは分解に相当 ) 3/ [ ( m m) T] 8 IT q q π + π tansqot 3 h h との並進分配関数 [ πmt] 3/ [ ] 3/
化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イ
 化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イオンと陰イオンの静電気的な引力による結合を 1 1 という ⑵ 2 個の水素原子は, それぞれ1 個の価電子を出し合い,
化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イオンと陰イオンの静電気的な引力による結合を 1 1 という ⑵ 2 個の水素原子は, それぞれ1 個の価電子を出し合い,
<4D F736F F F696E74202D C8B4089BB8D8795A882CC94BD899E A>
 I. 有機化合物の反応 (3) 1. 芳香族化合物 2. 芳香環における求電子置換反応 3. 置換基効果と配向性 4. 種々の化合物の合成反応 5. 置換基と酸 塩基の強さ I. 有機化合物の反応 (3) 1. 芳香族化合物 1. 芳香族化合物 ベンゼン,C 6 H 6 3 つの sp 2 混成軌道 結合を形成 すべての原子は同一平面上にある 正六角形, C ー C ー C = 120 残りの p
I. 有機化合物の反応 (3) 1. 芳香族化合物 2. 芳香環における求電子置換反応 3. 置換基効果と配向性 4. 種々の化合物の合成反応 5. 置換基と酸 塩基の強さ I. 有機化合物の反応 (3) 1. 芳香族化合物 1. 芳香族化合物 ベンゼン,C 6 H 6 3 つの sp 2 混成軌道 結合を形成 すべての原子は同一平面上にある 正六角形, C ー C ー C = 120 残りの p
PowerPoint プレゼンテーション
 MS NMR で検索 http://lab.agr.hokudai.ac.jp/ms-nmr/ N379 室図書室の上情報処理室の向かい窓なし金属ドア 高田祐輔平日 8:30-17:00 55 73 2017 年本試験 85 113 1727 1194 6.40 (1H, dd, J = 17.4, 1.8) 6.12 (1H, dd, J = 17.4, 10.4) 5.81 (1H, dd, J
MS NMR で検索 http://lab.agr.hokudai.ac.jp/ms-nmr/ N379 室図書室の上情報処理室の向かい窓なし金属ドア 高田祐輔平日 8:30-17:00 55 73 2017 年本試験 85 113 1727 1194 6.40 (1H, dd, J = 17.4, 1.8) 6.12 (1H, dd, J = 17.4, 10.4) 5.81 (1H, dd, J
 1 911 9001030 9:00 A B C D E F G H I J K L M 1A0900 1B0900 1C0900 1D0900 1E0900 1F0900 1G0900 1H0900 1I0900 1J0900 1K0900 1L0900 1M0900 9:15 1A0915 1B0915 1C0915 1D0915 1E0915 1F0915 1G0915 1H0915 1I0915
1 911 9001030 9:00 A B C D E F G H I J K L M 1A0900 1B0900 1C0900 1D0900 1E0900 1F0900 1G0900 1H0900 1I0900 1J0900 1K0900 1L0900 1M0900 9:15 1A0915 1B0915 1C0915 1D0915 1E0915 1F0915 1G0915 1H0915 1I0915
電子配置と価電子 P H 2He 第 4 回化学概論 3Li 4Be 5B 6C 7N 8O 9F 10Ne 周期表と元素イオン 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar 価電子数 陽
 電子配置と価電子 P11 1 2 13 14 15 16 17 18 1H 2He 第 4 回化学概論 3Li 4Be 5B 6C 7N 8O 9F 10Ne 周期表と元素イオン 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar 1 2 3 4 5 6 7 0 陽性元素陰性元素安定電子を失いやすい電子を受け取りやすい 原子番号と価電子の数 P16 元素の周期表 P17 最外殻の電子配置と周期表
電子配置と価電子 P11 1 2 13 14 15 16 17 18 1H 2He 第 4 回化学概論 3Li 4Be 5B 6C 7N 8O 9F 10Ne 周期表と元素イオン 11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar 1 2 3 4 5 6 7 0 陽性元素陰性元素安定電子を失いやすい電子を受け取りやすい 原子番号と価電子の数 P16 元素の周期表 P17 最外殻の電子配置と周期表
これまで がん細胞および昆虫細胞に対する細胞毒性活性 抗ボウフラ活性 植物病原性カビに対する抗カビ活性 植物生長調節活性を調べています これらの研究は 植物性食品を含む植物の機能評価 リグナン骨格を持つ新農薬 医薬開発につながるものです 今後は リグナン類の生物活性の発現メカニズム研究も行っていく予
 教授 : 山内聡 研究テーマ I リグナン類の立体異性体の合成と生物活性 II 酵母還元生成物を利用した天然物有機化合物の合成 研究テーマ I リグナン類の立体異性体の合成と生物活性食品性植物を含む植物は 多くの有機化合物を作り出す能力を持っています リグナン類は ベンゼン環部分 (C6) と 3 つの炭素鎖 (C3) の C6-C3 単位が 2 3 単位結合したもので 食品性植物を含む多くの植物が作り出す
教授 : 山内聡 研究テーマ I リグナン類の立体異性体の合成と生物活性 II 酵母還元生成物を利用した天然物有機化合物の合成 研究テーマ I リグナン類の立体異性体の合成と生物活性食品性植物を含む植物は 多くの有機化合物を作り出す能力を持っています リグナン類は ベンゼン環部分 (C6) と 3 つの炭素鎖 (C3) の C6-C3 単位が 2 3 単位結合したもので 食品性植物を含む多くの植物が作り出す
ochem1_03
 第 3 回 有機化合物の基礎 1. 炭化水素 炭素と水素のみ 炭化水素 hydrocarbon 4 飽和炭化水素 saturated hydrocarbon 不飽和 炭化水素 unsaturated hydrocarbon アルカン alkane methane ethane propane butane isobutane 1 直鎖アルカン straight-chain alkane 分岐アルカン
第 3 回 有機化合物の基礎 1. 炭化水素 炭素と水素のみ 炭化水素 hydrocarbon 4 飽和炭化水素 saturated hydrocarbon 不飽和 炭化水素 unsaturated hydrocarbon アルカン alkane methane ethane propane butane isobutane 1 直鎖アルカン straight-chain alkane 分岐アルカン
1. 構造式ファイルの作成について 平成 31 年度からの少量新規化学物質の申出には電子データ ( ML ファイル形式 ) の提出が必要となります 本講演資料における 構造式ファイル は ML ファイルのことを指しています 経済産業省推奨構造式描画ソフトウェア以下のソフトウェアを用いて ML ファイ
 少量新規化学物質の申出における 構造式ファイルの作成について 平成 30 年秋 独立行政法人製品評価技術基盤機構 (NITE) 1 1 1. 構造式ファイルの作成について 平成 31 年度からの少量新規化学物質の申出には電子データ ( ML ファイル形式 ) の提出が必要となります 本講演資料における 構造式ファイル は ML ファイルのことを指しています 経済産業省推奨構造式描画ソフトウェア以下のソフトウェアを用いて
少量新規化学物質の申出における 構造式ファイルの作成について 平成 30 年秋 独立行政法人製品評価技術基盤機構 (NITE) 1 1 1. 構造式ファイルの作成について 平成 31 年度からの少量新規化学物質の申出には電子データ ( ML ファイル形式 ) の提出が必要となります 本講演資料における 構造式ファイル は ML ファイルのことを指しています 経済産業省推奨構造式描画ソフトウェア以下のソフトウェアを用いて
平成 29 年度大学院博士前期課程入学試験問題 生物工学 I 基礎生物化学 生物化学工学から 1 科目選択ただし 内部受験生は生物化学工学を必ず選択すること 解答には 問題ごとに1 枚の解答用紙を使用しなさい 余った解答用紙にも受験番号を記載しなさい 試験終了時に回収します 受験番号
 平成 29 年度大学院博士前期課程入学試験問題 生物工学 I から 1 科目選択ただし 内部受験生はを必ず選択すること 解答には 問題ごとに1 枚の解答用紙を使用しなさい 余った解答用紙にも受験番号を記載しなさい 試験終了時に回収します 受験番号 問題 1. ( 配点率 33/100) 生体エネルギーと熱力学に関する以下の問に答えなさい (1) 細胞内の反応における ATP 加水分解時の実際の自由エネルギー変化
平成 29 年度大学院博士前期課程入学試験問題 生物工学 I から 1 科目選択ただし 内部受験生はを必ず選択すること 解答には 問題ごとに1 枚の解答用紙を使用しなさい 余った解答用紙にも受験番号を記載しなさい 試験終了時に回収します 受験番号 問題 1. ( 配点率 33/100) 生体エネルギーと熱力学に関する以下の問に答えなさい (1) 細胞内の反応における ATP 加水分解時の実際の自由エネルギー変化
有機合成化学
 21 章アミンおよびその誘導体 アミン類 ( 医薬品 ) ( 抗うつ剤 ) ダイエットピル N Cl ドリエル ( エスエス製薬 ) 抗ヒスタミン剤の眠気を利用 p1166 リン酸オセルタミビル ( タミフル ) 抗インフルエンザウイルス剤 タミフル (tamiflu: リン酸オセルタミビル ) はスイスロシュ社によって製造されている抗インフルエンザウイルス剤 作用機序は ノイラミニダーゼ (Neuraminidase)
21 章アミンおよびその誘導体 アミン類 ( 医薬品 ) ( 抗うつ剤 ) ダイエットピル N Cl ドリエル ( エスエス製薬 ) 抗ヒスタミン剤の眠気を利用 p1166 リン酸オセルタミビル ( タミフル ) 抗インフルエンザウイルス剤 タミフル (tamiflu: リン酸オセルタミビル ) はスイスロシュ社によって製造されている抗インフルエンザウイルス剤 作用機序は ノイラミニダーゼ (Neuraminidase)
O1-1 O1-2 O1-3 O1-4 O1-5 O1-6
 O1-1 O1-2 O1-3 O1-4 O1-5 O1-6 O1-7 O1-8 O1-9 O1-10 O1-11 O1-12 O1-13 O1-14 O1-15 O1-16 O1-17 O1-18 O1-19 O1-20 O1-21 O1-22 O1-23 O1-24 O1-25 O1-26 O1-27 O1-28 O1-29 O1-30 O1-31 O1-32 O1-33 O1-34 O1-35
O1-1 O1-2 O1-3 O1-4 O1-5 O1-6 O1-7 O1-8 O1-9 O1-10 O1-11 O1-12 O1-13 O1-14 O1-15 O1-16 O1-17 O1-18 O1-19 O1-20 O1-21 O1-22 O1-23 O1-24 O1-25 O1-26 O1-27 O1-28 O1-29 O1-30 O1-31 O1-32 O1-33 O1-34 O1-35
香りがナビゲートする 有機化学 理学博士長谷川登志夫著 コロナ社 コロナ社
 香りがナビゲートする 有機化学 理学博士長谷川登志夫著 . i OH C H ii iii. 1. 2.. 3.. 6. sp, sp, sp v r 8.. sp, sp, sp 8.. v r 9. 13.. 13.. 16.. 18.. 22. 25. 29.. 29 iv.. 31. 35. 36.. 36.. 38.. 40. 42. 43. 45. 48. 51.. 53.. 54. 60..
香りがナビゲートする 有機化学 理学博士長谷川登志夫著 . i OH C H ii iii. 1. 2.. 3.. 6. sp, sp, sp v r 8.. sp, sp, sp 8.. v r 9. 13.. 13.. 16.. 18.. 22. 25. 29.. 29 iv.. 31. 35. 36.. 36.. 38.. 40. 42. 43. 45. 48. 51.. 53.. 54. 60..
事業者ガイダンス-NITE MOLファイル作成システム(Marvin JS)の使い方-
 事業者ガイダンス -NITE MOL ファイル作成システム (Marvin JS) の使い方 - Marvin JS は 化審法の少量新規申出手続きの範囲での使用が認められています 商業目的での利用にあたっては Marvin JS のライセンス条項をご確認ください 08 年 9 月 08 年 0 月改訂 独立行政法人製品評価技術基盤機構 はじめに -NITE MOL ファイル作成システムの利用にあたり
事業者ガイダンス -NITE MOL ファイル作成システム (Marvin JS) の使い方 - Marvin JS は 化審法の少量新規申出手続きの範囲での使用が認められています 商業目的での利用にあたっては Marvin JS のライセンス条項をご確認ください 08 年 9 月 08 年 0 月改訂 独立行政法人製品評価技術基盤機構 はじめに -NITE MOL ファイル作成システムの利用にあたり
SO の場合 Leis の酸塩基説 ( 非プロトン性溶媒までも摘要可 一般化 ) B + B の化学反応の酸と塩基 SO + + SO SO + + SO 酸 塩基 酸 塩基 SO は酸にも塩基にもなっている 酸の強さ 酸が強い = 塩基へプロトンを供与する能力が大きい 強酸 ( 優れたプロトン供与
 溶液溶媒 + 溶質 均一な相 溶質を溶かしている物質 溶けている物質 固体 + 液体液体 + 固体 溶質 (solute) イオンの形に解離して溶けているもの ( 電解質 ) 酸と塩基 Copyrigt: A.Asno 1 水素イオン濃度 (ydrogenion concentrtion) 水素イオン指数 (ydrogenion exponent; p) 水の電離 O + O O + + O O +
溶液溶媒 + 溶質 均一な相 溶質を溶かしている物質 溶けている物質 固体 + 液体液体 + 固体 溶質 (solute) イオンの形に解離して溶けているもの ( 電解質 ) 酸と塩基 Copyrigt: A.Asno 1 水素イオン濃度 (ydrogenion concentrtion) 水素イオン指数 (ydrogenion exponent; p) 水の電離 O + O O + + O O +
< イオン 電離練習問題 > No. 1 次のイオンの名称を書きなさい (1) H + ( ) (2) Na + ( ) (3) K + ( ) (4) Mg 2+ ( ) (5) Cu 2+ ( ) (6) Zn 2+ ( ) (7) NH4 + ( ) (8) Cl - ( ) (9) OH -
 < イオン 電離練習問題 > No. 1 次のイオンの名称を書きなさい (1) + (2) Na + (3) K + (4) Mg 2+ (5) Cu 2+ (6) Zn 2+ (7) N4 + (8) Cl - (9) - (10) SO4 2- (11) NO3 - (12) CO3 2- 次の文中の ( ) に当てはまる語句を 下の選択肢から選んで書きなさい 物質の原子は (1 ) を失ったり
< イオン 電離練習問題 > No. 1 次のイオンの名称を書きなさい (1) + (2) Na + (3) K + (4) Mg 2+ (5) Cu 2+ (6) Zn 2+ (7) N4 + (8) Cl - (9) - (10) SO4 2- (11) NO3 - (12) CO3 2- 次の文中の ( ) に当てはまる語句を 下の選択肢から選んで書きなさい 物質の原子は (1 ) を失ったり
Microsoft PowerPoint - 第2回半導体工学
 17 年 1 月 16 日 月 1 限 8:5~1:15 IB15 第 回半導体工学 * バンド構造と遷移確率 天野浩 項目 1 章量子論入門 何故 Si は光らず GN は良く光るのか? *MOSFET ゲート SiO / チャネル Si 界面の量子輸送過程 MOSFET には どのようなゲート材料が必要なのか? http://www.iue.tuwien.c.t/ph/vsicek/noe3.html
17 年 1 月 16 日 月 1 限 8:5~1:15 IB15 第 回半導体工学 * バンド構造と遷移確率 天野浩 項目 1 章量子論入門 何故 Si は光らず GN は良く光るのか? *MOSFET ゲート SiO / チャネル Si 界面の量子輸送過程 MOSFET には どのようなゲート材料が必要なのか? http://www.iue.tuwien.c.t/ph/vsicek/noe3.html
PEC News 2004_3....PDF00
 2004 March 3 C O N T E N T S Petroleum Energy Center News 1 13 1 2 3 3 4 3 5 6 3 7 8 3 9 ロ 芳香環の水素化 通常の縮合多環芳香族の水素化には 図17 芳香環の水素化 水素化活性の強化 NiMo系あるいはNiW系触媒が有効であり これらの水素化活性を高めることでメチル 基による反応阻害を緩和し 4,6DMDBT等
2004 March 3 C O N T E N T S Petroleum Energy Center News 1 13 1 2 3 3 4 3 5 6 3 7 8 3 9 ロ 芳香環の水素化 通常の縮合多環芳香族の水素化には 図17 芳香環の水素化 水素化活性の強化 NiMo系あるいはNiW系触媒が有効であり これらの水素化活性を高めることでメチル 基による反応阻害を緩和し 4,6DMDBT等
Microsoft Word - 酸塩基
 化学基礎実験 : 酸 塩基と (1) 酸と塩基 の基本を学び の実験を通してこれらの事柄に関する認識を深めます さらに 緩衝液の性質に ついて学び 緩衝液の 変化に対する緩衝力を実験で確かめます 化学基礎実験 : 酸 塩基と 酸と塩基 水の解離 HCl H Cl - 塩酸 塩素イオン 酸 強酸 ヒドロニウムイオン H 3 O H O H OH - OH ー [H ] = [OH - ]= 1-7 M
化学基礎実験 : 酸 塩基と (1) 酸と塩基 の基本を学び の実験を通してこれらの事柄に関する認識を深めます さらに 緩衝液の性質に ついて学び 緩衝液の 変化に対する緩衝力を実験で確かめます 化学基礎実験 : 酸 塩基と 酸と塩基 水の解離 HCl H Cl - 塩酸 塩素イオン 酸 強酸 ヒドロニウムイオン H 3 O H O H OH - OH ー [H ] = [OH - ]= 1-7 M
スライド 1
 基礎無機化学第 8 回 原子パラメーター (II) 電子親和力, 電気陰性度, 分極率 本日のポイント 電子親和力 : 追加の電子の受け取りやすさ基本的に周期表の右の方が大きいハロゲンあたりで最大, 希ガスでは負 電気陰性度 : 結合を作った時の電子を引っ張る強さ値が大きいと, 結合相手から電子を引っ張る値の差の大きい原子間での結合 イオン的イオン化エネルギーと電子親和力の平均に近い 分極率 : 電子の分布がどのくらい変化しやすいか周期表の左,
基礎無機化学第 8 回 原子パラメーター (II) 電子親和力, 電気陰性度, 分極率 本日のポイント 電子親和力 : 追加の電子の受け取りやすさ基本的に周期表の右の方が大きいハロゲンあたりで最大, 希ガスでは負 電気陰性度 : 結合を作った時の電子を引っ張る強さ値が大きいと, 結合相手から電子を引っ張る値の差の大きい原子間での結合 イオン的イオン化エネルギーと電子親和力の平均に近い 分極率 : 電子の分布がどのくらい変化しやすいか周期表の左,
Microsoft PowerPoint - presentation2007_04_ComplexFormation.ppt
 錯生成平衡とその応用 金属イオン が配位子 (lignd) と反応し 錯体 (complex) を形成するときの平衡反応. 金属イオンは遷移金属の場合が多い. 遷移金属は d 軌道と その上の s 軌道や p 軌道の 電子を利用して混成軌道をつくる. 比較的容易に多様な酸化数をとれる [u(h ) テトラアンミン銅 (II) イオン [Fe() 6 ヘキサシアノ鉄 (III) イオン omplex
錯生成平衡とその応用 金属イオン が配位子 (lignd) と反応し 錯体 (complex) を形成するときの平衡反応. 金属イオンは遷移金属の場合が多い. 遷移金属は d 軌道と その上の s 軌道や p 軌道の 電子を利用して混成軌道をつくる. 比較的容易に多様な酸化数をとれる [u(h ) テトラアンミン銅 (II) イオン [Fe() 6 ヘキサシアノ鉄 (III) イオン omplex
記 者 発 表(予 定)
 平成 28 年 4 月 19 日 高効率で二酸化炭素を還元する鉄触媒を発見 ~2 つの近接した鉄原子が高活性の鍵 ~ 中部大学 Tel:0568-51-4852( 研究支援課 ) ポイント 従来の二酸化炭素還元触媒の多くは希少性の高い貴金属元素を使用し 触媒活性も高くなかった 安価で一般的な金属である鉄を用いて 一酸化炭素のみを生成する高い活性を持つ触媒の開発に成功した 太陽光など再生可能エネルギーを用いて
平成 28 年 4 月 19 日 高効率で二酸化炭素を還元する鉄触媒を発見 ~2 つの近接した鉄原子が高活性の鍵 ~ 中部大学 Tel:0568-51-4852( 研究支援課 ) ポイント 従来の二酸化炭素還元触媒の多くは希少性の高い貴金属元素を使用し 触媒活性も高くなかった 安価で一般的な金属である鉄を用いて 一酸化炭素のみを生成する高い活性を持つ触媒の開発に成功した 太陽光など再生可能エネルギーを用いて
New Color Chemosensors for Monosaccharides Based on Azo Dyes
 New olor hemoenor for Monocchride ed on zo Dye 著者 : Nicol Diere nd Joeph R. Lkowicz 雑誌 : rg.lett. 1, 3 (4), 3891-3893 紹介者 : 堀田隼 1 年 1 月 7 日 ボロン酸の性質 1 ci-ジオールと環状エステルを形成する 環状エステルを形成すると ボロン酸の酸性度が高まる btrct
New olor hemoenor for Monocchride ed on zo Dye 著者 : Nicol Diere nd Joeph R. Lkowicz 雑誌 : rg.lett. 1, 3 (4), 3891-3893 紹介者 : 堀田隼 1 年 1 月 7 日 ボロン酸の性質 1 ci-ジオールと環状エステルを形成する 環状エステルを形成すると ボロン酸の酸性度が高まる btrct
基礎化学 Ⅰ 第 5 講原子量とモル数 第 5 講原子量とモル数 1 原子量 (1) 相対質量 まず, 大きさの復習から 原子 ピンポン玉 原子の直径は, 約 1 億分の 1cm ( 第 1 講 ) 原子とピンポン玉の関係は, ピンポン玉と地球の関係と同じくらいの大きさです 地球 では, 原子 1
 第 5 講原子量とモル数 1 原子量 (1) 相対質量 まず, 大きさの復習から 原子 ピンポン玉 原子の直径は, 約 1 億分の 1cm ( 第 1 講 ) 原子とピンポン玉の関係は, ピンポン玉と地球の関係と同じくらいの大きさです 地球 では, 原子 1 つの質量は? 水素原子は,0.167 10-23 g 酸素原子は,2.656 10-23 g 炭素原子は,1.993 10-23 g 原子の質量は,
第 5 講原子量とモル数 1 原子量 (1) 相対質量 まず, 大きさの復習から 原子 ピンポン玉 原子の直径は, 約 1 億分の 1cm ( 第 1 講 ) 原子とピンポン玉の関係は, ピンポン玉と地球の関係と同じくらいの大きさです 地球 では, 原子 1 つの質量は? 水素原子は,0.167 10-23 g 酸素原子は,2.656 10-23 g 炭素原子は,1.993 10-23 g 原子の質量は,
Microsoft Word - H29統合版.doc
 毒物劇物取扱者試験 (14) ( 平成 29 年 8 月 8 日 ) 問 26 混合物の分離に関する次の a~c の記述について その操作方法として正しい組み合わせを下表から一つ選び その番号を解答用紙に記入しなさい a. 沸点の差を利用して 液体の混合物を適当な温度範囲に区切って蒸留し 留出物 ( 蒸留によって得られる物質 ) を分離する操作 b. ろ紙やシリカゲルのような吸着剤に 物質が吸着される強さの違いを利用して
毒物劇物取扱者試験 (14) ( 平成 29 年 8 月 8 日 ) 問 26 混合物の分離に関する次の a~c の記述について その操作方法として正しい組み合わせを下表から一つ選び その番号を解答用紙に記入しなさい a. 沸点の差を利用して 液体の混合物を適当な温度範囲に区切って蒸留し 留出物 ( 蒸留によって得られる物質 ) を分離する操作 b. ろ紙やシリカゲルのような吸着剤に 物質が吸着される強さの違いを利用して
Microsoft Word - note02.doc
 年度 物理化学 Ⅱ 講義ノート. 二原子分子の振動. 調和振動子近似 モデル 分子 = 理想的なバネでつながった原子 r : 核間距離, r e : 平衡核間距離, : 変位 ( = r r e ), k f : 力の定数ポテンシャルエネルギー ( ) k V = f (.) 古典運動方程式 [ 振動数 ] 3.3 d kf (.) dt μ : 換算質量 (m, m : 原子, の質量 ) mm
年度 物理化学 Ⅱ 講義ノート. 二原子分子の振動. 調和振動子近似 モデル 分子 = 理想的なバネでつながった原子 r : 核間距離, r e : 平衡核間距離, : 変位 ( = r r e ), k f : 力の定数ポテンシャルエネルギー ( ) k V = f (.) 古典運動方程式 [ 振動数 ] 3.3 d kf (.) dt μ : 換算質量 (m, m : 原子, の質量 ) mm
Microsoft PowerPoint - qchem3-11
 8 年度冬学期 量子化学 Ⅲ 章量子化学の応用.6. 溶液反応 9 年 1 月 6 日 担当 : 常田貴夫准教授 溶液中の反応 溶液反応の特徴は 反応する分子の周囲に常に溶媒分子が存在していること 反応過程が遅い 反応自体の化学的効果が重要 遷移状態理論の熱力学表示が適用できる反応過程が速い 反応物が相互に接近したり 生成物が離れていく拡散過程が律速 溶媒効果は拡散現象 溶液中の反応では 分子は周囲の溶媒分子のケージ内で衝突を繰り返す可能性が高い
8 年度冬学期 量子化学 Ⅲ 章量子化学の応用.6. 溶液反応 9 年 1 月 6 日 担当 : 常田貴夫准教授 溶液中の反応 溶液反応の特徴は 反応する分子の周囲に常に溶媒分子が存在していること 反応過程が遅い 反応自体の化学的効果が重要 遷移状態理論の熱力学表示が適用できる反応過程が速い 反応物が相互に接近したり 生成物が離れていく拡散過程が律速 溶媒効果は拡散現象 溶液中の反応では 分子は周囲の溶媒分子のケージ内で衝突を繰り返す可能性が高い
<4D F736F F F696E74202D A E90B6979D89C8816B91E63195AA96EC816C82DC82C682DF8D758DC03189BB8A7795CF89BB82C68CB48E AA8E E9197BF2E >
 中学 2 年理科まとめ講座 第 1 分野 1. 化学変化と原子 分子 物質の成り立ち 化学変化 化学変化と物質の質量 基本の解説と問題 講師 : 仲谷のぼる 1 物質の成り立ち 物質のつくり 物質をつくる それ以上分けることができない粒を原子という いくつかの原子が結びついてできたものを分子という いろいろな物質のうち 1 種類の原子からできている物質を単体 2 種類以上の原子からできている物質を化合物という
中学 2 年理科まとめ講座 第 1 分野 1. 化学変化と原子 分子 物質の成り立ち 化学変化 化学変化と物質の質量 基本の解説と問題 講師 : 仲谷のぼる 1 物質の成り立ち 物質のつくり 物質をつくる それ以上分けることができない粒を原子という いくつかの原子が結びついてできたものを分子という いろいろな物質のうち 1 種類の原子からできている物質を単体 2 種類以上の原子からできている物質を化合物という
解法 1 原子の性質を周期表で理解する 原子の結合について理解するには まずは原子の種類 (= 元素 ) による性質の違いを知る必要がある 原子の性質は 次の 3 つによって理解することができる イオン化エネルギー = 原子から電子 1 個を取り除くのに必要なエネルギー ( イメージ ) 電子 原子
 解法 1 原子の性質を周期表で理解する 原子の結合について理解するには まずは原子の種類 (= 元素 ) による性質の違いを知る必要がある 原子の性質は 次の 3 つによって理解することができる イオン化エネルギー = 原子から電子 1 個を取り除くのに必要なエネルギー ( イメージ ) 電子 原子 いやだ!! の強さ 電子親和力 = 原子が電子 1 個を受け取ったときに放出するエネルギー ( イメージ
解法 1 原子の性質を周期表で理解する 原子の結合について理解するには まずは原子の種類 (= 元素 ) による性質の違いを知る必要がある 原子の性質は 次の 3 つによって理解することができる イオン化エネルギー = 原子から電子 1 個を取り除くのに必要なエネルギー ( イメージ ) 電子 原子 いやだ!! の強さ 電子親和力 = 原子が電子 1 個を受け取ったときに放出するエネルギー ( イメージ
FdData理科3年
 FdData 中間期末 : 中学理科 3 年 : 中和 [ 中和とイオン数の変化 ] [ 問題 ](2 学期中間 ) 次の図は A 液に B 液を加えたときのようすを示している A 液は塩酸,B 液は水酸化ナトリウム水溶液である (1) 1~4 の水溶液はそれぞれ何性か (2) 4 の水溶液にフェノールフタレイン溶液を加えると何色になるか (3) 塩酸 (A 液 ) に水酸化ナトリウム水溶液 (B
FdData 中間期末 : 中学理科 3 年 : 中和 [ 中和とイオン数の変化 ] [ 問題 ](2 学期中間 ) 次の図は A 液に B 液を加えたときのようすを示している A 液は塩酸,B 液は水酸化ナトリウム水溶液である (1) 1~4 の水溶液はそれぞれ何性か (2) 4 の水溶液にフェノールフタレイン溶液を加えると何色になるか (3) 塩酸 (A 液 ) に水酸化ナトリウム水溶液 (B
内容 1. 化学結合 2. 種類と特性 3. 反応の種類 4. 反応機構 5. 高分子材料の特性 6. 高分子合成 7. 有機構造解析
 株式会社アイテス ( 株 ) アイテス 品質技術 清野智志 有機化学講義 http://www.ites.co.jp 内容 1. 化学結合 2. 種類と特性 3. 反応の種類 4. 反応機構 5. 高分子材料の特性 6. 高分子合成 7. 有機構造解析 1. 化学結合 1 イオン結合 Na + + Cl - Na + Cl - 2 金属結合 Al-Al Cu-Cu : Al -Al Cu - Cu
株式会社アイテス ( 株 ) アイテス 品質技術 清野智志 有機化学講義 http://www.ites.co.jp 内容 1. 化学結合 2. 種類と特性 3. 反応の種類 4. 反応機構 5. 高分子材料の特性 6. 高分子合成 7. 有機構造解析 1. 化学結合 1 イオン結合 Na + + Cl - Na + Cl - 2 金属結合 Al-Al Cu-Cu : Al -Al Cu - Cu
Microsoft Word - 10生物化学2.doc
 生物化学 2 回目 10 月 12 日 有機化合物の多様性 2. 立体構造の表示と異性体, 命名法いろいろな構造式 Kekulé 構造式簡略化した構造式結合を直線で示す式 2 2 2 2 破線 くさび形表記法例 1-butnol 三次元的構造式を示す 紙面上にある結合 : ( 実線 ) 紙面より手前に出ている結合 : 太線 ( 手前が太いくさび形 ) 紙面の裏側に向かっている結合 : 破線 フィッシャー投影式主炭素鎖を縦に並べ,
生物化学 2 回目 10 月 12 日 有機化合物の多様性 2. 立体構造の表示と異性体, 命名法いろいろな構造式 Kekulé 構造式簡略化した構造式結合を直線で示す式 2 2 2 2 破線 くさび形表記法例 1-butnol 三次元的構造式を示す 紙面上にある結合 : ( 実線 ) 紙面より手前に出ている結合 : 太線 ( 手前が太いくさび形 ) 紙面の裏側に向かっている結合 : 破線 フィッシャー投影式主炭素鎖を縦に並べ,
 Applied hemistry / ome page : http://www.apc.titech.ac.jp M E-mail EXT. FAX ST ttak@apc.titech.ac.jp thiroshi@apc.titech.ac.jp sfuse@apc.titech.ac.jp aohtomo@apc.titech.ac.jp 2145 2145 mokamoto@apc.titech.ac.jp
Applied hemistry / ome page : http://www.apc.titech.ac.jp M E-mail EXT. FAX ST ttak@apc.titech.ac.jp thiroshi@apc.titech.ac.jp sfuse@apc.titech.ac.jp aohtomo@apc.titech.ac.jp 2145 2145 mokamoto@apc.titech.ac.jp
無機化学 II 2018 年度期末試験 1. 窒素を含む化合物にヒドラジンと呼ばれる化合物 (N2H4, 右図 ) がある. この分子に関し, 以下の問いに答えよ.( 計 9 点 ) (1) N2 分子が 1 mol と H2 分子が 2 mol の状態と, ヒドラジン 1 mol となっている状態
 無機化学 II 2018 年度期末試験 1. 窒素を含む化合物にヒドラジンと呼ばれる化合物 (N2H4, 右図 ) がある. この分子に関し, 以下の問いに答えよ.( 計 9 点 ) (1) N2 分子が 1 mol と H2 分子が 2 mol の状態と, ヒドラジン 1 mol となっている状態を比較すると, どちらの分子がどの程度エネルギーが低いか (= 安定か ) を平均結合エンタルピーから計算して答えよ.
無機化学 II 2018 年度期末試験 1. 窒素を含む化合物にヒドラジンと呼ばれる化合物 (N2H4, 右図 ) がある. この分子に関し, 以下の問いに答えよ.( 計 9 点 ) (1) N2 分子が 1 mol と H2 分子が 2 mol の状態と, ヒドラジン 1 mol となっている状態を比較すると, どちらの分子がどの程度エネルギーが低いか (= 安定か ) を平均結合エンタルピーから計算して答えよ.
FdText理科1年
 中学理科 2 年 : 酸化 燃焼 [ http://www.fdtext.com/dat/ ] [ 要点 ] さんか (1) マグネシウムの酸化 物質が酸素と化合する反応を酸化という 熱や光を出しながらはげしく進む酸化を燃焼という 激しく熱と光を出し, 酸化マグネシウム ( 白色の酸化物 ) ができる マグネシウム+ 酸素 酸化マグネシウム,2Mg+O2 2MgO マグネシウム( 燃焼前 ) と酸化マグネシウム
中学理科 2 年 : 酸化 燃焼 [ http://www.fdtext.com/dat/ ] [ 要点 ] さんか (1) マグネシウムの酸化 物質が酸素と化合する反応を酸化という 熱や光を出しながらはげしく進む酸化を燃焼という 激しく熱と光を出し, 酸化マグネシウム ( 白色の酸化物 ) ができる マグネシウム+ 酸素 酸化マグネシウム,2Mg+O2 2MgO マグネシウム( 燃焼前 ) と酸化マグネシウム
図 2 ブタンの回転異性体に少しずつ回転させると, ポテンシャルエネルギーは 4 で極小となり,5 で極大となり 180 度回転した 6 (=2) で最小となる この間, ポテンシャルエネルギーは連続的に変化する 3 と 6 のエネルギー差は室温で約 26.4 kj/mol で, この程度の違いでは
 立体化学のための分析技術 立体化学入門 太田博道 本年前半の入門講座は 立体化学のための分析技術 と題して, 化合物の立体配置の決定や, 反応の立体選択性を研究されている先生方にご執筆をお願いしました 立体化学になじみのうすい読者があることも想定して, 立体化学の基礎から,X 線結晶解析,CD, NMR などによって立体構造を決定する手法について, やさしく解説いただきます ぶんせき 編集委員会 図
立体化学のための分析技術 立体化学入門 太田博道 本年前半の入門講座は 立体化学のための分析技術 と題して, 化合物の立体配置の決定や, 反応の立体選択性を研究されている先生方にご執筆をお願いしました 立体化学になじみのうすい読者があることも想定して, 立体化学の基礎から,X 線結晶解析,CD, NMR などによって立体構造を決定する手法について, やさしく解説いただきます ぶんせき 編集委員会 図
Microsoft PowerPoint - 11JUN03
 基礎量子化学 年 4 月 ~8 月 6 月 3 日第 7 回 章分子構造 担当教員 : 福井大学大学院工学研究科生物応用化学専攻准教授前田史郎 -ail:saea@u-fukui.a.p URL:http://abio.abio.u-fukui.a.p/phyhe/aea/kougi 教科書 : アトキンス物理化学 ( 第 8 版 ) 東京化学同人 章原子構造と原子スペクトル 章分子構造 分子軌道法
基礎量子化学 年 4 月 ~8 月 6 月 3 日第 7 回 章分子構造 担当教員 : 福井大学大学院工学研究科生物応用化学専攻准教授前田史郎 -ail:saea@u-fukui.a.p URL:http://abio.abio.u-fukui.a.p/phyhe/aea/kougi 教科書 : アトキンス物理化学 ( 第 8 版 ) 東京化学同人 章原子構造と原子スペクトル 章分子構造 分子軌道法
2012/10/17 第 3 章 Hückel 法 Schrödinger 方程式が提案された 1926 年から10 年を経た 1936 年に Hückel 法と呼ばれる分子軌道法が登場した 分子の化学的特徴を残しつつ 解法上で困難となる複雑な部分を最大限にカットした理論である Hückel 法は最
 //7 第 3 章 ükel 法 Shrödnger 方程式が提案された 96 年から 年を経た 936 年に ükel 法と呼ばれる分子軌道法が登場した 分子の化学的特徴を残しつつ 解法上で困難となる複雑な部分を最大限にカットした理論である ükel 法は最も単純な分子軌道法だが それによって生まれた考え方は化学者の概念となって現在に生き続けている ükel 近似の前提 ükel 近似の前提となっている主要な近似を列挙する
//7 第 3 章 ükel 法 Shrödnger 方程式が提案された 96 年から 年を経た 936 年に ükel 法と呼ばれる分子軌道法が登場した 分子の化学的特徴を残しつつ 解法上で困難となる複雑な部分を最大限にカットした理論である ükel 法は最も単純な分子軌道法だが それによって生まれた考え方は化学者の概念となって現在に生き続けている ükel 近似の前提 ükel 近似の前提となっている主要な近似を列挙する
木村の理論化学小ネタ 理想気体と実在気体 A. 標準状態における気体 1mol の体積 標準状態における気体 1mol の体積は気体の種類に関係なく 22.4L のはずである しかし, 実際には, その体積が 22.4L より明らかに小さい
 理想気体と実在気体 A. 標準状態における気体 1mol の体積 標準状態における気体 1mol の体積は気体の種類に関係なく.4L のはずである しかし, 実際には, その体積が.4L より明らかに小さい気体も存在する このような気体には, 気体分子に, 分子量が大きい, 極性が大きいなどの特徴がある そのため, 分子間力が大きく, 体積が.4L より小さくなる.4L とみなせる実在気体 H :.449
理想気体と実在気体 A. 標準状態における気体 1mol の体積 標準状態における気体 1mol の体積は気体の種類に関係なく.4L のはずである しかし, 実際には, その体積が.4L より明らかに小さい気体も存在する このような気体には, 気体分子に, 分子量が大きい, 極性が大きいなどの特徴がある そのため, 分子間力が大きく, 体積が.4L より小さくなる.4L とみなせる実在気体 H :.449
第3類危険物の物質別詳細 練習問題
 第 3 類危険物の物質別詳細練習問題 問題 1 第 3 類危険物の一般的な消火方法として 誤っているものは次のうちいくつあるか A. 噴霧注水は冷却効果と窒息効果があるので 有効である B. 乾燥砂は有効である C. 分子内に酸素を含むので 窒息消火法は効果がない D. 危険物自体は不燃性なので 周囲の可燃物を除去すればよい E. 自然発火性危険物の消火には 炭酸水素塩類を用いた消火剤は効果がある
第 3 類危険物の物質別詳細練習問題 問題 1 第 3 類危険物の一般的な消火方法として 誤っているものは次のうちいくつあるか A. 噴霧注水は冷却効果と窒息効果があるので 有効である B. 乾燥砂は有効である C. 分子内に酸素を含むので 窒息消火法は効果がない D. 危険物自体は不燃性なので 周囲の可燃物を除去すればよい E. 自然発火性危険物の消火には 炭酸水素塩類を用いた消火剤は効果がある
酸素を含む化合物
 2012 年度 化学 第 23 回 第 24 回 ( 担当 : 野島高彦 ) 酸素を含む有機化合物 1 酸素を含む有機化合物 注射針を刺す際には, エタノールで肌を拭いて消毒する. 手指の殺菌には, エタノールのかわりに 2 プロパノールが用いられることもある. 医療器具の殺菌にはクレゾールの水溶液も用いられている. 殺菌消毒にはこれまでに様々な有機化合物が用いられてきた.19 世紀には開腹手術時にフェノールを殺菌剤として噴霧することによって死亡率低下が達成された.
2012 年度 化学 第 23 回 第 24 回 ( 担当 : 野島高彦 ) 酸素を含む有機化合物 1 酸素を含む有機化合物 注射針を刺す際には, エタノールで肌を拭いて消毒する. 手指の殺菌には, エタノールのかわりに 2 プロパノールが用いられることもある. 医療器具の殺菌にはクレゾールの水溶液も用いられている. 殺菌消毒にはこれまでに様々な有機化合物が用いられてきた.19 世紀には開腹手術時にフェノールを殺菌剤として噴霧することによって死亡率低下が達成された.
<4D F736F F D B82C982C282A282C482512E646F63>
 サンプル条件および固定化分子の選択 Biacoreの実験ではセンサーチップに固定化する分子をリガンド それに対して結合を測定する分子をアナライトと呼びます いずれの分子をリガンドとし アナライトとするかは 実験系を構築する上で重要です 以下にサンプルに適したリガンド アナライトの設計方法やサンプルの必要条件などをご紹介します アナライト リガンド センサーチップ (1) タンパク質リガンドとしてもアナライトとしても用いることができます
サンプル条件および固定化分子の選択 Biacoreの実験ではセンサーチップに固定化する分子をリガンド それに対して結合を測定する分子をアナライトと呼びます いずれの分子をリガンドとし アナライトとするかは 実験系を構築する上で重要です 以下にサンプルに適したリガンド アナライトの設計方法やサンプルの必要条件などをご紹介します アナライト リガンド センサーチップ (1) タンパク質リガンドとしてもアナライトとしても用いることができます
 の実現は この分野の最大の課題となってい (a) た ゲージ中の 酸素イオンを 電子で置換 筆 者 ら の 研 究 グ ル ー プ は 23 年 に 12CaO 7Al2O3 結 晶 以 下 C12A7 を用 い て 安定なエレクトライド C12A7: を実現3) Al3+ O2 Cage wall O2 In cage その電子状態や物性を解明してきた4) 図 1 のように C12A7 の結晶構造は
の実現は この分野の最大の課題となってい (a) た ゲージ中の 酸素イオンを 電子で置換 筆 者 ら の 研 究 グ ル ー プ は 23 年 に 12CaO 7Al2O3 結 晶 以 下 C12A7 を用 い て 安定なエレクトライド C12A7: を実現3) Al3+ O2 Cage wall O2 In cage その電子状態や物性を解明してきた4) 図 1 のように C12A7 の結晶構造は
Microsoft PowerPoint - 20JUL12.ppt
 生物応用化学演習 Ⅰ 無機化学演習 3 2012 年 7 月 20 日 [1] 原子価殻電子対反発則 (VSEPR 則 ) を適用して金属錯体の構造を推定できる. 問 1.VSEPR 則を簡単に説明せよ. (1) 分子 ( イオン ) は電子対間の反発ができるだけ少なくなるような構造をとる. (2) 電子対間の反発は lp-lp>lp-bp>bp-bp の順に強い. (3) 電子対間の反発はその角度が
生物応用化学演習 Ⅰ 無機化学演習 3 2012 年 7 月 20 日 [1] 原子価殻電子対反発則 (VSEPR 則 ) を適用して金属錯体の構造を推定できる. 問 1.VSEPR 則を簡単に説明せよ. (1) 分子 ( イオン ) は電子対間の反発ができるだけ少なくなるような構造をとる. (2) 電子対間の反発は lp-lp>lp-bp>bp-bp の順に強い. (3) 電子対間の反発はその角度が
木村の化学重要問題集 2014 解答編解説補充 脂肪族化合物 ( 有機化合物の分類を含む ) 202. 代表的なアルデヒドとカルボン酸 フェーリング反応 銀鏡反応 : アルデヒド 還元糖の検出反応 1. フェーリング反応 フェーリン
 1. 脂肪族化合物 ( 有機化合物の分類を含む ) 0. 代表的なアルデヒドとカルボン酸 フェーリング反応 銀鏡反応 : アルデヒド 還元糖の検出反応 1. フェーリング反応 フェーリング溶液とは 硫酸銅五水和物 (us 4 5 )69.g を水 1L に溶解した溶液 (A 液 ) と 酒石酸ナトリウムカリウム 46g と水酸化ナトリウム 100g を水 1L に溶解した溶液 (B 液 ) を等量に混合した濃青色の溶液
1. 脂肪族化合物 ( 有機化合物の分類を含む ) 0. 代表的なアルデヒドとカルボン酸 フェーリング反応 銀鏡反応 : アルデヒド 還元糖の検出反応 1. フェーリング反応 フェーリング溶液とは 硫酸銅五水和物 (us 4 5 )69.g を水 1L に溶解した溶液 (A 液 ) と 酒石酸ナトリウムカリウム 46g と水酸化ナトリウム 100g を水 1L に溶解した溶液 (B 液 ) を等量に混合した濃青色の溶液
Microsoft Word 生体分子構造学.docx
 生体分子構造学 構造から生体分子の機能の解明へ 北里大学理学部 米田茂隆 2015 夏学期 http://www.kitasato-u.ac.jp/sci/resea/buturi/seitai/yoneda/text.html アミノ酸の化学構造アミノ酸はどれも左図のような基本的な構造をもっている 左図で側鎖と書いた球がアミノ酸の種類により異なる 1 側鎖以外の部分を主鎖という 主鎖の原子は N
生体分子構造学 構造から生体分子の機能の解明へ 北里大学理学部 米田茂隆 2015 夏学期 http://www.kitasato-u.ac.jp/sci/resea/buturi/seitai/yoneda/text.html アミノ酸の化学構造アミノ酸はどれも左図のような基本的な構造をもっている 左図で側鎖と書いた球がアミノ酸の種類により異なる 1 側鎖以外の部分を主鎖という 主鎖の原子は N
■ 質量分析計の原理 ■
 質量分析装置 1, 質量分析法とは? 質量分析法 (Mass Spectrometry, 以下 MS と略す ) は 極めて少量の試料 (1mg 以下, 最低必要量は 1 mmol/l の溶液が数 μl あれば測定可能 ) で 信頼性のある分子量を測定する方法である 実際には試料を高真空下 適当な方法でイオン化し そのイオンを電磁気的に分離して検出を行う 元素分析と MS を組み合わせれば 試料の分子式が決定できる
質量分析装置 1, 質量分析法とは? 質量分析法 (Mass Spectrometry, 以下 MS と略す ) は 極めて少量の試料 (1mg 以下, 最低必要量は 1 mmol/l の溶液が数 μl あれば測定可能 ) で 信頼性のある分子量を測定する方法である 実際には試料を高真空下 適当な方法でイオン化し そのイオンを電磁気的に分離して検出を行う 元素分析と MS を組み合わせれば 試料の分子式が決定できる
化学I
 化学 I 第 4 章 分子の構造 ( その 2) http://acbio2.acbio.u-fukui.ac.jp/indphy/hisada/chemistryi/ 授業計画 1 回物質観の進歩と自然科学の発展 2 回原子の電子構造 - 電子, 陽子, 原子量 - 3 回水素原子の電子スペクトル 4 回 Bohr の水素原子模型 5 回物質の波動性 6 回量子数 7 回原子の電子配置と周期律表
化学 I 第 4 章 分子の構造 ( その 2) http://acbio2.acbio.u-fukui.ac.jp/indphy/hisada/chemistryi/ 授業計画 1 回物質観の進歩と自然科学の発展 2 回原子の電子構造 - 電子, 陽子, 原子量 - 3 回水素原子の電子スペクトル 4 回 Bohr の水素原子模型 5 回物質の波動性 6 回量子数 7 回原子の電子配置と周期律表
フォルハルト法 NH SCN の標準液または KSCN の標準液を用い,Ag または Hg を直接沈殿滴定する方法 および Cl, Br, I, CN, 試料溶液に Fe SCN, S 2 を指示薬として加える 例 : Cl の逆滴定による定量 などを逆滴定する方法をいう Fe を加えた試料液に硝酸
 沈殿滴定とモール法 沈殿滴定沈殿とは溶液に試薬を加えたり加熱や冷却をしたとき, 溶液から不溶性固体が分離する現象, またはその不溶性固体を沈殿という 不溶性固体は, 液底に沈んでいいても微粒子 ( コロイド ) として液中を浮遊していても沈殿と呼ばれる 沈殿滴定とは沈殿が生成あるいは消失する反応を利用した滴定のことをいう 沈殿が生成し始めた点, 沈殿の生成が完了した点, または沈殿が消失した点が滴定の終点となる
沈殿滴定とモール法 沈殿滴定沈殿とは溶液に試薬を加えたり加熱や冷却をしたとき, 溶液から不溶性固体が分離する現象, またはその不溶性固体を沈殿という 不溶性固体は, 液底に沈んでいいても微粒子 ( コロイド ) として液中を浮遊していても沈殿と呼ばれる 沈殿滴定とは沈殿が生成あるいは消失する反応を利用した滴定のことをいう 沈殿が生成し始めた点, 沈殿の生成が完了した点, または沈殿が消失した点が滴定の終点となる
化 学 1 7 [ 解答にあたって, 必要があれば次の値を用いること ] 原子量 :H 1. 0, C 12, O 16 Ⅰ プロペンと等しい物質量の臭化水素を瓶の中に封じ込めたところ, 反応が開始した この反応に ついて, 問 ₁ ~ ₆ に答えよ 問 ₁ この反応では,₂ 種類の可能な構造異性体
![化 学 1 7 [ 解答にあたって, 必要があれば次の値を用いること ] 原子量 :H 1. 0, C 12, O 16 Ⅰ プロペンと等しい物質量の臭化水素を瓶の中に封じ込めたところ, 反応が開始した この反応に ついて, 問 ₁ ~ ₆ に答えよ 問 ₁ この反応では,₂ 種類の可能な構造異性体 化 学 1 7 [ 解答にあたって, 必要があれば次の値を用いること ] 原子量 :H 1. 0, C 12, O 16 Ⅰ プロペンと等しい物質量の臭化水素を瓶の中に封じ込めたところ, 反応が開始した この反応に ついて, 問 ₁ ~ ₆ に答えよ 問 ₁ この反応では,₂ 種類の可能な構造異性体](/thumbs/94/118733805.jpg) 1 [ 解答にあたって, 必要があれば次の値を用いること ] 原子量 :H 1. 0, C 12, O 16 Ⅰ プロペンと等しい物質量の臭水素を瓶の中に封じ込めたところ, 反応が開始した この反応に ついて, 問 ₁ ~ ₆ に答えよ 問 ₁ この反応では,₂ 種類の可能な構造異性体のうち, 一方が優先して生成する この現象を表 す法則の名称を示せ また, 得られた生成物を構造式で示せ 問 ₂ 速度定数
1 [ 解答にあたって, 必要があれば次の値を用いること ] 原子量 :H 1. 0, C 12, O 16 Ⅰ プロペンと等しい物質量の臭水素を瓶の中に封じ込めたところ, 反応が開始した この反応に ついて, 問 ₁ ~ ₆ に答えよ 問 ₁ この反応では,₂ 種類の可能な構造異性体のうち, 一方が優先して生成する この現象を表 す法則の名称を示せ また, 得られた生成物を構造式で示せ 問 ₂ 速度定数
57巻S‐A(総会号)/NKRP‐02(会長あいさつ)
 β β β β β β β β β β シンポジウム 1 創薬物語 科学者としての喜びの瞬間 4 レボフロキサシンに至る創薬研究 よりよい薬を求めて 第一三共株式会社 研究開発本部 研究開発企画部 早川勇夫 レボフロキサシン クラビット 1 は 1993 年上市された世界初の光学活性のニューキノロン系抗菌薬 以 下 ニューキノロンと略 である 1 は 1985 年に上市されたラセミ体のオフロキサシン
β β β β β β β β β β シンポジウム 1 創薬物語 科学者としての喜びの瞬間 4 レボフロキサシンに至る創薬研究 よりよい薬を求めて 第一三共株式会社 研究開発本部 研究開発企画部 早川勇夫 レボフロキサシン クラビット 1 は 1993 年上市された世界初の光学活性のニューキノロン系抗菌薬 以 下 ニューキノロンと略 である 1 は 1985 年に上市されたラセミ体のオフロキサシン
Microsoft Word - プレス原稿_0528【最終版】
 報道関係各位 2014 年 5 月 28 日 二酸化チタン表面における陽電子消滅誘起イオン脱離の観測に成功 ~ 陽電子を用いた固体最表面の改質に道 ~ 東京理科大学研究戦略 産学連携センター立教大学リサーチ イニシアティブセンター 本研究成果のポイント 二酸化チタン表面での陽電子の対消滅に伴って脱離する酸素正イオンの観測に成功 陽電子を用いた固体最表面の改質に道を拓いた 本研究は 東京理科大学理学部第二部物理学科長嶋泰之教授
報道関係各位 2014 年 5 月 28 日 二酸化チタン表面における陽電子消滅誘起イオン脱離の観測に成功 ~ 陽電子を用いた固体最表面の改質に道 ~ 東京理科大学研究戦略 産学連携センター立教大学リサーチ イニシアティブセンター 本研究成果のポイント 二酸化チタン表面での陽電子の対消滅に伴って脱離する酸素正イオンの観測に成功 陽電子を用いた固体最表面の改質に道を拓いた 本研究は 東京理科大学理学部第二部物理学科長嶋泰之教授










