国立がんセンター受託研究取扱規程
|
|
|
- ゆうりゅう ひろもり
- 4 years ago
- Views:
Transcription
1 平成 22 年 4 月 1 日規程第 31 号 国立研究開発法人国立がん研究センター受託研究取扱規程 第 1 版平成 22 年 4 月 1 日第 2 版平成 22 年 10 月 1 日第 3 版平成 23 年 4 月 1 日第 4 版平成 24 年 4 月 1 日第 5 版平成 24 年 7 月 1 日第 6 版平成 25 年 4 月 1 日第 7 版平成 27 年 4 月 1 日 ( 通則 ) 第 1 条この規程は 国立研究開発法人国立がん研究センター ( 以下 センターという ) が 国及びそれに準ずる機関以外の者等 ( 以下 依頼者 という ) から委託を受けて行う ヒトおよびヒト由来の材料を対象とした医学研究 ( 以下 受託研究 という ) を行うことの取り扱いを定めるものである 2 本規程にて定める 書式 は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 )( 以下 医薬品医療機器等法 という ) 第 2 条第 17 項に規定されている治験又は製造販売後臨床試験 ( 以下これらをまとめて 治験等 という ) 以外に用いるものであり 治験等に用いるものは 別途 国立研究開発法人国立がん研究センター治験等に係わる標準業務手順書 ( 以下 治験等標準業務手順書 という ) に定めるところによる ( 研究委託の申請 ) 第 2 条受託研究の申請に当たっては 研究の目的が医薬品医療機器等法に基づく医薬品 医療機器 又は再生医療等製品の承認申請等に該当する場合には 次のいずれに該当するかを明確にするものとする (1) 製造販売承認申請 (2) 製造販売承認事項一部変更承認申請 (3) 再審査申請 1 製造販売後臨床試験 2 使用成績調査 3 特定使用成績調査 (4) 再評価申請 1 製造販売後臨床試験 2 特定使用成績調査 (5) 副作用 感染症症例調査 (6) その他 2 理事長は 依頼者及び研究責任者から受託研究の申請を受け付ける際は以下の資料を提出させるものとする 但し 前項の (6) のうち 介入研究以外の研究については 原則として共同研究取扱規程に基づき申請させるものとする (1) 治験等治験等標準業務手順書に定める資料 (2) 医薬品の製造販売後の調査及び試験の実施の基準に関する省令 ( 平成 16 年 12 月 20 日厚生労働省令第 171 号 )( 以下 医薬品 GPSP 省令 という ) 医療機器の製造販売後の調査及び試験の実の基準に関する省令 ( 平成 17 年 3 月 23 日厚生労働省令第 38 号 )( 以下 医療機器 GPSP 1
2 省令 という ) 及び 再生医療等製品の製造販売後の調査及び試験の実施の基準に関する省令 ( 平成 26 年 7 月 30 日厚生労働省令第 90 号 )( 以下 再生医療等製品 GPSP 省令 という ) に規定される製造販売後調査等 ( 前条 (3)23 及び (4)2) 1 受託研究依頼書 (( 受 ) 書式 3) 2 研究実施計画書 ( プロトコール ) 3 添付文書 4 データ記録表 5 被験者の同意を得るに際しての説明同意書 ( 該当する場合 ) 6 履歴書 (( 受 ) 書式 1) 7 研究分担者 研究協力者リスト (( 受 ) 書式 2) 8 受託研究費積算書 (( 受 ) 様式 8) 9 その他 (3) 医薬品医療機器等法 ( 昭和 35 年法律第 145 号 ) 第 69 条 10の2の規定に基づく医薬品 医療機器又は再生医療等製品についての副作用 感染症及び不具合報告 ( 以下 副作用等報告 という )( 前条 (5)) 1 受託研究依頼書 (( 受 ) 書式 3) 2 データ記録表 3 添付文書 4 受託研究費積算書 (( 受 ) 様式 8) 5 その他 (4) その他の受託研究 ( 第 15 条に規定する各種指針に基づき実施する研究 ) 1 受託研究依頼書 (( 受 ) 書式 3) 2 研究実施計画書 ( プロトコール ) 3 受託研究費積算書 (( 受 ) 様式 8) 4 その他 3 受託研究の申請に必要な資料の提出先は治験事務局とする 4 申請があった受託研究が治験等に関するものである場合には 次の (1) から (3) のいずれに該当するかを明確にするものとする (1) 治験等の計画に関する研究治験等の計画に関する研究には 次の事項が含まれる 1 契約前に開催される治験責任医師等の治験計画に関する研究会等への参加 協議 (2) 治験等の実施に関する研究治験等の実施に関する研究には 次の事項が含まれる 1 治験等についての被験者への説明と同意の取得 2 被験者への治験等の実施 3 治験等に係る症例報告書の作成 4 契約期間内に開催される治験等の実施又は治験結果に関する研究会等への参加 協議 5 治験等に関する記録の保存 6 治験実施計画書等に記載されている計画等で示されているモニタリング 監査 (3) 治験等の実施後の継続研究治験等の実施後の継続研究には 次の事項が含まれる 1 契約期間終了後に開催される治験等の結果に関する研究会等への参加 協議 2 治験等に関する記録の保存 3 治験実施計画書等に記載されている計画等で示されているモニタリング 監査以外で 2
3 必要性が生じたために実施されるモニタリング 監査 (GCPの遵守) 第 3 条理事長は 申請のあった受託研究が医薬品医療機器等法に規定する治験等に該当する場合には 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日厚生省令第 28 号 )( 以下 医薬品 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令 という ) 及び 再生医療等製品の臨床試験の実施の基準に関する省令 ( 平成 26 年 7 月 30 日厚生労働省令第 89 号 )( 以下 再生医療等製品 GCP 省令 という ) 並びに関連諸通知に適合する取り扱いをするものとする 2 医薬品 GCP 省令 医療機器 GCP 省令及び再生医療等製品 GCP 省令等で規定されている 医療機関の長 は 理事長とする 3 理事長は 受託研究として治験等を行うため 国立研究開発法人国立がん研究センター治験等に係わる標準業務手順書 国立研究開発法人国立がん研究センターにおけるモニタリングの受入れに関する標準業務手順書 及び 国立研究開発法人国立がん研究センターにおける監査の受入れに関する標準業務手順書 を医薬品 GCP 省令 医療機器 GCP 省令及び再生医療等製品 GCP 省令に則って別途作成する ( 治験審査委員会 ) 第 4 条理事長は 受託研究の円滑な実施を図るため センターに 国立研究開発法人国立がん研究センター治験審査委員会 ( 以下 審査委員会 という ) を置くものとする 2 製造販売後調査等の場合 審査委員会は 次の事項について審査するものとする (1) 研究目的及び計画並びに実施の妥当性 (2) 研究結果及び発表の方法 (3) ヘルシンキ宣言の趣旨にそった倫理的配慮 ( 説明同意書の適切性を含む ) (4) 医薬品 GPSP 省令 医療機器 GPSP 省令及び再生医療等製品 GPSP 省令等への適合性 (5) その他必要事項 3 治験等の場合 審査委員会は医薬品 GCP 省令 医療機器 GCP 省令又は再生医療等製品 GCP 省令で規定する基準に基づいて審査するものとする 4 理事長は 審査委員会の円滑な運営のため 国立研究開発法人国立がん研究センター治験審査委員会標準業務手順書 を医薬品 GCP 省令 医療機器 GCP 省令及び再生医療等製品 GCP 省令に則って別途作成する 5 審査委員会の事務は研究支援センター被験者保護室 ( 治験審査委員会事務局 )( 以下 治験審査委員会事務局 ) が行う 6 審査委員会は 審議記録を備え 治験審査委員会事務局がこれを保管する ( 受託の決定等 ) 第 5 条申請のあった受託研究の受託の決定は理事長が行うものとする 但し 決定に当たっては 受託研究審査依頼書 ( 書式 4) 及び提出された資料をもって審査委員会の審査を依頼し 意見を聴かなければならない 2 理事長は センターの業務に関連のない研究 他の職務に支障を及ぼすおそれがあると判断される研究等 受託することが適当でないと認められるものについては 受託することができない 3 理事長は 当該研究の受託の承認又は不承認を依頼者及び研究責任者に受託研究審査結果 決定通知書 (( 受 ) 書式 9) にて通知するとともに 受託を承認したときは その内容を契約担当者に伝達しなければならない 3
4 4 理事長は 受託した治験等について 次の事項について治験等の継続又は変更の適否について審査委員会の意見を求め その意見に基づいて治験等の継続又は変更の可否を決定し 依頼者及び治験責任医師に通知するものとする (1) 重篤で予測できない副作用等について依頼者又は治験責任医師から通知を受けた場合 (2) 治験等に継続して参加するかどうかについて被験者の意思に影響を与えるものと認められる情報を入手し 被験者に対する説明文書を改訂した旨治験責任医師から報告を受けた場合 (3) 依頼者から治験実施計画書につき変更を行いたい旨の申請があった場合 (4) その他必要があると認められる場合 5 前項までに定める理事長の決定に当たっては 治験責任医師が所属する病院長からあらかじめ治験審査委員会の意見を踏まえた許可が得られていなければならない ( 契約の条件 ) 第 6 条契約担当者は 第 5 条第 3 項の規定に基づく伝達を受け 依頼者と研究の受託に関する契約を締結するときは 原則として次に掲げる条件を付さなければならない (1) 依頼者は 受託研究に要する経費のうち 受託研究の適正な実施に必要な事務的経費等 ( 以下 研究費 という ) については 請求書に定めた期限までに納付すること また 治験に係る保険外併用療養費の支給対象外の経費 ( 以下 支給対象外経費 という ) については 研究費とは別に診療月の翌月毎にその全額を請求書をもって依頼者に請求すること (2) 研究費により取得した物品等は 当該研究終了後も依頼者に返還しないこと (3) やむを得ない事由により受託研究を中止し 又はその期間を延長する場合 センターはその責を負わないこと 2 受託研究に随伴して生じた発明等による知的財産権の所有は原則として依頼者に帰属するが 治験責任医師より申し出があった場合は依頼者と協議を持って決定することが出来ること 3 研究費が請求書に定めた期限までに納付されなかった場合は 契約は解除するものとし すみやかに所要の手続きをとること 4 契約書は 二者契約の場合 正本を2 通作成し センターが1 通所持すること ( 受託研究の実施 ) 第 7 条研究者は 承認された受託研究実施計画書等に従い受託研究を実施する また 研究者は 被験者及びその代諾者にその趣旨を十分説明するとともに 当該受託研究が治験等である場合には 医薬品 GCP 省令第 51 条 52 条 医療機器 GCP 省令第 71 条 72 条又は再生医療等製品 GCP 省令第 71 条 第 72 条に基づき文書により 治験等の実施について説明し 同意 ( 被験者の診療に際して実施した検査 画像診断等の内容を依頼者に提出することがある旨の説明と同意を含む ) を得るものとし 被験者の安全について適切な配慮をしなければならない 2 依頼者と研究責任者は 受託研究の実施計画書等に変更が生じた場合には 受託研究に関する変更申請書 (( 受 ) 書式 5) にて 理事長に申請するとともに 変更に基づく研究の継続の可否について理事長の指示を受けること 3 研究責任者は 治験等の実施中に重篤な有害事象又は重大な不具合が発生した場合には 速やかに理事長及び依頼者に文書で報告するとともに 治験等の継続の可否について理事長の指示を受けること 4 研究責任者は 治験等の実施中に被験者の緊急の危険を回避するためその他医療上やむを得ない理由により治験実施計画書に従わなかった場合には 速やかに理事長及び依頼者に文書で報告すること 4
5 ( 治験等の継続 ) 第 8 条研究責任者は治験等の期間が 1 年を超えるものは 1 年に 1 回以上 理事長に治験等の実施状 況を報告するとともに 治験等の継続の可否について理事長の指示を受けること ( 研究結果の報告等 ) 第 9 条研究責任者は 当該研究を終了したときは 速やかに受託終了 ( 中止 中断 ) 報告書 (( 受 ) 書式 7) にて理事長へ報告しなければならない 2 理事長は 前項の報告があったときは 審査委員会及び依頼者に通知するものとする 3 研究責任者は 当該研究を中止したときは その旨を速やかに受託終了 ( 中止 中断 ) 報告書 (( 受 ) 書式 7) にて理事長へ報告し 必要な指示を受けなければならない 4 理事長は 前項の報告があったときは 契約担当者に伝達するとともに依頼者に通知するものとする ( 治験等のモニタリング及び監査 ) 第 10 条理事長は 治験等のモニタリング及び監査の実施について 依頼者と十分協議し 依頼者のモニタリング担当者及び監査担当者に 依頼者における被験者の情報の秘密保持について十分注意させるものとする ( 治験薬 治験機器及び治験製品等の管理 ) 第 11 条理事長は 中央病院及び東病院の薬剤部長を治験薬及び製造販売後臨床試験薬 ( 以下 治験薬等 という ) の管理者 ( 以下 治験薬管理者 という ) に定め 各々の病院内で使用される全ての治験薬等を適切な方法にて管理させるものとする 2 治験機器等の管理については 当該研究期間中は治験責任医師において保管 管理し 終了後は直ちに現状復帰するものとする 3 治験製品等の管理については その特性に応じ 治験薬管理者又は治験責任医師に適切な方法にて保管 管理させるものとする ( 人員の派遣 ) 第 12 条原則として人員の派遣は認めない 但し 機械開発等で研究者が研究の初期にその専門知識を持つ研究補助者の派遣を要する場合 又はセンターの研究者が開発した検査法等を用いて依頼者が検査試薬等の製造承認をとる目的で行う受託研究で かつ 依頼者側が専門知識の修得のため研究補助者の派遣を要する場合に限り 補助者届書等により申請し 審査委員会の承認を得るものとする なお 依頼者は同研究補助者に係る雇用上のすべての義務を負担するものとし また センターに一切の不利益を与えてはならない 2 派遣された研究補助者の管理上の責任者は 当該研究の研究責任者とする ( 記録等の保存責任者 ) 第 13 条理事長は 次に掲げる記録毎に保存責任者を定めるものとする (1) 診療録 検査データ等及び署名済みの同意文書は病院長とする (2) 研究責任者宛の通知書等は 研究責任者とする (3) 研究受託に関する書類 ( 受託研究申請書 契約書 願出整理簿等 ) は 治験事務局長とする (4) 審査委員会の運営に関する記録 ( 審査委員会議事録 ) は 委員長補佐とする (5) 治験薬等の管理に関する記録 ( 治験薬等の管理表 受領書 返却書等 ) は治験薬管理者とす 5
6 る (6) 治験機器等の管理に関する記録 ( 治験機器管理表 治験機器出納表 治験機器納品書等 ) は治験責任医師とする (7) 治験製品等の管理に関する記録 ((5) 又は (6) に準ずる ) は治験薬管理者又は治験責任医師とする (8) 研究課題別出納簿は 中央病院は財務経理部長 東病院は管理課長とする 2 前項の記録の保存期間は 当該受託研究終了後 5 年間保管するものとする 但し 治験等にあっては GCP 省令第 41 条第 2 項 医療機器 GCP 省令第 61 条第 2 項及び再生医療等製品 GCP 省令第 61 条第 2 項により 製造販売の承認を受ける日 承認申請書に資料として添付しないと通知を受けた日後 3 年を経過した日又は治験の中止若しくは終了の後 3 年を経過した日のうちいずれか遅い日までとする 製造販売後臨床試験の場合は 再審査又は再評価が終了した日から5 年間経過した日 但し 平成 17 年 4 月 1 日以降に製造販売後臨床試験実施計画書の提出が行われた臨床試験にあっては 当該被験薬の再審査又は再評価が終了した日とする ただし 治験依頼者がこれよりも長期間の保存を必要とする場合には 保存期間及び保存方法について治験依頼者と協議するものとする ( 治験事務局 ) 第 14 条理事長は 受託研究の円滑な実施を図るため 中央病院治験管理室及び東病院治験管理室に医薬品 GCP 省令第 38 条 医療機器 GCP 省令第 57 条及び再生医療等製品 GCP 省令第 57 条に規定されている治験事務局を置く 2 治験事務局に治験事務局長を置き 治験事務局長は理事長の指名する者とする 治験事務局長はやむ終えない事情によりその業務ができないときのために その業務を代理する者を指名することができる 3 治験事務局の業務は 国立研究開発法人国立がん研究センター治験等に係わる標準業務手順書 において別途定める ( 各種指針を遵守する受託研究の申請 ) 第 15 条研究責任者は 申請を行う受託研究が 人を対象とする医学系研究に関する倫理指針 ( 文部科学省 厚生労働省 ) ヒトゲノム 遺伝子解析研究に関する倫理指針( 文部科学省 厚生労働省 経済産業省 ) 又は 遺伝子治療臨床研究に関する指針( 文部科学省 厚生労働省 ) を遵守して行うものである場合には 別途 国立研究開発法人国立がん研究センター人を対象とした医学系研究に関する標準業務手順書 又は 国立研究開発法人国立がん研究センター遺伝子治療倫理審査取扱規程 等適用される規程等に従った申請も行うものとする 2 前項に該当する受託研究については 遵守する指針に応じた各研究倫理審査委員会の審査を受けるものとし 原則として治験審査委員会における審査を不要とする 附則この規程は 平成 22 年 4 月 1 日から施行する 附則 ( 第 2 版 ) 1 この規程は 平成 22 年 10 月 1 日から施行する 6
7 2 受託研究審査予備調査会に関する規定を削除したことにより 当規程の施行によって 独立行 政法人国立がん研究センター受託研究審査予備調査会規程 を廃止とする 附則 ( 平成 23 年規程第 号 ) この規程は 平成 23 年 4 月 1 日から施行する 附則 ( 平成 24 年規程第 18 号 ) この規程は 平成 24 年 4 月 1 日から施行する 附則 ( 平成 24 年規程第 38 号 ) この規程は 平成 24 年 7 月 1 日から施行する 附則 ( 平成 25 年規程第 33 号 ) 1 この規程は 平成 25 年 4 月 1 日から施行する 2 従前の受託研究審査委員会を治験審査委員会としたことにより 当規程の施行によって 独立行政法人国立がん研究センター受託研究審査委員会運営規程 を廃止とする 附則 ( 平成 27 年規程第 8 号 ) この規程は 平成 27 年 4 月 1 日から施行する 附則 ( 平成 27 年規程第 44 号 ) この規程は 平成 27 年 4 月 1 日から施行する ( 受 ) 書式 1 研究責任者 研究分担者履歴書 ( 受 ) 書式 2 研究分担者 研究協力者リスト ( 受 ) 書式 3 受託研究依頼書 ( 受 ) 書式 4 受託研究審査依頼書 7
8 ( 受 ) 書式 5 受託研究に関する変更申請書 ( 受 ) 書式 6 受託研究実施状況報告書 ( 受 ) 書式 7 受託終了 ( 中止 中断 ) 報告書 ( 受 ) 書式 8 受託研究費積算書 ( 受 ) 書式 9 受託研究審査結果 決定通知書 ( 受 ) 書式 10 受託研究 ( 治験以外 ) 契約書 ( 受 ) 書式 11 製造販売後調査契約書 8
国立仙台病院受託研究取扱規程
 独立行政法人国立病院機構仙台医療センター受託研究取扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構仙台医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程の定めるところによる 2 契約 経理及び書式等については 原則として独立行政法人国立病院機構
独立行政法人国立病院機構仙台医療センター受託研究取扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構仙台医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程の定めるところによる 2 契約 経理及び書式等については 原則として独立行政法人国立病院機構
規程書
 独立行政法人国立病院機構栃木医療センター 受託研究取扱規程 平成 25 年 4 月 1 日 独立行政法人国立病院機構栃木医療センター受託研究取 扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構栃木医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程定めるところによる
独立行政法人国立病院機構栃木医療センター 受託研究取扱規程 平成 25 年 4 月 1 日 独立行政法人国立病院機構栃木医療センター受託研究取 扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構栃木医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程定めるところによる
<4D F736F F D208EA18CB182C98AD682B782E995578F808BC696B18EE88F878F E38E748EE593B1816A E7B8D732E646F637
 治験に関する標準業務手順書 ( 医師主導治験 ) 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医師主導治験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 (
治験に関する標準業務手順書 ( 医師主導治験 ) 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医師主導治験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 (
国立研究開発法人国立循環器病研究センター受託研究取扱規程 ( )
 国立研究開発法人国立循環器病研究センター受託研究取扱規程 (20190401) 平成 22 年 4 月 1 日規程第 46 号 国立研究開発法人国立循環器病研究センター受託研究取扱規程 ( 通則 ) 第 1 条国立研究開発法人国立循環器病研究センター ( 以下 センター という ) においてセンター以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては
国立研究開発法人国立循環器病研究センター受託研究取扱規程 (20190401) 平成 22 年 4 月 1 日規程第 46 号 国立研究開発法人国立循環器病研究センター受託研究取扱規程 ( 通則 ) 第 1 条国立研究開発法人国立循環器病研究センター ( 以下 センター という ) においてセンター以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては
<4D F736F F D208EA18CB182C98AD682B782E995578F808BC696B18EE88F878F E7B8D732E646F6378>
 治験に関する標準業務手順書 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医薬品及び医療機器の臨床試験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和
治験に関する標準業務手順書 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医薬品及び医療機器の臨床試験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和
標準業務手順 目次
 浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会
 治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会 第 1 条 ( 目的 ) 1. 本手順書は 新光会治験審査委員会 ( 以下 委員会という ) において 医薬品及び医療機器 ( 以下 医薬品等という ) の治験の調査審議を実施するに当たり 薬事法 ( 昭和 35 年 8 月 10 日法律第 145 号 ) に基づく 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3
治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会 第 1 条 ( 目的 ) 1. 本手順書は 新光会治験審査委員会 ( 以下 委員会という ) において 医薬品及び医療機器 ( 以下 医薬品等という ) の治験の調査審議を実施するに当たり 薬事法 ( 昭和 35 年 8 月 10 日法律第 145 号 ) に基づく 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3
北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下
 北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下 モニタリング という ) 監査の受け入れ 並びに試験審査委員会( 治験審査委員会が兼ねる 以下 治験審査委員会
北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下 モニタリング という ) 監査の受け入れ 並びに試験審査委員会( 治験審査委員会が兼ねる 以下 治験審査委員会
国立病院機構大阪医療センター受託研究取扱細則
 国立病院機構大阪医療センター 受託研究取扱細則 ( 主旨 ) 第 1 条国立病院機構大阪医療センターにおける受託研究の取扱いに関しては 国立病院機構大阪医療センター受託研究取扱規程 ( 以下 規程 という ) 及び他に定めるもののほか 規程第 1 条第 2 項に規定するこの細則の定めるところによる ( 総則 ) 第 2 条研究責任者は 原則として医長職相当以上とする ただし 副作用報告及び感染症報告を受託研究として実施する場合
国立病院機構大阪医療センター 受託研究取扱細則 ( 主旨 ) 第 1 条国立病院機構大阪医療センターにおける受託研究の取扱いに関しては 国立病院機構大阪医療センター受託研究取扱規程 ( 以下 規程 という ) 及び他に定めるもののほか 規程第 1 条第 2 項に規定するこの細則の定めるところによる ( 総則 ) 第 2 条研究責任者は 原則として医長職相当以上とする ただし 副作用報告及び感染症報告を受託研究として実施する場合
実施医療機関治験審査委員会標準的業務手順書
 実施医療機関治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令 という
実施医療機関治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令 という
( 委員会の業務 ) 第 4 条委員会は その責務の遂行のために以下の最新資料を病院長から入手する なお あらかじめ 自ら治験を実施する者 委員会及び病院長の合意が得られている場合においては GCP 省令第 26 条の6 第 2 項に関する通知に限り 自ら治験を実施する者から入手することができる ま
 秋田大学医学部附属病院医師主導治験における治験審査委員会規程 第 1 章医師主導治験審査委員会 ( 目的と適用範囲 ) 第 1 条本規程は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 医薬品の臨床試験の実施の基準に関する省令( 平成 9 年 3 月 27 日厚生省令第 28 号 )( 以下 GCP 省令 という ) 並びにGCP 省令に関連する通知書等に基づいて
秋田大学医学部附属病院医師主導治験における治験審査委員会規程 第 1 章医師主導治験審査委員会 ( 目的と適用範囲 ) 第 1 条本規程は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 医薬品の臨床試験の実施の基準に関する省令( 平成 9 年 3 月 27 日厚生省令第 28 号 )( 以下 GCP 省令 という ) 並びにGCP 省令に関連する通知書等に基づいて
長崎大学病院治験審査委員会内規 平成 21 年 4 月 1 日 病院内規第 3 号 ( 趣旨 ) 第 1 条この内規は, 長崎大学病院における医薬品の臨床試験の実施に関する内規 ( 以下 治験内規 という ) 第 4 条第 2 項, 長崎大学病院における医療機器の臨床試験の実施に関する内規 ( 以下
 長崎大学病院治験審査委員会内規 平成 21 年 4 月 1 日 病院内規第 3 号 ( 趣旨 ) 第 1 条この内規は, 長崎大学病院における医薬品の臨床試験の実施に関する内規 ( 以下 治験内規 という ) 第 4 条第 2 項, 長崎大学病院における医療機器の臨床試験の実施に関する内規 ( 以下 医療機器治験内規 という ) 第 4 条第 2 項及び長崎大学病院における再生医療等製品の臨床試験の実施に関する内規
長崎大学病院治験審査委員会内規 平成 21 年 4 月 1 日 病院内規第 3 号 ( 趣旨 ) 第 1 条この内規は, 長崎大学病院における医薬品の臨床試験の実施に関する内規 ( 以下 治験内規 という ) 第 4 条第 2 項, 長崎大学病院における医療機器の臨床試験の実施に関する内規 ( 以下 医療機器治験内規 という ) 第 4 条第 2 項及び長崎大学病院における再生医療等製品の臨床試験の実施に関する内規
実施医療機関治験審査委員会標準的業務手順書
 地方独立行政法人静岡市立静岡病院 治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 及び医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器
地方独立行政法人静岡市立静岡病院 治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 及び医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器
川崎市水道局規程第 号
 川崎市立川崎病院治験取扱要綱 ( 要旨 ) 第 1 条川崎市立川崎病院 ( 川崎市病院事業の設置等に関する条例 ( 昭和 41 年川崎市条例第 42 号 ) 第 2 条第 2 項の表に規定する病院 以下 病院 という ) の医薬品等の臨床研究の実施については 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 以下 法 という ) 医薬品の臨床試験の実施の基準に関する省令
川崎市立川崎病院治験取扱要綱 ( 要旨 ) 第 1 条川崎市立川崎病院 ( 川崎市病院事業の設置等に関する条例 ( 昭和 41 年川崎市条例第 42 号 ) 第 2 条第 2 項の表に規定する病院 以下 病院 という ) の医薬品等の臨床研究の実施については 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 以下 法 という ) 医薬品の臨床試験の実施の基準に関する省令
3 治験実施計画書目的 当該治験について 治験実施計画書が手順書に従い適切に作成及び改訂されていることを確認する 次の事項を調べる (1) 治験実施計画書の記載項目 ( 再生医療等製品 GCP 省令第 7 条第 1 項に規定する項目 ) (2) 治験実施計画書の作成 改訂の手順と日付 (3) 治験計
 別添 10 再生医療等製品 GCP 省令チェックリスト Ⅰ 治験依頼者 ( 受託機関を含む ) 用 1 組織及び体制目的 治験の依頼及び管理に当たって 再生医療等製品 GCP 省令に沿った業務を行うために適切にして十分な人材を有し かつ 組織及び体制が確立していることを確認する 1 治験依頼者の組織 ( 当該被験機器の開発組織を含む ) と再生医療等製品 G CP 省令に係わる組織との関係 2 治験の依頼及び管理の業務に従事する者の氏名
別添 10 再生医療等製品 GCP 省令チェックリスト Ⅰ 治験依頼者 ( 受託機関を含む ) 用 1 組織及び体制目的 治験の依頼及び管理に当たって 再生医療等製品 GCP 省令に沿った業務を行うために適切にして十分な人材を有し かつ 組織及び体制が確立していることを確認する 1 治験依頼者の組織 ( 当該被験機器の開発組織を含む ) と再生医療等製品 G CP 省令に係わる組織との関係 2 治験の依頼及び管理の業務に従事する者の氏名
平成22年月1日要領第59号
 平成 22 年 4 月 1 日要領第 59 号 国立研究開発法人国立がん研究センター治験等に係わる標準業務手順書 第 1 版平成 22 年 4 月 1 日第 2 版平成 22 年 8 月 1 日第 3 版平成 22 年 10 月 1 日第 4 版平成 23 年 4 月 1 日第 5 版平成 24 年 4 月 1 日第 6 版平成 24 年 7 月 1 日第 7 版平成 25 年 4 月 1 日第 8
平成 22 年 4 月 1 日要領第 59 号 国立研究開発法人国立がん研究センター治験等に係わる標準業務手順書 第 1 版平成 22 年 4 月 1 日第 2 版平成 22 年 8 月 1 日第 3 版平成 22 年 10 月 1 日第 4 版平成 23 年 4 月 1 日第 5 版平成 24 年 4 月 1 日第 6 版平成 24 年 7 月 1 日第 7 版平成 25 年 4 月 1 日第 8
神戸市立医療センター西市民病院治験審査委員会業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関
 神戸市立医療センター西市民病院治験審査委員会 標準業務手順書 目次 第 1 章治験審査委員会 目的と適用範囲 1 治験審査委員会の責務 1 治験審査委員会の設置及び構成 1 治験審査委員会の業務 2 治験審査委員会の運営 4 第 2 章治験審査委員会事務局治験審査委員会事務局の業務 6 第 3 章記録の保存記録の保存責任者 6 記録の保存期間 6 手順書の改訂 7 第 4 章情報公開会議の記録等の公表
神戸市立医療センター西市民病院治験審査委員会 標準業務手順書 目次 第 1 章治験審査委員会 目的と適用範囲 1 治験審査委員会の責務 1 治験審査委員会の設置及び構成 1 治験審査委員会の業務 2 治験審査委員会の運営 4 第 2 章治験審査委員会事務局治験審査委員会事務局の業務 6 第 3 章記録の保存記録の保存責任者 6 記録の保存期間 6 手順書の改訂 7 第 4 章情報公開会議の記録等の公表
12_モニタリングの実施に関する手順書
 12_ モニタリングの実施に関する手順書 静岡県立大学大学院薬食生命科学総合学府薬学研究院薬食研究推進センター版数 :1.0 版作成年月日 :2014 月 8 月 1 日 ( 最終確定 :2015 年 1 月 14 日 ) 1. 目的と適用範囲 本手順書は 当該研究において モニターが モニタリングを適切に実施するための手順 その他必要な事項を定めるものである 2. 実施体制及び責務 2.1 研究責任者の責務研究責任者は
12_ モニタリングの実施に関する手順書 静岡県立大学大学院薬食生命科学総合学府薬学研究院薬食研究推進センター版数 :1.0 版作成年月日 :2014 月 8 月 1 日 ( 最終確定 :2015 年 1 月 14 日 ) 1. 目的と適用範囲 本手順書は 当該研究において モニターが モニタリングを適切に実施するための手順 その他必要な事項を定めるものである 2. 実施体制及び責務 2.1 研究責任者の責務研究責任者は
宮城県立がんセンター受託研究業務手順書
 平成 26 年 4 月 1 日一部改正使用成績調査 特定使用成績調査編 本編は 薬事法第 14 条の 4 及び第 14 条の 6 に基づく医薬品及び医療機器の再審査 再評価申請の際に提出すべき資料の収集のために行われる製造販売後調査 ( 使用成績調査及び特定使用成績調査 )( 以下 使用成績調査等 ) に適用するものとする 本編は 薬事法第 14 条の 4 第 4 項 薬事法第 14 条の 6 第
平成 26 年 4 月 1 日一部改正使用成績調査 特定使用成績調査編 本編は 薬事法第 14 条の 4 及び第 14 条の 6 に基づく医薬品及び医療機器の再審査 再評価申請の際に提出すべき資料の収集のために行われる製造販売後調査 ( 使用成績調査及び特定使用成績調査 )( 以下 使用成績調査等 ) に適用するものとする 本編は 薬事法第 14 条の 4 第 4 項 薬事法第 14 条の 6 第
治験の原則
 大阪大学医学部附属病院 治験に係わる標準業務手順書 平成 26 年 1 月 1 日作成平成 26 年 4 月 1 日改訂平成 27 年 4 月 1 日改訂平成 29 年 4 月 1 日改訂平成 30 年 10 月 16 日改訂平成 30 年 12 月 16 日改訂 目 次 治験の原則 第 1 章目的と適用範囲第 1 条目的と適用範囲 第 2 章病院長の業務 第 2 条 治験の申請等 第 3 条 治験実施の了承等
大阪大学医学部附属病院 治験に係わる標準業務手順書 平成 26 年 1 月 1 日作成平成 26 年 4 月 1 日改訂平成 27 年 4 月 1 日改訂平成 29 年 4 月 1 日改訂平成 30 年 10 月 16 日改訂平成 30 年 12 月 16 日改訂 目 次 治験の原則 第 1 章目的と適用範囲第 1 条目的と適用範囲 第 2 章病院長の業務 第 2 条 治験の申請等 第 3 条 治験実施の了承等
PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1
 PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1 項第 1 号に定める医療機器リスク管理計画書をもって 承認申請資料のうち臨床試験の試験成績に関する資料又はこれに代替するものとして厚生労働大臣が認める資料の一部に代えることができることとしたこと
PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1 項第 1 号に定める医療機器リスク管理計画書をもって 承認申請資料のうち臨床試験の試験成績に関する資料又はこれに代替するものとして厚生労働大臣が認める資料の一部に代えることができることとしたこと
独立行政法人国立病院機構仙台医療センターにおける医薬 品等の使用成績調査 特定使用成績調査及び副作用 感染 症報告 その他の受託研究の実施に関する標準業務手順書 2018 年 7 月 26 日第 9 版
 独立行政法人国立病院機構仙台医療センターにおける医薬 品等の使用成績調査 特定使用成績調査及び副作用 感染 症報告 その他の受託研究の実施に関する標準業務手順書 2018 年 7 月 26 日第 9 版 第 1 章総則 1. 目的と適用範囲この標準業務手順書は 独立行政法人国立病院機構仙台医療センターにおける医薬品の再審査申請 再評価申請の際に提出すべき資料の収集のための 使用成績調査 及び 特定使用成績調査
独立行政法人国立病院機構仙台医療センターにおける医薬 品等の使用成績調査 特定使用成績調査及び副作用 感染 症報告 その他の受託研究の実施に関する標準業務手順書 2018 年 7 月 26 日第 9 版 第 1 章総則 1. 目的と適用範囲この標準業務手順書は 独立行政法人国立病院機構仙台医療センターにおける医薬品の再審査申請 再評価申請の際に提出すべき資料の収集のための 使用成績調査 及び 特定使用成績調査
治験実施規程
 京都市立病院 治験実施要綱 平成 25 年 9 月 2 日 ( 第 7 版 ) 目次 第 Ⅰ 章総則 1 第 1 条 ( 目的 ) 1 第 2 条 ( 治験に関する原則事項 ) 1 第 3 条 ( 用語 ) 2 第 4 条 ( 秘密の保全 ) 2 第 5 条 ( 直接閲覧 ) 2 第 Ⅱ 章院長 2 第 6 条 ( 治験実施体制の構築 ) 2 第 7 条 ( 治験の受託 ) 3 第 8 条 ( 治験の継続
京都市立病院 治験実施要綱 平成 25 年 9 月 2 日 ( 第 7 版 ) 目次 第 Ⅰ 章総則 1 第 1 条 ( 目的 ) 1 第 2 条 ( 治験に関する原則事項 ) 1 第 3 条 ( 用語 ) 2 第 4 条 ( 秘密の保全 ) 2 第 5 条 ( 直接閲覧 ) 2 第 Ⅱ 章院長 2 第 6 条 ( 治験実施体制の構築 ) 2 第 7 条 ( 治験の受託 ) 3 第 8 条 ( 治験の継続
大学病院治験受託手順書
 千葉大学医学部附属病院治験審査委員会運営手順書 第 1 条目的本手順書は 千葉大学医学部附属病院各種委員会規程の定めるところにより 千葉大学医学部附属病院治験審査委員会 ( 以下 委員会 という ) の運営方法を定め 医薬品等の治験 製造販売後調査および臨床試験等に関わる業務手順を示すものである 第 2 条委員会の責務 1 本委員会は 千葉大学医学部附属病院 ( 以下 本院 という ) において 治験及び製造販売後臨床試験
千葉大学医学部附属病院治験審査委員会運営手順書 第 1 条目的本手順書は 千葉大学医学部附属病院各種委員会規程の定めるところにより 千葉大学医学部附属病院治験審査委員会 ( 以下 委員会 という ) の運営方法を定め 医薬品等の治験 製造販売後調査および臨床試験等に関わる業務手順を示すものである 第 2 条委員会の責務 1 本委員会は 千葉大学医学部附属病院 ( 以下 本院 という ) において 治験及び製造販売後臨床試験
実施医療機関治験審査委員会標準的業務手順書
 静岡市立清水病院治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令 という
静岡市立清水病院治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令 という
PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1
 薬生発 07 31 第 4 号 平成 29 年 7 月 31 日 各都道府県知事殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則の一部を改正する省令 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令の一部を改正する省令 及び 医療機器の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令
薬生発 07 31 第 4 号 平成 29 年 7 月 31 日 各都道府県知事殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則の一部を改正する省令 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令の一部を改正する省令 及び 医療機器の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令
<4D F736F F D E34208EA18CB18EE891B182AB977697CC C8E8DB782B591D682A688CB978A>
 Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
( 書式 4), 治験責任医師の履歴書及び治験実施計画書等の審査の対象となる文書を委員会に提出し, 治験の実施について意見を求めるものとする 2 病院長は, 委員会が治験の実施を承認する決定をし, 又は治験実施計画書, 症例報告書, 説明文書及び同意書並びにその他の手順について何らかの修正を条件に治
 秋田大学医学部附属病院医薬品等の受託研究取扱細則 病 7-07 [ 制定 ] 平成 16 年 4 月 1 日 ( 趣旨と適用範囲 ) 第 1 条この細則は, 秋田大学医学部附属病院医薬品等の受託研究取扱規程第 15 条に基づき, 治験の実施に必要な手続きと運営に関する手順を定めるものとする 本細則の運用に関しては医薬品の臨床試験の実施に関する省令 ( 平成 9 年厚生省令第 28 号 以下 医薬品
秋田大学医学部附属病院医薬品等の受託研究取扱細則 病 7-07 [ 制定 ] 平成 16 年 4 月 1 日 ( 趣旨と適用範囲 ) 第 1 条この細則は, 秋田大学医学部附属病院医薬品等の受託研究取扱規程第 15 条に基づき, 治験の実施に必要な手続きと運営に関する手順を定めるものとする 本細則の運用に関しては医薬品の臨床試験の実施に関する省令 ( 平成 9 年厚生省令第 28 号 以下 医薬品
<4D F736F F D EA18CB182C98C5782E98EE88F878F915F8EC08E7B88E397C38B408AD F392E30816A2E646F63>
 JA 静岡厚生連静岡厚生病院における治験に係る標準業務手順書 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP
JA 静岡厚生連静岡厚生病院における治験に係る標準業務手順書 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP
実施医療機関における治験に係る標準的業務手順書
 静岡市立清水病院における治験に係る標準業務手順書 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令
静岡市立清水病院における治験に係る標準業務手順書 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令
山形県立中央病院治験審査委員会業務手順書
 山形県立中央病院治験審査委員会業務手順書 第 1 目的この手順書は山形県立中央病院医薬品等臨床試験受託研究取扱要綱 ( 以下 取扱要綱 という ) に基づいて山形県立中央病院治験審査委員会 ( 以下 本委員会 という ) の運用方法を定め それに基づく業務手順書を示すものである なお 製造販売後臨床試験においては 以下 治験 とあるのを 製造販売後臨床試験 と読み替えるものとする 第 2 本委員会の責務本委員会は全ての被験者の人権の保護
山形県立中央病院治験審査委員会業務手順書 第 1 目的この手順書は山形県立中央病院医薬品等臨床試験受託研究取扱要綱 ( 以下 取扱要綱 という ) に基づいて山形県立中央病院治験審査委員会 ( 以下 本委員会 という ) の運用方法を定め それに基づく業務手順書を示すものである なお 製造販売後臨床試験においては 以下 治験 とあるのを 製造販売後臨床試験 と読み替えるものとする 第 2 本委員会の責務本委員会は全ての被験者の人権の保護
ICH-GCPとJ-GCPとの比較表
 参考資料 10 我が国の GCP と ICH-GCP の主な 1 治験の契約に関する規定 1-1 契約者に関する規定 1-2 実施医療機関の長との契約を規定したことに伴う規定 2 治験審査委員会 (IRB) に関する規定 2-1 IRB の設置に関する規定 2-2 IRB への審議依頼に関する規定 1/11 1. 治験の契約に関する規定 1-1. 契約者に関する規定 ICH-GCP 1.17( 用語の定義
参考資料 10 我が国の GCP と ICH-GCP の主な 1 治験の契約に関する規定 1-1 契約者に関する規定 1-2 実施医療機関の長との契約を規定したことに伴う規定 2 治験審査委員会 (IRB) に関する規定 2-1 IRB の設置に関する規定 2-2 IRB への審議依頼に関する規定 1/11 1. 治験の契約に関する規定 1-1. 契約者に関する規定 ICH-GCP 1.17( 用語の定義
大阪府立成人病センター治験標準業務手順書(平成23年12月21日改正案)
 大阪国際がんセンター治験標準業務手順書 制定平成 10 年 4 月 1 日改訂平成 21 年 3 月 1 日改訂平成 21 年 5 月 20 日改訂平成 21 年 8 月 19 日改訂平成 22 年 2 月 15 日改訂平成 22 年 5 月 17 日改訂平成 24 年 2 月 1 日改訂平成 24 年 5 月 1 日改訂平成 25 年 4 月 1 日改訂平成 25 年 12 月 1 日改訂平成 27
大阪国際がんセンター治験標準業務手順書 制定平成 10 年 4 月 1 日改訂平成 21 年 3 月 1 日改訂平成 21 年 5 月 20 日改訂平成 21 年 8 月 19 日改訂平成 22 年 2 月 15 日改訂平成 22 年 5 月 17 日改訂平成 24 年 2 月 1 日改訂平成 24 年 5 月 1 日改訂平成 25 年 4 月 1 日改訂平成 25 年 12 月 1 日改訂平成 27
医師主導治験取扱要覧
 15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
治 験 実 施 標 準 業 務 手 順 書
 治験審査委員会標準業務手順書 < 企業治験 > 横浜労災病院 目 次 第 1 章治験審査委員会 2 目的と適用範囲 2 治験審査委員会の責務 2 治験審査委員会の設置及び構成 2 治験審査委員会の業務 3 治験審査委員会の運営 5 第 2 章治験審査委員会事務局 6 治験審査委員会事務局の設置と業務 6 第 3 章記録の保存と公開 7 記録の保存責任者 7 記録の保存期間 7 記録の公開 8 1 第
治験審査委員会標準業務手順書 < 企業治験 > 横浜労災病院 目 次 第 1 章治験審査委員会 2 目的と適用範囲 2 治験審査委員会の責務 2 治験審査委員会の設置及び構成 2 治験審査委員会の業務 3 治験審査委員会の運営 5 第 2 章治験審査委員会事務局 6 治験審査委員会事務局の設置と業務 6 第 3 章記録の保存と公開 7 記録の保存責任者 7 記録の保存期間 7 記録の公開 8 1 第
<4D F736F F D20362D318EA18CB190528DB888CF88F589EF8BC696B18EE88F878F912E646F63>
 独立行政法人国立病院機構敦賀医療センターにおける企業主導治験に係る治験審査委員会業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は当院における 受託研究取扱規程 及び 企業主導治験に係る標準業務手順書 に基づいて 企業主導治験に係る標準業務手順書第 12 条第 1 項の規定により院内に設置された治験審査委員会の運営に関する手続き及び記録の保存方法等を定めるものである
独立行政法人国立病院機構敦賀医療センターにおける企業主導治験に係る治験審査委員会業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は当院における 受託研究取扱規程 及び 企業主導治験に係る標準業務手順書 に基づいて 企業主導治験に係る標準業務手順書第 12 条第 1 項の規定により院内に設置された治験審査委員会の運営に関する手続き及び記録の保存方法等を定めるものである
静岡県立静岡がんセンター臨床研究事務局の業務手順書
 治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 6.0 平成 20 年 1 月 28
治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 6.0 平成 20 年 1 月 28
Microsoft Word - 儻師主尔治é¨fiㆫ俇㇉樎溌æ¥�å‰Žæ›‰é€ƒæł¸( )
 国立研究開発法人国立長寿医療研究センターにおける 医師主導治験に係る標準業務手順書 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 医薬品の臨床試験の実施の基準に関する省令( 平成 9 年厚生省令第 28 号 )( 以下 医薬品 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令
国立研究開発法人国立長寿医療研究センターにおける 医師主導治験に係る標準業務手順書 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 医薬品の臨床試験の実施の基準に関する省令( 平成 9 年厚生省令第 28 号 )( 以下 医薬品 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令
<4D F736F F D2093D689EA88E397C3835A E815B8AE98BC68EE593B195578F808BC696B18EE88F878F BD90AC E378C8E313393FA89FC92F9816A2E646F6378>
 独立行政法人国立病院機構敦賀医療センターにおける 企業主導治験に係る業務手順書 第 1 章 目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本手順書は 独立行政法人国立病院機構敦賀医療センター受託研究取扱規程 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年厚生省令第 28 号 以下 医薬品 G CP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年厚生労働省令第
独立行政法人国立病院機構敦賀医療センターにおける 企業主導治験に係る業務手順書 第 1 章 目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本手順書は 独立行政法人国立病院機構敦賀医療センター受託研究取扱規程 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年厚生省令第 28 号 以下 医薬品 G CP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年厚生労働省令第
第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ; 平成 9 年厚生省令第 28 号 ( 以下 医薬品 GCP という ) 医療機器の臨床試験の実施の基準に関する省令 ; 平成 17 年厚生労働省令第 36 号 ( 以下 医療機器 G
 千葉大学医学部附属病院治験取扱手順書 ( 治験依頼者による治験 ) 治験の原則 治験は 次に掲げる原則に則って実施されなければならない 1. 治験は ヘルシンキ宣言に基づく倫理的原則及び GCP を遵守して行われなければならない 2. 治験を開始する前に 個々の被験者及び社会にとって期待される利益と予想される危険及び不便とを比較考量するものとする 期待される利益によって危険を冒すことが正当化される場合に限り
千葉大学医学部附属病院治験取扱手順書 ( 治験依頼者による治験 ) 治験の原則 治験は 次に掲げる原則に則って実施されなければならない 1. 治験は ヘルシンキ宣言に基づく倫理的原則及び GCP を遵守して行われなければならない 2. 治験を開始する前に 個々の被験者及び社会にとって期待される利益と予想される危険及び不便とを比較考量するものとする 期待される利益によって危険を冒すことが正当化される場合に限り
企業主導治験IRB標準業務手順書
 独立行政法人国立病院機構刀根山病院における 治験 受託研究審査委員会標準業務手順書 第 1 章治験 受託研究審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は当院における 受託研究取扱規程 企業主導治験に係る標準業務手順書 及び 受託研究に係る標準業務手順書 に基づいて 治験 受託研究審査委員会の運営に関する手続き及び記録の保存方法を定めるものである 2 製造販売後臨床試験に対しては 医薬品
独立行政法人国立病院機構刀根山病院における 治験 受託研究審査委員会標準業務手順書 第 1 章治験 受託研究審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は当院における 受託研究取扱規程 企業主導治験に係る標準業務手順書 及び 受託研究に係る標準業務手順書 に基づいて 治験 受託研究審査委員会の運営に関する手続き及び記録の保存方法を定めるものである 2 製造販売後臨床試験に対しては 医薬品
参考1
 独立行政法人国立病院機構北海道医療センターにおける 治験審査委員会標準業務手順書 ( 企業主導治験 ) 独立行政法人国立病院機構北海道医療センターにおける 企業主導治験に係る治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は当院における 受託研究取扱規程 及び 企業主導治験に係る標準業務手順書 に基づいて 企業主導治験に係る標準業務手順書第 12 条第
独立行政法人国立病院機構北海道医療センターにおける 治験審査委員会標準業務手順書 ( 企業主導治験 ) 独立行政法人国立病院機構北海道医療センターにおける 企業主導治験に係る治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は当院における 受託研究取扱規程 及び 企業主導治験に係る標準業務手順書 に基づいて 企業主導治験に係る標準業務手順書第 12 条第
目次 第 1 章治験審査委員会... 3 ( 目的と適用範囲 )... 3 ( 治験審査委員会の責務 )... 3 ( 治験審査委員会の設置及び構成 )... 3 ( 治験審査委員会の業務 )... 4 ( 治験審査委員会の運営 )... 6 第 2 章治験審査委員会事務局... 8 ( 治験審査委
 治験審査委員会標準業務手順書 < 医師主導治験 > 横浜労災病院 目次 第 1 章治験審査委員会... 3 ( 目的と適用範囲 )... 3 ( 治験審査委員会の責務 )... 3 ( 治験審査委員会の設置及び構成 )... 3 ( 治験審査委員会の業務 )... 4 ( 治験審査委員会の運営 )... 6 第 2 章治験審査委員会事務局... 8 ( 治験審査委員会事務局の設置と業務 )... 8
治験審査委員会標準業務手順書 < 医師主導治験 > 横浜労災病院 目次 第 1 章治験審査委員会... 3 ( 目的と適用範囲 )... 3 ( 治験審査委員会の責務 )... 3 ( 治験審査委員会の設置及び構成 )... 3 ( 治験審査委員会の業務 )... 4 ( 治験審査委員会の運営 )... 6 第 2 章治験審査委員会事務局... 8 ( 治験審査委員会事務局の設置と業務 )... 8
実施医療機関における治験に係る標準的業務手順書
 国立病院機構大阪医療センター 企業主導治験に係る業務細則 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本規程は 国立病院機構大阪医療センター受託研究取扱細則第 5 条に定める治験又は製造販売後臨床試験 ( 以下 治験等 という ) に関する研究の依頼 申請 契約並びに終了等 治験に関する書式とその取扱いについて定めるものとする 2 本細則は 平成 9 年 3 月 27 日厚生省令第
国立病院機構大阪医療センター 企業主導治験に係る業務細則 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本規程は 国立病院機構大阪医療センター受託研究取扱細則第 5 条に定める治験又は製造販売後臨床試験 ( 以下 治験等 という ) に関する研究の依頼 申請 契約並びに終了等 治験に関する書式とその取扱いについて定めるものとする 2 本細則は 平成 9 年 3 月 27 日厚生省令第
 独立行政法人国立病院機構 名古屋医療センター治験取扱規程 作成日 :2004.04.01 2004.10.01 2005.04.01 2005.07.01 2005.11.01 2006.05.01 2006.08.01 2007.04.02 2008.05.01 2009.03.02 2010.02.01 2012.04.01 2013.07.01 2015.03.13 2015.05.13 2016.12.07
独立行政法人国立病院機構 名古屋医療センター治験取扱規程 作成日 :2004.04.01 2004.10.01 2005.04.01 2005.07.01 2005.11.01 2006.05.01 2006.08.01 2007.04.02 2008.05.01 2009.03.02 2010.02.01 2012.04.01 2013.07.01 2015.03.13 2015.05.13 2016.12.07
医療機関における治験業務
 国立大学法人東京医科歯科大学医学部附属病院 治験等審査委員会標準手順書 東京医科歯科大学医学部附属病院 臨床試験管理センター 制定日 :2015 年 8 月 3 日 改訂日 : 年月日 目次 第 1 章治験等審査委員会 2 第 2 章治験等審査委員会事務局 7 第 3 章記録の保存 8 第 4 章調査 審議の受託 9 第 5 章その他 9-1 - 第 1 章治験等審査委員会 ( 目的と適用範囲 )
国立大学法人東京医科歯科大学医学部附属病院 治験等審査委員会標準手順書 東京医科歯科大学医学部附属病院 臨床試験管理センター 制定日 :2015 年 8 月 3 日 改訂日 : 年月日 目次 第 1 章治験等審査委員会 2 第 2 章治験等審査委員会事務局 7 第 3 章記録の保存 8 第 4 章調査 審議の受託 9 第 5 章その他 9-1 - 第 1 章治験等審査委員会 ( 目的と適用範囲 )
市立札幌病院治験に係わる業務手順書 治験の原則 治験は 次に掲げる原則に則って実施されなければならない 1. 治験は ヘルシンキ宣言に基づく倫理的原則及びGCPを遵守して行われなければならない (GCP: 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 以下薬機法とする ) 平成
 市立札幌病院治験に係わる業務手順書 市立札幌病院治験に係わる業務手順書 治験の原則 治験は 次に掲げる原則に則って実施されなければならない 1. 治験は ヘルシンキ宣言に基づく倫理的原則及びGCPを遵守して行われなければならない (GCP: 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 以下薬機法とする ) 平成 9 年厚生省令第 28 号 (GCP 省令 ) 平成 15 年厚生労働省令第
市立札幌病院治験に係わる業務手順書 市立札幌病院治験に係わる業務手順書 治験の原則 治験は 次に掲げる原則に則って実施されなければならない 1. 治験は ヘルシンキ宣言に基づく倫理的原則及びGCPを遵守して行われなければならない (GCP: 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 以下薬機法とする ) 平成 9 年厚生省令第 28 号 (GCP 省令 ) 平成 15 年厚生労働省令第
日本医科大学付属第二病院治験標準業務手順書
 日本医科大学武蔵小杉病院 薬物治験審査委員会標準業務手順書 日本医科大学武蔵小杉病院 治験管理事務局 設定 :1998.4.1 改訂 :2005.9.1 :2006.4.1 :2010.7.1 :2012.9.1 :2014.1.1 :2015.12.1 :2016.3.1 :2018.10.1-1 - 日本医科大学武蔵小杉病院薬物治験審査委員会標準業務手順書 目次第 1 章薬物治験審査委員会 3
日本医科大学武蔵小杉病院 薬物治験審査委員会標準業務手順書 日本医科大学武蔵小杉病院 治験管理事務局 設定 :1998.4.1 改訂 :2005.9.1 :2006.4.1 :2010.7.1 :2012.9.1 :2014.1.1 :2015.12.1 :2016.3.1 :2018.10.1-1 - 日本医科大学武蔵小杉病院薬物治験審査委員会標準業務手順書 目次第 1 章薬物治験審査委員会 3
静岡県立静岡がんセンター臨床研究事務局の業務手順書
 治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 1 目次 1. 目的と適用範囲...
治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 1 目次 1. 目的と適用範囲...
手順書03
 杏林大学医学部倫理委員会 人を対象とする医学系研究に関する業務手順書 ➂ 研究計画書の作成等に関する手続等 1 はじめに本手順書は 杏林大学医学部倫理委員会規程に基づき 杏林大学医学部及び医学部付属病院の専任教職員が行う人を対象とした医学系研究について 医の倫理に関するヘルシンキ宣言の趣旨に添い 人を対象とする医学系研究に関する倫理指針及び その他関連通知に基づいて適正かつ円滑に行われるよう これらの研究等に係る必要な手順を定めるものである
杏林大学医学部倫理委員会 人を対象とする医学系研究に関する業務手順書 ➂ 研究計画書の作成等に関する手続等 1 はじめに本手順書は 杏林大学医学部倫理委員会規程に基づき 杏林大学医学部及び医学部付属病院の専任教職員が行う人を対象とした医学系研究について 医の倫理に関するヘルシンキ宣言の趣旨に添い 人を対象とする医学系研究に関する倫理指針及び その他関連通知に基づいて適正かつ円滑に行われるよう これらの研究等に係る必要な手順を定めるものである
改正履歴 版番号改訂日改正内容 初版 1991/4/1 NA( 治験薬等臨床試験取扱要綱 ) 第 2.0 版 1994/4/1 第 2.1 版 1997/4/1 細則廃止 第 3.0 版 1998/4/1 第 4.0 版 2000/4/1 名称改正 : 昭和大学病院における臨床試験取扱規程改廃方法変
 臨床研究 ( 治験 / 臨床試験等 ) 標準業務手順書 改訂日 : 2015 年 10 月 1 日 版番号 : 第 12 版 承認日 : 2015 年 9 月 17 日 承認者 : 病院長有賀徹 医療機関名 : 昭和大学病院 1 改正履歴 版番号改訂日改正内容 初版 1991/4/1 NA( 治験薬等臨床試験取扱要綱 ) 第 2.0 版 1994/4/1 第 2.1 版 1997/4/1 細則廃止
臨床研究 ( 治験 / 臨床試験等 ) 標準業務手順書 改訂日 : 2015 年 10 月 1 日 版番号 : 第 12 版 承認日 : 2015 年 9 月 17 日 承認者 : 病院長有賀徹 医療機関名 : 昭和大学病院 1 改正履歴 版番号改訂日改正内容 初版 1991/4/1 NA( 治験薬等臨床試験取扱要綱 ) 第 2.0 版 1994/4/1 第 2.1 版 1997/4/1 細則廃止
<4D F736F F D EA18CB18EE88F878F E C5816A>
 第 Ⅰ 部 札幌医科大学附属病院 治験及び製造販売後臨床試験に係る業務手順書 目次第 1 章総則 1 ( 総則 )... 1 ( 原則 )... 1 第 2 章病院長 2 ( 病院長の責務 )... 2 ( 治験実施の承認等 )... 2 ( 治験実施の契約等 )... 4 ( 治験の継続 )... 5 ( 治験実施計画書の変更 )... 5 ( 治験実施計画書からの逸脱 )... 5 ( 有害事象の発生
第 Ⅰ 部 札幌医科大学附属病院 治験及び製造販売後臨床試験に係る業務手順書 目次第 1 章総則 1 ( 総則 )... 1 ( 原則 )... 1 第 2 章病院長 2 ( 病院長の責務 )... 2 ( 治験実施の承認等 )... 2 ( 治験実施の契約等 )... 4 ( 治験の継続 )... 5 ( 治験実施計画書の変更 )... 5 ( 治験実施計画書からの逸脱 )... 5 ( 有害事象の発生
< F2D CFA90B6984A93AD8FC897DF91E632368D868169>
 厚生労働省令第二十六号薬事法(昭和三十五年法律第百四十五号)第十二条の二第二号並びに第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む )の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令及び医薬品の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十五年三月十一日厚生労働大臣田村憲久医薬品
厚生労働省令第二十六号薬事法(昭和三十五年法律第百四十五号)第十二条の二第二号並びに第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む )の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令及び医薬品の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十五年三月十一日厚生労働大臣田村憲久医薬品
<4D F736F F D A835E838A F8B7982D18AC48DB85F20534F A68CEB8E9A E9A8F4390B38DCF2
 自治医科大学人を対象とした医学系研究に関するモニタリング及び監査の標準業務手順書 ver.1.0(2015 年 5 月 15 日 ) 1. 目的等 1) 目的 (1) 本手順書は 自治医科大学の教職員が 人を対象とする医学系研究に関する倫理指針 ( 平成 26 年文部科学省 厚生労働省告示第 3 号 ) 及び指針告示に伴う通知ならびにガイダンス ( 以下 指針 指針告示に伴う通知及びガイダンスを合わせて
自治医科大学人を対象とした医学系研究に関するモニタリング及び監査の標準業務手順書 ver.1.0(2015 年 5 月 15 日 ) 1. 目的等 1) 目的 (1) 本手順書は 自治医科大学の教職員が 人を対象とする医学系研究に関する倫理指針 ( 平成 26 年文部科学省 厚生労働省告示第 3 号 ) 及び指針告示に伴う通知ならびにガイダンス ( 以下 指針 指針告示に伴う通知及びガイダンスを合わせて
北海道大学病院治験取扱要項
 製造販売後調査 標準業務手順書 北海道大学病院 制定日 : 平成 26 年 2 月 1 日 北海道大学病院製造販売後調査標準業務手順書 平成 26 年 2 月 1 日制定 目 次 第 1 章総則第 1 条 : 趣旨第 2 条 : 目的と適用範囲第 3 条 : 定義 第 2 章病院長の業務第 4 条 : 製造販売後調査実施のための組織の設置第 5 条 : 製造販売後調査の新規申請等第 6 条 : 製造販売後調査実施の了承等第
製造販売後調査 標準業務手順書 北海道大学病院 制定日 : 平成 26 年 2 月 1 日 北海道大学病院製造販売後調査標準業務手順書 平成 26 年 2 月 1 日制定 目 次 第 1 章総則第 1 条 : 趣旨第 2 条 : 目的と適用範囲第 3 条 : 定義 第 2 章病院長の業務第 4 条 : 製造販売後調査実施のための組織の設置第 5 条 : 製造販売後調査の新規申請等第 6 条 : 製造販売後調査実施の了承等第
京都府立医科大学附属病院
 治験費用の取扱に関する手順書 京都府立医科大学附属病院 第 1 版平成 21 年 11 月 16 日 第 2 版平成 23 年 3 月 16 日 第 3 版平成 25 年 2 月 1 日 1. 目的 本手順書は 京都府立医科大学附属病院治験実施取扱規定の定めるところにより 治験 費用の取り扱いに関する運用方法を定め それに基づく業務手順を示すものである 2. 治験に係る経費の範囲 (1) 治験経費
治験費用の取扱に関する手順書 京都府立医科大学附属病院 第 1 版平成 21 年 11 月 16 日 第 2 版平成 23 年 3 月 16 日 第 3 版平成 25 年 2 月 1 日 1. 目的 本手順書は 京都府立医科大学附属病院治験実施取扱規定の定めるところにより 治験 費用の取り扱いに関する運用方法を定め それに基づく業務手順を示すものである 2. 治験に係る経費の範囲 (1) 治験経費
岩手医科大学医学部及び附属病院における人を対象とする医学系研究に係るモニタリング及び監査の実施に関する標準業務手順書 岩手医科大学医学部及び附属病院における 人を対象とする医学系研究に係る モニタリング及び監査の実施に関する標準業務手順書 岩手医科大学 第 1.0 版平成 29 年 10 月 1 日
 岩手医科大学医学部及び附属病院における 人を対象とする医学系研究に係る モニタリング及び監査の実施に関する標準業務手順書 岩手医科大学 第 1.0 版平成 29 年 10 月 1 日施行 目次 1. 目的...1 2. 研究機関の長の責務...1 3. 研究責任者の責務...1 4. モニタリング担当者の責務...1 5. 監査担当者の責務...2 6. 多施設共同研究におけるモニタリング及び監査の実施について...2
岩手医科大学医学部及び附属病院における 人を対象とする医学系研究に係る モニタリング及び監査の実施に関する標準業務手順書 岩手医科大学 第 1.0 版平成 29 年 10 月 1 日施行 目次 1. 目的...1 2. 研究機関の長の責務...1 3. 研究責任者の責務...1 4. モニタリング担当者の責務...1 5. 監査担当者の責務...2 6. 多施設共同研究におけるモニタリング及び監査の実施について...2
第1章 総則
 ( 第 1 章総則 ) 第 1 章総則 1. 治験実施に関する標準業務手順書 (SOP) 制定の目的医療法人防治会いずみの病院 ( 以下 当該医療機関 という ) において ヘルシンキ宣言に基づく倫理的原則及び薬事法第 14 条の第 3 項及び第 80 条の 2 の規定に基づき 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日厚生省令第 28 号 ) 医療機器の臨床試験の実施の基準に関する省令
( 第 1 章総則 ) 第 1 章総則 1. 治験実施に関する標準業務手順書 (SOP) 制定の目的医療法人防治会いずみの病院 ( 以下 当該医療機関 という ) において ヘルシンキ宣言に基づく倫理的原則及び薬事法第 14 条の第 3 項及び第 80 条の 2 の規定に基づき 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日厚生省令第 28 号 ) 医療機器の臨床試験の実施の基準に関する省令
第 4 章治験責任医師の業務 目次 1. 目的と適用範囲 1 2. 治験責任医師の要件 1 3. 治験実施計画書の遵守に関する合意 1 4. 同意説明文書の作成 1 5. 治験分担医師及び治験協力者のリストの作成 2 6. 治験の実施依頼 ( 新規 変更 継続 ) 3 7. 治験の実施等の了承 3
 第 4 章 治験責任医師の業務 第 4 章治験責任医師の業務 目次 1. 目的と適用範囲 1 2. 治験責任医師の要件 1 3. 治験実施計画書の遵守に関する合意 1 4. 同意説明文書の作成 1 5. 治験分担医師及び治験協力者のリストの作成 2 6. 治験の実施依頼 ( 新規 変更 継続 ) 3 7. 治験の実施等の了承 3 8. 治験の契約 3 9. 被験者の選定 3 10. 被験者の同意の取得
第 4 章 治験責任医師の業務 第 4 章治験責任医師の業務 目次 1. 目的と適用範囲 1 2. 治験責任医師の要件 1 3. 治験実施計画書の遵守に関する合意 1 4. 同意説明文書の作成 1 5. 治験分担医師及び治験協力者のリストの作成 2 6. 治験の実施依頼 ( 新規 変更 継続 ) 3 7. 治験の実施等の了承 3 8. 治験の契約 3 9. 被験者の選定 3 10. 被験者の同意の取得
医療機関における治験業務
 国立大学法人東京医科歯科大学医学部附属病院 企業治験業務標準手順書 東京医科歯科大学医学部附属病院 臨床試験管理センター 制定日 :1998 年 3 月 27 日改訂日 :1998 年 7 月 21 日 改訂日 :1998 年 10 月 21 日改訂日 :1999 年 8 月 4 日 改訂日 :2001 年 6 月 6 日改訂日 :2003 年 6 月 19 日 改訂日 :2004 年 4 月 1
国立大学法人東京医科歯科大学医学部附属病院 企業治験業務標準手順書 東京医科歯科大学医学部附属病院 臨床試験管理センター 制定日 :1998 年 3 月 27 日改訂日 :1998 年 7 月 21 日 改訂日 :1998 年 10 月 21 日改訂日 :1999 年 8 月 4 日 改訂日 :2001 年 6 月 6 日改訂日 :2003 年 6 月 19 日 改訂日 :2004 年 4 月 1
する 研究実施施設の環境 ( プライバシーの保護状態 ) について記載する < 実施方法 > どのような手順で研究を実施するのかを具体的に記載する アンケート等を用いる場合は 事前にそれらに要する時間を測定し 調査による患者への負担の度合いがわかるように記載する 調査手順で担当が複数名いる場合には
 参考 : 様式 2( 記載例 ) ( 研究責任者 ) ( 本会倫理審査委員会 ) 西暦年月日 研究計画書 ( 第版 ) 公益社団法人富山県薬剤師会倫理審査委員会委員長様 計画者 ( 研究責任者 ) 所属 : 職名 : 氏名 : 印 1. 研究の名称 : 2. 研究の実施体制 研究責任者名所属職名役割及び責任 薬局管理薬剤師 研究分担者名 所属 職名 役割及び責任 薬局 薬剤師 病院 科 病院薬剤部
参考 : 様式 2( 記載例 ) ( 研究責任者 ) ( 本会倫理審査委員会 ) 西暦年月日 研究計画書 ( 第版 ) 公益社団法人富山県薬剤師会倫理審査委員会委員長様 計画者 ( 研究責任者 ) 所属 : 職名 : 氏名 : 印 1. 研究の名称 : 2. 研究の実施体制 研究責任者名所属職名役割及び責任 薬局管理薬剤師 研究分担者名 所属 職名 役割及び責任 薬局 薬剤師 病院 科 病院薬剤部
前項に規定する事項のうち当該被験薬の治験薬概要書から予測できないもの に改め 同項を同条第三項とし 同条第一項の次に次の一項を加える 2治験依頼者は 被験薬について法第八十条の二第六項に規定する事項を知ったときは その発現症例一覧等を当該被験薬ごとに 当該被験薬について初めて治験の計画を届け出た日等
 厚生労働省令第二十四号薬事法(昭和三十五年法律第百四十五号)第十四条第三項(同条第九項及び同法第十九条の二第五項において準用する場合を含む ) 第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む ) 第八十条の二第一項 第四項及び第五項並びに第八十二条の規定に基づき 医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十年二月二十九日厚生労働大臣舛添要一医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令医薬品の臨床試験の実施の基準に関する省令(平成九年厚生省令第二十八号)の一部を次のように改正する
厚生労働省令第二十四号薬事法(昭和三十五年法律第百四十五号)第十四条第三項(同条第九項及び同法第十九条の二第五項において準用する場合を含む ) 第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む ) 第八十条の二第一項 第四項及び第五項並びに第八十二条の規定に基づき 医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十年二月二十九日厚生労働大臣舛添要一医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令医薬品の臨床試験の実施の基準に関する省令(平成九年厚生省令第二十八号)の一部を次のように改正する
1. 人を対象とする医学系研究の実施に係る手順書 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本規程は ヘルシンキ宣言の倫理的原則に則り 人を対象とする医学系研究に関する倫理指針 ( 平成 26 年文部科学省 厚生労働省告示第 3 号 ; 以下 倫理指針 という ) 及び関連する最新
 人を対象とする医学系研究に係る 標準業務手順書 2016 年 6 月 23 日 第 1 版 2016 年 7 月 28 日 第 2 版 2017 年 1 月 26 日 第 3 版 大垣市民病院 臨床研究審査委員会 1. 人を対象とする医学系研究の実施に係る手順書 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本規程は ヘルシンキ宣言の倫理的原則に則り 人を対象とする医学系研究に関する倫理指針
人を対象とする医学系研究に係る 標準業務手順書 2016 年 6 月 23 日 第 1 版 2016 年 7 月 28 日 第 2 版 2017 年 1 月 26 日 第 3 版 大垣市民病院 臨床研究審査委員会 1. 人を対象とする医学系研究の実施に係る手順書 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本規程は ヘルシンキ宣言の倫理的原則に則り 人を対象とする医学系研究に関する倫理指針
Microsoft Word - (発番)医療機器の製造販売承認申請について
 薬食発 1120 第 5 号 平成 26 年 11 月 20 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医療機器の製造販売承認申請について 医療機器の製造販売承認申請の取扱いについては 医療機器の製造販売承認申請について ( 平成 17 年 2 月 16 日付け薬食発第 0216002 号厚生労働省医薬食品局長通知 以下 旧通知 という ) 等により実施してきたところです 先般
薬食発 1120 第 5 号 平成 26 年 11 月 20 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医療機器の製造販売承認申請について 医療機器の製造販売承認申請の取扱いについては 医療機器の製造販売承認申請について ( 平成 17 年 2 月 16 日付け薬食発第 0216002 号厚生労働省医薬食品局長通知 以下 旧通知 という ) 等により実施してきたところです 先般
医師主導治験取扱要覧
 9. 安全性情報の取扱いに関する手順書 1. 目的及び適用範囲 本手順書は 安全性情報の取扱いに係る用語の定義を定め 当該治験に関与する者が 安全性情報を適 切に取扱うための手順その他必要な事項を定めるものである 2. 用語の定義等 2.1. 用語の定義 2.1.1. 治験責任医師等 本手順書は 自ら治験を実施する者を 治験責任医師 と記載し また 治験責任医師及び治験分担医師 を併せて 治験責任医師等
9. 安全性情報の取扱いに関する手順書 1. 目的及び適用範囲 本手順書は 安全性情報の取扱いに係る用語の定義を定め 当該治験に関与する者が 安全性情報を適 切に取扱うための手順その他必要な事項を定めるものである 2. 用語の定義等 2.1. 用語の定義 2.1.1. 治験責任医師等 本手順書は 自ら治験を実施する者を 治験責任医師 と記載し また 治験責任医師及び治験分担医師 を併せて 治験責任医師等
本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シ
 医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
( 委員以外の者の出席 ) 第 5 条委員長は 必要に応じ当該研究に必要な知見及び専門知識を持つ教員 産業医または看護師等を委員会の同意を得て出席させ 意見を聴くことができる ただし 上記の者の出席が困難な場合は 委員長又は委員長が指名した者が口頭等で意見を聴取し 委員会で報告することができる (
 一関工業高等専門学校における人を対象とする研究倫理審査委員会規則 ( 平成 28 年 6 月 9 日制定 ) ( 設置 ) 第 1 条一関工業高等専門学校 ( 以下 本校 という ) に, 人を対象とする研究における研究倫理について審査するため, 人を対象とする研究倫理審査委員会 ( 以下 委員会 という ) を置く ( 目的 ) 第 2 条委員会は, 本校における人を対象とする研究が, 独立行政法人国立高等専門学校機構における研究者等の行動規範
一関工業高等専門学校における人を対象とする研究倫理審査委員会規則 ( 平成 28 年 6 月 9 日制定 ) ( 設置 ) 第 1 条一関工業高等専門学校 ( 以下 本校 という ) に, 人を対象とする研究における研究倫理について審査するため, 人を対象とする研究倫理審査委員会 ( 以下 委員会 という ) を置く ( 目的 ) 第 2 条委員会は, 本校における人を対象とする研究が, 独立行政法人国立高等専門学校機構における研究者等の行動規範
Microsoft Word - 【案1】登録認証機関立入要領改正通知(Ver )
 薬食機参発 1121 第 38 号平成 26 年 11 月 21 日 各登録認証機関の長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) 登録認証機関等に対する立入検査の実施要領の改正について 薬事法 ( 昭和 35 年法律第 145 号 ) の規定による登録認証機関等に対する立入 検査の実施要領については 登録認証機関等に対する立入検査の実施要領について ( 平成 18
薬食機参発 1121 第 38 号平成 26 年 11 月 21 日 各登録認証機関の長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) 登録認証機関等に対する立入検査の実施要領の改正について 薬事法 ( 昭和 35 年法律第 145 号 ) の規定による登録認証機関等に対する立入 検査の実施要領については 登録認証機関等に対する立入検査の実施要領について ( 平成 18
【押印あり】日本医学会宛
 別紙 再生医療等製品患者登録システムへの参加協力のお願い 患者登録システムの目的 患者登録システムは 再生医療等製品の市販後の使用状況や患者予後等のデータを収集し 迅速な安全対策や新たな製品開発等を通じて 医療の向上に役立てることを目的としています 患者登録システムは 製品毎に構築 運用されます この患者登録システムは 一般的には レジストリ と呼ばれることもあります 構築形態例 患者登録システムの対象
別紙 再生医療等製品患者登録システムへの参加協力のお願い 患者登録システムの目的 患者登録システムは 再生医療等製品の市販後の使用状況や患者予後等のデータを収集し 迅速な安全対策や新たな製品開発等を通じて 医療の向上に役立てることを目的としています 患者登録システムは 製品毎に構築 運用されます この患者登録システムは 一般的には レジストリ と呼ばれることもあります 構築形態例 患者登録システムの対象
Microsoft PowerPoint - 運用 [互換モード]
![Microsoft PowerPoint - 運用 [互換モード] Microsoft PowerPoint - 運用 [互換モード]](/thumbs/91/105850431.jpg) 押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
臨床試験(治験)実施の手続き
 製造販売後調査実施の手続き はじめに 本書は 昭和大学藤が丘病院における製造販売後調査実施の手続き方法等について記載したものです 本書内のは当院が提供する書類を示し は審査等に必要な書類を示しております 調査内容により提出書類 資料に変更が生じる場合があります 詳細は支援室にご確認ください 申請する書類および資料は 事前に E-mail に添付して支援室にお送りください 内容の確認をし ご連絡させて頂きます
製造販売後調査実施の手続き はじめに 本書は 昭和大学藤が丘病院における製造販売後調査実施の手続き方法等について記載したものです 本書内のは当院が提供する書類を示し は審査等に必要な書類を示しております 調査内容により提出書類 資料に変更が生じる場合があります 詳細は支援室にご確認ください 申請する書類および資料は 事前に E-mail に添付して支援室にお送りください 内容の確認をし ご連絡させて頂きます
(3) 倫理学 法律学の専門家等 本法人に所属しない人文 社会科学の有識者若干名 (4) 一般の立場から意見を述べることができる者若干名 (5) 分子生物学 細胞生物学 遺伝学 臨床薬理学 病理学等の専門家若しくは遺伝子治療等臨床研究の対象となる疾患に係る臨床医として 日本医科大学長が推薦した者若干
 学校法人日本医科大学中央倫理委員会規程 ( 平成 28 年 1 月 1 日規程第 3 号 ) ( 目的 ) 第 1 条この規程は 医の倫理に関するヘルシンキ宣言の趣旨を尊重し 人を対象とする医学系研究に関する倫理指針 ヒトゲノム 遺伝子解析研究に関する倫理指針 遺伝子治療臨床研究に関する指針 ヒト受精胚の作成を行う生殖補助医療研究に関する倫理指針 等 国等が示した関係法令及び関係指針 ( 以下すべて併せて
学校法人日本医科大学中央倫理委員会規程 ( 平成 28 年 1 月 1 日規程第 3 号 ) ( 目的 ) 第 1 条この規程は 医の倫理に関するヘルシンキ宣言の趣旨を尊重し 人を対象とする医学系研究に関する倫理指針 ヒトゲノム 遺伝子解析研究に関する倫理指針 遺伝子治療臨床研究に関する指針 ヒト受精胚の作成を行う生殖補助医療研究に関する倫理指針 等 国等が示した関係法令及び関係指針 ( 以下すべて併せて
2) 治験薬概要書 (GCP 省令第 15 条の5 第 2 項の規定により改訂されたものを含む ) 3) 症例報告書の見本 ( 治験実施計画書において 症例報告書に記載すべき事項が十分に読み取れる場合は 当該治験実施計画書をもって症例報告書の見本に関する事項を含む ) 4) 説明文書 同意文書 (
 秋田大学医学部附属病院医師主導治験取扱規程 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本規程は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 医薬品の臨床試験の実施の基準に関する省令( 平成 9 年 3 月 27 日厚生省令第 28 号 )( 以下 GCP 省令 という ) 並びにGCP 省令に関連する通知書等に基づいて
秋田大学医学部附属病院医師主導治験取扱規程 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本規程は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 医薬品の臨床試験の実施の基準に関する省令( 平成 9 年 3 月 27 日厚生省令第 28 号 )( 以下 GCP 省令 という ) 並びにGCP 省令に関連する通知書等に基づいて
じ ) その他の処方せん医薬品又は高度管理医療機器の製造販売に係る業務の責任者との密接な連携を図らせること ( 安全確保業務に係る組織及び職員 ) 第四条第一種製造販売業者は 次に掲げる要件を満たす安全確保業務の統括に係る部門 ( 以下この章において 安全管理統括部門 という ) を置かなければなら
 厚生労働省令第百三十五号薬事法 ( 昭和三十五年法律第百四十五号 ) 第十二条の二第二号の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令を次のように定める 平成十六年九月二十二日厚生労働大臣坂口力 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令目次第一章総則 ( 第一条第二条 ) 第一種製造販売業者の製造販売後安全管理の基準
厚生労働省令第百三十五号薬事法 ( 昭和三十五年法律第百四十五号 ) 第十二条の二第二号の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令を次のように定める 平成十六年九月二十二日厚生労働大臣坂口力 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令目次第一章総則 ( 第一条第二条 ) 第一種製造販売業者の製造販売後安全管理の基準
臨床試験(治験)の手続きについて
 臨床試験 ( 治験 製造販売後臨床試験 ) の手続きについて 本書は 昭和大学横浜市北部病院における臨床試験 ( 治験 製造販売後臨床試験 ) の手続き等に関して記したものです 始める前にご一読下さい なお 下記手続きにおいて必要書類を提出される場合は臨床試験支援室 ( 連絡先 :10 ページ参照 ) までご連絡下さい - 試験依頼前 - 関係書類の入手 当院の臨床試験 ( 治験 製造販売後臨床試験
臨床試験 ( 治験 製造販売後臨床試験 ) の手続きについて 本書は 昭和大学横浜市北部病院における臨床試験 ( 治験 製造販売後臨床試験 ) の手続き等に関して記したものです 始める前にご一読下さい なお 下記手続きにおいて必要書類を提出される場合は臨床試験支援室 ( 連絡先 :10 ページ参照 ) までご連絡下さい - 試験依頼前 - 関係書類の入手 当院の臨床試験 ( 治験 製造販売後臨床試験
JCROA自主ガイドライン第4版案 GCP監査WG改訂案及び意見
 受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
<4D F736F F F696E74202D2090BB91A294CC94848CE392B28DB CC905C90BF82C982C282A282C45F F566F6C2E33>
 この冊 における製造販売後調査等とは 使 成績調査 特定使 成績調査 副作 感染症報告 です 1/Mar/2016 Vol.3 1 ホームページのご案内 1 当院ホームページに手続き内容や 必要書類等を UP しています 2 依頼者のページ 3 製造販売後調査について 1 治験のお知らせ 2 ホームページのご案内 2 当院ホームページに手続き内容や 必要書類等を UP しています 申請の内容に応じて
この冊 における製造販売後調査等とは 使 成績調査 特定使 成績調査 副作 感染症報告 です 1/Mar/2016 Vol.3 1 ホームページのご案内 1 当院ホームページに手続き内容や 必要書類等を UP しています 2 依頼者のページ 3 製造販売後調査について 1 治験のお知らせ 2 ホームページのご案内 2 当院ホームページに手続き内容や 必要書類等を UP しています 申請の内容に応じて
4 委員の任期は 2 年とする たた し 委員に欠員が生じた場合の後任の委員の任 期は 前任者の残任期間とする 5 委員は 再任を妨げない ( 委員長及び副委員長 ) 第 5 条委員会に委員長を置き 委員のうちから互選する 2 委員長は 委員会を招集し その議長となる 3 委員会に副委員長を置き 委
 日本美容外科学会 (JSAPS) 認定再生医療等委員会業務規程 第 1 章認定再生医療等委員会 ( 設置 ) 第 1 条日本美容外科学会 (JSAPS)( 以下 本学会 という ) に 再生医療等の 安全性の確保等に関する法律 ( 平成 25 年法律第 85 号 以下 法 という ) に定 める第三種再生医療等提供計画のみに係る審査等業務を行う委員会として 日本美容 外科学会 (JSAPS) 認定再生医療等委員会
日本美容外科学会 (JSAPS) 認定再生医療等委員会業務規程 第 1 章認定再生医療等委員会 ( 設置 ) 第 1 条日本美容外科学会 (JSAPS)( 以下 本学会 という ) に 再生医療等の 安全性の確保等に関する法律 ( 平成 25 年法律第 85 号 以下 法 という ) に定 める第三種再生医療等提供計画のみに係る審査等業務を行う委員会として 日本美容 外科学会 (JSAPS) 認定再生医療等委員会
IRB の 4 週間前までに事前確認に必要な資料をご提出ください 必要時にはヒアリングも実施いたします IRB 審議用確認資料 電子 ( メール ) にてご提出ください 製造販売後調査申請書 ( 様式 1) 1 部 審査用資料 1 薬品概要書 ( 添付文書でも可 ) 1 部 2 調査実施計画書 (
 国立大学法人信州大学医学部附属病院製造販売後調査実施に係わる手続き要領 2018 年 4 月 はじめにご確認ください 本要領の対象となる調査は 再審査 再評価のために GPSP で規定された日常診療下で実施される調査です 製薬会社が独自で行う調査 (= 観察研究 ) は対象外です 独自に実施する調査は 臨床研究として信州大学医学部医倫理委員会で審議となります 各種手続きについて担当医師又は信州大学医学部庶務係
国立大学法人信州大学医学部附属病院製造販売後調査実施に係わる手続き要領 2018 年 4 月 はじめにご確認ください 本要領の対象となる調査は 再審査 再評価のために GPSP で規定された日常診療下で実施される調査です 製薬会社が独自で行う調査 (= 観察研究 ) は対象外です 独自に実施する調査は 臨床研究として信州大学医学部医倫理委員会で審議となります 各種手続きについて担当医師又は信州大学医学部庶務係
目次 1. 目的と適用範囲 定義 原則 使用機器 審査資料交付システム タブレット端末 管理運用体制 電磁的記録管理運用責任者の役割 電磁的記録管理運用担当者の役割
 特定非営利活動法人臨床研究の倫理を考える会 治験審査委員会 倫理審査委員会における電磁的記録の 活用に係る標準業務手順書 版数 : 初版承認日 : 2014 年 4 月 18 日承認者 : 理事長橋爪敬三 この手順書は 2014 年 4 月 21 日から施行する 目次 1. 目的と適用範囲... 1 2. 定義... 1 3. 原則... 1 4. 使用機器... 2 4.1 審査資料交付システム...
特定非営利活動法人臨床研究の倫理を考える会 治験審査委員会 倫理審査委員会における電磁的記録の 活用に係る標準業務手順書 版数 : 初版承認日 : 2014 年 4 月 18 日承認者 : 理事長橋爪敬三 この手順書は 2014 年 4 月 21 日から施行する 目次 1. 目的と適用範囲... 1 2. 定義... 1 3. 原則... 1 4. 使用機器... 2 4.1 審査資料交付システム...
医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年
![医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年 医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年](/thumbs/91/107149459.jpg) 事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
雇用管理分野における個人情報のうち健康情報を取り扱うに当たっての留意事項 第 1 趣旨 この留意事項は 雇用管理分野における労働安全衛生法 ( 昭和 47 年法律第 57 号 以下 安衛法 という ) 等に基づき実施した健康診断の結果等の健康情報の取扱いについて 個人情報の保護に関する法律についての
 雇用管理分野における個人情報のうち健康情報を取り扱うに当たっての留意事項 第 1 趣旨 この留意事項は 雇用管理分野における労働安全衛生法 ( 昭和 47 年法律第 57 号 以下 安衛法 という ) 等に基づき実施した健康診断の結果等の健康情報の取扱いについて 個人情報の保護に関する法律についてのガイドライン ( 通則編 )( 平成 28 年 11 月個人情報保護委員会 以下 ガイドライン という
雇用管理分野における個人情報のうち健康情報を取り扱うに当たっての留意事項 第 1 趣旨 この留意事項は 雇用管理分野における労働安全衛生法 ( 昭和 47 年法律第 57 号 以下 安衛法 という ) 等に基づき実施した健康診断の結果等の健康情報の取扱いについて 個人情報の保護に関する法律についてのガイドライン ( 通則編 )( 平成 28 年 11 月個人情報保護委員会 以下 ガイドライン という
4
 4. 研究責任者標準業務手順書 制定年月日 :2017 年 4 月 1 日 4. 研究責任者標準業務手順書目次 第 1 章研究責任者の定義と責務 1 第 1 条研究責任者の定義 1 第 2 条研究責任者の責務 1 第 2 章研究責任者の要件 1 第 3 条研究責任者の要件 1 第 3 章研究責任者の業務 2 第 4 条研究責任者の業務 2 第 5 条委託を受けて実施する研究の実施の合意 4 第 6
4. 研究責任者標準業務手順書 制定年月日 :2017 年 4 月 1 日 4. 研究責任者標準業務手順書目次 第 1 章研究責任者の定義と責務 1 第 1 条研究責任者の定義 1 第 2 条研究責任者の責務 1 第 2 章研究責任者の要件 1 第 3 条研究責任者の要件 1 第 3 章研究責任者の業務 2 第 4 条研究責任者の業務 2 第 5 条委託を受けて実施する研究の実施の合意 4 第 6
Microsoft Word - 奈良県GQP-GVPガイドライン doc
 三. 安全確保措置の実施に関する手順 1. 目的安全確保措置の実施に関する手順の目的を記載する < 記載例 > 本手順は GVP 省令の第 9 条に基づき 安全確保措置の実施を適正かつ円滑に行うために必要な手順を定めるものである 2. 適用範囲安全確保措置の実施に関する手順の適用範囲を記載する < 記載例 > 本手順書は 二. 安全管理情報の検討及びその結果に基づく安全確保措置の立案に関する手順 で立案された安全確保措置の決定
三. 安全確保措置の実施に関する手順 1. 目的安全確保措置の実施に関する手順の目的を記載する < 記載例 > 本手順は GVP 省令の第 9 条に基づき 安全確保措置の実施を適正かつ円滑に行うために必要な手順を定めるものである 2. 適用範囲安全確保措置の実施に関する手順の適用範囲を記載する < 記載例 > 本手順書は 二. 安全管理情報の検討及びその結果に基づく安全確保措置の立案に関する手順 で立案された安全確保措置の決定
松本市補助金交付規則 昭和 37 年 7 月 27 日規則第 16 号改正昭和 45 年 9 月 12 日規則第 31 号昭和 53 年 12 月 8 日規則第 25 号昭和 63 年 4 月 1 日規則第 18 号 ( 目的 ) 第 1 条この規則は 法令又は条例等に特別の定めのあるもののほか 補
 松本市補助金交付規則 昭和 37 年 7 月 27 日規則第 16 号改正昭和 45 年 9 月 12 日規則第 31 号昭和 53 年 12 月 8 日規則第 25 号昭和 63 年 4 月 1 日規則第 18 号 ( 目的 ) 第 1 条この規則は 法令又は条例等に特別の定めのあるもののほか 補助金等の交付に関し 必要な事項を定めることを目的とする ( 用語の定義 ) 第 2 条この規則において
松本市補助金交付規則 昭和 37 年 7 月 27 日規則第 16 号改正昭和 45 年 9 月 12 日規則第 31 号昭和 53 年 12 月 8 日規則第 25 号昭和 63 年 4 月 1 日規則第 18 号 ( 目的 ) 第 1 条この規則は 法令又は条例等に特別の定めのあるもののほか 補助金等の交付に関し 必要な事項を定めることを目的とする ( 用語の定義 ) 第 2 条この規則において
本手順書で使用する用語の定義 用語電子的記録書面電子的記録利用システム実務担当者原データ治験関連文書サイボウズサイボウズメッセージ 定義人の知覚では認識できない, 電子式等の方法で記録され, コンピュータで処理される記録紙媒体による資料治験依頼者, 実施医療機関の長, 治験責任医師並びに治験審査委員
 ( 第 1 版 :2015 年 7 月 1 日 ) 本手順書で使用する用語の定義 用語電子的記録書面電子的記録利用システム実務担当者原データ治験関連文書サイボウズサイボウズメッセージ 定義人の知覚では認識できない, 電子式等の方法で記録され, コンピュータで処理される記録紙媒体による資料治験依頼者, 実施医療機関の長, 治験責任医師並びに治験審査委員会の間での電子的記録の作成, 交付, 受領及び保存に用いるシステム規定や文書等で責任者の行うべき業務の権限を与えられ,
( 第 1 版 :2015 年 7 月 1 日 ) 本手順書で使用する用語の定義 用語電子的記録書面電子的記録利用システム実務担当者原データ治験関連文書サイボウズサイボウズメッセージ 定義人の知覚では認識できない, 電子式等の方法で記録され, コンピュータで処理される記録紙媒体による資料治験依頼者, 実施医療機関の長, 治験責任医師並びに治験審査委員会の間での電子的記録の作成, 交付, 受領及び保存に用いるシステム規定や文書等で責任者の行うべき業務の権限を与えられ,
る として 平成 20 年 12 月に公表された 規制改革推進のための第 3 次答申 において 医療機器開発の円滑化の観点から 薬事法の適用範囲の明確化を図るためのガイドラインを作成すべきであると提言したところである 今般 薬事法の適用に関する判断の透明性 予見可能性の向上を図るため 臨床研究におい
 都道府県知事 各保健所設置市長殿 特別区長 薬食発 0331 第 7 号 平成 22 年 3 月 31 日 厚生労働省医薬食品局長 臨床研究において用いられる未承認医療機器の提供等に係る 薬事法の適用について 薬事法 ( 昭和 35 年法律第 145 号 ) は 医療機器について品質 有効性及び安全性の確保がなされた製品のみが流通するよう種々の規制を設けているが 薬事法第 14 条第 1 項の承認を受けていない医療機器
都道府県知事 各保健所設置市長殿 特別区長 薬食発 0331 第 7 号 平成 22 年 3 月 31 日 厚生労働省医薬食品局長 臨床研究において用いられる未承認医療機器の提供等に係る 薬事法の適用について 薬事法 ( 昭和 35 年法律第 145 号 ) は 医療機器について品質 有効性及び安全性の確保がなされた製品のみが流通するよう種々の規制を設けているが 薬事法第 14 条第 1 項の承認を受けていない医療機器
本手順書の構成 第 1 章総則... 1 ( 治験の原則 )... 1 ( 目的と適用範囲 )... 2 第 2 章病院長の業務... 2 ( 組織の設置及び運営 )... 2 ( 治験依頼の申請等 )... 2 ( 治験実施の了承等 )... 4 ( 治験実施の契約等 )... 5 ( 契約内容の
 学校法人藤田学園 藤田医科大学病院 治験標準業務手順書 2.0 版作成日 2018 年 10 月 10 日 i 本手順書の構成 第 1 章総則... 1 ( 治験の原則 )... 1 ( 目的と適用範囲 )... 2 第 2 章病院長の業務... 2 ( 組織の設置及び運営 )... 2 ( 治験依頼の申請等 )... 2 ( 治験実施の了承等 )... 4 ( 治験実施の契約等 )... 5 (
学校法人藤田学園 藤田医科大学病院 治験標準業務手順書 2.0 版作成日 2018 年 10 月 10 日 i 本手順書の構成 第 1 章総則... 1 ( 治験の原則 )... 1 ( 目的と適用範囲 )... 2 第 2 章病院長の業務... 2 ( 組織の設置及び運営 )... 2 ( 治験依頼の申請等 )... 2 ( 治験実施の了承等 )... 4 ( 治験実施の契約等 )... 5 (
治験は、医薬品として未だ認められていない物質を人(被験者)に投与して、有効性、安全性等を検討する臨床試験のことであり、新薬の承認申請資料の作成を目的としています
 このページでは 名古屋大学医学部附属病院において治験を実施する場合の手順を紹介しています ご不明な点がありましたら 臨床治験管理センターまでお問い合わせ下さい 治験責任医師の基本的な責務 治験責任医師は 治験に関連する医療上のすべての判断に責任を負う (GCP 第 45 条第 3 4 項 ) 治験責任医師は 治験依頼者と合意した治験実施計画書を遵守する (GCP 第 46 条第 1 項 ) 治験責任医師は
このページでは 名古屋大学医学部附属病院において治験を実施する場合の手順を紹介しています ご不明な点がありましたら 臨床治験管理センターまでお問い合わせ下さい 治験責任医師の基本的な責務 治験責任医師は 治験に関連する医療上のすべての判断に責任を負う (GCP 第 45 条第 3 4 項 ) 治験責任医師は 治験依頼者と合意した治験実施計画書を遵守する (GCP 第 46 条第 1 項 ) 治験責任医師は
目次 医薬品等臨床試験標準業務手順書治験審査委員会 (IRB) 標準業務手順書企業治験 製造販売後臨床試験標準業務手順書医師主導治験標準業務手順書製造販売後調査標準業務手順書治験事務局 CRC 標準業務手順書治験薬 治験機器 治験製品管理標準業務手順書モニタリング 監査標準業務手順書費用 契約標準業
 目次 医薬品等臨床試験標準業務手順書治験審査委員会 (IRB) 標準業務手順書企業治験 製造販売後臨床試験標準業務手順書医師主導治験標準業務手順書製造販売後調査標準業務手順書治験事務局 CRC 標準業務手順書治験薬 治験機器 治験製品管理標準業務手順書モニタリング 監査標準業務手順書費用 契約標準業務手順書個人情報取扱標準業務手順書治験関連文書電子化標準業務手順書 書式一覧 ( 企業治験 製造販売後臨床試験
目次 医薬品等臨床試験標準業務手順書治験審査委員会 (IRB) 標準業務手順書企業治験 製造販売後臨床試験標準業務手順書医師主導治験標準業務手順書製造販売後調査標準業務手順書治験事務局 CRC 標準業務手順書治験薬 治験機器 治験製品管理標準業務手順書モニタリング 監査標準業務手順書費用 契約標準業務手順書個人情報取扱標準業務手順書治験関連文書電子化標準業務手順書 書式一覧 ( 企業治験 製造販売後臨床試験
SOP(IRB有)1203版
 医療法人仁楡会 仁楡会病院 標準業務手順書 第 7 版 :( 西暦 )2014 年 8 月 14 日改訂 院長松村欣也 印 第 1 章 総則 1. 目的と適用範囲本標準業務手順書 ( 以下 本手順書 という ) は 当院において 医薬品の臨床試験の実施の基準に関する省令 ( 厚生省令第 28 号 平成 9 年 3 月 27 日 GCP 省令 ) 医療機器の臨床試験の実施の基準に関する省令 ( 厚生労働省令第
医療法人仁楡会 仁楡会病院 標準業務手順書 第 7 版 :( 西暦 )2014 年 8 月 14 日改訂 院長松村欣也 印 第 1 章 総則 1. 目的と適用範囲本標準業務手順書 ( 以下 本手順書 という ) は 当院において 医薬品の臨床試験の実施の基準に関する省令 ( 厚生省令第 28 号 平成 9 年 3 月 27 日 GCP 省令 ) 医療機器の臨床試験の実施の基準に関する省令 ( 厚生労働省令第
一
 医師主導治験の取り扱いに関する標準業務手順書 公立大学法人大阪市立大学 医学部附属病院 12 版 :2018 年 4 月 1 日 OCUMC-102 医師主導治験の取り扱いに関する標準業務手順書 12 版 OCUMC-102 医師主導治験の取り扱いに関する標準業務手順書 12 版 目次 治験の原則... 1 第 1 章目的と適用範囲... 2 ( 目的と適用範囲 )... 2 第 2 章組織...
医師主導治験の取り扱いに関する標準業務手順書 公立大学法人大阪市立大学 医学部附属病院 12 版 :2018 年 4 月 1 日 OCUMC-102 医師主導治験の取り扱いに関する標準業務手順書 12 版 OCUMC-102 医師主導治験の取り扱いに関する標準業務手順書 12 版 目次 治験の原則... 1 第 1 章目的と適用範囲... 2 ( 目的と適用範囲 )... 2 第 2 章組織...
特定臨床研究に関する手順書
 学校法人日本医科大学における特定臨床研究に関する手順書 ( 新規申請分 ) 1. 目的 本手順書は 学校法人日本医科大学における特定臨床研究に関する規程 ( 以下 規程 という ) を円滑に運用するために 本法人における手順を示すものである 2. 用語の定義 2.1 全般本手順書において使用する用語は 規程において使用する用語の例によるものとする 2.2 付属所属長規程第 5 条第 2 項により 理事長は実施医療機関の管理者の権限を次に定める付属所属長に委任しているため
学校法人日本医科大学における特定臨床研究に関する手順書 ( 新規申請分 ) 1. 目的 本手順書は 学校法人日本医科大学における特定臨床研究に関する規程 ( 以下 規程 という ) を円滑に運用するために 本法人における手順を示すものである 2. 用語の定義 2.1 全般本手順書において使用する用語は 規程において使用する用語の例によるものとする 2.2 付属所属長規程第 5 条第 2 項により 理事長は実施医療機関の管理者の権限を次に定める付属所属長に委任しているため
医療機関のの指示 決定に 医療機関のが 治験審査委員会の決定 関する文書 に基づく医療機関のの指示 決定を ( 治験に関する指 治験依頼者及びに通知す 示決定通知書 ) ( 治験審査委員会の通知文 る文書 書写しを含む ) 治験審査委員会の日付入り通知文書の 写し の業務内容に関 医療機関のがの業務
 必須文書保管管理 治験開始前 治験審査委員会の設置記録 医療機関のが 治験審査委員会 ( 同事 治験取扱要綱 務局を含む ) を設置したことを示す ( 第 5 条 ) 治験審査委員会委員の指名 治験審査委員会の設置者が治験審査委 治験審査委員会委 記録 員会の委員を指名した文書 員指名記録 治験審査委員会の運営に関 治験審査委員会の運営の手続き 及び記 治験審査委員会内 する文書 録の保存に関する事項を定めた文書
必須文書保管管理 治験開始前 治験審査委員会の設置記録 医療機関のが 治験審査委員会 ( 同事 治験取扱要綱 務局を含む ) を設置したことを示す ( 第 5 条 ) 治験審査委員会委員の指名 治験審査委員会の設置者が治験審査委 治験審査委員会委 記録 員会の委員を指名した文書 員指名記録 治験審査委員会の運営に関 治験審査委員会の運営の手続き 及び記 治験審査委員会内 する文書 録の保存に関する事項を定めた文書
製造販売後調査事務手続き等 について
 製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
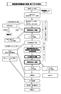
製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
GVP省令
 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令 ( ) 発簡日平成 16 年 9 月 22 日発簡番号省令第 135 号情報種別省令 目次 第 1 章総則 ( 第 1 条 - 第 2 条 ) 第 2 章 第一種製造販売業者の製造販売後安全管理の基準 ( 第 3 条 - 第 12 条 ) 第 3 章 第二種製造販売業者の製造販売後安全管理の基準 ( 第 13 条 - 第
医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令 ( ) 発簡日平成 16 年 9 月 22 日発簡番号省令第 135 号情報種別省令 目次 第 1 章総則 ( 第 1 条 - 第 2 条 ) 第 2 章 第一種製造販売業者の製造販売後安全管理の基準 ( 第 3 条 - 第 12 条 ) 第 3 章 第二種製造販売業者の製造販売後安全管理の基準 ( 第 13 条 - 第
料 情報の提供に関する記録 を作成する方法 ( 作成する時期 記録の媒体 作成する研究者等の氏名 別に作成する書類による代用の有無等 ) 及び保管する方法 ( 場所 第 12 の1⑴の解説 5に規定する提供元の機関における義務 8 個人情報等の取扱い ( 匿名化する場合にはその方法等を含む ) 9
 北里研究所病院研究倫理委員会研究申請時確認シート ( 補助資料 ) 20170425 Ver.2.0 < 研究計画書の確認 > 記載項目 1 研究の名称 2 研究の実施体制 ( 研究機関の名称及び研究者等の氏名を含む ) 3 研究の目的及び意義 4 研究の方法及び期間 5 研究対象者の選定方針 6 研究の科学的合理性の根拠 7インフォームド コンセントを受ける手続等 ( インフォームド コンセントを受ける場合には
北里研究所病院研究倫理委員会研究申請時確認シート ( 補助資料 ) 20170425 Ver.2.0 < 研究計画書の確認 > 記載項目 1 研究の名称 2 研究の実施体制 ( 研究機関の名称及び研究者等の氏名を含む ) 3 研究の目的及び意義 4 研究の方法及び期間 5 研究対象者の選定方針 6 研究の科学的合理性の根拠 7インフォームド コンセントを受ける手続等 ( インフォームド コンセントを受ける場合には
二頁第二章治験の準備に関する基準第一節治験の依頼をしようとする者による治験の準備に関する基準(第四条 第十五条)第二節自ら治験を実施しようとする者による治験の準備に関する基準(第十六条 第二十三条)第三章治験の管理に関する基準第一節治験依頼者による治験の管理に関する基準(第二十四条 第三十四条)第二
 一頁〇厚生労働省令第八十九号医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律(昭和三十五年法律第百四十五号)第二十三条の二十五第三項(同条第九項(同法第二十三条の三十七第五項において準用する場合を含む )及び同法第二十三条の三十七第五項において準用する場合並びに同法第二十三条の二十六第五項(同法第二十三条の三十七第五項において準用する場合を含む )において読み替えて適用する場合を含む
一頁〇厚生労働省令第八十九号医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律(昭和三十五年法律第百四十五号)第二十三条の二十五第三項(同条第九項(同法第二十三条の三十七第五項において準用する場合を含む )及び同法第二十三条の三十七第五項において準用する場合並びに同法第二十三条の二十六第五項(同法第二十三条の三十七第五項において準用する場合を含む )において読み替えて適用する場合を含む
審議するものとする 2 前項の審議は 当該任期付職員の在任中の勤務態度 業績等の評価及び無期労働契約に転換した場合に当該任期付職員に係る退職日までの人件費の当該部局における措置方法について行うものとする 3 教授会等は 第 1 項の審議に当たり 必要に応じて 確認書類の要求 対象者への面接等の措置を
 国立大学法人電気通信大学無期労働契約転換に関する規程 平成 29 年 3 月 22 日第 1 章総則 ( 趣旨 ) 第 1 条この規程は 労働契約法 ( 平成 19 年法律第 128 号 ) 第 18 条に基づき 国立大学法人電気通信大学 ( 以下 本学 という ) に期間を定めて雇用される職員 ( 以下 任期付職員 という ) について 期間の定めのない労働契約 ( 以下 無期労働契約 という )
国立大学法人電気通信大学無期労働契約転換に関する規程 平成 29 年 3 月 22 日第 1 章総則 ( 趣旨 ) 第 1 条この規程は 労働契約法 ( 平成 19 年法律第 128 号 ) 第 18 条に基づき 国立大学法人電気通信大学 ( 以下 本学 という ) に期間を定めて雇用される職員 ( 以下 任期付職員 という ) について 期間の定めのない労働契約 ( 以下 無期労働契約 という )
治験事務局標準業務マニュアル
 治験申請等に関する手順書 Ⅰ) 新規治験の申請 1. 実施体制 治験事務局院内スタッフが SMO との提携し 事務局を運営する なお SMO の費用は院内費用とは別に算定するため 別途相談とする CRC 院内スタッフを用いる場合 SMO を利用する場合 どちらの選択も可能とする 2. ヒアリング (a) 予約に際しての条件 プロトコールが固定され 責任医師との合意が文書で得られた時点で予約は可能とする
治験申請等に関する手順書 Ⅰ) 新規治験の申請 1. 実施体制 治験事務局院内スタッフが SMO との提携し 事務局を運営する なお SMO の費用は院内費用とは別に算定するため 別途相談とする CRC 院内スタッフを用いる場合 SMO を利用する場合 どちらの選択も可能とする 2. ヒアリング (a) 予約に際しての条件 プロトコールが固定され 責任医師との合意が文書で得られた時点で予約は可能とする
