Microsoft PowerPoint _KGRIミ二シンポ_Yokote_Ver4 - 互換モード
|
|
|
- とき ひらみね
- 3 years ago
- Views:
Transcription
1 KGRI ミニシンポジウム ~ 冬期感染症対策について ~ 日本におけるワクチン産業 2019 年 12 月 13 日 ( 金 ) バイオシュート株式会社横手公幸 年 8 月 7 日 : 第 21 回厚生科学審議会予防接種 ワクチン分科会研究開発及び生産 流通部会資料より 2 1
2 2019 年 8 月 7 日 : 第 21 回厚生科学審議会予防接種 ワクチン分科会研究開発及び生産 流通部会資料より 3 ワクチンの誕生 ジェンナー種痘像 ( ジェノア博物館 ) 最初の天然痘予防接種 1796 年 Vaccine Vacca( 雌牛 ) ine( 薬剤 ) ハ スツールによる命名 4 2
3 ワクチンとは 免疫が脆弱または未成熟な人 及び特定の免疫を有しない人に対して 感染症の予防または治療を目的として投与され 免疫を賦活させるもの ( 私見 ) 抗癌ワクチン等は意味が異なる 5 Public Health とワクチン 保健衛生 (Public Health) は 地域性 ( 自給の必要性 ) の高さについて 国の果たすべき役割と重なります およそ国のような地域共同体の最も基本的かつ必須の役割の一つは その地域共同体における人々の生活や活動の源泉である保健衛生 (Public Health) の維持 向上を図ることにあります がん 糖尿病 高血圧症等多くの疾病は 個体における 正常な生命活動の内的破綻 が原因であり 地域を問わず グローバルな課題として医薬品の開発 製造 供給が行われます 一方ワクチンは 人や動物に無差別に襲いかかり その健康を脅かす 病原微生物等のような外的脅威 による感染症流行等から共同体をいかに防御するかに端を発しています 外的脅威 は必然的に地域特有であることが多く ワクチンや抗毒素等を防御手段として地域共同体が自ら守る責務があります 6 6 3
4 関連法律 種痘法 ( 法律 35 号 ): 明治 42 年 (1909 年 ) 予防接種法 : 昭和 23 年 (1948 年 ) 予防接種施行令 ( 政令 197):(1948 年 ) 予防接種法施行規則 ( 厚生省令 36):(1948 年 ) 予防接種法実施規則 ( 厚生省令 27):(1958 年 ) 結核予防法 7 予防接種とは 予防接種法 : 昭和 23 年 (1948 年 ) 第一条 ( 目的 ): 伝染のおそれがある疾病の発生及びまん延を予防するために公衆衛生の見地から予防接種の実施その他必要な措置を講ずることにより 国民の健康の保持に寄与するとともに 予防接種による健康被害の迅速な救済を図ること 集団 ( 社会 ) 防衛 人が感染してそれによって自ら感染源となることを防ぐ 伝染病 天然痘 インフルエンザ 百日咳 個人防衛 疾病の悪性と対処法として予防が最も効果がある 伝染性がない 日本脳炎 破傷風 ジフテリア 8 4
5 予防接種の意義づけ 予防接種体制 強制接種 勧奨接種 ( 日本脳炎 MR DPT/IPV 等 ) 定期接種 (HPV 等 ) 臨時接種 ( 天然痘 ) 予防接種対策の対象疾患 集団 ( 社会 ) 防疫 ( インフルエンザ 麻しん 百日咳等 ) 個人防疫 ( 日本脳炎 B 型肝炎等 ) 費用負担 予防接種の副反応と補償 9 予防接種の法体系 2019 年 11 月 8 日 : 第 35 回厚生科学審議会予防接種 ワクチン分科会予防接種基本方針部会資料より 10 5
6 定期接種の対象疾患 対象者 2019 年 11 月 8 日 : 第 35 回厚生科学審議会予防接種 ワクチン分科会予防接種基本方針部会資料より 予防接種に関する基本的な計画厚生労働省告示第百二十一号 : 平成 26 年 3 月 28 日付 第五 - 四ワクチンの生産体制及び流通体制 ワクチンの生産体制については 危機管理の観点から 国は パ ンデミックが発生し世界的に供給が不足するおそれがあるワクチン を国内で製造できる生産体制を整備する必要がある その他のワクチンについても 危機管理の観点から 国内で製造 できる生産体制を確保する必要はあるものの 費用対効果の観点 から 基本的には国内外問わずより良いワクチンがより低価格で供 給されることが望ましい また 安定供給及び価格競争の観点から 同種のワクチンが複数のワクチン製造販売業者により供給されるこ とが望ましい 6
7 生産業者 :12 団体製品 :33 品目 (7) 日本のワクチン第 2 版 痘瘡ワクチンの生産量の推移日本のワクチン第 2 版より参照 14 7
8 コレラワクチンの生産量の推移日本のワクチン第 2 版より参照 15 腸チフス パラチフスワクチンの生産量の推移 日本のワクチン第 2 版より参照 16 8
9 Vaccines/the manufacturers in Japan Product Kitasato Takeda Kaketsuken Biken Denka Japan BCG MSD SP Pfizer GSK Influenza A A A A Japanese encephalitis (JE) A A A: domestic manuf. B: import Rabies A HB A B HA DPT A A A A A DPT/IPV A A A A TT A A A A A Live polio MR A A Chickenpox BCG Smallpox A A A A 国内生産生産業者 :6 団体製品 :19 品目 (12) gas gangrene antitoxin botulinus antitoxin diphtheria antitoxin Antivenenum Agkistrodon halys equinum A A A A Government Purchase Products Antivenenum Trimeresurus flavoviridis equinum A Pneumococcus B B(Heptavalent) Hib B HPV B B Yellow fever vaccine Rota B B B 生物学的製剤基準収載ワクチン 改正 : 平成 25 年 6 月 18 日厚生労働省告示第 205 号白 : 国内発緑 : 海外発赤 : 国内外発黄 : 遺伝子組換え技術青 : 生産中止 インフルエンザワクチンインフルエンザ HA ワクチン沈降インフルエンザワクチン (H5N1 株 ) 乾燥組織培養不活化 A 型肝炎ワクチン乾燥弱毒生おたふくかぜワクチンガスえそウマ抗毒素 ( ガスえそ抗毒素 ) 乾燥ガスえそウマ抗毒素 ( 乾燥ガスえそ抗毒素 ) 不活化狂犬病ワクチン乾燥組織培養不活化狂犬病ワクチンコレラワクチン乾燥ジフテリアウマ抗毒素 ( 乾燥ジフテリア抗毒素 ) ジフテリアトキソイド沈降ジフテリアトキソイド成人用沈降ジフテリアトキソイドジフテリア破傷風混合トキソイド沈降ジフテリア破傷風混合トキソイド乾燥弱毒生水痘ワクチン腸チフスパラチフス混合ワクチン精製ツベルクリン痘そうワクチン ( 痘苗 ) 乾燥痘そうワクチン ( 乾燥痘苗 ) 細胞培養痘そうワクチン乾燥細胞培養痘そうワクチン日本脳炎ワクチン乾燥日本脳炎ワクチン乾燥細胞培養日本脳炎ワクチン肺炎球菌ワクチン沈降 7 価肺炎球菌結合型ワクチン ( 無毒性変異ジフテリア毒素結合体 ) 沈降 13 価肺炎球菌結合型ワクチン ( 無毒性変異ジフテリア毒素結合体 ) 破傷風トキソイド沈降破傷風トキソイド沈降はぶトキソイド沈降 B 型肝炎ワクチン沈降 B 型肝炎ワクチン (hugk-14 細胞由来 ) 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) 組換え沈降 B 型肝炎ワクチン ( チャイニーズハムスター卵巣細胞由来 ) 組換え沈降 pre-s2 抗原 HBs 抗原含有 B 型肝炎ワクチン ( 酵母由来 ) 乾燥 BCG 膀胱ぼうこう内用 ( コンノート株 ) 乾燥 BCG 膀胱ぼうこう内用 ( 日本株 ) 乾燥 BCG ワクチン組換え沈降 2 価ヒトパピローマウイルス様粒子ワクチン ( イラクサギンウワバ細胞由来 ) 組換え沈降 4 価ヒトパピローマウイルス様粒子ワクチン ( 酵母由来 ) 経口弱毒生ヒトロタウイルスワクチン百日せきワクチン沈降精製百日せきワクチン百日せきジフテリア混合ワクチン百日せきジフテリア破傷風混合ワクチン沈降精製百日せきジフテリア破傷風混合ワクチン沈降精製百日せきジフテリア破傷風不活化ポリオ ( セービン株 ) 混合ワクチン乾燥弱毒生風しんワクチン乾燥ヘモフィルス b 型ワクチン ( 破傷風トキソイド結合体 ) 発しんチフスワクチン経口生ポリオワクチン乾燥弱毒生麻しんワクチン乾燥弱毒生麻しんおたふくかぜ風しん混合ワクチン乾燥弱毒生麻しん風しん混合ワクチン 5 価経口弱毒生ロタウイルスワクチンワイル病秋やみ混合ワクチン 18 9
10 各ワクチンの年間生産量と接種人数等 年 11 月 8 日 : 第 35 回厚生科学審議会予防接種 ワクチン分科会予防接種基本方針部会資料より 2019 年 11 月 8 日 : 第 35 回厚生科学審議会予防接種 ワクチン分科会予防接種基本方針部会資料より 20 10
11 2019 年 11 月 8 日 : 第 35 回厚生科学審議会予防接種 ワクチン分科会予防接種基本方針部会資料より 21 ウイルスワクチン 生ワクチン痘そうワクチン ( 痘苗 ) 経口生ポリオワクチン乾燥弱毒生風しんワクチン乾燥弱毒生麻しんワクチン乾燥弱毒生おたふくかぜワクチン乾燥弱毒水痘ワクチン 不活化ワクチンインフルエンザワクチン乾燥組織培養不活化 A 型肝炎ワクチン不活化狂犬病ワクチン日本脳炎ワクチン沈降 B 型肝炎ワクチン組換え沈降 2 価ヒトパピローマウイルス様粒子ワクチン 22 11
12 ウイルスワクチンの細胞培養 動物個体培養 孵化鶏卵 乳のみマウス 成熟マウス ウシ ヒツジ 細胞培養 / 組織培養初代細胞ニワトリ胚細胞 ウサギ腎細胞 アフリカミドリザル腎細胞継代細胞 株化細胞 MRC-5 GL37 Vero, CHO, hugk-14 イラクサギンウワバ由来細胞 23 ワクチンの製造の流れ 出典 : ワクチンの基礎 2018 資料より 24 12
13 他の医薬品との生産システムの違い 有効成分 製造方法上流工程下流工程 品質試験 Life Time 化 学 医 薬 品 MW: 数 K 純度 : 単一 合成 発酵 再結晶 工程数 :2-5 理化学分析ガスクロ 5 年 バイオテク医薬品 生物学的製剤 ( ワクチン ) 分子量 : 20K ~ 十数万 純度 :95% 以上 分子量 : 数 100~ 数 K 万 純度 :10~90% 継代細胞培養 動物個体培養初代細胞培養継代細胞培養細菌培養 クロマト膜沪過 工程数 : 沈殿クロマト遠心不活化 工程数 : In vitro 試験 ELISA レセプター活性 In vivo 試験免疫原性感染防御感染価不活化確認中和抗体 7 ー 10 年 年 年 11 月 8 日 : 第 35 回厚生科学審議会予防接種 ワクチン分科会予防接種基本方針部会資料より 26 13
14 2019 年 11 月 8 日 : 第 35 回厚生科学審議会予防接種 ワクチン分科会予防接種基本方針部会資料より 27 欧米のワクチンの調達状況 2019 年 11 月 8 日 : 第 35 回厚生科学審議会予防接種 ワクチン分科会予防接種基本方針部会資料より 28 14
15 2019 年 11 月 8 日 : 第 35 回厚生科学審議会予防接種 ワクチン分科会予防接種基本方針部会資料より 年 11 月 8 日 : 第 35 回厚生科学審議会予防接種 ワクチン分科会予防接種基本方針部会資料より 30 15
16 予防接種に関する基本的な計画厚生労働省告示第百二十一号 : 平成 26 年 3 月 28 日付 第五ー三研究開発を促進するための関係者による環境作りワクチンの研究開発には 基礎研究から臨床研究まで幅広い知見が必要とされるものであり 国の関係機関 関係団体及びワクチン製造販売業者との間において十分かつ適切な連携が図られることが重要である 国立感染症研究所においては ワクチン候補株の開発を始めとする基礎研究から臨床研究への橋渡し等を実施するとともに 新しい品質管理手法の開発と確立を行っているところである また 独立行政法人医薬基盤研究所においても 新規ワクチンの創出に必要な基盤的技術の研究開発を行っている さらに 関係機関との連携の下 国内の有望な基礎研究の成果を革新的新薬の創出につなげるための取組が実施されている 今後もこれらの研究開発を促進するための取組が継続されることが期待される 国は 以下の事項について 引き続き検討する必要がある (1) ワクチンの需給の見通しに関する情報提供 (2) 感染症対策の目標設定ワクチン製造販売業者が感染症に対する新たなワクチンの研究開発に着手するか否かの重要な判断材料となるため 国は 特定の感染症について目標を設定し 排除 撲滅を計画的に推進する必要がある (3) 感染症の疫学情報の整備 (4) 小児の治験を実施する環境の整備予防接種の対象者には小児が多いため 国は 小児の被験者の確保等 治験が円滑に実施できる体制を整備するよう努める必要がある (5) ワクチンの基礎研究並びに実用化に向けた支援及び産学官の協力新たなワクチンを開発するためには 基礎研究に対する支援及び基礎研究の成果を企業の臨床開発研究へと橋渡しすることが重要である また ワクチンの実用化を円滑に行えるよう 大学 企業 研究機関等の共同研究を推進する必要がある 31 順位 厚生労働省 : ワクチン分科会研究開発及び生産 流通部会 分類 ワクチン 国内の優先度 (5 点 ) 平均 疾病負荷 1 混合ワクチン MMR/MMRV/MRV 混合ワクチン DPT-IPV-HBV-Hib/DPT-IPV-Hib 4.83 /DPT-IPV-HBV 3 その他 インフルエンザ ( 経鼻 ) その他 帯状疱疹ワクチン 渡航者ワクチン A ー B 型肝炎混合ワクチン その他 髄膜炎菌ワクチン 渡航者ワクチン 腸チフスワクチン 渡航者ワクチン ダニ媒介性脳炎ワクチン 渡航者ワクチン コレラワクチン 2.17 優先度を以下の基準で評価する 国内の必要性について 1 点 ~5 点の 5 段階で評価する 世界の必要性について 1 点 ~3 点の 3 段階で評価する ワクチン開発の実現性について -1 点 ( 開発が困難と考えられるもの ) 0 点 ( 開発の実現性が不明なもの ) 1 点 ( 開発の実現性が高いと考えられるもの ) の 3 段階で評価する 32 : 患者又は死亡者が多くみられる : 患者又は死亡者が一定程度みられる : 患者又は死亡者の数は多くない 16
17 ワクチンの開発状況 分類 開発企業 開発状況 MRを含んだ混合ワクチン MMRワクチン 第一三共 /GSK 第 3 相 KMB/Merck 承認申請中 DPT-IPVワクチンを含んだ混 DPT-IPV-Hib 微研 / 田辺三菱 第 3 相 合ワクチン KMB 第 3 相 サノフィ 第 3 相 第一三共 第 3 相 経鼻投与ワクチンなど現行 経鼻 第一三共 /AZ 承認申請中 のワクチンよりも優れたインフルエンザワクチン 微研 第 3 相 高用量 サノフィ 第 1/2 相 不活化全粒子 KMB 第 1/2 相 RSVワクチン Janssen 海外第 2b 相 Pfizer 海外第 2 相 GSK 海外第 1 相 ノロウイルスワクチン 武田 海外第 2 相 日本製薬工業資料より 33 ワクチン開発のパイプライン ( IFPMA Inquiry July 2009)
18 国際感染症対抗医薬品開発の支援 国際感染症対抗医薬品の開発体制 ( 官 学 産 ) の強化 新薬の臨床開発には膨大な時間と莫大な費用を要するため 企業単独ではリスクと負担が大きい シードから基礎研究 開発までの一環した体制とその支援が必要 国際感染症対抗医薬品の開発促進 使用に関する法整備 非臨床試験から臨床研究の段階を経て最終的な新薬申請書提出まで一連の開発プロセスに当局が関与し 新薬審査の迅速化 合理化を推進する 開発段階の医薬品の備蓄及び使用に関する基準 ( ガイドライン ) の作成 国主導の基礎 臨床研究ネットワークの整備 : 有効性 安全性に関する継続的な研究の維持 特殊性及び緊急度を評価し 必要に応じて国が主導となり臨床研究ネットワークを構築し 臨床開発の迅速化を支援する 日本における規制強化 生物原料基準 製造販売承認書の記載要求 GMP 情報の承認書への記載要求 36 18
19 生物学的製剤基準 37 生物学的製剤基準 ( 通則 ) 22 医薬品各条の規定のうち, 小分製品の試験は, 通常, 同一製造番号ごとに行う. ただし, 21 項に該当する小分製品群については, 製造工程のバリデーション及び適切な管理と品質試験検査に関する記録より恒常的にその品質が均一であり生物学的製剤基準に適合することが保証されてい場合には, 医薬品各条の小分試験を省略できる. 34 生物学的製剤基準に規定する試験法に代わる方法で, それが規程以上の正確さと精密がある場合にはその方法を用いることができる. 35 生物学的な試験法の規定は, 本質に影響い限り方細部について変更することができる
20 生物学的製剤基準の製品各条の一例 ( 沈降インフルエンザワクチン (H5N1 株 )) 39 承認申請書と CTD 文書の関係 承認申請書 許可申請 第二部 承認事項 ( 概要 ) 第三部 ( 添付資料 ) GMP 要件 生データ 実験室レベル パイロットプラントレベル 実製造レベル 40 20
21 承認申請書イメージ : 細胞培養 ( 生産培養 ) 薬事法改正前のテキスト部分続けて生産培地 ( 培地 3) を用いた生産培養を37 で行う. 生産培養においては, 総細胞濃度 1 10E6 細胞 /ml 以上になった時点で, 培養液を抜き取り, 同量の生産培地を添加し, 培養を継続する. 改正薬事法後のテキスト部分種培養液を 1200 L の無血清培地( 培地 2) を有する連続培養装置 ( 容量 1.5 m 3 ) に播種し 37 で培養する. 総細胞濃度 10 10E5 細胞 /ml 以上 になった時点で, 培養液約 1000 L を抜き取る. 生産培地 ( 培地 3) を同量添加し 37 で培養を継続する 承認申請書イメージ : 精製工程 ( 疎水クロマト ) 薬事法改正前のテキスト部分この溶出液を疎水クロマトカラムに展開し, 非吸着たんぱく質を洗浄除去後, 塩化ナトリウムを含むリン酸緩衝液で溶出する 改正薬事法後のテキスト部分これを 4L のブチル系疎水クロマトカラム 基材 : アガロース系樹脂 に展開し, 非吸着たん白質を洗浄除去後, 0.4mol/L の塩化ナトリウムを含む 0.01mol/L リン酸緩衝液 ( ph 7.0 ) で溶出する
22 他の医薬品との生産システムの違い 有効成分 製造方法上流工程下流工程 品質試験 Life Time 化 学 医 薬 品 MW: 数 K 純度 : 単一 合成 発酵 再結晶 工程数 :2-5 理化学分析ガスクロ 5 年 バイオテク医薬品 生物学的製剤 ( ワクチン ) 分子量 : 20K ~ 十数万 純度 :95% 以上 分子量 : 数 100~ 数 K 万 純度 :10~90% 継代細胞培養 動物個体培養初代細胞培養継代細胞培養細菌培養 クロマト膜沪過 工程数 : 沈殿クロマト遠心不活化 工程数 : In vitro 試験 ELISA レセプター活性 In vivo 試験免疫原性感染防御感染価不活化確認中和抗体 7 ー 10 年 年 まとめ 日本おけるワクチンの供給体制と開発体制は 脆弱である 人の交流と国際化において 再興感染症 ( 赤痢 コレラ等 ) と新興感染症 ( デング エボラ等 ) の流行の可能性が高まりつつある ワクチンを国家安全保障の対抗医薬品と位置付けて その観点からの入札や供給備蓄体制を検討する 44 22
2012/02/22 ワクチン分科会 The Foundation of Medical and Veterinary Virology by utmb より 国内の天然痘発生状況 2012/02/22 ワクチン分科会引用 : 臨床とウイルス Vol 木村三生夫他 2
 バイオロジクスフォーラム第 9 回学術集会於 : タワーホール船堀 ワクチン分科会 日本のワクチン開発の活性化のために 座長横手公幸 ( 化血研 )/ 浜口功 ( 感染研 ) 2012/02/22 ワクチン分科会 1 2012/02/22 ワクチン分科会 The Foundation of Medical and Veterinary Virology by utmb より 1 2012/02/22
バイオロジクスフォーラム第 9 回学術集会於 : タワーホール船堀 ワクチン分科会 日本のワクチン開発の活性化のために 座長横手公幸 ( 化血研 )/ 浜口功 ( 感染研 ) 2012/02/22 ワクチン分科会 1 2012/02/22 ワクチン分科会 The Foundation of Medical and Veterinary Virology by utmb より 1 2012/02/22
2. 定期接種ンの 接種方法等について ( 表 2) ンの 種類 1 歳未満 生 BCG MR 麻疹風疹 接種回数接種方法接種回数 1 回上腕外側のほぼ中央部に菅針を用いて2か所に圧刺 ( 経皮接種 ) 1 期は1 歳以上 2 歳未満 2 期は5 歳以上 7 歳未満で小学校入学前の 1 年間 ( 年
 ンの種類と当院における オーダー時検索名について ンは 生ン 不活化ン トキソイド の3つに分けられ さらにわが国では接種の区分として定期接種 ( 対象者年齢は政令で規定 ) 任意接種の2つに分けられます ンと一言で言っても ンの製品名と成分名がほぼ同じものや全く異なるもの 略称で記載されることの多いものなど 一見すると分かりづらいため 今回日本で承認されているン ( 表 1) とその 接種方法等
ンの種類と当院における オーダー時検索名について ンは 生ン 不活化ン トキソイド の3つに分けられ さらにわが国では接種の区分として定期接種 ( 対象者年齢は政令で規定 ) 任意接種の2つに分けられます ンと一言で言っても ンの製品名と成分名がほぼ同じものや全く異なるもの 略称で記載されることの多いものなど 一見すると分かりづらいため 今回日本で承認されているン ( 表 1) とその 接種方法等
(資料1-1)わが国のワクチン産業と市場の動向ver3_4
 資料 1-1 わが国のワクチン産業と市場の動向 厚生科学審議会予防接種 ワクチン分科会研究開発及び生産 流通部会 Japanese Association of Vaccine Industries 平成 25 年 6 月 25 日 一般社団法人日本ワクチン産業協会 一般社団法人日本ワクチン産業協会について S.21(1946) 年 10 月 H.23(2011) 年 9 月 ( 社 ) 細菌製剤協会として設立
資料 1-1 わが国のワクチン産業と市場の動向 厚生科学審議会予防接種 ワクチン分科会研究開発及び生産 流通部会 Japanese Association of Vaccine Industries 平成 25 年 6 月 25 日 一般社団法人日本ワクチン産業協会 一般社団法人日本ワクチン産業協会について S.21(1946) 年 10 月 H.23(2011) 年 9 月 ( 社 ) 細菌製剤協会として設立
第1 入間市の概要
 第 6 予防接種事業 1 予防接種事業 (1) 乳幼児等の予防接種事業ア目的接種を受けた個人に免疫を付けることにより感染及び発症の予防 症状の軽減化を図る また 感染症の発生及びまん延を予防し 公衆衛生の向上及び増進を図ることを目的とする イ根拠 関連法令予防接種法 予防接種法施行令 予防接種法施行規則 予防接種実施規則 定期接種実施要領ウ対象 予防接種の種類 対象年齢 ヒブ (Hib) 小児用肺炎球菌
第 6 予防接種事業 1 予防接種事業 (1) 乳幼児等の予防接種事業ア目的接種を受けた個人に免疫を付けることにより感染及び発症の予防 症状の軽減化を図る また 感染症の発生及びまん延を予防し 公衆衛生の向上及び増進を図ることを目的とする イ根拠 関連法令予防接種法 予防接種法施行令 予防接種法施行規則 予防接種実施規則 定期接種実施要領ウ対象 予防接種の種類 対象年齢 ヒブ (Hib) 小児用肺炎球菌
Microsoft PowerPoint - 【配布資料】28予防接種従事者研修
 予防接種制度の概要について 3 目的 伝染のおそれがある疾病の発生及びまん延を予防するために公衆衛生の見地から予防接種の実施その他必要な措置を講ずることにより 国民の健康の保持に寄与する 予防接種による健康被害の迅速な救済を図る 予防接種の実施 予防接種法の概要 ( その 1) 対象疾病 A 類疾病 ( 主に集団予防 重篤な疾患の予防に重点 本人に努力義務 接種勧奨有り ) ジフテリア 百日せき 急性灰白髄炎
予防接種制度の概要について 3 目的 伝染のおそれがある疾病の発生及びまん延を予防するために公衆衛生の見地から予防接種の実施その他必要な措置を講ずることにより 国民の健康の保持に寄与する 予防接種による健康被害の迅速な救済を図る 予防接種の実施 予防接種法の概要 ( その 1) 対象疾病 A 類疾病 ( 主に集団予防 重篤な疾患の予防に重点 本人に努力義務 接種勧奨有り ) ジフテリア 百日せき 急性灰白髄炎
ロタウイルスワクチンは初回接種を1 価で始めた場合は 1 価の2 回接種 5 価で始めた場合は 5 価の3 回接種 となります 母子感染予防の場合のスケジュール案を示す 母子感染予防以外の目的で受ける場合は 4 週間の間隔をあけて2 回接種し 1 回目 の接種から20~24 週あけて3 回目を接種生
 注 1) 本スケジュール案は 2014 年 10 月現在 接種可能な主なワクチンをすべて受けると仮定して 1 例を示したものです 接種の順番や受けるワクチンの種類については お子様の体調や周りの感染症発生状況によって 異なってきます 詳しくはかかりつけの医療機関 保健所等でご相談ください 注 2) 接種に際しては次の決まりがあります スケジュールを立てるときの参考にしてください 別の種類のワクチンを接種する場合は
注 1) 本スケジュール案は 2014 年 10 月現在 接種可能な主なワクチンをすべて受けると仮定して 1 例を示したものです 接種の順番や受けるワクチンの種類については お子様の体調や周りの感染症発生状況によって 異なってきます 詳しくはかかりつけの医療機関 保健所等でご相談ください 注 2) 接種に際しては次の決まりがあります スケジュールを立てるときの参考にしてください 別の種類のワクチンを接種する場合は
00【議連提出資料】B型肝炎ワクチンの定期接種化について
 第 17 回 肝炎対策推進協議会 平成 28 年 3 月 17 日参考資料 5 B 型肝炎ワクチンの 定期接種化ついて B 型肝炎ワクチンの定期接種化について 平成 28 年 2 月 22 日の予防接種 ワクチン分科会において これまでの部会等の審議を踏まえ B 型肝炎ワクチンの定期接種化について 以下のとおり了承された 1. 開始時期平成 28 年 10 月 2. 分類 A 類疾病 3. 対象年齢平成
第 17 回 肝炎対策推進協議会 平成 28 年 3 月 17 日参考資料 5 B 型肝炎ワクチンの 定期接種化ついて B 型肝炎ワクチンの定期接種化について 平成 28 年 2 月 22 日の予防接種 ワクチン分科会において これまでの部会等の審議を踏まえ B 型肝炎ワクチンの定期接種化について 以下のとおり了承された 1. 開始時期平成 28 年 10 月 2. 分類 A 類疾病 3. 対象年齢平成
DPT, MR等混合ワクチンの推進に関する要望書
 平成 19 年 8 月 2 日厚生労働省健康局結核感染症課課長三宅智殿社団法人日本小児科学会会長別所文雄要望書 DPT, MR 等混合ワクチンの推進に関する要望 ( 既罹患者への混合ワクチン接種 ) 定期予防接種対象疾患であるジフテリア (D) 百日咳(P) 及び破傷風 (T) については かつては DPT 混合ワクチン DT 混合ワクチン またはそれぞれの単味ワクチンが定期予防接種の対象ワクチンとなっていましたが
平成 19 年 8 月 2 日厚生労働省健康局結核感染症課課長三宅智殿社団法人日本小児科学会会長別所文雄要望書 DPT, MR 等混合ワクチンの推進に関する要望 ( 既罹患者への混合ワクチン接種 ) 定期予防接種対象疾患であるジフテリア (D) 百日咳(P) 及び破傷風 (T) については かつては DPT 混合ワクチン DT 混合ワクチン またはそれぞれの単味ワクチンが定期予防接種の対象ワクチンとなっていましたが
スライド 1
 PhRMA 日本医師会シンポジウム 転換期を迎えた日本のワクチン政策 日本のワクチン政策に関する最新情報 川崎市健康安全研究所 ( 旧 : 川崎市衛生研究所 ) 岡部信彦平成 26 年 5 月 21 日 天然痘 ( 痘瘡 ) の予防接種 = 種痘 ( しゅとう ) 50 年 1796 年 1849 年 予防接種法 昭和 23(1948) 年 : 予防接種法の制定 - 痘そう *1 ジフテリア *1
PhRMA 日本医師会シンポジウム 転換期を迎えた日本のワクチン政策 日本のワクチン政策に関する最新情報 川崎市健康安全研究所 ( 旧 : 川崎市衛生研究所 ) 岡部信彦平成 26 年 5 月 21 日 天然痘 ( 痘瘡 ) の予防接種 = 種痘 ( しゅとう ) 50 年 1796 年 1849 年 予防接種法 昭和 23(1948) 年 : 予防接種法の制定 - 痘そう *1 ジフテリア *1
H30_業務の概要18.予防接種
 18. 予防接種 [1] 定期予防接種 ( 予防接種法 ) 感染症の発生及びまん延を予防するため 法令で定められた疾病 ( ポリオ ジフテリア 百日せき 破傷風 麻しん 風しん 日本脳炎 結核 Hib 小児の肺炎球菌 ヒトパピローマウィルス インフルエンザ ) の予防接種を行なっている 対象者に通知し 区内契約医療機関で実施している 平成 24 年 9 月 1 日から不活化ポリオワクチンの導入に伴い
18. 予防接種 [1] 定期予防接種 ( 予防接種法 ) 感染症の発生及びまん延を予防するため 法令で定められた疾病 ( ポリオ ジフテリア 百日せき 破傷風 麻しん 風しん 日本脳炎 結核 Hib 小児の肺炎球菌 ヒトパピローマウィルス インフルエンザ ) の予防接種を行なっている 対象者に通知し 区内契約医療機関で実施している 平成 24 年 9 月 1 日から不活化ポリオワクチンの導入に伴い
生ワクチン 不活化ワクチン ジフテリア 百日咳 破傷風 不活化ポリオ混合ワクチン の接種から20~24 週あけて3 回目を接種 別の種類のワクチンを接種する場合は 中 27 日 ( いわゆる4 週間 ) 以上あけて受けます 別の種類のワクチンを接種する場合は 中 6 日 ( いわゆる1 週間 ) 以
 注 1) 本スケジュール案は 2012 年現在 接種可能な主なワクチンをすべて受けると仮定して1 例を示したものです 接種の順番や受けるワクチンの種類については お子様の体調や周りの感染症発生状況によって 異なってきます 詳しくはかかりつけの医療機関 保健所等でご相談ください 注 2) 接種に際しては次の決まりがあります スケジュールを立てるときの参考にしてください 別の種類のワクチンを接種する場合は
注 1) 本スケジュール案は 2012 年現在 接種可能な主なワクチンをすべて受けると仮定して1 例を示したものです 接種の順番や受けるワクチンの種類については お子様の体調や周りの感染症発生状況によって 異なってきます 詳しくはかかりつけの医療機関 保健所等でご相談ください 注 2) 接種に際しては次の決まりがあります スケジュールを立てるときの参考にしてください 別の種類のワクチンを接種する場合は
事務連絡平成 28 年 2 月 5 日 各都道府県衛生主管部 ( 局 ) 御中 厚生労働省健康局健康課 厚生科学審議会予防接種 ワクチン分科会基本方針部会の審議について 本日開催された厚生科学審議会予防接種 ワクチン分科会基本方針部会における審議の結果 B 型肝炎ワクチンの定期接種化について 以下の
 ( 地 Ⅲ249F) 平成 28 年 2 月 26 日 都道府県医師会 感染症危機管理担当理事殿 日本医師会感染症危機管理対策室長 小森 貴 B 型肝炎ワクチンの定期接種化について B 型肝炎ワクチンの定期接種化については 本会といたしましても貴会ならびに会員等のご協力のもと予防接種キャンペーン 署名活動などの活動を展開してまいりました 今般 第 14 回厚生科学審議会予防接種 ワクチン分科会予防接種基本方針部会
( 地 Ⅲ249F) 平成 28 年 2 月 26 日 都道府県医師会 感染症危機管理担当理事殿 日本医師会感染症危機管理対策室長 小森 貴 B 型肝炎ワクチンの定期接種化について B 型肝炎ワクチンの定期接種化については 本会といたしましても貴会ならびに会員等のご協力のもと予防接種キャンペーン 署名活動などの活動を展開してまいりました 今般 第 14 回厚生科学審議会予防接種 ワクチン分科会予防接種基本方針部会
日本小児科学会が推奨する予防接種スケジュール
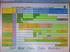 日本小児科学会推奨の予防接種スケジュールの主な変更点 2012 年 4 月 20 日 1) ヒブワクチン ヒブワクチンの追加接種 (4) に関して 添付文書上は 3 からおおむね 1 年あけるとありますが 追加接種による効果は 早期に得られるべきであると 考えます したがって 4 は 12 から接種することで適切な免疫が早期にえられる という 1 文を加えました 2) ワクチン 5 価ワクチンのスケジュールを加えました
日本小児科学会推奨の予防接種スケジュールの主な変更点 2012 年 4 月 20 日 1) ヒブワクチン ヒブワクチンの追加接種 (4) に関して 添付文書上は 3 からおおむね 1 年あけるとありますが 追加接種による効果は 早期に得られるべきであると 考えます したがって 4 は 12 から接種することで適切な免疫が早期にえられる という 1 文を加えました 2) ワクチン 5 価ワクチンのスケジュールを加えました
日本脳炎不活化ワクチン ( シード ) 平成 24 年 7 月 4 日 ( 告示第 1622 号 ) 新規追加 1 定義シードロット規格に適合した日本脳炎ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を不活化したワクチンである 2 製法 2.1 製造用株 名称日本脳炎ウイル
 日本脳炎不活化ワクチン ( シード ) 平成 24 年 7 月 4 日 ( 告示第 1622 号 ) 新規追加 1 定義シードロット規格に適合した日本脳炎ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を不活化したワクチンである 2 製法 2.1 製造用株 2.1.1 名称日本脳炎ウイルス中山株薬検系又はこれと同等と認められた株 2.1.2 性状豚腎初代細胞で増殖し がちょう 鶏初生ひな及びはとの赤血球を凝集する
日本脳炎不活化ワクチン ( シード ) 平成 24 年 7 月 4 日 ( 告示第 1622 号 ) 新規追加 1 定義シードロット規格に適合した日本脳炎ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を不活化したワクチンである 2 製法 2.1 製造用株 2.1.1 名称日本脳炎ウイルス中山株薬検系又はこれと同等と認められた株 2.1.2 性状豚腎初代細胞で増殖し がちょう 鶏初生ひな及びはとの赤血球を凝集する
再生医療の制度的な対応の検討について 薬事法等制度改正についてのとりまとめ平成 24 年 1 月 24 日厚生科学審議会医薬品制度改正部会 1 再生医療製品については 今後も 臓器機能の再生等を通じて 重篤で生命を脅かす疾患等の治療等に ますます重要な役割を果たすことが期待される 特に ips 細胞
 薬事戦略相談について ( 事業の概要等 ) 日本発の革新的な医薬品 医療機器の創出に向け 有望なシーズを持つ大学 研究機関 ベンチャー企業を主な対象として 開発初期から必要な試験 治験に関する指導 助言を実施するものとして 平成 23 年 7 月 1 日より開始した 基礎研究から実用化に向けては様々な課題があり 課題解決に向けた審査当局との早期相談が重要である 例えば 品質のデータや毒性データ等を適切に実施していない場合
薬事戦略相談について ( 事業の概要等 ) 日本発の革新的な医薬品 医療機器の創出に向け 有望なシーズを持つ大学 研究機関 ベンチャー企業を主な対象として 開発初期から必要な試験 治験に関する指導 助言を実施するものとして 平成 23 年 7 月 1 日より開始した 基礎研究から実用化に向けては様々な課題があり 課題解決に向けた審査当局との早期相談が重要である 例えば 品質のデータや毒性データ等を適切に実施していない場合
次の人は 医師が健康状態や体質に基づいて 接種の適否を判断します 心臓や血管 腎臓 肝臓 血液の障害や発育の障害などの基礎疾患がある人 他のワクチンの接種を受けて 2 日以内に発熱があった人や全身性の発疹などアレルギーが疑われる症状が出たことがある人 過去にけいれんをおこしたことがある人 過去に免疫
 ワクチン接種を受ける人へのガイド 2014 年 6 月作成 乾燥ヘモフィルス b 型ワクチン このワクチンの名前は? 販売名 一般名 アクトヒブ ActHIB 乾燥ヘモフィルス b 型ワクチン ( 破傷風トキソイド結合体 ) Haemophilus influenzae type b conjugate Vaccine ワクチン接種を受ける人へのガイドについてワクチンの正しい理解と 重大な副反応の早期発見などに役立てていただくために
ワクチン接種を受ける人へのガイド 2014 年 6 月作成 乾燥ヘモフィルス b 型ワクチン このワクチンの名前は? 販売名 一般名 アクトヒブ ActHIB 乾燥ヘモフィルス b 型ワクチン ( 破傷風トキソイド結合体 ) Haemophilus influenzae type b conjugate Vaccine ワクチン接種を受ける人へのガイドについてワクチンの正しい理解と 重大な副反応の早期発見などに役立てていただくために
<4D F736F F D E396F28AEE94D598418C67CCABB0D7D A90CE90EC964C90948E D5A90B38DCF82DD E342E36>
 ワクチン開発の現状について スライド1をご覧下さい 財団法人阪大微生物病研究会私は ご紹介頂きましたようにワクチンを製観音寺研究所造しているメーカーの人間でございまして 先いしかわとよかず副理事石川豊数程の3 人の先生方のようなアカデミックな話の内容とは少し異なりまして ワクチン製造メーカーが行っていますワクチン開発の現状というものと 問題点を紹介させて頂きたいと思います スライド2をご覧下さい このスライドは
ワクチン開発の現状について スライド1をご覧下さい 財団法人阪大微生物病研究会私は ご紹介頂きましたようにワクチンを製観音寺研究所造しているメーカーの人間でございまして 先いしかわとよかず副理事石川豊数程の3 人の先生方のようなアカデミックな話の内容とは少し異なりまして ワクチン製造メーカーが行っていますワクチン開発の現状というものと 問題点を紹介させて頂きたいと思います スライド2をご覧下さい このスライドは
ヒブ ( インフルエンザ菌 b 型 ) 対象者 : 生後 2ヶ月から5 歳未満までのお子さん標準的な接種開始期間は 生後 2ヶ月から7ヶ月未満です 生後 2ヶ月を過ぎたら 早目に接種しましょう 接種方法 : 接種開始時の年齢により接種方法が異なります 接種開始が生後 2ヶ月から7ヶ月未満の場合 (
 ヒブ ( インフルエンザ菌 b 型 ) 対象者 : 生後 2ヶ月から5 歳未満までのお子さん標準的な接種開始期間は 生後 2ヶ月から7ヶ月未満です 生後 2ヶ月を過ぎたら 早目に接種しましょう : 接種開始時の年齢によりが異なります 接種開始が生後 2ヶ月から7ヶ月未満の場合 ( 標準的な ) 回数 接種間隔等 1 回目 生後 2ヶ月から7ヶ月未満で接種開始 2 回目 1 回目接種後 27 日以上
ヒブ ( インフルエンザ菌 b 型 ) 対象者 : 生後 2ヶ月から5 歳未満までのお子さん標準的な接種開始期間は 生後 2ヶ月から7ヶ月未満です 生後 2ヶ月を過ぎたら 早目に接種しましょう : 接種開始時の年齢によりが異なります 接種開始が生後 2ヶ月から7ヶ月未満の場合 ( 標準的な ) 回数 接種間隔等 1 回目 生後 2ヶ月から7ヶ月未満で接種開始 2 回目 1 回目接種後 27 日以上
このワクチンの接種前に 確認すべきことは? ワクチン接種を受ける人または家族の方などは このワクチンの効果や副反応などの注意すべき点について十分理解できるまで説明を受けてください 説明に同意した上で接種を受けてください 医師が問診 検温および診察の結果から 接種できるかどうか判断します 次の人は こ
 ワクチン接種を受ける人へのガイド 2014 年 6 月作成 沈降 13 価肺炎球菌結合型ワクチン ( 無毒性変異ジフテリア毒素結合体 ) このワクチンの名前は? 販売名 一般名 プレベナー 13 水性懸濁注 Prevenar13 Suspension Liquid for Injection 沈降 13 価肺炎球菌結合型ワクチン ( 無毒性変異ジフテリア毒素結合体 ) Pneumococcal 13-valent
ワクチン接種を受ける人へのガイド 2014 年 6 月作成 沈降 13 価肺炎球菌結合型ワクチン ( 無毒性変異ジフテリア毒素結合体 ) このワクチンの名前は? 販売名 一般名 プレベナー 13 水性懸濁注 Prevenar13 Suspension Liquid for Injection 沈降 13 価肺炎球菌結合型ワクチン ( 無毒性変異ジフテリア毒素結合体 ) Pneumococcal 13-valent
スライド 1
 薬事承認に向けたワクチン開発の課題 厚生労働省医薬食品局総務課 紀平哲也 1 医薬品の開発 医薬品 感染症予防ワクチン 基礎 応用研究 基礎 応用研究 品質開発 品質開発 非臨床試験 非臨床試験 臨床研究 治験 臨床研究 治験 承認審査 承認審査 保険適用 定期接種化 市販後調査 市販後調査 2 おことわり 講演内容は演者個人の見解であり 必ずしも厚生労働省または PMDA の 見解ではありません
薬事承認に向けたワクチン開発の課題 厚生労働省医薬食品局総務課 紀平哲也 1 医薬品の開発 医薬品 感染症予防ワクチン 基礎 応用研究 基礎 応用研究 品質開発 品質開発 非臨床試験 非臨床試験 臨床研究 治験 臨床研究 治験 承認審査 承認審査 保険適用 定期接種化 市販後調査 市販後調査 2 おことわり 講演内容は演者個人の見解であり 必ずしも厚生労働省または PMDA の 見解ではありません
9 予防接種
 9 予防接種 1 予防接種実施体制 ( 平成 28 年度 七尾市 参考 : 平成 28 年度予防接種担当者連絡会資料 接種対象年齢接種方法接種場所周知方法未接種者への対応 ヒブ 生後 2 か月 ~5 歳に至るまで 赤ちゃん訪問 健診 教室時に個別指導 小児用肺炎球菌 生後 2 か月 ~5 歳に至るまで 赤ちゃん訪問 健診 教室時に個別指導 4 種混合百日咳破傷風ジフテリア不活化ポリオ 生後 3 か月
9 予防接種 1 予防接種実施体制 ( 平成 28 年度 七尾市 参考 : 平成 28 年度予防接種担当者連絡会資料 接種対象年齢接種方法接種場所周知方法未接種者への対応 ヒブ 生後 2 か月 ~5 歳に至るまで 赤ちゃん訪問 健診 教室時に個別指導 小児用肺炎球菌 生後 2 か月 ~5 歳に至るまで 赤ちゃん訪問 健診 教室時に個別指導 4 種混合百日咳破傷風ジフテリア不活化ポリオ 生後 3 か月
日本小児科学会が推奨する予防接種スケジュール 014 年 10 月 1 日版日本小児科学会 乳児期幼児期学童期 / 思春期 ワクチン 種類 直後 6 週 以上 インフルエンザ菌 b 型 ( ヒブ )
 日本小児科学会が推奨する予防接種スケジュールの主な変更点 014 年 10 月 1 日 1) 水痘ワクチンが定期接種化されました ) 定期接種のワクチンの接種間隔の上限が緩和されたことを受け インフルエンザ菌 b 型 4 種混合 日本脳炎 ヒトパピローマウイルスワクチンの定期接種としての接種間隔の記載が変更となりました 3) インフルエンザ菌 b 型 麻しんワクチンの接種期間に関する注意事項を追記しました
日本小児科学会が推奨する予防接種スケジュールの主な変更点 014 年 10 月 1 日 1) 水痘ワクチンが定期接種化されました ) 定期接種のワクチンの接種間隔の上限が緩和されたことを受け インフルエンザ菌 b 型 4 種混合 日本脳炎 ヒトパピローマウイルスワクチンの定期接種としての接種間隔の記載が変更となりました 3) インフルエンザ菌 b 型 麻しんワクチンの接種期間に関する注意事項を追記しました
日本小児科学会が推奨する予防接種スケジュールの主な変更点 2014 年 1 月 12 日 1)13 価結合型肺炎球菌ワクチンの追加接種についての記載を訂正 追加しました 2)B 型肝炎母子感染予防のためのワクチン接種時期が 生後 か月 から 生直後 1 6 か月 に変更と なりました (
 日本小児科学会が推奨する予防接種スケジュールの主な変更点 04 年 月 日 )3 価結合型肺炎球菌ワクチンの追加接種についての記載を訂正 追加しました )B 型肝炎母子感染予防のためのワクチン接種時期が 後 3 5 から 直後 6 に変更と なりました ( 現在 添付文書改定中 ) 日本小児科学会が推奨する予防接種スケジュール 04 年 月 日版日本小児科学会 乳児期幼児期学童期 ワクチン 種類 6
日本小児科学会が推奨する予防接種スケジュールの主な変更点 04 年 月 日 )3 価結合型肺炎球菌ワクチンの追加接種についての記載を訂正 追加しました )B 型肝炎母子感染予防のためのワクチン接種時期が 後 3 5 から 直後 6 に変更と なりました ( 現在 添付文書改定中 ) 日本小児科学会が推奨する予防接種スケジュール 04 年 月 日版日本小児科学会 乳児期幼児期学童期 ワクチン 種類 6
<B 型肝炎 (HBV)> ~ 平成 28 年 10 月 1 日から定期の予防接種になりました ~ このワクチンは B 型肝炎ウイルス (HBV) の感染を予防するためのワクチンです 乳幼児感染すると一過性感染あるいは持続性感染 ( キャリア ) を起こします そのうち約 10~15 パーセントは
 定期予防接種 ( 平成 28 年 10 月 1 日現在 ) B 型肝炎 (HBV) インフルエンザ菌 b 型 (Hib) 小児用肺炎球菌 四種混合(DPT-IPV) BCG 麻しん 風しん(MR) 水痘( 水ぼうそう ) 日本脳炎けい 子宮頸がん予防ワクチン 予防接種健康被害救済制度について ~ 平成 28 年 10 月 1 日から定期の予防接種になりました ~ このワクチンは
定期予防接種 ( 平成 28 年 10 月 1 日現在 ) B 型肝炎 (HBV) インフルエンザ菌 b 型 (Hib) 小児用肺炎球菌 四種混合(DPT-IPV) BCG 麻しん 風しん(MR) 水痘( 水ぼうそう ) 日本脳炎けい 子宮頸がん予防ワクチン 予防接種健康被害救済制度について ~ 平成 28 年 10 月 1 日から定期の予防接種になりました ~ このワクチンは
ロタテック内用液ワクチン接種を受ける人へのガイド
 ワクチン接種を受ける人へのガイド 2017 年 11 月更新 5 価経口弱毒生ロタウイルスワクチン このワクチンの名前は? 販売名 一般名 ロタテック内用液 RotaTeq Oral Solution 5 価経口弱毒生ロタウイルスワクチン Rotavirus Vaccine, Live, Attenuated, Oral, Pentavalent ワクチン接種を受ける人へのガイドについてワクチンの正しい理解と
ワクチン接種を受ける人へのガイド 2017 年 11 月更新 5 価経口弱毒生ロタウイルスワクチン このワクチンの名前は? 販売名 一般名 ロタテック内用液 RotaTeq Oral Solution 5 価経口弱毒生ロタウイルスワクチン Rotavirus Vaccine, Live, Attenuated, Oral, Pentavalent ワクチン接種を受ける人へのガイドについてワクチンの正しい理解と
馬ロタウイルス感染症 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 24 年 7 月 4 日 ( 告示第 1622 号 ) 新規追加 1 定義シードロット規格に適合した馬ロタウイルス (A 群 G3 型 ) を同規格に適合した株化細胞で増殖させて得たウイルス液を不活化し アジュバント
 馬ロタウイルス感染症 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 24 年 7 月 4 日 ( 告示第 1622 号 ) 新規追加 1 定義シードロット規格に適合した馬ロタウイルス (A 群 G3 型 ) を同規格に適合した株化細胞で増殖させて得たウイルス液を不活化し アジュバントを添加したワクチンである 2 製法 2.1 製造用株 2.1.1 名称馬ロタウイルス Ho-5MA 株又はこれと同等と認められた株
馬ロタウイルス感染症 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 24 年 7 月 4 日 ( 告示第 1622 号 ) 新規追加 1 定義シードロット規格に適合した馬ロタウイルス (A 群 G3 型 ) を同規格に適合した株化細胞で増殖させて得たウイルス液を不活化し アジュバントを添加したワクチンである 2 製法 2.1 製造用株 2.1.1 名称馬ロタウイルス Ho-5MA 株又はこれと同等と認められた株
1. 今回の変更に関する整理 効能 効果及び用法 用量 ( 添付文書より転載 ) 従来製剤 ( バイアル製剤 ) と製法変更製剤 ( シリンジ製剤 ) で変更はない 効能 効果 用法 容量 B 型肝炎の予防通常 0.5mL ずつ4 週間隔で2 回 更に 20~24 週を経過した後に1 回 0.5mL
 資料 6 MSD 社の製造する B 型肝炎単抗原ワクチンについて 経緯 1986 年米国メルク社製 B 型肝炎ワクチン ( 酵母由来 ) が米国で承認 1988 年 MSD 社製 B 型肝炎ワクチン ( 酵母由来 ) が日本で承認 2000 年欧州で HEXAVAC( ジフテリア 破傷風 百日咳 B 型肝炎 不活化ポリオ Hib 感染症を予防する 6 種混合ワクチン ) 承認 2001 年欧州で HEXAVAC
資料 6 MSD 社の製造する B 型肝炎単抗原ワクチンについて 経緯 1986 年米国メルク社製 B 型肝炎ワクチン ( 酵母由来 ) が米国で承認 1988 年 MSD 社製 B 型肝炎ワクチン ( 酵母由来 ) が日本で承認 2000 年欧州で HEXAVAC( ジフテリア 破傷風 百日咳 B 型肝炎 不活化ポリオ Hib 感染症を予防する 6 種混合ワクチン ) 承認 2001 年欧州で HEXAVAC
株化細胞 + 生ウイルスワクチン 特定の株名及びロット番号を記載 株変更は新規 また 6 製造方法ロットの更新は 事項変更 6.1 製造用株 名称弱毒 ウイルス 株 ( マスターシードウイルスロット〇 ) 株名 本数 継代方法等は GMP 省令第 7 条の 3 に基づく記録に関する文 書
 動物用生物学的製剤の製造方法欄のモックアップ ( シードロット製剤 ) はじめに : 本モックアップの原案は 平成 28 年度に実施された動物用医薬品の承認申請資料作成のためのガイドライン作成事業 生物学的製剤の製造方法欄のモックアップ ( シードロット製剤 ) において 動物用生物学的製剤の製造販売業者等の専門家からなるモックアップ作成検討委員会により作成された 本モックアップは モックアップ原案に必要な記載整備を行ったものである
動物用生物学的製剤の製造方法欄のモックアップ ( シードロット製剤 ) はじめに : 本モックアップの原案は 平成 28 年度に実施された動物用医薬品の承認申請資料作成のためのガイドライン作成事業 生物学的製剤の製造方法欄のモックアップ ( シードロット製剤 ) において 動物用生物学的製剤の製造販売業者等の専門家からなるモックアップ作成検討委員会により作成された 本モックアップは モックアップ原案に必要な記載整備を行ったものである
Microsoft Word - 【発送版】製造所の登録通知
 薬食機参発 1003 第 1 号 平成 26 年 10 月 3 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いについて 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業は登録制に移行され
薬食機参発 1003 第 1 号 平成 26 年 10 月 3 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いについて 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業は登録制に移行され
横浜市感染症発生状況 ( 平成 30 年 ) ( : 第 50 週に診断された感染症 ) 二類感染症 ( 結核を除く ) 月別届出状況 該当なし 三類感染症月別届出状況 1 月 2 月 3 月 4 月 5 月 6 月 7 月 8 月 9 月 10 月 11 月 12 月計 細菌性赤痢
 横浜市感染症発生状況 ( 平成 30 年第 46 週 ~ 第 50 週 ) ( : 第 50 週に診断された感染症 ) 二類感染症 ( 結核を除く ) 週別届出状況 該当なし 平成 30 年 12 月 19 日現在 三類感染症週別届出状況 46 週 47 週 48 週 49 週 50 週累計 細菌性赤痢 1 5 1 1 3 1 125 腸チフス 1 計 1 1 3 2 0 131 四類感染症週別届出状況
横浜市感染症発生状況 ( 平成 30 年第 46 週 ~ 第 50 週 ) ( : 第 50 週に診断された感染症 ) 二類感染症 ( 結核を除く ) 週別届出状況 該当なし 平成 30 年 12 月 19 日現在 三類感染症週別届出状況 46 週 47 週 48 週 49 週 50 週累計 細菌性赤痢 1 5 1 1 3 1 125 腸チフス 1 計 1 1 3 2 0 131 四類感染症週別届出状況
スライド 1
 資料 8 予防接種に係る費用負担の現状について 平成 22 年 7 月 7 日厚生労働省健康局結核感染症課 予防接種法の現行体系について 一類疾病 ジフテリア 百日せき 急性灰白髄炎 麻しん 風しん 日本脳炎 破傷風 結核 その他政令で定める疾病 ( 痘そう ) 二類疾病 インフルエンザ 定期接種 目的 疾病の発生及びまん延を予防 対象疾病 ジフテリア 百日せき 急性灰白髄炎 麻しん 風しん 日本脳炎
資料 8 予防接種に係る費用負担の現状について 平成 22 年 7 月 7 日厚生労働省健康局結核感染症課 予防接種法の現行体系について 一類疾病 ジフテリア 百日せき 急性灰白髄炎 麻しん 風しん 日本脳炎 破傷風 結核 その他政令で定める疾病 ( 痘そう ) 二類疾病 インフルエンザ 定期接種 目的 疾病の発生及びまん延を予防 対象疾病 ジフテリア 百日せき 急性灰白髄炎 麻しん 風しん 日本脳炎
豚繁殖 呼吸障害症候群生ワクチン ( シード ) 平成 24 年 3 月 13 日 ( 告示第 675 号 ) 新規追加 1 定義シードロット規格に適合した弱毒豚繁殖 呼吸障害症候群ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を凍結乾燥したワクチンである 2 製法 2.1 製造用株
 豚繁殖 呼吸障害症候群生ワクチン ( シード ) 平成 24 年 3 月 13 日 ( 告示第 675 号 ) 新規追加 1 定義シードロット規格に適合した弱毒豚繁殖 呼吸障害症候群ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を凍結乾燥したワクチンである 2 製法 2.1 製造用株 2.1.1 名称豚繁殖 呼吸障害症候群ウイルス JJ1882 株又はこれと同等と認められた株 2.1.2
豚繁殖 呼吸障害症候群生ワクチン ( シード ) 平成 24 年 3 月 13 日 ( 告示第 675 号 ) 新規追加 1 定義シードロット規格に適合した弱毒豚繁殖 呼吸障害症候群ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を凍結乾燥したワクチンである 2 製法 2.1 製造用株 2.1.1 名称豚繁殖 呼吸障害症候群ウイルス JJ1882 株又はこれと同等と認められた株 2.1.2
医師が問診 検温および診察の結果から 接種できるかどうか判断します 次の人は このワクチンの接種を受けることはできません 明らかに発熱 ( 通常 37.5 以上 ) している人 重篤な急性疾患にかかっている人 過去にこのワクチンに含まれている成分でアナフィラキシーをおこしたことがある人 上記以外に医
 ワクチン接種を受ける人へのガイド 2018 年 8 月更新 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) このワクチンの名前は? 販売名 一般名 ビームゲン注 0.25mL ビームゲン注 0.5mL Bimmugen 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) Recombinant Adsorbed Hepatitis B Vaccine (prepared from yeast) ワクチン接種を受ける人へのガイドについてワクチンの正しい理解と
ワクチン接種を受ける人へのガイド 2018 年 8 月更新 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) このワクチンの名前は? 販売名 一般名 ビームゲン注 0.25mL ビームゲン注 0.5mL Bimmugen 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) Recombinant Adsorbed Hepatitis B Vaccine (prepared from yeast) ワクチン接種を受ける人へのガイドについてワクチンの正しい理解と
法律 出典 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年 8 月 10 日法律第 145 号 ) 政令 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行令 ( 昭和 36 年 1 月 26 日政令第 11 号 ) 省令 医薬品 医療機器等の品質
 医療機器クラス分類表 ( 平成 30 年 10 月 19 日現在 ) 香川県健康福祉部薬務感染症対策課薬事指導グループ 法律 出典 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年 8 月 10 日法律第 145 号 ) 政令 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行令 ( 昭和 36 年 1 月 26 日政令第 11 号 ) 省令 医薬品
医療機器クラス分類表 ( 平成 30 年 10 月 19 日現在 ) 香川県健康福祉部薬務感染症対策課薬事指導グループ 法律 出典 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年 8 月 10 日法律第 145 号 ) 政令 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行令 ( 昭和 36 年 1 月 26 日政令第 11 号 ) 省令 医薬品
<4D F736F F F696E74202D208E9197BF375F90DA8EED94EF977082CC82A082E895FB82C982C282A282C42E B93C782DD8EE682E890EA97705D>
 資料 7 予防接種に係る費用負担の あり方について 予防接種法の現行体系について 一類疾病 ジフテリア 百日せき 急性灰白髄炎 麻しん 風しん 日本脳炎 破傷風 結核 その他政令で定める疾病 ( 痘そう ) 二類疾病インフルエンザ 定期接種 目的 疾病の発生及びまん延を予防 対象疾病 ジフテリア 百日せき 急性灰白髄炎 麻しん 風しん 目的 個人の発病又はその重症化を防止し 併せてこれによりそのまん延の予防に資する
資料 7 予防接種に係る費用負担の あり方について 予防接種法の現行体系について 一類疾病 ジフテリア 百日せき 急性灰白髄炎 麻しん 風しん 日本脳炎 破傷風 結核 その他政令で定める疾病 ( 痘そう ) 二類疾病インフルエンザ 定期接種 目的 疾病の発生及びまん延を予防 対象疾病 ジフテリア 百日せき 急性灰白髄炎 麻しん 風しん 目的 個人の発病又はその重症化を防止し 併せてこれによりそのまん延の予防に資する
はじめに 予防接種は感染症を予防するために最も特異的でかつ効果的な方法の一つです わが国では 1990 年代以降 新しいワクチンの導入が少なく 海外では受けられるワクチンが国内では受けることができないといった いわゆる ワクチンギャップ が問題になっていました しかし 近年の予防接種法の改正により
 接種前の確認がとても大切です (2016 年改訂版 ) はじめに 予防接種は感染症を予防するために最も特異的でかつ効果的な方法の一つです わが国では 1990 年代以降 新しいワクチンの導入が少なく 海外では受けられるワクチンが国内では受けることができないといった いわゆる ワクチンギャップ が問題になっていました しかし 近年の予防接種法の改正により 2013 年 4 月 2014 年 10 月
接種前の確認がとても大切です (2016 年改訂版 ) はじめに 予防接種は感染症を予防するために最も特異的でかつ効果的な方法の一つです わが国では 1990 年代以降 新しいワクチンの導入が少なく 海外では受けられるワクチンが国内では受けることができないといった いわゆる ワクチンギャップ が問題になっていました しかし 近年の予防接種法の改正により 2013 年 4 月 2014 年 10 月
卸-11-2.indd
 Q ①国家備蓄に関し およそこの10年 緊急にワク No.1450 コレラワクチンの販売中止について 2009年10月 チンを接種したケースがない ②現在のコレラの治療方針について 基本的には 経口または点滴で水分と電解質を補い 並行し て抗生物質による抗菌治療を実施するとされて コレラワクチンは コレラ菌による急性感染性 おり 以上の併用治療により 大体死亡率は 腸炎であるコレラの予防に用いるもので
Q ①国家備蓄に関し およそこの10年 緊急にワク No.1450 コレラワクチンの販売中止について 2009年10月 チンを接種したケースがない ②現在のコレラの治療方針について 基本的には 経口または点滴で水分と電解質を補い 並行し て抗生物質による抗菌治療を実施するとされて コレラワクチンは コレラ菌による急性感染性 おり 以上の併用治療により 大体死亡率は 腸炎であるコレラの予防に用いるもので
本日 お話しすること 予防接種行政の振り返り 平成 25 年予防接種法改正が目指したもの 現在の取り組み 今後の取り組み
 昨今の予防接種行政の課題 厚生労働省健康局健康課予防接種室予防接種評価分析専門官辰巳秀爾 1 本日 お話しすること 予防接種行政の振り返り 平成 25 年予防接種法改正が目指したもの 現在の取り組み 今後の取り組み 予防接種制度と社会状況の変化 昭和 23 年 (1948) 昭和 51 年 (1976) 平成 6 年 (1994) 平成 13 年 (2001) 平成 23 年 (2011) 平成 25
昨今の予防接種行政の課題 厚生労働省健康局健康課予防接種室予防接種評価分析専門官辰巳秀爾 1 本日 お話しすること 予防接種行政の振り返り 平成 25 年予防接種法改正が目指したもの 現在の取り組み 今後の取り組み 予防接種制度と社会状況の変化 昭和 23 年 (1948) 昭和 51 年 (1976) 平成 6 年 (1994) 平成 13 年 (2001) 平成 23 年 (2011) 平成 25
Taro-kv12250.jtd
 ニューカッスル病 マレック病 ( ニューカッスル病ウイルス由来 F 蛋白遺伝子導入マレック病ウイルス 1 型 ) 凍結生ワクチン 平成 22 年 8 月 12 日 ( 告示第 2288 号 ) 新規追加 ニューカッスル病ウイルスのF 蛋白をコードする遺伝子を弱毒マレック病ウイルス (1 型 ) に挿入して得られた組換え体ウイルスを培養細胞で増殖させて得た感染細胞浮遊液を凍結したワクチンである 1 小分製品の試験
ニューカッスル病 マレック病 ( ニューカッスル病ウイルス由来 F 蛋白遺伝子導入マレック病ウイルス 1 型 ) 凍結生ワクチン 平成 22 年 8 月 12 日 ( 告示第 2288 号 ) 新規追加 ニューカッスル病ウイルスのF 蛋白をコードする遺伝子を弱毒マレック病ウイルス (1 型 ) に挿入して得られた組換え体ウイルスを培養細胞で増殖させて得た感染細胞浮遊液を凍結したワクチンである 1 小分製品の試験
2018ワクチンの基礎_H1-H4
 28 ( 平成 3 年 ) ワクチンの基礎 ワクチン類の製造から流通まで 一般社団法人 日本ワクチン産業協会 はじめに ワクチン類の製造は 通常病原微生物等を原材料として行われるため その製造には他の医療用医薬品とは異なる特別な技術 設備を必要とし 十分に教育訓練された従事者によって行われている また 製品の保管や取扱いもそれぞれの製品により異なるため 細心の注意のもとに管理されている ワクチン類の大部分は感染症の予防に使用されるが
28 ( 平成 3 年 ) ワクチンの基礎 ワクチン類の製造から流通まで 一般社団法人 日本ワクチン産業協会 はじめに ワクチン類の製造は 通常病原微生物等を原材料として行われるため その製造には他の医療用医薬品とは異なる特別な技術 設備を必要とし 十分に教育訓練された従事者によって行われている また 製品の保管や取扱いもそれぞれの製品により異なるため 細心の注意のもとに管理されている ワクチン類の大部分は感染症の予防に使用されるが
平成 24 年 7 月改定版 すべての予防接種につきましては 次のページに記載してあります 平成 24 年度予防接種日程表 ( 国の通知により 内容が変わる場合があります 毎月の 広報みなみちた でご確認ください 新 麻しん風しん混合 3 期 4 期 ( 個別 ) 対象 :3 期 ( 中学 1 年生
 平成 24 年 7 月改定版 すべての予防接種につきましては 次のページに記載してあります 平成 24 年度予防接種日程表 ( 国の通知により 内容が変わる場合があります 毎月の 広報みなみちた でご確認ください 麻しん風しん混合 3 期 4 期 ( 個別 ) 対象 :3 期 ( 中学 1 年生 ) 4 期 ( 高校 3 年生 ) H24 年度より町内契約医療機関で個別接種となります 予約制 任意子宮頸がん
平成 24 年 7 月改定版 すべての予防接種につきましては 次のページに記載してあります 平成 24 年度予防接種日程表 ( 国の通知により 内容が変わる場合があります 毎月の 広報みなみちた でご確認ください 麻しん風しん混合 3 期 4 期 ( 個別 ) 対象 :3 期 ( 中学 1 年生 ) 4 期 ( 高校 3 年生 ) H24 年度より町内契約医療機関で個別接種となります 予約制 任意子宮頸がん
感染症対策・予防接種行政の 最近の動向について
 予防接種行政の 最近の動向について 厚生労働省健康局結核感染症課長正林督章 予防接種法改正の経緯 (1) 昭和 23 年 : 予防接種法の制定 - 痘そう *1 ジフテリア *1 腸チフス *1 パラチフス *1 百日せき *1 結核 *1 *2 発疹チフス ペスト コレラ しょう紅熱 インフルエンザ ワイル病の 12 疾患を対象 - 接種対象者を定めた定期の予防接種と 公衆衛生上の必要性に応じて行う臨時の予防接種
予防接種行政の 最近の動向について 厚生労働省健康局結核感染症課長正林督章 予防接種法改正の経緯 (1) 昭和 23 年 : 予防接種法の制定 - 痘そう *1 ジフテリア *1 腸チフス *1 パラチフス *1 百日せき *1 結核 *1 *2 発疹チフス ペスト コレラ しょう紅熱 インフルエンザ ワイル病の 12 疾患を対象 - 接種対象者を定めた定期の予防接種と 公衆衛生上の必要性に応じて行う臨時の予防接種
VACCINE PART.2 VACCINE PART.2 VACCINE PART.2 VACCINE PART.2 VACCINE 第 1 章 その魔力は薬か毒か ワクチンの効果を高める目的で添加されている補助剤がです しかし よいことだけではありません とはいったいどのようなもので ワクチンの
 PART.2 特集 VACCINE PART.2 VACCINE PART.2 VACCINE PART.2 VACCINE PART.2 ワクチン PART. 2 ワクチンに添加される物質 の正体と HPV ワクチン 特集 浜六郎 を 徹底解剖する 第 1 章 その魔力は薬か毒か 48 第 2 章とくに HPV ワクチンのについて 51 第 3 章病 56 ( はまろくろう : 内科医 本誌編集委員
PART.2 特集 VACCINE PART.2 VACCINE PART.2 VACCINE PART.2 VACCINE PART.2 ワクチン PART. 2 ワクチンに添加される物質 の正体と HPV ワクチン 特集 浜六郎 を 徹底解剖する 第 1 章 その魔力は薬か毒か 48 第 2 章とくに HPV ワクチンのについて 51 第 3 章病 56 ( はまろくろう : 内科医 本誌編集委員
48小児感染_一般演題リスト160909
 10000 E-1-13 11/19( 土 ) 13:00~14:00 E 会場一般演題 ( 口演 ) マイコプラズマ 1 10001 D-1-7 11/19( 土 ) 10:00~11:10 D 会場一般演題 ( 口演 ) インフルエンザ 1 10002 D-1-8 11/19( 土 ) 10:00~11:10 D 会場一般演題 ( 口演 ) インフルエンザ 1 10003 D-1-9 11/19(
10000 E-1-13 11/19( 土 ) 13:00~14:00 E 会場一般演題 ( 口演 ) マイコプラズマ 1 10001 D-1-7 11/19( 土 ) 10:00~11:10 D 会場一般演題 ( 口演 ) インフルエンザ 1 10002 D-1-8 11/19( 土 ) 10:00~11:10 D 会場一般演題 ( 口演 ) インフルエンザ 1 10003 D-1-9 11/19(
アレルギー疾患対策基本法 ( 平成二十六年六月二十七日法律第九十八号 ) 最終改正 : 平成二六年六月一三日法律第六七号 第一章総則 ( 第一条 第十条 ) 第二章アレルギー疾患対策基本指針等 ( 第十一条 第十三条 ) 第三章基本的施策第一節アレルギー疾患の重症化の予防及び症状の軽減 ( 第十四条
 アレルギー疾患対策基本法 ( 平成二十六年六月二十七日法律第九十八号 ) 最終改正 : 平成二六年六月一三日法律第六七号 第一章総則 ( 第一条 第十条 ) 第二章アレルギー疾患対策基本指針等 ( 第十一条 第十三条 ) 第三章基本的施策第一節アレルギー疾患の重症化の予防及び症状の軽減 ( 第十四条 第十五条 ) 第二節アレルギー疾患医療の均てん化の促進等 ( 第十六条 第十七条 ) 第三節アレルギー疾患を有する者の生活の質の維持向上
アレルギー疾患対策基本法 ( 平成二十六年六月二十七日法律第九十八号 ) 最終改正 : 平成二六年六月一三日法律第六七号 第一章総則 ( 第一条 第十条 ) 第二章アレルギー疾患対策基本指針等 ( 第十一条 第十三条 ) 第三章基本的施策第一節アレルギー疾患の重症化の予防及び症状の軽減 ( 第十四条 第十五条 ) 第二節アレルギー疾患医療の均てん化の促進等 ( 第十六条 第十七条 ) 第三節アレルギー疾患を有する者の生活の質の維持向上
Microsoft Word - ※set※報道発表資料(案)弁明込み
 Press Release 平成 28 年 10 月 4 日 照会先 医薬 生活衛生局監視指導 麻薬対策課課長伊澤知法 ( 内線 2759) 課長補佐江野英夫 ( 内線 2763) ( 代表電話 ) 03(5253)1111 ( 直通電話 ) 03(3595)2436 医薬 生活衛生局医薬品審査管理課 課長山田雅信 ( 内線 2733) 課長補佐清原宏眞 ( 内線 2746) ( 代表電話 ) 03(5253)1111
Press Release 平成 28 年 10 月 4 日 照会先 医薬 生活衛生局監視指導 麻薬対策課課長伊澤知法 ( 内線 2759) 課長補佐江野英夫 ( 内線 2763) ( 代表電話 ) 03(5253)1111 ( 直通電話 ) 03(3595)2436 医薬 生活衛生局医薬品審査管理課 課長山田雅信 ( 内線 2733) 課長補佐清原宏眞 ( 内線 2746) ( 代表電話 ) 03(5253)1111
<89FC B9E93738E7382B182DD292E786C7378>
 京都府感染症情報センター 全数報告 1 ページ / 12 全数報告感染症の疾病 保健所別の報告数 ( 総数 ) 感染症分類 1 類 2 類 3 類 4 類 エボラ出血熱 クリミア コンゴ出血熱 痘そう 米出血熱 ペスト マールブルグ病 ラッサ熱 急性灰白髄炎 結核 ジフテリア 重症急性呼吸器症候群 * 1 中東呼吸器症候群 * 2 鳥インフ鳥インフルエンザルエンザ (H5N1) (H7N9) 京都市
京都府感染症情報センター 全数報告 1 ページ / 12 全数報告感染症の疾病 保健所別の報告数 ( 総数 ) 感染症分類 1 類 2 類 3 類 4 類 エボラ出血熱 クリミア コンゴ出血熱 痘そう 米出血熱 ペスト マールブルグ病 ラッサ熱 急性灰白髄炎 結核 ジフテリア 重症急性呼吸器症候群 * 1 中東呼吸器症候群 * 2 鳥インフ鳥インフルエンザルエンザ (H5N1) (H7N9) 京都市
はじめて医療機器を製造販売または製造される方へ
 を製造 ( 輸入 ) 販売するには 国内で必要な許可等について を製造販売 製造 ( 輸入 ) するためには 医薬品 等の品質 有効性及び安全性の確保等に関する法律 ( 以下 薬機法という ) の許可等 ( 製造販売業許可 製造業登録 ) が必要になります 製品を市場に出荷するために必要な許可 販売する製品に対して最終責製造販売業任を持ち 自社の名前で市場へ出荷する この許可では製造することはできません
を製造 ( 輸入 ) 販売するには 国内で必要な許可等について を製造販売 製造 ( 輸入 ) するためには 医薬品 等の品質 有効性及び安全性の確保等に関する法律 ( 以下 薬機法という ) の許可等 ( 製造販売業許可 製造業登録 ) が必要になります 製品を市場に出荷するために必要な許可 販売する製品に対して最終責製造販売業任を持ち 自社の名前で市場へ出荷する この許可では製造することはできません
<89FC89FC B9E93738E7382B182DD292E786C7378>
 京都府感染症情報センター 全数報告 1 ページ / 12 全数報告感染症の疾病 保健所別の報告数 累積報告数 ( 総数 ) 1 類 2 類 3 類 4 類 エボラ出血熱 クリミア コンゴ出血熱 痘そう 米出血熱 ペスト マールブルグ病 ラッサ熱 急性灰白髄炎 結核 ジフテリア 重症急性呼吸器症候群 * 1 中東呼吸器症候群 * 2 (H5N 1) (H7N 9) コレラ 細菌性赤痢 腸管出血性大腸菌感染症
京都府感染症情報センター 全数報告 1 ページ / 12 全数報告感染症の疾病 保健所別の報告数 累積報告数 ( 総数 ) 1 類 2 類 3 類 4 類 エボラ出血熱 クリミア コンゴ出血熱 痘そう 米出血熱 ペスト マールブルグ病 ラッサ熱 急性灰白髄炎 結核 ジフテリア 重症急性呼吸器症候群 * 1 中東呼吸器症候群 * 2 (H5N 1) (H7N 9) コレラ 細菌性赤痢 腸管出血性大腸菌感染症
<89FC89FC B9E93738E7382B182DD292E786C7378>
 京都府感染症情報センター 全数報告 1 ページ / 12 全数報告感染症の疾病 保健所別の報告数 累積報告数 ( 総数 ) 1 類 2 類 3 類 4 類 エボラ出血熱 クリミア コンゴ出血熱 痘そう 米出血熱 ペスト マールブルグ病 ラッサ熱 急性灰白髄炎 結核 ジフテリア 重症急性呼吸器症候群 * 1 中東呼吸器症候群 * 2 (H5N 1) (H7N 9) コレラ 細菌性赤痢 腸管出血性大腸菌感染症
京都府感染症情報センター 全数報告 1 ページ / 12 全数報告感染症の疾病 保健所別の報告数 累積報告数 ( 総数 ) 1 類 2 類 3 類 4 類 エボラ出血熱 クリミア コンゴ出血熱 痘そう 米出血熱 ペスト マールブルグ病 ラッサ熱 急性灰白髄炎 結核 ジフテリア 重症急性呼吸器症候群 * 1 中東呼吸器症候群 * 2 (H5N 1) (H7N 9) コレラ 細菌性赤痢 腸管出血性大腸菌感染症
<89FC89FC B9E93738E7382B182DD292E786C7378>
 京都府感染症情報センター 全数報告 1 ページ / 12 全数報告感染症の疾病 保健所別の報告数 累積報告数 ( 総数 ) 1 類 2 類 3 類 4 類 エボラ出血熱 クリミア コンゴ出血熱 痘そう 米出血熱 ペスト マールブルグ病 ラッサ熱 急性灰白髄炎 結核 ジフテリア 重症急性呼吸器症候群 * 1 中東呼吸器症候群 * 2 (H5N 1) (H7N 9) コレラ 細菌性赤痢 腸管出血性大腸菌感染症
京都府感染症情報センター 全数報告 1 ページ / 12 全数報告感染症の疾病 保健所別の報告数 累積報告数 ( 総数 ) 1 類 2 類 3 類 4 類 エボラ出血熱 クリミア コンゴ出血熱 痘そう 米出血熱 ペスト マールブルグ病 ラッサ熱 急性灰白髄炎 結核 ジフテリア 重症急性呼吸器症候群 * 1 中東呼吸器症候群 * 2 (H5N 1) (H7N 9) コレラ 細菌性赤痢 腸管出血性大腸菌感染症
審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ]
![審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ] 審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ]](/thumbs/91/105024304.jpg) 審査報告書 平成 26 年 2 月 7 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所
審査報告書 平成 26 年 2 月 7 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所
出典 : 一般社団法人日本ワクチン産業協会 ( 予防接種に関する Q& 集 Q4 ついて不活化ワクチンは 大量に培養されたウイルスや細菌からウイルス粒子や細菌の菌体を集めて精製した後 ホルマリン等の薬剤を用いて処理し 病原体の活力を失わせて不活化し
 ワクチン類全般について46 出典 : 一般社団法人日本ワクチン産業協会 (http://www.wakutin.or.jp/) 予防接種に関する Q& 集 2 Q 1 ワクチン類全般について トキソイドとワクチンならびに抗毒素の違いを教えてください Q Q 2 3 トキソイドとは病原体が増殖する過程で産生される毒素 ( トキシン ) をホルマリンで処理し免疫 原性を失わせず無毒化したもので 成人用沈降ジフテリアトキソイド
ワクチン類全般について46 出典 : 一般社団法人日本ワクチン産業協会 (http://www.wakutin.or.jp/) 予防接種に関する Q& 集 2 Q 1 ワクチン類全般について トキソイドとワクチンならびに抗毒素の違いを教えてください Q Q 2 3 トキソイドとは病原体が増殖する過程で産生される毒素 ( トキシン ) をホルマリンで処理し免疫 原性を失わせず無毒化したもので 成人用沈降ジフテリアトキソイド
1
 健康づくり課 健康づくり課業務概要 1 特定健康診査 特定保健指導の実施生活習慣病の予防に重点を置いた取り組みが重要課題となるため 内臓脂肪型肥満に着目した 特定健康診査 を行い 健診結果によりメタボリックシンドローム該当者 予備群を選定し 特定保健指導 を行った 2 胃がん検診 40 歳以上の市民を対象に胃がんの早期発見の推進を図ることにより がんの死亡率を減少させることを目的として実施した 3
健康づくり課 健康づくり課業務概要 1 特定健康診査 特定保健指導の実施生活習慣病の予防に重点を置いた取り組みが重要課題となるため 内臓脂肪型肥満に着目した 特定健康診査 を行い 健診結果によりメタボリックシンドローム該当者 予備群を選定し 特定保健指導 を行った 2 胃がん検診 40 歳以上の市民を対象に胃がんの早期発見の推進を図ることにより がんの死亡率を減少させることを目的として実施した 3
<4D F736F F D208D B B835896F2938A975E82CC8D6C82A695FB2E646F63>
 事務連絡平成 21 年 5 月 28 日 都道府県 各 保健所設置市 衛生主管部 ( 局 ) 特別区 感染症対策担当者及び新型インフルエンザ対策担当者殿 厚生労働省新型インフルエンザ対策推進本部事務局 新型インフルエンザの診療等に関する情報 ( 抗インフルエンザ薬の予防投与の考え方等 ) に係る Q&A の送付について 平成 21 年 5 月 3 日付新型インフルエンザ対策推進本部事務連絡 新型インフルエンザの診療等に関する情報
事務連絡平成 21 年 5 月 28 日 都道府県 各 保健所設置市 衛生主管部 ( 局 ) 特別区 感染症対策担当者及び新型インフルエンザ対策担当者殿 厚生労働省新型インフルエンザ対策推進本部事務局 新型インフルエンザの診療等に関する情報 ( 抗インフルエンザ薬の予防投与の考え方等 ) に係る Q&A の送付について 平成 21 年 5 月 3 日付新型インフルエンザ対策推進本部事務連絡 新型インフルエンザの診療等に関する情報
【資料1】結核対策について
 資料 結核対策について 平成 6 年 7 月厚生労働省健康局結核感染症課 結核対策について 経緯 今般 厚生科学審議会感染症部会において 感染症法の関連法令について 医学医療の進歩の推移 国際交流の進展等を勘案しつつ感染症の範囲及びその類型の見直し等所要の事項に関して見直しの検討がなされ 感染症対策の見直しについて がとりまとめられたところ 結核対策についても 所要の事項に関して 同様に見直しの検討を行う必要がある
資料 結核対策について 平成 6 年 7 月厚生労働省健康局結核感染症課 結核対策について 経緯 今般 厚生科学審議会感染症部会において 感染症法の関連法令について 医学医療の進歩の推移 国際交流の進展等を勘案しつつ感染症の範囲及びその類型の見直し等所要の事項に関して見直しの検討がなされ 感染症対策の見直しについて がとりまとめられたところ 結核対策についても 所要の事項に関して 同様に見直しの検討を行う必要がある
3-2 全国と札幌市の定点あたり患者報告数の年平均値流行状況の年次推移を 全国的な状況と比較するため 全国と札幌市の定点あたり患者報告数の年平均値について解析した ( 図 2) 全国的には 調査期間の定点あたり患者報告数の年平均値は その年次推移にやや増減があるものの大きな変動は認められなかった 札
 札幌市衛研年報 41, 37-41 (2014) 札幌市における水痘の流行状況について 扇谷陽子花井潤師宮田淳 要旨水痘の感染予防の注意喚起に活用することを目的として 感染症発生動向調査で得られたデータを用いて 1999 年 ~2012 年の札幌市における水痘の流行状況を解析した この結果 札幌市では 例年初夏と冬季に患者報告数が増加すること 定点あたり患者報告数の年平均値が全国的な状況よりやや高い傾向にあること
札幌市衛研年報 41, 37-41 (2014) 札幌市における水痘の流行状況について 扇谷陽子花井潤師宮田淳 要旨水痘の感染予防の注意喚起に活用することを目的として 感染症発生動向調査で得られたデータを用いて 1999 年 ~2012 年の札幌市における水痘の流行状況を解析した この結果 札幌市では 例年初夏と冬季に患者報告数が増加すること 定点あたり患者報告数の年平均値が全国的な状況よりやや高い傾向にあること
感染症対策
 利用規約 提供している資料は 同じ会社内 施設内での研修 や 高校生 大学生のプレゼンテーション参考資料 市民向けの教材をボランティアで作成するため などを想定しています つまり 当サイトの資料の利用は 教育に対して 無償で貢献するために使用すること が大前提です そのため 社外や施設外の研修にこのサイトの資料を利用することは基本的にできません 例えば 製薬企業や医薬品卸が医療機関へ行う得意先研修としての利用は禁止します
利用規約 提供している資料は 同じ会社内 施設内での研修 や 高校生 大学生のプレゼンテーション参考資料 市民向けの教材をボランティアで作成するため などを想定しています つまり 当サイトの資料の利用は 教育に対して 無償で貢献するために使用すること が大前提です そのため 社外や施設外の研修にこのサイトの資料を利用することは基本的にできません 例えば 製薬企業や医薬品卸が医療機関へ行う得意先研修としての利用は禁止します
スライド 1
 資料 3 不活化ポリオワクチンの円滑な導入に関する検討会第 3 回会議 ポリオワクチン互換性についての諸外国におけるデータ 2012 年 4 月 23 日 ( 月 ) 中野貴司 ( 川崎医科大学小児科 ) ワクチンの互換性 Interchangeability of vaccines 同一疾患を予防するワクチン製剤の種類が増え また多価混合ワクチンが普及すると 対象者が過去に接種したものと同じ製剤が入手できなかったり
資料 3 不活化ポリオワクチンの円滑な導入に関する検討会第 3 回会議 ポリオワクチン互換性についての諸外国におけるデータ 2012 年 4 月 23 日 ( 月 ) 中野貴司 ( 川崎医科大学小児科 ) ワクチンの互換性 Interchangeability of vaccines 同一疾患を予防するワクチン製剤の種類が増え また多価混合ワクチンが普及すると 対象者が過去に接種したものと同じ製剤が入手できなかったり
02別添:日本脳炎ワクチン接種に関するQ&A[H28.3月版]
![02別添:日本脳炎ワクチン接種に関するQ&A[H28.3月版] 02別添:日本脳炎ワクチン接種に関するQ&A[H28.3月版]](/thumbs/91/105257320.jpg) 日本脳炎ワクチン接種に関する Q&A ( 平成 28 年 3 月改訂版 ) Q1 日本脳炎とは どのような病気ですか? 日本脳炎ウイルスの感染によって起こる中枢神経 ( 脳や脊髄など ) の疾患で 東アジア 南アジアにかけて広く分布しています ヒトからヒトへの感染はなく ブタなどの動物の体内でウイルスが増殖した後 そのブタを刺したコガタアカイエカ ( 水田などに発生する蚊の一種 ) などがヒトを刺すことによって感染します
日本脳炎ワクチン接種に関する Q&A ( 平成 28 年 3 月改訂版 ) Q1 日本脳炎とは どのような病気ですか? 日本脳炎ウイルスの感染によって起こる中枢神経 ( 脳や脊髄など ) の疾患で 東アジア 南アジアにかけて広く分布しています ヒトからヒトへの感染はなく ブタなどの動物の体内でウイルスが増殖した後 そのブタを刺したコガタアカイエカ ( 水田などに発生する蚊の一種 ) などがヒトを刺すことによって感染します
Microsoft PowerPoint _三重県研修会 - 配布用.pptx
 平成 29 年度第 2 回三重県感染対策支援ネットワーク研修会日時 : 平成 30 年 2 月 4 日 10:35 11 35 場所 : 三重大学医学部臨床第 3 講義室 ワクチンで防げる病気 (VPD) から医療関係者を守るには 国立感染症研究所感染症疫学センター神谷元 National Institute of Infectious Diseases Infectious Disease Surveillance
平成 29 年度第 2 回三重県感染対策支援ネットワーク研修会日時 : 平成 30 年 2 月 4 日 10:35 11 35 場所 : 三重大学医学部臨床第 3 講義室 ワクチンで防げる病気 (VPD) から医療関係者を守るには 国立感染症研究所感染症疫学センター神谷元 National Institute of Infectious Diseases Infectious Disease Surveillance
北海道における日本脳炎に係る定期の予防接種を実施することについての検討(概要)
 平成 26 年 8 月 22 日 北海道における日本脳炎に係る定期の予防接種を実施することについての検討 ( 概要 ) - 行政苦情救済推進会議の意見を踏まえたあっせん - 総務省行政評価局は 次の行政相談を受け 行政苦情救済推進会議 ( 座長 : 大森彌東京大学名誉教授 ) に諮り 同会議からの 北海道のみ日本脳炎に係る定期の予防接種が行われていないことは 国民の利便性や全国的な移動を考慮した場合
平成 26 年 8 月 22 日 北海道における日本脳炎に係る定期の予防接種を実施することについての検討 ( 概要 ) - 行政苦情救済推進会議の意見を踏まえたあっせん - 総務省行政評価局は 次の行政相談を受け 行政苦情救済推進会議 ( 座長 : 大森彌東京大学名誉教授 ) に諮り 同会議からの 北海道のみ日本脳炎に係る定期の予防接種が行われていないことは 国民の利便性や全国的な移動を考慮した場合
員長及び医薬品医療機器等法登録認証機関協議会代表幹事宛て送付するこ ととしていることを申し添えます 記 1. 基本要件基準第 13 条第 5 項及び第 6 項への適合性確認の基本的な考え方について (1)2023 年 ( 平成 35 年 )2 月 28 日 ( 以下 経過措置期間終了日 という )
 薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
Microsoft Word - 意見募集の結果
 予防接種法施行令の一部を改正する政令案に関する意見募集に対して寄せられた 御意見等について 平成 26 年 7 月 2 日 厚生労働省健康局 結核感染症課 予防接種法施行令の一部を改正する政令案について 平成 26 年 5 月 4 日から6 月 2 日までホームページ等を通じて御意見を募集しましたところ 計 5 件の御意見をいただきました お寄せいただきました御意見と それに対する当省の考え方について
予防接種法施行令の一部を改正する政令案に関する意見募集に対して寄せられた 御意見等について 平成 26 年 7 月 2 日 厚生労働省健康局 結核感染症課 予防接種法施行令の一部を改正する政令案について 平成 26 年 5 月 4 日から6 月 2 日までホームページ等を通じて御意見を募集しましたところ 計 5 件の御意見をいただきました お寄せいただきました御意見と それに対する当省の考え方について
バリデーション基準 1. 医薬品 医薬部外品 GMP 省令に規定するバリデーションについては 品質リスクを考慮し 以下の バリデーション基準 に基づいて実施すること 2. バリデーション基準 (1) バリデーションの目的バリデーションは 製造所の構造設備並びに手順 工程その他の製造管理及び品質管理の
 バリデーション基準 1. 医薬品 医薬部外品 GMP 省令に規定するバリデーションについては 品質リスクを考慮し 以下の バリデーション基準 に基づいて実施すること 2. バリデーション基準 (1) バリデーションの目的バリデーションは 製造所の構造設備並びに手順 工程その他の製造管理及び品質管理の方法 ( 以下この基準において 製造手順等 という ) が期待される結果を与えることを検証し これを文書とすることによって
バリデーション基準 1. 医薬品 医薬部外品 GMP 省令に規定するバリデーションについては 品質リスクを考慮し 以下の バリデーション基準 に基づいて実施すること 2. バリデーション基準 (1) バリデーションの目的バリデーションは 製造所の構造設備並びに手順 工程その他の製造管理及び品質管理の方法 ( 以下この基準において 製造手順等 という ) が期待される結果を与えることを検証し これを文書とすることによって
審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果
![審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果 審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果](/thumbs/92/108604766.jpg) 審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
薬事法における病院及び医師に対する主な規制について 特定生物由来製品に係る説明 ( 法第 68 条の 7 平成 14 年改正 ) 特定生物由来製品の特性を踏まえ 製剤のリスクとベネフィットについて患者に説明を行い 理解を得るように努めることを これを取り扱う医師等の医療関係者に義務づけたもの ( 特
 薬事法における病院及び医師に対する主な規制について 情報の提供等 ( 法第 77 条の 3 第 2 項及び第 3 項 第 2 項 : 昭和 54 年改正 第 3 項 : 平成 6 年改正 ) 医薬品の製造販売業者等が行う医薬品又は医療機器の適正な使用のために必要な情報の収集に協力するよう努めることを また 医薬品及び医療機器の適正な使用を確保するため 医薬品の製造販売業者等から提供される情報の活用その他必要な情報の収集
薬事法における病院及び医師に対する主な規制について 情報の提供等 ( 法第 77 条の 3 第 2 項及び第 3 項 第 2 項 : 昭和 54 年改正 第 3 項 : 平成 6 年改正 ) 医薬品の製造販売業者等が行う医薬品又は医療機器の適正な使用のために必要な情報の収集に協力するよう努めることを また 医薬品及び医療機器の適正な使用を確保するため 医薬品の製造販売業者等から提供される情報の活用その他必要な情報の収集
Microsoft Word - 【案1】登録認証機関立入要領改正通知(Ver )
 薬食機参発 1121 第 38 号平成 26 年 11 月 21 日 各登録認証機関の長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) 登録認証機関等に対する立入検査の実施要領の改正について 薬事法 ( 昭和 35 年法律第 145 号 ) の規定による登録認証機関等に対する立入 検査の実施要領については 登録認証機関等に対する立入検査の実施要領について ( 平成 18
薬食機参発 1121 第 38 号平成 26 年 11 月 21 日 各登録認証機関の長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) 登録認証機関等に対する立入検査の実施要領の改正について 薬事法 ( 昭和 35 年法律第 145 号 ) の規定による登録認証機関等に対する立入 検査の実施要領については 登録認証機関等に対する立入検査の実施要領について ( 平成 18
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社
 オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
スライド 1
 2010 年 10 月 4 日愛知感染予防ネットワーク講演会 こどもの感染予防 ー感染症に罹らないためには 罹ったらどうする? ー 一社アレルギー科 こどもクリニック副院長 小児科アレルギー専門医 鳥居明子 予防接種の基礎知識 定期接種 ( 無料 ) 黒字任意接種 ( 有料 ) 赤字 生ワクチン 異なる種類の ワクチン間に限ります ポリオ MR 麻しん 風しん BCG 水痘 おたふくかぜ 不活化ワクチン
2010 年 10 月 4 日愛知感染予防ネットワーク講演会 こどもの感染予防 ー感染症に罹らないためには 罹ったらどうする? ー 一社アレルギー科 こどもクリニック副院長 小児科アレルギー専門医 鳥居明子 予防接種の基礎知識 定期接種 ( 無料 ) 黒字任意接種 ( 有料 ) 赤字 生ワクチン 異なる種類の ワクチン間に限ります ポリオ MR 麻しん 風しん BCG 水痘 おたふくかぜ 不活化ワクチン
報告風しん
 平成 30 年度宮崎県感染症対策審議会 < 報告事項 > 〇 風しん対策について 風しん対策について 1 風しんについて発熱 発疹 リンパ節腫脹を特徴とし 感染力が強く くしゃみや咳のしぶきなどで感染する 症状は無症状 ~ 重篤な合併症併発まで幅広いが 一般的には症状は軽く 数日で治る 但し 風しんに対する免疫力が不十分な女性が妊娠初期 ( 妊娠 20 週頃まで ) に感染すると 出生児が先天性風しん症候群
平成 30 年度宮崎県感染症対策審議会 < 報告事項 > 〇 風しん対策について 風しん対策について 1 風しんについて発熱 発疹 リンパ節腫脹を特徴とし 感染力が強く くしゃみや咳のしぶきなどで感染する 症状は無症状 ~ 重篤な合併症併発まで幅広いが 一般的には症状は軽く 数日で治る 但し 風しんに対する免疫力が不十分な女性が妊娠初期 ( 妊娠 20 週頃まで ) に感染すると 出生児が先天性風しん症候群
バイオ医薬品は生物を用いて製造されます 通常 細菌や動物細胞などの生体の中で目的とするタンパク質を産生させます バイオ医薬品の特性は製造プロセスの状態に依存するところが大きく しばしば プロセスが製品 と喩えられます 事実 製造プロセスにおける小さな変更でも 最終製品の違いにつながる可能性があります
 バイオ医薬品とバイオシミラー ( バイオ後続品 ) に関する Q&A 1. バイオテクノロジーとは そしてバイオ医薬品の役割とはどのようなものでしょうか? バイオテクノロジーとは 製品やサービスを生み出するために生物やその一部による修飾を用いた一連の方法やプロセスです 1970 年代のいわゆる 組換えDNA 技術 の発展 展開により 分子レベル でのバイオテクノロジーという新たな時代が幕を開け 様々な分野で知識革命を引き起こしました
バイオ医薬品とバイオシミラー ( バイオ後続品 ) に関する Q&A 1. バイオテクノロジーとは そしてバイオ医薬品の役割とはどのようなものでしょうか? バイオテクノロジーとは 製品やサービスを生み出するために生物やその一部による修飾を用いた一連の方法やプロセスです 1970 年代のいわゆる 組換えDNA 技術 の発展 展開により 分子レベル でのバイオテクノロジーという新たな時代が幕を開け 様々な分野で知識革命を引き起こしました
0 歳 0カ月 乳幼児の予防接種スケジュール ( 例 : その 1) 同時接種を希望するが 1 回に受ける数は 2 種類以下を希望する場合 ( 受診回数 : インフルエンザを除いて 18 回 ) 1 歳 カ月 日本小児科学会推奨案 ジフテリア 百日咳 破傷風混合ワクチン生ワクチン別の種類のワクチンを
 注 1) 本スケジュール案は 20 年現在 接種可能な主なワクチンをすべて受けると仮定して 1 例を示したものです 接種の順番や受けるワクチンの種類については お子様の体調や周りの感染症発生状況によって 異なってきます 詳しくはかかりつけの小児科医 保健所等でご相談ください 注 2) 接種に際しては次の決まりがあります スケジュールを立てるときの参考にしてください 別の種類のワクチンを接種する場合は
注 1) 本スケジュール案は 20 年現在 接種可能な主なワクチンをすべて受けると仮定して 1 例を示したものです 接種の順番や受けるワクチンの種類については お子様の体調や周りの感染症発生状況によって 異なってきます 詳しくはかかりつけの小児科医 保健所等でご相談ください 注 2) 接種に際しては次の決まりがあります スケジュールを立てるときの参考にしてください 別の種類のワクチンを接種する場合は
スライド 1
 1. 感染症サーベイランスとは 感染症の流行を早期発見するため 感染症の発生状況を把握し 得られた情報を解析し 国民が疾病に罹患しないために還元 活用するもの 国内での感染症の発生 流行 発生した患者の情報 ( 患者発生サーベイランス ) 原因となる病原体の情報 ( 病原体サーベイランス ) 国民の抵抗力 ( 免疫 ) の情報 ( 流行予測調査 ) 通常と異なる感染症の発生 医療機関 都道府県政令市等
1. 感染症サーベイランスとは 感染症の流行を早期発見するため 感染症の発生状況を把握し 得られた情報を解析し 国民が疾病に罹患しないために還元 活用するもの 国内での感染症の発生 流行 発生した患者の情報 ( 患者発生サーベイランス ) 原因となる病原体の情報 ( 病原体サーベイランス ) 国民の抵抗力 ( 免疫 ) の情報 ( 流行予測調査 ) 通常と異なる感染症の発生 医療機関 都道府県政令市等
Taro-再製造単回使用医療機器基準
 厚生労働省告示第二百六十一号医薬品医療機器等の品質有効性及び安全性の確保等に関する法律 ( 昭和三十五年法律第百四十 五号 ) 第四十二条第二項の規定に基づき再製造単回使用医療機器基準を次のように定め平成二十 九年七月三十一日から適用す る平成二十九年七月三十一日厚生労働大臣塩崎恭久再製造単回使用医療機器基準第 1 定義 1 再生部品 とは 医療機関において使用された単回使用の医療機器の全部又は一部であって
厚生労働省告示第二百六十一号医薬品医療機器等の品質有効性及び安全性の確保等に関する法律 ( 昭和三十五年法律第百四十 五号 ) 第四十二条第二項の規定に基づき再製造単回使用医療機器基準を次のように定め平成二十 九年七月三十一日から適用す る平成二十九年七月三十一日厚生労働大臣塩崎恭久再製造単回使用医療機器基準第 1 定義 1 再生部品 とは 医療機関において使用された単回使用の医療機器の全部又は一部であって
Research 2 Vol.81, No.12013
 2 5 22 25 4 8 8 9 9 9 10 10 11 12 14 14 15 7 18 16 18 19 20 21 16 17 17 28 19 21 1 Research 2 Vol.81, No.12013 Vol.81, No.12013 3 P r o d u c t s 4 Vol.81, No.12013 Research Vol.81, No.12013 5 6 Vol.81,
2 5 22 25 4 8 8 9 9 9 10 10 11 12 14 14 15 7 18 16 18 19 20 21 16 17 17 28 19 21 1 Research 2 Vol.81, No.12013 Vol.81, No.12013 3 P r o d u c t s 4 Vol.81, No.12013 Research Vol.81, No.12013 5 6 Vol.81,
Microsoft Word - ①【修正】B型肝炎 ワクチンにおける副反応の報告基準について
 資料 1 B 型肝炎ワクチンの副反応報告基準について 予防接種法における副反応報告制度について 制度の趣旨副反応報告制度は 予防接種後に生じる種々の身体的反応や副反応が疑われる症状等について情報を収集し ワクチンの安全性について管理 検討を行うことで 広く国民に情報を提供すること及び今後の予防接種行政の推進に資することを目的としている 報告の義務 予防接種法第 12 条 1 項 ( 参考資料 1)
資料 1 B 型肝炎ワクチンの副反応報告基準について 予防接種法における副反応報告制度について 制度の趣旨副反応報告制度は 予防接種後に生じる種々の身体的反応や副反応が疑われる症状等について情報を収集し ワクチンの安全性について管理 検討を行うことで 広く国民に情報を提供すること及び今後の予防接種行政の推進に資することを目的としている 報告の義務 予防接種法第 12 条 1 項 ( 参考資料 1)
次の人は このワクチンの接種を受けることはできません 明らかに発熱 ( 通常 37.5 以上 ) している人 重篤な急性疾患にかかっている人 過去にこのワクチンに含まれている成分 ( ジフテリアトキソイドを含む ) でアナフィラキシーをおこしたことがある人 上記以外に医師が予防接種を行うことが不適当
 ワクチン接種を受ける人へのガイド 2018 年 4 月更新 4 価髄膜炎菌ワクチン ( ジフテリアトキソイド結合体 ) このワクチンの名前は? 販売名 一般名 メナクトラ筋注 Menactra intramuscular injection 4 価髄膜炎菌ワクチン ( ジフテリアトキソイド結合体 ) Tetravalent meningococcal vaccine (Diphtheria toxoid
ワクチン接種を受ける人へのガイド 2018 年 4 月更新 4 価髄膜炎菌ワクチン ( ジフテリアトキソイド結合体 ) このワクチンの名前は? 販売名 一般名 メナクトラ筋注 Menactra intramuscular injection 4 価髄膜炎菌ワクチン ( ジフテリアトキソイド結合体 ) Tetravalent meningococcal vaccine (Diphtheria toxoid
BSL4の稼働合意について
 平成 27 年 8 月 5 日 公益社団法人日本医師会 BSL4 の稼動に対する日本医師会の見解 去る 8 月 3 日に 塩崎恭久厚生労働大臣と武蔵村山市の藤野勝市長との会談において 国立感染症研究所村山庁舎を BSL4 として稼働させることで合意したことについて 日本医師会としての見解を以下に述べる 国立感染症研究所村山庁舎においては 1981 年に一種病原体を取り扱うことのできる BSL4 施設を整備していたが
平成 27 年 8 月 5 日 公益社団法人日本医師会 BSL4 の稼動に対する日本医師会の見解 去る 8 月 3 日に 塩崎恭久厚生労働大臣と武蔵村山市の藤野勝市長との会談において 国立感染症研究所村山庁舎を BSL4 として稼働させることで合意したことについて 日本医師会としての見解を以下に述べる 国立感染症研究所村山庁舎においては 1981 年に一種病原体を取り扱うことのできる BSL4 施設を整備していたが
動物用医薬品(医薬部外品)製造販売承認事項変更承認申請書
 別記様式 1 ( 一 ) 生ウイルス + 株化細胞ワクチン 動物用医薬品製造販売承認事項変更承認申請書 ( 例 ) SL 年月日 農林水産大臣 殿 住所 氏名 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第 14 条第 9 項の規定により動物用医薬品製造販売承認事項の変更の承認を受けたいので 下記により申請します 記承認年月日及び承認番号 1 製造業者又は認定外国製造業者の氏名又は名称及び住所既承認内容を記載
別記様式 1 ( 一 ) 生ウイルス + 株化細胞ワクチン 動物用医薬品製造販売承認事項変更承認申請書 ( 例 ) SL 年月日 農林水産大臣 殿 住所 氏名 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第 14 条第 9 項の規定により動物用医薬品製造販売承認事項の変更の承認を受けたいので 下記により申請します 記承認年月日及び承認番号 1 製造業者又は認定外国製造業者の氏名又は名称及び住所既承認内容を記載
<4D F736F F F696E74202D FA967B82CC96F28E9690A C982C282A282C42E >
 日本の薬事制度について 厚生労働省 医薬食品局審査管理課中西民二 本日の内容 医薬品の製造販売 外国製造業者の認定と GMP 適合性調査 外国製造業者の認定 承認審査における GMP 適合性調査 原薬等登録原簿 (MF) 医薬品の製造販売 医薬品の製造販売に関する規制 製造販売とは 製造等製造等 ( 他に委託して製造をする場合を含む ) をし 又は輸入をした医薬品 ( 原薬たる医薬品を除く ) を
日本の薬事制度について 厚生労働省 医薬食品局審査管理課中西民二 本日の内容 医薬品の製造販売 外国製造業者の認定と GMP 適合性調査 外国製造業者の認定 承認審査における GMP 適合性調査 原薬等登録原簿 (MF) 医薬品の製造販売 医薬品の製造販売に関する規制 製造販売とは 製造等製造等 ( 他に委託して製造をする場合を含む ) をし 又は輸入をした医薬品 ( 原薬たる医薬品を除く ) を
ワクチンの研究開発促進と生産基盤確保
 資料 2-5 ワクチンの研究開発促進と生産基盤確保 海外における政策と事例 日本製薬団体連合会 杉本俊二郎 2010 年 4 月 21 日 1 - 英国の政策と事例 - 英国保健省 (Dept. of Health) がワクチンに関する政策を決定し 開発の後期に対象を絞って少額の研究資金援助を行っている 新規ワクチンの開発に関しては基本的に経済性を重視し 投資判断ができる民間製薬大手に委ねている 安定供給を確保するためには複数のメーカーの存在と
資料 2-5 ワクチンの研究開発促進と生産基盤確保 海外における政策と事例 日本製薬団体連合会 杉本俊二郎 2010 年 4 月 21 日 1 - 英国の政策と事例 - 英国保健省 (Dept. of Health) がワクチンに関する政策を決定し 開発の後期に対象を絞って少額の研究資金援助を行っている 新規ワクチンの開発に関しては基本的に経済性を重視し 投資判断ができる民間製薬大手に委ねている 安定供給を確保するためには複数のメーカーの存在と
Microsoft Word - 2-① 補償ガイドライン平成27年版(本文)Ver3.1.1.do
 1. 総則 被験者の健康被害補償に関するガイドライン Ver. 3 Ver. 3. 1 Ver. 3. 1.1 : 2 0 1 5 ( 平成 2 7 ) 年 8 月 1 8 日 : 2 0 1 5 ( 平成 2 7 ) 年 1 2 月 2 1 日 : 2 0 1 6 ( 平成 2 8 ) 年 1 2 月 2 0 日 1-1 本ガイドラインは 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年厚生省令第
1. 総則 被験者の健康被害補償に関するガイドライン Ver. 3 Ver. 3. 1 Ver. 3. 1.1 : 2 0 1 5 ( 平成 2 7 ) 年 8 月 1 8 日 : 2 0 1 5 ( 平成 2 7 ) 年 1 2 月 2 1 日 : 2 0 1 6 ( 平成 2 8 ) 年 1 2 月 2 0 日 1-1 本ガイドラインは 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年厚生省令第
健発 0622 第 5 号 平成 28 年 6 月 22 日 各都道府県知事殿 厚生労働省健康局長 ( 公印省略 ) 予防接種法第 5 条第 1 項の規定による予防接種の実施について の一部改正について 予防接種法 ( 昭和 23 年法律第 68 号 ) 第 5 条第 1 項の規定により市町村長が行
 健第 461 号平成 28 年 6 月 24 日 ( 公社 ) 岡山県医師会長 ( 一社 ) 岡山県病院協会長殿 岡山県保健福祉部長 予防接種法第 5 条第 1 項の規定による予防接種の実施について の一部改正について このことについて 厚生労働省健康局長から別添のとおり通知がありましたので 御了知いただきますようよろしくお願いします なお 各保健所 保健所支所から周知を図ることとしておりますが 貴会におかれましても
健第 461 号平成 28 年 6 月 24 日 ( 公社 ) 岡山県医師会長 ( 一社 ) 岡山県病院協会長殿 岡山県保健福祉部長 予防接種法第 5 条第 1 項の規定による予防接種の実施について の一部改正について このことについて 厚生労働省健康局長から別添のとおり通知がありましたので 御了知いただきますようよろしくお願いします なお 各保健所 保健所支所から周知を図ることとしておりますが 貴会におかれましても
<4D F736F F F696E74202D E9197BF30322D31816A95E291AB90E096BE82502E B8CDD8AB B83685D>
 第 1 回部会の補足説明 資料 2 1. インフルエンザワクチンに関する効果等の評価 2. 各種ワクチンの状況 3. 健康被害救済の事務の流れと行政不服審査の関係 4. 各国の予防接種に関する組織等について 1. インフルエンザワクチンに関する効果等の評価 季節性インフルエンザワクチンに関する科学的知見 米国 CDC( 疾病管理センター )MMWR 53(RR 6):1 40,2004 対象結果指標相対危険度
第 1 回部会の補足説明 資料 2 1. インフルエンザワクチンに関する効果等の評価 2. 各種ワクチンの状況 3. 健康被害救済の事務の流れと行政不服審査の関係 4. 各国の予防接種に関する組織等について 1. インフルエンザワクチンに関する効果等の評価 季節性インフルエンザワクチンに関する科学的知見 米国 CDC( 疾病管理センター )MMWR 53(RR 6):1 40,2004 対象結果指標相対危険度
ヘプタバックス-Ⅱワクチン接種を受ける人へのガイド
 ワクチン接種を受ける人へのガイド 2018 年 8 月更新 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) このワクチンの名前は? 販売名 一般名 ヘプタバックス-Ⅱ ヘプタバックス-Ⅱ 水性懸濁注シリンジ 0.25mL ヘプタバックス-Ⅱ 水性懸濁注シリンジ 0.5mL HEPTAVAX-II HEPTAVAX-II HEPTAVAX-II Aqueous Suspension Aqueous
ワクチン接種を受ける人へのガイド 2018 年 8 月更新 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) このワクチンの名前は? 販売名 一般名 ヘプタバックス-Ⅱ ヘプタバックス-Ⅱ 水性懸濁注シリンジ 0.25mL ヘプタバックス-Ⅱ 水性懸濁注シリンジ 0.5mL HEPTAVAX-II HEPTAVAX-II HEPTAVAX-II Aqueous Suspension Aqueous
<945F96F B3816A2E786264>
 Q-14 食品衛生法 ( 昭和 22 年法律第 233 号 ) とは 1 食品衛生法について 食品衛生法とは食品の安全性の確保のために公衆衛生の見地から必要な規制その他の措置を講ずることにより 飲食に起因する衛生上の危害の発生を防止し もつて国民の健康の保護を図ることを目的として 食品の規格等の設定 検査の実施 健康を損なうおそれのある食品の販売の禁止などの事項を規定しています 適用範囲食品衛生法の中で
Q-14 食品衛生法 ( 昭和 22 年法律第 233 号 ) とは 1 食品衛生法について 食品衛生法とは食品の安全性の確保のために公衆衛生の見地から必要な規制その他の措置を講ずることにより 飲食に起因する衛生上の危害の発生を防止し もつて国民の健康の保護を図ることを目的として 食品の規格等の設定 検査の実施 健康を損なうおそれのある食品の販売の禁止などの事項を規定しています 適用範囲食品衛生法の中で
東京大会と感染症サーベイランス ~ 普段とどこがちがうのか ~ 疾患疫学が変化する可能性 多数の訪日外国人の流入 多くのマスギャザリングイベント 事前のリスク評価に基づいたサーベイランスと対応の強化の必要性を検討する 体制構築の観点から 行政と大会組織委員会の責任範囲と協力体制の構築が必要 国内移動
 東京オリンピック パラリンピック競技大会における感染症サーベイランスについて ~ 技術的側面から ~ 国立感染症研究所 感染症疫学センター 松井珠乃 東京大会と感染症サーベイランス ~ 普段とどこがちがうのか ~ 疾患疫学が変化する可能性 多数の訪日外国人の流入 多くのマスギャザリングイベント 事前のリスク評価に基づいたサーベイランスと対応の強化の必要性を検討する 体制構築の観点から 行政と大会組織委員会の責任範囲と協力体制の構築が必要
東京オリンピック パラリンピック競技大会における感染症サーベイランスについて ~ 技術的側面から ~ 国立感染症研究所 感染症疫学センター 松井珠乃 東京大会と感染症サーベイランス ~ 普段とどこがちがうのか ~ 疾患疫学が変化する可能性 多数の訪日外国人の流入 多くのマスギャザリングイベント 事前のリスク評価に基づいたサーベイランスと対応の強化の必要性を検討する 体制構築の観点から 行政と大会組織委員会の責任範囲と協力体制の構築が必要
成人用 (65 歳以上 ) 予防接種予診票 任意接種用 本冊子は 肺炎球菌ワクチン 沈降 13 価肺炎球菌結合型ワクチン ( 無毒性変異ジフテリ ア毒素結合体 ) プレベナー 13 水性懸濁注 の接種をご希望の方への説明文書および 予診票 ( 複写式 2 枚綴り ) で 1 セットになっております
 成人用 (65 歳以上 ) 予防接種予診票 任意接種用 本冊子は 肺炎球菌ワクチン 沈降 13 価肺炎球菌結合型ワクチン ( 無毒性変異ジフテリ ア毒素結合体 ) プレベナー 13 水性懸濁注 の接種をご希望の方への説明文書および 予診票 ( 複写式 2 枚綴り ) で 1 セットになっております 予診票の記入について 肺炎球菌の予防接種を実施するにあたって 接種を受けられる方の健康状態をよく把握する必要があります
成人用 (65 歳以上 ) 予防接種予診票 任意接種用 本冊子は 肺炎球菌ワクチン 沈降 13 価肺炎球菌結合型ワクチン ( 無毒性変異ジフテリ ア毒素結合体 ) プレベナー 13 水性懸濁注 の接種をご希望の方への説明文書および 予診票 ( 複写式 2 枚綴り ) で 1 セットになっております 予診票の記入について 肺炎球菌の予防接種を実施するにあたって 接種を受けられる方の健康状態をよく把握する必要があります
Microsoft Word - ワクチンガイド_DT_DSJVC版_ KDSV.doc
 ワクチン接種を受ける人へのガイド 2015 年 1 月更新 乾燥弱毒生おたふくかぜワクチン このワクチンの名前は? 販売名 一般名 おたふくかぜ生ワクチン 北里第一三共 乾燥弱毒生おたふくかぜワクチン Freeze-dried Live Attenuated Mumps Virus Vaccine ワクチン接種を受ける人へのガイドについてワクチンの正しい理解と 重大な副反応の早期発見などに役立てていただくために
ワクチン接種を受ける人へのガイド 2015 年 1 月更新 乾燥弱毒生おたふくかぜワクチン このワクチンの名前は? 販売名 一般名 おたふくかぜ生ワクチン 北里第一三共 乾燥弱毒生おたふくかぜワクチン Freeze-dried Live Attenuated Mumps Virus Vaccine ワクチン接種を受ける人へのガイドについてワクチンの正しい理解と 重大な副反応の早期発見などに役立てていただくために
豚丹毒 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 23 年 2 月 8 日 ( 告示第 358 号 ) 新規追加 1 定義シードロット規格に適合した豚丹毒菌の培養菌液を不活化し アルミニウムゲルアジュバントを添加したワクチンである 2 製法 2.1 製造用株 名称豚丹
 豚丹毒 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 23 年 2 月 8 日 ( 告示第 358 号 ) 新規追加 1 定義シードロット規格に適合した豚丹毒菌の培養菌液を不活化し アルミニウムゲルアジュバントを添加したワクチンである 2 製法 2.1 製造用株 2.1.1 名称豚丹毒菌多摩 96 株 ( 血清型 2 型 ) 又はこれと同等と認められた株 2.1.2 性状感受性豚に接種すると
豚丹毒 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 23 年 2 月 8 日 ( 告示第 358 号 ) 新規追加 1 定義シードロット規格に適合した豚丹毒菌の培養菌液を不活化し アルミニウムゲルアジュバントを添加したワクチンである 2 製法 2.1 製造用株 2.1.1 名称豚丹毒菌多摩 96 株 ( 血清型 2 型 ) 又はこれと同等と認められた株 2.1.2 性状感受性豚に接種すると
< F2D819B955C8EA692CA926D DC58F4994AD8F6F>
 薬食監麻発第 0331008 号平成 17 年 3 月 31 日 各都道府県衛生主管部 ( 局 ) 長 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 一部改正法 という ) 第 2 条の規定による改正後の薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 及び関係政省令等の規定に基づく医薬品 医薬部外品 化粧品及び医療機器 (
薬食監麻発第 0331008 号平成 17 年 3 月 31 日 各都道府県衛生主管部 ( 局 ) 長 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 一部改正法 という ) 第 2 条の規定による改正後の薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 及び関係政省令等の規定に基づく医薬品 医薬部外品 化粧品及び医療機器 (
医療用医薬品最新品質情報集 ( ブルーブック ) 初版 有効成分 ニカルジピン塩酸塩 品目名 ( 製造販売業者 ) 1 ニカルジピン塩酸塩徐放カプセル20mg 日医工 日医工 後発医薬品 2 ニカルジピン塩酸塩徐放カプセル40mg 日医工 日医工 品目名 ( 製造販売業者 )
 医療用医薬品最新品質情報集 ( ブルーブック ) 2018.10.25 初版 有効成分 ニカルジピン塩酸塩 品目名 ( 製造販売業者 ) 1 ニカルジピン塩酸塩徐放カプセル20mg 日医工 日医工 後発医薬品 2 ニカルジピン塩酸塩徐放カプセル40mg 日医工 日医工 品目名 ( 製造販売業者 ) 1 ペルジピンLAカプセル20mg アステラス製薬 先発医薬品 2 ペルジピンLAカプセル40mg アステラス製薬
医療用医薬品最新品質情報集 ( ブルーブック ) 2018.10.25 初版 有効成分 ニカルジピン塩酸塩 品目名 ( 製造販売業者 ) 1 ニカルジピン塩酸塩徐放カプセル20mg 日医工 日医工 後発医薬品 2 ニカルジピン塩酸塩徐放カプセル40mg 日医工 日医工 品目名 ( 製造販売業者 ) 1 ペルジピンLAカプセル20mg アステラス製薬 先発医薬品 2 ペルジピンLAカプセル40mg アステラス製薬
< F2D8E9197BF A836F815B2E6A7464>
 ( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
資料 10 HPV ワクチンの有効性及び安全性に関する疫学研究の概要 1. 研究事業名 厚生労働科学研究費補助金新興 再興感染症及び予防接種政策推進事業 2. 研究課題名 子宮頸がんワクチンの有効性と安全性の評価に関する疫学研究 3. 研究予定期間 平成 27 年 7 月 7 日から 3 年計画 (
 第 16 回厚生科学審議会予防接種 ワクチン分科会副反応検討部会 平成 27 年 度第 6 回薬事 食品衛生審議会医薬品等安全対策部会安全対策調査会 ( 合同開催 ) 資料一覧 資料 1 乾燥弱毒生麻しん風しん混合ワクチン (MR) の副反応報告状況資料 2 乾燥弱毒生麻しんワクチンの副反応報告状況資料 3 乾燥弱毒生風しんワクチンの副反応報告状況資料 4 乾燥弱毒生おたふくかぜワクチンの副反応報告状況資料
第 16 回厚生科学審議会予防接種 ワクチン分科会副反応検討部会 平成 27 年 度第 6 回薬事 食品衛生審議会医薬品等安全対策部会安全対策調査会 ( 合同開催 ) 資料一覧 資料 1 乾燥弱毒生麻しん風しん混合ワクチン (MR) の副反応報告状況資料 2 乾燥弱毒生麻しんワクチンの副反応報告状況資料 3 乾燥弱毒生風しんワクチンの副反応報告状況資料 4 乾燥弱毒生おたふくかぜワクチンの副反応報告状況資料
スライド 1
 平成 29 年度予防接種従事者研修会 ( 予防接種リサーチセンター ) 予防接種の基本的な知識 1. 歴史 2. 生ワクチンと不活化ワクチン 3. 予防接種の間違いを減らすために 4. 予防接種センターの果たす役割 福岡歯科大学医科歯科総合病院予防接種センター岡田賢司平成 29 年 10 月 31 日 ( 福岡会場 ) 予防接種 : IMMUNIZATION ワクチン : VACCINE 予防接種
平成 29 年度予防接種従事者研修会 ( 予防接種リサーチセンター ) 予防接種の基本的な知識 1. 歴史 2. 生ワクチンと不活化ワクチン 3. 予防接種の間違いを減らすために 4. 予防接種センターの果たす役割 福岡歯科大学医科歯科総合病院予防接種センター岡田賢司平成 29 年 10 月 31 日 ( 福岡会場 ) 予防接種 : IMMUNIZATION ワクチン : VACCINE 予防接種
Microsoft Word - (発番)医療機器の製造販売承認申請について
 薬食発 1120 第 5 号 平成 26 年 11 月 20 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医療機器の製造販売承認申請について 医療機器の製造販売承認申請の取扱いについては 医療機器の製造販売承認申請について ( 平成 17 年 2 月 16 日付け薬食発第 0216002 号厚生労働省医薬食品局長通知 以下 旧通知 という ) 等により実施してきたところです 先般
薬食発 1120 第 5 号 平成 26 年 11 月 20 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医療機器の製造販売承認申請について 医療機器の製造販売承認申請の取扱いについては 医療機器の製造販売承認申請について ( 平成 17 年 2 月 16 日付け薬食発第 0216002 号厚生労働省医薬食品局長通知 以下 旧通知 という ) 等により実施してきたところです 先般
子宮頸がん予防措置の実施の推進に関する法律案要綱
 第一総則 子宮頸がん予防措置の実施の推進に関する法律案要綱 一目的 けいりこの法律は 子宮頸がんの罹患が女性の生活の質に多大な影響を与えるものであり 近年の子宮頸が んの罹患の若年化の進行が当該影響を一層深刻なものとしている状況及びその罹患による死亡率が高い 状況にあること並びに大部分の子宮頸がんにヒトパピローマウイルスが関与しており 予防ワクチンの 接種及び子宮頸部の前がん病変 ( 子宮頸がんに係る子宮頸部の異形成その他の子宮頸がんの発症前にお
第一総則 子宮頸がん予防措置の実施の推進に関する法律案要綱 一目的 けいりこの法律は 子宮頸がんの罹患が女性の生活の質に多大な影響を与えるものであり 近年の子宮頸が んの罹患の若年化の進行が当該影響を一層深刻なものとしている状況及びその罹患による死亡率が高い 状況にあること並びに大部分の子宮頸がんにヒトパピローマウイルスが関与しており 予防ワクチンの 接種及び子宮頸部の前がん病変 ( 子宮頸がんに係る子宮頸部の異形成その他の子宮頸がんの発症前にお
スライド 1
 参考資料 1 水痘ワクチンの 接種対象者及び接種方法について 厚生労働省健康局結核感染症課予防接種室平成 25 年 7 月 10 日第 3 回予防接種基本方針部会 本資料は技術的検討であり 国民に対して広く接種機会を提供する仕組みとして実施するためには 前提として ワクチンの供給 実施体制の確保 必要となる財源の捻出方法等の検討を行った上で 関係者の理解を得るとともに 副反応も含めた予防接種施策に対する国民の理解等が必要
参考資料 1 水痘ワクチンの 接種対象者及び接種方法について 厚生労働省健康局結核感染症課予防接種室平成 25 年 7 月 10 日第 3 回予防接種基本方針部会 本資料は技術的検討であり 国民に対して広く接種機会を提供する仕組みとして実施するためには 前提として ワクチンの供給 実施体制の確保 必要となる財源の捻出方法等の検討を行った上で 関係者の理解を得るとともに 副反応も含めた予防接種施策に対する国民の理解等が必要
<4D F736F F D A835E838A F8B7982D18AC48DB85F20534F A68CEB8E9A E9A8F4390B38DCF2
 自治医科大学人を対象とした医学系研究に関するモニタリング及び監査の標準業務手順書 ver.1.0(2015 年 5 月 15 日 ) 1. 目的等 1) 目的 (1) 本手順書は 自治医科大学の教職員が 人を対象とする医学系研究に関する倫理指針 ( 平成 26 年文部科学省 厚生労働省告示第 3 号 ) 及び指針告示に伴う通知ならびにガイダンス ( 以下 指針 指針告示に伴う通知及びガイダンスを合わせて
自治医科大学人を対象とした医学系研究に関するモニタリング及び監査の標準業務手順書 ver.1.0(2015 年 5 月 15 日 ) 1. 目的等 1) 目的 (1) 本手順書は 自治医科大学の教職員が 人を対象とする医学系研究に関する倫理指針 ( 平成 26 年文部科学省 厚生労働省告示第 3 号 ) 及び指針告示に伴う通知ならびにガイダンス ( 以下 指針 指針告示に伴う通知及びガイダンスを合わせて
