PowerPoint プレゼンテーション
|
|
|
- わんど なみこし
- 5 years ago
- Views:
Transcription
1 分析化学用語集
2 1. 定量分析の手順について 1( ) 2( ) 3( ) 4( ) 5( ) 6( ) 2. 試料の採取と調整において大切なことを 3 つあげよ 3. 2 について 固体試料を乾燥させ吸着水分を取り除くのはなぜか 4. 試料の計りとりについて 最初に分析する試料の ( 1 ) あるいは ( 2 ) を測定することが必要 また 定量分析の結果はどう表わすのが普通か?( 3 ) 5. 固体試料を溶液にする操作をする上で注意することを 3 つあげよ 6. 妨害物質とはなにか 7. 測定値 ( データ ) は ( 1 ) (=( 2 ) + ( 3 )) で表わされる 8. 物質量について説明せよ 9. 物理量を表わす記号は ( 1 ) あるいは ( 2 ) の 1 字を ( 3 ) 体で示し 単位をあらわす記号は ( 4 ) 体で示す 10. SI 単位の 10 の整数乗を表わすために ( 1 ) を用いる その際 ( 1 ) の記号は ( 2 ) で書き ( 3 ) と ( 4 ) の間に ( 5 ) を置かない 11. 質量モル濃度の単位はどのように記述するか 12. モル濃度の単位はどのように記述するか 13. 式量濃度について 式量とは ( ) 1 グラム式量とは ( ) 分子量 =( ), 1 リットルの溶液中に 1 グラム式量の物質が含まれる時 その濃度を () と呼び () とかく 1. 1( 試料の採取と調整 ) 2( 試料の計りとり ) 3( 試料の溶解 ) 4( 妨害物質の分離 ) 5( 分析の完了 ) 6( 分析法の選択 ) 2. 1 目的の成分の偏在に注意し対象とする物質全体の組成を反映する試料を用いて分析を行う 2 固体試料は粉砕して粒子サイズを小さくし 十分に混合して均一にする 3 固体試料において一定の条件で乾燥させ 吸着水分を除くことが必要となる 3. 試料に水の吸脱着がある場合 成分の含有率が分析時の周囲の湿度に左右されることになるため 4. (1)(2) 質量 体積 ( 順不同 ) (3) 相対的な表示 すなわち試料の単位質量あるいは単位体積あたりの目的成分の量 ( 例えば百分率 ) で表わす 5. 1 操作はできる限り簡単に 2 使用する試薬や実験環境からの汚染が少なく 3 目的成分の損失がないもの 6. 定量しようとする成分の直接測定を妨げる化合物または元素 7. 1 物理量 2 数値 3 単位 8. 12g の 12C に含まれる 炭素原子と同数の単位粒子を含む系の物質の量を 1mol とする 単位粒子は原子 分子 イオン 電子 その他の粒子またはこれらの組み合わせ ( 集合体 ) でそれが明確に指定されていなければならない 9. 物理量を表わす記号は ( ローマ字 ) あるいは ( ギリシヤ文字 ) の 1 字を ( イタリック ) 体で示し 単位をあらわす記号は ( ローマン ) 体で示す 10. SI 単位の 10 の整数乗を表わすために ( 接頭語 ) を用いる その際 ( 接頭語 ) の記号は ( ローマン体 ) で書き ( 接頭語 ) と ( 単位記号 ) の間に ( スペース ) を置かない 11. 質量モル濃度の単位 :mol/kg 12. モル濃度の単位 :mol/l 13. 式量濃度について 式量とは ( 化学式に相当する原子単位の量 ) 1 グラム式量とは ( 式量に等しいグラム数の物質の量 ) 分子量 =( 式量 ), 1 リットルの溶液中に 1 グラム式量の物質が含まれる時 その濃度を (1foamal) と呼び (1F) とかく 2012/6/4 2
3 絶対誤差と測定誤差の求め方を答えよ 16. 系統誤差についてどう扱うか 17. 偶然誤差についてどう扱うか 18. 分析の正確さ またはカタヨリを調べたり 分析機器の校正を行うために調整 純度あるいは特定成分の含有量が明示されたものをなんという 19. 系統誤差にはどんなものがあるか 3 つあげよ 20. 機器誤差について説明し 誤差を減らすにはどうすればいいかをのべよ 21. 操作誤差について説明し 誤差を減らすにはどうすればいいかをのべよ 22. 方法誤差について説明し 誤差を減らすにはどうすればいいかをのべよ 23. 精度について説明せよ 24. 正確さについて説明せよ 25. 数値の丸め方 有効数字で表わされる桁数 n 桁に 1. (n+1) 桁目以下が n 桁目の 1 単位の 1/2 未満の時は ( ) 2. (n+1) 桁目以下が n 桁目の 1 単位の 1/2 を超える時は ( ) 15. 測定値をx, 真の値をXとすると 絶対誤差 (ε)=x-x 相対誤差 =100ε/X 16. 原因を調べることによって回避あるいは補正可能 17. 分析者が制御できない自然界のさまざまな原因が 複雑に作用して生じる 統計と確立に基づいて数学的に評価する 18. 標準物質 19. 機器誤差 操作誤差 方法誤差 20. 校正していないてんびんやピペットによって試料を採取した場合 何らかの欠陥をもつ装置で測定した場合に生じる 校正し 欠陥のない機器を使う 21. 分析に用いる試料の不十分な感想 試料溶液を加熱する際の突沸 試料溶液の不完全な移し替え 個人の読み取り癖などによって生じる 分析者が経験を積む 注意深くなることによって回避可能 22. 沈殿生成にあたっての不純物の供沈 沈殿物のわずかな溶解 不完全な反応 目的としない反応 ( 副反応 ) 試薬中の不純物などによって生じる 23. 同一試料を同一条件下で繰り返し分析して得られた測定値のバラツキを表わす用語 精度が高い バラツキが小さい 偶然誤差が小さい 24. 定値の真値からのカタヨリの程度を表わす用語 正確さが高い カタヨリが小さい 系統誤差が小さい 25. 数値の丸め方 有効数字で表わされる桁数 n 桁に 1. (n+1) 桁目以下が n 桁目の 1 単位の 1/2 未満の時は ( 切り捨てる ) 2. (n+1) 桁目以下が n 桁目の 1 単位の 1/2 を超える時は ( 切り上げる ) 2012/6/4 3
4 26. 数値の丸め方 有効数字で表わされる桁数 n 桁に 3. (n+1) 桁目以下が n 桁目の 1 単位のちょうど 1/2 時 n 桁目が偶数なら ( ) 奇数なら ( ) 27. 容量分析とは 28. 滴定 当量点 終点についてそれぞれ説明 29. 容量分析の特徴を 4 つあげよ 30. 容量分析に利用される反応の条件を 3 つ 31. 容量分析法の種類 1 反応の種類で分ける場合の例 2 終点判定の方法による分類 3 滴定のしかたによる分類 次標準 ( 溶液 ) とはなにか また純度は何 % 以上か 次標準 ( 溶液 ) とはなにか 34. イラストの測容器の名前 また何に使うか 26. 数値の丸め方 有効数字で表わされる桁数 n 桁に 3. (n+1) 桁目以下が n 桁目の 1 単位のちょうど 1/2 時 n 桁目が偶数なら ( 切り捨て ) 奇数なら ( 切り上げ ) 27. 容量分析とは 物質の量を知りたい ( 定量 ) とき この物質と反応する濃度既知のある試薬溶液 ( 標準溶液 ) を加え 反応が完結するために要した標準溶液の体積から目的物質の量を求める方法全般をいう 28. 滴定 : ビュレットを用いて標準溶液を滴下し 目的物と反応させる 当量点 : 標準溶液中の成分と目的物質が過不足なく反応したところ ( 理論的に反応がちょうど終わったところ ) 終点 : 実験的に反応が終わったと判定されたところ ビュレットのような簡単な測容器を用いるだけで精度 及び正確さの高い測定ができる 2 標準試料がいらない 絶対測定である 3 安価でどこでも精度の高い分析ができる 4 機器分析に比べて微量成分分析に不適 熟練が必要 反応が定量的に進行し 副反応が生じない 2 反応が迅速である 3 反応が完結したときを鋭敏に検知する手段がある 酸塩基滴定 ( 中和滴定 ) 沈殿滴定 酸化還元滴定 キレート滴定 2 電位差滴定 電量滴定 光度滴定 温度滴定 におい滴定 3 直接滴定 逆滴定 間接滴定 次標準物質 ( 一定組成 空気中で安定で 秤量 ( ひょうりょう ) に適当 純粋なものが得やすい ) の一定量を見ずに溶かして一定体積まで希釈することによって正確な濃度が決まる 純度は 99.98% 以上 次標準液を基準として これから直接的 間接的に濃度をきめることが出来るもの (Na2CO3 (1 次標準 ) の一定量を採取し これを水に溶かした溶液について HCl 濃度を決定したような例では HCl は 2 次標準 ) 34. 左からビュレット ( 目的物質との反応に要した標準溶液の体積を便利に測定できる ) ( ホール ) ピペット ( 溶液の一定量を正確にはかりとる ) メスフラスコ ( 一定量の溶液を正確につくりたいとき 溶液の体積を一定量まで正確に薄めたい時 ) 2012/6/4 4
5 35. ブレンステッドローリーの定義について述べよ 酸とは ~ 塩基とは ~ 36. 共役酸塩基対とは 37. アンモニアはなぜ塩基性を示すのか 38. 両性物質とはなにか 39. ルイスの定義について述べよ 酸とは~ 塩基とは~ 40. ルイスの定義の特徴を述べよ mol/l HCl 標準溶液について説明せよ mol/l NaOH 標準溶液について説明せよ 35. 酸とはプロトンを他に与えることのできる物質塩基とは他の物質からプロトンを受け取ることのできる物質 36. 共役酸塩基対とは, プロトン移動によって相互に変換する一対の化合物 37. アンモニアはそれ自身は水酸化物イオンを持っていないが 水溶液中からプロトンを受け取ることによって水酸化物イオンを生じ 塩基性を示す 38. 酸に対してはプロトンを受け取って塩基として作用 塩基に対しては プロトンを放出して酸として作用する いいかえると 酸とは水にプロトンを与える物質で塩基とは水からプロトンを受け取る物質 39. 酸とは共有電子対を受け取る塩基とは非共有電子対を与える 40. きわめて広範囲の化学反応を酸塩基反応として解釈可能 ( しかし 一般に酸塩基反応を扱う場合はプロトンの移動に注目することが多い ) 41. 濃塩酸 (36.0%, 密度 1.18)8.6ml を適当量の見ずに溶かし その溶液をメスフラスコに入れて全容を 1000ml にする 濃塩酸の濃度はもともと正確ではないので 一次標準物質である炭酸ナトリウムの濃度既知溶液を滴定して正確な濃度を決定する 42. 水酸化ナトリウム 4g を 500ml のビーカーに入れ 約 300ml の水を加えて溶かす これをメスフラスコに移して 水で全容を 1000ml とする 試薬 ( 固体 ) の水酸化ナトリウムは空気中の水や二酸化炭素を吸収して純度が悪くなっているのでフタル酸水素カリウム (1 次標準 ) または濃度既知の 0.1mol/lHCl 標準溶液 (2 次標準 ) で標定して正確な濃度を決定する この標準溶液は保存中にも濃度が変わりやすいので ときどき標定する 2012/6/4 5
6 正規分布 連続分布の一つ 数学者ガウスが導出 ( ガウスは超有名 ) いわゆる よくある分布 例 テスト結果分布 身長の分布 f x = e( 正規分布の確率密度分布関数 (x μ) 2 2σ 2 ) 2πσ 2012/6/4 6
7 正規分布の確率密度分布関数 記号の意味は以下のとおり σ: 母標準偏差 μ: 母平均 一般に x の期待値を E(x) と記す E は期待値を意味する Expectation の略 (x 2 の期待値 ) (x の期待値 ) 2 x の期待値 f x = e( 2πσ 2012/6/4 7 標準偏差の二乗を分散 と呼ぶ (x μ) 2 2σ 2 )
ウスターソース類の食塩分測定方法 ( モール法 ) 手順書 1. 適用範囲 この手順書は 日本農林規格に定めるウスターソース類及びその周辺製品に適用する 2. 測定方法の概要試料に水を加え ろ過した後 指示薬としてクロム酸カリウム溶液を加え 0.1 mol/l 硝酸銀溶液で滴定し 滴定終点までに消費
 ウスターソース類の食塩分測定方法 ( モール法 ) 手順書 1. 適用範囲 この手順書は 日本農林規格に定めるウスターソース類及びその周辺製品に適用する 2. 測定方法の概要試料に水を加え ろ過した後 指示薬としてクロム酸カリウム溶液を加え 0.1 mol/l 硝酸銀溶液で滴定し 滴定終点までに消費した硝酸銀溶液の量から塩化ナトリウム含有量を算出する 3. 注意事項 (a) クロム酸カリウムを取り扱う際には
ウスターソース類の食塩分測定方法 ( モール法 ) 手順書 1. 適用範囲 この手順書は 日本農林規格に定めるウスターソース類及びその周辺製品に適用する 2. 測定方法の概要試料に水を加え ろ過した後 指示薬としてクロム酸カリウム溶液を加え 0.1 mol/l 硝酸銀溶液で滴定し 滴定終点までに消費した硝酸銀溶液の量から塩化ナトリウム含有量を算出する 3. 注意事項 (a) クロム酸カリウムを取り扱う際には
2011年度 化学1(物理学科)
 014 年度スペシャルプログラム (1/17) 酸 塩基 : 酸 塩基の定義を確認する No.1 1 酸と塩基の定義に関する以下の文章の正を答えよ 場合は 間違いを指摘せよ 文章正指摘 1 酸と塩基の定義はアレニウスとブレンステッド ローリーの 種類である ルイスの定義もある アレニウスの定義によれば 酸とは H を含むものである 水に溶けて 電離して H+ を出すものである 3 アレニウスの定義によれば
014 年度スペシャルプログラム (1/17) 酸 塩基 : 酸 塩基の定義を確認する No.1 1 酸と塩基の定義に関する以下の文章の正を答えよ 場合は 間違いを指摘せよ 文章正指摘 1 酸と塩基の定義はアレニウスとブレンステッド ローリーの 種類である ルイスの定義もある アレニウスの定義によれば 酸とは H を含むものである 水に溶けて 電離して H+ を出すものである 3 アレニウスの定義によれば
フォルハルト法 NH SCN の標準液または KSCN の標準液を用い,Ag または Hg を直接沈殿滴定する方法 および Cl, Br, I, CN, 試料溶液に Fe SCN, S 2 を指示薬として加える 例 : Cl の逆滴定による定量 などを逆滴定する方法をいう Fe を加えた試料液に硝酸
 沈殿滴定とモール法 沈殿滴定沈殿とは溶液に試薬を加えたり加熱や冷却をしたとき, 溶液から不溶性固体が分離する現象, またはその不溶性固体を沈殿という 不溶性固体は, 液底に沈んでいいても微粒子 ( コロイド ) として液中を浮遊していても沈殿と呼ばれる 沈殿滴定とは沈殿が生成あるいは消失する反応を利用した滴定のことをいう 沈殿が生成し始めた点, 沈殿の生成が完了した点, または沈殿が消失した点が滴定の終点となる
沈殿滴定とモール法 沈殿滴定沈殿とは溶液に試薬を加えたり加熱や冷却をしたとき, 溶液から不溶性固体が分離する現象, またはその不溶性固体を沈殿という 不溶性固体は, 液底に沈んでいいても微粒子 ( コロイド ) として液中を浮遊していても沈殿と呼ばれる 沈殿滴定とは沈殿が生成あるいは消失する反応を利用した滴定のことをいう 沈殿が生成し始めた点, 沈殿の生成が完了した点, または沈殿が消失した点が滴定の終点となる
高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ
![高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ 高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ](/thumbs/94/118405200.jpg) 高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ溶質の20% 溶液 100gと30% 溶液 200gを混ぜると質量 % はいくらになるか ( 有効数字
高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ溶質の20% 溶液 100gと30% 溶液 200gを混ぜると質量 % はいくらになるか ( 有効数字
Microsoft Word - 酸塩基
 化学基礎実験 : 酸 塩基と (1) 酸と塩基 の基本を学び の実験を通してこれらの事柄に関する認識を深めます さらに 緩衝液の性質に ついて学び 緩衝液の 変化に対する緩衝力を実験で確かめます 化学基礎実験 : 酸 塩基と 酸と塩基 水の解離 HCl H Cl - 塩酸 塩素イオン 酸 強酸 ヒドロニウムイオン H 3 O H O H OH - OH ー [H ] = [OH - ]= 1-7 M
化学基礎実験 : 酸 塩基と (1) 酸と塩基 の基本を学び の実験を通してこれらの事柄に関する認識を深めます さらに 緩衝液の性質に ついて学び 緩衝液の 変化に対する緩衝力を実験で確かめます 化学基礎実験 : 酸 塩基と 酸と塩基 水の解離 HCl H Cl - 塩酸 塩素イオン 酸 強酸 ヒドロニウムイオン H 3 O H O H OH - OH ー [H ] = [OH - ]= 1-7 M
しょうゆの食塩分測定方法 ( モール法 ) 手順書 1. 適用範囲 この手順書は 日本農林規格に定めるしょうゆに適用する 2. 測定方法の概要 試料に水を加え 指示薬としてクロム酸カリウム溶液を加え 0.02 mol/l 硝酸銀溶液で滴定し 滴定終点までに消費した硝酸銀溶液の量から塩化ナトリウム含有
 しょうゆの食塩分測定方法 ( モール法 ) 手順書 1. 適用範囲 この手順書は 日本農林規格に定めるしょうゆに適用する 2. 測定方法の概要 試料に水を加え 指示薬としてクロム酸カリウム溶液を加え 0.02 mol/l 硝酸銀溶液で滴定し 滴定終点までに消費した硝酸銀溶液の量から塩化ナトリウム含有量を算出する 3. 注意事項 (a) クロム酸カリウムを取り扱う際には 皮膚に付けたり粉塵を吸入しないようゴーグル型保護メガネ
しょうゆの食塩分測定方法 ( モール法 ) 手順書 1. 適用範囲 この手順書は 日本農林規格に定めるしょうゆに適用する 2. 測定方法の概要 試料に水を加え 指示薬としてクロム酸カリウム溶液を加え 0.02 mol/l 硝酸銀溶液で滴定し 滴定終点までに消費した硝酸銀溶液の量から塩化ナトリウム含有量を算出する 3. 注意事項 (a) クロム酸カリウムを取り扱う際には 皮膚に付けたり粉塵を吸入しないようゴーグル型保護メガネ
キレート滴定
 4. キレート滴定 4.1 0.01MEDTA 標準溶液の調製 キレート滴定において標準溶液として用いられる EDTA は 普通 EDTA の2ナトリウム塩 H 2 Na 2 Y 2H 2 O で ETA と表示されている この試薬は結晶水以外に多少の水分を含んでいるので 通常は約 80 で数時間乾燥して使用するが 本実験では精密な分析を行うために 調製した EDTA 溶液をZnの一次標準溶液で標定して
4. キレート滴定 4.1 0.01MEDTA 標準溶液の調製 キレート滴定において標準溶液として用いられる EDTA は 普通 EDTA の2ナトリウム塩 H 2 Na 2 Y 2H 2 O で ETA と表示されている この試薬は結晶水以外に多少の水分を含んでいるので 通常は約 80 で数時間乾燥して使用するが 本実験では精密な分析を行うために 調製した EDTA 溶液をZnの一次標準溶液で標定して
<連載講座>アルマイト従事者のためのやさしい化学(XVII)--まとめと問題 (1)
 アルマイト従事者のためのやさしい化学 (ⅩⅦ) - まとめと問題 1- 野口駿雄 Ⅰ. はじめに前号までに化学の基礎 アルミニウム表面処理に使用されている前処理液 ( 特にアルカリ溶液 ) 及び硫酸電解液や蓚酸電解液の分析方法について その手順を 使用する分析用器具を図示し また簡単な使用方法を付け加えながら示し 初心者でもその図を見ながら順を追って操作を行えば それぞれの分析が出来るように心がけ
アルマイト従事者のためのやさしい化学 (ⅩⅦ) - まとめと問題 1- 野口駿雄 Ⅰ. はじめに前号までに化学の基礎 アルミニウム表面処理に使用されている前処理液 ( 特にアルカリ溶液 ) 及び硫酸電解液や蓚酸電解液の分析方法について その手順を 使用する分析用器具を図示し また簡単な使用方法を付け加えながら示し 初心者でもその図を見ながら順を追って操作を行えば それぞれの分析が出来るように心がけ
化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イ
 化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イオンと陰イオンの静電気的な引力による結合を 1 1 という ⑵ 2 個の水素原子は, それぞれ1 個の価電子を出し合い,
化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イオンと陰イオンの静電気的な引力による結合を 1 1 という ⑵ 2 個の水素原子は, それぞれ1 個の価電子を出し合い,
木村の理論化学小ネタ 熱化学方程式と反応熱の分類発熱反応と吸熱反応化学反応は, 反応の前後の物質のエネルギーが異なるため, エネルギーの出入りを伴い, それが, 熱 光 電気などのエネルギーの形で現れる とくに, 化学変化と熱エネルギーの関
 熱化学方程式と反応熱の分類発熱反応と吸熱反応化学反応は, 反応の前後の物質のエネルギーが異なるため, エネルギーの出入りを伴い, それが, 熱 光 電気などのエネルギーの形で現れる とくに, 化学変化と熱エネルギーの関係を扱う化学の一部門を熱化学という 発熱反応反応前の物質のエネルギー 大ネルギ熱エネルギーー小エ反応後の物質のエネルギー 吸熱反応 反応後の物質のエネルギー 大ネルギー熱エネルギー小エ反応前の物質のエネルギー
熱化学方程式と反応熱の分類発熱反応と吸熱反応化学反応は, 反応の前後の物質のエネルギーが異なるため, エネルギーの出入りを伴い, それが, 熱 光 電気などのエネルギーの形で現れる とくに, 化学変化と熱エネルギーの関係を扱う化学の一部門を熱化学という 発熱反応反応前の物質のエネルギー 大ネルギ熱エネルギーー小エ反応後の物質のエネルギー 吸熱反応 反応後の物質のエネルギー 大ネルギー熱エネルギー小エ反応前の物質のエネルギー
(Microsoft Word - \230a\225\266IChO46-Preparatory_Q36_\211\374\202Q_.doc)
 問題 36. 鉄 (Ⅲ) イオンとサリチルサリチル酸の錯形成 (20140304 修正 : ピンク色の部分 ) 1. 序論この簡単な実験では 水溶液中での鉄 (Ⅲ) イオンとサリチル酸の錯形成を検討する その錯体の実験式が求められ その安定度定数を見積もることができる 鉄 (Ⅲ) イオンとサリチル酸 H 2 Sal からなる安定な錯体はいくつか知られている それらの構造と組成はpHにより異なる 酸性溶液では紫色の錯体が生成する
問題 36. 鉄 (Ⅲ) イオンとサリチルサリチル酸の錯形成 (20140304 修正 : ピンク色の部分 ) 1. 序論この簡単な実験では 水溶液中での鉄 (Ⅲ) イオンとサリチル酸の錯形成を検討する その錯体の実験式が求められ その安定度定数を見積もることができる 鉄 (Ⅲ) イオンとサリチル酸 H 2 Sal からなる安定な錯体はいくつか知られている それらの構造と組成はpHにより異なる 酸性溶液では紫色の錯体が生成する
CERT化学2013前期_問題
 [1] から [6] のうち 5 問を選んで解答用紙に解答せよ. いずれも 20 点の配点である.5 問を超えて解答した場合, 正答していれば成績評価に加算する. 有効数字を適切に処理せよ. 断りのない限り大気圧は 1013 hpa とする. 0 C = 273 K,1 cal = 4.184 J,1 atm = 1013 hpa = 760 mmhg, 重力加速度は 9.806 m s 2, 気体
[1] から [6] のうち 5 問を選んで解答用紙に解答せよ. いずれも 20 点の配点である.5 問を超えて解答した場合, 正答していれば成績評価に加算する. 有効数字を適切に処理せよ. 断りのない限り大気圧は 1013 hpa とする. 0 C = 273 K,1 cal = 4.184 J,1 atm = 1013 hpa = 760 mmhg, 重力加速度は 9.806 m s 2, 気体
▲ 電離平衡
 電離平衡演習その 1 [04 金沢 ] 電離平衡 1 1 酢酸の濃度 C mol/l の水溶液がある 酢酸の電離度を とすると, 平衡状態で溶液中に存在する酢酸イオンの濃度は Ⅰ mol/l, 電離していない酢酸の濃度は Ⅱ mol/l, 水素イオンの濃度は Ⅲ mol/l と表される ここで, 電離度が 1より非常に小さく,1 1と近似すると, 電離定数は Ⅳ mol/l と表される いま,3.0
電離平衡演習その 1 [04 金沢 ] 電離平衡 1 1 酢酸の濃度 C mol/l の水溶液がある 酢酸の電離度を とすると, 平衡状態で溶液中に存在する酢酸イオンの濃度は Ⅰ mol/l, 電離していない酢酸の濃度は Ⅱ mol/l, 水素イオンの濃度は Ⅲ mol/l と表される ここで, 電離度が 1より非常に小さく,1 1と近似すると, 電離定数は Ⅳ mol/l と表される いま,3.0
分析化学講義資料 ( 容量分析 ) 林譲 (Lin, Rang) 容量分析概要容量分析法 (volumetric analysis) は滴定分析法 (titrimetric analysis) とも呼ばれている この方法は, フラスコ中の試料液の成分とビュレットに入れた濃度既知の標準液 (stand
 分析化学講義資料 ( 容量分析 ) 林譲 (Lin, Rang) 容量分析概要容量分析法 (volumetric analysis) は滴定分析法 (titrimetric analysis) とも呼ばれている この方法は, フラスコ中の試料液の成分とビュレットに入れた濃度既知の標準液 (standard solution) を反応させ, 適当な方法によって終点 (end point) を検出し,
分析化学講義資料 ( 容量分析 ) 林譲 (Lin, Rang) 容量分析概要容量分析法 (volumetric analysis) は滴定分析法 (titrimetric analysis) とも呼ばれている この方法は, フラスコ中の試料液の成分とビュレットに入れた濃度既知の標準液 (standard solution) を反応させ, 適当な方法によって終点 (end point) を検出し,
PowerPoint プレゼンテーション
 薬品分析化学第 8 回 HendersonHasselbalch の式 ( 復習 ) ph 緩衝液 (p 55 ~) 溶液中に共役酸 塩基対が存在しているとき ph p 共役酸 塩基の濃度関係を表す 8 弱酸 HA の平衡式 O H O A において HA H A = mol/l, [A= mol/l とすると O [A より O A A [A となり ph p が導かれる 〇弱酸 HA ( mol/l)
薬品分析化学第 8 回 HendersonHasselbalch の式 ( 復習 ) ph 緩衝液 (p 55 ~) 溶液中に共役酸 塩基対が存在しているとき ph p 共役酸 塩基の濃度関係を表す 8 弱酸 HA の平衡式 O H O A において HA H A = mol/l, [A= mol/l とすると O [A より O A A [A となり ph p が導かれる 〇弱酸 HA ( mol/l)
<4D F736F F D2089BB8A778AEE E631358D E5F89BB8AD28CB3>
 第 15 講 酸化と還元 酸化 還元とは切ったリンゴをそのまま放置すると, 時間が経つにつれて断面が変色します これはリンゴの断面が酸化した現象を示しています ピカピカの10 円玉も, しばらくすると黒く, くすんでいきます これも酸化です この10 円玉を水素ガスのなかに入れると, 元のきれいな10 円玉に戻ります これが還元です 1 酸化還元の定義 2 酸化数とは? 3 酸化剤 還元剤についての理解
第 15 講 酸化と還元 酸化 還元とは切ったリンゴをそのまま放置すると, 時間が経つにつれて断面が変色します これはリンゴの断面が酸化した現象を示しています ピカピカの10 円玉も, しばらくすると黒く, くすんでいきます これも酸化です この10 円玉を水素ガスのなかに入れると, 元のきれいな10 円玉に戻ります これが還元です 1 酸化還元の定義 2 酸化数とは? 3 酸化剤 還元剤についての理解
2017 年度一般入試前期 A 日程 ( 1 月 23 日実施 ) 化学問題 (63 ページ 74 ページ ) 問題は大問 Ⅰ Ⅳ までありますが 一部 他科目との共通問題となっています 大問 Ⅰ は 化学基礎 + 生物基礎 の大問 Ⅰ と共通の問題です 大問 Ⅱ は 化学基礎 + 生物基礎 の大問
 2017 年度一般入試前期 A 日程 ( 1 月 23 日実施 ) 化学問題 (63 ページ 74 ページ ) 問題は大問 Ⅰ Ⅳ までありますが 一部 他科目との共通問題となっています 大問 Ⅰ は 化学基礎 + 生物基礎 の大問 Ⅰ と共通の問題です 大問 Ⅱ は 化学基礎 + 生物基礎 の大問 Ⅱ と共通の問題です 63 必要があれば, 次の数値を使いなさい 原子量 H=1. 0,C=12,O=16,S=32
2017 年度一般入試前期 A 日程 ( 1 月 23 日実施 ) 化学問題 (63 ページ 74 ページ ) 問題は大問 Ⅰ Ⅳ までありますが 一部 他科目との共通問題となっています 大問 Ⅰ は 化学基礎 + 生物基礎 の大問 Ⅰ と共通の問題です 大問 Ⅱ は 化学基礎 + 生物基礎 の大問 Ⅱ と共通の問題です 63 必要があれば, 次の数値を使いなさい 原子量 H=1. 0,C=12,O=16,S=32
 様式第 19 別紙ロ 整理番号 SG150145 活動番号 002 科学研究実践活動のまとめ 1. タイトル 高知県産ゆずを化学する ゆずに含まれるビタミン のヨウ素滴定 2. 背景 目的高知県には, ゆずや文旦, ポンカンなど様々な柑橘系の果物がたくさんある それらには私たちの生活には欠かせない様々な栄養素が含まれている その中でもビタミン ( アスコルビン酸 ) は, 多くの柑橘系果物に含まれていて,
様式第 19 別紙ロ 整理番号 SG150145 活動番号 002 科学研究実践活動のまとめ 1. タイトル 高知県産ゆずを化学する ゆずに含まれるビタミン のヨウ素滴定 2. 背景 目的高知県には, ゆずや文旦, ポンカンなど様々な柑橘系の果物がたくさんある それらには私たちの生活には欠かせない様々な栄養素が含まれている その中でもビタミン ( アスコルビン酸 ) は, 多くの柑橘系果物に含まれていて,
< イオン 電離練習問題 > No. 1 次のイオンの名称を書きなさい (1) H + ( ) (2) Na + ( ) (3) K + ( ) (4) Mg 2+ ( ) (5) Cu 2+ ( ) (6) Zn 2+ ( ) (7) NH4 + ( ) (8) Cl - ( ) (9) OH -
 < イオン 電離練習問題 > No. 1 次のイオンの名称を書きなさい (1) + (2) Na + (3) K + (4) Mg 2+ (5) Cu 2+ (6) Zn 2+ (7) N4 + (8) Cl - (9) - (10) SO4 2- (11) NO3 - (12) CO3 2- 次の文中の ( ) に当てはまる語句を 下の選択肢から選んで書きなさい 物質の原子は (1 ) を失ったり
< イオン 電離練習問題 > No. 1 次のイオンの名称を書きなさい (1) + (2) Na + (3) K + (4) Mg 2+ (5) Cu 2+ (6) Zn 2+ (7) N4 + (8) Cl - (9) - (10) SO4 2- (11) NO3 - (12) CO3 2- 次の文中の ( ) に当てはまる語句を 下の選択肢から選んで書きなさい 物質の原子は (1 ) を失ったり
2014 年度大学入試センター試験解説 化学 Ⅰ 第 1 問物質の構成 1 問 1 a 1 g に含まれる分子 ( 分子量 M) の数は, アボガドロ定数を N A /mol とすると M N A 個 と表すことができる よって, 分子量 M が最も小さい分子の分子数が最も多い 分 子量は, 1 H
 01 年度大学入試センター試験解説 化学 Ⅰ 第 1 問物質の構成 1 問 1 a 1 g に含まれる分子 ( 分子量 M) の数は, アボガドロ定数を N A /mol とすると M N A 個 と表すことができる よって, 分子量 M が最も小さい分子の分子数が最も多い 分 子量は, 1 = 18 N = 8 3 6 = 30 Ne = 0 5 = 3 6 l = 71 となり,1 が解答 (
01 年度大学入試センター試験解説 化学 Ⅰ 第 1 問物質の構成 1 問 1 a 1 g に含まれる分子 ( 分子量 M) の数は, アボガドロ定数を N A /mol とすると M N A 個 と表すことができる よって, 分子量 M が最も小さい分子の分子数が最も多い 分 子量は, 1 = 18 N = 8 3 6 = 30 Ne = 0 5 = 3 6 l = 71 となり,1 が解答 (
イオン化傾向 イオン化傾向 1 金属の単体はいずれも酸化されて陽イオンになりうる 金属のイオンのなりやすさを表したものをイオン化傾向という イオン化傾向 K Ca Na Mg Al Zn Fe Ni Sn Pb (H) Cu Hg Ag Pt Au e- を出してイオンになりやすい酸化されやすい イ
 イオン化傾向 イオン化傾向 金属の単体はいずれも酸化されて陽イオンになりうる 金属のイオンのなりやすさを表したものをイオン化傾向という イオン化傾向 K Ca Na Mg Al Zn Fe Ni Sn Pb (H) Cu Hg Ag Pt Au e- を出してイオンになりやすい酸化されやすい イオンになりにくい酸化されにくい イオン化傾向の覚え方 K かそう Ca か Na な Mg ま Al あ
イオン化傾向 イオン化傾向 金属の単体はいずれも酸化されて陽イオンになりうる 金属のイオンのなりやすさを表したものをイオン化傾向という イオン化傾向 K Ca Na Mg Al Zn Fe Ni Sn Pb (H) Cu Hg Ag Pt Au e- を出してイオンになりやすい酸化されやすい イオンになりにくい酸化されにくい イオン化傾向の覚え方 K かそう Ca か Na な Mg ま Al あ
カールフィッシャー法と濃度計算問題
 酸化還元滴定の応用例 カールフィッシャー法 (Karl Fischer s method) 微量の水分を滴定で求める方法 試料を無水メタノールなどと振って水を抽出し これをカールフィッシャー試薬で滴定する カールフィッシャー試薬は ヨウ素 二酸化イオウ ピリジンを 1:3:10( モル比 ) の割合にメタノールに溶かしたもの 水の存在によってヨウ素が二酸化イオウによって定量的に還元され この両者がピリジンと化合して明るい黄色に変わる
酸化還元滴定の応用例 カールフィッシャー法 (Karl Fischer s method) 微量の水分を滴定で求める方法 試料を無水メタノールなどと振って水を抽出し これをカールフィッシャー試薬で滴定する カールフィッシャー試薬は ヨウ素 二酸化イオウ ピリジンを 1:3:10( モル比 ) の割合にメタノールに溶かしたもの 水の存在によってヨウ素が二酸化イオウによって定量的に還元され この両者がピリジンと化合して明るい黄色に変わる
student chemistry (2019), 1, 多価酸 1 価塩基滴定曲線と酸塩基滴定における学術用語についての考察 西野光太郎, 山口悟 * 茨城県立水戸第一高等学校化学部 茨城県水戸市三の丸 (2019 年 3 月 1 日受付 ;2019 年
 student chemistry () - 多価酸 価塩基滴定曲線と酸塩基滴定における学術用語についての考察 西野光太郎 山口悟 * 茨城県立水戸第一高等学校化学部 - 茨城県水戸市三の丸 -- ( 年 月 日受付 ; 年 月 日受理 ) Abstract 高校の化学基礎の教科書 資料において 多価酸 価塩基滴定曲線 は一部の資料に掲載されている しかしながら 多価酸 価塩基滴定曲線 はどの教科書
student chemistry () - 多価酸 価塩基滴定曲線と酸塩基滴定における学術用語についての考察 西野光太郎 山口悟 * 茨城県立水戸第一高等学校化学部 - 茨城県水戸市三の丸 -- ( 年 月 日受付 ; 年 月 日受理 ) Abstract 高校の化学基礎の教科書 資料において 多価酸 価塩基滴定曲線 は一部の資料に掲載されている しかしながら 多価酸 価塩基滴定曲線 はどの教科書
3
 ビタミン C の滴定 1. 研究の動機 研究者名森祐作番場孔士池井大介森本恵一指導教諭黒田順子先生 わたしたちにとって身近なビタミン C は どのようなものに多く含まれているのか またその量はどのくらいなのか という疑問が浮かんだため調べてみることにした 2. 研究の概要 ビタミンC 滴定の概要 ビタミンC( アスコルビン酸 ) はとても酸化されやすい物質で よく食品の酸化防止剤として使われている
ビタミン C の滴定 1. 研究の動機 研究者名森祐作番場孔士池井大介森本恵一指導教諭黒田順子先生 わたしたちにとって身近なビタミン C は どのようなものに多く含まれているのか またその量はどのくらいなのか という疑問が浮かんだため調べてみることにした 2. 研究の概要 ビタミンC 滴定の概要 ビタミンC( アスコルビン酸 ) はとても酸化されやすい物質で よく食品の酸化防止剤として使われている
平成27年度 前期日程 化学 解答例
 受験番号 平成 27 年度前期日程 化学 ( その 1) 解答用紙 工学部 応用化学科 志願者は第 1 問 ~ 第 4 問を解答せよ 農学部 生物資源科学科, 森林科学科 志願者は第 1 問と第 2 問を解答せよ 第 1 問 [ 二酸化炭素が発生する反応の化学反応式 ] 点 NaHCO 3 + HCl NaCl + H 2 O + CO 2 CO 2 の物質量を x mol とすると, 気体の状態方程式より,
受験番号 平成 27 年度前期日程 化学 ( その 1) 解答用紙 工学部 応用化学科 志願者は第 1 問 ~ 第 4 問を解答せよ 農学部 生物資源科学科, 森林科学科 志願者は第 1 問と第 2 問を解答せよ 第 1 問 [ 二酸化炭素が発生する反応の化学反応式 ] 点 NaHCO 3 + HCl NaCl + H 2 O + CO 2 CO 2 の物質量を x mol とすると, 気体の状態方程式より,
基礎化学 Ⅰ 第 5 講原子量とモル数 第 5 講原子量とモル数 1 原子量 (1) 相対質量 まず, 大きさの復習から 原子 ピンポン玉 原子の直径は, 約 1 億分の 1cm ( 第 1 講 ) 原子とピンポン玉の関係は, ピンポン玉と地球の関係と同じくらいの大きさです 地球 では, 原子 1
 第 5 講原子量とモル数 1 原子量 (1) 相対質量 まず, 大きさの復習から 原子 ピンポン玉 原子の直径は, 約 1 億分の 1cm ( 第 1 講 ) 原子とピンポン玉の関係は, ピンポン玉と地球の関係と同じくらいの大きさです 地球 では, 原子 1 つの質量は? 水素原子は,0.167 10-23 g 酸素原子は,2.656 10-23 g 炭素原子は,1.993 10-23 g 原子の質量は,
第 5 講原子量とモル数 1 原子量 (1) 相対質量 まず, 大きさの復習から 原子 ピンポン玉 原子の直径は, 約 1 億分の 1cm ( 第 1 講 ) 原子とピンポン玉の関係は, ピンポン玉と地球の関係と同じくらいの大きさです 地球 では, 原子 1 つの質量は? 水素原子は,0.167 10-23 g 酸素原子は,2.656 10-23 g 炭素原子は,1.993 10-23 g 原子の質量は,
木村の理論化学小ネタ 緩衝液 緩衝液とは, 酸や塩基を加えても,pH が変化しにくい性質をもつ溶液のことである A. 共役酸と共役塩基 弱酸 HA の水溶液中での電離平衡と共役酸 共役塩基 弱酸 HA の電離平衡 HA + H 3 A にお
 緩衝液 緩衝液とは, 酸や塩基を加えても,pH が変化しにくい性質をもつ溶液のことである A. 酸と塩基 弱酸 HA の水溶液中での電離平衡と酸 塩基 弱酸 HA の電離平衡 HA H 3 A において, O H O ( HA H A ) HA H O H 3O A の反応に注目すれば, HA が放出した H を H O が受け取るから,HA は酸,H O は塩基である HA H O H 3O A
緩衝液 緩衝液とは, 酸や塩基を加えても,pH が変化しにくい性質をもつ溶液のことである A. 酸と塩基 弱酸 HA の水溶液中での電離平衡と酸 塩基 弱酸 HA の電離平衡 HA H 3 A において, O H O ( HA H A ) HA H O H 3O A の反応に注目すれば, HA が放出した H を H O が受け取るから,HA は酸,H O は塩基である HA H O H 3O A
(b) 精密さ 精密度 * precision 測定値のばらつきの程度 標準偏差の大きさに相当する (c) 精度 accuracy 測定結果の正確さと精密さを含めた 測定量の真の値との一致の度合い 補正 correction は 正確さを期すために行われる ( 系統誤差を打ち消すために行われる )
 誤差の話 014.4.4. 内容 誤差の話... 1 正確さ 精密さ 精度... 1 不確かさの表示... 誤差のモデル... 誤差の伝播則... 3 測定の際の注意点 独立でかたよりのない測定の実現... 4 容量分析に見る誤差... 4 問題... 6 誤差の話 正確さ 精密さ 精度 測定値の精確さあるいは不確かさをめぐっては 品質工学の長足の進歩なども背景に この0 年余りの間にさまざまな概念の整理が行われてきた
誤差の話 014.4.4. 内容 誤差の話... 1 正確さ 精密さ 精度... 1 不確かさの表示... 誤差のモデル... 誤差の伝播則... 3 測定の際の注意点 独立でかたよりのない測定の実現... 4 容量分析に見る誤差... 4 問題... 6 誤差の話 正確さ 精密さ 精度 測定値の精確さあるいは不確かさをめぐっては 品質工学の長足の進歩なども背景に この0 年余りの間にさまざまな概念の整理が行われてきた
科学先取り岡山コース ( 大学先取り 化学分野 ) 2008 年 12 月 13 日 ( 土 ) 担当 : 大久保貴広 ( 岡山大学大学院自然科学研究科 ) 1 はじめに高校までの化学では 先人たちの努力により解き明かされた物質や基本的な現象を中心に勉強していることと思います それ故 覚えなければな
 科学先取り岡山コース ( 大学先取り 化学 ) キレート滴定による金属イオンの定量 ミネラルウォーターの硬度を求める 2008/12/13 科学先取り岡山コース ( 大学先取り 化学分野 ) 2008 年 12 月 13 日 ( 土 ) 担当 : 大久保貴広 ( 岡山大学大学院自然科学研究科 ) 1 はじめに高校までの化学では 先人たちの努力により解き明かされた物質や基本的な現象を中心に勉強していることと思います
科学先取り岡山コース ( 大学先取り 化学 ) キレート滴定による金属イオンの定量 ミネラルウォーターの硬度を求める 2008/12/13 科学先取り岡山コース ( 大学先取り 化学分野 ) 2008 年 12 月 13 日 ( 土 ) 担当 : 大久保貴広 ( 岡山大学大学院自然科学研究科 ) 1 はじめに高校までの化学では 先人たちの努力により解き明かされた物質や基本的な現象を中心に勉強していることと思います
Word Pro - matome_7_酸と塩基.lwp
 酸と 酸と 酸 acid 亜硫酸 pka =.6 pka =.9 酸 acid ( : 酸, すっぱいもの a : 酸の, すっぱい ) 酸性 p( ) 以下 酸っぱい味 ( 酸味 ) を持つ リトマス ( ) BTB( ) 金属と反応して ( ) を発生 ( 例 )Z l Zl リン酸 P pka =.5 pka =. pka =.8 P P P P P P P 酸性のもと 水素イオン 塩化水素
酸と 酸と 酸 acid 亜硫酸 pka =.6 pka =.9 酸 acid ( : 酸, すっぱいもの a : 酸の, すっぱい ) 酸性 p( ) 以下 酸っぱい味 ( 酸味 ) を持つ リトマス ( ) BTB( ) 金属と反応して ( ) を発生 ( 例 )Z l Zl リン酸 P pka =.5 pka =. pka =.8 P P P P P P P 酸性のもと 水素イオン 塩化水素
すとき, モサプリドのピーク面積の相対標準偏差は 2.0% 以下である. * 表示量 溶出規格 規定時間 溶出率 10mg/g 45 分 70% 以上 * モサプリドクエン酸塩無水物として モサプリドクエン酸塩標準品 C 21 H 25 ClFN 3 O 3 C 6 H 8 O 7 :
 モサプリドクエン酸塩散 Mosapride Citrate Powder 溶出性 6.10 本品の表示量に従いモサプリドクエン酸塩無水物 (C 21 H 25 ClFN 3 O 3 C 6 H 8 O 7 ) 約 2.5mgに対応する量を精密に量り, 試験液に溶出試験第 2 液 900mLを用い, パドル法により, 毎分 50 回転で試験を行う. 溶出試験を開始し, 規定時間後, 溶出液 20mL
モサプリドクエン酸塩散 Mosapride Citrate Powder 溶出性 6.10 本品の表示量に従いモサプリドクエン酸塩無水物 (C 21 H 25 ClFN 3 O 3 C 6 H 8 O 7 ) 約 2.5mgに対応する量を精密に量り, 試験液に溶出試験第 2 液 900mLを用い, パドル法により, 毎分 50 回転で試験を行う. 溶出試験を開始し, 規定時間後, 溶出液 20mL
Microsoft Word - VBA基礎(2).docx
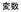 変数 test1 を実行してみてください 結果はメッセージボックスに 100 と表示されるはずです Sub test1() a = 10 このプルグラムでは a という文字がつかわれています MsgBox の機能はこの命令に続くものを画面に表示することで MsgBox a * a す つまり a*a を表示しています プログラムでは * は掛け算を意味しますの で画面に 100 が表示されたということは
変数 test1 を実行してみてください 結果はメッセージボックスに 100 と表示されるはずです Sub test1() a = 10 このプルグラムでは a という文字がつかわれています MsgBox の機能はこの命令に続くものを画面に表示することで MsgBox a * a す つまり a*a を表示しています プログラムでは * は掛け算を意味しますの で画面に 100 が表示されたということは
A 通 則 1. 添加物の適否は, 別に規定するもののほか, 通則, 一般試験法, 成分規格 保存基準各条等の規定によって判定する ただし, 性状の項目の形状は, 参考に供したもので, 適否の判定基準を示すものではない 2. 物質名の前後に を付けたものは, 成分規格 保存基準各条に規定する添加物を
 A 通 則 A 通 則 1. 添加物の適否は, 別に規定するもののほか, 通則, 一般試験法, 成分規格 保存基準各条等の規定によって判定する ただし, 性状の項目の形状は, 参考に供したもので, 適否の判定基準を示すものではない 2. 物質名の前後に を付けたものは, 成分規格 保存基準各条に規定する添加物を示す ただし, 成分規格 保存基準各条の表題, 製造基準及び使用基準ではこれを付けない 3.
A 通 則 A 通 則 1. 添加物の適否は, 別に規定するもののほか, 通則, 一般試験法, 成分規格 保存基準各条等の規定によって判定する ただし, 性状の項目の形状は, 参考に供したもので, 適否の判定基準を示すものではない 2. 物質名の前後に を付けたものは, 成分規格 保存基準各条に規定する添加物を示す ただし, 成分規格 保存基準各条の表題, 製造基準及び使用基準ではこれを付けない 3.
Microsoft Word - basic_15.doc
 分析の原理 15 電位差測定装置の原理と応用 概要 電位差測定法は 溶液内の目的成分の濃度 ( 活量 ) を作用電極と参照電極の起電力差から測定し 溶液中のイオン濃度や酸化還元電位の測定に利用されています また 滴定と組み合わせて当量点の決定を電極電位変化より行う電位差滴定法もあり 電気化学測定法の一つとして古くから研究 応用されています 本編では 電位差測定装置の原理を解説し その応用装置である
分析の原理 15 電位差測定装置の原理と応用 概要 電位差測定法は 溶液内の目的成分の濃度 ( 活量 ) を作用電極と参照電極の起電力差から測定し 溶液中のイオン濃度や酸化還元電位の測定に利用されています また 滴定と組み合わせて当量点の決定を電極電位変化より行う電位差滴定法もあり 電気化学測定法の一つとして古くから研究 応用されています 本編では 電位差測定装置の原理を解説し その応用装置である
土壌溶出量試験(簡易分析)
 土壌中の重金属等の 簡易 迅速分析法 標準作業手順書 * 技術名 : 吸光光度法による重金属等のオンサイト 簡易分析法 ( 超音波による前処理 ) 使用可能な分析項目 : 溶出量 : 六価クロム ふっ素 ほう素 含有量 : 六価クロム ふっ素 ほう素 実証試験者 : * 本手順書は実証試験者が作成したものである なお 使用可能な技術及び分析項目等の記載部分を抜粋して掲載した 1. 適用範囲この標準作業手順書は
土壌中の重金属等の 簡易 迅速分析法 標準作業手順書 * 技術名 : 吸光光度法による重金属等のオンサイト 簡易分析法 ( 超音波による前処理 ) 使用可能な分析項目 : 溶出量 : 六価クロム ふっ素 ほう素 含有量 : 六価クロム ふっ素 ほう素 実証試験者 : * 本手順書は実証試験者が作成したものである なお 使用可能な技術及び分析項目等の記載部分を抜粋して掲載した 1. 適用範囲この標準作業手順書は
1 次の問い ( 問 1~ 問 5) に答えよ (23 点 ) 問 1 次の単位変換のうち, 正しいもののみをすべて含む組み合わせは どれか マーク式解答欄 1 (a) 1.0 kg = mg (b) 1.0 dl = ml (c) 1.0 g/cm 3 = 1.
 問 1~ 問 25 の解答を, 指定された解答欄にマークせよ 必要があれば, 次の数値を用いよ 原子量 : H = 1.0, C = 12, N = 14, O = 16, Na = 23, S = 32, Cl = 35.5, Ca = 40, Cu = 64, Zn = 65 気体定数 :8.3 10 3 Pa L/(K mol) ファラデー定数 :9.65 10 4 C/mol セルシウス温度目盛りのゼロ点
問 1~ 問 25 の解答を, 指定された解答欄にマークせよ 必要があれば, 次の数値を用いよ 原子量 : H = 1.0, C = 12, N = 14, O = 16, Na = 23, S = 32, Cl = 35.5, Ca = 40, Cu = 64, Zn = 65 気体定数 :8.3 10 3 Pa L/(K mol) ファラデー定数 :9.65 10 4 C/mol セルシウス温度目盛りのゼロ点
<4D F736F F D2095BD90AC E93788D4C88E689C88A778BB389C88BB388E78A778CA48B868C6F94EF95F18D908F912E646F6378>
 平成 25 年度広域科学教科教育学研究経費報告書 研究課題 過酸化水素分解反応を利用した物理化学的考察に関する基礎検討 研究代表者 : 國仙久雄 研究メンバー : 生尾光 1. 緒言本申請で扱う鉄イオンを触媒とした過酸化水素分解反応速度に関する内容は高等学校 化学 で 発展 に含まれ 必ずしも全ての教科書で取り上げられない内容である しかしながら この化学反応を利用した実験を行うことで 化学を学習する際に重要な化学反応に関する物理化学的実験と思考法の獲得に関するプログラムの開発が可能となる
平成 25 年度広域科学教科教育学研究経費報告書 研究課題 過酸化水素分解反応を利用した物理化学的考察に関する基礎検討 研究代表者 : 國仙久雄 研究メンバー : 生尾光 1. 緒言本申請で扱う鉄イオンを触媒とした過酸化水素分解反応速度に関する内容は高等学校 化学 で 発展 に含まれ 必ずしも全ての教科書で取り上げられない内容である しかしながら この化学反応を利用した実験を行うことで 化学を学習する際に重要な化学反応に関する物理化学的実験と思考法の獲得に関するプログラムの開発が可能となる
木村の化学重要問題集 01 解答編解説補充 H S H HS ( 第 1 電離平衡 ) HS H S ( 第 電離平衡 ) そこで溶液を中性または塩基性にすることにより, つまり [ H ] を小さくすることにより, 上の電離平衡を右に片寄らせ,[ S ] を大きくする 193. 陽イオン分析 配位
![木村の化学重要問題集 01 解答編解説補充 H S H HS ( 第 1 電離平衡 ) HS H S ( 第 電離平衡 ) そこで溶液を中性または塩基性にすることにより, つまり [ H ] を小さくすることにより, 上の電離平衡を右に片寄らせ,[ S ] を大きくする 193. 陽イオン分析 配位 木村の化学重要問題集 01 解答編解説補充 H S H HS ( 第 1 電離平衡 ) HS H S ( 第 電離平衡 ) そこで溶液を中性または塩基性にすることにより, つまり [ H ] を小さくすることにより, 上の電離平衡を右に片寄らせ,[ S ] を大きくする 193. 陽イオン分析 配位](/thumbs/91/107310906.jpg) 木村の化学重要問題集 01 解答編解説補充 1. 無機物質の性質 反応 187. 気体の製法と性質補足ネスラー試薬とアンモニアの反応 1.. ネスラー試薬 [ HgI ] の調製 KI KI Hg ¾¾ HgI ¾¾ [ HgI ] 赤色沈殿. ネスラー試薬とアンモニアの反応 [ HgI ] ( NH ) [ ] NH HgI ( 微量 : 黄色, 多量 : 赤褐色 ) 190. 陽イオンの分離と性質
木村の化学重要問題集 01 解答編解説補充 1. 無機物質の性質 反応 187. 気体の製法と性質補足ネスラー試薬とアンモニアの反応 1.. ネスラー試薬 [ HgI ] の調製 KI KI Hg ¾¾ HgI ¾¾ [ HgI ] 赤色沈殿. ネスラー試薬とアンモニアの反応 [ HgI ] ( NH ) [ ] NH HgI ( 微量 : 黄色, 多量 : 赤褐色 ) 190. 陽イオンの分離と性質
SO の場合 Leis の酸塩基説 ( 非プロトン性溶媒までも摘要可 一般化 ) B + B の化学反応の酸と塩基 SO + + SO SO + + SO 酸 塩基 酸 塩基 SO は酸にも塩基にもなっている 酸の強さ 酸が強い = 塩基へプロトンを供与する能力が大きい 強酸 ( 優れたプロトン供与
 溶液溶媒 + 溶質 均一な相 溶質を溶かしている物質 溶けている物質 固体 + 液体液体 + 固体 溶質 (solute) イオンの形に解離して溶けているもの ( 電解質 ) 酸と塩基 Copyrigt: A.Asno 1 水素イオン濃度 (ydrogenion concentrtion) 水素イオン指数 (ydrogenion exponent; p) 水の電離 O + O O + + O O +
溶液溶媒 + 溶質 均一な相 溶質を溶かしている物質 溶けている物質 固体 + 液体液体 + 固体 溶質 (solute) イオンの形に解離して溶けているもの ( 電解質 ) 酸と塩基 Copyrigt: A.Asno 1 水素イオン濃度 (ydrogenion concentrtion) 水素イオン指数 (ydrogenion exponent; p) 水の電離 O + O O + + O O +
キレート滴定2014
 キレート滴定 本実験の目的本実験では 水道水や天然水に含まれるミネラル成分の指標である 硬度 を EDTA Na 塩 (EDTA:Ethylene Diamine Tetra Acetic acid) を利用して分析する手法を学ぶ さらに本手法を利用して 水道水および二種類の天然水の総硬度を決定する 調査項目キレート 標準溶液と標定 EDTA の構造ならびに性質 キレート生成定数 ( 安定度定数 )
キレート滴定 本実験の目的本実験では 水道水や天然水に含まれるミネラル成分の指標である 硬度 を EDTA Na 塩 (EDTA:Ethylene Diamine Tetra Acetic acid) を利用して分析する手法を学ぶ さらに本手法を利用して 水道水および二種類の天然水の総硬度を決定する 調査項目キレート 標準溶液と標定 EDTA の構造ならびに性質 キレート生成定数 ( 安定度定数 )
注釈 * ここでニッケルジメチルグリオキシム錯体としてのニッケルの重量分析を行う場合 恒量値を得るために乾燥操作が必要だが それにはかなりの時間を要するであろう ** この方法は, 銅の含有量が 0.5% 未満の合金において最も良い結果が得られる 化学物質および試薬 合金試料, ~0.5 g, ある
 問題 27. 錯滴定によるニッケル合金およびニッケル銅合金中のニッケルの定 量 ニッケルは銅 鉄 クロムなどの金属と単相の固溶体を形成し ニッケルと銅は制限なく相溶する 白銅とも呼ばれている銅ニッケル合金は 組成に依存して異なる性質を示す 最も利用されている白銅は 10~45 % のニッケルを含んでいる 70-90 % の銅を含むニッケル合金は, 高い腐食耐性 電気伝導性 延性 高温耐性を有するため
問題 27. 錯滴定によるニッケル合金およびニッケル銅合金中のニッケルの定 量 ニッケルは銅 鉄 クロムなどの金属と単相の固溶体を形成し ニッケルと銅は制限なく相溶する 白銅とも呼ばれている銅ニッケル合金は 組成に依存して異なる性質を示す 最も利用されている白銅は 10~45 % のニッケルを含んでいる 70-90 % の銅を含むニッケル合金は, 高い腐食耐性 電気伝導性 延性 高温耐性を有するため
ポリソルベート 80
 1/5 HIRANUMA APPLICATION DATA 水分データ シリーズデータ No 11 14/9/30 水分 1. 測定の概要 医薬品 逆滴定ポリソルベート 80 シリーズでは カールフィッシャー容量滴定法を採用しています 容量滴定法では 試料中の 水とカールフィッシャー試薬を反応させ 試薬中のヨウ素の消費量をもとに水分量を求めます H2O + I2 + SO2 + 3RN + CH3OH
1/5 HIRANUMA APPLICATION DATA 水分データ シリーズデータ No 11 14/9/30 水分 1. 測定の概要 医薬品 逆滴定ポリソルベート 80 シリーズでは カールフィッシャー容量滴定法を採用しています 容量滴定法では 試料中の 水とカールフィッシャー試薬を反応させ 試薬中のヨウ素の消費量をもとに水分量を求めます H2O + I2 + SO2 + 3RN + CH3OH
FdText理科1年
 中学理科 3 年 : 酸とアルカリ [ http://www.fdtext.com/dat/ ] [ 要点 ] 酸の性質 青色リトマスを赤に変える BTB 溶液を黄色に変える あえん金属 ( 亜鉛, マグネシウム, 鉄など ) と反応して水素を発生させる アルカリの性質 赤色リトマスを青色に変える BTB 溶液を青色に変える フェノールフタレイン溶液を赤色に変える ひふタンパク質をとかす ( 皮膚につけるとぬるぬるする
中学理科 3 年 : 酸とアルカリ [ http://www.fdtext.com/dat/ ] [ 要点 ] 酸の性質 青色リトマスを赤に変える BTB 溶液を黄色に変える あえん金属 ( 亜鉛, マグネシウム, 鉄など ) と反応して水素を発生させる アルカリの性質 赤色リトマスを青色に変える BTB 溶液を青色に変える フェノールフタレイン溶液を赤色に変える ひふタンパク質をとかす ( 皮膚につけるとぬるぬるする
必要があれば, 次の数値を使いなさい 原子量 O= 標準状態で mol の気体が占める体積. L 問題文中の体積の単位記号 L は, リットルを表す Ⅰ 次の問いに答えなさい 問 飲料水の容器であるペットボトルに使われているプラスチックを, 次の中から つ選び, 番号をマークしなさい ポリエチレン
 0 年度一般入試前期 A 日程 ( 月 日実施 ) 化学問題 (7 ページ 7 ページ ) 問題は大問 Ⅰ Ⅳ までありますが 一部 他科目との共通問題となっています 大問 Ⅰ は 化学基礎 + 生物基礎 の大問 Ⅰ と共通の問題です 大問 Ⅱ は 化学基礎 + 生物基礎 の大問 Ⅱ と共通の問題です 7 必要があれば, 次の数値を使いなさい 原子量 O= 標準状態で mol の気体が占める体積.
0 年度一般入試前期 A 日程 ( 月 日実施 ) 化学問題 (7 ページ 7 ページ ) 問題は大問 Ⅰ Ⅳ までありますが 一部 他科目との共通問題となっています 大問 Ⅰ は 化学基礎 + 生物基礎 の大問 Ⅰ と共通の問題です 大問 Ⅱ は 化学基礎 + 生物基礎 の大問 Ⅱ と共通の問題です 7 必要があれば, 次の数値を使いなさい 原子量 O= 標準状態で mol の気体が占める体積.
31608 要旨 ルミノール発光 3513 後藤唯花 3612 熊﨑なつみ 3617 新野彩乃 3619 鈴木梨那 私たちは ルミノール反応で起こる化学発光が強い光で長時間続く条件について興味をもち 研究を行った まず触媒の濃度に着目し 1~9% の値で実験を行ったところ触媒濃度が低いほど強い光で長
 31608 要旨 ルミノール発光 3513 後藤唯花 3612 熊﨑なつみ 3617 新野彩乃 3619 鈴木梨那 私たちは ルミノール反応で起こる化学発光が強い光で長時間続く条件について興味をもち 研究を行った まず触媒の濃度に着目し 1~9% の値で実験を行ったところ触媒濃度が低いほど強い光で長時間発光した 次にルミノール溶液の液温に着目し 0 ~60 にて実験を行ったところ 温度が低いほど強く発光した
31608 要旨 ルミノール発光 3513 後藤唯花 3612 熊﨑なつみ 3617 新野彩乃 3619 鈴木梨那 私たちは ルミノール反応で起こる化学発光が強い光で長時間続く条件について興味をもち 研究を行った まず触媒の濃度に着目し 1~9% の値で実験を行ったところ触媒濃度が低いほど強い光で長時間発光した 次にルミノール溶液の液温に着目し 0 ~60 にて実験を行ったところ 温度が低いほど強く発光した
PowerPoint プレゼンテーション
 電気 電子計測 第 2 回 http://cobayasi.com/keisoku/2nd/2nd.pdf 計測の基礎 ( テキストp9-p18) 1. どのような計測法があるか 2. 測定値は正しいだろうか 3. 測る時の単位を調べよう 1. どのような計測法があるか 測定量を 直接読むか? 間接的に読むか? 直接法測定量を 同じ種類の基準量と直接比較して測定する方法 測定量を直接読むことができる
電気 電子計測 第 2 回 http://cobayasi.com/keisoku/2nd/2nd.pdf 計測の基礎 ( テキストp9-p18) 1. どのような計測法があるか 2. 測定値は正しいだろうか 3. 測る時の単位を調べよう 1. どのような計測法があるか 測定量を 直接読むか? 間接的に読むか? 直接法測定量を 同じ種類の基準量と直接比較して測定する方法 測定量を直接読むことができる
品目 1 四アルキル鉛及びこれを含有する製剤 (1) 酸化隔離法多量の次亜塩素酸塩水溶液を加えて分解させたのち 消石灰 ソーダ灰等を加えて処理し 沈殿濾過し更にセメントを加えて固化し 溶出試験を行い 溶出量が判定基準以下であることを確認して埋立処分する (2) 燃焼隔離法アフターバーナー及びスクラバ
 品目 1 四アルキル鉛及びこれを含有する製剤 (1) 酸化隔離法多量の次亜塩素酸塩水溶液を加えて分解させたのち 消石灰 ソーダ灰等を加えて処理し 沈殿濾過し更にセメントを加えて固化し 溶出試験を行い 溶出量が判定基準以下であることを確認して埋立処分する (2) 燃焼隔離法アフターバーナー及びスクラバー ( 洗浄液にアルカリ液 ) を具備した焼却炉の火室へ噴霧し焼却する 洗浄液に消石灰ソーダ灰等の水溶液を加えて処理し
品目 1 四アルキル鉛及びこれを含有する製剤 (1) 酸化隔離法多量の次亜塩素酸塩水溶液を加えて分解させたのち 消石灰 ソーダ灰等を加えて処理し 沈殿濾過し更にセメントを加えて固化し 溶出試験を行い 溶出量が判定基準以下であることを確認して埋立処分する (2) 燃焼隔離法アフターバーナー及びスクラバー ( 洗浄液にアルカリ液 ) を具備した焼却炉の火室へ噴霧し焼却する 洗浄液に消石灰ソーダ灰等の水溶液を加えて処理し
生化学実験に用いる単位と量 単位 濃度 1:SI 基本単位 SI 基本単位 ( メートル法単位系に基づく国際単位系 SI) を表 1.1 に示す 参考 :SI=Le Systeme International d'unites 表 4.1 SI 基本単位 物理量名称記号 長さ メートル m 質量 キ
 生化学実験に用いる単位と量 1:SI 基本単位 SI 基本単位 ( メートル法単位系に基づく国際単位系 SI) を表 1.1 に示す 参考 :SI=Le Systeme International d'unites 表 4.1 SI 基本単位 物理量名称記号 長さ メートル m 質量 キログラム kg 時間 秒 s 物質の量 モル mol 熱力学的温度 ケルビン K 電流 アンペア A 光度 カンデラ
生化学実験に用いる単位と量 1:SI 基本単位 SI 基本単位 ( メートル法単位系に基づく国際単位系 SI) を表 1.1 に示す 参考 :SI=Le Systeme International d'unites 表 4.1 SI 基本単位 物理量名称記号 長さ メートル m 質量 キログラム kg 時間 秒 s 物質の量 モル mol 熱力学的温度 ケルビン K 電流 アンペア A 光度 カンデラ
土壌含有量試験(簡易分析)
 土壌中の重金属の 簡易 迅速分析法 標準作業手順書 * 技術名 : ストリッピング ボルタンメトリー法 ( 超音波による前処理 ) 使用可能な分析項目 : 砒素溶出量, 砒素含有量 実証試験者 : 北斗電工株式会社 株式会社フィールドテック * 本手順書は実証試験者が作成したものである なお 使用可能な技術及び分析項目等の記載部分を抜粋して掲載した 1. 適用範囲この標準作業手順書は 環告 18 号に対応する土壌溶出量試験
土壌中の重金属の 簡易 迅速分析法 標準作業手順書 * 技術名 : ストリッピング ボルタンメトリー法 ( 超音波による前処理 ) 使用可能な分析項目 : 砒素溶出量, 砒素含有量 実証試験者 : 北斗電工株式会社 株式会社フィールドテック * 本手順書は実証試験者が作成したものである なお 使用可能な技術及び分析項目等の記載部分を抜粋して掲載した 1. 適用範囲この標準作業手順書は 環告 18 号に対応する土壌溶出量試験
ミリモル毎リットル mmol/l マイクロジーメンス毎センチメートル µs/cm 度 ( 角度 ) 5. 質量百分率を示すには % の記号を用いる 液体又は気体 100mL 中の物質量 (g) を示すには w/v% の記号を用いる 物質 100g 中の物質量 (ml) を示すには v/w% の記号を
 A 通則 1. 添加物の適否は 別に規定するもののほか 通則 一般試験法 成分規格 保存基準各条等の規定によって判定する ただし 性状の項目の固体の形状は 参考に供するもので 適否の判定基準を示すものではない 2. 物質名の前後に を付けたものは 成分規格 保存基準各条に規定する添加物を示す ただし 成分規格 保存基準各条の表題 製造基準及び使用基準ではこれを付けない 3. 物質名の次に ( ) で分子式又は組成式を付けたものは
A 通則 1. 添加物の適否は 別に規定するもののほか 通則 一般試験法 成分規格 保存基準各条等の規定によって判定する ただし 性状の項目の固体の形状は 参考に供するもので 適否の判定基準を示すものではない 2. 物質名の前後に を付けたものは 成分規格 保存基準各条に規定する添加物を示す ただし 成分規格 保存基準各条の表題 製造基準及び使用基準ではこれを付けない 3. 物質名の次に ( ) で分子式又は組成式を付けたものは
(Microsoft Word \203r\203^\203~\203\223\230_\225\266)
 31009 ビタミン C の保存と損失に関する研究 要旨実験 Ⅰ: ビタミン C が時間や熱などの影響を受けて損失することを知り どのような状態に置くとより損失するのか追及することを目的とする カボチャを用い インドフェノール法 ( 中和滴定 ) でビタミン C 量の変化を求めようとしたところ 結果に誤差が生じ正確な値を導くことができなかった そこで より精密に値を求めることができるヒドラジン法 (
31009 ビタミン C の保存と損失に関する研究 要旨実験 Ⅰ: ビタミン C が時間や熱などの影響を受けて損失することを知り どのような状態に置くとより損失するのか追及することを目的とする カボチャを用い インドフェノール法 ( 中和滴定 ) でビタミン C 量の変化を求めようとしたところ 結果に誤差が生じ正確な値を導くことができなかった そこで より精密に値を求めることができるヒドラジン法 (
<4D F736F F F696E74202D A E90B6979D89C8816B91E63195AA96EC816C82DC82C682DF8D758DC03189BB8A7795CF89BB82C68CB48E AA8E E9197BF2E >
 中学 2 年理科まとめ講座 第 1 分野 1. 化学変化と原子 分子 物質の成り立ち 化学変化 化学変化と物質の質量 基本の解説と問題 講師 : 仲谷のぼる 1 物質の成り立ち 物質のつくり 物質をつくる それ以上分けることができない粒を原子という いくつかの原子が結びついてできたものを分子という いろいろな物質のうち 1 種類の原子からできている物質を単体 2 種類以上の原子からできている物質を化合物という
中学 2 年理科まとめ講座 第 1 分野 1. 化学変化と原子 分子 物質の成り立ち 化学変化 化学変化と物質の質量 基本の解説と問題 講師 : 仲谷のぼる 1 物質の成り立ち 物質のつくり 物質をつくる それ以上分けることができない粒を原子という いくつかの原子が結びついてできたものを分子という いろいろな物質のうち 1 種類の原子からできている物質を単体 2 種類以上の原子からできている物質を化合物という
DVIOUT-酸と塩
 中和反応 中和反応は H + + OH H 2 O 酸の溶質分子と塩基の溶質分子それぞれのイオン価数に注目するまた, 酸, 塩基の強さにも注目する イオンのモル数に注目中和は, 酸性溶液から出る水素イオンと塩基性溶液から出る 水酸化物イオンの物質量が一致したときに起こる 最も簡単な 例は塩酸と水酸化ナトリウム水溶液である 塩酸は 1 価の酸 で, 水酸化ナトリウム水溶液は 1 価の塩基なので HCl
中和反応 中和反応は H + + OH H 2 O 酸の溶質分子と塩基の溶質分子それぞれのイオン価数に注目するまた, 酸, 塩基の強さにも注目する イオンのモル数に注目中和は, 酸性溶液から出る水素イオンと塩基性溶液から出る 水酸化物イオンの物質量が一致したときに起こる 最も簡単な 例は塩酸と水酸化ナトリウム水溶液である 塩酸は 1 価の酸 で, 水酸化ナトリウム水溶液は 1 価の塩基なので HCl
Microsoft PowerPoint 基礎実験2
 環境基礎実験 2005.10.22( 土 ) 環境システム学科 1 年必修担当者 : 岩見, 宮脇, 伊藤, 大島 4-1 標準液の調製と標定 滴定とは, 溶液の反応体積を測定して定量分析を行う方法 定量しようとする物質の溶液 この物質と反応する物質の濃度既知溶液 ( 標準液 ) を用意し ビューレットを用いて滴定を行う 容量分析において標準液は分析の基礎その濃度は十分正確である必要大体の濃度の溶液を調整し
環境基礎実験 2005.10.22( 土 ) 環境システム学科 1 年必修担当者 : 岩見, 宮脇, 伊藤, 大島 4-1 標準液の調製と標定 滴定とは, 溶液の反応体積を測定して定量分析を行う方法 定量しようとする物質の溶液 この物質と反応する物質の濃度既知溶液 ( 標準液 ) を用意し ビューレットを用いて滴定を行う 容量分析において標準液は分析の基礎その濃度は十分正確である必要大体の濃度の溶液を調整し
醸造酢の全窒素分測定方法 ( ケルダール法 塩入奥田式蒸留 ) 手順書 1. 適用範囲 この方法は日本農林規格に定める醸造酢に適用する 2. 測定方法の概要 試料をケルダールフラスコに取り 電熱式分解台で分解した後 アンモニアを塩入 奥 田式蒸留装置等で水蒸気蒸留しビュレットを用いて滴定する 3.
 醸造酢の全窒素分 ( ケルダール法 ) 測定手順書 ページ 塩入奥田式蒸留 1 自動蒸留 9 共同試験結果 16 醸造酢の全窒素分測定方法 ( ケルダール法 塩入奥田式蒸留 ) 手順書 1. 適用範囲 この方法は日本農林規格に定める醸造酢に適用する 2. 測定方法の概要 試料をケルダールフラスコに取り 電熱式分解台で分解した後 アンモニアを塩入 奥 田式蒸留装置等で水蒸気蒸留しビュレットを用いて滴定する
醸造酢の全窒素分 ( ケルダール法 ) 測定手順書 ページ 塩入奥田式蒸留 1 自動蒸留 9 共同試験結果 16 醸造酢の全窒素分測定方法 ( ケルダール法 塩入奥田式蒸留 ) 手順書 1. 適用範囲 この方法は日本農林規格に定める醸造酢に適用する 2. 測定方法の概要 試料をケルダールフラスコに取り 電熱式分解台で分解した後 アンモニアを塩入 奥 田式蒸留装置等で水蒸気蒸留しビュレットを用いて滴定する
調査研究「教科等で考える異校種間の連携の工夫」〔理科〕
 事例 6 高等学校 化学 Ⅰ 学習指導案 平成 年 月 日 () 第 校時指導者教諭 学年第 1 学年生徒数 名 ( 男子 名女子 名 ) 1 単元名酸と塩基の反応 2 単元について (1) 単元観生徒は教科書の第 1 章で, 原子の構造が物質の性質を理解するうえで重要であること, さらに, 原子の電子配置モデルを用いたイオンを学習している また, 第 2 章では, 物質の量を表す概念として物質量とその単位のモルを,
事例 6 高等学校 化学 Ⅰ 学習指導案 平成 年 月 日 () 第 校時指導者教諭 学年第 1 学年生徒数 名 ( 男子 名女子 名 ) 1 単元名酸と塩基の反応 2 単元について (1) 単元観生徒は教科書の第 1 章で, 原子の構造が物質の性質を理解するうえで重要であること, さらに, 原子の電子配置モデルを用いたイオンを学習している また, 第 2 章では, 物質の量を表す概念として物質量とその単位のモルを,
Taro-化学3 酸塩基 最新版
 11 酸 塩基の反応 P oint.29 酸 塩基 ブレンステッドの酸 塩基 酸 水素イオンを 物質 塩基 水素イオンを 物質 NH3 + H2O NH4 + + OH - 酸 塩基の性質 1 リトマス紙 2 フェノールフタレイン溶液 3BTB 液 4 メチルオレンジ 5 金属と反応 6 味 7 水溶液中に存在するイオン 酸 塩基 酸 塩基の分類 1 価数による分類 1 価 2 価 3 価 酸 塩基
11 酸 塩基の反応 P oint.29 酸 塩基 ブレンステッドの酸 塩基 酸 水素イオンを 物質 塩基 水素イオンを 物質 NH3 + H2O NH4 + + OH - 酸 塩基の性質 1 リトマス紙 2 フェノールフタレイン溶液 3BTB 液 4 メチルオレンジ 5 金属と反応 6 味 7 水溶液中に存在するイオン 酸 塩基 酸 塩基の分類 1 価数による分類 1 価 2 価 3 価 酸 塩基
スライド 1
 計測工学第 12 回以降 測定値の誤差と精度編 2014 年 7 月 2 日 ( 水 )~7 月 16 日 ( 水 ) 知能情報工学科 横田孝義 1 授業計画 4/9 4/16 4/23 5/7 5/14 5/21 5/28 6/4 6/11 6/18 6/25 7/2 7/9 7/16 7/23 2 誤差とその取扱い 3 誤差 = 測定値 真の値 相対誤差 = 誤差 / 真の値 4 誤差 (error)
計測工学第 12 回以降 測定値の誤差と精度編 2014 年 7 月 2 日 ( 水 )~7 月 16 日 ( 水 ) 知能情報工学科 横田孝義 1 授業計画 4/9 4/16 4/23 5/7 5/14 5/21 5/28 6/4 6/11 6/18 6/25 7/2 7/9 7/16 7/23 2 誤差とその取扱い 3 誤差 = 測定値 真の値 相対誤差 = 誤差 / 真の値 4 誤差 (error)
Slide 1
 3. 溶解 沈殿反応 天然水の化学組成 大陸地殻表層 (mg kg ) 河川水 (mg kg ) Al 77.4.5 Fe 3.9.4 Ca 9.4 3.4 Na 5.7 5. 8.6.3 Mg 3.5 3.4 Andrews et al. (3) An introduction to Environmental Chemistry 天然水の特徴 天然水の金属イオンは主に岩石の風化により生じる ただし
3. 溶解 沈殿反応 天然水の化学組成 大陸地殻表層 (mg kg ) 河川水 (mg kg ) Al 77.4.5 Fe 3.9.4 Ca 9.4 3.4 Na 5.7 5. 8.6.3 Mg 3.5 3.4 Andrews et al. (3) An introduction to Environmental Chemistry 天然水の特徴 天然水の金属イオンは主に岩石の風化により生じる ただし
木村の有機化学小ネタ セルロース系再生繊維 再生繊維セルロースなど天然高分子物質を化学的処理により溶解後, 細孔から押し出し ( 紡糸 という), 再凝固させて繊維としたもの セルロース系の再生繊維には, ビスコースレーヨン, 銅アンモニア
 セルロース系再生繊維 再生繊維セルロースなど天然高分子物質を化学的処理により溶解後, 細孔から押し出し ( 紡糸 という), 再凝固させて繊維としたもの セルロース系の再生繊維には, ビスコースレーヨン, 銅アンモニアレーヨンがあり, タンパク質系では, カゼイン, 大豆タンパク質, 絹の糸くず, くず繭などからの再生繊維がある これに対し, セルロースなど天然の高分子物質の誘導体を紡糸して繊維としたものを半合成繊維と呼び,
セルロース系再生繊維 再生繊維セルロースなど天然高分子物質を化学的処理により溶解後, 細孔から押し出し ( 紡糸 という), 再凝固させて繊維としたもの セルロース系の再生繊維には, ビスコースレーヨン, 銅アンモニアレーヨンがあり, タンパク質系では, カゼイン, 大豆タンパク質, 絹の糸くず, くず繭などからの再生繊維がある これに対し, セルロースなど天然の高分子物質の誘導体を紡糸して繊維としたものを半合成繊維と呼び,
研究要旨 研究背景研究目的 意義研究手法結果 考察結論 展望 研究のタイトル 研究要旨 ( 概要 ) あなたの研究の全体像を文章で表現してみよう 乳酸菌を用いてハンドソープの殺菌力を上げる条件を調べる手を洗う時に どのくらいの時間をかければよいのかということと よく薄めて使うことがあるので薄めても効
 研究要旨 研究のタイトル 研究要旨 ( 概要 ) あなたの研究の全体像を文章で表現してみよう 乳酸菌を用いてハンドソープの殺菌力を上げる条件を調べる手を洗う時に どのくらいの時間をかければよいのかということと よく薄めて使うことがあるので薄めても効果があるのかということを調べようと考えた なので ハンドソープの殺菌効果が作用させる時間と濃度を変化させることでどう変わるのかを検証した 先輩方の研究より
研究要旨 研究のタイトル 研究要旨 ( 概要 ) あなたの研究の全体像を文章で表現してみよう 乳酸菌を用いてハンドソープの殺菌力を上げる条件を調べる手を洗う時に どのくらいの時間をかければよいのかということと よく薄めて使うことがあるので薄めても効果があるのかということを調べようと考えた なので ハンドソープの殺菌効果が作用させる時間と濃度を変化させることでどう変わるのかを検証した 先輩方の研究より
Problem P5
 問題 P5 メンシュトキン反応 三級アミンとハロゲン化アルキルの間の求核置換反応はメンシュトキン反応として知られている この実験では DABCO(1,4 ジアザビシクロ [2.2.2] オクタン というアミンと臭化ベンジルの間の反応速度式を調べる N N Ph Br N N Br DABCO Ph DABCO 分子に含まれるもう片方の窒素も さらに他の臭化ベンジルと反応する可能性がある しかし この実験では
問題 P5 メンシュトキン反応 三級アミンとハロゲン化アルキルの間の求核置換反応はメンシュトキン反応として知られている この実験では DABCO(1,4 ジアザビシクロ [2.2.2] オクタン というアミンと臭化ベンジルの間の反応速度式を調べる N N Ph Br N N Br DABCO Ph DABCO 分子に含まれるもう片方の窒素も さらに他の臭化ベンジルと反応する可能性がある しかし この実験では
Microsoft PowerPoint - Inoue-statistics [互換モード]
![Microsoft PowerPoint - Inoue-statistics [互換モード] Microsoft PowerPoint - Inoue-statistics [互換モード]](/thumbs/92/107910528.jpg) 誤差論 神戸大学大学院農学研究科 井上一哉 (Kazuya INOUE) 誤差論 2011 年度前期火曜クラス 1 講義内容 誤差と有効数字 (Slide No.2~8 Text p.76~78) 誤差の分布と標準偏差 (Slide No.9~18 Text p.78~80) 最確値とその誤差 (Slide No.19~25 Text p.80~81) 誤差の伝播 (Slide No.26~32 Text
誤差論 神戸大学大学院農学研究科 井上一哉 (Kazuya INOUE) 誤差論 2011 年度前期火曜クラス 1 講義内容 誤差と有効数字 (Slide No.2~8 Text p.76~78) 誤差の分布と標準偏差 (Slide No.9~18 Text p.78~80) 最確値とその誤差 (Slide No.19~25 Text p.80~81) 誤差の伝播 (Slide No.26~32 Text
留意点 指導面 物質量について物質を扱うとき, 体積や質量で表すことが多い しかし, 化学変化は, 物質の構成粒子が切り離されたり, 結合したりすることによっておこるため, 粒子の個数で表した方が都合がよい 一方, 物質の構成粒子は非常に小さく,1 個ずつ数えることはできない また, 私たちが日常取
 15 米 6,000 粒 ~ アボガドロ数を実感する ~ 難易度教材の入手日数準備時間実施時間 1 日 1 時間 50 分 目的と内容 物質量と粒子数, 質量, 気体の体積との関係につい て理解すること がこの単元の主なねらいである また, 粒子の数に基づく量の表し方である物質量の 概念を導入し, 物質量と質量, 気体の体積との関係につ いて理解させること がねらいである ここでは, 米など小さな粒子を数えることで,6.02
15 米 6,000 粒 ~ アボガドロ数を実感する ~ 難易度教材の入手日数準備時間実施時間 1 日 1 時間 50 分 目的と内容 物質量と粒子数, 質量, 気体の体積との関係につい て理解すること がこの単元の主なねらいである また, 粒子の数に基づく量の表し方である物質量の 概念を導入し, 物質量と質量, 気体の体積との関係につ いて理解させること がねらいである ここでは, 米など小さな粒子を数えることで,6.02
Microsoft PowerPoint - presentation2007_03_acid-base.ppt
 酸塩基平衡と中和滴定 ー復習ー酸塩基の定義 酸 (cid, ラテン語の cetum から と塩基 (se, [likli, アラビア語 lklj ( 植物の灰 J.R. Gluer ( アルカリは酸と相反するもので 塩はこれら つから構成される R. Boyle (79 青色リトマスが酸により赤変することを発見 J.L. GyLussc (775 酸には酸素酸と水素酸の 種類があると考える J. Lieig
酸塩基平衡と中和滴定 ー復習ー酸塩基の定義 酸 (cid, ラテン語の cetum から と塩基 (se, [likli, アラビア語 lklj ( 植物の灰 J.R. Gluer ( アルカリは酸と相反するもので 塩はこれら つから構成される R. Boyle (79 青色リトマスが酸により赤変することを発見 J.L. GyLussc (775 酸には酸素酸と水素酸の 種類があると考える J. Lieig
2019 年度大学入試センター試験解説 化学 第 1 問問 1 a 塩化カリウムは, カリウムイオン K + と塩化物イオン Cl - のイオン結合のみを含む物質であり, 共有結合を含まない ( 答 ) 1 1 b 黒鉛の結晶中では, 各炭素原子の 4 つの価電子のうち 3 つが隣り合う他の原子との
 219 年度大学入試センター試験解説 化学 第 1 問問 1 a 塩化カリウムは, カリウムイオン K + と塩化物イオン Cl - のイオン結合のみを含む物質であり, 共有結合を含まない ( 答 ) 1 1 b 黒鉛の結晶中では, 各炭素原子の 4 つの価電子のうち 3 つが隣り合う他の原子との共有結合に使われ, 残りの 1 つは結晶を構成する層上を自由に移動している そのため, 黒鉛は固体の状態で電気をよく通す
219 年度大学入試センター試験解説 化学 第 1 問問 1 a 塩化カリウムは, カリウムイオン K + と塩化物イオン Cl - のイオン結合のみを含む物質であり, 共有結合を含まない ( 答 ) 1 1 b 黒鉛の結晶中では, 各炭素原子の 4 つの価電子のうち 3 つが隣り合う他の原子との共有結合に使われ, 残りの 1 つは結晶を構成する層上を自由に移動している そのため, 黒鉛は固体の状態で電気をよく通す
日本食品成分表分析マニュアル第4章
 第 4 章 アミノ酸 34 一般のアミノ酸 *, ヒドロキシプロリン及びアンモニア * イソロイシン, ロイシン, リシン ( リジン ), フェニルアラニン, チロシン, トレオニン ( スレオニン ), バリン, ヒ スチジン, アルギニン, アラニン, アスパラギン酸 ( 注 1), グルタミン酸 ( 注 1), グリシン, プロリン, セリン 34 1. カラムクロマトグラフ法 適用食品全般に用いる
第 4 章 アミノ酸 34 一般のアミノ酸 *, ヒドロキシプロリン及びアンモニア * イソロイシン, ロイシン, リシン ( リジン ), フェニルアラニン, チロシン, トレオニン ( スレオニン ), バリン, ヒ スチジン, アルギニン, アラニン, アスパラギン酸 ( 注 1), グルタミン酸 ( 注 1), グリシン, プロリン, セリン 34 1. カラムクロマトグラフ法 適用食品全般に用いる
2004 年度センター化学 ⅠB p1 第 1 問問 1 a 水素結合 X HLY X,Y= F,O,N ( ) この形をもつ分子は 5 NH 3 である 1 5 b 昇華性の物質 ドライアイス CO 2, ヨウ素 I 2, ナフタレン 2 3 c 総電子数 = ( 原子番号 ) d CH 4 :6
 004 年度センター化学 ⅠB p 第 問問 a 水素結合 X HLY X,Y= F,O,N ( ) この形をもつ分子は 5 NH である 5 b 昇華性の物質 ドライアイス CO, ヨウ素 I, ナフタレン c 総電子数 = ( 原子番号 ) d CH 4 :6+ 4 = 0個 6+ 8= 4個 7+ 8= 5個 + 7= 8個 4 + 8= 0個 5 8= 6個 4 構造式からアプローチして電子式を書くと次のようになる
004 年度センター化学 ⅠB p 第 問問 a 水素結合 X HLY X,Y= F,O,N ( ) この形をもつ分子は 5 NH である 5 b 昇華性の物質 ドライアイス CO, ヨウ素 I, ナフタレン c 総電子数 = ( 原子番号 ) d CH 4 :6+ 4 = 0個 6+ 8= 4個 7+ 8= 5個 + 7= 8個 4 + 8= 0個 5 8= 6個 4 構造式からアプローチして電子式を書くと次のようになる
<4D F736F F D208EC08CB18C7689E68A E F AA957A82C682948C9F92E82E646F63>
 第 7 回 t 分布と t 検定 実験計画学 A.t 分布 ( 小標本に関する平均の推定と検定 ) 前々回と前回の授業では, 標本が十分に大きいあるいは母分散が既知であることを条件に正規分布を用いて推定 検定した. しかし, 母集団が正規分布し, 標本が小さい場合には, 標本分散から母分散を推定するときの不確実さを加味したt 分布を用いて推定 検定しなければならない. t 分布は標本分散の自由度 f(
第 7 回 t 分布と t 検定 実験計画学 A.t 分布 ( 小標本に関する平均の推定と検定 ) 前々回と前回の授業では, 標本が十分に大きいあるいは母分散が既知であることを条件に正規分布を用いて推定 検定した. しかし, 母集団が正規分布し, 標本が小さい場合には, 標本分散から母分散を推定するときの不確実さを加味したt 分布を用いて推定 検定しなければならない. t 分布は標本分散の自由度 f(
補足 中学校では塩基性ではなくアルカリ性という表現を使って学習する アルカリはアラビア語 (al qily) で, アル (al) は定冠詞, カリ (qily) はオカヒジキ属の植物を焼いた灰の意味 植物の灰には Na,K,Ca などの金属元素が含まれており, それに水を加えて溶かすと, NaOH
 酸 塩基の定義のいろいろ 酸と塩基の性質酸の水溶液の性質 1 すっぱい味がする 2 青色リトマス紙を赤色に変える 3 BTB( ブロムチモールブルー ) 溶液を黄色に変える 4 多くの金属 (Mg: マグネシウム,Zn: 亜鉛,Fe: 鉄など ) と反応し, 水素を発生 Zn2HCl ZnCl 2 H 2 ( イオン反応式で表すと,Zn2H Zn 2 H 2 ) 酸の水溶液が以上の性質をもつのは,
酸 塩基の定義のいろいろ 酸と塩基の性質酸の水溶液の性質 1 すっぱい味がする 2 青色リトマス紙を赤色に変える 3 BTB( ブロムチモールブルー ) 溶液を黄色に変える 4 多くの金属 (Mg: マグネシウム,Zn: 亜鉛,Fe: 鉄など ) と反応し, 水素を発生 Zn2HCl ZnCl 2 H 2 ( イオン反応式で表すと,Zn2H Zn 2 H 2 ) 酸の水溶液が以上の性質をもつのは,
Microsoft Word - H29統合版.doc
 毒物劇物取扱者試験 (14) ( 平成 29 年 8 月 8 日 ) 問 26 混合物の分離に関する次の a~c の記述について その操作方法として正しい組み合わせを下表から一つ選び その番号を解答用紙に記入しなさい a. 沸点の差を利用して 液体の混合物を適当な温度範囲に区切って蒸留し 留出物 ( 蒸留によって得られる物質 ) を分離する操作 b. ろ紙やシリカゲルのような吸着剤に 物質が吸着される強さの違いを利用して
毒物劇物取扱者試験 (14) ( 平成 29 年 8 月 8 日 ) 問 26 混合物の分離に関する次の a~c の記述について その操作方法として正しい組み合わせを下表から一つ選び その番号を解答用紙に記入しなさい a. 沸点の差を利用して 液体の混合物を適当な温度範囲に区切って蒸留し 留出物 ( 蒸留によって得られる物質 ) を分離する操作 b. ろ紙やシリカゲルのような吸着剤に 物質が吸着される強さの違いを利用して
CHEMISTRY: ART, SCIENCE, FUN THEORETICAL EXAMINATION ANSWER SHEETS JULY 20, 2007 MOSCOW, RUSSIA Official version team of Japan.
 CEMISTRY: ART, SCIENCE, FUN TEORETICAL EXAMINATION ANSWER SEETS JULY 20, 2007 MOSCOW, RUSSIA 1 Quest. 1.1 1.2 2.1 3.1 3.2 3.3 3.4 Tot Points Student code: Marks 3 3 2 4.5 2 4 6 24.5 7 1.1.1 構造 プロパンジアール
CEMISTRY: ART, SCIENCE, FUN TEORETICAL EXAMINATION ANSWER SEETS JULY 20, 2007 MOSCOW, RUSSIA 1 Quest. 1.1 1.2 2.1 3.1 3.2 3.3 3.4 Tot Points Student code: Marks 3 3 2 4.5 2 4 6 24.5 7 1.1.1 構造 プロパンジアール
Microsoft PowerPoint - 基礎・経済統計6.ppt
 . 確率変数 基礎 経済統計 6 確率分布 事象を数値化したもの ( 事象ー > 数値 の関数 自然に数値されている場合 さいころの目 量的尺度 数値化が必要な場合 質的尺度, 順序的尺度 それらの尺度に数値を割り当てる 例えば, コインの表が出たら, 裏なら 0. 離散確率変数と連続確率変数 確率変数の値 連続値をとるもの 身長, 体重, 実質 GDP など とびとびの値 離散値をとるもの 新生児の性別
. 確率変数 基礎 経済統計 6 確率分布 事象を数値化したもの ( 事象ー > 数値 の関数 自然に数値されている場合 さいころの目 量的尺度 数値化が必要な場合 質的尺度, 順序的尺度 それらの尺度に数値を割り当てる 例えば, コインの表が出たら, 裏なら 0. 離散確率変数と連続確率変数 確率変数の値 連続値をとるもの 身長, 体重, 実質 GDP など とびとびの値 離散値をとるもの 新生児の性別
EBNと疫学
 推定と検定 57 ( 復習 ) 記述統計と推測統計 統計解析は大きく 2 つに分けられる 記述統計 推測統計 記述統計 観察集団の特性を示すもの 代表値 ( 平均値や中央値 ) や ばらつきの指標 ( 標準偏差など ) 図表を効果的に使う 推測統計 観察集団のデータから母集団の特性を 推定 する 平均 / 分散 / 係数値などの推定 ( 点推定 ) 点推定値のばらつきを調べる ( 区間推定 ) 検定統計量を用いた検定
推定と検定 57 ( 復習 ) 記述統計と推測統計 統計解析は大きく 2 つに分けられる 記述統計 推測統計 記述統計 観察集団の特性を示すもの 代表値 ( 平均値や中央値 ) や ばらつきの指標 ( 標準偏差など ) 図表を効果的に使う 推測統計 観察集団のデータから母集団の特性を 推定 する 平均 / 分散 / 係数値などの推定 ( 点推定 ) 点推定値のばらつきを調べる ( 区間推定 ) 検定統計量を用いた検定
Microsoft PowerPoint - 測量学.ppt [互換モード]
![Microsoft PowerPoint - 測量学.ppt [互換モード] Microsoft PowerPoint - 測量学.ppt [互換モード]](/thumbs/92/109082022.jpg) 8/5/ 誤差理論 測定の分類 性格による分類 独立 ( な ) 測定 : 測定値がある条件を満たさなければならないなどの拘束や制約を持たないで独立して行う測定 条件 ( 付き ) 測定 : 三角形の 3 つの内角の和のように, 個々の測定値間に満たすべき条件式が存在する場合の測定 方法による分類 直接測定 : 距離や角度などを機器を用いて直接行う測定 間接測定 : 求めるべき量を直接測定するのではなく,
8/5/ 誤差理論 測定の分類 性格による分類 独立 ( な ) 測定 : 測定値がある条件を満たさなければならないなどの拘束や制約を持たないで独立して行う測定 条件 ( 付き ) 測定 : 三角形の 3 つの内角の和のように, 個々の測定値間に満たすべき条件式が存在する場合の測定 方法による分類 直接測定 : 距離や角度などを機器を用いて直接行う測定 間接測定 : 求めるべき量を直接測定するのではなく,
平成 29 年度大学院博士前期課程入学試験問題 生物工学 I 基礎生物化学 生物化学工学から 1 科目選択ただし 内部受験生は生物化学工学を必ず選択すること 解答には 問題ごとに1 枚の解答用紙を使用しなさい 余った解答用紙にも受験番号を記載しなさい 試験終了時に回収します 受験番号
 平成 29 年度大学院博士前期課程入学試験問題 生物工学 I から 1 科目選択ただし 内部受験生はを必ず選択すること 解答には 問題ごとに1 枚の解答用紙を使用しなさい 余った解答用紙にも受験番号を記載しなさい 試験終了時に回収します 受験番号 問題 1. ( 配点率 33/100) 生体エネルギーと熱力学に関する以下の問に答えなさい (1) 細胞内の反応における ATP 加水分解時の実際の自由エネルギー変化
平成 29 年度大学院博士前期課程入学試験問題 生物工学 I から 1 科目選択ただし 内部受験生はを必ず選択すること 解答には 問題ごとに1 枚の解答用紙を使用しなさい 余った解答用紙にも受験番号を記載しなさい 試験終了時に回収します 受験番号 問題 1. ( 配点率 33/100) 生体エネルギーと熱力学に関する以下の問に答えなさい (1) 細胞内の反応における ATP 加水分解時の実際の自由エネルギー変化
A6/25 アンモニウム ( インドフェノールブルー法 ) 測定範囲 : 0.20~8.00 mg/l NH 4-N 0.26~10.30 mg/l NH ~8.00 mg/l NH 3-N 0.24~9.73 mg/l NH 3 結果は mmol/l 単位でも表示できます 1. 試料の
 A6/25 アンモニウム ( インドフェノールブルー法 ) 測定範囲 : 0.20~8.00 mg/l NH 4-N 0.26~10.30 mg/l NH 4 0.20~8.00 mg/l NH 3-N 0.24~9.73 mg/l NH 3 2. ピペットで 1.0ml の試料を反応セルに取り ねじぶたで閉じて攪拌します 3. 青の計量キャップで 1 回分の試薬 NH 4-1K を加えて ねじぶたでセルを閉じます
A6/25 アンモニウム ( インドフェノールブルー法 ) 測定範囲 : 0.20~8.00 mg/l NH 4-N 0.26~10.30 mg/l NH 4 0.20~8.00 mg/l NH 3-N 0.24~9.73 mg/l NH 3 2. ピペットで 1.0ml の試料を反応セルに取り ねじぶたで閉じて攪拌します 3. 青の計量キャップで 1 回分の試薬 NH 4-1K を加えて ねじぶたでセルを閉じます
金属イオンのイオンの濃度濃度を調べるべる試薬中村博 私たちの身の回りには様々な物質があふれています 物の量を測るということは 環境を評価する上で重要な事です しかし 色々な物の量を測るにはどういう方法があるのでしょうか 純粋なもので kg や g mg のオーダーなら 直接 はかりで重量を測ることが
 金属イオンのイオンの濃度濃度を調べるべる試薬中村博 私たちの身の回りには様々な物質があふれています 物の量を測るということは 環境を評価する上で重要な事です しかし 色々な物の量を測るにはどういう方法があるのでしょうか 純粋なもので kg や g mg のオーダーなら 直接 はかりで重量を測ることが出来ます しかし 環境中の化学物質 ( 有害なものもあれば有用なものもある ) は ほとんどが水に溶けている状態であり
金属イオンのイオンの濃度濃度を調べるべる試薬中村博 私たちの身の回りには様々な物質があふれています 物の量を測るということは 環境を評価する上で重要な事です しかし 色々な物の量を測るにはどういう方法があるのでしょうか 純粋なもので kg や g mg のオーダーなら 直接 はかりで重量を測ることが出来ます しかし 環境中の化学物質 ( 有害なものもあれば有用なものもある ) は ほとんどが水に溶けている状態であり
水溶液を薄める際の計算方法薄める前の塩酸の濃度 % 体積 密度 = 薄めた後の塩酸の濃度 % 体積 密度であるから 3% の塩酸 200mL 作る場合は 35% XmL 密度 =3% 200mL 密度 X=17.1mL ここでは薄める前と薄めた後の塩酸の密度は同じくらいとして計算した よって 水に濃
 実験 水溶液の性質 での問題点の検討と実験成功のポイント 1 リトマス紙を用いた水溶液の分類をしたとき 正しい実験結果がでないことがある 考えられる原因と実験成功のポイント 1 中性のはずの食塩水や蒸留水が酸性を示した 蒸留水は 長期間保存しておくと 空気中の二酸化炭素をとかし 酸性になることがある 水溶液の実験の予備実験時に蒸留水の液性を調べておく 授業の直前にビーカーに集めた水道水 ( リトマス紙で調べて中性であればOK)
実験 水溶液の性質 での問題点の検討と実験成功のポイント 1 リトマス紙を用いた水溶液の分類をしたとき 正しい実験結果がでないことがある 考えられる原因と実験成功のポイント 1 中性のはずの食塩水や蒸留水が酸性を示した 蒸留水は 長期間保存しておくと 空気中の二酸化炭素をとかし 酸性になることがある 水溶液の実験の予備実験時に蒸留水の液性を調べておく 授業の直前にビーカーに集めた水道水 ( リトマス紙で調べて中性であればOK)
Microsoft Word - t26_江頭 _
 比の関係で計算する 石川県立金沢西高等学校江頭和子 ねらいこれから化学を学ぶにあたり, 計算や公式でつまずきそうだと思っていませんか? たしかに, 化学では数学の授業に先んじてアボガドロ定数 モルを学びます. また, 濃度の計算 ( 濃度, モル濃度 ) などみなさんが拒絶反応を示しそうな計算も必要です. 中学時代のつまずきを克服しないまま高校に来ている人はもちろんのこと, そうでない人も, 指数や分数を扱う計算に抵抗感をもつのではないでしょうか?
比の関係で計算する 石川県立金沢西高等学校江頭和子 ねらいこれから化学を学ぶにあたり, 計算や公式でつまずきそうだと思っていませんか? たしかに, 化学では数学の授業に先んじてアボガドロ定数 モルを学びます. また, 濃度の計算 ( 濃度, モル濃度 ) などみなさんが拒絶反応を示しそうな計算も必要です. 中学時代のつまずきを克服しないまま高校に来ている人はもちろんのこと, そうでない人も, 指数や分数を扱う計算に抵抗感をもつのではないでしょうか?
第 11 回化学概論 酸化と還元 P63 酸化還元反応 酸化数 酸化剤 還元剤 金属のイオン化傾向 酸化される = 酸素と化合する = 水素を奪われる = 電子を失う = 酸化数が増加する 還元される = 水素と化合する = 酸素を奪われる = 電子を得る = 酸化数が減少する 銅の酸化酸化銅の還元
 第 11 回化学概論 酸化と還元 P63 酸化還元反応 酸化数 酸化剤 還元剤 金属のイオン化傾向 酸化される = 酸素と化合する = 水素を奪われる = 電子を失う = 酸化数が増加する 還元される = 水素と化合する = 酸素を奪われる = 電子を得る = 酸化数が減少する 銅の酸化酸化銅の還元 2Cu + O 2 2CuO CuO + H 2 Cu + H 2 O Cu Cu 2+ + 2e
第 11 回化学概論 酸化と還元 P63 酸化還元反応 酸化数 酸化剤 還元剤 金属のイオン化傾向 酸化される = 酸素と化合する = 水素を奪われる = 電子を失う = 酸化数が増加する 還元される = 水素と化合する = 酸素を奪われる = 電子を得る = 酸化数が減少する 銅の酸化酸化銅の還元 2Cu + O 2 2CuO CuO + H 2 Cu + H 2 O Cu Cu 2+ + 2e
FdData理科3年
 FdData 中間期末 : 中学理科 3 年 [ 酸 アルカリとイオン ] [ 問題 ](1 学期期末 ) 次の各問いに答えよ (1) 塩酸の中に含まれている 酸 に共通するイオンは何か 1 イオンの名称を答えよ 2 また, このイオンの記号を書け (2) 水酸化ナトリウム水溶液の中に含まれている アルカリ に共通するイオンは何か 1 イオンの名称を答えよ 2 また, このイオンの記号を答えよ [
FdData 中間期末 : 中学理科 3 年 [ 酸 アルカリとイオン ] [ 問題 ](1 学期期末 ) 次の各問いに答えよ (1) 塩酸の中に含まれている 酸 に共通するイオンは何か 1 イオンの名称を答えよ 2 また, このイオンの記号を書け (2) 水酸化ナトリウム水溶液の中に含まれている アルカリ に共通するイオンは何か 1 イオンの名称を答えよ 2 また, このイオンの記号を答えよ [
XIII キレート滴定 Chelatometry 金属イオンにキレート生成試薬 ( 水溶性多座配位子 ) を加え 電離度の極めて小さい水 溶性キレート化合物 ( 分子内錯化合物 ) を生成させる キレート生成試薬 EDTA:Ethylenediaminetetraacetic Acid 最も一般的
 XIII キレート滴定 Chelatometry 金属イオンにキレート生成試薬 ( 水溶性多座配位子 ) を加え 電離度の極めて小さい水 溶性キレート化合物 ( 分子内錯化合物 ) を生成させる キレート生成試薬 EDTA:Ethylenediaminetetraacetic Acid 最も一般的 CyDTA:Cyclohexanediaminetetraacetic Acid NTA :Nitrilotriacetic
XIII キレート滴定 Chelatometry 金属イオンにキレート生成試薬 ( 水溶性多座配位子 ) を加え 電離度の極めて小さい水 溶性キレート化合物 ( 分子内錯化合物 ) を生成させる キレート生成試薬 EDTA:Ethylenediaminetetraacetic Acid 最も一般的 CyDTA:Cyclohexanediaminetetraacetic Acid NTA :Nitrilotriacetic
データ解析
 データ解析 ( 前期 ) 最小二乗法 向井厚志 005 年度テキスト 0 データ解析 - 最小二乗法 - 目次 第 回 Σ の計算 第 回ヒストグラム 第 3 回平均と標準偏差 6 第 回誤差の伝播 8 第 5 回正規分布 0 第 6 回最尤性原理 第 7 回正規分布の 分布の幅 第 8 回最小二乗法 6 第 9 回最小二乗法の練習 8 第 0 回最小二乗法の推定誤差 0 第 回推定誤差の計算 第
データ解析 ( 前期 ) 最小二乗法 向井厚志 005 年度テキスト 0 データ解析 - 最小二乗法 - 目次 第 回 Σ の計算 第 回ヒストグラム 第 3 回平均と標準偏差 6 第 回誤差の伝播 8 第 5 回正規分布 0 第 6 回最尤性原理 第 7 回正規分布の 分布の幅 第 8 回最小二乗法 6 第 9 回最小二乗法の練習 8 第 0 回最小二乗法の推定誤差 0 第 回推定誤差の計算 第
Xamテスト作成用テンプレート
 気体の性質 1 1990 年度本試験化学第 2 問 問 1 次の問い (a b) に答えよ a 一定質量の理想気体の温度を T 1 [K] または T 2 [K] に保ったまま, 圧力 P を変える このときの気体の体積 V[L] と圧力 P[atm] との関係を表すグラフとして, 最も適当なものを, 次の1~6のうちから一つ選べ ただし,T 1 >T 2 とする b 理想気体 1mol がある 圧力を
気体の性質 1 1990 年度本試験化学第 2 問 問 1 次の問い (a b) に答えよ a 一定質量の理想気体の温度を T 1 [K] または T 2 [K] に保ったまま, 圧力 P を変える このときの気体の体積 V[L] と圧力 P[atm] との関係を表すグラフとして, 最も適当なものを, 次の1~6のうちから一つ選べ ただし,T 1 >T 2 とする b 理想気体 1mol がある 圧力を
TNT820-1 化学的酸素要求量 (COD) (DR1900 用 ) DOC 加熱分解法方法 ULR (1~60 mg/l COD) TNTplus TM 820 用途 : 下水 処理水 地表水 冷却水 : 本測定方法は 分解を必要とします 測定の準備試薬パッケ
 TNT820-1 化学的酸素要求量 (COD) (DR1900 用 ) DOC316.53.01103 加熱分解法方法 10211 ULR (1~60 mg/l COD) TNTplus TM 820 用途 : 下水 処理水 地表水 冷却水 : 本測定方法は 分解を必要とします 測定の準備試薬パッケ-ジを確認してください本手順書は 右写真のパッケ-ジ試薬が対象です 異なるパッケ-ジの TNT820
TNT820-1 化学的酸素要求量 (COD) (DR1900 用 ) DOC316.53.01103 加熱分解法方法 10211 ULR (1~60 mg/l COD) TNTplus TM 820 用途 : 下水 処理水 地表水 冷却水 : 本測定方法は 分解を必要とします 測定の準備試薬パッケ-ジを確認してください本手順書は 右写真のパッケ-ジ試薬が対象です 異なるパッケ-ジの TNT820
14551 フェノール ( チアゾール誘導体法 ) 測定範囲 : 0.10~2.50 mg/l C 6H 5OH 結果は mmol/l 単位でも表示できます 1. 試料の ph が ph 2~11 であるかチェックします 必要な場合 水酸化ナトリウム水溶液または硫酸を 1 滴ずつ加えて ph を調整
 14551 フェノール ( チアゾール誘導体法 ) 0.10~2.50 mg/l C 6H 5OH 結果は mmol/l 単位でも表示できます 2. ピペットで 10 ml の試料を反応セルに取り ねじぶたで閉じて攪拌します 3. グレーのミクロスプーンで 1 回分の試薬 Ph-1K を加えて ねじぶたでセルを閉じます 4. セルをよく振とうして 固体物を溶かします 5. 緑のミクロスプーンで 1
14551 フェノール ( チアゾール誘導体法 ) 0.10~2.50 mg/l C 6H 5OH 結果は mmol/l 単位でも表示できます 2. ピペットで 10 ml の試料を反応セルに取り ねじぶたで閉じて攪拌します 3. グレーのミクロスプーンで 1 回分の試薬 Ph-1K を加えて ねじぶたでセルを閉じます 4. セルをよく振とうして 固体物を溶かします 5. 緑のミクロスプーンで 1
Taro-22 No19 大網中(中和と塩
 中和と塩 Ⅰ 視覚的に確認でき, イオンなどの粒子概念の形成に役立つ中和反応の観察 実験例 1 観察 実験のあらまし中和反応の実験は, 塩酸と水酸化ナトリウムで行うことが多い ところが, この反応では生成する塩は塩化ナトリウム ( 食塩 ) という水に溶ける塩であるため, 混ぜた瞬間に中和反応が起きていることがわからない そこで, 硫酸と水酸化バリウムの組み合わせで行うことで硫酸バリウムという水に溶けない塩が生成するので,1
中和と塩 Ⅰ 視覚的に確認でき, イオンなどの粒子概念の形成に役立つ中和反応の観察 実験例 1 観察 実験のあらまし中和反応の実験は, 塩酸と水酸化ナトリウムで行うことが多い ところが, この反応では生成する塩は塩化ナトリウム ( 食塩 ) という水に溶ける塩であるため, 混ぜた瞬間に中和反応が起きていることがわからない そこで, 硫酸と水酸化バリウムの組み合わせで行うことで硫酸バリウムという水に溶けない塩が生成するので,1
V ・環境保全
 Ⅷ 付帯資料 - 187 - 1. 化学分析の単位と計算式 単体と酸化物の表し方 SI 単位系一覧 1.1 化学分析に用いる単位と計算式 1) 重さの単位 (1)1mg( ミリグラム ):gの1000 分の1 1.0gは1000mg (2)μg( マイクログラム ):mgの1000 分の1 1.0mgは1000μg 2) 体積の単位 (1)mL( ミリリットル ):L( リットル ) の1000 分の1
Ⅷ 付帯資料 - 187 - 1. 化学分析の単位と計算式 単体と酸化物の表し方 SI 単位系一覧 1.1 化学分析に用いる単位と計算式 1) 重さの単位 (1)1mg( ミリグラム ):gの1000 分の1 1.0gは1000mg (2)μg( マイクログラム ):mgの1000 分の1 1.0mgは1000μg 2) 体積の単位 (1)mL( ミリリットル ):L( リットル ) の1000 分の1
Microsoft Word - 化学系演習 aG.docx
 有機化学反応の基礎 () 芳香族化合物 ) 芳香族化合物の性質 ベンゼンに代表される芳香族化合物は 環構造を構成する原子すべてが p 軌道をもち 隣同士の原子間で p 軌道が重なり合うことができるので 電子が非局在化 ( 共鳴安定化 ) している 芳香族性をもつため 求電子付加反応ではなく求電子置換反応を起こしやすい 全ての炭素が sp ² 混成 π 結合 p 軌道 π 電子がドーナツ状に分布し 極めて安定
有機化学反応の基礎 () 芳香族化合物 ) 芳香族化合物の性質 ベンゼンに代表される芳香族化合物は 環構造を構成する原子すべてが p 軌道をもち 隣同士の原子間で p 軌道が重なり合うことができるので 電子が非局在化 ( 共鳴安定化 ) している 芳香族性をもつため 求電子付加反応ではなく求電子置換反応を起こしやすい 全ての炭素が sp ² 混成 π 結合 p 軌道 π 電子がドーナツ状に分布し 極めて安定
競技の流れ 発泡入浴剤は, 炭酸水素ナトリウム ( 重曹 ) とクエン酸という物質を固めて作られている これを水に溶かすと, 水中で両者が反応して二酸化炭素が発生する この発泡は, 血行を良くする働きがあると考えられている 今日の実験は, 発泡入浴剤に関係する次の 3 テーマからなる 時間配分 (1
 全国大会 実技競技 2 発泡入浴剤を作ろう 競技の流れ 実験の手順 問題 都道府県名 チーム番号 競技の流れ 発泡入浴剤は, 炭酸水素ナトリウム ( 重曹 ) とクエン酸という物質を固めて作られている これを水に溶かすと, 水中で両者が反応して二酸化炭素が発生する この発泡は, 血行を良くする働きがあると考えられている 今日の実験は, 発泡入浴剤に関係する次の 3 テーマからなる 時間配分 (1)
全国大会 実技競技 2 発泡入浴剤を作ろう 競技の流れ 実験の手順 問題 都道府県名 チーム番号 競技の流れ 発泡入浴剤は, 炭酸水素ナトリウム ( 重曹 ) とクエン酸という物質を固めて作られている これを水に溶かすと, 水中で両者が反応して二酸化炭素が発生する この発泡は, 血行を良くする働きがあると考えられている 今日の実験は, 発泡入浴剤に関係する次の 3 テーマからなる 時間配分 (1)
第3類危険物の物質別詳細 練習問題
 第 3 類危険物の物質別詳細練習問題 問題 1 第 3 類危険物の一般的な消火方法として 誤っているものは次のうちいくつあるか A. 噴霧注水は冷却効果と窒息効果があるので 有効である B. 乾燥砂は有効である C. 分子内に酸素を含むので 窒息消火法は効果がない D. 危険物自体は不燃性なので 周囲の可燃物を除去すればよい E. 自然発火性危険物の消火には 炭酸水素塩類を用いた消火剤は効果がある
第 3 類危険物の物質別詳細練習問題 問題 1 第 3 類危険物の一般的な消火方法として 誤っているものは次のうちいくつあるか A. 噴霧注水は冷却効果と窒息効果があるので 有効である B. 乾燥砂は有効である C. 分子内に酸素を含むので 窒息消火法は効果がない D. 危険物自体は不燃性なので 周囲の可燃物を除去すればよい E. 自然発火性危険物の消火には 炭酸水素塩類を用いた消火剤は効果がある
数値計算法
 数値計算法 008 4/3 林田清 ( 大阪大学大学院理学研究科 ) 実験データの統計処理その 誤差について 母集団と標本 平均値と標準偏差 誤差伝播 最尤法 平均値につく誤差 誤差 (Error): 真の値からのずれ 測定誤差 物差しが曲がっていた 測定する対象が室温が低いため縮んでいた g の単位までしかデジタル表示されない計りで g 以下 計りの目盛りを読み取る角度によって値が異なる 統計誤差
数値計算法 008 4/3 林田清 ( 大阪大学大学院理学研究科 ) 実験データの統計処理その 誤差について 母集団と標本 平均値と標準偏差 誤差伝播 最尤法 平均値につく誤差 誤差 (Error): 真の値からのずれ 測定誤差 物差しが曲がっていた 測定する対象が室温が低いため縮んでいた g の単位までしかデジタル表示されない計りで g 以下 計りの目盛りを読み取る角度によって値が異なる 統計誤差
photolab 6x00 / 7x00 バーコードのない測定項目 バーコードのない測定項目 使用できる測定法 これらの測定項目の分析仕様は 付録 4 に記載されています ここでは 使用方法は カラム 5 の測定法番号を使用して手動で選択します 測定法の選択方法の説明は 光度計の機能説明の 測定法の
 photolab 6x00 / 7x00 バーコードのない測定項目 バーコードのない測定項目 使用できる測定法 これらの測定項目の分析仕様は 付録 4 に記載されています ここでは 使用方法は カラム 5 の測定法番号を使用して手動で選択します 測定法の選択方法の説明は 光度計の機能説明の 測定法の手動選択 のセクションに記載されています パラメータ / 名称 型式 独語 独語 独語 形式 ** 独語
photolab 6x00 / 7x00 バーコードのない測定項目 バーコードのない測定項目 使用できる測定法 これらの測定項目の分析仕様は 付録 4 に記載されています ここでは 使用方法は カラム 5 の測定法番号を使用して手動で選択します 測定法の選択方法の説明は 光度計の機能説明の 測定法の手動選択 のセクションに記載されています パラメータ / 名称 型式 独語 独語 独語 形式 ** 独語
B. モル濃度 速度定数と化学反応の速さ 1.1 段階反応 ( 単純反応 ): + I HI を例に H ヨウ化水素 HI が生成する速さ は,H と I のモル濃度をそれぞれ [ ], [ I ] [ H ] [ I ] に比例することが, 実験により, わかっている したがって, 比例定数を k
![B. モル濃度 速度定数と化学反応の速さ 1.1 段階反応 ( 単純反応 ): + I HI を例に H ヨウ化水素 HI が生成する速さ は,H と I のモル濃度をそれぞれ [ ], [ I ] [ H ] [ I ] に比例することが, 実験により, わかっている したがって, 比例定数を k B. モル濃度 速度定数と化学反応の速さ 1.1 段階反応 ( 単純反応 ): + I HI を例に H ヨウ化水素 HI が生成する速さ は,H と I のモル濃度をそれぞれ [ ], [ I ] [ H ] [ I ] に比例することが, 実験により, わかっている したがって, 比例定数を k](/thumbs/81/83835231.jpg) 反応速度 触媒 速度定数 反応次数について. 化学反応の速さの表し方 速さとは単位時間あたりの変化の大きさである 大きさの値は 0 以上ですから, 速さは 0 以上の値をとる 化学反応の速さは単位時間あたりの物質のモル濃度変化の大きさで表すのが一般的 たとえば, a + bb c (, B, は物質, a, b, c は係数 ) という反応において,, B, それぞれの反応の速さを, B, とし,
反応速度 触媒 速度定数 反応次数について. 化学反応の速さの表し方 速さとは単位時間あたりの変化の大きさである 大きさの値は 0 以上ですから, 速さは 0 以上の値をとる 化学反応の速さは単位時間あたりの物質のモル濃度変化の大きさで表すのが一般的 たとえば, a + bb c (, B, は物質, a, b, c は係数 ) という反応において,, B, それぞれの反応の速さを, B, とし,
PowerPoint プレゼンテーション
 反応工学 Raction Enginring 講義時間 ( 場所 : 火曜 限 (8-A 木曜 限 (S-A 担当 : 山村 火 限 8-A 期末試験中間試験以降 /7( 木 まで持ち込みなし要電卓 /4( 木 質問受付日講義なし 授業アンケート (li campus の入力をお願いします 晶析 (crystallization ( 教科書 p. 濃度 溶解度曲線 C C s A 安定 液 ( 気
反応工学 Raction Enginring 講義時間 ( 場所 : 火曜 限 (8-A 木曜 限 (S-A 担当 : 山村 火 限 8-A 期末試験中間試験以降 /7( 木 まで持ち込みなし要電卓 /4( 木 質問受付日講義なし 授業アンケート (li campus の入力をお願いします 晶析 (crystallization ( 教科書 p. 濃度 溶解度曲線 C C s A 安定 液 ( 気
IC-PC法による大気粉じん中の六価クロム化合物の測定
 Application Note IC-PC No.IC178 IC-PC 217 3 IC-PC ph IC-PC EPA 1-5.8 ng/m 3 11.8 ng/m 3 WHO.25 ng/m 3 11.25 ng/m 3 IC-PC.1 g/l. g/l 1 1 IC-PC EPA 1-5 WHO IC-PC M s ng/m 3 C = C 1/1 ng/m 3 ( M s M b ) x
Application Note IC-PC No.IC178 IC-PC 217 3 IC-PC ph IC-PC EPA 1-5.8 ng/m 3 11.8 ng/m 3 WHO.25 ng/m 3 11.25 ng/m 3 IC-PC.1 g/l. g/l 1 1 IC-PC EPA 1-5 WHO IC-PC M s ng/m 3 C = C 1/1 ng/m 3 ( M s M b ) x
2,3-ジメチルピラジンの食品添加物の指定に関する部会報告書(案)
 資料 3 粗製海水塩化マグネシウム の分析調査結果について 1. 経緯平成 19 年 3 月 30 日に 食品 添加物等の規格基準の一部を改正する件 ( 平成 19 年厚生労働省告示第 73 号 ) により 食品 添加物等の規格基準 ( 昭和 34 年厚生省告示第 370 号 ) が改正され 既存添加物 粗製海水塩化マグネシウム ( 以下 にがり という ) について 新たに成分規格が設定された なお
資料 3 粗製海水塩化マグネシウム の分析調査結果について 1. 経緯平成 19 年 3 月 30 日に 食品 添加物等の規格基準の一部を改正する件 ( 平成 19 年厚生労働省告示第 73 号 ) により 食品 添加物等の規格基準 ( 昭和 34 年厚生省告示第 370 号 ) が改正され 既存添加物 粗製海水塩化マグネシウム ( 以下 にがり という ) について 新たに成分規格が設定された なお
Microsoft PowerPoint - D.酸塩基(2)
 D. 酸塩基 (2) 1. 多塩基酸の ph 2. 塩の濃度と ph 3. 緩衝溶液と ph 4. 溶解度積と ph 5. 酸塩基指示薬 D. 酸塩基 (2) 1. 多塩基酸の ph 1. 多塩基酸の ph (1) 硫酸 H 2 SO 4 ( 濃度 C) 硫酸 H 2 SO 4 は2 段階で電離する K (C) (C) K a1 [H+ ][HSO 4 ] [H 2 SO 4 ] 10 5 第 1
D. 酸塩基 (2) 1. 多塩基酸の ph 2. 塩の濃度と ph 3. 緩衝溶液と ph 4. 溶解度積と ph 5. 酸塩基指示薬 D. 酸塩基 (2) 1. 多塩基酸の ph 1. 多塩基酸の ph (1) 硫酸 H 2 SO 4 ( 濃度 C) 硫酸 H 2 SO 4 は2 段階で電離する K (C) (C) K a1 [H+ ][HSO 4 ] [H 2 SO 4 ] 10 5 第 1
Microsoft Word - Stattext07.doc
 7 章正規分布 正規分布 (ormal dstrbuto) は 偶発的なデータのゆらぎによって生じる統計学で最も基本的な確率分布です この章では正規分布についてその性質を詳しく見て行きましょう 7. 一般の正規分布正規分布は 平均と分散の つの量によって完全に特徴付けられています 平均 μ 分散 の正規分布は N ( μ, ) 分布とも書かれます ここに N は ormal の頭文字を 表わしています
7 章正規分布 正規分布 (ormal dstrbuto) は 偶発的なデータのゆらぎによって生じる統計学で最も基本的な確率分布です この章では正規分布についてその性質を詳しく見て行きましょう 7. 一般の正規分布正規分布は 平均と分散の つの量によって完全に特徴付けられています 平均 μ 分散 の正規分布は N ( μ, ) 分布とも書かれます ここに N は ormal の頭文字を 表わしています
