本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2. 書面調査 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの見直し 3.2. 医薬品再審査適合性調査相談 ( 新設 ) 2
|
|
|
- りえ かせ
- 5 years ago
- Views:
Transcription
1 医薬品の製造販売後調査の 現状と留意点 1
2 本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2. 書面調査 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの見直し 3.2. 医薬品再審査適合性調査相談 ( 新設 ) 2
3 本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2. 書面調査 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの見直し 3.2. 医薬品再審査適合性調査相談 ( 新設 ) 3
4 再審査にかかる医薬品医療機器法の規定 医薬品医療機器法第 14 条の 4( 新医薬品等の再審査 ) 第 1 項次の各号に掲げる医薬品につき第十四条の承認を受けた者は 当該医薬品について 当該各号に定める期間内に申請して 厚生労働大臣の再審査を受けなければならない 第 3 項厚生労働大臣の再審査は 再審査を行う際に得られている知見に基づき 第一項各号に掲げる医薬品が第十四条第二項第三号イからハまでのいずれにも該当しないことを確認することにより行う 医薬品医療機器法第 14 条 ( 医薬品 医薬部外品及び化粧品の製造販売の承認 ) 第 2 項第 3 号 ( 中略 ) イ申請に係る医薬品 ( 中略 ) が その申請に係る効能又は効果を有すると認められないとき ロ申請に係る医薬品 ( 中略 ) が その効能又は効果に比して著しく有害な作用を有することにより 医薬品又は医薬部外品として使用価値がないと認められるとき ハイ又はロに掲げる場合のほか 医薬品 ( 中略 ) として不適当なものとして厚生労働省令で定める場合注 ) に該当するとき 注 ) 性状又は品質が保健衛生上著しく不適当な場合 4
5 再審査申請資料に関する調査 医薬品医療機器法第 14 条の 4( 新医薬品等の再審査 ) 第 4 項 ( 中略 ) 当該申請に係る医薬品が厚生労働省令で定める医薬であるときは 当該資料は 厚生労働省令で定める基準に従って収集され かつ 作成されたものでなければならない 第 5 項 ( 中略 ) 第一項各号に掲げる医薬品が前項後段に規定する厚生労働省令で定める医薬品であるときは あらかじめ 当該医薬品に係る資料が同項後段の規定に適合するかどうかについての書面による調査又は実地の調査を行うものとする 5
6 GPSP 厚生労働省令で定める基準 医薬品の製造販売後の調査及び試験の実施の基準に関する省令 ( 平成 16 年 12 月 20 日厚生労働省令第 171 号 ) 信頼性の基準医薬品医療機器法施行規則第 61 条 ( 第 43 条の準用 ) 法第 14 条の 4 第 4 項後段に規定する資料は,( 中略 ) 次に掲げるところにより, 収集され, かつ, 作成されたものでなければならない 一当該資料は, これを作成することを目的として行われた調査又は試験において得られた結果に基づき正確に作成されたものであること 二 ( 中略 ) 品質, 有効性又は安全性を有することを疑わせる調査結果, 試験成績等が得られた場合には, 当該調査結果, 試験成績等についても検討及び評価が行われ, その結果は当該資料に記載されていること 三当該資料の根拠になった資料は, 法第 14 条の 4 第 1 項の再審査の終了の日まで保存されていること ( 以下略 ) 6
7 本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2. 書面調査 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの見直し 3.2. 医薬品再審査適合性調査相談 ( 新設 ) 7
8 再審査申請後の標準的な流れ 査前 医薬品再審査適合性書面調査結果通知書 調当日 調査後1 事前情報の提出 再審査資料適合性調査における事前情報の収集の依頼について 2 日程調整 事前提出資料の提出 GPSP 実地調査及び書面調査の実施にあたり の依頼 3 実施通知書 再審査資料適合性調査及び担当者について 医薬品再審査適合性書面調査実施通知書 医薬品 GPSP 実地調査実施通知書 4 準備資料の提出 適合性調査 ( 品目名 ) に関する準備資料について 5 再審査申請資料適合性調査 (GPSP 実地調査 適合性書面調査 ) 調査実施 ( 資料目録 (GPSP 実地調査 適合性書面調査 )) 6 再審査申請資料適合性調査に係る照会 GPSP 実地調査及び適合性書面調査に係る照会事項について 7 結果通知書 医薬品 GPSP 実地調査結果通知書 8
9 医薬品 GPSP 実地調査における改善を要する事項 ( 件 ) ( 調査等の実施 ) 平成 24 年度結果通知発出分 (34 社 58 品目 ) 平成 25 年度結果通知発出分 (22 社 34 品目 ) 平成 26 年度結果通知発出分 (23 社 35 品目 ) 20 ( 管理責任者 ) 平成 27 年度結果通知発出分 (30 社 52 品目 ) ( 使用成績調査 ) ( 手順書 ) ( 自己点検 ) ( 委託 ) 5 0 ( 製造販売後臨床試験 ) ( 教育訓練 ) ( 記録の保存 ) 第 3 条第 4 条第 5 条第 6 条第 7 条第 8 条第 9 条第 10 条第 11 条 9
10 医薬品 GPSP 実地調査に関する問題事例と留意点事例 1 GPSP 第 3 条第 1 項 製造販売後調査等業務手順書の作成 製造販売後調査等業務手順書が製造販売業者等により作成されていなかった 製造販売後調査等業務手順書の作成は特定の役職の者に権限委譲されているが 作成者はその役職を離れた後にも作成していた 留意点 製造販売業者等は 製造販売後調査等業務手順書を作成しなければならない 製造販売業者等以外の者が作成する場合には 適切に権限委譲すること 10
11 医薬品 GPSP 実地調査に関する問題事例と留意点事例 2 GPSP 第 4 条第 3 項第 2 3 号 計画書の作成及び改訂の不備 製造販売後臨床試験実施計画書の作成 改訂について 製造販売後調査等管理責任者が確認した記録がなかった 製造販売後臨床試験実施計画書の改訂について 製造販売後調査等管理責任者へ適切な時期に報告されておらず 基本計画書の改訂が遅れた 留意点 製造販売後調査等管理責任者は 製造販売後臨床試験実施計画書を確認すること 基本計画書の改訂をすべきかどうか適切な時期に判断をすること 11
12 医薬品 GPSP 実地調査に関する問題事例と留意点事例 3 GPSP 第 6 条第 1 項使用成績調査 再調査の不備 調査票のコメント欄等の記載内容や再調査の回答内容で 再調査を要する記載があったにも関わらず再調査が行われていなかった 調査票には安全性に関わる情報が記載されていたにもかかわらず 再調査を実施しておらず 集計解析上 安全性集計対象外となっていた 留意点 再調査基準について 調査全体が一律の基準で取り扱われているか確認すること 必要な再調査を実施し 適切に申請資料を作成すること 12
13 医薬品 GPSP 実地調査に関する問題事例と留意点事例 4 GPSP 第 10 条第 2 項 第 3 項第 1 号 委託業務の確認の不備 契約締結日以前に委託業務の一部を実施した 委託業務が適正かつ円滑に行われているか製造販売後調査等管理責任者が確認していなかった 留意点 業務の委託においては 事前に委託先の能力確認を行い 業務契約締結後 委託した業務を開始すること 委託業務内容に応じ 委託業務が適正かつ円滑に行われているかの確認の方法及び確認の時期について委託先と合意しておくこと 13
14 医薬品 GPSP 実地調査に関する問題事例と留意点事例 5 承継品目について 承継前の会社において 製造販売後臨床試験の結果が製造販売業者に報告されていたことが確認できなかった 承継前の会社において 自己点検結果が製造販売業者に報告されていたことが確認できなかった 留意点 申請者は 再審査申請内容の確認を行える十分な資料及び情報を引き継ぎ 適合性調査時には承継前の GPSP 遵守状況についても説明できるようにしておくこと 承継前の会社において 自己点検が未実施であった事項について 承継後の会社は気づいた時点で適切に対応を行うこと 14
15 本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2. 書面調査 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの見直し 3.2. 医薬品再審査適合性調査相談 ( 新設 ) 15
16 再審査申請資料実施 ライティング適合性書面調査の視点 ( 使用成績調査 ) 実施計画書に従った評価がされているか? 調査票の内容に矛盾はないか? 有害事象情報の収集が適切に行われているか? 業務手順書 施設選定 契約計画書 録 調査票記登データマネジメ集計解析再調査ントQ C 点検入契約は文書で行われているか? 重複症例の有無 登録期限の確認はされているか? 根拠資料から申請資料までの適合性を保証する 16
17 知事項なし1) 平成 27 年 4 月 ~ 平成 28 年 3 月に適合性書面調査の結果通知を発出した再審査医薬品を対象 適合性書面調査における調査結果 (H27 年度 ) 1) 4 照会なし 6%(3 品目 ) 3 照会あり / 修正なし 27%(14 品目 ) 全 52 品目 3) 1 通知事項あり 2%(1 品目 ) 2 照会あり / 修正あり 65%(34 品目 ) 1 通知事項あり 結果の信頼性に影響を及ぼす事項又は改善すべき事項とされた場合 2 照会あり 2) / 修正あり 照会事項が発出され 回答にて承通認申請資料が一部修正された場合 3 照会あり 2) / 修正なし 照会事項が発出されたが 承認申請資料の修正は発生していない場合 4 照会なし 照会事項が発出されていない場合 2) 実地調査照会事項も含む 3) GPSP 実地調査及び適合性書面調査実施品目数 17
18 適合性書面調査の問題事例 安全管理情報の評価漏れや評価記録が不十分であった その後の対応 調査票を含めた安全管理情報を再度確認し 再評価を実施 評価記録に基づき 安全性 DB 入力 改めて 安全性 DB 入力情報と評価記録の一致性を確認 再審査申請資料の大幅差し替えを実施 適切な安全性 DB の管理 運用の重要性 18
19 本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2. 書面調査 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの見直し 3.2. 医薬品再審査適合性調査相談 ( 新設 ) 19
20 安全性情報のシステム調査 ( プロセス調査 ) の検討 これまでの適合性調査 ( 安全性情報について ) 1. 手順書等を用いた業務プロセスの確認 2. 抽出症例の確認 できるだけ繰り返しの確認を避け 適合性調査の効率化を目指す 平成 25 年 4 月以降に再審査申請される品目のうち ご協力頂ける申請者の対象品目にてプレパイロット調査を実施中 ( 平成 25 年 6 月以降 ) さらなる適合性調査の効率化に向け 安全性情報管理シートを今後どのように適合性調査に用いていくか 信頼性保証部内で検討中 20
21 本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2. 書面調査 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの見直し 3.2. 医薬品再審査適合性調査相談 ( 新設 ) 21
22 医薬品再審査適合性調査相談とは 現在の医薬品再審査による適合性調査では 製造販売後臨床試験や使用成績調査が終了後数年経過していることから 適合性調査実施時には企業の担当者等が退職しているなど 当時の状況の事実確認等に時間を要することが問題となっている 本相談は 医薬品再審査のために行われる製造販売後臨床試験等が終了した段階において 再審査申請資料として添付する予定の資料ついて 実質的な適合性に対する調査 ( 書面適合性調査および GPSP 実地調査 ) を行う メリット 1 メリット 2 メリット 3 企業担当者が在職しているため事実確認が容易 問題点の早期発見 体制の立直しが可能 再審査申請後の適合性調査の負担軽減 22
23 平成 28 年 7 月 21 日より事前面談の受付開始 ホーム > 審査関連業務 > 相談業務 > 対面助言 事前面談 ( 治験相談 簡易相談 ) 等 > 医薬品 医薬部外品 > 医薬品再審査適合性調査相談 review-services/f2f-pre/ consultations/0058.html 23
24 相談の内容 医薬品の再審査申請時に添付する予定の資料のうち 次のア又はイのいずれかについて 指導及び助言を行うもの ただし ア又はイの相談時には 当該試験 調査実施当時の GPSP 実施体制の確認及びデータマネージメント 解析等の実施状況の確認も同時に実施することとします ア既に終了した製造販売後臨床試験に関する資料について 信頼性基準への適合性に関する事項イ既に終了した使用成績調査もしくは特定使用成績調査に関する資料について 信頼性基準への適合性に関する事項 24
25 相談の流れ ( 概要 ) 事前面談 ( 必須 ) 手数料振り込み 申込書提出 資料搬入 相談の実施等のお知らせ 根拠資料提示 医薬品再審査適合性調査の実施 照会 回答 ( 必要に応じて ) 相談記録の伝達 25
26 相談の流れ ( 概要 ) 事前面談 ( 必須 ) 手数料振り込み 申込書提出 資料搬入 相談の実施等のお知らせ 根拠資料提示 医薬品再審査適合性調査の実施 照会 回答 ( 必要に応じて ) 相談記録の伝達 26
27 相談の流れ (1) 事前面談 ( 必須 ) 相談資料提出予定時期の 1 ヶ月程度前までに実施 相談事項 提出資料の内容 相談実施予定時期 申込書提出予定日等を確認 事前面談終了後 機構及び相談者において確認された事項について 事前面談確認書 を 併せて資料搬入時に必要な資料を記載した 搬入資料一覧表 を発行 受付時期 月曜日から金曜日 ( 国民の休日を除く ) 午前 9 時 30 分 ~ 正午 ( 厳守 ) 別紙様式 7 医薬品事前面談質問申込書 (Word, PDF) にて受付 27
28 相談の流れ ( 概要 ) 事前面談 ( 必須 ) 手数料振り込み 申込書提出 資料搬入 相談の実施等のお知らせ 根拠資料提示 医薬品再審査適合性調査の実施 照会 回答 ( 必要に応じて ) 相談記録の伝達 28
29 提出資料搬入 相談の流れ (2) 手数料を振り込んだ上で 医薬品再審査適合性調査相談申込書 に必要事項を記入し 下記 4 点と併せて 持参又は郵送によりお申込みください (1) 事前面談時に発行された確認書の写し (2) 振込金受取書等の写し (3) 医薬品再審査適合性調査相談に使用する資料目録 ( 再審査申請資料として添付を予定する資料及びその根拠資料の目録 ) (4) 医薬品の再審査申請時に添付する予定の資料 なお 事前面談時に発行された 搬入資料一覧表 の全ての項目にチェックを入れたものも併せて提出してください 受付時期 原則として 毎月第 3 週の火曜日の午前 10 時から午後 4 時 ( 厳守 ) なお 国民の祝日の場合等 状況に応じて 受付日を変更することがありますので申込書受付日を必ずご確認ください 様式第 22 号の 2: 医薬品再審査適合性調査相談申込書 (WORD, PDF) にて受付 29
30 相談の流れ ( 概要 ) 事前面談 ( 必須 ) 手数料振り込み 申込書提出 資料搬入 相談の実施等のお知らせ 根拠資料提示 医薬品再審査適合性調査の実施 照会 回答 ( 必要に応じて ) 相談記録の伝達 30
31 相談の流れ (3) 相談の実施等のお知らせ 機構の担当者が実施日時について調整をします 実施日時 場所等が確定した段階で 相談者の連絡先宛に郵送にてお知らせします 根拠資料提示 根拠資料は 医薬品再審査適合性調査相談当日に提示してください 相談実施 医薬品再審査適合性調査相談は 原則として 機構の担当者が企業へ訪問して行います なお 本相談の対象が製造販売後臨床試験である場合には 機構の担当者が医療機関へ訪問して調査を行うことがありますので 機構の担当者の指示に従ってください 31
32 相談の流れ ( 概要 ) 事前面談 ( 必須 ) 手数料振り込み 申込書提出 資料搬入 相談の実施等のお知らせ 根拠資料提示 医薬品再審査適合性調査の実施 照会 回答 ( 必要に応じて ) 相談記録の伝達 32
33 相談の流れ (4) 相談記録の伝達 相談終了後には 相談者に内容を確認した上で 機構にて記録を作成し 相談者に伝達します その他 医薬品再審査適合性調査相談の対象となった資料について 医薬品の再審査申請資料として使用する場合には 提出した資料の内容を変更していない旨の陳述書を提出していただきます また 医薬品再審査適合性調査相談記録は医薬品再審査申請資料の添付資料として提出してください 33
34 相談の留意点 1 適合性調査相談申込みの前に 事前面談を実施する必要があります 事前面談時には 主に以下の内容について確認 1 調査 試験の実施した背景 相談に至った経緯 2 適合性調査相談申込み時の申込資料 3 適合性調査相談申込み予定日 適合性調査相談申込みの 1 ヵ月程度前までに事前面談を実施してください 34
35 相談の留意点 2 相談申込み時に提出いただく相談資料は 相談の内容により提出が不要となる資料もありますが 再審査申請時に提出する資料 事前提出資料と基本的には同等の資料と考えています 実質的な再審査申請時の適合性調査 ( 書面調査および GPSP 実地調査 ) の早期実施となりますので 資料の品質管理や信頼性の担保の説明については再審査申請時と同等にご準備いただきますよう 十分ご配慮ください 35
36 最後に 再審査資料業務の効率化のため 事前に提出された資料で調査票回収の流れやデータマネジメント等を確認いたします ご対応にあたり 信頼性を担保する記録に基づいた資料の作成 保存をお願いします 36
本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シ
 医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
<4D F736F F F696E74202D20382E2088E396F CC90BB91A294CC94848CE392B28DB882CC8CBB8FF382C697AF88D3935F2E >
 医薬品の製造販売後調査の現状と留意点 1 本日の内容 1. 改正医薬品 GPSP 省令 再生医療等製品 GPSP 省令 の留意点について 2. 医薬品の再審査申請資料適合性調査 (GPSP 実地調査及び適合性書面調査 ) 2 1. 改正医薬品 GPSP 省令 再生医療等製品 GPSP 省令 の留意点について 3 改正医薬品 GVP GPSP 省令 < 平成 25 年 3 月 11 日 > 医薬品の製造販売業者による医薬品リスク管理計画
医薬品の製造販売後調査の現状と留意点 1 本日の内容 1. 改正医薬品 GPSP 省令 再生医療等製品 GPSP 省令 の留意点について 2. 医薬品の再審査申請資料適合性調査 (GPSP 実地調査及び適合性書面調査 ) 2 1. 改正医薬品 GPSP 省令 再生医療等製品 GPSP 省令 の留意点について 3 改正医薬品 GVP GPSP 省令 < 平成 25 年 3 月 11 日 > 医薬品の製造販売業者による医薬品リスク管理計画
< F2D CFA90B6984A93AD8FC897DF91E632368D868169>
 厚生労働省令第二十六号薬事法(昭和三十五年法律第百四十五号)第十二条の二第二号並びに第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む )の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令及び医薬品の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十五年三月十一日厚生労働大臣田村憲久医薬品
厚生労働省令第二十六号薬事法(昭和三十五年法律第百四十五号)第十二条の二第二号並びに第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む )の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令及び医薬品の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十五年三月十一日厚生労働大臣田村憲久医薬品
PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1
 PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1 項第 1 号に定める医療機器リスク管理計画書をもって 承認申請資料のうち臨床試験の試験成績に関する資料又はこれに代替するものとして厚生労働大臣が認める資料の一部に代えることができることとしたこと
PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1 項第 1 号に定める医療機器リスク管理計画書をもって 承認申請資料のうち臨床試験の試験成績に関する資料又はこれに代替するものとして厚生労働大臣が認める資料の一部に代えることができることとしたこと
PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1
 薬生発 07 31 第 4 号 平成 29 年 7 月 31 日 各都道府県知事殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則の一部を改正する省令 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令の一部を改正する省令 及び 医療機器の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令
薬生発 07 31 第 4 号 平成 29 年 7 月 31 日 各都道府県知事殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則の一部を改正する省令 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令の一部を改正する省令 及び 医療機器の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令
宮城県立がんセンター受託研究業務手順書
 平成 26 年 4 月 1 日一部改正使用成績調査 特定使用成績調査編 本編は 薬事法第 14 条の 4 及び第 14 条の 6 に基づく医薬品及び医療機器の再審査 再評価申請の際に提出すべき資料の収集のために行われる製造販売後調査 ( 使用成績調査及び特定使用成績調査 )( 以下 使用成績調査等 ) に適用するものとする 本編は 薬事法第 14 条の 4 第 4 項 薬事法第 14 条の 6 第
平成 26 年 4 月 1 日一部改正使用成績調査 特定使用成績調査編 本編は 薬事法第 14 条の 4 及び第 14 条の 6 に基づく医薬品及び医療機器の再審査 再評価申請の際に提出すべき資料の収集のために行われる製造販売後調査 ( 使用成績調査及び特定使用成績調査 )( 以下 使用成績調査等 ) に適用するものとする 本編は 薬事法第 14 条の 4 第 4 項 薬事法第 14 条の 6 第
医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など ) 医薬品候補物質のスクリーニン
 特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
【押印あり】日本医学会宛
 別紙 再生医療等製品患者登録システムへの参加協力のお願い 患者登録システムの目的 患者登録システムは 再生医療等製品の市販後の使用状況や患者予後等のデータを収集し 迅速な安全対策や新たな製品開発等を通じて 医療の向上に役立てることを目的としています 患者登録システムは 製品毎に構築 運用されます この患者登録システムは 一般的には レジストリ と呼ばれることもあります 構築形態例 患者登録システムの対象
別紙 再生医療等製品患者登録システムへの参加協力のお願い 患者登録システムの目的 患者登録システムは 再生医療等製品の市販後の使用状況や患者予後等のデータを収集し 迅速な安全対策や新たな製品開発等を通じて 医療の向上に役立てることを目的としています 患者登録システムは 製品毎に構築 運用されます この患者登録システムは 一般的には レジストリ と呼ばれることもあります 構築形態例 患者登録システムの対象
薬機発第 号平成 24 年 10 月 12 日一部改正平成 28 年 3 月 30 日 ( 別記 ) 殿 独立行政法人医薬品医療機器総合機構理事長 医療機器の再審査及び再評価申請資料の適合性書面調査及びGPSP 実地調査の実施手続きについて の一部改正について 医療機器の再審査及び再
 薬機発第 1012066 号平成 24 年 10 月 12 日一部改正平成 28 年 3 月 30 日 ( 別記 ) 殿 独立行政法人医薬品医療機器総合機構理事長 医療機器の再審査及び再評価申請資料の適合性書面調査及びGPSP 実地調査の実施手続きについて の一部改正について 医療機器の再審査及び再評価申請資料の適合性書面調査及びGPSP 実地調査の実施手続きについて ( 平成 24 年 10 月
薬機発第 1012066 号平成 24 年 10 月 12 日一部改正平成 28 年 3 月 30 日 ( 別記 ) 殿 独立行政法人医薬品医療機器総合機構理事長 医療機器の再審査及び再評価申請資料の適合性書面調査及びGPSP 実地調査の実施手続きについて の一部改正について 医療機器の再審査及び再評価申請資料の適合性書面調査及びGPSP 実地調査の実施手続きについて ( 平成 24 年 10 月
北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下
 北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下 モニタリング という ) 監査の受け入れ 並びに試験審査委員会( 治験審査委員会が兼ねる 以下 治験審査委員会
北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下 モニタリング という ) 監査の受け入れ 並びに試験審査委員会( 治験審査委員会が兼ねる 以下 治験審査委員会
じ ) その他の処方せん医薬品又は高度管理医療機器の製造販売に係る業務の責任者との密接な連携を図らせること ( 安全確保業務に係る組織及び職員 ) 第四条第一種製造販売業者は 次に掲げる要件を満たす安全確保業務の統括に係る部門 ( 以下この章において 安全管理統括部門 という ) を置かなければなら
 厚生労働省令第百三十五号薬事法 ( 昭和三十五年法律第百四十五号 ) 第十二条の二第二号の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令を次のように定める 平成十六年九月二十二日厚生労働大臣坂口力 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令目次第一章総則 ( 第一条第二条 ) 第一種製造販売業者の製造販売後安全管理の基準
厚生労働省令第百三十五号薬事法 ( 昭和三十五年法律第百四十五号 ) 第十二条の二第二号の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令を次のように定める 平成十六年九月二十二日厚生労働大臣坂口力 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令目次第一章総則 ( 第一条第二条 ) 第一種製造販売業者の製造販売後安全管理の基準
Microsoft Word - (発番)医療機器の製造販売承認申請について
 薬食発 1120 第 5 号 平成 26 年 11 月 20 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医療機器の製造販売承認申請について 医療機器の製造販売承認申請の取扱いについては 医療機器の製造販売承認申請について ( 平成 17 年 2 月 16 日付け薬食発第 0216002 号厚生労働省医薬食品局長通知 以下 旧通知 という ) 等により実施してきたところです 先般
薬食発 1120 第 5 号 平成 26 年 11 月 20 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医療機器の製造販売承認申請について 医療機器の製造販売承認申請の取扱いについては 医療機器の製造販売承認申請について ( 平成 17 年 2 月 16 日付け薬食発第 0216002 号厚生労働省医薬食品局長通知 以下 旧通知 という ) 等により実施してきたところです 先般
医師主導治験取扱要覧
 15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
GVP省令
 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令 ( ) 発簡日平成 16 年 9 月 22 日発簡番号省令第 135 号情報種別省令 目次 第 1 章総則 ( 第 1 条 - 第 2 条 ) 第 2 章 第一種製造販売業者の製造販売後安全管理の基準 ( 第 3 条 - 第 12 条 ) 第 3 章 第二種製造販売業者の製造販売後安全管理の基準 ( 第 13 条 - 第
医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令 ( ) 発簡日平成 16 年 9 月 22 日発簡番号省令第 135 号情報種別省令 目次 第 1 章総則 ( 第 1 条 - 第 2 条 ) 第 2 章 第一種製造販売業者の製造販売後安全管理の基準 ( 第 3 条 - 第 12 条 ) 第 3 章 第二種製造販売業者の製造販売後安全管理の基準 ( 第 13 条 - 第
国立仙台病院受託研究取扱規程
 独立行政法人国立病院機構仙台医療センター受託研究取扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構仙台医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程の定めるところによる 2 契約 経理及び書式等については 原則として独立行政法人国立病院機構
独立行政法人国立病院機構仙台医療センター受託研究取扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構仙台医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程の定めるところによる 2 契約 経理及び書式等については 原則として独立行政法人国立病院機構
Microsoft Word - 奈良県GQP-GVPガイドライン doc
 三. 安全確保措置の実施に関する手順 1. 目的安全確保措置の実施に関する手順の目的を記載する < 記載例 > 本手順は GVP 省令の第 9 条に基づき 安全確保措置の実施を適正かつ円滑に行うために必要な手順を定めるものである 2. 適用範囲安全確保措置の実施に関する手順の適用範囲を記載する < 記載例 > 本手順書は 二. 安全管理情報の検討及びその結果に基づく安全確保措置の立案に関する手順 で立案された安全確保措置の決定
三. 安全確保措置の実施に関する手順 1. 目的安全確保措置の実施に関する手順の目的を記載する < 記載例 > 本手順は GVP 省令の第 9 条に基づき 安全確保措置の実施を適正かつ円滑に行うために必要な手順を定めるものである 2. 適用範囲安全確保措置の実施に関する手順の適用範囲を記載する < 記載例 > 本手順書は 二. 安全管理情報の検討及びその結果に基づく安全確保措置の立案に関する手順 で立案された安全確保措置の決定
製造販売後調査事務手続き等 について
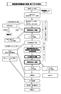 製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
前項に規定する事項のうち当該被験薬の治験薬概要書から予測できないもの に改め 同項を同条第三項とし 同条第一項の次に次の一項を加える 2治験依頼者は 被験薬について法第八十条の二第六項に規定する事項を知ったときは その発現症例一覧等を当該被験薬ごとに 当該被験薬について初めて治験の計画を届け出た日等
 厚生労働省令第二十四号薬事法(昭和三十五年法律第百四十五号)第十四条第三項(同条第九項及び同法第十九条の二第五項において準用する場合を含む ) 第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む ) 第八十条の二第一項 第四項及び第五項並びに第八十二条の規定に基づき 医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十年二月二十九日厚生労働大臣舛添要一医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令医薬品の臨床試験の実施の基準に関する省令(平成九年厚生省令第二十八号)の一部を次のように改正する
厚生労働省令第二十四号薬事法(昭和三十五年法律第百四十五号)第十四条第三項(同条第九項及び同法第十九条の二第五項において準用する場合を含む ) 第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む ) 第八十条の二第一項 第四項及び第五項並びに第八十二条の規定に基づき 医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十年二月二十九日厚生労働大臣舛添要一医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令医薬品の臨床試験の実施の基準に関する省令(平成九年厚生省令第二十八号)の一部を次のように改正する
&Aについて ( 平成 21 年 9 月 7 日付け厚生労働省医薬食品局審査管理課長 安全対策課長事務連絡 ) では 全例調査が承認条件として付される場合として 国内治験症例が少ないか又はない場合や 重篤な副作用等の発現が懸念される場合等がこれに該当するとされている また 再審査期間よりも早く症例数
 (2) 製造販売後の安全性確保のための各種調査の整合性の確保勧告説明図表番号 制度の概要等 1 医薬品又は医療機器の製造販売の承認を受けた者は 薬事法第 14 条の4 図表 3-(2)-1 第 1 項の規定により 承認後 同項第 1 号に規定する一定期間 ( 以下 再審査期間 という ) を経過した日から起算して三月以内の期間又は厚生労働大臣が指示する期間内に申請して 厚生労働大臣の再審査を受けなければならないとされている
(2) 製造販売後の安全性確保のための各種調査の整合性の確保勧告説明図表番号 制度の概要等 1 医薬品又は医療機器の製造販売の承認を受けた者は 薬事法第 14 条の4 図表 3-(2)-1 第 1 項の規定により 承認後 同項第 1 号に規定する一定期間 ( 以下 再審査期間 という ) を経過した日から起算して三月以内の期間又は厚生労働大臣が指示する期間内に申請して 厚生労働大臣の再審査を受けなければならないとされている
写 薬生発 0131 第 1 号 平成 30 年 1 月 31 日 都道府県知事 殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 関係手数料令の一部を改正する政令の公布について この度 医薬品 医療機器等の品質 有効性及び安全性の確
 薬生発 0131 第 3 号 平成 30 年 1 月 31 日 独立行政法人医薬品医療機器総合機構理事長殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 関係手数料令の一部を改正する政令の公布について 標記につきまして 別添写しのとおり都道府県知事宛てに通知しましたので お 知らせいたします 写 薬生発 0131 第 1 号 平成 30
薬生発 0131 第 3 号 平成 30 年 1 月 31 日 独立行政法人医薬品医療機器総合機構理事長殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 関係手数料令の一部を改正する政令の公布について 標記につきまして 別添写しのとおり都道府県知事宛てに通知しましたので お 知らせいたします 写 薬生発 0131 第 1 号 平成 30
GVPの基礎
 京都府健康福祉部薬務課 平成 29 年 3 月 8 日 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令 (GVP 省令 ) GVP 省令 第一章 ( 総則 ) 第二章 ( 第一種製販の製造販売後安全管理の基準 ) 第三章 ( 第二種製販の製造販売後安全管理の基準 ) 第四章 ( 第三種製販の製造販売後安全管理の基準 ) 第五章 ( 雑則 ) 第一種 ~
京都府健康福祉部薬務課 平成 29 年 3 月 8 日 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令 (GVP 省令 ) GVP 省令 第一章 ( 総則 ) 第二章 ( 第一種製販の製造販売後安全管理の基準 ) 第三章 ( 第二種製販の製造販売後安全管理の基準 ) 第四章 ( 第三種製販の製造販売後安全管理の基準 ) 第五章 ( 雑則 ) 第一種 ~
独立行政法人国立病院機構仙台医療センターにおける医薬 品等の使用成績調査 特定使用成績調査及び副作用 感染 症報告 その他の受託研究の実施に関する標準業務手順書 2018 年 7 月 26 日第 9 版
 独立行政法人国立病院機構仙台医療センターにおける医薬 品等の使用成績調査 特定使用成績調査及び副作用 感染 症報告 その他の受託研究の実施に関する標準業務手順書 2018 年 7 月 26 日第 9 版 第 1 章総則 1. 目的と適用範囲この標準業務手順書は 独立行政法人国立病院機構仙台医療センターにおける医薬品の再審査申請 再評価申請の際に提出すべき資料の収集のための 使用成績調査 及び 特定使用成績調査
独立行政法人国立病院機構仙台医療センターにおける医薬 品等の使用成績調査 特定使用成績調査及び副作用 感染 症報告 その他の受託研究の実施に関する標準業務手順書 2018 年 7 月 26 日第 9 版 第 1 章総則 1. 目的と適用範囲この標準業務手順書は 独立行政法人国立病院機構仙台医療センターにおける医薬品の再審査申請 再評価申請の際に提出すべき資料の収集のための 使用成績調査 及び 特定使用成績調査
Microsoft PowerPoint - ⑨140925,30日薬連講習会(後発RMP)930.ppt [互換モード]
![Microsoft PowerPoint - ⑨140925,30日薬連講習会(後発RMP)930.ppt [互換モード] Microsoft PowerPoint - ⑨140925,30日薬連講習会(後発RMP)930.ppt [互換モード]](/thumbs/101/151698947.jpg) 後発医薬品 RMP について 厚生労働省医薬食品局安全対策課磯﨑正季子 1 後発医薬品への RMP の適用 平成 24 年 4 月 11 日薬食安発 0411 第 1 号 薬食審査発 0411 第 2 号安全対策課長 審査管理課長連名通知 医薬品リスク管理計画指針について 適用範囲医療用医薬品 ( 新医薬品 バイオ後続品 後発医薬品 ) 策定検討の時点 承認申請時 新医薬品 バイオ後続品後発医薬品
後発医薬品 RMP について 厚生労働省医薬食品局安全対策課磯﨑正季子 1 後発医薬品への RMP の適用 平成 24 年 4 月 11 日薬食安発 0411 第 1 号 薬食審査発 0411 第 2 号安全対策課長 審査管理課長連名通知 医薬品リスク管理計画指針について 適用範囲医療用医薬品 ( 新医薬品 バイオ後続品 後発医薬品 ) 策定検討の時点 承認申請時 新医薬品 バイオ後続品後発医薬品
医療機器使用成績評価制度ガイダンス ( 一社 ) 日本医療機器産業連合会 使用成績評価制度のガイダンス作成 WG 2018 年 11 月 1 日 1
 医療機器使用成績評価制度ガイダンス ( 一社 ) 日本医療機器産業連合会 使用成績評価制度のガイダンス作成 WG 2018 年 11 月 1 日 1 目次 1 目的... 4 2 背景... 5 3 使用成績評価全体のプロセスと本ガイダンスの構成... 7 4 関連通知... 10 5 各プロセスの解説... 12 I. 体制構築... 12 Ⅰ-1. 調査に関連する社内組織体制の構築... 12
医療機器使用成績評価制度ガイダンス ( 一社 ) 日本医療機器産業連合会 使用成績評価制度のガイダンス作成 WG 2018 年 11 月 1 日 1 目次 1 目的... 4 2 背景... 5 3 使用成績評価全体のプロセスと本ガイダンスの構成... 7 4 関連通知... 10 5 各プロセスの解説... 12 I. 体制構築... 12 Ⅰ-1. 調査に関連する社内組織体制の構築... 12
<4D F736F F D E34208EA18CB18EE891B182AB977697CC C8E8DB782B591D682A688CB978A>
 Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リ
 薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リスク管理計画の実施状況及び得られた結果の評価に関する報告の様式 提出等の取扱いについては 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について
薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リスク管理計画の実施状況及び得られた結果の評価に関する報告の様式 提出等の取扱いについては 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について
<4D F736F F D2093FA96F AD91E D86>
 独立行政法人医薬品医療機器総合機構が行う対面助言 証明確認調査等の実施要綱等について新旧対照表 別添 改正後 改正前 ( 下線部分 : 改正部分 ) 今般 医薬部外品の審査の迅速化や円滑化を図ることを目的として 新たに医薬部外品 ( 防除用医薬部外品を除く 以下同じ ) 開発相談を新設するとともに 医薬品再審査適合性調査相談について 対象範囲を拡大する改訂を行いました ( 中略 ) 1. 対面助言
独立行政法人医薬品医療機器総合機構が行う対面助言 証明確認調査等の実施要綱等について新旧対照表 別添 改正後 改正前 ( 下線部分 : 改正部分 ) 今般 医薬部外品の審査の迅速化や円滑化を図ることを目的として 新たに医薬部外品 ( 防除用医薬部外品を除く 以下同じ ) 開発相談を新設するとともに 医薬品再審査適合性調査相談について 対象範囲を拡大する改訂を行いました ( 中略 ) 1. 対面助言
医療事故調査・支援センター~センターの役割と手引~
 医療事故調査 支援センター センターの役割と手続き 日本医療安全調査機構 医療事故調査 支援センター 木村壯介 medsafe.or.jp 医療事故調査 支援センターの役割 医療法第 6 条 16( 抜粋 ) 日本医療安全調査機構医療事故調査 支援センター 1 病院等が行った医療事故調査結果の報告により収集した情報の整理及び分析を行う 2 報告をした病院等の管理者に対し 情報の整理及び分析結果の報告を行う
医療事故調査 支援センター センターの役割と手続き 日本医療安全調査機構 医療事故調査 支援センター 木村壯介 medsafe.or.jp 医療事故調査 支援センターの役割 医療法第 6 条 16( 抜粋 ) 日本医療安全調査機構医療事故調査 支援センター 1 病院等が行った医療事故調査結果の報告により収集した情報の整理及び分析を行う 2 報告をした病院等の管理者に対し 情報の整理及び分析結果の報告を行う
記 1. 適用対象本通知は 製造販売業者等が GPSP 省令第 2 条第 3 項に規定する DB 事業者が提供する同条第 2 項に規定する医療情報データベースを用いて同条第 1 項第 2 号に規定する製造販売後データベース調査を実施し 医薬品の再審査等の申請資料を作成する場合に適用する GPSP 省
 記 1. 適用対象本通知は 製造販売業者等が GPSP 省令第 2 条第 3 項に規定する DB 事業者が提供する同条第 2 項に規定する医療情報データベースを用いて同条第 1 項第 2 号に規定する製造販売後データベース調査を実施し 医薬品の再審査等の申請資料を作成する場合に適用する GPSP 省令第 2 条第 2 項において 医療情報データベース とは 一定の期間において収集される診療録その他の診療に関する記録
記 1. 適用対象本通知は 製造販売業者等が GPSP 省令第 2 条第 3 項に規定する DB 事業者が提供する同条第 2 項に規定する医療情報データベースを用いて同条第 1 項第 2 号に規定する製造販売後データベース調査を実施し 医薬品の再審査等の申請資料を作成する場合に適用する GPSP 省令第 2 条第 2 項において 医療情報データベース とは 一定の期間において収集される診療録その他の診療に関する記録
薬事法における病院及び医師に対する主な規制について 特定生物由来製品に係る説明 ( 法第 68 条の 7 平成 14 年改正 ) 特定生物由来製品の特性を踏まえ 製剤のリスクとベネフィットについて患者に説明を行い 理解を得るように努めることを これを取り扱う医師等の医療関係者に義務づけたもの ( 特
 薬事法における病院及び医師に対する主な規制について 情報の提供等 ( 法第 77 条の 3 第 2 項及び第 3 項 第 2 項 : 昭和 54 年改正 第 3 項 : 平成 6 年改正 ) 医薬品の製造販売業者等が行う医薬品又は医療機器の適正な使用のために必要な情報の収集に協力するよう努めることを また 医薬品及び医療機器の適正な使用を確保するため 医薬品の製造販売業者等から提供される情報の活用その他必要な情報の収集
薬事法における病院及び医師に対する主な規制について 情報の提供等 ( 法第 77 条の 3 第 2 項及び第 3 項 第 2 項 : 昭和 54 年改正 第 3 項 : 平成 6 年改正 ) 医薬品の製造販売業者等が行う医薬品又は医療機器の適正な使用のために必要な情報の収集に協力するよう努めることを また 医薬品及び医療機器の適正な使用を確保するため 医薬品の製造販売業者等から提供される情報の活用その他必要な情報の収集
臨床試験(治験)実施の手続き
 製造販売後調査実施の手続き はじめに 本書は 昭和大学藤が丘病院における製造販売後調査実施の手続き方法等について記載したものです 本書内のは当院が提供する書類を示し は審査等に必要な書類を示しております 調査内容により提出書類 資料に変更が生じる場合があります 詳細は支援室にご確認ください 申請する書類および資料は 事前に E-mail に添付して支援室にお送りください 内容の確認をし ご連絡させて頂きます
製造販売後調査実施の手続き はじめに 本書は 昭和大学藤が丘病院における製造販売後調査実施の手続き方法等について記載したものです 本書内のは当院が提供する書類を示し は審査等に必要な書類を示しております 調査内容により提出書類 資料に変更が生じる場合があります 詳細は支援室にご確認ください 申請する書類および資料は 事前に E-mail に添付して支援室にお送りください 内容の確認をし ご連絡させて頂きます
平成14年8月 日
 平成 30 年 11 月 15 日福祉保健局 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 に基づく行政処分 ( 回収命令 ) について 都は本日 以下の事業者に対し 医薬品 医療機器等の品質 有効性及び安全性の確保 等に関する法律 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 70 条第 1 項の 規定に基づく 回収命令 を行ったので お知らせします 1 対象事業者氏名ピュアハートキングス株式会社
平成 30 年 11 月 15 日福祉保健局 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 に基づく行政処分 ( 回収命令 ) について 都は本日 以下の事業者に対し 医薬品 医療機器等の品質 有効性及び安全性の確保 等に関する法律 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 70 条第 1 項の 規定に基づく 回収命令 を行ったので お知らせします 1 対象事業者氏名ピュアハートキングス株式会社
はじめて医療機器を製造販売または製造される方へ
 を製造 ( 輸入 ) 販売するには 国内で必要な許可等について を製造販売 製造 ( 輸入 ) するためには 医薬品 等の品質 有効性及び安全性の確保等に関する法律 ( 以下 薬機法という ) の許可等 ( 製造販売業許可 製造業登録 ) が必要になります 製品を市場に出荷するために必要な許可 販売する製品に対して最終責製造販売業任を持ち 自社の名前で市場へ出荷する この許可では製造することはできません
を製造 ( 輸入 ) 販売するには 国内で必要な許可等について を製造販売 製造 ( 輸入 ) するためには 医薬品 等の品質 有効性及び安全性の確保等に関する法律 ( 以下 薬機法という ) の許可等 ( 製造販売業許可 製造業登録 ) が必要になります 製品を市場に出荷するために必要な許可 販売する製品に対して最終責製造販売業任を持ち 自社の名前で市場へ出荷する この許可では製造することはできません
3 治験実施計画書目的 当該治験について 治験実施計画書が手順書に従い適切に作成及び改訂されていることを確認する 次の事項を調べる (1) 治験実施計画書の記載項目 ( 再生医療等製品 GCP 省令第 7 条第 1 項に規定する項目 ) (2) 治験実施計画書の作成 改訂の手順と日付 (3) 治験計
 別添 10 再生医療等製品 GCP 省令チェックリスト Ⅰ 治験依頼者 ( 受託機関を含む ) 用 1 組織及び体制目的 治験の依頼及び管理に当たって 再生医療等製品 GCP 省令に沿った業務を行うために適切にして十分な人材を有し かつ 組織及び体制が確立していることを確認する 1 治験依頼者の組織 ( 当該被験機器の開発組織を含む ) と再生医療等製品 G CP 省令に係わる組織との関係 2 治験の依頼及び管理の業務に従事する者の氏名
別添 10 再生医療等製品 GCP 省令チェックリスト Ⅰ 治験依頼者 ( 受託機関を含む ) 用 1 組織及び体制目的 治験の依頼及び管理に当たって 再生医療等製品 GCP 省令に沿った業務を行うために適切にして十分な人材を有し かつ 組織及び体制が確立していることを確認する 1 治験依頼者の組織 ( 当該被験機器の開発組織を含む ) と再生医療等製品 G CP 省令に係わる組織との関係 2 治験の依頼及び管理の業務に従事する者の氏名
Basic Agreement for Marketing Certification Service under PMD Act / 医薬品医療機器法製造販売認証サービス基本合意書
 医薬品医療機器法に基づく製造販売認証サービスを申請されるにあたりご了解いただきたいこと テュフズードジャパン株式会社 MHS 事業部 弊社では 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 以下 医薬品医療機器法又は法 ) に基づく製造販売認証サービスを提供させていただくにあたり 次の各項についてご了解いただくよう全てのお客様にお願いしております 最初のご申請までにこの書面をお読みいただき最終ページに貴社の名称
医薬品医療機器法に基づく製造販売認証サービスを申請されるにあたりご了解いただきたいこと テュフズードジャパン株式会社 MHS 事業部 弊社では 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 以下 医薬品医療機器法又は法 ) に基づく製造販売認証サービスを提供させていただくにあたり 次の各項についてご了解いただくよう全てのお客様にお願いしております 最初のご申請までにこの書面をお読みいただき最終ページに貴社の名称
< F2D819B955C8EA692CA926D DC58F4994AD8F6F>
 薬食監麻発第 0331008 号平成 17 年 3 月 31 日 各都道府県衛生主管部 ( 局 ) 長 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 一部改正法 という ) 第 2 条の規定による改正後の薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 及び関係政省令等の規定に基づく医薬品 医薬部外品 化粧品及び医療機器 (
薬食監麻発第 0331008 号平成 17 年 3 月 31 日 各都道府県衛生主管部 ( 局 ) 長 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 一部改正法 という ) 第 2 条の規定による改正後の薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 及び関係政省令等の規定に基づく医薬品 医薬部外品 化粧品及び医療機器 (
< F2D CFA90B6984A93AD8FC897DF91E632368D869056>
 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令及び医薬品の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令新旧対照条文 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令(平成十六年厚生労働省令第百三十五号)(抄)(第一条関係)(傍線の部分は改正部分)改正案現行(定義)(定義)第二条(略)第二条(略)2(略)2(略)3この省令で
医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令及び医薬品の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令新旧対照条文 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令(平成十六年厚生労働省令第百三十五号)(抄)(第一条関係)(傍線の部分は改正部分)改正案現行(定義)(定義)第二条(略)第二条(略)2(略)2(略)3この省令で
JCROA自主ガイドライン第4版案 GCP監査WG改訂案及び意見
 受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
文書管理番号
 プライバシーマーク付与適格性審査実施規程 1. 一般 1.1 適用範囲この規程は プライバシーマーク付与の適格性に関する審査 ( 以下 付与適格性審査 という ) を行うプライバシーマーク指定審査機関 ( 以下 審査機関 という ) が その審査業務を遂行する際に遵守すべき事項を定める 1.2 用語この基準で用いる用語は 特段の定めがない限り プライバシーマーク制度基本綱領 プライバシーマーク指定審査機関指定基準
プライバシーマーク付与適格性審査実施規程 1. 一般 1.1 適用範囲この規程は プライバシーマーク付与の適格性に関する審査 ( 以下 付与適格性審査 という ) を行うプライバシーマーク指定審査機関 ( 以下 審査機関 という ) が その審査業務を遂行する際に遵守すべき事項を定める 1.2 用語この基準で用いる用語は 特段の定めがない限り プライバシーマーク制度基本綱領 プライバシーマーク指定審査機関指定基準
Ⅲ-4 調査 研究委託に関する基準 改定改定改定改定改定改定改定 平成 10 年 1 月 20 日公正取引委員会届出平成 13 年 6 月 14 日公正取引委員会届出平成 16 年 5 月 25 日公正取引委員会届出平成 17 年 3 月 29 日公正取引委員会届出平成 17 年 12 月 22 日
 Ⅲ-4 調査 研究委託に関する基準 改定改定改定改定改定改定改定 平成 10 年 1 月 20 日公正取引委員会届出平成 13 年 6 月 14 日公正取引委員会届出平成 16 年 5 月 25 日公正取引委員会届出平成 17 年 3 月 29 日公正取引委員会届出平成 17 年 12 月 22 日公正取引委員会届出平成 27 年 9 月 3 日公正取引委員会 消費者庁長官届出平成 29 年 9 月
Ⅲ-4 調査 研究委託に関する基準 改定改定改定改定改定改定改定 平成 10 年 1 月 20 日公正取引委員会届出平成 13 年 6 月 14 日公正取引委員会届出平成 16 年 5 月 25 日公正取引委員会届出平成 17 年 3 月 29 日公正取引委員会届出平成 17 年 12 月 22 日公正取引委員会届出平成 27 年 9 月 3 日公正取引委員会 消費者庁長官届出平成 29 年 9 月
Microsoft PowerPoint - 運用 [互換モード]
![Microsoft PowerPoint - 運用 [互換モード] Microsoft PowerPoint - 運用 [互換モード]](/thumbs/91/105850431.jpg) 押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
(3) 事前面談の日程等の連絡申込書を受け付けた後に 機構担当者より 電話で日程等を連絡します なお 事前面談の質問内容に応じて 電話による回答を行う場合があります (4) (5)( 略 ) (3) 事前面談の日程等の連絡申込書を受付けた後に 機構担当者より 電話で日程等を連絡します なお 事前面談
 レギュラトリーサイエンス戦略相談に関する実施要綱新旧対照表 改正後 3. 相談の種類 RS 戦略相談の申込みに際しては 予め 事前面談を申し込みいただき 機構の担当者と上に示した事項について面談を行ってください 事前面談の結果を踏まえた上で 対面助言の申込みをしていただくことになります 対面助言の対象については 原則として 優先分野 ( 下記 ) に該当し かつ 有望性が期待できるものとします (
レギュラトリーサイエンス戦略相談に関する実施要綱新旧対照表 改正後 3. 相談の種類 RS 戦略相談の申込みに際しては 予め 事前面談を申し込みいただき 機構の担当者と上に示した事項について面談を行ってください 事前面談の結果を踏まえた上で 対面助言の申込みをしていただくことになります 対面助言の対象については 原則として 優先分野 ( 下記 ) に該当し かつ 有望性が期待できるものとします (
<4D F736F F D2088E396F BB91A28BC EF C8EA695DB8AC78BE695AA816A C826F8AEE8F808F918EE88F878F B2E646F63>
 16 12 24 179 26 1 5 26 1 5 注意 品質部門は製造部門から独立していなければならない 各部門の業務を適切かつ円滑に実施しうる能力のある責任者を 組織 規模 業務の種類に応じ 適切な人数を配置すること ( 必要に応じ 上記に挙げた責任者の枠を増やしてもよい ) 各責任者は業務に支障がない限り兼務することができる ただし 製造部門責任者と品質部門責任者は兼務することはできない 出荷可否決定者は品質部門の者とすること
16 12 24 179 26 1 5 26 1 5 注意 品質部門は製造部門から独立していなければならない 各部門の業務を適切かつ円滑に実施しうる能力のある責任者を 組織 規模 業務の種類に応じ 適切な人数を配置すること ( 必要に応じ 上記に挙げた責任者の枠を増やしてもよい ) 各責任者は業務に支障がない限り兼務することができる ただし 製造部門責任者と品質部門責任者は兼務することはできない 出荷可否決定者は品質部門の者とすること
標準業務手順 目次
 浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
<4D F736F F D208EA18CB182C98AD682B782E995578F808BC696B18EE88F878F E38E748EE593B1816A E7B8D732E646F637
 治験に関する標準業務手順書 ( 医師主導治験 ) 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医師主導治験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 (
治験に関する標準業務手順書 ( 医師主導治験 ) 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医師主導治験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 (
員長及び医薬品医療機器等法登録認証機関協議会代表幹事宛て送付するこ ととしていることを申し添えます 記 1. 基本要件基準第 13 条第 5 項及び第 6 項への適合性確認の基本的な考え方について (1)2023 年 ( 平成 35 年 )2 月 28 日 ( 以下 経過措置期間終了日 という )
 薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
<4D F736F F D208EA18CB182C98AD682B782E995578F808BC696B18EE88F878F E7B8D732E646F6378>
 治験に関する標準業務手順書 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医薬品及び医療機器の臨床試験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和
治験に関する標準業務手順書 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医薬品及び医療機器の臨床試験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和
規程書
 独立行政法人国立病院機構栃木医療センター 受託研究取扱規程 平成 25 年 4 月 1 日 独立行政法人国立病院機構栃木医療センター受託研究取 扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構栃木医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程定めるところによる
独立行政法人国立病院機構栃木医療センター 受託研究取扱規程 平成 25 年 4 月 1 日 独立行政法人国立病院機構栃木医療センター受託研究取 扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構栃木医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程定めるところによる
厚生労働省令第 136 号 平成 16 年 9 月 22 日 薬事法 ( 昭和三十五年法律第百四十五号 ) 第十二条の二第一号の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の品質管理の基準に関する省令を次のように定める 平成十六年九月二十二日厚生労働大臣坂口力 医薬品 医薬部外品 化粧品及び
 厚生労働省令第 136 号 平成 16 年 9 月 22 日 薬事法 ( 昭和三十五年法律第百四十五号 ) 第十二条の二第一号の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の品質管理の基準に関する省令を次のように定める 平成十六年九月二十二日厚生労働大臣坂口力 医薬品 医薬部外品 化粧品及び医療機器の品質管理の基準に関する省令 目次第一章総則 ( 第一条 第二条 ) 第二章医薬品の品質管理の基準
厚生労働省令第 136 号 平成 16 年 9 月 22 日 薬事法 ( 昭和三十五年法律第百四十五号 ) 第十二条の二第一号の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の品質管理の基準に関する省令を次のように定める 平成十六年九月二十二日厚生労働大臣坂口力 医薬品 医薬部外品 化粧品及び医療機器の品質管理の基準に関する省令 目次第一章総則 ( 第一条 第二条 ) 第二章医薬品の品質管理の基準
Microsoft Word - 【案1】登録認証機関立入要領改正通知(Ver )
 薬食機参発 1121 第 38 号平成 26 年 11 月 21 日 各登録認証機関の長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) 登録認証機関等に対する立入検査の実施要領の改正について 薬事法 ( 昭和 35 年法律第 145 号 ) の規定による登録認証機関等に対する立入 検査の実施要領については 登録認証機関等に対する立入検査の実施要領について ( 平成 18
薬食機参発 1121 第 38 号平成 26 年 11 月 21 日 各登録認証機関の長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) 登録認証機関等に対する立入検査の実施要領の改正について 薬事法 ( 昭和 35 年法律第 145 号 ) の規定による登録認証機関等に対する立入 検査の実施要領については 登録認証機関等に対する立入検査の実施要領について ( 平成 18
国立病院機構大阪医療センター受託研究取扱細則
 国立病院機構大阪医療センター 受託研究取扱細則 ( 主旨 ) 第 1 条国立病院機構大阪医療センターにおける受託研究の取扱いに関しては 国立病院機構大阪医療センター受託研究取扱規程 ( 以下 規程 という ) 及び他に定めるもののほか 規程第 1 条第 2 項に規定するこの細則の定めるところによる ( 総則 ) 第 2 条研究責任者は 原則として医長職相当以上とする ただし 副作用報告及び感染症報告を受託研究として実施する場合
国立病院機構大阪医療センター 受託研究取扱細則 ( 主旨 ) 第 1 条国立病院機構大阪医療センターにおける受託研究の取扱いに関しては 国立病院機構大阪医療センター受託研究取扱規程 ( 以下 規程 という ) 及び他に定めるもののほか 規程第 1 条第 2 項に規定するこの細則の定めるところによる ( 総則 ) 第 2 条研究責任者は 原則として医長職相当以上とする ただし 副作用報告及び感染症報告を受託研究として実施する場合
ISO13485:2005 と本邦における QMS との違いについて ( いわゆる追加的要求事項と呼ばれる事項について よく質問があります 品質マニュアル ( 品質管 理監督基準書 ) 作成の際に参考になると幸いです 条項ごとに解説を記載しましたので 参考にしてください 追加的要求事項 1: 製造所
 追加的要求事項とは QMS 省令第 3 章 追加的要求事項 とは 製造販売業に要求されていた GQP が QMS に変更されたことに伴って変更された事項と ISO の要求事項との違いを追加的要求事項とされている 条項 第 71 条 背景変更点と背景 管理監督者と管理者の設置 第 65 条 第 66 条 第 69 条 GQP からの変更 製造委託先に対する製造管理 品質管理の管理責任 製造委託先に対する品質管理監督基準の作成の要請
追加的要求事項とは QMS 省令第 3 章 追加的要求事項 とは 製造販売業に要求されていた GQP が QMS に変更されたことに伴って変更された事項と ISO の要求事項との違いを追加的要求事項とされている 条項 第 71 条 背景変更点と背景 管理監督者と管理者の設置 第 65 条 第 66 条 第 69 条 GQP からの変更 製造委託先に対する製造管理 品質管理の管理責任 製造委託先に対する品質管理監督基準の作成の要請
(Microsoft PowerPoint - GVPGQP\203t\203H\203\215\201[\203A\203b\203v.pptx)
 平成 27 年度医薬品製造販売業におけるおける調査 (GVP GQP) 奈良県医療政策部薬務課振興係 調査状況 平成 26 年度末に 製造販売業は製造業と共と共に大更新に大更新を終えました 更新時は 製造業の GMP を重点に確認を行ったところ 1 平成 27 年度調査概要 調査 1 製造販売業の GQP G VP についてのフォローアップ調査 調査 2 製造業の追加 GMP 項目についての調査 調査スケジュール
平成 27 年度医薬品製造販売業におけるおける調査 (GVP GQP) 奈良県医療政策部薬務課振興係 調査状況 平成 26 年度末に 製造販売業は製造業と共と共に大更新に大更新を終えました 更新時は 製造業の GMP を重点に確認を行ったところ 1 平成 27 年度調査概要 調査 1 製造販売業の GQP G VP についてのフォローアップ調査 調査 2 製造業の追加 GMP 項目についての調査 調査スケジュール
事務連絡 平成 28 年 3 月 29 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局審査管理課 厚生労働省医薬 生活衛生局監視指導 麻薬対策課 医薬品等の製造業許可 外国製造業者認定等に関する質疑応答集 (Q&A) について 今般 標記 Q&A を別添のとおりとり
 事務連絡 平成 28 年 3 月 29 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局審査管理課 厚生労働省医薬 生活衛生局監視指導 麻薬対策課 医薬品等の製造業許可 外国製造業者認定等に関する質疑応答集 (Q&A) について 今般 標記 Q&A を別添のとおりとりまとめましたので 御了知の上 貴管下関係業 者に対して周知願います なお 本通知の写しを別記関係団体宛て送付することとしています
事務連絡 平成 28 年 3 月 29 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局審査管理課 厚生労働省医薬 生活衛生局監視指導 麻薬対策課 医薬品等の製造業許可 外国製造業者認定等に関する質疑応答集 (Q&A) について 今般 標記 Q&A を別添のとおりとりまとめましたので 御了知の上 貴管下関係業 者に対して周知願います なお 本通知の写しを別記関係団体宛て送付することとしています
医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年
![医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年 医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年](/thumbs/91/107149459.jpg) 事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
<4D F736F F D2090BB91A294CC94848CE392B28DB8905C90BF8E9E92F18F6F8F9197DE82A882E682D1928D88D38E968D E48DEC90AC816A
 申請時提出書類 ( 新規 ) 医薬品等の製造販売後調査実施依頼申請書 様式第 1 ( 以下 依頼書 ) 医薬品等の製造販売後調査実施申請書 様式第 2 ( 以下 申請書 ) 医薬品等の製造販売後調査実施に関する通知書 ( 病院用 依頼者用 ) 様式第 3 様式第 4 ( 以下 通知書 ) 医薬品等の製造販売後調査実施契約書 ( 病院用 依頼者用 ) 様式第 5 様式第 5の2 ( 以下 契約書 )
申請時提出書類 ( 新規 ) 医薬品等の製造販売後調査実施依頼申請書 様式第 1 ( 以下 依頼書 ) 医薬品等の製造販売後調査実施申請書 様式第 2 ( 以下 申請書 ) 医薬品等の製造販売後調査実施に関する通知書 ( 病院用 依頼者用 ) 様式第 3 様式第 4 ( 以下 通知書 ) 医薬品等の製造販売後調査実施契約書 ( 病院用 依頼者用 ) 様式第 5 様式第 5の2 ( 以下 契約書 )
( 別添 2) ( 別添 2) 平成 14 年 9 月 27 日保発第 号の別添 2 組合管掌健康保険一括適用取扱要領 組合管掌健康保険一括適用取扱要領 ( 準則 ) 第 1 健康保険法 ( 以下 法 という ) 第 34 条第 1 項の規定による厚生労働大臣の承認 ( 以下 一括適
 ( 別添 1) 新 ( 別添 1) 健康保険 厚生年金保険一括適用承認基準 健康保険一括適用承認基準 健康保険法第 34 条第 1 項又は厚生年金保険法第 8 条の 2 の規定による厚生労働大 臣の承認 ( 以下 一括適用の承認 という ) は 次の各項に定める基準に適合する適 用事業所について行うものとする 健康保険法第 34 条の規定による厚生労働大臣の承認 ( 以下 一括適用の承認 と いう
( 別添 1) 新 ( 別添 1) 健康保険 厚生年金保険一括適用承認基準 健康保険一括適用承認基準 健康保険法第 34 条第 1 項又は厚生年金保険法第 8 条の 2 の規定による厚生労働大 臣の承認 ( 以下 一括適用の承認 という ) は 次の各項に定める基準に適合する適 用事業所について行うものとする 健康保険法第 34 条の規定による厚生労働大臣の承認 ( 以下 一括適用の承認 と いう
12_モニタリングの実施に関する手順書
 12_ モニタリングの実施に関する手順書 静岡県立大学大学院薬食生命科学総合学府薬学研究院薬食研究推進センター版数 :1.0 版作成年月日 :2014 月 8 月 1 日 ( 最終確定 :2015 年 1 月 14 日 ) 1. 目的と適用範囲 本手順書は 当該研究において モニターが モニタリングを適切に実施するための手順 その他必要な事項を定めるものである 2. 実施体制及び責務 2.1 研究責任者の責務研究責任者は
12_ モニタリングの実施に関する手順書 静岡県立大学大学院薬食生命科学総合学府薬学研究院薬食研究推進センター版数 :1.0 版作成年月日 :2014 月 8 月 1 日 ( 最終確定 :2015 年 1 月 14 日 ) 1. 目的と適用範囲 本手順書は 当該研究において モニターが モニタリングを適切に実施するための手順 その他必要な事項を定めるものである 2. 実施体制及び責務 2.1 研究責任者の責務研究責任者は
< F2D8E9197BF A836F815B2E6A7464>
 ( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
(Microsoft Word -
 事務連絡 平成 30 年 2 月 28 日 医薬品 医療機器等製造販売業者殿 奈良県医療政策部薬務課薬物監視係長 医薬品 医療機器等の回収の取扱いについて 医薬品 医薬部外品 化粧品及び医療機器等の回収については 医薬品 医療機器等の回収について ( 平成 26 年 12 月 21 日付け薬食発 1121 第 10 号厚生労働省医薬食品局長通知 ) 及び 医薬品 医療機器等の回収の取扱いについて (
事務連絡 平成 30 年 2 月 28 日 医薬品 医療機器等製造販売業者殿 奈良県医療政策部薬務課薬物監視係長 医薬品 医療機器等の回収の取扱いについて 医薬品 医薬部外品 化粧品及び医療機器等の回収については 医薬品 医療機器等の回収について ( 平成 26 年 12 月 21 日付け薬食発 1121 第 10 号厚生労働省医薬食品局長通知 ) 及び 医薬品 医療機器等の回収の取扱いについて (
特定臨床研究に関する手順書
 学校法人日本医科大学における特定臨床研究に関する手順書 ( 新規申請分 ) 1. 目的 本手順書は 学校法人日本医科大学における特定臨床研究に関する規程 ( 以下 規程 という ) を円滑に運用するために 本法人における手順を示すものである 2. 用語の定義 2.1 全般本手順書において使用する用語は 規程において使用する用語の例によるものとする 2.2 付属所属長規程第 5 条第 2 項により 理事長は実施医療機関の管理者の権限を次に定める付属所属長に委任しているため
学校法人日本医科大学における特定臨床研究に関する手順書 ( 新規申請分 ) 1. 目的 本手順書は 学校法人日本医科大学における特定臨床研究に関する規程 ( 以下 規程 という ) を円滑に運用するために 本法人における手順を示すものである 2. 用語の定義 2.1 全般本手順書において使用する用語は 規程において使用する用語の例によるものとする 2.2 付属所属長規程第 5 条第 2 項により 理事長は実施医療機関の管理者の権限を次に定める付属所属長に委任しているため
申請ソフトの起動 申請ソフトを起動して ファイル 申請書の新規作成 を選択 様式から C04 を選択し 了解 クリック ( 参考 1) FD 申請ソフトでの申請書鑑の打出しは 印字されない空欄箇所がありますので 別途 書面による鑑の作成が必要です その方法は FD 申請ソフトの入力手順の次 (P14
 外国製造業者認定申請の作成例 - C04( 医療機器外国製造業者認定申請 ) の事例 - 本作成例は FD 申請ソフトで作成した申請書の提出を前提に その入力方法や申請時に必要な書類などの説明をしています FD 申請へのご協力をお願いします PMDA へ提出する 医療機器医療機器の外国製造業者認定外国製造業者認定申請において 入力情報を最小限にとどめた 簡易入力による簡易入力による FD 申請の受付を平成
外国製造業者認定申請の作成例 - C04( 医療機器外国製造業者認定申請 ) の事例 - 本作成例は FD 申請ソフトで作成した申請書の提出を前提に その入力方法や申請時に必要な書類などの説明をしています FD 申請へのご協力をお願いします PMDA へ提出する 医療機器医療機器の外国製造業者認定外国製造業者認定申請において 入力情報を最小限にとどめた 簡易入力による簡易入力による FD 申請の受付を平成
治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会
 治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会 第 1 条 ( 目的 ) 1. 本手順書は 新光会治験審査委員会 ( 以下 委員会という ) において 医薬品及び医療機器 ( 以下 医薬品等という ) の治験の調査審議を実施するに当たり 薬事法 ( 昭和 35 年 8 月 10 日法律第 145 号 ) に基づく 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3
治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会 第 1 条 ( 目的 ) 1. 本手順書は 新光会治験審査委員会 ( 以下 委員会という ) において 医薬品及び医療機器 ( 以下 医薬品等という ) の治験の調査審議を実施するに当たり 薬事法 ( 昭和 35 年 8 月 10 日法律第 145 号 ) に基づく 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3
<4D F736F F D E63188C4816A8D4C93878CA78BC696B18AC7979D91CC90A78A6D94468C9F8DB88EC08E7B97768D6A816989FC90B38CE3816A2E646F63>
 広島県介護サービス事業者業務管理体制確認検査実施要綱 第 1 目的この要綱は, 広島県知事 ( 以下 知事 という ) が介護保険法 ( 平成 9 年法律第 123 号 以下 法 という ) 第 115 条の33, 第 115 条の34の規定及び介護サービス事業者業務管理体制確認検査指針 ( 平成 21 年 3 月 30 日付老発第 0330077 老健局長通知 以下 検査指針 という ) に基づき,
広島県介護サービス事業者業務管理体制確認検査実施要綱 第 1 目的この要綱は, 広島県知事 ( 以下 知事 という ) が介護保険法 ( 平成 9 年法律第 123 号 以下 法 という ) 第 115 条の33, 第 115 条の34の規定及び介護サービス事業者業務管理体制確認検査指針 ( 平成 21 年 3 月 30 日付老発第 0330077 老健局長通知 以下 検査指針 という ) に基づき,
薬食機発 0131 第 1 号平成 25 年 1 月 31 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課医療機器審査管理室長 薬事法に基づく登録認証機関の基準改正に伴う留意事項について ( その 2) 薬事法 ( 昭和 35 年法律第 145 号 以下 法 という )
 薬食機発 0131 第 1 号平成 25 年 1 月 31 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課医療機器審査管理室長 薬事法に基づく登録認証機関の基準改正に伴う留意事項について ( その 2) 薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 23 条の 2 第 1 項の登録認証機関の登録申請等の取扱いについては 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律等の施行に関する適合性認証機関の登録申請等について
薬食機発 0131 第 1 号平成 25 年 1 月 31 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課医療機器審査管理室長 薬事法に基づく登録認証機関の基準改正に伴う留意事項について ( その 2) 薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 23 条の 2 第 1 項の登録認証機関の登録申請等の取扱いについては 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律等の施行に関する適合性認証機関の登録申請等について
Welcome!
 申請電子データ提出を伴う承認申請における経験 - 薬事担当者の視点から 2018 年 10 月 16 日申請時電子データ提出にかかる実務担当者のためのワークショップ ヤンセンファーマ株式会社開発薬事部開発薬事グループ鈴木雄大 Jane Kielt, Mystic Seaport A retired art teacher and world traveler, Jane finds painting
申請電子データ提出を伴う承認申請における経験 - 薬事担当者の視点から 2018 年 10 月 16 日申請時電子データ提出にかかる実務担当者のためのワークショップ ヤンセンファーマ株式会社開発薬事部開発薬事グループ鈴木雄大 Jane Kielt, Mystic Seaport A retired art teacher and world traveler, Jane finds painting
国立がんセンター受託研究取扱規程
 平成 22 年 4 月 1 日規程第 31 号 国立研究開発法人国立がん研究センター受託研究取扱規程 第 1 版平成 22 年 4 月 1 日第 2 版平成 22 年 10 月 1 日第 3 版平成 23 年 4 月 1 日第 4 版平成 24 年 4 月 1 日第 5 版平成 24 年 7 月 1 日第 6 版平成 25 年 4 月 1 日第 7 版平成 27 年 4 月 1 日 ( 通則 ) 第
平成 22 年 4 月 1 日規程第 31 号 国立研究開発法人国立がん研究センター受託研究取扱規程 第 1 版平成 22 年 4 月 1 日第 2 版平成 22 年 10 月 1 日第 3 版平成 23 年 4 月 1 日第 4 版平成 24 年 4 月 1 日第 5 版平成 24 年 7 月 1 日第 6 版平成 25 年 4 月 1 日第 7 版平成 27 年 4 月 1 日 ( 通則 ) 第
法改正の目的 1 Ⅰ 医療機器等の特性を踏まえた規制の構築 1. 医療機器等の製造販売業及び製造業の章の新設 2. 体外診断用医薬品の製造販売業の新設 3. 医療機器等の製造業の登録制への移行 4. プログラムの位置付けの明確化 5. QMS 調査の見直し 6. 認証制度に関する見直し 7. 医療機
 医薬品医療機器等法の概要について ~ 医療機器等 ( ) を中心に ~ 東京都健康安全研究センター広域監視部医療機器監視課 ( ) 医療機器等 : 医療機器及び体外診断用医薬品 1 薬事法から医薬品医療機器等法へ 薬事法が 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 に改正されました 以下 医薬品医療機器等法 とします 2-1 - 法改正の目的 1 Ⅰ 医療機器等の特性を踏まえた規制の構築
医薬品医療機器等法の概要について ~ 医療機器等 ( ) を中心に ~ 東京都健康安全研究センター広域監視部医療機器監視課 ( ) 医療機器等 : 医療機器及び体外診断用医薬品 1 薬事法から医薬品医療機器等法へ 薬事法が 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 に改正されました 以下 医薬品医療機器等法 とします 2-1 - 法改正の目的 1 Ⅰ 医療機器等の特性を踏まえた規制の構築
3. 実施時期平成 29 年 4 月 3 日より本件改修後のQMS 調査申請書の作成及び機構受付が可能となります 4. その他 本改修により承認申請書とQMS 調査申請書の同時申請が可能となるのは 両申請書をDW APで作成した場合に限ります (FD 申請ソフトによる申請の場合は同時申請できません
 事務連絡平成 29 年 3 月 17 日 一般社団法人日本医療機器産業連合会御中 独立行政法人医薬品医療機器総合機構審査業務部 承認申請書及び QMS 調査申請書の同時申請にかかる DWAP の改修について 今般 医療機器 WEB 申請プラットフォーム ( 以下 DWAP という ) を活用した医療機器製造販売承認申請書又は外国製造医療機器製造販売承認申請書 ( 一部変更承認申請書を含む 以下 承認申請書
事務連絡平成 29 年 3 月 17 日 一般社団法人日本医療機器産業連合会御中 独立行政法人医薬品医療機器総合機構審査業務部 承認申請書及び QMS 調査申請書の同時申請にかかる DWAP の改修について 今般 医療機器 WEB 申請プラットフォーム ( 以下 DWAP という ) を活用した医療機器製造販売承認申請書又は外国製造医療機器製造販売承認申請書 ( 一部変更承認申請書を含む 以下 承認申請書
医療機器製造販売業者用 GVP チェックリスト 平成 28 年 3 月版 略語 項目 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年 8 月 10 日法律第 145 号 ) 規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則
 医療機器製造販売業者用 GVP チェックリスト 平成 28 年 3 月版 略語 項目 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年 8 月 10 日法律第 145 号 ) 規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年 2 月 1 日厚生第 1 号 ) : 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する
医療機器製造販売業者用 GVP チェックリスト 平成 28 年 3 月版 略語 項目 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年 8 月 10 日法律第 145 号 ) 規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年 2 月 1 日厚生第 1 号 ) : 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する
社会福祉法人○○会 個人情報保護規程
 社会福祉法人恩心会個人情報保護規程 ( 目的 ) 第 1 条本規程は 個人の尊厳を最大限に尊重するという基本理念のもと 社会福祉法人恩心会 ( 以下 本会 という ) が保有する個人情報の適正な取り扱いに関して必要な事項を定めることにより 個人情報の保護に関する法律 及びその他の関連法令等を遵守することを目的とする ( 利用目的の特定 ) 第 2 条本会が個人情報を取り扱うに当たっては その利用目的をできる限り特定する
社会福祉法人恩心会個人情報保護規程 ( 目的 ) 第 1 条本規程は 個人の尊厳を最大限に尊重するという基本理念のもと 社会福祉法人恩心会 ( 以下 本会 という ) が保有する個人情報の適正な取り扱いに関して必要な事項を定めることにより 個人情報の保護に関する法律 及びその他の関連法令等を遵守することを目的とする ( 利用目的の特定 ) 第 2 条本会が個人情報を取り扱うに当たっては その利用目的をできる限り特定する
都道府県知事各政令市長殿特別区長 薬食発第 号平成 16 年 9 月 22 日 厚生労働省医薬食品局長 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令及び薬事法施行規則の一部を改正する省令の施行について 薬事法及び採血及び供血あつせん業取締法の一部を改正
 都道府県知事各政令市長殿特別区長 薬食発第 0922005 号平成 16 年 9 月 22 日 厚生労働省医薬食品局長 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令及び薬事法施行規則の一部を改正する省令の施行について 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 薬事法等一部改正法 という ) については 平成
都道府県知事各政令市長殿特別区長 薬食発第 0922005 号平成 16 年 9 月 22 日 厚生労働省医薬食品局長 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令及び薬事法施行規則の一部を改正する省令の施行について 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 薬事法等一部改正法 という ) については 平成
<4D F736F F F696E74202D EA98CC8935F8C9F E9E935F816996F28DDC8E7489EF95F18D90816A292E B8CDD8AB B83685D>
 製造販売後安全管理業務における現状 ノバルティス社やファイザー社等で 安全管理情報 ( 副作用等 ) の処理や国報告に問題があったことが判明 安全管理情報の処理と副作用報告その 1 ( 安全管理情報の処理を中心に ) 当県でも GQP GVP フォローアップ調査で安全管理情報が適切に処理されているかを重点的に確認 副作用報告漏れや安全管理情報の処理が適切でない事例が見られた 調査での指摘事例と GVP
製造販売後安全管理業務における現状 ノバルティス社やファイザー社等で 安全管理情報 ( 副作用等 ) の処理や国報告に問題があったことが判明 安全管理情報の処理と副作用報告その 1 ( 安全管理情報の処理を中心に ) 当県でも GQP GVP フォローアップ調査で安全管理情報が適切に処理されているかを重点的に確認 副作用報告漏れや安全管理情報の処理が適切でない事例が見られた 調査での指摘事例と GVP
個人情報の保護に関する規程(案)
 公益財団法人いきいき埼玉個人情報保護規程 ( 趣旨 ) 第 1 条この規程は 埼玉県個人情報保護条例 ( 平成 16 年埼玉県条例第 65 号 ) 第 59 条の規定に基づき 公益財団法人いきいき埼玉 ( 以下 財団 という ) による個人情報の適正な取扱いを確保するために必要な事項を定めるものとする ( 定義 ) 第 2 条この規程において 個人情報 個人情報取扱事業者 個人データ 保有個人データ
公益財団法人いきいき埼玉個人情報保護規程 ( 趣旨 ) 第 1 条この規程は 埼玉県個人情報保護条例 ( 平成 16 年埼玉県条例第 65 号 ) 第 59 条の規定に基づき 公益財団法人いきいき埼玉 ( 以下 財団 という ) による個人情報の適正な取扱いを確保するために必要な事項を定めるものとする ( 定義 ) 第 2 条この規程において 個人情報 個人情報取扱事業者 個人データ 保有個人データ
改正後第 2 章通関業 第 1 節許可 新旧対照表 別紙 3 通関業法基本通達( 昭和 47 年 3 月 1 日蔵関第 105 号 ) ( 注 ) 下線を付した箇所が改正部分である 改正前第 2 章通関業第 1 節許可 3-8 削除 ( 譲渡 相続 合併又は分割の場合における通関業の許可の効果 )
 第 2 章通関業 第 1 節許可 第 2 章通関業第 1 節許可 3-8 削除 ( 譲渡 相続 合併又は分割の場合における通関業の許可の効果 ) 3-8 通関業について譲渡 相続 合併又は分割が行われた場合において 当該譲渡 相続 合併又は分割後 通関業を営もうとする者についての通関業の許可の要否の判定については 次による なお 当該譲渡等により通関業の許可が消滅した者については 法第 12 条第
第 2 章通関業 第 1 節許可 第 2 章通関業第 1 節許可 3-8 削除 ( 譲渡 相続 合併又は分割の場合における通関業の許可の効果 ) 3-8 通関業について譲渡 相続 合併又は分割が行われた場合において 当該譲渡 相続 合併又は分割後 通関業を営もうとする者についての通関業の許可の要否の判定については 次による なお 当該譲渡等により通関業の許可が消滅した者については 法第 12 条第
評価 条項号安全確保業務に係る組織及び職員 ( 第 4 条関係 ) ( 評価に際しての参考事項 ) 確認事項等 再生 第 1 種 第 2 種 第 3 種 4 1 製造販売業者は 以下に掲げる要件を満たす安全管理統括部門を置いているか A B C D A B C D 総括製造販売責任者の監
 評価 条項号安全確保業務に係る組織及び職員 ( 第 4 条関係 ) ( 評価に際しての参考事項 ) 確認事項等 再生 第 1 種 第 2 種 第 3 種 4 1 製造販売業者は 以下に掲げる要件を満たす安全管理統括部門を置いているか 4 1 1 総括製造販売責任者の監督下にあること 4 1 2 安全確保業務 ( 第 4 項の規定により安全管理責任者以外の者に行わせる業務を除く ) を適正かつ円滑に遂行しうる能力を有する人員を十分に有すること
評価 条項号安全確保業務に係る組織及び職員 ( 第 4 条関係 ) ( 評価に際しての参考事項 ) 確認事項等 再生 第 1 種 第 2 種 第 3 種 4 1 製造販売業者は 以下に掲げる要件を満たす安全管理統括部門を置いているか 4 1 1 総括製造販売責任者の監督下にあること 4 1 2 安全確保業務 ( 第 4 項の規定により安全管理責任者以外の者に行わせる業務を除く ) を適正かつ円滑に遂行しうる能力を有する人員を十分に有すること
薬生発 0926 第 5 号 平成 29 年 9 月 26 日 都道府県知事 各保健所設置市長殿 特別区長 厚生労働省医薬 生活衛生局長 ( 公印省略 ) コンタクトレンズの適正使用に関する情報提供等の徹底について コンタクトレンズ ( カラーコンタクトレンズを含む ) の販売に関しては これまで
 薬生発 0926 第 5 号 平成 29 年 9 月 26 日 都道府県知事 各保健所設置市長殿 特別区長 厚生労働省医薬 生活衛生局長 ( 公印省略 ) コンタクトレンズの適正使用に関する情報提供等の徹底について コンタクトレンズ ( カラーコンタクトレンズを含む ) の販売に関しては これまで コンタクトレンズの適正使用に関する情報提供等の徹底について ( 平成 24 年 7 月 18 日付け薬食発
薬生発 0926 第 5 号 平成 29 年 9 月 26 日 都道府県知事 各保健所設置市長殿 特別区長 厚生労働省医薬 生活衛生局長 ( 公印省略 ) コンタクトレンズの適正使用に関する情報提供等の徹底について コンタクトレンズ ( カラーコンタクトレンズを含む ) の販売に関しては これまで コンタクトレンズの適正使用に関する情報提供等の徹底について ( 平成 24 年 7 月 18 日付け薬食発
ネットワーク保守サービス 契約約款 2016 年 4 月 関西国際空港情報通信ネットワーク株式会社
 ネットワーク保守サービス 契約約款 2016 年 4 月 関西国際空港情報通信ネットワーク株式会社 目次 第 1 条 ( 目的 )... 1 第 2 条 ( 提供地域 )... 1 第 3 条 ( 申込みの方法 )... 1 第 4 条 ( 保守対象とする設備 )... 1 第 5 条 ( 保守サービスの内容 )... 1 第 6 条 ( 予備機器の取り扱い )... 2 第 7 条 ( 予備配線設備の取り扱い
ネットワーク保守サービス 契約約款 2016 年 4 月 関西国際空港情報通信ネットワーク株式会社 目次 第 1 条 ( 目的 )... 1 第 2 条 ( 提供地域 )... 1 第 3 条 ( 申込みの方法 )... 1 第 4 条 ( 保守対象とする設備 )... 1 第 5 条 ( 保守サービスの内容 )... 1 第 6 条 ( 予備機器の取り扱い )... 2 第 7 条 ( 予備配線設備の取り扱い
医師主導治験取扱要覧
 9. 安全性情報の取扱いに関する手順書 1. 目的及び適用範囲 本手順書は 安全性情報の取扱いに係る用語の定義を定め 当該治験に関与する者が 安全性情報を適 切に取扱うための手順その他必要な事項を定めるものである 2. 用語の定義等 2.1. 用語の定義 2.1.1. 治験責任医師等 本手順書は 自ら治験を実施する者を 治験責任医師 と記載し また 治験責任医師及び治験分担医師 を併せて 治験責任医師等
9. 安全性情報の取扱いに関する手順書 1. 目的及び適用範囲 本手順書は 安全性情報の取扱いに係る用語の定義を定め 当該治験に関与する者が 安全性情報を適 切に取扱うための手順その他必要な事項を定めるものである 2. 用語の定義等 2.1. 用語の定義 2.1.1. 治験責任医師等 本手順書は 自ら治験を実施する者を 治験責任医師 と記載し また 治験責任医師及び治験分担医師 を併せて 治験責任医師等
Microsoft Word - GVP省令施行通知(知事宛て)140812
 薬食発 0812 第 4 号 平成 26 年 8 月 12 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の 製造販売後安全管理の基準に関する省令等の施行について 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) については 平成 25 年 11 月 27 日に公布されたところです その後
薬食発 0812 第 4 号 平成 26 年 8 月 12 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の 製造販売後安全管理の基準に関する省令等の施行について 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) については 平成 25 年 11 月 27 日に公布されたところです その後
様式 2 特許庁長官殿 平成年月日 特定登録調査機関 印 特定登録調査機関代表者 印 先行技術調査業務規程届出書 工業所有権に関する手続等の特例に関する法律第 39 条の 7 に従い 先行技術調 査業務規程を届け出ます 添付書類 先行技術調査業務規程平成 年 月特定登録調査機関
 先行技術調査業務規程について 平成 27 年 3 月 特許庁 1. 特定登録調査機関は 業務を開始しようとする日の 2 週間前までに (1) 先行技 術調査業務規程届出書及び (2) 先行技術調査業務規程を届け出なければなりま せん 2. 先行技術調査業務規程届出書は 所定の様式に従い押印して下さい 3. 先行技術調査業務規程は 以下の全項目を記載したものを 先行技術調査業務規程 ( 例 ) を参考に作成して下さい
先行技術調査業務規程について 平成 27 年 3 月 特許庁 1. 特定登録調査機関は 業務を開始しようとする日の 2 週間前までに (1) 先行技 術調査業務規程届出書及び (2) 先行技術調査業務規程を届け出なければなりま せん 2. 先行技術調査業務規程届出書は 所定の様式に従い押印して下さい 3. 先行技術調査業務規程は 以下の全項目を記載したものを 先行技術調査業務規程 ( 例 ) を参考に作成して下さい
MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1
 MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1 MDSAP 報告書の受入れの概要 (1/2) 日本は 平成 27 年 6 月にMDSAPに参加する旨を発表 関係者との意見交換を行い MDSAP 報告書の受け入れについて 以下の通知を発出した 平成 28 年 6 月 22 日薬生監麻発 0622 第 3 号 薬生機審発 0622
MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1 MDSAP 報告書の受入れの概要 (1/2) 日本は 平成 27 年 6 月にMDSAPに参加する旨を発表 関係者との意見交換を行い MDSAP 報告書の受け入れについて 以下の通知を発出した 平成 28 年 6 月 22 日薬生監麻発 0622 第 3 号 薬生機審発 0622
別添 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について < 半年ごとの定期報告の受け付け> Q1 平成 26 年 6 月 30 日までの間は 治験依頼者 ( 自ら治験を実施する者を除く ) が提出する副作用等症例の定期報告は なお従前の例によることができる とあるが 平成 26 年
 事務連絡 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局審査管理課 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 第 273 条第 3 項に基づく治験副作用等定期報告については 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について ( 平成 24 年
事務連絡 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局審査管理課 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 第 273 条第 3 項に基づく治験副作用等定期報告については 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について ( 平成 24 年
H 平成 28 年青森県登録販売者試験について 1 概要出願者 612 名受験者 592 名合格者 277 名合格率 46.8%( 四捨五入 ) 2 合格基準総得点の7 割であって かつ 各項目の得点が4 割以上 3 試験成績 手引き第 1 章 手引き第 2 章 手引き第 3 章 手引
 H28.10.3 平成 28 年青森県登録販売者試験について 1 概要出願者 612 名受験者 592 名合格者 277 名合格率 46.8%( 四捨五入 ) 2 合格基準総得点の7 割であって かつ 各項目の得点が4 割以上 3 試験成績 手引き第 1 章 手引き第 2 章 手引き第 3 章 手引き第 4 章 手引き第 5 章 総得点 (40 点 ) (120 点 ) 最高得点 20 20 40
H28.10.3 平成 28 年青森県登録販売者試験について 1 概要出願者 612 名受験者 592 名合格者 277 名合格率 46.8%( 四捨五入 ) 2 合格基準総得点の7 割であって かつ 各項目の得点が4 割以上 3 試験成績 手引き第 1 章 手引き第 2 章 手引き第 3 章 手引き第 4 章 手引き第 5 章 総得点 (40 点 ) (120 点 ) 最高得点 20 20 40
Microsoft Word - 【発送版】製造所の登録通知
 薬食機参発 1003 第 1 号 平成 26 年 10 月 3 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いについて 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業は登録制に移行され
薬食機参発 1003 第 1 号 平成 26 年 10 月 3 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いについて 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業は登録制に移行され
薬局を利用するために必要な情報の掲示 ( 薬事法第 9 条の 4) 次の事項について 掲示板等により 薬局内に掲示 しなければなりません また 第 3 については 特定販売を行うことについての広告をする場合 ホームページ等に表示しなければなりません < 具体例 > 第 1 薬局の管理及び運営に関する
 薬局を利用するために必要な情報の掲示 ( 薬事法第 9 条の 4) 次の事項について 掲示板等により 薬局内に掲示 しなければなりません また 第 3 については 特定販売を行うことについての広告をする場合 ホームページ等に表示しなければなりません < 具体例 > 第 1 薬局の管理及び運営に関する事項 1 許可の区分の別薬局 開設者氏名 株式会社 開設者の氏名又は名称その 薬局の名称 薬局 店 2
薬局を利用するために必要な情報の掲示 ( 薬事法第 9 条の 4) 次の事項について 掲示板等により 薬局内に掲示 しなければなりません また 第 3 については 特定販売を行うことについての広告をする場合 ホームページ等に表示しなければなりません < 具体例 > 第 1 薬局の管理及び運営に関する事項 1 許可の区分の別薬局 開設者氏名 株式会社 開設者の氏名又は名称その 薬局の名称 薬局 店 2
寝屋川市母子家庭等自立支援教育訓練給付金事業実施要綱 ( 目的 ) 第 1 条この要綱は 雇用の安定及び就職の促進を図るために必要な教育訓練に係る講座 ( 以下 講座 という ) を受講する母子家庭の母 又は父子家庭の父に対し 母子及び父子並びに寡婦福祉法 ( 昭和 39 年法律第 129 号 以下
 寝屋川市母子家庭等自立支援教育訓練給付金事業実施要綱 ( 目的 ) 第 1 条この要綱は 雇用の安定及び就職の促進を図るために必要な教育訓練に係る講座 ( 以下 講座 という ) を受講する母子家庭の母 又は父子家庭の父に対し 母子及び父子並びに寡婦福祉法 ( 昭和 39 年法律第 129 号 以下 法 という ) 第 31 条第 1 号 ( 同法第 31 条の 10 において準用する場合を含む )
寝屋川市母子家庭等自立支援教育訓練給付金事業実施要綱 ( 目的 ) 第 1 条この要綱は 雇用の安定及び就職の促進を図るために必要な教育訓練に係る講座 ( 以下 講座 という ) を受講する母子家庭の母 又は父子家庭の父に対し 母子及び父子並びに寡婦福祉法 ( 昭和 39 年法律第 129 号 以下 法 という ) 第 31 条第 1 号 ( 同法第 31 条の 10 において準用する場合を含む )
2 調査の実施 回収ア調査の実施方法受託者はセキュリティを確保し ストレスチェックの結果は実施者以外閲覧不可にして インターネットを活用して実施することとする 機構は 受託者に対し職員番号 氏名 所属部署 性別 生年月日 個人メールアドレス等のストレスチェックの実施に必要な情報を提供する 受託者はこ
 仕様書 1. 契約件名 平成 30 年度ストレスチェック業務の委託 2. 委託業務の内容 (1) 業務の内容独立行政法人医薬品医療機器総合機構 ( 以下 機構 という ) に勤務する全ての者に対して 業務受託者 ( 以下 受託者 という ) は労働安全衛生法に基づくストレスチェックについて 厚生労働省推奨の職業性ストレス簡易調査票 (57 項目調査票 ) を利用し 調査 分析を実施する 委託内容は以下のとおりとする
仕様書 1. 契約件名 平成 30 年度ストレスチェック業務の委託 2. 委託業務の内容 (1) 業務の内容独立行政法人医薬品医療機器総合機構 ( 以下 機構 という ) に勤務する全ての者に対して 業務受託者 ( 以下 受託者 という ) は労働安全衛生法に基づくストレスチェックについて 厚生労働省推奨の職業性ストレス簡易調査票 (57 項目調査票 ) を利用し 調査 分析を実施する 委託内容は以下のとおりとする
医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令に資するために 医療関係者を訪問すること等により安全管理情報を収集し 提供することを主な業務として行う者をいう 7 この省令で 第一種製造販売業者 とは 法第四十九条第一項に規定する厚生労働大臣の指定する医薬
 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令 第 1 種製造販売業 第 2 種製造販売業 第 3 種製造販売業 施行通知薬食発 0 8 1 2 第 4 号平成 26 年 8 月 12 日 第一章総則 ( 趣旨 ) 第 1 改正の概要 1.GVP 省令について 第一条この省令は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 以下 法
医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令 第 1 種製造販売業 第 2 種製造販売業 第 3 種製造販売業 施行通知薬食発 0 8 1 2 第 4 号平成 26 年 8 月 12 日 第一章総則 ( 趣旨 ) 第 1 改正の概要 1.GVP 省令について 第一条この省令は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 以下 法
IRB の 4 週間前までに事前確認に必要な資料をご提出ください 必要時にはヒアリングも実施いたします IRB 審議用確認資料 電子 ( メール ) にてご提出ください 製造販売後調査申請書 ( 様式 1) 1 部 審査用資料 1 薬品概要書 ( 添付文書でも可 ) 1 部 2 調査実施計画書 (
 国立大学法人信州大学医学部附属病院製造販売後調査実施に係わる手続き要領 2018 年 4 月 はじめにご確認ください 本要領の対象となる調査は 再審査 再評価のために GPSP で規定された日常診療下で実施される調査です 製薬会社が独自で行う調査 (= 観察研究 ) は対象外です 独自に実施する調査は 臨床研究として信州大学医学部医倫理委員会で審議となります 各種手続きについて担当医師又は信州大学医学部庶務係
国立大学法人信州大学医学部附属病院製造販売後調査実施に係わる手続き要領 2018 年 4 月 はじめにご確認ください 本要領の対象となる調査は 再審査 再評価のために GPSP で規定された日常診療下で実施される調査です 製薬会社が独自で行う調査 (= 観察研究 ) は対象外です 独自に実施する調査は 臨床研究として信州大学医学部医倫理委員会で審議となります 各種手続きについて担当医師又は信州大学医学部庶務係
Microsoft Word - 奈良県GQP-GVPガイドライン doc
 Ⅴ. 製造業者等との取決め - 67 - 1. はじめに製造業者等との取決めは GQP 省令 ( 平成 16 年 9 月 22 日厚生労働省令第 136 号 ) の第 7 条に基づき 製造業者等における医薬品の製造管理及び品質管理の適正かつ円滑な実施を確保するため 製造販売業者が製造業者等に製造委託する製品に関し 必要な事項を取り決めるものである 2. 取決め対象取決めを行う 製造業者等 とは 製造販売承認書の製造方法欄に記載された以下の者である
Ⅴ. 製造業者等との取決め - 67 - 1. はじめに製造業者等との取決めは GQP 省令 ( 平成 16 年 9 月 22 日厚生労働省令第 136 号 ) の第 7 条に基づき 製造業者等における医薬品の製造管理及び品質管理の適正かつ円滑な実施を確保するため 製造販売業者が製造業者等に製造委託する製品に関し 必要な事項を取り決めるものである 2. 取決め対象取決めを行う 製造業者等 とは 製造販売承認書の製造方法欄に記載された以下の者である
( 別紙 ) 承認申請時の電子データ提出に関する基本的考え方について ( 平成 26 年 6 月 20 日付け薬食審査発 0620 第 6 号厚生労働省医薬食品局審査管理課長通知 ) 新旧対照表 ( 別添 ) 改正後 承認申請時の電子データ提出に関する基本的考え方 1. 承認申請時に電子データ提出を
 ( 別紙 ) 承認申請時の電子データ提出に関する基本的考え方について ( 平成 26 年 6 月 20 日付け薬食審査発 0620 第 6 号厚生労働省医薬食品局審査管理課長通知 ) 新旧対照表 ( 別添 ) 改正後 承認申請時の電子データ提出に関する基本的考え方 1. 承認申請時に電子データ提出を求める背景 2. 電子データの提出対象となる品目と資料の範囲 (1) 対象となる品目 原則として 医薬品の承認申請について
( 別紙 ) 承認申請時の電子データ提出に関する基本的考え方について ( 平成 26 年 6 月 20 日付け薬食審査発 0620 第 6 号厚生労働省医薬食品局審査管理課長通知 ) 新旧対照表 ( 別添 ) 改正後 承認申請時の電子データ提出に関する基本的考え方 1. 承認申請時に電子データ提出を求める背景 2. 電子データの提出対象となる品目と資料の範囲 (1) 対象となる品目 原則として 医薬品の承認申請について
Ⅰ 概要について 一次下請契約者を社会保険等加入業者に限定します 平成 29 年 4 月 1 日以降に契約締結した工事において 受注者は 原則として社会保険等未加入業者を下請契約 ( 受注者が直接契約締結するものに限る 以下 一次下請契約 という ) の相手方としないこととします 追加 建設工事契約
 鶴岡市発注工事における社会保険等未加入対策について ( 概要 Q&A フロー ) 平成 29 年 1 月 鶴岡市 - 0 - Ⅰ 概要について 一次下請契約者を社会保険等加入業者に限定します 平成 29 年 4 月 1 日以降に契約締結した工事において 受注者は 原則として社会保険等未加入業者を下請契約 ( 受注者が直接契約締結するものに限る 以下 一次下請契約 という ) の相手方としないこととします
鶴岡市発注工事における社会保険等未加入対策について ( 概要 Q&A フロー ) 平成 29 年 1 月 鶴岡市 - 0 - Ⅰ 概要について 一次下請契約者を社会保険等加入業者に限定します 平成 29 年 4 月 1 日以降に契約締結した工事において 受注者は 原則として社会保険等未加入業者を下請契約 ( 受注者が直接契約締結するものに限る 以下 一次下請契約 という ) の相手方としないこととします
確定版【都道府県宛】
 薬生発 0329 第 10 号 平成 29 年 3 月 29 日 各都道府県知事 殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律関係手数料令 の一部改正について この度 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律関係手数料令の一部を改正する政令 ( 平成 29 年政令第 62 号 以下 改正政令 という ) が平成
薬生発 0329 第 10 号 平成 29 年 3 月 29 日 各都道府県知事 殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律関係手数料令 の一部改正について この度 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律関係手数料令の一部を改正する政令 ( 平成 29 年政令第 62 号 以下 改正政令 という ) が平成
大阪府立成人病センター治験標準業務手順書(平成23年12月21日改正案)
 大阪国際がんセンター治験標準業務手順書 制定平成 10 年 4 月 1 日改訂平成 21 年 3 月 1 日改訂平成 21 年 5 月 20 日改訂平成 21 年 8 月 19 日改訂平成 22 年 2 月 15 日改訂平成 22 年 5 月 17 日改訂平成 24 年 2 月 1 日改訂平成 24 年 5 月 1 日改訂平成 25 年 4 月 1 日改訂平成 25 年 12 月 1 日改訂平成 27
大阪国際がんセンター治験標準業務手順書 制定平成 10 年 4 月 1 日改訂平成 21 年 3 月 1 日改訂平成 21 年 5 月 20 日改訂平成 21 年 8 月 19 日改訂平成 22 年 2 月 15 日改訂平成 22 年 5 月 17 日改訂平成 24 年 2 月 1 日改訂平成 24 年 5 月 1 日改訂平成 25 年 4 月 1 日改訂平成 25 年 12 月 1 日改訂平成 27
Taro-化学物質の審査及び製造等の規制に関する法律の一部を改正する法律案 新旧対照条文
 化学物質の審査及び製造等の規制に関する法律の一部を改正する法律案新旧対照条文 化学物質の審査及び製造等の規制に関する法律(昭和四十八年法律第百十七号) 1 - 1 - 化学物質の審査及び製造等の規制に関する法律(昭和四十八年法律第百十七号)(傍線部分は改正部分)改正案現行目次目次第一章 第二章(略)第一章 第二章(略)第三章一般化学物質等に関する措置(第八条 第八条の二)第三章一般化学物質等に関する届出(第八条)第四章~第八章(略)第四章~第八章(略)附則附則(定義等)(定義等)第二条(略)第二条(略)2~5(略)2~5(略)6この法律において
化学物質の審査及び製造等の規制に関する法律の一部を改正する法律案新旧対照条文 化学物質の審査及び製造等の規制に関する法律(昭和四十八年法律第百十七号) 1 - 1 - 化学物質の審査及び製造等の規制に関する法律(昭和四十八年法律第百十七号)(傍線部分は改正部分)改正案現行目次目次第一章 第二章(略)第一章 第二章(略)第三章一般化学物質等に関する措置(第八条 第八条の二)第三章一般化学物質等に関する届出(第八条)第四章~第八章(略)第四章~第八章(略)附則附則(定義等)(定義等)第二条(略)第二条(略)2~5(略)2~5(略)6この法律において
Microsoft Word - (発出)マル製通知案
 薬食機参発 1119 第 7 号 薬食監麻発 1119 第 12 号 平成 26 年 11 月 19 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 厚生労働省医薬食品局監視指導 麻薬対策課長 ( 公印省略 ) 医療機器及び体外診断用医薬品の製造所の変更又は追加に係る手続 の迅速化について 医療機器及び体外診断用医薬品の製造所の変更に係る手続きの迅速化については
薬食機参発 1119 第 7 号 薬食監麻発 1119 第 12 号 平成 26 年 11 月 19 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 厚生労働省医薬食品局監視指導 麻薬対策課長 ( 公印省略 ) 医療機器及び体外診断用医薬品の製造所の変更又は追加に係る手続 の迅速化について 医療機器及び体外診断用医薬品の製造所の変更に係る手続きの迅速化については
中央教育審議会(第119回)配付資料
 第 18 回 (10 月 15 日開催 ) 学校における働き方改革特別部会資料 一年単位の変形労働時間制について ( 労働基準法第 32 条の 4) 資料 2-3 休日の増加による労働者のゆとりの創造 時間外 休日労働の減少による総労働時間の短縮を実現するため 1 箇月を超え1 年以内の期間を平均して1 週間当たりの労働時間が40 時間を超えないことを条件として 業務の繁閑に応じ労働時間を配分することを認める制度
第 18 回 (10 月 15 日開催 ) 学校における働き方改革特別部会資料 一年単位の変形労働時間制について ( 労働基準法第 32 条の 4) 資料 2-3 休日の増加による労働者のゆとりの創造 時間外 休日労働の減少による総労働時間の短縮を実現するため 1 箇月を超え1 年以内の期間を平均して1 週間当たりの労働時間が40 時間を超えないことを条件として 業務の繁閑に応じ労働時間を配分することを認める制度
目次 1. はじめに 2. 実際の応募手続き 3. 応募手続き完了の確認 2
 革新的バイオ医薬品創出基盤技術開発事業 H27 年度公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 1 目次 1. はじめに 2. 実際の応募手続き 3. 応募手続き完了の確認 2 1-a. はじめに 1 注意事項 1. 平成 27 年度の革新的バイオ医薬品創出基盤技術開発事業への応募は 必ず e-rad を利用して下さい 2. e-rad の使用に当たっては 研究機関および研究者の事前登録が必要です
革新的バイオ医薬品創出基盤技術開発事業 H27 年度公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 1 目次 1. はじめに 2. 実際の応募手続き 3. 応募手続き完了の確認 2 1-a. はじめに 1 注意事項 1. 平成 27 年度の革新的バイオ医薬品創出基盤技術開発事業への応募は 必ず e-rad を利用して下さい 2. e-rad の使用に当たっては 研究機関および研究者の事前登録が必要です
別添 2 租税特別措置法施行令第 39 条の25 第 1 項第 1 号に規定する厚生労働大臣が財務大臣と協議して定める基準を満たすものである旨の証明願平成年月日厚生労働大臣殿 租税特別措置法施行令第 39 条の25 第 1 項第 1 号に規定する厚生労働大臣が財務大臣と協議して定める下記の基準を満た
 別添 2 租税特別措置法施行令第 39 条の25 第 1 項第 1 号に規定する厚生労働大臣が財務大臣と協議して定める基準を満たすものである旨の証明願平成年月日厚生労働大臣殿 租税特別措置法施行令第 39 条の25 第 1 項第 1 号に規定する厚生労働大臣が財務大臣と協議して定める下記の基準を満たすものであることについて証明願います 記 1 社会保険診療 ( 租税特別措置法 ( 昭和 32 年法律第
別添 2 租税特別措置法施行令第 39 条の25 第 1 項第 1 号に規定する厚生労働大臣が財務大臣と協議して定める基準を満たすものである旨の証明願平成年月日厚生労働大臣殿 租税特別措置法施行令第 39 条の25 第 1 項第 1 号に規定する厚生労働大臣が財務大臣と協議して定める下記の基準を満たすものであることについて証明願います 記 1 社会保険診療 ( 租税特別措置法 ( 昭和 32 年法律第
