<4D F736F F F696E74202D2090BB91A294CC94848CE392B28DB CC905C90BF82C982C282A282C45F F566F6C2E33>
|
|
|
- ゆりな なかきむら
- 5 years ago
- Views:
Transcription
1 この冊 における製造販売後調査等とは 使 成績調査 特定使 成績調査 副作 感染症報告 です 1/Mar/2016 Vol.3
2 1 ホームページのご案内 1 当院ホームページに手続き内容や 必要書類等を UP しています 2 依頼者のページ 3 製造販売後調査について 1 治験のお知らせ
3 2 ホームページのご案内 2 当院ホームページに手続き内容や 必要書類等を UP しています 申請の内容に応じて こちらから書類をダウンロードしてください 受託研究審査委員会の開催 ( 年間予定表も含む ) 資料締切 はこちらに掲載しています
4 3 申請から契約までのスケジュール例 SUN MON TUE WED THU FRI SAT 3/27 3/28 3/29 3/30 3/ /1 5/2 5/3 5/4 5/5 5/6 5/7 受託 4 April 2016 申請資料締切 1 週間 10 前までにヒアリングを実施 (15 分程度 ) 申請資料締切 5/2 以降に契約書 請求書をお渡しします 基本的には末 契約ですが 早めの契約をご希望の場合はご相談ください 最短で委員会の翌 契約も可能です 契約締結 請求書の 払期限 : 原則 契約締結後 2 ヶ 以内 ( 例 :4 29 締結の場合 6 末 が 払期限 ) 受託 : 受託研究審査委員会 ( 製造販売後調査等を審議する委員会 ) 原則 毎 第 2 曜 開催 ( 薬剤管理委員会と同時開催 ) 審議内容治験 製造販売後臨床試験以外の受託研究の実施 継続の適否 使 成績調査 特定使 成績調査 副作 感染症報告等 委員 13 名 ( 兼任 員あり現在 11 名 ) 年間開催予定をホームページに掲載しています ヒアリング : 調査の対象の医薬品 医療機器 調査の概要について 15 分程度のヒアリングをお願いします 説明資料はパワーポイント 審議資料 ( 提出資料 ) のどちらでも結構です
5 4 新規申請について ( 使用成績調査 ) 申請から契約まで 書式 3 一般名を記載 依頼者印は特に必要ではありません 書式 3 調査様式 10-1 はメールでの提出も可能です 1 調査責任医師との合意 契約症例数, 開始時期など プロトコール番号がない場合は記載不要 2ヒアリング 3 申請書類の提出 前ページのスケジュール例参照 書式 3 治験依頼書 1 部 調査様式 10-1 受託研究費積算書 1 部 ( 使用成績調査に係る経費算出基準 ) 書式 19-2 契約書 2 通 ( 押印済のもの ) 新規申請用添付書類各 15 部実施要綱調査票の見本 (EDCの場合入力見本でも可) 登録票の見本, 添付文書, その他 ( 必要なもの ) 4 委員会承認後 結果通知書 契約書等を送付 調査開始 使用成績調査の場合 : 1 調査票あたり作成経費 20,000 円 + 事務費 + 管理費 + 消費税 8% 合計 30,888 円になります 調査様式 に契約症例数 20,000 円を入力すると 自動的に計算されます
6 5 新規申請について ( 特定使用成績調査 ) 申請から契約まで 書式 3 一般名を記載 依頼者印は特に必要ではありません 書式 3 調査様式 10-2 はメールでの提出も可能です 1 調査責任医師との合意 契約症例数, 開始時期など プロトコール番号がない場合は記載不要 2 ヒアリング 前ページのスケジュール例参照 調査様式 申請書類の提出 書式 3 治験依頼書 1 部 調査様式 10-2 受託研究費積算書 1 部 ( 特定使用成績調査に係る経費算出基準 ) 書式 19-2 契約書 2 通 ( 押印済のもの ) 新規申請用添付書類各 15 部実施要綱調査票の見本 (EDCの場合入力見本でも可) 登録票の見本, 添付文書, その他 ( 必要なもの ) 4 委員会承認後 結果通知書 契約書等を送付 調査開始 特定使用成績調査の場合 : 1 調査票あたり作成経費 30,000 円 + 事務費 + 管理費 + 消費税 8% 合計 46,332 円になります 3 に契約症例数 30,000 円を入力すると 自動的に計算されます
7 6 新規申請について ( 副作用 感染症報告 ) 申請から契約まで 書式 3 調査様式 10-3 はメールでの提出も可能です 1 調査責任医師との合意 2 報告書の記入 3 報告書の回収 副作用 感染症報告の申請に関しては 報告が完了してからの後払いとなります 4 申請書類の提出 書式 3 治験依頼書 1 部 調査様式 10-3 受託研究費積算書 1 部 ( 副作用 感染症報告に係る経費算出基準 ) 書式 19-2 契約書 2 通 ( 押印済のもの ) 添付文書 15 部 副作用 感染症報告書( 記入済 ) のコピー 1 部 5 委員会承認後 結果通知書 契約書等を送付 書式 3 副作用 感染症報告の場合 : 1 調査票あたり作成経費 20,000 円 + 事務費 + 管理費 + 消費税 8% 合計 30,888 円になります 一般名を記載 調査様式 10-3 依頼者印は特に必要ではありません 記載不要 3 に契約症例数 20,000 円を入力すると 自動的に計算されます
8 7 主な変更申請について 申請に必要な書類 こちらについては 迅速審査の対応も可能ですので ご相談ください 書式 10 調査様式 はメールでの提出も可能です 書式 10 一般名を記載 依頼者印は特に必要ではありません 1 契約症例数の追加 プロトコール番号がない場合は記載不要 書式 10 治験に関する変更申請書 1 部 調査様式 10-1or2 受託研究費積算書 1 部 書式 19-5 覚書 2 通 ( 押印済のもの ) 調査様式 10-1or 契約期間の延長 書式 10 治験に関する変更申請書 1 部 書式 19-5 覚書 2 通 ( 押印済のもの ) 期間延長の場合は特に費用追加はありません 3 調査分担医師の追加 書式 10 治験に関する変更申請書 1 部 書式 19-5 覚書 2 通 ( 押印済のもの ) 4 契約締結者 ( 代表者 ) 移転等に伴う住所の変更 特別な事情がない場合はレターで読み替えます 3 には 追加する症例数分の報告書作成経費を入力してください 3 に契約追加症例数 30,000or20,000 円を入力すると 自動的に計算されます
9 8 実施状況報告書 終了報告書について 実施状況報告書 1 年に 1 回 3 月の受託研究審査委員会へ提出をお願い致します メールでの提出も可能です 終了報告書 調査終了後 終了報告書の提出をお願い致します メールでの提出も可能です 書式 11 書式 17 プロトコール番号がない場合は記載不要一般名を記載 一般名を記載 プロトコール番号がない場合は記載不要 契約症例数に対する調査票の回収状況などご報告ください 有効性 安全性については 特記すべき事項がある場合 ご報告ください
10 9 契約書 覚書について 書式が新しくなりました! 契約書の本文を変更する場合は 覚書でご対応ください 書式 19-2 日付欄はこちらで記入しますので 記載は不要です 書式 19-5 責任医師署名 押印欄がなくなりました 責任医師署名 押印欄がなくなりました 契約書作成時のお願い サイズ :A4 印刷 : 片面 両面可 契約書が複数枚の場合は袋とじ 表表紙 裏表紙に割印 契約合計金額ではなく 1 症例あたりの単価 ( 税抜き ) の記載に変わりました 最終頁の ( 別表 ) については 物品等の提供がなければ記載は不要です 手続きの簡素化により 責任医師署名 押印欄がなくなりましたが 申請前に必ず責任医師に内容を確認していただきますようお願い 致します
11 10 よくあるご質問 1 Q.1 使 成績調査などの製造販売後調査の契約 を出来 払いにしてほしい A.1 製造販売後調査については 出来 払いの治験のように進捗を把握できないため 進捗管理を依頼者さまに依存する状況です 契約症例数 1 例でスタートし 症例追加するなど 経費の負担を軽減するよう対応致しますので ご相談ください ただし 副作 感染症報告については 調査票の作成終了後の事後申請 後払いとなります Q.2 調査票が分冊の場合 全額前納となるか A.2 転院などにより 調査続 が不可能となった場合 返 することができません 1 症例 1 分冊から契約をし 次の分冊に った時点で 追加の契約を うなどの 続きが可能ですので ご相談ください
12 11 よくあるご質問 2 Q.3 申請書類の押印は不要か A.3 各種申請書類については 依頼者 調査責任医師の押印を不要とし 続きの簡素化を進めています 必ず申請前に調査責任医師に申請内容を確認し 了承を得た上で 申請 続きを うようにしてください Q.4 新規申請の添付資料 15 部について ファイリングの 法など指定はあるか A.4 特に指定はありませんので 調査実施要綱等の添付資料を 各 15 部ずつご提出ください Q.5 同じ調査を いろいろな診療科で実施する際の申請や契約について A.5 申し訳ございませんが 研究費の処理の関係で 診療科ごとの申請 契約をお願いしております お問い合わせ先 東京医療センター臨床研究 治験推進室 TEL(03) nakagawayumi@kankakuki.go.jp
IRB の 4 週間前までに事前確認に必要な資料をご提出ください 必要時にはヒアリングも実施いたします IRB 審議用確認資料 電子 ( メール ) にてご提出ください 製造販売後調査申請書 ( 様式 1) 1 部 審査用資料 1 薬品概要書 ( 添付文書でも可 ) 1 部 2 調査実施計画書 (
 国立大学法人信州大学医学部附属病院製造販売後調査実施に係わる手続き要領 2018 年 4 月 はじめにご確認ください 本要領の対象となる調査は 再審査 再評価のために GPSP で規定された日常診療下で実施される調査です 製薬会社が独自で行う調査 (= 観察研究 ) は対象外です 独自に実施する調査は 臨床研究として信州大学医学部医倫理委員会で審議となります 各種手続きについて担当医師又は信州大学医学部庶務係
国立大学法人信州大学医学部附属病院製造販売後調査実施に係わる手続き要領 2018 年 4 月 はじめにご確認ください 本要領の対象となる調査は 再審査 再評価のために GPSP で規定された日常診療下で実施される調査です 製薬会社が独自で行う調査 (= 観察研究 ) は対象外です 独自に実施する調査は 臨床研究として信州大学医学部医倫理委員会で審議となります 各種手続きについて担当医師又は信州大学医学部庶務係
<4D F736F F D E34208EA18CB18EE891B182AB977697CC C8E8DB782B591D682A688CB978A>
 Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
臨床試験(治験)実施の手続き
 製造販売後調査実施の手続き はじめに 本書は 昭和大学藤が丘病院における製造販売後調査実施の手続き方法等について記載したものです 本書内のは当院が提供する書類を示し は審査等に必要な書類を示しております 調査内容により提出書類 資料に変更が生じる場合があります 詳細は支援室にご確認ください 申請する書類および資料は 事前に E-mail に添付して支援室にお送りください 内容の確認をし ご連絡させて頂きます
製造販売後調査実施の手続き はじめに 本書は 昭和大学藤が丘病院における製造販売後調査実施の手続き方法等について記載したものです 本書内のは当院が提供する書類を示し は審査等に必要な書類を示しております 調査内容により提出書類 資料に変更が生じる場合があります 詳細は支援室にご確認ください 申請する書類および資料は 事前に E-mail に添付して支援室にお送りください 内容の確認をし ご連絡させて頂きます
製造販売後調査事務手続き等 について
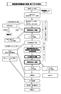 製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
M. 旅行計画書 A. 1 申請の際には当院の標準業務手順書 契約書 ( 案 ) 覚書 ( 案 ) マニュアル等を熟読の上 目標症例数を責任医師と依頼者で十分協議 し 実施可能な症例数を申し込んでくだ 1 申請の際には当院の標準業務手順書 契約書 ( 案 ) マニュアル等を熟 読の上
 広島大学病院製造販売後医薬品調査マニュアル変更対比表 変更前 変更後 頁 項目等 Ver.6.20 2015 年 1 月 30 日 Ver.6.30 2017 年 2 月 27 日 (2015 年 2 月 1 日より適用 ) (2017 年 3 月 1 日より適用 ) 表紙 (ver.6.20) (ver.6.30) ver.6.30 2017 年 2 月 27 日 (2017 年 3 月 1 日より適用
広島大学病院製造販売後医薬品調査マニュアル変更対比表 変更前 変更後 頁 項目等 Ver.6.20 2015 年 1 月 30 日 Ver.6.30 2017 年 2 月 27 日 (2015 年 2 月 1 日より適用 ) (2017 年 3 月 1 日より適用 ) 表紙 (ver.6.20) (ver.6.30) ver.6.30 2017 年 2 月 27 日 (2017 年 3 月 1 日より適用
????? 1???
 SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT SUN MON
SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT SUN MON
Microsoft PowerPoint - 運用 [互換モード]
![Microsoft PowerPoint - 運用 [互換モード] Microsoft PowerPoint - 運用 [互換モード]](/thumbs/91/105850431.jpg) 押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
<4D F736F F D2090BB91A294CC94848CE392B28DB8905C90BF8E9E92F18F6F8F9197DE82A882E682D1928D88D38E968D E48DEC90AC816A
 申請時提出書類 ( 新規 ) 医薬品等の製造販売後調査実施依頼申請書 様式第 1 ( 以下 依頼書 ) 医薬品等の製造販売後調査実施申請書 様式第 2 ( 以下 申請書 ) 医薬品等の製造販売後調査実施に関する通知書 ( 病院用 依頼者用 ) 様式第 3 様式第 4 ( 以下 通知書 ) 医薬品等の製造販売後調査実施契約書 ( 病院用 依頼者用 ) 様式第 5 様式第 5の2 ( 以下 契約書 )
申請時提出書類 ( 新規 ) 医薬品等の製造販売後調査実施依頼申請書 様式第 1 ( 以下 依頼書 ) 医薬品等の製造販売後調査実施申請書 様式第 2 ( 以下 申請書 ) 医薬品等の製造販売後調査実施に関する通知書 ( 病院用 依頼者用 ) 様式第 3 様式第 4 ( 以下 通知書 ) 医薬品等の製造販売後調査実施契約書 ( 病院用 依頼者用 ) 様式第 5 様式第 5の2 ( 以下 契約書 )
臨床試験(治験)の手続きについて
 臨床試験 ( 治験 製造販売後臨床試験 ) の手続きについて 本書は 昭和大学横浜市北部病院における臨床試験 ( 治験 製造販売後臨床試験 ) の手続き等に関して記したものです 始める前にご一読下さい なお 下記手続きにおいて必要書類を提出される場合は臨床試験支援室 ( 連絡先 :10 ページ参照 ) までご連絡下さい - 試験依頼前 - 関係書類の入手 当院の臨床試験 ( 治験 製造販売後臨床試験
臨床試験 ( 治験 製造販売後臨床試験 ) の手続きについて 本書は 昭和大学横浜市北部病院における臨床試験 ( 治験 製造販売後臨床試験 ) の手続き等に関して記したものです 始める前にご一読下さい なお 下記手続きにおいて必要書類を提出される場合は臨床試験支援室 ( 連絡先 :10 ページ参照 ) までご連絡下さい - 試験依頼前 - 関係書類の入手 当院の臨床試験 ( 治験 製造販売後臨床試験
国立病院機構大阪医療センター受託研究取扱細則
 国立病院機構大阪医療センター 受託研究取扱細則 ( 主旨 ) 第 1 条国立病院機構大阪医療センターにおける受託研究の取扱いに関しては 国立病院機構大阪医療センター受託研究取扱規程 ( 以下 規程 という ) 及び他に定めるもののほか 規程第 1 条第 2 項に規定するこの細則の定めるところによる ( 総則 ) 第 2 条研究責任者は 原則として医長職相当以上とする ただし 副作用報告及び感染症報告を受託研究として実施する場合
国立病院機構大阪医療センター 受託研究取扱細則 ( 主旨 ) 第 1 条国立病院機構大阪医療センターにおける受託研究の取扱いに関しては 国立病院機構大阪医療センター受託研究取扱規程 ( 以下 規程 という ) 及び他に定めるもののほか 規程第 1 条第 2 項に規定するこの細則の定めるところによる ( 総則 ) 第 2 条研究責任者は 原則として医長職相当以上とする ただし 副作用報告及び感染症報告を受託研究として実施する場合
 2016 5.14 6.3 6.22 7.16 )22 5.14()22() ) 6.3()5() W)26 )18 6.22(W)26() 26( 7.16()18(M) 18(M 2016 V2 0 www.imageforumfestival.com 0 V7 V9 V2 0 11:00 13:45 16:30 19:00 5/14 [sat] 5/15 [sun ] 5/16 [mon
2016 5.14 6.3 6.22 7.16 )22 5.14()22() ) 6.3()5() W)26 )18 6.22(W)26() 26( 7.16()18(M) 18(M 2016 V2 0 www.imageforumfestival.com 0 V7 V9 V2 0 11:00 13:45 16:30 19:00 5/14 [sat] 5/15 [sun ] 5/16 [mon
untitled
 2013. Apr.4 Mon Tue Wed Thu Fri Sat Sun 4/1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 5/1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 TEL WEB 1 2 3 4 1 2 3! ENTER 2013. 329 2013.
2013. Apr.4 Mon Tue Wed Thu Fri Sat Sun 4/1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 5/1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 TEL WEB 1 2 3 4 1 2 3! ENTER 2013. 329 2013.
13koki_koza.indd
 Tokyo University of Science Calendar 2013. 10~2014. 3 2013 6 13 20 27 7 14 21 28 1 8 15 22 29 10 Sun Mon Tue Wed Thu Fri Sat 2 9 16 23 30 3 10 17 24 31 4 11 18 25 5 12 19 26 3 10 17 24 4 11 18 25 5 12
Tokyo University of Science Calendar 2013. 10~2014. 3 2013 6 13 20 27 7 14 21 28 1 8 15 22 29 10 Sun Mon Tue Wed Thu Fri Sat 2 9 16 23 30 3 10 17 24 31 4 11 18 25 5 12 19 26 3 10 17 24 4 11 18 25 5 12
0ニ0・モgqNャX1TJf・
 2013 Summer 2012.4.1 >>> 2013.3.31 01 Masayuki Shimada 02 6: 6: 6: 03 SUN SAT FRI THU WED TUE MON 18 17 19 20 22 23 24 21 54 58 45 58 58 54 58 55 25 12 05 54 54 58 27 58 35 54 54 54 6: 5: 04 10: 10:54
2013 Summer 2012.4.1 >>> 2013.3.31 01 Masayuki Shimada 02 6: 6: 6: 03 SUN SAT FRI THU WED TUE MON 18 17 19 20 22 23 24 21 54 58 45 58 58 54 58 55 25 12 05 54 54 58 27 58 35 54 54 54 6: 5: 04 10: 10:54
Step1 Step2 Step3 Step4 Step5 COLUMN.1 Step1 Step2 Step3 Step4 Step5 Step6 Step7 Step8 COLUMN.2 Step1 Step2 Step3 Step4 Step5 COLUMN.3 Step1 Step2 Ste
 2 0 1 2 C A L E N D A R 7 8 9 SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT 1 2 3 4 5 6 7 1 2 3 4 8 9 10 11 12 13 14 5 6 7 8 9 10 11 15 16 17 18 19 20 21 12 13 14
2 0 1 2 C A L E N D A R 7 8 9 SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT SUN MON TUE WED THU FRI SAT 1 2 3 4 5 6 7 1 2 3 4 8 9 10 11 12 13 14 5 6 7 8 9 10 11 15 16 17 18 19 20 21 12 13 14
目次 Ⅰ. はじめに からのお願い 開始から終了までの流れ... 4 Ⅱ. 新規申込みの提出資料 書類について 使用成績調査 特定使用成績調査 ) 審査ファイル (A4 判 ) について 副作用 感染症症例報告
 製造販売後調査の申し込み手続き 使用成績調査特定使用成績調査 副作用 感染症症例報告 - 調 1 / 11- 目次 Ⅰ. はじめに... 3 1. からのお願い... 3 2. 開始から終了までの流れ... 4 Ⅱ. 新規申込みの提出資料 書類について... 5 1. 使用成績調査 特定使用成績調査... 5 1) 審査ファイル (A4 判 ) について... 5 2. 副作用 感染症症例報告...
製造販売後調査の申し込み手続き 使用成績調査特定使用成績調査 副作用 感染症症例報告 - 調 1 / 11- 目次 Ⅰ. はじめに... 3 1. からのお願い... 3 2. 開始から終了までの流れ... 4 Ⅱ. 新規申込みの提出資料 書類について... 5 1. 使用成績調査 特定使用成績調査... 5 1) 審査ファイル (A4 判 ) について... 5 2. 副作用 感染症症例報告...
平成11年 10月 日
 広島大学病院製造販売後医薬品調査マニュアル (Ver.6.31) 使用成績調査 特定使用成績調査 副作用 感染症報告 作成 : 広島大学病院総合医療研究推進センター Ver.6.00 作成年月日 :2008 年 10 月 24 日 2008 年 11 月 1 日より適用 Ver.6.10 作成年月日 :2014 年 8 月 11 日 Ver.6.20 作成年月日 :2015 年 1 月 30 日 2015
広島大学病院製造販売後医薬品調査マニュアル (Ver.6.31) 使用成績調査 特定使用成績調査 副作用 感染症報告 作成 : 広島大学病院総合医療研究推進センター Ver.6.00 作成年月日 :2008 年 10 月 24 日 2008 年 11 月 1 日より適用 Ver.6.10 作成年月日 :2014 年 8 月 11 日 Ver.6.20 作成年月日 :2015 年 1 月 30 日 2015
T OPICS 1 5.3 1430 1500 1700 6.2 1830 1900 T OPICS 4.16 1330 1400 6.4 1730 1800 1845 6.23 1815 1900 5.5 5.4 1430 1500 1615 1215 1300 1415 1515 TEL 011
 2016. 1 2 3 2016 4 5 SAPPORO CONCERT HALLPERFORMANCE CALENDAR 2016. 5 3 5 5 tue thu 1 2 3 5 3 SAPPORO CONCERT HALLPERFORMANCE CALENDAR 5 tue thu 5 2016 4 5 T OPICS 1 5.3 1430 1500 1700 6.2 1830 1900 T
2016. 1 2 3 2016 4 5 SAPPORO CONCERT HALLPERFORMANCE CALENDAR 2016. 5 3 5 5 tue thu 1 2 3 5 3 SAPPORO CONCERT HALLPERFORMANCE CALENDAR 5 tue thu 5 2016 4 5 T OPICS 1 5.3 1430 1500 1700 6.2 1830 1900 T
宮城県立がんセンター受託研究業務手順書
 平成 26 年 4 月 1 日一部改正使用成績調査 特定使用成績調査編 本編は 薬事法第 14 条の 4 及び第 14 条の 6 に基づく医薬品及び医療機器の再審査 再評価申請の際に提出すべき資料の収集のために行われる製造販売後調査 ( 使用成績調査及び特定使用成績調査 )( 以下 使用成績調査等 ) に適用するものとする 本編は 薬事法第 14 条の 4 第 4 項 薬事法第 14 条の 6 第
平成 26 年 4 月 1 日一部改正使用成績調査 特定使用成績調査編 本編は 薬事法第 14 条の 4 及び第 14 条の 6 に基づく医薬品及び医療機器の再審査 再評価申請の際に提出すべき資料の収集のために行われる製造販売後調査 ( 使用成績調査及び特定使用成績調査 )( 以下 使用成績調査等 ) に適用するものとする 本編は 薬事法第 14 条の 4 第 4 項 薬事法第 14 条の 6 第
Ⅲ 治験に係る直接費用と間接費用 ( 但し 治験検討会議出席に係る旅費については 下記 Ⅳにて記載する ) 1. 算出方法 (1) 治験に係る経費設定( 表 1) に従い費用を算出する 2. 覚書の作成と請求方法 (1) 治験契約の際 病院長と治験依頼者は 治験契約書 ( 別記様式第 12 号第 3
 治験費用に関する手順書 ( 改訂第 5 版 ) Ⅰ 目的 本手順書は 当院で実施される治験費用の事務手続き方法を定めたものである Ⅱ 治験に係る経費の範囲 1. 治験に係る直接費用 間接費用 及び治験検討会議出席に係る指導料 ( 表 1) (1) 直接費用 1) 研究費 2) 治験検討会議出席に係る旅費 3) 治験審査委員会外部委員の講師指導 4) 治験に関し雇用したアルバイト賃金及び備品費 5)
治験費用に関する手順書 ( 改訂第 5 版 ) Ⅰ 目的 本手順書は 当院で実施される治験費用の事務手続き方法を定めたものである Ⅱ 治験に係る経費の範囲 1. 治験に係る直接費用 間接費用 及び治験検討会議出席に係る指導料 ( 表 1) (1) 直接費用 1) 研究費 2) 治験検討会議出席に係る旅費 3) 治験審査委員会外部委員の講師指導 4) 治験に関し雇用したアルバイト賃金及び備品費 5)
独立行政法人国立病院機構仙台医療センターにおける医薬 品等の使用成績調査 特定使用成績調査及び副作用 感染 症報告 その他の受託研究の実施に関する標準業務手順書 2018 年 7 月 26 日第 9 版
 独立行政法人国立病院機構仙台医療センターにおける医薬 品等の使用成績調査 特定使用成績調査及び副作用 感染 症報告 その他の受託研究の実施に関する標準業務手順書 2018 年 7 月 26 日第 9 版 第 1 章総則 1. 目的と適用範囲この標準業務手順書は 独立行政法人国立病院機構仙台医療センターにおける医薬品の再審査申請 再評価申請の際に提出すべき資料の収集のための 使用成績調査 及び 特定使用成績調査
独立行政法人国立病院機構仙台医療センターにおける医薬 品等の使用成績調査 特定使用成績調査及び副作用 感染 症報告 その他の受託研究の実施に関する標準業務手順書 2018 年 7 月 26 日第 9 版 第 1 章総則 1. 目的と適用範囲この標準業務手順書は 独立行政法人国立病院機構仙台医療センターにおける医薬品の再審査申請 再評価申請の際に提出すべき資料の収集のための 使用成績調査 及び 特定使用成績調査
申請等の手引き
 新規治験の手続きについて 治験に関する問い合わせ先臨床研究支援センター治験事務局 Tel:06-6692-1201 ( 内線 2024) 平日 9:00~17:00 新規治験を実施する場合は 医師へ問い合わせ前に必ず治験事務局へご連絡ください 本文中のはホームページ上の をご確認ください 手順書等は最新版をホームページに掲載しております 各自ダウンロードしてください
新規治験の手続きについて 治験に関する問い合わせ先臨床研究支援センター治験事務局 Tel:06-6692-1201 ( 内線 2024) 平日 9:00~17:00 新規治験を実施する場合は 医師へ問い合わせ前に必ず治験事務局へご連絡ください 本文中のはホームページ上の をご確認ください 手順書等は最新版をホームページに掲載しております 各自ダウンロードしてください
.....Q.........\..A
 Osaka University of Commerce vol.01 2009 July 4. ( 2. ( 6. ( 5. ( 3. ( 1. ( ! 5 1 8 9 5 1 8 9 11 4 8 5 13 20 27 10 7 14 28 6 10 20 18 17 7 1 8 15 22 30 11 4 25 1 13 20 2 12 13 910 282 1923 1723 12 2 9
Osaka University of Commerce vol.01 2009 July 4. ( 2. ( 6. ( 5. ( 3. ( 1. ( ! 5 1 8 9 5 1 8 9 11 4 8 5 13 20 27 10 7 14 28 6 10 20 18 17 7 1 8 15 22 30 11 4 25 1 13 20 2 12 13 910 282 1923 1723 12 2 9
京都府立医科大学附属病院
 治験費用の取扱に関する手順書 京都府立医科大学附属病院 第 1 版平成 21 年 11 月 16 日 第 2 版平成 23 年 3 月 16 日 第 3 版平成 25 年 2 月 1 日 1. 目的 本手順書は 京都府立医科大学附属病院治験実施取扱規定の定めるところにより 治験 費用の取り扱いに関する運用方法を定め それに基づく業務手順を示すものである 2. 治験に係る経費の範囲 (1) 治験経費
治験費用の取扱に関する手順書 京都府立医科大学附属病院 第 1 版平成 21 年 11 月 16 日 第 2 版平成 23 年 3 月 16 日 第 3 版平成 25 年 2 月 1 日 1. 目的 本手順書は 京都府立医科大学附属病院治験実施取扱規定の定めるところにより 治験 費用の取り扱いに関する運用方法を定め それに基づく業務手順を示すものである 2. 治験に係る経費の範囲 (1) 治験経費
C01-C04
 1 January 20 21 22 23 24 25 26 27 28 29 30 31 sun mon tue wed thu fri s a t sun mon tue wed thu fri s a t 13 14 15 16 1 January 17 18 19 sun mon tue wed thu fri s a t sun mon tue wed thu fri s a t 13 20
1 January 20 21 22 23 24 25 26 27 28 29 30 31 sun mon tue wed thu fri s a t sun mon tue wed thu fri s a t 13 14 15 16 1 January 17 18 19 sun mon tue wed thu fri s a t sun mon tue wed thu fri s a t 13 20
1. 各項目に共通する注意点等について *IRB 審査資料の提出期限は IRB 開催日の 2 週間前までとします * 事前確認依頼については 資料提出期限の 1 週間前を目安に電子にて事務局担当者までご依頼ください スケジュールについては 当センター HP の IRB 年間開催日程と書類提出締切日
 西暦 2016 年 9 月 1 日 大阪市立大学医学部附属病院 医薬品 食品効能評価センター 治験事務局 新規契約締結以降の IRB 等の対応について 1. 各項目に共通する注意事項 2. 安全性情報 ( 委員会審査 ) 3.1 変更申請 ( 委員会審査 ) 2 変更申請 ( 軽微な変更委員会審査及び迅速審査 ) 3 変更契約書 各種覚書の締結について 4. 継続審査 ( 委員会審査 ) 5. 症例数確定後の手続きについて
西暦 2016 年 9 月 1 日 大阪市立大学医学部附属病院 医薬品 食品効能評価センター 治験事務局 新規契約締結以降の IRB 等の対応について 1. 各項目に共通する注意事項 2. 安全性情報 ( 委員会審査 ) 3.1 変更申請 ( 委員会審査 ) 2 変更申請 ( 軽微な変更委員会審査及び迅速審査 ) 3 変更契約書 各種覚書の締結について 4. 継続審査 ( 委員会審査 ) 5. 症例数確定後の手続きについて
<ヒアリング内容 > 1 依頼者からの説明 ( 概要書 プロトコールの要点 をそれぞれ10 分程度で ) ハンドアウト等の資料を準備すること 2 質疑 応答 ( 手順の確認を中心に ) 3 提出資料の確認 検討 修正指示 4その他 当該治験で検討を要する事項についての協議 保険外併用療養費の支給対象
 Ⅰ) 新規治験の申請 藤田医科大学病院治験申請等に関する手順書 1. 実施体制 治験事務局 SMO 費用は院内費用とは別に算定するため 別途相談とする 臨床研究コーディネーター (CRC) CRC は 院内または SMO のどちらの選択も可能とする 2. ヒアリング (a) 予約に際しての条件 プロトコールが固定され ( 治験届提出後 14 日 ( 初回届けの場合は 30 日 ) 経過したか否かは問わない
Ⅰ) 新規治験の申請 藤田医科大学病院治験申請等に関する手順書 1. 実施体制 治験事務局 SMO 費用は院内費用とは別に算定するため 別途相談とする 臨床研究コーディネーター (CRC) CRC は 院内または SMO のどちらの選択も可能とする 2. ヒアリング (a) 予約に際しての条件 プロトコールが固定され ( 治験届提出後 14 日 ( 初回届けの場合は 30 日 ) 経過したか否かは問わない
目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2
 免疫アレルギー疾患等実用化研究事業 ( 移植医療技術開発研究分野 ) 2019 年度 1 次公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 戦略推進部 難病研究課 2018 年 11 月 1 目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2 1. はじめに
免疫アレルギー疾患等実用化研究事業 ( 移植医療技術開発研究分野 ) 2019 年度 1 次公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 戦略推進部 難病研究課 2018 年 11 月 1 目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2 1. はじめに
広報ひめじ2013年6月号
 黒 田 官 兵 衛 人 と 生 涯 2 黒 田 官 兵 衛 人 と 生 涯 2 黒 田 官 兵 衛 人 と 生 涯 2 織 田 に 味 方 せ よ 信 長 か ら 名 刀 授 か る 織 田 に 味 方 せ よ 信 長 か ら 名 刀 授 か る 織 田 に 味 方 せ よ 信 長 か ら 名 刀 授 か る Mon Tue Wed Thu Fri Sat Sun 3
黒 田 官 兵 衛 人 と 生 涯 2 黒 田 官 兵 衛 人 と 生 涯 2 黒 田 官 兵 衛 人 と 生 涯 2 織 田 に 味 方 せ よ 信 長 か ら 名 刀 授 か る 織 田 に 味 方 せ よ 信 長 か ら 名 刀 授 か る 織 田 に 味 方 せ よ 信 長 か ら 名 刀 授 か る Mon Tue Wed Thu Fri Sat Sun 3
山形県立中央病院治験審査委員会業務手順書
 山形県立中央病院治験審査委員会業務手順書 第 1 目的この手順書は山形県立中央病院医薬品等臨床試験受託研究取扱要綱 ( 以下 取扱要綱 という ) に基づいて山形県立中央病院治験審査委員会 ( 以下 本委員会 という ) の運用方法を定め それに基づく業務手順書を示すものである なお 製造販売後臨床試験においては 以下 治験 とあるのを 製造販売後臨床試験 と読み替えるものとする 第 2 本委員会の責務本委員会は全ての被験者の人権の保護
山形県立中央病院治験審査委員会業務手順書 第 1 目的この手順書は山形県立中央病院医薬品等臨床試験受託研究取扱要綱 ( 以下 取扱要綱 という ) に基づいて山形県立中央病院治験審査委員会 ( 以下 本委員会 という ) の運用方法を定め それに基づく業務手順書を示すものである なお 製造販売後臨床試験においては 以下 治験 とあるのを 製造販売後臨床試験 と読み替えるものとする 第 2 本委員会の責務本委員会は全ての被験者の人権の保護
1998
 新潟県立中央病院医療機器製造販売後調査及び臨床研究取扱い要領 2012.7.5 (1) 製造販売後調査及び臨床研究の対象医療機器は 当院採用の医療機器に限るものとする 当該医療機器は保険適用内で使用し 医薬品の市販後調査の基準に関する省令 ( 平成 9 年 3 月 10 日厚生省令第 10 号 :GPMSP 省令 (Good Post-marketing Surveillance Practice)
新潟県立中央病院医療機器製造販売後調査及び臨床研究取扱い要領 2012.7.5 (1) 製造販売後調査及び臨床研究の対象医療機器は 当院採用の医療機器に限るものとする 当該医療機器は保険適用内で使用し 医薬品の市販後調査の基準に関する省令 ( 平成 9 年 3 月 10 日厚生省令第 10 号 :GPMSP 省令 (Good Post-marketing Surveillance Practice)
治験事務局標準業務マニュアル
 治験申請等に関する手順書 Ⅰ) 新規治験の申請 1. 実施体制 治験事務局院内スタッフが SMO との提携し 事務局を運営する なお SMO の費用は院内費用とは別に算定するため 別途相談とする CRC 院内スタッフを用いる場合 SMO を利用する場合 どちらの選択も可能とする 2. ヒアリング (a) 予約に際しての条件 プロトコールが固定され 責任医師との合意が文書で得られた時点で予約は可能とする
治験申請等に関する手順書 Ⅰ) 新規治験の申請 1. 実施体制 治験事務局院内スタッフが SMO との提携し 事務局を運営する なお SMO の費用は院内費用とは別に算定するため 別途相談とする CRC 院内スタッフを用いる場合 SMO を利用する場合 どちらの選択も可能とする 2. ヒアリング (a) 予約に際しての条件 プロトコールが固定され 責任医師との合意が文書で得られた時点で予約は可能とする
治験実施に必要な手続きについて (HP 用 ) 治験 製造販売後臨床試験 聖マリアンナ医科大学病院治験管理室 聖マリアンナ医科大学病院治験管理室 2011 年 10 月作成 2013 年 1 月改訂 2014 年 4 月改訂 2018 年 4 月改定 2018 年 5 月改定 Ⅰ. 治験審査委員会
 治験実施に必要な手続きについて (HP 用 ) 治験 製造販売後臨床試験 2011 年 10 月作成 2013 年 1 月改訂 2014 年 4 月改訂 2018 年 4 月改定 2018 年 5 月改定 Ⅰ. 治験審査委員会 (IRB) と連絡先 治験審査委員会名称 治験審査委員会設置者 聖マリアンナ医科大学附属病院等治験審査委員会 St. Marianna University Group Institutional
治験実施に必要な手続きについて (HP 用 ) 治験 製造販売後臨床試験 2011 年 10 月作成 2013 年 1 月改訂 2014 年 4 月改訂 2018 年 4 月改定 2018 年 5 月改定 Ⅰ. 治験審査委員会 (IRB) と連絡先 治験審査委員会名称 治験審査委員会設置者 聖マリアンナ医科大学附属病院等治験審査委員会 St. Marianna University Group Institutional
北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下
 北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下 モニタリング という ) 監査の受け入れ 並びに試験審査委員会( 治験審査委員会が兼ねる 以下 治験審査委員会
北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下 モニタリング という ) 監査の受け入れ 並びに試験審査委員会( 治験審査委員会が兼ねる 以下 治験審査委員会
新規申請に関する手順書
 新規申請に関する手順書 - 新規申請から契約までの手順 - ( 改訂第 8 版 ) Ⅰ 目的 本手順書は 当院で実施する治験を申請する際の手続きを定めたものである Ⅱ 申請前の手順 1. 新規相談 ( 施設調査も含む ) (1) 相談受付 1) 治験依頼者又は自ら治験を実施する者 ( 以下 治験依頼者等 という ) は 臨床試験推進部にあらかじめ予約を入れ新規治験相談を行う a) 予約の受付時間 8
新規申請に関する手順書 - 新規申請から契約までの手順 - ( 改訂第 8 版 ) Ⅰ 目的 本手順書は 当院で実施する治験を申請する際の手続きを定めたものである Ⅱ 申請前の手順 1. 新規相談 ( 施設調査も含む ) (1) 相談受付 1) 治験依頼者又は自ら治験を実施する者 ( 以下 治験依頼者等 という ) は 臨床試験推進部にあらかじめ予約を入れ新規治験相談を行う a) 予約の受付時間 8
企業登録の更新 1. メインメニュー の 有効期限の更新 ( 期限 30 日前から手続可能 ) をします 有効期限切れまでの日数を警告 2. 登録申請書を作成する をし 企業情報に変更がなければ ( 変更がある場合は修正し ) 署名者 ( サイナー ) 登録リストへ をします 1 登録申請書を作成す
 発給システムにおける 企業登録の更新 / 変更および署名者 ( サイナー ) の変更 / 追加 / 削除 操作説明書 目 次 企業登録の更新 2 企業情報の変更 5 署名者 ( サイナー ) の変更 9 署名者 ( サイナー ) の追加 削除 13 2018 年 11 月日本商工会議所 1 企業登録の更新 1. メインメニュー の 有効期限の更新 ( 期限 30 日前から手続可能 ) をします 有効期限切れまでの日数を警告
発給システムにおける 企業登録の更新 / 変更および署名者 ( サイナー ) の変更 / 追加 / 削除 操作説明書 目 次 企業登録の更新 2 企業情報の変更 5 署名者 ( サイナー ) の変更 9 署名者 ( サイナー ) の追加 削除 13 2018 年 11 月日本商工会議所 1 企業登録の更新 1. メインメニュー の 有効期限の更新 ( 期限 30 日前から手続可能 ) をします 有効期限切れまでの日数を警告
規程書
 独立行政法人国立病院機構栃木医療センター 受託研究取扱規程 平成 25 年 4 月 1 日 独立行政法人国立病院機構栃木医療センター受託研究取 扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構栃木医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程定めるところによる
独立行政法人国立病院機構栃木医療センター 受託研究取扱規程 平成 25 年 4 月 1 日 独立行政法人国立病院機構栃木医療センター受託研究取 扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構栃木医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程定めるところによる
治験実施規程
 京都市立病院 治験実施要綱 平成 25 年 9 月 2 日 ( 第 7 版 ) 目次 第 Ⅰ 章総則 1 第 1 条 ( 目的 ) 1 第 2 条 ( 治験に関する原則事項 ) 1 第 3 条 ( 用語 ) 2 第 4 条 ( 秘密の保全 ) 2 第 5 条 ( 直接閲覧 ) 2 第 Ⅱ 章院長 2 第 6 条 ( 治験実施体制の構築 ) 2 第 7 条 ( 治験の受託 ) 3 第 8 条 ( 治験の継続
京都市立病院 治験実施要綱 平成 25 年 9 月 2 日 ( 第 7 版 ) 目次 第 Ⅰ 章総則 1 第 1 条 ( 目的 ) 1 第 2 条 ( 治験に関する原則事項 ) 1 第 3 条 ( 用語 ) 2 第 4 条 ( 秘密の保全 ) 2 第 5 条 ( 直接閲覧 ) 2 第 Ⅱ 章院長 2 第 6 条 ( 治験実施体制の構築 ) 2 第 7 条 ( 治験の受託 ) 3 第 8 条 ( 治験の継続
目次 1. この手引きについて 変更交付申請について 変更交付申請書の書類の作成 住宅リフォーム補助金変更交付申請書 ( 様式第 4 号 ) 変更する内容の分かる見積書の写し 変更する内容の分かる現場写
 安中市住宅リフォーム補助金変更交付申請 完了報告の手引き 平成 30 年度安中市 お問い合わせ 提出先 379-0192 安中市安中一丁目 23-13 安中市役所建設部建築住宅課指導係 ( 本庁 1 階 ) 電話 :027-382-1111( 内線 1255 1256 1257) FAX:027-381-7020-1 - 目次 1. この手引きについて... 3 2. 変更交付申請について... 4
安中市住宅リフォーム補助金変更交付申請 完了報告の手引き 平成 30 年度安中市 お問い合わせ 提出先 379-0192 安中市安中一丁目 23-13 安中市役所建設部建築住宅課指導係 ( 本庁 1 階 ) 電話 :027-382-1111( 内線 1255 1256 1257) FAX:027-381-7020-1 - 目次 1. この手引きについて... 3 2. 変更交付申請について... 4
「給与・年金の方」からの確定申告書作成編
 所得が 給与のみ 年金のみ 給与と年金のみ の 方で 入力方法選択 画面で 給与 年金の方 を選択さ れた場合の確定申告書作成の操作手順を説明します ~ この操作の手引きをご利用になる前に ~ この操作の手引きでは 確定申告書の作成方法をご説明しています 操作を始める前に 以下の内容をご確認ください 共通の操作の手引きの確認入力方法などを説明した ( 共通 )e-tax で送信するための準備編 又は
所得が 給与のみ 年金のみ 給与と年金のみ の 方で 入力方法選択 画面で 給与 年金の方 を選択さ れた場合の確定申告書作成の操作手順を説明します ~ この操作の手引きをご利用になる前に ~ この操作の手引きでは 確定申告書の作成方法をご説明しています 操作を始める前に 以下の内容をご確認ください 共通の操作の手引きの確認入力方法などを説明した ( 共通 )e-tax で送信するための準備編 又は
<4D F736F F D208EA18CB182C98AD682B782E995578F808BC696B18EE88F878F E7B8D732E646F6378>
 治験に関する標準業務手順書 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医薬品及び医療機器の臨床試験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和
治験に関する標準業務手順書 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医薬品及び医療機器の臨床試験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和
「給与・年金の方」からの確定申告書作成編
 所得が 年金のみ の方で 入力方法選択 画面で 給 与 年金の方 を選択された場合の確定申告書作成の入力例を 説明します 1 作成開始 ---------------------------------------------------------------------- 1 2 作成の流れや画面の案内 操作方法について ---------------------------------------
所得が 年金のみ の方で 入力方法選択 画面で 給 与 年金の方 を選択された場合の確定申告書作成の入力例を 説明します 1 作成開始 ---------------------------------------------------------------------- 1 2 作成の流れや画面の案内 操作方法について ---------------------------------------
国立仙台病院受託研究取扱規程
 独立行政法人国立病院機構仙台医療センター受託研究取扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構仙台医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程の定めるところによる 2 契約 経理及び書式等については 原則として独立行政法人国立病院機構
独立行政法人国立病院機構仙台医療センター受託研究取扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構仙台医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程の定めるところによる 2 契約 経理及び書式等については 原則として独立行政法人国立病院機構
治験手続きについて
 2 国立研究開発法人国立精神 神経医療研究センターにおける治験手続き要領 治験申込みは 治験審査依頼を希望する IRB の原則として 8 週間前が締切りです 当センター IRB は 毎月第 4 木曜に実施しています 新規申請の流れと必要な書類 1. 電話受付 新規申込み希望の場合は 治験主任 ( 内線 3783) へ電話連絡下さい その際に施設選定受入の日程 調整を行います 2. 施設選定受入 治験実施計画内容等の説明をお願いします
2 国立研究開発法人国立精神 神経医療研究センターにおける治験手続き要領 治験申込みは 治験審査依頼を希望する IRB の原則として 8 週間前が締切りです 当センター IRB は 毎月第 4 木曜に実施しています 新規申請の流れと必要な書類 1. 電話受付 新規申込み希望の場合は 治験主任 ( 内線 3783) へ電話連絡下さい その際に施設選定受入の日程 調整を行います 2. 施設選定受入 治験実施計画内容等の説明をお願いします
<955C8E862E6169>
 JAPAN INTERNATIONAL CONTENTS FESTIVAL 9/30 TUE 10/1 WED 2 THU 3 FRI 4 SAT 5 SUN 6 MON 7 TUE 8 WED 9 THU 10 FRI 11 SAT 12 SUN 13 MON 14 TUE 2008 / EVENT MAP 15 WED 16 THU 17 FRI 18 SAT 19 SUN 20 MON 21
JAPAN INTERNATIONAL CONTENTS FESTIVAL 9/30 TUE 10/1 WED 2 THU 3 FRI 4 SAT 5 SUN 6 MON 7 TUE 8 WED 9 THU 10 FRI 11 SAT 12 SUN 13 MON 14 TUE 2008 / EVENT MAP 15 WED 16 THU 17 FRI 18 SAT 19 SUN 20 MON 21
医師主導治験取扱要覧
 15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
目次 1. はじめに 2. 実際の応募手続き 3. 応募手続き完了の確認 2
 革新的バイオ医薬品創出基盤技術開発事業 H27 年度公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 1 目次 1. はじめに 2. 実際の応募手続き 3. 応募手続き完了の確認 2 1-a. はじめに 1 注意事項 1. 平成 27 年度の革新的バイオ医薬品創出基盤技術開発事業への応募は 必ず e-rad を利用して下さい 2. e-rad の使用に当たっては 研究機関および研究者の事前登録が必要です
革新的バイオ医薬品創出基盤技術開発事業 H27 年度公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 1 目次 1. はじめに 2. 実際の応募手続き 3. 応募手続き完了の確認 2 1-a. はじめに 1 注意事項 1. 平成 27 年度の革新的バイオ医薬品創出基盤技術開発事業への応募は 必ず e-rad を利用して下さい 2. e-rad の使用に当たっては 研究機関および研究者の事前登録が必要です
 目 め 隠 か く し 陶 と う 芸 げ い の 心 こころ 旅 た び の 巻 ま き 闇 の 中 に 見 えてくるイメージを 形 に キッズゴルファーへの 道 の 巻 週 末 体 験 くらぶの 夏 休 み 期 間 中 の 予 定 です 週 末 体 験 くらぶの 夏 休 み 期 間 中 の 予 定 です 8 SUN MON TUE WED THU FRI SAT 2 3 4 5 6
目 め 隠 か く し 陶 と う 芸 げ い の 心 こころ 旅 た び の 巻 ま き 闇 の 中 に 見 えてくるイメージを 形 に キッズゴルファーへの 道 の 巻 週 末 体 験 くらぶの 夏 休 み 期 間 中 の 予 定 です 週 末 体 験 くらぶの 夏 休 み 期 間 中 の 予 定 です 8 SUN MON TUE WED THU FRI SAT 2 3 4 5 6
ニュース10-11月号
 2 TOKYO NATIONAL MUSEUM NEWS 8 1201 3PICK UP DATA 1250 1081212 1300 1,5001,200 1,200900 900600 20 1 03-5777-8600 http:// todaiji2010.jp/ 10 8 200 1121121 3 EVENT 12 13 12 13 12 13 3 10301330151161330153
2 TOKYO NATIONAL MUSEUM NEWS 8 1201 3PICK UP DATA 1250 1081212 1300 1,5001,200 1,200900 900600 20 1 03-5777-8600 http:// todaiji2010.jp/ 10 8 200 1121121 3 EVENT 12 13 12 13 12 13 3 10301330151161330153
薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リ
 薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リスク管理計画の実施状況及び得られた結果の評価に関する報告の様式 提出等の取扱いについては 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について
薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リスク管理計画の実施状況及び得られた結果の評価に関する報告の様式 提出等の取扱いについては 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について
標準業務手順 目次
 浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
10 届書の作成編 ねんきんネット ご利用ガイド ねんきんネット ご利用ガイド 届書の作成 編 平成 30 年 10 月 1 日
 届書の作成 編 平成 30 年 10 月 1 日 目次 10 届書の作成 1 届書の作成とは 1.1 届書の作成の概要... 10-2 2 お手続きの流れ 3 操作の流れ 3.1 届書を作成する... 10-4 3.2 届書を印刷する... 10-8 3.3 届書を保存する... 10-9 4 画面の説明 4.1 住所検索条件入力 画面の説明... 10-10 4.2 金融機関名検索( 条件入力 )
届書の作成 編 平成 30 年 10 月 1 日 目次 10 届書の作成 1 届書の作成とは 1.1 届書の作成の概要... 10-2 2 お手続きの流れ 3 操作の流れ 3.1 届書を作成する... 10-4 3.2 届書を印刷する... 10-8 3.3 届書を保存する... 10-9 4 画面の説明 4.1 住所検索条件入力 画面の説明... 10-10 4.2 金融機関名検索( 条件入力 )
【押印あり】日本医学会宛
 別紙 再生医療等製品患者登録システムへの参加協力のお願い 患者登録システムの目的 患者登録システムは 再生医療等製品の市販後の使用状況や患者予後等のデータを収集し 迅速な安全対策や新たな製品開発等を通じて 医療の向上に役立てることを目的としています 患者登録システムは 製品毎に構築 運用されます この患者登録システムは 一般的には レジストリ と呼ばれることもあります 構築形態例 患者登録システムの対象
別紙 再生医療等製品患者登録システムへの参加協力のお願い 患者登録システムの目的 患者登録システムは 再生医療等製品の市販後の使用状況や患者予後等のデータを収集し 迅速な安全対策や新たな製品開発等を通じて 医療の向上に役立てることを目的としています 患者登録システムは 製品毎に構築 運用されます この患者登録システムは 一般的には レジストリ と呼ばれることもあります 構築形態例 患者登録システムの対象
<93648EA593498B4C985E82C98AD682B782E E838A F E315F C668DDA95AA292E786C7378>
 1 実施医療機関の長等の承諾 電磁的記録として扱う治験関連文書 ( 範囲 ) の承諾 SOP 等 施設の正式文書の記載 実施医療機関の長からの確認 実務担当者からの確認 電磁的記録の交付 受領手段の承諾 SOP 等 施設の正式文書の記載 実施医療機関の長からの確認 実務担当者からの確認 ( 版 :2013 年 9 月 1 日 ver2.0) 2 3 電磁的記録として扱う治験関連文書 電磁的記録の交付
1 実施医療機関の長等の承諾 電磁的記録として扱う治験関連文書 ( 範囲 ) の承諾 SOP 等 施設の正式文書の記載 実施医療機関の長からの確認 実務担当者からの確認 電磁的記録の交付 受領手段の承諾 SOP 等 施設の正式文書の記載 実施医療機関の長からの確認 実務担当者からの確認 ( 版 :2013 年 9 月 1 日 ver2.0) 2 3 電磁的記録として扱う治験関連文書 電磁的記録の交付
<4D F736F F D208EA18CB182C98AD682B782E995578F808BC696B18EE88F878F E38E748EE593B1816A E7B8D732E646F637
 治験に関する標準業務手順書 ( 医師主導治験 ) 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医師主導治験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 (
治験に関する標準業務手順書 ( 医師主導治験 ) 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医師主導治験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 (
 商業 法人登記申請は オンラインによる登記事項の提出 が簡単便利です!! 提出のメリット 申請書が簡単に作成できる! 受付番号 書類訂正 登記完了がわかる! 電子署名及び電子証明書の添付が不要 オンライン提出の流れソフトのダウンロード登記事項の作成オンラインで送信 検索はコレで 法務省オンライン提出 印刷した申請書の提出 ( 持参又は郵送 ) 申請書 オンライン送信後, 申請書 ( 17 ケタ番号
商業 法人登記申請は オンラインによる登記事項の提出 が簡単便利です!! 提出のメリット 申請書が簡単に作成できる! 受付番号 書類訂正 登記完了がわかる! 電子署名及び電子証明書の添付が不要 オンライン提出の流れソフトのダウンロード登記事項の作成オンラインで送信 検索はコレで 法務省オンライン提出 印刷した申請書の提出 ( 持参又は郵送 ) 申請書 オンライン送信後, 申請書 ( 17 ケタ番号
Microsoft Word - 21_提出方法(電子申告).doc
 確定申告書の内容の入力を終了した方で e-tax( 電子申告 ) により確定申告書等を提出する場合の操作手順を説明します ~ この操作の手引きをご利用になる前に ~ この操作の手引きでは e-tax( 電子申告 ) により申告書を提出する場合の操作について 住所 氏名等入力 画面からご説明しています 申告書の作成については 申告内容に応じた操作の手引きをご覧ください 操作を始める前に 以下の内容をご確認ください
確定申告書の内容の入力を終了した方で e-tax( 電子申告 ) により確定申告書等を提出する場合の操作手順を説明します ~ この操作の手引きをご利用になる前に ~ この操作の手引きでは e-tax( 電子申告 ) により申告書を提出する場合の操作について 住所 氏名等入力 画面からご説明しています 申告書の作成については 申告内容に応じた操作の手引きをご覧ください 操作を始める前に 以下の内容をご確認ください
( 書式 4), 治験責任医師の履歴書及び治験実施計画書等の審査の対象となる文書を委員会に提出し, 治験の実施について意見を求めるものとする 2 病院長は, 委員会が治験の実施を承認する決定をし, 又は治験実施計画書, 症例報告書, 説明文書及び同意書並びにその他の手順について何らかの修正を条件に治
 秋田大学医学部附属病院医薬品等の受託研究取扱細則 病 7-07 [ 制定 ] 平成 16 年 4 月 1 日 ( 趣旨と適用範囲 ) 第 1 条この細則は, 秋田大学医学部附属病院医薬品等の受託研究取扱規程第 15 条に基づき, 治験の実施に必要な手続きと運営に関する手順を定めるものとする 本細則の運用に関しては医薬品の臨床試験の実施に関する省令 ( 平成 9 年厚生省令第 28 号 以下 医薬品
秋田大学医学部附属病院医薬品等の受託研究取扱細則 病 7-07 [ 制定 ] 平成 16 年 4 月 1 日 ( 趣旨と適用範囲 ) 第 1 条この細則は, 秋田大学医学部附属病院医薬品等の受託研究取扱規程第 15 条に基づき, 治験の実施に必要な手続きと運営に関する手順を定めるものとする 本細則の運用に関しては医薬品の臨床試験の実施に関する省令 ( 平成 9 年厚生省令第 28 号 以下 医薬品
北海道大学病院治験取扱要項
 製造販売後調査 標準業務手順書 北海道大学病院 制定日 : 平成 26 年 2 月 1 日 北海道大学病院製造販売後調査標準業務手順書 平成 26 年 2 月 1 日制定 目 次 第 1 章総則第 1 条 : 趣旨第 2 条 : 目的と適用範囲第 3 条 : 定義 第 2 章病院長の業務第 4 条 : 製造販売後調査実施のための組織の設置第 5 条 : 製造販売後調査の新規申請等第 6 条 : 製造販売後調査実施の了承等第
製造販売後調査 標準業務手順書 北海道大学病院 制定日 : 平成 26 年 2 月 1 日 北海道大学病院製造販売後調査標準業務手順書 平成 26 年 2 月 1 日制定 目 次 第 1 章総則第 1 条 : 趣旨第 2 条 : 目的と適用範囲第 3 条 : 定義 第 2 章病院長の業務第 4 条 : 製造販売後調査実施のための組織の設置第 5 条 : 製造販売後調査の新規申請等第 6 条 : 製造販売後調査実施の了承等第
PowerPoint プレゼンテーション
 発注者 条件付一般競争一般競争入札業務フロー 応札者 1 システムへのログイン 公告 / 発注図書公開 2 調達情報確認 / 発注図書取得 3 質問書の提出 ( システム外 ) 4 電子入札システムログイン 競争参加資格確認申請書受付 5 競争参加資格確認申請書提出 6 競争参加資格確認申請書受付票受信 競争参加資格確認通知書発行質問回答書の公開入札書受付締切通知書発行 7 競争参加資格確認通知書受信
発注者 条件付一般競争一般競争入札業務フロー 応札者 1 システムへのログイン 公告 / 発注図書公開 2 調達情報確認 / 発注図書取得 3 質問書の提出 ( システム外 ) 4 電子入札システムログイン 競争参加資格確認申請書受付 5 競争参加資格確認申請書提出 6 競争参加資格確認申請書受付票受信 競争参加資格確認通知書発行質問回答書の公開入札書受付締切通知書発行 7 競争参加資格確認通知書受信
サービス付き高齢者向け住宅整備事業WEB申請マニュアル
 WEB 申請マニュアル 交付申請書の作成 ( 調査設計計画を除く ) や 審査中の整備事業事務局 ( 以下 : 事務局 ) とのやり取り および書類の再提出等はすべて WEB 上で行います 交付申請の手続きの流れは下記のとおりです 交付申請書の提出までの流れ 交付申請者 事務局 STEP 1 アカウントの登録 ( 事業者情報 パスワード等の入力 ) アカウント情報の蓄積 添付書類の作成 交付申請情報を入力する前に添付資料
WEB 申請マニュアル 交付申請書の作成 ( 調査設計計画を除く ) や 審査中の整備事業事務局 ( 以下 : 事務局 ) とのやり取り および書類の再提出等はすべて WEB 上で行います 交付申請の手続きの流れは下記のとおりです 交付申請書の提出までの流れ 交付申請者 事務局 STEP 1 アカウントの登録 ( 事業者情報 パスワード等の入力 ) アカウント情報の蓄積 添付書類の作成 交付申請情報を入力する前に添付資料
„‰“⁄†Fno.8-01.pdf
 Contents No.8 2006.October Takeo Public Relations Magazine 2 TAKEO Public Relations 3 TAKEO Public Relations 4 TAKEO Public Relations TAKEO Public Relations 6 7 TAKEO Public Relations 8 TAKEO Public Relations
Contents No.8 2006.October Takeo Public Relations Magazine 2 TAKEO Public Relations 3 TAKEO Public Relations 4 TAKEO Public Relations TAKEO Public Relations 6 7 TAKEO Public Relations 8 TAKEO Public Relations
NACCS をはじめてご利用される方 1. 仮アカウントの発行 NACCS をはじめてご利用される方 NACCS をはじめてご利用される場合または事業所追加の申込をされる場合は 仮アカウントの発行から新 規の利用申込を行います ご利用いただける手続きはログイン画面から始めます NACCS のご利用開
 . 仮アカウントの発行 NACCS をはじめてご利用される場合または事業所追加の申込をされる場合は 仮アカウントの発行から新 規の利用申込を行います ご利用いただける手続きはログイン画面から始めます NACCS のご利用開始までは 新規の利用申込の後 継続して システム設定の申込 を行う必要があります 継続の手続きについては 利用開始までのガイダンス (P9) をご参照ください ログイン画面 ログインのリンク
. 仮アカウントの発行 NACCS をはじめてご利用される場合または事業所追加の申込をされる場合は 仮アカウントの発行から新 規の利用申込を行います ご利用いただける手続きはログイン画面から始めます NACCS のご利用開始までは 新規の利用申込の後 継続して システム設定の申込 を行う必要があります 継続の手続きについては 利用開始までのガイダンス (P9) をご参照ください ログイン画面 ログインのリンク
山梨県〇〇〇〇システム
 4. 変更申請手続き 4 変更申請手続き 作業手順を確認してください 申請データの作成 ( 条件入力 ) 4.1 を参照 変更届 ( 申請データ ) を Web 画面上に表示するための条件を入力します ( 従来の申請 データ作成プログラムのダウンロード及びインストール作業は不要となりました ) 申請データの作成 4.2 を参照 Web 画面上に表示された入力フォームに記入し 変更届 ( 申請データ
4. 変更申請手続き 4 変更申請手続き 作業手順を確認してください 申請データの作成 ( 条件入力 ) 4.1 を参照 変更届 ( 申請データ ) を Web 画面上に表示するための条件を入力します ( 従来の申請 データ作成プログラムのダウンロード及びインストール作業は不要となりました ) 申請データの作成 4.2 を参照 Web 画面上に表示された入力フォームに記入し 変更届 ( 申請データ
「給与・年金の方」からの確定申告書作成編
 所得が 給与のみ 年金のみ 給与と年金のみ の 方で 入力方法選択 画面で 給与 年金の方 を選択さ れた場合の確定申告書作成の操作手順を説明します ~ この操作の手引きをご利用になる前に ~ この操作の手引きでは 確定申告書の作成方法をご説明しています 操作を始める前に 以下の内容をご確認ください 共通の操作の手引きの確認入力方法などを説明した ( 共通 )e-tax で送信するための準備編 又は
所得が 給与のみ 年金のみ 給与と年金のみ の 方で 入力方法選択 画面で 給与 年金の方 を選択さ れた場合の確定申告書作成の操作手順を説明します ~ この操作の手引きをご利用になる前に ~ この操作の手引きでは 確定申告書の作成方法をご説明しています 操作を始める前に 以下の内容をご確認ください 共通の操作の手引きの確認入力方法などを説明した ( 共通 )e-tax で送信するための準備編 又は
<4D F736F F D20352D F6F88EA816A81798DDD90D C70817A D E646F63>
 1. フローチャート 出産育児一時金 ( 在職者 任意継続被保険者 ) 1 妊娠 4ヵ月 (85 日 ) 以上の出産ですか? 妊娠 4ヵ月 (85 日 ) 未満のため請求できません 2 当組合加入後 6ヵ月以内の出産ですか? 3 以前加入していた健保組合等から出産育児一時金を受給していますか? 重複して受給することができないため請求できません 4 直接支払制度を利用されますか? 直接支払制度とは 分娩予定の医療機関等と被保険者等との合意に基づき
1. フローチャート 出産育児一時金 ( 在職者 任意継続被保険者 ) 1 妊娠 4ヵ月 (85 日 ) 以上の出産ですか? 妊娠 4ヵ月 (85 日 ) 未満のため請求できません 2 当組合加入後 6ヵ月以内の出産ですか? 3 以前加入していた健保組合等から出産育児一時金を受給していますか? 重複して受給することができないため請求できません 4 直接支払制度を利用されますか? 直接支払制度とは 分娩予定の医療機関等と被保険者等との合意に基づき
H29 年度再生医療の産業化に向けた評価基盤技術開発事業 ( 再生医療技術を応用した創薬支援基盤技術の開発 ) 新規公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 1
 H29 年度再生医療の産業化に向けた評価基盤技術開発事業 ( 再生医療技術を応用した創薬支援基盤技術の開発 ) 新規公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 1 目次 1. はじめに 2. 実際の応募手続き 3. 応募手続き完了の確認 2 1-a. はじめに 1 注意事項 1. 平成 29 年度の 再生医療の産業化に向けた評価基盤技術開発事業 ( 再生医療技術を応用した創薬支援基盤技術の開発
H29 年度再生医療の産業化に向けた評価基盤技術開発事業 ( 再生医療技術を応用した創薬支援基盤技術の開発 ) 新規公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 1 目次 1. はじめに 2. 実際の応募手続き 3. 応募手続き完了の確認 2 1-a. はじめに 1 注意事項 1. 平成 29 年度の 再生医療の産業化に向けた評価基盤技術開発事業 ( 再生医療技術を応用した創薬支援基盤技術の開発
【01-1】H28末〆通知(案) ver
 乗車賃立替払 謝金 旅費について 別紙 1. 乗車賃立替払 1 平成 28 年 12 月 31 日までの乗車分 : 平成 29 年 1 月 20 日 ( 金 ) 2 平成 29 年 2 月 28 日までの乗車分 : 平成 29 年 3 月 13 日 ( 月 ) 3 平成 29 年 3 月 31 日までの乗車分 : 平成 29 年 4 月 3 日 ( 月 ) 2. 謝金 物品等請求システムへの入力 (
乗車賃立替払 謝金 旅費について 別紙 1. 乗車賃立替払 1 平成 28 年 12 月 31 日までの乗車分 : 平成 29 年 1 月 20 日 ( 金 ) 2 平成 29 年 2 月 28 日までの乗車分 : 平成 29 年 3 月 13 日 ( 月 ) 3 平成 29 年 3 月 31 日までの乗車分 : 平成 29 年 4 月 3 日 ( 月 ) 2. 謝金 物品等請求システムへの入力 (
建設コンサルタンツ協会CPD制度の手引き
 7. 各種変更 届出について CPD システムに登録している会員情報に変更が生じた場合や その他の届出については その都度速やか に行ってください 7-1 氏名の変更婚姻 改名等により氏名が変更になった場合は 届出様式 CPD 会員情報変更届兼会員カード再発行申請書 に必要事項を記載の上 添付書類と併せてCPD 事務局に郵送してください CPD 記録申請においては CPDシステムに登録されている氏名
7. 各種変更 届出について CPD システムに登録している会員情報に変更が生じた場合や その他の届出については その都度速やか に行ってください 7-1 氏名の変更婚姻 改名等により氏名が変更になった場合は 届出様式 CPD 会員情報変更届兼会員カード再発行申請書 に必要事項を記載の上 添付書類と併せてCPD 事務局に郵送してください CPD 記録申請においては CPDシステムに登録されている氏名
医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能
 医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 1 2 3 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能 ) ( 医薬品の名称のみで検索する場合 34 の項目は未選択 未入力で可 ) 検索結果で表示したい文書を選択
医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 1 2 3 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能 ) ( 医薬品の名称のみで検索する場合 34 の項目は未選択 未入力で可 ) 検索結果で表示したい文書を選択
ICH-GCPとJ-GCPとの比較表
 参考資料 10 我が国の GCP と ICH-GCP の主な 1 治験の契約に関する規定 1-1 契約者に関する規定 1-2 実施医療機関の長との契約を規定したことに伴う規定 2 治験審査委員会 (IRB) に関する規定 2-1 IRB の設置に関する規定 2-2 IRB への審議依頼に関する規定 1/11 1. 治験の契約に関する規定 1-1. 契約者に関する規定 ICH-GCP 1.17( 用語の定義
参考資料 10 我が国の GCP と ICH-GCP の主な 1 治験の契約に関する規定 1-1 契約者に関する規定 1-2 実施医療機関の長との契約を規定したことに伴う規定 2 治験審査委員会 (IRB) に関する規定 2-1 IRB の設置に関する規定 2-2 IRB への審議依頼に関する規定 1/11 1. 治験の契約に関する規定 1-1. 契約者に関する規定 ICH-GCP 1.17( 用語の定義
治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会
 治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会 第 1 条 ( 目的 ) 1. 本手順書は 新光会治験審査委員会 ( 以下 委員会という ) において 医薬品及び医療機器 ( 以下 医薬品等という ) の治験の調査審議を実施するに当たり 薬事法 ( 昭和 35 年 8 月 10 日法律第 145 号 ) に基づく 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3
治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会 第 1 条 ( 目的 ) 1. 本手順書は 新光会治験審査委員会 ( 以下 委員会という ) において 医薬品及び医療機器 ( 以下 医薬品等という ) の治験の調査審議を実施するに当たり 薬事法 ( 昭和 35 年 8 月 10 日法律第 145 号 ) に基づく 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3
1. はじめに ログイン 初回ユーザ登録 投稿者メニュー 新規投稿 論文基本情報入力 アップロードファイル情報入力 登録内容確認 登録
 日本ハンドセラピィ学会機関誌オンライン投稿フォーム 操作説明書 第 1 版 :2011 年 10 月 1 日 1 1. はじめに... 3 2. ログイン... 4 3. 初回ユーザ登録... 5 4. 投稿者メニュー... 6 4-1. 新規投稿... 7 4-1-1. 論文基本情報入力... 7 4-1-2. アップロードファイル情報入力... 8 4-1-3. 登録内容確認... 10 4-1-4.
日本ハンドセラピィ学会機関誌オンライン投稿フォーム 操作説明書 第 1 版 :2011 年 10 月 1 日 1 1. はじめに... 3 2. ログイン... 4 3. 初回ユーザ登録... 5 4. 投稿者メニュー... 6 4-1. 新規投稿... 7 4-1-1. 論文基本情報入力... 7 4-1-2. アップロードファイル情報入力... 8 4-1-3. 登録内容確認... 10 4-1-4.
治 験 実 施 標 準 業 務 手 順 書
 治験審査委員会標準業務手順書 < 企業治験 > 横浜労災病院 目 次 第 1 章治験審査委員会 2 目的と適用範囲 2 治験審査委員会の責務 2 治験審査委員会の設置及び構成 2 治験審査委員会の業務 3 治験審査委員会の運営 5 第 2 章治験審査委員会事務局 6 治験審査委員会事務局の設置と業務 6 第 3 章記録の保存と公開 7 記録の保存責任者 7 記録の保存期間 7 記録の公開 8 1 第
治験審査委員会標準業務手順書 < 企業治験 > 横浜労災病院 目 次 第 1 章治験審査委員会 2 目的と適用範囲 2 治験審査委員会の責務 2 治験審査委員会の設置及び構成 2 治験審査委員会の業務 3 治験審査委員会の運営 5 第 2 章治験審査委員会事務局 6 治験審査委員会事務局の設置と業務 6 第 3 章記録の保存と公開 7 記録の保存責任者 7 記録の保存期間 7 記録の公開 8 1 第
治験は、医薬品として未だ認められていない物質を人(被験者)に投与して、有効性、安全性等を検討する臨床試験のことであり、新薬の承認申請資料の作成を目的としています
 このページでは 名古屋大学医学部附属病院において治験を実施する場合の手順を紹介しています ご不明な点がありましたら 臨床治験管理センターまでお問い合わせ下さい 治験責任医師の基本的な責務 治験責任医師は 治験に関連する医療上のすべての判断に責任を負う (GCP 第 45 条第 3 4 項 ) 治験責任医師は 治験依頼者と合意した治験実施計画書を遵守する (GCP 第 46 条第 1 項 ) 治験責任医師は
このページでは 名古屋大学医学部附属病院において治験を実施する場合の手順を紹介しています ご不明な点がありましたら 臨床治験管理センターまでお問い合わせ下さい 治験責任医師の基本的な責務 治験責任医師は 治験に関連する医療上のすべての判断に責任を負う (GCP 第 45 条第 3 4 項 ) 治験責任医師は 治験依頼者と合意した治験実施計画書を遵守する (GCP 第 46 条第 1 項 ) 治験責任医師は
目次 1. 平成 30 年改正対応 ( 平成 31 年 1 月リリース予定 ) (1) 改正内容 (2) 様式変更 (3) 画面イメージ (4) 帳票イメージ 1-2. 電子申告 (1) 様式変更 (2) メッセージボックスセキュリティ強化 (3) 納付手続き手順の変更 2. 注意事項 1
 ネット de 記帳 平成 30 年度申告対応版について 2019 年 1 月 9 日 目次 1. 平成 30 年改正対応 ( 平成 31 年 1 月リリース予定 ) (1) 改正内容 (2) 様式変更 (3) 画面イメージ (4) 帳票イメージ 1-2. 電子申告 (1) 様式変更 (2) メッセージボックスセキュリティ強化 (3) 納付手続き手順の変更 2. 注意事項 1 (1) 改正内容 平成
ネット de 記帳 平成 30 年度申告対応版について 2019 年 1 月 9 日 目次 1. 平成 30 年改正対応 ( 平成 31 年 1 月リリース予定 ) (1) 改正内容 (2) 様式変更 (3) 画面イメージ (4) 帳票イメージ 1-2. 電子申告 (1) 様式変更 (2) メッセージボックスセキュリティ強化 (3) 納付手続き手順の変更 2. 注意事項 1 (1) 改正内容 平成
<4D F736F F D A7790B A F838D815B836F838B91CE899E8A438A4F97AF8A E815B CC295CA905C90BF814097AF8A CA944692E882CC97AC82EA>
 グローバル人材育成特別コース 留学 単位認定 ( 個別申請 ) 手続 グローバル人材育成院のグローバル人材育成特別コース単位認定対象プログラムリストに掲載のないプログラムに参加して, グローバル人材育成特別コースの単位の修得を希望する場合は, 必ず事前に申請が必要なのでご注意ください グローバル 材育成特別コースで単位認定の対象となる科 グローバル海外短期実習 1 単位 グローバル対応海外留学 インターンシップ(
グローバル人材育成特別コース 留学 単位認定 ( 個別申請 ) 手続 グローバル人材育成院のグローバル人材育成特別コース単位認定対象プログラムリストに掲載のないプログラムに参加して, グローバル人材育成特別コースの単位の修得を希望する場合は, 必ず事前に申請が必要なのでご注意ください グローバル 材育成特別コースで単位認定の対象となる科 グローバル海外短期実習 1 単位 グローバル対応海外留学 インターンシップ(
内容 1. はじめに 大規模治験ネットワーク登録医療機関への支援内容 治験実施医療機関情報の登録と公開 登録の条件 事前確認 大規模治験ネットワーク への登録方法 登録の手順 登録でき
 大規模治験ネットワーク 登録マニュアル Ver1.1 2013/4/1 公益社団法人日本医師会治験促進センター 0 内容 1. はじめに... 2 2. 大規模治験ネットワーク登録医療機関への支援内容... 2 3. 治験実施医療機関情報の登録と公開... 3 4. 登録の条件... 4 5. 事前確認... 5 6. 大規模治験ネットワーク への登録方法... 6 6-1 登録の手順... 6 6-2
大規模治験ネットワーク 登録マニュアル Ver1.1 2013/4/1 公益社団法人日本医師会治験促進センター 0 内容 1. はじめに... 2 2. 大規模治験ネットワーク登録医療機関への支援内容... 2 3. 治験実施医療機関情報の登録と公開... 3 4. 登録の条件... 4 5. 事前確認... 5 6. 大規模治験ネットワーク への登録方法... 6 6-1 登録の手順... 6 6-2
医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年
![医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年 医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年](/thumbs/91/107149459.jpg) 事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
1. 会員情報の照会 / 変更 ご登録の 会員情報 の確認および変更できます (1) 左側のサブメニューで [ 基本情報 ] を選択すると お客様の基本情報が表示します (1) (2) [ 変更 ] [ ご登録回線の確認 / 変更 ] [ ログイン ID/ ログインパスワードの変更 ] [Web ビ
![1. 会員情報の照会 / 変更 ご登録の 会員情報 の確認および変更できます (1) 左側のサブメニューで [ 基本情報 ] を選択すると お客様の基本情報が表示します (1) (2) [ 変更 ] [ ご登録回線の確認 / 変更 ] [ ログイン ID/ ログインパスワードの変更 ] [Web ビ 1. 会員情報の照会 / 変更 ご登録の 会員情報 の確認および変更できます (1) 左側のサブメニューで [ 基本情報 ] を選択すると お客様の基本情報が表示します (1) (2) [ 変更 ] [ ご登録回線の確認 / 変更 ] [ ログイン ID/ ログインパスワードの変更 ] [Web ビ](/thumbs/91/106240086.jpg) Web ビリングご利用ガイド ( 4 会員情報の変更 編 ) 本書は NTT ファイナンスが提供している Web ビリングサービスのご利用方法をご案内しております お客さまのお支払い方法等によっては 実際の画面と異なる場合がございますので ご注意ください 会員情報の変更 編もくじ 1. 会員情報の照会 / 変更 4-1 2. 連絡先電話番号変更 4-2 3. 照会する回線の追加 廃止 4-3 4.
Web ビリングご利用ガイド ( 4 会員情報の変更 編 ) 本書は NTT ファイナンスが提供している Web ビリングサービスのご利用方法をご案内しております お客さまのお支払い方法等によっては 実際の画面と異なる場合がございますので ご注意ください 会員情報の変更 編もくじ 1. 会員情報の照会 / 変更 4-1 2. 連絡先電話番号変更 4-2 3. 照会する回線の追加 廃止 4-3 4.
静岡県立静岡がんセンター臨床研究事務局の業務手順書
 治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 6.0 平成 20 年 1 月 28
治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 6.0 平成 20 年 1 月 28
eRequest - Frequently Asked Questions
 2018 年度 UCBJ 研究支援申請方法 1. 趣旨 ユーシービージャパン株式会社 ( 以下 UCBJ ) は 革新的な医薬品を開発し 患者の皆様の治療に貢献するとともに 医学 薬学領域の学術研究活動を支援いたします UCBJ は 2017 年から研究支援の公募を開始いたしました 患者の皆様にとって有益な治療につながる革新的で独創性のある研究に対して 研究支援金 ( 以下 支援金 ) の拠出をもって支援いたします
2018 年度 UCBJ 研究支援申請方法 1. 趣旨 ユーシービージャパン株式会社 ( 以下 UCBJ ) は 革新的な医薬品を開発し 患者の皆様の治療に貢献するとともに 医学 薬学領域の学術研究活動を支援いたします UCBJ は 2017 年から研究支援の公募を開始いたしました 患者の皆様にとって有益な治療につながる革新的で独創性のある研究に対して 研究支援金 ( 以下 支援金 ) の拠出をもって支援いたします
 本人確認資料について ( 変更 ) 当社での手続きの際に本人確認資料の有効期限が切れていた場合 お受けできません ご確認のうえお送りください ご提出資料の有効性を確認するため 発行元の名称や登録番号など すべての情報が確認できる状態でご用意ください 1 運転免許証 ( コピー ) 住所変更をご依頼のお客さま ご用意いただくコピー おもて面 変更内容の記載がある場合はうら面も必要 ( うら面 ) (1)
本人確認資料について ( 変更 ) 当社での手続きの際に本人確認資料の有効期限が切れていた場合 お受けできません ご確認のうえお送りください ご提出資料の有効性を確認するため 発行元の名称や登録番号など すべての情報が確認できる状態でご用意ください 1 運転免許証 ( コピー ) 住所変更をご依頼のお客さま ご用意いただくコピー おもて面 変更内容の記載がある場合はうら面も必要 ( うら面 ) (1)
Microsoft PowerPoint - 【e-Rad設定】研究者用(H30年度)二次新システム未対応
 厚生労働科学研究費補助金の応募に係る 府省共通研究開発管理システム (e-rad) への 入力方法について < 注意事項 > e-radは平成 30 年 2 月 28 日 ( 水 ) から 新システムに移行しました ユーザビリティ改善の観点から 画面デザイン メニュー構成等が全面的に刷新されました 新システムのマニュアルは e-radポータルサイトに掲載しています 主な変更点についても記載しておりますので
厚生労働科学研究費補助金の応募に係る 府省共通研究開発管理システム (e-rad) への 入力方法について < 注意事項 > e-radは平成 30 年 2 月 28 日 ( 水 ) から 新システムに移行しました ユーザビリティ改善の観点から 画面デザイン メニュー構成等が全面的に刷新されました 新システムのマニュアルは e-radポータルサイトに掲載しています 主な変更点についても記載しておりますので
Microsoft PowerPoint - 統合版
 登録申請関係 新規登録申請書 P.3 更新登録申請書 P.3 ( 新規登録と更新登録は同じ様式を使用します ) 添付書類 誓約書 P.8 実務経験者等証明書 P.9 証拠書類 ( 上記証明書とセット ) 業務経歴書 P.10 又は賃貸不動産経営管理士証の写し のうち 該当するもの その他の添付書類 賃貸住宅管理業の登録について の表 1 でご確認ください P.20 申請書等記入例 ( 近畿地方整備局長提出版
登録申請関係 新規登録申請書 P.3 更新登録申請書 P.3 ( 新規登録と更新登録は同じ様式を使用します ) 添付書類 誓約書 P.8 実務経験者等証明書 P.9 証拠書類 ( 上記証明書とセット ) 業務経歴書 P.10 又は賃貸不動産経営管理士証の写し のうち 該当するもの その他の添付書類 賃貸住宅管理業の登録について の表 1 でご確認ください P.20 申請書等記入例 ( 近畿地方整備局長提出版
 横浜市市民利用施設 予約システムガイドブック スポーツ施設編 予約システムについての問い合わせ先 インターネット 電話の操作方法 利用者登録についてはこちらへお問い合わせください 横浜市市民利用施設予約システムサービスセンター 220-0004 西区北幸 2-6-26 HI 横浜ビル 5F 759-3737 FAX 329-1368 お問い合わせは9:00~17:00( 年末年始を除く ) eメール
横浜市市民利用施設 予約システムガイドブック スポーツ施設編 予約システムについての問い合わせ先 インターネット 電話の操作方法 利用者登録についてはこちらへお問い合わせください 横浜市市民利用施設予約システムサービスセンター 220-0004 西区北幸 2-6-26 HI 横浜ビル 5F 759-3737 FAX 329-1368 お問い合わせは9:00~17:00( 年末年始を除く ) eメール
はじめに 本マニュアルでは ふじのくに電子申請サービス手続き案内記載画面 申請画面へのアクセス方法と 電子申請 ( 画面入力 ) を行う際の留意事項についてご案内します ふじのくに電子申請サービスページURL < ( 静岡県
 静岡県入札参加資格電子申請マニュアル 平成 30 31 年度建設関連業務 ( 定期受付 ) 1 はじめに 本マニュアルでは ふじのくに電子申請サービス手続き案内記載画面 申請画面へのアクセス方法と 電子申請 ( 画面入力 ) を行う際の留意事項についてご案内します ふじのくに電子申請サービスページURL ( 静岡県のホームページ内の左側
静岡県入札参加資格電子申請マニュアル 平成 30 31 年度建設関連業務 ( 定期受付 ) 1 はじめに 本マニュアルでは ふじのくに電子申請サービス手続き案内記載画面 申請画面へのアクセス方法と 電子申請 ( 画面入力 ) を行う際の留意事項についてご案内します ふじのくに電子申請サービスページURL ( 静岡県のホームページ内の左側
過誤申立書のみで結構です Q7. 過誤申立手続きが可能なのは 何か月前の利用分までですか? A7. 再請求の有無や再請求する額の増減によって異なります 各区 支所の介護医療係または神戸市役所介護保険課保険事業係にご相談ください Q8. 今月 10 日に提出したレセプト ( 介護給付費明細書 ) に入
 過誤申立には大きく2 種類の方法があります 一般の過誤を 通常過誤 と言い もうひとつを 同月過誤 と言います 神戸市では 通常過誤 を原則としています 同月過誤 の詳細 資料については 神戸市役所介護保険課保険事業係 (078-322-6323) にお問い合わせください 以下に 通常過誤 に関して よくご質問いただく内容を掲載します 手続きの際 の参考としてください 通常過誤申立に関する Q&A
過誤申立には大きく2 種類の方法があります 一般の過誤を 通常過誤 と言い もうひとつを 同月過誤 と言います 神戸市では 通常過誤 を原則としています 同月過誤 の詳細 資料については 神戸市役所介護保険課保険事業係 (078-322-6323) にお問い合わせください 以下に 通常過誤 に関して よくご質問いただく内容を掲載します 手続きの際 の参考としてください 通常過誤申立に関する Q&A
綾瀬市家具転倒防止器具等設置費助成事業実施要綱 ( 目的 ) 第 1 条この要綱は 家具転倒防止器具等 ( 以下 器具等 という ) を取付けることが困難な世帯が 家庭内において所有する家具に器具等を取付ける事により これらの世帯の者の生命及び財産を地震災害から守る一助とし 併せてその費用の助成を行
 綾瀬市家具転倒防止器具等設置費助成事業実施要綱 ( 目的 ) 第 1 条この要綱は 家具転倒防止器具等 ( 以下 器具等 という ) を取付けることが困難な世帯が 家庭内において所有する家具に器具等を取付ける事により これらの世帯の者の生命及び財産を地震災害から守る一助とし 併せてその費用の助成を行うことにより 福祉の向上を図ることを目的とする ( 対象世帯 ) 第 2 条この要綱により器具等の取付け及び費用の助成を受けることができる世帯は
綾瀬市家具転倒防止器具等設置費助成事業実施要綱 ( 目的 ) 第 1 条この要綱は 家具転倒防止器具等 ( 以下 器具等 という ) を取付けることが困難な世帯が 家庭内において所有する家具に器具等を取付ける事により これらの世帯の者の生命及び財産を地震災害から守る一助とし 併せてその費用の助成を行うことにより 福祉の向上を図ることを目的とする ( 対象世帯 ) 第 2 条この要綱により器具等の取付け及び費用の助成を受けることができる世帯は
Ver 年 10 月 15 日 改訂履歴 版数 改訂 年月日 改訂 頁 改訂内容 年 3 月 19 日 - 初版作成 年 6 月 12 日 4~ 手順の細分化 年 8 月 21 日 9, 13 複数研究対応に関する内容の追加 1
 臨床研究実施計画 研究概要公開システム 操作マニュアル 登録者編 Ver.1.3 2018 年 10 月 15 日 改訂履歴 版数 改訂 年月日 改訂 頁 改訂内容 1.0 2018 年 3 月 19 日 - 初版作成 1.1 2018 年 6 月 12 日 4~ 手順の細分化 1.2 2018 年 8 月 21 日 9, 13 複数研究対応に関する内容の追加 1.3 2018 年 10 月 15
臨床研究実施計画 研究概要公開システム 操作マニュアル 登録者編 Ver.1.3 2018 年 10 月 15 日 改訂履歴 版数 改訂 年月日 改訂 頁 改訂内容 1.0 2018 年 3 月 19 日 - 初版作成 1.1 2018 年 6 月 12 日 4~ 手順の細分化 1.2 2018 年 8 月 21 日 9, 13 複数研究対応に関する内容の追加 1.3 2018 年 10 月 15
平成 30 年度 CO2 削減ポテンシャル診断事業 精算払請求書 記入例 一般社団法人低炭素エネルギー技術事業組合
 平成 30 年度 CO2 削減ポテンシャル診断事業 精算払請求書 記入例 精算払請求書の提出の流れ 受診事業所 送付 ( メール及び原本郵送 ) 組合 ( 受診窓口 ) 様式第 2 交付額確定通知 様式第 3 精算払請求書事前提示 押印前のものをメール添付により送付 様式第 3 精算払請求書原本送付依頼 ( メール ) 確認 様式第 3 精算払請求書原本提出 配送記録が残る方法により送付 確認 補助金交付
平成 30 年度 CO2 削減ポテンシャル診断事業 精算払請求書 記入例 精算払請求書の提出の流れ 受診事業所 送付 ( メール及び原本郵送 ) 組合 ( 受診窓口 ) 様式第 2 交付額確定通知 様式第 3 精算払請求書事前提示 押印前のものをメール添付により送付 様式第 3 精算払請求書原本送付依頼 ( メール ) 確認 様式第 3 精算払請求書原本提出 配送記録が残る方法により送付 確認 補助金交付
untitled
 INDEX April. 2013 No.113 Contents 2.20 WED 2.16 SAT T opics! Aizawa Event Calendar 5 May TUE 5.14 TUE 5.28 TUE 6.11 6 13 20 27 5 12 19 26 7 14 21 28 1 8 15 22 29 2 9 16 23 30 3 10 17 24 31 4 11 18 25 MON
INDEX April. 2013 No.113 Contents 2.20 WED 2.16 SAT T opics! Aizawa Event Calendar 5 May TUE 5.14 TUE 5.28 TUE 6.11 6 13 20 27 5 12 19 26 7 14 21 28 1 8 15 22 29 2 9 16 23 30 3 10 17 24 31 4 11 18 25 MON
国立がんセンター受託研究取扱規程
 平成 22 年 4 月 1 日規程第 31 号 国立研究開発法人国立がん研究センター受託研究取扱規程 第 1 版平成 22 年 4 月 1 日第 2 版平成 22 年 10 月 1 日第 3 版平成 23 年 4 月 1 日第 4 版平成 24 年 4 月 1 日第 5 版平成 24 年 7 月 1 日第 6 版平成 25 年 4 月 1 日第 7 版平成 27 年 4 月 1 日 ( 通則 ) 第
平成 22 年 4 月 1 日規程第 31 号 国立研究開発法人国立がん研究センター受託研究取扱規程 第 1 版平成 22 年 4 月 1 日第 2 版平成 22 年 10 月 1 日第 3 版平成 23 年 4 月 1 日第 4 版平成 24 年 4 月 1 日第 5 版平成 24 年 7 月 1 日第 6 版平成 25 年 4 月 1 日第 7 版平成 27 年 4 月 1 日 ( 通則 ) 第
平成 28 年 4 月版 別紙様式 3 研究に係る利益相反状況申告書 Q&A Q1. 学内研究分担者等の氏名 Q1-1 Q1-2 Q1-3 Q1-4 質問学外の研究分担者名を記載しなくてもよいのですか? 学内研究分担者等 というのは どのような人をいうのですか? モニタリング 監査とはどのようなもの
 別紙様式 3 研究に係る利益相反状況申告書 Q&A Q1. 学内研究分担者等の氏名 Q1-1 Q1-2 Q1-3 Q1-4 質問学外の研究分担者名を記載しなくてもよいのですか? 学内研究分担者等 というのは どのような人をいうのですか? モニタリング 監査とはどのようなものですか? 欄が足りない場合はどうすればよいですか? 回答記載する必要はありません ただし その研究者が本学において研究を実施する場合には記載してください
別紙様式 3 研究に係る利益相反状況申告書 Q&A Q1. 学内研究分担者等の氏名 Q1-1 Q1-2 Q1-3 Q1-4 質問学外の研究分担者名を記載しなくてもよいのですか? 学内研究分担者等 というのは どのような人をいうのですか? モニタリング 監査とはどのようなものですか? 欄が足りない場合はどうすればよいですか? 回答記載する必要はありません ただし その研究者が本学において研究を実施する場合には記載してください
( 委員会の業務 ) 第 4 条委員会は その責務の遂行のために以下の最新資料を病院長から入手する なお あらかじめ 自ら治験を実施する者 委員会及び病院長の合意が得られている場合においては GCP 省令第 26 条の6 第 2 項に関する通知に限り 自ら治験を実施する者から入手することができる ま
 秋田大学医学部附属病院医師主導治験における治験審査委員会規程 第 1 章医師主導治験審査委員会 ( 目的と適用範囲 ) 第 1 条本規程は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 医薬品の臨床試験の実施の基準に関する省令( 平成 9 年 3 月 27 日厚生省令第 28 号 )( 以下 GCP 省令 という ) 並びにGCP 省令に関連する通知書等に基づいて
秋田大学医学部附属病院医師主導治験における治験審査委員会規程 第 1 章医師主導治験審査委員会 ( 目的と適用範囲 ) 第 1 条本規程は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 医薬品の臨床試験の実施の基準に関する省令( 平成 9 年 3 月 27 日厚生省令第 28 号 )( 以下 GCP 省令 という ) 並びにGCP 省令に関連する通知書等に基づいて
マニュアル ( 共通編 ) 改訂 パスワード の再設定をします 手順 ホームページより ログイン名 パスワードがわからない をクリックします URL ログイン名 パスワードがわからない をクリックします 請求書送付先作成 Copyri
 マニュアル ( 共通編 ) 206.09.05 改訂 にログイン ( ) ができなくなった この章では にログイン ( ) ができなくなった時の対処方法を説明します 区分別にログイン ( ) ができなくなる理由として以下の場合が考えられます ログイン名 を忘れた場合 責任者 ログイン名の再発行 をおこないます 詳しい手順は以下を参照ください 参照 登録者 作成者 閲覧者 責任者 が 登録権限 作成権限
マニュアル ( 共通編 ) 206.09.05 改訂 にログイン ( ) ができなくなった この章では にログイン ( ) ができなくなった時の対処方法を説明します 区分別にログイン ( ) ができなくなる理由として以下の場合が考えられます ログイン名 を忘れた場合 責任者 ログイン名の再発行 をおこないます 詳しい手順は以下を参照ください 参照 登録者 作成者 閲覧者 責任者 が 登録権限 作成権限




