CROCO について
|
|
|
- わんど なかきむら
- 5 years ago
- Views:
Transcription
1 CROCO について
2 CROCO とは コース 正式名称 Clinical Research Online Professional Certification Program at Osaka University といい 大阪大学医学部附属病院が提供する 臨床研究に関する教育の e-learning サイトです 臨床研究を実施する研究者 専門職の方 倫理審査委員会の委員 事務局の方を対象に 臨床研究に必要な情報 知識を幅広く 豊富なコースで提供しております 詳しくは CROCO コース 一覧をご覧ください 受講管理 e-learning の受講履歴以外にもご自身が受講した教育 研修の履歴登録 管理が可能です 修了証 コースごとに修了証が発行されます
3 2018 年度大阪大学医学部附属病院臨床研究 治験研究者研修要件 大阪大学大学院医学系研究科 医学部および大阪大学医学部附属病院所属で臨床研究 ( 臨床研究法準拠を含む ) 治験 再生医療 疫学研究等 人を対象とする医学系研究を実施する研究責任者 研究分担者は 受講が必須です 受講内容 導入教育研修対象者 ( 大阪大学で初めて研究を実施する者 ) < 研究開始までに受講すべき内容 > CROCO 基礎編より 従事する研究に該当するコースを受講修了すること 介入試験研究者コース: 約 7 時間 観察研究研究者コース: 約 3 時間 治験研究者コース : 約 6 時間 再生研究者コース : 約 5 時間 臨床研究における研究不正と行動規範 を受講修了すること 詳細は CROCOコース 一覧の 臨床研究における研究不正と行動規範 をご確認ください 平成 29 年 3 月臨時臨床研究講習会コース~ 統合指針改正への対応 ~ のうち 統合指針改正への対応-1 を受講すること 臨床研究法準拠の研究を実施する場合は CROCO 更新編の 臨床研究法 ( 研究者コース内 ) も受講すること <2019 年 3 月末までに受講すべき内容 > 以下の臨床研究講習会を受講すること臨床研究の留意点 (60 分 ) 2018 年度後半に実施予定 継続教育研修対象者 (2017 年度に左記導入教育研修を修了した者 ) <2019 年 3 月末までに受講すべき内容 > 30 分のを 1 ポイントとし 従事する研究に該当する下表のポイントを取得すること ポイント数は対象等に提示 従事する研究 臨床研究法介入試験 ( 統合指針 ) 治験再生医療等 観察研究 ( 統合指針 ) 必要ポイント数 8 ポイント 4 ポイント ポイント対象の e-learning 講習会 セミナーなど CROCO 更新編の 臨床研究講習会 GCP セミナー モニタリング講習 その他研究倫理関連の CROCO 更新編 臨床研究法 橋渡し研究について プロジェクトマネジメント 統計( アンケート調査の方法 ) 統計( 中間解析 ) リスクベーストモニタリングと中央モニタリング その1: 方法論編 リスクベーストモニタリングと中央モニタリング その2: 実践編 臨床研究における監査 医薬品開発におけるヒト初回投与試験 医師主導治験( 自ら治験を実施する者の治験の準備と管理 ) 臨床研究講習会 (60 分 :2ポイント) の受講は必須とし 上記ポイントに含めること 2018 年度後半に実施予定 注 ) 医学系研究科 医学部附属病院以外の所属の方は CROCO の受講は必須ではありません 他部局の方でも受講は可能ですが 臨床研究における研究不正と行動規範 のについては 各々の部局に研究倫理教育がある場合は それに従ってください
4 CROCO コース 一覧 ( 基礎編 ) 印 : 各コースの必須です 時間目安 ( 分 ) 人を対象とする医学系研究に関する倫理指針 ( 統合指針 ) 介入試験観察研究 コース治験再生医療等 研究者委員事務局研究者委員事務局研究者委員事務局研究者委員事務局 研究支援スタッフ (CRC CR A DM 監査 臨床研究の歴史と被験者保護 25 GCP-1 20 GCP-2 20 人を対象とする医学系研究に関する倫理指針 人を対象とする医学系研究に関する倫理指針 再生医療等の安全性の確保等に関する法律 25 倫理審査委員会 20 臨床研究の統計 臨床研究の統計 観察研究の統計 データマネジメント 30 臨床試験 ( 治験 ) の計画と準備 臨床試験 ( 治験 ) の計画と準備 臨床試験の実施 30 データマネジメント データマネジメント 品質管理 品質保証 30 医薬品 医療機器開発 25 人を対象とする医学系研究に関する倫理指針用語の定義人を対象とする医学系研究に関する倫理指針倫理審査委員会の役割 責務人を対象とする医学系研究に関する倫理指針研究実施のための体制 規程の整備治験に関する事務局業務事務局員 ( 実務担当者 ) 向き 治験審査委員会について治験審査委員会委員向き 30 認定再生医療等委員会の審査等業務について 新規申請 認定再生医療等委員会の審査等業務について 疾病等報告 定期報告等 臨床研究における研究不正と行動規範 は 以下のいずれかのプログラム 教材を受講してください 大阪大学大学院医学系研究科 医学部 大阪大学医学部附属病院に所属する方は APRIN eラーニングプログラム (9 単元 ) を受講してください 受講が完了されましたら CROCO 受講履歴 の CROCO 以外の受講履歴 に登録してください 既に受講が完了されている場合は 新たに受講する必要はございません APRIN e ラーニングプログラム (eaprin)( 年 10 月 1 日に CITI Japan より eaprin に名称変更されました 次の 9 単元を受講してください 責任ある研究行為について 研究における不正行為 データの扱い 共同研究のルール 臨床研究における研究不正と行動規範 - オーサーシップ 盗用 公的研究資金の取扱い 利益相反 研究における個人に関わる情報の取扱い APRIN eラーニングプログラムはeラーニングによる研究者行動規範教育を提供している登録制のサービスです 受講するためには 機関登録および受講者登録が必要となります 特定の機関に所属していない個人の方 および企業や病院 学会などに所属している方は有料です < 登録依頼先 > 大阪大学大学院医学系研究科 医学部に所属する方 教職員 総務課企画係 TEL: 学生 教務室教務係 TEL: 大阪大学医学部附属病院に所属する方 : 教育研究支援課総括係 TEL: 科学の健全な発展のために - 誠実な科学者の心得 - ( 日本学術振興会 科学の健全な発展のために 編集委員会 ) URL: どなたでも無料で受講できます
5 CROCO コース 一覧 ( 更新編 ) 付与 ポイント 数 時間目安 ( 分 ) 研究者コース 臨床研究法 橋渡し研究について 1 30 プロジェクトマネジメント 1 30 アンケート調査の方法 1 30 中間解析計画 実施段階で留意すべきこと 1 35 リスクベーストモニタリングと中央モニタリングその1: 方法論編 1 25 リスクベーストモニタリングと中央モニタリングその2: 実践編 1 20 臨床研究における監査 1 30 大阪大学大学院医学系研究科 医学部および大阪大学医学部附属病院所属で臨床研究 ( 臨床研究準拠を含む ) 治験 再生医療 疫学研究等 人を対象とする医学系研究を実施する方は 2018 年度大阪大学医学部附属病院臨床研究 治験研究者研修要件 の通り受講ください 医薬品開発におけるヒト初回投与試験 1 30 医師主導治験 ( 自ら治験を実施する者の治験の準備と管理 ) 1 30
Microsoft PowerPoint - 利用手引書_v2_ pptx
 臨床研究教育研修 受講管理システム 利用の手引き 慶應義塾大学病院臨床研究推進センター教育研修事務局 1 はじめに 受講管理システムとは? 臨床研究に関するセミナーへの申込や eラーニングコンテンツを受講するための 臨床研究に関する生涯学習 研修支援システムです URL https://education.ctr.hosp.keio.ac.jp/ 2 目次 ( 流れ ) 倫理審査申請資格の取得方法とその他各種研修会の受講方法
臨床研究教育研修 受講管理システム 利用の手引き 慶應義塾大学病院臨床研究推進センター教育研修事務局 1 はじめに 受講管理システムとは? 臨床研究に関するセミナーへの申込や eラーニングコンテンツを受講するための 臨床研究に関する生涯学習 研修支援システムです URL https://education.ctr.hosp.keio.ac.jp/ 2 目次 ( 流れ ) 倫理審査申請資格の取得方法とその他各種研修会の受講方法
平成 30 年度データマネジャー養成研修 研修生募集要項 主催千葉大学医学部附属病院実施千葉大学医学部附属病院臨床試験部 1. 研修の目的 ICH-GCP の改訂や CDISC(Clinical Data Interchange Standards Consortium) 標準の規格での PMDA
 平成 30 年度データマネジャー養成研修 研修生募集要項 主催千葉大学医学部附属病院実施千葉大学医学部附属病院臨床試験部 1. 研修の目的 ICH-GCP の改訂や CDISC(Clinical Data Interchange Standards Consortium) 標準の規格での PMDA への申請データの提出など 治験や臨床研究のデータ管理を取り巻く環境が変化しています その中で 臨床試験のデータの質の維持
平成 30 年度データマネジャー養成研修 研修生募集要項 主催千葉大学医学部附属病院実施千葉大学医学部附属病院臨床試験部 1. 研修の目的 ICH-GCP の改訂や CDISC(Clinical Data Interchange Standards Consortium) 標準の規格での PMDA への申請データの提出など 治験や臨床研究のデータ管理を取り巻く環境が変化しています その中で 臨床試験のデータの質の維持
特定臨床研究に関する手順書
 学校法人日本医科大学における特定臨床研究に関する手順書 ( 新規申請分 ) 1. 目的 本手順書は 学校法人日本医科大学における特定臨床研究に関する規程 ( 以下 規程 という ) を円滑に運用するために 本法人における手順を示すものである 2. 用語の定義 2.1 全般本手順書において使用する用語は 規程において使用する用語の例によるものとする 2.2 付属所属長規程第 5 条第 2 項により 理事長は実施医療機関の管理者の権限を次に定める付属所属長に委任しているため
学校法人日本医科大学における特定臨床研究に関する手順書 ( 新規申請分 ) 1. 目的 本手順書は 学校法人日本医科大学における特定臨床研究に関する規程 ( 以下 規程 という ) を円滑に運用するために 本法人における手順を示すものである 2. 用語の定義 2.1 全般本手順書において使用する用語は 規程において使用する用語の例によるものとする 2.2 付属所属長規程第 5 条第 2 項により 理事長は実施医療機関の管理者の権限を次に定める付属所属長に委任しているため
する 研究実施施設の環境 ( プライバシーの保護状態 ) について記載する < 実施方法 > どのような手順で研究を実施するのかを具体的に記載する アンケート等を用いる場合は 事前にそれらに要する時間を測定し 調査による患者への負担の度合いがわかるように記載する 調査手順で担当が複数名いる場合には
 参考 : 様式 2( 記載例 ) ( 研究責任者 ) ( 本会倫理審査委員会 ) 西暦年月日 研究計画書 ( 第版 ) 公益社団法人富山県薬剤師会倫理審査委員会委員長様 計画者 ( 研究責任者 ) 所属 : 職名 : 氏名 : 印 1. 研究の名称 : 2. 研究の実施体制 研究責任者名所属職名役割及び責任 薬局管理薬剤師 研究分担者名 所属 職名 役割及び責任 薬局 薬剤師 病院 科 病院薬剤部
参考 : 様式 2( 記載例 ) ( 研究責任者 ) ( 本会倫理審査委員会 ) 西暦年月日 研究計画書 ( 第版 ) 公益社団法人富山県薬剤師会倫理審査委員会委員長様 計画者 ( 研究責任者 ) 所属 : 職名 : 氏名 : 印 1. 研究の名称 : 2. 研究の実施体制 研究責任者名所属職名役割及び責任 薬局管理薬剤師 研究分担者名 所属 職名 役割及び責任 薬局 薬剤師 病院 科 病院薬剤部
( 委員会の業務 ) 第 4 条委員会は その責務の遂行のために以下の最新資料を病院長から入手する なお あらかじめ 自ら治験を実施する者 委員会及び病院長の合意が得られている場合においては GCP 省令第 26 条の6 第 2 項に関する通知に限り 自ら治験を実施する者から入手することができる ま
 秋田大学医学部附属病院医師主導治験における治験審査委員会規程 第 1 章医師主導治験審査委員会 ( 目的と適用範囲 ) 第 1 条本規程は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 医薬品の臨床試験の実施の基準に関する省令( 平成 9 年 3 月 27 日厚生省令第 28 号 )( 以下 GCP 省令 という ) 並びにGCP 省令に関連する通知書等に基づいて
秋田大学医学部附属病院医師主導治験における治験審査委員会規程 第 1 章医師主導治験審査委員会 ( 目的と適用範囲 ) 第 1 条本規程は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 医薬品の臨床試験の実施の基準に関する省令( 平成 9 年 3 月 27 日厚生省令第 28 号 )( 以下 GCP 省令 という ) 並びにGCP 省令に関連する通知書等に基づいて
研修プログラム関係 Q_ 副分野の研修は 30 時間程度となっています これは 30 時間を超える必要があるという意味でし ょうか A_ 時間は目安です 各プログラムで十分な研修効果が上がることを前提に 研修を計画してください Q_ 研修プログラムの実施状況について 協会への報告が求められるのでしょ
 研修プログラム関係 Q_ 副分野の研修は 30 時間程度となっています これは 30 時間を超える必要があるという意味でし ょうか A_ 時間は目安です 各プログラムで十分な研修効果が上がることを前提に 研修を計画してください Q_ 研修プログラムの実施状況について 協会への報告が求められるのでしょうか A_ 年に 1 回 プログラムの実績報告と専攻医の研修記録を提出していただきます 報告の締切りは
研修プログラム関係 Q_ 副分野の研修は 30 時間程度となっています これは 30 時間を超える必要があるという意味でし ょうか A_ 時間は目安です 各プログラムで十分な研修効果が上がることを前提に 研修を計画してください Q_ 研修プログラムの実施状況について 協会への報告が求められるのでしょうか A_ 年に 1 回 プログラムの実績報告と専攻医の研修記録を提出していただきます 報告の締切りは
平成29年度 第1回 臨床研究に関する研修会
 平成 29 年度臨床研究に関する研修会 1 臨床研究とは 人を対象とする医学系研究 人 ( 試料 情報を含む ) を対象として 疾病の成因及び病態の理解並びに疾病の予防方法並びに医療における診断方法及び治療方法の改善又は有効性の検証を通じて 国民の健康の保持増進又は患者の疾病からの回復若しくは生活の質の向上に資する知識を得ることを目的として実施される活動をいう 2 指針の対象になる研究 個人の健康に関する情報を用いた疫学的手法による研究
平成 29 年度臨床研究に関する研修会 1 臨床研究とは 人を対象とする医学系研究 人 ( 試料 情報を含む ) を対象として 疾病の成因及び病態の理解並びに疾病の予防方法並びに医療における診断方法及び治療方法の改善又は有効性の検証を通じて 国民の健康の保持増進又は患者の疾病からの回復若しくは生活の質の向上に資する知識を得ることを目的として実施される活動をいう 2 指針の対象になる研究 個人の健康に関する情報を用いた疫学的手法による研究
医師主導治験取扱要覧
 15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
<4D F736F F D A835E838A F8B7982D18AC48DB85F20534F A68CEB8E9A E9A8F4390B38DCF2
 自治医科大学人を対象とした医学系研究に関するモニタリング及び監査の標準業務手順書 ver.1.0(2015 年 5 月 15 日 ) 1. 目的等 1) 目的 (1) 本手順書は 自治医科大学の教職員が 人を対象とする医学系研究に関する倫理指針 ( 平成 26 年文部科学省 厚生労働省告示第 3 号 ) 及び指針告示に伴う通知ならびにガイダンス ( 以下 指針 指針告示に伴う通知及びガイダンスを合わせて
自治医科大学人を対象とした医学系研究に関するモニタリング及び監査の標準業務手順書 ver.1.0(2015 年 5 月 15 日 ) 1. 目的等 1) 目的 (1) 本手順書は 自治医科大学の教職員が 人を対象とする医学系研究に関する倫理指針 ( 平成 26 年文部科学省 厚生労働省告示第 3 号 ) 及び指針告示に伴う通知ならびにガイダンス ( 以下 指針 指針告示に伴う通知及びガイダンスを合わせて
手順書03
 杏林大学医学部倫理委員会 人を対象とする医学系研究に関する業務手順書 ➂ 研究計画書の作成等に関する手続等 1 はじめに本手順書は 杏林大学医学部倫理委員会規程に基づき 杏林大学医学部及び医学部付属病院の専任教職員が行う人を対象とした医学系研究について 医の倫理に関するヘルシンキ宣言の趣旨に添い 人を対象とする医学系研究に関する倫理指針及び その他関連通知に基づいて適正かつ円滑に行われるよう これらの研究等に係る必要な手順を定めるものである
杏林大学医学部倫理委員会 人を対象とする医学系研究に関する業務手順書 ➂ 研究計画書の作成等に関する手続等 1 はじめに本手順書は 杏林大学医学部倫理委員会規程に基づき 杏林大学医学部及び医学部付属病院の専任教職員が行う人を対象とした医学系研究について 医の倫理に関するヘルシンキ宣言の趣旨に添い 人を対象とする医学系研究に関する倫理指針及び その他関連通知に基づいて適正かつ円滑に行われるよう これらの研究等に係る必要な手順を定めるものである
平成 28 年 4 月版 別紙様式 3 研究に係る利益相反状況申告書 Q&A Q1. 学内研究分担者等の氏名 Q1-1 Q1-2 Q1-3 Q1-4 質問学外の研究分担者名を記載しなくてもよいのですか? 学内研究分担者等 というのは どのような人をいうのですか? モニタリング 監査とはどのようなもの
 別紙様式 3 研究に係る利益相反状況申告書 Q&A Q1. 学内研究分担者等の氏名 Q1-1 Q1-2 Q1-3 Q1-4 質問学外の研究分担者名を記載しなくてもよいのですか? 学内研究分担者等 というのは どのような人をいうのですか? モニタリング 監査とはどのようなものですか? 欄が足りない場合はどうすればよいですか? 回答記載する必要はありません ただし その研究者が本学において研究を実施する場合には記載してください
別紙様式 3 研究に係る利益相反状況申告書 Q&A Q1. 学内研究分担者等の氏名 Q1-1 Q1-2 Q1-3 Q1-4 質問学外の研究分担者名を記載しなくてもよいのですか? 学内研究分担者等 というのは どのような人をいうのですか? モニタリング 監査とはどのようなものですか? 欄が足りない場合はどうすればよいですか? 回答記載する必要はありません ただし その研究者が本学において研究を実施する場合には記載してください
標準業務手順 目次
 浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
一般財団法人公正研究推進協会 (APRIN) CITI Japan e ラーニングアカウント登録 受講手順 ( 個人受講 ) 1. お申込み まずは一般財団法人公正研究推進協会 (APRIN) のホームページより 個人会員のお申込みを行ってください 個人会員お申込みページ (
 一般財団法人公正研究推進協会 (APRIN) CITI Japan e ラーニングアカウント登録 受講手順 ( 個人受講 ) 1. お申込み まずは一般財団法人公正研究推進協会 (APRIN) のホームページより 個人会員のお申込みを行ってください 個人会員お申込みページ (https://www.aprin.or.jp/entry4) 2. アカウント登録 (1) お申込み後 ご登録メールアドレス宛に
一般財団法人公正研究推進協会 (APRIN) CITI Japan e ラーニングアカウント登録 受講手順 ( 個人受講 ) 1. お申込み まずは一般財団法人公正研究推進協会 (APRIN) のホームページより 個人会員のお申込みを行ってください 個人会員お申込みページ (https://www.aprin.or.jp/entry4) 2. アカウント登録 (1) お申込み後 ご登録メールアドレス宛に
JCROA自主ガイドライン第4版案 GCP監査WG改訂案及び意見
 受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
臨床研究に関する研修会1
 臨床研究に関する研修会 Ⅱ 長崎大学病院臨床研究センター 平成 27 年 9 月 24 日 倫理委員会申請時の注意点 臨床研究センター 副センター長福島千鶴 e-learning の受講 研究を申請する研究者及び 研究分担者は 申請前に必ず e-learning を受講して下さい CITI JAPAN プロジェクト ( 医学研究者標準コース ) 所属関係なし 研究責任者は研究分担者の受講状況を確認の上
臨床研究に関する研修会 Ⅱ 長崎大学病院臨床研究センター 平成 27 年 9 月 24 日 倫理委員会申請時の注意点 臨床研究センター 副センター長福島千鶴 e-learning の受講 研究を申請する研究者及び 研究分担者は 申請前に必ず e-learning を受講して下さい CITI JAPAN プロジェクト ( 医学研究者標準コース ) 所属関係なし 研究責任者は研究分担者の受講状況を確認の上
<4D F736F F D208EA18CB182C98AD682B782E995578F808BC696B18EE88F878F E38E748EE593B1816A E7B8D732E646F637
 治験に関する標準業務手順書 ( 医師主導治験 ) 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医師主導治験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 (
治験に関する標準業務手順書 ( 医師主導治験 ) 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医師主導治験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 (
臨床研究に関する標準業務手順書
 臨床研究に関する標準業務手順書 2018/04/01 第 15 版 改定履歴 日付 版 改定理由 改定箇所 内容 2010/02/06 1 新規制定 2010/04/14 2 COI 関連手順の明確化 フローチャートに COI に関する手順の追記 2010/08/19 3 様式 必要書類の追加 COI 関連様式の追記 安全性に関する報告の手順および様式 ( 様式 11) の追加 委託研究に関する手順
臨床研究に関する標準業務手順書 2018/04/01 第 15 版 改定履歴 日付 版 改定理由 改定箇所 内容 2010/02/06 1 新規制定 2010/04/14 2 COI 関連手順の明確化 フローチャートに COI に関する手順の追記 2010/08/19 3 様式 必要書類の追加 COI 関連様式の追記 安全性に関する報告の手順および様式 ( 様式 11) の追加 委託研究に関する手順
<4D F736F F F696E74202D2089D489AA90E690B C835B8393>
 ARO と製薬企業による産学連携の 現在と未来 千葉大学医学部附属病院花岡英紀 概略 大学における臨床研究とは何か? 大学の本質とその活用のあり方 具体的な連携事案 大学における臨床研究とは何か? 人の資料を用いた研究 遺伝子解析 疫学研究 ( 観察研究 横断研究 ) 介入試験 仮説の設定 科学性 倫理性 症例の組み入れ 利益相反 副次解析 症例報告書の作成 データの保管 モニタリング 統計解析 監査
ARO と製薬企業による産学連携の 現在と未来 千葉大学医学部附属病院花岡英紀 概略 大学における臨床研究とは何か? 大学の本質とその活用のあり方 具体的な連携事案 大学における臨床研究とは何か? 人の資料を用いた研究 遺伝子解析 疫学研究 ( 観察研究 横断研究 ) 介入試験 仮説の設定 科学性 倫理性 症例の組み入れ 利益相反 副次解析 症例報告書の作成 データの保管 モニタリング 統計解析 監査
なお モニタリングの実務経験がない方で 以下の資格を有している方は 原則 2 講義 ( 初級編 ) か らご参加いただきますようお願いいたします CRC 経験 2 年以上 SMONA 公認 CRC 日本 CRO 協会 CRA 日本 SMO 協会公認 CRC SoCRA 公認 CRP JSCTR 認定
 主催 / [ 日本医療研究開発機構文部科学省 ] 橋渡し研究戦略的推進プログラム拠点間ネットワークモニタリングに係る取組ワーキンググループ共催 / 一般社団法人日本臨床試験学会 平成 30 年度初級モニター研修会募集要項 1. 目的 国立研究開発法人日本医療研究開発機構文部科学省橋渡し研究戦略的推進プログラム拠点間ネットワークモニタリングに係る取組 ( 代表東北大学病院臨床試験データセンター / 東北大学大学院医学系研究科医学統計学分野山口拓洋
主催 / [ 日本医療研究開発機構文部科学省 ] 橋渡し研究戦略的推進プログラム拠点間ネットワークモニタリングに係る取組ワーキンググループ共催 / 一般社団法人日本臨床試験学会 平成 30 年度初級モニター研修会募集要項 1. 目的 国立研究開発法人日本医療研究開発機構文部科学省橋渡し研究戦略的推進プログラム拠点間ネットワークモニタリングに係る取組 ( 代表東北大学病院臨床試験データセンター / 東北大学大学院医学系研究科医学統計学分野山口拓洋
新 e ラーニングシステム APRIN e ラーニングプログラム (CITI Japan) での管理体制例と管理者区分 2
 APRIN e ラーニングプログラム (CITI Japan) について APRIN e ラーニングプログラム (CITI Japan) 説明資料 一般財団法人公正研究推進協会 (APRIN) 平成 29 年 9 月 15 日 (10 月 23 日改 ) 1 新 e ラーニングシステム APRIN e ラーニングプログラム (CITI Japan) での管理体制例と管理者区分 2 維持機関会員制度と各機関における
APRIN e ラーニングプログラム (CITI Japan) について APRIN e ラーニングプログラム (CITI Japan) 説明資料 一般財団法人公正研究推進協会 (APRIN) 平成 29 年 9 月 15 日 (10 月 23 日改 ) 1 新 e ラーニングシステム APRIN e ラーニングプログラム (CITI Japan) での管理体制例と管理者区分 2 維持機関会員制度と各機関における
倫理審査電子申請システム
 山梨大学医学部 倫理審査電子申請システム 利用ガイド 平成 27 年 11 月版 目 次 1 システムの利用準備 1.1 システムの起動 2 1.2 ユーザー登録 3 1.3 ログイン 4 1.4 個人設定の変更 5 1.5 ログアウト 6 2 新規申請 2.1 新規申請書の作成及び提出 7 2.2 利益相反自己申告書の作成及び提出 13 2.3 審査結果の表示 18 2.4 申請内容の修正及び提出
山梨大学医学部 倫理審査電子申請システム 利用ガイド 平成 27 年 11 月版 目 次 1 システムの利用準備 1.1 システムの起動 2 1.2 ユーザー登録 3 1.3 ログイン 4 1.4 個人設定の変更 5 1.5 ログアウト 6 2 新規申請 2.1 新規申請書の作成及び提出 7 2.2 利益相反自己申告書の作成及び提出 13 2.3 審査結果の表示 18 2.4 申請内容の修正及び提出
1. 次期 e-learning システム移行の目的 1. 大規模受講者への対応 年間 40 万人以上の受講者情報の保有に耐えるシステム 管理能の強化 可用性 スケーラビリティの確保 2. セキュリティの強化 ユーザから信頼されるセキュリティ管理の実現 学認 等との連携によるSSOの実現 外部攻撃に
 次期 e-learning システムについて CITI Japan プロジェクト 一般財団法人公正研究推進協会 平成 29 年 1 月 27 日 1. 次期 e-learning システム移行の目的 1. 大規模受講者への対応 年間 40 万人以上の受講者情報の保有に耐えるシステム 管理能の強化 可用性 スケーラビリティの確保 2. セキュリティの強化 ユーザから信頼されるセキュリティ管理の実現 学認
次期 e-learning システムについて CITI Japan プロジェクト 一般財団法人公正研究推進協会 平成 29 年 1 月 27 日 1. 次期 e-learning システム移行の目的 1. 大規模受講者への対応 年間 40 万人以上の受講者情報の保有に耐えるシステム 管理能の強化 可用性 スケーラビリティの確保 2. セキュリティの強化 ユーザから信頼されるセキュリティ管理の実現 学認
国立病院機構大阪医療センター受託研究取扱細則
 国立病院機構大阪医療センター 受託研究取扱細則 ( 主旨 ) 第 1 条国立病院機構大阪医療センターにおける受託研究の取扱いに関しては 国立病院機構大阪医療センター受託研究取扱規程 ( 以下 規程 という ) 及び他に定めるもののほか 規程第 1 条第 2 項に規定するこの細則の定めるところによる ( 総則 ) 第 2 条研究責任者は 原則として医長職相当以上とする ただし 副作用報告及び感染症報告を受託研究として実施する場合
国立病院機構大阪医療センター 受託研究取扱細則 ( 主旨 ) 第 1 条国立病院機構大阪医療センターにおける受託研究の取扱いに関しては 国立病院機構大阪医療センター受託研究取扱規程 ( 以下 規程 という ) 及び他に定めるもののほか 規程第 1 条第 2 項に規定するこの細則の定めるところによる ( 総則 ) 第 2 条研究責任者は 原則として医長職相当以上とする ただし 副作用報告及び感染症報告を受託研究として実施する場合
同意説明文書(見本)
 同意説明文書 患者さんへ 膠原病の皮膚症状と血管障害の関連性について に関する研究の説明 これは臨床研究への参加についての説明文書です 本臨床研究についてわかりやすく説明しますので 内容を十分ご理解されたうえで 参加するかどうか患者さんご自身の意思でお決め下さい また ご不明な点などがございましたら遠慮なくご質問下さい 臨床研究代表者群馬大学大学院医学系研究科皮膚科学講師茂木精一郎 臨床研究責任医師群馬大学大学院医学系研究科皮膚科学講師茂木精一郎
同意説明文書 患者さんへ 膠原病の皮膚症状と血管障害の関連性について に関する研究の説明 これは臨床研究への参加についての説明文書です 本臨床研究についてわかりやすく説明しますので 内容を十分ご理解されたうえで 参加するかどうか患者さんご自身の意思でお決め下さい また ご不明な点などがございましたら遠慮なくご質問下さい 臨床研究代表者群馬大学大学院医学系研究科皮膚科学講師茂木精一郎 臨床研究責任医師群馬大学大学院医学系研究科皮膚科学講師茂木精一郎
Microsoft Word - 報告書 最終1116.doc
 で薬剤師 臨床検査技師 臨床心理士等となっている 一方 同調査では CRC 養成研修修了者の約半数は CRC 業務や治験事務局業務に携わることなく 治験以外の業務に従事している実態が明らかとなっており CRC の現状について詳細な調査が必要である CRC の認定制度は 現在 我が国では 日本臨床薬理学会 日本 SMO 協会 SoCRA(The Society of Clinical Research
で薬剤師 臨床検査技師 臨床心理士等となっている 一方 同調査では CRC 養成研修修了者の約半数は CRC 業務や治験事務局業務に携わることなく 治験以外の業務に従事している実態が明らかとなっており CRC の現状について詳細な調査が必要である CRC の認定制度は 現在 我が国では 日本臨床薬理学会 日本 SMO 協会 SoCRA(The Society of Clinical Research
大学病院治験受託手順書
 千葉大学医学部附属病院治験審査委員会運営手順書 第 1 条目的本手順書は 千葉大学医学部附属病院各種委員会規程の定めるところにより 千葉大学医学部附属病院治験審査委員会 ( 以下 委員会 という ) の運営方法を定め 医薬品等の治験 製造販売後調査および臨床試験等に関わる業務手順を示すものである 第 2 条委員会の責務 1 本委員会は 千葉大学医学部附属病院 ( 以下 本院 という ) において 治験及び製造販売後臨床試験
千葉大学医学部附属病院治験審査委員会運営手順書 第 1 条目的本手順書は 千葉大学医学部附属病院各種委員会規程の定めるところにより 千葉大学医学部附属病院治験審査委員会 ( 以下 委員会 という ) の運営方法を定め 医薬品等の治験 製造販売後調査および臨床試験等に関わる業務手順を示すものである 第 2 条委員会の責務 1 本委員会は 千葉大学医学部附属病院 ( 以下 本院 という ) において 治験及び製造販売後臨床試験
ただし 対象となることを希望されないご連絡が 2016 年 5 月 31 日以降にな った場合には 研究に使用される可能性があることをご了承ください 研究期間 研究を行う期間は医学部長承認日より 2019 年 3 月 31 日までです 研究に用いる試料 情報の項目群馬大学医学部附属病院産科婦人科で行
 人を対象とする医学系研究についての 情報公開文書 研究課題名 : 予定帝王切開における脊椎麻酔による血圧変動と出生後の児への影響についての検討 はじめに現在 日本のほとんどの施設の標準的な麻酔方法は脊椎麻酔であり 当院でも帝王切開に対する標準的な麻酔方法を脊椎麻酔としています 脊椎麻酔では全身麻酔と比較し児への麻酔の影響が少ないとされていますが 麻酔導入後のお母さんの血圧低下を認めることが多く その際に赤ちゃんへどのような影響があるかは明らかにされていません
人を対象とする医学系研究についての 情報公開文書 研究課題名 : 予定帝王切開における脊椎麻酔による血圧変動と出生後の児への影響についての検討 はじめに現在 日本のほとんどの施設の標準的な麻酔方法は脊椎麻酔であり 当院でも帝王切開に対する標準的な麻酔方法を脊椎麻酔としています 脊椎麻酔では全身麻酔と比較し児への麻酔の影響が少ないとされていますが 麻酔導入後のお母さんの血圧低下を認めることが多く その際に赤ちゃんへどのような影響があるかは明らかにされていません
3 治験実施計画書目的 当該治験について 治験実施計画書が手順書に従い適切に作成及び改訂されていることを確認する 次の事項を調べる (1) 治験実施計画書の記載項目 ( 再生医療等製品 GCP 省令第 7 条第 1 項に規定する項目 ) (2) 治験実施計画書の作成 改訂の手順と日付 (3) 治験計
 別添 10 再生医療等製品 GCP 省令チェックリスト Ⅰ 治験依頼者 ( 受託機関を含む ) 用 1 組織及び体制目的 治験の依頼及び管理に当たって 再生医療等製品 GCP 省令に沿った業務を行うために適切にして十分な人材を有し かつ 組織及び体制が確立していることを確認する 1 治験依頼者の組織 ( 当該被験機器の開発組織を含む ) と再生医療等製品 G CP 省令に係わる組織との関係 2 治験の依頼及び管理の業務に従事する者の氏名
別添 10 再生医療等製品 GCP 省令チェックリスト Ⅰ 治験依頼者 ( 受託機関を含む ) 用 1 組織及び体制目的 治験の依頼及び管理に当たって 再生医療等製品 GCP 省令に沿った業務を行うために適切にして十分な人材を有し かつ 組織及び体制が確立していることを確認する 1 治験依頼者の組織 ( 当該被験機器の開発組織を含む ) と再生医療等製品 G CP 省令に係わる組織との関係 2 治験の依頼及び管理の業務に従事する者の氏名
表紙1−4/木下 中村
 平成15年度 長崎大学概要 長崎養生所のスケッチ 附属図書館医学分館 医学部附属病院の前身である我国最初の洋式病院 120病床 文久元年 1861年 8月16日開院 平成15年度 長崎大学概要 編集発行 長崎大学総務部総務課 852-8521 長崎市文教町1-14 TEL 095-819-2014 Homepage http://www.nagasaki-u.ac.jp/ 20 03 長崎大学概要
平成15年度 長崎大学概要 長崎養生所のスケッチ 附属図書館医学分館 医学部附属病院の前身である我国最初の洋式病院 120病床 文久元年 1861年 8月16日開院 平成15年度 長崎大学概要 編集発行 長崎大学総務部総務課 852-8521 長崎市文教町1-14 TEL 095-819-2014 Homepage http://www.nagasaki-u.ac.jp/ 20 03 長崎大学概要
本手順書で使用する用語の定義 用語電子的記録書面電子的記録利用システム実務担当者原データ治験関連文書サイボウズサイボウズメッセージ 定義人の知覚では認識できない, 電子式等の方法で記録され, コンピュータで処理される記録紙媒体による資料治験依頼者, 実施医療機関の長, 治験責任医師並びに治験審査委員
 ( 第 1 版 :2015 年 7 月 1 日 ) 本手順書で使用する用語の定義 用語電子的記録書面電子的記録利用システム実務担当者原データ治験関連文書サイボウズサイボウズメッセージ 定義人の知覚では認識できない, 電子式等の方法で記録され, コンピュータで処理される記録紙媒体による資料治験依頼者, 実施医療機関の長, 治験責任医師並びに治験審査委員会の間での電子的記録の作成, 交付, 受領及び保存に用いるシステム規定や文書等で責任者の行うべき業務の権限を与えられ,
( 第 1 版 :2015 年 7 月 1 日 ) 本手順書で使用する用語の定義 用語電子的記録書面電子的記録利用システム実務担当者原データ治験関連文書サイボウズサイボウズメッセージ 定義人の知覚では認識できない, 電子式等の方法で記録され, コンピュータで処理される記録紙媒体による資料治験依頼者, 実施医療機関の長, 治験責任医師並びに治験審査委員会の間での電子的記録の作成, 交付, 受領及び保存に用いるシステム規定や文書等で責任者の行うべき業務の権限を与えられ,
北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下
 北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下 モニタリング という ) 監査の受け入れ 並びに試験審査委員会( 治験審査委員会が兼ねる 以下 治験審査委員会
北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下 モニタリング という ) 監査の受け入れ 並びに試験審査委員会( 治験審査委員会が兼ねる 以下 治験審査委員会
PowerPoint プレゼンテーション
 研究開発課題名難病 希少疾患の医薬品開発におけるクリニカルイノベーションネットワーク構想の推進を目指した疾患登録システム ( 患者レジストリ ) の構築 研究開発代表者 国立研究開発法人国立精神 神経医療研究センター 資料 2-3 トランスレーショナルメディカルセンター 臨床研究支援室長 発表内容 本研究の目標 実施体制 Remudy の実績と課題 目指すもの 疾患登録システム レジストリの信頼性について
研究開発課題名難病 希少疾患の医薬品開発におけるクリニカルイノベーションネットワーク構想の推進を目指した疾患登録システム ( 患者レジストリ ) の構築 研究開発代表者 国立研究開発法人国立精神 神経医療研究センター 資料 2-3 トランスレーショナルメディカルセンター 臨床研究支援室長 発表内容 本研究の目標 実施体制 Remudy の実績と課題 目指すもの 疾患登録システム レジストリの信頼性について
APRIN e ラーニングプログラム (CITI Japan) 受講者マニュアル バージョン 3.1 系 第 2.3 版 2018 年 8 月 9 日 一般財団法人公正研究推進協会 (APRIN) 1
 APRIN e ラーニングプログラム (CITI Japan) 受講者マニュアル バージョン 3.1 系 第 2.3 版 2018 年 8 月 9 日 一般財団法人公正研究推進協会 (APRIN) 1 目次 1 初期設定と基本操作 3 1.1 ログイン... 3 1.2 初回ログイン時の確認... 4 1.3 メインメニュー... 7 1.4 ログアウト... 8 1.5 プロファイル 受講コース
APRIN e ラーニングプログラム (CITI Japan) 受講者マニュアル バージョン 3.1 系 第 2.3 版 2018 年 8 月 9 日 一般財団法人公正研究推進協会 (APRIN) 1 目次 1 初期設定と基本操作 3 1.1 ログイン... 3 1.2 初回ログイン時の確認... 4 1.3 メインメニュー... 7 1.4 ログアウト... 8 1.5 プロファイル 受講コース
応募書類の提出方法
 付録 e-rad による応募情報入力の方法 応募前の注意事項 応募の前に 必ず所属研究機関および研究者が府省共通研究開発管理システム (e-rad) に登録済みであることを確認してください 本公募への応募は e-rad を通じて行います e-rad を使用するには 所属する研究機関及び研究者の事前登録が必要です 未登録の場合は e-rad ポータルサイト (https://www.e-rad.go.jp/)
付録 e-rad による応募情報入力の方法 応募前の注意事項 応募の前に 必ず所属研究機関および研究者が府省共通研究開発管理システム (e-rad) に登録済みであることを確認してください 本公募への応募は e-rad を通じて行います e-rad を使用するには 所属する研究機関及び研究者の事前登録が必要です 未登録の場合は e-rad ポータルサイト (https://www.e-rad.go.jp/)
検討課題の整理 1 第 1 回合同会議での意見及びその後委員から提出された意見を 第 1 回合同会議の 検討の進め方 ( 下記参照 ) に沿って分類 第 1 回合同会議資料 合同会議における検討の進め方 の抜粋 合同会議においては 以下の順で検討を進める (1) ゲノム指針と医学系指針との条文の整合
 第 1 回医学研究等に係る倫理指針の見直しに関する合同会議 TF 平成 30 年 10 月 29 日 参考資料 1 合同会議における委員コメント ( 追記版 ) 検討課題の整理 1 第 1 回合同会議での意見及びその後委員から提出された意見を 第 1 回合同会議の 検討の進め方 ( 下記参照 ) に沿って分類 第 1 回合同会議資料 合同会議における検討の進め方 の抜粋 合同会議においては 以下の順で検討を進める
第 1 回医学研究等に係る倫理指針の見直しに関する合同会議 TF 平成 30 年 10 月 29 日 参考資料 1 合同会議における委員コメント ( 追記版 ) 検討課題の整理 1 第 1 回合同会議での意見及びその後委員から提出された意見を 第 1 回合同会議の 検討の進め方 ( 下記参照 ) に沿って分類 第 1 回合同会議資料 合同会議における検討の進め方 の抜粋 合同会議においては 以下の順で検討を進める
岩手医科大学医学部及び附属病院における人を対象とする医学系研究に係るモニタリング及び監査の実施に関する標準業務手順書 岩手医科大学医学部及び附属病院における 人を対象とする医学系研究に係る モニタリング及び監査の実施に関する標準業務手順書 岩手医科大学 第 1.0 版平成 29 年 10 月 1 日
 岩手医科大学医学部及び附属病院における 人を対象とする医学系研究に係る モニタリング及び監査の実施に関する標準業務手順書 岩手医科大学 第 1.0 版平成 29 年 10 月 1 日施行 目次 1. 目的...1 2. 研究機関の長の責務...1 3. 研究責任者の責務...1 4. モニタリング担当者の責務...1 5. 監査担当者の責務...2 6. 多施設共同研究におけるモニタリング及び監査の実施について...2
岩手医科大学医学部及び附属病院における 人を対象とする医学系研究に係る モニタリング及び監査の実施に関する標準業務手順書 岩手医科大学 第 1.0 版平成 29 年 10 月 1 日施行 目次 1. 目的...1 2. 研究機関の長の責務...1 3. 研究責任者の責務...1 4. モニタリング担当者の責務...1 5. 監査担当者の責務...2 6. 多施設共同研究におけるモニタリング及び監査の実施について...2
先進医療の実績報告要領 Ⅰ 実績報告の実施について (1) 実績報告の目的先進医療の実施状況を把握し 保険導入等に係る検討のための基礎資料とすることを目的とするものである (2) 実績報告の対象医療機関平成 30 年 6 月 30 日現在において 先進医療を実施している医療機関平成 30 年 3 月
 先進医療の実績報告要領 Ⅰ 実績報告の実施について (1) 実績報告の目的先進医療の実施状況を把握し 保険導入等に係る検討のための基礎資料とすることを目的とするものである (2) 実績報告の対象医療機関平成 30 年 6 月 30 日現在において 先進医療を実施している医療機関平成 30 年 3 月 31 日現在において 先進医療を実施している医療機関 ( 保険導入等分 ) 先進医療 A 告示番号
先進医療の実績報告要領 Ⅰ 実績報告の実施について (1) 実績報告の目的先進医療の実施状況を把握し 保険導入等に係る検討のための基礎資料とすることを目的とするものである (2) 実績報告の対象医療機関平成 30 年 6 月 30 日現在において 先進医療を実施している医療機関平成 30 年 3 月 31 日現在において 先進医療を実施している医療機関 ( 保険導入等分 ) 先進医療 A 告示番号
内容 1. はじめに 大規模治験ネットワーク登録医療機関への支援内容 治験実施医療機関情報の登録と公開 登録の条件 事前確認 大規模治験ネットワーク への登録方法 登録の手順 登録でき
 大規模治験ネットワーク 登録マニュアル Ver1.1 2013/4/1 公益社団法人日本医師会治験促進センター 0 内容 1. はじめに... 2 2. 大規模治験ネットワーク登録医療機関への支援内容... 2 3. 治験実施医療機関情報の登録と公開... 3 4. 登録の条件... 4 5. 事前確認... 5 6. 大規模治験ネットワーク への登録方法... 6 6-1 登録の手順... 6 6-2
大規模治験ネットワーク 登録マニュアル Ver1.1 2013/4/1 公益社団法人日本医師会治験促進センター 0 内容 1. はじめに... 2 2. 大規模治験ネットワーク登録医療機関への支援内容... 2 3. 治験実施医療機関情報の登録と公開... 3 4. 登録の条件... 4 5. 事前確認... 5 6. 大規模治験ネットワーク への登録方法... 6 6-1 登録の手順... 6 6-2
(3) 倫理学 法律学の専門家等 本法人に所属しない人文 社会科学の有識者若干名 (4) 一般の立場から意見を述べることができる者若干名 (5) 分子生物学 細胞生物学 遺伝学 臨床薬理学 病理学等の専門家若しくは遺伝子治療等臨床研究の対象となる疾患に係る臨床医として 日本医科大学長が推薦した者若干
 学校法人日本医科大学中央倫理委員会規程 ( 平成 28 年 1 月 1 日規程第 3 号 ) ( 目的 ) 第 1 条この規程は 医の倫理に関するヘルシンキ宣言の趣旨を尊重し 人を対象とする医学系研究に関する倫理指針 ヒトゲノム 遺伝子解析研究に関する倫理指針 遺伝子治療臨床研究に関する指針 ヒト受精胚の作成を行う生殖補助医療研究に関する倫理指針 等 国等が示した関係法令及び関係指針 ( 以下すべて併せて
学校法人日本医科大学中央倫理委員会規程 ( 平成 28 年 1 月 1 日規程第 3 号 ) ( 目的 ) 第 1 条この規程は 医の倫理に関するヘルシンキ宣言の趣旨を尊重し 人を対象とする医学系研究に関する倫理指針 ヒトゲノム 遺伝子解析研究に関する倫理指針 遺伝子治療臨床研究に関する指針 ヒト受精胚の作成を行う生殖補助医療研究に関する倫理指針 等 国等が示した関係法令及び関係指針 ( 以下すべて併せて
受講マニュアル
 研究倫理 e ラーニング受講マニュアル (ver.1.0) 日本学術振興会 Copyright 2016 JSPS All Rights Reserved. 2 目次 受講の進め方についてご説明します 1. マイルーム へログイン P3 2. マイルーム から学習ページに入る P4 3. 本 eラーニング内での学習 P5 3-1. 各種メニューボタン ページ遷移ボタン P6 3-2. 事例学習の進め方
研究倫理 e ラーニング受講マニュアル (ver.1.0) 日本学術振興会 Copyright 2016 JSPS All Rights Reserved. 2 目次 受講の進め方についてご説明します 1. マイルーム へログイン P3 2. マイルーム から学習ページに入る P4 3. 本 eラーニング内での学習 P5 3-1. 各種メニューボタン ページ遷移ボタン P6 3-2. 事例学習の進め方
研究活動における不正行為への対応等に関する規程 ( 目的 ) 第 1 条 本規程は小池化学株式会社 ( 以下 当社 という ) における研究活動での不正行為を防止 すると共に 不正行為が行われ 又はそのおそれがある場合の取扱いに関し 必要な事項を 定める ( 定義 ) 第 2 条本規程において 不正
 研究活動における不正行為への対応等に関する規程 ( 目的 ) 第 1 条 本規程は小池化学株式会社 ( 以下 当社 という ) における研究活動での不正行為を防止 すると共に 不正行為が行われ 又はそのおそれがある場合の取扱いに関し 必要な事項を 定める ( 定義 ) 第 2 条本規程において 不正行為 とは 研究者倫理に背馳し研究活動やその発表においてなされる次に掲げる行為をいう (1) 捏造存在しないデータ
研究活動における不正行為への対応等に関する規程 ( 目的 ) 第 1 条 本規程は小池化学株式会社 ( 以下 当社 という ) における研究活動での不正行為を防止 すると共に 不正行為が行われ 又はそのおそれがある場合の取扱いに関し 必要な事項を 定める ( 定義 ) 第 2 条本規程において 不正行為 とは 研究者倫理に背馳し研究活動やその発表においてなされる次に掲げる行為をいう (1) 捏造存在しないデータ
説明文書
 説明文書 研究対象施設の皆様へ 全国を対象とした抗菌薬使用動向調査に関する研究 : Japan Antimicrobial Consumption Surveillance (JACS) へのご協力のお願い 研究代表者 : 三重大学医学部附属病院薬剤部 村木優一 研究事務局 : 三重大学医学部附属病院薬剤部村木優一 514-8507 三重県津市江戸橋 2-174 電話 :059-231-7402 FAX:059-232-1201
説明文書 研究対象施設の皆様へ 全国を対象とした抗菌薬使用動向調査に関する研究 : Japan Antimicrobial Consumption Surveillance (JACS) へのご協力のお願い 研究代表者 : 三重大学医学部附属病院薬剤部 村木優一 研究事務局 : 三重大学医学部附属病院薬剤部村木優一 514-8507 三重県津市江戸橋 2-174 電話 :059-231-7402 FAX:059-232-1201
<93648EA593498B4C985E82C98AD682B782E E838A F E315F C668DDA95AA292E786C7378>
 1 実施医療機関の長等の承諾 電磁的記録として扱う治験関連文書 ( 範囲 ) の承諾 SOP 等 施設の正式文書の記載 実施医療機関の長からの確認 実務担当者からの確認 電磁的記録の交付 受領手段の承諾 SOP 等 施設の正式文書の記載 実施医療機関の長からの確認 実務担当者からの確認 ( 版 :2013 年 9 月 1 日 ver2.0) 2 3 電磁的記録として扱う治験関連文書 電磁的記録の交付
1 実施医療機関の長等の承諾 電磁的記録として扱う治験関連文書 ( 範囲 ) の承諾 SOP 等 施設の正式文書の記載 実施医療機関の長からの確認 実務担当者からの確認 電磁的記録の交付 受領手段の承諾 SOP 等 施設の正式文書の記載 実施医療機関の長からの確認 実務担当者からの確認 ( 版 :2013 年 9 月 1 日 ver2.0) 2 3 電磁的記録として扱う治験関連文書 電磁的記録の交付
群馬大学人を対象とする医学系研究倫理審査委員会 _ 情報公開 通知文書 人を対象とする医学系研究についての 情報公開文書 研究課題名 : がんサバイバーの出産の実際調査 はじめに近年 がん治療の進歩によりがん治療後に長期間生存できる いわゆる若年のがんサバイバーが増加しています これらのがんサバイバ
 人を対象とする医学系研究についての 情報公開文書 研究課題名 : がんサバイバーの出産の実際調査 はじめに近年 がん治療の進歩によりがん治療後に長期間生存できる いわゆる若年のがんサバイバーが増加しています これらのがんサバイバーにおいて生命の質の維持 向上は重要な問題で 中でもがん治療による妊孕性 ( 将来の妊娠の可能性 ) への影響は人生を左右する大きな問題と考えられますが 我が国においては がん患者の妊孕性温存治療に対する一定の指針がないのが現状です
人を対象とする医学系研究についての 情報公開文書 研究課題名 : がんサバイバーの出産の実際調査 はじめに近年 がん治療の進歩によりがん治療後に長期間生存できる いわゆる若年のがんサバイバーが増加しています これらのがんサバイバーにおいて生命の質の維持 向上は重要な問題で 中でもがん治療による妊孕性 ( 将来の妊娠の可能性 ) への影響は人生を左右する大きな問題と考えられますが 我が国においては がん患者の妊孕性温存治療に対する一定の指針がないのが現状です
資料1:「生命倫理に関する研究機関における検討について」(赤林先生資料)
 資料 1 命倫理に関する研究機関における検討について 東京 学医学部医療倫理学分野 林朗 次 医学系研究における法令 指針等 機関の の役割 倫理審査委員会の役割 倫理審査委員会の構成 研究実施にあたっての検討の流れ 医学系研究における法令 指針等 医学系研究に関する法律 医薬品医療機器等法 (2015 年改訂 ) 治験 再 医療等安全性確保法 (2013 年 ) 再 医療研究 医学系研究に関する基本的な指針
資料 1 命倫理に関する研究機関における検討について 東京 学医学部医療倫理学分野 林朗 次 医学系研究における法令 指針等 機関の の役割 倫理審査委員会の役割 倫理審査委員会の構成 研究実施にあたっての検討の流れ 医学系研究における法令 指針等 医学系研究に関する法律 医薬品医療機器等法 (2015 年改訂 ) 治験 再 医療等安全性確保法 (2013 年 ) 再 医療研究 医学系研究に関する基本的な指針
( 委員以外の者の出席 ) 第 5 条委員長は 必要に応じ当該研究に必要な知見及び専門知識を持つ教員 産業医または看護師等を委員会の同意を得て出席させ 意見を聴くことができる ただし 上記の者の出席が困難な場合は 委員長又は委員長が指名した者が口頭等で意見を聴取し 委員会で報告することができる (
 一関工業高等専門学校における人を対象とする研究倫理審査委員会規則 ( 平成 28 年 6 月 9 日制定 ) ( 設置 ) 第 1 条一関工業高等専門学校 ( 以下 本校 という ) に, 人を対象とする研究における研究倫理について審査するため, 人を対象とする研究倫理審査委員会 ( 以下 委員会 という ) を置く ( 目的 ) 第 2 条委員会は, 本校における人を対象とする研究が, 独立行政法人国立高等専門学校機構における研究者等の行動規範
一関工業高等専門学校における人を対象とする研究倫理審査委員会規則 ( 平成 28 年 6 月 9 日制定 ) ( 設置 ) 第 1 条一関工業高等専門学校 ( 以下 本校 という ) に, 人を対象とする研究における研究倫理について審査するため, 人を対象とする研究倫理審査委員会 ( 以下 委員会 という ) を置く ( 目的 ) 第 2 条委員会は, 本校における人を対象とする研究が, 独立行政法人国立高等専門学校機構における研究者等の行動規範
国立研究開発法人国立循環器病研究センター受託研究取扱規程 ( )
 国立研究開発法人国立循環器病研究センター受託研究取扱規程 (20190401) 平成 22 年 4 月 1 日規程第 46 号 国立研究開発法人国立循環器病研究センター受託研究取扱規程 ( 通則 ) 第 1 条国立研究開発法人国立循環器病研究センター ( 以下 センター という ) においてセンター以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては
国立研究開発法人国立循環器病研究センター受託研究取扱規程 (20190401) 平成 22 年 4 月 1 日規程第 46 号 国立研究開発法人国立循環器病研究センター受託研究取扱規程 ( 通則 ) 第 1 条国立研究開発法人国立循環器病研究センター ( 以下 センター という ) においてセンター以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては
平成28年度 第1回 臨床研究に関する研修会
 平成 28 年度第 1 回 臨床研究に関する研修会 臨床研究センター臨床研究ユニット 平成 28 年 4 月 22 日 1 人を対象とする医学系研究に関する倫理指針について 2 臨床研究における様々な指針 医薬品 医療機器 再生医療等製品の承認申請を目的としているか? Yes 治験 No 治験以外の臨床研究 法律 医薬品医療機器等法 ( 旧薬事法 ) 省令 臨床試験の実施の基準に関する省令 (GCP)
平成 28 年度第 1 回 臨床研究に関する研修会 臨床研究センター臨床研究ユニット 平成 28 年 4 月 22 日 1 人を対象とする医学系研究に関する倫理指針について 2 臨床研究における様々な指針 医薬品 医療機器 再生医療等製品の承認申請を目的としているか? Yes 治験 No 治験以外の臨床研究 法律 医薬品医療機器等法 ( 旧薬事法 ) 省令 臨床試験の実施の基準に関する省令 (GCP)
07案3団体あて臨床研究法COI通知
 様式 A 利益相反管理基準 ver.3.0 日付所属機関立場氏名利用基準 研究課題 : 基準 1 基準 2 研究責任医師は 次に掲げる事項について 研究計画書及び説明文書に記載し 研究結果の公表時に開示すること 研究責任医師以外の者が研究成果を公表する場合も 同様に開示すること 1 規則第 21 条第 1 項第 1 号に規定する関与 ( 研究に対する関与 ) として 次に掲げる関与が有る場合には その内容ア医薬品等製造販売業者
様式 A 利益相反管理基準 ver.3.0 日付所属機関立場氏名利用基準 研究課題 : 基準 1 基準 2 研究責任医師は 次に掲げる事項について 研究計画書及び説明文書に記載し 研究結果の公表時に開示すること 研究責任医師以外の者が研究成果を公表する場合も 同様に開示すること 1 規則第 21 条第 1 項第 1 号に規定する関与 ( 研究に対する関与 ) として 次に掲げる関与が有る場合には その内容ア医薬品等製造販売業者
記 1. 適用対象本通知は 製造販売業者等が GPSP 省令第 2 条第 3 項に規定する DB 事業者が提供する同条第 2 項に規定する医療情報データベースを用いて同条第 1 項第 2 号に規定する製造販売後データベース調査を実施し 医薬品の再審査等の申請資料を作成する場合に適用する GPSP 省
 記 1. 適用対象本通知は 製造販売業者等が GPSP 省令第 2 条第 3 項に規定する DB 事業者が提供する同条第 2 項に規定する医療情報データベースを用いて同条第 1 項第 2 号に規定する製造販売後データベース調査を実施し 医薬品の再審査等の申請資料を作成する場合に適用する GPSP 省令第 2 条第 2 項において 医療情報データベース とは 一定の期間において収集される診療録その他の診療に関する記録
記 1. 適用対象本通知は 製造販売業者等が GPSP 省令第 2 条第 3 項に規定する DB 事業者が提供する同条第 2 項に規定する医療情報データベースを用いて同条第 1 項第 2 号に規定する製造販売後データベース調査を実施し 医薬品の再審査等の申請資料を作成する場合に適用する GPSP 省令第 2 条第 2 項において 医療情報データベース とは 一定の期間において収集される診療録その他の診療に関する記録
CPD申請案内171208
 認定情報技術者 (CITP ) 2017 年度更新申請案内 主要項目 主な対象者 2014 年度 CITP 資格取得者 ( 認定番号 :14000***) 申請書配布 申請書に記す過 去 3 年間の活動 期間 :2017 年 12 月 11 日 ( 月 )~2018 年 1 月 12 日 ( 金 ) ダウンロードサイト : 認定情報技術者制度のホームページ参照 2015 年 1 月 1 日 ~2017
認定情報技術者 (CITP ) 2017 年度更新申請案内 主要項目 主な対象者 2014 年度 CITP 資格取得者 ( 認定番号 :14000***) 申請書配布 申請書に記す過 去 3 年間の活動 期間 :2017 年 12 月 11 日 ( 月 )~2018 年 1 月 12 日 ( 金 ) ダウンロードサイト : 認定情報技術者制度のホームページ参照 2015 年 1 月 1 日 ~2017
(2) 利益相反についての事務局勉強会 ( 平成 20 年 8 月 25 日 ~8 月 27 日 ) 利益相反に関する業務を知的財産 ベンチャー育成 (TLO) センターで行うのにあたり 利益相反マネジメント委員会の学外委員である弁護士 2 名から 利益相反に関する基礎的な事項についてレクチャーを受
 利益相反マネジメント委員会 1. 構成員について平成 20 年 4 月 1 日に 学校法人日本医科大学に利益相反マネジメント委員会を設置し 日本医科大学及び日本獣医生命科学大学の利益相反問題については 法人としてマネジメントを行っていくものとして 下記のメンバーで本委員会が発足した 委員長 : 隈崎達夫 ( 学校法人日本医科大学常務理事 ) 副委員長 : 鎌田隆 ( 弁護士 学校法人日本医科大学理事
利益相反マネジメント委員会 1. 構成員について平成 20 年 4 月 1 日に 学校法人日本医科大学に利益相反マネジメント委員会を設置し 日本医科大学及び日本獣医生命科学大学の利益相反問題については 法人としてマネジメントを行っていくものとして 下記のメンバーで本委員会が発足した 委員長 : 隈崎達夫 ( 学校法人日本医科大学常務理事 ) 副委員長 : 鎌田隆 ( 弁護士 学校法人日本医科大学理事
<4D F736F F D20819D95BD90AC E93788E528CFB91E58A778CA48B86817C91E682548FCD C >
 第 4 章研究者アンケート調査結果 1 研究者アンケート要点 -2 アンケート全体調査結果 -3 工学部アンケート調査結果 -4 理学部アンケート調査結果 -5 農学部アンケート調査結果 -6 医学部アンケート調査結果 第 4 章研究者アンケート調査結果 4-1 研究者アンケート要点 研究者属性や研究分野が 特許情報活用行動に影響を与えているか否かを調査するために研究者を対象とするアンケート調査を実施した
第 4 章研究者アンケート調査結果 1 研究者アンケート要点 -2 アンケート全体調査結果 -3 工学部アンケート調査結果 -4 理学部アンケート調査結果 -5 農学部アンケート調査結果 -6 医学部アンケート調査結果 第 4 章研究者アンケート調査結果 4-1 研究者アンケート要点 研究者属性や研究分野が 特許情報活用行動に影響を与えているか否かを調査するために研究者を対象とするアンケート調査を実施した
ICH-GCPとJ-GCPとの比較表
 参考資料 10 我が国の GCP と ICH-GCP の主な 1 治験の契約に関する規定 1-1 契約者に関する規定 1-2 実施医療機関の長との契約を規定したことに伴う規定 2 治験審査委員会 (IRB) に関する規定 2-1 IRB の設置に関する規定 2-2 IRB への審議依頼に関する規定 1/11 1. 治験の契約に関する規定 1-1. 契約者に関する規定 ICH-GCP 1.17( 用語の定義
参考資料 10 我が国の GCP と ICH-GCP の主な 1 治験の契約に関する規定 1-1 契約者に関する規定 1-2 実施医療機関の長との契約を規定したことに伴う規定 2 治験審査委員会 (IRB) に関する規定 2-1 IRB の設置に関する規定 2-2 IRB への審議依頼に関する規定 1/11 1. 治験の契約に関する規定 1-1. 契約者に関する規定 ICH-GCP 1.17( 用語の定義
12_モニタリングの実施に関する手順書
 12_ モニタリングの実施に関する手順書 静岡県立大学大学院薬食生命科学総合学府薬学研究院薬食研究推進センター版数 :1.0 版作成年月日 :2014 月 8 月 1 日 ( 最終確定 :2015 年 1 月 14 日 ) 1. 目的と適用範囲 本手順書は 当該研究において モニターが モニタリングを適切に実施するための手順 その他必要な事項を定めるものである 2. 実施体制及び責務 2.1 研究責任者の責務研究責任者は
12_ モニタリングの実施に関する手順書 静岡県立大学大学院薬食生命科学総合学府薬学研究院薬食研究推進センター版数 :1.0 版作成年月日 :2014 月 8 月 1 日 ( 最終確定 :2015 年 1 月 14 日 ) 1. 目的と適用範囲 本手順書は 当該研究において モニターが モニタリングを適切に実施するための手順 その他必要な事項を定めるものである 2. 実施体制及び責務 2.1 研究責任者の責務研究責任者は
final_生命科学データ保存GL_ver
 東京大学大学院医学系研究科 医学部 生命科学系研究データ保存のガイドライン ( 第 1 版 ) ( 平成 28 年 4 月 1 日 ) 1 要旨 1 電子化された研究資料の保存期間は当該論文等の発表後 10 年間 論文や学位など 研究成果発表のもととなった研究資料は電子化し 当該論文等の発表後教室内 に 10 年間保存する 電子化した研究資料の作成日や分類等の付加情報 ( メタデータ ) や研究試料等の情報は研究資料
東京大学大学院医学系研究科 医学部 生命科学系研究データ保存のガイドライン ( 第 1 版 ) ( 平成 28 年 4 月 1 日 ) 1 要旨 1 電子化された研究資料の保存期間は当該論文等の発表後 10 年間 論文や学位など 研究成果発表のもととなった研究資料は電子化し 当該論文等の発表後教室内 に 10 年間保存する 電子化した研究資料の作成日や分類等の付加情報 ( メタデータ ) や研究試料等の情報は研究資料
Microsoft PowerPoint - 運用 [互換モード]
![Microsoft PowerPoint - 運用 [互換モード] Microsoft PowerPoint - 運用 [互換モード]](/thumbs/91/105850431.jpg) 押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
1. はじめに我が国では 臨床研究 治験活性化 5 か年計画 2012 をはじめとした種々の取り組みにより治験実施体制の整備が行われ 治験環境に改善がみられてきた しかし 医療機関の一部の治験業務において治験依頼者からの支援を要する医療機関が少なからず存在すること 治験担当医師の GCP 関連知識や
 治験実施医療機関への治験環境改善のための各種提案について [ 筆者 ( 資料作成者 )] 日本製薬工業協会医薬品評価委員会臨床評価部会タスクフォースチーム大村泉美神谷勇輝岸本早江子横山領介西島壮一郎鈴木健太青柳充顕中島唯善近藤充弘 1. はじめに我が国では 臨床研究 治験活性化 5 か年計画 2012 をはじめとした種々の取り組みにより治験実施体制の整備が行われ 治験環境に改善がみられてきた しかし
治験実施医療機関への治験環境改善のための各種提案について [ 筆者 ( 資料作成者 )] 日本製薬工業協会医薬品評価委員会臨床評価部会タスクフォースチーム大村泉美神谷勇輝岸本早江子横山領介西島壮一郎鈴木健太青柳充顕中島唯善近藤充弘 1. はじめに我が国では 臨床研究 治験活性化 5 か年計画 2012 をはじめとした種々の取り組みにより治験実施体制の整備が行われ 治験環境に改善がみられてきた しかし
Microsoft Word - adr (1)
 平成 29 年 9 月吉日 日本不動産仲裁機構 ADR センター ( 法務大臣認証裁判外紛争解決機関 ) 調停人基礎資格認定のお知らせ NPO 法人日本ホームインスペクターズ協会 皆様方に置かれましては ますますご清栄のこととお喜び申し上げます 日頃は 当協会の活動につきご理解とご協力を賜り誠にありがとうございます さて 当協会が加盟する一般社団法人日本不動産仲裁機構 ( 以下 仲裁機構 といいます
平成 29 年 9 月吉日 日本不動産仲裁機構 ADR センター ( 法務大臣認証裁判外紛争解決機関 ) 調停人基礎資格認定のお知らせ NPO 法人日本ホームインスペクターズ協会 皆様方に置かれましては ますますご清栄のこととお喜び申し上げます 日頃は 当協会の活動につきご理解とご協力を賜り誠にありがとうございます さて 当協会が加盟する一般社団法人日本不動産仲裁機構 ( 以下 仲裁機構 といいます
東京大学
 第 13 回治験 IT 化部会 2013 年 7 月 17 日 ( 水 ) PM5:05-5:30 産業技術総合研究所臨海副都心センター別館 11F 第 1~2 会議室 臨床研究 治験の e-learning 東京大学大学院医学系研究科 臨床疫学研究システム学講座特任准教授小出大介 1 本日の内容 様々な臨床研究 治験の e-learning 厚生科研の事業の紹介 2 様々な臨床研究 治験の e-learning
第 13 回治験 IT 化部会 2013 年 7 月 17 日 ( 水 ) PM5:05-5:30 産業技術総合研究所臨海副都心センター別館 11F 第 1~2 会議室 臨床研究 治験の e-learning 東京大学大学院医学系研究科 臨床疫学研究システム学講座特任准教授小出大介 1 本日の内容 様々な臨床研究 治験の e-learning 厚生科研の事業の紹介 2 様々な臨床研究 治験の e-learning
e-rad による応募情報入力の方法 府省共通研究開発管理システム (e-rad) について府省共通研究開発管理システム (e-rad) は 各府省が所管する公募型研究資金制度の管理に係る一連のプロセス (( 応募受付 採択 採択課題の管理 研究成果 会計実績の登録受付等 )) をオンライン化する府
 e-rad による応募情報入力の方法 府省共通研究開発管理システム (e-rad) について府省共通研究開発管理システム (e-rad) は 各府省が所管する公募型研究資金制度の管理に係る一連のプロセス (( 応募受付 採択 採択課題の管理 研究成果 会計実績の登録受付等 )) をオンライン化する府省横断的なシステムです 1 府省共通研究開発管理システム (e-rad) による応募に当たっての注意事項研究提案の応募は
e-rad による応募情報入力の方法 府省共通研究開発管理システム (e-rad) について府省共通研究開発管理システム (e-rad) は 各府省が所管する公募型研究資金制度の管理に係る一連のプロセス (( 応募受付 採択 採択課題の管理 研究成果 会計実績の登録受付等 )) をオンライン化する府省横断的なシステムです 1 府省共通研究開発管理システム (e-rad) による応募に当たっての注意事項研究提案の応募は
国立がんセンター受託研究取扱規程
 平成 22 年 4 月 1 日規程第 31 号 国立研究開発法人国立がん研究センター受託研究取扱規程 第 1 版平成 22 年 4 月 1 日第 2 版平成 22 年 10 月 1 日第 3 版平成 23 年 4 月 1 日第 4 版平成 24 年 4 月 1 日第 5 版平成 24 年 7 月 1 日第 6 版平成 25 年 4 月 1 日第 7 版平成 27 年 4 月 1 日 ( 通則 ) 第
平成 22 年 4 月 1 日規程第 31 号 国立研究開発法人国立がん研究センター受託研究取扱規程 第 1 版平成 22 年 4 月 1 日第 2 版平成 22 年 10 月 1 日第 3 版平成 23 年 4 月 1 日第 4 版平成 24 年 4 月 1 日第 5 版平成 24 年 7 月 1 日第 6 版平成 25 年 4 月 1 日第 7 版平成 27 年 4 月 1 日 ( 通則 ) 第
実施基準、実施計画及び研究計画書の関係と流れ
 臨床研究法による医薬品等の臨床研究の手続きについて (07022018 版 ) 臨床研究法 については 厚生労働省の HP に詳しく記載がされていますので 参照にしてください https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html 臨床研究開発センター西川政勝 1 臨床研究における規制の区分と研究倫理委員会 ( 三重大学病院
臨床研究法による医薬品等の臨床研究の手続きについて (07022018 版 ) 臨床研究法 については 厚生労働省の HP に詳しく記載がされていますので 参照にしてください https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html 臨床研究開発センター西川政勝 1 臨床研究における規制の区分と研究倫理委員会 ( 三重大学病院
費 複写費 現像 焼付費 通信費 ( 切手 電話等 ) 運搬費 研究実施場所借り上げ費 ( 研究機関の施設において補助事業の遂行が困難な場合に限る ) 会議費 ( 会場借料 食事 ( アルコール類を除く ) 費用等 ) リース レンタル費用 ( コンピュータ 自動車 実験機器 器具等 ) 機器修理費
 別紙 7 平成 29 年度科学研究費助成事業における交付条件等の主な変更点について 1. 科学研究費助成事業- 科研費 -( 基盤研究 (B) 若手研究(A))( 平成 24 年度から平成 26 年度に採択された研究課題 ) 研究者使用ルール ( 交付条件 ) の主な変更点平成 28 年度平成 29 年度 1 総則 1 総則 2 直接経費の使用 2 直接経費の使用 直接経費の各費目の対象となる経費
別紙 7 平成 29 年度科学研究費助成事業における交付条件等の主な変更点について 1. 科学研究費助成事業- 科研費 -( 基盤研究 (B) 若手研究(A))( 平成 24 年度から平成 26 年度に採択された研究課題 ) 研究者使用ルール ( 交付条件 ) の主な変更点平成 28 年度平成 29 年度 1 総則 1 総則 2 直接経費の使用 2 直接経費の使用 直接経費の各費目の対象となる経費
医療機関における治験業務
 国立大学法人東京医科歯科大学医学部附属病院 治験等審査委員会標準手順書 東京医科歯科大学医学部附属病院 臨床試験管理センター 制定日 :2015 年 8 月 3 日 改訂日 : 年月日 目次 第 1 章治験等審査委員会 2 第 2 章治験等審査委員会事務局 7 第 3 章記録の保存 8 第 4 章調査 審議の受託 9 第 5 章その他 9-1 - 第 1 章治験等審査委員会 ( 目的と適用範囲 )
国立大学法人東京医科歯科大学医学部附属病院 治験等審査委員会標準手順書 東京医科歯科大学医学部附属病院 臨床試験管理センター 制定日 :2015 年 8 月 3 日 改訂日 : 年月日 目次 第 1 章治験等審査委員会 2 第 2 章治験等審査委員会事務局 7 第 3 章記録の保存 8 第 4 章調査 審議の受託 9 第 5 章その他 9-1 - 第 1 章治験等審査委員会 ( 目的と適用範囲 )
9 中止基準 ( 研究対象者の中止 研究全体の中止について ) 10 研究対象者への研究実施後の医療提供に関する対応 通常の診療を超える医療行為 を伴う研究を実施した場合 研究実施後において 研究対象者が研究の結果より得られた利用可能な最善の予防 診断及び治療が受けられるように努めること 11 研究
 倫理審査書類 ( 研究計画書 ) チェックシート 研究計画書には 原則として以下の項目を含めてください 申請時 提出は不要です 2017.5.2 1 研究の名称 ( 標題 ) 2 研究の実施体制 ( 研究組織 ) 多施設共同研究の場合 共同研究機関の研究者名 役割も詳細に記載 3 研究の背景及び意義 研究を実施する意義 必要性に関して 文献等を用いて研究の 科学的合理性の根拠 と 本研究で得られる成果
倫理審査書類 ( 研究計画書 ) チェックシート 研究計画書には 原則として以下の項目を含めてください 申請時 提出は不要です 2017.5.2 1 研究の名称 ( 標題 ) 2 研究の実施体制 ( 研究組織 ) 多施設共同研究の場合 共同研究機関の研究者名 役割も詳細に記載 3 研究の背景及び意義 研究を実施する意義 必要性に関して 文献等を用いて研究の 科学的合理性の根拠 と 本研究で得られる成果
申請について 研究の概要 に機密情報を含めることはできますか 研究の概要 内の 研究内容に関連する業績( 原著論文 ) は英語論文のみですか また 記載する論文は in press でもよいですか 申請をした後で申請内容を修正したい場合はどのようにすればよいですか 申請をしましたが 都合により取り下
 MSD 奨学寄付 に関する F 最終更新日 :2018 年 4 月 奨学寄付 ( 学術研究支援 ) について 奨学寄付 ( 学術研究支援 ) の目的を教えてください 寄付対象について 研究期間が複数年におよびますが 複数年分の寄付を申請できますか アカウント ID 登録 / パスワードについて アカウント ID を登録せず申請できますか 公益活動寄付で登録したアカウントで奨学寄付 ( 学術研究支援
MSD 奨学寄付 に関する F 最終更新日 :2018 年 4 月 奨学寄付 ( 学術研究支援 ) について 奨学寄付 ( 学術研究支援 ) の目的を教えてください 寄付対象について 研究期間が複数年におよびますが 複数年分の寄付を申請できますか アカウント ID 登録 / パスワードについて アカウント ID を登録せず申請できますか 公益活動寄付で登録したアカウントで奨学寄付 ( 学術研究支援
募集要項別紙 e-rad 入力手順 1 はじめに 1-1 諸注意 e-rad への登録研究代表者および全ての主たる共同研究者がe-Rad に研究者情報を登録し ログイン ID パスワードを事前に取得する必要があります ( 他の公募への応募の際に登録済みの場合 再登録は不要です ) 入力情報は 一時保
 e-rad 入力手順 はじめに - 諸注意 e-rad への登録研究代表者および全ての主たる共同研究者がe-Rad に研究者情報を登録し ログイン ID パスワードを事前に取得する必要があります ( 他の公募への応募の際に登録済みの場合 再登録は不要です ) 入力情報は 一時保存 が可能です 応募情報の入力を途中で中断し 一時保存することができます ( 詳細は 応募情報の一時保存 入力の再開について
e-rad 入力手順 はじめに - 諸注意 e-rad への登録研究代表者および全ての主たる共同研究者がe-Rad に研究者情報を登録し ログイン ID パスワードを事前に取得する必要があります ( 他の公募への応募の際に登録済みの場合 再登録は不要です ) 入力情報は 一時保存 が可能です 応募情報の入力を途中で中断し 一時保存することができます ( 詳細は 応募情報の一時保存 入力の再開について
埼玉医科大学倫理委員会
 全国大腸癌肝転移登録事業および登録情報に基づく研究 研究計画書 研究責任者 埼玉医科大学総合医療センター消化管 一般外科 石橋敬一郎 Version 1.0 2017 年 10 月 31 日 0 1. 研究の名称 全国大腸癌肝転移登録事業および登録情報に基づく研究 2. 研究組織について研究代表者 : 大腸癌研究会大腸癌肝転移データベース合同委員会委員長高橋慶一がん 感染症センター都立駒込病院外科副委員長山本雅一東京女子医科大学消化器外科研究事務局
全国大腸癌肝転移登録事業および登録情報に基づく研究 研究計画書 研究責任者 埼玉医科大学総合医療センター消化管 一般外科 石橋敬一郎 Version 1.0 2017 年 10 月 31 日 0 1. 研究の名称 全国大腸癌肝転移登録事業および登録情報に基づく研究 2. 研究組織について研究代表者 : 大腸癌研究会大腸癌肝転移データベース合同委員会委員長高橋慶一がん 感染症センター都立駒込病院外科副委員長山本雅一東京女子医科大学消化器外科研究事務局
<4D F736F F D F30315F95CA8E CA48B868A8893AE82C98AD682B782E B396688E7E8CA48F4393E097658B7982D18EF38D7595FB >
 別紙 2 研究活動に関する不正防止研修内容及び受講方法 本研修は, 本学で作成している 研究活動に関するハンドブック ( 平成 30 年度版 ) に沿って実施するため, 当該ハンドブックを用意する 研究活動に関するハンドブック ( 本学ホームページ ) https://www.hokudai.ac.jp/research/injustice/handbook/ 1. 研修内容 研修種別 1 研究活動上の不正行為防止
別紙 2 研究活動に関する不正防止研修内容及び受講方法 本研修は, 本学で作成している 研究活動に関するハンドブック ( 平成 30 年度版 ) に沿って実施するため, 当該ハンドブックを用意する 研究活動に関するハンドブック ( 本学ホームページ ) https://www.hokudai.ac.jp/research/injustice/handbook/ 1. 研修内容 研修種別 1 研究活動上の不正行為防止
臨床研究実施計画書
 心臓超音波検査を用いた臨床研究について 御理解 御協力いただける方へ 心エコー図法による心不全患者の予後予測に 関する研究 に関する説明 これは心臓超音波検査の所見の一部を用いた臨床研究への参加についての説明文書です 本臨床研究についてわかりやすく説明しますので 内容を十分ご理解されたうえで 参加するかどうかお決め下さい また ご不明な点などがございましたら遠慮なくご質問下さい 臨床研究代表者 群馬大学医学部附属病院循環器内科
心臓超音波検査を用いた臨床研究について 御理解 御協力いただける方へ 心エコー図法による心不全患者の予後予測に 関する研究 に関する説明 これは心臓超音波検査の所見の一部を用いた臨床研究への参加についての説明文書です 本臨床研究についてわかりやすく説明しますので 内容を十分ご理解されたうえで 参加するかどうかお決め下さい また ご不明な点などがございましたら遠慮なくご質問下さい 臨床研究代表者 群馬大学医学部附属病院循環器内科
CFP®認定に向けて
 CFP エントリー研修 e ラーニング学習の手引き 1. 学習の流れ 以下の流れに沿って学習を進めてください なお FAX にてお申込みをされた場合は e ラーニング学習を選択できませんのでご注意ください (1)e ラーニングサイト (Learning Cast) にアクセス 1 My ページ (https://members.jafp.or.jp/) クイックメニューの CFP エントリー研修 をクリックします
CFP エントリー研修 e ラーニング学習の手引き 1. 学習の流れ 以下の流れに沿って学習を進めてください なお FAX にてお申込みをされた場合は e ラーニング学習を選択できませんのでご注意ください (1)e ラーニングサイト (Learning Cast) にアクセス 1 My ページ (https://members.jafp.or.jp/) クイックメニューの CFP エントリー研修 をクリックします
スライド 1
 専門医共通 / 領域講習の申請について ( 外科領域 ;2018 年 7 月時点 ) Japan Surgical Society 1 専門医共通講習 定 種 形 義 : 各領域の枠を超えた 医師として必要な知識や態度 ( 人間性や社会性を含む ) を扱う講習 別 : 別項 式 : 講習会 / 講演会 講演者は講習内容に精通し 専門的経験を有する者を 1 時間あたり 2 名以内とすること シンポジウム
専門医共通 / 領域講習の申請について ( 外科領域 ;2018 年 7 月時点 ) Japan Surgical Society 1 専門医共通講習 定 種 形 義 : 各領域の枠を超えた 医師として必要な知識や態度 ( 人間性や社会性を含む ) を扱う講習 別 : 別項 式 : 講習会 / 講演会 講演者は講習内容に精通し 専門的経験を有する者を 1 時間あたり 2 名以内とすること シンポジウム
目次 第 1 章治験審査委員会... 3 ( 目的と適用範囲 )... 3 ( 治験審査委員会の責務 )... 3 ( 治験審査委員会の設置及び構成 )... 3 ( 治験審査委員会の業務 )... 4 ( 治験審査委員会の運営 )... 6 第 2 章治験審査委員会事務局... 8 ( 治験審査委
 治験審査委員会標準業務手順書 < 医師主導治験 > 横浜労災病院 目次 第 1 章治験審査委員会... 3 ( 目的と適用範囲 )... 3 ( 治験審査委員会の責務 )... 3 ( 治験審査委員会の設置及び構成 )... 3 ( 治験審査委員会の業務 )... 4 ( 治験審査委員会の運営 )... 6 第 2 章治験審査委員会事務局... 8 ( 治験審査委員会事務局の設置と業務 )... 8
治験審査委員会標準業務手順書 < 医師主導治験 > 横浜労災病院 目次 第 1 章治験審査委員会... 3 ( 目的と適用範囲 )... 3 ( 治験審査委員会の責務 )... 3 ( 治験審査委員会の設置及び構成 )... 3 ( 治験審査委員会の業務 )... 4 ( 治験審査委員会の運営 )... 6 第 2 章治験審査委員会事務局... 8 ( 治験審査委員会事務局の設置と業務 )... 8
る として 平成 20 年 12 月に公表された 規制改革推進のための第 3 次答申 において 医療機器開発の円滑化の観点から 薬事法の適用範囲の明確化を図るためのガイドラインを作成すべきであると提言したところである 今般 薬事法の適用に関する判断の透明性 予見可能性の向上を図るため 臨床研究におい
 都道府県知事 各保健所設置市長殿 特別区長 薬食発 0331 第 7 号 平成 22 年 3 月 31 日 厚生労働省医薬食品局長 臨床研究において用いられる未承認医療機器の提供等に係る 薬事法の適用について 薬事法 ( 昭和 35 年法律第 145 号 ) は 医療機器について品質 有効性及び安全性の確保がなされた製品のみが流通するよう種々の規制を設けているが 薬事法第 14 条第 1 項の承認を受けていない医療機器
都道府県知事 各保健所設置市長殿 特別区長 薬食発 0331 第 7 号 平成 22 年 3 月 31 日 厚生労働省医薬食品局長 臨床研究において用いられる未承認医療機器の提供等に係る 薬事法の適用について 薬事法 ( 昭和 35 年法律第 145 号 ) は 医療機器について品質 有効性及び安全性の確保がなされた製品のみが流通するよう種々の規制を設けているが 薬事法第 14 条第 1 項の承認を受けていない医療機器
01事務局頭紙(千葉大) 千葉大確認後 修正
 申請医療機関からの報告について ( 千葉大学医学部附属病院 ) 1. 経緯 [ 有害事象報告とそれに伴う対応 ] 告示番号 B16 NKT 細胞を用いた免疫療法 ( 頭頸部扁平上皮がん ) において 平成 28 年 11 月 26 日 試験中の患者に急性呼吸不全が生じ 平成 28 年 12 月 18 日に死亡されるという事案が発生した 事務局は平成 28 年 12 月 14 日付け第 1 報を受理
申請医療機関からの報告について ( 千葉大学医学部附属病院 ) 1. 経緯 [ 有害事象報告とそれに伴う対応 ] 告示番号 B16 NKT 細胞を用いた免疫療法 ( 頭頸部扁平上皮がん ) において 平成 28 年 11 月 26 日 試験中の患者に急性呼吸不全が生じ 平成 28 年 12 月 18 日に死亡されるという事案が発生した 事務局は平成 28 年 12 月 14 日付け第 1 報を受理
料 情報の提供に関する記録 を作成する方法 ( 作成する時期 記録の媒体 作成する研究者等の氏名 別に作成する書類による代用の有無等 ) 及び保管する方法 ( 場所 第 12 の1⑴の解説 5に規定する提供元の機関における義務 8 個人情報等の取扱い ( 匿名化する場合にはその方法等を含む ) 9
 北里研究所病院研究倫理委員会研究申請時確認シート ( 補助資料 ) 20170425 Ver.2.0 < 研究計画書の確認 > 記載項目 1 研究の名称 2 研究の実施体制 ( 研究機関の名称及び研究者等の氏名を含む ) 3 研究の目的及び意義 4 研究の方法及び期間 5 研究対象者の選定方針 6 研究の科学的合理性の根拠 7インフォームド コンセントを受ける手続等 ( インフォームド コンセントを受ける場合には
北里研究所病院研究倫理委員会研究申請時確認シート ( 補助資料 ) 20170425 Ver.2.0 < 研究計画書の確認 > 記載項目 1 研究の名称 2 研究の実施体制 ( 研究機関の名称及び研究者等の氏名を含む ) 3 研究の目的及び意義 4 研究の方法及び期間 5 研究対象者の選定方針 6 研究の科学的合理性の根拠 7インフォームド コンセントを受ける手続等 ( インフォームド コンセントを受ける場合には
エ事務部門 (9) 利用者 教職員 学生等及び臨時利用者で 本学情報システムを利用する者をいう (10) 教職員 本学に勤務する常勤又は非常勤の教職員 ( 派遣職員を含む ) をいう (11) 学生等 本学学則に定める学部学生 大学院学生 大学院研究生 科目等履修生及び聴講生 等をいう (12) 臨
 国立大学法人東京医科歯科大学情報システム運用基本規程 平成 21 年 1 月 8 日 規程第 2 号 ( 目的 ) 第 1 条この規程は 国立大学法人東京医科歯科大学 ( 以下 本学 という ) 情報システ ム運用基本方針に基づき 本学情報システムの運用について定める ( 適用範囲 ) 第 2 条この規程は 本学情報システムを運用 管理 利用するすべての者に適用する ( 定義 ) 第 3 条この規程において
国立大学法人東京医科歯科大学情報システム運用基本規程 平成 21 年 1 月 8 日 規程第 2 号 ( 目的 ) 第 1 条この規程は 国立大学法人東京医科歯科大学 ( 以下 本学 という ) 情報システ ム運用基本方針に基づき 本学情報システムの運用について定める ( 適用範囲 ) 第 2 条この規程は 本学情報システムを運用 管理 利用するすべての者に適用する ( 定義 ) 第 3 条この規程において
個人情報保護方針の例
 個人情報の取扱いについて シミックヘルスケア株式会社個人情報保護管理責任者 シミックヘルスケア株式会社 ( 以下 当社 といいます ) は お客様 お取引先様 従業員の方々の個人情報について 個人情報保護方針 ( プライバシー ポリシー ) に従い適正な管理を行うとともに 個人情報の保護に努めます 具体的には 以下の内容に従って個人情報の取り扱いを行います 1. 個人情報取扱事業者の名称シミックヘルスケア株式会社
個人情報の取扱いについて シミックヘルスケア株式会社個人情報保護管理責任者 シミックヘルスケア株式会社 ( 以下 当社 といいます ) は お客様 お取引先様 従業員の方々の個人情報について 個人情報保護方針 ( プライバシー ポリシー ) に従い適正な管理を行うとともに 個人情報の保護に努めます 具体的には 以下の内容に従って個人情報の取り扱いを行います 1. 個人情報取扱事業者の名称シミックヘルスケア株式会社
Microsoft Word - JONIE-TR 患者説明書.docx
 患者さんへ :JONIE-1 試験の付随研究の説明 原発乳癌に対する術前化学療法にゾレドロン酸併用のランダム化比較試験にご参加いただいた患者様に 本試験の付随研究としてゾレドロン酸の治療効果を予測する仕組みを解明するために以下の追加研究を計画しましたのご報告するとともに すでに各病院にて保管されています病理組織検体を利用させて頂くことに関してご理解いただきたく存じます 研究対象は組織検体ですので
患者さんへ :JONIE-1 試験の付随研究の説明 原発乳癌に対する術前化学療法にゾレドロン酸併用のランダム化比較試験にご参加いただいた患者様に 本試験の付随研究としてゾレドロン酸の治療効果を予測する仕組みを解明するために以下の追加研究を計画しましたのご報告するとともに すでに各病院にて保管されています病理組織検体を利用させて頂くことに関してご理解いただきたく存じます 研究対象は組織検体ですので
PowerPoint プレゼンテーション
 研修申込システム 利用者マニュアル 第二版 2019/2/04 東京都医師会広報学術情報課 変更履歴 版変更自由日付担当者備考 初版初回作成 2018/12/7 黒木 第二版決済機能追加 2019/2/4 黒木 1 目次 1. 全体像 (1) 概要図 3 (2) 説明 3 2. 利用者 ID 4 3. システム利用方法 (1) 個人情報登録 5 (2) 個人情報入力画面 6 (3) 研修一覧画面 7
研修申込システム 利用者マニュアル 第二版 2019/2/04 東京都医師会広報学術情報課 変更履歴 版変更自由日付担当者備考 初版初回作成 2018/12/7 黒木 第二版決済機能追加 2019/2/4 黒木 1 目次 1. 全体像 (1) 概要図 3 (2) 説明 3 2. 利用者 ID 4 3. システム利用方法 (1) 個人情報登録 5 (2) 個人情報入力画面 6 (3) 研修一覧画面 7
改訂履歴 (2015 年度 ~) 版数 改訂日 概要 第 9 版 2015 年 4 月 1 日 - 第 10 版 2015 年 4 月 1 日 領域名対応表の改訂 受講者リスト ( グループ毎 ) の説明の追加 第 11 版 2015 年 6 月 1 日 仕様変更にともない全受講者リストの説明を修正
 CITI Japan プロジェクト CITI Japan 成績管理者マニュアル 第 17.1 版 平成 28 年 10 月 11 日 CITI JAPAN PROGRAM 1/36 改訂履歴 (2015 年度 ~) 版数 改訂日 概要 第 9 版 2015 年 4 月 1 日 - 第 10 版 2015 年 4 月 1 日 領域名対応表の改訂 受講者リスト ( グループ毎 ) の説明の追加 第 11
CITI Japan プロジェクト CITI Japan 成績管理者マニュアル 第 17.1 版 平成 28 年 10 月 11 日 CITI JAPAN PROGRAM 1/36 改訂履歴 (2015 年度 ~) 版数 改訂日 概要 第 9 版 2015 年 4 月 1 日 - 第 10 版 2015 年 4 月 1 日 領域名対応表の改訂 受講者リスト ( グループ毎 ) の説明の追加 第 11
受講マニュアル
 研究倫理 e ラーニング受講マニュアル (ver.2.3) 日本学術振興会 Copyright 2018 JSPS All Rights Reserved. 2 目次 受講の進め方についてご説明します 1. 推奨環境 P3 2. マイルーム へログイン P4 3. マイルーム から学習ページに入る P5 4. 本 eラーニング内での学習 P6 4-1. 各種メニューボタン ページ遷移ボタン P7 4-2.
研究倫理 e ラーニング受講マニュアル (ver.2.3) 日本学術振興会 Copyright 2018 JSPS All Rights Reserved. 2 目次 受講の進め方についてご説明します 1. 推奨環境 P3 2. マイルーム へログイン P4 3. マイルーム から学習ページに入る P5 4. 本 eラーニング内での学習 P6 4-1. 各種メニューボタン ページ遷移ボタン P7 4-2.
個人としての利益相反マネジメントの運用指針 平成 30 年 7 月 9 日 利益相反マネジメント委員会決定 個人としての利益相反を適切に管理するため 以下の運用指針を定め実施することとする 1. 利益相反マネジメントの対象事象国立大学法人岡山大学利益相反マネジメント規程第 3 条に規定される行為につ
 個人としての利益相反マネジメントの運用指針 平成 30 年 7 月 9 日 利益相反マネジメント委員会決定 個人としての利益相反を適切に管理するため 以下の運用指針を定め実施することとする 1. 利益相反マネジメントの対象事象国立大学法人岡山大学利益相反マネジメント規程第 3 条に規定される行為について 次に掲げるものを対象とする (1) 国立大学法人岡山大学職員兼業規程により承認を得て行う兼業 1
個人としての利益相反マネジメントの運用指針 平成 30 年 7 月 9 日 利益相反マネジメント委員会決定 個人としての利益相反を適切に管理するため 以下の運用指針を定め実施することとする 1. 利益相反マネジメントの対象事象国立大学法人岡山大学利益相反マネジメント規程第 3 条に規定される行為について 次に掲げるものを対象とする (1) 国立大学法人岡山大学職員兼業規程により承認を得て行う兼業 1
緩和ケア研修会における e-learning の導 について 市 札幌病院精神医療センター副医 上村恵 ( 特定 営利活動法 本緩和医療学会委託事業委員会委員 )
 緩和ケア研修会における e-learning の導 について 市 札幌病院精神医療センター副医 上村恵 ( 特定 営利活動法 本緩和医療学会委託事業委員会委員 ) これまでの緩和ケア研修会 研修対象者 がん診療に携わる全ての医師 科医師が対象 その他の医療従事者の参加は妨げない がん診療連携拠点病院に所属しているがん診療 に携わる医師 科医師は全て受講すること 開催期間 2 以上で開催し 実質的な研修会時間の合計は
緩和ケア研修会における e-learning の導 について 市 札幌病院精神医療センター副医 上村恵 ( 特定 営利活動法 本緩和医療学会委託事業委員会委員 ) これまでの緩和ケア研修会 研修対象者 がん診療に携わる全ての医師 科医師が対象 その他の医療従事者の参加は妨げない がん診療連携拠点病院に所属しているがん診療 に携わる医師 科医師は全て受講すること 開催期間 2 以上で開催し 実質的な研修会時間の合計は
<4D F736F F F696E74202D EA18CB18AD B68F9182C982A882AF82E993648EA593498B4C985E82CC8A C98AD682B782E98AEE967B93498D6C82A695FB817682CC82DC82C682DF817C8F4390B32E >
 治験関連文書における電磁的記録の 活用に関する基本的考え方 のまとめ JSQA GCP 部会特別プロジェクト 3 1 GCPにおいて 治験に係る様々な文書の交付及び保存が規定されていますが 治験関連業務の効率化として電磁的記録の更なる活用が期待されています これに伴い 平成 25 年 7 月 1 日に事務連絡 1) が発出され その後 平成 26 年 7 月 1 日に一部改正 された事務連絡 2)
治験関連文書における電磁的記録の 活用に関する基本的考え方 のまとめ JSQA GCP 部会特別プロジェクト 3 1 GCPにおいて 治験に係る様々な文書の交付及び保存が規定されていますが 治験関連業務の効率化として電磁的記録の更なる活用が期待されています これに伴い 平成 25 年 7 月 1 日に事務連絡 1) が発出され その後 平成 26 年 7 月 1 日に一部改正 された事務連絡 2)
( 様式 1-1) 日本専門医機構認定形成外科専門医資格更新申請書 20 年月日フリガナ 氏 名 生年月日年月日 所属施設 ( 病院 医院 ) 名 勤務先住所 連絡先 ( 電話 : - - ) ( FAX : - - ) アドレス 1: アドレス 2: 専門医登録番号 - 医籍登録番号
 形成外科領域専門医更新様式等一覧 様式 1-1 日本専門医機構認定形成外科専門医資格更新申請書 1-2 単位集計表 様式 2 勤務実態の自己申告書 様式 3 形成外科診療実績記録 ( 過去 5 年間 ) 様式 4 手術症例一覧表 (4-1~4-5) 様式 5 症例一覧表 (5-1~5-5) 様式 6-1 専門医共通講習受講実績記録 6-2 専門医共通講習受講証明書類貼付台紙 様式 7 形成外科領域講習受講実績記録
形成外科領域専門医更新様式等一覧 様式 1-1 日本専門医機構認定形成外科専門医資格更新申請書 1-2 単位集計表 様式 2 勤務実態の自己申告書 様式 3 形成外科診療実績記録 ( 過去 5 年間 ) 様式 4 手術症例一覧表 (4-1~4-5) 様式 5 症例一覧表 (5-1~5-5) 様式 6-1 専門医共通講習受講実績記録 6-2 専門医共通講習受講証明書類貼付台紙 様式 7 形成外科領域講習受講実績記録
( 様式第 6) 病院の管理及び運営に関する諸記録の閲覧方法に関する書類 病院の管理及び運営に関する諸記録の閲覧方法 計画 現状の別 1. 計画 2. 現状 閲 覧 責 任 者 氏 名 閲 覧 担 当 者 氏 名 閲覧の求めに応じる場所 閲覧の手続の概要 ( 注 ) 既に医療法施行規則第 9 条の
 ( 様式第 6) 病院の管理及び運営に関する諸記録の閲覧方法に関する書類 病院の管理及び運営に関する諸記録の閲覧方法 計画 現状の別 1. 計画 2. 現状 閲 覧 責 任 者 氏 名 閲 覧 担 当 者 氏 名 閲覧の求めに応じる場所 閲覧の手続の概要 ( 注 ) 既に医療法施行規則第 9 条の 20 第 5 号の規定に合致する方法により記録を閲覧させている病院は現状について その他の病院は計画について記載することとし
( 様式第 6) 病院の管理及び運営に関する諸記録の閲覧方法に関する書類 病院の管理及び運営に関する諸記録の閲覧方法 計画 現状の別 1. 計画 2. 現状 閲 覧 責 任 者 氏 名 閲 覧 担 当 者 氏 名 閲覧の求めに応じる場所 閲覧の手続の概要 ( 注 ) 既に医療法施行規則第 9 条の 20 第 5 号の規定に合致する方法により記録を閲覧させている病院は現状について その他の病院は計画について記載することとし
1. 人を対象とする医学系研究の実施に係る手順書 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本規程は ヘルシンキ宣言の倫理的原則に則り 人を対象とする医学系研究に関する倫理指針 ( 平成 26 年文部科学省 厚生労働省告示第 3 号 ; 以下 倫理指針 という ) 及び関連する最新
 人を対象とする医学系研究に係る 標準業務手順書 2016 年 6 月 23 日 第 1 版 2016 年 7 月 28 日 第 2 版 2017 年 1 月 26 日 第 3 版 大垣市民病院 臨床研究審査委員会 1. 人を対象とする医学系研究の実施に係る手順書 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本規程は ヘルシンキ宣言の倫理的原則に則り 人を対象とする医学系研究に関する倫理指針
人を対象とする医学系研究に係る 標準業務手順書 2016 年 6 月 23 日 第 1 版 2016 年 7 月 28 日 第 2 版 2017 年 1 月 26 日 第 3 版 大垣市民病院 臨床研究審査委員会 1. 人を対象とする医学系研究の実施に係る手順書 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本規程は ヘルシンキ宣言の倫理的原則に則り 人を対象とする医学系研究に関する倫理指針
別紙 1 平成 31 年度 (2019 年度 ) 科学研究費助成事業 ( 科学研究費補助金 )( 奨励研究 ) 交付申請要項 個人で補助金の管理を行うこととなる研究代表者は 以下により交付申請に係る手続きを遺漏なく行ってください なお 応募以降 交付申請までに新たに 科学研究費補助金取扱規程 ( 昭
 別紙 1 平成 31 年度 (2019 年度 ) 科学研究費助成事業 ( 科学研究費補助金 )( 奨励研究 ) 交付申請要項 個人で補助金の管理を行うこととなる研究代表者は 以下により交付申請に係る手続きを遺漏なく行ってください なお 応募以降 交付申請までに新たに 科学研究費補助金取扱規程 ( 昭和 40 年 3 月 30 日文部省告示 ) 第 2 条に規定する研究機関 ( 別紙 2 参照 ) に所属することとなった研究代表者又は所属する研究機関を変更する研究代表者は
別紙 1 平成 31 年度 (2019 年度 ) 科学研究費助成事業 ( 科学研究費補助金 )( 奨励研究 ) 交付申請要項 個人で補助金の管理を行うこととなる研究代表者は 以下により交付申請に係る手続きを遺漏なく行ってください なお 応募以降 交付申請までに新たに 科学研究費補助金取扱規程 ( 昭和 40 年 3 月 30 日文部省告示 ) 第 2 条に規定する研究機関 ( 別紙 2 参照 ) に所属することとなった研究代表者又は所属する研究機関を変更する研究代表者は
倫理審査申請システム利用ガイド(申請者編)
 京都大学大学院医学研究科 医学部 及び医学部附属病院医の倫理委員会 京都大学特定認定再生医療等委員会 倫理審査申請システム利用ガイド 申請者編 平成 30 年 5 月版 目 次 1 システムの利用準備...- 3-1.1 システムの起動...- 3-1.2 ログイン (SPS-ID または ECS-ID をお持ちの方 )...- 4-1.3 ログイン ( 学外ユーザー )...- 4-1.4 ユーザー登録依頼...-
京都大学大学院医学研究科 医学部 及び医学部附属病院医の倫理委員会 京都大学特定認定再生医療等委員会 倫理審査申請システム利用ガイド 申請者編 平成 30 年 5 月版 目 次 1 システムの利用準備...- 3-1.1 システムの起動...- 3-1.2 ログイン (SPS-ID または ECS-ID をお持ちの方 )...- 4-1.3 ログイン ( 学外ユーザー )...- 4-1.4 ユーザー登録依頼...-
受講マニュアル
 研究倫理 e ラーニング受講マニュアル (ver.2.1) 日本学術振興会 2 目次 受講の進め方についてご説明します 1. 推奨環境 P3 2. マイルーム へログイン P4 3. マイルーム から学習ページに入る P5 4. 本 eラーニング内での学習 P6 4-1. 各種メニューボタン ページ遷移ボタン P7 4-2. 事例学習の進め方 P8 4-3. テストの受験 P10 4-4. コースレビュー
研究倫理 e ラーニング受講マニュアル (ver.2.1) 日本学術振興会 2 目次 受講の進め方についてご説明します 1. 推奨環境 P3 2. マイルーム へログイン P4 3. マイルーム から学習ページに入る P5 4. 本 eラーニング内での学習 P6 4-1. 各種メニューボタン ページ遷移ボタン P7 4-2. 事例学習の進め方 P8 4-3. テストの受験 P10 4-4. コースレビュー
目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2
 免疫アレルギー疾患等実用化研究事業 ( 移植医療技術開発研究分野 ) 2019 年度 1 次公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 戦略推進部 難病研究課 2018 年 11 月 1 目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2 1. はじめに
免疫アレルギー疾患等実用化研究事業 ( 移植医療技術開発研究分野 ) 2019 年度 1 次公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 戦略推進部 難病研究課 2018 年 11 月 1 目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2 1. はじめに
Microsoft Word - 要綱変更 最終.docx
 一般社団法人日本医学教育学会認定医学教育専門家資格制度要綱 2014 年 8 月 10 日制定 2016 年 4 月 22 日改正 日本医学教育学会 ( 以下 本学会 ) によって 1974 年に医学教育者のためのワークショップ ( 富士研 ) が実施されて以降 40 年近くの間に 臨床研修指導医養成講習会や各大学主催の医学教育のワークショップを通じてワークショップ形式による医学教育の指導者 教員養成が定着した
一般社団法人日本医学教育学会認定医学教育専門家資格制度要綱 2014 年 8 月 10 日制定 2016 年 4 月 22 日改正 日本医学教育学会 ( 以下 本学会 ) によって 1974 年に医学教育者のためのワークショップ ( 富士研 ) が実施されて以降 40 年近くの間に 臨床研修指導医養成講習会や各大学主催の医学教育のワークショップを通じてワークショップ形式による医学教育の指導者 教員養成が定着した
 別冊 平成 30 年度 科学研究費助成事業 募集要領 特別研究員奨励費 特別研究員 ( 応募書類の様式 入力要領 ) 平成 30 年 1 月 独立行政法人日本学術振興会 (http://www.jsps.go.jp/) 1 平成 30 年度科学研究費助成事業 ( 特別研究員奨励費 )( 特別研究員 ) 研究計画調書 (Web 入力項目 ) 画面イメージ ----------------------------------------------------
別冊 平成 30 年度 科学研究費助成事業 募集要領 特別研究員奨励費 特別研究員 ( 応募書類の様式 入力要領 ) 平成 30 年 1 月 独立行政法人日本学術振興会 (http://www.jsps.go.jp/) 1 平成 30 年度科学研究費助成事業 ( 特別研究員奨励費 )( 特別研究員 ) 研究計画調書 (Web 入力項目 ) 画面イメージ ----------------------------------------------------
静岡県立静岡がんセンター臨床研究事務局の業務手順書
 治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 6.0 平成 20 年 1 月 28
治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 6.0 平成 20 年 1 月 28
<4D F736F F F696E74202D C E9197BF A90EA96E58AC58CEC8E E88AC58CEC8E F0977B90AC82B782E98AF991B682CC89DB92F682C682CC8AD68C5782C982C282A282C42E >
 カリキュラムについて 専門看護師 等を養成する既存の課程との関係について 論点 1 資料 2 専門看護師 等を養成する既存の課程が 特定行為の習得のための教育を併せて行う場合 当該課程を指定する際に留意すべき事項は何か 教育 研修を行う機関では 専門看護師 等を養成するための教育内容と 特定行為の習得のための教育内容等基準とを組み合わせ 独自のカリキュラム (123) を策定すると想定している その場合
カリキュラムについて 専門看護師 等を養成する既存の課程との関係について 論点 1 資料 2 専門看護師 等を養成する既存の課程が 特定行為の習得のための教育を併せて行う場合 当該課程を指定する際に留意すべき事項は何か 教育 研修を行う機関では 専門看護師 等を養成するための教育内容と 特定行為の習得のための教育内容等基準とを組み合わせ 独自のカリキュラム (123) を策定すると想定している その場合
製造販売後調査事務手続き等 について
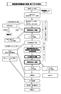 製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
医師主導治験実施医療機関を対象とした調査協力のお願い Ver 医師主導治験における治験調整事務局業務の標準化 効率化に関する研究 班へのご協力をいただき ありがとうございます 本研究班では 医師主導治験を実施する医療機関において 準備や実施に役立つ教育コンテンツやモデル標準業務手順
 医師主導治験実施医療機関を対象とした調査協力のお願い 医師主導治験における治験調整事務局業務の標準化 効率化に関する研究 班へのご協力をいただき ありがとうございます 本研究班では 医師主導治験を実施する医療機関において 準備や実施に役立つ教育コンテンツやモデル標準業務手順書 ロードマップなどを作成し 公開することを目指しています 本調査では 医師主導治験の現状やニーズに沿った成果物を提供するため
医師主導治験実施医療機関を対象とした調査協力のお願い 医師主導治験における治験調整事務局業務の標準化 効率化に関する研究 班へのご協力をいただき ありがとうございます 本研究班では 医師主導治験を実施する医療機関において 準備や実施に役立つ教育コンテンツやモデル標準業務手順書 ロードマップなどを作成し 公開することを目指しています 本調査では 医師主導治験の現状やニーズに沿った成果物を提供するため
治 験 実 施 標 準 業 務 手 順 書
 治験審査委員会標準業務手順書 < 企業治験 > 横浜労災病院 目 次 第 1 章治験審査委員会 2 目的と適用範囲 2 治験審査委員会の責務 2 治験審査委員会の設置及び構成 2 治験審査委員会の業務 3 治験審査委員会の運営 5 第 2 章治験審査委員会事務局 6 治験審査委員会事務局の設置と業務 6 第 3 章記録の保存と公開 7 記録の保存責任者 7 記録の保存期間 7 記録の公開 8 1 第
治験審査委員会標準業務手順書 < 企業治験 > 横浜労災病院 目 次 第 1 章治験審査委員会 2 目的と適用範囲 2 治験審査委員会の責務 2 治験審査委員会の設置及び構成 2 治験審査委員会の業務 3 治験審査委員会の運営 5 第 2 章治験審査委員会事務局 6 治験審査委員会事務局の設置と業務 6 第 3 章記録の保存と公開 7 記録の保存責任者 7 記録の保存期間 7 記録の公開 8 1 第
