目次 1. 法改正の動き 輸入規制 手続き 流通販売時の規制 手続き 化粧品規格基準 表示ラベル規則 容器包装規制 関税 付加価値税等国内諸税 問い合わせ先リスト インドネシアの化粧品に関
|
|
|
- かつかげ こうい
- 8 years ago
- Views:
Transcription
1 H23 年度海外輸入制度調査 インドネシアにおける化粧品の輸入制度 2011 年 12 月 独立行政法人日本貿易振興機構ジャカルタ事務所
2 目次 1. 法改正の動き 輸入規制 手続き 流通販売時の規制 手続き 化粧品規格基準 表示ラベル規則 容器包装規制 関税 付加価値税等国内諸税 問い合わせ先リスト インドネシアの化粧品に関する規則リンク一覧... 9
3 1. 法改正の動き 2009 年 9 月にアセアン加盟国が署名した化粧品の管理 規制に関する統一規則の枠組み (ASEAN Harmonized Cosmetic Regulatory Scheme) にて アセアン各国は 2003 ~07 年の間に化粧品登録認証の相互承認協定 (MRA) を批准すること さらに 2008 年からは化粧品の管理に関する統一規則であるアセアン化粧品指令 (ASEAN Cosmetic Directive: ACD) を各国内で適用すること が決まった このうちインドネシアは ACD の適用のみ実行する方針を固めていたが 2008 年の即実行はならず 2010 年になってようやく国内法令の改訂が始まった まずは 化粧品の国内販売のための流通許可制度が見直された これは ACD において それまでの事前許可 ( pre-market approval ) 制度から流通後監督 (post-market-surveillance) 制度に移行させることが定められていることによるものとされており 2010 年 8 月 20 日付け保健大臣規則 No.1176/MENKES/PER/VIII/2010 により化粧品の流通許可は Notification= 通知のかたちで行われることに変更された 流通許可の Notification 形式への移行により 化粧品の輸入についての法令も 2011 年 4 月 20 日付けインドネシア国家食品医薬品監督庁 (BPOM) 長官規則 No. HK にて改められている また 2010 年 8 月 20 日付け保健大臣規則 No.1176/MENKES/PER/VIII/2010 により BPOM による化粧品の流通後監督活動に備え 化粧品の品質 安全性 効用についてのデータで構成される製品情報書類 (Dokumen Informasi Produk: DIP) を準備しておくことも定められ DIP についての実施細則として 2010 年 12 月 16 日付け BPOM 長官規則 No が発行された 一方 2010 年 12 月 27 日付け BPOM 長官規則 No.HK において 化粧品の品質条件は ACD 第 9 条の規定に従う と明記された 同規則は品質条件のほか 安全性の条件やラベル クレームなどについても規定したもので 化粧品全般について定められた旧令の 2003 年 5 月 5 日付け BPOM 長官規則 No.HK はいまだ有効であるものの ACD を意識した方向に動いたことになる 化粧品の原材料についての規則も 上記の化粧品の Notification による流通許可について定めた保健大臣規則 No.1176/Menkes/Per/VIII/2010 を受けて改訂された これは 2011 年 9 月 29 日付け BPOM 長官規則 No. HK で 使用が認められる原材料および使用が禁止される原材料の一覧には ACD 番号も出ており ACD を意識しているのは明らかである 安全面では 化粧品の微生物や重金属による汚染上限を決めた規定が見直された 新令は 2011 年 7 月 12 日付け BPOM 長官規則 HK で 2007 年のアセア 1
4 ン化粧品委員会 (ACC) での合意規定に合わせた とその目的がうたわれている なお 化粧品優良製造方法 (CPKB) についてはいまだ 1992 年 11 月 4 日付け保健大臣規則 No.965/MENKES/SK/XI/1992 および 2003 年 10 月 20 日付け BPOM 長官規則 No.HK が有効であるが 2010 年に入り 2010 年 6 月 21 日付け BPOM 長官規則 No.HK にてさらに CPKB の指針が示されており アセアン CPKB が反映されたものと期待される 2. 輸入規制 手続き 化粧品の輸入について改めた 2011 年 4 月 20 日付け BPOM 長官規則 No. HK では 化粧品の輸入が認められるのは商業省からの輸入者認定番号 (API) を有する輸入業者 としか規定されておらず 一般の輸入業者でも可能のように読めるが 化粧品の国内流通許可について改訂した 2010 年 8 月 20 日付け保健大臣規則 No.1176/MENKES/PER/VIII/2010 では 化粧品の輸入者は API のほか 原産国の製造者からの代理店指名を有することとしている つまり 化粧品の輸入ができるのは インドネシアでの代理店としての指名を得た API ホルダーでなければならないことになる 一方で BPOM 長官規則 No. HK はまた 化粧品の輸入はシップメントごとに BPOM 長官から国内への搬入承認を取得するよう定めている この申請は 輸入しようとする化粧品の流通許可を取得した者 / 流通許可のための Notification を行った者が行うこととされており 化粧品の輸入は API を有し 原産国の製造業者からの代理店指名を受けているほか 当該の化粧品の流通許可保有者 / 流通許可のための Notification を有する者自身でなければならない 当然のことながら 輸入が認められる化粧品は インドネシア国内での化粧品流通許可を取得した商品に限られている ( 以上 流通許可 /Notification については後述 ) なお 化粧品輸入の搬入承認の申請には 次の書類が必要である : a. 化粧品の分析証明 b. インボイス : 記載される商品名は 流通許可 / 流通許可のための Notification に記載されている名称と同じでなければならない c. B/L あるいは AWB d. 申請人の納税者番号 (NPWP) e. 申請人の API 2
5 f. プロポーザルおよび / あるいはその他の必要な書類 ( 調査研究や展示会でのサンプルの目的で限られた数量だけ輸入される化粧品の場合 ) 搬入承認の申請は BPOM のサイトを通じた電子申請も可能になった ( アドレスは 審査を経て 搬入承認が輸入証明書(SKI) のかたちで発行される このほか 化粧品 (HS3304) シャンプー類(HS3305) 石鹸類(HS3401) を含む特定の品目の輸入は 商業大臣より特定製品登録輸入業者 (IT-Produk Tertentu) に認定された輸入業者に限定する政策がとられている 最新の法令 2010 年 12 月 29 日付け商業大臣規則 No.57/M-DAG/PER/12/2010 は 2011 年内有効とされているが この政策は今後も継続される可能性もあるので 注意が必要である 参考までに商業大臣規則 No.57/M-DAG/PER/12/2010 を紹介すると IT-Produk Tertentu の指名を受けるには 商業省国際貿易総局輸入局長宛てに申請する この申請には次の書類を添付する : a. API コピー b. 商業省が発行する会社登録証 (TDP) のコピー c. NPWP コピー d. 財務省関税総局が交付する通関基本番号 (NIK) のコピー e. 過去 12 カ月間における化粧品の輸入実現累積についての表明書 HS コード 10 桁ベースで報告 f. 向こう 1 年間の輸入計画 数量 輸入品の種類 HS コード 目的港などまた 化粧品の輸入は次の港に限られている : a. 海洋港 : ブラワン港 ( 北スマトラ州メダン ) タンジュンプリオク港( ジャカルタ ) タンジュンマス港 ( 中部ジャワ州スマラン ) タンジュンペラック港( 東ジャワ州スラバヤ ) スカルノハッタ港( 南スラウェシ州マカッサル ) b. 全国の国際空港なお 船積み前検査は課されていない 以上より 輸入通関時には 通常の輸入と同様に API TDP NIK 納税者番号(NPWP) のコピー インボイス パッキングリスト BL/AWB(Bill of lading/air way Bill) 保険証券 輸入関税および輸入関連諸税の納付証明 (SSPCP) のほか 搬入承認である輸入証明書 (SKI) の添付が必要である 場合によっては 化粧品の流通許可 / 流通許可のための Notification や特定製品登録輸入業者 (IT-Produk Tertentu) の認定書の提示も求められることが予想される 3
6 3. 流通販売時の規制 手続き 化粧品の国内流通許可について改めた 2010 年 8 月 20 日付け保健大臣規則 No.1176/MENKES/PER/VIII/2010 およびその細則である同年 12 月 13 日付け BPOM 長官規則 No.HK によると 国内で販売される化粧品にはすべて事前に流通許可 (Izin Edar) を取得することが引き続き義務付けられているが その形式は ACD に合わせて Notification= 通知のかたちに改められた 流通許可の申請 /Notification は BPOM へ 当該の化粧品の国内流通前に提出する 海外からの化粧品の場合は 上述のように輸入に際して流通許可 /Notification の提示が必要なため 輸入実施の前に行わなければならない 申請者の条件は : a. インドネシア国内で化粧品製造を行う 化粧品製造許可を保有する製造業者 b. API および原産国の製造者からの代理店指名を有する化粧品輸入業者 c. 化粧品製造許可を有する化粧品製造業者と生産契約を結び これを実行している個人あるいは事業体申請は BPOM の専用サイト ( を通じて行えるようになり その手順は : 1. 申請者登録する 2. 化粧品流通登録のための通知 (Notification) 申請フォームに記入 3. 申請受付から 14 営業日以内に申請拒否通知がない場合 Notification は認められたものと見なされる なお 流通許可 /Notification の有効期間は 従来の 5 年から 3 年に短縮された 更新は可能である 流通許可 /Notification が認められる化粧品は 化粧品優良製造方法 (CPKB) を適用 し 技術的条件 ( 安全性 原料 表示 クレームの条件を含む ) を満たして製造された 化粧品とされている ( 以上 CPKB および技術的条件については後述参照 ) 保健大臣規則 No.1176/MENKES/PER/VIII/2010 および BPOM 長官規則 No.HK はまた 化粧品の輸入業者には化粧品流通登録のための Notification をする前に 製品情報書類 (DIP) を準備しておく必要があると定めている DIP については 2010 年 12 月 16 日付け BPOM 長官規則 No に規定があるが 当該の化粧品の品質 安全性 効用についてのデータで BPOM の調査 / 監査時などにいつでも提示できるように準備しておかなければならないとされている 4
7 4. 化粧品規格基準 2003 年 5 月 5 日付け BPOM 長官決定 No.HK にて インドネシアで流通する化粧品は インドネシア保健大臣令で定められる化粧品基準書 Kodeks Kosmetika Indonesia またはその他の認められた基準に従った品質条件を満たしたものでなければならないと規定されている Kodeks Kosmetika Indonesia については BPOM または保健省に問い合わせる必要がある なお インドネシア国家規格 (Standar Nasional Indonesia: SNI) の強制認証は 化粧品には現時点ではまだ課されていない また前述のとおり 国内で販売される化粧品は化粧品優良製造方法 (CPKB) を適用し 技術的条件を満たして製造されたものでなければならないとされている CPKB については 1992 年 11 月 4 日付け保健大臣規則 No.965/MENKES/SK/XI/ 年 10 月 20 日付け BPOM 長官規則 No.HK 年 6 月 21 日付け BPOM 長官規則 No.HK に規定があるが メーカーにおける人的資源 施設と設備 衛生面 製造 / 加工と梱包 品質管理 内部検査 / 監査 書類保管 蔵置 クレーム処理と製品回収についての指針や基準を示したもので 輸入化粧品についても生産国での体制がこれら基準を満たしていないとならないとしている 一方 化粧品の技術的条件については 2010 年 12 月 27 日付け BPOM 長官規則 No.HK に規定がある ここでいう技術的条件とは 安全性 原料 表示 クレームの条件を含むもので BPOM 長官規則 No.HK では ACD 第 9 条の品質基準を満たすことなど 定めている ( うち 表示については後述参照 ) 特に化粧品の原材料については 2011 年 9 月 29 日付け BPOM 長官規則 No. HK にて見直され 条件付で使用が認められる化粧品の原料 110 種類 ( 旧 76 種類 ) 色料 保存材 紫外線防止剤として使用が認められる原料( 順に 種類 旧は 種類 ) 使用が禁止される原材料 1,370 種類 ( 旧 1,243 種類 ) が示されている 使用が認められる原材料は増加したが 使用禁止原材料も増えた これら使用が禁止される原料 使用が条件付きで認められる原料 使用が全面的に認められる原料の一覧は BPOM 長官規定 HK の添付 I から V にあり 詳細は BPOM のサイト ( の法令のページで確認できる なお 化粧品の微生物や重金属による汚染上限の定めもある 2011 年 7 月 12 日付け BPOM 長官規則 HK によると インドネシア国内に流通する化粧品は 一般生菌数 (Total Plate Count) カビ 酵母数値 緑膿菌 黄色ブドウ球菌 カンジダ アルビカンスの含有が 次のような基準を上回ってはならないとされている 5
8 微生物汚染の条件 以下に使用する化粧品 ⅰ. 幼児用 (3 歳以下 ) ⅱ. 目の周辺に使用 ⅲ. 咽喉部に使用 それ以外の化粧品 一般生菌数 (Total Plate Count) コロニー /g(ml) 未満 コロニー /g(ml) 未満 カビ 酵母数値 コロニー /g(ml) 未満 コロニー /g(ml) 未満 緑膿菌 陰性サンプル 0.1g(ml) あたり 陰性サンプル 0.1g(ml) あたり 黄色ブドウ球菌 陰性サンプル 0.1g(ml) あたり 陰性サンプル 0.1g(ml) あたり カンジダ アルビカンス 陰性サンプル 0.1g(ml) あたり 陰性サンプル 0.1g(ml) あたり 重金属物質の条件 汚染物資 条件 水銀 鉛 ヒ素 1 mg /kg あるいは 1 mg /l(1ppm) 未満 20 mg /kg あるいは 20 mg /l(20ppm) 未満 5 mg /kg あるいは 5 mg /l(5ppm) 未満 5. 表示ラベル規則 容器包装規制 化粧品の表示義務については 化粧品全般について定めた 2003 年 5 月 5 日付け BPOM 長官決定 No.HK に 化粧品の容器および包装に製品情報の表示をしなければならないと定められている 表示の内容は事前に BPOM に届けて承認を受けなければならず 実際の表示内容はこの承認されたデータと同じでなければならない これ以外の表示をする場合には BPOM 長官の承認を事前に追加で受ける なお 医薬品を思わせるような表示は許可されない 化粧品の技術的条件について定めた 2010 年 12 月 27 日付け BPOM 長官規則 No.HK によると 表示はインドネシア語で効用 使用方法 警告や説明などについて記載することとされている さらに 同法令は最低限の表示内容として 次も列挙しているが これは外国語でもよいようである : a. 製品名 : 一般的な製品名でも商品名でもよい b. 効用 c. 使用方法 d. 原材料 : 化粧品原料の国際命名法 (International Nomenclature of Cosmetic Ingredients=INCI) に従ったもの 6
9 e. 製造者の名称と国名 f. 化粧品流通登録のための通知 (Notification) 申請者の名称と住所 g. バッチ番号 h. サイズ 内容量 ( ネット ) i. 使用有効期限 j. 警告 注意書き その他の説明 輸入化粧品の場合 パッケージなどに外国語で上記にかかわる表示があるが こうし た場合はインドネシア語で効用 使用方法 その他の説明や警告について記載したシー ルが別にパッケージに貼られていることが多い 6. 関税 付加価値税等国内諸税 化粧品の輸入時に輸入関税が 10%(CEPT 適用の場合は 5%) 付加価値税が 10% かかる また 所得税の前払い (PPh-22) の義務もあり ( 年次申告時に法人税と相殺 ) その税率は API を有する輸入業者の場合は 2.5% その他の者による輸入の場合は 7.5% である 7. 問い合わせ先リスト a. 国家食品医薬品監督庁 (Badan Pengawasan Obat dan Makanan: BPOM) 住所 :Jl. Percetakan Negara No.23, Jakarta 10560, Indonesia 電話 : /4288/3309/4288/3462 Fax : [email protected] Web : b. インドネシア保健省住所 :Jl. H. S. Rasuna Said Blok X.5, Kav. 4-9, Kuningan, Jakarta 12950, Indonesia Web : c. インドネシア財務省関税総局住所 :Jl. Jend. Ahmad Yani, Jakarta 10710, Indonesia Web : d. インドネシア商業省住所 :Jl. M.I.Ridwan Rais No.5, Jakarta Pusat, Indonesia 7
10 電話 : Web : e. インドネシア化粧品会社連合 (PERKOSMI) 住所 :Plaza Tendean 3 rd Floor, Jl.Kapt. Tendean No.45, Jakarta, Indonesia 電話 : f. 輸入業者リスト (1) PT Clarindotama Perdana ( 取り扱いブランド Clarins) 住所 :Mayapada Tower 16 th Fl., Jl. Jend. Sudirman Kav. 28, JAKARTA, Indonesia 電話 : Fax : (2) PT Dian Tarunaguna 住所 :ITC Cempaka Mas 11 th Fl., Jl. Letjen. Suprapto Kav. I, JAKARTA 10640, Indonesia 電話 : Fax : (3) CV Elite Lestari Jaya( 同 la prairie) 住所 :Jl. Hang Tuah Raya I, Kebayoran Baru, JAKARTA 12120, Indonesia 電話 : Fax : (4) PT L OREAL INDONESIA 住所 :Graha Surya Internusa 6 th Fl., Jl HR Rasuna Said Kav X-O, JAKARTA 12950, Indonesia 電話 : Fax : (5) PT Mirabo Ayu ( 同 Elizabeth Arden) 住所 :Graha Irama 5 th Fl., Jl HR Rasuna Said Blok X-1 Kav I-II, JAKARTA 12950, Indonesia 電話 : Fax :
11 8. インドネシアの化粧品に関する規則リンク一覧 BPOM 長官規則 No. HK (2003) BPOM 長官規則 HK Tahun BPOM 長官規則 HK Tahun BPOM 長官規則 HK Tahun BPOM 長官規則 HK (2010) At.6 NO.57/M-DAG/PER/12/ ulasi/2010/12/57_produk_tertentu.pdf BPOM 長官規則 HK Tahun BPOM 長官規則 HK Tahun BPOM 長官規則 HK Tahun 保健大臣規制 No.117/MENKES/PER/VIII/ 以上 9
12 調査委託先 : PT. Indomalco Info Center 本報告書の利用についての注意 免責事項本調査報告書は 日本貿易振興機構 ( ジェトロ ) の各海外事務所を通じ委託調査を行い ビジネス情報サービス部で取りまとめをしたものですが 本書の記述 所見 結論 および提言は必ずしも日本貿易振興機構 ( ジェトロ ) の見解を反映したものではありません 海外の制度 規制等は日々変化するため 最新の情報を確認する必要がある場合は 必ずご自身で最新情報をご確認ください ジェトロは 本報告書の記載内容に関して生じた直接的 間接的 派生的 特別の 付随的 あるいは懲罰的損害および利益の喪失については それが契約 不法行為 無過失責任 あるいはその他の原因に基づき生じたか否かにかかわらず 一切の責任を負いません これは たとえ ジェトロがかかる損害の可能性を知らされていても同様とします 10
目次 1. 医療機器の定義 輸入規制 規格基準と認証 販売規制 関税率とその他の税および税率 その他 管轄省庁 業界団体 主要な輸入業者 / 販売業者
 H23 年度海外輸入制度調査 インドネシアにおける医療機器の輸入制度 2011 年 12 月 独立行政法人日本貿易振興機構ジャカルタ事務所 目次 1. 医療機器の定義... 1 2. 輸入規制... 1 3. 規格基準と認証... 2 4. 販売規制... 3 5. 関税率とその他の税および税率... 8 6. その他... 8 7. 管轄省庁... 9 8. 業界団体... 9 9. 主要な輸入業者
H23 年度海外輸入制度調査 インドネシアにおける医療機器の輸入制度 2011 年 12 月 独立行政法人日本貿易振興機構ジャカルタ事務所 目次 1. 医療機器の定義... 1 2. 輸入規制... 1 3. 規格基準と認証... 2 4. 販売規制... 3 5. 関税率とその他の税および税率... 8 6. その他... 8 7. 管轄省庁... 9 8. 業界団体... 9 9. 主要な輸入業者
1 関税法上の用語の定義 輸入 外国貨物を本邦に引き取ること輸出 内国貨物を外国に向けて送り出すこと 外国貨物 1 輸出の許可を受けた貨物 2 外国から本邦に到着した貨物 ( 外国の船舶により公海で採捕された水産物を含む ) で輸入が許可される前のもの内国貨物 1 本邦にある貨物で外国貨物でないもの
 2018 年 合格目標 Registered Customs Specialist 通関士講座 体験入学用テキスト 入門レジュメ ご案内 これは 入門講義 で使用する教材のコピーです 当教材掲載の内容は 2018 年合格目標コースのものです 実際のテキストはA5 版です 1 関税法上の用語の定義 輸入 外国貨物を本邦に引き取ること輸出 内国貨物を外国に向けて送り出すこと 外国貨物 1 輸出の許可を受けた貨物
2018 年 合格目標 Registered Customs Specialist 通関士講座 体験入学用テキスト 入門レジュメ ご案内 これは 入門講義 で使用する教材のコピーです 当教材掲載の内容は 2018 年合格目標コースのものです 実際のテキストはA5 版です 1 関税法上の用語の定義 輸入 外国貨物を本邦に引き取ること輸出 内国貨物を外国に向けて送り出すこと 外国貨物 1 輸出の許可を受けた貨物
文書管理番号
 プライバシーマーク付与適格性審査実施規程 1. 一般 1.1 適用範囲この規程は プライバシーマーク付与の適格性に関する審査 ( 以下 付与適格性審査 という ) を行うプライバシーマーク指定審査機関 ( 以下 審査機関 という ) が その審査業務を遂行する際に遵守すべき事項を定める 1.2 用語この基準で用いる用語は 特段の定めがない限り プライバシーマーク制度基本綱領 プライバシーマーク指定審査機関指定基準
プライバシーマーク付与適格性審査実施規程 1. 一般 1.1 適用範囲この規程は プライバシーマーク付与の適格性に関する審査 ( 以下 付与適格性審査 という ) を行うプライバシーマーク指定審査機関 ( 以下 審査機関 という ) が その審査業務を遂行する際に遵守すべき事項を定める 1.2 用語この基準で用いる用語は 特段の定めがない限り プライバシーマーク制度基本綱領 プライバシーマーク指定審査機関指定基準
~ 輸入通関 ~ 輸入通関で一般的に必要となる書類 インボイス / パッキングリスト ( 共に原本が必要 パッキングリストはNET WEIGHT GROSS WEIGHT 両方の記載必要 ) 保険証書原本 NPWP ( 納税者登録番号 ) NIK( 通関基本番号 ) ISPM 燻蒸処理証明書 TDP
 輸送ハンドブックインドネシア ~ 輸入通関 ~ 輸入通関で一般的に必要となる書類 インボイス / パッキングリスト ( 共に原本が必要 パッキングリストはNET WEIGHT GROSS WEIGHT 両方の記載必要 ) 保険証書原本 NPWP ( 納税者登録番号 ) NIK( 通関基本番号 ) ISPM 燻蒸処理証明書 TDP ( 会社登録証 ) API ( 輸入業者認定証 ) SIUP ( 営業許可証
輸送ハンドブックインドネシア ~ 輸入通関 ~ 輸入通関で一般的に必要となる書類 インボイス / パッキングリスト ( 共に原本が必要 パッキングリストはNET WEIGHT GROSS WEIGHT 両方の記載必要 ) 保険証書原本 NPWP ( 納税者登録番号 ) NIK( 通関基本番号 ) ISPM 燻蒸処理証明書 TDP ( 会社登録証 ) API ( 輸入業者認定証 ) SIUP ( 営業許可証
Microsoft Word - ☆【HP】インドネシア制度調査
 輸出国事前調査について ( インドネシア ) 1. 調査期間等 (1) 時期 :2013 年 2 月 (2) 内容 : インドネシアにおける食品安全管理体制の制度調査 (3) 対象 : インドネシア医薬品食品監督庁 農業省 海洋水産省 2. 調査結果 ( 概要 ) (1) インドネシア政府の組織構造及び所掌業務 1インドネシア医薬品食品監督庁 (National Agency for Drug and
輸出国事前調査について ( インドネシア ) 1. 調査期間等 (1) 時期 :2013 年 2 月 (2) 内容 : インドネシアにおける食品安全管理体制の制度調査 (3) 対象 : インドネシア医薬品食品監督庁 農業省 海洋水産省 2. 調査結果 ( 概要 ) (1) インドネシア政府の組織構造及び所掌業務 1インドネシア医薬品食品監督庁 (National Agency for Drug and
SGEC 附属文書 理事会 統合 CoC 管理事業体の要件 目次序文 1 適用範囲 2 定義 3 統合 CoC 管理事業体組織の適格基準 4 統合 CoC 管理事業体で実施される SGEC 文書 4 CoC 認証ガイドライン の要求事項に関わる責任の適用範囲 序文
 SGEC 附属文書 2-8 2012 理事会 2016.1.1 統合 CoC 管理事業体の要件 目次序文 1 適用範囲 2 定義 3 統合 CoC 管理事業体組織の適格基準 4 統合 CoC 管理事業体で実施される SGEC 文書 4 CoC 認証ガイドライン の要求事項に関わる責任の適用範囲 序文この文書の目的は 生産拠点のネットワークをする組織によるCoC 認証を実施のための指針を設定し このことにより
SGEC 附属文書 2-8 2012 理事会 2016.1.1 統合 CoC 管理事業体の要件 目次序文 1 適用範囲 2 定義 3 統合 CoC 管理事業体組織の適格基準 4 統合 CoC 管理事業体で実施される SGEC 文書 4 CoC 認証ガイドライン の要求事項に関わる責任の適用範囲 序文この文書の目的は 生産拠点のネットワークをする組織によるCoC 認証を実施のための指針を設定し このことにより
一方 通関前の輸入品の保管は一時保管所 (TPS) の他 特定の輸入品についてはTPS と同等に扱える場所でも保管が可能 ただし 管轄の税関長からの許可が必要 輸入品の保管期間は 港エリア内にあるTPS においては保管開始から30 日以内 港エリア外にあるTPS では40 日以内 TPS と同等の地
 インドネシア貿易管理制度 輸入関連法 詳細 1. 通関法... 1 (1) 通関法の改正 (2) 通関法の実施細則 2. 輸入一般規定...5 3. バタムのシングルドキュメント通関...5 4. オンラインによる輸出入許認可の供与...6 5. 商業法...6 6. 国内流通規程...7 7. 参考...8 1. 通関法 (1) 通関法の改正インドネシア政府は 2006 年 11 月 15 日付法律
インドネシア貿易管理制度 輸入関連法 詳細 1. 通関法... 1 (1) 通関法の改正 (2) 通関法の実施細則 2. 輸入一般規定...5 3. バタムのシングルドキュメント通関...5 4. オンラインによる輸出入許認可の供与...6 5. 商業法...6 6. 国内流通規程...7 7. 参考...8 1. 通関法 (1) 通関法の改正インドネシア政府は 2006 年 11 月 15 日付法律
水産物 鉄鋼 鉄鋼製品 家畜 家畜製品 真珠 作物製品 携帯電話 携帯コンピュータ タブレット端末 麻薬 向精神薬 医薬用前駆体 家禽とその生肉 内臓 および加工品 スチール精錬産業用再生原材料 一部の空調設備 冷蔵 冷凍庫など 林業製品 バティックの繊維 繊維製品 トウモロコシ 大型反芻家畜 牛肉
 インドネシア貿易管理制度 輸入品目規制 詳細 1. 輸入禁止品目 :... 2 危険 有毒原料廃棄物 オゾン層破壊原料 エビ モッツァレラチーズ 特定の魚 中古車 フロンを使用した空調設備 冷蔵 冷凍庫など 2. 輸入制限品目 :... 4 にんにく 小麦 小麦粉 大豆など8 品目 乳製品 丁子 穀類粉など計 19 品目 砂糖 塩 自動車関連 47 品目 潤滑油 廃棄物 4 クロロ-3.5 ジメチルフェノール
インドネシア貿易管理制度 輸入品目規制 詳細 1. 輸入禁止品目 :... 2 危険 有毒原料廃棄物 オゾン層破壊原料 エビ モッツァレラチーズ 特定の魚 中古車 フロンを使用した空調設備 冷蔵 冷凍庫など 2. 輸入制限品目 :... 4 にんにく 小麦 小麦粉 大豆など8 品目 乳製品 丁子 穀類粉など計 19 品目 砂糖 塩 自動車関連 47 品目 潤滑油 廃棄物 4 クロロ-3.5 ジメチルフェノール
15 変更管理
 ISO22716 の要求事項 (15. 変更管理 ) 15 変更管理 (Change control) 製品の品質に影響を及ぼす可能性のある変更 十分なデータに基づいて権限所有者が承認 変更管理及び内部監査 2 1 製品の品質に影響を及ぼす可能性のある変更 化粧品等の品質 有効性及び安全性に影響を及ぼすと考えられる原料 包装材料 製造 包装手順 構造設備 規格 試験方法の変更 1) 成分 分量の変更
ISO22716 の要求事項 (15. 変更管理 ) 15 変更管理 (Change control) 製品の品質に影響を及ぼす可能性のある変更 十分なデータに基づいて権限所有者が承認 変更管理及び内部監査 2 1 製品の品質に影響を及ぼす可能性のある変更 化粧品等の品質 有効性及び安全性に影響を及ぼすと考えられる原料 包装材料 製造 包装手順 構造設備 規格 試験方法の変更 1) 成分 分量の変更
1 アルゼンチン産業財産権庁 (INPI) への特許審査ハイウェイ試行プログラム (PPH) 申請に 係る要件及び手続 Ⅰ. 背景 上記組織の代表者は
 1 アルゼンチン産業財産権庁 (INPI) への特許審査ハイウェイ試行プログラム (PPH) 申請に 係る要件及び手続 -------------------------------------------------------------------------- Ⅰ. 背景 上記組織の代表者は 2016 年 10 月 5 日 ジュネーブにおいて署名された 特許審査手続における協力意向に係る共同声明
1 アルゼンチン産業財産権庁 (INPI) への特許審査ハイウェイ試行プログラム (PPH) 申請に 係る要件及び手続 -------------------------------------------------------------------------- Ⅰ. 背景 上記組織の代表者は 2016 年 10 月 5 日 ジュネーブにおいて署名された 特許審査手続における協力意向に係る共同声明
目次 1. はじめに 2. 実際の応募手続き 3. 応募手続き完了の確認 2
 革新的バイオ医薬品創出基盤技術開発事業 H27 年度公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 1 目次 1. はじめに 2. 実際の応募手続き 3. 応募手続き完了の確認 2 1-a. はじめに 1 注意事項 1. 平成 27 年度の革新的バイオ医薬品創出基盤技術開発事業への応募は 必ず e-rad を利用して下さい 2. e-rad の使用に当たっては 研究機関および研究者の事前登録が必要です
革新的バイオ医薬品創出基盤技術開発事業 H27 年度公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 1 目次 1. はじめに 2. 実際の応募手続き 3. 応募手続き完了の確認 2 1-a. はじめに 1 注意事項 1. 平成 27 年度の革新的バイオ医薬品創出基盤技術開発事業への応募は 必ず e-rad を利用して下さい 2. e-rad の使用に当たっては 研究機関および研究者の事前登録が必要です
<4D F736F F D2088E396F BB91A28BC EF C8EA695DB8AC78BE695AA816A C826F8AEE8F808F918EE88F878F B2E646F63>
 16 12 24 179 26 1 5 26 1 5 注意 品質部門は製造部門から独立していなければならない 各部門の業務を適切かつ円滑に実施しうる能力のある責任者を 組織 規模 業務の種類に応じ 適切な人数を配置すること ( 必要に応じ 上記に挙げた責任者の枠を増やしてもよい ) 各責任者は業務に支障がない限り兼務することができる ただし 製造部門責任者と品質部門責任者は兼務することはできない 出荷可否決定者は品質部門の者とすること
16 12 24 179 26 1 5 26 1 5 注意 品質部門は製造部門から独立していなければならない 各部門の業務を適切かつ円滑に実施しうる能力のある責任者を 組織 規模 業務の種類に応じ 適切な人数を配置すること ( 必要に応じ 上記に挙げた責任者の枠を増やしてもよい ) 各責任者は業務に支障がない限り兼務することができる ただし 製造部門責任者と品質部門責任者は兼務することはできない 出荷可否決定者は品質部門の者とすること
第 11 章許認可 進出手続き (1) 投資申請インドネシアへの投資にあたっては BKPM に対して外国投資 (PMA) 認可申請を行い 認可を得る必要がある 認可申請は オンラインで行う必要がある 外国投資認可申請を行うには 必要事項を記入した所定の申請書フォームと図表 11-2 の添付書類を 2
 インドネシアの投資環境 第 11 章許認可 進出手続き 1. 株式会社の設立手続きと必要書類インドネシアに進出し操業を開始するまでの通常の手続きの流れは図表 11-1 の通りである 尚 投資調整庁 (BKPM) は 1,000 億ルピア以上の投資または 1,000 人以上の従業員雇用を予定する場合には ( バタム島等への投資の場合には要件が緩和される ) 申請後 3 時間で投資ライセンスなどの必要許認可を発行する制度を導入している
インドネシアの投資環境 第 11 章許認可 進出手続き 1. 株式会社の設立手続きと必要書類インドネシアに進出し操業を開始するまでの通常の手続きの流れは図表 11-1 の通りである 尚 投資調整庁 (BKPM) は 1,000 億ルピア以上の投資または 1,000 人以上の従業員雇用を予定する場合には ( バタム島等への投資の場合には要件が緩和される ) 申請後 3 時間で投資ライセンスなどの必要許認可を発行する制度を導入している
Microsoft Word - 規則11.2版_FSSC22000Ver.4特例.doc
 マネジメントシステム審査登録規則 FSSC22000Ver.4 特例 第 11.2 版改訂 :2017 年 9 月 15 日 発効 :2017 年 9 月 15 日 一般財団法人日本品質保証機構 マネジメントシステム部門 はじめに本特例は 一般財団法人日本品質保証機構 ( 以下 JQA という ) が運営する JQA マネジメントシステム審査登録制度 ( 以下 審査登録制度 という ) の詳細を規定した
マネジメントシステム審査登録規則 FSSC22000Ver.4 特例 第 11.2 版改訂 :2017 年 9 月 15 日 発効 :2017 年 9 月 15 日 一般財団法人日本品質保証機構 マネジメントシステム部門 はじめに本特例は 一般財団法人日本品質保証機構 ( 以下 JQA という ) が運営する JQA マネジメントシステム審査登録制度 ( 以下 審査登録制度 という ) の詳細を規定した
Microsoft Word - 【発送版】製造所の登録通知
 薬食機参発 1003 第 1 号 平成 26 年 10 月 3 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いについて 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業は登録制に移行され
薬食機参発 1003 第 1 号 平成 26 年 10 月 3 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いについて 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業は登録制に移行され
「NACCS 貿易管理サブシステム」 平成29年度機能追加 変更内容説明(申請業務編)
 NACCS 貿易管理サブシステム 平成 29 年度機能追加変更内容説明 ( 申請業務編 ) 2018 年 3 月 輸出入 港湾関連情報処理センター株式会社 目次 1. 機能追加の概要 2. 申請様式別機能の詳細 3. 業務別機能の詳細 1 1. 機能追加の概要申請様式別機能 ( 輸出 ) 申請様式 業務 機能追加項目 機能追加概要 輸出承認 申請 1 申請項目の見直し 申請項目を変更します [ 麻薬等原材料
NACCS 貿易管理サブシステム 平成 29 年度機能追加変更内容説明 ( 申請業務編 ) 2018 年 3 月 輸出入 港湾関連情報処理センター株式会社 目次 1. 機能追加の概要 2. 申請様式別機能の詳細 3. 業務別機能の詳細 1 1. 機能追加の概要申請様式別機能 ( 輸出 ) 申請様式 業務 機能追加項目 機能追加概要 輸出承認 申請 1 申請項目の見直し 申請項目を変更します [ 麻薬等原材料
 3001-12-1 3001-12-2 yyyy/mm/dd HH:mm 1 / 2 S****** 帳票タイトル ( 輸出申告控 ( 大額 ))******E 代表統番 申告種別 区分 あて先税関 提出先 申告年月日 申告番号 XXXE X X X X [ X ] XXX E XXXXXXXXXE XE yyyy/mm/dd XXX XXXX XX1E 申告条件 [ X ] 搬入
3001-12-1 3001-12-2 yyyy/mm/dd HH:mm 1 / 2 S****** 帳票タイトル ( 輸出申告控 ( 大額 ))******E 代表統番 申告種別 区分 あて先税関 提出先 申告年月日 申告番号 XXXE X X X X [ X ] XXX E XXXXXXXXXE XE yyyy/mm/dd XXX XXXX XX1E 申告条件 [ X ] 搬入
第 5 部 : 認定機関に対する要求事項 目次 1 目的 IAF 加盟 ISO/IEC 認定審査員の力量 連絡要員... Error! Bookmark not defined. 2 CB の認定
 Part 第 5 部 5: : Requirements 認定機関に対する要求事項 for ABs 食品安全システム認証 22000 第 5 部 : 認定機関に対する要求事項 バージョン 4.1 2017 年 7 月 1 / 6 バージョン 4.1:2017 年 7 月 第 5 部 : 認定機関に対する要求事項 目次 1 目的... 4 1.1 IAF 加盟... 4 1.2 ISO/IEC 17011...
Part 第 5 部 5: : Requirements 認定機関に対する要求事項 for ABs 食品安全システム認証 22000 第 5 部 : 認定機関に対する要求事項 バージョン 4.1 2017 年 7 月 1 / 6 バージョン 4.1:2017 年 7 月 第 5 部 : 認定機関に対する要求事項 目次 1 目的... 4 1.1 IAF 加盟... 4 1.2 ISO/IEC 17011...
Microsoft PowerPoint - US cGMP検討会用080226(資料3-1).ppt
 資料 3-1 米国 FDA による ダイエタリーサプリメントの cgmp 21 CFR Part 111 2008 年 2 月 26 日 日本健康食品規格協会理事長大濱宏文 1 正式名称 ダイエタリーサプリメントの製造 包装 表示および保管のための cgmp (Current Good Manufacturing Practice in Manufacturing, Packaging, Labeling,
資料 3-1 米国 FDA による ダイエタリーサプリメントの cgmp 21 CFR Part 111 2008 年 2 月 26 日 日本健康食品規格協会理事長大濱宏文 1 正式名称 ダイエタリーサプリメントの製造 包装 表示および保管のための cgmp (Current Good Manufacturing Practice in Manufacturing, Packaging, Labeling,
原産地証明書の種類と内容 内容 用途 根拠協定 / 法律など 一般原産地証明書 原産地証明書発給の要請 : (1) 輸入国の法律 規則に基づく要請 (2) 契約や信用状の指定ただし 記載事項はあくまで発給機関の定める発給規則に基づいて作成される 契約および L/C 条件が発給規則に矛盾しないように注
 経済連携協定の特定原産地証明書 50 原産地証明書の種類と内容 内容 用途 根拠協定 / 法律など 一般原産地証明書 原産地証明書発給の要請 : (1) 輸入国の法律 規則に基づく要請 (2) 契約や信用状の指定ただし 記載事項はあくまで発給機関の定める発給規則に基づいて作成される 契約および L/C 条件が発給規則に矛盾しないように注意必要 関税手続きの簡素化に関する国際条約 ( ジュネーブ条約
経済連携協定の特定原産地証明書 50 原産地証明書の種類と内容 内容 用途 根拠協定 / 法律など 一般原産地証明書 原産地証明書発給の要請 : (1) 輸入国の法律 規則に基づく要請 (2) 契約や信用状の指定ただし 記載事項はあくまで発給機関の定める発給規則に基づいて作成される 契約および L/C 条件が発給規則に矛盾しないように注意必要 関税手続きの簡素化に関する国際条約 ( ジュネーブ条約
<4D F736F F D D BB95698ADC974C89BB8A7795A88EBF8AC7979D91CE899E834B >
 製品含有化学物質管理対応ガイドライン 第 1.0 版 2014 年 3 月 1 日制定 ニチユ三菱フォークリフト株式会社 目次 1. はじめに 1 2. 方針 2 3. 適用範囲 2 3.1 適用法規 2 3.2 禁止物質 2 3.3 管理物質 2 4. 取引先様へのお願い事項 3 4.1 物質規制対応連絡先窓口の届出 3 4.2 物質規制管理体制の構築 3 4.3 禁止物質の不使用 非含有宣言書の提出
製品含有化学物質管理対応ガイドライン 第 1.0 版 2014 年 3 月 1 日制定 ニチユ三菱フォークリフト株式会社 目次 1. はじめに 1 2. 方針 2 3. 適用範囲 2 3.1 適用法規 2 3.2 禁止物質 2 3.3 管理物質 2 4. 取引先様へのお願い事項 3 4.1 物質規制対応連絡先窓口の届出 3 4.2 物質規制管理体制の構築 3 4.3 禁止物質の不使用 非含有宣言書の提出
MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1
 MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1 MDSAP 報告書の受入れの概要 (1/2) 日本は 平成 27 年 6 月にMDSAPに参加する旨を発表 関係者との意見交換を行い MDSAP 報告書の受け入れについて 以下の通知を発出した 平成 28 年 6 月 22 日薬生監麻発 0622 第 3 号 薬生機審発 0622
MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1 MDSAP 報告書の受入れの概要 (1/2) 日本は 平成 27 年 6 月にMDSAPに参加する旨を発表 関係者との意見交換を行い MDSAP 報告書の受け入れについて 以下の通知を発出した 平成 28 年 6 月 22 日薬生監麻発 0622 第 3 号 薬生機審発 0622
<945F96F B3816A2E786264>
 Q-14 食品衛生法 ( 昭和 22 年法律第 233 号 ) とは 1 食品衛生法について 食品衛生法とは食品の安全性の確保のために公衆衛生の見地から必要な規制その他の措置を講ずることにより 飲食に起因する衛生上の危害の発生を防止し もつて国民の健康の保護を図ることを目的として 食品の規格等の設定 検査の実施 健康を損なうおそれのある食品の販売の禁止などの事項を規定しています 適用範囲食品衛生法の中で
Q-14 食品衛生法 ( 昭和 22 年法律第 233 号 ) とは 1 食品衛生法について 食品衛生法とは食品の安全性の確保のために公衆衛生の見地から必要な規制その他の措置を講ずることにより 飲食に起因する衛生上の危害の発生を防止し もつて国民の健康の保護を図ることを目的として 食品の規格等の設定 検査の実施 健康を損なうおそれのある食品の販売の禁止などの事項を規定しています 適用範囲食品衛生法の中で
まもりすまいオンラインサービス 基本編
 OM( 基 )-005 目次 はじめに 2 まもりすまいオンラインサービスマニュアル基本編について I. ご利用までに必要な手続き 3 1 ご利用のお申し込み 2 ご利用の PC 環境の確認 3 ログイン方法とログイン画面について Ⅱ. 概要 4 まもりすまいオンラインサービスで出来ることまもりすまいオンラインサービスで出来ないことまもりすまいオンラインサービスご利用に際しお願いすることまもりすまいオンラインサービスのユーザのお取り扱いについて
OM( 基 )-005 目次 はじめに 2 まもりすまいオンラインサービスマニュアル基本編について I. ご利用までに必要な手続き 3 1 ご利用のお申し込み 2 ご利用の PC 環境の確認 3 ログイン方法とログイン画面について Ⅱ. 概要 4 まもりすまいオンラインサービスで出来ることまもりすまいオンラインサービスで出来ないことまもりすまいオンラインサービスご利用に際しお願いすることまもりすまいオンラインサービスのユーザのお取り扱いについて
目次 電子申請を使用した申請の流れ 1ページ 申請書 ( 概算保険料申告書 ) の作成 2ページ 作成した申請書の送信 31ページ 状況照会 電子納付を行う 62ページ 返送書類の取得 74ページ お問い合わせ先 82ページ その他注意事項 83ページ 平成 30 年 6 月 1 日 Ver.1.5
 労働保険概算保険料の申告 ( 継続 ) 電子申請操作マニュアル 目次 電子申請を使用した申請の流れ 1ページ 申請書 ( 概算保険料申告書 ) の作成 2ページ 作成した申請書の送信 31ページ 状況照会 電子納付を行う 62ページ 返送書類の取得 74ページ お問い合わせ先 82ページ その他注意事項 83ページ 平成 30 年 6 月 1 日 Ver.1.5 電子申請を使用した申請の流れ ~ 電子申請を使用した概算保険料の申告の手順
労働保険概算保険料の申告 ( 継続 ) 電子申請操作マニュアル 目次 電子申請を使用した申請の流れ 1ページ 申請書 ( 概算保険料申告書 ) の作成 2ページ 作成した申請書の送信 31ページ 状況照会 電子納付を行う 62ページ 返送書類の取得 74ページ お問い合わせ先 82ページ その他注意事項 83ページ 平成 30 年 6 月 1 日 Ver.1.5 電子申請を使用した申請の流れ ~ 電子申請を使用した概算保険料の申告の手順
<タイトル>
 NACCS 業務資料 電子インボイス 輸出入 港湾関連情報処理センター株式会社 平成 28 年 8 月更新 目次 1 電子インボイスの活用 電子インボイスの活用について IVA02 業務の入力内容についてインボイス仕分け情報登録について IVB01 業務の入力内容について IVB 業務の入力内容についてインボイス仕分け情報登録業務について IVB02 業務及びIVB03 業務の入力内容について RSI
NACCS 業務資料 電子インボイス 輸出入 港湾関連情報処理センター株式会社 平成 28 年 8 月更新 目次 1 電子インボイスの活用 電子インボイスの活用について IVA02 業務の入力内容についてインボイス仕分け情報登録について IVB01 業務の入力内容について IVB 業務の入力内容についてインボイス仕分け情報登録業務について IVB02 業務及びIVB03 業務の入力内容について RSI
員長及び医薬品医療機器等法登録認証機関協議会代表幹事宛て送付するこ ととしていることを申し添えます 記 1. 基本要件基準第 13 条第 5 項及び第 6 項への適合性確認の基本的な考え方について (1)2023 年 ( 平成 35 年 )2 月 28 日 ( 以下 経過措置期間終了日 という )
 薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
<4D F736F F D F8E FEE95F1836C F8EE88F878F F88979D8BC68ED2976C A2E646F63>
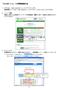 さんぱいくん への情報登録方法 1. まず http://www2.sanpainet.or.jp にアクセスします 産廃情報ネット http://www.sanpainet.or.jp からもリンクをたどることができます 2. メニュー画面情報を公表する公表項目セットデータの新規登録 編集や公表 公表停止の設定を行なうことができます 処理業者データ登録 変更 をクリック 3. ログインする処理業者向けのログイン画面が表示されます
さんぱいくん への情報登録方法 1. まず http://www2.sanpainet.or.jp にアクセスします 産廃情報ネット http://www.sanpainet.or.jp からもリンクをたどることができます 2. メニュー画面情報を公表する公表項目セットデータの新規登録 編集や公表 公表停止の設定を行なうことができます 処理業者データ登録 変更 をクリック 3. ログインする処理業者向けのログイン画面が表示されます
目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2
 免疫アレルギー疾患等実用化研究事業 ( 移植医療技術開発研究分野 ) 2019 年度 1 次公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 戦略推進部 難病研究課 2018 年 11 月 1 目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2 1. はじめに
免疫アレルギー疾患等実用化研究事業 ( 移植医療技術開発研究分野 ) 2019 年度 1 次公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 戦略推進部 難病研究課 2018 年 11 月 1 目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2 1. はじめに
<4D F736F F F696E74202D C8E8DC58F4994C5817A88C092E890AB A835E838A F2E B8CDD8AB B83685D>
 製薬セミナー 5 月期 安定性モニタリング 薬務課振興係 1 安定性モニタリング 2 1 安定性モニタリングとは 製造した最終製品あるいは原薬が定められた保存条件下で 有効期間 リテスト期間又は使用の期限にわたり 保存により影響を受け易い測定項目及び品質 安全性又は有効性に影響を与えるような測定項目が規格内に留まっており また留まり続けることが期待できることを 適切な継続的プログラムに従った安定性モニタリングにより監視し
製薬セミナー 5 月期 安定性モニタリング 薬務課振興係 1 安定性モニタリング 2 1 安定性モニタリングとは 製造した最終製品あるいは原薬が定められた保存条件下で 有効期間 リテスト期間又は使用の期限にわたり 保存により影響を受け易い測定項目及び品質 安全性又は有効性に影響を与えるような測定項目が規格内に留まっており また留まり続けることが期待できることを 適切な継続的プログラムに従った安定性モニタリングにより監視し
HACCP 自主点検リスト ( 一般食品 ) 別添 1-2 手順番号 1 HACCP チームの編成 項目 評価 ( ) HACCP チームは編成できましたか ( 従業員が少数の場合 チームは必ずしも複数名である必要はありません また 外部の人材を活用することもできます ) HACCP チームには製品
 HACCP 自主点検票 ( 一般食品 ) 別添 1-1 施設名 所在地 対象製品等 手順番号 ( 原則番号 ) 項目 説明 評価 1 HACCP チームの編成 2 製品説明書の作成 3 意図する用途等の確認 4 製造工程一覧図の作成 5 製造工程一覧図の現場確認 6( 原則 1) 危害要因の分析 (HA) 7( 原則 2) 重要管理点 (CCP) の決定 8( 原則 3) 管理基準 (CL) の設定
HACCP 自主点検票 ( 一般食品 ) 別添 1-1 施設名 所在地 対象製品等 手順番号 ( 原則番号 ) 項目 説明 評価 1 HACCP チームの編成 2 製品説明書の作成 3 意図する用途等の確認 4 製造工程一覧図の作成 5 製造工程一覧図の現場確認 6( 原則 1) 危害要因の分析 (HA) 7( 原則 2) 重要管理点 (CCP) の決定 8( 原則 3) 管理基準 (CL) の設定
<4D F736F F F696E74202D E AC7979D95A88EBF895E97708EE88F E B8CDD8AB B83685D>
 1 アイシン管理物質禁止物質 登録手順 2017 年 4 月 10 日改訂 アイシン精機安全衛生環境部 アイシン精機への成分情報について 2 実施項目 日本国内法規に対応したもの ( 日本語のもの ) GHS 対応版 成分情報登録 PRTR WORLD にアップロード PRTR WORLD にアイシン管理 禁止物質の成分情報を登録 ( 全成分開示ではありません ) 納入資材成分報告書作成 ( 当社の書式
1 アイシン管理物質禁止物質 登録手順 2017 年 4 月 10 日改訂 アイシン精機安全衛生環境部 アイシン精機への成分情報について 2 実施項目 日本国内法規に対応したもの ( 日本語のもの ) GHS 対応版 成分情報登録 PRTR WORLD にアップロード PRTR WORLD にアイシン管理 禁止物質の成分情報を登録 ( 全成分開示ではありません ) 納入資材成分報告書作成 ( 当社の書式
JCROA自主ガイドライン第4版案 GCP監査WG改訂案及び意見
 受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
5、ロット付番
 購買管理基準書 (CPC-C4) 目 次 1. 目的 2 2. 適用範囲 2 3. 購買品の区分 2 4. 新規購買先の評価 選定 2 4-1 校正委託先の評価 選定 3 4-2 検査委託先の評価 選定 3 5. 購買先リスト 4 6. 購買品の発注及び検収検証 4 6-1 購買品の発注 4 6-2 購買品の検収検証 4 6-3 機器の登録 5 6-4 発注及び検収検証の記録 5 7. 購買先の継続評価
購買管理基準書 (CPC-C4) 目 次 1. 目的 2 2. 適用範囲 2 3. 購買品の区分 2 4. 新規購買先の評価 選定 2 4-1 校正委託先の評価 選定 3 4-2 検査委託先の評価 選定 3 5. 購買先リスト 4 6. 購買品の発注及び検収検証 4 6-1 購買品の発注 4 6-2 購買品の検収検証 4 6-3 機器の登録 5 6-4 発注及び検収検証の記録 5 7. 購買先の継続評価
PowerPoint プレゼンテーション
 日 EU EPA 及び TPP11 の 原産地規則について 2018 年 5 月 18 日 財務省関税局 目次 日 EU EPA 1. 日 EU EPAについて 2. 日 EU EPA 原産地規則の概要 3. セクションA( 原産地基準 ) について 4. セクションB( 原産地手続 ) について 5. 品目別規則等の附属書について TPP11 6. TPP11 原産地規則の概要 1 1. 日 EU
日 EU EPA 及び TPP11 の 原産地規則について 2018 年 5 月 18 日 財務省関税局 目次 日 EU EPA 1. 日 EU EPAについて 2. 日 EU EPA 原産地規則の概要 3. セクションA( 原産地基準 ) について 4. セクションB( 原産地手続 ) について 5. 品目別規則等の附属書について TPP11 6. TPP11 原産地規則の概要 1 1. 日 EU
ユーザー一覧をファイル出力する ユーザーを検索する 登録したユーザー数を確認する
 目次 はじめに サービス内容............................................................ 8 基本サービス.......................................................... 8 お客様のご利用環境について............................................
目次 はじめに サービス内容............................................................ 8 基本サービス.......................................................... 8 お客様のご利用環境について............................................
目次 1. 一般 目的 適用範囲 参照文書 用語及び定義 内部監査 一般 内部監査における観点 内部監査の機会 監査室
 連携プログラム技術評価機関内部監査及びマネジメントレビュー手順 平成 25 年 10 月 7 日 独立行政法人情報処理推進機構 RP-02-E 目次 1. 一般... 1 1.1. 目的... 1 1.2. 適用範囲... 1 2. 参照文書... 1 3. 用語及び定義... 1 4. 内部監査... 1 4.1. 一般... 1 4.2. 内部監査における観点... 1 4.3. 内部監査の機会...
連携プログラム技術評価機関内部監査及びマネジメントレビュー手順 平成 25 年 10 月 7 日 独立行政法人情報処理推進機構 RP-02-E 目次 1. 一般... 1 1.1. 目的... 1 1.2. 適用範囲... 1 2. 参照文書... 1 3. 用語及び定義... 1 4. 内部監査... 1 4.1. 一般... 1 4.2. 内部監査における観点... 1 4.3. 内部監査の機会...
この証明書は マレーシア木材産業庁 (MTIB) が半島部またはサバ州の木材製品に使用した原木の合法性を EU 以外の輸出国に証明するために発行している 図 木材産業庁が発行している木材合法性証明書 23
 この証明書は マレーシア木材産業庁 (MTIB) が半島部またはサバ州の木材製品に使用した原木の合法性を EU 以外の輸出国に証明するために発行している 図 4.1.6 木材産業庁が発行している木材合法性証明書 23 この輸出ライセンスは マレーシア木材産業庁が EU 向けに輸出する荷別に審査した上で発行し 合法性証明書を兼ねている 図 4.1.7 合法性を証明する半島部の輸出ライセンス 24 ゴム材を原料とした製品の合法性証明のためには
この証明書は マレーシア木材産業庁 (MTIB) が半島部またはサバ州の木材製品に使用した原木の合法性を EU 以外の輸出国に証明するために発行している 図 4.1.6 木材産業庁が発行している木材合法性証明書 23 この輸出ライセンスは マレーシア木材産業庁が EU 向けに輸出する荷別に審査した上で発行し 合法性証明書を兼ねている 図 4.1.7 合法性を証明する半島部の輸出ライセンス 24 ゴム材を原料とした製品の合法性証明のためには
<90528DB88EBF96E2955B2E786C73>
 4. 品質マネジメントシステム 4.1 一般要求事項 1 組織が品質マネジメントシステムを確立する上で必要としたプロセスは何ですか? 2 営業 / 購買 / 設計のプロセスについて 1このプロセスはどのプロセスと繋がっていますか? また関係していますか? 2このプロセスの役割と目的は何ですか? 3このプロセスの運用 管理の判断基準と 方法は何ですか? 4このプロセスの運用 管理での必要な資源と情報は何ですか?(
4. 品質マネジメントシステム 4.1 一般要求事項 1 組織が品質マネジメントシステムを確立する上で必要としたプロセスは何ですか? 2 営業 / 購買 / 設計のプロセスについて 1このプロセスはどのプロセスと繋がっていますか? また関係していますか? 2このプロセスの役割と目的は何ですか? 3このプロセスの運用 管理の判断基準と 方法は何ですか? 4このプロセスの運用 管理での必要な資源と情報は何ですか?(
