会社概要と沿革
|
|
|
- うたろう ひろもり
- 7 years ago
- Views:
Transcription
1 会社案内 1. 会社概要と沿革 2. 会社役員 組織図 3. サービスと業務 4. 受託実績 5. 売上と従業員数の推移 6.EPSグループ November 1st, 2018 会社案内
2 会社概要と沿革 代表者 設立 2014 年 7 月 資本金 U R L 代表取締役社長安藤秀高 10,000 万円 センターオフィス 東京都新宿区下宮比町 2 番 23 号つるやビル 代表 : 第二オフィス 東京都新宿区新小川町 1 番 1 号飯田橋 MF ビル 第三オフィス 東京都新宿区新小川町 6 番 29 号アクロポリス東京 第五オフィス 東京都新宿区下宮比町 2 番 26 号 KDX 飯田橋ビル 鶴瀬研究所 埼玉県富士見市鶴馬 2662 番地 代表 : 大阪事務所 大阪市淀川区宮原三丁目 4 番 30 ニッセイ新大阪ビル 代表 : 名古屋事務所 名古屋市西区牛島町 6 番 1 号名古屋ルーセントタワー 代表 : 甲府事務所 山梨県甲府市川田町アリア 101 代表 : 沿革 1991 年 5 月 株式会社エプス東京を設立 1993 年 4 月 臨床試験関連の症例登録 割付業務を開始 1993 年 10 月 厚生省薬剤疫学研究関連の大規模臨床試験サポートシステムを開発 1995 年 8 月 データマネジメント部門を設置 1998 年 4 月 臨床開発部門を設置 開発治験向けモニタリング業務を開始 1999 年 3 月 中国にてCROおよびソフト開発業務を開始 2000 年 10 月 部門制を柱とした組織改正を実施 臨床企画部 統計解析部を設置 2001 年 4 月 イーピーエス株式会社に商号変更 7 月 CROとして初めてJASDAQへ株式を上場 2002 年 4 月 医療機器に関する臨床開発 薬事業務受託事業を開始 10 月 安全性情報室を設置 2004 年 7 月 東証二部へ株式を上場 2006 年 9 月 東証一部へ株式を上場 2014 年 2 月 日揮ファーマ株式会社の株式を100% 取得 2014 年 7 月 分割準備会社設立 2015 年 1 月 吸収分割によりCRO 事業を継承 会社案内 1
3 会社役員 組織図 EPS 役員 組織図 取締役 監査役 代表取締役社長 : 安藤 秀高 代表取締役 : 田中 尚 取締役 : 玉井 康治 取締役 ( 非常勤 ) : 長岡 達磨 監査役 ( 非常勤 ) : 冨永 倶弘 (2018 年 11 月 1 日現在 ) 株主総会取締役会代表取締役社長 監査役開発事業本部 臨床開発事業部医療機器開発センターデータサイエンス事業部開発薬事センター 開発 1 部 ~ 開発 8 部品質管理部 鶴瀬研究所 医療機器開発部 / 医療機器薬事部 データマネジメント部 / 統計解析 1 部症例登録部 開発薬事室 / メディカルライティング部 クリニカルアソシエイションセンター 執行役員 リアルワールト エヒ テ ンス事業本部 PMS 事業部 PMS1 部 ~2 部 / 統計解析 2 部企画推進部 執行役員会長 ( 非常勤 ): 田代伸郎 安全性情報事業部 安全性情報 1 部 ~2 部 代表執行役員社長 : 安藤秀高 臨床研究推進部 上席執行役員上席執行役員執行役員 : 佐々明 : 島田明典 : 丸山利雄 事業推進本部 第一事業推進センター第ニ事業推進センター 事業推進部 / プロジェクトマネジメント室営業 1 部 ~2 部 試験基盤整備室 / 医療情報戦略室再生医療推進室 執行役員執行役員 : 佐久間健次 : 藤澤清人 GCP 監査部 品質マネジメント部 執行役員執行役員 : 横瀬久幸 : 阿部裕明 (2018 年 11 月 1 日現在 ) 管理本部 人財戦略室 / 経営支援室 / 人事室総務室 / 経理室 / IT 室リスクマネジメント室 (2018 年 10 月 1 日現在 ) 会社案内 2
4 サービスと業務 サービス領域 業務一覧 医薬品開発支援サービス 医薬品に関わる下記試験 調査業務全般国内臨床試験 / アジア及びグローバル臨床試験 / 製造販売後調査 / 製造販売後臨床試験 / 医師主導治験 / 大規模疫学調査 / 臨床研究 医療機器開発支援サービス 一般医療機器 管理医療機器及び高度管理医療機器に関わる下記業務全般薬事申請支援 / 臨床試験 / 製造販売後調査 後発医薬品開発支援サービス 下記試験に関わる開発業務及び計画立案 コンサルティング 申請支援生物学的同等性試験 / 安全性試験 教育研修サービス 臨床試験入門 / CRA 教育 / CRC 教育 / MR 教育 / 座学研修の実施 / e ラーニングコンテンツ制作 CDISC 標準業務サービス モニタリング 高度な専門知識を有するモニタリングスペシャリストが お客様のご要望を承りながら 高品質かつスピーディなモニタリングを実現 症例登録センター 厳格な品質管理基準に沿って症例データを取得 様々な割付方法の組合せにより割付作業を実施 試験進捗状況もリアルタイムに掌握 データマネジメント データ入力から論理チェック 最終データ作成まで 徹底した品質管理で高品質データをご提供 安全性情報対応 治験 製造販売後臨床試験 調査等で発生した安全性情報の収集 評価分析 厚生労働省等への報告を経験豊富な専門スタッフが支援 GCP 監査 臨床試験が GCP 等関連法規 治験実施計画書及び標準業務手順書を遵守して行われているかを評価 検証し 信頼性を向上 コンサルティング 薬事 その他 海外からの導入計画や 欧米 アジアでの臨床開発を支援など 医薬品 医療機器開発に関わる薬事戦略支援から許可取得までをサポート サービス強化ソリューション分析業務サービス 薬物濃度測定 / 製剤試験 ( 安定性試験 配合変化試験 ) 統計解析 多数の専門家の幅広い知識と 経験を基にデータ解析処理を実施 臨床開発関連システムと ASP サービス 豊富なシステム開発経験と実績により 関連法規を遵守し 臨床試験のスピードおよび品質を向上させる臨床 IT ソリューションをご提供 お問合せは 営業部 [email protected] TEL: FAX: メディカルライティング 各種申請書類 各種報告書を可能な限り短時間で作成 幅広い専門知識をもつスタッフにより 効果的な薬事戦略をアドバイス 分析業務サービス 生体試料中の薬物濃度測定 製剤試験 ( 規格試験 安定性試験 配合変化試験等 ) を実施 会社案内 3
5 受託実績 フェーズ別受託数の割合 領域別受託数の割合 業務別受注額の割合 過去 5 ヶ年受託プロトコール数 :2,072 件 (2018 年 9 月末現在 ) 会社案内 4
6 売上と従業員数の推移 (2017 年 9 月末現在 ) 会社案内 5
7 EPS グループ EPS ホールディングス株式会社 持株会社 東京都新宿区津久戸町 1-8 神楽坂 AK ビル 6 階 TEL: /FAX: 株式会社 EP ファーマライン コントラクト MR 事業 DI を中心としたコールセンター事業 関連 BPO サービス 医療機器サポートサービス 東京都豊島区西池袋 池袋ウェストパークビル /TEL: /FAX: 事業所 : 東京 大阪 福岡 仙台株式会社 ES リンク 製薬企業向け業務改革を支援する BPO サービス 東京都新宿区津久戸町 1-8 イーピーエス株式会社 CRO 事業 CRO 事業セグメント統括 東京都新宿区下宮比町 2-23 つるやビル /TEL: /FAX: 事業所 : 東京 大阪 名古屋 埼玉 ( 鶴瀬 ) 山梨 ( 甲府 ) 株式会社 EPS アソシエイト CRO 事業 東京都新宿区津久戸町 1-8 神楽坂 AK ビル 7 階 /TEL: /FAX: 事業所 : 東京 大阪株式会社イーピーメイト 人材派遣型 CRO 事業 東京都新宿区津久戸町 1-8 神楽坂 AK ビル 4 階 /TEL: /FAX: 株式会社 EP 綜合 SMO 事業 東京都新宿区津久戸町 1-8 神楽坂 AK ビル /TEL: /FAX: 事業所 : 北海道 東北 東京 中部 関西 中国 四国 九州 沖縄 EP クルーズ株式会社 臨床研究の企画 プロジェクトマネジメント業務 事務局業務 モニタリング業務 データセンター業務他 東京都新宿区新小川町 6-29 アクロポリス東京 3 階 /TEL: /FAX: 事業所 : 東京 中国 ( 蘇州 ) イートライアル株式会社 医薬 医療系 IT 事業 東京都新宿区津久戸町 1-8 神楽坂 AK ビル 9 階 /TEL: /FAX: EPI 山梨株式会社 治験 臨床研究のデータマネジメント業務支援他 山梨県甲府市川田町アリア 101/TEL: /FAX: 株式会社綜合臨床メデフィ CRO 事業 東京都新宿区西新宿 KDX 新宿ビル 9 階 /TEL: /FAX: EPS インターナショナル株式会社 アジアを中心とする海外 CRO SMO 及びその他関連事業 GR 事業セグメント統括 東京都新宿区津久戸町 1-8 神楽坂 AK ビル 8 階 /TEL: /FAX: 事業所 : 東京 米国 中国 ( 上海 北京 広州 ) シンガポール 韓国 台湾 他アジア パシフィック諸地域 EPS 益新株式会社 ヘルスケア産業分野における日本 中国 東南アジアをつなぐ専門商社事業 益新事業セグメント統括 東京都新宿区神楽坂 4-8 神楽坂プラザビル地下 1 階 /TEL: /FAX: 事業所 : 東京 中国 ( 蘇州他 各都市 ) 株式会社イーピービズ EPS グループ会社向けシェアードサービス 東京都新宿区新小川町 6-29 アクロポリス東京 7 階 /TEL: /FAX: 会社案内 6
8 サービス 1. 医薬品開発支援サービス 2. 医療機器開発支援サービス 3. 後発医薬品開発支援サービス 4. 教育研修サービス 5.CDISC 標準業務サービス November 1st, 2018 サービス
9 医薬品開発支援サービス 迅速で高品質な医薬品開発をフルサービスでご提供します イーピーエスは データマネジメント 統計解析をはじめとして モニタリング等の開発業務全般 さらには製造販売後調査支援に至るまで 臨床試験における CRO 業務すべてに対応しています また EPS グループのスケールメリットを活かし アジア及びグローバルでの臨床試験支援や これまでのサービスや仕組みを進化させた 付加価値の高い臨床開発ソリューションの提供により スピーディで高品質な医薬品開発支援を実現しています 対応分野 治験 その他臨床試験 製造販売後調査 医師主導治験 大規模疫学調査 臨床研究 開発スケール 国内臨床試験 アジア及びグローバル臨床試験 支援業務 モニタリング 登録センター業務 データマネジメント 統計解析 メディカルライティング 安全性情報対応 GCP 監査業務 コンサルティング その他 臨床開発関連システムと ASP サービス 強化ソリューション グローバル臨床開発支援サービスアジア各国の子会社ネットワークと世界有数の CRO との業務提携により ハイクオリティなアジア及びグローバル臨床試験をサポートします データセンターサービス大規模な製造販売後調査において イーピーエスのノウハウとリソースを活用することができる クライアント特化型 のデータマネジメントサービスです オフショア業務サービスデータマネジメントを中国 CRO 最大手の当社子会社にてオフショアリング 低コストながら 国内と同レベルのスピードと品質を保証します 臨床試験 ~ 製造販売後調査に関わる全業務を受託できる フルサービス体制 構築 癌や循環器などの慢性疾患を多数経験 メガスタディへの対応も可能 標準化された業務手順や専門知識を有するスペシャリストにより 高水準のサービス品質を保証 EPS グループの海外ネットワークにより アジア及びグローバル臨床試験受託が可能 数多くの受託実績により社内にノウハウが蓄積され クライアントへの提案が可能 サービス 1
10 医療機器開発支援サービス 医薬品開発で培われた経験と医療機器の幅広い専門知識により 迅速な承認 認証取得を実現します 医療機器の安全性 有効性及び 製造販売する企業の品質管理 安全対策が厳しく問われる現在 承認申請には専門的な知識と手順が必要となります また 高度管理医療機器においては 科学的 倫理的妥当性に基づく臨床試験 ( 治験 ) の実施 有効性 安全性に関する製造販売後情報収集の徹底が要求されます イーピーエスでは 経験豊富な専門スタッフの知識とノウハウを活かして 医療機器の薬事 臨床試験 製造販売後調査に関する業務を 幅広く支援いたします 臨床開発業務 コンサルティング 薬事申請業務 コンサルティング 1. 臨床試験関連業務 ( 試験実施計画書作成 モニタリング等 ) 2. 製造販売後調査関連業務 ( 調査票回収 使用成績報告書作成等 ) 3. 海外臨床試験の品質点検業務 4. コンサルティング業務 ( 試験デザイン検討 臨床試験実施体制の構築等 ) 臨床試験主なサービスフロー 安全性情報 安全性情報 ( Q A ) G C P 監査 モニタリング品質管理 (QC) 上 プロトコール等作成支援 症例登録 データマネジメント 統計解析 総括報告書 市 申請書類作成支援 症例登録 データマネジメント 統計解析 使用成績調査等報告書 使用成績評価 計画 治験の実施 臨床試験 ( 治験 ) 承認申請 使用成績等調査 開発 医療機器の設計及び製造 臨床必要品目 臨床試験 GCP 使用成績等調査 G P S P 非臨床試験 承認申請 承認 保険適用申請 販売 臨床不要品目 海外製造所認定 製造業登録 Q M S 製造販売業許可 Q M S, G V P イーピーエスの支援薬事申請業務臨床開発業務 非臨床試験においてはコンサルティングのみのサービス 1. 薬事コンサルティング業務 ( 申請区分調査 薬事戦略立案等 ) 2. 認証 承認申請 届出に関する業務 ( 書類作成サポート等 ) 3. 業許可及び登録申請関連業務 ( 各業態取得サポート 手順書作成等 ) 4. 保険適用申請業務 機器実績 放射線治療装置 画像診断装置 カテーテル 低周波治療器 消化器系機器 整形外科用治療器 循環器系機器 歯科用ユニット 眼科機器 その他の検査機器 医療機器専門のセクションにて 臨床開発から認証 承認申請までフルサポートが可能 医薬品開発サポートで培った経験をもとに 関連法規を遵守したクオリティの高い臨床試験を実現 電気 生物及び化学のバックグラウンドを有する専門スタッフにて対応 チーム編成による業務体制により スムーズで偏りのない業務を遂行 サービス 2
11 後発医薬品開発支援サービス 新薬開発のノウハウを活かし 高品質ながらコストを抑えた後発医薬品開発をサポートします 弊社は 新薬開発におけるノウハウを活かし 後発医薬品開発に係る業務を高品質で提供いたします 試験の企画から総括報告書作成までの一連の業務に加え 実施医療機関との調整および血中濃度計測業務を含めて フルサービスで対応が可能です フルサービス支援体制 EPS グループ各社との連携により 低コストでのフルサービス支援が可能です 主なサポート 薬事コンサルティング 臨床試験の企画 治験薬概要書作成 プロトコール CRF 等の試験関連資料の作成 薬剤割付 モニタリング データマネジメント 統計解析 総括報告書作成 分析機関 分析法バリデーション 薬物濃度測定 報告書作成 ( 信頼性保証含む ) 分析機関 : 医療機関 施設サポート 被験者募集 治験審査委員会対応業務 (IRB 対応業務 ) 施設事務サポート 試験進捗管理 医療機関支援 : 低コスト高品質の理由 治験と同等のプロセスで精査 クオリティポリシーを確認の上 開発予算に応じた最大限の品質管理を行う 標準化 ( 業務手順 症例報告書等 ) により 依頼者との摺り合わせやデータマネジメントシステム ( データベース ) の構築等に要する時間を短縮 EDC による運用により 初回のデータ回収および再調査の効率化 新薬開発と同等の品質でサービスを提供 対象患者を対象とした臨床薬理試験の対応が可能 豊富な新薬開発のノウハウにより柔軟性の高い対応が可能 特殊な剤形での開発経験あり サービス 3
12 教育研修サービス 臨床試験のノウハウを活かした e ラーニングと座学の融合により 実践的かつ効果的な教育を実現 イーピーエスでは CRO で培った臨床試験のノウハウを活かし e ラーニングシステムによる効率的で均質な教育 研修と 開発経験豊富な専任講師による実践的な座学講座での新人教育を提案しています 経費 時間を削減し 弊社内で実証された 実践的かつ効果的な教育 研修サービスを実現いたします e ラーニング メリット 研修場所や講師にかかる経費 時間を削減 自由な時間での受講が可能 専門のナレーターによる講義 管理者による受講状況確認が可能 法改正に合わせた実践的テスト 100 問 テスト不正解時の解説 システムの特徴 インターネット初心者でも迷わない操作方法 受講生の受講履歴 成績などの管理が容易 集合研修 モニター (CRA) 導入研修 モニターには GCP 等の規制要件 高い倫理観 また臨床開発担当者としての必要な科学的な知識のみならず 治験関係者との折衝能力が求められます イーピーエスでは これからモニターを目指す方に モニターとしての基本的な知識を約 4 週間にわたり研修致します 講師陣は 製薬会社臨床開発出身者や 専門の外部講師 現在臨床現場で活躍しているモニターが行い 実務経験を交えた実践的な講義を実施致します 研修方法は 知識を学ぶ講義形式だけでなく 治験責任医師や CRC 等の治験関係者と直接コミュニケーションをとるための経験を擬似的に体験できるロールプレイング研修を取り入れております コンテンツの特徴 CRO として臨床試験の経験をフィードバックした実務的な内容 法改正を踏まえたタイムリーなコンテンツ内容 オンラインテストの実施 即時採点 評価が可能 講義 ( 約 2 週間 ) <モニタリング業務の概論 > モニタリング概論 モニタリング関連法規 治験薬概要書の構成と内容 同意説明文書 補償と賠償など ロールプレイング ( 約 2 週間 ) 選定 依頼手続き < モニタリング業務の実際 > 選定 治験の依頼 直接閲覧 変更手続 情報提供 など 医局説明会 SDV( 症例報告書と原資料の照合による確認 ) GCP 研修 臨床試験の基礎 臨床試験の進め方 臨床試験の様々な業務 確認テスト e ラーニングと座学 ロールプレイングの研修受講によるモニター基礎知識習得 毎日の復習テストと定期的な確認テストによる知識の定着 最新の法改正に合わせた e ラーニングコンテンツ サービス 4
13 CDISC 標準業務サービス CDISC 標準 による承認申請に向けた トータルサポートを提供するパートナーへ 弊社は お客様の要望に合わせた業務プロセスを構築 遂行することが可能です また CDISC 標準準拠での業務については 提案型 でサービスを提供いたします 加えて CDISC 標準による承認申請に向けたサポートとして 承認申請と製造販売後データを見据えたトータルサービスをご提案いたします CDISC 標準電子データ申請サポートモデル 弊社では社内標準 (EPS 標準 ) を設けており CDISC 標準全面準拠にて対応いたします 主なサポート CDISC 標準サービス でご提案する CDISC 準拠された成果物は CDISC 標準モデル別に CDASH SDTM 及び ADaM があります 更に弊社では これら標準モデルに加えて Controlled Terminorogy 変数命名ルール 解析結果出力など お客様のご要望に合わせて対応いたします 3 種類の臨床試験標準データの作成業務に加え Submission ready とするための資料作成 当局提出用データの作成 Controlled Terminorogy 変数命名ルール 解析結果出力 IT インフラ Validation tool SAS CDI CDISC 標準 への取り組み CDISC 標準 は臨床領域のデータを相互交換するための標準モデルで それに対応した新たなサービスをご提供するため 弊社では 2012 年 1 月から取り組みを開始しました 更に同年 4 月からは EPS グループ全体での取り組みを開始し EPS グループとしてのサービスも展開しています 以降 CDISC 標準プロジェクト として CDISC 公式トレーニング の受講 社内業務フローの検討 資料や IT ツールの作成 社内本格導入を見据えた教育資料の作成及び 情報共有に積極的に取り組み CDISC 標準 に一貫して対応可能な体制構築を実現しています また CDISC 標準プロジェクト では 社内部署間で横断的にメンバーを招集して取り組んでいます Milestones 1. Phase-I 試験 2. Phase-II 試験 3. Phase-III 試験 電子データ申請のセットアップ 4. 電子データ (ISS ISE 等含 ) ectd 申請完了 5. 申請 ectd サービス 実績豊富な協力先企業との連携により フルサービスをご提供します 準備 申請サポート コンサルティング PDF PDF 化 編纂 ectd 編纂 提出 ectd 提出サポート ( 印刷等 ) ライフサイクル ectd ライフサイクル これまでの経験に基づく日本の臨床データの特性に関する豊富な知識で対応 CDISC 標準との関係を含め 申請プロジェクトレベルで理解したサービスを提供 コンサルテーションの実施に加え 規制適合性と業務効率化の両立が可能な CDISC 標準全面準拠による 業務の一括受託が可能 サービス 5
14 業務案内 1. モニタリング 2. 症例登録センター 3. データマネジメント 4. 統計解析 / メディカルライティング 5. 安全性情報対応 / 臨床開発関連システムとASPサービス 6.GCP 監査 / コンサルティング 薬事 その他 November 1st, 2018 業務案内
15 モニタリング 高品質かつスピーディなモニタリングを実現 弊社のモニター専門教育を経た高度な専門知識を有するモニター (CRA) が クライアント様のご要望を承りながら GCP はもちろん SOP プロトコールに厳格に従って業務を遂行します また これらの過程で作成 収集される各種文書は 弊社の品質管理部門において厳格な品質チェックを行い保管 保存されます きめの細かい適切なチェックでモニタリング品質を向上 臨床試験 主にモニタリングの業務が関連法規を遵守して実施されているか否かを品質保証の一環として 品質管理の手法にて点検いたします 客観的な眼で きめの細かい適切なチェックをタイムリーに行うことにより モニタリングの品質の維持 向上に努めています 即戦力のモニターを養成 主なサービス 実施医療機関および治験責任医師に関する GCP 適合性調査 治験責任医師への治験実施計画の説明および合意書作成 治験計画届出 変更届出 中止 終了届出の支援 実施医療機関への治験依頼および契約手続き IRB 審議結果への対応 契約締結 スタートアップ ミーティングの実施 治験薬の交付 回収 実施医療機関への訪問 情報伝達 専門知識の充実 業務能力の向上を図り 常に即戦力として業務を行えるモニター育成を行うため モニター教育委員会 を設けています 導入教育で研修 ロールプレイング OJT( 内外勤 ) を行い 達成度を確認する試験を実施後モニター認定を取得します その後 さらに実践的 専門的な教育を受けることで即戦力としてのモニターを養成しています 様々な領域 疾患における試験支援の経験により モニタリングだけでなく 試験計画の立案などのご提案も可能です 専門性の高い疾患 特に癌 中枢神経系 代謝系の試験においては豊富な実績を持っております 品質管理 (QC) 専門のスタッフを配置し 常時品質をチェック 品質を高めています 治験依頼者 治験実施者から独立した中立的な立場で 効果安全性評価委員会の事務局運営などもサポートいたします 業務案内 1
16 症例登録センター 症例登録 プロトコールに従った適格性判定をスピーディに 電話 FAX WEB を利用した中央登録方式による症例のエントリーにより 弊社の厳格な品質管理基準に沿って 解析に耐えうる信憑性の高いデータを取得 プロトコールに従った選択基準および除外基準を照合し 症例の適格性チェックをスピーディに行います 主なサービス 電話 /FAX/WEB による症例受付 ( データベース一元管理 ) コンピュータによる施設契約情報 医師情報登録チェック 治療群割付 予後因子における群間バランシング ( 動的割付 ) 使用治験薬剤の割り当て 記載事項漏れ 不整合の報告 プロトコールに従った適格性の判定 登録の状況管理 薬剤割付 緊急時のエマージェンシーキー開示 24 時間緊急受付も可能 盲検試験等において キーコードの作成およびキーコードに基づいた治験薬への割付作業 エマージェンシーキーの作成を行うと共に 臨床試験 ( 調査含む ) 終了時までキーコードを保管し 盲験性を維持致します また 緊急時のエマージェンシーキーの開示 および 24 時間の緊急受付業務も行うことが可能です 主なサービス キーコードの作成 保管 識別不能性の確認作業 エマージェンシーキーの作成 治験薬の割付作業 エマージェンシーキーの開示業務 24 時間緊急受付業務 進捗管理 試験の進行プロセスを適正管理し 進捗状況をリアルタイムに掌握 検査時期のお知らせや調査票の発送 回収状況の管理などを中心とした臨床試験の進捗状況の管理を行い FAX メールにて通知 進捗状況は WEB でリアルタイム確認可能です 主なサービス 症例毎における来院ポイント / 予定検査項目の連絡 臨床試験 ( 調査含む ) の進捗状況レポートの作成 症例登録状況の管理 臨床試験 ( 調査含む ) の進行状況の管理 検査時期等のスケジュール連絡 医師からの中止 終了状況の受付 各種連絡書 CRF QOL 発送回収管理 GCP に対応した症例登録業務手順書を作成し 品質管理プロセスに沿った教育訓練を実施 WEB による動的割付等を利用した登録も可能です CRF QOL 発送回収管理が可能です 症例登録状況をグラフ等でご提供することが可能です 割付作業手順書の作成により 大量な薬剤割付でも正確な作業工程をご提案いたします 記録類の作成 識別不能性の確認を行っています 業務案内 2
17 データマネジメント 高品質かつスピーディな徹底した品質管理で 高品質データのご提供をお約束します 膨大なデータの科学的妥当性 整合性を確認しながら GCP GPSP ならびに関連法規要件を満たし データマネジメント (DM) 業務計画書に基づいた一貫したサービスを提供します ダブルエントリーによるデータ入力から論理チェック 最終データ作成まで 徹底した品質管理で 高品質データのご提供をお約束します 準備期間が短い急なご要望にも対応 常時 150~180 プロトコール程度の DM 業務が稼働 約 500 本の受託実績から得られたマネージメントノウハウと規模により 準備期間が短い急なご要望にも対応いたします データマネジメント強化ソリューション 主なサービス CRF 設計 DM 計画書の作成 データベース設計 / 入力画面設計 ロジカルチェック マニュアルチェック仕様の作成 データマネジメントシステム作成 システムバリデーションの実施 データ入力 / 修正 / コード化 ( 有害事象 合併症 薬剤 ) ロジカルチェック マニュアルチェックの実施 クエリ (DCF) の作成 症例検討会用資料の作成 データベースロック 解析用データセットの作成 データセンターサービス 大規模な製造販売後調査でネックとなるリソースと質の確保において クライアントの多様なニーズに対応できるノウハウとリソースをご活用いただける クライアント特化型 のデータマネジメントサービスです オフショア業務サービス 中国 CRO 最大手の当社子会社 上海日新医薬有限公司 にてオフショアリング クライアント対応および QC をイーピーエス ( 国内 ) DM のコア業務をオフショアで行うことにより コストを抑えつつ品質と納期を担保できるサービスです 弊社の強みである IT を利用し 効率的なデータマネジメントを行っています 豊富な受託実績により 癌をはじめとして 幅広い領域への対応が可能です 常時 150~180 プロトコールが稼動し 多くのスタッフを擁しているため 急なご要望にも対応が可能です 業務案内 3
18 統計解析 統計解析に関する計画の立案から解析報告書の作成まで 弊社が擁する多数の専門家の幅広い知識と 経験を基にデータを解析 有効性 安全性に関する適切な評価を行い 薬剤の特長を導き出します 解析処理はもちろんのこと 統計解析に関する計画の立案から解析報告書の作成まで 一連の業務に対応します メディカルライティング 各種疾患領域において効果的な薬事戦略をアドバイス 医薬品 医療機器の開発計画から承認までに必要な各種申請書類 各種報告書を 厳格な品質管理の下 可能な限り短時間で作成 各種疾患領域において 幅広い専門知識をもつ経験豊富なスタッフが 効果的な薬事戦略をご提案させていただきます 主なサービス 主なサービス プロトコール作成支援 ( 解析関連部分 症例数設計含む ) 解析計画書作成 解析プログラムの作成 結果出力 バリデーション 中間解析の実施 キーオープン会での解析実施 解析報告書作成 総括報告書 ( 解析関連部分 ) の作成支援 申請資料 (CTD 対応 ) 作成のための解析の実施 臨床試験の解析業務に関する各種コンサルティング 治験ならびに製造販売後臨床試験等に関する資料作成支援 ( 治験計画届 試験実施計画書 同意説明文書 症例報告書 治験薬概要書等 ) 臨床試験に於ける様々な報告書作成支援 ( 副作用報告書 総括報告書 ) 承認申請 再審査申請のための資料作成支援 (CTD に対応した申請資料 再審査申請資料 ) 論文作成支援 オーファンドラッグ指定申請書作成支援 インタビューフォーム作成または改訂支援 薬事コンサルティング 英文報告書の和訳とその品質管理 各種報告書 申請書類の英訳とその品質管理 ダブルプログラミング ダブルチェックによりプロセスを保証することで 解析プログラムならびに結果の品質を保証しています 様々な領域における中間解析を行うことが可能です 豊富な経験により 短期間で精度の高い解析を実現しています 専門性の高い人材を積極採用 専門教育プログラム等 教育面でも力を入れています 業務開始時に依頼者と十分に協議し 仕様書や報告書骨子等を作成することで要望事項を確実に把握し 成果物に反映するように努めています 手順書 仕様書等に従い記録を確実に残す等 画一的なプロセスにより品質を保証しています 業務案内 4
19 安全性情報対応 経験豊富な専門スタッフが迅速かつ的確にサポート 臨床開発関連システムと ASP サービス 臨床試験のスピードおよび品質を向上させる臨床 IT ソリューション 治験 製造販売後臨床試験 ( 調査 ) 文献学会調査等で発生した安全性情報の収集 評価分析 医薬品医療機器総合機構への報告書作成を 経験豊富な専門スタッフが支援 また 海外からの副作用 感染症例報告を 当局提出用フォーマットにコンバートします 主なサービス CIOMS Med Watch フォームによる海外情報の一次評価 和訳 国内における治験 製造販売後安全性情報の一次評価英訳 英語訳 (CIOMS Med Watch 作成 ) 業務 モニター MR への指示業務サポート 文献 学会等医薬品医療機器総合機構への研究報告 医薬品副作用感染症報告書 ( 案 ) 作成 医薬品医療機器総合機構への副作用 感染症等報告書 研究報告 措置報告 不具合報告書 ( 案 ) の作成と SGML 化 海外事業所 各国規制当局等宛の副作用報告書 ( 案 ) 作成および英訳 安全性情報管理業務全般のコンサルティング並びにその他関連業務全般 当社契約専門医師による有害事象のコンサルティング 各種報告書作成業務 ( 社内安全性評価委員会用資料 ( 案 ) 作成 HQ 海外提携会社用報告書 ( 案 ) 作成 ) 設立当初より症例登録 割付等 クライアントのニーズに合わせた多くのコンピューターシステムを開発 これらの豊富な開発経験と実績を活かし GCP GPSP ならびに関連法規を遵守し 臨床試験のスピードおよび品質を向上させる臨床 IT ソリューションをご提供します 主なサービス 受託試験 ( 業務 ) に特化した社内システムの開発 運用 臨床開発フルサポートシステムおよび個別業務サポートシステムの開発 販売 運用 システムを含めた臨床試験の人的サポート EPS の IT ソリューション E-DMS( ローカル ) / E-DMS Online(ASP 版 ) 看護計画支援システム 症例登録から解析データセット作成まで 臨床開発をフルサポートする ASP 版の臨床開発統合パッケージ モニタリングシステム 電子カルテシステム サービス提供 : 英語力のある製薬会社の経験者により フルサポートでの支援も可能です 安全性情報業務 MedDRA の知識を持った医師との契約により MedDRA のコーディングが可能です 当社契約専門医師による判断の困難な有害事象のコンサルティングが可能です CRO 業務の豊富な経験 ノウハウを生かし 現場を重視した適切で高いレベルのシステム開発を行います 蓄積されたノウハウは 随時システム開発に反映されます 関係会社である往来技術株式会社とのコラボレーションにより 大型システム開発の受託も可能です 日本の現場のニーズにマッチしたシステムをご提案いたします 業務案内 5
20 GCP 監査 独立した立場で臨床試験を評価 検証 コンサルティング 薬事 その他 経験豊富なスタッフと当社ネットワークで様々なニーズに対応 GCP 監査業務は 品質保証活動の一環として 臨床試験が GCP(GPSP) 薬事法 治験実施計画書 標準業務手順書等を遵守して行われているか否かを被監査部門から独立して評価 検証することにより 臨床試験の信頼性を向上させます 医薬品開発に関わる様々なニーズに対して 経験豊かなスタッフが対応いたします また 海外からの導入計画や 欧米 アジアでの臨床開発を 当社のネットワークを活かし 支援いたします 主なサポート コンサルティング 開発戦略 試験計画の立案 各種レビュー 海外からの導入 海外での臨床試験に対するコンサルティング 薬事コンサルティング その他 医薬品 医療機器開発全般に関するコンサルティング 主なサービス GCP および関連法規基準に従ったコンサルティング システム監査 治験実施医療機関の監査 個々の受託業務の社内および社外監査 医師主導治験に係る監査 薬事 標準業務手順書 (SOP) の整備ならびに運用支援 規制当局 ( 総合機構等 ) との相談サポート プロトコール作成支援 同意説明文書の作成支援 薬事代行業務 薬事申請サポート 国内管理人業務 その他 健康食品 保健機能食品におけるヒト試験実施支援 医師主導の臨床試験 大規模疫学調査等の実施支援 後発医薬品に対する生物学的同等性試験 申請支援 ISO9000 の概念を熟知し 臨床試験に精通したスタッフが対応いたします 製薬会社等で監査業務経験を持つスタッフにより 効率的で質の高い監査を実現いたします コミュニケーションスキルが高いスタッフにより 各種要求事項に的確に対応いたします 常に向上する意欲をもって 業務を行っています 悪性腫瘍系疾患 循環器系疾患 中枢神経系疾患をはじめとする各種疾病領域に特化したコンサルティングが可能です 薬事代行業務から医薬品 医療機器のコンサルティングまで ニーズに応じて 柔軟に対応いたします 業務案内 6
会社案内
 会社案内 1. 会社概要と沿革 2. 会社役員 組織図 3. サービスと業務 4. 受託実績 5. 売上と従業員数の推移 6.EPSグループ 会社案内 会社概要と沿革 代表者 設立 2014 年 7 月 資本金 U R L 代表取締役社長田中尚 1 億円 http://www.eps.co.jp センターオフィス 162-0822 東京都新宿区下宮比町 2 番 23 号つるやビル 代表 :03-5684-7797
会社案内 1. 会社概要と沿革 2. 会社役員 組織図 3. サービスと業務 4. 受託実績 5. 売上と従業員数の推移 6.EPSグループ 会社案内 会社概要と沿革 代表者 設立 2014 年 7 月 資本金 U R L 代表取締役社長田中尚 1 億円 http://www.eps.co.jp センターオフィス 162-0822 東京都新宿区下宮比町 2 番 23 号つるやビル 代表 :03-5684-7797
医師主導治験取扱要覧
 15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
JCROA自主ガイドライン第4版案 GCP監査WG改訂案及び意見
 受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
はじめに 個人情報保護法への対策を支援いたします!! 2005 年 4 月 個人情報保護法 全面施行致しました 個人情報が漏洩した場合の管理 責任について民事での損害賠償請求や行政処分などのリスクを追う可能性がござい ます 個人情報を取り扱う企業は いち早く法律への対応が必要になります コラボレーシ
 人材業界会社様向け プライバシーマーク取得支援サービスについてのご提案 コラボレーションプラス有限会社 104-0053 東京都中央区晴海 4-1-1 晴海 4 丁目ビル 3F TEL:03-5548-0886 E-Mail:[email protected] URL:www.colllaboration-plus.co.jp はじめに 個人情報保護法への対策を支援いたします!!
人材業界会社様向け プライバシーマーク取得支援サービスについてのご提案 コラボレーションプラス有限会社 104-0053 東京都中央区晴海 4-1-1 晴海 4 丁目ビル 3F TEL:03-5548-0886 E-Mail:[email protected] URL:www.colllaboration-plus.co.jp はじめに 個人情報保護法への対策を支援いたします!!
目次 自己紹介会社概要 (EPSグループについて) 業界概要 ( 業界を取り巻く環境 ) 各セグメントの概要株式について 2
 EPSグループのご紹介 EPSホールディングス株式会社 代表取締役社長 田代 伸郎 2016年9月10日 目次 自己紹介会社概要 (EPSグループについて) 業界概要 ( 業界を取り巻く環境 ) 各セグメントの概要株式について 2 自己紹介 代表取締役社長 田代 伸郎 たしろ しんろう 1955年 2月 宮崎県生まれ 1978年 3月 明治大学農学部卒 1978年 4月 株式会社相互生物医学研究所(現
EPSグループのご紹介 EPSホールディングス株式会社 代表取締役社長 田代 伸郎 2016年9月10日 目次 自己紹介会社概要 (EPSグループについて) 業界概要 ( 業界を取り巻く環境 ) 各セグメントの概要株式について 2 自己紹介 代表取締役社長 田代 伸郎 たしろ しんろう 1955年 2月 宮崎県生まれ 1978年 3月 明治大学農学部卒 1978年 4月 株式会社相互生物医学研究所(現
<4D F736F F D E34208EA18CB18EE891B182AB977697CC C8E8DB782B591D682A688CB978A>
 Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シ
 医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
標準業務手順 目次
 浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
CRO業界+EPSグループのご紹介
 CRO 業界 + のご紹介 イーピーエス株式会社 代表取締役社長田代伸郎 2014 年 10 月 11 日 次第 自己紹介 業界概要 EPSグループの概要 株式について 2 次第 自己紹介 業界概要 EPSグループの概要 株式について 3 自己紹介 代表取締役社長田代伸郎 ( たしろしんろう ) 1955 年 2 月宮崎県生まれ 1978 年 3 月明治大学農学部卒 1978 年 4 月株式会社相互生物医学研究所
CRO 業界 + のご紹介 イーピーエス株式会社 代表取締役社長田代伸郎 2014 年 10 月 11 日 次第 自己紹介 業界概要 EPSグループの概要 株式について 2 次第 自己紹介 業界概要 EPSグループの概要 株式について 3 自己紹介 代表取締役社長田代伸郎 ( たしろしんろう ) 1955 年 2 月宮崎県生まれ 1978 年 3 月明治大学農学部卒 1978 年 4 月株式会社相互生物医学研究所
SGEC 附属文書 理事会 統合 CoC 管理事業体の要件 目次序文 1 適用範囲 2 定義 3 統合 CoC 管理事業体組織の適格基準 4 統合 CoC 管理事業体で実施される SGEC 文書 4 CoC 認証ガイドライン の要求事項に関わる責任の適用範囲 序文
 SGEC 附属文書 2-8 2012 理事会 2016.1.1 統合 CoC 管理事業体の要件 目次序文 1 適用範囲 2 定義 3 統合 CoC 管理事業体組織の適格基準 4 統合 CoC 管理事業体で実施される SGEC 文書 4 CoC 認証ガイドライン の要求事項に関わる責任の適用範囲 序文この文書の目的は 生産拠点のネットワークをする組織によるCoC 認証を実施のための指針を設定し このことにより
SGEC 附属文書 2-8 2012 理事会 2016.1.1 統合 CoC 管理事業体の要件 目次序文 1 適用範囲 2 定義 3 統合 CoC 管理事業体組織の適格基準 4 統合 CoC 管理事業体で実施される SGEC 文書 4 CoC 認証ガイドライン の要求事項に関わる責任の適用範囲 序文この文書の目的は 生産拠点のネットワークをする組織によるCoC 認証を実施のための指針を設定し このことにより
PowerPoint プレゼンテーション
 研究開発課題名難病 希少疾患の医薬品開発におけるクリニカルイノベーションネットワーク構想の推進を目指した疾患登録システム ( 患者レジストリ ) の構築 研究開発代表者 国立研究開発法人国立精神 神経医療研究センター 資料 2-3 トランスレーショナルメディカルセンター 臨床研究支援室長 発表内容 本研究の目標 実施体制 Remudy の実績と課題 目指すもの 疾患登録システム レジストリの信頼性について
研究開発課題名難病 希少疾患の医薬品開発におけるクリニカルイノベーションネットワーク構想の推進を目指した疾患登録システム ( 患者レジストリ ) の構築 研究開発代表者 国立研究開発法人国立精神 神経医療研究センター 資料 2-3 トランスレーショナルメディカルセンター 臨床研究支援室長 発表内容 本研究の目標 実施体制 Remudy の実績と課題 目指すもの 疾患登録システム レジストリの信頼性について
MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1
 MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1 MDSAP 報告書の受入れの概要 (1/2) 日本は 平成 27 年 6 月にMDSAPに参加する旨を発表 関係者との意見交換を行い MDSAP 報告書の受け入れについて 以下の通知を発出した 平成 28 年 6 月 22 日薬生監麻発 0622 第 3 号 薬生機審発 0622
MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1 MDSAP 報告書の受入れの概要 (1/2) 日本は 平成 27 年 6 月にMDSAPに参加する旨を発表 関係者との意見交換を行い MDSAP 報告書の受け入れについて 以下の通知を発出した 平成 28 年 6 月 22 日薬生監麻発 0622 第 3 号 薬生機審発 0622
4.7.4 プロセスのインプットおよびアウトプット (1) プロセスへのインプット情報 インプット情報 作成者 承認者 備 考 1 開発に関するお客様から お客様 - の提示資料 2 開発に関する当社収集資 リーダ - 料 3 プロジェクト計画 完了報 リーダ マネージャ 告書 ( 暫定計画 ) 4
 サンプル : プロジェクト管理規定 4.7 プロジェクト立ち上げ 4.7.1 目的 本プロセスはリーダ主導で プロジェクト体制の確立とプロジェクト内容 分担 業務指示 プロジェクト目標 担当者別プロジェクト目標を開発メンバに周知徹底することによって 組織としての意識統一を図るとともに開発プロセスをスムーズに立ち上げることを目的とする 4.7.2 このプロセスにかかわる人物の役割と責務 部門 略記 参加
サンプル : プロジェクト管理規定 4.7 プロジェクト立ち上げ 4.7.1 目的 本プロセスはリーダ主導で プロジェクト体制の確立とプロジェクト内容 分担 業務指示 プロジェクト目標 担当者別プロジェクト目標を開発メンバに周知徹底することによって 組織としての意識統一を図るとともに開発プロセスをスムーズに立ち上げることを目的とする 4.7.2 このプロセスにかかわる人物の役割と責務 部門 略記 参加
8. 内部監査部門を設置し 当社グループのコンプライアンスの状況 業務の適正性に関する内部監査を実施する 内部監査部門はその結果を 適宜 監査等委員会及び代表取締役社長に報告するものとする 9. 当社グループの財務報告の適正性の確保に向けた内部統制体制を整備 構築する 10. 取締役及び執行役員は
 内部統制システム構築の基本方針 サントリー食品インターナショナル株式会社 ( 以下 当社 という ) は 下記のとおり 内部統制システム構築の基本方針を策定する Ⅰ. 当社の取締役 執行役員及び使用人並びに当社子会社の取締役 執行役員その他これ らの者に相当する者 ( 以下 取締役等 という ) 及び使用人の職務の執行が法令及び定款 に適合することを確保するための体制 1. 当社及び当社子会社 (
内部統制システム構築の基本方針 サントリー食品インターナショナル株式会社 ( 以下 当社 という ) は 下記のとおり 内部統制システム構築の基本方針を策定する Ⅰ. 当社の取締役 執行役員及び使用人並びに当社子会社の取締役 執行役員その他これ らの者に相当する者 ( 以下 取締役等 という ) 及び使用人の職務の執行が法令及び定款 に適合することを確保するための体制 1. 当社及び当社子会社 (
12_モニタリングの実施に関する手順書
 12_ モニタリングの実施に関する手順書 静岡県立大学大学院薬食生命科学総合学府薬学研究院薬食研究推進センター版数 :1.0 版作成年月日 :2014 月 8 月 1 日 ( 最終確定 :2015 年 1 月 14 日 ) 1. 目的と適用範囲 本手順書は 当該研究において モニターが モニタリングを適切に実施するための手順 その他必要な事項を定めるものである 2. 実施体制及び責務 2.1 研究責任者の責務研究責任者は
12_ モニタリングの実施に関する手順書 静岡県立大学大学院薬食生命科学総合学府薬学研究院薬食研究推進センター版数 :1.0 版作成年月日 :2014 月 8 月 1 日 ( 最終確定 :2015 年 1 月 14 日 ) 1. 目的と適用範囲 本手順書は 当該研究において モニターが モニタリングを適切に実施するための手順 その他必要な事項を定めるものである 2. 実施体制及び責務 2.1 研究責任者の責務研究責任者は
< F2D8E9197BF A836F815B2E6A7464>
 ( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
CROCO について
 CROCO について CROCO とは コース 正式名称 Clinical Research Online Professional Certification Program at Osaka University といい 大阪大学医学部附属病院が提供する 臨床研究に関する教育の e-learning サイトです 臨床研究を実施する研究者 専門職の方 倫理審査委員会の委員 事務局の方を対象に 臨床研究に必要な情報
CROCO について CROCO とは コース 正式名称 Clinical Research Online Professional Certification Program at Osaka University といい 大阪大学医学部附属病院が提供する 臨床研究に関する教育の e-learning サイトです 臨床研究を実施する研究者 専門職の方 倫理審査委員会の委員 事務局の方を対象に 臨床研究に必要な情報
静岡県立静岡がんセンター臨床研究事務局の業務手順書
 治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 6.0 平成 20 年 1 月 28
治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 6.0 平成 20 年 1 月 28
Microsoft PowerPoint - 運用 [互換モード]
![Microsoft PowerPoint - 運用 [互換モード] Microsoft PowerPoint - 運用 [互換モード]](/thumbs/91/105850431.jpg) 押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
[ 指針 ] 1. 組織体および組織体集団におけるガバナンス プロセスの改善に向けた評価組織体の機関設計については 株式会社にあっては株主総会の専決事項であり 業務運営組織の決定は 取締役会等の専決事項である また 組織体集団をどのように形成するかも親会社の取締役会等の専決事項である したがって こ
![[ 指針 ] 1. 組織体および組織体集団におけるガバナンス プロセスの改善に向けた評価組織体の機関設計については 株式会社にあっては株主総会の専決事項であり 業務運営組織の決定は 取締役会等の専決事項である また 組織体集団をどのように形成するかも親会社の取締役会等の専決事項である したがって こ [ 指針 ] 1. 組織体および組織体集団におけるガバナンス プロセスの改善に向けた評価組織体の機関設計については 株式会社にあっては株主総会の専決事項であり 業務運営組織の決定は 取締役会等の専決事項である また 組織体集団をどのように形成するかも親会社の取締役会等の専決事項である したがって こ](/thumbs/92/109921559.jpg) 実務指針 6.1 ガバナンス プロセス 平成 29( 2017) 年 5 月公表 [ 根拠とする内部監査基準 ] 第 6 章内部監査の対象範囲第 1 節ガバナンス プロセス 6.1.1 内部監査部門は ガバナンス プロセスの有効性を評価し その改善に貢献しなければならない (1) 内部監査部門は 以下の視点から ガバナンス プロセスの改善に向けた評価をしなければならない 1 組織体として対処すべき課題の把握と共有
実務指針 6.1 ガバナンス プロセス 平成 29( 2017) 年 5 月公表 [ 根拠とする内部監査基準 ] 第 6 章内部監査の対象範囲第 1 節ガバナンス プロセス 6.1.1 内部監査部門は ガバナンス プロセスの有効性を評価し その改善に貢献しなければならない (1) 内部監査部門は 以下の視点から ガバナンス プロセスの改善に向けた評価をしなければならない 1 組織体として対処すべき課題の把握と共有
品質マニュアル(サンプル)|株式会社ハピネックス
 文書番号 QM-01 制定日 2015.12.01 改訂日 改訂版数 1 株式会社ハピネックス (TEL:03-5614-4311 平日 9:00~18:00) 移行支援 改訂コンサルティングはお任せください 品質マニュアル 承認 作成 品質マニュアル 文書番号 QM-01 改訂版数 1 目次 1. 適用範囲... 1 2. 引用規格... 2 3. 用語の定義... 2 4. 組織の状況... 3
文書番号 QM-01 制定日 2015.12.01 改訂日 改訂版数 1 株式会社ハピネックス (TEL:03-5614-4311 平日 9:00~18:00) 移行支援 改訂コンサルティングはお任せください 品質マニュアル 承認 作成 品質マニュアル 文書番号 QM-01 改訂版数 1 目次 1. 適用範囲... 1 2. 引用規格... 2 3. 用語の定義... 2 4. 組織の状況... 3
バリデーション基準 1. 医薬品 医薬部外品 GMP 省令に規定するバリデーションについては 品質リスクを考慮し 以下の バリデーション基準 に基づいて実施すること 2. バリデーション基準 (1) バリデーションの目的バリデーションは 製造所の構造設備並びに手順 工程その他の製造管理及び品質管理の
 バリデーション基準 1. 医薬品 医薬部外品 GMP 省令に規定するバリデーションについては 品質リスクを考慮し 以下の バリデーション基準 に基づいて実施すること 2. バリデーション基準 (1) バリデーションの目的バリデーションは 製造所の構造設備並びに手順 工程その他の製造管理及び品質管理の方法 ( 以下この基準において 製造手順等 という ) が期待される結果を与えることを検証し これを文書とすることによって
バリデーション基準 1. 医薬品 医薬部外品 GMP 省令に規定するバリデーションについては 品質リスクを考慮し 以下の バリデーション基準 に基づいて実施すること 2. バリデーション基準 (1) バリデーションの目的バリデーションは 製造所の構造設備並びに手順 工程その他の製造管理及び品質管理の方法 ( 以下この基準において 製造手順等 という ) が期待される結果を与えることを検証し これを文書とすることによって
医療機器開発マネジメントにおけるチェック項目
 2018 年 11 月作成 医療機器開発マネジメントにおけるチェック項目 1. 各ステージゲートにおけるチェック項目 (1) チェック項目作成の目的従来個々の事業において実施されていた 事前 中間 事後の各ゲートにおける評価項目 Go/no-go の判断を 医療機器開発全期間を通して整理し 共通認識化する 技術的観点及び事業化の観点の双方を意識し 医療機器開発の特性を考慮したチェック項目を設定する
2018 年 11 月作成 医療機器開発マネジメントにおけるチェック項目 1. 各ステージゲートにおけるチェック項目 (1) チェック項目作成の目的従来個々の事業において実施されていた 事前 中間 事後の各ゲートにおける評価項目 Go/no-go の判断を 医療機器開発全期間を通して整理し 共通認識化する 技術的観点及び事業化の観点の双方を意識し 医療機器開発の特性を考慮したチェック項目を設定する
目次 4. 組織 4.1 組織及びその状況の理解 利害関係者のニーズ 適用範囲 環境活動の仕組み 3 5. リーダーシップ 5.1 経営者の責務 環境方針 役割 責任及び権限 5 6. 計画 6.1 リスクへの取り組み 環境目標
 版名 管理番号 4 版 原本 環境マニュアル 環境企業株式会社 目次 4. 組織 4.1 組織及びその状況の理解 2 4.2 利害関係者のニーズ 2 4.3 適用範囲 2 4.4 環境活動の仕組み 3 5. リーダーシップ 5.1 経営者の責務 4 5.2 環境方針 4 5.3 役割 責任及び権限 5 6. 計画 6.1 リスクへの取り組み 7 6.2 環境目標及び計画 8 6.3 変更の計画 9
版名 管理番号 4 版 原本 環境マニュアル 環境企業株式会社 目次 4. 組織 4.1 組織及びその状況の理解 2 4.2 利害関係者のニーズ 2 4.3 適用範囲 2 4.4 環境活動の仕組み 3 5. リーダーシップ 5.1 経営者の責務 4 5.2 環境方針 4 5.3 役割 責任及び権限 5 6. 計画 6.1 リスクへの取り組み 7 6.2 環境目標及び計画 8 6.3 変更の計画 9
授業計画書
 ICT 分野におけるプロジェクトマネージャーの育成促進を図るための PBL 授業計画書 i 目次 はじめに... 1 全体この授業の全体像... 2 1. 授業内容の概要... 2 2. 学習目標... 2 3. 対象者... 2 4. 進行計画... 3 5. 評価方法... 3 STEP1 プロジェクトの概要分析... 4 1. 授業内容の概要... 4 2. 学習目標... 4 3. 受講の前提条件
ICT 分野におけるプロジェクトマネージャーの育成促進を図るための PBL 授業計画書 i 目次 はじめに... 1 全体この授業の全体像... 2 1. 授業内容の概要... 2 2. 学習目標... 2 3. 対象者... 2 4. 進行計画... 3 5. 評価方法... 3 STEP1 プロジェクトの概要分析... 4 1. 授業内容の概要... 4 2. 学習目標... 4 3. 受講の前提条件
ISO19011の概要について
 3 技術資料 3-1 ISO19011 の概要について 従来の環境マネジメントシステムの監査の指針であった ISO14010 ISO14011 ISO1401 2 が改正 統合され 2002 年 10 月に ISO19011 として発行されました この指針は 単に審査登録機関における審査の原則であるばかりでなく 環境マネジメントシステムの第二者監査 ( 取引先等利害関係対象の審査 ) や内部監査に適用できる有効な指針です
3 技術資料 3-1 ISO19011 の概要について 従来の環境マネジメントシステムの監査の指針であった ISO14010 ISO14011 ISO1401 2 が改正 統合され 2002 年 10 月に ISO19011 として発行されました この指針は 単に審査登録機関における審査の原則であるばかりでなく 環境マネジメントシステムの第二者監査 ( 取引先等利害関係対象の審査 ) や内部監査に適用できる有効な指針です
臨床試験(治験)の手続きについて
 臨床試験 ( 治験 製造販売後臨床試験 ) の手続きについて 本書は 昭和大学横浜市北部病院における臨床試験 ( 治験 製造販売後臨床試験 ) の手続き等に関して記したものです 始める前にご一読下さい なお 下記手続きにおいて必要書類を提出される場合は臨床試験支援室 ( 連絡先 :10 ページ参照 ) までご連絡下さい - 試験依頼前 - 関係書類の入手 当院の臨床試験 ( 治験 製造販売後臨床試験
臨床試験 ( 治験 製造販売後臨床試験 ) の手続きについて 本書は 昭和大学横浜市北部病院における臨床試験 ( 治験 製造販売後臨床試験 ) の手続き等に関して記したものです 始める前にご一読下さい なお 下記手続きにおいて必要書類を提出される場合は臨床試験支援室 ( 連絡先 :10 ページ参照 ) までご連絡下さい - 試験依頼前 - 関係書類の入手 当院の臨床試験 ( 治験 製造販売後臨床試験
審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果
![審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果 審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果](/thumbs/92/108604766.jpg) 審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
スキル領域 職種 : マーケティング スキル領域と MK 経済産業省, 独立行政法人情報処理推進機構
 スキル領域と (1) マーケティング スキル領域と MK-1 2012 経済産業省, 独立行政法人情報処理推進機構 スキル領域 職種 : マーケティング スキル領域と MK-2 2012 経済産業省, 独立行政法人情報処理推進機構 専門分野 マーケティングのスキル領域 スキル項目 職種共通スキル 項目 全専門分野 市場機会の評価と選定市場機会の発見と選択 市場調査概念と方法論 市場分析 市場細分化
スキル領域と (1) マーケティング スキル領域と MK-1 2012 経済産業省, 独立行政法人情報処理推進機構 スキル領域 職種 : マーケティング スキル領域と MK-2 2012 経済産業省, 独立行政法人情報処理推進機構 専門分野 マーケティングのスキル領域 スキル項目 職種共通スキル 項目 全専門分野 市場機会の評価と選定市場機会の発見と選択 市場調査概念と方法論 市場分析 市場細分化
Microsoft Word - 第40回開催報告.doc
 第 40 回 GCP 教育支援講座 QC/QA ビキナーズコース 開催報告 GCP 部会特別プロジェクト 2 イーピーエス株式会社篠原真紀 2014 年 7 月 31 日 仏教伝道センタービル (BDK 会議室 )8 階 和 にて第 40 回となる GCP 教育支援講座 QC/QA ビキナーズコース を開催しました 講座開催当日は晴天にも恵まれ 78 名の方々にご参加いただきました 当該教育支援講座は
第 40 回 GCP 教育支援講座 QC/QA ビキナーズコース 開催報告 GCP 部会特別プロジェクト 2 イーピーエス株式会社篠原真紀 2014 年 7 月 31 日 仏教伝道センタービル (BDK 会議室 )8 階 和 にて第 40 回となる GCP 教育支援講座 QC/QA ビキナーズコース を開催しました 講座開催当日は晴天にも恵まれ 78 名の方々にご参加いただきました 当該教育支援講座は
静岡県立静岡がんセンター臨床研究事務局の業務手順書
 治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 1 目次 1. 目的と適用範囲...
治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 1 目次 1. 目的と適用範囲...
<90528DB88EBF96E2955B2E786C73>
 4. 品質マネジメントシステム 4.1 一般要求事項 1 組織が品質マネジメントシステムを確立する上で必要としたプロセスは何ですか? 2 営業 / 購買 / 設計のプロセスについて 1このプロセスはどのプロセスと繋がっていますか? また関係していますか? 2このプロセスの役割と目的は何ですか? 3このプロセスの運用 管理の判断基準と 方法は何ですか? 4このプロセスの運用 管理での必要な資源と情報は何ですか?(
4. 品質マネジメントシステム 4.1 一般要求事項 1 組織が品質マネジメントシステムを確立する上で必要としたプロセスは何ですか? 2 営業 / 購買 / 設計のプロセスについて 1このプロセスはどのプロセスと繋がっていますか? また関係していますか? 2このプロセスの役割と目的は何ですか? 3このプロセスの運用 管理の判断基準と 方法は何ですか? 4このプロセスの運用 管理での必要な資源と情報は何ですか?(
<4D F736F F D208DBB939C97DE8FEE95F18CB48D EA98EE58D7393AE8C7689E6816A2E646F63>
 信頼性向上のための 5 つの基本原則 基本原則 1 消費者基点の明確化 1. 取組方針 精糖工業会の加盟会社は 消費者を基点として 消費者に対して安全で信頼される砂糖製品 ( 以下 製品 ) を提供することを基本方針とします 1 消費者を基点とした経営を行い 消費者に対して安全で信頼される製品を提供することを明確にします 2フードチェーン ( 食品の一連の流れ ) の一翼を担っているという自覚を持って
信頼性向上のための 5 つの基本原則 基本原則 1 消費者基点の明確化 1. 取組方針 精糖工業会の加盟会社は 消費者を基点として 消費者に対して安全で信頼される砂糖製品 ( 以下 製品 ) を提供することを基本方針とします 1 消費者を基点とした経営を行い 消費者に対して安全で信頼される製品を提供することを明確にします 2フードチェーン ( 食品の一連の流れ ) の一翼を担っているという自覚を持って
製造販売後調査事務手続き等 について
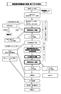 製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
スキル領域 職種 : ソフトウェアデベロップメント スキル領域と SWD 経済産業省, 独立行政法人情報処理推進機構
 スキル領域と (8) ソフトウェアデベロップメント スキル領域と SWD-1 2012 経済産業省, 独立行政法人情報処理推進機構 スキル領域 職種 : ソフトウェアデベロップメント スキル領域と SWD-2 2012 経済産業省, 独立行政法人情報処理推進機構 専門分野 ソフトウェアデベロップメントのスキル領域 スキル項目 職種共通スキル 項目 全専門分野 ソフトウェアエンジニアリング Web アプリケーション技術
スキル領域と (8) ソフトウェアデベロップメント スキル領域と SWD-1 2012 経済産業省, 独立行政法人情報処理推進機構 スキル領域 職種 : ソフトウェアデベロップメント スキル領域と SWD-2 2012 経済産業省, 独立行政法人情報処理推進機構 専門分野 ソフトウェアデベロップメントのスキル領域 スキル項目 職種共通スキル 項目 全専門分野 ソフトウェアエンジニアリング Web アプリケーション技術
<4D F736F F D A8D CA48F43834B C E FCD817A E
 介護支援専門員専門 ( 更新 ) 研修 ガイドラインの基本的考え方 2 介護支援専門員専門 ( 更新 ) 研修ガイドラインの基本的考え方 1. 基本方針 (1) 介護支援専門員の研修の目的 要介護者等が可能な限り住み慣れた地域で その人らしい 自立した生活を送るためには 多様なサービス主体が連携をして要介護者等を支援できるよう 適切にケアマネジメントを行うことが重要である その中核的な役割を担う介護支援専門員について
介護支援専門員専門 ( 更新 ) 研修 ガイドラインの基本的考え方 2 介護支援専門員専門 ( 更新 ) 研修ガイドラインの基本的考え方 1. 基本方針 (1) 介護支援専門員の研修の目的 要介護者等が可能な限り住み慣れた地域で その人らしい 自立した生活を送るためには 多様なサービス主体が連携をして要介護者等を支援できるよう 適切にケアマネジメントを行うことが重要である その中核的な役割を担う介護支援専門員について
臨床試験(治験)実施の手続き
 製造販売後調査実施の手続き はじめに 本書は 昭和大学藤が丘病院における製造販売後調査実施の手続き方法等について記載したものです 本書内のは当院が提供する書類を示し は審査等に必要な書類を示しております 調査内容により提出書類 資料に変更が生じる場合があります 詳細は支援室にご確認ください 申請する書類および資料は 事前に E-mail に添付して支援室にお送りください 内容の確認をし ご連絡させて頂きます
製造販売後調査実施の手続き はじめに 本書は 昭和大学藤が丘病院における製造販売後調査実施の手続き方法等について記載したものです 本書内のは当院が提供する書類を示し は審査等に必要な書類を示しております 調査内容により提出書類 資料に変更が生じる場合があります 詳細は支援室にご確認ください 申請する書類および資料は 事前に E-mail に添付して支援室にお送りください 内容の確認をし ご連絡させて頂きます
臨床評価とは何か ( 独 ) 医薬品医療機器総合機構医療機器審査第一部方眞美
 臨床評価とは何か ( 独 ) 医薬品医療機器総合機構医療機器審査第一部方眞美 本日の Agenda 1. 臨床評価とは 2. 医療機器の特性を踏まえた有効性 安全性評価 3. 各国の規制の違い 4. 臨床評価報告書について 5. 臨床評価報告書の概念 6. 臨床研究と治験の違いは? 7. 文献評価の問題点 8. 治験活性化にむけて 臨床評価 とは そのものの有効性と安全性をヒトで評価すること 自己認証の欧州から出てきた概念
臨床評価とは何か ( 独 ) 医薬品医療機器総合機構医療機器審査第一部方眞美 本日の Agenda 1. 臨床評価とは 2. 医療機器の特性を踏まえた有効性 安全性評価 3. 各国の規制の違い 4. 臨床評価報告書について 5. 臨床評価報告書の概念 6. 臨床研究と治験の違いは? 7. 文献評価の問題点 8. 治験活性化にむけて 臨床評価 とは そのものの有効性と安全性をヒトで評価すること 自己認証の欧州から出てきた概念
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社
 オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
<4D F736F F F696E74202D F817993FA967B90BB8E8695A897AC817A89DD95A892C790D F6C30362E707074>
 - スマートフォン (Android ) 利用による - 貨物追跡システム ( 位置情報サービス ASP サービス DP2) 日本製紙物流株式会社 http://www.np-log.co.jp/ システム導入目的について 導入目的 自社 / 配車センターと車両 ( トラック ) との情報共有 システム導入時のユーザー要望について 1. 配送進捗状況 車両最新位置 をリアルタイムで把握したい ユーザーからの配送
- スマートフォン (Android ) 利用による - 貨物追跡システム ( 位置情報サービス ASP サービス DP2) 日本製紙物流株式会社 http://www.np-log.co.jp/ システム導入目的について 導入目的 自社 / 配車センターと車両 ( トラック ) との情報共有 システム導入時のユーザー要望について 1. 配送進捗状況 車両最新位置 をリアルタイムで把握したい ユーザーからの配送
<4D F736F F F696E74202D E48FE A92C789C192CA926D82C982C282A282C45F696E6F75652E >
 E2B(R3) 追加通知について 日本製薬団体連合会 E2B(R3) 実装プロジェクト井上学 1 本日のお話 追加通知の概要 これから検討すべきこと 2 追加通知 ( 公開 ) 予定の概要 2013 年 9 月 17 日の通知で 追って通知 とされた部分 ICH E2Bでの検討結果に伴う変更 技術的な部分の補足 Q&A 3 R2 と R3 の比較 R2 R3 報告様式 SGML XML(HL7 形式
E2B(R3) 追加通知について 日本製薬団体連合会 E2B(R3) 実装プロジェクト井上学 1 本日のお話 追加通知の概要 これから検討すべきこと 2 追加通知 ( 公開 ) 予定の概要 2013 年 9 月 17 日の通知で 追って通知 とされた部分 ICH E2Bでの検討結果に伴う変更 技術的な部分の補足 Q&A 3 R2 と R3 の比較 R2 R3 報告様式 SGML XML(HL7 形式
J-SOX 自己点検評価プロセスの構築
 統制自己評価 (CSA) 支援サービスのご案内 目次 1. 弊社がご提供するサービス 2. 各サービスの詳細 1. 自己点検における評価モデルの構築支援 2. 請負を含めた実地指導 3. 会社による自己点検状況の評価とアドバイス ( 参考 1) 実施基準における自己点検の取扱い ( 参考 2) 実務指針 ( 改正案 ) における自己点検の取扱い ( 参考 3) 自己点検導入のメリット デメリット (
統制自己評価 (CSA) 支援サービスのご案内 目次 1. 弊社がご提供するサービス 2. 各サービスの詳細 1. 自己点検における評価モデルの構築支援 2. 請負を含めた実地指導 3. 会社による自己点検状況の評価とアドバイス ( 参考 1) 実施基準における自己点検の取扱い ( 参考 2) 実務指針 ( 改正案 ) における自己点検の取扱い ( 参考 3) 自己点検導入のメリット デメリット (
JISQ 原案(本体)
 目次 ページ序文 1 1 適用範囲 1 2 引用規格 1 3 用語及び定義 2 4 力量要求事項 2 5 労働安全衛生マネジメントシステム審査員に対する力量要求事項 2 5.1 一般 2 5.2 OH&Sの用語, 原則, プロセス及び概念 2 5.3 組織の状況 2 5.4 リーダーシップ, 働く人の協議及び参加 2 5.5 法的要求事項及びその他の要求事項 2 5.6 OH&Sリスク,OH&S 機会並びにその他のリスク及びその他の機会
目次 ページ序文 1 1 適用範囲 1 2 引用規格 1 3 用語及び定義 2 4 力量要求事項 2 5 労働安全衛生マネジメントシステム審査員に対する力量要求事項 2 5.1 一般 2 5.2 OH&Sの用語, 原則, プロセス及び概念 2 5.3 組織の状況 2 5.4 リーダーシップ, 働く人の協議及び参加 2 5.5 法的要求事項及びその他の要求事項 2 5.6 OH&Sリスク,OH&S 機会並びにその他のリスク及びその他の機会
ISO9001:2015規格要求事項解説テキスト(サンプル) 株式会社ハピネックス提供資料
 テキストの構造 1. 適用範囲 2. 引用規格 3. 用語及び定義 4. 規格要求事項 要求事項 網掛け部分です 罫線を引いている部分は Shall 事項 (~ すること ) 部分です 解 ISO9001:2015FDIS 規格要求事項 Shall 事項は S001~S126 まで計 126 個あります 説 網掛け部分の規格要求事項を講師がわかりやすく解説したものです
テキストの構造 1. 適用範囲 2. 引用規格 3. 用語及び定義 4. 規格要求事項 要求事項 網掛け部分です 罫線を引いている部分は Shall 事項 (~ すること ) 部分です 解 ISO9001:2015FDIS 規格要求事項 Shall 事項は S001~S126 まで計 126 個あります 説 網掛け部分の規格要求事項を講師がわかりやすく解説したものです
監査に関する品質管理基準の設定に係る意見書
 監査に関する品質管理基準の設定に係る意見書 監査に関する品質管理基準の設定について 平成 17 年 10 月 28 日企業会計審議会 一経緯 当審議会は 平成 17 年 1 月の総会において 監査の品質管理の具体化 厳格化に関する審議を開始することを決定し 平成 17 年 3 月から監査部会において審議を進めてきた これは 監査法人の審査体制や内部管理体制等の監査の品質管理に関連する非違事例が発生したことに対応し
監査に関する品質管理基準の設定に係る意見書 監査に関する品質管理基準の設定について 平成 17 年 10 月 28 日企業会計審議会 一経緯 当審議会は 平成 17 年 1 月の総会において 監査の品質管理の具体化 厳格化に関する審議を開始することを決定し 平成 17 年 3 月から監査部会において審議を進めてきた これは 監査法人の審査体制や内部管理体制等の監査の品質管理に関連する非違事例が発生したことに対応し
PowerPoint プレゼンテーション
 ectd v4.0 関連通知概要説明会 ectd v4.0 運用に向けた企業での準備 ICH プロジェクト委員会 M8 比留間良一 Disclaimer 本日の内容は一部, 演者の個人的見解を含んでいます 本資料の内容は今後の情勢の変化などにより, 変更されることがあります 皆さまが今後, 通知を読み,eCTD v4.0 対応を検討する上で, 本発表が参考になれば幸いです 日本製薬工業協会 ICHプロジェクト委員会
ectd v4.0 関連通知概要説明会 ectd v4.0 運用に向けた企業での準備 ICH プロジェクト委員会 M8 比留間良一 Disclaimer 本日の内容は一部, 演者の個人的見解を含んでいます 本資料の内容は今後の情勢の変化などにより, 変更されることがあります 皆さまが今後, 通知を読み,eCTD v4.0 対応を検討する上で, 本発表が参考になれば幸いです 日本製薬工業協会 ICHプロジェクト委員会
PowerPoint プレゼンテーション
 治験の電子化 IRB 5 分間セミナー 第 1 回臨床研究の分類と治験 第 11 回 CRCの業務 ( その2) 第 2 回治験とGCPの動向 第 12 回治験中の臨床検査等の精度管理 第 3 回治験の計画 選定 合意 第 13 回 ALCOA 原則とは 第 4 回治験審査委員会の役割 第 14 回治験の電子化 第 5 回 CROとSMOの業務 第 15 回有害事象と副作用 第 6 回被験者の選定と同意取得
治験の電子化 IRB 5 分間セミナー 第 1 回臨床研究の分類と治験 第 11 回 CRCの業務 ( その2) 第 2 回治験とGCPの動向 第 12 回治験中の臨床検査等の精度管理 第 3 回治験の計画 選定 合意 第 13 回 ALCOA 原則とは 第 4 回治験審査委員会の役割 第 14 回治験の電子化 第 5 回 CROとSMOの業務 第 15 回有害事象と副作用 第 6 回被験者の選定と同意取得
「GMP担当者研修・認定講座」の運用規定(案)
 GMP 担当者研修 認定講座 の概要 改訂 8 版 2018 年 8 月 1 日 NPO-QA センター 品質保証委員会 1 1. 趣旨 目的 2002 年の薬事法の全面改正により GQP 省令第 10 条では 製造販売業者は医薬品製造業者の GMP 実施状況の管理監督を義務づけられ GMP 省令第 18 条では 医薬品製造業者は GMP 実施状況の自己点検を義務づけられている GMP の実施については
GMP 担当者研修 認定講座 の概要 改訂 8 版 2018 年 8 月 1 日 NPO-QA センター 品質保証委員会 1 1. 趣旨 目的 2002 年の薬事法の全面改正により GQP 省令第 10 条では 製造販売業者は医薬品製造業者の GMP 実施状況の管理監督を義務づけられ GMP 省令第 18 条では 医薬品製造業者は GMP 実施状況の自己点検を義務づけられている GMP の実施については
GCP下での再委託における組織体制及び実施手順
 平成 25 年度政策委員会検討報告書 GCP 下での再委託における 組織体制及び実施手順 日本 CRO 協会 政策委員会 1. 背景 2. 用語 3. 目的 4. 本報告書の適用範囲 5. 再委託における品質管理 / 品質保証の基本的考え方 6. 再委託における調査及び監査の基本的考え方 7. 再委託における組織体制及び実施手順 8. その他留意すべき事項 2 1. 背景 再委託のニーズの拡大 CRO
平成 25 年度政策委員会検討報告書 GCP 下での再委託における 組織体制及び実施手順 日本 CRO 協会 政策委員会 1. 背景 2. 用語 3. 目的 4. 本報告書の適用範囲 5. 再委託における品質管理 / 品質保証の基本的考え方 6. 再委託における調査及び監査の基本的考え方 7. 再委託における組織体制及び実施手順 8. その他留意すべき事項 2 1. 背景 再委託のニーズの拡大 CRO
「GMP担当者研修・認定講座」の運用規定(案)
 GMP 担当者研修 認定講座 の概要 改訂 7 版 2017 年 9 月 1 日 NPO-QA センター 品質保証委員会 1 1. 趣旨 目的 2002 年の薬事法の全面改正により GQP 省令第 10 条では 製造販売業者は医薬品製造業者の GMP 実施状況の管理監督を義務づけられ GMP 省令第 18 条では 医薬品製造業者は GMP 実施状況の自己点検を義務づけられている GMP の実施については
GMP 担当者研修 認定講座 の概要 改訂 7 版 2017 年 9 月 1 日 NPO-QA センター 品質保証委員会 1 1. 趣旨 目的 2002 年の薬事法の全面改正により GQP 省令第 10 条では 製造販売業者は医薬品製造業者の GMP 実施状況の管理監督を義務づけられ GMP 省令第 18 条では 医薬品製造業者は GMP 実施状況の自己点検を義務づけられている GMP の実施については
ISO9001:2015内部監査チェックリスト
 ISO9001:2015 規格要求事項 チェックリスト ( 質問リスト ) ISO9001:2015 規格要求事項に準拠したチェックリスト ( 質問リスト ) です このチェックリストを参考に 貴社品質マニュアルをベースに貴社なりのチェックリストを作成してください ISO9001:2015 規格要求事項を詳細に分解し 212 個の質問リストをご用意いたしました ISO9001:2015 は Shall
ISO9001:2015 規格要求事項 チェックリスト ( 質問リスト ) ISO9001:2015 規格要求事項に準拠したチェックリスト ( 質問リスト ) です このチェックリストを参考に 貴社品質マニュアルをベースに貴社なりのチェックリストを作成してください ISO9001:2015 規格要求事項を詳細に分解し 212 個の質問リストをご用意いたしました ISO9001:2015 は Shall
はじめて医療機器を製造販売または製造される方へ
 を製造 ( 輸入 ) 販売するには 国内で必要な許可等について を製造販売 製造 ( 輸入 ) するためには 医薬品 等の品質 有効性及び安全性の確保等に関する法律 ( 以下 薬機法という ) の許可等 ( 製造販売業許可 製造業登録 ) が必要になります 製品を市場に出荷するために必要な許可 販売する製品に対して最終責製造販売業任を持ち 自社の名前で市場へ出荷する この許可では製造することはできません
を製造 ( 輸入 ) 販売するには 国内で必要な許可等について を製造販売 製造 ( 輸入 ) するためには 医薬品 等の品質 有効性及び安全性の確保等に関する法律 ( 以下 薬機法という ) の許可等 ( 製造販売業許可 製造業登録 ) が必要になります 製品を市場に出荷するために必要な許可 販売する製品に対して最終責製造販売業任を持ち 自社の名前で市場へ出荷する この許可では製造することはできません
