2月20日議事録
|
|
|
- れれ まるこ
- 5 years ago
- Views:
Transcription
1 薬事 食品衛生審議会動物用医薬品等部会議事録 日時 : 平成 14 年 2 月 20 日 ( 水 14:00~17:00 場所 : 農林水産省第 1 特別会議室 出席者委員 青木 宙 明石博臣 赤堀文昭 岡本信明 澤田拓士 辻本 元 中川秀樹 平山紀夫 星 欽彌 前田昌子 山口惠三 山本 亮 吉川泰弘 吉倉 廣 吉田仁夫 : 座長 衛生課 栗本まさ子 大石弘司 角田隆則 鎌田晶子 松尾佳典 関口秀人 山本欣也 水産庁 小關良二 増田真人 松本聡司 動物医薬品検査所牧江弘孝田村豊 議事 { } は事務局の回答 Ⅰ 審議事項 (1) 動物用医薬品の製造 ( 輸入 ) 承認の可否 毒 劇薬等の指定及び再審査期間の指定について [ 新規審議 ] 水産用医薬品調査会関係 新効能動物用医薬品 ( 製造承認事項変更承認 ) 5イリド不活化ワクチン ビケン ( 財 ) 阪大微生物病研究会 15ページの薬理試験のところで 高い有効性があると確認された とあるが この 高い とはどういう意味か { フィッシャーの直接確率計算法により 統計学的な有意差が認められたということである 不適当であれば 表現を直し 資料を整備する } { 承認を可とし 薬事分科会に報告する 再審査期間は事項変更前と同様 平成 16 年 12 月 24 日までとする }
2 [ 継続審議 ] 動物用生物学的製剤調査会関係 新有効成分含有動物用医薬品 新動物用配合剤 ( 輸入承認 ) 1 フェロバックス 5 共立製薬 ( 株 ) 当日配付資料 2-2 の対象動物に対する注意と資料 1 の下の枠の対象動物に対する注意のどちらがより理解しやすいか 一昨日の再評価調査会で 資料 1 の注意事項で 注射後 2 ヶ月以降 とすると 注射後 2 ヶ月経ってから現れるということになる しかし 注射後現れて 2 ヶ月前後で消失する場合もあるし 消失しないで持続する場合もあるので この表現では適切ではないのではないかという指摘があった そこで 当日配付資料の資料 2-2 の 注射後およそ 2 ヶ月を経過した後に となったのであるが これについて 委員のご意見を頂きたい 資料 2-2 だと 2 ヶ月前後の更にその前後は関係ないというようにとれる いかに啓蒙するかという問題なので 適切な表現はないか 資料 1 だと 2 ヶ月以降 となっているので 2 ヶ月より後ということで 2 ヶ月より前は関係ないということになる 資料 2-2 だと 2 ヶ月経過 となっており 経過であるから注射後の経過をずっと追っているわけであり こちらの方が適切であると思う 2 ヶ月 は 2 か月 が正しい { 追加で説明させて頂くと 平成 14 年 1 月 30 日の動物用生物学的製剤調査会で この 2 月 という表現も議論された 文献情報では 3 か月が一番短かったが 3 か月以降ということでは十分でないので それより短い 2 か月とし 以降という言葉をつければ十分ではないかということになった 硬結は出る場合もあるし 出ない場合もある それが続いて腫瘤となってしまうもの 途中から腫瘤ができてしまうものなど様々である ここで表現したいのは 肉腫化したものが存在する傾向にあるような時に 獣医師の診察を受けてほしいというように指導してほしいということである } 1 か月以内などの早い時期の発生の報告はないのか { 報告はないが 実際にはわからない } 今回の記載事項は 獣医師に正確な情報を提供して対応してもらうためのものだと思う 文献データでは 3 か月から 2 年が多いということを 対象動物に対する注意 の副作用の項に入れ 猫においては不活化ワクチンの注射の後 約 3 か月から 2 年の間において まれに線維肉腫等の肉腫が発生するおそれがある とし 下の方の適用上の注意の項は 時期については書かないほうが 獣医師としては正確な対応がしやすいのではないか 資料 2-2 を読むのは獣医師であるという考え方であり あくまでも客観的にこういう報告があるということを表現したほうがよい 情報は 対象動物に対する注意 の副作用の項に入れ 適用上の注意の項には期間などは書かなくてもよいのではないか 肉腫は 2 か月以前は発生しないという考えでよいのか 文献情報では一番短くて 3 か月である 注意を喚起するという意味で 副作用の項と適用上の注意の項は別にした方がわかりやすい 硬結といっても注射痕もあるが 2 か月たっても消失しないようなものに注意する 注射後の注意を喚起するとうことで およそ 2 か月 という表現を入れた方がよい 2 か月経っても硬結があるのはおかしい 接種後の注射痕と肉腫の見分けは 獣医師でないとできない 何か月以降という日数を記載する必要はないが 注射後に硬結腫脹が持続する場合には獣医師の治療を受けるというようにしたほうがよい
3 確率は入れるのか 確率を入れ 3 か月から 2 年くらいのあいだに発生したという報告を入れる 1/1,000 から 1/10,000 の確率で 3 か月以降 2 年くらいの間に発生したとる ということを記載すれば ワクチンを扱う獣医師は意味がわかる 資料 2-2 のような書き方をすると 現場の人間から 2 か月以前の発生はないという証明ができるのかという論議が出てきてしまう 副作用の項には事実をはっきり書き 獣医師に対して情報を提供する 適用上の注意には期間まで書かなくても 接種した後に増殖性の異常を認めたときに対応するというようにした方がわかりやすい 資料 2-2 の文章だと 2 か月前に何かが起こらなければよいというようにも読める 2 か月を過ぎれば大丈夫というようにも見える 注射後 2~3 か月硬結が持続し それが肉腫になるのか そういう場合もあるし 硬結が一旦治まって 2~3 か月から半年から 1 年後に肉腫になることがある その両方を含んだ表現法はないか 線維肉腫については発症の機序がよくわかっていない 獣医師の対応もまだあいまいである ここではっきりと決めてしまうのも不自然である なるべく獣医師の判断に任せたほうがいいのではないか 硬結があった場合 獣医師はどのように対応するのか 病理組織学的検査で 線維性か肉腫かを判断する 文献の情報をきちんと入れて 後の対応の仕方を表現するということで 承認を頂いたものとする { 資料 2-2 の 対象動物に対する注意 の副作用の項に 3 か月から 2 年の間に肉腫が発生したという報告があることを記載し 適用上の注意の項の 注射後およそ 2 か月経過した後 を削除し 注射部位に硬結や腫瘤が認められた場合は という部分を 注射部位に硬結や腫瘤が持続的に認められた場合 とすることを条件に 承認を可とし 薬事分科会に報告する 再審査期間は新有効成分含有医薬品 新動物用配合剤ということで 6 年とする } [ 新規審議 ] 動物用生物学的製剤調査会関係 新動物用配合剤 ( 製造承認 ) 2 京都微研 ピッグウィン -EA ( 株 ) 微生物化学研究所 アクチノバシラスは アクチノミセスとバチラスのどちらに近いのか { 昔はヘモフィルスと言っていた } これは 2 種類が混ざっているのか 抗原は何か アクチノバシラスの方は有効抗原としては Apx という細菌毒素である 細胞外に出てくる蛋白か そうである 豚丹毒菌の方は 細胞表面の蛋白である
4 培養上清と書いてあるが分泌蛋白か いわゆる外毒素ではない 豚丹毒菌はグラム陽性か陰性か グラム陽性桿菌である 概要 38 ページの表で 頭羽数 となっているが これは正しいのか { 頭数 に改める } 免疫の持続は抗体価で判断しているのか { はい } 抗体価はどのように測定しているのか 抗原は何を用いているのか { ワクチンの品質検査において モルモットに注射後の血清抗体価を測定することとしている 豚丹毒は 申請書の 28 ページに ELISA の抗原について規定されている 水酸化ナトム抽出抗原で 感染防御抗原である 67kDa タンパクに対する単クローン抗体を用いてイムブロッティングを行ったとき単一のバンドを認める アクチノバシラスは 申請書の 29 ページの付記 17 で CF 抗原を設定している 全菌体である } 薬理試験において 豚に接種した場合 ELISA により抗体価を測定している 2 回目の注射をしてから 少なくとも 90 日出荷しないということか { はい } { 承認を可とし 薬事分科会に報告する 再審査期間は新動物用配合剤ということで 6 年とする } 動物用抗菌性物質製剤調査会関係 新効能動物用医薬品 ( 製造承認 ) 3 動物用アミペニックス三鷹製薬 ( 株 ) 38 ページ 表 7-2 の総合評価判定基準で 細菌学的効果判定が減少あるいは消失した とはどういう意味か { 表 7-3 で 細菌が消失するかどうかというところで 減少あるいは消失しているということである } 25 ページに 何をもって消失 減少とするかを書いてあるが 詳しくは書いていない 申請者が減少としているのをそのまま減少としているのか 人間の場合 一般的には 10 の二乗のオーダーで減少したものを減少とする 動物の場合には設定されていないのか {38 ページで 消失とは観察終了時に菌が検出されなかった場合 減少とは開始時と比べて菌数が 1 オーダー以上低下した場合というように判定している } 起因菌が減少 消失したというのはわかるが 効果判定が減少したとはどういう意味か 表 7-2 の中の表現は事務局が然るべく修正してほしい 一点は 動物用医薬品製造承認経過表の中で 適応症が細菌性皮膚感染症となっているが なぜ皮膚疾患にこだわっているのか もう一点は 血中濃度は 6 時間でほとんどなくなってしまう この抗生剤は 人体では長い間使われてきたものだが 通常継続的に抗菌作
5 用を持続させて3 日間で抗菌作用の効果判定ができるとするなら 血中濃度は一定に保たないといけないが なぜ1 日 1 回の投与でよいのか 基本的な理由がわからない 現場の人間として この製剤をなぜ今販売しなければならないのかわからない アンピシリンは耐性菌が多いが こういう使用法は耐性菌を増加させるのではないか 本剤がなぜ申請されたかということであるが 臨床の現場では人体用のペニシリン系抗菌薬が注射薬として使われている 使い勝手として 動物用でもこのようなものがあった方がよいということであった アンピシリンは確かに耐性菌が多い 特に Staphyloco aureus の9 割は ペニシリナーゼを産生するので 効かないということになるが ここで申請されてきている黄色ブドウ球菌にはほとんど効いている 大腸菌にも効いているし シュードモナスは一般的には効かないが ここで分離されいるものについては効いている そういう事実はあった 1 日 1 回の投与については ペニシリンについてはpost - a effectということがあり 球菌に対しては高濃度を投与すれば ある程度効果は持続すいう考え方がある また 1 回の投与法で 対照群と比べて有意の差をもって効いているという事実がある そういうことで 本剤の有効性が認められたという経過であった 効果は非常に疑問である 効能効果では この 3 種類の細菌に対する感染症と書くべきであり なぜ皮膚疾患にこだわっているのかがよくわからない 症例として皮膚疾患などといれるのであれば それはかまわない アンピシリンがこのような形で小動物を対象として承認されて市販されるようになれば 従来の使い方でこの承認された薬を動物薬として使用するようになるだろう 当然 皮膚疾患に限らず広範に使うことになる その時 使用説明書を見ると 1 日 1 回で効くということで使われるだろう 著効はいいのだが 菌が減少した場合 そこで打ち切られると おそらく耐性菌ができるという心配もある 現場としては非常に疑問である 従って この場合は対象疾患が皮膚感染症 こういう菌種に対して 1 日 1 回の使用で有意差をもって効果があった という論法でいくとそれを否定する理由はない { 平成 13 年 7 月に行われた動物用抗菌性物質製剤調査会で部会に上程して差し支えないというご判断をいただいたが 再審査期間は 2 年間あるので 有効菌種のペニシリナーゼ産生に関する資料を整備するということであった } 申請された細菌をチェックしやすいということで 皮膚病に限定したのではないか それから先ほどのご指摘でもあったが 小動物でのアンピシリン製剤はない 人体用を流用している PL 法のからみで 犬用があってもいいというような狙いではないか 使う側からみると 動物用のアンピシリンが限られた範囲の適応症しかないと 現場のとまどいがあるかもしれない それから 1 日 1 回の使用だと 耐性菌が心配である { 市販された後の使用は個々の獣医師のご判断ということになるが ご要望が多ければ メーカーのほうで考えていくということもあるだろう 少なくとも 2 年間は再審査期間ということで 耐性菌についても調査していくということになっている } 1 日 1 回使うというのは 獣医の臨床をやっているものにとってはナンセンスである バックグラウンドとして 大動物では 1 日 1 回しか打てないということでそういう形で承認されているという流れで 犬でもそのような形で申請されていると思う 農林水産省に申請があった時点で 大動物に対する抗生物質と小動物に対する抗生物質で判断を変えて 小動物の臨床での使い方に合った形で申請するようにやり直させた方がよい 今回はデータから否定することはできないが 今後はそのように指導してほしい ヒアリング段階あるいは最初に実験を組む段階で指導するということか はい 1 日 1 回で用法用量を厳守することと書いてあるが 厳守しない方がいい 例えば 外国でのアンピシリンの犬での使用法はだいたい決まっているが 日本ではこうだ
6 というと 遅れていると思われるだろう その辺りを 小動物臨床の現場に即した形で指導していただきたいというのが希望である 現実に 1 日 1 回注射を打ち その後注射を打てなければ 錠剤を飲ませて血中濃度を維持するということは可能である 今のご意見は 一般論として抗生物質ならどのように使わせるかということである 今回は注射薬として申請してきているので 効能が切れるときにもう一度病院に行きなさいというのか 後は獣医師の判断に任せるのか つまり実情に即していないということである 今後はそのあたりを考慮してほしい どういう薬の時は 何回に分けて投与しなければいけない ということか 人の場合 1 回法はむしろ副作用が少なくて効果があるというものが 特にフルオロキノロンなどで出てきている あるいはカルバペネム系などでは post-antibiotic effect 量を上げておいて 1 回にするということもある 今回の試験は 何回かに分けて投与した場合との比較がないのでなんとも言えないが 1 回が悪いと否定する理由もない 調査会の中で こういう方法を守らなければいけないというスタンスがあれば 従来法と比べて 1 回法がどうであるという比較をしなさい という形で助言しないといけない 現場に即したという形をどういうようにしたいのか 調査会でコメントがなくて この場でいきなりそのような話をされても非常にとまどう 確かに この申請を否定しなければいけない理由はない しかし 1 日 2 回投与した場合は 1 回よりもいい効果が出るだろう そうであれば 実際にはそういった形で臨床試験をするように指導してほしい アンピシリンの場合は 人間でも犬でも猫でも 1 日 2~3 回というのが普通の使い方であろうし 1 回の方がいいとは誰も言っていないと思うので 現在の妥当な使用法に即した形で申請してほしい このような使い方をする製剤が小動物になかったので 比較ができなかったということだが 欧米での使い方を参考にして助言をしたらどうかということはあっただろう 犬の細菌性皮膚感染症自体が非常に曖昧である 実際に 抗生剤を必要とするものが どれくらいあるか評価するのは難しい 今回は客観的なデータが出ているので それは認めざるを得ない これがアンピシリンの最初の承認であって 次に出てきたものは違う使い方をするようであればいいが やり方として これを変えた方がいい と言えば変えられるが 変えるのは難しい それはヒアリングの段階で言うべきであって 部会で言うべきではない 販売名が 動物用アミペニックス で 既に人体用は アミペニックス という製剤が販売されている 今まで人体用の アミペニックス を使っていたのが 動物用アミペニックス は 1 日 1 回で効くということで 人体用とどのように違うのかが明確でなく 現場は混乱するのではないか { 先ほどヒアリングの段階で指導すべきというご指摘があったが ヒアリングでも データを見て それが適切であれば調査会にかけるというのが基本的な姿勢である 現場でいかに使われているかということは ヒアリングの段階ではこちらは承知していないので そのようなことを指摘するように言われても困難である } ヒアリングの時既にあるデータがある { ある製剤を開発する時に どこまで試験の組み方を指導するかは やり方によっては申請者に過大な負担をかけるおそれがある 小動物の場合 人体用の製剤がかなり使用されているが できる限り動物用の製剤を開発してもらう方が望ましい 負担が大きくなり 人体用の製剤をそのまま使うという方向に向かってしまうことは好ましくないので これから検討が必要である この製剤は 2 年間再審査期間があり その間使用実態について 皮膚疾患に使われたものだけでなく 色々な形で使われたものについてもデータを集めて検討するよ
7 う指導することは可能だと思う } その際 投与量を本当に守ったのか それとも もっと広げて考えたのかも調査するべきである { 何か薬を使用しようと思ったとき 必ずしもそれに適した承認品目があるとは限らないのが実態 そのようなときは 効能が承認されていなくても 獣医師の責任で使用することになるが この製剤についても そのようになることはあるだろう } 最初の段階で 臨床の状況はわからないから指摘できないということであったが その体制は変えた方がよい 今後は 小動物の薬であれば 小動物の臨床についてわかっている人間がヒアリングするという状況を作った方がいいのではないか { ヒアリングはあくまで事務局の審査であり 調査会では当然小動物の臨床の先生もいらっしゃる ヒアリングの段階では データに問題がなければ さらにデータを要求することはできない } 現場で 2 回打たなければいけないという理由もない 1 回で効けばよい この 3 種の細菌の感染が疑われる場合 第一選択でアンピシリンは使わない 心配なのは こういう製剤が出てくると 従来は人体用薬を使っていたのが 動物用は 1 日 1 回で効果があるんだという考え方で漫然と使っていって その中で耐性菌が増えていくことによって逆にアンピシリンが効かなくなるということである それを予防するために アンピシリンは一定の血中濃度を維持して使わなければならない 先ほど言われたような postantibiotic effect を期待するのであれば 新たに そういう話をしていかい 耐性菌を出さないということであれば 血中濃度を高く上げておいて 中途半端な濃度にしないということが重要である 皮膚疾患のような場合 1 回で効果があるのかどうかは非常に不安であるが きちんとしたデザインの実験で この結果では効いている 2 回法と比較するというデザインではなかったので ここではそれについて言及することはできない 今後 投与法について 日本ではなかったからということではなくて 諸外国に同様の製剤があるのであれば それを参考としてそれとの比較においてみるという形にすれば ヒアリングの段階でも指摘できるのではないか 動物薬メーカーは 一般的に今まで産業動物の方に目が向いていて 小動物の現場を必ずしもご存じない これからは小動物にも目を向けるように指導してもらえれば 今回のようなことはこれから少なくなるだろう だんだん動物専用の薬は増えると思われるが 指導の方をよろしくお願いする それでは承認ということでよろしいか { 承認を可とし 薬事分科会に報告する 再審査期間は 新効能動物用医薬品ということで 2 年とする } 動物用抗菌性物質製剤調査会 動物用医薬品残留問題調査会関係 新効能動物用医薬品 ( 輸入承認 ) 4 経口用ミコラル日本イーライリリー ( 株 ) ミコラル経口液日本全薬工業 ( 株 ) 資料の 54 ページで アイソトープを用いた試験を行っているが これは外国で行った試験か それとも国内で行った試験か { イーライリリー社が海外で行った試験である }
8 概要の 62 ページの効果判定結果というところで 表 ⅩⅡ-1 で 実施機関で A は経口投与 B は強制経口投与という分け方で試験を行っている 結果として A ではほとんどが著効で有効はゼロ B では著効はゼロで全部有効となっている どのような考察がなされたのか { 概要書には載っていないが 申請書の資料の方で 実施施設の B ではウイルス性の呼吸器感染症が発生したため やや効果が低くなったという考察がされている } 投与の方法による違いについては 考察していないのか { そこまでは考察していない } 74 ページの用法用量というところで 経口または強制的に経口投与する という書き方であるが あえて 強制的に経口投与 とは記載しなくてもよいのではないか 経口投与 は 強制も通常の投与も含む このように書くと強制的に経口投与した方が効果があるように誤解される可能性もあるし 自分で飲める状態であれば 自分で飲ませるのが自然である 飲めないのを無理に飲ませるのは 生体にとって好ましい状態ではない 試験の成績で 強制経口投与の方がいいという結果が出ているのなら話は別であるが 強制経口投与は削除して 経口投与だけでよいと思う また 混和するものということで なぜ飲水が含まれていないのか 通常薬を投与する場合 水で投与するのが一番効果がある 子牛は下痢の合併症が多いが その場合は断乳する その時 どうやって飲ませればよいのか 通常の水もここに入れておくべきではないのか 経口補液という意味は ミネラルを含んだような液か 経口補液剤というものがある 用法用量について 一番最初に認可されたイタリアの例では飲水が入っている なぜ飲水をとったのか { 国内で行われた試験では症例として飲水投与がなかった } 試験の方法をみると 代用乳と混和し としか書いていない 乳も経口補液もない 試験はただ代用乳だけの試験である { ヒアリング指摘事項回答書 3 つめの 1 ページ 12 月 14 日のところで 一番下に最初 代乳等 と書いてあって その 等 とは何かとヒアリングで指摘している 回答では 代用乳を用いた強制経口投与ということを明確にした } 今のところで 代用乳を添加せず強制経口投与 となっているが これはただの水を用いたのか これは液剤なので 液剤を飲ませたということではないか 乳に混ぜなければいけない 補液剤でなければいけないということではなく あくまで液状にして飲みやすくするということではないのか そうすると 単純に水ではいけないのか { ヒアリング指摘事項で明確にしてほしいとの指摘をして それに回答してきているのであるから 飲水を加えても問題はないと考える } 是非 飲水を加えてほしい そうでないと使いづらい 飲水を使って飲ませて 同様な血中濃度が得られるとか体内動態であるというようなデータは欧米でないのか 生後 6 か月以内に投与するということであるが 液体を投与した場合に 第一胃に入るのか あるいは第三胃に直接入るのか 最終的に腸管で吸収されるのなら どちらでも同じかもしれないが 第一胃に入った場合は少し異なるのではないか なぜ強制経口投与になったかというと 自由に飲ませるとばらつきが出る可能性があるため しっかり飲ませるという形で試験を行うということでこのようになったのであろう それはわかるが 経口投与という表現ですべてが包含される あえて強制経口投与と書くと なぜ強調しているのか疑問に思う 食欲のないものに無理して投与してはいけないと注
9 意書きに書いてあるにもかかわらず 用法用量で強制経口投与という書き方はいかがなものか 飲水を加えていいかどうかは 単純に考えていいのではないか { 水だけで投与したデータは今手持ちではないが この場で飲水を加えた方がいいということであれば 加えても支障はないのではないか } 溶かし方によって 吸収も違ってくるだろう 実際に試験は行っていないが 大体同じだろうということでやるのか それとも吸排のデータがあれば それをもとに適用を拡大するのか 74 ページの国外における用法及び用量 添付資料 1 で 代用乳または飲水に添加し経口投与する となっている おそらくデータはあるのではないか なければ飲水を加えるのは難しいだろう 代用乳は 通常 生後 40~50 日までにしか与えない その後 どうやって飲ませるのか わざわざ代用乳を調達して飲ませるのか 現場では使いづらい データがないのに可とするのはどうか 先ほどの添付資料 1 で データが確認できればよいのではないか 強制経口投与にも 瓶などから飲ませるのと カテーテルを胃まで入れて飲ませるのと 2 種類ある すべて経口投与に含まれるので あえて加えなくてもよいのではないか 今回は データを取るときに条件を同じにしてばらつきを押さえるために強制経口投与したのであろう 表現上は経口投与だけでよいのではないか { 使用規制省令で 製剤の分類がかなり細かくなっている 飲水添加 飼料添加 強制経口投与という分類になっている } 強制という言葉が妥当ではない 人では監視下投与という しっかり飲んだことを確認するという方法がある 飲水投与の場合 投与量はどのように確認するのか { 飲むであろう量より少し少ない量の水に薬剤を溶き 全量飲ませる } { 用法用量の書き方としては 経口投与で十分わかるので 使用規制省令の分類との関係を検討することとしたい } 飲水添加の資料がなかった場合には その実験を加える 拡大解釈で飲水添加を加えるということはしないということでよいのか そうである 国内外の文献 実験系をチェックして 乳 代用乳 水 経口補液剤の 4 種類のデータが揃っていれば 問題はない もし欠落しているものがあれば それは除く 中途半端な拡大解釈はしないということでよろしいか { 海外のデータで 臨床試験成績はおそらくあるだろう それだけでもよろしいか } 臨床試験で効果があれば問題ない 希釈なしの投与はどうするのか データがなければ難しい { おそらく飲水に添加した場合と強制経口投与の臨床試験の成績はあるだろう データが揃ったところでお知らせをして それで了とさせて頂きたい } それを確認した上で承認ということでよろしいか
10 { 以下のとおり申請書を検討 整備した上で各委員の了承を得ることを条件に 承認を可とし 薬事分科会に報告する 再審査期間は新効能動物用医薬品ということで 2 年とする (1) 本剤の用法は 代用乳 乳 経口補液に均一に混和して経口投与又は強制的に経口投与する とすると設定されているが 申請書の薬理試験は代用乳添加により 臨床試験は代用乳添加及び強制経口投与により また 残留試験は 代用乳添加により実施されている これらの申請書の添付資料からは 本剤の用法は 代用乳に均一に混和して経口投与又は強制的に経口投与する とすることが適当と考えられるが 代用乳 乳 経口補液に均一に混和して と設定した根拠を明確にするとともに 関係資料を整備すること (2) 本剤は 6 か月までの牛を対象としているが およそ 3 か月以降の乳牛には代用乳が使用されないため 飲水投与されることが多いと想定される また 概要の 3 ページのイタリアにおける用法では 飲水添加が設定されているので 想定される使用実態に合わせるため 関連資料を整備し 用法に飲水添加を追加することについて検討すること (3) 本剤の用法として 強制的に経口投与する が設定されているにもかかわらず 使用上の注意では 強制経口投与の対象とされると考えられる 食欲が著しく低下したり 廃絶した症例 には 十分な吸収が得られないため 使用しないこと とされており 矛盾している 本剤の用法としての強制経口投与についてその必要性等を再考すること } (2) 動物用抗生物質医薬品基準の一部改正案について 動物用抗菌性物質製剤調査会関係 特になし { 原案通り 薬事分科会に報告する } (3) 動物用医薬品の使用の規制に関する省令の一部改正案について 動物用医薬品残留問題調査会関係 { 用法が 代用乳 乳 経口補液に混和ということなので 飼料添加剤 強制経口投与剤という 2 種類を設定することとしているが 飲水添加剤についても 申請者による用法の整備とともに整備したい } 経口補液剤はどうか { 強制経口で与える場合 経口補液剤に混ぜて与えることを想定していた 直接経口で与えることが想定されるのであれば 強制経口投与剤は残しておいて 飲水添加剤という項目を作った方がよいと思う } 当日配付資料 No.4 の 2 枚目で 強制的に経口投与すること とあるが 薬物そのままも水に溶いてもいいと拡大解釈することはできる そうすればこのままでも問題はない { 自由に摂取するという意味の飲水添加剤を加えた方がいいのではないか } 飲水添加の場合も カテーテルで飲ませたり 瓶で飲ませたりすることもある 飼料添加ということであれば 必ず強制的というのも含まれる { 使用規制省令の中で飼料添加剤 飲水添加剤 強制経口投与剤の定義があるので それとの関連を検討して整備する }
11 薬剤によっては強制投与はあり得る これに関しては強制はいけないのかということは議論していない 経口の場合 自由に摂取する場合と強制的に飲まされる場合がある その時の担体として飲水の時もあれば 単味の時もあるというものを 縦につなごうとするから混乱が起こる 事務局に どういう表現が可能かを検討してもらうということで承認とする { 指摘事項を検討した上で 薬事分科会に報告する } (4) 動物用医薬品の再評価について 動物用医薬品再評価調査会関係 1 カルバドックス Codex で再評価される結果が出るまで こちらでは判断しないのか それとも 情報をきながら判断するのか {Codex の判断を待つつもりはないが その場合はここに書かない方がよいか } 再評価に指定する条件の一つとしてあげられるが これによって左右されるものではない ここで通れば薬事 食品衛生審議会薬事分科会までダイレクトにいくのか { 審議ではなく 報告である } { その後の手順をご説明すると 分科会に報告してご了承いただければ その後告示となる 再評価指定した段階で 承認をもっている業者から 引き続きこの製剤について販売を続けたいということであれば 再評価申請をして頂く その後 調査会 部会 薬事分科会と処理していく } チェックは入るのか { 今回の審議で すべての判断をするわけではない } その場合の調査会は 抗菌性物質製剤調査会か { まず 再評価調査会である } 資料 6 の 26 ページと 27 ページで 製造量と販売量が違っている { 在庫があったということである } そうだとは思うが 危ないからさっさと売ってしまえというようなことだと怖い { 数字については確認する } { 原案どおり 本成分を再評価指定することとし 薬事分科会に報告する } 2 酸化エチレン 現実に養蚕分野でどのくらい使われているのか {23 ページをご覧いただきたいが 大部分を全農が取り扱っている 全農に問い合わせたところ 4 製剤のうちカポックスについては全く使っていない エポンミニについても平成 12 年度までは在庫のみあったが 13 年度においては在庫もない おそらくほとんど使われていないと考えられる } これだけ見ると 日本では使われていないように見える
12 { 今回対象にしている成分はおそらくほとんど使われていないことを確認した } { 原案どおり 本成分を再評価指定することとし 薬事分科会に報告する } Ⅱ 報告事項 (5) 動物用医薬品の再評価について 動物用医薬品再評価調査会関係 1 ナリジクス酸 2 ピペロニルブトキサイド 3 アロエ 4 フェノール < 特に質疑なし > < 質疑結果 > 報告を了承した (6) 動物用医薬品の再審査について 動物用医薬品再評価調査会関係 1 オイルバックス NB 2 AC 2 オイルバックス NB 2 G 3 豚 Hpn3 価ワクチン 北研 4 馬鼻肺炎不活化ワクチン 日生研 5マリンサワー SP30 < 特に質疑なし> < 質疑結果 > 報告を了承した ( 財 ) 化学及血清療法研究所 ( 財 ) 化学及血清療法研究所 ( 社 ) 北里研究所 ( 株 ) 日生研株式会社 ( 株 ) 片山化学工業研究所 (7) 動物用医薬品の諮問 承認状況について < 特に質疑なし > < 質疑結果 > 報告を了承した Ⅲ その他 (1) オルビフロキサシンを含有する外用剤の取扱いについて < 特に質疑なし > < 質疑結果 > 原案を了承した (2) 薬事法の一部を改正する法律案について < 特に質疑なし > < 質疑結果 > 報告を了承した (3) 次回の開催予定は平成 14 年 5 月 22 日とした
審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ]
![審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ] 審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ]](/thumbs/91/105024304.jpg) 審査報告書 平成 26 年 2 月 7 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所
審査報告書 平成 26 年 2 月 7 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所
審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7
![審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7 審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7](/thumbs/92/110490968.jpg) 審査報告書 平成 26 年 1 月 6 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [
審査報告書 平成 26 年 1 月 6 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [
医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など ) 医薬品候補物質のスクリーニン
 特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
シプロフロキサシン錠 100mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを
 シプロフロキサシン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを有し 上気道感染症 尿路感染症 皮膚感染症などに有効なニューキノロン系の合成抗菌剤である シプロキサン 錠
シプロフロキサシン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを有し 上気道感染症 尿路感染症 皮膚感染症などに有効なニューキノロン系の合成抗菌剤である シプロキサン 錠
抗菌薬の殺菌作用抗菌薬の殺菌作用には濃度依存性と時間依存性の 2 種類があり 抗菌薬の効果および用法 用量の設定に大きな影響を与えます 濃度依存性タイプでは 濃度を高めると濃度依存的に殺菌作用を示します 濃度依存性タイプの抗菌薬としては キノロン系薬やアミノ配糖体系薬が挙げられます 一方 時間依存性
 2012 年 1 月 4 日放送 抗菌薬の PK-PD 愛知医科大学大学院感染制御学教授三鴨廣繁抗菌薬の PK-PD とは薬物動態を解析することにより抗菌薬の有効性と安全性を評価する考え方は アミノ配糖体系薬などの副作用を回避するための薬物血中濃度モニタリング (TDM) の分野で発達してきました 近年では 耐性菌の増加 コンプロマイズド ホストの増加 新規抗菌薬の開発の停滞などもあり 現存の抗菌薬をいかに科学的に使用するかが重要な課題となっており
2012 年 1 月 4 日放送 抗菌薬の PK-PD 愛知医科大学大学院感染制御学教授三鴨廣繁抗菌薬の PK-PD とは薬物動態を解析することにより抗菌薬の有効性と安全性を評価する考え方は アミノ配糖体系薬などの副作用を回避するための薬物血中濃度モニタリング (TDM) の分野で発達してきました 近年では 耐性菌の増加 コンプロマイズド ホストの増加 新規抗菌薬の開発の停滞などもあり 現存の抗菌薬をいかに科学的に使用するかが重要な課題となっており
2012 年 2 月 29 日放送 CLSI ブレイクポイント改訂の方向性 東邦大学微生物 感染症学講師石井良和はじめに薬剤感受性試験成績を基に誰でも適切な抗菌薬を選択できるように考案されたのがブレイクポイントです 様々な国の機関がブレイクポイントを提唱しています この中でも 日本化学療法学会やアメ
 2012 年 2 月 29 日放送 CLSI ブレイクポイント改訂の方向性 東邦大学微生物 感染症学講師石井良和はじめに薬剤感受性試験成績を基に誰でも適切な抗菌薬を選択できるように考案されたのがブレイクポイントです 様々な国の機関がブレイクポイントを提唱しています この中でも 日本化学療法学会やアメリカ臨床検査標準委員会 :Clinical and Laboratory Standards Institute
2012 年 2 月 29 日放送 CLSI ブレイクポイント改訂の方向性 東邦大学微生物 感染症学講師石井良和はじめに薬剤感受性試験成績を基に誰でも適切な抗菌薬を選択できるように考案されたのがブレイクポイントです 様々な国の機関がブレイクポイントを提唱しています この中でも 日本化学療法学会やアメリカ臨床検査標準委員会 :Clinical and Laboratory Standards Institute
Taro-プレミアム第66号PDF.jtd
 ソフトテニス誰でも 10 倍上達しますプレミアム PDF 版 no66 攻め 守りの新機軸 著作制作 :OYA 転載転用禁止です 2013/2/25 編 1, 攻め 守り後衛と対峙する前衛にとっては 相手後衛が攻撃してくるのか 守ってくるのかは とても重要な問題です 相手後衛が攻めてくるのであれば ポジション的に守らなければならないし 相手が守りでくるならば スマッシュを待ったり 飛び出したりする準備をしなければいけません
ソフトテニス誰でも 10 倍上達しますプレミアム PDF 版 no66 攻め 守りの新機軸 著作制作 :OYA 転載転用禁止です 2013/2/25 編 1, 攻め 守り後衛と対峙する前衛にとっては 相手後衛が攻撃してくるのか 守ってくるのかは とても重要な問題です 相手後衛が攻めてくるのであれば ポジション的に守らなければならないし 相手が守りでくるならば スマッシュを待ったり 飛び出したりする準備をしなければいけません
審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果
![審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果 審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果](/thumbs/92/108604766.jpg) 審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
<4D F736F F D204E6F2E342D F28DDC91CF90AB8BDB82C982C282A282C482CC C668DDA94C5816A F315F372E646F63>
 薬剤耐性菌についての Q&A 農林水産省 動物医薬品検査所 検査第二部抗生物質製剤検査室 初版 第二版 平成 21 年 11 月 24 日 平成 22 年 1 月 7 日 目 次 I. 抗菌性物質 3 1. 抗菌性物質とは? 2. 家畜における抗菌性物質の使用目的は? 3. 動物用医薬品として使われている抗菌性物質の種類を教えてください II. 薬剤耐性 ( 一般 ) 4 1. 薬剤耐性菌とは? 2.
薬剤耐性菌についての Q&A 農林水産省 動物医薬品検査所 検査第二部抗生物質製剤検査室 初版 第二版 平成 21 年 11 月 24 日 平成 22 年 1 月 7 日 目 次 I. 抗菌性物質 3 1. 抗菌性物質とは? 2. 家畜における抗菌性物質の使用目的は? 3. 動物用医薬品として使われている抗菌性物質の種類を教えてください II. 薬剤耐性 ( 一般 ) 4 1. 薬剤耐性菌とは? 2.
豚丹毒 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 23 年 2 月 8 日 ( 告示第 358 号 ) 新規追加 1 定義シードロット規格に適合した豚丹毒菌の培養菌液を不活化し アルミニウムゲルアジュバントを添加したワクチンである 2 製法 2.1 製造用株 名称豚丹
 豚丹毒 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 23 年 2 月 8 日 ( 告示第 358 号 ) 新規追加 1 定義シードロット規格に適合した豚丹毒菌の培養菌液を不活化し アルミニウムゲルアジュバントを添加したワクチンである 2 製法 2.1 製造用株 2.1.1 名称豚丹毒菌多摩 96 株 ( 血清型 2 型 ) 又はこれと同等と認められた株 2.1.2 性状感受性豚に接種すると
豚丹毒 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 23 年 2 月 8 日 ( 告示第 358 号 ) 新規追加 1 定義シードロット規格に適合した豚丹毒菌の培養菌液を不活化し アルミニウムゲルアジュバントを添加したワクチンである 2 製法 2.1 製造用株 2.1.1 名称豚丹毒菌多摩 96 株 ( 血清型 2 型 ) 又はこれと同等と認められた株 2.1.2 性状感受性豚に接種すると
畜水産物の安全確保のための取組
 目的 ( 第 1 条 ) 定義 ( 第 2 条 ) 医薬品及び医薬部外品の製造販売業及び製造業の許可 製造販売の承認等 ( 第 12 条 ~ 第 23 条 ) 販売業の許可等 ( 第 24 条 ~ 第 40 条の 7) 基準及び検定 ( 第 41~ 第 43 条 ) 取扱い 広告 安全対策等 ( 第 44 条 ~ 第 82 条 ) 動物用医薬品の安全確保 1 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律
目的 ( 第 1 条 ) 定義 ( 第 2 条 ) 医薬品及び医薬部外品の製造販売業及び製造業の許可 製造販売の承認等 ( 第 12 条 ~ 第 23 条 ) 販売業の許可等 ( 第 24 条 ~ 第 40 条の 7) 基準及び検定 ( 第 41~ 第 43 条 ) 取扱い 広告 安全対策等 ( 第 44 条 ~ 第 82 条 ) 動物用医薬品の安全確保 1 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律
記載データ一覧 品目名 製造販売業者 BE 品質再評価 1 マグミット錠 250mg 協和化学工業 2 酸化マグネシウム錠 250mg TX みらいファーマ 3 酸化マグネシウム錠 250mg モチダ 持田製薬販売 # 4 酸化マグネシウム錠 250mg マイラン マイラン製薬 # 5 酸化マグネシ
 医療用医薬品最新品質情報集 ( ブルーブック ) 2017.7.7 初版 有効成分 酸化マグネシウム 品目名 ( 製造販売業者 ) 1 マグミット錠 250mg 協和化学工業 後発医薬品 2 酸化マグネシウム錠 250mg TX みらいファーマ 3 酸化マグネシウム錠 250mg モチダ 持田製薬販売 4 酸化マグネシウム錠 250mg マイラン マイラン製薬 5 酸化マグネシウム錠 250mg ケンエー
医療用医薬品最新品質情報集 ( ブルーブック ) 2017.7.7 初版 有効成分 酸化マグネシウム 品目名 ( 製造販売業者 ) 1 マグミット錠 250mg 協和化学工業 後発医薬品 2 酸化マグネシウム錠 250mg TX みらいファーマ 3 酸化マグネシウム錠 250mg モチダ 持田製薬販売 4 酸化マグネシウム錠 250mg マイラン マイラン製薬 5 酸化マグネシウム錠 250mg ケンエー
よる感染症は これまでは多くの有効な抗菌薬がありましたが ESBL 産生菌による場合はカルバペネム系薬でないと治療困難という状況になっています CLSI 標準法さて このような薬剤耐性菌を患者検体から検出するには 微生物検査という臨床検査が不可欠です 微生物検査は 患者検体から感染症の原因となる起炎
 2014 年 7 月 9 日放送 薬剤耐性菌の動向と最近の CLSI 標準法の変更点 順天堂大学 臨床検査部係長 三澤 成毅 薬剤耐性菌の動向まず 薬剤耐性菌の動向についてお話しします 薬剤耐性菌の歴史は 1940 年代に抗菌薬の第一号としてペニシリンが臨床応用された頃から始まったと言えます 以来 新しい抗菌薬の開発 導入と これに対する薬剤耐性菌の出現が繰り返され 今日に至っています 薬剤耐性菌の近年の特徴は
2014 年 7 月 9 日放送 薬剤耐性菌の動向と最近の CLSI 標準法の変更点 順天堂大学 臨床検査部係長 三澤 成毅 薬剤耐性菌の動向まず 薬剤耐性菌の動向についてお話しします 薬剤耐性菌の歴史は 1940 年代に抗菌薬の第一号としてペニシリンが臨床応用された頃から始まったと言えます 以来 新しい抗菌薬の開発 導入と これに対する薬剤耐性菌の出現が繰り返され 今日に至っています 薬剤耐性菌の近年の特徴は
<945F96F B3816A2E786264>
 Q-14 食品衛生法 ( 昭和 22 年法律第 233 号 ) とは 1 食品衛生法について 食品衛生法とは食品の安全性の確保のために公衆衛生の見地から必要な規制その他の措置を講ずることにより 飲食に起因する衛生上の危害の発生を防止し もつて国民の健康の保護を図ることを目的として 食品の規格等の設定 検査の実施 健康を損なうおそれのある食品の販売の禁止などの事項を規定しています 適用範囲食品衛生法の中で
Q-14 食品衛生法 ( 昭和 22 年法律第 233 号 ) とは 1 食品衛生法について 食品衛生法とは食品の安全性の確保のために公衆衛生の見地から必要な規制その他の措置を講ずることにより 飲食に起因する衛生上の危害の発生を防止し もつて国民の健康の保護を図ることを目的として 食品の規格等の設定 検査の実施 健康を損なうおそれのある食品の販売の禁止などの事項を規定しています 適用範囲食品衛生法の中で
ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル
 ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル 1mg は 1 カプセル中ロペラミド塩酸塩 1 mg を含有し消化管から吸収されて作用を発現する このことから
ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル 1mg は 1 カプセル中ロペラミド塩酸塩 1 mg を含有し消化管から吸収されて作用を発現する このことから
JAO正会員としての知識確認テスト
 2013/03/07 薬事法 景品表示法に関する知識度テスト - 問題 - テスト実施日 受講者名 以下の問いに答えなさい 1. 景表法の正式名称を答えなさい 2. 景表法とはなにか説明しなさい 3. 使用の際特に注意をするべきワードとして お肉 NO1 カシミヤ 100% 利回り やせる 最安値 動物性鉄 ( 豚 ) などがあるが このワードを使用する際の注意点を述べなさい 4. 優良誤認表示とは何か説明しなさい
2013/03/07 薬事法 景品表示法に関する知識度テスト - 問題 - テスト実施日 受講者名 以下の問いに答えなさい 1. 景表法の正式名称を答えなさい 2. 景表法とはなにか説明しなさい 3. 使用の際特に注意をするべきワードとして お肉 NO1 カシミヤ 100% 利回り やせる 最安値 動物性鉄 ( 豚 ) などがあるが このワードを使用する際の注意点を述べなさい 4. 優良誤認表示とは何か説明しなさい
平成 26 年 8 月 6 日 於 農林水産省動物医薬品検査所研修室 一般医薬品調査会議事要旨 農林水産省
 平成 26 年 8 月 6 日 於 農林水産省動物医薬品検査所研修室 一般医薬品調査会議事要旨 農林水産省 動物用一般医薬品調査会 1. 日時及び場所 平成 26 年 8 月 6 日 10:30~ 農林水産省動物医薬品検査所研修室 2. 出席委員 (10 名 ) 五十音順 ( 敬称略 ) 座長安藤哲柿市徳英河上栄一小暮一雄児玉幸夫土屋亮冨田隆史 野上貞雄吉浦信幸渡邊忠男 欠席委員 (5 名 ) 大野耕一下田実袴塚高志藤井洋子武藤敦彦
平成 26 年 8 月 6 日 於 農林水産省動物医薬品検査所研修室 一般医薬品調査会議事要旨 農林水産省 動物用一般医薬品調査会 1. 日時及び場所 平成 26 年 8 月 6 日 10:30~ 農林水産省動物医薬品検査所研修室 2. 出席委員 (10 名 ) 五十音順 ( 敬称略 ) 座長安藤哲柿市徳英河上栄一小暮一雄児玉幸夫土屋亮冨田隆史 野上貞雄吉浦信幸渡邊忠男 欠席委員 (5 名 ) 大野耕一下田実袴塚高志藤井洋子武藤敦彦
調査概要 1 日 2 回でずっと効く コンタック 600 プラス を製造販売するグラクソ スミスクライン株式会社のコンタック総合研究所 ( は 花粉シーズン到来を前に ドラッグストアや薬局 薬店で販売されている鼻炎薬を含めた 市販薬の知識 & イメージ
 コンタック総合研究所 市販薬の知識 & イメージテスト調査 2012 年 2 月 グラクソ スミスクライン株式会社 1 調査概要 1 日 2 回でずっと効く コンタック 600 プラス を製造販売するグラクソ スミスクライン株式会社のコンタック総合研究所 (http://contac.jp/soken/) は 花粉シーズン到来を前に ドラッグストアや薬局 薬店で販売されている鼻炎薬を含めた 市販薬の知識
コンタック総合研究所 市販薬の知識 & イメージテスト調査 2012 年 2 月 グラクソ スミスクライン株式会社 1 調査概要 1 日 2 回でずっと効く コンタック 600 プラス を製造販売するグラクソ スミスクライン株式会社のコンタック総合研究所 (http://contac.jp/soken/) は 花粉シーズン到来を前に ドラッグストアや薬局 薬店で販売されている鼻炎薬を含めた 市販薬の知識
卸-11-2.indd
 Q ①国家備蓄に関し およそこの10年 緊急にワク No.1450 コレラワクチンの販売中止について 2009年10月 チンを接種したケースがない ②現在のコレラの治療方針について 基本的には 経口または点滴で水分と電解質を補い 並行し て抗生物質による抗菌治療を実施するとされて コレラワクチンは コレラ菌による急性感染性 おり 以上の併用治療により 大体死亡率は 腸炎であるコレラの予防に用いるもので
Q ①国家備蓄に関し およそこの10年 緊急にワク No.1450 コレラワクチンの販売中止について 2009年10月 チンを接種したケースがない ②現在のコレラの治療方針について 基本的には 経口または点滴で水分と電解質を補い 並行し て抗生物質による抗菌治療を実施するとされて コレラワクチンは コレラ菌による急性感染性 おり 以上の併用治療により 大体死亡率は 腸炎であるコレラの予防に用いるもので
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社
 オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
日本脳炎不活化ワクチン ( シード ) 平成 24 年 7 月 4 日 ( 告示第 1622 号 ) 新規追加 1 定義シードロット規格に適合した日本脳炎ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を不活化したワクチンである 2 製法 2.1 製造用株 名称日本脳炎ウイル
 日本脳炎不活化ワクチン ( シード ) 平成 24 年 7 月 4 日 ( 告示第 1622 号 ) 新規追加 1 定義シードロット規格に適合した日本脳炎ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を不活化したワクチンである 2 製法 2.1 製造用株 2.1.1 名称日本脳炎ウイルス中山株薬検系又はこれと同等と認められた株 2.1.2 性状豚腎初代細胞で増殖し がちょう 鶏初生ひな及びはとの赤血球を凝集する
日本脳炎不活化ワクチン ( シード ) 平成 24 年 7 月 4 日 ( 告示第 1622 号 ) 新規追加 1 定義シードロット規格に適合した日本脳炎ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を不活化したワクチンである 2 製法 2.1 製造用株 2.1.1 名称日本脳炎ウイルス中山株薬検系又はこれと同等と認められた株 2.1.2 性状豚腎初代細胞で増殖し がちょう 鶏初生ひな及びはとの赤血球を凝集する
保健機能食品制度 特定保健用食品 には その摂取により当該保健の目的が期待できる旨の表示をすることができる 栄養機能食品 には 栄養成分の機能の表示をすることができる 食品 医薬品 健康食品 栄養機能食品 栄養成分の機能の表示ができる ( 例 ) カルシウムは骨や歯の形成に 特別用途食品 特定保健用
 資料 1 食品の機能性表示に関する制度 平成 25 年 4 月 4 日 消費者庁 保健機能食品制度 特定保健用食品 には その摂取により当該保健の目的が期待できる旨の表示をすることができる 栄養機能食品 には 栄養成分の機能の表示をすることができる 食品 医薬品 健康食品 栄養機能食品 栄養成分の機能の表示ができる ( 例 ) カルシウムは骨や歯の形成に 特別用途食品 特定保健用食品 保健の機能の表示ができる
資料 1 食品の機能性表示に関する制度 平成 25 年 4 月 4 日 消費者庁 保健機能食品制度 特定保健用食品 には その摂取により当該保健の目的が期待できる旨の表示をすることができる 栄養機能食品 には 栄養成分の機能の表示をすることができる 食品 医薬品 健康食品 栄養機能食品 栄養成分の機能の表示ができる ( 例 ) カルシウムは骨や歯の形成に 特別用途食品 特定保健用食品 保健の機能の表示ができる
添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示され
 添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示されます 検索条件設定時の注意 検索はテキスト文章 (SGML 又は XML) が対象となっており 画像及び
添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示されます 検索条件設定時の注意 検索はテキスト文章 (SGML 又は XML) が対象となっており 画像及び
57巻S‐A(総会号)/NKRP‐02(会長あいさつ)
 β β β β β β β β β β シンポジウム 1 創薬物語 科学者としての喜びの瞬間 4 レボフロキサシンに至る創薬研究 よりよい薬を求めて 第一三共株式会社 研究開発本部 研究開発企画部 早川勇夫 レボフロキサシン クラビット 1 は 1993 年上市された世界初の光学活性のニューキノロン系抗菌薬 以 下 ニューキノロンと略 である 1 は 1985 年に上市されたラセミ体のオフロキサシン
β β β β β β β β β β シンポジウム 1 創薬物語 科学者としての喜びの瞬間 4 レボフロキサシンに至る創薬研究 よりよい薬を求めて 第一三共株式会社 研究開発本部 研究開発企画部 早川勇夫 レボフロキサシン クラビット 1 は 1993 年上市された世界初の光学活性のニューキノロン系抗菌薬 以 下 ニューキノロンと略 である 1 は 1985 年に上市されたラセミ体のオフロキサシン
ども これを用いて 患者さんが来たとき 例えば頭が痛いと言ったときに ではその頭痛の程度はどうかとか あるいは呼吸困難はどの程度かということから 5 段階で緊急度を判定するシステムになっています ポスター 3 ポスター -4 研究方法ですけれども 研究デザインは至ってシンプルです 導入した前後で比較
 助成研究演題 - 平成 22 年度国内共同研究 ( 年齢制限なし ) JTAS 導入前後の看護師によるトリアージの変化 山勢博彰 ( やませひろあき ) 山口大学大学院医学系研究科教授 ポスター -1 テーマは JTAS 導入前後の看護師によるトリアージの変化 ということで 研究の背景は 救急医療ではコンビニ化ということが問題になっていて 真に緊急性が高い患者さんがなかなか効率よく受診できない あるいは診療まで流れないという問題があります
助成研究演題 - 平成 22 年度国内共同研究 ( 年齢制限なし ) JTAS 導入前後の看護師によるトリアージの変化 山勢博彰 ( やませひろあき ) 山口大学大学院医学系研究科教授 ポスター -1 テーマは JTAS 導入前後の看護師によるトリアージの変化 ということで 研究の背景は 救急医療ではコンビニ化ということが問題になっていて 真に緊急性が高い患者さんがなかなか効率よく受診できない あるいは診療まで流れないという問題があります
2006 年 3 月 3 日放送 抗菌薬の適正使用 市立堺病院薬剤科科長 阿南節子 薬剤師は 抗菌薬投与計画の作成のためにパラメータを熟知すべき 最初の抗菌薬であるペニシリンが 実質的に広く使用されるようになったのは第二次世界大戦後のことです それまで致死的な状況であった黄色ブドウ球菌による感染症に
 2006 年 3 月 3 日放送 抗菌薬の適正使用 市立堺病院薬剤科科長 阿南節子 薬剤師は 抗菌薬投与計画の作成のためにパラメータを熟知すべき 最初の抗菌薬であるペニシリンが 実質的に広く使用されるようになったのは第二次世界大戦後のことです それまで致死的な状況であった黄色ブドウ球菌による感染症に対して ペニシリンは劇的な効果を発揮しました しかし その後ペニシリンが広範囲に使用されたことによって
2006 年 3 月 3 日放送 抗菌薬の適正使用 市立堺病院薬剤科科長 阿南節子 薬剤師は 抗菌薬投与計画の作成のためにパラメータを熟知すべき 最初の抗菌薬であるペニシリンが 実質的に広く使用されるようになったのは第二次世界大戦後のことです それまで致死的な状況であった黄色ブドウ球菌による感染症に対して ペニシリンは劇的な効果を発揮しました しかし その後ペニシリンが広範囲に使用されたことによって
未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名要望された医薬品要望内容 CSL ベーリング株式会社要望番号 Ⅱ-175 成分名 (10%) 人免疫グロブリン G ( 一般名 ) プリビジェン (Privigen) 販売名 未承認薬 適応 外薬の分類
 未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名要望された医薬品要望内容 CSL ベーリング株式会社要望番号 Ⅱ-175 成分名 (10%) 人免疫グロブリン G ( 一般名 ) プリビジェン (Privigen) 販売名 未承認薬 適応 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) ( 要望されたについて記載する
未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名要望された医薬品要望内容 CSL ベーリング株式会社要望番号 Ⅱ-175 成分名 (10%) 人免疫グロブリン G ( 一般名 ) プリビジェン (Privigen) 販売名 未承認薬 適応 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) ( 要望されたについて記載する
< F2D838F815B834E B B>
 ワークシート ディベートは こうていがわひていがわ肯定側と否定側に分かれて行う 討論ゲーム です ディベートの様子をビデオで見てみましょう ディベートをすると 筋道を立てて考えることわかりやすく話すこと相手の話をしっかり聴くことよくメモを取ることなどの練習ができます ディベートの討論するテーマを 論題といいます -- これから, みなさんといっしょに ディベート学習 を通して 筋道立てて考える力 (
ワークシート ディベートは こうていがわひていがわ肯定側と否定側に分かれて行う 討論ゲーム です ディベートの様子をビデオで見てみましょう ディベートをすると 筋道を立てて考えることわかりやすく話すこと相手の話をしっかり聴くことよくメモを取ることなどの練習ができます ディベートの討論するテーマを 論題といいます -- これから, みなさんといっしょに ディベート学習 を通して 筋道立てて考える力 (
耐性菌届出基準
 37 ペニシリン耐性肺炎球菌感染症 (1) 定義ペニシリン G に対して耐性を示す肺炎球菌による感染症である (2) 臨床的特徴小児及び成人の化膿性髄膜炎や中耳炎で検出されるが その他 副鼻腔炎 心内膜炎 心嚢炎 腹膜炎 関節炎 まれには尿路生殖器感染から菌血症を引き起こすこともある 指定届出機関の管理者は 当該指定届出機関の医師が (2) の臨床的特徴を有する者を診察した結果 症状や所見からペニシリン耐性肺炎球菌感染症が疑われ
37 ペニシリン耐性肺炎球菌感染症 (1) 定義ペニシリン G に対して耐性を示す肺炎球菌による感染症である (2) 臨床的特徴小児及び成人の化膿性髄膜炎や中耳炎で検出されるが その他 副鼻腔炎 心内膜炎 心嚢炎 腹膜炎 関節炎 まれには尿路生殖器感染から菌血症を引き起こすこともある 指定届出機関の管理者は 当該指定届出機関の医師が (2) の臨床的特徴を有する者を診察した結果 症状や所見からペニシリン耐性肺炎球菌感染症が疑われ
医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能
 医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 1 2 3 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能 ) ( 医薬品の名称のみで検索する場合 34 の項目は未選択 未入力で可 ) 検索結果で表示したい文書を選択
医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 1 2 3 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能 ) ( 医薬品の名称のみで検索する場合 34 の項目は未選択 未入力で可 ) 検索結果で表示したい文書を選択
1 2
 1 2 ECO 3 4 5 6 7 8 全てのゾーンには 新規納入からメンテナンスに至るまで お客様をサポートします 抗菌が要求されます 一般清潔区域 病院内全てのゾーンで生活環境を汚染する菌類からの汚染防止対策として 抗菌フィルター をお勧めします 高度清潔区域 清 潔 区 域 準清潔区域 ① 細菌類 ② 真菌類 酵母類 製 作 ご 提 案 銀 ゼ オライトの 抗 菌 抗 カ ビ の メ カ ニ
1 2 ECO 3 4 5 6 7 8 全てのゾーンには 新規納入からメンテナンスに至るまで お客様をサポートします 抗菌が要求されます 一般清潔区域 病院内全てのゾーンで生活環境を汚染する菌類からの汚染防止対策として 抗菌フィルター をお勧めします 高度清潔区域 清 潔 区 域 準清潔区域 ① 細菌類 ② 真菌類 酵母類 製 作 ご 提 案 銀 ゼ オライトの 抗 菌 抗 カ ビ の メ カ ニ
項目 薬剤耐性 (AMR) 対策アクションプランについて 耐性菌の基礎知識 薬剤耐性モニタリング (JVARM) の成績 コリスチン耐性について 薬剤耐性菌のリスク分析 動物用医薬品の慎重使用について 2
 項目 薬剤耐性 (AMR) 対策アクションプランについて 耐性菌の基礎知識 薬剤耐性モニタリング (JVARM) の成績 コリスチン耐性について 薬剤耐性菌のリスク分析 動物用医薬品の慎重使用について 2 1,000 万人 120 万人 820 万人 70 万人 厚労省が 政策会議 ( 第 1 回薬剤耐性に関する検討調整会議 ;H27.12) に提出した資料 ( 首相官邸 HP より ); 一部改変
項目 薬剤耐性 (AMR) 対策アクションプランについて 耐性菌の基礎知識 薬剤耐性モニタリング (JVARM) の成績 コリスチン耐性について 薬剤耐性菌のリスク分析 動物用医薬品の慎重使用について 2 1,000 万人 120 万人 820 万人 70 万人 厚労省が 政策会議 ( 第 1 回薬剤耐性に関する検討調整会議 ;H27.12) に提出した資料 ( 首相官邸 HP より ); 一部改変
Ⅲ-3 試用医薬品に関する基準 平成 10 年 1 月 20 日公正取引委員会届出改定平成 13 年 3 月 19 日公正取引委員会届出改定平成 16 年 5 月 25 日公正取引委員会届出改定平成 17 年 3 月 29 日公正取引委員会届出改定平成 26 年 6 月 16 日公正取引委員会 消費
 Ⅲ-3 試用医薬品に関する基準 平成 10 年 1 月 20 日公正取引委員会届出改定平成 13 年 3 月 19 日公正取引委員会届出改定平成 16 年 5 月 25 日公正取引委員会届出改定平成 17 年 3 月 29 日公正取引委員会届出改定平成 26 年 6 月 16 日公正取引委員会 消費者庁長官届出 本基準は規約第 5 条第 3 号 施行規則第 2 条 ( 試用医薬品提供基準 ) に基づくものである
Ⅲ-3 試用医薬品に関する基準 平成 10 年 1 月 20 日公正取引委員会届出改定平成 13 年 3 月 19 日公正取引委員会届出改定平成 16 年 5 月 25 日公正取引委員会届出改定平成 17 年 3 月 29 日公正取引委員会届出改定平成 26 年 6 月 16 日公正取引委員会 消費者庁長官届出 本基準は規約第 5 条第 3 号 施行規則第 2 条 ( 試用医薬品提供基準 ) に基づくものである
2009年8月17日
 医師 2,000 人超の調査結果を多数掲載中です https://www.facebook.com/medpeer 2013 年 8 月 22 日 メドピア株式会社 医薬部外品の安全性 について 安全性に問題を抱える場合があると考える医師が 8 割以上 医師約 6 万人が参加する医師専用サイト MedPeer ( メドピア https://medpeer.jp/) を運営するメドピア 株式会社
医師 2,000 人超の調査結果を多数掲載中です https://www.facebook.com/medpeer 2013 年 8 月 22 日 メドピア株式会社 医薬部外品の安全性 について 安全性に問題を抱える場合があると考える医師が 8 割以上 医師約 6 万人が参加する医師専用サイト MedPeer ( メドピア https://medpeer.jp/) を運営するメドピア 株式会社
( 別添 ) 御意見 該当箇所 一般用医薬品のリスク区分 ( 案 ) のうち イブプロフェン ( 高用量 )(No.4) について 意見内容 <イブプロフェン ( 高用量 )> 本剤は 低用量製剤 ( 最大 400mg/ 日 ) と比べても製造販売後調査では重篤な副作用の報告等はない 一方で 今まで
 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第三十六条の七第一項第一号及び第二号の規定に基づき厚生労働大臣が指定する第一類医薬品及び第二類医薬品 の一部改正に係る意見の募集について に対して寄せられた御意見について 厚生労働省医薬 生活衛生局安全対策課 1. 意見募集期間 : 平成 28 年 6 月 3 日 ( 金 ) から平成 28 年 7 月 2 日 ( 土 ) まで 2. 提出意見数
医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第三十六条の七第一項第一号及び第二号の規定に基づき厚生労働大臣が指定する第一類医薬品及び第二類医薬品 の一部改正に係る意見の募集について に対して寄せられた御意見について 厚生労働省医薬 生活衛生局安全対策課 1. 意見募集期間 : 平成 28 年 6 月 3 日 ( 金 ) から平成 28 年 7 月 2 日 ( 土 ) まで 2. 提出意見数
馬ロタウイルス感染症 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 24 年 7 月 4 日 ( 告示第 1622 号 ) 新規追加 1 定義シードロット規格に適合した馬ロタウイルス (A 群 G3 型 ) を同規格に適合した株化細胞で増殖させて得たウイルス液を不活化し アジュバント
 馬ロタウイルス感染症 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 24 年 7 月 4 日 ( 告示第 1622 号 ) 新規追加 1 定義シードロット規格に適合した馬ロタウイルス (A 群 G3 型 ) を同規格に適合した株化細胞で増殖させて得たウイルス液を不活化し アジュバントを添加したワクチンである 2 製法 2.1 製造用株 2.1.1 名称馬ロタウイルス Ho-5MA 株又はこれと同等と認められた株
馬ロタウイルス感染症 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 24 年 7 月 4 日 ( 告示第 1622 号 ) 新規追加 1 定義シードロット規格に適合した馬ロタウイルス (A 群 G3 型 ) を同規格に適合した株化細胞で増殖させて得たウイルス液を不活化し アジュバントを添加したワクチンである 2 製法 2.1 製造用株 2.1.1 名称馬ロタウイルス Ho-5MA 株又はこれと同等と認められた株
大学院博士課程共通科目ベーシックプログラム
 平成 30 年度医科学専攻共通科目 共通基礎科目実習 ( 旧コア実習 ) 概要 1 ). 大学院生が所属する教育研究分野における実習により単位認定可能な実習項目 ( コア実習項目 ) 1. 組換え DNA 技術実習 2. 生体物質の調製と解析実習 3. 薬理学実習 4. ウイルス学実習 5. 免疫学実習 6. 顕微鏡試料作成法実習 7. ゲノム医学実習 8. 共焦点レーザー顕微鏡実習 2 ). 実習を担当する教育研究分野においてのみ単位認定可能な実習項目
平成 30 年度医科学専攻共通科目 共通基礎科目実習 ( 旧コア実習 ) 概要 1 ). 大学院生が所属する教育研究分野における実習により単位認定可能な実習項目 ( コア実習項目 ) 1. 組換え DNA 技術実習 2. 生体物質の調製と解析実習 3. 薬理学実習 4. ウイルス学実習 5. 免疫学実習 6. 顕微鏡試料作成法実習 7. ゲノム医学実習 8. 共焦点レーザー顕微鏡実習 2 ). 実習を担当する教育研究分野においてのみ単位認定可能な実習項目
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 <その他分野 ( 消化器官用薬 解毒剤 その他 )> 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号
 資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
緑膿菌 Pseudomonas aeruginosa グラム陰性桿菌 ブドウ糖非発酵 緑色色素産生 水まわりなど生活環境中に広く常在 腸内に常在する人も30%くらい ペニシリンやセファゾリンなどの第一世代セフェム 薬に自然耐性 テトラサイクリン系やマクロライド系抗生物質など の抗菌薬にも耐性を示す傾
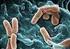 2 緑膿菌 Pseudomonas aeruginosa グラム陰性桿菌 ブドウ糖非発酵 緑色色素産生 水まわりなど生活環境中に広く常在 腸内に常在する人も30%くらい ペニシリンやセファゾリンなどの第一世代セフェム 薬に自然耐性 テトラサイクリン系やマクロライド系抗生物質など の抗菌薬にも耐性を示す傾向が強い 多剤耐性緑膿菌は5類感染症定点把握疾患 赤痢菌属 グラム陰性通性嫌気性桿菌 腸内細菌科
2 緑膿菌 Pseudomonas aeruginosa グラム陰性桿菌 ブドウ糖非発酵 緑色色素産生 水まわりなど生活環境中に広く常在 腸内に常在する人も30%くらい ペニシリンやセファゾリンなどの第一世代セフェム 薬に自然耐性 テトラサイクリン系やマクロライド系抗生物質など の抗菌薬にも耐性を示す傾向が強い 多剤耐性緑膿菌は5類感染症定点把握疾患 赤痢菌属 グラム陰性通性嫌気性桿菌 腸内細菌科
助成研究演題 - 平成 23 年度国内共同研究 (39 歳以下 ) 重症心不全の集学的治療確立のための QOL 研究 東京大学医学系研究科重症心不全治療開発講座客員研究員 ( 助成時 : 東京大学医学部附属病院循環器内科日本学術振興会特別研究員 PD) 加藤尚子 私は 重症心不全の集学的治療確立のた
 助成研究演題 - 平成 23 年度国内共同研究 (39 歳以下 ) 重症心不全の集学的治療確立のための QOL 研究 東京大学医学系研究科重症心不全治療開発講座客員研究員 ( 助成時 : 東京大学医学部附属病院循環器内科日本学術振興会特別研究員 PD) 加藤尚子 私は 重症心不全の集学的治療確立のための QOL 研究 という題目で ファイザーヘ ルスリサーチ振興財団より助成をいただきました 本日はその結果を報告したいと思います
助成研究演題 - 平成 23 年度国内共同研究 (39 歳以下 ) 重症心不全の集学的治療確立のための QOL 研究 東京大学医学系研究科重症心不全治療開発講座客員研究員 ( 助成時 : 東京大学医学部附属病院循環器内科日本学術振興会特別研究員 PD) 加藤尚子 私は 重症心不全の集学的治療確立のための QOL 研究 という題目で ファイザーヘ ルスリサーチ振興財団より助成をいただきました 本日はその結果を報告したいと思います
別添 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について < 半年ごとの定期報告の受け付け> Q1 平成 26 年 6 月 30 日までの間は 治験依頼者 ( 自ら治験を実施する者を除く ) が提出する副作用等症例の定期報告は なお従前の例によることができる とあるが 平成 26 年
 事務連絡 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局審査管理課 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 第 273 条第 3 項に基づく治験副作用等定期報告については 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について ( 平成 24 年
事務連絡 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局審査管理課 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 第 273 条第 3 項に基づく治験副作用等定期報告については 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について ( 平成 24 年
平成 29 年度食品安全モニター課題報告 食品の安全性に関する意識等について I. 食品の安全性に係る危害要因等について 問 1 A~G に掲げる事項についてリスクの観点からあなたはどう思いますか それぞれ の事項について 選択肢 1~6 の中から 1 つずつ選んでください 事項 A 環境問題 B
 平成 29 年度食品安全モニター課題報告 食品の安全性に関する意識等について I. 食品の安全性に係る危害要因等について 問 1 A~G に掲げる事項についてリスクの観点からあなたはどう思いますか それぞれ の事項について 選択肢 1~6 の中から 1 つずつ選んでください 事項 A 環境問題 B 自然災害 C 食品安全 D 重症感染症 E 犯罪 F 戦争 テロ G 交通事故 選択肢 1 とても不安を感じる
平成 29 年度食品安全モニター課題報告 食品の安全性に関する意識等について I. 食品の安全性に係る危害要因等について 問 1 A~G に掲げる事項についてリスクの観点からあなたはどう思いますか それぞれ の事項について 選択肢 1~6 の中から 1 つずつ選んでください 事項 A 環境問題 B 自然災害 C 食品安全 D 重症感染症 E 犯罪 F 戦争 テロ G 交通事故 選択肢 1 とても不安を感じる
ROCKY NOTE 食物アレルギー ( ) 症例目を追加記載 食物アレルギー関連の 2 例をもとに考察 1 例目 30 代男性 アレルギーについて調べてほしいというこ
 食物アレルギー (100909 101214) 101214 2 症例目を追加記載 食物アレルギー関連の 2 例をもとに考察 1 例目 30 代男性 アレルギーについて調べてほしいということで来院 ( 患者 ) エビやカニを食べると唇が腫れるんです 多分アレルギーだと思うんですが 検査は出来ますか? ( 私 ) 検査は出来ますが おそらく検査をするまでも無く アレルギーだと思いますよ ( 患者 )
食物アレルギー (100909 101214) 101214 2 症例目を追加記載 食物アレルギー関連の 2 例をもとに考察 1 例目 30 代男性 アレルギーについて調べてほしいということで来院 ( 患者 ) エビやカニを食べると唇が腫れるんです 多分アレルギーだと思うんですが 検査は出来ますか? ( 私 ) 検査は出来ますが おそらく検査をするまでも無く アレルギーだと思いますよ ( 患者 )
ン (LVFX) 耐性で シタフロキサシン (STFX) 耐性は1% 以下です また セフカペン (CFPN) およびセフジニル (CFDN) 耐性は 約 6% と耐性率は低い結果でした K. pneumoniae については 全ての薬剤に耐性はほとんどありませんが 腸球菌に対して 第 3 世代セフ
 2012 年 12 月 5 日放送 尿路感染症 産業医科大学泌尿器科学教授松本哲朗はじめに感染症の分野では 抗菌薬に対する耐性菌の話題が大きな問題点であり 耐性菌を増やさないための感染制御と適正な抗菌薬の使用が必要です 抗菌薬は 使用すれば必ず耐性菌が出現し 増加していきます 新規抗菌薬の開発と耐性菌の増加は 永遠に続く いたちごっこ でしょう しかし 近年 抗菌薬の開発は世界的に鈍化していますので
2012 年 12 月 5 日放送 尿路感染症 産業医科大学泌尿器科学教授松本哲朗はじめに感染症の分野では 抗菌薬に対する耐性菌の話題が大きな問題点であり 耐性菌を増やさないための感染制御と適正な抗菌薬の使用が必要です 抗菌薬は 使用すれば必ず耐性菌が出現し 増加していきます 新規抗菌薬の開発と耐性菌の増加は 永遠に続く いたちごっこ でしょう しかし 近年 抗菌薬の開発は世界的に鈍化していますので
習う ということで 教育を受ける側の 意味合いになると思います また 教育者とした場合 その構造は 義 ( 案 ) では この考え方に基づき 教える ことと学ぶことはダイナミックな相互作用 と捉えています 教育する 者 となると思います 看護学教育の定義を これに当てはめると 教授学習過程する者 と
 2015 年 11 月 24 日 看護学教育の定義 ( 案 ) に対するパブリックコメントの提出意見と回答 看護学教育制度委員会 2011 年から検討を重ねてきました 看護学教育の定義 について 今年 3 月から 5 月にかけて パブリックコメントを実施し 5 件のご意見を頂きました ご協力いただき ありがとうござい ました 看護学教育制度委員会からの回答と修正した 看護学教育の定義 をお知らせ致します
2015 年 11 月 24 日 看護学教育の定義 ( 案 ) に対するパブリックコメントの提出意見と回答 看護学教育制度委員会 2011 年から検討を重ねてきました 看護学教育の定義 について 今年 3 月から 5 月にかけて パブリックコメントを実施し 5 件のご意見を頂きました ご協力いただき ありがとうござい ました 看護学教育制度委員会からの回答と修正した 看護学教育の定義 をお知らせ致します
医療用医薬品最新品質情報集 ( ブルーブック ) 初版有効成分リトドリン塩酸塩 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 (25 ) 1) 溶解度 (37 ) 1 ウテロン錠 5mg サンド 2
 医療用医薬品最新品質情報集 ( ブルーブック ) 2018.7.13 初版有効成分リトドリン塩酸塩 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 (25 ) 1) 溶解度 (37 ) 1 ウテロン錠 5mg サンド 2 塩酸リトドリン錠 5mg YD 陽進堂 3 リトドリン錠 5mg PP ポーラファルマ 4 ルテオニン錠
医療用医薬品最新品質情報集 ( ブルーブック ) 2018.7.13 初版有効成分リトドリン塩酸塩 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 (25 ) 1) 溶解度 (37 ) 1 ウテロン錠 5mg サンド 2 塩酸リトドリン錠 5mg YD 陽進堂 3 リトドリン錠 5mg PP ポーラファルマ 4 ルテオニン錠
目 次 1. はじめに 1 2. 組成および性状 2 3. 効能 効果 2 4. 特徴 2 5. 使用方法 2 6. 即時効果 持続効果および累積効果 3 7. 抗菌スペクトル 5 サラヤ株式会社スクラビイン S4% 液製品情報 2/ PDF
 サラヤ株式会社スクラビイン S4% 液製品情報 1/8 52-0198-01-4PDF 目 次 1. はじめに 1 2. 組成および性状 2 3. 効能 効果 2 4. 特徴 2 5. 使用方法 2 6. 即時効果 持続効果および累積効果 3 7. 抗菌スペクトル 5 サラヤ株式会社スクラビイン S4% 液製品情報 2/8 52-0198-01-4PDF 1. はじめに 医療関連感染の原因となる微生物の多くは
サラヤ株式会社スクラビイン S4% 液製品情報 1/8 52-0198-01-4PDF 目 次 1. はじめに 1 2. 組成および性状 2 3. 効能 効果 2 4. 特徴 2 5. 使用方法 2 6. 即時効果 持続効果および累積効果 3 7. 抗菌スペクトル 5 サラヤ株式会社スクラビイン S4% 液製品情報 2/8 52-0198-01-4PDF 1. はじめに 医療関連感染の原因となる微生物の多くは
参考 < これまでの合同会合における検討経緯 > 1 第 1 回合同会合 ( 平成 15 年 1 月 21 日 ) 了承事項 1 平成 14 年末に都道府県及びインターネットを通じて行った調査で情報提供のあった資材のうち 食酢 重曹 及び 天敵 ( 使用される場所の周辺で採取されたもの ) の 3
 資料 3 特定防除資材 ( 特定農薬 ) 指定に係る今後の進め方について ( 案 ) < 特定農薬制度の趣旨 > 無登録農薬の販売 使用が問題を契機として 平成 14 年の臨時国会で農薬取締法が大幅に改正 農薬の製造 使用等の規制を強化 農家が自家製造して使用している防除資材等で 明らかに安全上問題のないものにまで登録の義務を課すことは過剰規制となるおそれ 原材料に照らし農作物等 人畜及び水産動植物に害を及ぼすおそれがないことが明らかなものとして農林水産大臣及び環境大臣が指定する農薬
資料 3 特定防除資材 ( 特定農薬 ) 指定に係る今後の進め方について ( 案 ) < 特定農薬制度の趣旨 > 無登録農薬の販売 使用が問題を契機として 平成 14 年の臨時国会で農薬取締法が大幅に改正 農薬の製造 使用等の規制を強化 農家が自家製造して使用している防除資材等で 明らかに安全上問題のないものにまで登録の義務を課すことは過剰規制となるおそれ 原材料に照らし農作物等 人畜及び水産動植物に害を及ぼすおそれがないことが明らかなものとして農林水産大臣及び環境大臣が指定する農薬
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠 50mg 医薬品リスク管理計画書 (RMP) の概要 有効成分 タペンタ 錠 100mg 製造販売業者 ヤンセンファーマ株式会社 薬効分類 821 提出年月 平成 30 年
 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
染症であり ついで淋菌感染症となります 病状としては外尿道口からの排膿や排尿時痛を呈する尿道炎が最も多く 病名としてはクラミジア性尿道炎 淋菌性尿道炎となります また 淋菌もクラミジアも検出されない尿道炎 ( 非クラミジア性非淋菌性尿道炎とよびます ) が その次に頻度の高い疾患ということになります
 2015 年 3 月 4 日放送 淋菌 クラミジア感染症の現状と問題点 産業医科大学泌尿器科講師濵砂良一主な性感染症淋菌感染症およびクラミジア感染症は 性感染症の一つであり 性感染症のなかで最も頻度の高い疾患です 性感染症とは 主に性的な行為によって病原体が感染する疾患であり この淋菌 クラミジア感染症の他に 梅毒 性器ヘルペス 尖圭コンジローマ HIV 感染症など数多くの疾患が含まれます これらの疾患の一部は
2015 年 3 月 4 日放送 淋菌 クラミジア感染症の現状と問題点 産業医科大学泌尿器科講師濵砂良一主な性感染症淋菌感染症およびクラミジア感染症は 性感染症の一つであり 性感染症のなかで最も頻度の高い疾患です 性感染症とは 主に性的な行為によって病原体が感染する疾患であり この淋菌 クラミジア感染症の他に 梅毒 性器ヘルペス 尖圭コンジローマ HIV 感染症など数多くの疾患が含まれます これらの疾患の一部は
審査結果 平成 25 年 9 月 27 日 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 審査結果 ] 平成 25 年 4 月 26 日開
![審査結果 平成 25 年 9 月 27 日 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 審査結果 ] 平成 25 年 4 月 26 日開 審査結果 平成 25 年 9 月 27 日 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 審査結果 ] 平成 25 年 4 月 26 日開](/thumbs/53/31072016.jpg) 審査報告書 平成 25 年 9 月 27 日独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 剤形 含量 ]
審査報告書 平成 25 年 9 月 27 日独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 剤形 含量 ]
 概要 (2006 年 1 2 3 月分 ) 本サーベイランスは 参加医療機関において血液および髄液から分離された各種細菌の検出状況や薬剤感受性パターンの動 向を把握するとともに 新たな耐性菌の早期検出等を目的とする これらのデータを経時的に解析し臨床の現場に還元することによって 抗菌薬の安全で有効な使用方法や院内感染制御における具体的かつ確実な情報を提供する 検体 2005 年 2006 年 10~12
概要 (2006 年 1 2 3 月分 ) 本サーベイランスは 参加医療機関において血液および髄液から分離された各種細菌の検出状況や薬剤感受性パターンの動 向を把握するとともに 新たな耐性菌の早期検出等を目的とする これらのデータを経時的に解析し臨床の現場に還元することによって 抗菌薬の安全で有効な使用方法や院内感染制御における具体的かつ確実な情報を提供する 検体 2005 年 2006 年 10~12
0001 ......
 ツリヌス菌などがあります 食中毒では感染原因となる微生物の検出は重要であす ①感染型食中毒 サルモネラ カンピロバクターなど 細菌に汚染された食品を口にすることで 生きた菌自 らが食中毒を引き起こすもので 腸管にたどり着いた菌が腸管内でさらに増殖し 腸管組織に 侵入し 組織を壊し 炎症を起こします このため 腹痛や下痢などの症状を引き起こし ひ どい場合には血便が起こります ②感染 生体内毒素型食中毒
ツリヌス菌などがあります 食中毒では感染原因となる微生物の検出は重要であす ①感染型食中毒 サルモネラ カンピロバクターなど 細菌に汚染された食品を口にすることで 生きた菌自 らが食中毒を引き起こすもので 腸管にたどり着いた菌が腸管内でさらに増殖し 腸管組織に 侵入し 組織を壊し 炎症を起こします このため 腹痛や下痢などの症状を引き起こし ひ どい場合には血便が起こります ②感染 生体内毒素型食中毒
平成 15 年 11 月 10 日 家畜に使用する抗菌性物質に関する意見交換会 配布 抗生物質の使用と薬剤耐性菌の発生について - 家畜用の抗生物質の見直し - 農林水産省消費 安全局 平成 15 年 11 月 10 日
 抗生物質の使用と薬剤耐性菌の発生について - 家畜用の抗生物質の見直し - 農林水産省消費 安全局 平成 15 年 11 月 10 日 消費者からの声 1. 人の薬剤耐性菌が増加し 治療を困難にしている 2. 薬剤耐性菌が増加しているのは 抗生物質を家畜に使用しているためではないか 3. 抗生物質を家畜の成長促進目的で使うのは不適切ではないか 抗生物質の利用 と耐性菌問題の解説 抗生物質とは 高等生物に対す殺菌作用などる作用消毒薬その他
抗生物質の使用と薬剤耐性菌の発生について - 家畜用の抗生物質の見直し - 農林水産省消費 安全局 平成 15 年 11 月 10 日 消費者からの声 1. 人の薬剤耐性菌が増加し 治療を困難にしている 2. 薬剤耐性菌が増加しているのは 抗生物質を家畜に使用しているためではないか 3. 抗生物質を家畜の成長促進目的で使うのは不適切ではないか 抗生物質の利用 と耐性菌問題の解説 抗生物質とは 高等生物に対す殺菌作用などる作用消毒薬その他
審査報告 (1) 別紙 平成 29 年 4 月 3 日 本申請において 申請者が提出した資料及び医薬品医療機器総合機構における審査の概略等は 以下 のとおりである 申請品目 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノ
![審査報告 (1) 別紙 平成 29 年 4 月 3 日 本申請において 申請者が提出した資料及び医薬品医療機器総合機構における審査の概略等は 以下 のとおりである 申請品目 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノ 審査報告 (1) 別紙 平成 29 年 4 月 3 日 本申請において 申請者が提出した資料及び医薬品医療機器総合機構における審査の概略等は 以下 のとおりである 申請品目 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノ](/thumbs/92/110667825.jpg) 審査報告書 平成 29 年 5 月 17 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノバルティスファーマ株式会社 [ 申請年月日 ] 平成 28 年 7 月 28 日 [ 剤形 含量
審査報告書 平成 29 年 5 月 17 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノバルティスファーマ株式会社 [ 申請年月日 ] 平成 28 年 7 月 28 日 [ 剤形 含量
ともに 申請者が承認審査のスケジュールに沿って法令上求められる製造体制を整備することや承認後円滑に医療現場に提供するための対応が十分になされることで 更なる迅速な実用化を促すものである この制度では 原則として新規原理 新規作用機序等により 生命に重大な影響がある重篤な疾患等に対して 極めて高い有効
 ともに 申請者が承認審査のスケジュールに沿って法令上求められる製造体制を整備することや承認後円滑に医療現場に提供するための対応が十分になされることで 更なる迅速な実用化を促すものである この制度では 原則として新規原理 新規作用機序等により 生命に重大な影響がある重篤な疾患等に対して 極めて高い有効性が期待される医療機器 体外診断用医薬品 再生医療等製品を指定することとする また 本制度では PMDA
ともに 申請者が承認審査のスケジュールに沿って法令上求められる製造体制を整備することや承認後円滑に医療現場に提供するための対応が十分になされることで 更なる迅速な実用化を促すものである この制度では 原則として新規原理 新規作用機序等により 生命に重大な影響がある重篤な疾患等に対して 極めて高い有効性が期待される医療機器 体外診断用医薬品 再生医療等製品を指定することとする また 本制度では PMDA
Microsoft Word - 日薬連宛抗インフル薬通知(写).doc
 薬生安発 0821 第 1 号 平成 3 0 年 8 月 2 1 日 日本製薬団体連合会 安全性委員会委員長 殿 厚生労働省医薬 生活衛生局医薬安全対策課長 抗インフルエンザウイルス薬の 使用上の注意 の改訂について 平成 30 年度第 1 回薬事 食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会 ( 平成 30 年 5 月 16 日開催 ) 及び平成 30 年度第 4 回薬事 食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会
薬生安発 0821 第 1 号 平成 3 0 年 8 月 2 1 日 日本製薬団体連合会 安全性委員会委員長 殿 厚生労働省医薬 生活衛生局医薬安全対策課長 抗インフルエンザウイルス薬の 使用上の注意 の改訂について 平成 30 年度第 1 回薬事 食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会 ( 平成 30 年 5 月 16 日開催 ) 及び平成 30 年度第 4 回薬事 食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会
糖尿病診療における早期からの厳格な血糖コントロールの重要性
 2019 年 2 月 13 日放送 ESBL 産生菌と尿路感染症の治療戦略 岡山大学病院泌尿器科講師和田耕一郎はじめに私が頂きましたテーマは ESBL 産生菌と尿路感染症の治療戦略 です これから ESBL 産生菌の分離状況や薬剤感受性 さらに岡山大学病院泌尿器科における抗菌薬の使用例について紹介したいと思います 尿路感染症を取り巻く状況まず 尿路感染症を取り巻く状況について説明します 近年 各種抗菌薬に耐性を示す細菌の増加が国内外で大きな問題となっていることに加えて
2019 年 2 月 13 日放送 ESBL 産生菌と尿路感染症の治療戦略 岡山大学病院泌尿器科講師和田耕一郎はじめに私が頂きましたテーマは ESBL 産生菌と尿路感染症の治療戦略 です これから ESBL 産生菌の分離状況や薬剤感受性 さらに岡山大学病院泌尿器科における抗菌薬の使用例について紹介したいと思います 尿路感染症を取り巻く状況まず 尿路感染症を取り巻く状況について説明します 近年 各種抗菌薬に耐性を示す細菌の増加が国内外で大きな問題となっていることに加えて
がんの診療の流れ この図は がんの 受診 から 経過観察 への流れです 大まかでも 流れがみえると心にゆとりが生まれます ゆとりは 医師とのコミュニケーションを後押ししてくれるでしょう あなたらしく過ごすためにお役立てください がんの疑い 体調がおかしいな と思ったまま 放っておかないでください な
 各種がん 101 がんの診療の流れ この図は がんの 受診 から 経過観察 への流れです 大まかでも 流れがみえると心にゆとりが生まれます ゆとりは 医師とのコミュニケーションを後押ししてくれるでしょう あなたらしく過ごすためにお役立てください がんの疑い 体調がおかしいな と思ったまま 放っておかないでください なるべく早く受診しましょう 受診 受診のきっかけや 気になっていること 症状など 何でも担当医に伝えてください
各種がん 101 がんの診療の流れ この図は がんの 受診 から 経過観察 への流れです 大まかでも 流れがみえると心にゆとりが生まれます ゆとりは 医師とのコミュニケーションを後押ししてくれるでしょう あなたらしく過ごすためにお役立てください がんの疑い 体調がおかしいな と思ったまま 放っておかないでください なるべく早く受診しましょう 受診 受診のきっかけや 気になっていること 症状など 何でも担当医に伝えてください
2012 年 1 月 25 日放送 歯性感染症における経口抗菌薬療法 東海大学外科学系口腔外科教授金子明寛 今回は歯性感染症における経口抗菌薬療法と題し歯性感染症からの分離菌および薬 剤感受性を元に歯性感染症の第一選択薬についてお話し致します 抗菌化学療法のポイント歯性感染症原因菌は嫌気性菌および好
 2012 年 1 月 25 日放送 歯性感染症における経口抗菌薬療法 東海大学外科学系口腔外科教授金子明寛 今回は歯性感染症における経口抗菌薬療法と題し歯性感染症からの分離菌および薬 剤感受性を元に歯性感染症の第一選択薬についてお話し致します 抗菌化学療法のポイント歯性感染症原因菌は嫌気性菌および好気性菌の複数菌感染症です 嫌気性菌の占める割合が 高くおよそ 2:1 の頻度で検出されます 嫌気性菌では
2012 年 1 月 25 日放送 歯性感染症における経口抗菌薬療法 東海大学外科学系口腔外科教授金子明寛 今回は歯性感染症における経口抗菌薬療法と題し歯性感染症からの分離菌および薬 剤感受性を元に歯性感染症の第一選択薬についてお話し致します 抗菌化学療法のポイント歯性感染症原因菌は嫌気性菌および好気性菌の複数菌感染症です 嫌気性菌の占める割合が 高くおよそ 2:1 の頻度で検出されます 嫌気性菌では
ジェネリック医薬品とは 内容 ジェネリック医薬品は 新薬 ( 先発医薬品 ) の特許期間を満了した 同じ有効成分を使った 品質 効き目 安全性が同等で 低価格な おくすりです とっきょきかん 1. ジェネリック医薬品とは 2. どうして低価格なの? 医療用医薬品 新薬 3. 効き目も安全性も同等 4
 ジェネリック医薬品ガイドブック不安をなくして かしこく使おう! GE 薬協 どうして安いの? 安いけど 効くの? 品質は? 添加剤がちがっても大丈夫なの? どれくらいやすくなるの? かんたん差額計算 をご利用ください 2016 年 11 月発行 ジェネリック医薬品とは 内容 ジェネリック医薬品は 新薬 ( 先発医薬品 ) の特許期間を満了した 同じ有効成分を使った 品質 効き目 安全性が同等で 低価格な
ジェネリック医薬品ガイドブック不安をなくして かしこく使おう! GE 薬協 どうして安いの? 安いけど 効くの? 品質は? 添加剤がちがっても大丈夫なの? どれくらいやすくなるの? かんたん差額計算 をご利用ください 2016 年 11 月発行 ジェネリック医薬品とは 内容 ジェネリック医薬品は 新薬 ( 先発医薬品 ) の特許期間を満了した 同じ有効成分を使った 品質 効き目 安全性が同等で 低価格な
豚繁殖 呼吸障害症候群生ワクチン ( シード ) 平成 24 年 3 月 13 日 ( 告示第 675 号 ) 新規追加 1 定義シードロット規格に適合した弱毒豚繁殖 呼吸障害症候群ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を凍結乾燥したワクチンである 2 製法 2.1 製造用株
 豚繁殖 呼吸障害症候群生ワクチン ( シード ) 平成 24 年 3 月 13 日 ( 告示第 675 号 ) 新規追加 1 定義シードロット規格に適合した弱毒豚繁殖 呼吸障害症候群ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を凍結乾燥したワクチンである 2 製法 2.1 製造用株 2.1.1 名称豚繁殖 呼吸障害症候群ウイルス JJ1882 株又はこれと同等と認められた株 2.1.2
豚繁殖 呼吸障害症候群生ワクチン ( シード ) 平成 24 年 3 月 13 日 ( 告示第 675 号 ) 新規追加 1 定義シードロット規格に適合した弱毒豚繁殖 呼吸障害症候群ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を凍結乾燥したワクチンである 2 製法 2.1 製造用株 2.1.1 名称豚繁殖 呼吸障害症候群ウイルス JJ1882 株又はこれと同等と認められた株 2.1.2
資料 2-4 イソプロピルアンチピリン製剤の安全対策について 平成 23 年 6 月 23 日平成 23 年度薬事 食品衛生審議会医薬品等安全対策部会安全対策調査会 ( 第 2 回 ) 1. イソプロピルアンチピリン製剤の安全性に係る調査結果報告書 ( 別紙 ) 1 ページ
 資料 2-4 イソプロピルアンチピリン製剤の安全対策について 平成 23 年 6 月 23 日平成 23 年度薬事 食品衛生審議会医薬品等安全対策部会安全対策調査会 ( 第 2 回 ) 1. イソプロピルアンチピリン製剤の安全性に係る調査結果報告書 ( 別紙 ) 1 ページ 別紙 調査結果報告書 平成 23 年 6 月 13 日 独立行政法人医薬品医療機器総合機構 I. 品目の概要 [ 販売名 ]
資料 2-4 イソプロピルアンチピリン製剤の安全対策について 平成 23 年 6 月 23 日平成 23 年度薬事 食品衛生審議会医薬品等安全対策部会安全対策調査会 ( 第 2 回 ) 1. イソプロピルアンチピリン製剤の安全性に係る調査結果報告書 ( 別紙 ) 1 ページ 別紙 調査結果報告書 平成 23 年 6 月 13 日 独立行政法人医薬品医療機器総合機構 I. 品目の概要 [ 販売名 ]
CW3_AZ259A01.indd
 薬 に関する セルフチェック確認チャレンジ!! 医薬品の正しい使い方 医薬品と健康 についての学習はいかがでしたか 学習後に 再度 薬 に 関するセルフチェック の確認のためにチャレンジしてみてください なお の数字は冊子の各章に対応しています 病院などで出される 薬 は ① といい 医師 歯科医師による ② ラッグストア 等でも買える 薬 は ③ といい ② が必要です 一方 薬店 ド は不要ですが
薬 に関する セルフチェック確認チャレンジ!! 医薬品の正しい使い方 医薬品と健康 についての学習はいかがでしたか 学習後に 再度 薬 に 関するセルフチェック の確認のためにチャレンジしてみてください なお の数字は冊子の各章に対応しています 病院などで出される 薬 は ① といい 医師 歯科医師による ② ラッグストア 等でも買える 薬 は ③ といい ② が必要です 一方 薬店 ド は不要ですが
第 88 回日本感染症学会学術講演会第 62 回日本化学療法学会総会合同学会採択演題一覧 ( 一般演題ポスター ) 登録番号 発表形式 セッション名 日にち 時間 部屋名 NO. 発表順 一般演題 ( ポスター ) 尿路 骨盤 性器感染症 1 6 月 18 日 14:10-14:50 ア
 登録番号 発表形式 セッション名 日にち 時間 部屋名 NO. 発表順 10431 一般演題 ( ポスター ) 尿路 骨盤 性器感染症 1 6 月 18 日 14:10-14:50 アルゴスC-D P-01 1 10473 一般演題 ( ポスター ) 尿路 骨盤 性器感染症 1 6 月 18 日 14:10-14:50 アルゴスC-D P-01 2 10347 一般演題 ( ポスター ) 尿路 骨盤
登録番号 発表形式 セッション名 日にち 時間 部屋名 NO. 発表順 10431 一般演題 ( ポスター ) 尿路 骨盤 性器感染症 1 6 月 18 日 14:10-14:50 アルゴスC-D P-01 1 10473 一般演題 ( ポスター ) 尿路 骨盤 性器感染症 1 6 月 18 日 14:10-14:50 アルゴスC-D P-01 2 10347 一般演題 ( ポスター ) 尿路 骨盤
肝臓の細胞が壊れるる感染があります 肝B 型慢性肝疾患とは? B 型慢性肝疾患は B 型肝炎ウイルスの感染が原因で起こる肝臓の病気です B 型肝炎ウイルスに感染すると ウイルスは肝臓の細胞で増殖します 増殖したウイルスを排除しようと体の免疫機能が働きますが ウイルスだけを狙うことができず 感染した肝
 エンテカビル トーワ を服用されている方へ B 型慢性肝疾患の治療のために 監修 国立大学法人高知大学医学部消化器内科学講座 教授西原利治先生 施設名 2017 年 10 月作成 (C-1) 肝臓の細胞が壊れるる感染があります 肝B 型慢性肝疾患とは? B 型慢性肝疾患は B 型肝炎ウイルスの感染が原因で起こる肝臓の病気です B 型肝炎ウイルスに感染すると ウイルスは肝臓の細胞で増殖します 増殖したウイルスを排除しようと体の免疫機能が働きますが
エンテカビル トーワ を服用されている方へ B 型慢性肝疾患の治療のために 監修 国立大学法人高知大学医学部消化器内科学講座 教授西原利治先生 施設名 2017 年 10 月作成 (C-1) 肝臓の細胞が壊れるる感染があります 肝B 型慢性肝疾患とは? B 型慢性肝疾患は B 型肝炎ウイルスの感染が原因で起こる肝臓の病気です B 型肝炎ウイルスに感染すると ウイルスは肝臓の細胞で増殖します 増殖したウイルスを排除しようと体の免疫機能が働きますが
このドッグランは、人と愛犬との豊かな共生を願って作られました
 目次 Q 1 利用登録制度とは? Q 2 利用登録に必要なものは? Q 3 鑑札と狂犬病予防注射済票を見ないと登録できないの? Q 4 鑑札を紛失した場合は? Q 5 狂犬病予防注射を受ける時期は決まっているの? Q 6 狂犬病予防注射を4 月から6 月に受けない場合 ドッグラン登録は? Q 7 狂犬病予防注射は1 年に一度打てばいいと聞いたけど? Q 8 動物病院等で狂犬病予防注射を受けた場合 Q
目次 Q 1 利用登録制度とは? Q 2 利用登録に必要なものは? Q 3 鑑札と狂犬病予防注射済票を見ないと登録できないの? Q 4 鑑札を紛失した場合は? Q 5 狂犬病予防注射を受ける時期は決まっているの? Q 6 狂犬病予防注射を4 月から6 月に受けない場合 ドッグラン登録は? Q 7 狂犬病予防注射は1 年に一度打てばいいと聞いたけど? Q 8 動物病院等で狂犬病予防注射を受けた場合 Q
切片 ( 定数項 ) ダミー 以下の単回帰モデルを考えよう これは賃金と就業年数の関係を分析している : ( 賃金関数 ) ここで Y i = α + β X i + u i, i =1,, n, u i ~ i.i.d. N(0, σ 2 ) Y i : 賃金の対数値, X i : 就業年数. (
 統計学ダミー変数による分析 担当 : 長倉大輔 ( ながくらだいすけ ) 1 切片 ( 定数項 ) ダミー 以下の単回帰モデルを考えよう これは賃金と就業年数の関係を分析している : ( 賃金関数 ) ここで Y i = α + β X i + u i, i =1,, n, u i ~ i.i.d. N(0, σ 2 ) Y i : 賃金の対数値, X i : 就業年数. ( 実際は賃金を就業年数だけで説明するのは現実的はない
統計学ダミー変数による分析 担当 : 長倉大輔 ( ながくらだいすけ ) 1 切片 ( 定数項 ) ダミー 以下の単回帰モデルを考えよう これは賃金と就業年数の関係を分析している : ( 賃金関数 ) ここで Y i = α + β X i + u i, i =1,, n, u i ~ i.i.d. N(0, σ 2 ) Y i : 賃金の対数値, X i : 就業年数. ( 実際は賃金を就業年数だけで説明するのは現実的はない
より詳細な情報を望まれる場合は 担当の医師または薬剤師におたずねください また 患者向医薬品ガイド 医療専門家向けの 添付文書情報 が医薬品医療機器総合機構のホームページに掲載されています
 くすりのしおり内服剤 2014 年 6 月作成薬には効果 ( ベネフィット ) だけでなく副作用 ( リスク ) があります 副作用をなるべく抑え 効果を最大限に引き出すことが大切です そのために この薬を使用される患者さんの理解と協力が必要です 商品名 : バルサルタン錠 20mg AA 主成分 : バルサルタン (Valsartan) 剤形 : 淡黄色の錠剤 直径約 7.2mm 厚さ約 3.1mm
くすりのしおり内服剤 2014 年 6 月作成薬には効果 ( ベネフィット ) だけでなく副作用 ( リスク ) があります 副作用をなるべく抑え 効果を最大限に引き出すことが大切です そのために この薬を使用される患者さんの理解と協力が必要です 商品名 : バルサルタン錠 20mg AA 主成分 : バルサルタン (Valsartan) 剤形 : 淡黄色の錠剤 直径約 7.2mm 厚さ約 3.1mm
3. 安全性本治験において治験薬が投与された 48 例中 1 例 (14 件 ) に有害事象が認められた いずれの有害事象も治験薬との関連性は あり と判定されたが いずれも軽度 で処置の必要はなく 追跡検査で回復を確認した また 死亡 その他の重篤な有害事象が認められなか ったことから 安全性に問
 フェキソフェナジン塩酸塩錠 6mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにフェキソフェナジン塩酸塩は 第二世代抗ヒスタミン薬の一つであり 抗原抗体反応に伴って起こる肥満細胞からのヒスタミンなどのケミカルメディエーターの遊離を抑制すると共に ヒスタミンの H1 作用に拮抗することにより アレルギー症状を緩和する 今回 フェキソフェナジン塩酸塩錠 6mg
フェキソフェナジン塩酸塩錠 6mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにフェキソフェナジン塩酸塩は 第二世代抗ヒスタミン薬の一つであり 抗原抗体反応に伴って起こる肥満細胞からのヒスタミンなどのケミカルメディエーターの遊離を抑制すると共に ヒスタミンの H1 作用に拮抗することにより アレルギー症状を緩和する 今回 フェキソフェナジン塩酸塩錠 6mg
岐阜市における「医薬品の正しい使い方」に関する調査アンケート結果
 岐阜市における 医薬品の正しい使い方 に関する調査アンケート結果 岐阜薬科大学実践薬学大講座病院薬学研究室寺町ひとみ ( 学長勝野眞吾 ) 平成 20 年 3 月改訂の新学習指導要領では 医薬品に関する内容が中学校保健体育科保健分野に盛り込まれました このような状況の中で 平成 24 年度 医薬品に関する教育 の導入に向け 現在の日本の医薬品に関する知識 態度 行動を明らかにするため 岐阜市の児童生徒の
岐阜市における 医薬品の正しい使い方 に関する調査アンケート結果 岐阜薬科大学実践薬学大講座病院薬学研究室寺町ひとみ ( 学長勝野眞吾 ) 平成 20 年 3 月改訂の新学習指導要領では 医薬品に関する内容が中学校保健体育科保健分野に盛り込まれました このような状況の中で 平成 24 年度 医薬品に関する教育 の導入に向け 現在の日本の医薬品に関する知識 態度 行動を明らかにするため 岐阜市の児童生徒の
医薬品タンパク質は 安全性の面からヒト型が常識です ではなぜ 肌につける化粧品用コラーゲンは ヒト型でなくても良いのでしょうか? アレルギーは皮膚から 最近の学説では 皮膚から侵入したアレルゲンが 食物アレルギー アトピー性皮膚炎 喘息 アレルギー性鼻炎などのアレルギー症状を引き起こすきっかけになる
 化粧品用コラーゲンの原料 現在は 魚由来が中心 かつては ウシの皮膚由来がほとんど BSE 等病原体混入の危険 人に感染する病原体をもたない アレルギーの問題は未解決 ( むしろ問題は大きくなったかもしれない ) アレルギーを引き起こす可能性 医薬品タンパク質は 安全性の面からヒト型が常識です ではなぜ 肌につける化粧品用コラーゲンは ヒト型でなくても良いのでしょうか? アレルギーは皮膚から 最近の学説では
化粧品用コラーゲンの原料 現在は 魚由来が中心 かつては ウシの皮膚由来がほとんど BSE 等病原体混入の危険 人に感染する病原体をもたない アレルギーの問題は未解決 ( むしろ問題は大きくなったかもしれない ) アレルギーを引き起こす可能性 医薬品タンパク質は 安全性の面からヒト型が常識です ではなぜ 肌につける化粧品用コラーゲンは ヒト型でなくても良いのでしょうか? アレルギーは皮膚から 最近の学説では
家畜における薬剤耐性菌の制御 薬剤耐性菌の実態把握 対象菌種 食中毒菌 耐性菌の特徴 出現の予防 79
 項目 薬剤耐性 (AMR) 対策アクションプランについて 耐性菌の基礎知識 薬剤耐性モニタリング (JVARM) の成績 コリスチン耐性について 薬剤耐性菌のリスク分析 動物用医薬品の慎重使用について 78 家畜における薬剤耐性菌の制御 薬剤耐性菌の実態把握 対象菌種 食中毒菌 耐性菌の特徴 出現の予防 79 薬剤耐性菌の広まり 選 択 圧 抗 菌 剤 使 用 によ る 薬剤耐性菌 ( 遺伝子 )
項目 薬剤耐性 (AMR) 対策アクションプランについて 耐性菌の基礎知識 薬剤耐性モニタリング (JVARM) の成績 コリスチン耐性について 薬剤耐性菌のリスク分析 動物用医薬品の慎重使用について 78 家畜における薬剤耐性菌の制御 薬剤耐性菌の実態把握 対象菌種 食中毒菌 耐性菌の特徴 出現の予防 79 薬剤耐性菌の広まり 選 択 圧 抗 菌 剤 使 用 によ る 薬剤耐性菌 ( 遺伝子 )
モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム 製造販売業者 EA ファーマ株式会社 薬効分類 提出年月 平成 30 年 10 月 1.1. 安全
 モビコール配合内用剤 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はEAファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません EA ファーマ株式会社 モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム
モビコール配合内用剤 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はEAファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません EA ファーマ株式会社 モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム
< F2D C D838A8BDB92CA926D2E6A7464>
 保医発 0221 第 31 号平成 25 年 2 月 21 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 ヘリコバクター ピロリ感染の診断及び治療に関する取扱いについて の一部改正について 今般 ヘリコバクター ピロリ感染の診断及び治療に使用する医薬品の効能
保医発 0221 第 31 号平成 25 年 2 月 21 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 ヘリコバクター ピロリ感染の診断及び治療に関する取扱いについて の一部改正について 今般 ヘリコバクター ピロリ感染の診断及び治療に使用する医薬品の効能
薬食発第 号平成 21 年 3 月 4 日 各都道府県知事殿 厚生労働省医薬食品局長 バイオ後続品の承認申請について 医薬品の製造販売の承認申請の取扱いについては 平成 17 年 3 月 31 日付け薬食発第 号医薬食品局長通知 医薬品の承認申請について ( 以下 局
 薬食発第 0304004 号平成 21 年 3 月 4 日 各都道府県知事殿 厚生労働省医薬食品局長 バイオ後続品の承認申請について 医薬品の製造販売の承認申請の取扱いについては 平成 17 年 3 月 31 日付け薬食発第 0331015 号医薬食品局長通知 医薬品の承認申請について ( 以下 局長通知 という ) により取り扱ってきたところであるが 今般 バイオ後続品の承認申請書に添付すべき資料の範囲に関して
薬食発第 0304004 号平成 21 年 3 月 4 日 各都道府県知事殿 厚生労働省医薬食品局長 バイオ後続品の承認申請について 医薬品の製造販売の承認申請の取扱いについては 平成 17 年 3 月 31 日付け薬食発第 0331015 号医薬食品局長通知 医薬品の承認申請について ( 以下 局長通知 という ) により取り扱ってきたところであるが 今般 バイオ後続品の承認申請書に添付すべき資料の範囲に関して
Microsoft Word - JAID_JSC 2014 正誤表_ 原稿
 JAID/JSC 感染症治療ガイド 2014 表 記載にりがありましたので, 下記のように追加 訂させていただきます 2016 年 9 月 JAID/JSC 感染症治療ガイド ガイドライン作成委員会 P106 Ⅶ 呼吸器感染症,A-2 院内肺炎 3 Definitive Therapy P. aeruginosa 多剤耐性の場合 CL:5mg/kg 1 回ローディング その 24 時間後に以下の維持用量を開始する
JAID/JSC 感染症治療ガイド 2014 表 記載にりがありましたので, 下記のように追加 訂させていただきます 2016 年 9 月 JAID/JSC 感染症治療ガイド ガイドライン作成委員会 P106 Ⅶ 呼吸器感染症,A-2 院内肺炎 3 Definitive Therapy P. aeruginosa 多剤耐性の場合 CL:5mg/kg 1 回ローディング その 24 時間後に以下の維持用量を開始する
医療用医薬品最新品質情報集 ( ブルーブック ) 初版有効成分クリンダマイシンリン酸エステル 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 1) 溶解度 原薬の安定水 性 1) 液性 (ph) 1
 医療用医薬品最新品質情報集 ( ブルーブック ) 2018.7.13 初版有効成分クリンダマイシンリン酸エステル 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 1) 溶解度 原薬の安定水 性 1) 液性 (ph) 1 クリンダマイシン注射液 300mg タイヨー 武田テバファーマ 2 クリンダマイシンリン酸エステル注射液
医療用医薬品最新品質情報集 ( ブルーブック ) 2018.7.13 初版有効成分クリンダマイシンリン酸エステル 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 1) 溶解度 原薬の安定水 性 1) 液性 (ph) 1 クリンダマイシン注射液 300mg タイヨー 武田テバファーマ 2 クリンダマイシンリン酸エステル注射液
ータについては Table 3 に示した 両製剤とも投与後血漿中ロスバスタチン濃度が上昇し 試験製剤で 4.7±.7 時間 標準製剤で 4.6±1. 時間に Tmaxに達した また Cmaxは試験製剤で 6.3±3.13 標準製剤で 6.8±2.49 であった AUCt は試験製剤で 62.24±2
 ロスバスタチン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロスバスタチンは HMG-CoA 還元酵素を競合的に阻害することにより HMG-CoA のメバロン酸への変更を減少させ コレステロール生合成における早期の律速段階を抑制する高コレステロール血症治療剤である 今回 ロスバスタチン錠 mg TCK とクレストール 錠 mg の生物学的同等性を検討するため
ロスバスタチン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロスバスタチンは HMG-CoA 還元酵素を競合的に阻害することにより HMG-CoA のメバロン酸への変更を減少させ コレステロール生合成における早期の律速段階を抑制する高コレステロール血症治療剤である 今回 ロスバスタチン錠 mg TCK とクレストール 錠 mg の生物学的同等性を検討するため
課題研究の進め方 これは,10 年経験者研修講座の各教科の課題研究の研修で使っている資料をまとめたものです 課題研究の進め方 と 課題研究報告書の書き方 について, 教科を限定せずに一般的に紹介してありますので, 校内研修などにご活用ください
 課題研究の進め方 これは,10 年経験者研修講座の各教科の課題研究の研修で使っている資料をまとめたものです 課題研究の進め方 と 課題研究報告書の書き方 について, 教科を限定せずに一般的に紹介してありますので, 校内研修などにご活用ください 課題研究の進め方 Ⅰ 課題研究の進め方 1 課題研究 のねらい日頃の教育実践を通して研究すべき課題を設定し, その究明を図ることにより, 教員としての資質の向上を図る
課題研究の進め方 これは,10 年経験者研修講座の各教科の課題研究の研修で使っている資料をまとめたものです 課題研究の進め方 と 課題研究報告書の書き方 について, 教科を限定せずに一般的に紹介してありますので, 校内研修などにご活用ください 課題研究の進め方 Ⅰ 課題研究の進め方 1 課題研究 のねらい日頃の教育実践を通して研究すべき課題を設定し, その究明を図ることにより, 教員としての資質の向上を図る
 概要 (2004 年分 ) 本サーベイランスは 参加医療機関において血液および髄液から分離された各種細菌の検出状況や薬剤感受性パターンの動向を把握するとともに 新たな耐性菌の早期検出等を目的とする これらのデータを経時的に解析し臨床の現場に還元することによって 抗菌薬の安全で有効な使用方法や院内感染制御における具体的かつ確実な情報を提供する 検体 ( ) 内は施設数 2002 年 2003 年 2004
概要 (2004 年分 ) 本サーベイランスは 参加医療機関において血液および髄液から分離された各種細菌の検出状況や薬剤感受性パターンの動向を把握するとともに 新たな耐性菌の早期検出等を目的とする これらのデータを経時的に解析し臨床の現場に還元することによって 抗菌薬の安全で有効な使用方法や院内感染制御における具体的かつ確実な情報を提供する 検体 ( ) 内は施設数 2002 年 2003 年 2004
Ⅰ. 改訂内容 ( 部変更 ) ペルサンチン 錠 12.5 改 訂 後 改 訂 前 (1) 本剤投与中の患者に本薬の注射剤を追加投与した場合, 本剤の作用が増強され, 副作用が発現するおそれがあるので, 併用しないこと ( 過量投与 の項参照) 本剤投与中の患者に本薬の注射剤を追加投与した場合, 本
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意 改訂のお知らせ 2006 年 1 月日本ベーリンガーインゲルハイム株式会社 注 ) 処方せん医薬品 ( ジピリダモール製剤 ) = 登録商標注 ) 注意 - 医師等の処方せんにより使用すること 謹啓時下ますますご清祥のこととお慶び申し上げます 平素は弊社製品につきましてご愛顧を賜り厚く御礼申し上げます さて, この度, 自主改訂によりペルサンチン
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意 改訂のお知らせ 2006 年 1 月日本ベーリンガーインゲルハイム株式会社 注 ) 処方せん医薬品 ( ジピリダモール製剤 ) = 登録商標注 ) 注意 - 医師等の処方せんにより使用すること 謹啓時下ますますご清祥のこととお慶び申し上げます 平素は弊社製品につきましてご愛顧を賜り厚く御礼申し上げます さて, この度, 自主改訂によりペルサンチン
スライド 1
 薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
薬事法等の一部改正に伴う特許法施行令改正に係る事前評価書
 薬事法等の一部改正に伴う特許法施行令改正に係る事前評価書 1. 政策の名称 薬事法改正に伴い新たに定義される再生医療等製品に係る製造販売の承認を特許権 の存続期間の延長登録の理由となる処分に追加するべく措置を講じる政策 2. 担当部局 経済産業省特許庁審査第一部調整課審査基準室長滝口尚良 電話番号 : 03-3501-0046 e-mail: PA2A10@jpo.go.jp 3. 評価実施時期 平成
薬事法等の一部改正に伴う特許法施行令改正に係る事前評価書 1. 政策の名称 薬事法改正に伴い新たに定義される再生医療等製品に係る製造販売の承認を特許権 の存続期間の延長登録の理由となる処分に追加するべく措置を講じる政策 2. 担当部局 経済産業省特許庁審査第一部調整課審査基準室長滝口尚良 電話番号 : 03-3501-0046 e-mail: PA2A10@jpo.go.jp 3. 評価実施時期 平成
<4D F736F F D208D B B835896F2938A975E82CC8D6C82A695FB2E646F63>
 事務連絡平成 21 年 5 月 28 日 都道府県 各 保健所設置市 衛生主管部 ( 局 ) 特別区 感染症対策担当者及び新型インフルエンザ対策担当者殿 厚生労働省新型インフルエンザ対策推進本部事務局 新型インフルエンザの診療等に関する情報 ( 抗インフルエンザ薬の予防投与の考え方等 ) に係る Q&A の送付について 平成 21 年 5 月 3 日付新型インフルエンザ対策推進本部事務連絡 新型インフルエンザの診療等に関する情報
事務連絡平成 21 年 5 月 28 日 都道府県 各 保健所設置市 衛生主管部 ( 局 ) 特別区 感染症対策担当者及び新型インフルエンザ対策担当者殿 厚生労働省新型インフルエンザ対策推進本部事務局 新型インフルエンザの診療等に関する情報 ( 抗インフルエンザ薬の予防投与の考え方等 ) に係る Q&A の送付について 平成 21 年 5 月 3 日付新型インフルエンザ対策推進本部事務連絡 新型インフルエンザの診療等に関する情報
株化細胞 + 生ウイルスワクチン 特定の株名及びロット番号を記載 株変更は新規 また 6 製造方法ロットの更新は 事項変更 6.1 製造用株 名称弱毒 ウイルス 株 ( マスターシードウイルスロット〇 ) 株名 本数 継代方法等は GMP 省令第 7 条の 3 に基づく記録に関する文 書
 動物用生物学的製剤の製造方法欄のモックアップ ( シードロット製剤 ) はじめに : 本モックアップの原案は 平成 28 年度に実施された動物用医薬品の承認申請資料作成のためのガイドライン作成事業 生物学的製剤の製造方法欄のモックアップ ( シードロット製剤 ) において 動物用生物学的製剤の製造販売業者等の専門家からなるモックアップ作成検討委員会により作成された 本モックアップは モックアップ原案に必要な記載整備を行ったものである
動物用生物学的製剤の製造方法欄のモックアップ ( シードロット製剤 ) はじめに : 本モックアップの原案は 平成 28 年度に実施された動物用医薬品の承認申請資料作成のためのガイドライン作成事業 生物学的製剤の製造方法欄のモックアップ ( シードロット製剤 ) において 動物用生物学的製剤の製造販売業者等の専門家からなるモックアップ作成検討委員会により作成された 本モックアップは モックアップ原案に必要な記載整備を行ったものである
葉酸とビタミンQ&A_201607改訂_ indd
 L FO AT E VI TAMI NB12 医療関係者用 葉酸 とビタミンB ビタミンB12 アリムタ投与に際して 警告 1 本剤を含むがん化学療法に際しては 緊急時に十分対応できる医療施設において がん化学療 法に十分な知識 経験を持つ医師のもとで 本剤の投与が適切と判断される症例についてのみ投 与すること 適応患者の選択にあたっては 各併用薬剤の添付文書を参照して十分注意すること また 治療開始に先立ち
L FO AT E VI TAMI NB12 医療関係者用 葉酸 とビタミンB ビタミンB12 アリムタ投与に際して 警告 1 本剤を含むがん化学療法に際しては 緊急時に十分対応できる医療施設において がん化学療 法に十分な知識 経験を持つ医師のもとで 本剤の投与が適切と判断される症例についてのみ投 与すること 適応患者の選択にあたっては 各併用薬剤の添付文書を参照して十分注意すること また 治療開始に先立ち
第51回日本小児感染症学会総会・学術集会 採択結果演題一覧
 登録番号 演題番号 日にち 時間 会場 発表形式 セッション名 10000 D-1-19 10 月 26 日 14:10 ~ 15:10 D 会場 一般演題 ( 口演 ) インフルエンザ2 10001 D-2-5 10 月 27 日 8:40 ~ 9:30 D 会場 一般演題 ( 口演 ) 予防接種 ワクチン1 10002 G-2-14 10 月 27 日 14:20 ~ 15:10 G 会場 一般演題
登録番号 演題番号 日にち 時間 会場 発表形式 セッション名 10000 D-1-19 10 月 26 日 14:10 ~ 15:10 D 会場 一般演題 ( 口演 ) インフルエンザ2 10001 D-2-5 10 月 27 日 8:40 ~ 9:30 D 会場 一般演題 ( 口演 ) 予防接種 ワクチン1 10002 G-2-14 10 月 27 日 14:20 ~ 15:10 G 会場 一般演題
Research 2 Vol.81, No.12013
 2 5 22 25 4 8 8 9 9 9 10 10 11 12 14 14 15 7 18 16 18 19 20 21 16 17 17 28 19 21 1 Research 2 Vol.81, No.12013 Vol.81, No.12013 3 P r o d u c t s 4 Vol.81, No.12013 Research Vol.81, No.12013 5 6 Vol.81,
2 5 22 25 4 8 8 9 9 9 10 10 11 12 14 14 15 7 18 16 18 19 20 21 16 17 17 28 19 21 1 Research 2 Vol.81, No.12013 Vol.81, No.12013 3 P r o d u c t s 4 Vol.81, No.12013 Research Vol.81, No.12013 5 6 Vol.81,
資料2発酵乳
 資料 2 乳及び乳製品の成分規格等に関する省令における 発酵乳の規格基準等の見直しについて 平成 26 年 2 月 1. 経緯発酵乳については 食品衛生法第 11 条第 1 項に基づき規定された乳及び乳製品の成 分規格等に関する省令 ( 以下 乳等省令 という ) により規格基準が定められている 近年における製造方法や製品の多様化を踏まえ 実態に即した規格基準となるよう関係業界団体から要望がきており
資料 2 乳及び乳製品の成分規格等に関する省令における 発酵乳の規格基準等の見直しについて 平成 26 年 2 月 1. 経緯発酵乳については 食品衛生法第 11 条第 1 項に基づき規定された乳及び乳製品の成 分規格等に関する省令 ( 以下 乳等省令 という ) により規格基準が定められている 近年における製造方法や製品の多様化を踏まえ 実態に即した規格基準となるよう関係業界団体から要望がきており
<4D F736F F F696E74202D D58FB08E8E8CB15F88F38DFC FC92F994C532816A>
 2007 年 12 月 15 日第 3 回市民向けがん情報講演会論より科学的根拠! 信頼できるがん情報とは 最新の治療が最善の治療とは限らない - 臨床試験 - がん対策情報センター臨床試験 診療支援部薬事 安全管理室長柴田大朗 本日のお話の内容 (1) なぜ新しい治療法の効果や安全性を評価しなければならないのでしょうか? 新しいお薬候補のほとんどは効かないことをご存じでしたか? (2) どうして新しい治療法の評価をするために
2007 年 12 月 15 日第 3 回市民向けがん情報講演会論より科学的根拠! 信頼できるがん情報とは 最新の治療が最善の治療とは限らない - 臨床試験 - がん対策情報センター臨床試験 診療支援部薬事 安全管理室長柴田大朗 本日のお話の内容 (1) なぜ新しい治療法の効果や安全性を評価しなければならないのでしょうか? 新しいお薬候補のほとんどは効かないことをご存じでしたか? (2) どうして新しい治療法の評価をするために
査を実施し 必要に応じ適切な措置を講ずること (2) 本品の警告 効能 効果 性能 用法 用量及び使用方法は以下のとお りであるので 特段の留意をお願いすること なお その他の使用上の注意については 添付文書を参照されたいこと 警告 1 本品投与後に重篤な有害事象の発現が認められていること 及び本品
 薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
2017 年 8 月 9 日放送 結核診療における QFT-3G と T-SPOT 日本赤十字社長崎原爆諫早病院副院長福島喜代康はじめに 2015 年の本邦の新登録結核患者は 18,820 人で 前年より 1,335 人減少しました 新登録結核患者数も人口 10 万対 14.4 と減少傾向にあります
 2017 年 8 月 9 日放送 結核診療における QFT-3G と T-SPOT 日本赤十字社長崎原爆諫早病院副院長福島喜代康はじめに 2015 年の本邦の新登録結核患者は 18,820 人で 前年より 1,335 人減少しました 新登録結核患者数も人口 10 万対 14.4 と減少傾向にありますが 本邦の結核では高齢者結核が多いのが特徴です 結核診療における主な検査法を示します ( 図 1) 従来の細菌学的な抗酸菌の塗抹
2017 年 8 月 9 日放送 結核診療における QFT-3G と T-SPOT 日本赤十字社長崎原爆諫早病院副院長福島喜代康はじめに 2015 年の本邦の新登録結核患者は 18,820 人で 前年より 1,335 人減少しました 新登録結核患者数も人口 10 万対 14.4 と減少傾向にありますが 本邦の結核では高齢者結核が多いのが特徴です 結核診療における主な検査法を示します ( 図 1) 従来の細菌学的な抗酸菌の塗抹
5_使用上の注意(37薬効)Web作業用.indd
 34 ビタミン主薬製剤 1 ビタミン A 主薬製剤 使用上の注意と記載条件 1. 次の人は服用前に医師又は薬剤師に相談することあ医師の治療を受けている人 い妊娠 3 ヵ月以内の妊婦, 妊娠していると思われる人又は妊娠を希望する人 ( 妊娠 3 ヵ月前から妊娠 3 ヵ月までの間にビタミン A を 1 日 10,000 国際単位以上摂取した妊婦から生まれた児に先天異常の割合が上昇したとの報告がある )
34 ビタミン主薬製剤 1 ビタミン A 主薬製剤 使用上の注意と記載条件 1. 次の人は服用前に医師又は薬剤師に相談することあ医師の治療を受けている人 い妊娠 3 ヵ月以内の妊婦, 妊娠していると思われる人又は妊娠を希望する人 ( 妊娠 3 ヵ月前から妊娠 3 ヵ月までの間にビタミン A を 1 日 10,000 国際単位以上摂取した妊婦から生まれた児に先天異常の割合が上昇したとの報告がある )
動物用医薬品(医薬部外品)製造販売承認事項変更承認申請書
 別記様式 1 ( 一 ) 生ウイルス + 株化細胞ワクチン 動物用医薬品製造販売承認事項変更承認申請書 ( 例 ) SL 年月日 農林水産大臣 殿 住所 氏名 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第 14 条第 9 項の規定により動物用医薬品製造販売承認事項の変更の承認を受けたいので 下記により申請します 記承認年月日及び承認番号 1 製造業者又は認定外国製造業者の氏名又は名称及び住所既承認内容を記載
別記様式 1 ( 一 ) 生ウイルス + 株化細胞ワクチン 動物用医薬品製造販売承認事項変更承認申請書 ( 例 ) SL 年月日 農林水産大臣 殿 住所 氏名 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第 14 条第 9 項の規定により動物用医薬品製造販売承認事項の変更の承認を受けたいので 下記により申請します 記承認年月日及び承認番号 1 製造業者又は認定外国製造業者の氏名又は名称及び住所既承認内容を記載
スライド 1
 キャリアコンサルティング技能検定 2 級論述問題の解き方について キャリア コンサルタントの相談の基本は何であろうか? 相談過程の基本は 相談場面の設定 自己理解支援 仕事理解支援 啓発的経験支援 意思決定支援 方策の実行支援 新たな仕事への適応支援 相談過程の総括であったと思う この過程へのこだわりが強い問題が出題されたら はっきり言って厳しい 実技試験でも必要だから この相談過程 ここで頭にいれておいてね
キャリアコンサルティング技能検定 2 級論述問題の解き方について キャリア コンサルタントの相談の基本は何であろうか? 相談過程の基本は 相談場面の設定 自己理解支援 仕事理解支援 啓発的経験支援 意思決定支援 方策の実行支援 新たな仕事への適応支援 相談過程の総括であったと思う この過程へのこだわりが強い問題が出題されたら はっきり言って厳しい 実技試験でも必要だから この相談過程 ここで頭にいれておいてね
鑑-H リンゼス錠他 留意事項通知の一部改正等について
 日医発第 617 号 ( 保 154) 平成 30 年 8 月 29 日 都道府県医師会長殿 日本医師会長横倉義武 医薬品医療機器等法上の効能 効果等の変更に伴う留意事項の一部改正等について 平成 30 年 8 月 21 日付け保医発 0821 第 1 号厚生労働省保険局医療課長通知により 添付資料の通り保険適用上の取扱いに関する留意事項が一部改正されましたのでお知らせ申し上げます 今回の改正は 同日付けで添付資料の医薬品の効能
日医発第 617 号 ( 保 154) 平成 30 年 8 月 29 日 都道府県医師会長殿 日本医師会長横倉義武 医薬品医療機器等法上の効能 効果等の変更に伴う留意事項の一部改正等について 平成 30 年 8 月 21 日付け保医発 0821 第 1 号厚生労働省保険局医療課長通知により 添付資料の通り保険適用上の取扱いに関する留意事項が一部改正されましたのでお知らせ申し上げます 今回の改正は 同日付けで添付資料の医薬品の効能
平成17年5月18日 豊岡市国民健康保険運営協議会シナリオ
 平成 30 年度第 2 回豊岡市国民健康保険運営協議会会議録 1 日時平成 30 年 5 月 15 日 ( 火 ) 午後 1 時 30 分開会午後 2 時 20 分閉会 2 場所豊岡市役所本庁 3 階庁議室 3 出席者 9 名 11 名 4 議事 協議事項 (1) 平成 30 年度豊岡市国民健康保険事業の基本方針 1 国民健康保険税率算定結果について 2 答申 ( 案 ) について 1/5 会議録
平成 30 年度第 2 回豊岡市国民健康保険運営協議会会議録 1 日時平成 30 年 5 月 15 日 ( 火 ) 午後 1 時 30 分開会午後 2 時 20 分閉会 2 場所豊岡市役所本庁 3 階庁議室 3 出席者 9 名 11 名 4 議事 協議事項 (1) 平成 30 年度豊岡市国民健康保険事業の基本方針 1 国民健康保険税率算定結果について 2 答申 ( 案 ) について 1/5 会議録
変更一覧表 変更内容新現備考 Peak 50~60 Trough 4 未満 Peak 20.0~30.0 Trough 8.0 以下 アミカシン 静注投与後 1 時間 Trough 1 未満 Peak 4.0~9.0 Trough 2.0 以下 トブラマイシン 静注投与後
 No.2017-14 変更 2017 年 4 月 検査内容変更のお知らせ 謹啓時下ますますご清栄のこととお喜び申し上げます 平素は格別のご高配を賜り厚くお礼申し上げます このたび下記におきまして 検査内容を変更させていただきたくご案内いたします 何卒ご了承賜りますようよろしくお願い申し上げます 敬白 変更実施日 2 017 年 7 月 7 日 ( 金 ) ご依頼分より 項目名称の変更は 7 月 10
No.2017-14 変更 2017 年 4 月 検査内容変更のお知らせ 謹啓時下ますますご清栄のこととお喜び申し上げます 平素は格別のご高配を賜り厚くお礼申し上げます このたび下記におきまして 検査内容を変更させていただきたくご案内いたします 何卒ご了承賜りますようよろしくお願い申し上げます 敬白 変更実施日 2 017 年 7 月 7 日 ( 金 ) ご依頼分より 項目名称の変更は 7 月 10
ロタウイルスワクチンは初回接種を1 価で始めた場合は 1 価の2 回接種 5 価で始めた場合は 5 価の3 回接種 となります 母子感染予防の場合のスケジュール案を示す 母子感染予防以外の目的で受ける場合は 4 週間の間隔をあけて2 回接種し 1 回目 の接種から20~24 週あけて3 回目を接種生
 注 1) 本スケジュール案は 2014 年 10 月現在 接種可能な主なワクチンをすべて受けると仮定して 1 例を示したものです 接種の順番や受けるワクチンの種類については お子様の体調や周りの感染症発生状況によって 異なってきます 詳しくはかかりつけの医療機関 保健所等でご相談ください 注 2) 接種に際しては次の決まりがあります スケジュールを立てるときの参考にしてください 別の種類のワクチンを接種する場合は
注 1) 本スケジュール案は 2014 年 10 月現在 接種可能な主なワクチンをすべて受けると仮定して 1 例を示したものです 接種の順番や受けるワクチンの種類については お子様の体調や周りの感染症発生状況によって 異なってきます 詳しくはかかりつけの医療機関 保健所等でご相談ください 注 2) 接種に際しては次の決まりがあります スケジュールを立てるときの参考にしてください 別の種類のワクチンを接種する場合は
