(Microsoft PowerPoint - \202V\214\216\203Z\203~\203i\201[\216\221\227\277.pptx)
|
|
|
- あきみ めいこ
- 5 years ago
- Views:
Transcription
1 医薬品適合性調査申請及び医薬品承認申請の取扱い 医薬品適合性調査申請の取扱い 奈良県医療政策部薬務課 医薬品適合性調査の実施 (1) 製造販売承認申請 承認事項一変申請に係る調査 (2)5 年毎の定期調査 (3) 輸出用医薬品等の輸出届に伴う調査輸出 医薬品の製造開始後 5 年毎の定期調査 適合性調査申請は 輸出届を届出た医薬品等輸出業者が誰であるかに関わらず 当該医薬品等の製造をする製造業者が うこと 医薬品適合性調査申請の 数料 数料は奈良県収 証紙で納付してください 奈良県収 証紙は奈良県庁地下売店等で購 できます 承認申請時( 部変更承認申請を含む ) 輸出時無菌区分 48,800 一般区分 : 28,700 円包装 表示 保管区分 : 13,300 円外部試験検査機関等 : 18,600 円 申請区分をよく確認のうえ申請してください 包装 表 保管区分の申請を 般区分で提出された事例がありましたので十分注意して下さい 1
2 適合性調査申請時提出物 ( 承認 一変時 ) 1) 適合性調査申請書 :2 部 ( 提出 1 部 + 自社控え 1 部 ) 外字がある場合は 外字表 2) 申請データ :FD 申請ソフトで作成した申請データを フロッピーディ スク は CD-R へ提出 出 して持参して下さい 3) 適合性調査申請提出資料申出書 :1 部 4) チェックシート :1 部 奈良県ホームページ 5) 添付資料 適合性調査申請時提出物 ( 承認 一変時 ) 1. 承認申請書の写し ( 申請区分を確認しますので必ず提出してください ) 変の場合 : 当該申請に係る 部変更承認申請書の写し及び当該品目にかかる承認書等の写し 2.GMP 組織図 構造設備の概要及び図面 3. 原料試験の 順 記録様式 試験結果 ( PV に使 した原料試験結果 ) 4. 製造方法のフロー図等手順書 製造指図 記録書 5. 標準的仕込量及びその根拠 6. 重要 程における 程内試験の概要と 程管理値 7. バリデーションに関する資料 (PQ PV 洗浄バリデーション) 8. 製造販売業者との取決め ( 写し ) 適合性調査の流れ ( 承認 変 ) 1) 申請者より承認適合性調査申請 ( 申請に必要な資料がそろった時点 ( 承認申請書は 最終差換え済み )) 2) 薬務課より実地調査 書面調査の連絡 書 調査を希望される場合は 下記の資料の提出が必要 1. 調査 から 2 年以内の実地の適合性調査結果通知の提出 2. 調査 から 2 年以内の実地の適合性調査結果通知の品目と今回の品目の対 表 対比表には 処方 使用機器 ( 重要工程以外も含む ) を記載 ( 様式は問いません ) 実地調査 3) 実地調査日の通知 ( 申請者へ通知 ( 調査日は 製造所と相談のうえ決定 )) 4) 実地調査 ( 講評時に指示内容を伝達する ) 口頭指示か書面指示になるかは 課に戻って判断 5) 指示書発出 ( 書面指示がある場合 ) 6) 指 書回答提出 受理 7) 適合性調査結果通知発出 ( 承認権者 許可権者 申請者宛 ) 急ぐ場合は 指示書に対する回答を速やかに って下さい 8) 適合性調査結果報告書発出 ( 調査対象製造所宛 ) 2
3 書面調査 3) 照会事項の発出 ( 照会がある場合 ) 4) 照会事項に対する回答 5) 指示書発出 ( 指示がある場合 ) 6) 指 書回答提出 受理 急ぐ場合は 回答を速やかに って下さい 7) 適合性調査結果通知発出 ( 承認権者 許可権者 申請者宛 ) 指 書に対する回答の留意事項 十分に内容を精査した上で回答してください 作業手順書等を改訂した場合には 改訂箇所が確認できるコピーを提出してください 改善の完了に時間を要する場合には 改善計画内容と完了予定時期を記載して提出してください また 改善終了後には 速やかに改善完了報告書を提出してください 適合性調査申請書作成時注意事項 全般的事項 1 申請者の住所 役職名 氏名を正しく記載してください ( 役職名の記載漏れがよくあります ) 2 奈良県知事名を正しく記載してください 3 業者コードを正しく記載してください 4 提出年 を正しく記載してください ( 提出 を間違える場合がよくあります ) 5 再提出を示す記号は 新規提出 としてください 適合性調査申請書作成時注意事項 調査対象品目の別 欄一般区分の許可を取得の製造所であっても 包装等の工程のみを実施する場合は 包装 表示 保管 を選択してください システム受付番号 欄新規及び一変の承認申請書を申請した際に附番されたシステム受付番号を記載してください ( 間違わないように十分注意してください ) 承認申請年 は承認年 欄 新規及び 変の申請書の申請年 を記載してください 変の場合 部変更承認申請の申請年 を記載してください ( 承認年 ではありませんので注意してください ) 3
4 適合性調査申請書作成時注意事項 備考 欄 1 原薬の製造所に関する適合性調査申請については 原料名 原薬中間体名 MF に登録された原薬名 (MF 番号 ) MF に登録された原薬中間体名 (MF 番号 ) の旨を記載してください 2 外部試験検査機関に係る適合性調査申請については 外部試験検査機関 の旨を記載してください 3 物多名称となる複数の品目を 括して適合性調査申請を う場合は 一括申請である旨を記載してください 医療 後発医薬品に係る適合性調査申請の注意事項 医療 後発医薬品にかかる承認審査及び GMP 適合性調査申請等のス ケジュール等について に基づき対応すること ( 平成 28 年 付け事務連絡 ) GMP 適合性調査結果通知の期限が決められていますので先ほどの適合 性調査の事務処理期間を考えて余裕をもって申請していただきますようお願いします ぎりぎりの申請が多くみられますので余裕をもって申請してください 適合性調査の標準処理期間医薬品適合性調査申請 ( その他 ) 標準処理期間 :60 医薬品適合性調査申請 ( 包装 表示 保管区分 ) 標準処理期間 :60 医薬品製造販売承認申請の取扱い 標準処理期間には 申請等の補正に要する 数 県の休 の日数は除きます 希望日の 3 か月前には申請を提出していただきますようお願いします ( 申請時には 添付資料をそろえて下さい ) 4
5 地方委任品目について 医薬品 1 および医薬部外品 2 は 業許可とは別に 品目ごとに厚生労働大臣の承認を取得しなければ製造販売を うことができません 品目ごとの承認は厚 労働 が いますが 部の品目については地方委任医薬品として 承認権限が都道府県知事に委任されています 1 厚生労働大臣が基準を定めて指定する医薬品及び第 23 条の 2 第 1 項 の規定により指定する体外診断用医薬品を除く 地方委任品目について 県が承認する品目とは 医薬品医療機器等法第 四条第一項に品目ごとの承認に係る医薬品の種類並びに当該種類ごとの有効成分の種類 配合割合及び分量並びに効能及び効果の範囲が されている 薬事法施 令第 80 条第 2 項第 5 号の規定に基づき厚生労働大臣が指定する医薬品の種類等 ( 昭和 45 年厚 省告 第 366 号 ) 2 厚生労働大臣が基準を定めて指定する医薬部外品を除く 医薬品製造販売承認申請の申請資料 ( 地 委任品目 ) 1) 承認申請書 :4 部 ( 提出 3 部 + 自社控え 1 部 ) 2) 申請データ :FD 申請ソフトで作成した申請データを フロッピーディスク は CD-R へ提出 出 して持参して下さい 3) 添付資料 : 規格及び試験 法に関する資料 安定性試験に関する資料 適合性調査申請を省略する場合は その根拠となる資料を添付して下さい 4) 地方委任品目チェックシート :1 部 奈良県ホームページ : 20 5
6 医薬品製造販売承認申請の 数料 医薬品製造販売承認申請にかかる 数料 数料は奈良県収 証紙で納付してください 奈良県収 証紙は奈良県庁地下売店等で購 できます 製造販売承認医薬品 ( その他 ) : 69,300 円製造販売承認事項 部変更承認医薬品 ( その他 ) : 30,100 円 医薬品承認審査の流れ ( 新規承認品目 ) 1) 申請者より承認申請 ( 申請に必要な資料がそろった時点 ) 2) 薬務課 薬事研究センター照会事項発出 ( 申請から1か 程度 ) 3) 申請者より薬務課 薬事研究センターへ回答送付 ( 再照会が必要な場合あり ) 4) 薬務課 薬事研究センター回答確認 審査終了 医薬品承認審査の流れ ( 新規承認品目 ) 5) 差換え指示 ( 必要な場合 ) 6) 差換え願を提出 ( 差換え指示があった場合 ) 7) 適合性調査の実施 8) 適合性調査の結果通知確認後に承認 回答時の注意事項 十分に内容を精査した上で回答してください 照会した内容以外の内容は 原則変更しないで下さい やむを得ず変更する場合は 回答を提出する前に担当者に連絡してください 承認書 添付書類を訂正する場合は 訂正箇所が明確にわかるように下線等を付してください 6
7 回答時の注意事項 訂正を うことにより 他の部分に影響がある場合は 適切に訂正してください 製造 法欄の連番を変更する等 薬務課照会事項と薬事研究センター照会事項に対する照会回答は別々に作成し 薬務課には 薬務課照会事項に対する回答を 薬事研究センターには 薬事研究センターに対する回答を提出してください 差換え願提出時の注意事項 最終回答の内容が反映できているかを十分確認したうえで提出してください 差換え願の鑑を含め 4 部提出してください 販売名に変更がある場合は 申請書の鑑を 4 部提出してください 製造所の許可年 は認定年 が更新されている場合は 変更してください ( 成分及び分量 は本質欄テキスト欄 ) 11 量及び 1 錠 ( カプセル 包 ) あたりの質量を記載してください 2 配合する成分で濃度を規定する必要があるものは その濃度を記載してください ( 例 :D- ソルビトール液 ) 3 配合する成分で置換度タイプ及び粘度を記載する必要があるものは 置換度タイプ及び粘度を点記載してください ( 例 : ヒプロメロース ) ( 成分及び分量 は本質欄テキスト欄 ) 4 配合する成分の平均重合度 乾燥減量値 かさ密度を記載する必要があるものは 平均重合度 乾燥減量値 かさ密度を幅で記載してください ( 例 : 結晶セルロース ) 5 配合する成分で K 値を記載する必要があるものは K 値を記載してください 6 コーティング錠については 素錠部とコーティング部のそれぞれの成分及び小計を記載してください 7 成分名と別紙規格中の名称が異なる場合 成分名 は, 別紙規格 である. と記載してください 7
8 ( 成分及び分量 は本質欄テキスト欄 ) 8 物由来原料基準反芻動物由来原料基準の対象となる成分について その基準に適合する旨を記載すること なお 平成 26 年 10 月 2 付通知 物由来原料基準の運 について の記載例に従って記載してください < 記載例 > ( 成分名 ) は ( ウシ等の動物名 )( 原産国 ) の ( 使用部位 ) に由来する 製造方法は別紙規格 ( 又は公定書規格 ) によるほか 健康な動物に由来する原料を使 し BSE に感染している動物由来の原料及び 物由来原料基準反芻動物由来原料基準に定める使 してはならない部位が製造 程中で混 しないよう 採取した を原料として製する ( なお 本原料については 同基準の第 4 項の規定に基づき 平成 13 年 10 月 2 日付け医薬発第 1069 号医薬局 通知の記の 2 の (1) の 2 の条件に適合するものである ) ( 備考 1) 該当する承認 製造販売業の許可の種類 許可番号 許可年 を記載してください 要指導 一般用 の別を記載してください コンビネーション製品に該当する場合は 1 を該当しない場合は 2 を記載してください 基準を記載してください 一物多名称の場合 その旨を記載してください ( 備考 2) 申請区分は 一般用医薬品 (8)( その他 ) と記載してください 物多名称申請において実測値資料 安定性データ等の添付を省略する場合は その他備考欄に 本品は 年 日承認 ( 承認番号 )( 申請中 ) の販売名 と同一であるため添付は省略する 等と記載してください ( 備考 2) 申請時点で安定性試験継続中の場合は 安定性試験中 とし その他備考欄に 試験終了予定年 平成 年 と記載してください 適合性調査結果通知書の写しをもって 適合性調査申請を省略する場合については 備考欄にその旨を記載してください 申請品目の薬効群が新指定医薬部外品および新範囲医薬部外品に重なる場合には 般 医薬品としての申請となる理由 ( 部外品から外れる箇所 : 成分 分量 効能 効果など ) について記載してください 8
9 医薬品製造販売承認申請標準処理期間 医薬品製造販売承認申請 ( その他 ) 標準処理期間 :60 標準処理期間には 申請等の補正に要する 数 県の休日の日数は除きます ご静聴ありがとうございました 9
このモックアップに示した内容 ( 申請者情報 処方及び個々の数値等 ) は すべて架空のものです 共通ヘッダ等の記載例 様式 様式の別を示す記号 :E01( 医薬品製造販売承認申請書 ) 提出先 提出先の別 :2( 都道府県 ) 提出年月日 : ( 平成 30 年 12 月 01 日 )
 共通ヘッダ等の記載例 様式 様式の別を示す記号 :E01( 医薬品製造販売承認申請書 ) 提出先 提出先の別 :2( 都道府県 ) 提出年月日 :2301201( 平成 30 年 12 月 01 日 ) 提出者 業者コード :123456000 管理番号 :101 郵便番号 :111-1111 住所 : 東京都新宿区 町 1-1-1 法人名 : 新宿製薬株式会社 法人名ふりがな : しんじゅくせいやくかぶしきかいしゃ
共通ヘッダ等の記載例 様式 様式の別を示す記号 :E01( 医薬品製造販売承認申請書 ) 提出先 提出先の別 :2( 都道府県 ) 提出年月日 :2301201( 平成 30 年 12 月 01 日 ) 提出者 業者コード :123456000 管理番号 :101 郵便番号 :111-1111 住所 : 東京都新宿区 町 1-1-1 法人名 : 新宿製薬株式会社 法人名ふりがな : しんじゅくせいやくかぶしきかいしゃ
改正薬事法の施行に伴う製造販売の承認を要しない医薬品等の取扱い等について
 薬食審査発第 0331015 号平成 17 年 3 月 31 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 改正薬事法の施行に伴う製造販売の承認を要しない医薬品等の取扱い等について 薬事法及び採血及び供血あっせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 薬事法等一部改正法 という ) による改正後の薬事法 ( 昭和 35 年法律第 145
薬食審査発第 0331015 号平成 17 年 3 月 31 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 改正薬事法の施行に伴う製造販売の承認を要しない医薬品等の取扱い等について 薬事法及び採血及び供血あっせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 薬事法等一部改正法 という ) による改正後の薬事法 ( 昭和 35 年法律第 145
MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1
 MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1 MDSAP 報告書の受入れの概要 (1/2) 日本は 平成 27 年 6 月にMDSAPに参加する旨を発表 関係者との意見交換を行い MDSAP 報告書の受け入れについて 以下の通知を発出した 平成 28 年 6 月 22 日薬生監麻発 0622 第 3 号 薬生機審発 0622
MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1 MDSAP 報告書の受入れの概要 (1/2) 日本は 平成 27 年 6 月にMDSAPに参加する旨を発表 関係者との意見交換を行い MDSAP 報告書の受け入れについて 以下の通知を発出した 平成 28 年 6 月 22 日薬生監麻発 0622 第 3 号 薬生機審発 0622
薬食審査発第 号
 薬食審査発第 0928004 号 平成 19 年 9 月 28 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 第十五改正日本薬局方第一追補の制定に伴う 医薬品製造販売承認申請等の取扱いについて 平成 19 年 9 月 28 日厚生労働省告示第 316 号をもって第十五改正日本薬局方第一追補 ( 以下 第一追補 という ) が告示され 平成 19 年 9 月 28 日付け薬食発第
薬食審査発第 0928004 号 平成 19 年 9 月 28 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 第十五改正日本薬局方第一追補の制定に伴う 医薬品製造販売承認申請等の取扱いについて 平成 19 年 9 月 28 日厚生労働省告示第 316 号をもって第十五改正日本薬局方第一追補 ( 以下 第一追補 という ) が告示され 平成 19 年 9 月 28 日付け薬食発第
管下関係業者に周知いただくとともに 適切な指導を行い その実施に遺漏な きようお願いいたします 記 第 1 体外診断用医薬品の製造販売業又は製造業を行う旨の届出等について 1. 届出対象者旧薬事法に基づき 体外診断用医薬品を取り扱う以下の者 (1) 旧薬事法第 12 条第 1 項の第二種医薬品製造販
 薬食機参発 0 8 2 1 第 1 号 薬食安発 0 8 2 1 第 1 号 平成 2 6 年 8 月 2 1 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 厚生労働省医薬食品局安全対策課長 ( 公印省略 ) 体外診断用医薬品の製造販売業又は製造業を行う旨の届出等について 薬事法等の一部を改正する法律 ( 平成
薬食機参発 0 8 2 1 第 1 号 薬食安発 0 8 2 1 第 1 号 平成 2 6 年 8 月 2 1 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 厚生労働省医薬食品局安全対策課長 ( 公印省略 ) 体外診断用医薬品の製造販売業又は製造業を行う旨の届出等について 薬事法等の一部を改正する法律 ( 平成
Microsoft Word - ‡e‡c.doc
 医薬品等電子申請ソフトによる医療機器適合性調査申請書作成の手引き 厚生労働省医薬食品局から配布されている医薬品等電子申請ソフト (FD 申請ソフト ) を使用して 医療機器適合性調査申請を行うための手引きです FD 申請ソフトを使用することで申請書の作成および管理が容易となります ソフトは以下のホームページからダウンロードしてください なお インストールは 別途ホームページに掲載のマニュアルを参照してください
医薬品等電子申請ソフトによる医療機器適合性調査申請書作成の手引き 厚生労働省医薬食品局から配布されている医薬品等電子申請ソフト (FD 申請ソフト ) を使用して 医療機器適合性調査申請を行うための手引きです FD 申請ソフトを使用することで申請書の作成および管理が容易となります ソフトは以下のホームページからダウンロードしてください なお インストールは 別途ホームページに掲載のマニュアルを参照してください
<4D F736F F F696E74202D C8E90BB96F2835A837E B A838C E B8CDD8AB B83685D>
 コンカレントバリデーションの取扱いについて 薬務課振興係 まずは 少しおさらい バリデーションについて GMP 省令第 13 条 ( バリデーションの実施 ) 1 製造業者は あらかじめ指定した者に 手順書に基づき 次に掲げる業務を行わせなければならない 一次に掲げる場合においてバリデーションを行うこと イ当該製造所において新たに医薬品の製造を開始する場合ロ製造手順等に製品の品質に大きな影響を及ぼす変更がある場合ハその他製品の製造管理及び品質管理を適切に行うために必要と認められる場合二バリデーションの計画及び結果を品質部門に対して文書により報告すること
コンカレントバリデーションの取扱いについて 薬務課振興係 まずは 少しおさらい バリデーションについて GMP 省令第 13 条 ( バリデーションの実施 ) 1 製造業者は あらかじめ指定した者に 手順書に基づき 次に掲げる業務を行わせなければならない 一次に掲げる場合においてバリデーションを行うこと イ当該製造所において新たに医薬品の製造を開始する場合ロ製造手順等に製品の品質に大きな影響を及ぼす変更がある場合ハその他製品の製造管理及び品質管理を適切に行うために必要と認められる場合二バリデーションの計画及び結果を品質部門に対して文書により報告すること
(Microsoft PowerPoint - GVPGQP\203t\203H\203\215\201[\203A\203b\203v.pptx)
 平成 27 年度医薬品製造販売業におけるおける調査 (GVP GQP) 奈良県医療政策部薬務課振興係 調査状況 平成 26 年度末に 製造販売業は製造業と共と共に大更新に大更新を終えました 更新時は 製造業の GMP を重点に確認を行ったところ 1 平成 27 年度調査概要 調査 1 製造販売業の GQP G VP についてのフォローアップ調査 調査 2 製造業の追加 GMP 項目についての調査 調査スケジュール
平成 27 年度医薬品製造販売業におけるおける調査 (GVP GQP) 奈良県医療政策部薬務課振興係 調査状況 平成 26 年度末に 製造販売業は製造業と共と共に大更新に大更新を終えました 更新時は 製造業の GMP を重点に確認を行ったところ 1 平成 27 年度調査概要 調査 1 製造販売業の GQP G VP についてのフォローアップ調査 調査 2 製造業の追加 GMP 項目についての調査 調査スケジュール
はじめて医療機器を製造販売または製造される方へ
 を製造 ( 輸入 ) 販売するには 国内で必要な許可等について を製造販売 製造 ( 輸入 ) するためには 医薬品 等の品質 有効性及び安全性の確保等に関する法律 ( 以下 薬機法という ) の許可等 ( 製造販売業許可 製造業登録 ) が必要になります 製品を市場に出荷するために必要な許可 販売する製品に対して最終責製造販売業任を持ち 自社の名前で市場へ出荷する この許可では製造することはできません
を製造 ( 輸入 ) 販売するには 国内で必要な許可等について を製造販売 製造 ( 輸入 ) するためには 医薬品 等の品質 有効性及び安全性の確保等に関する法律 ( 以下 薬機法という ) の許可等 ( 製造販売業許可 製造業登録 ) が必要になります 製品を市場に出荷するために必要な許可 販売する製品に対して最終責製造販売業任を持ち 自社の名前で市場へ出荷する この許可では製造することはできません
タスクフォース 1 ( TF1 ) 質疑応答その 1 ついでの変更 Q 1-01 Q 1-10 事前確認簡易相談 Q 2-01 Q 2-25 平成 30 年 3 TF1 質疑応答その 1
 タスクフォース 1 ( TF1 ) 質疑応答その 1 ついでの変更 Q 1-01 Q 1-10 事前確認簡易相談 Q 2-01 Q 2-25 タスクフォース 1 ( TF1 ) 質疑応答その 1 ついでの変更 Q1-01 今回新たに追加された ついでの変更 について, 変申請 は軽微変更届出を う機会に変更しなかった場合はどうなるのか. タスクフォース 1 ( TF1 ) 質疑応答その 1 ついでの変更
タスクフォース 1 ( TF1 ) 質疑応答その 1 ついでの変更 Q 1-01 Q 1-10 事前確認簡易相談 Q 2-01 Q 2-25 タスクフォース 1 ( TF1 ) 質疑応答その 1 ついでの変更 Q1-01 今回新たに追加された ついでの変更 について, 変申請 は軽微変更届出を う機会に変更しなかった場合はどうなるのか. タスクフォース 1 ( TF1 ) 質疑応答その 1 ついでの変更
2 規格 試験方法 規格 試験方法 承認申請書の規格及び試験方法欄は 以前より何の規格及び試験方法か分るように 錠の規格及び試験方法 とタイトルを付していたが この試験名は 標題 とすることで構わないか 更に 局方品のように 日本薬局方による と簡略記載した場合の試験名は 日局 とすることで構わない
 1 チェック機能 電子申請ソフトで入力できない文字もコピー貼り付けで入力でき ( 例 : 手数料欄の金額に, ) チェックをクリックしてもエラーが出ないため FD へ出力できたが 機構での受付時に FD 取り込みができないことがあった 電子申請ソフトのチェックで問題がなければ 機構での FD 取り込みもできるようなチェック機能にして欲しい 基本的に申請ソフトのチェックで問題なければ総合機構で受付可能です
1 チェック機能 電子申請ソフトで入力できない文字もコピー貼り付けで入力でき ( 例 : 手数料欄の金額に, ) チェックをクリックしてもエラーが出ないため FD へ出力できたが 機構での受付時に FD 取り込みができないことがあった 電子申請ソフトのチェックで問題がなければ 機構での FD 取り込みもできるようなチェック機能にして欲しい 基本的に申請ソフトのチェックで問題なければ総合機構で受付可能です
Microsoft Word - 【発送版】製造所の登録通知
 薬食機参発 1003 第 1 号 平成 26 年 10 月 3 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いについて 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業は登録制に移行され
薬食機参発 1003 第 1 号 平成 26 年 10 月 3 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いについて 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業は登録制に移行され
<4D F736F F F696E74202D A838C F838A B C982C282A282C42E B8CDD8AB B83685D>
 の 取扱いについて 薬務課振興係 バリデーションの種類 ( 要件 ) ( バリデーション基準 ) 適格性評価 設計時適格性評価(DQ) 設備据付時適格性評価(IQ) 運転時適格性評価(OQ) 性能適格性評価(PQ) プロセスバリデーション (PV) 予測的バリデーション 洗浄バリデーション 再バリデーション 変更時のバリデーション とは バリデーション基準 GMP 事例集 (PIC/S GMP ガイドラインアネックス
の 取扱いについて 薬務課振興係 バリデーションの種類 ( 要件 ) ( バリデーション基準 ) 適格性評価 設計時適格性評価(DQ) 設備据付時適格性評価(IQ) 運転時適格性評価(OQ) 性能適格性評価(PQ) プロセスバリデーション (PV) 予測的バリデーション 洗浄バリデーション 再バリデーション 変更時のバリデーション とは バリデーション基準 GMP 事例集 (PIC/S GMP ガイドラインアネックス
Microsoft Word - 【発送版】記載整備通知
 薬食機参発 0929 第 1 号 平成 26 年 9 月 29 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の承認書又は認証書の記載整備について 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業が登録制に移行されること等に伴い
薬食機参発 0929 第 1 号 平成 26 年 9 月 29 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の承認書又は認証書の記載整備について 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業が登録制に移行されること等に伴い
<4D F736F F F696E74202D CA9976C A A4F8D9190BB91A28BC68ED282CC944692E890A793782E E B8CDD8AB B83685D>
 外国製造業者の認定制度 独立行政法人医薬品医療機器総合機構機構 品質管理部長 新見裕一 2009 年 6 月 23 日 CPhI China 2009 1 本日の話題 1. 外国製造業者認定制度の概要 2. 申請手続き 3. 提出資料 4. 申請から認定を受けるまでの流れ 5.PMDA のホームページの紹介 2 1. 外国製造業者認定制度の概要 (1) 認定とは (2) 外国製造業者の認定の区分 (3)
外国製造業者の認定制度 独立行政法人医薬品医療機器総合機構機構 品質管理部長 新見裕一 2009 年 6 月 23 日 CPhI China 2009 1 本日の話題 1. 外国製造業者認定制度の概要 2. 申請手続き 3. 提出資料 4. 申請から認定を受けるまでの流れ 5.PMDA のホームページの紹介 2 1. 外国製造業者認定制度の概要 (1) 認定とは (2) 外国製造業者の認定の区分 (3)
(Microsoft Word -
 事務連絡 平成 30 年 2 月 28 日 医薬品 医療機器等製造販売業者殿 奈良県医療政策部薬務課薬物監視係長 医薬品 医療機器等の回収の取扱いについて 医薬品 医薬部外品 化粧品及び医療機器等の回収については 医薬品 医療機器等の回収について ( 平成 26 年 12 月 21 日付け薬食発 1121 第 10 号厚生労働省医薬食品局長通知 ) 及び 医薬品 医療機器等の回収の取扱いについて (
事務連絡 平成 30 年 2 月 28 日 医薬品 医療機器等製造販売業者殿 奈良県医療政策部薬務課薬物監視係長 医薬品 医療機器等の回収の取扱いについて 医薬品 医薬部外品 化粧品及び医療機器等の回収については 医薬品 医療機器等の回収について ( 平成 26 年 12 月 21 日付け薬食発 1121 第 10 号厚生労働省医薬食品局長通知 ) 及び 医薬品 医療機器等の回収の取扱いについて (
<4D F736F F F696E74202D FA967B82CC96F28E9690A C982C282A282C42E >
 日本の薬事制度について 厚生労働省 医薬食品局審査管理課中西民二 本日の内容 医薬品の製造販売 外国製造業者の認定と GMP 適合性調査 外国製造業者の認定 承認審査における GMP 適合性調査 原薬等登録原簿 (MF) 医薬品の製造販売 医薬品の製造販売に関する規制 製造販売とは 製造等製造等 ( 他に委託して製造をする場合を含む ) をし 又は輸入をした医薬品 ( 原薬たる医薬品を除く ) を
日本の薬事制度について 厚生労働省 医薬食品局審査管理課中西民二 本日の内容 医薬品の製造販売 外国製造業者の認定と GMP 適合性調査 外国製造業者の認定 承認審査における GMP 適合性調査 原薬等登録原簿 (MF) 医薬品の製造販売 医薬品の製造販売に関する規制 製造販売とは 製造等製造等 ( 他に委託して製造をする場合を含む ) をし 又は輸入をした医薬品 ( 原薬たる医薬品を除く ) を
申請ソフトの起動 申請ソフトを起動して ファイル 申請書の新規作成 を選択 様式から C04 を選択し 了解 クリック ( 参考 1) FD 申請ソフトでの申請書鑑の打出しは 印字されない空欄箇所がありますので 別途 書面による鑑の作成が必要です その方法は FD 申請ソフトの入力手順の次 (P14
 外国製造業者認定申請の作成例 - C04( 医療機器外国製造業者認定申請 ) の事例 - 本作成例は FD 申請ソフトで作成した申請書の提出を前提に その入力方法や申請時に必要な書類などの説明をしています FD 申請へのご協力をお願いします PMDA へ提出する 医療機器医療機器の外国製造業者認定外国製造業者認定申請において 入力情報を最小限にとどめた 簡易入力による簡易入力による FD 申請の受付を平成
外国製造業者認定申請の作成例 - C04( 医療機器外国製造業者認定申請 ) の事例 - 本作成例は FD 申請ソフトで作成した申請書の提出を前提に その入力方法や申請時に必要な書類などの説明をしています FD 申請へのご協力をお願いします PMDA へ提出する 医療機器医療機器の外国製造業者認定外国製造業者認定申請において 入力情報を最小限にとどめた 簡易入力による簡易入力による FD 申請の受付を平成
資料編 に委託して製造をする場合を含み 他から委託を受けて製 造する場合を含まない ) をし 又は輸入した化粧品を製造 販売のために出荷することをいう 製造販売業者 とは 会社の経営陣 ( 取締役等 ) を指します 薬事法施行規則第 92 条 (4) ロット とは 一の製造期間内に一連の製造工程によ
 品質管理業務手順書は GQP 省令の基準を満たしていれば 決まった書式はありません このモデル手順書は 許可要件をクリアするように作成してありますが 実情にあわせ 使いやすい形に改めてください 各項目に対応する法令 通知については p.49 75を参照してください 化粧品品質管理業務手順書 (GQP 手順書 ) 製造販売業者 制定年月日 平成年月日承認 これらの手順書は 総括製造販売責任者が作成し
品質管理業務手順書は GQP 省令の基準を満たしていれば 決まった書式はありません このモデル手順書は 許可要件をクリアするように作成してありますが 実情にあわせ 使いやすい形に改めてください 各項目に対応する法令 通知については p.49 75を参照してください 化粧品品質管理業務手順書 (GQP 手順書 ) 製造販売業者 制定年月日 平成年月日承認 これらの手順書は 総括製造販売責任者が作成し
( 別添 2) ( 別添 2) 平成 14 年 9 月 27 日保発第 号の別添 2 組合管掌健康保険一括適用取扱要領 組合管掌健康保険一括適用取扱要領 ( 準則 ) 第 1 健康保険法 ( 以下 法 という ) 第 34 条第 1 項の規定による厚生労働大臣の承認 ( 以下 一括適
 ( 別添 1) 新 ( 別添 1) 健康保険 厚生年金保険一括適用承認基準 健康保険一括適用承認基準 健康保険法第 34 条第 1 項又は厚生年金保険法第 8 条の 2 の規定による厚生労働大 臣の承認 ( 以下 一括適用の承認 という ) は 次の各項に定める基準に適合する適 用事業所について行うものとする 健康保険法第 34 条の規定による厚生労働大臣の承認 ( 以下 一括適用の承認 と いう
( 別添 1) 新 ( 別添 1) 健康保険 厚生年金保険一括適用承認基準 健康保険一括適用承認基準 健康保険法第 34 条第 1 項又は厚生年金保険法第 8 条の 2 の規定による厚生労働大 臣の承認 ( 以下 一括適用の承認 という ) は 次の各項に定める基準に適合する適 用事業所について行うものとする 健康保険法第 34 条の規定による厚生労働大臣の承認 ( 以下 一括適用の承認 と いう
平成14年8月 日
 平成 30 年 11 月 15 日福祉保健局 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 に基づく行政処分 ( 回収命令 ) について 都は本日 以下の事業者に対し 医薬品 医療機器等の品質 有効性及び安全性の確保 等に関する法律 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 70 条第 1 項の 規定に基づく 回収命令 を行ったので お知らせします 1 対象事業者氏名ピュアハートキングス株式会社
平成 30 年 11 月 15 日福祉保健局 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 に基づく行政処分 ( 回収命令 ) について 都は本日 以下の事業者に対し 医薬品 医療機器等の品質 有効性及び安全性の確保 等に関する法律 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 70 条第 1 項の 規定に基づく 回収命令 を行ったので お知らせします 1 対象事業者氏名ピュアハートキングス株式会社
確定版【都道府県宛】
 薬生発 0329 第 10 号 平成 29 年 3 月 29 日 各都道府県知事 殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律関係手数料令 の一部改正について この度 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律関係手数料令の一部を改正する政令 ( 平成 29 年政令第 62 号 以下 改正政令 という ) が平成
薬生発 0329 第 10 号 平成 29 年 3 月 29 日 各都道府県知事 殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律関係手数料令 の一部改正について この度 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律関係手数料令の一部を改正する政令 ( 平成 29 年政令第 62 号 以下 改正政令 という ) が平成
Microsoft Word - (発出)マル製通知案
 薬食機参発 1119 第 7 号 薬食監麻発 1119 第 12 号 平成 26 年 11 月 19 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 厚生労働省医薬食品局監視指導 麻薬対策課長 ( 公印省略 ) 医療機器及び体外診断用医薬品の製造所の変更又は追加に係る手続 の迅速化について 医療機器及び体外診断用医薬品の製造所の変更に係る手続きの迅速化については
薬食機参発 1119 第 7 号 薬食監麻発 1119 第 12 号 平成 26 年 11 月 19 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 厚生労働省医薬食品局監視指導 麻薬対策課長 ( 公印省略 ) 医療機器及び体外診断用医薬品の製造所の変更又は追加に係る手続 の迅速化について 医療機器及び体外診断用医薬品の製造所の変更に係る手続きの迅速化については
事務連絡 平成 28 年 3 月 29 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局審査管理課 厚生労働省医薬 生活衛生局監視指導 麻薬対策課 医薬品等の製造業許可 外国製造業者認定等に関する質疑応答集 (Q&A) について 今般 標記 Q&A を別添のとおりとり
 事務連絡 平成 28 年 3 月 29 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局審査管理課 厚生労働省医薬 生活衛生局監視指導 麻薬対策課 医薬品等の製造業許可 外国製造業者認定等に関する質疑応答集 (Q&A) について 今般 標記 Q&A を別添のとおりとりまとめましたので 御了知の上 貴管下関係業 者に対して周知願います なお 本通知の写しを別記関係団体宛て送付することとしています
事務連絡 平成 28 年 3 月 29 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局審査管理課 厚生労働省医薬 生活衛生局監視指導 麻薬対策課 医薬品等の製造業許可 外国製造業者認定等に関する質疑応答集 (Q&A) について 今般 標記 Q&A を別添のとおりとりまとめましたので 御了知の上 貴管下関係業 者に対して周知願います なお 本通知の写しを別記関係団体宛て送付することとしています
ICH Q4B Annex12
 薬食審査発 0321 第 1 号平成 2 5 年 3 月 21 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) ICHQ4B ガイドラインに基づく事項別付属文書 ( エンドトキシン試験法 ) について 今般 日米 EU 医薬品規制調和国際会議 (ICH) において ICHQ4B ガイドライン ( 平成 21 年 5 月 26 日付け薬食審査発第 0526001
薬食審査発 0321 第 1 号平成 2 5 年 3 月 21 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) ICHQ4B ガイドラインに基づく事項別付属文書 ( エンドトキシン試験法 ) について 今般 日米 EU 医薬品規制調和国際会議 (ICH) において ICHQ4B ガイドライン ( 平成 21 年 5 月 26 日付け薬食審査発第 0526001
<4D F736F F D2088E396F BB91A28BC EF C8EA695DB8AC78BE695AA816A C826F8AEE8F808F918EE88F878F B2E646F63>
 16 12 24 179 26 1 5 26 1 5 注意 品質部門は製造部門から独立していなければならない 各部門の業務を適切かつ円滑に実施しうる能力のある責任者を 組織 規模 業務の種類に応じ 適切な人数を配置すること ( 必要に応じ 上記に挙げた責任者の枠を増やしてもよい ) 各責任者は業務に支障がない限り兼務することができる ただし 製造部門責任者と品質部門責任者は兼務することはできない 出荷可否決定者は品質部門の者とすること
16 12 24 179 26 1 5 26 1 5 注意 品質部門は製造部門から独立していなければならない 各部門の業務を適切かつ円滑に実施しうる能力のある責任者を 組織 規模 業務の種類に応じ 適切な人数を配置すること ( 必要に応じ 上記に挙げた責任者の枠を増やしてもよい ) 各責任者は業務に支障がない限り兼務することができる ただし 製造部門責任者と品質部門責任者は兼務することはできない 出荷可否決定者は品質部門の者とすること
法改正の目的 1 Ⅰ 医療機器等の特性を踏まえた規制の構築 1. 医療機器等の製造販売業及び製造業の章の新設 2. 体外診断用医薬品の製造販売業の新設 3. 医療機器等の製造業の登録制への移行 4. プログラムの位置付けの明確化 5. QMS 調査の見直し 6. 認証制度に関する見直し 7. 医療機
 医薬品医療機器等法の概要について ~ 医療機器等 ( ) を中心に ~ 東京都健康安全研究センター広域監視部医療機器監視課 ( ) 医療機器等 : 医療機器及び体外診断用医薬品 1 薬事法から医薬品医療機器等法へ 薬事法が 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 に改正されました 以下 医薬品医療機器等法 とします 2-1 - 法改正の目的 1 Ⅰ 医療機器等の特性を踏まえた規制の構築
医薬品医療機器等法の概要について ~ 医療機器等 ( ) を中心に ~ 東京都健康安全研究センター広域監視部医療機器監視課 ( ) 医療機器等 : 医療機器及び体外診断用医薬品 1 薬事法から医薬品医療機器等法へ 薬事法が 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 に改正されました 以下 医薬品医療機器等法 とします 2-1 - 法改正の目的 1 Ⅰ 医療機器等の特性を踏まえた規制の構築
本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2. 書面調査 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの見直し 3.2. 医薬品再審査適合性調査相談 ( 新設 ) 2
 医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2. 書面調査 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの見直し 3.2. 医薬品再審査適合性調査相談 ( 新設 ) 2 本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2.
医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2. 書面調査 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの見直し 3.2. 医薬品再審査適合性調査相談 ( 新設 ) 2 本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2.
Microsoft Word - (発番)医療機器の製造販売承認申請について
 薬食発 1120 第 5 号 平成 26 年 11 月 20 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医療機器の製造販売承認申請について 医療機器の製造販売承認申請の取扱いについては 医療機器の製造販売承認申請について ( 平成 17 年 2 月 16 日付け薬食発第 0216002 号厚生労働省医薬食品局長通知 以下 旧通知 という ) 等により実施してきたところです 先般
薬食発 1120 第 5 号 平成 26 年 11 月 20 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医療機器の製造販売承認申請について 医療機器の製造販売承認申請の取扱いについては 医療機器の製造販売承認申請について ( 平成 17 年 2 月 16 日付け薬食発第 0216002 号厚生労働省医薬食品局長通知 以下 旧通知 という ) 等により実施してきたところです 先般
本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シ
 医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
員長及び医薬品医療機器等法登録認証機関協議会代表幹事宛て送付するこ ととしていることを申し添えます 記 1. 基本要件基準第 13 条第 5 項及び第 6 項への適合性確認の基本的な考え方について (1)2023 年 ( 平成 35 年 )2 月 28 日 ( 以下 経過措置期間終了日 という )
 薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
Microsoft Word - 奈良県GQP-GVPガイドライン doc
 Ⅴ. 製造業者等との取決め - 67 - 1. はじめに製造業者等との取決めは GQP 省令 ( 平成 16 年 9 月 22 日厚生労働省令第 136 号 ) の第 7 条に基づき 製造業者等における医薬品の製造管理及び品質管理の適正かつ円滑な実施を確保するため 製造販売業者が製造業者等に製造委託する製品に関し 必要な事項を取り決めるものである 2. 取決め対象取決めを行う 製造業者等 とは 製造販売承認書の製造方法欄に記載された以下の者である
Ⅴ. 製造業者等との取決め - 67 - 1. はじめに製造業者等との取決めは GQP 省令 ( 平成 16 年 9 月 22 日厚生労働省令第 136 号 ) の第 7 条に基づき 製造業者等における医薬品の製造管理及び品質管理の適正かつ円滑な実施を確保するため 製造販売業者が製造業者等に製造委託する製品に関し 必要な事項を取り決めるものである 2. 取決め対象取決めを行う 製造業者等 とは 製造販売承認書の製造方法欄に記載された以下の者である
化粧品製造販売届入力方法等.pptx
 1 2 3 4 5 6 提出先 : 大阪府を選択この項目は再読み込みをする場合 その都度消えますので その都度選択して下さい また 知事名をデータベースメンテナンスで変更した時は 一度この欄を空白にして TAG 内容を更新 ( 完了ボタンを押す ) して 再度大阪府を選択すると変更しないと鑑の知事名は変更されません 提出年月日 : 旧バージョンのソフトでは元号に 昭和 が選択可能です 昭和 を選択した場合
1 2 3 4 5 6 提出先 : 大阪府を選択この項目は再読み込みをする場合 その都度消えますので その都度選択して下さい また 知事名をデータベースメンテナンスで変更した時は 一度この欄を空白にして TAG 内容を更新 ( 完了ボタンを押す ) して 再度大阪府を選択すると変更しないと鑑の知事名は変更されません 提出年月日 : 旧バージョンのソフトでは元号に 昭和 が選択可能です 昭和 を選択した場合
写 薬生発 0131 第 1 号 平成 30 年 1 月 31 日 都道府県知事 殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 関係手数料令の一部を改正する政令の公布について この度 医薬品 医療機器等の品質 有効性及び安全性の確
 薬生発 0131 第 3 号 平成 30 年 1 月 31 日 独立行政法人医薬品医療機器総合機構理事長殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 関係手数料令の一部を改正する政令の公布について 標記につきまして 別添写しのとおり都道府県知事宛てに通知しましたので お 知らせいたします 写 薬生発 0131 第 1 号 平成 30
薬生発 0131 第 3 号 平成 30 年 1 月 31 日 独立行政法人医薬品医療機器総合機構理事長殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 関係手数料令の一部を改正する政令の公布について 標記につきまして 別添写しのとおり都道府県知事宛てに通知しましたので お 知らせいたします 写 薬生発 0131 第 1 号 平成 30
Ⅲ-3 試用医薬品に関する基準 平成 10 年 1 月 20 日公正取引委員会届出改定平成 13 年 3 月 19 日公正取引委員会届出改定平成 16 年 5 月 25 日公正取引委員会届出改定平成 17 年 3 月 29 日公正取引委員会届出改定平成 26 年 6 月 16 日公正取引委員会 消費
 Ⅲ-3 試用医薬品に関する基準 平成 10 年 1 月 20 日公正取引委員会届出改定平成 13 年 3 月 19 日公正取引委員会届出改定平成 16 年 5 月 25 日公正取引委員会届出改定平成 17 年 3 月 29 日公正取引委員会届出改定平成 26 年 6 月 16 日公正取引委員会 消費者庁長官届出 本基準は規約第 5 条第 3 号 施行規則第 2 条 ( 試用医薬品提供基準 ) に基づくものである
Ⅲ-3 試用医薬品に関する基準 平成 10 年 1 月 20 日公正取引委員会届出改定平成 13 年 3 月 19 日公正取引委員会届出改定平成 16 年 5 月 25 日公正取引委員会届出改定平成 17 年 3 月 29 日公正取引委員会届出改定平成 26 年 6 月 16 日公正取引委員会 消費者庁長官届出 本基準は規約第 5 条第 3 号 施行規則第 2 条 ( 試用医薬品提供基準 ) に基づくものである
通知(一括更新手続き)
 薬食審査発 0330 第 6 号 平成 27 年 3 月 30 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) 化粧品製造販売届書の届出先の都道府県が変更になる場合等の取扱いについて 化粧品製造販売届書の取扱いについては 改正薬事法の施行に伴う製造販売の承認を要しない医薬品等の取扱い等について ( 平成 17 年 3 月 31 日付け薬食審査発第 0331015
薬食審査発 0330 第 6 号 平成 27 年 3 月 30 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) 化粧品製造販売届書の届出先の都道府県が変更になる場合等の取扱いについて 化粧品製造販売届書の取扱いについては 改正薬事法の施行に伴う製造販売の承認を要しない医薬品等の取扱い等について ( 平成 17 年 3 月 31 日付け薬食審査発第 0331015
薬食審査発 0318 第 1 号薬食監麻発 0318 第 6 号平成 22 年 3 月 18 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 厚生労働省医薬食品局監視指導 麻薬対策課長 改正法施行に伴う経過措置等終了にあたっての対応について 薬事法及び採血及び供血あつせ
 薬食審査発 0318 第 1 号薬食監麻発 0318 第 6 号平成 22 年 3 月 18 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 厚生労働省医薬食品局監視指導 麻薬対策課長 改正法施行に伴う経過措置等終了にあたっての対応について 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 9 6 号 以下 改正法 という ) の施行及び改正法による改正後の薬事法
薬食審査発 0318 第 1 号薬食監麻発 0318 第 6 号平成 22 年 3 月 18 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 厚生労働省医薬食品局監視指導 麻薬対策課長 改正法施行に伴う経過措置等終了にあたっての対応について 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 9 6 号 以下 改正法 という ) の施行及び改正法による改正後の薬事法
<4D F736F F D F985E A E397C38B408AED C90BF B F816A82C98AD682B782E98EBF8B5E899E939A8F572E646F63>
 医療機器 WEB 申請プラットフォーム (DWAP) に関する質疑応答集 (Q&A) Ver.8 < 目次 > 頁 1. 全体的事項 2 2.ID パスワードについて 4 3. 提出日等について 6 4. 仮受付 本受付について 7 5. 業者情報登録について 8 6. 入力文字について 8 7. ローカル保存 データ読み込みについて 9 8. 一時保存について 9 9. 申請書等の鑑について 10
医療機器 WEB 申請プラットフォーム (DWAP) に関する質疑応答集 (Q&A) Ver.8 < 目次 > 頁 1. 全体的事項 2 2.ID パスワードについて 4 3. 提出日等について 6 4. 仮受付 本受付について 7 5. 業者情報登録について 8 6. 入力文字について 8 7. ローカル保存 データ読み込みについて 9 8. 一時保存について 9 9. 申請書等の鑑について 10
バリデーション基準 1. 医薬品 医薬部外品 GMP 省令に規定するバリデーションについては 品質リスクを考慮し 以下の バリデーション基準 に基づいて実施すること 2. バリデーション基準 (1) バリデーションの目的バリデーションは 製造所の構造設備並びに手順 工程その他の製造管理及び品質管理の
 バリデーション基準 1. 医薬品 医薬部外品 GMP 省令に規定するバリデーションについては 品質リスクを考慮し 以下の バリデーション基準 に基づいて実施すること 2. バリデーション基準 (1) バリデーションの目的バリデーションは 製造所の構造設備並びに手順 工程その他の製造管理及び品質管理の方法 ( 以下この基準において 製造手順等 という ) が期待される結果を与えることを検証し これを文書とすることによって
バリデーション基準 1. 医薬品 医薬部外品 GMP 省令に規定するバリデーションについては 品質リスクを考慮し 以下の バリデーション基準 に基づいて実施すること 2. バリデーション基準 (1) バリデーションの目的バリデーションは 製造所の構造設備並びに手順 工程その他の製造管理及び品質管理の方法 ( 以下この基準において 製造手順等 という ) が期待される結果を与えることを検証し これを文書とすることによって
3. 実施時期平成 29 年 4 月 3 日より本件改修後のQMS 調査申請書の作成及び機構受付が可能となります 4. その他 本改修により承認申請書とQMS 調査申請書の同時申請が可能となるのは 両申請書をDW APで作成した場合に限ります (FD 申請ソフトによる申請の場合は同時申請できません
 事務連絡平成 29 年 3 月 17 日 一般社団法人日本医療機器産業連合会御中 独立行政法人医薬品医療機器総合機構審査業務部 承認申請書及び QMS 調査申請書の同時申請にかかる DWAP の改修について 今般 医療機器 WEB 申請プラットフォーム ( 以下 DWAP という ) を活用した医療機器製造販売承認申請書又は外国製造医療機器製造販売承認申請書 ( 一部変更承認申請書を含む 以下 承認申請書
事務連絡平成 29 年 3 月 17 日 一般社団法人日本医療機器産業連合会御中 独立行政法人医薬品医療機器総合機構審査業務部 承認申請書及び QMS 調査申請書の同時申請にかかる DWAP の改修について 今般 医療機器 WEB 申請プラットフォーム ( 以下 DWAP という ) を活用した医療機器製造販売承認申請書又は外国製造医療機器製造販売承認申請書 ( 一部変更承認申請書を含む 以下 承認申請書
Microsoft Word - 【案1】登録認証機関立入要領改正通知(Ver )
 薬食機参発 1121 第 38 号平成 26 年 11 月 21 日 各登録認証機関の長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) 登録認証機関等に対する立入検査の実施要領の改正について 薬事法 ( 昭和 35 年法律第 145 号 ) の規定による登録認証機関等に対する立入 検査の実施要領については 登録認証機関等に対する立入検査の実施要領について ( 平成 18
薬食機参発 1121 第 38 号平成 26 年 11 月 21 日 各登録認証機関の長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) 登録認証機関等に対する立入検査の実施要領の改正について 薬事法 ( 昭和 35 年法律第 145 号 ) の規定による登録認証機関等に対する立入 検査の実施要領については 登録認証機関等に対する立入検査の実施要領について ( 平成 18
<4D F736F F D208CE394AD88E396F C98C5782E E DEC90AC8EE888F882AB82C691E E >
 後発医薬品に係る CTD 第 1 部 ( モジュール 1) 作成の手引き及び CTD 第 2 部 ( モジュール 2) 記載例 ( モックアップ ) に関する質疑応答集 (Q&A) 平成 27 年 8 月に日本ジェネリック製薬協会では 後発医薬品の CTD 形式での申請資料のレベルを一定にすること及び審査において非効率な照会を避け本質的な議論を進めることができるように CTD 第 1 部作成の手引き及び第
後発医薬品に係る CTD 第 1 部 ( モジュール 1) 作成の手引き及び CTD 第 2 部 ( モジュール 2) 記載例 ( モックアップ ) に関する質疑応答集 (Q&A) 平成 27 年 8 月に日本ジェネリック製薬協会では 後発医薬品の CTD 形式での申請資料のレベルを一定にすること及び審査において非効率な照会を避け本質的な議論を進めることができるように CTD 第 1 部作成の手引き及び第
15 変更管理
 ISO22716 の要求事項 (15. 変更管理 ) 15 変更管理 (Change control) 製品の品質に影響を及ぼす可能性のある変更 十分なデータに基づいて権限所有者が承認 変更管理及び内部監査 2 1 製品の品質に影響を及ぼす可能性のある変更 化粧品等の品質 有効性及び安全性に影響を及ぼすと考えられる原料 包装材料 製造 包装手順 構造設備 規格 試験方法の変更 1) 成分 分量の変更
ISO22716 の要求事項 (15. 変更管理 ) 15 変更管理 (Change control) 製品の品質に影響を及ぼす可能性のある変更 十分なデータに基づいて権限所有者が承認 変更管理及び内部監査 2 1 製品の品質に影響を及ぼす可能性のある変更 化粧品等の品質 有効性及び安全性に影響を及ぼすと考えられる原料 包装材料 製造 包装手順 構造設備 規格 試験方法の変更 1) 成分 分量の変更
youkou
 生食用食肉の安全確保に関する取扱要綱 第 1 目的この要綱は 食品 添加物等の規格基準 ( 昭和 34 年 12 月 28 日厚生省告示第 370 号 以下 規格基準 という )D 各条の食肉及び鯨肉の目名中の生食用食肉の取扱い並びに食品衛生法第 19 条第 1 項の規定に基づく表示の基準に関する内閣府令 ( 平成 23 年内閣府令第 45 号 ) に規定する牛の食肉であって生食用のものの表示の取扱いついて
生食用食肉の安全確保に関する取扱要綱 第 1 目的この要綱は 食品 添加物等の規格基準 ( 昭和 34 年 12 月 28 日厚生省告示第 370 号 以下 規格基準 という )D 各条の食肉及び鯨肉の目名中の生食用食肉の取扱い並びに食品衛生法第 19 条第 1 項の規定に基づく表示の基準に関する内閣府令 ( 平成 23 年内閣府令第 45 号 ) に規定する牛の食肉であって生食用のものの表示の取扱いついて
03-01【局長通知・特例】施術管理者の要件に係る取扱の特例について
 保発 0116 第 3 号 平成 30 年 1 月 16 日 都道府県知事 地方厚生 ( 支 ) 局長 殿 厚生労働省保険局長 ( 公印省略 ) 柔道整復師の施術に係る療養費の受領委任を取扱う 施術管理者の要件の特例について 柔道整復師の施術に係る療養費の受領委任を取扱う施術管理者の要件に係る取扱は 柔道整復師の施術に係る療養費について ( 平成 22 年 5 月 24 日付け保発 0524 第 2
保発 0116 第 3 号 平成 30 年 1 月 16 日 都道府県知事 地方厚生 ( 支 ) 局長 殿 厚生労働省保険局長 ( 公印省略 ) 柔道整復師の施術に係る療養費の受領委任を取扱う 施術管理者の要件の特例について 柔道整復師の施術に係る療養費の受領委任を取扱う施術管理者の要件に係る取扱は 柔道整復師の施術に係る療養費について ( 平成 22 年 5 月 24 日付け保発 0524 第 2
Microsoft Word - 奈良県GQP-GVPガイドライン doc
 三. 安全確保措置の実施に関する手順 1. 目的安全確保措置の実施に関する手順の目的を記載する < 記載例 > 本手順は GVP 省令の第 9 条に基づき 安全確保措置の実施を適正かつ円滑に行うために必要な手順を定めるものである 2. 適用範囲安全確保措置の実施に関する手順の適用範囲を記載する < 記載例 > 本手順書は 二. 安全管理情報の検討及びその結果に基づく安全確保措置の立案に関する手順 で立案された安全確保措置の決定
三. 安全確保措置の実施に関する手順 1. 目的安全確保措置の実施に関する手順の目的を記載する < 記載例 > 本手順は GVP 省令の第 9 条に基づき 安全確保措置の実施を適正かつ円滑に行うために必要な手順を定めるものである 2. 適用範囲安全確保措置の実施に関する手順の適用範囲を記載する < 記載例 > 本手順書は 二. 安全管理情報の検討及びその結果に基づく安全確保措置の立案に関する手順 で立案された安全確保措置の決定
< F2D819B955C8EA692CA926D DC58F4994AD8F6F>
 薬食監麻発第 0331008 号平成 17 年 3 月 31 日 各都道府県衛生主管部 ( 局 ) 長 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 一部改正法 という ) 第 2 条の規定による改正後の薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 及び関係政省令等の規定に基づく医薬品 医薬部外品 化粧品及び医療機器 (
薬食監麻発第 0331008 号平成 17 年 3 月 31 日 各都道府県衛生主管部 ( 局 ) 長 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 一部改正法 という ) 第 2 条の規定による改正後の薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 及び関係政省令等の規定に基づく医薬品 医薬部外品 化粧品及び医療機器 (
Basic Agreement for Marketing Certification Service under PMD Act / 医薬品医療機器法製造販売認証サービス基本合意書
 医薬品医療機器法に基づく製造販売認証サービスを申請されるにあたりご了解いただきたいこと テュフズードジャパン株式会社 MHS 事業部 弊社では 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 以下 医薬品医療機器法又は法 ) に基づく製造販売認証サービスを提供させていただくにあたり 次の各項についてご了解いただくよう全てのお客様にお願いしております 最初のご申請までにこの書面をお読みいただき最終ページに貴社の名称
医薬品医療機器法に基づく製造販売認証サービスを申請されるにあたりご了解いただきたいこと テュフズードジャパン株式会社 MHS 事業部 弊社では 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 以下 医薬品医療機器法又は法 ) に基づく製造販売認証サービスを提供させていただくにあたり 次の各項についてご了解いただくよう全てのお客様にお願いしております 最初のご申請までにこの書面をお読みいただき最終ページに貴社の名称
<4D F736F F D F28DDC8E7489EF90E096BE8E9197BF5F2E646F63>
 平成 25 年 4 月 20 日福岡市保健福祉局健康医療部地域医療課 薬事法改正に伴う権限移譲について ( 権限が移譲された事務について ) 平成 25 年 4 月 1 日から 地域の自主性及び自立性を高めるための改革の推進を図るための関係法律の整備に関する法律 により改正された 薬事法 が施行され 都道府県知事が処理することとされていた事務の一部が保健所設置市の市長に移譲されました 1 福岡県から移譲された事務について
平成 25 年 4 月 20 日福岡市保健福祉局健康医療部地域医療課 薬事法改正に伴う権限移譲について ( 権限が移譲された事務について ) 平成 25 年 4 月 1 日から 地域の自主性及び自立性を高めるための改革の推進を図るための関係法律の整備に関する法律 により改正された 薬事法 が施行され 都道府県知事が処理することとされていた事務の一部が保健所設置市の市長に移譲されました 1 福岡県から移譲された事務について
00 事務連絡案
 事務連絡 平成 30 年 10 月 30 日 都道府県知事 各保健所設置市 特別区 衛生検査所業務担当部 ( 局 ) 御中 厚生労働省医政局地域医療計画課 医療関連サービス室 衛生検査所において新たに作成する標準作業書及び台帳の参考例について 医療法等の一部を改正する法律 ( 平成 29 年法律第 57 号 以下 改正法 という ) の一部の規定が平成 30 年 12 月 1 日に施行されることに伴い
事務連絡 平成 30 年 10 月 30 日 都道府県知事 各保健所設置市 特別区 衛生検査所業務担当部 ( 局 ) 御中 厚生労働省医政局地域医療計画課 医療関連サービス室 衛生検査所において新たに作成する標準作業書及び台帳の参考例について 医療法等の一部を改正する法律 ( 平成 29 年法律第 57 号 以下 改正法 という ) の一部の規定が平成 30 年 12 月 1 日に施行されることに伴い
別紙 1 販売名 医療機器保険適用希望書 ( 決定区分 A1( 包括 )) 整理番号 : 空欄で提出 薬事法承認又は認証された販売名を記載 製品名 製品コード 製品名 製品コード JAN コードの場合必ず 13 桁 薬事法承認書又は認証書上 薬事法承認書又は認証書上記載 記載された類別を記載 された
 事務連絡 平成 24 年 3 月 19 日 日本医療機器産業連合会会長 米国医療機器 IVD 工業会会長 欧州ビジネス協会医療機器委員会委員長 殿 厚生労働省医政局経済課医療機器政策室 医療機器保険適用希望書の記載例等について 平素より 厚生労働行政にご協力いただきありがとうございます 医療機器保険適用希望書の提出に関連した通知として 医療機器の保険適用等に関する取扱いについて ( 平成 24 年
事務連絡 平成 24 年 3 月 19 日 日本医療機器産業連合会会長 米国医療機器 IVD 工業会会長 欧州ビジネス協会医療機器委員会委員長 殿 厚生労働省医政局経済課医療機器政策室 医療機器保険適用希望書の記載例等について 平素より 厚生労働行政にご協力いただきありがとうございます 医療機器保険適用希望書の提出に関連した通知として 医療機器の保険適用等に関する取扱いについて ( 平成 24 年
<4D F736F F D2088E396F295698BC691D D836A B816988F38DFC A2E646F63>
 医薬品の製造販売業製造販売業 製造業製造業について 医薬品の定義定義 ( 薬事法第 2 条第 1 項 ) 医薬品とは 以下のようなものをいいます 1 号 : 日本薬局方に収められている物 2 号 : 人又は動物の疾病の診断 治療又は予防に使用されることが目的とされている物であつて 機械器具 歯科材料 医療用品及び衛生用品 ( 以下 機械器具等 という ) でないもの ( 医薬部外品を除きます ) 3
医薬品の製造販売業製造販売業 製造業製造業について 医薬品の定義定義 ( 薬事法第 2 条第 1 項 ) 医薬品とは 以下のようなものをいいます 1 号 : 日本薬局方に収められている物 2 号 : 人又は動物の疾病の診断 治療又は予防に使用されることが目的とされている物であつて 機械器具 歯科材料 医療用品及び衛生用品 ( 以下 機械器具等 という ) でないもの ( 医薬部外品を除きます ) 3
改正後
 改正後第 2 章関税の確定 納付 徴収及び還付 第 2 節申告納税方式による関税の確定 新旧対照表 関税法基本通達( 昭和 47 年 3 月 1 日蔵関第 100 号 ) ( 注 ) 下線を付した箇所が改正部分である 改正前第 2 章関税の確定 納付 徴収及び還付第 2 節申告納税方式による関税の確定 7 の 2-8 令第 4 条の 5 第 5 項の規定に基づく特例輸入者の承認内容の変更の届出は 特例輸入者等承認
改正後第 2 章関税の確定 納付 徴収及び還付 第 2 節申告納税方式による関税の確定 新旧対照表 関税法基本通達( 昭和 47 年 3 月 1 日蔵関第 100 号 ) ( 注 ) 下線を付した箇所が改正部分である 改正前第 2 章関税の確定 納付 徴収及び還付第 2 節申告納税方式による関税の確定 7 の 2-8 令第 4 条の 5 第 5 項の規定に基づく特例輸入者の承認内容の変更の届出は 特例輸入者等承認
H 平成 28 年青森県登録販売者試験について 1 概要出願者 612 名受験者 592 名合格者 277 名合格率 46.8%( 四捨五入 ) 2 合格基準総得点の7 割であって かつ 各項目の得点が4 割以上 3 試験成績 手引き第 1 章 手引き第 2 章 手引き第 3 章 手引
 H28.10.3 平成 28 年青森県登録販売者試験について 1 概要出願者 612 名受験者 592 名合格者 277 名合格率 46.8%( 四捨五入 ) 2 合格基準総得点の7 割であって かつ 各項目の得点が4 割以上 3 試験成績 手引き第 1 章 手引き第 2 章 手引き第 3 章 手引き第 4 章 手引き第 5 章 総得点 (40 点 ) (120 点 ) 最高得点 20 20 40
H28.10.3 平成 28 年青森県登録販売者試験について 1 概要出願者 612 名受験者 592 名合格者 277 名合格率 46.8%( 四捨五入 ) 2 合格基準総得点の7 割であって かつ 各項目の得点が4 割以上 3 試験成績 手引き第 1 章 手引き第 2 章 手引き第 3 章 手引き第 4 章 手引き第 5 章 総得点 (40 点 ) (120 点 ) 最高得点 20 20 40
GVPの基礎
 京都府健康福祉部薬務課 平成 29 年 3 月 8 日 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令 (GVP 省令 ) GVP 省令 第一章 ( 総則 ) 第二章 ( 第一種製販の製造販売後安全管理の基準 ) 第三章 ( 第二種製販の製造販売後安全管理の基準 ) 第四章 ( 第三種製販の製造販売後安全管理の基準 ) 第五章 ( 雑則 ) 第一種 ~
京都府健康福祉部薬務課 平成 29 年 3 月 8 日 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令 (GVP 省令 ) GVP 省令 第一章 ( 総則 ) 第二章 ( 第一種製販の製造販売後安全管理の基準 ) 第三章 ( 第二種製販の製造販売後安全管理の基準 ) 第四章 ( 第三種製販の製造販売後安全管理の基準 ) 第五章 ( 雑則 ) 第一種 ~
< F2D816992CA926D342E A947A8BF48ED282A982E782CC965C>
 庁保険発第 0425001 号平成 20 年 4 月 25 日 地方社会保険事務局長 殿 社会保険庁運営部医療保険課長 ( 公印省略 ) 配偶者からの暴力を受けた被扶養者の取扱い等について 標記については 平成 20 年 1 月 11 日付けで告示された 配偶者からの暴力の防止及び被害者の保護のための施策に関する基本的な方針 ( 平成 20 年内閣府 国家公安委員会 法務省 厚生労働省告示第 1 号
庁保険発第 0425001 号平成 20 年 4 月 25 日 地方社会保険事務局長 殿 社会保険庁運営部医療保険課長 ( 公印省略 ) 配偶者からの暴力を受けた被扶養者の取扱い等について 標記については 平成 20 年 1 月 11 日付けで告示された 配偶者からの暴力の防止及び被害者の保護のための施策に関する基本的な方針 ( 平成 20 年内閣府 国家公安委員会 法務省 厚生労働省告示第 1 号
2 有効成分名 添付文書及び審査報告書に基づき記載する 3 品目名 ( 後発医薬品 ) 添付文書及び審査報告書のほか薬価基準収載品目リストにより記載する 複数の品目がある場合は 個別医薬品コード (YJ コード ) 順に番号を振り 記載する ( 複数規格があっても 全規格まとめて YJ コード順とす
 第 18 回ジェネリック医薬品品質情報検討会 参考資料 2 医療用医薬品最新品質情報集 ( ブルーブック ) 作成要領 ( 案 ) 1 対象品目 別途定めるブルーブック作成対象品目に基づく なお 薬価削除経過措置期間中のものは記載対象外とする 2 記載項目 1 作成年月日 2 有効成分名 3 品目名 ( 後発医薬品 ) 4 品目名 ( 先発医薬品 ) 5 効能 効果 6 用法 用量 7 添加物 8
第 18 回ジェネリック医薬品品質情報検討会 参考資料 2 医療用医薬品最新品質情報集 ( ブルーブック ) 作成要領 ( 案 ) 1 対象品目 別途定めるブルーブック作成対象品目に基づく なお 薬価削除経過措置期間中のものは記載対象外とする 2 記載項目 1 作成年月日 2 有効成分名 3 品目名 ( 後発医薬品 ) 4 品目名 ( 先発医薬品 ) 5 効能 効果 6 用法 用量 7 添加物 8
Microsoft Word _正当理由通知(薬局医薬品) (反映)
 薬食発 0318 第 4 号 平成 26 年 3 月 18 日 都道府県知事 各保健所設置市長殿 特別区長 厚生労働省医薬食品局長 ( 公印省略 ) 薬局医薬品の取扱いについて 薬事法及び薬剤師法の一部を改正する法律 ( 平成 25 年法律第 103 号 以下 改正法 という ) については 薬事法及び薬剤師法の一部を改正する法律の施行期日を定める政令 ( 平成 26 年政令第 24 号 ) により
薬食発 0318 第 4 号 平成 26 年 3 月 18 日 都道府県知事 各保健所設置市長殿 特別区長 厚生労働省医薬食品局長 ( 公印省略 ) 薬局医薬品の取扱いについて 薬事法及び薬剤師法の一部を改正する法律 ( 平成 25 年法律第 103 号 以下 改正法 という ) については 薬事法及び薬剤師法の一部を改正する法律の施行期日を定める政令 ( 平成 26 年政令第 24 号 ) により
財営第 号
 静岡県発注建設工事における社会保険等加入対応マニュアル 1 下請契約における社会保険等未加入建設業者の確認等発注者は 受注者から提出された施工体制台帳及び再下請負通知書に記載された全ての建設業者 ( 建設業法 ( 昭和 24 年法律第 100 号 ) 第 2 条第 3 項に定める建設業者 以下同じ ) について 健康保険 厚生年金保険及び雇用保険 ( 以下 社会保険等 という ) 未加入者 ( 以下に定める届出の義務を履行していない者
静岡県発注建設工事における社会保険等加入対応マニュアル 1 下請契約における社会保険等未加入建設業者の確認等発注者は 受注者から提出された施工体制台帳及び再下請負通知書に記載された全ての建設業者 ( 建設業法 ( 昭和 24 年法律第 100 号 ) 第 2 条第 3 項に定める建設業者 以下同じ ) について 健康保険 厚生年金保険及び雇用保険 ( 以下 社会保険等 という ) 未加入者 ( 以下に定める届出の義務を履行していない者
PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1
 薬生発 07 31 第 4 号 平成 29 年 7 月 31 日 各都道府県知事殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則の一部を改正する省令 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令の一部を改正する省令 及び 医療機器の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令
薬生発 07 31 第 4 号 平成 29 年 7 月 31 日 各都道府県知事殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則の一部を改正する省令 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令の一部を改正する省令 及び 医療機器の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令
2005年版GQP事例集最終
 GQP 事例集 1. 第 3 条 ( 品質管理業務に係る組織及び職員 ) 関係 問 Q3-01 第 4 号の その他品質管理業務に関係する部門 とは どのような部門が想定されるか 答 品質管理業務は 品質保証部門 だけで行うものでなく 製造販売業におけるすべての品質管理に関連する業務を含むものである 例えば購買 設計 品質等に関する情報及び品質不良等の処理 回収処理その他製品の品質の管理に必要な業務を行う部門を指す
GQP 事例集 1. 第 3 条 ( 品質管理業務に係る組織及び職員 ) 関係 問 Q3-01 第 4 号の その他品質管理業務に関係する部門 とは どのような部門が想定されるか 答 品質管理業務は 品質保証部門 だけで行うものでなく 製造販売業におけるすべての品質管理に関連する業務を含むものである 例えば購買 設計 品質等に関する情報及び品質不良等の処理 回収処理その他製品の品質の管理に必要な業務を行う部門を指す
特別の事情 が認められる場合( 2) 特殊な技術 機器又は設備等 ( 以下 特殊技術等 という ) を必要とする工事で 特殊技術等を有する者と下請契約を締結しなければ契約の目的を達することができないことや その下請業者でなければ目的を達することが困難となることが明らかな場合 特別の事情 に該当しない
 社会保険等未加入対策に係る契約約款の改正について 平成 30 年 10 月 1 日以降 入札公告又は指名通知等 ( 随意契約を含む ) を行う工事のうち 下請総額が3,000 万円 ( 建築一式工事は4,500 万円 ) 以上の工事について 一次下請業者は原則社会保険等加入業者に限定することに伴い 以下のとおり契約約款の条項を追加することとしますのでお知らせします 1 工事請負契約書の追加条項 (
社会保険等未加入対策に係る契約約款の改正について 平成 30 年 10 月 1 日以降 入札公告又は指名通知等 ( 随意契約を含む ) を行う工事のうち 下請総額が3,000 万円 ( 建築一式工事は4,500 万円 ) 以上の工事について 一次下請業者は原則社会保険等加入業者に限定することに伴い 以下のとおり契約約款の条項を追加することとしますのでお知らせします 1 工事請負契約書の追加条項 (
法律 出典 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年 8 月 10 日法律第 145 号 ) 政令 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行令 ( 昭和 36 年 1 月 26 日政令第 11 号 ) 省令 医薬品 医療機器等の品質
 医療機器クラス分類表 ( 平成 30 年 10 月 19 日現在 ) 香川県健康福祉部薬務感染症対策課薬事指導グループ 法律 出典 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年 8 月 10 日法律第 145 号 ) 政令 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行令 ( 昭和 36 年 1 月 26 日政令第 11 号 ) 省令 医薬品
医療機器クラス分類表 ( 平成 30 年 10 月 19 日現在 ) 香川県健康福祉部薬務感染症対策課薬事指導グループ 法律 出典 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年 8 月 10 日法律第 145 号 ) 政令 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行令 ( 昭和 36 年 1 月 26 日政令第 11 号 ) 省令 医薬品
別添 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について < 半年ごとの定期報告の受け付け> Q1 平成 26 年 6 月 30 日までの間は 治験依頼者 ( 自ら治験を実施する者を除く ) が提出する副作用等症例の定期報告は なお従前の例によることができる とあるが 平成 26 年
 事務連絡 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局審査管理課 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 第 273 条第 3 項に基づく治験副作用等定期報告については 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について ( 平成 24 年
事務連絡 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局審査管理課 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 第 273 条第 3 項に基づく治験副作用等定期報告については 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について ( 平成 24 年
ア事業担当課長 ( 岐阜市上下水道事業部契約規程 ( 昭和 41 年水道部管理規程第 3 号 ) 第 4 条に規定する部長 ) は 工事請負契約約款第 7 条の2 第 2 項の規定に基づき 受注者に対して 期限を定め 当該下請契約を締結した具体的な理由を載した書面を求めるものとする ( 様式 1)
 建設業者の社会保険等未加入対策について 第 1 状況近年のダンピング受注による下請業者へのしわ寄せが 労働者の賃金水準の低下や社会保険等への未加入といった処遇悪化を招き 産業の継続に不可欠な若年者層の確保に大きな支障となっている 建設工事には 元来 健康保険料や厚生年金保険料など企業が負担すべき法定福利費が 現場管理費 として計上されている しかし いまだに医療保険 年金 雇用保険制度に未加入の企業が存在しており
建設業者の社会保険等未加入対策について 第 1 状況近年のダンピング受注による下請業者へのしわ寄せが 労働者の賃金水準の低下や社会保険等への未加入といった処遇悪化を招き 産業の継続に不可欠な若年者層の確保に大きな支障となっている 建設工事には 元来 健康保険料や厚生年金保険料など企業が負担すべき法定福利費が 現場管理費 として計上されている しかし いまだに医療保険 年金 雇用保険制度に未加入の企業が存在しており
MF 登録申請書類申請前チェックリスト 1 ( 原薬等登録原簿登録申請書 ( 新規登録申請 ) の例 ) 2015/10/1 追記及び補 を った箇所については 字とした 様式 様式の別を す記号 : H01( 原薬等登録原簿登録申請書 ) 提出先 提出先の別 : 3( 総合機構 ) 提出年 申請書
 MF 販売名 MF 有効成分名 平成 年 月 日 MF 登録者 MF 登録申請書類申請前チェックリスト 1 全体 2015/10/1 追記及び補足を行った箇所については 赤字とした レ点チェック 〇申請ソフトのサポートは 申請ソフトヘルプデスク (FAX:03-3507-0114 E-mail:fd_iyaku@pmda.go.jp) へご質問ください TEL での対応は行っておりませんので ご了承ください
MF 販売名 MF 有効成分名 平成 年 月 日 MF 登録者 MF 登録申請書類申請前チェックリスト 1 全体 2015/10/1 追記及び補足を行った箇所については 赤字とした レ点チェック 〇申請ソフトのサポートは 申請ソフトヘルプデスク (FAX:03-3507-0114 E-mail:fd_iyaku@pmda.go.jp) へご質問ください TEL での対応は行っておりませんので ご了承ください
一について第一に 感染症の予防及び感染症の患者に対する医療に関する法律(平成十年法律第百十四号 以下 感染症法 という )第十二条の規定に基づき 後天性免疫不全症候群(以下 エイズという )の患者及びその病原体を保有している者であって無症状のもの(以下 HIV感染者 という )(以下 エイズの患者等
 平成十一年八月十日受領答弁第三七号衆議院議員家西悟君提出血液製剤による感染被害の救済に関する質問に対し 別紙答弁書を送付する 内閣衆質一四五第三七号平成十一年八月十日衆議院議長伊宗一郎殿内閣総理大臣小渕恵三 一について第一に 感染症の予防及び感染症の患者に対する医療に関する法律(平成十年法律第百十四号 以下 感染症法 という )第十二条の規定に基づき 後天性免疫不全症候群(以下 エイズという )の患者及びその病原体を保有している者であって無症状のもの(以下
平成十一年八月十日受領答弁第三七号衆議院議員家西悟君提出血液製剤による感染被害の救済に関する質問に対し 別紙答弁書を送付する 内閣衆質一四五第三七号平成十一年八月十日衆議院議長伊宗一郎殿内閣総理大臣小渕恵三 一について第一に 感染症の予防及び感染症の患者に対する医療に関する法律(平成十年法律第百十四号 以下 感染症法 という )第十二条の規定に基づき 後天性免疫不全症候群(以下 エイズという )の患者及びその病原体を保有している者であって無症状のもの(以下
医療用医薬品最新品質情報集 ( ブルーブック ) 初版有効成分ベンフォチアミン B6 B12 配合剤 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 1) 溶解度 1 ダイメジンスリービー配合カプセル
 医療用医薬品最新品質情報集 ( ブルーブック ) 2018.2.23 初版有効成分ベンフォチアミン B6 B12 配合剤 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 1) 溶解度 1 ダイメジンスリービー配合カプセル25 日医工 2 シグマビタン配合カプセルB25 東和薬品 1 ビタメジン配合カプセルB25 第一三共
医療用医薬品最新品質情報集 ( ブルーブック ) 2018.2.23 初版有効成分ベンフォチアミン B6 B12 配合剤 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 1) 溶解度 1 ダイメジンスリービー配合カプセル25 日医工 2 シグマビタン配合カプセルB25 東和薬品 1 ビタメジン配合カプセルB25 第一三共
医薬品説明会資料 ジェネリック (後発医薬品)
 17 2 12 13 GMP 14 GVP 2 日医工MPS2010 基本的なジェネリック発売までの流れ 製造販売元A社 管理 開発部門 製造部門 A社 管理 開発 販売部門 A社工場 製造指示 出荷 製造業者 Z 製造委託 承認 製造販売承認の申請 A社 営業部門 医療機関 卸売業者 厚生労働大臣 医薬品医療機器総合機構 9 Z社工場 基本的には 各社で製剤に関する研究 開発を行い 製造に関する申請書の提出
17 2 12 13 GMP 14 GVP 2 日医工MPS2010 基本的なジェネリック発売までの流れ 製造販売元A社 管理 開発部門 製造部門 A社 管理 開発 販売部門 A社工場 製造指示 出荷 製造業者 Z 製造委託 承認 製造販売承認の申請 A社 営業部門 医療機関 卸売業者 厚生労働大臣 医薬品医療機器総合機構 9 Z社工場 基本的には 各社で製剤に関する研究 開発を行い 製造に関する申請書の提出
PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1
 PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1 項第 1 号に定める医療機器リスク管理計画書をもって 承認申請資料のうち臨床試験の試験成績に関する資料又はこれに代替するものとして厚生労働大臣が認める資料の一部に代えることができることとしたこと
PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1 項第 1 号に定める医療機器リスク管理計画書をもって 承認申請資料のうち臨床試験の試験成績に関する資料又はこれに代替するものとして厚生労働大臣が認める資料の一部に代えることができることとしたこと
<4D F736F F D2090BB91A294CC94848CE392B28DB8905C90BF8E9E92F18F6F8F9197DE82A882E682D1928D88D38E968D E48DEC90AC816A
 申請時提出書類 ( 新規 ) 医薬品等の製造販売後調査実施依頼申請書 様式第 1 ( 以下 依頼書 ) 医薬品等の製造販売後調査実施申請書 様式第 2 ( 以下 申請書 ) 医薬品等の製造販売後調査実施に関する通知書 ( 病院用 依頼者用 ) 様式第 3 様式第 4 ( 以下 通知書 ) 医薬品等の製造販売後調査実施契約書 ( 病院用 依頼者用 ) 様式第 5 様式第 5の2 ( 以下 契約書 )
申請時提出書類 ( 新規 ) 医薬品等の製造販売後調査実施依頼申請書 様式第 1 ( 以下 依頼書 ) 医薬品等の製造販売後調査実施申請書 様式第 2 ( 以下 申請書 ) 医薬品等の製造販売後調査実施に関する通知書 ( 病院用 依頼者用 ) 様式第 3 様式第 4 ( 以下 通知書 ) 医薬品等の製造販売後調査実施契約書 ( 病院用 依頼者用 ) 様式第 5 様式第 5の2 ( 以下 契約書 )
医療用医薬品最新品質情報集 ( ブルーブック ) 初版 有効成分 ニカルジピン塩酸塩 品目名 ( 製造販売業者 ) 1 ニカルジピン塩酸塩徐放カプセル20mg 日医工 日医工 後発医薬品 2 ニカルジピン塩酸塩徐放カプセル40mg 日医工 日医工 品目名 ( 製造販売業者 )
 医療用医薬品最新品質情報集 ( ブルーブック ) 2018.10.25 初版 有効成分 ニカルジピン塩酸塩 品目名 ( 製造販売業者 ) 1 ニカルジピン塩酸塩徐放カプセル20mg 日医工 日医工 後発医薬品 2 ニカルジピン塩酸塩徐放カプセル40mg 日医工 日医工 品目名 ( 製造販売業者 ) 1 ペルジピンLAカプセル20mg アステラス製薬 先発医薬品 2 ペルジピンLAカプセル40mg アステラス製薬
医療用医薬品最新品質情報集 ( ブルーブック ) 2018.10.25 初版 有効成分 ニカルジピン塩酸塩 品目名 ( 製造販売業者 ) 1 ニカルジピン塩酸塩徐放カプセル20mg 日医工 日医工 後発医薬品 2 ニカルジピン塩酸塩徐放カプセル40mg 日医工 日医工 品目名 ( 製造販売業者 ) 1 ペルジピンLAカプセル20mg アステラス製薬 先発医薬品 2 ペルジピンLAカプセル40mg アステラス製薬
札幌市総合設計制度許可取扱要綱
 1 様式 ( 4 条関係 ) 長期優良住宅建築等計画に係る技術的審査適合証 ( 依頼者の氏名又は名称 ) ( 登録住宅性能評価機関名 ) 長期優良住宅建築等計画に係る技術的審査業務規程に基づき 長期優良住宅の普及の促進に関する法律 6 条 1 項の認定基準のうち 以下に掲げる基準に適合していることを証します 1 住宅の位置 2 住宅又は建築物の名称 3 住宅の建て方 4 工事種別 5 認定申請先の所管行政庁名奈良県
1 様式 ( 4 条関係 ) 長期優良住宅建築等計画に係る技術的審査適合証 ( 依頼者の氏名又は名称 ) ( 登録住宅性能評価機関名 ) 長期優良住宅建築等計画に係る技術的審査業務規程に基づき 長期優良住宅の普及の促進に関する法律 6 条 1 項の認定基準のうち 以下に掲げる基準に適合していることを証します 1 住宅の位置 2 住宅又は建築物の名称 3 住宅の建て方 4 工事種別 5 認定申請先の所管行政庁名奈良県
個人情報の取扱いに関する規則 平成 12 年 9 月 29 日 奈良県規則第 2 2 号 改正 平成 13 年 3 月 30 日 規則第 68 号 改正 平成 17 年 3 月 29 日 規則第 30 号 改正 平成 18 年 3 月 31 日 規則第 38 号 改正 平成 27 年 9 月 25
 個人情報の取扱いに関する規則 平成 12 年 9 月 29 日 奈良県規則第 2 2 号 改正 平成 13 年 3 月 30 日 規則第 68 号 改正 平成 17 年 3 月 29 日 規則第 30 号 改正 平成 18 年 3 月 31 日 規則第 38 号 改正 平成 27 年 9 月 25 日 規則第 19 号 ( 趣旨 ) 第 1 条この規則は 奈良県個人情報保護条例 ( 平成 12 年
個人情報の取扱いに関する規則 平成 12 年 9 月 29 日 奈良県規則第 2 2 号 改正 平成 13 年 3 月 30 日 規則第 68 号 改正 平成 17 年 3 月 29 日 規則第 30 号 改正 平成 18 年 3 月 31 日 規則第 38 号 改正 平成 27 年 9 月 25 日 規則第 19 号 ( 趣旨 ) 第 1 条この規則は 奈良県個人情報保護条例 ( 平成 12 年
ただし 受注者が下請業者と直接契約を締結 ( 以下 一次下請契約 という ) した請負代金の総額が3,000 万円 ( 建築一式工事の場合は4,500 万円 ) 以上の場合は 次のとおり取り扱うものとする ア主管部長 ( 岐阜市契約規則 ( 昭和 39 年規則第 7 号 ) 第 4 条に規定する部長
 建設業者の社会保険等未加入対策について 平成 27 年 3 月 31 日決裁 第 1 状況近年のダンピング受注による下請業者へのしわ寄せが 労働者の賃金水準の低下や社会保険等への未加入といった処遇悪化を招き 産業の継続に不可欠な若年者層の確保に大きな支障となっている 建設工事には 元来 健康保険料や厚生年金保険料など企業が負担すべき法定福利費が 現場管理費 として計上されている しかし いまだに医療保険
建設業者の社会保険等未加入対策について 平成 27 年 3 月 31 日決裁 第 1 状況近年のダンピング受注による下請業者へのしわ寄せが 労働者の賃金水準の低下や社会保険等への未加入といった処遇悪化を招き 産業の継続に不可欠な若年者層の確保に大きな支障となっている 建設工事には 元来 健康保険料や厚生年金保険料など企業が負担すべき法定福利費が 現場管理費 として計上されている しかし いまだに医療保険
(Microsoft PowerPoint - \202S\214\216\212\372\220\273\226\362\203Z\203~\203i\201[.pptx)
 本日の内容 ビタミン含有保健剤の承認基準の一部改正について 奈良県医療政策部薬務課 〇告示 関連する通知〇都道府県知事の承認に係る医薬部外品の一部を改正する件について〇〇〇〇既承認品目の取扱い 2 告示 関連する通知 都道府県知事の承認に係る医薬部外品の一部を改正する件 ( 平成 29 年厚 労働省告 第 90 号 ) 都道府県知事の承認に係る医薬部外品の一部を改正する件について ( 平成 29 年
本日の内容 ビタミン含有保健剤の承認基準の一部改正について 奈良県医療政策部薬務課 〇告示 関連する通知〇都道府県知事の承認に係る医薬部外品の一部を改正する件について〇〇〇〇既承認品目の取扱い 2 告示 関連する通知 都道府県知事の承認に係る医薬部外品の一部を改正する件 ( 平成 29 年厚 労働省告 第 90 号 ) 都道府県知事の承認に係る医薬部外品の一部を改正する件について ( 平成 29 年
登録販売者関係手続き一覧 手続き対象となる場合添付書類手数料 1 登録販売者試験に合格後 一般用医薬品の販売 詳細は別紙 又は授与に従事しようとするとき 1 販売従事登録 2 薬種商の許可を受けている ( いた ) 者で 一般用 合格通知書の原本 申請 医薬品の販売に従事している ( しようとする
 登録販売者関係手続き一覧 手続き対象となる場合添付書類手数料 1 登録販売者試験に合格後 一般用医薬品の販売 詳細は別紙 又は授与に従事しようとするとき 1 販売従事登録 2 薬種商の許可を受けている ( いた ) 者で 一般用 合格通知書の原本 申請 医薬品の販売に従事している ( しようとする ) とき 戸籍の謄( 抄 ) 本 7,100 円 診断書 複数の都道府県での登録はできません 使用関係を証する
登録販売者関係手続き一覧 手続き対象となる場合添付書類手数料 1 登録販売者試験に合格後 一般用医薬品の販売 詳細は別紙 又は授与に従事しようとするとき 1 販売従事登録 2 薬種商の許可を受けている ( いた ) 者で 一般用 合格通知書の原本 申請 医薬品の販売に従事している ( しようとする ) とき 戸籍の謄( 抄 ) 本 7,100 円 診断書 複数の都道府県での登録はできません 使用関係を証する
藤沢市木造住宅簡易耐震改修工事補助金交付要綱 ( 趣旨 ) 第 1 条この要綱は, 木造住宅の耐震改修工事を促進することにより, 災害に強い安全なまちづくりを推進するため, 藤沢市耐震改修促進計画に基づき, 簡易耐震改修工事のための補強設計及び簡易耐震改修工事並びに工事監理に要する費用に対する補助金
 藤沢市木造住宅簡易耐震改修工事補助金交付要綱 ( 趣旨 ) 第 1 条この要綱は, 木造住宅の耐震改修工事を促進することにより, 災害に強い安全なまちづくりを推進するため, 藤沢市耐震改修促進計画に基づき, 簡易耐震改修工事のための補強設計及び簡易耐震改修工事並びに工事監理に要する費用に対する補助金を交付することに関し, 必要な事項を定めるものとする ( 定義 ) 第 2 条この要綱において, 次の各号に掲げる用語の定義は,
藤沢市木造住宅簡易耐震改修工事補助金交付要綱 ( 趣旨 ) 第 1 条この要綱は, 木造住宅の耐震改修工事を促進することにより, 災害に強い安全なまちづくりを推進するため, 藤沢市耐震改修促進計画に基づき, 簡易耐震改修工事のための補強設計及び簡易耐震改修工事並びに工事監理に要する費用に対する補助金を交付することに関し, 必要な事項を定めるものとする ( 定義 ) 第 2 条この要綱において, 次の各号に掲げる用語の定義は,
薬局を利用するために必要な情報の掲示 ( 薬事法第 9 条の 4) 次の事項について 掲示板等により 薬局内に掲示 しなければなりません また 第 3 については 特定販売を行うことについての広告をする場合 ホームページ等に表示しなければなりません < 具体例 > 第 1 薬局の管理及び運営に関する
 薬局を利用するために必要な情報の掲示 ( 薬事法第 9 条の 4) 次の事項について 掲示板等により 薬局内に掲示 しなければなりません また 第 3 については 特定販売を行うことについての広告をする場合 ホームページ等に表示しなければなりません < 具体例 > 第 1 薬局の管理及び運営に関する事項 1 許可の区分の別薬局 開設者氏名 株式会社 開設者の氏名又は名称その 薬局の名称 薬局 店 2
薬局を利用するために必要な情報の掲示 ( 薬事法第 9 条の 4) 次の事項について 掲示板等により 薬局内に掲示 しなければなりません また 第 3 については 特定販売を行うことについての広告をする場合 ホームページ等に表示しなければなりません < 具体例 > 第 1 薬局の管理及び運営に関する事項 1 許可の区分の別薬局 開設者氏名 株式会社 開設者の氏名又は名称その 薬局の名称 薬局 店 2
<4D F736F F F696E74202D CF6955C A8CF6957A8E9EB1C4DE838C834E8E9197BF2E707074>
 薬事法施行規則等の一部を改正する省令の概要 公布日平成 21 年 2 月 6 日 ( 金 ) 本省令により改正される主な法規類 1. 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 2. 薬局等構造設備規則 ( 昭和 36 年厚生省令第 2 号 ) 3. 薬局及び一般販売業の薬剤師の員数を定める省令 ( 昭和 39 年厚生省令第 3 号 ) 施行日平成 21 年 6 月 1 日 ( 月 )
薬事法施行規則等の一部を改正する省令の概要 公布日平成 21 年 2 月 6 日 ( 金 ) 本省令により改正される主な法規類 1. 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 2. 薬局等構造設備規則 ( 昭和 36 年厚生省令第 2 号 ) 3. 薬局及び一般販売業の薬剤師の員数を定める省令 ( 昭和 39 年厚生省令第 3 号 ) 施行日平成 21 年 6 月 1 日 ( 月 )
別記様式 2 地方整備局長 知事 支社支社長 印 公共工事の入札及び契約の適正化の促進に関する法律第 11 条 社会保険等未加入 業者 の通知について 公共工事の入札及び契約の適正化の促進に関する法律 ( 以下 法 という ) 第 11 条に基づき 弊社の発注工事において社会保険等未加入業者の存在が
 別記様式 1 支社長契約責任者監督員 支社 事務所点検実施者 印 施工体制点検の結果について 下記の工事について施工体制点検を行った結果 公共工事の入札及び契約の適正化の促進に関する法律第 11 条に該当すると疑うに足りる 契約書第 7 条の 2 に違反すると認められる 事実がありましたので報告します 記 1. 工事名 2. 施工場所 3. 請負業者名代表者名住所建設業許可番号 4. 法第 11 条に該当すると疑うに足りる事実について
別記様式 1 支社長契約責任者監督員 支社 事務所点検実施者 印 施工体制点検の結果について 下記の工事について施工体制点検を行った結果 公共工事の入札及び契約の適正化の促進に関する法律第 11 条に該当すると疑うに足りる 契約書第 7 条の 2 に違反すると認められる 事実がありましたので報告します 記 1. 工事名 2. 施工場所 3. 請負業者名代表者名住所建設業許可番号 4. 法第 11 条に該当すると疑うに足りる事実について
厚生労働省令第 136 号 平成 16 年 9 月 22 日 薬事法 ( 昭和三十五年法律第百四十五号 ) 第十二条の二第一号の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の品質管理の基準に関する省令を次のように定める 平成十六年九月二十二日厚生労働大臣坂口力 医薬品 医薬部外品 化粧品及び
 厚生労働省令第 136 号 平成 16 年 9 月 22 日 薬事法 ( 昭和三十五年法律第百四十五号 ) 第十二条の二第一号の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の品質管理の基準に関する省令を次のように定める 平成十六年九月二十二日厚生労働大臣坂口力 医薬品 医薬部外品 化粧品及び医療機器の品質管理の基準に関する省令 目次第一章総則 ( 第一条 第二条 ) 第二章医薬品の品質管理の基準
厚生労働省令第 136 号 平成 16 年 9 月 22 日 薬事法 ( 昭和三十五年法律第百四十五号 ) 第十二条の二第一号の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の品質管理の基準に関する省令を次のように定める 平成十六年九月二十二日厚生労働大臣坂口力 医薬品 医薬部外品 化粧品及び医療機器の品質管理の基準に関する省令 目次第一章総則 ( 第一条 第二条 ) 第二章医薬品の品質管理の基準
3 治験実施計画書目的 当該治験について 治験実施計画書が手順書に従い適切に作成及び改訂されていることを確認する 次の事項を調べる (1) 治験実施計画書の記載項目 ( 再生医療等製品 GCP 省令第 7 条第 1 項に規定する項目 ) (2) 治験実施計画書の作成 改訂の手順と日付 (3) 治験計
 別添 10 再生医療等製品 GCP 省令チェックリスト Ⅰ 治験依頼者 ( 受託機関を含む ) 用 1 組織及び体制目的 治験の依頼及び管理に当たって 再生医療等製品 GCP 省令に沿った業務を行うために適切にして十分な人材を有し かつ 組織及び体制が確立していることを確認する 1 治験依頼者の組織 ( 当該被験機器の開発組織を含む ) と再生医療等製品 G CP 省令に係わる組織との関係 2 治験の依頼及び管理の業務に従事する者の氏名
別添 10 再生医療等製品 GCP 省令チェックリスト Ⅰ 治験依頼者 ( 受託機関を含む ) 用 1 組織及び体制目的 治験の依頼及び管理に当たって 再生医療等製品 GCP 省令に沿った業務を行うために適切にして十分な人材を有し かつ 組織及び体制が確立していることを確認する 1 治験依頼者の組織 ( 当該被験機器の開発組織を含む ) と再生医療等製品 G CP 省令に係わる組織との関係 2 治験の依頼及び管理の業務に従事する者の氏名
製造販売後調査事務手続き等 について
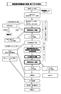 製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年
![医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年 医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年](/thumbs/91/107149459.jpg) 事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
2. 流れのポイント < 企業としての責任体制の審査 > 1 製造販売業許可申請 説明医薬品を製造販売するにあたって 製品の市場に対する最終責任 品質保証業務責任 安全管理業務責任を担う能力を持っていることを都道府県へ申請し 許可を受ける必要があります 製造販売業許可の権限について 各都道府県知事の
 < 医薬品の製造販売手順について > わが国で医薬品を市場へ業として出荷 ( 製造販売 ) することは 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 医薬品医療機器等法 ) で規制されており 規制当局 ( 厚生労働省及び各都道府県 ) の許可 承認を得ないとおこなうことはできません 本書は 製造販売をおこなうための手順を簡単にまとめたものです 1. 製造販売をおこなうための流れ
< 医薬品の製造販売手順について > わが国で医薬品を市場へ業として出荷 ( 製造販売 ) することは 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 医薬品医療機器等法 ) で規制されており 規制当局 ( 厚生労働省及び各都道府県 ) の許可 承認を得ないとおこなうことはできません 本書は 製造販売をおこなうための手順を簡単にまとめたものです 1. 製造販売をおこなうための流れ
文書管理番号
 プライバシーマーク付与適格性審査実施規程 1. 一般 1.1 適用範囲この規程は プライバシーマーク付与の適格性に関する審査 ( 以下 付与適格性審査 という ) を行うプライバシーマーク指定審査機関 ( 以下 審査機関 という ) が その審査業務を遂行する際に遵守すべき事項を定める 1.2 用語この基準で用いる用語は 特段の定めがない限り プライバシーマーク制度基本綱領 プライバシーマーク指定審査機関指定基準
プライバシーマーク付与適格性審査実施規程 1. 一般 1.1 適用範囲この規程は プライバシーマーク付与の適格性に関する審査 ( 以下 付与適格性審査 という ) を行うプライバシーマーク指定審査機関 ( 以下 審査機関 という ) が その審査業務を遂行する際に遵守すべき事項を定める 1.2 用語この基準で用いる用語は 特段の定めがない限り プライバシーマーク制度基本綱領 プライバシーマーク指定審査機関指定基準
じ ) その他の処方せん医薬品又は高度管理医療機器の製造販売に係る業務の責任者との密接な連携を図らせること ( 安全確保業務に係る組織及び職員 ) 第四条第一種製造販売業者は 次に掲げる要件を満たす安全確保業務の統括に係る部門 ( 以下この章において 安全管理統括部門 という ) を置かなければなら
 厚生労働省令第百三十五号薬事法 ( 昭和三十五年法律第百四十五号 ) 第十二条の二第二号の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令を次のように定める 平成十六年九月二十二日厚生労働大臣坂口力 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令目次第一章総則 ( 第一条第二条 ) 第一種製造販売業者の製造販売後安全管理の基準
厚生労働省令第百三十五号薬事法 ( 昭和三十五年法律第百四十五号 ) 第十二条の二第二号の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令を次のように定める 平成十六年九月二十二日厚生労働大臣坂口力 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令目次第一章総則 ( 第一条第二条 ) 第一種製造販売業者の製造販売後安全管理の基準
GMP 適合性調査申請 ( 都道府県調査品目 ) ( 承取得後 5 年毎時 ) ( 法第 4 条第 6 項 令第 20 条 2 条 22 条 規則第 50 条 ) GMP 適合性調査申請 ( 国調査及び証関調査品目 ) ( 承 ( 証 ) 取得後 5 年毎時 ) ( 法第 4
 製造販売業許可関係 ( 製造販売業者が行う手続き ) 製造販売業許可申請 ( 法第 2 条第 項 令第 3 条 規則第 9 条 ) 医療器 許可希望日の 登記簿謄本 申請者及び薬事に関する業務を行う役製造販売業許可要件を整備し 許可を受けたい時期の約員の診断書 薬事に関する業務を行う役員の組織 に申請する 図 総括製造販売責任者の雇用契約書等使用関係を証明する書類 総括製造販売責任者の資格を証する書類
製造販売業許可関係 ( 製造販売業者が行う手続き ) 製造販売業許可申請 ( 法第 2 条第 項 令第 3 条 規則第 9 条 ) 医療器 許可希望日の 登記簿謄本 申請者及び薬事に関する業務を行う役製造販売業許可要件を整備し 許可を受けたい時期の約員の診断書 薬事に関する業務を行う役員の組織 に申請する 図 総括製造販売責任者の雇用契約書等使用関係を証明する書類 総括製造販売責任者の資格を証する書類
<4D F736F F F696E74202D C8E8DC58F4994C5817A88C092E890AB A835E838A F2E B8CDD8AB B83685D>
 製薬セミナー 5 月期 安定性モニタリング 薬務課振興係 1 安定性モニタリング 2 1 安定性モニタリングとは 製造した最終製品あるいは原薬が定められた保存条件下で 有効期間 リテスト期間又は使用の期限にわたり 保存により影響を受け易い測定項目及び品質 安全性又は有効性に影響を与えるような測定項目が規格内に留まっており また留まり続けることが期待できることを 適切な継続的プログラムに従った安定性モニタリングにより監視し
製薬セミナー 5 月期 安定性モニタリング 薬務課振興係 1 安定性モニタリング 2 1 安定性モニタリングとは 製造した最終製品あるいは原薬が定められた保存条件下で 有効期間 リテスト期間又は使用の期限にわたり 保存により影響を受け易い測定項目及び品質 安全性又は有効性に影響を与えるような測定項目が規格内に留まっており また留まり続けることが期待できることを 適切な継続的プログラムに従った安定性モニタリングにより監視し
<4D F736F F F696E74202D20382E2088E396F CC90BB91A294CC94848CE392B28DB882CC8CBB8FF382C697AF88D3935F2E >
 医薬品の製造販売後調査の現状と留意点 1 本日の内容 1. 改正医薬品 GPSP 省令 再生医療等製品 GPSP 省令 の留意点について 2. 医薬品の再審査申請資料適合性調査 (GPSP 実地調査及び適合性書面調査 ) 2 1. 改正医薬品 GPSP 省令 再生医療等製品 GPSP 省令 の留意点について 3 改正医薬品 GVP GPSP 省令 < 平成 25 年 3 月 11 日 > 医薬品の製造販売業者による医薬品リスク管理計画
医薬品の製造販売後調査の現状と留意点 1 本日の内容 1. 改正医薬品 GPSP 省令 再生医療等製品 GPSP 省令 の留意点について 2. 医薬品の再審査申請資料適合性調査 (GPSP 実地調査及び適合性書面調査 ) 2 1. 改正医薬品 GPSP 省令 再生医療等製品 GPSP 省令 の留意点について 3 改正医薬品 GVP GPSP 省令 < 平成 25 年 3 月 11 日 > 医薬品の製造販売業者による医薬品リスク管理計画
Microsoft Word - 沖縄県サービス管理責任者フォローアップ研修事業指定事務取扱要領
 沖縄県サービス管理責任者フォローアップ研修事業指定事務取扱要領 ( 目的 ) 第 1 条この要領は沖縄県サービス管理責任者フォローアップ研修事業実施要綱 ( 以下 実施要綱 という ) 第 13 条の規定により サービス管理責任者フォローアップ研修を行う研修事業者の指定等にあたって 必要な事項を定めるものとする ( 指定の基準 ) 第 2 条研修事業者の指定を受け研修を実施しようとする者 ( 以下
沖縄県サービス管理責任者フォローアップ研修事業指定事務取扱要領 ( 目的 ) 第 1 条この要領は沖縄県サービス管理責任者フォローアップ研修事業実施要綱 ( 以下 実施要綱 という ) 第 13 条の規定により サービス管理責任者フォローアップ研修を行う研修事業者の指定等にあたって 必要な事項を定めるものとする ( 指定の基準 ) 第 2 条研修事業者の指定を受け研修を実施しようとする者 ( 以下
Microsoft PowerPoint - ⑨140925,30日薬連講習会(後発RMP)930.ppt [互換モード]
![Microsoft PowerPoint - ⑨140925,30日薬連講習会(後発RMP)930.ppt [互換モード] Microsoft PowerPoint - ⑨140925,30日薬連講習会(後発RMP)930.ppt [互換モード]](/thumbs/101/151698947.jpg) 後発医薬品 RMP について 厚生労働省医薬食品局安全対策課磯﨑正季子 1 後発医薬品への RMP の適用 平成 24 年 4 月 11 日薬食安発 0411 第 1 号 薬食審査発 0411 第 2 号安全対策課長 審査管理課長連名通知 医薬品リスク管理計画指針について 適用範囲医療用医薬品 ( 新医薬品 バイオ後続品 後発医薬品 ) 策定検討の時点 承認申請時 新医薬品 バイオ後続品後発医薬品
後発医薬品 RMP について 厚生労働省医薬食品局安全対策課磯﨑正季子 1 後発医薬品への RMP の適用 平成 24 年 4 月 11 日薬食安発 0411 第 1 号 薬食審査発 0411 第 2 号安全対策課長 審査管理課長連名通知 医薬品リスク管理計画指針について 適用範囲医療用医薬品 ( 新医薬品 バイオ後続品 後発医薬品 ) 策定検討の時点 承認申請時 新医薬品 バイオ後続品後発医薬品
( メール施行 ) 薬第 号平成 29 年 2 月 14 日 各保健所 支所長殿 ( 薬事担当班扱い ) 保健福祉部長 ( 公印省略 ) 温泉資源の保護に関するガイドライン ( 地熱発電関係 ) の一部改正に伴う運用について ( 通知 ) 温泉資源の保護に関するガイドライン ( 地熱
 ( メール施行 ) 薬第 1 1 0 0 号平成 29 年 2 月 14 日 各保健所 支所長殿 ( 薬事担当班扱い ) 保健福祉部長 ( 公印省略 ) 温泉資源の保護に関するガイドライン ( 地熱発電関係 ) の一部改正に伴う運用について ( 通知 ) 温泉資源の保護に関するガイドライン ( 地熱発電関係 ) の一部改正については, 平成 27 年 1 月 30 日付け薬第 1196 号で通知したところですが,
( メール施行 ) 薬第 1 1 0 0 号平成 29 年 2 月 14 日 各保健所 支所長殿 ( 薬事担当班扱い ) 保健福祉部長 ( 公印省略 ) 温泉資源の保護に関するガイドライン ( 地熱発電関係 ) の一部改正に伴う運用について ( 通知 ) 温泉資源の保護に関するガイドライン ( 地熱発電関係 ) の一部改正については, 平成 27 年 1 月 30 日付け薬第 1196 号で通知したところですが,
医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など ) 医薬品候補物質のスクリーニン
 特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
Ⅰ 概要について 一次下請契約者を社会保険等加入業者に限定します 平成 29 年 4 月 1 日以降に契約締結した工事において 受注者は 原則として社会保険等未加入業者を下請契約 ( 受注者が直接契約締結するものに限る 以下 一次下請契約 という ) の相手方としないこととします 追加 建設工事契約
 鶴岡市発注工事における社会保険等未加入対策について ( 概要 Q&A フロー ) 平成 29 年 1 月 鶴岡市 - 0 - Ⅰ 概要について 一次下請契約者を社会保険等加入業者に限定します 平成 29 年 4 月 1 日以降に契約締結した工事において 受注者は 原則として社会保険等未加入業者を下請契約 ( 受注者が直接契約締結するものに限る 以下 一次下請契約 という ) の相手方としないこととします
鶴岡市発注工事における社会保険等未加入対策について ( 概要 Q&A フロー ) 平成 29 年 1 月 鶴岡市 - 0 - Ⅰ 概要について 一次下請契約者を社会保険等加入業者に限定します 平成 29 年 4 月 1 日以降に契約締結した工事において 受注者は 原則として社会保険等未加入業者を下請契約 ( 受注者が直接契約締結するものに限る 以下 一次下請契約 という ) の相手方としないこととします
Taro-再製造単回使用医療機器基準
 厚生労働省告示第二百六十一号医薬品医療機器等の品質有効性及び安全性の確保等に関する法律 ( 昭和三十五年法律第百四十 五号 ) 第四十二条第二項の規定に基づき再製造単回使用医療機器基準を次のように定め平成二十 九年七月三十一日から適用す る平成二十九年七月三十一日厚生労働大臣塩崎恭久再製造単回使用医療機器基準第 1 定義 1 再生部品 とは 医療機関において使用された単回使用の医療機器の全部又は一部であって
厚生労働省告示第二百六十一号医薬品医療機器等の品質有効性及び安全性の確保等に関する法律 ( 昭和三十五年法律第百四十 五号 ) 第四十二条第二項の規定に基づき再製造単回使用医療機器基準を次のように定め平成二十 九年七月三十一日から適用す る平成二十九年七月三十一日厚生労働大臣塩崎恭久再製造単回使用医療機器基準第 1 定義 1 再生部品 とは 医療機関において使用された単回使用の医療機器の全部又は一部であって
医療用医薬品最新品質情報集 ( ブルーブック ) 初版有効成分リトドリン塩酸塩 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 (25 ) 1) 溶解度 (37 ) 1 ウテロン錠 5mg サンド 2
 医療用医薬品最新品質情報集 ( ブルーブック ) 2018.7.13 初版有効成分リトドリン塩酸塩 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 (25 ) 1) 溶解度 (37 ) 1 ウテロン錠 5mg サンド 2 塩酸リトドリン錠 5mg YD 陽進堂 3 リトドリン錠 5mg PP ポーラファルマ 4 ルテオニン錠
医療用医薬品最新品質情報集 ( ブルーブック ) 2018.7.13 初版有効成分リトドリン塩酸塩 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 (25 ) 1) 溶解度 (37 ) 1 ウテロン錠 5mg サンド 2 塩酸リトドリン錠 5mg YD 陽進堂 3 リトドリン錠 5mg PP ポーラファルマ 4 ルテオニン錠
Microsoft Word - 4-2”©„Èfi_„�Ł\.doc
 自己点検表 高度管理医療機器当販売業 賃貸業を想定して作成してあります 自社の取扱う医療機器の種類に応じて作成してください 1 2 3 4 5 実施日 : 担当者 : 許可証の掲示 店舗の見やすい場所に原本が掲示されているか 営業所の構造設備 採光 照明 換気は適切か 清掃 整理整頓がされているか (3) 保管場所等は申請した図面と変更されていないか 変更届の提出 営業所の住所及び氏名 ( 法人の場合は登記上の住所及び法人名称
自己点検表 高度管理医療機器当販売業 賃貸業を想定して作成してあります 自社の取扱う医療機器の種類に応じて作成してください 1 2 3 4 5 実施日 : 担当者 : 許可証の掲示 店舗の見やすい場所に原本が掲示されているか 営業所の構造設備 採光 照明 換気は適切か 清掃 整理整頓がされているか (3) 保管場所等は申請した図面と変更されていないか 変更届の提出 営業所の住所及び氏名 ( 法人の場合は登記上の住所及び法人名称
書類名
 別送書類一覧 ( 建設工事 ) 書類名 摘要 納税証明書 ( 国税 ) 代表審査自治体が蒲郡市の場合 次の書類を⑶の提出先へ郵送してください 1 法人の方納税証明書 その3の3 ( 法人税 消費税及地方消費税 ) 2 個人の方納税証明書 その3の2 ( 申告所得税及復興特別所得税 消費税及地方消費税 ) 本店所在地を管轄する税務署 ( 窓口又はオンライン ) で交付を受けることができます 代表審査自治体が蒲郡市以
別送書類一覧 ( 建設工事 ) 書類名 摘要 納税証明書 ( 国税 ) 代表審査自治体が蒲郡市の場合 次の書類を⑶の提出先へ郵送してください 1 法人の方納税証明書 その3の3 ( 法人税 消費税及地方消費税 ) 2 個人の方納税証明書 その3の2 ( 申告所得税及復興特別所得税 消費税及地方消費税 ) 本店所在地を管轄する税務署 ( 窓口又はオンライン ) で交付を受けることができます 代表審査自治体が蒲郡市以
