Microsoft PowerPoint - 運用 [互換モード]
|
|
|
- てるえ こけい
- 7 years ago
- Views:
Transcription
1 押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター Ver.1.0
2 東京医療センターにおける 書式運用基本方針
3 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4) 院長から治験審査委員会への審査依頼書 ( 書式 4) の作成 (5) 治験審査結果通知書 ( 書式 5) それに基づく院長の治験に関する指示 決定通知書( 書式 5 又は参考書式 1) の作成と及び治験責任医師への通知書の交付 ( 治験審査委員会の審査結果を確認するために必要とする文書のへの交付も含む ) (6) 治験契約に係わる手続き等の業務 (7) 治験終了 ( 中止 中断 ) 報告書 ( 書式 17) の受領及び 治験審査委員会への通知書 ( 書式 17) の作成と交付 (8) 開発の中止等に関する報告書 ( 書式 18) の受領及び 治験審査委員会への通知書 ( 書式 18) の作成と交付 ( 略 ) 手順書で規定されている通り 実施医療機関の長による結果通知書等の作成 交付は治験事務局が行います
4 東京医療センターの書式運用基本方針 2 新たな 治験の依頼等に係る統一書式 について ( 厚生労働省医政局研究開発振興課発厚生労働省医薬食品局審査管理課発 / 平成 24 年 3 月 7 日 ) に基づき 簡素化 統一化 統一書式の遵守を推進し 効率化を図ります 書類への押印は省略させていただきます
5 東京医療センターの書式運用基本方針 3 書類への押印を省略した際の原本保証について 授受メールを印刷し ともにファイリングすることで原本保証とします 責任医師が作成する文書について CRCや治験事務局がその作成を補助した場合 責任医師の指示や最終確認を保証するメール等をともにファイリングし 原本保証とします ファイルの改変が不可な措置を講じ ファイルの取り違い 送信先間違い等がないよう 適切に送付します
6 具体的な運用について ー各書式の脚注に基づいて運用しますー
7 IRB 審査文書 結果通知書等の作成 医療機関で作成する文書については こちらで作成します 治験審査委員会委員長 院長 治験責任医師 の印は省略します 書式番号 資料名 医療機関作成 依頼者作成 書式 1 履歴書 書式 2 治験分担医師 治験協力者リスト 書式 3 治験依頼書 書式 4 治験審査依頼書 書式 5 治験審査結果通知書 書式 6 治験実施計画書等修正報告書 書式 8 緊急の危険を回避するための治験実施計画書からの逸脱に関する報告書 書式 9 緊急の危険を回避するための治験実施計画書からの逸脱に関する通知書 書式 10 治験に関する変更申請書 書式 11 治験実施状況報告書 書式 12-1 重篤な有害事象に関する報告書 ( 医薬品治験 ) 書式 12-2 重篤な有害事象に関する報告書 ( 医薬品治験 : 詳細記載用 ) 書式 13-1 有害事象に関する報告書 ( 医薬品製造販売後臨床試験 ) 書式 13-2 有害事象に関する報告書 ( 医薬品製造販売後臨床試験 : 詳細記載用 ) 書式 14 重篤な有害事象及び不具合に関する報告書 ( 医療機器治験 ) 書式 15 有害事象及び不具合に関する報告書 ( 医療機器製造販売後臨床試験 ) 書式 16 安全性情報等に関する報告書 書式 17 治験終了 ( 中止 中断 ) 報告書 書式 18 開発の中止等に関する報告書 参考書式 1 治験に関する指示 決定通知書 参考書式 2 直接閲覧実施連絡票 同意説明文書の改訂のみの場合 医療機関にて作成
8 書式 1 履歴書 書式 1 履歴書は 責任医師 治験事務局が作成し メール送付します 治験責任医師 書式 1 正本メール送付 cc: 治験責任医師 cc: 担当 CRC cc: 治験事務局 書式 1 正本 2 部を作成 書式 1 正本ファイリング 書式 1 正本をファイリング
9 書式 2 治験分担医師 治験協力者リスト 書式 2 治験分担医師 治験協力者リストは 責任医師 治験事務局が作成し 実施医療機関の長の了承が得られましたら メール送付します 治験責任医師 IRB 後 書式 2 写しメール送付 cc: 治験責任医師 cc: 担当 CRC cc: 治験事務局 書式 2 ファイリング 責任医師ファイル 書式 2 正本 1 部を作成 下部に了承日 実施医療機関の長欄を記載 書式 2 正本をファイリング 書式 2 写しをファイリング
10 書式 3 治験依頼書 書式 3 治験依頼書は 治験事務局宛にメールでお送りください cc: 治験責任医師 cc: 担当 CRC 書式 3 メール送付 書式 3 正本ファイリング 書式 3 正本をファイリング 書式 3 正本 1 部を作成
11 書式 4 治験審査依頼書 書式 4 治験審査依頼書は 治験事務局が作成します 書式 4 正本ファイリング 書式 4 正本をファイリング 書式 4 正本 1 部を作成
12 書式 5 治験審査結果通知書 書式 5 治験審査結果通知書は 治験事務局が作成 写し 2 部に通知日 医療機関の長欄を記載し メール送付します 書式 5 正本メール送付 cc: 治験責任医師 cc: 担当 CRC cc: 治験事務局 書式 5 ファイリング 責任医師ファイル 書式 5 正本 1 部を作成 写し 2 部に通知日 実施医療機関の長欄を記載 書式 5 正本 ( 下部記載 ) をファイリング 書式 5 正本をファイリング
13 書式 6 治験実施計画書等修正報告書 ( 説明文書 同意文書の修正のみの場合 ) 書式 6 治験実施計画書等修正報告書 ( 説明文書 同意文書の修正のみの場合 ) は 治験事務局が作成し 写しをメール送付します 治験責任医師 同意文書の修正が終わりました 書式 6 写しメール送付 cc: 治験責任医師 cc: 担当 CRC cc: 治験事務局 欄は 該当なし と記載 書式 6 正本 1 部を作成 修正確認後 下部に確認日 実施医療機関の長欄を記載 書式 6 ファイリング 書式 6 正本をファイリング 責任医師ファイル 書式 6 写しをファイリング
14 書式 の運用について 書式 は CRC が作成を補助する場合があります その場合 責任医師の確認日 責任医師の承認日 責任医師の指示事項などを 記録として残す必要があります ここでは 書式 12-1 重篤な有害事象に関する報告書 を例に 1 責任医師に直接面会して 内容を確認する場合 2 責任医師にメールで 内容を確認する場合の運用をご説明します 書式番号 資料名 医療機関作成 書式 8 緊急の危険を回避するための治験実施計画書からの逸脱に関する報告書 書式 12-1 重篤な有害事象に関する報告書 ( 医薬品治験 ) 書式 12-2 重篤な有害事象に関する報告書 ( 医薬品治験 : 詳細記載用 ) 書式 13-1 有害事象に関する報告書 ( 医薬品製造販売後臨床試験 ) 書式 13-2 有害事象に関する報告書 ( 医薬品製造販売後臨床試験 : 詳細記載用 ) 書式 14 重篤な有害事象及び不具合に関する報告書 ( 医療機器治験 ) 書式 15 有害事象及び不具合に関する報告書 ( 医療機器製造販売後臨床試験 )
15 書式 12-1 重篤な有害事象に関する報告書 1 1 責任医師に直接面会して内容を確認する場合 CRC 治験責任医師 書式 12-1 CRC が案を作成し 責任医師に面会 内容を確認する 案 Dr.: このように修正して 提出をしてください 連絡 CRC 連絡 治験事務局に 責任医師と面会 確認した日時と 報告書の内容が確定した旨を連絡 責任医師と面会 確認した日時と 報告書を PDF 化し へメール送付 cc: 治験責任医師 cc: 担当 CRC cc: 治験事務局 書式 12-1 メール送付 < メール例 > 株式会社 さま (CC; 責任医師,CRC, 治験事務局 ) いつもお世話になっております 重篤な有害事象に関する報告書 ( 第 1 報 ) 正本 を送らせていただきます 1 重篤な有害事象に関する報告書 ( 第 1 報 ) 2012 年 9 月 6 日付 1 につきましては 御社にて印刷し 正本 としていただきますよう お願い申し上げます 本日 9 月 6 日 12:50 頃 CRC が 責任医師と面会し 報告書の内容を確認していただきましたので 合わせてご報告致します 今後ともよろしくお願い致します 正本
16 書式 12-1 重篤な有害事象に関する報告書 2 2 責任医師にメールで内容を確認する場合 連絡 CRC 書式 12-1 CRCが案を作成し 責任医師にメール送付 < メール例 > 内科 先生 (CC;CRC, 治験事務局 ) いつも治験等お世話になっております 重篤な有害事象に関する報告書 ( 第 1 報 ) 案 を作成しましたので 内容のご確認をお願い致します 1 重篤な有害事象に関する報告書 ( 第 1 報 ) 2012 年 9 月 6 日付 内容をご確認いただきましたら CRC 治験事務局宛にご返信いただきたく お願い申し上げます 東京医療センター治験管理室 CRC (PHS:8888) 治験責任医師 内容確認し その結果を CRC に返信 案 Dr.: この内容で OK です! 連絡 責任医師が内容を確認した旨のメール本文を貼り付けるなどして 報告書を PDF 化し へメール送付 cc: 治験責任医師 cc: 担当 CRC cc: 治験事務局 CRC 治験事務局に 報告書の内容が確定した旨を連絡 書式 12-1 メール送付 < メール例 > 株式会社 さま (CC; 責任医師,CRC, 治験事務局 ) いつもお世話になっております 重篤な有害事象に関する報告書 ( 第 1 報 ) 正本 を送らせていただきます 1 重篤な有害事象に関する報告書 ( 第 1 報 ) 2012 年 9 月 6 日付 1 につきましては 御社にて印刷し 正本 としていただきますよう お願い申し上げます 責任医師が この報告書の内容を確認した際のメールを 下記に添付致します 今後ともよろしくお願い致します >Wrote:2012 年 9 月 6 日 12:50 > CRC さんへ > 重篤な有害事象に関する報告書の内容を確かに確認致しました こちらを提出してください 内科 正本
17 書式 9 緊急の危険を回避するための治験実施計画書からの逸脱に関する通知書 書式 9 緊急の危険を回避するための治験実施計画書からの逸脱に関する通知書は 治験事務局宛にメールでお送りください cc: 治験責任医師 cc: 担当 CRC cc: 治験事務局書式 9 メール送付 書式 9 正本ファイリング 書式 9 正本をファイリング 書式 9 正本 1 部を作成
18 書式 10 治験に関する変更申請書 書式 10 治験に関する変更申請書は 治験責任医師 治験事務局宛にメールでお送りください 説明文書 同意文書 のみの変更の場合書式 10 治験に関する変更申請書 正本は 治験事務局で作成します へは写しを送付します cc: 担当 CRC 書式 10 メール送付 書式 10 添付資料 3 部郵送 治験責任医師 書式 10 正本ファイリング 書式 10 正本をファイリング 書式 10 正本 1 部を作成
19 書式 11 治験実施状況報告書 書式 11 治験実施状況報告書は 責任医師 CRC 治験事務局が作成し 写しをメール送付します 治験責任医師 CRC 書式 11 写しメール送付 cc: 治験責任医師 cc: 担当 CRC cc: 治験事務局 書式 11 正本 1 部を作成 書式 11 正本ファイリング 書式 11 正本をファイリング
20 書式 16 安全性情報等に関する報告書 書式 16 安全性情報等に関する報告書は 治験責任医師 治験事務局宛にメールでお送りください cc: 担当 CRC 書式 16 メール送付 治験責任医師 責任医師ファイル 書式 16 正本をファイリング 書式 16 正本ファイリング 書式 16 正本 2 部を作成 書式 16 添付資料 3 部郵送 書式 16 正本をファイリング
21 書式 17 治験終了 ( 中止 中断 ) 報告書 書式 17 治験終了報告書は 責任医師 CRC 治験事務局が作成し 写し 2 部に通知日 医療機関の長欄を記載し メール送付します 治験責任医師 CRC 書式 17 メール送付 cc: 治験責任医師 cc: 担当 CRC cc: 治験事務局 書式 17 ファイリング 書式 17 正本 1 部を作成 下部に了承日 実施医療機関の長欄を記載 書式 17 正本をファイリング
22 書式 18 開発の中止等に関する報告書 書式 18 開発の中止等に関する報告書は 治験事務局宛にお送りください 写し 2 部に通知日 医療機関の長欄を記載し IRB にて報告します cc: 治験責任医師 cc: 担当 CRC 書式 18 正本をファイリング 書式 18 メール送付 書式 18 ファイリング 書式 18 正本 1 部を作成 下部に了承日 実施医療機関の長欄を記載 責任医師ファイル 書式 18 正本をファイリング
23 東京医療センター 治験管理室 ホームページ こちらの 東京医療センター 統一書式の運用について を 当院ホームページにUPしています 患者さん役 某治験主任 CRC 実在のCRC この写真が治験管理室HPの目印です お問い合わせはこちらまでお願いします
<4D F736F F D E34208EA18CB18EE891B182AB977697CC C8E8DB782B591D682A688CB978A>
 Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
臨床試験(治験)の手続きについて
 臨床試験 ( 治験 製造販売後臨床試験 ) の手続きについて 本書は 昭和大学横浜市北部病院における臨床試験 ( 治験 製造販売後臨床試験 ) の手続き等に関して記したものです 始める前にご一読下さい なお 下記手続きにおいて必要書類を提出される場合は臨床試験支援室 ( 連絡先 :10 ページ参照 ) までご連絡下さい - 試験依頼前 - 関係書類の入手 当院の臨床試験 ( 治験 製造販売後臨床試験
臨床試験 ( 治験 製造販売後臨床試験 ) の手続きについて 本書は 昭和大学横浜市北部病院における臨床試験 ( 治験 製造販売後臨床試験 ) の手続き等に関して記したものです 始める前にご一読下さい なお 下記手続きにおいて必要書類を提出される場合は臨床試験支援室 ( 連絡先 :10 ページ参照 ) までご連絡下さい - 試験依頼前 - 関係書類の入手 当院の臨床試験 ( 治験 製造販売後臨床試験
臨床試験(治験)実施の手続き
 製造販売後調査実施の手続き はじめに 本書は 昭和大学藤が丘病院における製造販売後調査実施の手続き方法等について記載したものです 本書内のは当院が提供する書類を示し は審査等に必要な書類を示しております 調査内容により提出書類 資料に変更が生じる場合があります 詳細は支援室にご確認ください 申請する書類および資料は 事前に E-mail に添付して支援室にお送りください 内容の確認をし ご連絡させて頂きます
製造販売後調査実施の手続き はじめに 本書は 昭和大学藤が丘病院における製造販売後調査実施の手続き方法等について記載したものです 本書内のは当院が提供する書類を示し は審査等に必要な書類を示しております 調査内容により提出書類 資料に変更が生じる場合があります 詳細は支援室にご確認ください 申請する書類および資料は 事前に E-mail に添付して支援室にお送りください 内容の確認をし ご連絡させて頂きます
山形県立中央病院治験審査委員会業務手順書
 山形県立中央病院治験審査委員会業務手順書 第 1 目的この手順書は山形県立中央病院医薬品等臨床試験受託研究取扱要綱 ( 以下 取扱要綱 という ) に基づいて山形県立中央病院治験審査委員会 ( 以下 本委員会 という ) の運用方法を定め それに基づく業務手順書を示すものである なお 製造販売後臨床試験においては 以下 治験 とあるのを 製造販売後臨床試験 と読み替えるものとする 第 2 本委員会の責務本委員会は全ての被験者の人権の保護
山形県立中央病院治験審査委員会業務手順書 第 1 目的この手順書は山形県立中央病院医薬品等臨床試験受託研究取扱要綱 ( 以下 取扱要綱 という ) に基づいて山形県立中央病院治験審査委員会 ( 以下 本委員会 という ) の運用方法を定め それに基づく業務手順書を示すものである なお 製造販売後臨床試験においては 以下 治験 とあるのを 製造販売後臨床試験 と読み替えるものとする 第 2 本委員会の責務本委員会は全ての被験者の人権の保護
12_モニタリングの実施に関する手順書
 12_ モニタリングの実施に関する手順書 静岡県立大学大学院薬食生命科学総合学府薬学研究院薬食研究推進センター版数 :1.0 版作成年月日 :2014 月 8 月 1 日 ( 最終確定 :2015 年 1 月 14 日 ) 1. 目的と適用範囲 本手順書は 当該研究において モニターが モニタリングを適切に実施するための手順 その他必要な事項を定めるものである 2. 実施体制及び責務 2.1 研究責任者の責務研究責任者は
12_ モニタリングの実施に関する手順書 静岡県立大学大学院薬食生命科学総合学府薬学研究院薬食研究推進センター版数 :1.0 版作成年月日 :2014 月 8 月 1 日 ( 最終確定 :2015 年 1 月 14 日 ) 1. 目的と適用範囲 本手順書は 当該研究において モニターが モニタリングを適切に実施するための手順 その他必要な事項を定めるものである 2. 実施体制及び責務 2.1 研究責任者の責務研究責任者は
標準業務手順 目次
 浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
実施医療機関における治験に係る標準的業務手順書
 静岡市立清水病院における治験に係る標準業務手順書 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令
静岡市立清水病院における治験に係る標準業務手順書 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令
医師主導治験取扱要覧
 15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会
 治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会 第 1 条 ( 目的 ) 1. 本手順書は 新光会治験審査委員会 ( 以下 委員会という ) において 医薬品及び医療機器 ( 以下 医薬品等という ) の治験の調査審議を実施するに当たり 薬事法 ( 昭和 35 年 8 月 10 日法律第 145 号 ) に基づく 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3
治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会 第 1 条 ( 目的 ) 1. 本手順書は 新光会治験審査委員会 ( 以下 委員会という ) において 医薬品及び医療機器 ( 以下 医薬品等という ) の治験の調査審議を実施するに当たり 薬事法 ( 昭和 35 年 8 月 10 日法律第 145 号 ) に基づく 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3
実施医療機関治験審査委員会標準的業務手順書
 実施医療機関治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令 という
実施医療機関治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令 という
実施医療機関における治験に係る標準的業務手順書
 国立病院機構大阪医療センター 企業主導治験に係る業務細則 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本規程は 国立病院機構大阪医療センター受託研究取扱細則第 5 条に定める治験又は製造販売後臨床試験 ( 以下 治験等 という ) に関する研究の依頼 申請 契約並びに終了等 治験に関する書式とその取扱いについて定めるものとする 2 本細則は 平成 9 年 3 月 27 日厚生省令第
国立病院機構大阪医療センター 企業主導治験に係る業務細則 第 1 章目的と適用範囲 ( 目的と適用範囲 ) 第 1 条本規程は 国立病院機構大阪医療センター受託研究取扱細則第 5 条に定める治験又は製造販売後臨床試験 ( 以下 治験等 という ) に関する研究の依頼 申請 契約並びに終了等 治験に関する書式とその取扱いについて定めるものとする 2 本細則は 平成 9 年 3 月 27 日厚生省令第
治験事務局標準業務マニュアル
 治験申請等に関する手順書 Ⅰ) 新規治験の申請 1. 実施体制 治験事務局院内スタッフが SMO との提携し 事務局を運営する なお SMO の費用は院内費用とは別に算定するため 別途相談とする CRC 院内スタッフを用いる場合 SMO を利用する場合 どちらの選択も可能とする 2. ヒアリング (a) 予約に際しての条件 プロトコールが固定され 責任医師との合意が文書で得られた時点で予約は可能とする
治験申請等に関する手順書 Ⅰ) 新規治験の申請 1. 実施体制 治験事務局院内スタッフが SMO との提携し 事務局を運営する なお SMO の費用は院内費用とは別に算定するため 別途相談とする CRC 院内スタッフを用いる場合 SMO を利用する場合 どちらの選択も可能とする 2. ヒアリング (a) 予約に際しての条件 プロトコールが固定され 責任医師との合意が文書で得られた時点で予約は可能とする
長崎大学病院治験審査委員会内規 平成 21 年 4 月 1 日 病院内規第 3 号 ( 趣旨 ) 第 1 条この内規は, 長崎大学病院における医薬品の臨床試験の実施に関する内規 ( 以下 治験内規 という ) 第 4 条第 2 項, 長崎大学病院における医療機器の臨床試験の実施に関する内規 ( 以下
 長崎大学病院治験審査委員会内規 平成 21 年 4 月 1 日 病院内規第 3 号 ( 趣旨 ) 第 1 条この内規は, 長崎大学病院における医薬品の臨床試験の実施に関する内規 ( 以下 治験内規 という ) 第 4 条第 2 項, 長崎大学病院における医療機器の臨床試験の実施に関する内規 ( 以下 医療機器治験内規 という ) 第 4 条第 2 項及び長崎大学病院における再生医療等製品の臨床試験の実施に関する内規
長崎大学病院治験審査委員会内規 平成 21 年 4 月 1 日 病院内規第 3 号 ( 趣旨 ) 第 1 条この内規は, 長崎大学病院における医薬品の臨床試験の実施に関する内規 ( 以下 治験内規 という ) 第 4 条第 2 項, 長崎大学病院における医療機器の臨床試験の実施に関する内規 ( 以下 医療機器治験内規 という ) 第 4 条第 2 項及び長崎大学病院における再生医療等製品の臨床試験の実施に関する内規
静岡県立静岡がんセンター臨床研究事務局の業務手順書
 治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 6.0 平成 20 年 1 月 28
治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 6.0 平成 20 年 1 月 28
倫理審査申請システム利用ガイド(申請者編)
 東京慈恵会医科大学 倫理審査申請システム利用ガイド 申請者編 平成 28 年 3 月版 目 次 1. システムの利用準備...- 3 - ( ア ) システムの起動...- 3 - ( イ ) ユーザー登録 ( 教員の方向 )...- 4 - ( ウ ) ユーザー登録 ( 職員の方 )...- 5 - ( エ ) パスワードの再作成...- 7 - ( オ ) ログイン...- 8 - ( カ )
東京慈恵会医科大学 倫理審査申請システム利用ガイド 申請者編 平成 28 年 3 月版 目 次 1. システムの利用準備...- 3 - ( ア ) システムの起動...- 3 - ( イ ) ユーザー登録 ( 教員の方向 )...- 4 - ( ウ ) ユーザー登録 ( 職員の方 )...- 5 - ( エ ) パスワードの再作成...- 7 - ( オ ) ログイン...- 8 - ( カ )
臨床研究に関する標準業務手順書
 臨床研究に関する標準業務手順書 2018/04/01 第 15 版 改定履歴 日付 版 改定理由 改定箇所 内容 2010/02/06 1 新規制定 2010/04/14 2 COI 関連手順の明確化 フローチャートに COI に関する手順の追記 2010/08/19 3 様式 必要書類の追加 COI 関連様式の追記 安全性に関する報告の手順および様式 ( 様式 11) の追加 委託研究に関する手順
臨床研究に関する標準業務手順書 2018/04/01 第 15 版 改定履歴 日付 版 改定理由 改定箇所 内容 2010/02/06 1 新規制定 2010/04/14 2 COI 関連手順の明確化 フローチャートに COI に関する手順の追記 2010/08/19 3 様式 必要書類の追加 COI 関連様式の追記 安全性に関する報告の手順および様式 ( 様式 11) の追加 委託研究に関する手順
 治験責任医師のための 治験実施チェックリスト 平成 24 年 4 月版 日本製薬工業協会医薬品評価委員会 臨床評価部会治験啓発チーム Ver.3 はじめに 日夜 世界中の製薬企業では病気の原因を解明するための研究をしています 医薬品の開発は その病気の原因に対して 効果があると推定される新しい化合物を合成したり 天然に存在している物質から抽出したりすることから始まります そのようにしてできた化合物類は
治験責任医師のための 治験実施チェックリスト 平成 24 年 4 月版 日本製薬工業協会医薬品評価委員会 臨床評価部会治験啓発チーム Ver.3 はじめに 日夜 世界中の製薬企業では病気の原因を解明するための研究をしています 医薬品の開発は その病気の原因に対して 効果があると推定される新しい化合物を合成したり 天然に存在している物質から抽出したりすることから始まります そのようにしてできた化合物類は
治験実施に必要な手続きについて (HP 用 ) 治験 製造販売後臨床試験 聖マリアンナ医科大学病院治験管理室 聖マリアンナ医科大学病院治験管理室 2011 年 10 月作成 2013 年 1 月改訂 2014 年 4 月改訂 2018 年 4 月改定 2018 年 5 月改定 Ⅰ. 治験審査委員会
 治験実施に必要な手続きについて (HP 用 ) 治験 製造販売後臨床試験 2011 年 10 月作成 2013 年 1 月改訂 2014 年 4 月改訂 2018 年 4 月改定 2018 年 5 月改定 Ⅰ. 治験審査委員会 (IRB) と連絡先 治験審査委員会名称 治験審査委員会設置者 聖マリアンナ医科大学附属病院等治験審査委員会 St. Marianna University Group Institutional
治験実施に必要な手続きについて (HP 用 ) 治験 製造販売後臨床試験 2011 年 10 月作成 2013 年 1 月改訂 2014 年 4 月改訂 2018 年 4 月改定 2018 年 5 月改定 Ⅰ. 治験審査委員会 (IRB) と連絡先 治験審査委員会名称 治験審査委員会設置者 聖マリアンナ医科大学附属病院等治験審査委員会 St. Marianna University Group Institutional
公益社団法人日本医師会治験促進センターの事業は 国立研究開発法人日本医療研究開発機構 (AMED) の委託研究であり本日はその成果の一部を発表します カット ドゥ スクエアが 実現する電磁化と etmf 対応について 電磁化推進シンポジウム医療機関の治験関連文書の電磁化に係る課題解決に向けて < 東
 公益社団法人日本医師会治験促進センターの事業は 国立研究開発法人日本医療研究開発機構 (AMED) の委託研究であり本日はその成果の一部を発表します カット ドゥ スクエアが 実現する電磁化と etmf 対応について 電磁化推進シンポジウム医療機関の治験関連文書の電磁化に係る課題解決に向けて < 東京会場 >2017 年 10 月 25 日 ( 水 ) 日本医師会館 < 福岡会場 >2017 年 11
公益社団法人日本医師会治験促進センターの事業は 国立研究開発法人日本医療研究開発機構 (AMED) の委託研究であり本日はその成果の一部を発表します カット ドゥ スクエアが 実現する電磁化と etmf 対応について 電磁化推進シンポジウム医療機関の治験関連文書の電磁化に係る課題解決に向けて < 東京会場 >2017 年 10 月 25 日 ( 水 ) 日本医師会館 < 福岡会場 >2017 年 11
製造販売後調査事務手続き等 について
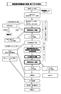 製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
untitled
 1 2 GCP 第 38 条ガイダンスで 実施医療機関の長は治験の実施に関する事務及び支援を行う者を指定し その組織 治験事務局を設けることとなっています また IRB 事務局 (GCP 第 28 条の IRB の事務を行う者 ) は IRB 設置者が指定します IRB 事務局は 治験事務局が兼ねることもできます 治験事務局の役割は 治験の契約手続き等の業務 施設 SOP 作成 治験審査依頼書 の
1 2 GCP 第 38 条ガイダンスで 実施医療機関の長は治験の実施に関する事務及び支援を行う者を指定し その組織 治験事務局を設けることとなっています また IRB 事務局 (GCP 第 28 条の IRB の事務を行う者 ) は IRB 設置者が指定します IRB 事務局は 治験事務局が兼ねることもできます 治験事務局の役割は 治験の契約手続き等の業務 施設 SOP 作成 治験審査依頼書 の
スライド 1
 薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
