(3) その他 本キットは Abbott m2000rt アナライザーの試薬である 用法 用量( 操作方法 ) (1) 試薬の調製方法 1) 所定量の内部コントロールと所定量のライシス溶液を混合する 2) 所定量の酵素試薬に所定量のオリゴヌクレオチド試薬及び活性化試薬を加える この混合溶液をマスター
|
|
|
- しょうじ おまた
- 5 years ago
- Views:
Transcription
1 /R07 この添付文書をよく読んでから使用してください 体外診断用医薬品 2015 年 7 月改訂 ( 第 5 版 ) 2013 年 6 月改訂 ( 第 4 版 ) 製造販売承認番号 22200AMX B 型肝炎ウイルス表面核酸キット アキュジーン m - HBV 全般的な注意 1. 本製品は体外診断用であり それ以外の目的に使用しないこと 2. 診断は 他の関連する検査結果や臨床症状等に基づいて総合的に判断すること 3. 添付文書に記載された使用方法に従って使用すること 本添付文書に記載された使用方法および使用目的以外での使用については 測定結果の信頼性は保証しない 4. 本測定で使用する試薬類には ヒト由来成分が含まれているものがあり 感染の危険があるので感染性のあるものとして取り扱うこと 詳細は 形状 構造等 ( キットの構成 ) または 用法 用量( 操作方法 ) を参照のこと 5. 本測定で使用する試薬類には 保存剤としてアジ化ナトリウムが含まれているものがある 誤って目や口に入れたり皮膚に付着した場合には 水で十分に洗い流す等の応急措置を行い 必要があれば医師の手当て等を受けること 詳細は 形状 構造等 ( キットの構成 ) または 用法 用量( 操作方法 ) を参照のこと 6. 使用する機器の添付文書および取扱説明書をよく読んでから使用すること 形状 構造等( キットの構成 ) 1. 増幅 検出用試薬パック オリゴヌクレオチド試薬 HBV PCR フォワードプライマー HBV PCR リバースプライマー HBV PCR プローブ 1 HBV PCR プローブ 2 dntp 1 Mix 1 dntp: デオキシリボヌクレオシド三リン酸 dntp Mix は以下の 4 成分を有するヌクレオチド-Na の同濃度の混合物である 2 -デオキシアデノシン5 - 三リン酸 (datp) 2 -デオキシシチジン5 - 三リン酸 (dctp) 2 -デオキシチミジン5 - 三リン酸 (dttp) 2 -デオキシグアノシン5 - 三リン酸 (dgtp) ( 他の含有物 : 緩衝液 色素保存剤 : アジ化ナトリウム ProClin 950) 酵素試薬 AmpliTaq Gold 2 DNA ポリメラーゼ 2 AmpliTaq Gold:recombinant Thermus aquaticus ( 他の含有物 : 緩衝液 安定化剤 ) 活性化試薬 ( 主な含有物 : 緩衝液 塩化マグネシウム保存剤 : アジ化ナトリウム ProClin 950) 2. 内部コントロール ( 主な含有物 : 緩衝液 非感染性リニアプラスミド DNA 保存剤 : アジ化ナトリウム ProClin 950) 注 : 増幅 検出用試薬パックを再使用するには バーコードの上に 6 桁のシリアル番号が印字されている増幅 検出用試薬パックが必要である 使用目的 血清又は血漿中の B 型肝炎ウイルス (HBV)DNA の測定 (B 型肝炎ウイルス感染の診断補助 ) 測定原理 本品は HBV DNA の PCR 法 ( ポリメラーゼ連鎖反応法 ) による DNA 合成と増幅 及び核酸ハイブリダイゼーションを用いたヒト血清又は血漿中の HBV DNA を測定するキットであり 以下の 5 つの主な反応ステップから成り立っている 1) 検体からの HBV DNA の抽出 精製検体に核酸抽出用緩衝液 ( 内部コントロールの DNA を含む ) を加え 核酸抽出装置にて 所定の操作を行い HBV DNA を抽出 精製する 2) ポリメラーゼ連鎖反応 (PCR) による HBV DNA の増幅標的 DNA を dntp Mix(dATP dctp dttp dgtp) と HBV PCR フォワードプライマーと HBV PCR リバースプライマーをそれぞれの標的とする配列に結合させ AmpliTaq Gold DNA ポリメラーゼを用いて PCR 反応を行うことにより二本鎖 HBV DNA を増幅する 3) 標識プローブと増幅 DNA とのハイブリダイゼーション熱変性処理により生じた一本鎖 HBV DNA の鋳型 ( アンチセンス )DNA に特異的に結合する蛍光標識した HBV PCR プローブ 1 又は HBV PCR プローブ 2 をハイブリダイズさせる 4) 蛍光強度の測定標的に結合した HBV PCR プローブ 1 又は HBV PCR プローブ 2 からの蛍光強度を測 定波長 505 ~ 535 nm で測定する ( 同時に増幅された内部コントロールの蛍光強度は測定波長 546 ~ 569 nm で測定する ) 5)HBV DNA 濃度の算出検体の Ct 値 (Threshold Cycle 値 ) を 2 濃度のキャリブレータで作成した検量線にあてはめ HBV DNA 量 (IU/mL Log IU/mL Copies/mL 又は Log Copies/mL) を算出する (1 IU = 3.41 Copies 1 Copy = 0.29 IU として換算する ) Ct 値 : 検体の蛍光強度が閾値に達したときのサイクル数 操作上の注意 (1) 測定試料の性質 採取法検体の採取と保存 検体には ヒト血清 ( 血清分離剤入り採血管で採取した血清を含む ) またはヒト血漿 (EDTA ACD 入り ) を使用すること シリカ以外の凝固促進剤またはトロンビン入りの血清用採血管を使用しないこと 採血管の使用に関しては 採血管の製造元の指示に従うこと 採血後の新鮮検体 ( 全血 ) は 遠心分離を行う前に 2 ~ 30 で 6 時間まで保存することができる 遠心分離後は血球を除去すること 血清または血漿検体は 15 ~ 30 で 24 時間まで 2 ~ 8 で 3 日間まで 20 以下で長期保存することができる 検体の凍結融解の繰り返しは避けること また 凍結した検体の融解は 15 ~ 30 または 2 ~ 8 で行うこと 一度融解した検体をすぐに使用しない場合は 2 ~ 8 で 6 時間まで保存することができる 検体の輸送 検体は凍結し ドライアイス中で保存して輸送すること 検体を国内または海外に輸送する場合は 臨床検体 診断目的検体 生物学的検体に対する適切な法規等に対応した包装 表示を行うこと (2) 妨害物質 妨害薬剤潜在的妨害物質 内因性物質が本キットに与える影響を検討した 検討には HBV 陰性サンプルと HBV DNA 2,933 IU/mL を含有するサンプルを使用した 次の濃度の物質を添加したすべての HBV 陽性サンプルおよび HBV 陰性サンプルにおいて 本キットの測定値に影響は認められなかった 物質濃度ヘモグロビン 500 mg/dl トリグリセライド 3,000 mg/dl ビリルビン 20 mg/dl タンパク質 9 g/dl 血漿および血清のピーク値以上の濃度の抗ウイルス剤および抗生物質を 5 群に分けて検討した 次の薬剤群を添加したすべての HBV 陽性サンプルおよび HBV 陰性サンプルにおいて 本キットの測定値に影響は認められなかった 薬剤群 No 薬剤 1 ジドブジン サキナビル リトナビル クラリスロマイシン インターフェロン 2a インターフェロン 2b ジダノシン 2 硫酸アバカビル アンプレナビル ペグインターフェロン 2a ペグインターフェロン 2b リバビリン エンテカビル アデホビル 3 テノホビル ラミブジン インジナビル ガンシクロビル バルガンシクロビル アシクロビル パロキセチン 4 サニルブジン エファビレンツ ロピナビル Enfuvirtide シプロフロキサシン Fluoxetine 5 ザルシタビン ネビラピン ネルフィナビル アジスロマイシン バラシクロビル セルトラリン ここに示したデータは代表的な例であり 各施設の結果とは異なる場合がある 次の DNA ウイルスマーカーが 2 つ以上陽性である患者検体計 15 例を評価した Epstein-barr ウイルス単純ヘルペスウイルス 1 型単純ヘルペスウイルス 2 型サイトメガロウイルス評価した 15 検体すべてにおいて 本キットの測定結果は Not Detected( 検出されず ) であった 交差反応性 次のウイルスおよび微生物との交差反応性について検討した 各微生物またはウイルスの精製核酸 またはウイルス溶解液を HBV DNA 陰性サンプルおよび HBV DNA 2,933 IU/mL を含有するサンプルに添加した ヒト免疫不全ウイルス 1 型ワクチニアウイルスヒト免疫不全ウイルス 2 型ヒトポリオーマウイルス BK ヒト T リンパ球向性ウイルス 1 型ヒト乳頭腫ウイルス 16 型 C 型肝炎ウイルスヒト乳頭腫ウイルス 18 型 A 型肝炎ウイルス淋菌 Epstein-barr ウイルストラコーマクラミジア単純ヘルペスウイルス 1 型カンジダアルビカンス単純ヘルペスウイルス 2 型黄色ブドウ球菌サイトメガロウイルス表皮ブドウ球菌ヒトヘルペスウイルス 6B Mycobacterium gordonae ヒトヘルペスウイルス 8 スメグマ菌水痘 - 帯状疱疹ウイルス試験したすべての HBV 陽性サンプルおよび HBV 陰性サンプルにおいて 本キットの測定値に影響は認められなかった 1
2 (3) その他 本キットは Abbott m2000rt アナライザーの試薬である 用法 用量( 操作方法 ) (1) 試薬の調製方法 1) 所定量の内部コントロールと所定量のライシス溶液を混合する 2) 所定量の酵素試薬に所定量のオリゴヌクレオチド試薬及び活性化試薬を加える この混合溶液をマスターミックスとする 具体的な試薬の調製方法は 使用する核酸抽出装置で異なる (3) 測定 ( 操作 ) 法を参照のこと (2) 必要な器具 器材 試料等 AccuGene m-hbv キャリブレータ ( 製品番号 :2G34-78) キャリブレータ A(1.3 ml 12) ( 主な含有物 : 緩衝液 非感染性 HBV リニアプラスミド DNA 保存剤 : アジ化ナトリウム ProClin 950) キャリブレータ B(1.3 ml 12) ( 主な含有物 : 緩衝液 非感染性 HBV リニアプラスミド DNA 保存剤 : アジ化ナトリウム ProClin 950) キャリブレータの濃度については 付属のキットカードを参照のこと AccuGene m-hbv キャリブレータは本キットに対してのみ使用すること AccuGene m-hbv コントロール ( 製品番号 :2G34-88) 陰性コントロール (1.3 ml 8) ( 主な含有物 : 陰性ヒト血漿 (HBs 抗原陰性 HBV DNA 陰性 HIV RNA 陰性 HCV RNA 陰性 HIV-1/HIV-2 抗体陰性 HCV 抗体陰性 ) 保存剤 :ProClin 300 ProClin 950) 陽性コントロール L(1.3 ml 8) ( 主な含有物 : 陰性ヒト血漿 (HBs 抗原陰性 HBV DNA 陰性 HIV RNA 陰性 HCV RNA 陰性 HIV-1/HIV-2 抗体陰性 HCV 抗体陰性 ) 熱不活化処理済み HBV DNA 陽性血漿保存剤 :ProClin 300 ProClin 950) 陽性コントロール H(1.3 ml 8) ( 主な含有物 : 陰性ヒト血漿 (HBs 抗原陰性 HBV DNA 陰性 HIV RNA 陰性 HCV RNA 陰性 HIV-1/HIV-2 抗体陰性 HCV 抗体陰性 ) 熱不活化処理済み HBV DNA 陽性血漿保存剤 :ProClin 300 ProClin 950) コントロールの濃度については 付属のキットカードを参照のこと AccuGene m-hbv コントロールは本キットに対してのみ使用すること 検体調製 Abbott m2000sp 自動核酸抽出装置 ( 増幅 検出用試薬パックを再使用する場合は ソフトウェアバージョン 6.0 以上 ) DNA 核酸抽出試薬 (Abbott msample Preparation System DNA ) ( 製品番号 :6K12-24):24 回用 4 ライシス溶液 (mlysis DNA ) ( 主な含有物 :TRIS 緩衝液 グアニジンチオシアン酸塩 界面活性剤 ) 洗浄液 1(mWash 1 DNA ) ( 主な含有物 :TRIS 緩衝液 グアニジンチオシアン酸塩 界面活性剤 ) 洗浄液 2(mWash 2 DNA ) ( 主な含有物 : ヌクレアーゼフリー水 ) 溶出液 (melution Buffer DNA ) ( 主な含有物 : ヌクレアーゼフリー水 ) 磁性粒子溶液 (mmicroparticles DNA ) ( 主な含有物 : 磁性粒子 グアニジン塩酸塩 ) プロテアーゼ K PCR グレード (Proteinase K, Recombinant, PCR Grade) ( 製品番号 :3L78-60):24 回用 4(2.45 ml 4) ( 主な含有物 : プロテアーゼ K) m2000 HBV アプリケーションディスク ( 製品番号 :8L35 増幅 検出用試薬パックを再使用する場合は 製品番号 :8L35-04 以降 ) サンプルラック 反応チューブ 5 ml m2000sp 200 ml 試薬容器 マスターミックスチューブ( 製品番号 :4J71-80) 96 ウェルオプティカルリアクションプレート 96 ウェルディープウェルプレート スプラッシュフリーサポートベース オプティカル接着カバー (Abbott Optical Adhesive Cover) 接着カバーアプリケータ mm 丸底サンプルチューブ ボルテックスミキサー ポリプロピレン製遠心チューブ 50 ml 2,000 g の出力可能な遠心機 分注量 10 ~ 1,000μL の較正済みピペット 分注量 20 ~ 1,000μL のピペット用フィルター付きピペットチップ 95 ~ 100% エタノール変性剤を含有するエタノールは 使用しないこと アキュジーン試薬ボトル交換用キャップ ( 製品番号 :3N20-01) メスピペット メスシリンダー 100 ml 分子生物学グレード水 1.7 ml 分子生物学グレードマイクロチューブ 綿棒 注 : 施設の汚染のモニタリングに使用する (3) 測定 ( 操作 ) 法 7. 汚染のモニタリングを参照のこと 増幅 m2000 HBV アプリケーションディスク ( 製品番号 :8L35 増幅 検出用試薬パックを再使用する場合は 製品番号 :8L35-04 以降 ) m2000rt オプティカルキャリブレーションキット ( 製品番号 :4J71-93) その他の器具 規格を満たしている安全キャビネット チャック付きビニール袋 (3) 測定 ( 操作 ) 法 核酸抽出装置として Abbott m2000sp 自動核酸抽出装置 又は弊社の指定した同等品 1 を用いること 使用する核酸抽出装置に応じた試薬を別途用意すること 1) 血清又は血漿 (0.5 ml 又は 0.2 ml) から 使用する核酸抽出装置にて所定の操作 ( 内部コントロール 3μL を含む混合液を加える ) を行い 核酸抽出液を得る 2)96 ウェルオプティカルリアクションプレートに1ウェル当たりマスターミックス 50μL 及び核酸抽出液 50μL を分注する 3) 専用の遺伝子解析装置 Abbott m2000rt アナライザー に 96 ウェルオプティカルリアクションプレートをセットし PCR 反応を繰り返し 測定波長 505 ~535 nm における蛍光強度を測定する 4)HBV DNA の Ct 値 (Threshold Cycle 値 ) を 2 濃度のキャリブレータで作成した検量線にあてはめ HBV DNA 量 (IU/mL Log IU/mL Copies/mL 又は Log Copies/mL) を算出する 核酸抽出装置 Abbott m2000sp 自動核酸抽出装置 DNA 核酸抽出試薬と遺伝子解析装置 Abbott m2000rt アナライザー を用いた場合の手順を示す 反応槽 核酸抽出用緩衝液 2150μL 2 内部コントロール : ライシス溶液 = 0.1 ml:70 ml で調製 検体 ( 血清又は血漿 )0.5 ml 又は 0.2 ml プロテアーゼ K 溶液 3 1, ml 3 プロテアーゼ K PCR グレード : 分子生物学グレード水 = 2.45 ml:17.15 ml で調製 核酸抽出用緩衝液 1.95 ml 磁性粒子溶液 40μL DNA 抽出 磁性粒子への吸着 DNA 結合粒子 洗浄液 ml 2 洗浄液 ml ml 2 DNA 結合粒子 溶出液 110μL 核酸抽出液 (70μL) 96 ウェルオプティカルリアクションプレート 核酸抽出液 50μL マスターミックス 4 50μL オリゴヌクレオチド試薬 (0.918 ml) 4 活性化試薬 (0.357 ml) 酵素試薬 (0.081 ml) 転写及び増幅反応 92.5 で 10 分...1 サイクル 92.5 で 30 秒 57 で 60 秒...45 サイクル各サイクルでの蛍光強度測定 ( 測定波長 :505 ~ 535 nm) HBV DNA 濃度算出 1 同等品の核酸抽出装置を使用する場合は 使用する機器の取扱説明書等を参照すること ( 参考 ) 操作法 1. 増幅 検出用試薬パックの再使用増幅 検出用試薬パックを再使用する場合の概要図を示す 増幅 検出用試薬パックは必要に応じて再使用することができる 一度使用したマスターミックス調製済みの増幅 検出用試薬パックは キャップを閉めて遮光し 2 ~ 8 で保存した場合 次回使用するまで最大 14 日間保存することができる 内部コントロールについても バイアルのキャップを閉めて 2 ~ 8 で保存した場合 次回使用するまで最大 14 日間保存することができる 増幅 検出用試薬パックの再使用については Abbott m2000sp 自動核酸抽出装置の取扱説明書でも説明されている 増幅 検出用試薬パックの再使用は サンプル調製を Abbott m2000sp 自動核酸抽出装置で行う場合にのみ可能である 本添付文書で使用する用語の定義増幅 検出用試薬パックと内部コントロールはそれぞれ 2 回まで使用することができる 本添付文書では 未使用の増幅 検出用試薬パックと内部コントロールを 新しい増幅 検出用試薬パック 新しい内部コントロールと表現する ( すなわち使用 1 回目 ) 一度使用したマスターミックス調製済みの増幅 検出用試薬パックは 再使用する増幅 検出用試薬パックと表現する 一度使用した内部コントロールのバイアルは 再使用する内部コントロールバイアルと表現する 2
3 増幅 検出用試薬パックを再使用する場合の概要増幅 検出用試薬パックと内部コントロールは計 2 回使用することができる マスターミックスを調製していない未使用の増幅 検出用試薬パックは 新しい増幅 検出用試薬パックと表現する 一度使用したマスターミックス調製済みの増幅 検出用試薬パックは 再使用する増幅 検出用試薬パックと表現する その他の詳細は 本添付文書の指示に従うこと 保存条件 ( 増幅 検出用試薬パックおよび内部コントロールバイアル ) 対象 保存温度 使用期限 新しい増幅 検出用試薬パック 10 以下 試薬キットの使用期限まで 新しい内部コントロール 10 以下 試薬キットの使用期限まで 再使用する増幅 検出用試薬パック 2 ~ 8 ( 遮光下 ) 初回使用日から 14 日間まで 再使用する内部コントロール 2~8 初回使用日から 14 日間まで 増幅 検出用試薬パックの再使用は バーコードの上に 6 桁のシリアル番号が印字されている増幅 検出用試薬パックでのみ可能である 再使用する増幅 検出用試薬パックは 1 回目に使用した時と同じ機器でのみ再使用可能である 2 回目に違う機器を使用するとエラーになり 結果的にサンプルの調製が遅れる可能性がある 再使用する増幅 検出用試薬パックと新しい増幅 検出用試薬パックは 同時に機器にセットすることができる ただし 増幅 検出用試薬パックのロット番号が同じでなければならない 3
4 2. 測定手順 初めて測定を行う場合 m2000 HBV アプリケーションディスクからアプリケーションファイルを使用する機器にインストールすること 増幅 検出用試薬パックを再使用する場合は 製品番号 :8L35-04 以降の m2000 HBV アプリケーションディスクから再使用機能付きのアプリケーションファイルをインストールすること インストール方法の詳細については 使用する機器の取扱説明書を参照のこと 核酸抽出を始める前に 本添付文書の指示をよく読むこと 増幅 検出用試薬パックと内部コントロールはそれぞれ 2 回まで使用することができる キャリブレータ 陰性コントロール 陽性コントロール L および H のバイアルは使い捨てのため 使用後は廃棄すること サンプルチューブ内の泡の有無を確認すること 泡がある場合 滅菌ピペットチップで取り除くこと 試薬の泡は 試薬容器内での正確な試薬量の検知を妨げる可能性がある その結果 試薬が十分に吸引されず 測定結果に影響を与える可能性がある チューブごとに新しい滅菌ピペットチップを使用して サンプル間の交差汚染をおこさないように注意すること ピペッティングの際は 使い捨てのフィルター付きピペットチップまたはピペットを使用すること ピペッティング中のピペットの汚染を防止するため ピペット本体がサンプルチューブや容器の内側に接触しないように注意すること また 十分な長さのフィルター付きピペットチップを使用すること 増幅産物のモニタリングについての詳細は 7. 汚染のモニタリングを参照のこと 核酸汚染の危険性を低減するため 検体がこぼれた場合は 1.0% 次亜塩素酸ナトリウムやその他の適切な消毒液で拭き取るなどして 清掃および除染すること 検量線は 検体の測定前に作成すること 本キットの測定には キャリブレータとコントロールを必ず使用すること 詳細は 4. キャリブレーションおよび 6. 陰性コントロールと陽性コントロールを参照のこと 重要: 再使用する増幅 検出用試薬パックは マスターミックス分注のプロトコール終了後 60 分以内に 2 ~ 8 に保存すること プロトコール 検体調製区域 すべての検体の保存と調製は 検体調製区域内で行うこと 検体調製を行う前に 使用上又は取扱い上の注意 (2) 使用上の注意を参照のこと 機器の操作方法についての詳細は 使用する機器の取扱説明書を参照のこと 使用する機器の操作は トレーニングを受けた者が行うこと オペレータは アプリケーションについてよく理解し 施設の基準に従うこと 1. 1 回の測定につき 最高 48 サンプルの測定が可能である 各測定ごとに陰性コントロール 陽性コントロール L および H を各 1 本測定するため 1 回の測定につき 最高 45 検体の測定が可能である 注 :24 サンプル以上の処理を行う場合 廃棄物があれば測定前に固形廃棄物容器を空にし 新しいバイオハザードバッグに交換すること サンプル量を確認する 最少サンプル量と Abbott m2000sp 自動核酸抽出装置のラック要件を次に示す アッセイ最少サンプル量アッセイアプリケーションラックチューブの直径 0.2 ml 0.5 ml 13 mm 11.5 ~ 14.0 mm 0.4 ~ 0.8 ml 0.7 ~ 1.2 ml 16 mm 14.5 ~ 16.0 mm 0.4 ~ 1.0 ml 0.8 ~ 1.4 ml サンプルチューブの外径 最少サンプル量は チューブの形状やサイズにより異なる 推奨サンプル量については Abbott m2000sp 自動核酸抽出装置の取扱説明書を参照のこと 凍結した検体の融解は 15 ~ 30 または 2 ~ 8 で行うこと 一度融解した検体をすぐに使用しない場合は 2 ~ 8 で 6 時間まで保存する 検体は使用前に ボルテックスミキサーで 1 回 2 ~ 3 秒間 3 回攪拌すること 泡が生成されていないことを確認すること 泡があるときは チューブごとに新しい滅菌ピペットチップで取り除くこと 不溶物または濁りがある検体は 測定前に 2,000 g で 5 分間遠心分離し 上清を使用すること 必要に応じて 検体を清潔なチューブまたはバイアルに分取すること チューブのサイズについては Abbott m2000sp 自動核酸抽出装置の取扱説明書を参照のこと チューブを開封する際は キャップの内側に接触しないこと 2. コントロールを 15 ~ 30 または 2 ~ 8 で融解する キャリブレーションを行う場合は キャリブレータを 15 ~ 30 または 2 ~ 8 で融解すること 詳細は 4. キャリブレーションを参照のこと 新しい内部コントロールを使用する場合は バイアル 1 本を 15 ~ 30 または 2 ~ 8 で融解する 一度融解したキャリブレータ コントロール 新しい内部コントロールをすぐに使用しない場合は 2 ~ 8 で 24 時間まで保存することができる キャリブレータとコントロールは 使用前にボルテックスミキサーで 1 回 2 ~ 3 秒間 3 回攪拌すること 泡が生成されていないことを確認すること 泡があるときは チューブごとに新しい滅菌ピペットチップで取り除くこと 攪拌後 各バイアルを作業台の上で軽く叩き 内容液をバイアルの底部に移動させる 内容物が底にあることを確認する 3. 機器にセットする新しい増幅 検出用試薬パックや再使用する増幅 検出用試薬パックを選ぶ 増幅 検出用試薬パックの残量管理方法については Abbott m2000sp 自動核酸抽出装置の取扱説明書を参照すること 増幅 検出用試薬パックはロット番号が同じでなければならない サンプルの数に対して 必要な増幅 検出用試薬パックの数を次の表に示す 増幅 検出用試薬パックの必要数 1 ~ 24 サンプル 25 ~ 48 サンプル 新しい増幅 検出用試薬パックの場合 1 個 再使用する増幅 検出用試薬パックの場合最大 4 個 内部コントロール 新しいバイアル 1 本または再使用するバイアル 1 本 新しい増幅 検出用試薬パックの場合 2 個 再使用する増幅 検出用試薬パックの場合最大 4 個 増幅 検出用試薬パックの残量を管理し 再使用する増幅 検出用試薬パックで測定できるサンプル数を把握する方法は Abbott m2000sp 自動核酸抽出装置の取扱説明書を参照すること 再使用する増幅 検出用試薬パックは 1 回目に使用した時と同じ Abbott m2000sp 自動核酸抽出装置でのみ使用可能である 2 回目に違う機器を使用するとエラーになるため 結果としてサンプルの調製が遅れる可能性がある 再使用する増幅 検出用試薬パックと新しい増幅 検出用試薬パックは同時に機器にセットすることができる ただし 増幅 検出用試薬パックのロット番号はすべて同じでなければならない マスターミックスを調製するまでに 新しい増幅 検出用試薬パックを 15 ~ 30 または 2 ~ 8 で融解する 本ステップ ( ステップ 3) は 核酸抽出手順の終了前に開始することができる 注 : 増幅 検出用試薬パックをボルテックスミキサーで攪拌しないこと 一度融解した新しい増幅 検出用試薬パックをすぐに使用しない場合は キャップを閉めた状態で 2 ~ 8 で 24 時間まで保存することができる 注 : 再使用する増幅 検出用試薬パックは 2 回目の使用直前まで 2 ~ 8 で保存しておくこと 2 ~ 8 の保存場所から取り出した後は 室温での積算時間が 25 分を超えないようにすること この積算時間には 取り出してから使用するまでの時間も含まれる 増幅 検出用試薬パックを室温に出した後 25 分を超えた場合は廃棄すること 4. プロテアーゼ K PCR グレードを開封する 分子生物学グレード水 ml を 50 ml ポリプロピレン製遠心チューブに分注する プロテアーゼ K PCR グレード 2.45 ml を分子生物学グレード水が入った容器に分注する 穏やかに 10 ~ 15 回転倒混和する プロテアーゼ K PCR グレードのバーコードラベルを貼付した試薬容器に すべての内溶液を移す 試薬容器を試薬容器キャリア #1 のポジション 2 にセットする サンプル数に対して 必要な核酸抽出試薬と内部コントロールの数を次の表に示す 核酸抽出試薬 内部コントロールの必要数試薬 / コントロール 1 ~ 24 サンプル 25 ~ 48 サンプルプロテアーゼ K PCR グレード 1 本 2 本磁性粒子溶液 1 本 1 本ライシス溶液 1 本 2 本洗浄液 1 1 本 2 本洗浄液 2 1 本 2 本溶出液 1 本 2 本 新しいバイアル 1 本または再使用するバイアル 2 本 内部コントロールは新しいバイアルと再使用するバイアルを一緒に使用することもできる 5. DNA 核酸抽出試薬を開封する 各試薬ボトルの開封時に結晶が見られる場合は 結晶がなくなるまで室温で溶解させること 結晶が溶解されるまで試薬を使用しないこと 6. DNA 核酸抽出試薬の Product Information に従って 95 ~ 100% エタノール 70 ml を洗浄液 2 のボトルに分注し 洗浄液 2 を調製する 変性剤を含有するエタノールは使用しないこと 7. 内部コントロールのバイアルは 使用前にボルテックスミキサーで 1 回 2 ~ 3 秒間 3 回攪拌すること 8. 較正済みの内部コントロール専用ピペットのみを使用し 内部コントロール 100μL をライシス溶液のボトルに添加する 泡の生成を抑えるため 容器を穏やかに 5 ~ 10 回転倒混和すること 残った内部コントロールはバイアルのキャップを閉めて 2 ~ 8 で保存し 再使用することができる 9. DNA 核酸抽出試薬のすべてのボトルを穏やかに転倒混和する 溶液が均一になっていることを確認し Abbott m2000sp 自動核酸抽出装置の取扱説明書に従って溶液を適切な試薬容器に注ぐ 10. 患者検体 陽性コントロール L および H 陰性コントロール 必要に応じてキャリブレータを m2000sp サンプルラックにセットする 11. m2000sp 用の反応チューブ5 ml をサブシステムキャリアにセットする 12. Abbott m2000sp 自動核酸抽出装置の取扱説明書に従い DNA 核酸抽出試薬およびプロテアーゼ K 溶液をセットした試薬容器キャリアと 96 ウェルディープウェルプレートをワークテーブルにセットする 13. < Run Sample Extraction > 画面で サンプル量に合った適切なアプリケーションファイルを選択する Abbott m2000sp 自動核酸抽出装置の取扱説明書に従って核酸抽出のプロトコールを開始する キャリブレータとコントロールのロット固有の値を< Sample Extraction:Assay Details > 画面に入力する ( 検量線がすでに Abbott m2000rt アナライザーに保存されている場合は キャリブレータの値の入力は不要である ) ロット固有の値は キャリブレータおよびコントロールのキットカードに記載されている 4
5 注 : 入力した値と キットカードに記載されている値が一致していることを確認する マスターミックス分注のプロトコール ( ステップ 14) は 核酸抽出のプロトコール終了後 60 分以内に開始すること 注 : 増幅 検出用試薬パックを取り扱う前に手袋を交換すること 14. 核酸抽出終了後 増幅 検出用試薬パックとマスターミックスチューブ ( 必要に応じて ) をワークテーブルにセットする 増幅 検出用試薬パックを 1 個しか使用しない場合はマスターミックスチューブは必要ない 新しい増幅 検出用試薬パックは 使用前に完全に融解していることを確認する 新しい増幅 検出用試薬パックを開封する前に 試薬パックを垂直に持って作業台の上で軽く叩き 溶液をバイアルの底に落とす 溶液がバイアルの底にあることを確認すること 再使用する増幅 検出用試薬パックは 作業台の上で叩かないこと 叩くことでマスターミックスがキャップに飛んで付着し 液量が減る恐れがある キャップを外す 次回使用するために新しい増幅 検出用試薬パックを保存したい場合は 分注プロトコール終了後に各試薬バイアルのキャップを閉める必要がある 試薬バイアルに付いていたキャップを使う場合は 外したキャップを保管しておく 別の新しいキャップを使う場合は 外したキャップを廃棄してよい 増幅 検出用試薬パックを Abbott m2000sp 自動核酸抽出装置のワークテーブルにセットする際は 再使用する増幅 検出用試薬パックを新しい増幅 検出用試薬パックの左側にセットすること 増幅 検出用試薬パックが機器に確実にセットされていることを確認する 15. 適切な 96 ウェルディープウェルプレートを 該当する核酸抽出と一致する< Run Master Mix Addition > 画面から選択する マスターミックスの分注プロトコールを開始する Abbott m2000sp 自動核酸抽出装置の取扱説明書を参照のこと Abbott m2000rt アナライザーのプロトコール ( ステップ 20) は マスターミックス分注のプロトコール ( ステップ 15) 終了後 60 分以内に開始すること 増幅区域 16. 増幅区域内に設置されている Abbott m2000rt アナライザーの電源を入れ 初期化を行う 初期化には 15 分を要する 注 : 検体調製区域に戻る前に 手袋を外すこと 検体調製区域 17. Abbott m2000sp 自動核酸抽出装置でのサンプルとマスターミックスの分注完了後 Abbott m2000sp 自動核酸抽出装置の取扱説明書に従って 96 ウェルオプティカルリアクションプレートをオプティカル接着カバー (Abbott Optical Adhesive Cover) で密封する ウェルオプティカルリアクションプレートを Abbott m2000rt アナライザーに移動させるため スプラッシュフリーサポートベースにセットする 19. 終了した 96 ウェルオプティカルリアクションプレートの結果を CD またはネットワーク ドライブに保存する 増幅区域 20. Abbott m2000rt アナライザーに 96 ウェルオプティカルリアクションプレートをセットする Abbott m2000rt アナライザーの取扱説明書に従い CD またはネットワーク ドライブから Abbott m2000sp 自動核酸抽出装置で作成したテストオーダーを取り込む 検体調製区域 21. 調製済みのマスターミックスが残っている増幅 検出用試薬パックを次回に再使用する場合は 保管しておいたキャップまたは新しいキャップ ( 製品番号 :3N20-01) で 3 本の試薬バイアルの蓋を閉め 直ちに真っすぐに立てた状態で遮光して 2 ~ 8 で保存すること 空になった増幅 検出用試薬パックや 2 回使用した増幅 検出用試薬パックはすべて廃棄する 重要 : 増幅 検出用試薬パックを次回も使用する場合は マスターミックス分注プロトコール終了後 1 時間以内に 2 ~ 8 で保存すること 測定後の手順 ウェルディープウェルプレートをワークテーブルから取り外し Abbott m2000sp 自動核酸抽出装置の取扱説明書に従って廃棄する 23. Abbott m2000rt アナライザーの取扱説明書に従い 96 ウェルオプティカルリアクションプレートをプレートを取り扱う際に使用した手袋と共にチャック付きビニール袋に入れ 廃棄する 24. Abbott m2000rt アナライザーの取扱説明書に従い スプラッシュフリーサポートベースを次回使用前に清掃すること 3. 試薬の劣化判定陽性または陰性コントロールの測定値が管理範囲を外れている場合 試薬が劣化している可能性がある 得られた測定結果は無効とし 再測定を行うこと 必要に応じて再キャリブレーションを行うこと 4. キャリブレーション m2000rt オプティカルキャリブレーション m2000rt オプティカルキャリブレーションの方法についての詳細は Abbott m2000rt アナライザーの取扱説明書を参照のこと 正確な蛍光色素の測定と識別を行うために 本キットの測定には Abbott m2000rt アナライザーのオプティカルキャリブレーションを行う必要がある 本測定では 次の m2000rt オプティカルキャリブレーションプレートを使用して Abbott m2000rt アナライザーを較正する FAM プレート ( カルボキシフルオレセイン ) ROX プレート ( カルボキシ -X- ローダミン ) VIC プレート ( 情報非公開の色素 ) アッセイキャリブレーション 検量線は 検体とコントロールの HBV DNA を定量化するために必要である 検量線 ( 蛍光強度が閾値に達した時の Threshold cycle(ct) 値に対する HBV 濃度 [Log IU /ml]) 作成では キャリブレータ A B を3 重測定する キャリブレータ A およびキャリブレータ B のロット固有の値は キャリブレータのキットカードに記載されている キャリブレーションを行う際には テストオーダーに必ず入力すること 検量線の傾きと切片は 機器上で算出された後 保存される サンプル中の HBV DNA 濃度は 検量線を基に算出される 測定結果は 自動的に Abbott m2000rt アナライザーのシステムコントロールセンター (SCC) に表示される キャリブレーションを行う際は 陽性コントロール L および H 陰性コントロールを測定すること 核酸抽出 試薬分注 増幅と検出のプロトコールの手順については 使用する機器の取扱説明書を参照のこと 最終的なコントロールの測定値が コントロールのキットカードに記載されている管理範囲に入っていることを確認する 一度キャリブレーションが保存されると 6 ヶ月間使用することができる この間 次の場合を除いて 以後処理する検体はキャリブレーションを行わなくても測定することができる 新しいロット番号の本キットを使用する場合 新しいロット番号の DNA 核酸抽出試薬を使用する場合 異なるサンプル量のアプリケーションファイル ( プロトコール ) を使用する場合 新しいアプリケーションファイル ( プロトコール ) をインストールした場合 5. 阻害の検出 キャリブレーションでは 内部コントロールの Threshold cycle(ct) アッセイパラメータの規格が設定される 検体処理の正確さと測定の有効性を評価するため 核酸抽出開始時に 規定量の内部コントロールが検体 キャリブレータ コントロールへ分注され 測定される 内部コントロールは HBV DNA 配列とは無関係の DNA 配列で構成されている キャリブレーションサンプル中の内部コントロールの標的配列の蛍光信号が検出される増幅サイクル中央値によって 以後処理する全検体に対する内部コントロール Ct 値の管理範囲が検量線により設定される 検体またはコントロールが規格を外れた場合 エラーが表示される エラーコードの対策についての詳細は Abbott m2000rt アナライザーの取扱説明書を参照のこと 内部コントロールの Ct 値が管理範囲を超える検体は 核酸抽出のステップから再測定を行うこと 6. 陰性コントロールと陽性コントロール 各測定ごとに陰性コントロール 陽性コントロール L および H を各 1 本測定して 測定の有効性を評価する 陽性コントロール L および H のロット固有の値は コントロールのキットカードに記載されている 測定の際には テストオーダーに必ず入力すること コントロール値が管理範囲を外れている場合は エラーが表示される エラーコードの対策についての詳細は Abbott m2000rt アナライザーの取扱説明書を参照のこと 陰性または陽性コントロールが管理範囲に入っていない場合 その測定で使用したすべての検体とコントロールは 核酸抽出のステップから再処理を行うこと 陰性コントロールでは HBV DNA は検出されない 陰性コントロールで HBV DNA が検出された場合 核酸抽出または 96 ウェルオプティカルリアクションプレートの調製の過程で 他のサンプルまたは増幅産物によりコントロールが汚染したことを示す 汚染を防ぐためには 機器の清掃を行い 2. 測定手順に従って コントロールと検体を用いて再処理を行うこと 陰性コントロールが一貫して陽性を示す場合は 弊社へご連絡ください 7. 汚染のモニタリング増幅産物による作業場所や器具の汚染をモニタリングするため 少なくとも月に 1 回は汚染の有無の確認を行うこと 調製した検体 コントロール キャリブレータまたは増幅産物にさらされた可能性があるすべての区域を確認すること 日常的に使用するピペット 機器のファンクションキー 作業台表面 マイクロ遠心機およびローターなどの器具も確認すること 1. 分子生物学グレード水 0.8 ml を 1.7 ml 分子生物学グレードマイクロチューブに分注する 2. マイクロチューブの分子生物学グレード水に 綿棒を浸す 3. 分子生物学グレード水が染みこんだ綿棒を使用して モニタリング区域を軽くこするように拭く 綿棒をマイクロチューブに入れる 4. 綿棒を分子生物学グレード水中で 10 回転させた後 液がマイクロチューブの底に戻るようにマイクロチューブの内側に沿って押し付ける その後 綿棒は廃棄する 5. 内部コントロール専用のピペットを使用し 洗浄液 1:0.5 ml を新しいチューブに分注する 6. 洗浄液 1:20μL を各マイクロチューブに分注する 7. マイクロチューブのキャップを閉める 8. サンプルを測定する 詳細は 2. 測定手順を参照のこと 9. マイクロチューブ内の溶液を反応チューブ 5 ml へ移す 10. 分子生物学グレード水を足して 容量を 1.5 ml にする 11. 綿棒の拭き取りサンプルから HBV DNA が検出された場合 汚染が存在していることを示す 5
6 12. 器具から HBV DNA が検出された場合の清掃と除染の方法については 使用する器具の取扱説明書を参照のこと 作業場所から HBV DNA が検出された場合 汚染区域を 1.0% 次亜塩素酸ナトリウム溶液で拭いた後 70% エタノールまたは水で拭くこと 注 : 塩素溶液により器具や金属が腐食する可能性がある 残留している塩素がなくなるまで 70% エタノールまたは水を使用して拭き取ること 13. ステップ 1 ~ 10 に従って汚染区域の確認を繰り返すこと 測定結果の判定法 (1) 算出サンプルまたはコントロール中の HBV DNA 濃度は 保存されている検量線または同一測定内で作成された検量線を基に計算される 結果は 自動的に Abbott m2000rt アナライザーのシステムコントロールセンターに表示される 測定結果の単位は IU/mL または Log IU/mL で表示される また 結果は換算係数 3.41 を用いて Copies/mL または Log Copies/mL でも表示することができる (1 IU = 3.41 Copies) 注 : 本キットは WHO International Standard for HBV DNA 3 で較正されている 換算係数 3.41 は 測定範囲における換算係数の平均値に基づいている (2) 測定結果の表示と判定 検体量 結果 判定 0.5 ml Not Detected 検出されず < 1.00 Log IU/mL a 検出 ( 最小検出感度未満 ) c 1.00 ~ 9.00 Log IU/mL 濃度表示される d > 9.00 Log IU/mL 定量上限を超える e 0.2 ml Not Detected 検出されず < 1.18 Log IU/mL b 検出 ( 最小検出感度未満 ) c 1.18 ~ 9.00 Log IU/mL 濃度表示される d > 9.00 Log IU/mL 定量上限を超える e a 10 IU/mL b 15 IU/mL c HBV DNA は定量化できない d 算出された測定結果は測定範囲内である 測定結果が数値で得られた場合 Interpretation 欄は空欄である e 測定単位が IU/mL の場合には ">1,000,000,000 IU/mL HBV DNA." と表示される 判定上の注意 正しい測定結果を得るためには 適切な検体採取 保存 輸送を行う必要がある ( 詳細は 操作上の注意 (1) 測定試料の性質 採取法を参照のこと ) 検体は ヒト血清 ( 血清分離剤入り採血管で採取した血清を含む ) または血漿 (EDTA ACD 入り ) を使用すること 本キットでは 他の抗凝固剤の使用について評価されていない シリカ以外の凝固促進剤またはトロンビン入りの血清用採血管で採取した検体を使用した場合 正しい結果が得られない可能性がある そのため シリカ以外の凝固促進剤またはトロンビン入りの血清用採血管を使用しないこと 本キットには シリカ以外の凝固促進剤またはトロンビンの入っていない血清用採血管および血清分離剤入り採血管 または血漿 (EDTA ACD 入り ) を使用すること 使用する機器と測定方法により 増幅産物による汚染の危険性は低減される しかし 施設の基準と本添付文書に記載された手順を遵守して キャリブレータ 陽性コントロール 検体による核酸汚染の管理を必ず行うこと 非常に高値の検体を測定した場合 交差汚染により まれに他の検体が極低値の陽性結果を示すおそれがあるので 取扱いに注意すること 主な検討結果では キャリーオーバーは 0 ~ 2% の範囲内であった 海外の治療ガイドラインによると 患者の管理に影響を及ぼすには 1 log の測定値上昇が必要である 4, 5 さらに ガイドラインでは患者管理の変更条件として 2 度の連続した測定値上昇が求められている 6 本キットで Not Detected( 検出されず ) と判定された場合でも HBV DNA が存在しないことを保証するものではない 本キットは 血液 血漿または組織提供者の HBV スクリーニング検査には使用できない また 本キット単独で HBV 感染の確定診断をすることはできない 他の診断テストと同様 測定結果は他の関連する臨床所見や臨床検査等と合わせて総合的に判断すること 性能 本キットを用いて 管理パネルを試料として 8 重測定を行い 少なくとも 7 つの測定値から中央値を計算し パネルの表示値との差を計算した結果 その差は 0.11 ~ 0.15 Log IU/mL の範囲内 であった ここで示したデータは代表的な例であり 各施設の結果とは異なる 次に示す本キットの性能は 検体量 0.5 ml で検討した ( 特記されている場合を除く ) (1) 最小検出感度最小検出感度は 95% 以上の確率で検出される HBV DNA 濃度とした 1. 検体量 0.5 ml の最小検出感度検体量 0.5 ml の最小検出感度は 10 IU/mL である 本キットの最小検出感度は WHO International Standard for Hepatitis B Virus DNA (NIBSC code 97/746) 3 を HBV 陰性ヒト血漿で希釈したサンプルを用いて検討した 本キット 3 ロットを用いて Abbott m2000sp 核酸抽出装置および Abbott m2000rt アナライザー各 3 台の機器で試験を行った 結果を次に示す ここに示したデータは代表的な例である 表 1 濃度 (IU/mL) 測定数 検出数 検出率 (%) プロビット解析 7 では 95% の確率で検出される HBV DNA 濃度は 6.40 IU/mL (95% 信頼区間 :3.97 ~ IU/mL) であった 2. 検体量 0.2 ml の最小検出感度 検体量 0.2 ml の最小検出感度は 15 IU/mL である 検討は 検体量 0.5 ml と同様 に行った 結果を次に示す ここに示したデータは代表的な例である 表 2 濃度 (IU/mL) 測定数 検出数 検出率 (%) プロビット解析では 95% の確率で検出される HBV DNA 濃度は IU/mL(95% 信頼区間 :7.11 ~ IU/mL) であった (2) 直線性本キットの定量上限は 1,000,000,000 IU/mL であり 定量下限は最小検出感度と同等 ( 検体量 0.5 ml:10 IU/mL 検体量 0.2 ml:15 IU/mL) である HBV 陰性ヒト血漿で HBV 陽性検体を 9.13 ~ 0.29 Log IU/mL の範囲で希釈した 13 例のパネルを測定した 各パネルは 6 重測定 (3 重測定を計 2 回 ) した 0.29 Log IU/mL のパネルでは HBV が検出されなかった測定が 1 回あり この測定はデータ解析から除外した 結果を次に示す ここに示したデータは代表的な例である CLSI EP6-A 8 に従って 最小二乗直線回帰分析を行った 本キットは 検討を行った血漿 HBV DNA 濃度の範囲で直線性を示した 図 1 本キットの直線性 (3) 再現性 8 例の HBV DNA パネルを調製し 本キットの検体量 0.5 ml の再現性を評価した 高値の患者検体を陰性ヒト血漿で希釈し パネル 1, 4, 6, 8 を調製した 高値の患者検体を陰性ヒト血清で希釈し パネル 2, 3, 5, 7 を調製した 本キット 3 ロットを使用して Abbott m2000sp 核酸抽出装置および Abbott m2000rt アナライザー各 3 台で測定した パネルは 5 日間にわたり 3 重測定で計 15 回測定した CLSI EP10-A2 9 に従って解析を行い 測定内 測定間 アッセイ間 ( 測定内 測定間 ) の標準偏差を算出した 結果を次に示す ここに示したデータは代表的な例である 本キットのアッセイ間の標準偏差 (SD) は HBV 濃度が 26 ~ 278,000,000 IU/mL のサンプルにおいて HBV DNA が 0.25 Log IU/mL 以下である 6
7 パネル n 平均濃度 (IU/mL) 表 3 本キットの再現性 平均濃度 (Log IU/mL) 測定内 SD a 測定間 SD a アッセイ間 SD a,b , , , ,425, ,815, ,687, a 標準偏差を Log IU/mL で示す b アッセイ間 SD は 測定内成分と測定間成分を含んでいる (4) 特異性 本キットにおける特異性は 99.5% 以上である HBV 陰性血清検体 59 例および HBV 陰性血漿検体 58 例を測定して特異性を評価した 本キット 3 ロットを使用して Abbott m2000sp 核酸抽出装置および Abbott m2000rt アナライザー各 1 台で測定した HBV DNA は検出されず 特異性は 100%(117/117) であった ( 二項分布に基づく 95% 信頼区間 :96.90 ~ %) (5) キャリーオーバー陰性サンプルと陰性サンプルの間に高コピー HBV 陽性サンプルを測定し キャリーオーバーの検討を 3 回行なった 検討で使用した高コピー HBV 陽性サンプルは 8 log IU/mL を超えていた これらの検討結果では キャリーオーバーは 0 ~ 2% の範囲内であった LoD 以上のみをキャリーオーバーとした場合には 全体のキャリーオーバーの割合は 0.63%(95% 信頼区間 0.08 ~ 2.24%) であった これら3 回の検討の結果を次に示す 表 4 本キットのキャリーオーバー 検討 測定回数 陰性サンプル数 検出数 検出率 (%) 検出数 (>LoD) 検出率 (%) (>LoD) 検出率の 95% 信頼区間 (0.00, 3.62) (0.24, 7.04) (0.00, 3.03) 全体 (0.08, 2.24) (6) 各 HBV 遺伝子型検体の評価 HBV 遺伝子型判定済み検体を用いた本キットの性能を 2 種類の試験で評価した 1 つ目の試験では 遺伝子型 A ~ H 各 1 検体の合計 8 検体を 4.47 Log IU/mL 3.47 Log IU/mL 2.47 Log IU/mL 1.17 Log IU/mL になるように希釈し 希釈直線性試験を行なった 各遺伝子型 各濃度について 3 重測定を行なった 主な結果の最小二乗直線回帰分析を次に示す 相関係数は ~ であった 図 2 本キットの各遺伝子型の評価 ( 希釈直線性 ) 2 つ目の試験では 各遺伝子型を含む合計 33 検体を測定した 結果を次に示す また 最小二乗回帰分析を用いた本キットと A 社キットの測定結果の相関を示す 検討は CLSI EP9-A2 10 に従って行った 表 5 HBV 遺伝子型 検体数 検出数 検出率 (%) A B C D E F G H 合計 図 3 本キットの各遺伝子型の評価 (7) 測定範囲検体量 0.5 ml の場合は 10 ~ 1,000,000,000 IU/mL (1.00 ~ 9.00 Log IU/mL) 検体量 0.2 ml の場合は 15 ~ 1,000,000,000 IU/mL (1.18 ~ 9.00 Log IU/mL) である 測定範囲の下限は 最小検出感度である (8) 相関性試験成績及び較正用の基準物質 1. 相関性試験成績 本キットとA 社キットとの間の相関性を 103 例の陽性患者検体を対象に検討した 両測定間の相関式は y = 0.96 x 0.04 相関係数 r = と良好なものであった 本キットとB 社キットとの間の相関性を 83 例の国内検体を対象に検討した 両測定間の相関式は y = 0.99 x 0.76 相関係数 r = と良好なものであった 本キットとC 社キットとの間の相関性を 33 例の国内検体を対象に検討した 両測定間の相関式は y = 0.93 x 0.08 相関係数 r = と良好なものであった 2. 較正用の基準物質 本キットでは 較正用基準物質として WHO International Standard for HBV DNA (NIBSC code 97/746) 3 を用いている 測定結果は IU/mL 又は Copies/mL として報告される 使用上又は取扱い上の注意 (1) 取扱い上 ( 危険防止 ) の注意 本キットの測定では ヒト検体を取り扱う 検体は HIV HBV HCV 等の感染の恐れがあるものとして取り扱うこと 検査にあたっては 感染の危険を避けるため 専用の着衣 眼鏡 マスクおよび使い捨て手袋を着用し また口によるピペッティングは行わないこと 検体や試薬類を扱う場所では 飲食 喫煙 化粧およびコンタクトレンズの取り扱いをしないこと 注意 : 本測定で使用する試薬類には ヒト由来および / または潜在的に感染性のある物質が含まれている ヒト血液由来物質は FDA が承認した測定キットにおいて HCV 抗体陰性 HIV-1 抗体陰性 HIV-2 抗体陰性 HBs 抗原陰性であり また FDA が承認した PCR 法において HIV-1 RNA 陰性および HCV RNA 陰性である ヒト由来物質または不活化微生物が完全に感染伝播しないことを保証する試験は知られていない 感染性物質を含む またはその疑いがある物質については Biosafety in Microbiological and Biomedical Laboratories 11 OSHA Standards on Bloodborne Pathogens 12 CLSI Document M29-A3 13 または他の適切なバイオセイフティ基準 14 に従って取り扱うこと すべてのヒト由来物質は潜在的に感染性があると考えること 7
8 試薬が誤って目や口に入った場合には水で十分に洗い流す等の応急措置を行い 必要があれば医師の手当て等を受けること 本測定で使用する試薬類には 保存剤としてアジ化ナトリウムが含まれているものがある 詳細は 形状 構造等 ( キットの構成 ) または 用法 用量( 操作方法 ) を参照のこと 酸との接触により非常に毒性の強いガスが発生する 内容物および容器は適切な方法で廃棄すること 洗浄液 2 の調製には 95 ~ 100% エタノールのみを使用すること 変性剤を含有するエタノールは使用しないこと 安全上の注意については 使用する機器の取扱説明書を参照のこと 本キット ( 製品番号 :2G34-98) キャリブレータ( 製品番号 :2G34-78) コントロール ( 製品番号 :2G34-88) には次の物質が含まれている 2- メチル -2H- イソチアゾール -3- オン アジ化ナトリウム 5- クロロ -2- メチル -4- イソチアゾリン -3- オン (EC No ) と 2- メチル -2H- イソチアゾール -3- オン (EC No ) の混合物 (3:1) 5- クロロ -2- メチル -4- イソチアゾリン -3- オン (EC No ) と 2- メチル -4- イソチアゾリン -3- オン (EC No ) の混合物 (3:1) 危険有害性情報 注意事項を次に示す 警告 H317 アレルギー性皮膚反応を起こすおそれ EUH032 酸との接触により非常に毒性の強いガスが発生する P261 ミスト / 蒸気 / スプレーの吸入を避けること P280 保護手袋 / 保護衣 / 保護眼鏡を着用すること P272 汚染された作業衣は作業場から出さないこと P333+P313 皮膚刺激または発疹が生じた場合 : 医師の診察 / 手当てを受けること P302+P352 皮膚に付着した場合 : 多量の水で洗うこと P362+P364 汚染された衣類を脱ぎ 再使用する場合には洗濯をすること P501 内容物 / 容器を適切な方法で廃棄すること 次の試薬類に関する危険有害性情報 注意事項を示す DNA 核酸抽出試薬のライシス溶液 DNA 核酸抽出試薬の洗浄液 1 警告 H302+H332 H412 EUH032 P261 P264 P280 P271 P273 P301+P312 P304+P340 P312 P330 P501 グアニジンチオシアン酸塩を含む飲み込んだり吸入すると有害長期継続的影響により水生生物に有害酸との接触により非常に毒性の強いガスが発生する ミスト / 蒸気 / スプレーの吸入を避けること 取扱後は手をよく洗うこと 保護手袋 / 保護衣 / 保護眼鏡を着用すること 屋外または換気の良い場所でのみ使用すること 環境への放出を避けること 飲み込んだ場合 : 気分が悪い時は医師に連絡すること 吸入した場合 : 空気の新鮮な場所に移し 呼吸しやすい姿勢で休息させること 気分が悪い時は医師に連絡すること 口をすすぐこと 内容物 / 容器を適切な方法で廃棄すること DNA 核酸抽出試薬の磁性粒子溶液 警告 グアニジン塩酸塩を含む H302 飲み込むと有害 H315 皮膚刺激 H319 強い眼刺激 P280 保護手袋 / 保護衣 / 保護眼鏡を着用すること P264 取扱後は手をよく洗うこと P305+P351 +P338 P301+P312 P302+P352 P332+P313 P330 P362+P364 P501 眼に入った場合 : 水で数分間注意深く洗うこと 次にコンタクトレンズを着用していて容易に外せる場合は外すこと その後も洗浄を続けること 飲み込んだ場合 : 気分が悪い時は医師に連絡すること 皮膚に付着した場合 : 多量の水で洗うこと 皮膚刺激が生じた場合 : 医師の診断 / 手当てを受けること 口をすすぐこと 汚染された衣類を脱ぎ 再使用する場合には洗濯をすること 内容物 / 容器を適切な方法で廃棄すること プロテアーゼ K PCR グレード ( 製品番号 :3L78-60) には次の物質が含まれている プロテアーゼ K(CAS: ) 危険有害性情報 注意事項を次に示す 危険 H334 吸入するとアレルギー 喘息または呼吸困難を起こす おそれ H317 アレルギー性皮膚反応を起こすおそれ P284 [ 換気が不十分な場合 ] 呼吸用保護具を着用すること P261 ミスト / 蒸気 / スプレーの吸入を避けること P280 保護手袋 / 保護衣 / 保護眼鏡を着用すること P272 汚染された作業衣は作業場から出さないこと P304+P340 吸入した場合 : 空気の新鮮な場所に移し 呼吸しやす い姿勢で休息させること P333+P313 皮膚刺激または発疹が生じた場合 : 医師の診察 / 手当 てを受けること P302+P352 皮膚に付着した場合 : 多量の水で洗うこと P362+P364 汚染された衣類を脱ぎ 再使用する場合には洗濯をす ること P342+P311 呼吸に関する症状が出た場合 : 医師に連絡すること P501 内容物 / 容器を適切な方法で廃棄すること 安全データシート : 試薬類の安全な取り扱い 輸送および廃棄に関する重要な情報 が記載されている (2) 使用上の注意 使用期限を過ぎた試薬類を使用しないこと 同一のロット番号の試薬であっても試薬を注ぎ足すことはしないこと 本キットには 操作上の注意 (1) 測定試料の性質 採取法に記載されているキャップ付き採血管で取扱いおよび保存されたヒト血清または血漿検体のみを使用すること サンプル間交差汚染の危険性や核酸抽出中または抽出後にヌクレアーゼが誤ってサンプル中に混入することを最小限に抑えるため サンプル調製中は必ず施設の適切な基準に従うこと DNA を扱う場合は 常に無菌操作で行うこと PCR などの増幅反応は 過去に行った測定の増幅産物混入による影響を受けやすい たとえ数分子の増幅産物の混入であっても 増幅過程に使用する検体または試薬が汚染された場合 偽陽性となる可能性がある 施設の基準に従い PCR の実施に関わる作業を物理的に分けること等により汚染の危険性が低減される 本キットの測定には 施設内に 2 箇所の専用区域を設けること サンプル ( 検体 コントロール キャリブレータ ) の調製 および調製された検体 コントロール キャリブレータの 96 ウェルオプティカルリアクションプレートへの分注は 検体調製区域で行うこと Abbott m2000sp 自動核酸抽出装置は マスターミックスを調製するための増幅 検出用試薬の混合や 96 ウェルオプティカルリアクションプレートへのマスターミックスの分注を行う 検体調製区域で使用するすべての試薬は 常に区域内にとどめること 検体調製区域で使用する白衣 ピペット ピペットチップ ボルテックスミキサーは 必ず区域内にとどめ 増幅区域に持ち出さないこと 増幅産物を検体調製区域に持ち込まないこと 増幅と増幅産物の検出は 増幅区域で行うこと 増幅区域で使用する白衣や器具は 必ず区域内にとどめ 検体調製区域に持ち出さないこと キット内の構成品は 一緒に使用すること 異なるロットのキット構成品を組み合わせて使用しないこと 例 : コントロールキットのロットが X である陰性コントロールと コントロールキットのロットが Y である陽性コントロールを組み合わせて使用しないこと 作業場所と機器は 潜在的汚染源とみなすこと 潜在的汚染源 ( 検体 核酸抽出液 増幅産物 ) と接触した場合は 未開封の試薬 陰性コントロール 陽性コントロール キャリブレータ または検体を取り扱う前に手袋を交換すること 機器の清掃手順については 使用する機器の取扱説明書を参照のこと Abbott m2000sp 自動核酸抽出装置の作動が中止された場合は Abbott m2000sp 自動核酸抽出装置の取扱説明書に従い すべての消耗品と試薬を廃棄すること 注 : 増幅 検出用試薬パックは 本添付文書の記載に従って保存および再使用することができる Abbott m2000sp 自動核酸抽出装置のマスターミックス分注のプロトコールが中止された場合は Abbott m2000sp 自動核酸抽出装置の取扱説明書に従い 96 ウェルオプティカルリアクションプレートをプレートを取り扱う際に使用した手袋と共にチャック付きビニール袋に入れて密封し廃棄すること Abbott m2000rt アナライザーによる測定が中断または中止された場合は Abbott m2000rt アナライザーの取扱説明書に従い 96 ウェルオプティカルリアクションプレートをプレートを取り扱う際に使用した手袋と共にチャック付きビニール袋に入れて密封し廃棄すること すべての検体 試薬類 および他の潜在的生物学的危険物質は 適切な法規等に従い除染および廃棄すること 15, 16 作業場所を汚染する可能性を最小限に抑える方法で すべての物質を取り扱うこと マニュアルピペッティングの際に形成されるエアロゾルによる核酸汚染の危険性を低減するため マニュアルピペッティングを行う際は必ずフィルター付きピペットチップを使用すること ピペットチップは 必ず使い捨てにすること こぼれた検体および試薬類は 使用する機器の取扱説明書に記載されている方法で清掃 除染すること 8
9 DNase 汚染 サンプル間交差汚染および反応阻害のリスクを最小限に抑えるため 次の注意事項を遵守すること 適切な保護用具を常に着用すること パウダーフリー手袋を使用すること 潜在的汚染源 ( 検体 核酸抽出液 増幅産物 ) に接触した場合は 手袋を交換すること ピペッティングの際に形成されるエアロゾルによる核酸汚染の危険性を低減するため ピペッティングを行う際は必ずフィルター付きピペットチップを使用すること ピペットへの汚染を防ぐため チップは十分に長い必要がある ピペッティング中は ピペットがサンプルチューブや容器の内側に接触しないように注意すること 十分な長さのフィルター付きピペットチップを使用すること 液体をマニュアルで分注する場合 各分注ごとにフィルター付きピペットチップを交換すること 完全に または一部使用した 200μL および 1,000μL の使い捨てピペットチップトレイは 各測定前にチップがすべて充填されたトレイと交換すること DNA 核酸抽出試薬またはプロテアーゼ K PCR グレードは 使い捨てにすること 新規測定ごとに 新しい試薬容器 反応チューブ 新規に開封した DNA 核酸抽出試薬を使用すること 各測定の後 ワークテーブルに残っている試薬は Abbott m2000sp 自動核酸抽出装置の取扱説明書 DNA 核酸抽出試薬の Product Information およびプロテアーゼ K PCR グレードの Package insert に従って廃棄すること 新しい増幅 検出用試薬パックと内部コントロールのバイアルは 使用するまで 10 以下で保存すること 一度使用し 再使用する増幅 検出用試薬パックは キャップを閉め 真っすぐに立てた状態で遮光して 2 ~ 8 で保存すること 調製済みのマスターミックスが残っており 次回再使用する増幅 検出用試薬パックは このように保存した場合 1 回目の使用日から 14 日以内であれば再使用することができる 内部コントロールについても キャップを閉めて 2 ~ 8 で保存した場合 融解後 14 日以内であれば再使用することができる 2 回使用した増幅 検出用試薬パックや内部コントロールは廃棄すること 新しい増幅 検出用試薬パックあるいは再使用する増幅 検出用試薬パックを使用する際は 増幅 検出用試薬パックがサンプルやコントロールに直接接触しないように注意すること 陰性および陽性コントロールは 10 以下で保存すること キャリブレータ A および B は 10 以下で保存すること DNA 核酸抽出試薬は 15 ~ 30 で保存すること プロテアーゼ K PCR グレードは 2 ~ 8 で保存すること 本キット コントロール キャリブレータは ドライアイス中で保存して輸送される 主要文献 1. Boom R, Sol CJA, Heijtink R, et al. Rapid purification of hepatitis B virus DNA from serum. J Clin Microbiol 1991;29(9): Read SJ. Recovery efficiencies of nucleic acid extraction kits as measured by quantitative LightCycler PCR. J Clin Pathol: Mol Pathol 2001;54: Saldanha J, Gerlich W, Lelie N, et al. An International Collaborative Study to Establish a WHO International Standard for HBV DNA Nucleic Acid Amplification Technology Assay. WHO Expert Committee on Biological Standardization: Fiftieth Report, Geneva, Switzerland; WHO Technical Report Series No. 904;BS/ American Association for the Study of Liver Diseases Practice Guideline: Chronic Hepatitis B. Hepatology. 2007;45(2): National Institutes of Health Consensus Development Conference Statement: Management of Hepatitis B. Ann Intern Med. 2009;150(2): Virologic Monitoring of Hepatitis B Virus Therapy in Clinical Trials and Practice: Recommendations for a Standard Approach. Gastroenterology. 2008;134: Agresti A. Categorical Data Analysis. New York, NY: John Wiley and Sons; National Committee for Clinical Laboratory Standards. Evaluation of the Linearity of Quantitative Measurement Procedures: A Statistical Approach; Approved Guideline - NCCLS Document EP6-A, NCCLS:Wayne, PA, National Committee for Clinical Laboratory Standards. Preliminary Evaluation of Quantitative Clinical Laboratory Methods; Approved Guideline - Second Edition. NCCLS Document EP10-A2. NCCLS: Wayne, PA, National Committee for Clinical Laboratory Standards. Method Comparison and Bias Estimation Using Patient Samples; Approved Guideline - Second Edition. NCCLS Document EP9-A2, NCCLS Wayne, PA, US Department of Health and Human Services. Biosafety in Microbiological and Biomedical Laboratories. 5th ed. Washington, DC: US Government Printing Office; December [Also available online. Type> search>bmbl5>look up sections III and IV.] 12. US Department of Labor, Occupational Safety and Health Administration. 29 CFR Part Bloodborne Pathogens. 13. Clinical and Laboratory Standards Institute. Protection of Laboratory Workers from Occupationally Acquired Infections: Approved Guideline - Third Edition. CLSI Document M29-A3. Wayne, PA: Clinical and Laboratory Standards Institute; World Health Organization. Laboratory Biosafety Manual. 3rd ed. Geneva, Switzerland: World Health Organization; すべての商標の所有権は 各商標の所有権者に帰属します (3) 廃棄上の注意 検体中には HIV HBV HCV 等の感染性のものが存在する恐れがあるので 廃液 使用済み器具などは次亜塩素酸ナトリウム ( 有効塩素濃度 1,000 ppm 1 時間以上浸漬 ) またはグルタルアルデヒド (2% 1 時間以上浸漬 ) による消毒処理 あるいはオートクレーブ ( 分以上 ) による滅菌処理を行うこと 注 : 反応済の 96 ウェルオプティカルリアクションプレートはオートクレーブ処理を行わないこと 密封した 96 ウェルオプティカルリアクションプレートをオートクレーブ滅菌しても 増幅産物は分解されず プレートを密封しているカバーがはがれることにより増幅産物の放出を引き起こす可能性がある 増幅産物により検査室が汚染される可能性があるため 各工程の前後には 廃棄物を慎重に取り扱い密封すること 96 ウェルオプティカルリアクションプレートはチャック付きビニール袋に入れて密封し廃棄すること 注 : DNA 核酸抽出試薬の廃液は 次亜塩素酸ナトリウム溶液などの酸化作用のある物質と混合することにより有毒ガスが発生するため 混合しないこと 試薬および器具等を廃棄する場合には 廃棄物の処理および清掃に関する法律 水質汚濁防止法等の規定に従って処理すること 試薬類や検体が飛散した場合には 飛散した溶液を吸収剤で吸収し 飛散した場所を洗浄液で拭き取った後 さらに 1.0 % 次亜塩素酸ナトリウム溶液などの適切な消毒剤 11 で拭き取ること 作業は適切な保護用具 ( 手袋 安全眼鏡 実験衣など ) を着用して行うこと 本測定で使用する試薬類には 保存剤としてアジ化ナトリウムが含まれているものがある 詳細は 形状 構造等 ( キットの構成 ) または 用法 用量( 操作方法 ) を参照のこと アジ化ナトリウムは 鉛管 銅管と反応して爆発性の金属アジドを生成することがあるので 廃棄する場合には 大量の水と共に流すこと すべての検体 試薬類 他の潜在的汚染源および潜在的感染性物質は 適切な法規等 14 に従い除染および廃棄すること 貯蔵方法 有効期間 貯蔵方法 : 10 以下に保存する 有効期間 : 18 箇月使用期限は 外装に表示されている 包装単位 アキュジーン m-hbv 製品番号 2G34-98:96 回用 (24 回用 4) 〇増幅 検出用試薬パック オリゴヌクレオチド試薬 ml 4 酵素試薬 ml 4 活性化試薬 ml 4 〇内部コントロール 0.2 ml 4 問い合わせ先 アボットジャパン株式会社 カストマーサポートセンター 千葉県松戸市松飛台 278 TEL 製造販売業者の名称及び住所 アボットジャパン株式会社 千葉県松戸市松飛台 278 TEL 047(385)2211( 代表 ) ABBOTT JAPAN CO., LTD
ISOSPIN Blood & Plasma DNA
 血液 血清 血しょうからの DNA 抽出キット ISOSPIN Blood & Plasma DNA マニュアル ( 第 2 版 ) Code No. 312-08131 NIPPON GENE CO., LTD. I 製品説明 ISOSPIN Blood & Plasma DNA( アイソスピンブラッド & プラズマ DNA) は 血液 血清 血しょうから DNAを抽出するためのキットです 本キットは
血液 血清 血しょうからの DNA 抽出キット ISOSPIN Blood & Plasma DNA マニュアル ( 第 2 版 ) Code No. 312-08131 NIPPON GENE CO., LTD. I 製品説明 ISOSPIN Blood & Plasma DNA( アイソスピンブラッド & プラズマ DNA) は 血液 血清 血しょうから DNAを抽出するためのキットです 本キットは
遺伝子検査の基礎知識
 リアルタイム PCR( インターカレーター法 ) 実験ガイドこの文書では インターカレーター法 (TB Green 検出 ) によるリアルタイム PCR について 蛍光検出の原理や実験操作の流れなどを解説します 実際の実験操作の詳細については 各製品の取扱説明書をご参照ください - 目次 - 1 蛍光検出の原理 2 実験に必要なもの 3 実験操作法 4 結果の解析 1 1 蛍光検出の原理 インターカレーターによる蛍光検出の原理
リアルタイム PCR( インターカレーター法 ) 実験ガイドこの文書では インターカレーター法 (TB Green 検出 ) によるリアルタイム PCR について 蛍光検出の原理や実験操作の流れなどを解説します 実際の実験操作の詳細については 各製品の取扱説明書をご参照ください - 目次 - 1 蛍光検出の原理 2 実験に必要なもの 3 実験操作法 4 結果の解析 1 1 蛍光検出の原理 インターカレーターによる蛍光検出の原理
Microsoft Word - FMB_Text(PCR) _ver3.doc
 2.PCR 法による DNA の増幅 現代の分子生物学において その進歩に最も貢献した実験法の1つが PCR(Polymerase chain reaction) 法である PCR 法は極めて微量の DNA サンプルから特定の DNA 断片を短時間に大量に増幅することができる方法であり 多大な時間と労力を要した遺伝子クローニングを過去のものとしてしまった また その操作の簡便さから 現在では基礎研究のみならず臨床遺伝子診断から食品衛生検査
2.PCR 法による DNA の増幅 現代の分子生物学において その進歩に最も貢献した実験法の1つが PCR(Polymerase chain reaction) 法である PCR 法は極めて微量の DNA サンプルから特定の DNA 断片を短時間に大量に増幅することができる方法であり 多大な時間と労力を要した遺伝子クローニングを過去のものとしてしまった また その操作の簡便さから 現在では基礎研究のみならず臨床遺伝子診断から食品衛生検査
遺伝子検査の基礎知識
 遺伝子検査の準備と注意事項 PCR はわずか 1 分子の鋳型 DNA でも検出可能であるため 反応液調製時に鋳型となりうる核酸等が混入しないように細心の注意が必要です この文書では 正確な遺伝子検査を行うために必要な実験器具類やコンタミネーション防止のための注意事項について解説します - 目次 - 1 実験環境の整備 2 必要な実験器具と装置 1 実験環境の整備 コンタミネーションの原因 PCR は非常に高感度な検出法であるため
遺伝子検査の準備と注意事項 PCR はわずか 1 分子の鋳型 DNA でも検出可能であるため 反応液調製時に鋳型となりうる核酸等が混入しないように細心の注意が必要です この文書では 正確な遺伝子検査を行うために必要な実験器具類やコンタミネーション防止のための注意事項について解説します - 目次 - 1 実験環境の整備 2 必要な実験器具と装置 1 実験環境の整備 コンタミネーションの原因 PCR は非常に高感度な検出法であるため
パナテスト ラットβ2マイクログロブリン
 研究用試薬 2014 年 4 月作成 EIA 法ラット β 2 マイクログロブリン測定キット PRH111 パナテスト A シリーズラット β 2- マイクロク ロフ リン 1. はじめに β 2 - マイクログロブリンは, 血液, 尿, および体液中に存在し, ヒトでは腎糸球体障害, 自己免疫疾患, 悪性腫瘍, 肝疾患などによって血中濃度が変化するといわれています. また,β 2 - マイクログロブリンの尿中濃度は,
研究用試薬 2014 年 4 月作成 EIA 法ラット β 2 マイクログロブリン測定キット PRH111 パナテスト A シリーズラット β 2- マイクロク ロフ リン 1. はじめに β 2 - マイクログロブリンは, 血液, 尿, および体液中に存在し, ヒトでは腎糸球体障害, 自己免疫疾患, 悪性腫瘍, 肝疾患などによって血中濃度が変化するといわれています. また,β 2 - マイクログロブリンの尿中濃度は,
■リアルタイムPCR実践編
 リアルタイム PCR 実践編 - SYBR Green I によるリアルタイム RT-PCR - 1. プライマー設計 (1)Perfect Real Time サポートシステムを利用し 設計済みのものを購入する ヒト マウス ラットの RefSeq 配列の大部分については Perfect Real Time サポートシステムが利用できます 目的の遺伝子を検索して購入してください (2) カスタム設計サービスを利用する
リアルタイム PCR 実践編 - SYBR Green I によるリアルタイム RT-PCR - 1. プライマー設計 (1)Perfect Real Time サポートシステムを利用し 設計済みのものを購入する ヒト マウス ラットの RefSeq 配列の大部分については Perfect Real Time サポートシステムが利用できます 目的の遺伝子を検索して購入してください (2) カスタム設計サービスを利用する
DNA/RNA調製法 実験ガイド
 DNA/RNA 調製法実験ガイド PCR の鋳型となる DNA を調製するにはいくつかの方法があり 検体の種類や実験目的に応じて適切な方法を選択します この文書では これらの方法について実際の操作方法を具体的に解説します また RNA 調製の際の注意事項や RNA 調製用のキット等をご紹介します - 目次 - 1 実験に必要なもの 2 コロニーからの DNA 調製 3 増菌培養液からの DNA 調製
DNA/RNA 調製法実験ガイド PCR の鋳型となる DNA を調製するにはいくつかの方法があり 検体の種類や実験目的に応じて適切な方法を選択します この文書では これらの方法について実際の操作方法を具体的に解説します また RNA 調製の際の注意事項や RNA 調製用のキット等をご紹介します - 目次 - 1 実験に必要なもの 2 コロニーからの DNA 調製 3 増菌培養液からの DNA 調製
Microsoft PowerPoint - LEGEND MAX Protocol
 Sandwich ELISA Protocol LEGEND MAX TM ELISA Kit with Pre coated Plates トミーデジタルバイオロジーアライアンストプロダクトカスタマーサポート 試薬の構成 試薬 包装単位 1プレート包装 5プレート包装 容量 ( ボトル ) プレコート96ウエルマイクロタイタープレート 1 5 ディテクション抗体 1 5 12ml スタンダード 1
Sandwich ELISA Protocol LEGEND MAX TM ELISA Kit with Pre coated Plates トミーデジタルバイオロジーアライアンストプロダクトカスタマーサポート 試薬の構成 試薬 包装単位 1プレート包装 5プレート包装 容量 ( ボトル ) プレコート96ウエルマイクロタイタープレート 1 5 ディテクション抗体 1 5 12ml スタンダード 1
安全データシート LOCTITE SI 5920 RTV SILICONE COPPER known as LOCTITE CO RTV SIL 70ML EN Page 1 of 6 SDS No. : V001.3 改訂 : 発行日 :
 安全データシート LOCTITE CO RTV SIL 70ML EN Page 1 of 6 SDS No. : 152854 改訂 : 14.04.2016 発行日 : 22.08.2016 1. 化学物質等及び会社情報 製品コード : 198818 製品名 : 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8 スフィアタワー天王洲 14F 140-0002 電話番号 : +81
安全データシート LOCTITE CO RTV SIL 70ML EN Page 1 of 6 SDS No. : 152854 改訂 : 14.04.2016 発行日 : 22.08.2016 1. 化学物質等及び会社情報 製品コード : 198818 製品名 : 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8 スフィアタワー天王洲 14F 140-0002 電話番号 : +81
培養細胞からの Total RNA 抽出の手順 接着細胞のプロトコル 1. プレート ( またはウエル ) より培地を除き PBSでの洗浄を行う 2. トリプシン処理を行い 全量を1.5ml 遠心チューブに移す スクレイパーを使って 細胞を掻き集める方法も有用です 3. 低速遠心 ( 例 300 g
 Maxwell RSC simplyrna Cells / Tissue Kit ( カタログ番号 AS1340/AS1390) 簡易マニュアル 注意 : キットを受け取りましたら 1-Thioglycerolを取り出し キット箱は室温で保存してください 取り出した1-Thioglycerolは2~10 で保存してください ご用意いただくもの 細胞 組織の両方の場合で共通 ボルテックスミキサー ピペットマン
Maxwell RSC simplyrna Cells / Tissue Kit ( カタログ番号 AS1340/AS1390) 簡易マニュアル 注意 : キットを受け取りましたら 1-Thioglycerolを取り出し キット箱は室温で保存してください 取り出した1-Thioglycerolは2~10 で保存してください ご用意いただくもの 細胞 組織の両方の場合で共通 ボルテックスミキサー ピペットマン
** この添付文書をよく読んでから使用してください 体外診断用医薬品 ** 2015 年 10 月改訂 ( 第 7 版 ) * 2015 年 4 月改訂 ( 第 6 版 ) 製造販売承認番号 22100AMX B 型肝炎ウイルスコア抗体キット HBc アボット ja Anti-HBc
 この添付文書をよく読んでから使用してください 体外診断用医薬品 2015 年 10 月改訂 ( 第 7 版 ) 2015 年 4 月改訂 ( 第 6 版 ) 製造販売承認番号 22100AMX02283000 B 型肝炎ウイルスコア抗体キット HBc アボット ja Anti-HBc II 8L44 G0-2490/R08 B8L44J 全般的な注意 1. 本製品は体外診断用であり それ以外の目的に使用しないこと
この添付文書をよく読んでから使用してください 体外診断用医薬品 2015 年 10 月改訂 ( 第 7 版 ) 2015 年 4 月改訂 ( 第 6 版 ) 製造販売承認番号 22100AMX02283000 B 型肝炎ウイルスコア抗体キット HBc アボット ja Anti-HBc II 8L44 G0-2490/R08 B8L44J 全般的な注意 1. 本製品は体外診断用であり それ以外の目的に使用しないこと
この添付文書をよく読んでから使用してください 体外診断用医薬品 2017 年 8 月作成 ( 第 1 版 ) 製造販売承認番号 21000AMY B 型肝炎ウイルス表面抗体キット オーサブ アボット ja Anti-HBs 07P R01 B7P89J 全般的な注意
 この添付文書をよく読んでから使用してください 体外診断用医薬品 2017 年 8 月作成 ( 第 1 版 ) 製造販売承認番号 21000AMY00120000 B 型肝炎ウイルス表面抗体キット オーサブ アボット ja Anti-HBs 07P89 470696R01 B7P89J 全般的な注意 本製品は体外診断用であり それ以外の目的に使用しないこと 診断は 他の関連する検査結果や臨床症状等に基づいて総合的に判断すること
この添付文書をよく読んでから使用してください 体外診断用医薬品 2017 年 8 月作成 ( 第 1 版 ) 製造販売承認番号 21000AMY00120000 B 型肝炎ウイルス表面抗体キット オーサブ アボット ja Anti-HBs 07P89 470696R01 B7P89J 全般的な注意 本製品は体外診断用であり それ以外の目的に使用しないこと 診断は 他の関連する検査結果や臨床症状等に基づいて総合的に判断すること
改訂履歴 登録 発行 年月日 文書番号 ( 改訂番号 ) 改訂内容 改訂理由 年月日 エンドトキシン簡便法 2 / 9 日本核医学会
 院内製造 PET 薬剤のための簡便なエンドトキシン試験法 ( エンドトキシン簡便法 ) エンドトキシン簡便法 1 / 9 日本核医学会 改訂履歴 登録 発行 年月日 文書番号 ( 改訂番号 ) 改訂内容 改訂理由 年月日 エンドトキシン簡便法 2 / 9 日本核医学会 目次 表紙... 1 改訂履歴... 2 目次... 3 院内製造 PET 薬剤のための簡便なエンドトキシン試験法 ( エンドトキシン簡便法
院内製造 PET 薬剤のための簡便なエンドトキシン試験法 ( エンドトキシン簡便法 ) エンドトキシン簡便法 1 / 9 日本核医学会 改訂履歴 登録 発行 年月日 文書番号 ( 改訂番号 ) 改訂内容 改訂理由 年月日 エンドトキシン簡便法 2 / 9 日本核医学会 目次 表紙... 1 改訂履歴... 2 目次... 3 院内製造 PET 薬剤のための簡便なエンドトキシン試験法 ( エンドトキシン簡便法
2 参考 検体投入部遠心機開栓機感染症検査装置 感染症検査装置 (CL4800)
 1 平成 19 年 11 月 14 日血液事業部会運営委員会配布資料 資料 1 検査法の変更について (CLEIA 法の導入について ) 1. 対象検査項目現在の検査項目 HBs 抗原 HBc 抗体 HBs 抗体 HTLV-1 抗体 HIV1/2 抗体 HCV 抗体 梅毒 TP 抗体 パルボウイルス B19 抗原のすべての検査項目について 検査方法を凝集法から化学発光酵素免疫法 (CLEIA 法 )
1 平成 19 年 11 月 14 日血液事業部会運営委員会配布資料 資料 1 検査法の変更について (CLEIA 法の導入について ) 1. 対象検査項目現在の検査項目 HBs 抗原 HBc 抗体 HBs 抗体 HTLV-1 抗体 HIV1/2 抗体 HCV 抗体 梅毒 TP 抗体 パルボウイルス B19 抗原のすべての検査項目について 検査方法を凝集法から化学発光酵素免疫法 (CLEIA 法 )
操作上の注意 1. 測定試料の性質 採取法 (1) 本品の測定には血漿を使用して下さい (2) 赤血球 その他の有形成分 沈殿物 浮遊物が含まれている検体 ( 特にフィブリンクロット クリオグロブリン沈殿など ) では 正しい測定結果が得られない場合があります 使用前に遠心または濾過による除去を行っ
 AK(No.150232) 体外診断用医薬品 血液凝固因子検査用 PIVKA-Ⅱ キット デタミナー CL 化学発光酵素免疫測定法キット この添付文書をよく読んでから使用してください ピブカルテスト 2011 年 11 月作成 ( 第 1 版 ) 製造販売認証番号 :224AAAMX00008000 全般的な注意 1. 本品は体外診断用であり それ以外の目的に使用しないで下さい 2. 診断は他の関連する検査結果や臨床症状等に基づいて総合的に判断して下さい
AK(No.150232) 体外診断用医薬品 血液凝固因子検査用 PIVKA-Ⅱ キット デタミナー CL 化学発光酵素免疫測定法キット この添付文書をよく読んでから使用してください ピブカルテスト 2011 年 11 月作成 ( 第 1 版 ) 製造販売認証番号 :224AAAMX00008000 全般的な注意 1. 本品は体外診断用であり それ以外の目的に使用しないで下さい 2. 診断は他の関連する検査結果や臨床症状等に基づいて総合的に判断して下さい
1. 測定原理 弱酸性溶液中で 遊離塩素はジエチル p フェニレンジアミンと反応して赤紫色の色素を形成し これを光学的に測定します 本法は EPA330.5 および US Standard Methods 4500-Cl₂ G EN ISO7393 に準拠しています 2. アプリケーション サンプル
 00595 塩素 (DPD 法 ) 遊離塩素の測定 測定範囲 : 0.03~6.00mg/l Cl 2 結果は mmol/l 単位でも表示できます 2. ピペットで 5.0ml の試料を丸セルに取ります 3. 青のミクロスプーンで 1 回分の試薬 Cl 1 を加えて ねじぶたで閉じます 4. セルをよく振とうして 固体物を溶かします 5. 反応時間 :1 分間 6. 各セルをセルコンパートメントにセットし
00595 塩素 (DPD 法 ) 遊離塩素の測定 測定範囲 : 0.03~6.00mg/l Cl 2 結果は mmol/l 単位でも表示できます 2. ピペットで 5.0ml の試料を丸セルに取ります 3. 青のミクロスプーンで 1 回分の試薬 Cl 1 を加えて ねじぶたで閉じます 4. セルをよく振とうして 固体物を溶かします 5. 反応時間 :1 分間 6. 各セルをセルコンパートメントにセットし
リアルタイムPCRの基礎知識
 1. リアルタイム PCR の用途リアルタイム PCR 法は 遺伝子発現解析の他に SNPs タイピング 遺伝子組み換え食品の検査 ウイルスや病原菌の検出 導入遺伝子のコピー数の解析などさまざまな用途に応用されている 遺伝子発現解析のような定量解析は まさにリアルタイム PCR の得意とするところであるが プラス / マイナス判定だけの定性的な解析にもその威力を発揮する これは リアルタイム PCR
1. リアルタイム PCR の用途リアルタイム PCR 法は 遺伝子発現解析の他に SNPs タイピング 遺伝子組み換え食品の検査 ウイルスや病原菌の検出 導入遺伝子のコピー数の解析などさまざまな用途に応用されている 遺伝子発現解析のような定量解析は まさにリアルタイム PCR の得意とするところであるが プラス / マイナス判定だけの定性的な解析にもその威力を発揮する これは リアルタイム PCR
プロトコール集 ( 研究用試薬 ) < 目次 > 免疫組織染色手順 ( 前処理なし ) p2 免疫組織染色手順 ( マイクロウェーブ前処理 ) p3 免疫組織染色手順 ( オートクレーブ前処理 ) p4 免疫組織染色手順 ( トリプシン前処理 ) p5 免疫組織染色手順 ( ギ酸処理 ) p6 免疫
 < 目次 > 免疫組織染色手順 ( 前処理なし ) p2 免疫組織染色手順 ( マイクロウェーブ前処理 ) p3 免疫組織染色手順 ( オートクレーブ前処理 ) p4 免疫組織染色手順 ( トリプシン前処理 ) p5 免疫組織染色手順 ( ギ酸処理 ) p6 免疫組織染色手順 ( ギ酸処理後 マイクロウェーブまたはオートクレーブ処理 )p7 抗原ペプチドによる抗体吸収試験 p8 ウエスタン ブロッティング
< 目次 > 免疫組織染色手順 ( 前処理なし ) p2 免疫組織染色手順 ( マイクロウェーブ前処理 ) p3 免疫組織染色手順 ( オートクレーブ前処理 ) p4 免疫組織染色手順 ( トリプシン前処理 ) p5 免疫組織染色手順 ( ギ酸処理 ) p6 免疫組織染色手順 ( ギ酸処理後 マイクロウェーブまたはオートクレーブ処理 )p7 抗原ペプチドによる抗体吸収試験 p8 ウエスタン ブロッティング
Virus Test Kit (HIV, HTLV, HCV, HBV, ParvoB19) Ver.2
 研究用 Virus Test Kit (HIV, HTLV, HCV, HBV, ParvoB19) Ver.2 説明書 v201902da 本製品は 6 種類のウイルス [ HIV1 (pol, LTR) HIV2 HBV HCV HTLV1&2 parvovirus B19 ] をリアルタイム RT-PCR により検出するためのキットです 本製品では 操作が簡便で高感度なワンステップのリアルタイム
研究用 Virus Test Kit (HIV, HTLV, HCV, HBV, ParvoB19) Ver.2 説明書 v201902da 本製品は 6 種類のウイルス [ HIV1 (pol, LTR) HIV2 HBV HCV HTLV1&2 parvovirus B19 ] をリアルタイム RT-PCR により検出するためのキットです 本製品では 操作が簡便で高感度なワンステップのリアルタイム
取扱説明書
 Realtime PCR Master Mix Realtime PCR Master Mix トラブルシューティング SYBR Green Realtime PCR Master Mix トラブルシューティングは p3 へ 1. 増幅がみられない 乱れる原因対策検出機器の設定などが蛍光色標識に用いられている蛍光色素の種類によって 検素に適合していない出機器の設定を変更する必要があります 設定を適正化して再解析してください
Realtime PCR Master Mix Realtime PCR Master Mix トラブルシューティング SYBR Green Realtime PCR Master Mix トラブルシューティングは p3 へ 1. 増幅がみられない 乱れる原因対策検出機器の設定などが蛍光色標識に用いられている蛍光色素の種類によって 検素に適合していない出機器の設定を変更する必要があります 設定を適正化して再解析してください
5
 QCWS 参考プロトコル 抗 HLA 抗体検査 (ICFA) 2019 年度版 作成者日本組織適合性学会認定制度委員会ワーキンググループ抗 HLA 抗体 WG 制定 改訂履歴 版数 制定日 施行日 制定理由 作成責任者 初版 日本組織適合性学会が開催する QCWS での HLA 検査を実施する際に用いる QCWS 参考プロトコルとして制定した WG 版数 改訂日 施行日 改訂理由 改訂内容 改訂責任者
QCWS 参考プロトコル 抗 HLA 抗体検査 (ICFA) 2019 年度版 作成者日本組織適合性学会認定制度委員会ワーキンググループ抗 HLA 抗体 WG 制定 改訂履歴 版数 制定日 施行日 制定理由 作成責任者 初版 日本組織適合性学会が開催する QCWS での HLA 検査を実施する際に用いる QCWS 参考プロトコルとして制定した WG 版数 改訂日 施行日 改訂理由 改訂内容 改訂責任者
しょうゆの食塩分測定方法 ( モール法 ) 手順書 1. 適用範囲 この手順書は 日本農林規格に定めるしょうゆに適用する 2. 測定方法の概要 試料に水を加え 指示薬としてクロム酸カリウム溶液を加え 0.02 mol/l 硝酸銀溶液で滴定し 滴定終点までに消費した硝酸銀溶液の量から塩化ナトリウム含有
 しょうゆの食塩分測定方法 ( モール法 ) 手順書 1. 適用範囲 この手順書は 日本農林規格に定めるしょうゆに適用する 2. 測定方法の概要 試料に水を加え 指示薬としてクロム酸カリウム溶液を加え 0.02 mol/l 硝酸銀溶液で滴定し 滴定終点までに消費した硝酸銀溶液の量から塩化ナトリウム含有量を算出する 3. 注意事項 (a) クロム酸カリウムを取り扱う際には 皮膚に付けたり粉塵を吸入しないようゴーグル型保護メガネ
しょうゆの食塩分測定方法 ( モール法 ) 手順書 1. 適用範囲 この手順書は 日本農林規格に定めるしょうゆに適用する 2. 測定方法の概要 試料に水を加え 指示薬としてクロム酸カリウム溶液を加え 0.02 mol/l 硝酸銀溶液で滴定し 滴定終点までに消費した硝酸銀溶液の量から塩化ナトリウム含有量を算出する 3. 注意事項 (a) クロム酸カリウムを取り扱う際には 皮膚に付けたり粉塵を吸入しないようゴーグル型保護メガネ
安全データシート LOCTITE 242 MEDIUM STRENGTH THREADLOCKER known as 242 Threadlocker 250ML EN/CH/JP Page 1 of 7 SDS No. : V001.3 改訂 : 発行日 : 2
 安全データシート as 242 Threadlocker 250ML EN/CH/JP Page 1 of 7 SDS No. : 150233 改訂 : 04.11.2015 発行日 : 29.12.2015 1. 化学物質等及び会社情報 製品コード : 235195 製品名 : as 242 Threadlocker 250ML EN/CH/JP 会社名 : ヘンケルジャパン株式会社東京都品川区東品川
安全データシート as 242 Threadlocker 250ML EN/CH/JP Page 1 of 7 SDS No. : 150233 改訂 : 04.11.2015 発行日 : 29.12.2015 1. 化学物質等及び会社情報 製品コード : 235195 製品名 : as 242 Threadlocker 250ML EN/CH/JP 会社名 : ヘンケルジャパン株式会社東京都品川区東品川
ISOSPIN Plasmid
 プラスミド DNA 抽出キット ISOSPIN Plasmid マニュアル ( 第 5 版 ) Code No. 318-07991 NIPPON GENE CO., LTD. I 製品説明 ISOSPIN Plasmid( アイソスピンプラスミド ) は スピンカラムを用いて簡単に大腸菌から高純度なプラスミド DNA を抽出できるキットです 本キットは カオトロピックイオン存在下で DNA がシリカへ吸着する原理を応用しており
プラスミド DNA 抽出キット ISOSPIN Plasmid マニュアル ( 第 5 版 ) Code No. 318-07991 NIPPON GENE CO., LTD. I 製品説明 ISOSPIN Plasmid( アイソスピンプラスミド ) は スピンカラムを用いて簡単に大腸菌から高純度なプラスミド DNA を抽出できるキットです 本キットは カオトロピックイオン存在下で DNA がシリカへ吸着する原理を応用しており
Microsoft PowerPoint - ELISA MAX Standard Protocol
 Sandwich ELISA Protocol ELISA MAX TM Standard set トミーデジタルバイオロジーアライアンストプロダクトカスタマーサポート 試薬の構成 1 Capture Antibody (200 倍 ) 2 Detection Antibody (200 倍 ) 3 Standard 4 Avidin - HRP (1000 倍 ) 5 Instruction Sheet
Sandwich ELISA Protocol ELISA MAX TM Standard set トミーデジタルバイオロジーアライアンストプロダクトカスタマーサポート 試薬の構成 1 Capture Antibody (200 倍 ) 2 Detection Antibody (200 倍 ) 3 Standard 4 Avidin - HRP (1000 倍 ) 5 Instruction Sheet
Multiplex PCR Assay Kit
 研究用 Multiplex PCR Assay Kit 説明書 v201510da マルチプレックス PCR は 一つの PCR 反応系に複数のプライマー対を同時に使用することで 複数の遺伝子領域を同時に増幅する方法です マルチプレックス PCR を行うことで 試薬や機材の節約による経済性 同時検出による迅速性でのメリットに加え 貴重なサンプルの有効利用も可能です しかし マルチプレックス PCR
研究用 Multiplex PCR Assay Kit 説明書 v201510da マルチプレックス PCR は 一つの PCR 反応系に複数のプライマー対を同時に使用することで 複数の遺伝子領域を同時に増幅する方法です マルチプレックス PCR を行うことで 試薬や機材の節約による経済性 同時検出による迅速性でのメリットに加え 貴重なサンプルの有効利用も可能です しかし マルチプレックス PCR
本日の内容 HbA1c 測定方法別原理と特徴 HPLC 法 免疫法 酵素法 原理差による測定値の乖離要因
 HbA1c 測定系について ~ 原理と特徴 ~ 一般社団法人日本臨床検査薬協会 技術運営委員会副委員長 安部正義 本日の内容 HbA1c 測定方法別原理と特徴 HPLC 法 免疫法 酵素法 原理差による測定値の乖離要因 HPLC 法 HPLC 法原理 高速液体クロマトグラフィー 混合物の分析法の一つ 固体または液体の固定相 ( 吸着剤 ) 中で 液体または気体の移動相 ( 展開剤 ) に試料を加えて移動させ
HbA1c 測定系について ~ 原理と特徴 ~ 一般社団法人日本臨床検査薬協会 技術運営委員会副委員長 安部正義 本日の内容 HbA1c 測定方法別原理と特徴 HPLC 法 免疫法 酵素法 原理差による測定値の乖離要因 HPLC 法 HPLC 法原理 高速液体クロマトグラフィー 混合物の分析法の一つ 固体または液体の固定相 ( 吸着剤 ) 中で 液体または気体の移動相 ( 展開剤 ) に試料を加えて移動させ
14551 フェノール ( チアゾール誘導体法 ) 測定範囲 : 0.10~2.50 mg/l C 6H 5OH 結果は mmol/l 単位でも表示できます 1. 試料の ph が ph 2~11 であるかチェックします 必要な場合 水酸化ナトリウム水溶液または硫酸を 1 滴ずつ加えて ph を調整
 14551 フェノール ( チアゾール誘導体法 ) 0.10~2.50 mg/l C 6H 5OH 結果は mmol/l 単位でも表示できます 2. ピペットで 10 ml の試料を反応セルに取り ねじぶたで閉じて攪拌します 3. グレーのミクロスプーンで 1 回分の試薬 Ph-1K を加えて ねじぶたでセルを閉じます 4. セルをよく振とうして 固体物を溶かします 5. 緑のミクロスプーンで 1
14551 フェノール ( チアゾール誘導体法 ) 0.10~2.50 mg/l C 6H 5OH 結果は mmol/l 単位でも表示できます 2. ピペットで 10 ml の試料を反応セルに取り ねじぶたで閉じて攪拌します 3. グレーのミクロスプーンで 1 回分の試薬 Ph-1K を加えて ねじぶたでセルを閉じます 4. セルをよく振とうして 固体物を溶かします 5. 緑のミクロスプーンで 1
安全データシート 物質または混合物情報 セクション 1: 化学物質 / 混合物および会社 / 企業情報 製品コード製品名 Ampicillin Sodium Salt, irradiated 会社 / 企業情報 Life Technologies 5791 Van Allen Wa
 安全データシート 物質または混合物情報 セクション 1: 化学物質 / 混合物および会社 / 企業情報 製品コード 会社 / 企業情報 Life Technologies 5791 Van Allen Way PO Box 6482 Carlsbad, CA 92008 +1 760 603 7200 108-0023 東京都港区芝浦四丁目 2 番 8 号住友不動産三田ツインビル東館ライフテクノロジーズジャパン株式会社
安全データシート 物質または混合物情報 セクション 1: 化学物質 / 混合物および会社 / 企業情報 製品コード 会社 / 企業情報 Life Technologies 5791 Van Allen Way PO Box 6482 Carlsbad, CA 92008 +1 760 603 7200 108-0023 東京都港区芝浦四丁目 2 番 8 号住友不動産三田ツインビル東館ライフテクノロジーズジャパン株式会社
Microsoft Word - PI-LY 615-JP-V3 amends Japanese only
 Leucosep Tube LTK.615 添付文書 体外診断用医薬品 取扱説明書 用途 Leucosep 管は 全血から末梢血単核細胞 (PBMC) を収集および分離するために使用される Leucosep 管の使用により ELISPOT 検査にて全血から FICOLL-PAQUE* PLUS を用いて PBMC を分離する作業よりも容易に PBMC を分離することができる 概要 ELISPOT 検査は
Leucosep Tube LTK.615 添付文書 体外診断用医薬品 取扱説明書 用途 Leucosep 管は 全血から末梢血単核細胞 (PBMC) を収集および分離するために使用される Leucosep 管の使用により ELISPOT 検査にて全血から FICOLL-PAQUE* PLUS を用いて PBMC を分離する作業よりも容易に PBMC を分離することができる 概要 ELISPOT 検査は
Microsoft Word D_コバス システム HBV_第5校(再校了用)(最終校)
 体外診断用医薬品 ** 2017 年 7 月改訂 ( 第 4 版 ) * 2017 年 3 月改訂 ( 第 3 版 ) 製造販売承認番号 :22800EZX00052000 B 型肝炎ウイルスコア核酸キットコバス 6800/8800 システム HBV 全般的な注意 1. 本品は体外診断用であり それ以外の目的には使用しないでください 2. 測定結果に基づく臨床診断は 臨床症状やほかの検査結果などと併せて
体外診断用医薬品 ** 2017 年 7 月改訂 ( 第 4 版 ) * 2017 年 3 月改訂 ( 第 3 版 ) 製造販売承認番号 :22800EZX00052000 B 型肝炎ウイルスコア核酸キットコバス 6800/8800 システム HBV 全般的な注意 1. 本品は体外診断用であり それ以外の目的には使用しないでください 2. 測定結果に基づく臨床診断は 臨床症状やほかの検査結果などと併せて
この添付文書をよく読んでから使用してください 体外診断用医薬品 2019 年 2 月作成 ( 第 1 版 ) 製造販売承認番号 22700AMX PIVKA-Ⅱ キット P I V K A -Ⅱ アボット ja PIVKA 01R R02 B1R17J 全般的な注意
 この添付文書をよく読んでから使用してください 体外診断用医薬品 2019 年 2 月作成 ( 第 1 版 ) 製造販売承認番号 22700AMX00710000 PIVKA-Ⅱ キット P I V K A -Ⅱ アボット ja PIVKA 01R17 470735R02 B1R17J 全般的な注意 本製品は体外診断用であり それ以外の目的に使用しないこと 診断は 他の関連する検査結果や臨床症状等に基づいて総合的に判断すること
この添付文書をよく読んでから使用してください 体外診断用医薬品 2019 年 2 月作成 ( 第 1 版 ) 製造販売承認番号 22700AMX00710000 PIVKA-Ⅱ キット P I V K A -Ⅱ アボット ja PIVKA 01R17 470735R02 B1R17J 全般的な注意 本製品は体外診断用であり それ以外の目的に使用しないこと 診断は 他の関連する検査結果や臨床症状等に基づいて総合的に判断すること
(2) 必要な器具 器材 試料等 ARCHITECT i システムアッセイ CD-ROM BNP-JP 用 ARCHITECT BNP-JP キャリブレータ (ARCHITECT BNP-JP Calibrators) ( 製品番号 :2P14-01):4 ml 6 キャリブレータ (pg/ml)
 ** 612-030 3/16 この添付文書をよく読んでから使用してください 体外診断用医薬品 ** 2016 年 7 月改訂 ( 第 7 版 ) * 2015 年 2 月改訂 ( 第 6 版 ) 製造販売認証番号 220AIAMX00002000 ヒト脳性ナトリウム利尿ペプチドキット B N P -J P アボット 室温または 2 ~ 8 に保存した検体を先に示した時間以内に測定できない場合には
** 612-030 3/16 この添付文書をよく読んでから使用してください 体外診断用医薬品 ** 2016 年 7 月改訂 ( 第 7 版 ) * 2015 年 2 月改訂 ( 第 6 版 ) 製造販売認証番号 220AIAMX00002000 ヒト脳性ナトリウム利尿ペプチドキット B N P -J P アボット 室温または 2 ~ 8 に保存した検体を先に示した時間以内に測定できない場合には
Taro-kv12250.jtd
 ニューカッスル病 マレック病 ( ニューカッスル病ウイルス由来 F 蛋白遺伝子導入マレック病ウイルス 1 型 ) 凍結生ワクチン 平成 22 年 8 月 12 日 ( 告示第 2288 号 ) 新規追加 ニューカッスル病ウイルスのF 蛋白をコードする遺伝子を弱毒マレック病ウイルス (1 型 ) に挿入して得られた組換え体ウイルスを培養細胞で増殖させて得た感染細胞浮遊液を凍結したワクチンである 1 小分製品の試験
ニューカッスル病 マレック病 ( ニューカッスル病ウイルス由来 F 蛋白遺伝子導入マレック病ウイルス 1 型 ) 凍結生ワクチン 平成 22 年 8 月 12 日 ( 告示第 2288 号 ) 新規追加 ニューカッスル病ウイルスのF 蛋白をコードする遺伝子を弱毒マレック病ウイルス (1 型 ) に挿入して得られた組換え体ウイルスを培養細胞で増殖させて得た感染細胞浮遊液を凍結したワクチンである 1 小分製品の試験
国立感染症研究所血液 安全性研究部 HBV-DNA 国内標準品及び HIV-RNA 国内標準品の力価の再評価のための共同研究 1. 背景と目的血液製剤のウイルス安全性の確保対策として実施されている原料血漿と輸血用血液のウイルス核酸増幅試験 (NAT) のための HCV HBV 及び HIV の国内標
 血液事業部会安全技術調査会 平成 28 年 8 月 日国立感染症研究所血液 安全性研究部 HBV-DNA 国内標準品及び HIV-RNA 国内標準品の力価の再評価 血液製剤のウイルス安全性の確保対策として実施されている原料血漿と輸血用血液のウイルス核酸増幅試験 (NAT) のための HCV HBV 及び HIV の国内標準品が製造されてから 10 年以上が経過した これらの国内標準品は当時の WHO
血液事業部会安全技術調査会 平成 28 年 8 月 日国立感染症研究所血液 安全性研究部 HBV-DNA 国内標準品及び HIV-RNA 国内標準品の力価の再評価 血液製剤のウイルス安全性の確保対策として実施されている原料血漿と輸血用血液のウイルス核酸増幅試験 (NAT) のための HCV HBV 及び HIV の国内標準品が製造されてから 10 年以上が経過した これらの国内標準品は当時の WHO
組織からのゲノム DNA 抽出キット Tissue Genomic DNA Extraction Mini Kit 目次基本データ 3 キットの内容 3 重要事項 4 操作 4 サンプル別プロトコール 7 トラブルシューティング 9 * 本製品は研究用です *
 組織からのゲノム DNA 抽出キット Tissue Genomic DNA Extraction Mini Kit 目次基本データ 3 キットの内容 3 重要事項 4 操作 4 サンプル別プロトコール 7 トラブルシューティング 9 * 本製品は研究用です * 2 本キットは動物の組織からトータル DNA を迅速に効率よく抽出するようにデザインされています また 細菌 固定組織 酵母用のプロトコールも用意しています
組織からのゲノム DNA 抽出キット Tissue Genomic DNA Extraction Mini Kit 目次基本データ 3 キットの内容 3 重要事項 4 操作 4 サンプル別プロトコール 7 トラブルシューティング 9 * 本製品は研究用です * 2 本キットは動物の組織からトータル DNA を迅速に効率よく抽出するようにデザインされています また 細菌 固定組織 酵母用のプロトコールも用意しています
TaKaRa PCR Human Papillomavirus Detection Set
 研究用 TaKaRa PCR Human Papillomavirus Detection Set 説明書 v201703da 本製品は子宮頸癌において最も高頻度に検出される Human Papillomavirus(HPV)16 18 および 33 型をそれぞれ特異的に増幅し 検出するセットです HPV16 18 および 33 型の E6 を含む領域 (140 bp ただし HPV33 型は 141
研究用 TaKaRa PCR Human Papillomavirus Detection Set 説明書 v201703da 本製品は子宮頸癌において最も高頻度に検出される Human Papillomavirus(HPV)16 18 および 33 型をそれぞれ特異的に増幅し 検出するセットです HPV16 18 および 33 型の E6 を含む領域 (140 bp ただし HPV33 型は 141
* G0-2462/R05 全般的な注意 この添付文書をよく読んでから使用してください 体外診断用医薬品 ** 2015 年 8 月改訂 ( 第 8 版 ) * 2015 年 6 月改訂 ( 第 7 版 ) 製造販売承認番号 21800AMY ヒト免疫不全症ウイルス 1p24 抗原
 * G0-2462/R05 全般的な注意 この添付文書をよく読んでから使用してください 体外診断用医薬品 ** 2015 年 8 月改訂 ( 第 8 版 ) * 2015 年 6 月改訂 ( 第 7 版 ) 製造販売承認番号 21800AMY10140000 ヒト免疫不全症ウイルス 1p24 抗原 HIV 抗体キット HIV Ag/Ab コンボアッセイ アボット 1. 本製品は体外診断用であり それ以外の目的に使用しないこと
* G0-2462/R05 全般的な注意 この添付文書をよく読んでから使用してください 体外診断用医薬品 ** 2015 年 8 月改訂 ( 第 8 版 ) * 2015 年 6 月改訂 ( 第 7 版 ) 製造販売承認番号 21800AMY10140000 ヒト免疫不全症ウイルス 1p24 抗原 HIV 抗体キット HIV Ag/Ab コンボアッセイ アボット 1. 本製品は体外診断用であり それ以外の目的に使用しないこと
体外診断用医薬品 この添付文書をよく読んでから使用してください *2018 年 2 月改訂 ( 第 2 版 ) 製造販売承認番号 : 22900EZX 年 3 月作成 ( 第 1 版 ) ROS1 融合遺伝子検出キット OncoGuide AmoyDx R
 体外診断用医薬品 この添付文書をよく読んでから使用してください *208 年 2 月改訂 ( 第 2 版 ) 製造販売承認番号 : 22900EZX00002000 207 年 3 月作成 ( 第 版 ) ROS 融合遺伝子検出キット 84090000 OncoGuide AmoyDx ROS 融合遺伝子検出キット 全般的な注意. 本製品は 体外診断用医薬品であり それ以外の目的には使用しないでください
体外診断用医薬品 この添付文書をよく読んでから使用してください *208 年 2 月改訂 ( 第 2 版 ) 製造販売承認番号 : 22900EZX00002000 207 年 3 月作成 ( 第 版 ) ROS 融合遺伝子検出キット 84090000 OncoGuide AmoyDx ROS 融合遺伝子検出キット 全般的な注意. 本製品は 体外診断用医薬品であり それ以外の目的には使用しないでください
安全データシート Page 1 of 7 LOCTITE 601 SDS No. : V001.5 改訂 : 発行日 : 製品コード : 製品名 : LOCTITE 化学物質等及び会社情報 会社名 : ヘンケルジャ
 安全データシート Page 1 of 7 SDS No. : 173085 改訂 : 08.02.2016 発行日 : 06.06.2016 製品コード : 234623 製品名 : 1. 化学物質等及び会社情報 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8 スフィアタワー天王洲 14F 140-0002 電話番号 : +81 (45) 758-1820 FAX 番号 : +81
安全データシート Page 1 of 7 SDS No. : 173085 改訂 : 08.02.2016 発行日 : 06.06.2016 製品コード : 234623 製品名 : 1. 化学物質等及び会社情報 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8 スフィアタワー天王洲 14F 140-0002 電話番号 : +81 (45) 758-1820 FAX 番号 : +81
実験操作方法
 実験操作方法 A. サンプル ( 菌液 ) の調製検出目的の菌種に適した方法でサンプル調製を行い 最終的に100μl 程度の菌懸濁液を用意してください このサンプル液のうち40μlを B.EMA 処理 に使用します 残りは氷上もしくは4 で保存し EMA 処理なしサンプルを用意するために40μlを B.EMA 処理 8) 加熱殺菌 ( 不活化処理 ) の操作を行った後 C. 核酸抽出 に使用します
実験操作方法 A. サンプル ( 菌液 ) の調製検出目的の菌種に適した方法でサンプル調製を行い 最終的に100μl 程度の菌懸濁液を用意してください このサンプル液のうち40μlを B.EMA 処理 に使用します 残りは氷上もしくは4 で保存し EMA 処理なしサンプルを用意するために40μlを B.EMA 処理 8) 加熱殺菌 ( 不活化処理 ) の操作を行った後 C. 核酸抽出 に使用します
生物学に関する実験例 - 生化学 / 医療に関する実験例 ラジオアッセイ法によるホルモン測定 [ 目的 ] 本実習では, 放射免疫測定 (Radioimmunoassay,RIA) 法による血中インスリンとイムノラジオメトリックアッセイ ( 免疫放射定測定 Immunoradiometric ass
![生物学に関する実験例 - 生化学 / 医療に関する実験例 ラジオアッセイ法によるホルモン測定 [ 目的 ] 本実習では, 放射免疫測定 (Radioimmunoassay,RIA) 法による血中インスリンとイムノラジオメトリックアッセイ ( 免疫放射定測定 Immunoradiometric ass 生物学に関する実験例 - 生化学 / 医療に関する実験例 ラジオアッセイ法によるホルモン測定 [ 目的 ] 本実習では, 放射免疫測定 (Radioimmunoassay,RIA) 法による血中インスリンとイムノラジオメトリックアッセイ ( 免疫放射定測定 Immunoradiometric ass](/thumbs/104/163903931.jpg) 生物学に関する実験例 - 生化学 / 医療に関する実験例 ラジオアッセイ法によるホルモン測定 [ 目的 ] 本実習では, 放射免疫測定 (Radioimmunoassay,RIA) 法による血中インスリンとイムノラジオメトリックアッセイ ( 免疫放射定測定 Immunoradiometric assay, IRMA) 法による血清中のレニンを定量を通して 今日用いられている種々のインビトロ検査法の原理並びに両者の違い等を理解する
生物学に関する実験例 - 生化学 / 医療に関する実験例 ラジオアッセイ法によるホルモン測定 [ 目的 ] 本実習では, 放射免疫測定 (Radioimmunoassay,RIA) 法による血中インスリンとイムノラジオメトリックアッセイ ( 免疫放射定測定 Immunoradiometric assay, IRMA) 法による血清中のレニンを定量を通して 今日用いられている種々のインビトロ検査法の原理並びに両者の違い等を理解する
Gen とるくん™(酵母用)High Recovery
 研究用 Gen とるくん ( 酵母用 ) High Recovery 説明書 v201510da Gen とるくん ( 酵母用 )High Recovery は 細胞壁分解酵素による酵母菌体処理と塩析による DNA 精製の組み合わせにより 効率良く酵母ゲノム DNA を抽出 精製するためのキットです 本キットを用いた酵母ゲノム DNA 調製操作は 遠心による酵母菌体の回収 GenTLE Yeast
研究用 Gen とるくん ( 酵母用 ) High Recovery 説明書 v201510da Gen とるくん ( 酵母用 )High Recovery は 細胞壁分解酵素による酵母菌体処理と塩析による DNA 精製の組み合わせにより 効率良く酵母ゲノム DNA を抽出 精製するためのキットです 本キットを用いた酵母ゲノム DNA 調製操作は 遠心による酵母菌体の回収 GenTLE Yeast
Microsoft Word - SDS_9P _9P40H_CSC506-1_Alinity Cyfra CNJ
 シフラ アボット アボットジャパン株式会社 CSC506-1 2018/09/03 1/7 安全データシート 1. 製品及び会社情報 製品名シフラ アボット ( コンジュゲート ) 製品コード 9P40-02-01_9P40H (100 x 2 回用 ) 会社名アボットジャパン株式会社住所東京都港区三田三丁目 5 番 27 号 担当部門 電話番号 0120-031441 緊急連絡先 整理番号 2.
シフラ アボット アボットジャパン株式会社 CSC506-1 2018/09/03 1/7 安全データシート 1. 製品及び会社情報 製品名シフラ アボット ( コンジュゲート ) 製品コード 9P40-02-01_9P40H (100 x 2 回用 ) 会社名アボットジャパン株式会社住所東京都港区三田三丁目 5 番 27 号 担当部門 電話番号 0120-031441 緊急連絡先 整理番号 2.
A6/25 アンモニウム ( インドフェノールブルー法 ) 測定範囲 : 0.20~8.00 mg/l NH 4-N 0.26~10.30 mg/l NH ~8.00 mg/l NH 3-N 0.24~9.73 mg/l NH 3 結果は mmol/l 単位でも表示できます 1. 試料の
 A6/25 アンモニウム ( インドフェノールブルー法 ) 測定範囲 : 0.20~8.00 mg/l NH 4-N 0.26~10.30 mg/l NH 4 0.20~8.00 mg/l NH 3-N 0.24~9.73 mg/l NH 3 2. ピペットで 1.0ml の試料を反応セルに取り ねじぶたで閉じて攪拌します 3. 青の計量キャップで 1 回分の試薬 NH 4-1K を加えて ねじぶたでセルを閉じます
A6/25 アンモニウム ( インドフェノールブルー法 ) 測定範囲 : 0.20~8.00 mg/l NH 4-N 0.26~10.30 mg/l NH 4 0.20~8.00 mg/l NH 3-N 0.24~9.73 mg/l NH 3 2. ピペットで 1.0ml の試料を反応セルに取り ねじぶたで閉じて攪拌します 3. 青の計量キャップで 1 回分の試薬 NH 4-1K を加えて ねじぶたでセルを閉じます
安全データシート Page 1 of 8 LOCTITE 263 THREADLOCKER SDS No. : V001.3 改訂 : 発行日 : 化学物質等及び会社情報 製品コード : 製品名 : LOCTITE 26
 安全データシート Page 1 of 8 SDS No. : 347828 改訂 : 17.03.2016 発行日 : 28.03.2016 1. 化学物質等及び会社情報 製品コード : 1307415 製品名 : 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8 スフィアタワー天王洲 14F 140-0002 電話番号 : +81 (45) 758-1820 FAX 番号 : +81
安全データシート Page 1 of 8 SDS No. : 347828 改訂 : 17.03.2016 発行日 : 28.03.2016 1. 化学物質等及び会社情報 製品コード : 1307415 製品名 : 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8 スフィアタワー天王洲 14F 140-0002 電話番号 : +81 (45) 758-1820 FAX 番号 : +81
Cytotoxicity LDH Assay Kit-WST
 ytotoxicity L ssay Kit-WST はじめに 本説明書は ytotoxicity L ssay Kit-WST を用いた抗体依存性細胞傷害測定用 (ntibody-dependent cellmediated cytotoxicity: ) です 本製品のキット内容や Working Solution の調製方法に関して 製品添付の取扱い説明書も合わせてご覧ください 正確な測定のために
ytotoxicity L ssay Kit-WST はじめに 本説明書は ytotoxicity L ssay Kit-WST を用いた抗体依存性細胞傷害測定用 (ntibody-dependent cellmediated cytotoxicity: ) です 本製品のキット内容や Working Solution の調製方法に関して 製品添付の取扱い説明書も合わせてご覧ください 正確な測定のために
Page 2 of 6 危険有害性情報 : 安全対策 H315 皮膚刺激 H317 アレルギ一性皮膚反応を起こすおそれ H318 重篤な眼の損傷 H401 水生生物に毒性 H412 長期継続的影響によって水生生物に有害 P261 粉じん / 煙 / ガス / ミスト / 蒸気 / スプレーの吸入を避
 安全データシート Page 1 of 6 SDS No. : 450822 改訂 : 01.05.2015 発行日 : 29.12.2015 1. 化学物質等及び会社情報 製品コード : 1835937 製品名 : 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8 スフィアタワー天王洲 14F 140-0002 電話番号 : +81 (45) 758-1820 FAX 番号 : +81
安全データシート Page 1 of 6 SDS No. : 450822 改訂 : 01.05.2015 発行日 : 29.12.2015 1. 化学物質等及び会社情報 製品コード : 1835937 製品名 : 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8 スフィアタワー天王洲 14F 140-0002 電話番号 : +81 (45) 758-1820 FAX 番号 : +81
危険有害性情報 H302 - 飲み込むと有害 H312 - 皮膚に接触すると有害 H332 - 吸入すると有害 注意書き P301 + P312 - 飲み込んだ場合 : 気分が悪い時は医師に連絡すること P302 + P352 - 皮膚に付着した場合 : 多量の水と石鹸で洗うこと P304 + P3
 安全データシート セクション1: 化学物質 / 混合物および会社 / 企業情報物質または混合物情報 製品コード製品名 R0821 BCIP-T 会社 / 企業情報 Life Technologies Corporation 5781 Van Allen Way PO Box 6482 Carlsbad, CA 92008 +1 760 603 7200 Thermo Fisher Scientific
安全データシート セクション1: 化学物質 / 混合物および会社 / 企業情報物質または混合物情報 製品コード製品名 R0821 BCIP-T 会社 / 企業情報 Life Technologies Corporation 5781 Van Allen Way PO Box 6482 Carlsbad, CA 92008 +1 760 603 7200 Thermo Fisher Scientific
針刺し切創発生時の対応
 1. 初期対応 1) 発生直後の対応 (1) 曝露部位 ( 針刺し 切創等の経皮的創傷 粘膜 皮膚など ) を確認する (2) 曝露部位を直ちに洗浄する 1 創傷 粘膜 正常な皮膚 創傷のある皮膚 : 流水 石鹸で十分に洗浄する 2 口腔 : 大量の水でうがいする 3 眼 : 生理食塩水で十分に洗浄する (3) 曝露の程度 ( 深さ 体液注入量 直接接触量 皮膚の状態 ) を確認する (4) 原因鋭利器材の種類
1. 初期対応 1) 発生直後の対応 (1) 曝露部位 ( 針刺し 切創等の経皮的創傷 粘膜 皮膚など ) を確認する (2) 曝露部位を直ちに洗浄する 1 創傷 粘膜 正常な皮膚 創傷のある皮膚 : 流水 石鹸で十分に洗浄する 2 口腔 : 大量の水でうがいする 3 眼 : 生理食塩水で十分に洗浄する (3) 曝露の程度 ( 深さ 体液注入量 直接接触量 皮膚の状態 ) を確認する (4) 原因鋭利器材の種類
[PDF] GST融合タンパク質バッチ精製プロトコール
![[PDF] GST融合タンパク質バッチ精製プロトコール [PDF] GST融合タンパク質バッチ精製プロトコール](/thumbs/54/33323027.jpg) Glutathione Sepharose 4B, 4FF を用いた GST 融合タンパク質のバッチ精製プロトコール 1 予め準備する試薬と装置 Glutathione Sepharose 担体製品名 包装単位 コード番号 Glutathione Sepharose 4B 10 ml 17-0756-01 Glutathione Sepharose 4B 3 10 ml 72-0239-03 Glutathione
Glutathione Sepharose 4B, 4FF を用いた GST 融合タンパク質のバッチ精製プロトコール 1 予め準備する試薬と装置 Glutathione Sepharose 担体製品名 包装単位 コード番号 Glutathione Sepharose 4B 10 ml 17-0756-01 Glutathione Sepharose 4B 3 10 ml 72-0239-03 Glutathione
医薬品タンパク質は 安全性の面からヒト型が常識です ではなぜ 肌につける化粧品用コラーゲンは ヒト型でなくても良いのでしょうか? アレルギーは皮膚から 最近の学説では 皮膚から侵入したアレルゲンが 食物アレルギー アトピー性皮膚炎 喘息 アレルギー性鼻炎などのアレルギー症状を引き起こすきっかけになる
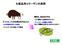 化粧品用コラーゲンの原料 現在は 魚由来が中心 かつては ウシの皮膚由来がほとんど BSE 等病原体混入の危険 人に感染する病原体をもたない アレルギーの問題は未解決 ( むしろ問題は大きくなったかもしれない ) アレルギーを引き起こす可能性 医薬品タンパク質は 安全性の面からヒト型が常識です ではなぜ 肌につける化粧品用コラーゲンは ヒト型でなくても良いのでしょうか? アレルギーは皮膚から 最近の学説では
化粧品用コラーゲンの原料 現在は 魚由来が中心 かつては ウシの皮膚由来がほとんど BSE 等病原体混入の危険 人に感染する病原体をもたない アレルギーの問題は未解決 ( むしろ問題は大きくなったかもしれない ) アレルギーを引き起こす可能性 医薬品タンパク質は 安全性の面からヒト型が常識です ではなぜ 肌につける化粧品用コラーゲンは ヒト型でなくても良いのでしょうか? アレルギーは皮膚から 最近の学説では
安全データシート LOCTITE 262 HIGH STRENGTH THREADLOCKER known as 262 Threadlocker 50ML EN/CH/JP Page 1 of 6 SDS No. : V001.4 改訂 : 発行日 : 26.0
 安全データシート 262 Threadlocker 50ML EN/CH/JP Page 1 of 6 SDS No. : 153483 改訂 : 22.03.2016 発行日 : 26.09.2016 1. 化学物質等及び会社情報 製品コード : 232073 製品名 : 262 Threadlocker 50ML EN/CH/JP 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8
安全データシート 262 Threadlocker 50ML EN/CH/JP Page 1 of 6 SDS No. : 153483 改訂 : 22.03.2016 発行日 : 26.09.2016 1. 化学物質等及び会社情報 製品コード : 232073 製品名 : 262 Threadlocker 50ML EN/CH/JP 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8
3. 安全性本治験において治験薬が投与された 48 例中 1 例 (14 件 ) に有害事象が認められた いずれの有害事象も治験薬との関連性は あり と判定されたが いずれも軽度 で処置の必要はなく 追跡検査で回復を確認した また 死亡 その他の重篤な有害事象が認められなか ったことから 安全性に問
 フェキソフェナジン塩酸塩錠 6mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにフェキソフェナジン塩酸塩は 第二世代抗ヒスタミン薬の一つであり 抗原抗体反応に伴って起こる肥満細胞からのヒスタミンなどのケミカルメディエーターの遊離を抑制すると共に ヒスタミンの H1 作用に拮抗することにより アレルギー症状を緩和する 今回 フェキソフェナジン塩酸塩錠 6mg
フェキソフェナジン塩酸塩錠 6mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにフェキソフェナジン塩酸塩は 第二世代抗ヒスタミン薬の一つであり 抗原抗体反応に伴って起こる肥満細胞からのヒスタミンなどのケミカルメディエーターの遊離を抑制すると共に ヒスタミンの H1 作用に拮抗することにより アレルギー症状を緩和する 今回 フェキソフェナジン塩酸塩錠 6mg
目 次 Ⅰ. キットの構成 3 Ⅱ. その他必要な器具 装置 3 Ⅲ. 試薬の調製法 4 Ⅳ. 操作手順 ( ローレンジ法 ) 5 小麦タンパク質濃度の算出法 6 標準曲線の例 6 グルテン含量の算出法 7 Ⅴ. 操作手順 ( ハイレンジ法 ) 7 グルテン含量の算出法 8 Ⅵ. キットの保存条件と
 2018 年 7 月第 2 版 研究用試薬 Wheat/Gluten ELISA Kit 操作手順書 お願い 製品をご使用になる前に キット添付の取扱説明書 ( 英語 ) を必ずお読みください 横浜市金沢区幸浦 2-1-16 236-0003 URL:http://www.miobs.com E-MAIL:info@miobs.com 目 次 Ⅰ. キットの構成 3 Ⅱ. その他必要な器具 装置 3
2018 年 7 月第 2 版 研究用試薬 Wheat/Gluten ELISA Kit 操作手順書 お願い 製品をご使用になる前に キット添付の取扱説明書 ( 英語 ) を必ずお読みください 横浜市金沢区幸浦 2-1-16 236-0003 URL:http://www.miobs.com E-MAIL:info@miobs.com 目 次 Ⅰ. キットの構成 3 Ⅱ. その他必要な器具 装置 3
(Microsoft Word - FlowPRA\220\335\222\350ADC.docx)
 Navios における FlowPRA プロトコルの自動感度設定 設定に必要な試薬 機器類 1.) プロトコルの 動感度設定には以下のベックマン コールター社製の試薬が必要です 製品番号製品名内容定価 177018 QuickComp 2 キット CD45-FITC/CD45-PE 各 1 ml(50 テスト ) 32,000 6607023 CYTO-COMP Cell キット 10 テスト 5
Navios における FlowPRA プロトコルの自動感度設定 設定に必要な試薬 機器類 1.) プロトコルの 動感度設定には以下のベックマン コールター社製の試薬が必要です 製品番号製品名内容定価 177018 QuickComp 2 キット CD45-FITC/CD45-PE 各 1 ml(50 テスト ) 32,000 6607023 CYTO-COMP Cell キット 10 テスト 5
16S (V3-V4) Metagenomic Library Construction Kit for NGS
 研究用 16S (V3-V4) Metagenomic Library Construction Kit for NGS 説明書 v201705da 本製品は イルミナ社 MiSeq で 16S rrna 細菌叢解析を行うための PCR 増幅キットです 細菌 16S rrna 遺伝子の V3-V4 領域を対象とし PCR 酵素に 多様な配列を効率よく増幅可能な Tks Gflex DNA Polymerase
研究用 16S (V3-V4) Metagenomic Library Construction Kit for NGS 説明書 v201705da 本製品は イルミナ社 MiSeq で 16S rrna 細菌叢解析を行うための PCR 増幅キットです 細菌 16S rrna 遺伝子の V3-V4 領域を対象とし PCR 酵素に 多様な配列を効率よく増幅可能な Tks Gflex DNA Polymerase
Microsoft Word - A5_FlowCount.DOC
 >> http://www.bc-cytometry.com Flow-Count TM を用いた細胞絶対数の測定 5 はじめに - 目印の効用 従来 フローサイトメトリー (FCM) の使用目的は 細胞集団の中のあるポピュレーションの割合 ( 陽性率 ) を調べることが中心でした しかし 今日 造血幹細胞 残存白血球 CD4 陽性 T 細胞数などポピュレーションの割合と同時に その細胞実数 ( 絶対数
>> http://www.bc-cytometry.com Flow-Count TM を用いた細胞絶対数の測定 5 はじめに - 目印の効用 従来 フローサイトメトリー (FCM) の使用目的は 細胞集団の中のあるポピュレーションの割合 ( 陽性率 ) を調べることが中心でした しかし 今日 造血幹細胞 残存白血球 CD4 陽性 T 細胞数などポピュレーションの割合と同時に その細胞実数 ( 絶対数
検体採取 患者の検査前準備 検体採取のタイミング 記号 添加物 ( キャップ色等 ) 採取材料 採取量 測定材料 F 凝固促進剤 + 血清分離剤 ( 青 細 ) 血液 3 ml 血清 H 凝固促進剤 + 血清分離剤 ( ピンク ) 血液 6 ml 血清 I 凝固促進剤 + 血清分離剤 ( 茶色 )
 toxoplasma gondii antibody-igg 連絡先 : 3764 基本情報 分析物 5E156 JLAC10 診療報酬 識別材料 023 血清 測定法 052 化学 生物発光イムノアッセイ (CLEIA) 結果識別 第 2 章 特掲診療料 D012 14 トキソプラズマ抗体 第 3 部 検査 第 1 節 検体検査料 第 1 款 検体検査実施料 ( 免疫学的検査 ) 93 点 加算等
toxoplasma gondii antibody-igg 連絡先 : 3764 基本情報 分析物 5E156 JLAC10 診療報酬 識別材料 023 血清 測定法 052 化学 生物発光イムノアッセイ (CLEIA) 結果識別 第 2 章 特掲診療料 D012 14 トキソプラズマ抗体 第 3 部 検査 第 1 節 検体検査料 第 1 款 検体検査実施料 ( 免疫学的検査 ) 93 点 加算等
Probe qPCR Mix
 研究用 Probe qpcr Mix 説明書 v201710da Probe qpcr Mix は プローブ検出 (5 - ヌクレアーゼ法 ) によるリアルタイム PCR(qPCR) 専用の試薬です 抗体を利用したホットスタート PCR 酵素とリアルタイム PCR 用バッファーをそれぞれ改良することにより PCR 阻害物質に対する高い抵抗性 特異性の高い増幅 高い増幅効率 高い検出感度を実現しました
研究用 Probe qpcr Mix 説明書 v201710da Probe qpcr Mix は プローブ検出 (5 - ヌクレアーゼ法 ) によるリアルタイム PCR(qPCR) 専用の試薬です 抗体を利用したホットスタート PCR 酵素とリアルタイム PCR 用バッファーをそれぞれ改良することにより PCR 阻害物質に対する高い抵抗性 特異性の高い増幅 高い増幅効率 高い検出感度を実現しました
豚繁殖 呼吸障害症候群生ワクチン ( シード ) 平成 24 年 3 月 13 日 ( 告示第 675 号 ) 新規追加 1 定義シードロット規格に適合した弱毒豚繁殖 呼吸障害症候群ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を凍結乾燥したワクチンである 2 製法 2.1 製造用株
 豚繁殖 呼吸障害症候群生ワクチン ( シード ) 平成 24 年 3 月 13 日 ( 告示第 675 号 ) 新規追加 1 定義シードロット規格に適合した弱毒豚繁殖 呼吸障害症候群ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を凍結乾燥したワクチンである 2 製法 2.1 製造用株 2.1.1 名称豚繁殖 呼吸障害症候群ウイルス JJ1882 株又はこれと同等と認められた株 2.1.2
豚繁殖 呼吸障害症候群生ワクチン ( シード ) 平成 24 年 3 月 13 日 ( 告示第 675 号 ) 新規追加 1 定義シードロット規格に適合した弱毒豚繁殖 呼吸障害症候群ウイルスを同規格に適合した株化細胞で増殖させて得たウイルス液を凍結乾燥したワクチンである 2 製法 2.1 製造用株 2.1.1 名称豚繁殖 呼吸障害症候群ウイルス JJ1882 株又はこれと同等と認められた株 2.1.2
GPS 安全性要約書 塩酸(35%)
 作成 :2014 年 2 月 14 日 GPS 安全性要約書塩酸 (35%) この GPS 安全性要約書は 化学産業界の自主的化学物質管理の取組み (GPS : Global Product Strategy) に基づいて 弊社が製造する化学製品の安全な取り扱いに関する概要を提供することを目的としています ヒト健康や環境への影響あるいはリスク評価の詳細 法規制情報や分類 ラベル情報等の専門的な情報を提供するものではありません
作成 :2014 年 2 月 14 日 GPS 安全性要約書塩酸 (35%) この GPS 安全性要約書は 化学産業界の自主的化学物質管理の取組み (GPS : Global Product Strategy) に基づいて 弊社が製造する化学製品の安全な取り扱いに関する概要を提供することを目的としています ヒト健康や環境への影響あるいはリスク評価の詳細 法規制情報や分類 ラベル情報等の専門的な情報を提供するものではありません
試 プロゲステロン IVF-プロゲステロン 低値の特異性が向上し 交差反応が低減される改良試薬へ変更いたします ( 試薬は販売中止となります ) 併せてプロゲステロンの基準値を再設定させていただきます (IVF- プロゲステロンは基準値を設定しており
 トラコマチス DNA 同時同定検査内容変更のお知らせ No.2017-02 変更 2017 年 1 月 謹啓時下ますますご清栄のこととお喜び申し上げます 平素は格別のご高配を賜り厚くお礼申し上げます このたび下記におきまして 検査内容を変更させていただきたくご案内いたします 何卒ご了承賜りますようよろしくお願い申し上げます 敬白 変更実施日 変更項目 プロゲステロン 2017 年 4 月 3 日 (
トラコマチス DNA 同時同定検査内容変更のお知らせ No.2017-02 変更 2017 年 1 月 謹啓時下ますますご清栄のこととお喜び申し上げます 平素は格別のご高配を賜り厚くお礼申し上げます このたび下記におきまして 検査内容を変更させていただきたくご案内いたします 何卒ご了承賜りますようよろしくお願い申し上げます 敬白 変更実施日 変更項目 プロゲステロン 2017 年 4 月 3 日 (
シプロフロキサシン錠 100mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを
 シプロフロキサシン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを有し 上気道感染症 尿路感染症 皮膚感染症などに有効なニューキノロン系の合成抗菌剤である シプロキサン 錠
シプロフロキサシン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを有し 上気道感染症 尿路感染症 皮膚感染症などに有効なニューキノロン系の合成抗菌剤である シプロキサン 錠
Microsoft Word - H30eqa麻疹風疹実施手順書(案)v13日付記載.docx
 平成 30 年度外部精度管理事業 課題 1 麻疹 風疹 実施手順書 ( ウイルスの核酸検出検査 ) 1) 検体を受け取りましたら 外部精度管理事業ホームページ (https://www.niid.go.jp/niid/ja/reference/eqa.html) にてお手続きください 2) 検体到着後 各チューブのスピンダウンを行ってから 500 マイクロリットルの Nuclease-free water
平成 30 年度外部精度管理事業 課題 1 麻疹 風疹 実施手順書 ( ウイルスの核酸検出検査 ) 1) 検体を受け取りましたら 外部精度管理事業ホームページ (https://www.niid.go.jp/niid/ja/reference/eqa.html) にてお手続きください 2) 検体到着後 各チューブのスピンダウンを行ってから 500 マイクロリットルの Nuclease-free water
ウスターソース類の食塩分測定方法 ( モール法 ) 手順書 1. 適用範囲 この手順書は 日本農林規格に定めるウスターソース類及びその周辺製品に適用する 2. 測定方法の概要試料に水を加え ろ過した後 指示薬としてクロム酸カリウム溶液を加え 0.1 mol/l 硝酸銀溶液で滴定し 滴定終点までに消費
 ウスターソース類の食塩分測定方法 ( モール法 ) 手順書 1. 適用範囲 この手順書は 日本農林規格に定めるウスターソース類及びその周辺製品に適用する 2. 測定方法の概要試料に水を加え ろ過した後 指示薬としてクロム酸カリウム溶液を加え 0.1 mol/l 硝酸銀溶液で滴定し 滴定終点までに消費した硝酸銀溶液の量から塩化ナトリウム含有量を算出する 3. 注意事項 (a) クロム酸カリウムを取り扱う際には
ウスターソース類の食塩分測定方法 ( モール法 ) 手順書 1. 適用範囲 この手順書は 日本農林規格に定めるウスターソース類及びその周辺製品に適用する 2. 測定方法の概要試料に水を加え ろ過した後 指示薬としてクロム酸カリウム溶液を加え 0.1 mol/l 硝酸銀溶液で滴定し 滴定終点までに消費した硝酸銀溶液の量から塩化ナトリウム含有量を算出する 3. 注意事項 (a) クロム酸カリウムを取り扱う際には
このたびは「 」(3次元ヒト皮膚モデル)をお買い上げ頂きありがとうございます
 ヒト 3 次元培養表皮 LabCyte EPI-MODEL24 を用いた 皮膚刺激性試験法 OECD TG439 (in vitro 皮膚刺激性試験 ) 収載 目次 1. 皮膚刺激性試験法について... 1 1.1 試験の概要... 1 1.2 作業スケジュール例... 2 1.3 適用 のタイムスケジュール例... 3 2. 準備... 4 2.1 皮膚刺激性試験セットセット構成... 4 2.2
ヒト 3 次元培養表皮 LabCyte EPI-MODEL24 を用いた 皮膚刺激性試験法 OECD TG439 (in vitro 皮膚刺激性試験 ) 収載 目次 1. 皮膚刺激性試験法について... 1 1.1 試験の概要... 1 1.2 作業スケジュール例... 2 1.3 適用 のタイムスケジュール例... 3 2. 準備... 4 2.1 皮膚刺激性試験セットセット構成... 4 2.2
安全データシート LOCTITE 222 LOW STRENGTH THREADLOCKER known as LOCTITE ML EN/CH/JP Page 1 of 6 SDS No. : V001.3 改訂 : 発行日 :
 安全データシート LOCTITE 222 10ML EN/CH/JP Page 1 of 6 SDS No. : 153481 改訂 : 12.02.2016 発行日 : 28.04.2016 1. 化学物質等及び会社情報 製品コード : 1595017 製品名 : 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8 スフィアタワー天王洲 14F 140-0002 電話番号 : +81
安全データシート LOCTITE 222 10ML EN/CH/JP Page 1 of 6 SDS No. : 153481 改訂 : 12.02.2016 発行日 : 28.04.2016 1. 化学物質等及び会社情報 製品コード : 1595017 製品名 : 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8 スフィアタワー天王洲 14F 140-0002 電話番号 : +81
Page 2 of 7 危険有害性情報 : 安全対策 H315 皮膚刺激 H317 アレルギ一性皮膚反応を起こすおそれ H318 重篤な眼の損傷 H335 呼吸器への刺激のおそれ H412 長期継続的影響によって水生生物に有害 P261 粉じん / 煙 / ガス / ミスト / 蒸気 / スプレーの
 安全データシート Page 1 of 7 SDS No. : 450730 改訂 : 14.03.2016 発行日 : 23.06.2016 1. 化学物質等及び会社情報 製品コード : 1835922 製品名 : 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8 スフィアタワー天王洲 14F 140-0002 電話番号 : +81 (45) 758-1820 FAX 番号 : +81
安全データシート Page 1 of 7 SDS No. : 450730 改訂 : 14.03.2016 発行日 : 23.06.2016 1. 化学物質等及び会社情報 製品コード : 1835922 製品名 : 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8 スフィアタワー天王洲 14F 140-0002 電話番号 : +81 (45) 758-1820 FAX 番号 : +81
1-4. 免疫抗体染色 抗体とは何かリンパ球 (B 細胞 ) が作る物質 特定の ( タンパク質 ) 分子に結合する 体の中に侵入してきた病原菌や毒素に結合して 破壊したり 無毒化したりする作用を持っている 例 : 抗血清馬などに蛇毒を注射し 蛇毒に対する抗体を作らせたもの マムシなどの毒蛇にかまれ
 1. 血液細胞の免疫蛍光染色とフローサイトメトリー解析 1-1. フローサイトメトリー ( Flow Cytometory ) とは細胞浮遊液をフローセル内を高速で流し 個々の細胞の形質等についてレーザー光を用いて解析する研究手法 フローサイトメーター( Flow Cytometer ) フローサイトメトリーにおいて使用する細胞解析用の装置今回は BD Accuri C6 を使用する 1-2. フローサイトメーターで何ができるか?
1. 血液細胞の免疫蛍光染色とフローサイトメトリー解析 1-1. フローサイトメトリー ( Flow Cytometory ) とは細胞浮遊液をフローセル内を高速で流し 個々の細胞の形質等についてレーザー光を用いて解析する研究手法 フローサイトメーター( Flow Cytometer ) フローサイトメトリーにおいて使用する細胞解析用の装置今回は BD Accuri C6 を使用する 1-2. フローサイトメーターで何ができるか?
MLPA 法 Q&A 集
 MLPA 法 Q&A 集 目次 1. MLPA 法の導入 Q1. 導入にあたり 何が必要になりますか? Q2. 実験にはどのようなサンプルが必要でしょうか? Q3. サンプルDNAはどれくらい用意すれば良いですか? Q4. キャピラリーシーケンサが自施設に無い場合でも実験はできますか? Q5. FFPE 検体でも実験はできますか? 2. 実験のセットアップ Q1. 実験において重要なポイントはありますか?
MLPA 法 Q&A 集 目次 1. MLPA 法の導入 Q1. 導入にあたり 何が必要になりますか? Q2. 実験にはどのようなサンプルが必要でしょうか? Q3. サンプルDNAはどれくらい用意すれば良いですか? Q4. キャピラリーシーケンサが自施設に無い場合でも実験はできますか? Q5. FFPE 検体でも実験はできますか? 2. 実験のセットアップ Q1. 実験において重要なポイントはありますか?
プロトコル 細胞 増殖 / 毒性酸化ストレス分子生物学細胞内蛍光プローブ細胞染色ミトコンドリア関連試薬細菌研究用試薬膜タンパク質可溶化剤ラベル化剤二価性試薬イオン電極 その他 機能性有機材料 酵素 (POD,ALP) を標識したい 利用製品 < 少量抗体 (10μg) 標識用 > Ab-10 Rap
 増殖 / 毒性酸化ストレス分子生物学内蛍光プローブ染色ミトコンドリア関連試薬細菌研究用試薬膜タンパク質可溶化剤ラベル化剤二価性試薬イオン電極 機能性有機材料 酵素 (PD,ALP) を標識したい 利用製品 < 少量抗体 (0μg) 標識用 > Ab-0 Rapid Peroxidase Labeling Kit < 抗体 タンパク質 (0-00μg) 標識用 > Peroxidase Labeling
増殖 / 毒性酸化ストレス分子生物学内蛍光プローブ染色ミトコンドリア関連試薬細菌研究用試薬膜タンパク質可溶化剤ラベル化剤二価性試薬イオン電極 機能性有機材料 酵素 (PD,ALP) を標識したい 利用製品 < 少量抗体 (0μg) 標識用 > Ab-0 Rapid Peroxidase Labeling Kit < 抗体 タンパク質 (0-00μg) 標識用 > Peroxidase Labeling
PowerPoint プレゼンテーション
 植物 DA の抽出と増幅 1 背景 植物種子から DA 抽出する際 有機溶媒や酵素を用いた処理 遠心分離装置を使った操作など 煩雑で時間のかかる工程が用いられてきた カ技ネ術カの 検体採取 簡易 DA 抽出キット version2( 抽出キット ) と高速増幅用 DA Polymerase ( 増幅キット ) を組合わせる事で 遺伝子検査時間を短縮可能! 抽出キット * 抽出 DA を 増幅キット
植物 DA の抽出と増幅 1 背景 植物種子から DA 抽出する際 有機溶媒や酵素を用いた処理 遠心分離装置を使った操作など 煩雑で時間のかかる工程が用いられてきた カ技ネ術カの 検体採取 簡易 DA 抽出キット version2( 抽出キット ) と高速増幅用 DA Polymerase ( 増幅キット ) を組合わせる事で 遺伝子検査時間を短縮可能! 抽出キット * 抽出 DA を 増幅キット
はじめてのリアルタイムPCR
 はじめてのリアルタイム PCR 1. はじめにリアルタイム PCR 法は PCR 増幅産物の増加をリアルタイムでモニタリングし 解析する技術です エンドポイントで PCR 増幅産物を確認する従来の PCR 法に比べて 1DNA や RNA の正確な定量ができること 2 電気泳動が不要なので迅速かつ簡便に解析できコンタミネーションの危険性も小さいことなど多くの利点があります 今や 遺伝子発現解析や SNP
はじめてのリアルタイム PCR 1. はじめにリアルタイム PCR 法は PCR 増幅産物の増加をリアルタイムでモニタリングし 解析する技術です エンドポイントで PCR 増幅産物を確認する従来の PCR 法に比べて 1DNA や RNA の正確な定量ができること 2 電気泳動が不要なので迅速かつ簡便に解析できコンタミネーションの危険性も小さいことなど多くの利点があります 今や 遺伝子発現解析や SNP
( 別添 ) ヒラメからの Kudoa septempunctata 検査法 ( 暫定 ) 1. 検体採取方法食後数時間程度で一過性の嘔吐や下痢を呈し, 軽症で終わる有症事例で, 既知の病因物質が不検出, あるいは検出した病因物質と症状が合致せず, 原因不明として処理された事例のヒラメを対象とする
 平成 23 年 7 月 11 日 食安監発 0711 第 1 号 都道府県知事 各保健所設置市長殿 特別区長 厚生労働省医薬食品局食品安全部監視安全課長 Kudoa septempunctata の検査法について ( 暫定版 ) 平成 23 年 6 月 17 日付け食安発 0617 第 3 号 生食用生鮮食品による病因物質不明有症事例への対応について ( 厚生労働省医薬食品局食品安全部長通知 ) において
平成 23 年 7 月 11 日 食安監発 0711 第 1 号 都道府県知事 各保健所設置市長殿 特別区長 厚生労働省医薬食品局食品安全部監視安全課長 Kudoa septempunctata の検査法について ( 暫定版 ) 平成 23 年 6 月 17 日付け食安発 0617 第 3 号 生食用生鮮食品による病因物質不明有症事例への対応について ( 厚生労働省医薬食品局食品安全部長通知 ) において
資料 イミダゾリジンチオン 測定 分析手法に関する検討結果報告書
 資料 1-2 2- イミダゾリジンチオン 測定 分析手法に関する検討結果報告書 目次 1. はじめに... 1 2. 文献調査... 1 3. 捕集及び分析条件... 2 4. 捕集効率... 2 5. クロマトグラム... 3 6. 検量線... 4 7. 検出下限及び定量下限... 4 8. 添加回収率 ( 通気試験 )... 5 9. 保存性... 5 10. まとめ... 5 11. 検討機関...
資料 1-2 2- イミダゾリジンチオン 測定 分析手法に関する検討結果報告書 目次 1. はじめに... 1 2. 文献調査... 1 3. 捕集及び分析条件... 2 4. 捕集効率... 2 5. クロマトグラム... 3 6. 検量線... 4 7. 検出下限及び定量下限... 4 8. 添加回収率 ( 通気試験 )... 5 9. 保存性... 5 10. まとめ... 5 11. 検討機関...
目 次 1. はじめに 1 2. 組成および性状 2 3. 効能 効果 2 4. 特徴 2 5. 使用方法 2 6. 即時効果 持続効果および累積効果 3 7. 抗菌スペクトル 5 サラヤ株式会社スクラビイン S4% 液製品情報 2/ PDF
 サラヤ株式会社スクラビイン S4% 液製品情報 1/8 52-0198-01-4PDF 目 次 1. はじめに 1 2. 組成および性状 2 3. 効能 効果 2 4. 特徴 2 5. 使用方法 2 6. 即時効果 持続効果および累積効果 3 7. 抗菌スペクトル 5 サラヤ株式会社スクラビイン S4% 液製品情報 2/8 52-0198-01-4PDF 1. はじめに 医療関連感染の原因となる微生物の多くは
サラヤ株式会社スクラビイン S4% 液製品情報 1/8 52-0198-01-4PDF 目 次 1. はじめに 1 2. 組成および性状 2 3. 効能 効果 2 4. 特徴 2 5. 使用方法 2 6. 即時効果 持続効果および累積効果 3 7. 抗菌スペクトル 5 サラヤ株式会社スクラビイン S4% 液製品情報 2/8 52-0198-01-4PDF 1. はじめに 医療関連感染の原因となる微生物の多くは
Bacterial 16S rDNA PCR Kit
 研究用 Bacterial 16S rdna PCR Kit 説明書 v201802da 微生物の同定は 形態的特徴 生理 生化学的性状 化学分類学的性状などを利用して行われますが これらの方法では同定までに時間を要します また 同定が困難な場合や正しい結果が得られない場合もあります 近年 微生物同定にも分子生物学を利用した方法が採用されるようになり 微生物の持つ DNA を対象として解析を行う方法が活用されています
研究用 Bacterial 16S rdna PCR Kit 説明書 v201802da 微生物の同定は 形態的特徴 生理 生化学的性状 化学分類学的性状などを利用して行われますが これらの方法では同定までに時間を要します また 同定が困難な場合や正しい結果が得られない場合もあります 近年 微生物同定にも分子生物学を利用した方法が採用されるようになり 微生物の持つ DNA を対象として解析を行う方法が活用されています
BKL Kit (Blunting Kination Ligation Kit)
 製品コード 6126/6127 BKL Kit (Blunting Kination Ligation Kit) 説明書 PCR 産物を平滑末端ベクターにクローニングする場合 使用するポリメラーゼ酵素の種類により 3' 末端に余分に付加された塩基を除去し さらに 5' 末端をリン酸化する必要があります 本製品は これらの一連の反応を簡便に短時間に行うためのキットです PCR 産物の末端平滑化とリン酸化を同時に行うことにより
製品コード 6126/6127 BKL Kit (Blunting Kination Ligation Kit) 説明書 PCR 産物を平滑末端ベクターにクローニングする場合 使用するポリメラーゼ酵素の種類により 3' 末端に余分に付加された塩基を除去し さらに 5' 末端をリン酸化する必要があります 本製品は これらの一連の反応を簡便に短時間に行うためのキットです PCR 産物の末端平滑化とリン酸化を同時に行うことにより
安全データシート Page 1 of 6 Loctite(R) 603 Retaining Compound Press Fit SDS No. : V001.4 改訂 : 発行日 : 化学物質等及び会社情報 製品コード : 23109
 安全データシート Page 1 of 6 SDS No. : 153475 改訂 : 30.07.2015 発行日 : 29.12.2015 1. 化学物質等及び会社情報 製品コード : 231099 製品名 : 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8 スフィアタワー天王洲 14F 140-0002 電話番号 : +81 (45) 758-1820 FAX 番号 : +81
安全データシート Page 1 of 6 SDS No. : 153475 改訂 : 30.07.2015 発行日 : 29.12.2015 1. 化学物質等及び会社情報 製品コード : 231099 製品名 : 会社名 : ヘンケルジャパン株式会社東京都品川区東品川 2-2-8 スフィアタワー天王洲 14F 140-0002 電話番号 : +81 (45) 758-1820 FAX 番号 : +81
コメDNA 抽出キット(精米20 粒スケール)
 食品 環境分析用 コメ DNA 抽出キット ( 精米 20 粒スケール ) ( コメ判別用 PCR Kit 用 ) 説明書 v201703da 本キットは未加熱の精米 20 粒から DNA の調製を行う際に使用します 最終的に回収された DNA 溶液は 直接 PCR 反応に利用することができます 本キットを用いた DNA 調製には 劇物であるフェノールやクロロホルムは使用しません I. 内容 (50
食品 環境分析用 コメ DNA 抽出キット ( 精米 20 粒スケール ) ( コメ判別用 PCR Kit 用 ) 説明書 v201703da 本キットは未加熱の精米 20 粒から DNA の調製を行う際に使用します 最終的に回収された DNA 溶液は 直接 PCR 反応に利用することができます 本キットを用いた DNA 調製には 劇物であるフェノールやクロロホルムは使用しません I. 内容 (50
安全データシート 製品名 :OxyICC Oxidized Protein Detection Kit 作成日 2013 年 02 月 25 日改訂日 2016 年 06 月 17 日 1. 化学品及び会社情報 製品番号 :S7350 製品名 :OxyICC Oxidized Protein Det
 安全データシート 製品名 :OxyICC Oxidized Protein Detection Kit 1. 化学品及び会社情報 Protein Detection Kit (2-8 ) (2,4-Dinitrophenylhydrazine 製品和名 :OxyICC Oxidized Protein Detection Kit (OxyICC Oxidized Protein Detection
安全データシート 製品名 :OxyICC Oxidized Protein Detection Kit 1. 化学品及び会社情報 Protein Detection Kit (2-8 ) (2,4-Dinitrophenylhydrazine 製品和名 :OxyICC Oxidized Protein Detection Kit (OxyICC Oxidized Protein Detection
Mouse IgG EIA Kit
 製品コード MK137 研究用 Mouse IgG EIA Kit 説明書 生体防御のひとつ 液性免疫の主役となる抗体 : 免疫グロブリン (Ig) は動物体内では 5 種類のクラス (IgG, IgA, IgM, IgE, IgD) が存在し 血液中で 80% を占めるのが IgG クラスです 血液中の IgG は 免疫応答によりその含有量は大きく変動しますが 一般的に 3 ~ 10 mg/ml
製品コード MK137 研究用 Mouse IgG EIA Kit 説明書 生体防御のひとつ 液性免疫の主役となる抗体 : 免疫グロブリン (Ig) は動物体内では 5 種類のクラス (IgG, IgA, IgM, IgE, IgD) が存在し 血液中で 80% を占めるのが IgG クラスです 血液中の IgG は 免疫応答によりその含有量は大きく変動しますが 一般的に 3 ~ 10 mg/ml
Microsoft Word - iBind Western System 日本語簡易取扱説明書
 簡易取扱説明書 ibind Western System 簡易取扱説明書 ver.2 ibind Western System 日本語簡易取扱説明書 ver.2 サンプルブロッティング済みメンブレン 試薬 ibind Solution kit 抗体反応用試薬 ibind Detection Kits 検出試薬 (AP 用の二次抗体も含む ) 一次抗体脱イオン水装置と器具 ibind Device ibind
簡易取扱説明書 ibind Western System 簡易取扱説明書 ver.2 ibind Western System 日本語簡易取扱説明書 ver.2 サンプルブロッティング済みメンブレン 試薬 ibind Solution kit 抗体反応用試薬 ibind Detection Kits 検出試薬 (AP 用の二次抗体も含む ) 一次抗体脱イオン水装置と器具 ibind Device ibind
Microsoft Word - 143A277,143A279,0BA00001_ふっ化物イオン測定用全イオン強度調整剤 TISAB-01_ doc
 1/5 作成日 1997 年 08 月 20 日改訂日 2014 年 06 月 19 日 安全データシート 1. 製品及び会社情報 製 品 名 : ふっ化物イオン測定用全イオン強度調整剤 TISAB-01 品目コード : 143A277, 143A279, 0BA00001 会 社 名 : 東亜ディーケーケー株式会社 住 所 : 東京都新宿区高田馬場 1-29-10 担当部門 : センサ技術部 電話番号
1/5 作成日 1997 年 08 月 20 日改訂日 2014 年 06 月 19 日 安全データシート 1. 製品及び会社情報 製 品 名 : ふっ化物イオン測定用全イオン強度調整剤 TISAB-01 品目コード : 143A277, 143A279, 0BA00001 会 社 名 : 東亜ディーケーケー株式会社 住 所 : 東京都新宿区高田馬場 1-29-10 担当部門 : センサ技術部 電話番号
免疫学的検査 >> 5E. 感染症 ( 非ウイルス ) 関連検査 >> 5E301. 検体採取 患者の検査前準備 検体採取のタイミング 記号 添加物 ( キャップ色等 ) 採取材料 採取量 測定材料 イ ヘパリンナトリウム ( 緑 ) 血液 5 ml 全血 検体ラベル ( 単項目オー
 6938 5. 免疫学的検査 >> 5E. 感染症 ( 非ウイルス ) 関連検査 >> 5E301. 結核菌特異蛋白刺激性遊離インターフェロン -γ interferon-gamma released by Mycobacterium tuberculosis specific protein 連絡先 : 3764 基本情報 5E301 分析物 JLAC10 診療報酬 識別材料 019 全血 ( 添加物入り
6938 5. 免疫学的検査 >> 5E. 感染症 ( 非ウイルス ) 関連検査 >> 5E301. 結核菌特異蛋白刺激性遊離インターフェロン -γ interferon-gamma released by Mycobacterium tuberculosis specific protein 連絡先 : 3764 基本情報 5E301 分析物 JLAC10 診療報酬 識別材料 019 全血 ( 添加物入り
siRNA / miRNA transfection KIT
 sirna / mirna transfection KIT GenomONE - Si 取扱説明書 ( 第 2 版 ) 1. 概要... 1 1-1: トランスフェクション原理 概要... 1 1-2: 製品仕様... 2 2. 細胞への sirna/mirna の導入... 3 2-1: プロトコル (1) 基本プロトコル... 3 2-2: プロトコル (2) 基本プロトコル + 遠心処理...
sirna / mirna transfection KIT GenomONE - Si 取扱説明書 ( 第 2 版 ) 1. 概要... 1 1-1: トランスフェクション原理 概要... 1 1-2: 製品仕様... 2 2. 細胞への sirna/mirna の導入... 3 2-1: プロトコル (1) 基本プロトコル... 3 2-2: プロトコル (2) 基本プロトコル + 遠心処理...
この添付文書をよく読んでから使用してください 体外診断用医薬品 2017 年 7 月作成 ( 第 1 版 ) 製造販売承認番号 21800AMY ヒト免疫不全症ウイルス 1p24 抗原 HIV 抗体キット HIV Ag/Ab コンボアッセイ アボット ja HIV Ag/Ab 08P
 この添付文書をよく読んでから使用してください 体外診断用医薬品 2017 年 7 月作成 ( 第 1 版 ) 製造販売承認番号 21800AMY10140000 ヒト免疫不全症ウイルス 1p24 抗原 HIV 抗体キット HIV Ag/Ab コンボアッセイ アボット ja HIV Ag/Ab 08P07 470726R02 B8P07J 全般的な注意 本製品は体外診断用であり それ以外の目的に使用しないこと
この添付文書をよく読んでから使用してください 体外診断用医薬品 2017 年 7 月作成 ( 第 1 版 ) 製造販売承認番号 21800AMY10140000 ヒト免疫不全症ウイルス 1p24 抗原 HIV 抗体キット HIV Ag/Ab コンボアッセイ アボット ja HIV Ag/Ab 08P07 470726R02 B8P07J 全般的な注意 本製品は体外診断用であり それ以外の目的に使用しないこと
GMP-140 (P-selectin) EIA Kit
 製品コード MK112 研究用 GMP-140 (P-selectin) EIA Kit 説明書 GMP-140(CD62 PADGEM) は活性化状態にある血小板 血管内皮細胞 巨核球の細胞膜表面に特異的に出現する分子量 14 万の糖蛋白質であり 1) 血管内皮傷害などの炎症部位において 単球や好中球などのリンパ球を結合および誘引する白血球接着分子として機能していると考えられています GMP- 140
製品コード MK112 研究用 GMP-140 (P-selectin) EIA Kit 説明書 GMP-140(CD62 PADGEM) は活性化状態にある血小板 血管内皮細胞 巨核球の細胞膜表面に特異的に出現する分子量 14 万の糖蛋白質であり 1) 血管内皮傷害などの炎症部位において 単球や好中球などのリンパ球を結合および誘引する白血球接着分子として機能していると考えられています GMP- 140
バンコマイシンを含まないヒト血清に 次の各物質を濃度 500μg/mL になるよう ( メ トトレキサートおよび CDP-1 は除く ) 添加して測定した メトトレキサートは濃度 227μg/mL になるよう添加した 各物質の交差反応による濃度は 0.24μg/mL 未満 であった 物質 アセトアミ
 この添付文書をよく読んでから使用してください 体外診断用医薬品 ** 2015 年 3 月改訂 ( 第 8 版 ) * 2014 年 12 月改訂 ( 第 7 版 ) 製造販売届出番号 12A2X00009000024 バンコマイシンキット アーキテクト バンコマイシン ja ivancomycin 1P30 47-0180/R04 B1P3ZJ 全般的な注意 1. 本製品は体外診断用であり それ以外の目的に使用しないこと
この添付文書をよく読んでから使用してください 体外診断用医薬品 ** 2015 年 3 月改訂 ( 第 8 版 ) * 2014 年 12 月改訂 ( 第 7 版 ) 製造販売届出番号 12A2X00009000024 バンコマイシンキット アーキテクト バンコマイシン ja ivancomycin 1P30 47-0180/R04 B1P3ZJ 全般的な注意 1. 本製品は体外診断用であり それ以外の目的に使用しないこと
この添付文書をよく読んでから使用してください
 この添付文書をよく読んでから使用してください また 必要時に読めるように保管しておいてください 体外診断用医薬品 ** 2018 年 1 月改訂 ( 第 3 版 ) * 2017 年 3 月改訂 ( 第 2 版 ) 製造販売承認番号 :22800EZX00058000 単純ヘルペスウイルス核酸キットコバス 4800 システム HSV 1 and 2 全般的な注意 1. 本キットは体外診断用であり それ以外の目的には使用しないでください
この添付文書をよく読んでから使用してください また 必要時に読めるように保管しておいてください 体外診断用医薬品 ** 2018 年 1 月改訂 ( 第 3 版 ) * 2017 年 3 月改訂 ( 第 2 版 ) 製造販売承認番号 :22800EZX00058000 単純ヘルペスウイルス核酸キットコバス 4800 システム HSV 1 and 2 全般的な注意 1. 本キットは体外診断用であり それ以外の目的には使用しないでください
遺伝子検査の基礎知識
 リアルタイム PCR(Probe 法 ) 実験ガイドこの文書では Probe 法によるリアルタイム PCR について 蛍光検出の原理や実験操作の流れなどを解説します 実際の実験操作の詳細については 各製品の取扱説明書をご参照ください - 目次 - 1 蛍光検出の原理 2 実験に必要なもの 3 実験操作法 4 結果の解析 1 蛍光検出の原理 サイクリングプローブによる検出系 (Cycleave PCR
リアルタイム PCR(Probe 法 ) 実験ガイドこの文書では Probe 法によるリアルタイム PCR について 蛍光検出の原理や実験操作の流れなどを解説します 実際の実験操作の詳細については 各製品の取扱説明書をご参照ください - 目次 - 1 蛍光検出の原理 2 実験に必要なもの 3 実験操作法 4 結果の解析 1 蛍光検出の原理 サイクリングプローブによる検出系 (Cycleave PCR
Microsoft Word - AL003C_AL003F
 製品名 :AlphaLISA Lysis Buffer (5X) 1 / 5 製品安全データシート 作成 改訂日 :2011 年 4 月 22 日 1 化学物質等及び会社の概要 化学物質の名称 :AlphaLISA Lysis Buffer (5X) 製品コード :AL003C ( 包装 :10mL) AL003F ( 包装 :100mL) 会社名 : 株式会社パーキンエルマージャパン 住所 : 神奈川県横浜市保土ヶ谷区神戸町
製品名 :AlphaLISA Lysis Buffer (5X) 1 / 5 製品安全データシート 作成 改訂日 :2011 年 4 月 22 日 1 化学物質等及び会社の概要 化学物質の名称 :AlphaLISA Lysis Buffer (5X) 製品コード :AL003C ( 包装 :10mL) AL003F ( 包装 :100mL) 会社名 : 株式会社パーキンエルマージャパン 住所 : 神奈川県横浜市保土ヶ谷区神戸町
pdf エンドトキシン試験法
 00-0909.pdf.0 エンドトキシン試験法 3 5 6 7 9 0 3 5 6 7 9 0 3 5 6 7 9 30 3 3 33 3 35 36 37 3 39 0 3 5 6 次のように改める. 本試験法は, 三薬局方での調和合意に基づき規定した試験法である. エンドトキシン試験法は, カブトガニ (Limulus polyphemus 又は Tachypleus tridentatus)
00-0909.pdf.0 エンドトキシン試験法 3 5 6 7 9 0 3 5 6 7 9 0 3 5 6 7 9 30 3 3 33 3 35 36 37 3 39 0 3 5 6 次のように改める. 本試験法は, 三薬局方での調和合意に基づき規定した試験法である. エンドトキシン試験法は, カブトガニ (Limulus polyphemus 又は Tachypleus tridentatus)
3M ポリエステルテープ 8411,8412,8437,850( 黒 金 銀 透明 白色 ) 853,856 3M スコッチガード 1001,1002,1004 3M 表面保護テープ 1614,1675 YR36R87 3M スコッチ ファインラインマスキングテープ 222 安全データシート Cop
 安全データシート Copyright,2014,3M Company All right reserved. 本情報は 3M の製品を適切にご使用頂くために作成したものです 複製ないしダウンロードする場合には 以下の条件をお守り下さい (1) 当社から書面による事前承認を得ることなく情報を変更したり 一部を抜粋して使用しないで下さい (2) 本情報を営利目的で転売もしくは配布しないで下さい SDS
安全データシート Copyright,2014,3M Company All right reserved. 本情報は 3M の製品を適切にご使用頂くために作成したものです 複製ないしダウンロードする場合には 以下の条件をお守り下さい (1) 当社から書面による事前承認を得ることなく情報を変更したり 一部を抜粋して使用しないで下さい (2) 本情報を営利目的で転売もしくは配布しないで下さい SDS
成分 CAS 番号 重量 % 金属蒸着積層フィルム なし 応急措置 応急措置 吸入した場合応急処置は不要 皮膚に付着した場合応急処置は不要 眼に入った場合応急処置は不要 飲み込んだ場合応急処置は不要 予想できる急性症状及び遅発性症状の最も重要な徴候症状毒性学的影響についてはセクション
 安全データシート Copyright,2014,3M Company All right reserved. 本情報は 3M の製品を適切にご使用頂くために作成したものです 複製ないしダウンロードする場合には 以下の条件をお守り下さい (1) 当社から書面による事前承認を得ることなく情報を変更したり 一部を抜粋して使用しないで下さい (2) 本情報を営利目的で転売もしくは配布しないで下さい SDS
安全データシート Copyright,2014,3M Company All right reserved. 本情報は 3M の製品を適切にご使用頂くために作成したものです 複製ないしダウンロードする場合には 以下の条件をお守り下さい (1) 当社から書面による事前承認を得ることなく情報を変更したり 一部を抜粋して使用しないで下さい (2) 本情報を営利目的で転売もしくは配布しないで下さい SDS
ダイノックフィルムネオシリーズタイル壁面用 安全データシート Copyright,2016,3M Company All right reserved. 本情報は 3M の製品を適切にご使用頂くために作成したものです 複製ないしダウンロードする場合には 以下の条件をお守り下さい (1) 当社から書面
 安全データシート Copyright,2016,3M Company All right reserved. 本情報は 3M の製品を適切にご使用頂くために作成したものです 複製ないしダウンロードする場合には 以下の条件をお守り下さい (1) 当社から書面による事前承認を得ることなく情報を変更したり 一部を抜粋して使用しないで下さい (2) 本情報を営利目的で転売もしくは配布しないで下さい SDS
安全データシート Copyright,2016,3M Company All right reserved. 本情報は 3M の製品を適切にご使用頂くために作成したものです 複製ないしダウンロードする場合には 以下の条件をお守り下さい (1) 当社から書面による事前承認を得ることなく情報を変更したり 一部を抜粋して使用しないで下さい (2) 本情報を営利目的で転売もしくは配布しないで下さい SDS
Western BLoT Rapid Detect
 研究用 Western BLoT Rapid Detect 説明書 v201212 Western BLoT Rapid Detect は 標識二次抗体の代わりに独自の IgG Detector(HRP labeled) を利用して一次抗体を検出するウェスタンブロッティング専用の検出試薬キットです 本製品を利用することで 標識二次抗体を用いて検出する従来法ではできなかった迅速検出 高感度検出 シグナルの増強
研究用 Western BLoT Rapid Detect 説明書 v201212 Western BLoT Rapid Detect は 標識二次抗体の代わりに独自の IgG Detector(HRP labeled) を利用して一次抗体を検出するウェスタンブロッティング専用の検出試薬キットです 本製品を利用することで 標識二次抗体を用いて検出する従来法ではできなかった迅速検出 高感度検出 シグナルの増強
検体採取 患者の検査前準備 検体採取のタイミング 記号 添加物 ( キャップ色等 ) 採取材料 採取量 測定材料 P EDTA-2Na( 薄紫 ) 血液 7 ml RNA 検体ラベル ( 単項目オーダー時 ) ホンハ ンテスト 注 外 N60 氷 MINテイリョウ. 採取容器について 0
 0868010 8. その他の検体検査 >> 8C. 遺伝子関連検査 >> minor bcr-abl, mrna quantitative 連絡先 : 3664 基本情報 8C127 minor bcr-abl 分析物 JLAC10 診療報酬 識別 9962 mrna 定量 材料 019 全血 ( 添加物入り ) 測定法 875 リアルタイムRT-PCR 法 結果識別 第 2 章 特掲診療料 D006-2
0868010 8. その他の検体検査 >> 8C. 遺伝子関連検査 >> minor bcr-abl, mrna quantitative 連絡先 : 3664 基本情報 8C127 minor bcr-abl 分析物 JLAC10 診療報酬 識別 9962 mrna 定量 材料 019 全血 ( 添加物入り ) 測定法 875 リアルタイムRT-PCR 法 結果識別 第 2 章 特掲診療料 D006-2
医療機器添付文書の手引書第 5 版 第 3 章第 3 節 < テンプレート > についての補足解説 1. パルスオキシメータ (WG2 6.1から6.4) テンプレートを利用する場合 以下 5 点の解説を参照すること パルスオキシメータ ( 本体 ) 6.2 パルスオキシメータ ( 一体
 医療機器添付文書の手引書第 5 版 第 3 章第 3 節 < テンプレート > についての補足解説 1. パルスオキシメータ (WG2 6.1から6.4) テンプレートを利用する場合 以下 5 点の解説を参照すること 1 6.1 パルスオキシメータ ( 本体 ) 6.2 パルスオキシメータ ( 一体型アラームなし ) 及び 6.3 再使用可能なパルスオキシメータプローブの 保守 点検に係る事項 に関して局長通知では
医療機器添付文書の手引書第 5 版 第 3 章第 3 節 < テンプレート > についての補足解説 1. パルスオキシメータ (WG2 6.1から6.4) テンプレートを利用する場合 以下 5 点の解説を参照すること 1 6.1 パルスオキシメータ ( 本体 ) 6.2 パルスオキシメータ ( 一体型アラームなし ) 及び 6.3 再使用可能なパルスオキシメータプローブの 保守 点検に係る事項 に関して局長通知では
