TruSeq Nano DNA Libary Prep Reference Guide
|
|
|
- つねたけ こしの
- 7 years ago
- Views:
Transcription
1 TruSeq Nano DNA Library Prep Reference Guide 本製品の使用目的は研究に限定されます 診断での使用はできません 改訂履歴 3 はじめに 5 DNAインプットの推奨 6 追加リソース 7 はじめに 8 チップと手法 9 ライブラリー調製ワークフロー 10 プーリングの準備 11 DNAの断片化 12 末端修復およびライブラリーサイズの選択 15 3 末端のアデニル化 18 アダプターのライゲート 20 DNA 断片の濃縮 23 ライブラリーの検証 26 ライブラリーの基準化およびプール 27 補足情報 29 テクニカルサポート 39 ILLUMINA PROPRIETARY パーツ番号 : Rev. D JPN 2015 年 6 月カタログ番号 :FC DOC
2 本文書およびその内容は Illumina, Inc. およびその関連会社 ( 以下 イルミナ という ) の所有物であり 本文書に記載された製品の使用に関連して イルミナの顧客が契約上使用することのみを意図したものであり その他の目的を意図したものではありません 本文書およびその内容を イルミナの書面による事前同意を得ずにその他の目的で利用または配布してはならず また方法を問わず その他伝達 開示または複製してはなりません イルミナは 本文書によって 自身の特許 商標 著作権またはコモンロー上の権利に基づくいかなるライセンスも譲渡せず また第三者の同様の権利も譲渡しないものとします 本文書に記載された製品の適切かつ安全な使用を徹底するため 資格を有した 適切なトレーニングを受けた担当者が 本文書の指示を厳密かつ明確に遵守しなければなりません 当該製品の使用に先立ち 本文書のすべての内容を熟読し 理解する必要があるものとします 本文書に含まれるすべての指示を熟読せず 明確に遵守しない場合 製品を損ない 使用者または他者を含む個人に傷害を負わせ その他の財産に損害を与える結果となる可能性があります イルミナは 本文書に記載された製品 ( その部品またはソフトウェアを含む ) の不適切な使用から生じる責任を一切負わないものとします 2015 Illumina, Inc. All rights reserved. Illumina 24sure BaseSpace BeadArray BlueFish BlueFuse BlueGnome cbot CSPro CytoChip DesignStudio Epicentre GAIIx Genetic Energy Genome Analyzer GenomeStudio GoldenGate HiScan HiSeq HiSeq X Infinium iscan iselect MiSeq NeoPrep Nextera NextBio NextSeq Powered by Illumina SeqMonitor SureMDA TruGenome TruSeq TruSight Understand Your Genome UYG VeraCode verifi VeriSeq パンプキンオレンジ色および遺伝子エネルギーの流れをベースとしたデザインは 米国および / またはその他の国にある Illumina, Inc および / またはその関連会社の商標です その他すべての名称 ロゴ その他の商標の所有権は 各所有者に帰属します
3 改訂履歴 パーツ番号改訂年月変更内容 D 2015 年 6 月 キット内容 : キットにはERP2またはERP3および ATLまたはATL2が含まれます に変更した ボックスおよびチューブのパーツ番号を削除した この文書の表題をリファレンスガイドに変更した ワークフロー図のデザインを変更した 必要に応じて一部手順の名前の変更および手順の集約を行い 一貫性を高めた HS および LS のプロトコールオプションを単一のワークフローに集約した 各セクションの先頭に消耗品の説明を簡単に記載した 段階的な説明となるよう修正し 簡潔を期した 現在使用されていない Experienced User Cards への参照を削除し 新しいプロトコールガイドおよびチェックリストへの参照を追加した BaseSpace リソースの参照先をヘルプセンターに変更した ERP サーマルサイクリングプログラムを実行してオーバーハングの変換する場合の容量を 100 µl に修正 改訂履歴 TruSeq Nano DNA Library Prep Reference Guide 3
4 パーツ番号改訂年月変更内容 C 2014 年 12 月 キットの名前を サンプル 調製から ライブラ リー 調製に変更した サンプル ライブラリー プール およびランを整理するための BaseSpace への参照を追加した 各手順の最初と最後の例以外で プレートの名前 (IMP プレートなど ) を削除した HS プロトコールで CFP の作成手順を修正して DNA プレートが midi プレートであることを明確にした PCR の精製 HS プロトコールを修正し midi プレートへのサンプルの移動を削除した ビーズの精製の手順を修正し サンプル風乾前の EtOH を削除した LS プロトコールで 各サーマルサイクラーのインキュベーション前に 遠心の手順を追加した ヒートインキュベーションの手順にウェルの容量を追加した Microseal A 粘着フィルムを消耗品および装置に追加した プーリングの準備セクションを更新した 追加リソースを更新した 表目次を削除した SDS のリンク先を support.illumina.com/sds.html に変更した B 2013 年 11 月 インキュベータ1 IMPをインキュベータIMPに変更 した A 2013 年 5 月最初のリリース 推奨されたサーマルサイクラーの設定を消耗品および装置に追加した 4 パーツ番号 : Rev. D JPN
5 はじめに 本プロトコールでは Illumina TruSeq Nano DNA PCR-Free Library Prep kits に付属の試薬を使用して 最大 96 の独自にインデックスされたゲノム DNA(gDNA) のペアエンドライブラリーを調製する方法について説明します 本プロトコールの目的は アダプターシーケンスを DNA 断片の末端に追加して インデックスされたシングルリードまたはペアエンドのシーケンスライブラリーを作製することです TruSeq Nano DNA Library Prep プロトコールにより 以下が実現されます } ワークフローの合理化 試薬容器およびピペット操作を削減らすマスターミックス試薬 シングルリード ペアエンド およびインデックスの調製に対するユニバーサルアダプター } 全ゲノムを最適に剪断してリシーケンスする 350 bp および 550 bp インサートサイズワークフロー } 各キットに含まれる ビーズを基にしたサイズ選択試薬 } ローサンプル (LS) およびハイサンプル (HS) 処理用のオプション付きシングルワークフロー } 低スループット (LT) および高スループット (HT) キット構成品 } 高スループット アダプタープレートにより デュアルインデックスされた 96 の DNA サンプルの同時調製が可能 標準的な 96 ウェルプレートに最適化された容量 } すべてのサンプルを標識するインデックスアダプター 追加のアダプターおよびプライマーは不要 各 TruSeq Nano DNA LT Library Prep Kit には シーケンス用に最大 24 個のサンプルを調製することが推奨されるアダプターインデックスチューブが含まれます キット A および B の併用で 最大 24 サンプルのプーリングが可能です TruSeq Nano DNA HT Library Prep Kit には 96 の独自にインデックスされたサンプルを手動または自動で調製するように設計された 96 の独自にインデックスされたアダプターの組み合わせを有する 96 ウェルプレートが含まれています 本プロトコールは 単一サンプルのシーケンス またはさらに低いインデックスプーリングレベルまで対応できます はじめに TruSeq Nano DNA Library Prep Reference Guide 5
6 DNA インプットの推奨 ベストな結果を得るために インプットに関する以下の推奨事項に従ってください ライブラリー調製を行う前に インプット gdna を定量して gdna の品質を評価してください } 350 bp インサートサイズの場合は 100 ng のインプット gdna を使用します } 550 bp の場合は 200 ng のインプット gdna を使用します } インプットの量が指定された量よりも少ないと 収量が低くなり 重複する割合が高くなります インプット DNA の定量 DNA 品質の評価 以下の推奨事項に従ってインプット DNA を定量してください } ライブラリー調製の成否は 正確に定量されたインプット DNA 量を使用しているかどうかによって左右されます 複数の定量手法を用いて結果を検証してください } 定量には Qubit または PicoGreen などの蛍光定量ベースの定量法を使用します } 蛍光色素のインターカレーションに依存する DNA 定量化方法は二本鎖 DNA のみを検出し 余分な核酸の影響を受けにくくなっています } NanoDrop などスペクトラムベースの方法ではヌクレオチドも検出され gdna の測定が不正確になるおそれがあるため使用しないでください } 定量手法は正確なピペッティングよって左右されます ピペットは性能仕様で定められている容量の極限値では使用しないでください ピペットが補正されていることを確認してください DNA 品質の評価には 260 nm での吸光度測定が一般的に使用されます } 260 nm と 280 nm での吸光度の比率が サンプル純度を示すものとして使用されます 1.8~2.0 の値は比較的純度の高い DNA を示しています } RNA またはヌクレオチドなどの核酸の小断片があることによって 260 nm と 280 nm での吸光度は精度が落ちることがあります } コンタミネーションが起きないよう サンプルの抽出は慎重に行ってください ポジティブコントロール イルミナでは このプロトコールに対するポジティブコントロールサンプルとして Coriell Human-1 DNA(NA18507) または Promega Human ゲノム DNA(G3041) を使用することを推奨しています 6 パーツ番号 : Rev. D JPN
7 追加リソース 以下の文書は イルミナのウェブサイトからダウンロードできます リソース TruSeq Nano DNA Library Prep Protocol Guide ( パーツ番号 : ) 内容 プロトコール取扱説明書のみ提供しています このプロトコールガイドは経験豊富なユーザー用です 追加リソース TruSeq Nano DNA Library Prep Checklist ( パーツ番号 : ) Dual Index Sequencing with TruSeq HT Library Prep ( パーツ番号 : ) TruSeq Library Prep Pooling Guide ( パーツ番号 : ) Illumina Experiment Manager Guide ( パーツ番号 : ) および IEM TruSeq DNA, RNA, or ChIP Quick Reference Card ( パーツ番号 : ) BaseSpace ヘルプ (help.basespace.illumina.com) プロトコール手順のチェックリストを提供しています このチェックリストは経験豊富なユーザー用です TruSeq Nano DNA HT Library Prep Kit を使用する場合の デュアルインデックスシーケンスの調製のためのガイドラインを提供しています バランスの取れたインデックスの組み合わせを要するイルミナシーケンサーシステムのライブラリーを調製するための TruSeq プーリングガイドラインを提供しています ライブラリーの調製を開始する前にこのガイドを参照してください イルミナシーケンサーシステムと分析ソフトウェア用の適切なサンプルシートの作成および編集 ならびにサンプルプレートのパラメータ記録に関する情報を提供しています サンプル ライブラリー プール シーケンスランを 1 つの環境で整理することもできる BaseSpace シーケンスデータ分析ツールに関する情報を提供しています イルミナのウェブサイトにアクセスし TruSeq Nano DNA LT Library Prep Kit サポートページまたは TruSeq Nano DNA HT Library Prep Kit サポートページを閲覧してください 要件および互換性 追加文書 ソフトウェアのダウンロード オンライントレーニング よくある質問 およびベストプラクティスについて記載しています TruSeq Nano DNA Library Prep Reference Guide 7
8 はじめに 本章では TruSeq Nano DNA Library Prep プロトコールについて説明します } 記載された順序でプロトコールに従い 指定された量およびインキュベーションパラメーターを用います } 本プロトコールでは オプションで異なるタイプのプレートを容器として用いる シングルワークフローについても説明しています 各オプションの違いは [HS] または [LS] で示します 使用している容器の説明に従ってください いずれのオプションでも同等の結果が得られます ただし [HS] ではサンプル間でより一貫性のある結果が得られます プロトコールオプションの特徴的な要素は以下のとおりです 表 1 ワークフローオプション ワークフローの識別子 HS LS LT キット : 一度に処理されるサンプル数 HT キット : 一度に処理されるサンプル数 プレートタイプ インキュベーション装置 混合手法 インデックスアダプターチューブを用いて 24 超 * インデックスアダプタープレートを用いて 24 超 96 ウェルハードシェル PCR 96 ウェル midi マイクロヒーティングシステム マイクロプレートシェーカー インデックスアダプターチューブを用いて 24 以下 * インデックスアダプタープレートを用いて 24 以下 96 ウェル 0.3 ml PCR 96 ウェル midi 96 ウェルサーマルサイクラー ピペッティング * 各 TruSeq Nano DNA LT Library Prep Kit には 最大 24 サンプルを調製するのに十分な量の試薬が含まれています TruSeq Nano DNA LT Library Prep Kit A および B を併用した場合 各キットに含まれている 12 の異なるインデックスを使用して 最大 24 サンプルをプーリングすることができます } 実験に進む前にベストプラクティスを閲覧します イルミナウェブサイト上の TruSeq Nano DNA Library Prep ベストプラクティスにアクセスする方法については 7 ページの追加リソースを参照してください } 実験に進む前に キットの内容を把握し 必要な装置および消耗品が揃っていることを確認します 詳細は 29 ページの補足情報を参照してください 8 パーツ番号 : Rev. D JPN
9 チップと手法 プロトコールに安全な停止ポイントが明記されていない場合は すぐに次の手順へ進みます クロスコンタミネーションの防止 } サンプルを追加または移動する場合は それぞれのサンプル間のチップを交換してください } アダプターまたはプライマーを追加する場合は 各行および各カラム間のチップを交換してください } 作業台から使用しないインデックスアダプターチューブを取り除いてください チップと手法 プレートの密封 } プロトコールの以下の手順に進む前に必ず 96 ウェルプレートを密封してください 撹拌手順 遠心手順 サーマルサイクリング手順 } 粘着シールをプレートを覆うように貼り ゴムローラーで密封してください } Microseal B 粘着シールは -40 C から 110 C で有効で スカート付きまたはセミスカート付きの PCR プレートに適合します } Microseal A 粘着フィルムは サーマルサイクリングに有効で 96 ウェルすべてを使用しない場合には簡単に切り取れます プレート移動 } プレート間の容量を移す場合 1 つのプレートの各ウェルから他のプレートの対応するウェルに規定された容量を移します TruSeq Nano DNA Library Prep Reference Guide 9
10 ライブラリー調製ワークフロー 図 1 TruSeq Nano DNA Library Prep ワークフロー 10 パーツ番号 : Rev. D JPN
11 プーリングの準備 プーリングする場合は ライブラリー調製を開始する前に IEM または BaseSpace を使用してサンプルに関する情報を記録します } IEM を使用して イルミナのシーケンサーシステムと分析ソフトウェアのサンプルシートの作成および編集を行います } BaseSpace 調製タブを使用して イルミナシーケンサーシステムと分析ソフトウェアのサンプル ライブラリー プール およびランを整理します バランスの取れたインデックスの組み合わせを要するイルミナシーケンサーシステムのライブラリーを調製する場合には TruSeq Library Prep Pooling Guide ( パーツ番号 : ) で予定している手順を検証してください プーリングの準備 TruSeq Nano DNA Library Prep Reference Guide 11
12 DNA の断片化 このプロセスでは gdnaを最適に断片化する方法を説明します 350 bp または550 bp インサートサイズ Covaris 剪断では 3' または5' 末端オーバーハングを有する二本鎖 DNA 断片が生成されます 消耗品 } gdna サンプル インサートサイズが 350 bp の場合は サンプルあたり 100 ng 550 bp の場合はサンプルあたり 200 ng } RSB (Resuspension Buffer) } SPB( サンプル精製ビーズ ) } バーコードラベル CFP(Covaris 断片化プレート ) CSP( クリーンアップ剪断 DNA プレート ) DNA(DNA プレート ) IMP (Insert Modification Plate) } 新たに調製された 80% エタノール (EtOH) } 以下の容器から選択してください : [HS]96 ウェル midi プレート (3) および 96 ウェルハードシェル 0.3 ml PCR プレート (1) [LS]96 ウェル 0.3 ml PCR プレート セミスカート付きまたはスカートレス (4) } Covaris チューブ (1 サンプルにつき 1 本 ) } Microseal B 粘着シール 試薬について } 試薬を使用する前に毎回 SPB をボルテックスしてください } ビーズが均等に分散されるように SPB を頻繁にボルテックスします } 溶液には粘性があるため SPB を吸引および分配する際はゆっくり行ってください 調製 1 以下の消耗品を準備してください アイテム 保存 説明 RSB -25 C~-15 C 室温で融解します 最初の融解後は2 C~8 C SPB 2 C~8 C 室温になるよう 30 分間放置します 後でプロトコールで使用するために室温で保持します 2 Covaris 装置を起動し メーカーのガイドラインに従ってセットアップします 3 [HS] ストロボスコープを使用してマイクロプレートシェイカーを較正し 1800 rpm に設定します 12 パーツ番号 : Rev. D JPN
13 手順 4 以下のとおりバーコードラベルをプレートに貼ります DNA(midi または PCR プレート ) CFP( ハードシェル PCR または PCR プレート ) CSP(midi または PCR プレート ) IMP(midi または PCR プレート ) DNA の断片化 gdna の基準化 1 蛍光定量を使用した手法で gdna を定量します 2 gdna サンプルを 最終量が 52.5 µl になるように DNA プレートで RSB を用いて基準化します インサートサイズが 350 bp の場合は 100 ng インサートサイズが 550 bp の場合は 200 ng 3 以下のとおり しっかり混ぜ合わせます [HS]1800 rpm で 2 分間撹拌します [LS] 上下にピペッティングします 4 以下のとおり遠心します [HS]280 x g で 1 分間遠心します [LS] 軽く遠心します DNA の断片化 1 DNA サンプル 52.5 µl を別の Covaris チューブに移します CFP プレートのウェルを使用して Covaris チューブを直立させてください xg で 5 秒間遠心します 3 以下の Covaris の設定で DNA を断片化します 表 bp インサートの設定 Covarisの設定 M220 S220 S2 E210 デューティー比 (%) 強度 5.0 ピーク放射電力 (W) バーストあたりのサイクル 200 持続時間 ( 秒 ) モード 周波数掃引 温度 ( C) ~6 TruSeq Nano DNA Library Prep Reference Guide 13
14 表 bp インサートの設定 Covaris の設定 M220 S220 S2 E210 デューティー比 (%) 強度 2.0 ピーク放射電力 (W) バーストあたりのサイクル 200 持続時間 ( 秒 ) モード 周波数掃引 温度 ( C) ~ xg で 5 秒間遠心します 5 各 Covaris チューブから CSP プレートの対応するウェルに上清 50 µl を移します 断片化された DNA の精製 1 十分に分散されるまで SPB をボルテックスします 2 各ウェルに SPB 80 µl を添加し その後しっかり混ぜ合わせます [HS]1800 rpm で 2 分間撹拌します [LS] 上下にピペッティングします 3 室温で 5 分間インキュベートします 4 [HS]280 x g で 1 分間遠心します 5 磁気スタンドの上に置き 溶液が透明になるまで放置します (~8 分 ) 6 各ウェルから上清をすべて取り除いて廃棄します 7 以下のとおり洗浄を 2 回行います a 各ウェルに新しく調製した 80% エタノール (EtOH)200 µlを添加します b 磁気スタンドの上で 30 秒間インキュベートします c 各ウェルから上清をすべて取り除いて廃棄します 8 20 µl のピペットを使用して 各ウェルから残っている EtOH を取り除きます 9 磁気スタンド上で 5 分間風乾させます 10 各ウェルに RSB 62.5 µl を添加します 11 磁気スタンドから取り外し その後しっかり混ぜ合わせます [HS]1800 rpm で 2 分間撹拌します [LS] 上下にピペッティングします 12 室温で 2 分間インキュベートします 13 [HS]280 x g で 1 分間遠心します 14 磁気スタンドの上に置き 溶液が透明になるまで放置します (2~5 分間 ) 15 上澄み液 60 µl を IMP プレートの対応するウェルに移します 14 パーツ番号 : Rev. D JPN
15 末端修復およびライブラリーサイズの選択 このプロセスでは End Repair Mix 2 を使用して 断片化によって生じたオーバーハングを平滑末端に変換します このミックスの 3' から 5' のエキソヌクレアーゼ活性は 3' オーバーハングを取り除き 5' から 3' のポリメラーゼ活性は 5' オーバーハングを埋めます 末端修復の後に 割合の異なる SPB( サンプル精製ビーズ ) を用いて適切なライブラリーサイズが選択されます 消耗品 } ERP2 または ERP3 (End Repair Mix) } RSB (Resuspension Buffer) } SPB( サンプル精製ビーズ ) } バーコードラベル ALP (Adapter Ligation Plate) CEP( クリーンアップ末端修復プレート ) } 新たに調製された 80% エタノール (EtOH) } PCR グレード水 } チューブ 6 サンプル以上を処理する場合 -1.7 ml 微量遠心分離チューブ 6 サンプル未満を処理する場合 -15 ml コニカルチューブ } 以下の容器から選択してください : [HS]96 ウェル midi プレート (2) [LS]96 ウェル 0.3 ml PCR プレート セミスカート付きまたはスカートレス (2) } Microseal B 粘着シール 試薬について } キットには ERP2 または ERP3 が入っています } 試薬を使用する前に毎回 SPB をボルテックスしてください } ビーズが均等に分散されるように SPB を頻繁にボルテックスします } 溶液には粘性があるため SPB を吸引および分配する際はゆっくり行ってください 末端修復およびライブラリーサイズの選択 調製 1 以下の消耗品を準備してください アイテム保存説明 ERP2 または ERP3-25 C~-15 C 室温で融解し 氷の上に置いてください 使用後は保管場所に戻してください RSB 2 C~8 C 室温になるよう 30 分間放置します SPB 2 C~8 C 室温になるよう 30 分間放置します 2 [HS] マイクロヒーティングシステムを 30 C に予熱します 3 [LS] サーマルサイクラーに以下の ERP プログラムを保存します プレヒートリッドオプションを選択し 100 C に設定します 30 C で 30 分間 4 C で保持 TruSeq Nano DNA Library Prep Reference Guide 15
16 4 以下のとおりバーコードラベルをプレートに貼ります ALP(midi または PCR プレート ) CEP(midi または PCR プレート ) 手順 オーバーハングの変換 1 ERP2 または ERP3 を 600 x g で 5 秒間遠心します 2 各ウェルに ERP2 または ERP3 を 40 µl 添加し その後以下のとおりしっかり混ぜ合わせます [HS]1800 rpm で 2 分間撹拌します [LS] 上下にピペッティングします 3 [HS]280 x g で 1 分間遠心します 4 以下のとおりインキュベートします [HS] 予熱し蓋を閉じた 30 C のマイクロヒーティングシステムに 30 分間置き その後氷の上に置きます [LS] サーマルサイクラーの上に置き ERP プログラムを実施します 各ウェルには 100 µl 入っています 大きい DNA 断片の除去 1 十分に分散されるまで SPB をボルテックスします 2 PCR グレード水で SPB を末端修復サンプル 100 µl あたり 160µl に希釈します 6 サンプル以下を処理する場合 新しい 1.7 ml 微量遠心分離チューブを使用します 6 サンプルを超えて処理する場合 新しい 15 ml コニカルチューブを使用します 以下の計算式を用い 多くのサンプルについて 15% の過剰量を含む量を決定します 表 bp インサートサイズ用の希釈されたビーズミックス 計算式 12 サンプルあたりの量の例 SPB サンプル数 X µl 1311 µl PCR グレード水サンプル数 X µl 897 µl ユーザーの計算 表 bp インサートサイズ用の希釈されたビーズミックス 計算式 12 サンプルあたりの量の例 SPB サンプル数 X 92 µl 1104 µl PCR グレード水サンプル数 X 92 µl 1104 µl 3 十分に分散されるまで希釈された SPB をボルテックスします ユーザーの計算 4 希釈された SPB160 µl を 各ウェルに添加し その後以下のとおりしっかり混ぜ合わせます [HS]1800 rpm で 2 分間撹拌します [LS] 上下にピペッティングします 5 室温で 5 分間インキュベートします 6 [HS]280 xg で 1 分間遠心します 16 パーツ番号 : Rev. D JPN
17 7 磁気スタンドの上に置き 溶液が透明になるまで放置します (~5 分 ) 8 上清 250 µl を CEP プレートの対応するウェルに移します 9 残留している希釈 SPB を廃棄します 小さい DNA 断片の除去 1 希釈していない SPB を 十分に分散されるまでボルテックスします 2 希釈していない SPB 30 µl を各ウェルに添加し その後以下のとおりしっかり混ぜ合わせます [HS]1800 rpm で 2 分間撹拌します [LS] 上下にピペッティングします 3 室温で 5 分間インキュベートします 4 [HS]280 x g で 1 分間遠心します 5 磁気スタンドの上に置き 溶液が透明になるまで放置します (~5 分 ) 6 各ウェルから上清をすべて取り除いて廃棄します 7 以下のとおり洗浄を 2 回行います a 各ウェルに新しく調製した 80% エタノール (EtOH)200 µlを添加します b 磁気スタンドの上で 30 秒間インキュベートします c 各ウェルから上清をすべて取り除いて廃棄します 8 20 µl のピペットを使用して 各ウェルから残っている EtOH を取り除きます 9 磁気スタンド上で 5 分間風乾させます 10 各ウェルに RSB 20 µl を添加します 11 磁気スタンドから取り外し その後以下のとおりしっかり混ぜ合わせます [HS]1800 rpm で 2 分間撹拌します [LS] 上下にピペッティングします 12 室温で 2 分間インキュベートします 13 [HS]280 xg で 1 分間遠心します 14 磁気スタンドの上に置き 溶液が透明になるまで放置します (~5 分 ) 15 上澄み液 17.5 µl を ALP プレートの対応するウェルに移します 末端修復およびライブラリーサイズの選択 安全なストップポイント 停止する場合 プレートを密封し -25 C~-15 C で最長 7 日間保管してください TruSeq Nano DNA Library Prep Reference Guide 17
18 3 末端のアデニル化 アダプターライゲーションの反応の間に DNA 断片同士が互いにライゲートするのを防ぐ目的で 平滑化された 3' 末端に 1 塩基の A ヌクレオチドを添加します これに対応する形でアダプターの 3 末端に相補的にオーバーハングして存在する 1 塩基の T ヌクレオチドによって アダプターと断片がライゲートします この方法により キメラ ( 連結したテンプレート ) の生成率が低減されます 消耗品 } ATL または ATL2(A-Tailing Mix) } RSB (Resuspension Buffer) } [HS]Microseal B 粘着シール 調製 1 以下の消耗品を準備してください アイテム保存説明 ATL または ATL2-25 C~-15 C 室温で融解します 使用後は保管場所に戻してください RSB 2 C~8 C 室温になるよう 30 分間放置します 2 [HS]2 つのマイクロヒーティングシステムを予熱します システム 1 は 37 C システム 2 は 70 C に予熱します 3 [LS] サーマルサイクラーに以下の ATAIL70 プログラムを保存します プレヒートリッドオプションを選択し 100 C に設定します 37 C で 30 分間 70 C で 5 分間 4 C で 5 分間 4 C で保持 手順 1 ATL または ATL2 を 600 x g で 5 秒間遠心します 2 各ウェルに ATL または ATL212.5 µl を添加し その後以下のとおりしっかり混ぜ合わせます [HS]1800 rpm で 2 分間撹拌します [LS] 上下にピペッティングします x g で 1 分間遠心します 18 パーツ番号 : Rev. D JPN
19 4 以下のとおりインキュベートします [HS] a 37 Cのマイクロヒーティングシステムに蓋を閉じて 30 分間置きます b 70 Cのマイクロヒーティングシステムに移し 蓋を閉じて 5 分間置きます c 氷の上に5 分間置きます [LS] a サーマルサイクラーの上に置き ATAIL70プログラムを実行します 各ウェルには 30 µl 含まれています b 280 x gで1 分間遠心します 3 末端のアデニル化 TruSeq Nano DNA Library Prep Reference Guide 19
20 アダプターのライゲート このプロセスでは 複数のインデックスアダプターを DNA 断片の末端にライゲートし フローセルへのハイブリダイゼーション用に調製します 消耗品 } DNA アダプター ( チューブまたは DAP) } LIG2 (Ligation Mix 2) } RSB (Resuspension Buffer) } SPB( サンプル精製ビーズ ) } STL (Stop Ligation Buffer) } バーコードラベル CAP( クリーンアップ ALP プレート ) DAP(DNA アダプタープレート ) PCR( ポリメラーゼ連鎖反応プレート ) } 新たに調製された 80% エタノール (EtOH) } 以下の容器から選択してください : [HS]96 ウェル midi プレート (1) および 96 ウェルハードシェル 0.3 ml PCR プレート (1) [LS]96 ウェル 0.3 ml PCR プレート セミスカート付きまたはスカートレス (2) } [HS]Microseal B 粘着シール 試薬について } 手順書で指示されるまで 保場場所から LIG2 を取り出さないでください } LIG2 は使用後直ちに保場場所に戻してください } 試薬を使用する前に毎回 SPB をボルテックスしてください } ビーズが均等に分散されるように SPB を頻繁にボルテックスします } 溶液には粘性があるため SPB を吸引および分配する際はゆっくり行ってください 調製 1 以下の消耗品を準備してください アイテム保存説明 DNA アダプター -25 C~-15 C 室温で 10 分間融解します 使用後は保管場所に戻してください DAP に対しては 凍結融解サイクルを最大 4 回行うことができます RSB 2 C~8 C 室温になるよう 30 分間放置します STL -25 C~-15 C 室温で融解します 使用後は保管場所に戻してください SPB 2 C から 8 C 室温になるよう 30 分間放置します 2 [HS] マイクロヒーティングシステムを 30 C に予熱します 20 パーツ番号 : Rev. D JPN
21 手順 3 [LS] サーマルサイクラーに以下の LIG プログラムを保存します プレヒートリッドオプションを選択し 100 C に設定します 30 C で 10 分間 4 C で保持 4 以下のとおりバーコードラベルをプレートに貼ります CAP(midi または PCR) PCR ( ハードシェル PCR または PCR) インデックスアダプターの追加 1 [HT キット ]DAP からテープシールを剝がします 2 以下のとおり DNA アダプターを遠心します アダプターのライゲート 試薬速度時間 アダプターチューブ DAP 600 x g 5 秒間 280 x g 1 分間 3 [HTキット] 以下のとおりDAP を準備してください a プラスチックカバーを外します 同時にすべてのプレートを処理しない場合は カバーは取って置いてください b DAPバーコードを貼ります 4-25 C から -15 C の貯蔵庫から LIG 2 を取り出します 5 以下の試薬を記載の順序で各ウェルに添加し その後しっかり混ぜ合わせます 試薬 RSB 2.5 LIG2 2.5 DNA アダプター 2.5 [HS]1800 rpm で 2 分間撹拌します [LS] 上下にピペッティングします x g で 1 分間遠心します 容量 (µl) 7 以下のとおりインキュベートします [HS]30 C のマイクロヒーティングシステムに蓋を閉じて 10 分間置き その後氷の上に置きます [LS] サーマルサイクラーの上に置き LIG プログラムを実行します 各ウェルには 37.5 µl 入っています 8 STL を 600 x g で 5 秒間遠心します 9 各ウェルに STL 5 µl を添加し その後しっかり混ぜ合わせます [HS]1800 rpm で 2 分間撹拌します [LS] 上下にピペッティングします 10 [HS]280 x g で 1 分間遠心します TruSeq Nano DNA Library Prep Reference Guide 21
22 ライゲートした断片の精製 1 十分に分散されるまで SPB をボルテックスします 2 Round1の容量を用いて 手順 2aから2mを実施します a 各ウェルにSPB を添加し その後しっかり混ぜ合わせます SPB Round1 Round µl 50 µl [HS]1800 rpmで2 分間撹拌します [LS] 上下にピペッティングします b 室温で5 分間インキュベートします c [HS]280 x gで1 分間遠心します d 磁気スタンドの上に置き 溶液が透明になるまで放置します (2~5 分間 ) e 各ウェルから上清をすべて取り除いて廃棄します f 以下のとおり2 回洗浄します 各ウェルに新しく調製した 80% エタノール (EtOH)200 µlを添加します 磁気スタンドの上で 30 秒間インキュベートします 各ウェルから上清をすべて取り除いて廃棄します g 20 µlのピペットを使用して 各ウェルから残っている EtOHを取り除きます h 磁気スタンド上で 5 分間風乾させます i 各ウェルにRSB を添加します Round1 Round2 RSB 52.5 µl 27.5 µl j 磁気スタンドから取り外し その後しっかり混ぜ合わせます [HS]1800 rpmで2 分間撹拌します [LS] 上下にピペッティングします k 室温で2 分間インキュベートします l [HS]280 x gで1 分間遠心します m 磁気スタンドの上に置き 溶液が透明になるまで放置します (2~5 分間 ) 3 上清 50 µl を CAP プレートの対応するウェルに移します 4 新しいプレートで 手順 2a から 2m を Round2 の容量で繰り返します 5 上澄み液 25 µl を PCR プレートの対応するウェルに移します 安全なストップポイント 停止する場合 プレートを密封し -25 C~-15 C で最長 7 日間保管してください 22 パーツ番号 : Rev. D JPN
23 DNA 断片の濃縮 このプロセスでは PCR を使用して 両末端にアダプター分子のある DNA 断片を選択的に濃縮し ライブラリー内にある DNA の量を増幅します PCR は アダプター末端にアニールする PCR Primer Cocktail を用いて実行されます ライブラリーの発現を保持するために PCR サイクル数は最小限にしてください 注記 PCR はアダプターが両端にライゲートされている断片を濃縮します 末端にアダプターが 1 つだけ または全くない断片は 非効率的なライゲーション反応の副産物です いずれの種もクラスターを形成するために使用することはできません アダプターを持たない断片は フローセルの表面結合プライマーにハイブリダイズできません 片端にアダプターを持つ断片は 表面結合プライマーにハイブリダイズできますが クラスターを形成できません DNA 断片の濃縮 消耗品 } EPM (Enhanced PCR Mix) } PPC (PCR Primer Cocktail) } RSB (Resuspension Buffer) } SPB( サンプル精製ビーズ ) } TSP1 (Target Sample Plate) バーコードラベル } 新たに調製された 80% エタノール (EtOH) } 以下の容器から選択してください : [HS]96 ウェル Hard-Shell 0.3 ml PCR プレート (1) [LS]96 ウェル 0.3 ml PCR プレート セミスカート付きまたはスカートレス (1) } [HS]Microseal A フィルム } Microseal B 粘着シール 試薬について } 試薬を使用する前に毎回 SPB をボルテックスしてください } ビーズが均等に分散されるように SPB を頻繁にボルテックスします } 溶液には粘性があるため SPB を吸引および分配する際はゆっくり行ってください 調製 1 以下の消耗品を準備してください 試薬保管条件説明 PPC -25 Cから-15 C 室温で融解します 上下に混ぜ合わせてから 600 xgで1 分間遠心してください ボルテックスしないでください 使用後は貯蔵庫に戻してください EPM -25 Cから-15 C 氷の上で融解します 上下に混ぜ合わせてから 600 xgで1 分間遠心してください ボルテックスしないでください 使用後は貯蔵庫に戻してください SPB 2 C から 8 C 室温になるよう 30 分間放置します RSB 2 C から 8 C 室温になるよう 30 分間放置します TruSeq Nano DNA Library Prep Reference Guide 23
24 2 以下の PCR Nano プログラムをサーマルサイクラーに保存します プレヒートリッドオプションを選択し 100 C に設定します 95 C で 3 分間 以下を 8 サイクル : 98 C で 20 秒間 60 C で 15 秒間 72 C で 30 秒間 72 C で 5 分間 4 C で保持 3 TSP1 バーコードを Hard-Shell PCR または PCR プレートに貼ります 手順 DNA 断片の増幅 1 氷の上に置き 各ウェルに PPC 5 µl を添加します 2 各ウェルに EPM 20 µl を添加し 以下のとおりしっかり混ぜ合わせます [HS]1600 rpm で 20 秒間撹拌します [LS] 上下にピペッティングします x g で 1 分間遠心します 4 サーマルサイクラーの上に置き PCRNano プログラムを実行します 各ウェルには 50 µl 含まれています 増幅 DNA の精製 x g で 1 分間遠心します 2 十分に分散されるまで SPB をボルテックスします 3 SPB を各ウェルに添加します 容量は使用したアダプターのタイプにより異なります アダプターのタイプ SPB の容量 アダプターチューブ 50 µl DAP 47.5 µl 4 以下のとおり しっかり混ぜ合わせます [HS]1800 rpm で 2 分間撹拌します [LS] 上下にピペッティングします 5 室温で 5 分間インキュベートします 6 [HS]280 x g で 1 分間遠心します 7 磁気スタンドの上に置き 溶液が透明になるまで放置します (2~5 分間 ) 8 各ウェルから上清をすべて取り除いて廃棄します 9 以下のとおり洗浄を 2 回行います a 各ウェルに新しく調製した 80% エタノール (EtOH)200 µlを添加します b 磁気スタンドの上で 30 秒間インキュベートします c 各ウェルから上清をすべて取り除いて廃棄します µl のピペットを使用して 各ウェルから残っている EtOH を取り除きます 24 パーツ番号 : Rev. D JPN
25 11 磁気スタンド上で 5 分間風乾させます 12 各ウェルに RSB 32.5 µl を添加します 13 磁気スタンドから取り外し その後以下のとおりしっかり混ぜ合わせます [HS]1800 rpm で 2 分間撹拌します [LS] 上下にピペッティングします 14 室温で 2 分間インキュベートします 15 [HS]280 x g で 1 分間遠心します 16 磁気スタンドの上に置き 溶液が透明になるまで放置します (2~5 分間 ) 17 上清 30 µl を TSP1 プレートの対応するウェルに移します DNA 断片の濃縮 安全なストップポイント 停止する場合 プレートを密封し -25 C~-15 C で最長 7 日間保管してください TruSeq Nano DNA Library Prep Reference Guide 25
26 ライブラリーの検証 ライブラリーの品質管理分析および定量化のために以下の手順を実行してください ライブラリーの定量 イルミナシーケンスプラットフォーム上で最高品質のデータを取得するには フローセルのすべてのレーンにわたって 最適な濃度でクラスターを作成することが重要です クラスター密度を最適化するには DNA ライブラリーの正確な定量が必要です dsdna 結合染料または qpcr を用いる蛍光定量法を使用して ライブラリーを定量してください TruSeq Nano DNA Library Prep ライブラリーの定量は 33 ページの消耗品および装置 KAPA 標準液を用い KAPA 取扱説明書に従ってください nm でライブラリー濃度を計算するためには 以下のインサートサイズ調整を行ってください 350 bp ライブラリーには 平均断片長 470 bp を使用します 550 bp ライブラリーには 平均断片長 670 bp を使用します イルミナシーケンスプラットフォーム技術データシート用の KAPA ライブラリー定量キットは Kapa Biosystems ウェブサイト ( からダウンロードできます ライブラリーの品質チェック 断片サイズを確認するために ライブラリーサイズの分布をチェックします Agilent Technologies 2100 Bioanalyzer のサンプルの実行は定性目的にのみ使用してください 1 以下のことを行ってください : 高感度 DNA チップを使用する場合 : DNA ライブラリーを 1:100 の割合で水と希釈します 希釈した DNA ライブラリー 1µl を実行してください DNA7500 チップを使用する場合には 未希釈 DNA ライブラリー 1µl を実行してください 図 bp インサートライブラリー分布の例 図 bp インサートライブラリー分布の例 26 パーツ番号 : Rev. D JPN
27 ライブラリーの基準化およびプール 本プロセスでは クラスター形成のために DNAテンプレートを調製する方法について説明します インデックスされた DNAライブラリーは DCTプレートで10 nmに基準化された後 PDPプレートにおいて等量がプーリングされます インデックスされていない DNAライブラリーは DCTプレートで10 nmに基準化されます 消耗品 } 1.7 ml 微量遠心分離チューブ (1)(48 を超えるサンプルをプーリングする場合 ) } 以下の容器から選択してください : [HS] 96 ウェル midi プレート (2)( プーリング専用のセカンドプレート ) [LS] 96 ウェル midi プレート (2)(40 を超えるサンプルをプーリングする場合 プーリング専用のセカンドプレート ) 96 ウェル 0.3 ml PCR プレート セミスカート付きまたはスカートレス (1) (40 以下のサンプルをプーリングする場合 ) } Microseal B 粘着シール } Tris-HCl 10 mm(ph % Tween 20 添加 ) } バーコードラベル DCT (Diluted Cluster Template) PDP(Pooled DCT プレート )( プーリング専用 ) ライブラリーの基準化およびプール 調製 1 以下のとおりバーコードラベルをプレートに貼ります DCT(midi プレート ) [ プーリング専用 ]PDP(midi(40 サンプル超えてプーリングする場合 ) または PCR(40 サンプル以下をプーリングする場合 ) プレート ) 手順 DCT の作製 1 ライブラリー 10 µl を DCT プレートの対応するウェルに移します 2 Tris-HCl 10 mm(ph % Tween20 添加 ) を用いて ライブラリーの濃度を 10nM に基準化し その後以下のとおりしっかり混ぜ合わせます [HS]1000 rpm で 2 分間撹拌します [LS] 上下にピペッティングします 注記各ライブラリーの収率定量化データにより 各ウェルの最終量は 10~400 µl の範囲で変わります 3 [HS]280 xg で 1 分間遠心します 4 以下を実行します ライブラリーをプールする場合 ワークフローの次の手順に進んでください ライブラリーをプールしない場合 クラスター形成に進んでください 詳細は イルミナプラットフォームのシステムガイドを参照してください TruSeq Nano DNA Library Prep Reference Guide 27
28 PDP の作製 1 2~24 サンプルをプーリングする場合 基準化された各サンプルライブラリー 10 µl を PDP プレートのウェルの 1 つに移します 2 25~48サンプルプーリングする場合 以下を実行してください a 基準化されたライブラリーの各カラムから 5 µlをpdpプレートのカラム 1に移し その後以下のとおりしっかり混ぜ合わせます [HS]1800 rpmで2 分間撹拌します [LS] 上下にピペッティングします b [HS]280 x gで1 分間遠心します c カラム1の各ウェルの溶液をウェル A2に移します 3 49~96サンプルをプーリングする場合 以下を実行してください a 基準化されたライブラリーの各カラムから 5 µlをpdpプレートのカラム 1に移し その後以下のとおりしっかり混ぜ合わせます [HS]1800 rpmで2 分間撹拌します [LS] 上下にピペッティングします b [HS]280 x gで1 分間遠心します c カラム1の各ウェルの溶液を 1.7 ml 微量遠心分離チューブに移します 4 以下のとおり しっかり混ぜ合わせます [HS] プレートを 1800 rpm で 2 分間撹拌 またはチューブをボルテックスします [LS] 上下にピペッティングします 5 [HS]280 x g で 1 分間遠心します 6 クラスター形成に進みます 詳細は イルミナシーケンスプラットフォームのシステムガイドを参照してください 安全なストップポイント 停止する場合 プレートを密封するかチューブに蓋をして -25 C~-15 C で最長 7 日間保管してください 28 パーツ番号 : Rev. D JPN
29 補足情報 このガイドに記載されたプロトコールでは ユーザーがこの章の内容を十分に理解し 必要な装置と消耗品を揃えていることを前提としています 補足情報 頭文字 頭文字 ALP ATL CAP CEP CFP CSP DAP DCT DNA EPM ERP HS HT IEM IMP LIG LS LT PDP PPC RSB SPB 定義 Adapter Ligation Plate A-Tailing Mix クリーンアップALPプレートクリーンアップ末端修復プレート Covaris 断片化プレートクリーンアップ剪断 DNAプレート DNAアダプタープレート Diluted Cluster Template Plate 顧客サンプルDNAプレート Enhanced PCR Mix End Repair Mix ハイサンプル高スループット Illumina Experiment Manager Insert Modification Plate Ligation Mix ローサンプル低スループットプーリングされた希釈プレート PCR Primer Cocktail Resuspension Buffer サンプル精製ビーズ TruSeq Nano DNA Library Prep Reference Guide 29
30 頭文字 STL 定義 Stop Ligation Buffer TSP1 標的サンプルプレート 1 キット内容 プロトコールを始める前に 本セクションで指定された試薬がすべて揃っていることを確認します TruSeq Nano DNA LT Library Prep Kit は セット A およびセット B として利用できます 各 TruSeq Nano DNA LT Library Prep Kit には 最高 24 サンプル調製するのに十分な量の試薬が含まれています セット A および B をともに使用した場合 各キットの異なる 12 インデックスを用いて最高 24 サンプルをプールすることができます 表 6 TruSeq Nano DNA Library Prep キット キット名カタログ番号サポートサンプル 数 インデックス 番号 TruSeq Nano DNA LT Library Prep Kit- セット A TruSeq Nano DNA LT Library Prep Kit- セット B TruSeq Nano DNA HT Library Prep Kit FC FC FC TruSeq Nano DNA LT Library Prep Kit TruSeq Nano DNA LT Library Prep Kit には セット A またはセット B のボックス SP ビーズボックスの 2 ボックスがあります 24 サンプル - セット A またはセット B ボックス -25 C~-15 C で保存 注文したセットに応じて キットが入ったボックス A または B のいずれかを受け取ります これらのボックスには プレートバーコードラベルも入っています 注記キットには ERP2 または ERP3 および ATL または ATL2 が入っています 30 パーツ番号 : Rev. D JPN
31 セット A 数量試薬内容 1 RSB Resuspension Buffer 補足情報 1 ERP2またはERP3 End Repair Mix 1 ATLまたはATL2 A-Tailing Mix 1 LIG2 Ligation Mix 2 1 STL Stop Ligation Buffer 1 PPC PCR Primer Cocktail 1 EPM Enhanced PCR Mix 1 AD002 DNAアダプターインデックス2 1 AD004 DNAアダプターインデックス4 1 AD005 DNAアダプターインデックス5 1 AD006 DNAアダプターインデックス6 1 AD007 DNAアダプターインデックス7 1 AD012 DNAアダプターインデックス12 1 AD013 DNAアダプターインデックス13 1 AD014 DNAアダプターインデックス14 1 AD015 DNAアダプターインデックス15 1 AD016 DNAアダプターインデックス16 1 AD018 DNAアダプターインデックス18 1 AD019 DNAアダプターインデックス19 TruSeq Nano DNA Library Prep Reference Guide 31
32 セット B 数量 試薬 内容 1 RSB Resuspension Buffer 1 ERP2またはERP3 End Repair Mix 1 ATLまたはATL2 A-Tailing Mix 1 LIG2 Ligation Mix 2 1 STL Stop Ligation Buffer 1 PPC PCR Primer Cocktail 1 EPM Enhanced PCR Mix 1 AD001 DNAアダプターインデックス1 1 AD003 DNAアダプターインデックス3 1 AD008 DNAアダプターインデックス8 1 AD009 DNAアダプターインデックス9 1 AD010 DNAアダプターインデックス10 1 AD011 DNAアダプターインデックス11 1 AD020 DNAアダプターインデックス20 1 AD021 DNAアダプターインデックス21 1 AD022 DNAアダプターインデックス22 1 AD023 DNAアダプターインデックス23 1 AD025 DNAアダプターインデックス25 1 AD027 DNAアダプターインデックス27 24 サンプル -SP ビーズボックス 2 C~8 C で保存 数量試薬内容 1 SPB サンプル精製ビーズ TruSeq Nano DNA HT Library Prep Kit TruSeq Nano DNA HT Library Prep Kit には コア試薬ボックス アダプタープレートボックス SP ビーズボックスの 3 ボックスがあります 96 サンプル -( ボックス 2 の 1) -25 C~-15 C で保存 このボックスには プレートバーコードラベルも入っています 注記キットには ERP2 または ERP3 および ATL または ATL2 が入っています 32 パーツ番号 : Rev. D JPN
33 表 7 TruSeq Nano DNA HT Library Prep Kit96サンプル ( ボックス2の1) パーツ番号 数量 試薬 内容 1 RSB Resuspension Buffer 補足情報 2 ERP2またはERP3 End Repair Mix 2 ATLまたはATL2 A-Tailing Mix 2 LIG2 Ligation Mix 2 2 STL Stop Ligation Buffer 2 PPC PCR Primer Cocktail 2 EPM Enhanced PCR Mix 96 サンプル - アダプタープレートボックス -25 C~-15 C で保存 数量試薬内容 1 DAP DNA アダプタープレート 96 プレックス 96 サンプル -SP ビーズボックス 2 C~8 C で保存 数量試薬内容 6 SPB サンプル精製ビーズ 消耗品および装置 プロトコールを始める前に ユーザが用意する必要な消耗品および備品のすべてが揃っていることを確認します いくつかの物品の要件は 実施するワークフロー (HS または LS) によって決まります これらの物品は別表に記載しています プロトコールは リストした物品を用いて最適化され 検証されました 消耗品や装置を非純正品で代用した場合 同等の性能は保証されません 表 8 ユーザーが用意する消耗品 消耗品 サプライヤー 1.7 ml 微小遠心分離チューブ 一般研究室のサプライヤー 15 mlコニカルチューブ 一般研究室のサプライヤー 10 µlバリアピペットチップ 一般研究室のサプライヤー 10 µlマルチチャネルピペット 一般研究室のサプライヤー 10 µlシングルチャネルピペット 一般研究室のサプライヤー 20 µlバリアピペットチップ 一般研究室のサプライヤー TruSeq Nano DNA Library Prep Reference Guide 33
34 消耗品 サプライヤー 20 µlマルチチャネルピペット 一般研究室のサプライヤー 20 μlシングルチャネルピペット 一般研究室のサプライヤー 200 μlバリアピペットチップ 一般研究室のサプライヤー 200 μlマルチチャネルピペット 一般研究室のサプライヤー 200 μlシングルチャネルピペット 一般研究室のサプライヤー 1000 μlバリアピペットチップ 一般研究室のサプライヤー 1000 μlマルチチャネルピペット 一般研究室のサプライヤー 1000 μlシングルチャネルピペット 一般研究室のサプライヤー 96 ウェル保存用プレート ラウンドウェル 0.8 ml(midi プレート ) 以下のいずれか : DNA 7500 キット 高感度 DNA キット エタノール 200 プルーフ ( アブソルート ) 分子生物学用 (500 ml) アイスバケット KAPA ライブラリー定量キット - Illumina/Universal Microseal A フィルム Microseal B 粘着シール micro TUBE AFA Fiber 6x16mm クライムキャップ または プレスリットスナップキャップ (Covaris M220 用 ) 付き PCR グレード水 Qubit dsdna HS アッセイキット RNaseZap( 表面除染用 ) RNase/DNase フリーの 8 連チューブストリップおよびキャップ Fisher Scientific パーツ番号 :AB-0859 Agilent Technologies パーツ番号 : Sigma-Aldrich パーツ番号 :E7023 一般研究室のサプライヤー KAPA Biosystems パーツ番号 :KK4824 Bio-Rad パーツ番号 :MSA-5001 Bio-Rad パーツ番号 :MSB-1001 Covaris パーツ番号 : または 一般研究室のサプライヤー Life Technologies カタログ番号 :Q32851 一般研究室のサプライヤー 一般研究室のサプライヤー 34 パーツ番号 : Rev. D JPN
35 消耗品 RNase/DNase フリーのマルチチャネル試薬リザーバー 使い捨て Tris-HCl 10 mm ph 8.5 サプライヤー VWR パーツ番号 : 一般研究室のサプライヤー 補足情報 Tween 20 Sigma-Aldrich パーツ番号 :P7949 ( オプション )dsdna 結合色素試薬による蛍光定量 一般研究室のサプライヤー 表 9 ユーザーが用意する消耗品 -HS ワークフロー用追加物品 消耗品 サプライヤー 96 ウェルハードシェル 0.3 ml PCR プレート Bio-Rad パーツ番号 :HSP-9601 スカートのない 96 ウェル 0.3ml PCR プレートまたは Twin.tec 96 ウェル PCR プレート E&K Scientific パーツ番号 または Eppendorf パーツ番号 表 10 ユーザーが用意する装置 装置 サプライヤー 2100 Bioanalyzer デスクトップシステム Agilent Technologies パーツ番号 :G2940CA 96 ウェルサーマルサイクラー ( ヒートリッド付き ) 36 ページのサーマルサイクラーを参照 以下の Covaris システムのいずれか : S2 S220 E210 M220 磁気スタンド 96 マイクロプレート遠心機 ボルテックス qpcr システム 36 ページの qpcr システムを参照 ( オプション )dsdna 結合色素試薬による蛍光定量 一般研究室のサプライヤー Covaris M220 パーツ番号 : 他のすべてのモデルについては Covaris にお問い合わせください Life Technologies カタログ番号 :AM10027 一般研究室のサプライヤー 一般研究室のサプライヤー 一般研究室のサプライヤー 一般研究室のサプライヤー TruSeq Nano DNA Library Prep Reference Guide 35
36 表 11 装置 ユーザーが用意する装置 -HS ワークフロー用の追加物品 サプライヤー 高速マイクロプレートシェーカー VWR カタログ番号 : (110 V/120 V) または (230 V) SciGene TruTemp 加熱システム注意 : 連続加熱処理をサポートする 2 つのシステムを推奨します 加熱システム用の midi プレートインサート 注意 : 連続加熱処理をサポートする 2 つのインサートを推奨します ストロボスコープ Illumina カタログ番号 : SC (110 V) または SC (220 V) Illumina カタログ番号 :BD 一般研究室のサプライヤー サーマルサイクラー 以下の表は イルミナが推奨するサーマルサイクラーおよびその他の同等モデルに関する推奨設定を示します 表に記載されていないサーマルサイクラーに関しては TruSeq Nano DNA Library Prep プロトコールを実行する前に検証してください サーマルサイクラー温度モード蓋の温度容器のタイプ Bio-Rad DNA Engine Tetrad 2 MJ Research PTC-225 DNA Engine Tetrad 計算 100 C で一定に加熱プレート 計算 100 C で一定に加熱プレート Bio-Rad S1000 N/A 100 C で一定に加熱プレート qpcr システム 下表は TruSeq Nano DNA Library Prep プロトコール用に検証された qpcr システムを示します 装置 CFX96 Touch リアルタイム PCR 検出システム * サプライヤー Bio-Rad パーツ番号 : Mx3000P qpcr システム Agilent パーツ番号 : *CFX Manager software バージョン 3.0 で Cq Determination モード (Single Threshold[ 単一閾値 ] モード ベースラインの設定 : ベースライン補正曲線フィットおよびデータ分析用蛍光ドリフト補正適用 ) を使用してください この設定により 機器によって蛍光強度の標準曲線に生じた異常を修正することができます ソフトウェアのインストールについては Bio-Rad にお問い合わせください 36 パーツ番号 : Rev. D JPN
37 インデックスアダプターシーケンス 本章では インデックスアダプターシーケンスについて説明します インデックスアダプターチューブのシーケンス TruSeq Nano DNA LT Library Prep Kit には 以下のインデックスアダプターのシーケンスが含まれています } インデックスの番号付けは連続していません インデックス はありません } シーケンスには 7 塩基が含まれています かっこ () 内に示された第 7 塩基はインデックスリードに含まれません 最初の 6 塩基のみサンプルシートに記録します インデックス 13 以上では インデックスリードの 7 番目のサイクルにみられるように ( かっこ内の ) 第 7 塩基が A ではない場合があります } インデックスリードのシーケンスに使用するサイクル数に関する詳細については ご使用のイルミナシーケンスプラットフォームのシステムガイドを参照してください 補足情報 表 12 TruSeq Nano DNA LT Library Prep Kit セット A インデックスアダプターシーケンス アダプター シーケンス アダプター シーケンス AD002 CGATGT(A) AD013 AGTCAA(C) AD004 TGACCA(A) AD014 AGTTCC(G) AD005 ACAGTG(A) AD015 ATGTCA(G) AD006 GCCAAT(A) AD016 CCGTCC(C) AD007 CAGATC(A) AD018 GTCCGC(A) AD012 CTTGTA(A) AD019 GTGAAA(C) 表 13 TruSeq Nano DNA LT Library Prep Kit セット B インデックスアダプターシーケンス アダプター シーケンス アダプター シーケンス AD001 ATCACG(A) AD020 GTGGCC(T) AD003 TTAGGC(A) AD021 GTTTCG(G) AD008 ACTTGA(A) AD022 CGTACG(T) AD009 GATCAG(A) AD023 GAGTGG(A) AD010 TAGCTT(A) AD025 ACTGAT(A) AD011 GGCTAC(A) AD027 ATTCCT(A) TruSeq Nano DNA Library Prep Reference Guide 37
38 インデックスアダプタープレートのシーケンス TruSeq Nano DNA HT Library Prep Kit の DAP には以下のインデックスアダプターのシーケンスが含まれています サンプルシートに記録されるインデックスアダプターのシーケンスには 8 塩基が含まれ インデックスリード中に 8 塩基すべてがシーケンスされます 表 14 インデックスアダプター 1 のシーケンス アダプター シーケンス アダプター シーケンス D701 ATTACTCG D707 CTGAAGCT D702 TCCGGAGA D708 TAATGCGC D703 CGCTCATT D709 CGGCTATG D704 GAGATTCC D710 TCCGCGAA D705 ATTCAGAA D711 TCTCGCGC D706 GAATTCGT D712 AGCGATAG 表 15 インデックスアダプター 2 のシーケンス アダプター シーケンス アダプター シーケンス D501 TATAGCCT D505 AGGCGAAG D502 ATAGAGGC D506 TAATCTTA D503 CCTATCCT D507 CAGGACGT D504 GGCTCTGA D508 GTACTGAC 図 4 DAP デュアルインデックスのレイアウト 38 パーツ番号 : Rev. D JPN
39 テクニカルサポート テクニカルサポートについては イルミナテクニカルサポートにお問い合わせください 表 16 イルミナ一般問合せ先 ウェブサイト jp.illumina.com Eメール 表 17 イルミナカスタマーサポート電話番号 地域 電話番号 地域 電話番号 日本 スペイン 北米 デンマーク アイルランド ドイツ イタリア ニュージーランド 英国 ノルウェー オーストリア フィンランド オランダ フランス スイス ベルギー スウェーデン テクニカルサポート 製品安全データシート 製品安全データシート (SDS) は イルミナのウェブサイト support.illumina.com/sds.html で入手できます 製品文書 PDF の製品文書は イルミナのウェブサイトからダウンロードして入手できます support.illumina.com にアクセスして 製品 を選択し [Documentation & Literature] を選択します TruSeq Nano DNA Library Prep Reference Guide
40 イルミナ株式会社 東京都港区芝 三田ベルジュビル 22 階サポート専用フリーダイヤル jp.illumina.com * * パーツ番号 : Rev. D JPN
Microsoft PowerPoint - 社外資料_TruSeq Synthetic Long-Read DNA Library Prep.pptx
 TruSeq Synthetic Long- Read DNA ライブラリー調製キット イルミナ株式会社マーケティング部 2014 Illumina, Inc. All rights reserved. Illumina, 24sure, IlluminaDx, BaseSpace, BeadArray, BeadArray, BlueFish, BeadXpress, BlueFuse, cbot,
TruSeq Synthetic Long- Read DNA ライブラリー調製キット イルミナ株式会社マーケティング部 2014 Illumina, Inc. All rights reserved. Illumina, 24sure, IlluminaDx, BaseSpace, BeadArray, BeadArray, BlueFish, BeadXpress, BlueFuse, cbot,
Slide 1
 Dual Index を持つ Library のシーケンサーセットアップ 小林孝史テクニカルアプリケーションサイエンティスト 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress, cbot, CSPro, DASL, DesignStudio, Eco, GAIIx,
Dual Index を持つ Library のシーケンサーセットアップ 小林孝史テクニカルアプリケーションサイエンティスト 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress, cbot, CSPro, DASL, DesignStudio, Eco, GAIIx,
サンプルのマルチプレックスおよび下流の解析におけるインデックスのミスアサインメントの影響
 サンプルのマルチプレックスおよび下流の解析におけるインデックスのミスアサインメントの影響 インデックスのミスアサインメントの原因と インデックスホッピングの影響を軽減するベストプラクティス はじめに 次世代シーケンス (NGS) 技術の改良により シーケンススピードが大幅に向上し データ出力が飛躍的に増加したことで 現在のシーケンスプラットフォームにおいて大規模なサンプルの解析が可能になりました 10
サンプルのマルチプレックスおよび下流の解析におけるインデックスのミスアサインメントの影響 インデックスのミスアサインメントの原因と インデックスホッピングの影響を軽減するベストプラクティス はじめに 次世代シーケンス (NGS) 技術の改良により シーケンススピードが大幅に向上し データ出力が飛躍的に増加したことで 現在のシーケンスプラットフォームにおいて大規模なサンプルの解析が可能になりました 10
Microsoft PowerPoint _illumina_techsupport_session02_公開用_RevB [互換モード]
![Microsoft PowerPoint _illumina_techsupport_session02_公開用_RevB [互換モード] Microsoft PowerPoint _illumina_techsupport_session02_公開用_RevB [互換モード]](/thumbs/100/147813922.jpg) トラブルシューティング編 Nextera ライブラリー調製キットシリーズで期待通りのライブラリーを得るためのヒント March 6, 2015 150511 RevB: 一部修正 小林孝史イルミナ株式会社テクニカルサポート部テクニカルアプリケーションサイエンティスト 2014 Illumina, Inc. All rights reserved.illumina, 24sure, BaseSpace,
トラブルシューティング編 Nextera ライブラリー調製キットシリーズで期待通りのライブラリーを得るためのヒント March 6, 2015 150511 RevB: 一部修正 小林孝史イルミナ株式会社テクニカルサポート部テクニカルアプリケーションサイエンティスト 2014 Illumina, Inc. All rights reserved.illumina, 24sure, BaseSpace,
Troubleshooting Nextera Sample Preparation
 Nextera/Nextera XT サンプル調製キットの使用法とトラブルシューティング 酒井名朋子 Sr. Technical Applications Scientist イルミナ株式会社 2011 Illumina, Inc. All rights reserved. Illumina, illuminadx, BeadArray, BeadXpress, cbot, CSPro, DASL,
Nextera/Nextera XT サンプル調製キットの使用法とトラブルシューティング 酒井名朋子 Sr. Technical Applications Scientist イルミナ株式会社 2011 Illumina, Inc. All rights reserved. Illumina, illuminadx, BeadArray, BeadXpress, cbot, CSPro, DASL,
進化したNextera DNA Flex を用いたライブラリー調製
 進化した Nextera DNA Flex を用いたライブラリー調製 フィールドアプリケーションサイエンティスト大出明 2018/10/31 2016 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro, CytoChip,
進化した Nextera DNA Flex を用いたライブラリー調製 フィールドアプリケーションサイエンティスト大出明 2018/10/31 2016 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro, CytoChip,
RNA-Seqをはじめよう ライブラリー調製編 絶対に失敗しないライブラリー調製
 RNA-Seq をはじめようライブラリー調製編絶対に失敗しないライブラリー調製 フィールドアプリケーションサイエンティスト仲健太 2018/2/28 2016 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro, CytoChip,
RNA-Seq をはじめようライブラリー調製編絶対に失敗しないライブラリー調製 フィールドアプリケーションサイエンティスト仲健太 2018/2/28 2016 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro, CytoChip,
Slide 1
 NGS をはじめよう!RNA-Seq 入門 ( キットの選び方 実験デザイン ) April 18, 2014 米田瑞穂イルミナ株式会社テクニカルアプリケーションサイエンティスト 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress, cbot, CSPro, DASL,
NGS をはじめよう!RNA-Seq 入門 ( キットの選び方 実験デザイン ) April 18, 2014 米田瑞穂イルミナ株式会社テクニカルアプリケーションサイエンティスト 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress, cbot, CSPro, DASL,
16S (V3-V4) Metagenomic Library Construction Kit for NGS
 研究用 16S (V3-V4) Metagenomic Library Construction Kit for NGS 説明書 v201705da 本製品は イルミナ社 MiSeq で 16S rrna 細菌叢解析を行うための PCR 増幅キットです 細菌 16S rrna 遺伝子の V3-V4 領域を対象とし PCR 酵素に 多様な配列を効率よく増幅可能な Tks Gflex DNA Polymerase
研究用 16S (V3-V4) Metagenomic Library Construction Kit for NGS 説明書 v201705da 本製品は イルミナ社 MiSeq で 16S rrna 細菌叢解析を行うための PCR 増幅キットです 細菌 16S rrna 遺伝子の V3-V4 領域を対象とし PCR 酵素に 多様な配列を効率よく増幅可能な Tks Gflex DNA Polymerase
Slide 1
 ラン間のサンプル持ち込みを最大限に防ぐための MiSeq のメンテナンステンプレート洗浄のプロトコール August 22, 2014 崎川真里イルミナ株式会社アソシエイトテクニカルアプリケーションサイエンティスト 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress,
ラン間のサンプル持ち込みを最大限に防ぐための MiSeq のメンテナンステンプレート洗浄のプロトコール August 22, 2014 崎川真里イルミナ株式会社アソシエイトテクニカルアプリケーションサイエンティスト 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress,
Slide 1
 NGS をはじめよう! これだけは知っておきたい MiSeq ~ 解析原理と必要な試薬キット 装置の使い方 ~ June 27, 2014 米田瑞穂イルミナ株式会社テクニカルアプリケーションサイエンティスト 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress,
NGS をはじめよう! これだけは知っておきたい MiSeq ~ 解析原理と必要な試薬キット 装置の使い方 ~ June 27, 2014 米田瑞穂イルミナ株式会社テクニカルアプリケーションサイエンティスト 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress,
Microsoft PowerPoint - Final _LibraryQC_andTroubleshooting_August2013
 BioAnayzer を使用した Library QC と トラブルシューティング 田中敦成イルミナ株式会社 テクニカルアプリケーションサイエンティスト 2012 Iumina, Inc. A rights reserved. Iumina, iuminadx, BaseSpace, BeadArray, BeadXpress, cbot, CSPro, DASL, DesignStudio, Eco,
BioAnayzer を使用した Library QC と トラブルシューティング 田中敦成イルミナ株式会社 テクニカルアプリケーションサイエンティスト 2012 Iumina, Inc. A rights reserved. Iumina, iuminadx, BaseSpace, BeadArray, BeadXpress, cbot, CSPro, DASL, DesignStudio, Eco,
Slide 1
 イルミナ NGS でロングリードを可能にする TruSeq Synthetic Long-Read ライブラリー調製キット : ワークフローのご紹介および注意点 November 28, 2014 崎川真里イルミナ株式会社テクニカルアプリケーションサイエンティスト 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace,
イルミナ NGS でロングリードを可能にする TruSeq Synthetic Long-Read ライブラリー調製キット : ワークフローのご紹介および注意点 November 28, 2014 崎川真里イルミナ株式会社テクニカルアプリケーションサイエンティスト 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace,
Microsoft PowerPoint - LongRangePCR+Nextera webinar (with cover) RevC (本番)
 狙った領域を高カバレッジにカバーする Long Range PCR + Nextera 法のご紹介 : ヒトミトコンドリアゲノム解析を例に Oct 3, 2014 ( 注意 ) 一部動画ファイル (http://www.illuminakk.co.jp/events/webinar_japan.ilmn?ws=ss) に修正を入れさせていただきアップロードいたします 小林孝史イルミナ株式会社テクニカルサポート部テクニカルアプリケーションサイエンティスト
狙った領域を高カバレッジにカバーする Long Range PCR + Nextera 法のご紹介 : ヒトミトコンドリアゲノム解析を例に Oct 3, 2014 ( 注意 ) 一部動画ファイル (http://www.illuminakk.co.jp/events/webinar_japan.ilmn?ws=ss) に修正を入れさせていただきアップロードいたします 小林孝史イルミナ株式会社テクニカルサポート部テクニカルアプリケーションサイエンティスト
■リアルタイムPCR実践編
 リアルタイム PCR 実践編 - SYBR Green I によるリアルタイム RT-PCR - 1. プライマー設計 (1)Perfect Real Time サポートシステムを利用し 設計済みのものを購入する ヒト マウス ラットの RefSeq 配列の大部分については Perfect Real Time サポートシステムが利用できます 目的の遺伝子を検索して購入してください (2) カスタム設計サービスを利用する
リアルタイム PCR 実践編 - SYBR Green I によるリアルタイム RT-PCR - 1. プライマー設計 (1)Perfect Real Time サポートシステムを利用し 設計済みのものを購入する ヒト マウス ラットの RefSeq 配列の大部分については Perfect Real Time サポートシステムが利用できます 目的の遺伝子を検索して購入してください (2) カスタム設計サービスを利用する
NGS_KAPA RNA HyperPrep Kit
 シークエンシングワークフロー ライブラリー調製 サンプル 調製 末端修復 エンドポイントライブラリー増幅 A-TAILING アダプター ライゲーション サイズセレクション & サイズ確認 または リアルタイムライブラリー増幅 ライブラリー 定量 クラスター 増幅 KAPA RNA HyperPrep Kit illumina社用ライブラリー調製キット KAPA RNA HyperPrep Kit
シークエンシングワークフロー ライブラリー調製 サンプル 調製 末端修復 エンドポイントライブラリー増幅 A-TAILING アダプター ライゲーション サイズセレクション & サイズ確認 または リアルタイムライブラリー増幅 ライブラリー 定量 クラスター 増幅 KAPA RNA HyperPrep Kit illumina社用ライブラリー調製キット KAPA RNA HyperPrep Kit
16Sサンプル調製ガイド A JPN
 16S Metagenomic Sequencing Library Preparation イルミナ MiSeq システム向け 16S リボソーム RNA 遺伝子アンプリコンの調製 はじめに 2 16Sライブラリー調製のワークフロー 5 アンプリコンPCR 6 PCRクリーンアップ 8 インデックスPCR 10 PCRクリーンアップ 2 13 ( オプション ) ライブラリーの検証 15 ライブラリーの定量
16S Metagenomic Sequencing Library Preparation イルミナ MiSeq システム向け 16S リボソーム RNA 遺伝子アンプリコンの調製 はじめに 2 16Sライブラリー調製のワークフロー 5 アンプリコンPCR 6 PCRクリーンアップ 8 インデックスPCR 10 PCRクリーンアップ 2 13 ( オプション ) ライブラリーの検証 15 ライブラリーの定量
PowerPoint プレゼンテーション
 NGS 超入門 MiSeq システムのご紹介 イルミナ株式会社サービス サポート部仲健太 2014 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro, CytoChip, DesignStudio, Epicentre,
NGS 超入門 MiSeq システムのご紹介 イルミナ株式会社サービス サポート部仲健太 2014 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro, CytoChip, DesignStudio, Epicentre,
Slide 1
 イルミナテクニカルセミナー session3 Illumina Experiment Manager の使い方 サービス サポート部テクニカルサポートサイエンティスト渡辺真子 2011 Illumina, Inc. All rights reserved. Illumina, illuminadx, BeadArray, BeadXpress, cbot, CSPro, DASL, Eco, Genetic
イルミナテクニカルセミナー session3 Illumina Experiment Manager の使い方 サービス サポート部テクニカルサポートサイエンティスト渡辺真子 2011 Illumina, Inc. All rights reserved. Illumina, illuminadx, BeadArray, BeadXpress, cbot, CSPro, DASL, Eco, Genetic
Slide 1
 Bioanalyzer と qpcr を使用したライブラリの定性 定量評価 酒井名朋子イルミナ株式会社テクニカルサポート 2010 Illumina, Inc. All rights reserved. Illumina, illuminadx, Solexa, Making Sense Out of Life, Oligator, Sentrix, GoldenGate, GoldenGate Indexing,
Bioanalyzer と qpcr を使用したライブラリの定性 定量評価 酒井名朋子イルミナ株式会社テクニカルサポート 2010 Illumina, Inc. All rights reserved. Illumina, illuminadx, Solexa, Making Sense Out of Life, Oligator, Sentrix, GoldenGate, GoldenGate Indexing,
DNA/RNA調製法 実験ガイド
 DNA/RNA 調製法実験ガイド PCR の鋳型となる DNA を調製するにはいくつかの方法があり 検体の種類や実験目的に応じて適切な方法を選択します この文書では これらの方法について実際の操作方法を具体的に解説します また RNA 調製の際の注意事項や RNA 調製用のキット等をご紹介します - 目次 - 1 実験に必要なもの 2 コロニーからの DNA 調製 3 増菌培養液からの DNA 調製
DNA/RNA 調製法実験ガイド PCR の鋳型となる DNA を調製するにはいくつかの方法があり 検体の種類や実験目的に応じて適切な方法を選択します この文書では これらの方法について実際の操作方法を具体的に解説します また RNA 調製の際の注意事項や RNA 調製用のキット等をご紹介します - 目次 - 1 実験に必要なもの 2 コロニーからの DNA 調製 3 増菌培養液からの DNA 調製
Introduction to Illumina Next Generation Sequencing (NGS)
 イルミナ Sequencing By Synthesis (SBS) ケミストリーのご紹介 小林孝史イルミナ株式会社 テクニカルアプリケーションサイエンティスト 2013 Illumina, Inc. ll rights reserved. Illumina, IlluminaDx, BaseSpace, Beadrray, BeadXpress, cbot, SPro, DSL, DesignStudio,
イルミナ Sequencing By Synthesis (SBS) ケミストリーのご紹介 小林孝史イルミナ株式会社 テクニカルアプリケーションサイエンティスト 2013 Illumina, Inc. ll rights reserved. Illumina, IlluminaDx, BaseSpace, Beadrray, BeadXpress, cbot, SPro, DSL, DesignStudio,
2015 年 5 月 15 日イルミナサポートウェビナー Nextera Rapid Capture Exome キットを用いたエクソームシーケンス - ドライ編 BaseSpace で行うかんたん NGS データ解析 < Enrichment アプリ > イルミナ株式会社バイオインフォマティクスサ
 2015 年 5 月 15 日イルミナサポートウェビナー Nextera Rapid Capture Exome キットを用いたエクソームシーケンス - ドライ編 BaseSpace で行うかんたん NGS データ解析 < アプリ > イルミナ株式会社バイオインフォマティクスサポートサイエンティスト癸生川絵里 (Eri Kibukawa) 2014 Illumina, Inc. All rights
2015 年 5 月 15 日イルミナサポートウェビナー Nextera Rapid Capture Exome キットを用いたエクソームシーケンス - ドライ編 BaseSpace で行うかんたん NGS データ解析 < アプリ > イルミナ株式会社バイオインフォマティクスサポートサイエンティスト癸生川絵里 (Eri Kibukawa) 2014 Illumina, Inc. All rights
培養細胞からの Total RNA 抽出の手順 接着細胞のプロトコル 1. プレート ( またはウエル ) より培地を除き PBSでの洗浄を行う 2. トリプシン処理を行い 全量を1.5ml 遠心チューブに移す スクレイパーを使って 細胞を掻き集める方法も有用です 3. 低速遠心 ( 例 300 g
 Maxwell RSC simplyrna Cells / Tissue Kit ( カタログ番号 AS1340/AS1390) 簡易マニュアル 注意 : キットを受け取りましたら 1-Thioglycerolを取り出し キット箱は室温で保存してください 取り出した1-Thioglycerolは2~10 で保存してください ご用意いただくもの 細胞 組織の両方の場合で共通 ボルテックスミキサー ピペットマン
Maxwell RSC simplyrna Cells / Tissue Kit ( カタログ番号 AS1340/AS1390) 簡易マニュアル 注意 : キットを受け取りましたら 1-Thioglycerolを取り出し キット箱は室温で保存してください 取り出した1-Thioglycerolは2~10 で保存してください ご用意いただくもの 細胞 組織の両方の場合で共通 ボルテックスミキサー ピペットマン
BaseSpaceで達成するSmall RNA発現解析
 BaseSpace で達成する Small RNA 発現解析 March 28, 2016 寺倉伸治イルミナ株式会社アプリケーションコンサルタント 2015 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro, CytoChip,
BaseSpace で達成する Small RNA 発現解析 March 28, 2016 寺倉伸治イルミナ株式会社アプリケーションコンサルタント 2015 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro, CytoChip,
遺伝子検査の基礎知識
 リアルタイム PCR( インターカレーター法 ) 実験ガイドこの文書では インターカレーター法 (TB Green 検出 ) によるリアルタイム PCR について 蛍光検出の原理や実験操作の流れなどを解説します 実際の実験操作の詳細については 各製品の取扱説明書をご参照ください - 目次 - 1 蛍光検出の原理 2 実験に必要なもの 3 実験操作法 4 結果の解析 1 1 蛍光検出の原理 インターカレーターによる蛍光検出の原理
リアルタイム PCR( インターカレーター法 ) 実験ガイドこの文書では インターカレーター法 (TB Green 検出 ) によるリアルタイム PCR について 蛍光検出の原理や実験操作の流れなどを解説します 実際の実験操作の詳細については 各製品の取扱説明書をご参照ください - 目次 - 1 蛍光検出の原理 2 実験に必要なもの 3 実験操作法 4 結果の解析 1 1 蛍光検出の原理 インターカレーターによる蛍光検出の原理
Microsoft PowerPoint - 111513 TANAKA Optimizing Clusters passing filter2
 Clusters Passing Filterを 最 適 化 するには イルミナ 株 式 会 社 テクニカルアプリケーションサイエンティスト 田 中 敦 成 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress, cbot, CSPro, DASL, DesignStudio,
Clusters Passing Filterを 最 適 化 するには イルミナ 株 式 会 社 テクニカルアプリケーションサイエンティスト 田 中 敦 成 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress, cbot, CSPro, DASL, DesignStudio,
Microsoft PowerPoint - Webinar_April10_b.pptx
 NGS をはじめよう! NextSeq500 で何ができるのか? April 10, 2015 崎川真里イルミナ株式会社テクニカルアプリケーションサイエンティスト 2014 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro,
NGS をはじめよう! NextSeq500 で何ができるのか? April 10, 2015 崎川真里イルミナ株式会社テクニカルアプリケーションサイエンティスト 2014 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro,
BKL Kit (Blunting Kination Ligation Kit)
 製品コード 6126/6127 BKL Kit (Blunting Kination Ligation Kit) 説明書 PCR 産物を平滑末端ベクターにクローニングする場合 使用するポリメラーゼ酵素の種類により 3' 末端に余分に付加された塩基を除去し さらに 5' 末端をリン酸化する必要があります 本製品は これらの一連の反応を簡便に短時間に行うためのキットです PCR 産物の末端平滑化とリン酸化を同時に行うことにより
製品コード 6126/6127 BKL Kit (Blunting Kination Ligation Kit) 説明書 PCR 産物を平滑末端ベクターにクローニングする場合 使用するポリメラーゼ酵素の種類により 3' 末端に余分に付加された塩基を除去し さらに 5' 末端をリン酸化する必要があります 本製品は これらの一連の反応を簡便に短時間に行うためのキットです PCR 産物の末端平滑化とリン酸化を同時に行うことにより
ISOSPIN Blood & Plasma DNA
 血液 血清 血しょうからの DNA 抽出キット ISOSPIN Blood & Plasma DNA マニュアル ( 第 2 版 ) Code No. 312-08131 NIPPON GENE CO., LTD. I 製品説明 ISOSPIN Blood & Plasma DNA( アイソスピンブラッド & プラズマ DNA) は 血液 血清 血しょうから DNAを抽出するためのキットです 本キットは
血液 血清 血しょうからの DNA 抽出キット ISOSPIN Blood & Plasma DNA マニュアル ( 第 2 版 ) Code No. 312-08131 NIPPON GENE CO., LTD. I 製品説明 ISOSPIN Blood & Plasma DNA( アイソスピンブラッド & プラズマ DNA) は 血液 血清 血しょうから DNAを抽出するためのキットです 本キットは
Microsoft Word - FMB_Text(PCR) _ver3.doc
 2.PCR 法による DNA の増幅 現代の分子生物学において その進歩に最も貢献した実験法の1つが PCR(Polymerase chain reaction) 法である PCR 法は極めて微量の DNA サンプルから特定の DNA 断片を短時間に大量に増幅することができる方法であり 多大な時間と労力を要した遺伝子クローニングを過去のものとしてしまった また その操作の簡便さから 現在では基礎研究のみならず臨床遺伝子診断から食品衛生検査
2.PCR 法による DNA の増幅 現代の分子生物学において その進歩に最も貢献した実験法の1つが PCR(Polymerase chain reaction) 法である PCR 法は極めて微量の DNA サンプルから特定の DNA 断片を短時間に大量に増幅することができる方法であり 多大な時間と労力を要した遺伝子クローニングを過去のものとしてしまった また その操作の簡便さから 現在では基礎研究のみならず臨床遺伝子診断から食品衛生検査
My Document
 MiSeq Sample Sheet Quick Reference Guide (MiSeq サンプルシートクイックリファレンスガイド ) FOR RESEARCH USE ONLY Introduction ( はじめに ) 3 Setting Up the Sample Sheet ( サンプルシートのセットアップ ) 5 Sample Sheet Parameters ( サンプルシート )
MiSeq Sample Sheet Quick Reference Guide (MiSeq サンプルシートクイックリファレンスガイド ) FOR RESEARCH USE ONLY Introduction ( はじめに ) 3 Setting Up the Sample Sheet ( サンプルシートのセットアップ ) 5 Sample Sheet Parameters ( サンプルシート )
予算申請ウェビナー ウイルス、微生物編
 予算申請ウェビナーウイルス 微生物編 イルミナ株式会社マーケティング本部 プロダクトマーケティング部 2016 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro, CytoChip, DesignStudio, Epicentre,
予算申請ウェビナーウイルス 微生物編 イルミナ株式会社マーケティング本部 プロダクトマーケティング部 2016 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro, CytoChip, DesignStudio, Epicentre,
Cytotoxicity LDH Assay Kit-WST
 ytotoxicity L ssay Kit-WST はじめに 本説明書は ytotoxicity L ssay Kit-WST を用いた抗体依存性細胞傷害測定用 (ntibody-dependent cellmediated cytotoxicity: ) です 本製品のキット内容や Working Solution の調製方法に関して 製品添付の取扱い説明書も合わせてご覧ください 正確な測定のために
ytotoxicity L ssay Kit-WST はじめに 本説明書は ytotoxicity L ssay Kit-WST を用いた抗体依存性細胞傷害測定用 (ntibody-dependent cellmediated cytotoxicity: ) です 本製品のキット内容や Working Solution の調製方法に関して 製品添付の取扱い説明書も合わせてご覧ください 正確な測定のために
mRNA-Seq_SamplePrep.book
 mrna Sequencing Sample Preparation Guide Topics 3 Introduction 4 RNA Input Recommendations 6 mrna-seq Sample Preparation Kit Contents 8 User-Supplied Consumables and Equipment 9 Purify the mrna 12 Fragment
mrna Sequencing Sample Preparation Guide Topics 3 Introduction 4 RNA Input Recommendations 6 mrna-seq Sample Preparation Kit Contents 8 User-Supplied Consumables and Equipment 9 Purify the mrna 12 Fragment
組織からのゲノム DNA 抽出キット Tissue Genomic DNA Extraction Mini Kit 目次基本データ 3 キットの内容 3 重要事項 4 操作 4 サンプル別プロトコール 7 トラブルシューティング 9 * 本製品は研究用です *
 組織からのゲノム DNA 抽出キット Tissue Genomic DNA Extraction Mini Kit 目次基本データ 3 キットの内容 3 重要事項 4 操作 4 サンプル別プロトコール 7 トラブルシューティング 9 * 本製品は研究用です * 2 本キットは動物の組織からトータル DNA を迅速に効率よく抽出するようにデザインされています また 細菌 固定組織 酵母用のプロトコールも用意しています
組織からのゲノム DNA 抽出キット Tissue Genomic DNA Extraction Mini Kit 目次基本データ 3 キットの内容 3 重要事項 4 操作 4 サンプル別プロトコール 7 トラブルシューティング 9 * 本製品は研究用です * 2 本キットは動物の組織からトータル DNA を迅速に効率よく抽出するようにデザインされています また 細菌 固定組織 酵母用のプロトコールも用意しています
MLPA 法 Q&A 集
 MLPA 法 Q&A 集 目次 1. MLPA 法の導入 Q1. 導入にあたり 何が必要になりますか? Q2. 実験にはどのようなサンプルが必要でしょうか? Q3. サンプルDNAはどれくらい用意すれば良いですか? Q4. キャピラリーシーケンサが自施設に無い場合でも実験はできますか? Q5. FFPE 検体でも実験はできますか? 2. 実験のセットアップ Q1. 実験において重要なポイントはありますか?
MLPA 法 Q&A 集 目次 1. MLPA 法の導入 Q1. 導入にあたり 何が必要になりますか? Q2. 実験にはどのようなサンプルが必要でしょうか? Q3. サンプルDNAはどれくらい用意すれば良いですか? Q4. キャピラリーシーケンサが自施設に無い場合でも実験はできますか? Q5. FFPE 検体でも実験はできますか? 2. 実験のセットアップ Q1. 実験において重要なポイントはありますか?
Infinium BeadChip COGS BeadChip 4 * iselect 3 SNP 25 1 SNP NGS Sequencing by Synthesis SBS HiSeq MiSeq WGS 1 RNA-Seq ChIP-Seq 1 1 * icogs BCAC OCAC PR
 Infinium BeadChip COGS BeadChip 4 * iselect 3 SNP 25 1 SNP NGS Sequencing by SynthesisSBSHiSeq MiSeq WGS 1 RNA-Seq ChIP-Seq 1 1 * icogs BCACOCAC PRACTICALBRCA1/2 CIMBA www.illuminakk.co.jp DNA CE DNA DNA
Infinium BeadChip COGS BeadChip 4 * iselect 3 SNP 25 1 SNP NGS Sequencing by SynthesisSBSHiSeq MiSeq WGS 1 RNA-Seq ChIP-Seq 1 1 * icogs BCACOCAC PRACTICALBRCA1/2 CIMBA www.illuminakk.co.jp DNA CE DNA DNA
サンプルシート作成ツール: Illumina Experimental Manager(IEM)の使用方法 -最新バージョンIEMv1.15のご紹介-
 サンプルシート作成ツール : Illumina Experimental Manager (IEM) の使用方法 - 最新バージョン v1.15.1 のご紹介 - 上利佳弘フィールドアプリケーションスーパーバイザー 25-Jul-2018 2017 Illumina, Inc. All rights reserved. For Research Use Only. Not for use in diagnostic
サンプルシート作成ツール : Illumina Experimental Manager (IEM) の使用方法 - 最新バージョン v1.15.1 のご紹介 - 上利佳弘フィールドアプリケーションスーパーバイザー 25-Jul-2018 2017 Illumina, Inc. All rights reserved. For Research Use Only. Not for use in diagnostic
MiSeqのランのセットアップ時・開始時 に起こるトラブルの対処方法
 イルミナソフトウェアを用いた NGS データの解析におけるヒント Dec 4, 2015 渡邊大イルミナ株式会社テクニカルアプリケーションサイエンティスト 2015 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro,
イルミナソフトウェアを用いた NGS データの解析におけるヒント Dec 4, 2015 渡邊大イルミナ株式会社テクニカルアプリケーションサイエンティスト 2015 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro,
Microsoft PowerPoint _webinar_RNAExpress.erikibukawa_配布用.pptx
 2014 年 10 月 17 日イルミナサポートウェビナー RNA Seq を始めよう! BaseSpace で行う かんたん NGS データ解析 < RNA Express > イルミナ株式会社バイオインフォマティクスサポートサイエンティスト癸生川絵里 (Eri Kibukawa) 2013 2014 Illumina, Inc. All rights reserved. Illumina, 24sure,
2014 年 10 月 17 日イルミナサポートウェビナー RNA Seq を始めよう! BaseSpace で行う かんたん NGS データ解析 < RNA Express > イルミナ株式会社バイオインフォマティクスサポートサイエンティスト癸生川絵里 (Eri Kibukawa) 2013 2014 Illumina, Inc. All rights reserved. Illumina, 24sure,
Bacterial 16S rDNA PCR Kit
 研究用 Bacterial 16S rdna PCR Kit 説明書 v201802da 微生物の同定は 形態的特徴 生理 生化学的性状 化学分類学的性状などを利用して行われますが これらの方法では同定までに時間を要します また 同定が困難な場合や正しい結果が得られない場合もあります 近年 微生物同定にも分子生物学を利用した方法が採用されるようになり 微生物の持つ DNA を対象として解析を行う方法が活用されています
研究用 Bacterial 16S rdna PCR Kit 説明書 v201802da 微生物の同定は 形態的特徴 生理 生化学的性状 化学分類学的性状などを利用して行われますが これらの方法では同定までに時間を要します また 同定が困難な場合や正しい結果が得られない場合もあります 近年 微生物同定にも分子生物学を利用した方法が採用されるようになり 微生物の持つ DNA を対象として解析を行う方法が活用されています
150602_AN_SureSelect と KAPA Hyper Prep.indd
 Agilent SureSelect KAPA Hyper Prep Kit DNA 10 ng : FFPE DNA DNA V2.5BJ 2015 5 & : KAPA Hyper Prep Kit SureSelect XT :KAPA Hyper Prep Kit, SureSelect, Agilent SureSelect XT PCR Primer KAPA Hyper Prep Kit
Agilent SureSelect KAPA Hyper Prep Kit DNA 10 ng : FFPE DNA DNA V2.5BJ 2015 5 & : KAPA Hyper Prep Kit SureSelect XT :KAPA Hyper Prep Kit, SureSelect, Agilent SureSelect XT PCR Primer KAPA Hyper Prep Kit
Slide 1
 FFPE サンプルを用いたシーケンス November 6, 2015 山重りえイルミナ株式会社テクニカルアプリケーションサイエンティスト 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress, cbot, CSPro, DASL, DesignStudio, Eco,
FFPE サンプルを用いたシーケンス November 6, 2015 山重りえイルミナ株式会社テクニカルアプリケーションサイエンティスト 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress, cbot, CSPro, DASL, DesignStudio, Eco,
NGS検査_SOP(案)v1
 平成 29 年 2 月 6 日 次世代シークエンサー (Next-generation sequencing: NGS) 網羅的病原体検査法手順書 必要な試薬 DNA/RNA 精製キット ( 以下の DNA/RNA 精製試薬を推奨 ) q Roche MagNA Pure Compact Nucleic Acid Isolation Kit I 特徴 : 自動精製 キャリアー RNA 使用せず マグネットビーズ精製
平成 29 年 2 月 6 日 次世代シークエンサー (Next-generation sequencing: NGS) 網羅的病原体検査法手順書 必要な試薬 DNA/RNA 精製キット ( 以下の DNA/RNA 精製試薬を推奨 ) q Roche MagNA Pure Compact Nucleic Acid Isolation Kit I 特徴 : 自動精製 キャリアー RNA 使用せず マグネットビーズ精製
Microsoft Word - ケミストリープロトコル_v5_2012_Final.doc
 GenomeLab GeXP Genetic Analysis System Sequenci Chemistry Protocol シークエンスケミストリープロトコル V.5 1. 反応試薬と消耗品について 1-1. 弊社供給試薬 製品名製品番号保存条件 DTCS クイックスタートキット (100 反応 ) 608120-20 DTCS クイックスタートキットに含まれている試薬キット内の試薬はミネラルオイル以外
GenomeLab GeXP Genetic Analysis System Sequenci Chemistry Protocol シークエンスケミストリープロトコル V.5 1. 反応試薬と消耗品について 1-1. 弊社供給試薬 製品名製品番号保存条件 DTCS クイックスタートキット (100 反応 ) 608120-20 DTCS クイックスタートキットに含まれている試薬キット内の試薬はミネラルオイル以外
DNA Fragmentation Kit
 研究用 DNA Fragmentation Kit 説明書 v201712da 本製品は 超音波破砕装置などの特殊な装置を使用せず 酵素処理によってゲノム DNA 等の長鎖 DNA をランダムに断片化し さらに平滑化するためのキットです 平滑化した断片はそのまま平滑末端ベクターに組み込むことができます また 平滑化を必要としない場合は 断片化までで反応を止めることもできます メチル化 DNA 濃縮や高速シーケンス解析のための前処理にも
研究用 DNA Fragmentation Kit 説明書 v201712da 本製品は 超音波破砕装置などの特殊な装置を使用せず 酵素処理によってゲノム DNA 等の長鎖 DNA をランダムに断片化し さらに平滑化するためのキットです 平滑化した断片はそのまま平滑末端ベクターに組み込むことができます また 平滑化を必要としない場合は 断片化までで反応を止めることもできます メチル化 DNA 濃縮や高速シーケンス解析のための前処理にも
Microsoft PowerPoint - Focus error webinar 本番 RevC
 トラブルシューティング編 : MiSeq でフォーカスエラーが出た! どうしたら良い? July 25, 2014 小林孝史イルミナ株式会社テクニカルサポート部テクニカルアプリケーションサイエンティスト 2014 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse,
トラブルシューティング編 : MiSeq でフォーカスエラーが出た! どうしたら良い? July 25, 2014 小林孝史イルミナ株式会社テクニカルサポート部テクニカルアプリケーションサイエンティスト 2014 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse,
Gen とるくん™(酵母用)High Recovery
 研究用 Gen とるくん ( 酵母用 ) High Recovery 説明書 v201510da Gen とるくん ( 酵母用 )High Recovery は 細胞壁分解酵素による酵母菌体処理と塩析による DNA 精製の組み合わせにより 効率良く酵母ゲノム DNA を抽出 精製するためのキットです 本キットを用いた酵母ゲノム DNA 調製操作は 遠心による酵母菌体の回収 GenTLE Yeast
研究用 Gen とるくん ( 酵母用 ) High Recovery 説明書 v201510da Gen とるくん ( 酵母用 )High Recovery は 細胞壁分解酵素による酵母菌体処理と塩析による DNA 精製の組み合わせにより 効率良く酵母ゲノム DNA を抽出 精製するためのキットです 本キットを用いた酵母ゲノム DNA 調製操作は 遠心による酵母菌体の回収 GenTLE Yeast
Bacterial 16S rDNA PCR Kit
 研究用 Bacterial 16S rdna PCR Kit 説明書 v201307da 微生物の同定は 形態的特徴 生理 生化学的性状 化学分類学的性状などを利用して行われますが これらの方法では同定までに時間を要します また 同定が困難な場合や正しい結果が得られない場合もあります 近年 微生物同定にも分子生物学を利用した方法が採用されるようになり 微生物の持つ DNA を対象として解析を行う方法が活用されています
研究用 Bacterial 16S rdna PCR Kit 説明書 v201307da 微生物の同定は 形態的特徴 生理 生化学的性状 化学分類学的性状などを利用して行われますが これらの方法では同定までに時間を要します また 同定が困難な場合や正しい結果が得られない場合もあります 近年 微生物同定にも分子生物学を利用した方法が採用されるようになり 微生物の持つ DNA を対象として解析を行う方法が活用されています
Slide 1
 RNA-Seq ~ 研究に合わせたアプリケーションの選び方 ~ June 12, 2015 山重りえイルミナ株式会社テクニカルアプリケーションサイエンティスト 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress, cbot, CSPro, DASL, DesignStudio,
RNA-Seq ~ 研究に合わせたアプリケーションの選び方 ~ June 12, 2015 山重りえイルミナ株式会社テクニカルアプリケーションサイエンティスト 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress, cbot, CSPro, DASL, DesignStudio,
はじめてのリアルタイムPCR
 はじめてのリアルタイム PCR 1. はじめにリアルタイム PCR 法は PCR 増幅産物の増加をリアルタイムでモニタリングし 解析する技術です エンドポイントで PCR 増幅産物を確認する従来の PCR 法に比べて 1DNA や RNA の正確な定量ができること 2 電気泳動が不要なので迅速かつ簡便に解析できコンタミネーションの危険性も小さいことなど多くの利点があります 今や 遺伝子発現解析や SNP
はじめてのリアルタイム PCR 1. はじめにリアルタイム PCR 法は PCR 増幅産物の増加をリアルタイムでモニタリングし 解析する技術です エンドポイントで PCR 増幅産物を確認する従来の PCR 法に比べて 1DNA や RNA の正確な定量ができること 2 電気泳動が不要なので迅速かつ簡便に解析できコンタミネーションの危険性も小さいことなど多くの利点があります 今や 遺伝子発現解析や SNP
Microsoft PowerPoint - kobayashi-SAV webinar
 Sequence Analysis Viewer (SAV) で MiSeq の Run 結果を評価する 小林孝史イルミナ株式会社 テクニカルアプリケーションサイエンティスト 2013 Illumina, Inc. All rights reserved. Illumina, IlluminaDx, BaseSpace, BeadArray, BeadXpress, cbot, CSPro, DASL,
Sequence Analysis Viewer (SAV) で MiSeq の Run 結果を評価する 小林孝史イルミナ株式会社 テクニカルアプリケーションサイエンティスト 2013 Illumina, Inc. All rights reserved. Illumina, IlluminaDx, BaseSpace, BeadArray, BeadXpress, cbot, CSPro, DASL,
リアルタイムPCRの基礎知識
 1. リアルタイム PCR の用途リアルタイム PCR 法は 遺伝子発現解析の他に SNPs タイピング 遺伝子組み換え食品の検査 ウイルスや病原菌の検出 導入遺伝子のコピー数の解析などさまざまな用途に応用されている 遺伝子発現解析のような定量解析は まさにリアルタイム PCR の得意とするところであるが プラス / マイナス判定だけの定性的な解析にもその威力を発揮する これは リアルタイム PCR
1. リアルタイム PCR の用途リアルタイム PCR 法は 遺伝子発現解析の他に SNPs タイピング 遺伝子組み換え食品の検査 ウイルスや病原菌の検出 導入遺伝子のコピー数の解析などさまざまな用途に応用されている 遺伝子発現解析のような定量解析は まさにリアルタイム PCR の得意とするところであるが プラス / マイナス判定だけの定性的な解析にもその威力を発揮する これは リアルタイム PCR
QNAP vsphere Client 用プラグイン : ユーザーガイド 2012 年 12 月更新 QNAP Systems, Inc. All Rights Reserved. 1
 QNAP vsphere Client 用プラグイン : ユーザーガイド 2012 年 12 月更新 2012. QNAP Systems, Inc. All Rights Reserved. 1 注意 : 提示する情報は 通知なく変更することがあります 商標 QNAP および QNAP ロゴは QNAP Systems, Inc. の商標です 引用されるすべてのブランド名および製品名は各所有者の商標です
QNAP vsphere Client 用プラグイン : ユーザーガイド 2012 年 12 月更新 2012. QNAP Systems, Inc. All Rights Reserved. 1 注意 : 提示する情報は 通知なく変更することがあります 商標 QNAP および QNAP ロゴは QNAP Systems, Inc. の商標です 引用されるすべてのブランド名および製品名は各所有者の商標です
パナテスト ラットβ2マイクログロブリン
 研究用試薬 2014 年 4 月作成 EIA 法ラット β 2 マイクログロブリン測定キット PRH111 パナテスト A シリーズラット β 2- マイクロク ロフ リン 1. はじめに β 2 - マイクログロブリンは, 血液, 尿, および体液中に存在し, ヒトでは腎糸球体障害, 自己免疫疾患, 悪性腫瘍, 肝疾患などによって血中濃度が変化するといわれています. また,β 2 - マイクログロブリンの尿中濃度は,
研究用試薬 2014 年 4 月作成 EIA 法ラット β 2 マイクログロブリン測定キット PRH111 パナテスト A シリーズラット β 2- マイクロク ロフ リン 1. はじめに β 2 - マイクログロブリンは, 血液, 尿, および体液中に存在し, ヒトでは腎糸球体障害, 自己免疫疾患, 悪性腫瘍, 肝疾患などによって血中濃度が変化するといわれています. また,β 2 - マイクログロブリンの尿中濃度は,
手順 ) 1) プライマーの設計 発注変異導入部位がプライマーのほぼ中央になるようにする 可能であれば 制限酵素サイトができるようにすると確認が容易になる プライマーは 25-45mer で TM 値が 78 以上になるようにする Tm= (%GC)-675/N-%mismatch
 Mutagenesis 目的 ) 既存の遺伝子に PCR を利用して変異を導入する 1 点変異導入方法 ) Quik Change Site-Directed Mutagenesis Kit(Stratagene) のプロトコールを流用 http://www.stratagene.com/products/showproduct.aspx?pid=131 Kit 中では DNA polymerase
Mutagenesis 目的 ) 既存の遺伝子に PCR を利用して変異を導入する 1 点変異導入方法 ) Quik Change Site-Directed Mutagenesis Kit(Stratagene) のプロトコールを流用 http://www.stratagene.com/products/showproduct.aspx?pid=131 Kit 中では DNA polymerase
プロトコール集 ( 研究用試薬 ) < 目次 > 免疫組織染色手順 ( 前処理なし ) p2 免疫組織染色手順 ( マイクロウェーブ前処理 ) p3 免疫組織染色手順 ( オートクレーブ前処理 ) p4 免疫組織染色手順 ( トリプシン前処理 ) p5 免疫組織染色手順 ( ギ酸処理 ) p6 免疫
 < 目次 > 免疫組織染色手順 ( 前処理なし ) p2 免疫組織染色手順 ( マイクロウェーブ前処理 ) p3 免疫組織染色手順 ( オートクレーブ前処理 ) p4 免疫組織染色手順 ( トリプシン前処理 ) p5 免疫組織染色手順 ( ギ酸処理 ) p6 免疫組織染色手順 ( ギ酸処理後 マイクロウェーブまたはオートクレーブ処理 )p7 抗原ペプチドによる抗体吸収試験 p8 ウエスタン ブロッティング
< 目次 > 免疫組織染色手順 ( 前処理なし ) p2 免疫組織染色手順 ( マイクロウェーブ前処理 ) p3 免疫組織染色手順 ( オートクレーブ前処理 ) p4 免疫組織染色手順 ( トリプシン前処理 ) p5 免疫組織染色手順 ( ギ酸処理 ) p6 免疫組織染色手順 ( ギ酸処理後 マイクロウェーブまたはオートクレーブ処理 )p7 抗原ペプチドによる抗体吸収試験 p8 ウエスタン ブロッティング
1-4. 免疫抗体染色 抗体とは何かリンパ球 (B 細胞 ) が作る物質 特定の ( タンパク質 ) 分子に結合する 体の中に侵入してきた病原菌や毒素に結合して 破壊したり 無毒化したりする作用を持っている 例 : 抗血清馬などに蛇毒を注射し 蛇毒に対する抗体を作らせたもの マムシなどの毒蛇にかまれ
 1. 血液細胞の免疫蛍光染色とフローサイトメトリー解析 1-1. フローサイトメトリー ( Flow Cytometory ) とは細胞浮遊液をフローセル内を高速で流し 個々の細胞の形質等についてレーザー光を用いて解析する研究手法 フローサイトメーター( Flow Cytometer ) フローサイトメトリーにおいて使用する細胞解析用の装置今回は BD Accuri C6 を使用する 1-2. フローサイトメーターで何ができるか?
1. 血液細胞の免疫蛍光染色とフローサイトメトリー解析 1-1. フローサイトメトリー ( Flow Cytometory ) とは細胞浮遊液をフローセル内を高速で流し 個々の細胞の形質等についてレーザー光を用いて解析する研究手法 フローサイトメーター( Flow Cytometer ) フローサイトメトリーにおいて使用する細胞解析用の装置今回は BD Accuri C6 を使用する 1-2. フローサイトメーターで何ができるか?
ChIP Reagents マニュアル
 ChIP Reagents ~ クロマチン免疫沈降 (ChIP) 法用ストック溶液セット ~ マニュアル ( 第 1 版 ) Code No. 318-07131 NIPPON GENE CO., LTD. 目次 Ⅰ 製品説明 1 Ⅱ セット内容 1 Ⅲ 保存 2 Ⅳ 使用上の注意 2 Ⅴ 使用例 2 < 本品以外に必要な試薬 機器など> 2 1) 磁気ビーズと一次抗体の反応 3 2)-1 細胞の調製
ChIP Reagents ~ クロマチン免疫沈降 (ChIP) 法用ストック溶液セット ~ マニュアル ( 第 1 版 ) Code No. 318-07131 NIPPON GENE CO., LTD. 目次 Ⅰ 製品説明 1 Ⅱ セット内容 1 Ⅲ 保存 2 Ⅳ 使用上の注意 2 Ⅴ 使用例 2 < 本品以外に必要な試薬 機器など> 2 1) 磁気ビーズと一次抗体の反応 3 2)-1 細胞の調製
Western BLoT Immuno Booster
 研究用 Western BLoT Immuno Booster 説明書 v201211 Western BLoT Immuno Booster は 抗体の反応性を増強させる成分を含む溶液で 抗体の希釈液に用いるだけで 抗原抗体反応を促進します 本製品は ウェスタンブロット ELISA 等の各種イムノアッセイに対応しており 各アッセイにおいて数倍から数十倍の検出感度向上が期待できます 西洋ワサビペルオキシダーゼ
研究用 Western BLoT Immuno Booster 説明書 v201211 Western BLoT Immuno Booster は 抗体の反応性を増強させる成分を含む溶液で 抗体の希釈液に用いるだけで 抗原抗体反応を促進します 本製品は ウェスタンブロット ELISA 等の各種イムノアッセイに対応しており 各アッセイにおいて数倍から数十倍の検出感度向上が期待できます 西洋ワサビペルオキシダーゼ
OpenLAB Data Store Release Notes
 Agilent OpenLAB Data Store バージョン A.02.02 リリースノートおよび更新履歴 注意 Agilent Technologies, Inc. 2014 本マニュアルは米国著作権法および国際著作権法によって保護されており Agilent Technologies, Inc. の書面による事前の許可なく 本書の一部または全部を複製することはいかなる形式や方法 ( 電子媒体による保存や読み出し
Agilent OpenLAB Data Store バージョン A.02.02 リリースノートおよび更新履歴 注意 Agilent Technologies, Inc. 2014 本マニュアルは米国著作権法および国際著作権法によって保護されており Agilent Technologies, Inc. の書面による事前の許可なく 本書の一部または全部を複製することはいかなる形式や方法 ( 電子媒体による保存や読み出し
cDNA cloning by PCR
 cdna cloning/subcloning by PCR 1. 概要 2014. 4 ver.1 by A. Goto & K. Takeda 一般的に 細胞または組織由来の RNA から作製した cdna(cdna pool) から 特定の cdna をベクターに組み込む操作を cdna cloning と呼ぶ その際 制限酵素認識配列を付与したオリゴ DNA primer を用いた PCR
cdna cloning/subcloning by PCR 1. 概要 2014. 4 ver.1 by A. Goto & K. Takeda 一般的に 細胞または組織由来の RNA から作製した cdna(cdna pool) から 特定の cdna をベクターに組み込む操作を cdna cloning と呼ぶ その際 制限酵素認識配列を付与したオリゴ DNA primer を用いた PCR
第 10 回シーケンス講習会 RNA-seq library 調製法の特徴と選び方 理化学研究所 (RIKEN) ライフサイエンス技術基盤研究センター (CLST) 機能性ゲノム解析部門 (DGT) ゲノムネットワーク解析支援施設 (GeNAS) 野間将平
 第 10 回シーケンス講習会 RNA-seq library 調製法の特徴と選び方 理化学研究所 (RIKEN) ライフサイエンス技術基盤研究センター (CLST) 機能性ゲノム解析部門 (DGT) ゲノムネットワーク解析支援施設 (GeNAS) 野間将平 l シーケンスをする目的は? 概略 l よいシーケンスライブラリーとは? RNA-seq ライブラリーのムリ ムダ ムラ l いろいろな RNA-seq
第 10 回シーケンス講習会 RNA-seq library 調製法の特徴と選び方 理化学研究所 (RIKEN) ライフサイエンス技術基盤研究センター (CLST) 機能性ゲノム解析部門 (DGT) ゲノムネットワーク解析支援施設 (GeNAS) 野間将平 l シーケンスをする目的は? 概略 l よいシーケンスライブラリーとは? RNA-seq ライブラリーのムリ ムダ ムラ l いろいろな RNA-seq
改訂履歴 登録 発行 年月日 文書番号 ( 改訂番号 ) 改訂内容 改訂理由 年月日 エンドトキシン簡便法 2 / 9 日本核医学会
 院内製造 PET 薬剤のための簡便なエンドトキシン試験法 ( エンドトキシン簡便法 ) エンドトキシン簡便法 1 / 9 日本核医学会 改訂履歴 登録 発行 年月日 文書番号 ( 改訂番号 ) 改訂内容 改訂理由 年月日 エンドトキシン簡便法 2 / 9 日本核医学会 目次 表紙... 1 改訂履歴... 2 目次... 3 院内製造 PET 薬剤のための簡便なエンドトキシン試験法 ( エンドトキシン簡便法
院内製造 PET 薬剤のための簡便なエンドトキシン試験法 ( エンドトキシン簡便法 ) エンドトキシン簡便法 1 / 9 日本核医学会 改訂履歴 登録 発行 年月日 文書番号 ( 改訂番号 ) 改訂内容 改訂理由 年月日 エンドトキシン簡便法 2 / 9 日本核医学会 目次 表紙... 1 改訂履歴... 2 目次... 3 院内製造 PET 薬剤のための簡便なエンドトキシン試験法 ( エンドトキシン簡便法
Pyrobest ® DNA Polymerase
 Pyrobest DNA Polymerase 説明書 v201102da 対活Pyrobest DNA Polymerase は Pyrococcus sp. 由来の 3' 5' exonuclease 活性 (proof reading 活性 ) を有する耐熱性 α 型 DNA ポリメラーゼです α 型 DNA ポリメラーゼは Pol I 型ポリメラーゼ (Taq DNA ポリメラーゼなど )
Pyrobest DNA Polymerase 説明書 v201102da 対活Pyrobest DNA Polymerase は Pyrococcus sp. 由来の 3' 5' exonuclease 活性 (proof reading 活性 ) を有する耐熱性 α 型 DNA ポリメラーゼです α 型 DNA ポリメラーゼは Pol I 型ポリメラーゼ (Taq DNA ポリメラーゼなど )
MiSeq Reporter Software Overview
 MiSeq を使用した研究計画のご提案 小林孝史 (Takafumi KOBAYASHI, PhD) イルミナ株式会社テクニカルサポート Email:[email protected] 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress, cbot,
MiSeq を使用した研究計画のご提案 小林孝史 (Takafumi KOBAYASHI, PhD) イルミナ株式会社テクニカルサポート Email:[email protected] 2012 Illumina, Inc. All rights reserved. Illumina, illuminadx, BaseSpace, BeadArray, BeadXpress, cbot,
PrimeScript RT reagent Kit (Perfect Real Time)
 製品コード RR037A PrimeScript RT reagent Kit (Perfect Real Time) 説明書 本製品は リアルタイム RT-PCR に最適化された逆転写反応キットです 伸長性能に優れた PrimeScript RTase を使用し短時間の反応で効率良くリアルタイム PCR 用の鋳型 cdna を合成することができます 実験操作も簡単でハイスループットな解析にも適しています
製品コード RR037A PrimeScript RT reagent Kit (Perfect Real Time) 説明書 本製品は リアルタイム RT-PCR に最適化された逆転写反応キットです 伸長性能に優れた PrimeScript RTase を使用し短時間の反応で効率良くリアルタイム PCR 用の鋳型 cdna を合成することができます 実験操作も簡単でハイスループットな解析にも適しています
無細胞タンパク質合成試薬キット Transdirect insect cell
 発現プラスミドの構築 1. インサート DNA の調製開始コドンは出来るだけ 5'UTR に近い位置に挿入して下さい 経験的に ptd1 の EcoRV/KpnI サイトへのライゲーション効率が最も高いことを確認しています 本プロトコルに従うと インサートサイズにも依りますが 90% 以上のコロニーがインサートの挿入されたクローンとして得られます 可能な限り EcoRV/KpnI サイトへ挿入されるお奨めします
発現プラスミドの構築 1. インサート DNA の調製開始コドンは出来るだけ 5'UTR に近い位置に挿入して下さい 経験的に ptd1 の EcoRV/KpnI サイトへのライゲーション効率が最も高いことを確認しています 本プロトコルに従うと インサートサイズにも依りますが 90% 以上のコロニーがインサートの挿入されたクローンとして得られます 可能な限り EcoRV/KpnI サイトへ挿入されるお奨めします
遺伝子検査の基礎知識
 遺伝子検査の準備と注意事項 PCR はわずか 1 分子の鋳型 DNA でも検出可能であるため 反応液調製時に鋳型となりうる核酸等が混入しないように細心の注意が必要です この文書では 正確な遺伝子検査を行うために必要な実験器具類やコンタミネーション防止のための注意事項について解説します - 目次 - 1 実験環境の整備 2 必要な実験器具と装置 1 実験環境の整備 コンタミネーションの原因 PCR は非常に高感度な検出法であるため
遺伝子検査の準備と注意事項 PCR はわずか 1 分子の鋳型 DNA でも検出可能であるため 反応液調製時に鋳型となりうる核酸等が混入しないように細心の注意が必要です この文書では 正確な遺伝子検査を行うために必要な実験器具類やコンタミネーション防止のための注意事項について解説します - 目次 - 1 実験環境の整備 2 必要な実験器具と装置 1 実験環境の整備 コンタミネーションの原因 PCR は非常に高感度な検出法であるため
鳥インフルエンザA(H7N9)ウイルス検出マニュアル(第2版)公開用
 鳥インフルエンザ A(H7N9) ウイルス 検出マニュアル ( 第 2 版 ) 1 目次 1 臨床検体またはウイルス培養液からの RNA の抽出 ( 参考 ) ---------- 3 2 リアルタイム RT-PCR(TaqMan Probe 法 ) による鳥インフルエンザ A(H7N9) ウイルスの検出方法 ---------- 4 3 Conventional RT-PCR 法よる鳥インフルエンザ
鳥インフルエンザ A(H7N9) ウイルス 検出マニュアル ( 第 2 版 ) 1 目次 1 臨床検体またはウイルス培養液からの RNA の抽出 ( 参考 ) ---------- 3 2 リアルタイム RT-PCR(TaqMan Probe 法 ) による鳥インフルエンザ A(H7N9) ウイルスの検出方法 ---------- 4 3 Conventional RT-PCR 法よる鳥インフルエンザ
コメDNA 抽出キット(精米、玄米1 粒スケール)
 食品 環境分析用 コメ DNA 抽出キット ( 精米 玄米 1 粒スケール ) 説明書 v201703da 本キットは未加熱の精米あるいは玄米 1 粒から DNA の調製を行う際に使用します 最終的に回収された DNA 溶液は 直接 PCR 反応などに利用することができ また 制限酵素処理やサブクローニングに使用することもできます 本キットを用いた DNA 調製には 劇物であるフェノールやクロロホルムは使用しません
食品 環境分析用 コメ DNA 抽出キット ( 精米 玄米 1 粒スケール ) 説明書 v201703da 本キットは未加熱の精米あるいは玄米 1 粒から DNA の調製を行う際に使用します 最終的に回収された DNA 溶液は 直接 PCR 反応などに利用することができ また 制限酵素処理やサブクローニングに使用することもできます 本キットを用いた DNA 調製には 劇物であるフェノールやクロロホルムは使用しません
Polycom RealConnect for Microsoft Office 365
 ユーザガイド Polycom RealConnect for Microsoft Office 365 1.0 4 月 2017 年 3725-06676-005 A Copyright 2017, Polycom, Inc. All rights reserved. 本書のいかなる部分も Polycom, Inc. の明示的な許可なしに いかなる目的でも 電子的または機械的などいかなる手段でも 複製
ユーザガイド Polycom RealConnect for Microsoft Office 365 1.0 4 月 2017 年 3725-06676-005 A Copyright 2017, Polycom, Inc. All rights reserved. 本書のいかなる部分も Polycom, Inc. の明示的な許可なしに いかなる目的でも 電子的または機械的などいかなる手段でも 複製
Western BLoT Rapid Detect
 研究用 Western BLoT Rapid Detect 説明書 v201212 Western BLoT Rapid Detect は 標識二次抗体の代わりに独自の IgG Detector(HRP labeled) を利用して一次抗体を検出するウェスタンブロッティング専用の検出試薬キットです 本製品を利用することで 標識二次抗体を用いて検出する従来法ではできなかった迅速検出 高感度検出 シグナルの増強
研究用 Western BLoT Rapid Detect 説明書 v201212 Western BLoT Rapid Detect は 標識二次抗体の代わりに独自の IgG Detector(HRP labeled) を利用して一次抗体を検出するウェスタンブロッティング専用の検出試薬キットです 本製品を利用することで 標識二次抗体を用いて検出する従来法ではできなかった迅速検出 高感度検出 シグナルの増強
遺伝子検査の基礎知識
 リアルタイム PCR(Probe 法 ) 実験ガイドこの文書では Probe 法によるリアルタイム PCR について 蛍光検出の原理や実験操作の流れなどを解説します 実際の実験操作の詳細については 各製品の取扱説明書をご参照ください - 目次 - 1 蛍光検出の原理 2 実験に必要なもの 3 実験操作法 4 結果の解析 1 蛍光検出の原理 サイクリングプローブによる検出系 (Cycleave PCR
リアルタイム PCR(Probe 法 ) 実験ガイドこの文書では Probe 法によるリアルタイム PCR について 蛍光検出の原理や実験操作の流れなどを解説します 実際の実験操作の詳細については 各製品の取扱説明書をご参照ください - 目次 - 1 蛍光検出の原理 2 実験に必要なもの 3 実験操作法 4 結果の解析 1 蛍光検出の原理 サイクリングプローブによる検出系 (Cycleave PCR
Microsoft PowerPoint _webinar_NextSeq500_bcl2fastq2_Use - コピー.pptx
 2014 年 11 月 14 日サポートウェビナー NextSeq 500 から得られる データの FASTQ 変換 - bcl2fastq バージョン 2 ほか イルミナ株式会社バイオインフォマティクスサポートサイエンティスト癸生川絵里 (Eri Kibukawa) 2013 2014 Illumina, Inc. All rights reserved. Illumina, 24sure, IlluminaDx,
2014 年 11 月 14 日サポートウェビナー NextSeq 500 から得られる データの FASTQ 変換 - bcl2fastq バージョン 2 ほか イルミナ株式会社バイオインフォマティクスサポートサイエンティスト癸生川絵里 (Eri Kibukawa) 2013 2014 Illumina, Inc. All rights reserved. Illumina, 24sure, IlluminaDx,
Veritas System Recovery 16 Management Solution Readme
 Veritas System Recovery 16 Management Solution Readme この README について Veritas System Recovery 16 のソフトウェア配信ポリシーのシステム要件 Veritas System Recovery 16 Management Solution のシステム要件 Veritas System Recovery 16 Management
Veritas System Recovery 16 Management Solution Readme この README について Veritas System Recovery 16 のソフトウェア配信ポリシーのシステム要件 Veritas System Recovery 16 Management Solution のシステム要件 Veritas System Recovery 16 Management
目次 IPS 細胞の継代... 3 細胞継代後の培地交換... 5 IPS 細胞の凍結... 6 凍結ストックの解凍... 8 細胞融解後の培地交換 融解後 1 日目 ON-FEEDER IPS 細胞を FEEDER-FREE 条件にて継代する方法 参考資料 AC
 プロトコール フィーダーフリーでのヒト ips 細胞の培養 1 目次 IPS 細胞の継代... 3 細胞継代後の培地交換... 5 IPS 細胞の凍結... 6 凍結ストックの解凍... 8 細胞融解後の培地交換 融解後 1 日目... 10 ON-FEEDER IPS 細胞を FEEDER-FREE 条件にて継代する方法... 11 参考資料... 14 ACIM 培地の調製... 14 0.5X
プロトコール フィーダーフリーでのヒト ips 細胞の培養 1 目次 IPS 細胞の継代... 3 細胞継代後の培地交換... 5 IPS 細胞の凍結... 6 凍結ストックの解凍... 8 細胞融解後の培地交換 融解後 1 日目... 10 ON-FEEDER IPS 細胞を FEEDER-FREE 条件にて継代する方法... 11 参考資料... 14 ACIM 培地の調製... 14 0.5X
HiSeq X System Lab Setup and Site Prep Guide( )
 HiSeq X System Lab Setup and Site Prep Guide 研究目的での使用に限定 診断での使用はできません はじめに 3 配送と設置 4 ラボの生産レイアウトと設計の原理 5 スペース要件 8 ラボ要件 13 電源要件 16 無停電電源装置 (UPS) 17 環境要件 18 装置制御コンピューター 19 ネットワーク要件 20 データ解析と保管要件 22 ユーザーが用意する消耗品および機器
HiSeq X System Lab Setup and Site Prep Guide 研究目的での使用に限定 診断での使用はできません はじめに 3 配送と設置 4 ラボの生産レイアウトと設計の原理 5 スペース要件 8 ラボ要件 13 電源要件 16 無停電電源装置 (UPS) 17 環境要件 18 装置制御コンピューター 19 ネットワーク要件 20 データ解析と保管要件 22 ユーザーが用意する消耗品および機器
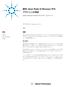
細辛 (Asari Radix Et Rhizoma) 中の アサリニンの測定 Agilent InfinityLab Poroshell 120 EC-C µm カラム アプリケーションノート 製薬 著者 Rongjie Fu Agilent Technologies Shanghai
 細辛 (Asari Radix Et Rhizoma) 中の アサリニンの測定 Agilent InfinityLab Poroshell 2 EC-C8.9 µm カラム アプリケーションノート 製薬 著者 Rongjie Fu Agilent Technologies Shanghai 概要 細辛 (Asari Radix Et Rhizoma) 中の活性化合物アサリニンをサブ 2 µm の Agilent
細辛 (Asari Radix Et Rhizoma) 中の アサリニンの測定 Agilent InfinityLab Poroshell 2 EC-C8.9 µm カラム アプリケーションノート 製薬 著者 Rongjie Fu Agilent Technologies Shanghai 概要 細辛 (Asari Radix Et Rhizoma) 中の活性化合物アサリニンをサブ 2 µm の Agilent
PowerPoint プレゼンテーション
 Oncology Breakthrough ウェビナーシリーズ - 3 がん研究者のための FFPE サンプルからの変異解析 イルミナ株式会社マーケティング本部 2014 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro,
Oncology Breakthrough ウェビナーシリーズ - 3 がん研究者のための FFPE サンプルからの変異解析 イルミナ株式会社マーケティング本部 2014 Illumina, Inc. All rights reserved. Illumina, 24sure, BaseSpace, BeadArray, BlueFish, BlueFuse, BlueGnome, cbot, CSPro,
