<986291E882CC8B4C8E962E786C73>
|
|
|
- さみら あかさか
- 7 years ago
- Views:
Transcription
1 医療機器 海外医療機器便り <7> 生体工学のすすめ鈴木啓介 医療機器 シリーズ 医療機器をめぐる現状と展望 <90> 医療機器イノベーション推進と持続可能なエコシステム構築 -リアル ワールド データからリアル ワールド エビデンスへ- 佐瀬一洋 他 <6> 米国の医療保険制度 州政府の係わり 鈴木啓介 医療機器 シリーズ 医療機器をめぐる現状と展望 <89> 診療報酬改定から見える医療安全 感染防止への新たな対応に 向けて 鍵谷昭典, 野口雄司 <5> MDMA Forum: PMA/510(k) Workshopのレポート 鈴木啓介 医療機器 シリーズ 医療機器をめぐる現状と展望 <88> 医療機器のQMS-ISO13485の統計的手法とサンプルサイズ- 中村雅彦 <4> 米国と日本での承認審査と保険収載の差 鈴木啓介 医療機器 シリーズ 医療機器をめぐる現状と展望 <87> 人工心臓を中心に 山根隆志 <3> 米国での医療機器の保険収載 鈴木啓介 医療機器 シリーズ 医療機器をめぐる現状と展望 <86> 21st Century Cures Act 及び MDUFA IV 下における, 規格活用 に関するUS FDA の取り組み 野澤進 医療機器 シリーズ 医療機器をめぐる現状と展望 <85> 医療機器に係るイノベーションと医療技術の適切な評価に向けて - 特に日本とドイツを比較して- 佐藤智晶 他 医療機器 総説 医療ガスの安全管理について 新見裕一 <2> 海外から見た日本の医療機器審査 -デバイスラグ- 鈴木啓介 医療機器 シリーズ 医療機器をめぐる現状と展望 <84> 造影 CT 検査における医療安全情報の連携の重要性とその取り組み事例紹介 ~CT 用造影剤注入情報を例として~ 野口雄司, 鍵谷昭典 <1> 米国における医療機器関連企業の実際 鈴木啓介 医療機器 シリーズ 医療機器をめぐる現状と展望 <83> リアル ワールド エビデンスと医療機器レジストリ -IMDRFレジストリ分科会における国際整合化の流れと戦略的 レジストリ連携の方法論 - 佐瀬一洋 他 医療機器 総説 経営の視点からみた医療機器 野口雄司 他 医療機器 シリーズ 医療機器をめぐる現状と展望 <82> 医療機器の管理の重要性とその取組み事例紹介 野口雄司, 鍵谷昭典 医療機器シリーズ医療機器をめぐる現状と展望 <81> 医療機器の検証と妥当性確認と QMS 監査中村雅彦 医療機器 シリーズ 医療機器をめぐる現状と展望 <80> 産学官 医工連携による医療イノベーションの最近の動向 - 医療機器やヘルスケアサービスを中心に- 妙中義之 医療機器 総説 放射線部門における感染管理 ( 感染防止対策 ) の必要性と課題 野口雄司, 鍵谷昭典 医療機器 シリーズ 医療機器をめぐる現状と展望 <79> 米国 CDRHの現在と今後の方向性 野澤進 医療機器 シリーズ 医療機器をめぐる現状と展望 <78> 新欧州 MD 規則予想される変更 年 7 月時点 - 藤本安宏, 昌子久仁 子 医療機器 シリーズ 医療機器をめぐる現状と展望 <77> 体外診断用医薬品タイムクロック調査結果と審査迅速化協働 計画への期待 佐藤しのぶ 医療機器 シリーズ 医療機器をめぐる現状と展望 <76> ふくしま医療機器開発支援センター の開所に向けて 大越正弘, 菊地眞 医療機器 シリーズ 医療機器をめぐる現状と展望 <75> 高額医療機器の購入に際して考えるべき税制上の側面と医療 機器の進歩 野口雄司 他 医療機器 総説 医療法の安全確保 - 医療機器の保守点検と感染防止対策 野口雄司, 鍵谷昭典
2 医療機器 総説 医療機器に係るイノベーションと医療技術の適切な評価に向けて - 特に日本とフランスの制度を比較して- 佐藤智晶 他 医療機器 シリーズ 医療機器をめぐる現状と展望 <74> 医療機器を介した健康 医療の更なる分野横断的なイノベーションに向けて - 米国における新しい規制を考える- 大西昭郎 他 医療機器 シリーズ 医療機器をめぐる現状と展望 <73> 戦略的レジストリ連携ネットワークによる次世代医療機器臨床評価システムの構築 - 米国 FDAを中心とした産官学連携 MDEpiNet-PPPからの最新 報告とその日本への影響 - 佐瀬一洋 他 医療機器 シリーズ 医療機器をめぐる現状と展望 <72> 厚生労働省との意見交換を通じた重要テーマとその実現に向けて 野口雄司, 鍵谷昭典 医療機器 シリーズ 医療機器をめぐる現状と展望 <71> 診療報酬上での評価手法におけるイノベーション評価の大きな隔たりと齟齬 - 単なる機器のスペック ( 仕様 ) 性能のみでの点数の階層化は 臨床上有用な議論が欠落している- 野口雄司, 鍵谷昭典 医療機器 シリーズ 医療機器をめぐる現状と展望 <70> 検体検査の価値と課題 ~ 臨床医へのアンケート調査から~ 佐藤しのぶ 医療機器 シリーズ 医療機器をめぐる現状と展望 <69> 薬機法と製造販売業のQMS 中村雅彦 医療機器 シリーズ 医療機器をめぐる現状と展望 <68> 医療機器の研究開発と設立 30 周年を迎える医療機器センター の使命 新見裕一 医療機器 シリーズ 医療機器をめぐる現状と展望 <67> 米国における遺伝子検査に関する規制と課題 野澤恵 医療機器 シリーズ 医療機器をめぐる現状と展望 <66> 医療機器を介した健康 医療の更なる分野横断的なイノベーションに向けて - 遺伝子検査ビジネスの展開を例に- 大西昭郎 他 医療機器 シリーズ 医療機器をめぐる現状と展望 <65> 医療機器関連の中国新法規について 白須理恵, 昌子久仁 子 医療機器 シリーズ 医療機器をめぐる現状と展望 <64> 持続可能なエコシステムとしての分散型レジストリとUDI - 薬事法の改正から国際医療機器レジストリ連携まで- 佐瀬一洋 医療機器 シリーズ 医療機器をめぐる現状と展望 <63> 平成 26 年度診療報酬改定 <2> - 次回改定に向けての新たな課題と取り組みについて- 野口雄司 医療機器 シリーズ 医療機器をめぐる現状と展望 <62> 医薬品医療機器等法による新しい医療機器規制 小泉和夫 医療機器 シリーズ 医療機器をめぐる現状と展望 <61> 単体プログラムの医療機器化 -その位置付けとこれからの 展望 大竹正規 医療機器 シリーズ 医療機器をめぐる現状と展望 <60> アカデミアにおける医療機器開発と製品化に関する現状と展望 中野敦 他 医療機器 シリーズ 医療機器をめぐる現状と展望 <59> 日台連携による医療機器事業化の可能性 ~ 台日医療器材産業シンポジウム の開催とその意義につい て~ 菊地克史 医療機器 シリーズ 医療機器をめぐる現状と展望 <58> 米国におけるヘルスケア分野におけるIT 技術の規制 野澤進 医療機器 シリーズ 医療機器をめぐる現状と展望 <57> 2014 年度診療報酬改定概要 - 特定保険医療材料について- 昌子久仁子 医療機器 シリーズ 医療機器をめぐる現状と展望 <56> 医療機器を介した健康 医療の分野横断的なイノベーションに 向けて - 遺伝子検査ビジネスを例に- 大西昭郎, 佐藤智晶 医療機器 シリーズ 医療機器をめぐる現状と展望 <55> レギュラトリーサイエンスと持続可能な医療機器レジストリ -TAVRレジストリにおけるUDIの活用と日本の貢献- 佐瀬一洋 医療機器 シリーズ 医療機器をめぐる現状と展望 <54> 2014 年度診療報酬改定概要と今後の影響 鍵谷昭典
3 医療機器 シリーズ 医療機器をめぐる現状と展望 <53> 人への初使用を含む初期フィージビリティー試験のIDEについて の米国の新指針 小泉和夫 医療機器 シリーズ 医療機器をめぐる現状と展望 <52> 医療機器の審査迅速化アクションプログラム - 最終年次の検証と新しい協働計画 - 児玉順子 医療機器 シリーズ 医療機器をめぐる現状と展望 <51> 研究医療機関での機器開発拠点化の現況と展望 - 産学連携をともなった知的資産活用の観点から- 赤川英毅 他 医療機器 シリーズ 医療機器をめぐる現状と展望 <50> 医療機器等事業化促進プラットフォーム - 神戸発の医療機器 実用化を目指して- 菊地克史 他 医療機器 シリーズ 医療機器をめぐる現状と展望 <49> わが国アカデミアで加速化する革新的医療機器の開発 永井洋士 他 医療機器 シリーズ 医療機器をめぐる現状と展望 <48> 医療機器のサイバーセキュリティ 野澤進 医療機器 シリーズ 医療機器をめぐる現状と展望 <47> 欧州規制 : 予想される変更 フィン アーツ 他 医療機器 シリーズ 医療機器をめぐる現状と展望 <46> ビッグ データの時代における医療機器安全監視イノベーション -UDIを活用した国際心血管レジストリ連携(ICCR)- 佐瀬一洋 医療機器 シリーズ 医療機器をめぐる現状と展望 <45> 医療機器産業の将来展開 野口雄司, 土居篤博 医療機器 シリーズ 医療機器をめぐる現状と展望 <44> 医療機器を介した健康 医療分野の更なるイノベーションに 向けて 大西昭郎, 佐藤智晶 医療機器 シリーズ 医療機器をめぐる現状と展望 <43> EUの新しい医療機器規制について 小泉和夫 医療機器 シリーズ 医療機器をめぐる現状と展望 <42> C2 保険適用申請の事例から学ぶ包括制度への提言 児玉順子 医療機器 シリーズ 医療機器をめぐる現状と展望 <41> 日本発シーズの実用化について考える 文山日出夫, 菊地克 史 医療機器 シリーズ 医療機器をめぐる現状と展望 <40> 医療 診断機器をNICE( 英国医療技術評価機構 ) はどう評価 するか 妙中義之 他 医療機器 シリーズ 医療機器をめぐる現状と展望 <39> Unique Device Identifier - 流通プロセスの効率化と市販後安全管理 - 野澤進, デニス ブラッ ク 医療機器総説パークドクトリン - エグゼクティブの責任 - 野澤進 医療機器 シリーズ 医療機器をめぐる現状と展望 <38> 中医協費用対効果評価専門部会概要 昌子久仁子 医療機器 シリーズ 医療機器をめぐる現状と展望 <37> 医療機器の市販後安全監視イノベーション -より早く, より安全に, より効率的に- 佐瀬一洋 医療機器 シリーズ 医療機器をめぐる現状と展望 <36> 医療安全 ( 医療機器の安全確保 ) からみた関連法規と診療 報酬制度 ( 追補版 ) 野口雄司 医療機器 総説 医療機器における 薬事戦略相談事業 の現状 石川廣 医療機器 シリーズ 医療機器をめぐる現状と展望 <35> 欧米での保険収載 償還制度における医療機器や医療技術 イノベーションの評価 大西昭郎, 佐藤智晶 医療機器 シリーズ 医療機器をめぐる現状と展望 <34> 米国の510(k) 第三者審査制度 小泉和夫 医療機器 シリーズ 医療機器をめぐる現状と展望 <33> 医療機器の審査迅速化アクションプログラム :3 年次の検証 児玉順子 医療機器 総説 刀根山病院における人工呼吸器のリスクマネージメントについて 藤嵜孝次 医療機器 シリーズ 医療機器をめぐる現状と展望 <32> 阿部健治, 中村雅彦 医療機器 QMS - 製造プロセスのリスクマネジメント 医療機器 シリーズ 医療機器をめぐる現状と展望 <31> 医療機器の早期承認に向けて 山根隆志
4 医療機器 シリーズ 医療機器をめぐる現状と展望 <30> 米国 FDAレギュラトリー リフォーム -IOMレポートとその後- 野澤進 医療機器 シリーズ 医療機器をめぐる現状と展望 <29> 三澤裕, 昌子久仁子 わが国の医療機器産業の現状と展望について 医療機器 シリーズ 医療機器をめぐる現状と展望 <28> 医療機器規制の国際整合化と日米共同試験 共同審査の実践 - 補助人工心臓のレジストリ研究から臨床データの標準化まで- 佐瀬一洋 医療機器 シリーズ 医療機器をめぐる現状と展望 <27> 第 5 回アクションプログラムレビュー部会から医療機器審査の現 状報告及び薬事法制度改正に向けた途中経過報告 佐藤則子 医療機器 シリーズ 医療機器をめぐる現状と展望 <26> 医療機器の改良をめぐる医療機器規制 小林江梨子 他 医療機器 提言 日本における医療機器規制の問題点とその解決に向けて (2011 年 7 月 ) 米国医療機器 IVD 工業会 医療機器 シリーズ 医療機器をめぐる現状と展望 <25> 眼内レンズと特定包括 児玉順子 医療機器 総説 医療安全 ( 医療機器の安全確保 ) からみた関連法規と診療報酬制度 野口雄司 医療機器 シリーズ 医療機器をめぐる現状と展望 <24> 大西昭郎, 佐藤智晶 医療機器に関わる規制の方向性について 医療機器 シリーズ 医療機器をめぐる現状と展望 <23> 臨床工学技士とは 小泉和夫 医療機器 シリーズ 医療機器をめぐる現状と展望 <22> 医療機器と広告規制 中村雅彦 医療機器 シリーズ 医療機器をめぐる現状と展望 <21> 国際整合化活動 (GHTF) におけるUDIについて 石川廣 医療機器 総説 経済産業省の医療機器分野への参入 部材供給の活性化に向けた研究会の検討結果 日吉和彦 医療機器 シリーズ 医療機器をめぐる現状と展望 <20> 医療機器の臨床試験の実施の基準 ( 医療機器 GCP) について 妙中義之 他 医療機器 シリーズ 医療機器をめぐる現状と展望 <19> 医療機器の審査迅速化アクションプログラム : 折り返し地点からの展望 タイムクロック調査 より- 児玉順子 医療機器 シリーズ 医療機器をめぐる現状と展望 <18> 左心補助人工心臓システムの開発 ~ 上市までを振り返って 昌子久仁子 医療機器 総説 わが国における医療機器の特性に応じた不具合評価の現状と課題 笠貫宏 医療機器 シリーズ 医療機器をめぐる現状と展望 <16> 医療機器の臨床評価と国際ハーモナイゼーション -GHTF 及びISOの最新動向からHBDまで- 佐瀬一洋 医療機器 シリーズ 医療機器をめぐる現状と展望 <15> 米国 FDAレギュラトリ リフォームとIVD 業界へのインパクト 野澤進 医療機器 シリーズ 医療機器をめぐる現状と展望 <14> 医療機器 技術の発展の背景 : 革新的医療機器の開発を促す医師の企業家精神 大西昭郎 他 医療機器 総説 医療機器臨床研究の課題と今後 川上浩司 医療機器 座談会 わが国の医療機器をめぐる課題と展望 - 規制と診療報酬を超えて ~1 菊地克史, 佐瀬一 洋, 津田重城 医療機器 シリーズ 医療機器をめぐる現状と展望 <13> 医療機器の製造販売認証 小泉和夫 医療機器 シリーズ 医療機器をめぐる現状と展望 <12> 東北大学未来医工学治療開発センターにおけるトランスレーショ ナルリサーチ 菊地克史 医療機器 総説 APECにおける医療分野 LSIFと規制の整合化活動について 石川廣 医療機器 総説 米国における医療機器の部材等に関する製造物責任の考え方 佐藤智晶 医療機器 シリーズ 医療機器をめぐる現状と展望 <11> 米国 FDAにおけるPMAの臨床データ 中野壮陛 医療機器 シリーズ 医療機器をめぐる現状と展望 <10> 平成 22 年度診療報酬改定と医療機器への影響 菊地克史 医療機器 総説 アジアにおける医療機器規制の整合活動について -AHWP 活動の紹介 - 石川廣
5 医療機器 シリーズ 医療機器をめぐる現状と展望 <9> 米国 FDAにおける510(k) リフォームと最近の規制動向 野澤進 医療機器 総説 医療機器規制における国際整合化活動 (GHTF) について 石川廣 医療機器 シリーズ 医療機器をめぐる現状と展望 <8> 医療機器の研究開発の促進への取り組み : 先端医療開発特区 ( スーパー特区 ) の構築 妙中義之 医療機器 総説 日本における医療機器における添付文書の成り立ち 石川廣 医療機器 シリーズ 医療機器をめぐる現状と展望 <7> 医療機器 ( 特定保険医療材料 ) の保険償還制度について考える 昌子久仁子 医療機器 シリーズ 医療機器をめぐる現状と展望 <6> 医療機器審査のパラダイムシフト : 米国 HDE(Humanitarian Device Extemption) 制度に学ぶ 児玉順子 医療機器 シリーズ 医療機器をめぐる現状と展望 <5> おしゃれ用カラーコンタクトレンズの規制 小泉和夫 医療機器 シリーズ 医療機器をめぐる現状と展望 <4> 医療機器 技術の発展の背景 :1990 年代における欧米の施策の動向 大西昭郎 他 医療機器 シリーズ 医療機器をめぐる現状と展望 <3> 冠動脈インターベンションの発展と医療機器の国際ハーモナイゼーション 佐瀬一洋 医療機器 シリーズ 医療機器をめぐる現状と展望 <2> 医療機器の臨床評価における課題 土井功夫 医療機器 シリーズ 医療機器をめぐる現状と展望 <1> 医療機器の安全確保と診療報酬上の評価 菊地克史, 野口雄司
IMDRFにおけるUDI活動とFDAの動向 国際動向の面からのUDIとは
 IMDRF における UDI 活動と FDA の動向 国際動向の面からの UDI とは 独立行政法人医薬品医療機器総合機構 PMDA 審査マネジメント部薬事戦略相談課 テクニカルエキスパート石川廣 IMDRF と UDI 1 UDI とは何のための UDI 誰のための UDI IMDRF(GHTF) における UDI 活動 米国の状況 欧州の状況 日本の状況 まとめ 本発表は GHTF,IMDRF
IMDRF における UDI 活動と FDA の動向 国際動向の面からの UDI とは 独立行政法人医薬品医療機器総合機構 PMDA 審査マネジメント部薬事戦略相談課 テクニカルエキスパート石川廣 IMDRF と UDI 1 UDI とは何のための UDI 誰のための UDI IMDRF(GHTF) における UDI 活動 米国の状況 欧州の状況 日本の状況 まとめ 本発表は GHTF,IMDRF
医療機器開発マネジメントにおけるチェック項目
 2018 年 11 月作成 医療機器開発マネジメントにおけるチェック項目 1. 各ステージゲートにおけるチェック項目 (1) チェック項目作成の目的従来個々の事業において実施されていた 事前 中間 事後の各ゲートにおける評価項目 Go/no-go の判断を 医療機器開発全期間を通して整理し 共通認識化する 技術的観点及び事業化の観点の双方を意識し 医療機器開発の特性を考慮したチェック項目を設定する
2018 年 11 月作成 医療機器開発マネジメントにおけるチェック項目 1. 各ステージゲートにおけるチェック項目 (1) チェック項目作成の目的従来個々の事業において実施されていた 事前 中間 事後の各ゲートにおける評価項目 Go/no-go の判断を 医療機器開発全期間を通して整理し 共通認識化する 技術的観点及び事業化の観点の双方を意識し 医療機器開発の特性を考慮したチェック項目を設定する
臨床評価とは何か ( 独 ) 医薬品医療機器総合機構医療機器審査第一部方眞美
 臨床評価とは何か ( 独 ) 医薬品医療機器総合機構医療機器審査第一部方眞美 本日の Agenda 1. 臨床評価とは 2. 医療機器の特性を踏まえた有効性 安全性評価 3. 各国の規制の違い 4. 臨床評価報告書について 5. 臨床評価報告書の概念 6. 臨床研究と治験の違いは? 7. 文献評価の問題点 8. 治験活性化にむけて 臨床評価 とは そのものの有効性と安全性をヒトで評価すること 自己認証の欧州から出てきた概念
臨床評価とは何か ( 独 ) 医薬品医療機器総合機構医療機器審査第一部方眞美 本日の Agenda 1. 臨床評価とは 2. 医療機器の特性を踏まえた有効性 安全性評価 3. 各国の規制の違い 4. 臨床評価報告書について 5. 臨床評価報告書の概念 6. 臨床研究と治験の違いは? 7. 文献評価の問題点 8. 治験活性化にむけて 臨床評価 とは そのものの有効性と安全性をヒトで評価すること 自己認証の欧州から出てきた概念
員長及び医薬品医療機器等法登録認証機関協議会代表幹事宛て送付するこ ととしていることを申し添えます 記 1. 基本要件基準第 13 条第 5 項及び第 6 項への適合性確認の基本的な考え方について (1)2023 年 ( 平成 35 年 )2 月 28 日 ( 以下 経過措置期間終了日 という )
 薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
Microsoft Word - 【発送版】製造所の登録通知
 薬食機参発 1003 第 1 号 平成 26 年 10 月 3 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いについて 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業は登録制に移行され
薬食機参発 1003 第 1 号 平成 26 年 10 月 3 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いについて 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業は登録制に移行され
Microsoft PowerPoint 医療機器ビジョン添付資料(差し替え)
 医療機器産業ビジョン 213 資料編 厚生労働省 目次 資料 1. 我が国の医療機器産業の市場規模資料 2. 医療機器の生産 輸出 輸入の現状資料 3. 医療機器の国内売上高に占める輸入額の推移資料 4. 医療機器の輸出入金額の推移資料 5. 治療系機器及び診断系機器の市場規模の推移資料 6. 治療系機器及び診断系機器の輸出 輸入の現状資料 7. 製品分類別の国内売上額と輸入依存度資料 8. 製品分類別の市場規模の推移資料
医療機器産業ビジョン 213 資料編 厚生労働省 目次 資料 1. 我が国の医療機器産業の市場規模資料 2. 医療機器の生産 輸出 輸入の現状資料 3. 医療機器の国内売上高に占める輸入額の推移資料 4. 医療機器の輸出入金額の推移資料 5. 治療系機器及び診断系機器の市場規模の推移資料 6. 治療系機器及び診断系機器の輸出 輸入の現状資料 7. 製品分類別の国内売上額と輸入依存度資料 8. 製品分類別の市場規模の推移資料
セキュリティ委員会活動報告
 2015 年度セキュリティ委員会成果報告 2016 年 2 月 26 日セキュリティ委員会委員長西田慎一郎 ( 島津製作所 ) 1 2015 年度活動内容 1)ISO/TC215 WG4( セキュリティ & プライバシ ) で検討されている国際標準への対応を行った 2) 厚生労働省 医療情報システムの安全管理に関するガイドライン に対して ベンダの立場で取り組みを行った 3) 医療機器におけるサイバーセキュリティへの対応を行った
2015 年度セキュリティ委員会成果報告 2016 年 2 月 26 日セキュリティ委員会委員長西田慎一郎 ( 島津製作所 ) 1 2015 年度活動内容 1)ISO/TC215 WG4( セキュリティ & プライバシ ) で検討されている国際標準への対応を行った 2) 厚生労働省 医療情報システムの安全管理に関するガイドライン に対して ベンダの立場で取り組みを行った 3) 医療機器におけるサイバーセキュリティへの対応を行った
<4D F736F F F696E74202D20322E35208D918DDB88CF88F589EF8A8893AE95F18D905F F42205B8CDD8AB B83685D>
 2013 年度 国際展開とDITTA 活動について国際委員会活動報告 2014 年 6 月 2 日国際委員会委員長内山進 国際委員会活動報告 国際展開と DITTA 活動 2 JIRA 国際活動の基本戦略 会員企業の海外への事業展開推進支援 環境整備 1. 国際画像診断 医療 IT 治療機器産業連合会 (DITTA) による 国際機関や各国 地域へのグローバルな提言活動 DITTA ; Global
2013 年度 国際展開とDITTA 活動について国際委員会活動報告 2014 年 6 月 2 日国際委員会委員長内山進 国際委員会活動報告 国際展開と DITTA 活動 2 JIRA 国際活動の基本戦略 会員企業の海外への事業展開推進支援 環境整備 1. 国際画像診断 医療 IT 治療機器産業連合会 (DITTA) による 国際機関や各国 地域へのグローバルな提言活動 DITTA ; Global
審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果
![審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果 審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果](/thumbs/92/108604766.jpg) 審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
独立行政法人と承認審査の今後
 薬事塾 (2014 年 5 月 ) 医療機器に関する最近の薬事行政について - 薬事法改正を中心に - 2014 年 5 月 10 日 千葉県健康福祉部 古元重和 ( 前厚生労働省医療機器審査管理室長 ) 自己紹介 本日の内容 1. 薬事法改正について 2. 医療機器の審査迅速化に向けた取り組みについて 1. 薬事法改正について 薬事法の改正 ( 概要 ) 薬事法 から 医薬品 医療機器等の品質
薬事塾 (2014 年 5 月 ) 医療機器に関する最近の薬事行政について - 薬事法改正を中心に - 2014 年 5 月 10 日 千葉県健康福祉部 古元重和 ( 前厚生労働省医療機器審査管理室長 ) 自己紹介 本日の内容 1. 薬事法改正について 2. 医療機器の審査迅速化に向けた取り組みについて 1. 薬事法改正について 薬事法の改正 ( 概要 ) 薬事法 から 医薬品 医療機器等の品質
MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1
 MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1 MDSAP 報告書の受入れの概要 (1/2) 日本は 平成 27 年 6 月にMDSAPに参加する旨を発表 関係者との意見交換を行い MDSAP 報告書の受け入れについて 以下の通知を発出した 平成 28 年 6 月 22 日薬生監麻発 0622 第 3 号 薬生機審発 0622
MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1 MDSAP 報告書の受入れの概要 (1/2) 日本は 平成 27 年 6 月にMDSAPに参加する旨を発表 関係者との意見交換を行い MDSAP 報告書の受け入れについて 以下の通知を発出した 平成 28 年 6 月 22 日薬生監麻発 0622 第 3 号 薬生機審発 0622
2 改善命令 1への対応 TIB 審査会は ファーマコビジランス部門が委員長および事務局を務め 営業部門から独立した組織として運営しており 更に 2014 年 4 月より 審査体制の強化を目指し 法的観点から法務部員を メディカルサイエンスの立場からメディカルアフェアーズ部員 ( 医師 ) を委員に
 2015 年 7 月 10 日 武田薬品工業株式会社 厚生労働省発薬食 0612 第 7 号に係る改善命令に対する改善計画 弊社は 2014 年 3 月以降 医療関係者向けの広告資材に関する審査 管理体制を強化してまいりましたが 今般の改善命令を受け 再発防止のため 下記のとおり新たな改善策を実施いたします なお 改善策の実施状況につきましては 今後 定期的に厚生労働省医薬食品局監視指導 麻薬対策課までご報告いたしますとともに
2015 年 7 月 10 日 武田薬品工業株式会社 厚生労働省発薬食 0612 第 7 号に係る改善命令に対する改善計画 弊社は 2014 年 3 月以降 医療関係者向けの広告資材に関する審査 管理体制を強化してまいりましたが 今般の改善命令を受け 再発防止のため 下記のとおり新たな改善策を実施いたします なお 改善策の実施状況につきましては 今後 定期的に厚生労働省医薬食品局監視指導 麻薬対策課までご報告いたしますとともに
< F2D8E9197BF A836F815B2E6A7464>
 ( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
ISO 9001:2015 改定セミナー (JIS Q 9001:2015 準拠 ) 第 4.2 版 株式会社 TBC ソリューションズ プログラム 年版改定の概要 年版の6 大重点ポイントと対策 年版と2008 年版の相違 年版への移行の実務
 ISO 9001:2015 改定セミナー (JIS Q 9001:2015 準拠 ) 第 4.2 版 株式会社 TBC ソリューションズ プログラム 1.2015 年版改定の概要 2.2015 年版の6 大重点ポイントと対策 3.2015 年版と2008 年版の相違 4.2015 年版への移行の実務 TBC Solutions Co.Ltd. 2 1.1 改定の背景 ISO 9001(QMS) ISO
ISO 9001:2015 改定セミナー (JIS Q 9001:2015 準拠 ) 第 4.2 版 株式会社 TBC ソリューションズ プログラム 1.2015 年版改定の概要 2.2015 年版の6 大重点ポイントと対策 3.2015 年版と2008 年版の相違 4.2015 年版への移行の実務 TBC Solutions Co.Ltd. 2 1.1 改定の背景 ISO 9001(QMS) ISO
はじめて医療機器を製造販売または製造される方へ
 を製造 ( 輸入 ) 販売するには 国内で必要な許可等について を製造販売 製造 ( 輸入 ) するためには 医薬品 等の品質 有効性及び安全性の確保等に関する法律 ( 以下 薬機法という ) の許可等 ( 製造販売業許可 製造業登録 ) が必要になります 製品を市場に出荷するために必要な許可 販売する製品に対して最終責製造販売業任を持ち 自社の名前で市場へ出荷する この許可では製造することはできません
を製造 ( 輸入 ) 販売するには 国内で必要な許可等について を製造販売 製造 ( 輸入 ) するためには 医薬品 等の品質 有効性及び安全性の確保等に関する法律 ( 以下 薬機法という ) の許可等 ( 製造販売業許可 製造業登録 ) が必要になります 製品を市場に出荷するために必要な許可 販売する製品に対して最終責製造販売業任を持ち 自社の名前で市場へ出荷する この許可では製造することはできません
本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シ
 医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
Microsoft Word - (発番)医療機器の製造販売承認申請について
 薬食発 1120 第 5 号 平成 26 年 11 月 20 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医療機器の製造販売承認申請について 医療機器の製造販売承認申請の取扱いについては 医療機器の製造販売承認申請について ( 平成 17 年 2 月 16 日付け薬食発第 0216002 号厚生労働省医薬食品局長通知 以下 旧通知 という ) 等により実施してきたところです 先般
薬食発 1120 第 5 号 平成 26 年 11 月 20 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医療機器の製造販売承認申請について 医療機器の製造販売承認申請の取扱いについては 医療機器の製造販売承認申請について ( 平成 17 年 2 月 16 日付け薬食発第 0216002 号厚生労働省医薬食品局長通知 以下 旧通知 という ) 等により実施してきたところです 先般
< F2D819B955C8EA692CA926D DC58F4994AD8F6F>
 薬食監麻発第 0331008 号平成 17 年 3 月 31 日 各都道府県衛生主管部 ( 局 ) 長 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 一部改正法 という ) 第 2 条の規定による改正後の薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 及び関係政省令等の規定に基づく医薬品 医薬部外品 化粧品及び医療機器 (
薬食監麻発第 0331008 号平成 17 年 3 月 31 日 各都道府県衛生主管部 ( 局 ) 長 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 一部改正法 という ) 第 2 条の規定による改正後の薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 及び関係政省令等の規定に基づく医薬品 医薬部外品 化粧品及び医療機器 (
<4D F736F F D2093C192E895578F8089BB8B408AD A8EC08E7B977697CC FC90B394C5816A2E646F6378>
 特定標準化機関 (CSB) 制度実施要領 平成 15 年 8 月 27 日 ( 制定 ) 平成 29 年 3 月 15 日 ( 改正 ) 日本工業標準調査会 標準第一部会 標準第二部会 1. 制度名称 制度名称は 特定標準化機関 (Competent Standardization Body) 制度 ( 通称 シー エ ス ビー制度 ) とする 2. 目的日本工業規格 (JIS) の制定等のための原案作成
特定標準化機関 (CSB) 制度実施要領 平成 15 年 8 月 27 日 ( 制定 ) 平成 29 年 3 月 15 日 ( 改正 ) 日本工業標準調査会 標準第一部会 標準第二部会 1. 制度名称 制度名称は 特定標準化機関 (Competent Standardization Body) 制度 ( 通称 シー エ ス ビー制度 ) とする 2. 目的日本工業規格 (JIS) の制定等のための原案作成
JAB の認定 ~ 最新情報 公益財団法人日本適合性認定協会認定センター
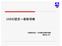 JAB の認定 ~ 最新情報 公益財団法人日本適合性認定協会認定センター JAB のマネジメントシステムと認定システム 地域社会 国際社会 17011 JAB MS 認定システム 認定サービス実現プロセス 規制当局 顧客 MS 認証機関要員認証機関製品認証機関 GHG 妥当性確認 検証機関 試験所臨床検査室検査機関校正機関 組織 産業界 利害関係者ニーズ CB 2 適合性評価の機能と 文書 機関 機能
JAB の認定 ~ 最新情報 公益財団法人日本適合性認定協会認定センター JAB のマネジメントシステムと認定システム 地域社会 国際社会 17011 JAB MS 認定システム 認定サービス実現プロセス 規制当局 顧客 MS 認証機関要員認証機関製品認証機関 GHG 妥当性確認 検証機関 試験所臨床検査室検査機関校正機関 組織 産業界 利害関係者ニーズ CB 2 適合性評価の機能と 文書 機関 機能
J I S J A S O 廃止提案書 1. 対象規格 JASO M 304:02 ( 自動車用発泡体 ) 2. 廃止の背景と理由この規格は自動車用の断熱 防音 防振及びクッション用材料の性能 試験方法を標準化する趣旨で 1969 年に制定され 以後 4 回の改正が行われた なお 本年度の定期見直し
 1. 対象規格 JASO M 304:02 ( 自動車用発泡体 ) 2. 廃止の背景と理由この規格は自動車用の断熱 防音 防振及びクッション用材料の性能 試験方法を標準化する趣旨で 1969 年に制定され 以後 4 回の改正が行われた なお 本年度の定期見直しにおいて この規格の維持要否を確認した結果 現在は各社個別の社内規定での運用 または 2004 年に制定された JIS K6400-1~-8(
1. 対象規格 JASO M 304:02 ( 自動車用発泡体 ) 2. 廃止の背景と理由この規格は自動車用の断熱 防音 防振及びクッション用材料の性能 試験方法を標準化する趣旨で 1969 年に制定され 以後 4 回の改正が行われた なお 本年度の定期見直しにおいて この規格の維持要否を確認した結果 現在は各社個別の社内規定での運用 または 2004 年に制定された JIS K6400-1~-8(
スキル領域 職種 : ソフトウェアデベロップメント スキル領域と SWD 経済産業省, 独立行政法人情報処理推進機構
 スキル領域と (8) ソフトウェアデベロップメント スキル領域と SWD-1 2012 経済産業省, 独立行政法人情報処理推進機構 スキル領域 職種 : ソフトウェアデベロップメント スキル領域と SWD-2 2012 経済産業省, 独立行政法人情報処理推進機構 専門分野 ソフトウェアデベロップメントのスキル領域 スキル項目 職種共通スキル 項目 全専門分野 ソフトウェアエンジニアリング Web アプリケーション技術
スキル領域と (8) ソフトウェアデベロップメント スキル領域と SWD-1 2012 経済産業省, 独立行政法人情報処理推進機構 スキル領域 職種 : ソフトウェアデベロップメント スキル領域と SWD-2 2012 経済産業省, 独立行政法人情報処理推進機構 専門分野 ソフトウェアデベロップメントのスキル領域 スキル項目 職種共通スキル 項目 全専門分野 ソフトウェアエンジニアリング Web アプリケーション技術
QbDを用いた新薬申請の審査とGMP適合性調査 -現状及び課題-
 QbD を用いた新薬申請の 審査と GMP 適合性調査 - 現状及び課題 - 医薬品医療機器総合機構 新薬審査第五部 松田嘉弘 品質管理部 森末政利 審査の視点から 本日の内容 ICH Q8 Q9 Q10 Q11について QbD 申請の状況 審査の事例 審査における課題 調査の視点から GMP 調査とQbD 調査のポイント 調査の事例 QbDが実現すること ICH Q8 Q9 Q10 Q11 について
QbD を用いた新薬申請の 審査と GMP 適合性調査 - 現状及び課題 - 医薬品医療機器総合機構 新薬審査第五部 松田嘉弘 品質管理部 森末政利 審査の視点から 本日の内容 ICH Q8 Q9 Q10 Q11について QbD 申請の状況 審査の事例 審査における課題 調査の視点から GMP 調査とQbD 調査のポイント 調査の事例 QbDが実現すること ICH Q8 Q9 Q10 Q11 について
9100 Key Changes Presentation
 管理者向け資料 注意事項 : この資料は,IAQG の Web サイトに掲載されている 9100 次期改正動向説明資料の 9100 revision 2016 Executive Level Presentation October 2016 を翻訳 / 一部補足したものです 和訳の内容が不明確な場合は原文 ( 英文 ) を参照願います 翻訳 編集 :JAQG 規格検討ワーキンググループ作成 :IAQG
管理者向け資料 注意事項 : この資料は,IAQG の Web サイトに掲載されている 9100 次期改正動向説明資料の 9100 revision 2016 Executive Level Presentation October 2016 を翻訳 / 一部補足したものです 和訳の内容が不明確な場合は原文 ( 英文 ) を参照願います 翻訳 編集 :JAQG 規格検討ワーキンググループ作成 :IAQG
説明項目 1. 審査で注目すべき要求事項の変化点 2. 変化点に対応した審査はどうあるべきか 文書化した情報 外部 内部の課題の特定 リスク 機会 利害関係者の特定 QMS 適用範囲 3. ISO 9001:2015への移行 リーダーシップ パフォーマンス 組織の知識 その他 ( 考慮する 必要に応
 ISO/FDIS 9001 ~ 認証審査における考え方 ~ 2015 年 7 月 14 日 23 日 JAB 認定センター 1 説明項目 1. 審査で注目すべき要求事項の変化点 2. 変化点に対応した審査はどうあるべきか 文書化した情報 外部 内部の課題の特定 リスク 機会 利害関係者の特定 QMS 適用範囲 3. ISO 9001:2015への移行 リーダーシップ パフォーマンス 組織の知識 その他
ISO/FDIS 9001 ~ 認証審査における考え方 ~ 2015 年 7 月 14 日 23 日 JAB 認定センター 1 説明項目 1. 審査で注目すべき要求事項の変化点 2. 変化点に対応した審査はどうあるべきか 文書化した情報 外部 内部の課題の特定 リスク 機会 利害関係者の特定 QMS 適用範囲 3. ISO 9001:2015への移行 リーダーシップ パフォーマンス 組織の知識 その他
<4D F736F F D F193B994AD955C D9E82DD835C EC091D492B28DB8816A2E646F63>
 2007 年 6 月 27 日経済産業省 の概要 経済産業省は 今般 急速に拡大している自動車 携帯電話等に内蔵されているソフトウェア ( 組込みソフトウェア ) に関し その実態を把握するために 組込みソフトウェアに係わる企業 技術者等を対象として調査を行いました その結果 組込みソフトウェア品質の二極化やスキルレベルの高い技術者の不足などの課題が浮き彫りになりました それらを踏まえ 経済産業省では
2007 年 6 月 27 日経済産業省 の概要 経済産業省は 今般 急速に拡大している自動車 携帯電話等に内蔵されているソフトウェア ( 組込みソフトウェア ) に関し その実態を把握するために 組込みソフトウェアに係わる企業 技術者等を対象として調査を行いました その結果 組込みソフトウェア品質の二極化やスキルレベルの高い技術者の不足などの課題が浮き彫りになりました それらを踏まえ 経済産業省では
<90528DB88EBF96E2955B2E786C73>
 4. 品質マネジメントシステム 4.1 一般要求事項 1 組織が品質マネジメントシステムを確立する上で必要としたプロセスは何ですか? 2 営業 / 購買 / 設計のプロセスについて 1このプロセスはどのプロセスと繋がっていますか? また関係していますか? 2このプロセスの役割と目的は何ですか? 3このプロセスの運用 管理の判断基準と 方法は何ですか? 4このプロセスの運用 管理での必要な資源と情報は何ですか?(
4. 品質マネジメントシステム 4.1 一般要求事項 1 組織が品質マネジメントシステムを確立する上で必要としたプロセスは何ですか? 2 営業 / 購買 / 設計のプロセスについて 1このプロセスはどのプロセスと繋がっていますか? また関係していますか? 2このプロセスの役割と目的は何ですか? 3このプロセスの運用 管理の判断基準と 方法は何ですか? 4このプロセスの運用 管理での必要な資源と情報は何ですか?(
ISO13485:2005 と本邦における QMS との違いについて ( いわゆる追加的要求事項と呼ばれる事項について よく質問があります 品質マニュアル ( 品質管 理監督基準書 ) 作成の際に参考になると幸いです 条項ごとに解説を記載しましたので 参考にしてください 追加的要求事項 1: 製造所
 追加的要求事項とは QMS 省令第 3 章 追加的要求事項 とは 製造販売業に要求されていた GQP が QMS に変更されたことに伴って変更された事項と ISO の要求事項との違いを追加的要求事項とされている 条項 第 71 条 背景変更点と背景 管理監督者と管理者の設置 第 65 条 第 66 条 第 69 条 GQP からの変更 製造委託先に対する製造管理 品質管理の管理責任 製造委託先に対する品質管理監督基準の作成の要請
追加的要求事項とは QMS 省令第 3 章 追加的要求事項 とは 製造販売業に要求されていた GQP が QMS に変更されたことに伴って変更された事項と ISO の要求事項との違いを追加的要求事項とされている 条項 第 71 条 背景変更点と背景 管理監督者と管理者の設置 第 65 条 第 66 条 第 69 条 GQP からの変更 製造委託先に対する製造管理 品質管理の管理責任 製造委託先に対する品質管理監督基準の作成の要請
社会的責任に関する円卓会議の役割と協働プロジェクト 1. 役割 本円卓会議の役割は 安全 安心で持続可能な経済社会を実現するために 多様な担い手が様々な課題を 協働の力 で解決するための協働戦略を策定し その実現に向けて行動することにあります この役割を果たすために 現在 以下の担い手の代表等が参加
 私たちの社会的責任 宣言 ~ 協働の力 で新しい公共を実現する~ 平成 22 年 5 月 12 日社会的責任に関する円卓会議 社会的責任に関する円卓会議 ( 以下 本円卓会議 という ) は 経済 社会 文化 生活など 様々な分野における多様な担い手が対等 平等に意見交換し 政府だけでは解決できない諸課題を 協働の力 で解決するための道筋を見出していく会議体として 平成 21 年 3 月に設立されました
私たちの社会的責任 宣言 ~ 協働の力 で新しい公共を実現する~ 平成 22 年 5 月 12 日社会的責任に関する円卓会議 社会的責任に関する円卓会議 ( 以下 本円卓会議 という ) は 経済 社会 文化 生活など 様々な分野における多様な担い手が対等 平等に意見交換し 政府だけでは解決できない諸課題を 協働の力 で解決するための道筋を見出していく会議体として 平成 21 年 3 月に設立されました
untitled
 品質マネジメントシステム - 基本及び用語 JIS Q 9000 :2015 (ISO 9000:2015) (JSA) 平成 27 年 11 月 20 日 改正 日本工業標準調査会審議 ( 日本規格協会発行 ) 日本工業標準調査会標準第一部会適合性評価 管理システム規格専門委員会構成表 氏名 所属 ( 委員会長 ) 棟近雅彦 早稲田大学 ( 委員 ) 阿部 隆 一般社団法人日本鉄鋼連盟 石飛博之
品質マネジメントシステム - 基本及び用語 JIS Q 9000 :2015 (ISO 9000:2015) (JSA) 平成 27 年 11 月 20 日 改正 日本工業標準調査会審議 ( 日本規格協会発行 ) 日本工業標準調査会標準第一部会適合性評価 管理システム規格専門委員会構成表 氏名 所属 ( 委員会長 ) 棟近雅彦 早稲田大学 ( 委員 ) 阿部 隆 一般社団法人日本鉄鋼連盟 石飛博之
Basic Agreement for Marketing Certification Service under PMD Act / 医薬品医療機器法製造販売認証サービス基本合意書
 医薬品医療機器法に基づく製造販売認証サービスを申請されるにあたりご了解いただきたいこと テュフズードジャパン株式会社 MHS 事業部 弊社では 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 以下 医薬品医療機器法又は法 ) に基づく製造販売認証サービスを提供させていただくにあたり 次の各項についてご了解いただくよう全てのお客様にお願いしております 最初のご申請までにこの書面をお読みいただき最終ページに貴社の名称
医薬品医療機器法に基づく製造販売認証サービスを申請されるにあたりご了解いただきたいこと テュフズードジャパン株式会社 MHS 事業部 弊社では 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 以下 医薬品医療機器法又は法 ) に基づく製造販売認証サービスを提供させていただくにあたり 次の各項についてご了解いただくよう全てのお客様にお願いしております 最初のご申請までにこの書面をお読みいただき最終ページに貴社の名称
SGEC 附属文書 理事会 統合 CoC 管理事業体の要件 目次序文 1 適用範囲 2 定義 3 統合 CoC 管理事業体組織の適格基準 4 統合 CoC 管理事業体で実施される SGEC 文書 4 CoC 認証ガイドライン の要求事項に関わる責任の適用範囲 序文
 SGEC 附属文書 2-8 2012 理事会 2016.1.1 統合 CoC 管理事業体の要件 目次序文 1 適用範囲 2 定義 3 統合 CoC 管理事業体組織の適格基準 4 統合 CoC 管理事業体で実施される SGEC 文書 4 CoC 認証ガイドライン の要求事項に関わる責任の適用範囲 序文この文書の目的は 生産拠点のネットワークをする組織によるCoC 認証を実施のための指針を設定し このことにより
SGEC 附属文書 2-8 2012 理事会 2016.1.1 統合 CoC 管理事業体の要件 目次序文 1 適用範囲 2 定義 3 統合 CoC 管理事業体組織の適格基準 4 統合 CoC 管理事業体で実施される SGEC 文書 4 CoC 認証ガイドライン の要求事項に関わる責任の適用範囲 序文この文書の目的は 生産拠点のネットワークをする組織によるCoC 認証を実施のための指針を設定し このことにより
サマリー記載について
 第 64 回 HL7 セミナー HL7 標準規格 退院時サマリー のご紹介 退院時サマリー標準規格 開発検討の経緯 平成 30 年 3 月 豊田建日本 HL7 協会 ( 株式会社 HCI) HL7 CDA について HL7 Clinical Document Architecture (CDA) 文書構造を有する診療情報を記述するためのXMLによる言語 2009 年 11 月 ISO 規格 ISO/HL7
第 64 回 HL7 セミナー HL7 標準規格 退院時サマリー のご紹介 退院時サマリー標準規格 開発検討の経緯 平成 30 年 3 月 豊田建日本 HL7 協会 ( 株式会社 HCI) HL7 CDA について HL7 Clinical Document Architecture (CDA) 文書構造を有する診療情報を記述するためのXMLによる言語 2009 年 11 月 ISO 規格 ISO/HL7
ISO 9001 ISO ISO 9001 ISO ISO 9001 ISO 14001
 ISO 9001 ISO 14001 ISO 9001 ISO 14001 ISO 9001 ISO 14001 ISO 9001 ISO 14001 JAB/ISO 9001 JAB/ISO 14001 2009 ISO 9001 ISO 14001 1,500 797 797 53.1 2009 10 797 125 15.790 11.3 65 8.264 8.0 51 6.4 16 16 7
ISO 9001 ISO 14001 ISO 9001 ISO 14001 ISO 9001 ISO 14001 ISO 9001 ISO 14001 JAB/ISO 9001 JAB/ISO 14001 2009 ISO 9001 ISO 14001 1,500 797 797 53.1 2009 10 797 125 15.790 11.3 65 8.264 8.0 51 6.4 16 16 7
第3章 指導・監査等の実施
 指導 監査等の実施 - 63 - 目次第 1 節 1 事業の体系 65 2 指導監査部事業関連統計 66 第 2 節 1 社会福祉法人 施設 事業等に対する指導検査等 67 2 保険医療機関等に対する指導等 67 3 社会福祉法人の認可等 68 4 社会福祉法人経営力強化事業 68 5 区市町村指導検査支援事業等 69 6 福祉サービス第三者評価制度 69-64 - 第 1 節 1 事業の体系 指導
指導 監査等の実施 - 63 - 目次第 1 節 1 事業の体系 65 2 指導監査部事業関連統計 66 第 2 節 1 社会福祉法人 施設 事業等に対する指導検査等 67 2 保険医療機関等に対する指導等 67 3 社会福祉法人の認可等 68 4 社会福祉法人経営力強化事業 68 5 区市町村指導検査支援事業等 69 6 福祉サービス第三者評価制度 69-64 - 第 1 節 1 事業の体系 指導
PowerPoint プレゼンテーション
 コンパニオン診断の現状 ~ 肺がんを例に ~ 2017 年 7 月 29 日 個別化医療に必要なコンパニオン診断薬 コンパニオン診断薬 ~ 肺癌治療を例に ~ NGS によるコンパニオン診断システム 個別化医療の概念 効果と安全性の両面で優れた治療法として世界的に関心が高まっており 特にがん治療などにおいて 今後の中心的役割を担うものと考えられています 薬剤投与前にバイオマーカーと呼ばれる特定の分子や遺伝子を診断し
コンパニオン診断の現状 ~ 肺がんを例に ~ 2017 年 7 月 29 日 個別化医療に必要なコンパニオン診断薬 コンパニオン診断薬 ~ 肺癌治療を例に ~ NGS によるコンパニオン診断システム 個別化医療の概念 効果と安全性の両面で優れた治療法として世界的に関心が高まっており 特にがん治療などにおいて 今後の中心的役割を担うものと考えられています 薬剤投与前にバイオマーカーと呼ばれる特定の分子や遺伝子を診断し
医師主導治験取扱要覧
 15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
JIS Q 27001:2014への移行に関する説明会 資料1
 JIS Q 27001:2014 への 対応について 一般財団法人日本情報経済社会推進協会情報マネジメント推進センターセンター長高取敏夫 2014 年 10 月 3 日 http://www.isms.jipdec.or.jp/ Copyright JIPDEC ISMS, 2014 1 アジェンダ ISMS 認証の移行 JIS Q 27001:2014 改正の概要 Copyright JIPDEC
JIS Q 27001:2014 への 対応について 一般財団法人日本情報経済社会推進協会情報マネジメント推進センターセンター長高取敏夫 2014 年 10 月 3 日 http://www.isms.jipdec.or.jp/ Copyright JIPDEC ISMS, 2014 1 アジェンダ ISMS 認証の移行 JIS Q 27001:2014 改正の概要 Copyright JIPDEC
鑑-H リンゼス錠他 留意事項通知の一部改正等について
 日医発第 617 号 ( 保 154) 平成 30 年 8 月 29 日 都道府県医師会長殿 日本医師会長横倉義武 医薬品医療機器等法上の効能 効果等の変更に伴う留意事項の一部改正等について 平成 30 年 8 月 21 日付け保医発 0821 第 1 号厚生労働省保険局医療課長通知により 添付資料の通り保険適用上の取扱いに関する留意事項が一部改正されましたのでお知らせ申し上げます 今回の改正は 同日付けで添付資料の医薬品の効能
日医発第 617 号 ( 保 154) 平成 30 年 8 月 29 日 都道府県医師会長殿 日本医師会長横倉義武 医薬品医療機器等法上の効能 効果等の変更に伴う留意事項の一部改正等について 平成 30 年 8 月 21 日付け保医発 0821 第 1 号厚生労働省保険局医療課長通知により 添付資料の通り保険適用上の取扱いに関する留意事項が一部改正されましたのでお知らせ申し上げます 今回の改正は 同日付けで添付資料の医薬品の効能
IAF 活動報告 公益財団法人日本適合性認定協会認定センター
 IAF 活動報告 公益財団法人日本適合性認定協会認定センター 報告項目 IAFの活動 MLA( 相互承認 Multilateral Recognition Arrangement) 2015 IAF 総会報告 ~ 総会 TC( 技術委員会 ) 2 IAF (International Accreditation Forum) 1993 年発足 適合性評価を認定する機関および関係機関の国際組織 マネジメントシステム認証
IAF 活動報告 公益財団法人日本適合性認定協会認定センター 報告項目 IAFの活動 MLA( 相互承認 Multilateral Recognition Arrangement) 2015 IAF 総会報告 ~ 総会 TC( 技術委員会 ) 2 IAF (International Accreditation Forum) 1993 年発足 適合性評価を認定する機関および関係機関の国際組織 マネジメントシステム認証
Microsoft Word (最終) 通知案(基本要件12条2項)
 薬生機審発 0517 第 1 号 平成 29 年 5 月 17 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の基本要件基準第 12 条第 2 項の適用について 薬事法第 41 条第 3 項の規定により厚生労働大臣が定める医療機器の基準の一部を改正する件 ( 平成 26 年厚生労働省告示第 403 号 ) による改正後の 医薬品
薬生機審発 0517 第 1 号 平成 29 年 5 月 17 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の基本要件基準第 12 条第 2 項の適用について 薬事法第 41 条第 3 項の規定により厚生労働大臣が定める医療機器の基準の一部を改正する件 ( 平成 26 年厚生労働省告示第 403 号 ) による改正後の 医薬品
PowerPoint プレゼンテーション
 背景 クリニカル イノベーション ネットワーク (CIN) の背景と概要 資料 3 新しい医薬品 医療機器等の開発に当たっては 世界的にコストが高騰している 特に 医薬品にあっては タフツ大学の試算によると 1 新薬当たり $2,558 million( 約 3,000 億円 ) 要するといわれている (Nov. 18, 2014, Tufts Center for the Study of Drug
背景 クリニカル イノベーション ネットワーク (CIN) の背景と概要 資料 3 新しい医薬品 医療機器等の開発に当たっては 世界的にコストが高騰している 特に 医薬品にあっては タフツ大学の試算によると 1 新薬当たり $2,558 million( 約 3,000 億円 ) 要するといわれている (Nov. 18, 2014, Tufts Center for the Study of Drug
パラダイムシフトブック.indb
 3. 記録管理プログラムの作成記録管理のプログラムとは 組織ごとの記録管理の方針からルール ( 管理規則 実施手順など ) 教育計画 監査基準まで すべてがセットになったものであり 組織における包括的な記録管理の仕組みである この項では ISO15489の考え方をベースに国際標準に基づいた記録管理プログラムとはどのようなものか示す 記録管理のプログラムを作成する場合 先に述べた基本的な記録管理の要求事項
3. 記録管理プログラムの作成記録管理のプログラムとは 組織ごとの記録管理の方針からルール ( 管理規則 実施手順など ) 教育計画 監査基準まで すべてがセットになったものであり 組織における包括的な記録管理の仕組みである この項では ISO15489の考え方をベースに国際標準に基づいた記録管理プログラムとはどのようなものか示す 記録管理のプログラムを作成する場合 先に述べた基本的な記録管理の要求事項
2018 年度事業計画書 Ⅰ 基本方針 1. 健康関連分野を取り巻く環境と直近の動向 健康医療分野が政府の日本再興戦略の重点分野に位置づけられ 健康 医療戦略が策定されるなど 予防や健康管理 生活支援サービスの充実 医療 介護技術の進化などにより 成長分野としてマーケットは大きく拡大することが期待さ
 2018 年度事業計画書 (2018 年 4 月 1 日 ~ 2019 年 3 月 31 日 ) 健康科学ビジネス推進機構 2018 年度事業計画書 Ⅰ 基本方針 1. 健康関連分野を取り巻く環境と直近の動向 健康医療分野が政府の日本再興戦略の重点分野に位置づけられ 健康 医療戦略が策定されるなど 予防や健康管理 生活支援サービスの充実 医療 介護技術の進化などにより 成長分野としてマーケットは大きく拡大することが期待されています
2018 年度事業計画書 (2018 年 4 月 1 日 ~ 2019 年 3 月 31 日 ) 健康科学ビジネス推進機構 2018 年度事業計画書 Ⅰ 基本方針 1. 健康関連分野を取り巻く環境と直近の動向 健康医療分野が政府の日本再興戦略の重点分野に位置づけられ 健康 医療戦略が策定されるなど 予防や健康管理 生活支援サービスの充実 医療 介護技術の進化などにより 成長分野としてマーケットは大きく拡大することが期待されています
JISQ 原案(本体)
 目次 ページ序文 1 1 適用範囲 1 2 引用規格 1 3 用語及び定義 2 4 力量要求事項 2 5 労働安全衛生マネジメントシステム審査員に対する力量要求事項 2 5.1 一般 2 5.2 OH&Sの用語, 原則, プロセス及び概念 2 5.3 組織の状況 2 5.4 リーダーシップ, 働く人の協議及び参加 2 5.5 法的要求事項及びその他の要求事項 2 5.6 OH&Sリスク,OH&S 機会並びにその他のリスク及びその他の機会
目次 ページ序文 1 1 適用範囲 1 2 引用規格 1 3 用語及び定義 2 4 力量要求事項 2 5 労働安全衛生マネジメントシステム審査員に対する力量要求事項 2 5.1 一般 2 5.2 OH&Sの用語, 原則, プロセス及び概念 2 5.3 組織の状況 2 5.4 リーダーシップ, 働く人の協議及び参加 2 5.5 法的要求事項及びその他の要求事項 2 5.6 OH&Sリスク,OH&S 機会並びにその他のリスク及びその他の機会

