<4D F736F F F696E74202D20332E208EA18CB18C7689E693CD8F6F81418EA18CB B8DEC BEF8D8795F18D C982C282A282C42
|
|
|
- ゆりか やまがた
- 5 years ago
- Views:
Transcription
1 治験計画届出 治験中副作用 不具合報告等について 医薬品医療機器総合機構審査マネジメント部審査企画課東京 : 春日寛司大阪 : 御前智子 1
2 本日の内容 1. 薬物及び機械器具等 * の治験届の届出実績について 2. 最近の変更点 薬物の治験届について 薬物の治験中の副作用報告等について 機械器具等の治験中の不具合報告等について 3. 加工細胞等に係る治験について 4. 治験コンビネーション製品に係る治験届及び治験不具合等の報告について 5. 最近のお問い合わせから * 機械器具等 : 機械器具 歯科材料 医療用品及び衛生用品 2
3 本日の内容 1. 薬物及び機械器具等の治験届の届出実績について 3
4 薬物の治験計画届出件数 ( 件数 ) 初回治験届出件数 N 回届出件数 治験届出件数 年度 17 年度 18 年度 19 年度 20 年度 21 年度 22 年度 23 年度 24 年度 25 年度 上記届出件数のうち 医師主導治験の件数は 16 年度 7 件 17 年度 11 件 18 年度 5 件 19 年度 15 件 20 年度 8 件 21 年度 15 件 22 年度 10 件 23 年度 59 件 24 年度 32 件 25 年度 31 件 4
5 国際共同治験届出件数 薬物の国際共同治験の届出推移 n 回治験届件数のうち国際共同治験届出件数 初回治験届件数のうち国際共同治験届出件数 治験計画届出件数全数 ( 初回 +n 回 ) に占める国際共同治験届出件数の割合 年度 20 年度 21 年度 22 年度 23 年度 24 年度 25 年度 初回 3 件 9 件 15 件 28 件 23 件 28 件 23 件 N 回 35 件 73 件 98 件 106 件 98 件 102 件 146 件 割合 7.4% 15.6% 20.2% 21.2% 17.6% 23.4% 28.1% * 国際共同治験 とは 新薬の世界的規模での開発 承認を目指して企画される治験であって 1 つの治験に複数の国の医療機関が参加し 共通の治験実施計画書に基づき 同時並行的に進行する治験をいう 年度 20 年度 21 年度 22 年度 23 年度 24 年度 25 年度 治験届出件数に占める国際共同治験届出件数の割合(%)3
6 薬物の治験届出件数 ( 薬効分類別 ) 医薬品医療機器総合機構 HPより 注 1) 上記件数は初回治験届出件数とN 回治験届出件数を合わせたものである 注 2)[ ] 内の件数は該当薬効分類内の [ ] に記載の詳細項目の件数を示している 6
7 機械器具等の治験計画届出件数 ( 件数 ) 初回届出件数治験届出件数 N 回届出件数 年度 18 年度 19 年度 20 年度 21 年度 22 年度 23 年度 24 年度 25 年度 上記届出件数のうち 医師主導治験の件数は 17 年度 1 件 18 年度 0 件 19 年度 0 件 20 年度 2 件 21 年度 3 件 22 年度 1 件 23 年度 3 件 24 年度 3 件 25 年度 4 件 7
8 本日の内容 2. 最近の変更点 薬物の治験届について 8
9 薬物の治験の計画の届出に関する取り扱いについて Q1 電子媒体は 原則として 1 つの届出毎に XML ファイル用の電子媒体 1 枚 PDF ファイル及び管理情報用の電子媒体 1 枚を提出すること とされていますが XML ファイルと PDF ファイルを 1 枚の電子媒体にまとめることは可能でしょうか? A1 可能です なお まとめて提出する場合 電子媒体のラベルにはファイルの種類を記載する必要はございません 治験の依頼をしようとする者による薬物に係る治験の計画の届出等に関する取扱いについて ( 薬食審査発 0531 第 8 号厚生労働省医薬食品局審査管理課長通知平成 25 年 5 月 31 日 ) 及び当該通知の Q&A 9
10 本日の内容 2. 最近の変更点 薬物の治験中の副作用報告等について 10
11 薬物の治験副作用等報告について 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則第 273 条 治験の依頼をした者又は自ら治験を実施した者は 被験薬について次の各号に掲げる事項を知つたときは それぞれ当該各号に定める期間内にその旨を厚生労働大臣に報告しなければならない ( 中略 ) 3 治験の依頼をした者又は自ら治験を実施した者は 第一項第一号並びに第二号イ及びロに掲げる事項並びに同号イ (1) から (5) までに掲げる症例等の発生であつて当該被験薬等の副作用によるものと疑われるもの又はそれらの使用によるものと疑われる感染症によるもの ( 同号に掲げるものを除く ) について その発現症例一覧等を当該被験薬ごとに 当該被験薬について初めて治験の計画を届け出た日等から起算して一年ごとに その期間の満了後二月以内に厚生労働大臣に報告しなければならない ただし 自ら治験を実施した者が既に製造販売の承認を与えられている医薬品に係る治験を行つた場合又は既に当該被験薬について治験の依頼をした者が治験を行つている場合については この限りでない 11
12 治験中副作用症例報告の報告対象 報告期限について (1) (1) 新有効成分 その他 (2) 以外の治験の場合 予測性 重篤性 国内症例 ( 国内治験 ) 外国症例 ( 外国臨床試 験 外国市販後自発報告 等 ) 予測できない ( 未知 ) 死亡 死亡につながる恐れのある症例 個別 (7 日以内 ) 定期 (1 年ごと ) 個別 (7 日以内 ) 定期 (1 年ごと ) その他重篤な症例個別 (15 日以内 ) 定期 (1 年ごと ) 個別 (15 日以内 ) 定期 (1 年ごと ) 予測できる ( 既知 ) 死亡 死亡につながる恐れのある症例 個別 (15 日以内 ) 定期 (1 年ごと ) 個別 (15 日以内 ) 定期 (1 年ごと ) その他重篤な症例 定期 (1 年ごと ) 定期 (1 年ごと ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則第 273 条第 3 項 ( 平成 24 年 12 月 28 日改正 ) において 治験を依頼した者又は自ら治験を実施した者は 治験中副作用あるいは感染症について その発現症例の一覧を 1 年ごとに報告することが義務づけられた (DSUR) 12
13 治験中副作用症例報告の報告対象 報告期限について (2) (2) 一変治験 ( 用法 用量又は効能 効果の追加 変更又は削除に係るものに限る ) の場合 予測性 重篤性 国内症例 ( 国内治験 ) 外国症例 ( 外国臨床試 験 外国市販後自発報告 等 ) 予測できない ( 未知 ) 死亡 死亡につながる恐れのある症例 個別 (7 日以内 ) 定期 (1 年ごと ) * 定期 (1 年ごと ) その他重篤な症例個別 (15 日以内 ) 定期 (1 年ごと ) * 定期 (1 年ごと ) 予測できる ( 既知 ) 死亡 死亡につながる恐れのある症例 個別 (15 日以内 ) 定期 (1 年ごと ) 定期 (1 年ごと ) その他重篤な症例 定期 (1 年ごと ) 定期 (1 年ごと ) * 既に製造販売の承認を与えられている医薬品について 承認事項の一部の変更 ( 用法 用量又は効能 効果の追加 変更又は削除に係るものに限る ) の申請に係る申請書に添付しなければならない資料の収集を目的とする治験を実施した場合は 外国症例 ( 外国臨床試験 外国市販後自発報告等 ) については 報告することを要しない 副作用報告に関する通知 13
14 治験副作用等症例の定期報告についての留意事項 < 年次報告の起算日 > Q5 年次報告の起算日を初回治験届出日 開発国際誕生日又は国際誕生日以外に設定したい場合 審査マネジメント部審査企画課に相談するとあるが 具体的にはどのようにすればよいか A5 年次報告の起算日を変更する前に 報告起算日の変更願 ( 案 ) を審査マネジメント部審査企画課に提出すること 報告起算日の変更願 ( 案 ) ( 自由形式 ) は 治験成分記号 元の起算日 新しい起算日 起算日を変更する理由 次回の予定調査単位期間 を記載する また 起算日を初回治験届出日 開発国際誕生日又は国際誕生日以外の日に変更した場合は 別紙様式 1 の備考欄にその旨を記載しておくこと 調査単位期間は 起算日 ~ 翌年の起算日 -1 日となりますのでご注意ください 平成 25 年 7 月 1 日付厚生労働省医薬食品局審査管理課事務連絡 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 14
15 治験副作用等症例の定期報告についての留意事項 提出部数及び提出方法 控えが必要な場合 控えが必要な場合には 別途写しを 1 部 (1 社につき 1 部 ) 準備してください また 直接持参 郵送の別に関わらず 控えの返却は郵送により行うこととなるため 送り先を明記し 切手又は信書を送付できる宅配業者の着払い伝票を貼付した封筒を必ず同封してください 治験副作用等定期報告の留意事項 ( 平成 24 年 12 月 28 日付薬食審査発 1228 第 11 号 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について 関連 ) ( 25-toriatsukai_ pdf) 15
16 治験副作用等症例の定期報告についての留意事項 その他留意事項 提出書類 別紙様式 2 国内重篤副作用等症例の発現状況一覧は 副作用がなかった場合にも必要となります 年次報告は ア ) 別紙様式 1 イ ) 別紙様式 2 ウ )DSUR の全てが必要となります 書類不足の場合は受領できませんので ご注意ください 治験副作用等定期報告の留意事項 ( 平成 24 年 12 月 28 日付薬食審査発 1228 第 11 号 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について 関連 ) ( 25-toriatsukai_ pdf) 16
17 治験副作用等症例の定期報告についての留意事項 提出部数及び提出方法 DSUR について 1.(9) 複数の開発がなされている場合について に関し 原則一有効成分ごとに報告することとなっていますが 同日に提出される複数の年次報告において DSUR が同一の場合には DSUR を重複して提出する必要はありません その場合 DSUR の重複提出を行なわない年次報告には 別紙様式 1 の 備考 欄に DSUR は〇〇〇 (DSUR を提出する治験成分記号 ) の年次報告にて提出している DSUR と同一であることから本報告での提出を省略した と記載してください 治験副作用等定期報告の留意事項 ( 平成 24 年 12 月 28 日付薬食審査発 1228 第 11 号 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について 関連 ) ( 25-toriatsukai_ pdf) 17
18 本日の内容 2. 最近の変更点 機械器具等の治験中の不具合報告等について 18
19 機械器具等に係る治験不具合等報告について 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則第 274 条の 2 治験 ( 機械器具等を対象とするものに限る 以下この条及び次条において同じ ) の依頼をした者又は自ら治験を実施した者は 治験の対象とされる機械器具等 ( 以下この条において 被験機器 という ) について次の各号に掲げる事項を知ったときは それぞれ当該各号に定める期間内にその旨を厚生労働大臣に報告しなければならない ( 中略 ) 3 治験の依頼をした者又は自ら治験を実施した者は 第一項第一号並びに第二号イ及びロに掲げる事項 同号イ (1) から (5) までに掲げる症例等の発生であつて当該被験機器等の使用による影響であると疑われるもの又はそれらの使用によるものと疑われる感染症によるもの ( 同号に掲げるものを除く ) 並びに同項第三号に掲げる事項について その発現症例一覧等を当該被験機器ごとに 当該被験機器について初めて治験の計画を届け出た日等から起算して一年ごとに その期間の満了後二月以内に厚生労働大臣に報告しなければならない ただし 自ら治験を実施した者が既に製造販売の承認を与えられている医療機器に係る治験を行つた場合又は既に当該被験機器について治験の依頼をした者が治験を行つている場合については この限りでない 19
20 新医療機器等の治験に係る不具合等の規制当局への報告 予測性重篤性国内症例外国症例 予測できない 死亡 死亡につながるおそれ 個別 ( 7 日以内 ) 個別 ( 7 日以内 ) 定期(1 年ごと ) 個別 ( 7 日以内 ) 個別 ( 7 日以内 ) 定期(1 年ごと ) ( 未知 ) その他重篤 個別 (15 日以内 ) 個別 (15 日以内 ) 定期(1 年ごと ) 個別 (15 日以内 ) 個別 (15 日以内 ) 定期(1 年ごと ) 予測できる 死亡 死亡につながるおそれ 個別 (15 日以内 ) 個別 (15 日以内 ) 定期(1 年ごと ) 個別 (15 日以内 ) 個別 (15 日以内 ) 定期(1 年ごと ) ( 既知 ) その他重篤 なし なし 定期(1 年ごと ) なし なし 定期(1 年ごと ) 不具合 重篤な症例等が発生するおそれ 個別 (7 日 15 日以内 : 局長通知 ) 個別 (30 日以内 ) 定期(1 年ごと ) 個別 (7 日 15 日以内 : 局長通知 ) 個別 (30 日以内 ) 定期(1 年ごと ) ( 注 ) ( ) は 平成 25 年 2 月の省令改正後の制度 施行は 平成 26 年 7 月 1 日 旧制度における症例ごとの個別報告に加え 1 年ごとに定期報告を導入 旧制度における報告対象の不具合は 平成 19 年薬食発第 号通知記の1.(6) に規定 新様式を含む通知 : 平成 25 年 3 月 29 日付薬食発 0329 第 14 号 独立行政法人医薬品医療機器総合機構に対する機械器具等に係る治験不具合等報告について 20
21 効能効果等の一変治験に係る不具合等の規制当局への報告 予測性重篤性国内症例外国症例 予測できない 死亡 死亡につながるおそれ 個別 ( 7 日以内 ) 個別 ( 7 日以内 ) 定期(1 年ごと ) 個別 ( 7 日以内 ) なし 定期(1 年ごと ) ( 未知 ) その他重篤 個別 (15 日以内 ) 個別 (15 日以内 ) 定期(1 年ごと ) 個別 (15 日以内 ) なし 定期(1 年ごと ) 予測できる 死亡 死亡につながるおそれ 個別 (15 日以内 ) 個別 (15 日以内 ) 定期(1 年ごと ) 個別 (15 日以内 ) なし 定期(1 年ごと ) ( 既知 ) その他重篤 なし なし 定期(1 年ごと ) なし なし 定期(1 年ごと ) 不具合 重篤な症例等が発生するおそれ 個別 (7 日 15 日以内 : 局長通知 ) 個別 (30 日以内 ) 定期(1 年ごと ) 個別 (7 日 15 日以内 : 局長通知 ) なし 定期(1 年ごと ) ( 注 ) ( ) は 平成 25 年 2 月の省令改正後の制度 施行は 平成 26 年 7 月 1 日 旧制度における症例ごとの個別報告に加え 1 年ごとに定期報告を導入 未知の外国症例については 市販後安全対策の枠組みにおいて報告された情報を活用 旧制度における報告対象の不具合は 平成 19 年薬食発第 号通知記の1.(6) に規定 新様式を含む通知 : 平成 25 年 3 月 29 日付薬食発 0329 第 14 号 独立行政法人医薬品医療機器総合機構に対する機械器具等に係る治験不具合等報告について 21
22 医療機器の治験不具合等報告の定期報告についての留意事項 平成 25 年 2 月 8 日の法改正により 治験機器不具合等報告の新様式による報告及び治験機器安全性定期報告書の提出が義務づけられました 適用時期 これらの報告は H26 年 7 月 1 日以降に実施された治験から適用となります 改正省令の施行時期に関する経過措置 H26 年 7 月 1 日より前に実施された治験及び実施中の治験並びに H26 年 7 月 1 日より前に治験実施計画書が作成された治験については なお従前 の例によることとされています したがって これら経過措置の対象となる治験に係る不具合等報告書の様式は旧様式で作成いただく必要があり また安全性定期報告の提出は不要です 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則及び医療機器の臨床試験の実施の基準に関する省令の一部を改正する省令の施行について ( 薬食発 0208 第 4 号厚生労働省医薬食品局長平成 25 年 2 月 8 日 ) 22
23 本日の内容 3. 加工細胞等に係る治験について 23
24 加工細胞等に係る治験の計画等の届出等について 治験の計画の届出治験の依頼をしようとする者又は自ら治験を実施しようとする者が 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 ) による改正後の 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 第 80 条の 2 第 2 項及び 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年厚生省令第 1 号 以下 規則 という ) 第 275 条の 2 の規定により 計画を届け出なければならない治験は 再生医療等製品となることが見込まれる加工細胞等 ( 人若しくは動物の細胞に培養その他の加工を施したもの又は人若しくは動物の細胞に導入され これらの体内で発現する遺伝子を含有させたものをいう 以下同じ ) に係る治験であること 加工細胞等に係る治験の計画等の届出の取扱い等について ( 薬食発 0812 第 26 号厚生労働省医薬食品局長平成 26 年 8 月 12 日 ) 24
25 加工細胞等に係る治験の計画等の届出等について 届書は専用の様式が適用されます 機構の HP に様式 PDF 及び治験届入力マニュアル掲載されています 施行の対象 平成 26 年 11 月 25 日以降に届け出る計画届 平成 26 年 11 月 25 日以降に届け出た計画届に係る変更届 終了届 中止届 加工細胞等に係る治験の計画等の届出の取扱い等について ( 薬食発 0812 第 26 号厚生労働省医薬食品局長平成 26 年 8 月 12 日 ) 25
26 加工細胞等に係る治験中の不具合等の報告について 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則第 275 条の 3 治験 ( 加工細胞等を対象とするものに限る 以下この条において同じ ) の依頼をした者又は自ら治験を実施した者は 治験の対象とされる加工細胞等 ( 以下この条において 被験製品 という ) について次の各号に掲げる事項を知つたときは それぞれ当該各号に定める期間内にその旨を厚生労働大臣に報告しなければならない 一次に掲げる症例等の発生のうち 当該被験製品又は外国で使用されている物であつて当該被験製品と構成細胞又は導入遺伝子が同一性を有すると認められるもの ( 以下この条において 当該被験製品等 という ) の使用による影響であると疑われるもの又はそれらの使用によるものと疑われる感染症によるものであり かつ そのような症例等の発生又は発生数 発生頻度 発生条件等の発生傾向が当該被験製品の治験製品概要書 ( 当該被験製品の品質 有効性及び安全性に関する情報等を記載した文書をいう 以下この条において同じ ) から予測できないもの七日イ死亡ロ死亡につながるおそれのある症例 二次に掲げる事項 ( 前号に掲げるものを除く ) 十五日イ次に掲げる症例等の発生のうち 当該被験製品等の使用による影響であると疑われるもの又はそれらの使用によるものと疑われる感染症によるものであり かつ そのような症例等の発生又は発生数 発生頻度 発生条件等の発生傾向が当該被験製品の治験製品概要書から予測できないもの (1) 治療のために病院又は診療所への入院又は入院期間の延長が必要とされる症例 (2) 障害 (3) 障害につながるおそれのある症例 (4)(1) から (3) まで並びに前号イ及びロに掲げる症例に準じて重篤である症例 (5) 後世代における先天性の疾病又は異常ロ前号イ又はロに掲げる症例等の発生のうち 当該被験製品等の使用による影響であると疑われるもの又はそれらの使用によるものと疑われる感染症によるものハ外国で使用されている物であつて被験製品と構成細胞又は導入遺伝子が同一性を有すると認められるものに係る製造 輸入又は販売の中止 回収 廃棄その他保健衛生上の危害の発生又は拡大を防止するための措置の実施ニ当該被験製品等の使用による影響若しくはそれらの使用による感染症によりがんその他の重大な疾病 障害若しくは死亡が発生するおそれがあること 当該被験製品等の使用による影響であると疑われる疾病等若しくはそれらの使用によるものと疑われる感染症の発生数 発生頻度 発生条件等の発生傾向が著しく変化したこと又は当該被験製品等が治験の対象となる疾患に対して効能 効果若しくは性能を有しないことを示す研究報告 三当該被験製品等の不具合の発生であつて 当該不具合によつて第一号イ若しくはロ又は前号イ (1) から (5) までに掲げる症例等が発生するおそれがあるもの ( 前二号に掲げるものを除く ) 三十日 26
27 加工細胞等に係る治験中の不具合等の報告について 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則第 275 条の 3 2 前項の規定にかかわらず 治験の依頼をした者又は自ら治験を実施した者は 当該治験が既に製造販売の承認を与えられている再生医療等製品について法第二十三条の二十五第九項 ( 法第二十三条の三十七第五項において準用する場合を含む ) の規定による承認事項の一部の変更 ( 当該変更が第百三十七条の二十八第四号に該当するものに限る ) の申請に係る申請書に添付しなければならない資料の収集を目的とするものである場合においては 前項第一号並びに第二号イ及びロに掲げる事項のうち 外国で使用されている物であつて当該治験に係る被験製品と構成細胞又は導入遺伝子が同一性を有すると認められるものの使用による影響であると疑われるもの又はそれらの使用によるものと疑われる感染症によるものについては 報告することを要しない 3 治験の依頼をした者又は自ら治験を実施した者は 第一項第一号並びに第二号イ及びロに掲げる事項並びに同号イ (1) から (5) までに掲げる症例等の発生であつて当該被験製品等の使用による影響であると疑われるもの又はそれらの使用によるものと疑われる感染症によるもの ( 同号に掲げるものを除く ) 並びに同項第三号に掲げる事項について その発現症例一覧等を当該被験製品ごとに 当該被験製品について初めて治験の計画を届け出た日等から起算して一年ごとに その期間の満了後二月以内に厚生労働大臣に報告しなければならない ただし 自ら治験を実施した者が既に製造販売の承認を与えられている再生医療等製品に係る治験を行つた場合又は既に当該被験製品について治験の依頼をした者が治験を行つている場合については この限りでない 27
28 加工細胞等に係る治験中の不具合等の報告について 報告上の留意点 再生医療等製品たるコンビネーション製品にあっては 薬物又は機械器具の影響による有害事象の発生が疑われる場合も 報告の対象となります 生物由来の原料若しくは材料又はそれらの原材料からの病原体等の混入も報告の対象となります 施行の対象と報告方法 平成 26 年 11 月 25 日以降に届け出る計画届が対象 平成 26 年 11 月 25 日以前に報告された不具合等報告については 当該治験に係る再生医療等製品の承認を受け 又は開発を中止するまでの間は 改正省令による改正前の薬事法施行規則第 273 条又は第 274 条の 2 の規定に基づく報告を行うこと 施行前に届出た薬物又は機械器具等の治験の報告と重複する場合は 重複しての報告は不要とすること なお 平成 26 年 11 月 25 日以前に報告された不具合等報告について 複数回目の報告をする場合は 初回の方法によること 加工細胞等に係る治験中の不具合等の報告について ( 薬食発 1002 第 23 号厚生労働省医薬食品局長平成 26 年 10 月 2 日 ) 28
29 加工細胞等に係る治験中の不具合等の報告について 予測性重篤性国内症例外国症例 予測できない ( 未知 ) 死亡 死亡につながるおそれ 個別 ( 7 日以内 ) 定期 (1 年ごと ) 個別 ( 7 日以内 ) 定期 (1 年ごと ) その他重篤個別 (15 日以内 ) 定期 (1 年ごと ) 個別 (15 日以内 ) 定期 (1 年ごと ) 予測できる ( 既知 ) 死亡 死亡につながるおそれ 個別 (15 日以内 ) 定期 (1 年ごと ) 個別 (15 日以内 ) 定期 (1 年ごと ) その他重篤なし 定期 (1 年ごと ) なし 定期 (1 年ごと ) 不具合 重篤な症例等が発生するおそれ 個別 (30 日以内 ) 定期 (1 年ごと ) 個別 (30 日以内 ) 定期 (1 年ごと ) 29
30 本日の内容 4. 治験コンビネーション製品に係る治験の計画の届出及び治験中副作用又は不具合の報告について 30
31 治験コンビネーション製品に係る治験の計画の届出及び治験中副作用又は不具合の報告について 5 治験の計画の届出並びに副作用及び不具合の取扱いについて (1) 製造販売された際にコンビネーション製品に該当すると考えられるもの ( 以下この項において 治験コンビネーション製品 という ) について 治験の計画を届け出ようとする場合は 備考欄に コンビネーション製品に関する治験 と記載した上で 薬物 機械器具又は加工細胞等のいずれかとして一の治験の計画を届け出ること (2) (1) にかかわらず 治験コンビネーション製品を構成する薬物等の評価を別途行おうとする場合等は 治験コンビネーション製品に係る治験の計画に加えて 治験コンビネーション製品を構成する薬物等に係る治験の計画について届け出ることを妨げるものではないこと その場合 治験計画届の備考欄には 別途届け出る治験に係る届出年月日 届出回数及び治験成分記号又は治験識別記号を 相互に記載すること なお 治験コンビネーション製品及び治験コンビネーション製品を構成する薬物等の治験の計画を届け出る者は 別の者であっても差し支えないこと コンビネーション製品の承認申請における取扱いについて ( 薬食審査発 1024 第 2 号薬食機参発 1024 第 1 号薬食安発 1024 第 9 号薬食監麻発 1024 第 15 号厚生労働省医薬食品局審査管理課長厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) 厚生労働省医薬食品局安全対策課長厚生労働省医薬食品局監視指導 麻薬対策課長平成 26 年 10 月 24 日 ) 31
32 治験コンビネーション製品に係る治験の計画の届出及び治験中副作用又は不具合の報告について 5 治験の計画の届出並びに副作用及び不具合の取扱いについて (3) 治験中の副作用又は不具合の報告については 治験コンビネーション製品の治験の計画を届け出た者が行うこと ただし (2) の場合にあっては 治験コンビネーション製品に係る副作用又は不具合 ( 治験コンビネーション製品を構成する薬物等に係る副作用又は不具合を除く ) にあっては当該治験コンビネーション製品の治験の計画を届け出た者が 治験コンビネーション製品を構成する薬物等に係る副作用又は不具合にあっては 当該薬物等に係る治験の計画を届け出た者が行うこと コンビネーション製品の承認申請における取扱いについて ( 薬食審査発 1024 第 2 号薬食機参発 1024 第 1 号薬食安発 1024 第 9 号薬食監麻発 1024 第 15 号厚生労働省医薬食品局審査管理課長厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) 厚生労働省医薬食品局安全対策課長厚生労働省医薬食品局監視指導 麻薬対策課長平成 26 年 10 月 24 日 ) 32
33 本日の内容 5. 最近のお問い合わせから 33
34 1. 治験副作用等症例の定期報告についてのお問い合わせ Q1: グローバルで DSUR を作成していないので 提出を免除してもらえないか A1: 不可 DSUR 提出の免除規定はないので 作成して提出していただきたい Q2:DSUR の添付資料 (Appendix) のページ数が多く 一冊のファイルに綴れないため 紙資料の提出を電子媒体の提出に代えることは可能か A2:DSURの添付資料部分を電子媒体の提出に代えることは可能であるが DSUR 本体の紙資料での提出は必須である なお 電子媒体を提出する場合 DSUR 本体と添付資料のファイルを分割せずDUSR として一のファイルとして提出することで差し支えない 34
35 2. 留保解除についてのお問い合わせ Q1: 以前に治験副作用等報告の留保申出書を出しており 今回開発中止届を提出予定だが 留保解除の申出書は必要か A1: 必要である 開発中止届を出すより以前に 留保解除の申出書を提出すること Q2: 留保解除申出書を提出するにあたり 留保期間中の発現状況一覧において 報告回数はどう記入すればよいか A2: 定期報告の様式を用いるが 定期報告ではないので報告回数欄は空欄とすること 35
36 2. 留保解除についてのお問い合わせ Q3: 留保解除申出書を提出するにあたり 留保期間中の発現状況一覧において 定期報告の様式を用いるとのことであるが 調査単位期間はどのように設定するのか A3: 留保申出書を提出する直前に報告した定期報告の調査単位期間の翌日以降 留保解除申出書を提出する直近の調査単位期間の末日までとなる ただし DSUR については ICH E2F の DSUR のガイドライン 治験安全性最新報告について ( 薬食審査発 1228 第 1 号厚生労働省医薬食品局審査管理課長平成 24 年 12 月 28 日 ) の趣旨を鑑み 直近 1 年分の DSUR を提出することで差し支えない 36
37 3. 治験計画届書等の様式についてのお問い合わせ Q1: 局長通知の別紙様式又は課長通知の別紙様式 1( 開発中止届書 ) により届け出る場合には 事前に機構審査マネジメント部審査企画課に相談すること とあるが 具体的な手続きを教えてほしい A1: 届書は原則として 電子媒体の内容を紙に出力し 社印等を捺印した書面により届け出ることとされている 原則に沿った対応が困難である場合は その理由を当課に連絡すること 37
38 4. 治験から引き続き 承認後市販薬が提供可能になるまで薬剤を提供することはできる?(1/3) 臨床試験を治験として実施できるのは 承認日まで 以下の臨床試験は 承認後も治験から製造販売後臨床試験又は特定使用成績調査 ( 以下製販後臨床試験等 ) に切り替えて実施することが考えられる ( 医薬審第 1061 号厚生省医薬安全局審査管理課長通知 平成 10 年 12 月 1 日 ) ⅰ) 抗悪性腫瘍薬の第 Ⅲ 相試験 ( 予備試験 (Ⅰ-Ⅱ) を含む ) を承認前から実施する場合 ⅱ) 致命的でない疾患の長期投与ガイドラインに基づく試験の継続 ⅲ) 重篤な疾患に対する治療薬等の試験の継続 ⅳ) その他 患者で血中薬物動態を調べる試験等 38
39 4. 治験から引き続き 承認後市販薬が提供可能になるまで薬剤を提供することはできる?(2/3) 治験を製販後臨床試験等に切り替える場合の注意点 1 治験から製販後臨床試験等に切り替える場合は あらかじめその旨とその理由を治験計画届及び治験実施計画書に記載しておくこと ➁ 医療機関に対して あらかじめ以下の対応を取っておくこと 治験と製販後臨床試験等で経費の算出基準 健康被害の補償の範囲が異なる場合には 医療機関に十分説明する 治験を承認後も製販後臨床試験等として継続すること ( 実施計画書の読み替えもしくは改訂 説明文書の改訂 必要に応じ費用の負担及び健康被害の補償等の文書も含む ) について IRB の承認を得る 承認後は 治験 を 製販後臨床試験等 に読み替える との契約を締結する 39
40 4. 治験から引き続き 承認後市販薬が提供可能になるまで薬剤を提供することはできる?(3/3) 治験を製販後臨床試験等に切り替える場合の注意 ( 続き ) 3 薬剤について承認後製販後臨床試験等として実施する場合 原則治験薬は製販後臨床試験薬表示の薬剤に切り替えること 4 被験者の同意製販後臨床試験では IRB にて承認された説明文書を用いて再同意が必要である 40
41 ご清聴ありがとうございました 41
別添 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について < 半年ごとの定期報告の受け付け> Q1 平成 26 年 6 月 30 日までの間は 治験依頼者 ( 自ら治験を実施する者を除く ) が提出する副作用等症例の定期報告は なお従前の例によることができる とあるが 平成 26 年
 事務連絡 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局審査管理課 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 第 273 条第 3 項に基づく治験副作用等定期報告については 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について ( 平成 24 年
事務連絡 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局審査管理課 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 第 273 条第 3 項に基づく治験副作用等定期報告については 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について ( 平成 24 年
医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年
![医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年 医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年](/thumbs/91/107149459.jpg) 事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
医師主導治験取扱要覧
 9. 安全性情報の取扱いに関する手順書 1. 目的及び適用範囲 本手順書は 安全性情報の取扱いに係る用語の定義を定め 当該治験に関与する者が 安全性情報を適 切に取扱うための手順その他必要な事項を定めるものである 2. 用語の定義等 2.1. 用語の定義 2.1.1. 治験責任医師等 本手順書は 自ら治験を実施する者を 治験責任医師 と記載し また 治験責任医師及び治験分担医師 を併せて 治験責任医師等
9. 安全性情報の取扱いに関する手順書 1. 目的及び適用範囲 本手順書は 安全性情報の取扱いに係る用語の定義を定め 当該治験に関与する者が 安全性情報を適 切に取扱うための手順その他必要な事項を定めるものである 2. 用語の定義等 2.1. 用語の定義 2.1.1. 治験責任医師等 本手順書は 自ら治験を実施する者を 治験責任医師 と記載し また 治験責任医師及び治験分担医師 を併せて 治験責任医師等
Microsoft Word - 奈良県GQP-GVPガイドライン doc
 三. 安全確保措置の実施に関する手順 1. 目的安全確保措置の実施に関する手順の目的を記載する < 記載例 > 本手順は GVP 省令の第 9 条に基づき 安全確保措置の実施を適正かつ円滑に行うために必要な手順を定めるものである 2. 適用範囲安全確保措置の実施に関する手順の適用範囲を記載する < 記載例 > 本手順書は 二. 安全管理情報の検討及びその結果に基づく安全確保措置の立案に関する手順 で立案された安全確保措置の決定
三. 安全確保措置の実施に関する手順 1. 目的安全確保措置の実施に関する手順の目的を記載する < 記載例 > 本手順は GVP 省令の第 9 条に基づき 安全確保措置の実施を適正かつ円滑に行うために必要な手順を定めるものである 2. 適用範囲安全確保措置の実施に関する手順の適用範囲を記載する < 記載例 > 本手順書は 二. 安全管理情報の検討及びその結果に基づく安全確保措置の立案に関する手順 で立案された安全確保措置の決定
員長及び医薬品医療機器等法登録認証機関協議会代表幹事宛て送付するこ ととしていることを申し添えます 記 1. 基本要件基準第 13 条第 5 項及び第 6 項への適合性確認の基本的な考え方について (1)2023 年 ( 平成 35 年 )2 月 28 日 ( 以下 経過措置期間終了日 という )
 薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
Microsoft Word - 【案1】登録認証機関立入要領改正通知(Ver )
 薬食機参発 1121 第 38 号平成 26 年 11 月 21 日 各登録認証機関の長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) 登録認証機関等に対する立入検査の実施要領の改正について 薬事法 ( 昭和 35 年法律第 145 号 ) の規定による登録認証機関等に対する立入 検査の実施要領については 登録認証機関等に対する立入検査の実施要領について ( 平成 18
薬食機参発 1121 第 38 号平成 26 年 11 月 21 日 各登録認証機関の長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) 登録認証機関等に対する立入検査の実施要領の改正について 薬事法 ( 昭和 35 年法律第 145 号 ) の規定による登録認証機関等に対する立入 検査の実施要領については 登録認証機関等に対する立入検査の実施要領について ( 平成 18
管下関係業者に周知いただくとともに 適切な指導を行い その実施に遺漏な きようお願いいたします 記 第 1 体外診断用医薬品の製造販売業又は製造業を行う旨の届出等について 1. 届出対象者旧薬事法に基づき 体外診断用医薬品を取り扱う以下の者 (1) 旧薬事法第 12 条第 1 項の第二種医薬品製造販
 薬食機参発 0 8 2 1 第 1 号 薬食安発 0 8 2 1 第 1 号 平成 2 6 年 8 月 2 1 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 厚生労働省医薬食品局安全対策課長 ( 公印省略 ) 体外診断用医薬品の製造販売業又は製造業を行う旨の届出等について 薬事法等の一部を改正する法律 ( 平成
薬食機参発 0 8 2 1 第 1 号 薬食安発 0 8 2 1 第 1 号 平成 2 6 年 8 月 2 1 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 厚生労働省医薬食品局安全対策課長 ( 公印省略 ) 体外診断用医薬品の製造販売業又は製造業を行う旨の届出等について 薬事法等の一部を改正する法律 ( 平成
本日の内容 1. 未承認対照薬等の取り扱い別添の 4.(3) ウ.( ア ) 2. 対象疾患の悪化等を評価項目にする試験別添の 7.(3) イ.( ア ) 3. 承認取得者以外の治験国内管理人が治験 依頼者となる場合別添の7.(3) オ. 4. 医師主導治験との情報共有別添の7.(3) カ. 5.
 治験の安全性対応シンポジウム 安全性二課長通知の改訂点平成 25 年 5 月 15 日付二課長通知 ( 薬食審査発 0515 第 1 号 薬食安発 0515 第 1 号 ) 2013 年 12 月 16 日 日本製薬工業協会医薬品評価委員会臨床評価部会五十嵐元 山城恭子 1 本日の内容 1. 未承認対照薬等の取り扱い別添の 4.(3) ウ.( ア ) 2. 対象疾患の悪化等を評価項目にする試験別添の
治験の安全性対応シンポジウム 安全性二課長通知の改訂点平成 25 年 5 月 15 日付二課長通知 ( 薬食審査発 0515 第 1 号 薬食安発 0515 第 1 号 ) 2013 年 12 月 16 日 日本製薬工業協会医薬品評価委員会臨床評価部会五十嵐元 山城恭子 1 本日の内容 1. 未承認対照薬等の取り扱い別添の 4.(3) ウ.( ア ) 2. 対象疾患の悪化等を評価項目にする試験別添の
Microsoft Word - 【発送版】製造所の登録通知
 薬食機参発 1003 第 1 号 平成 26 年 10 月 3 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いについて 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業は登録制に移行され
薬食機参発 1003 第 1 号 平成 26 年 10 月 3 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いについて 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業は登録制に移行され
薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リ
 薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リスク管理計画の実施状況及び得られた結果の評価に関する報告の様式 提出等の取扱いについては 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について
薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リスク管理計画の実施状況及び得られた結果の評価に関する報告の様式 提出等の取扱いについては 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について
Microsoft Word - (発番)医療機器の製造販売承認申請について
 薬食発 1120 第 5 号 平成 26 年 11 月 20 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医療機器の製造販売承認申請について 医療機器の製造販売承認申請の取扱いについては 医療機器の製造販売承認申請について ( 平成 17 年 2 月 16 日付け薬食発第 0216002 号厚生労働省医薬食品局長通知 以下 旧通知 という ) 等により実施してきたところです 先般
薬食発 1120 第 5 号 平成 26 年 11 月 20 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医療機器の製造販売承認申請について 医療機器の製造販売承認申請の取扱いについては 医療機器の製造販売承認申請について ( 平成 17 年 2 月 16 日付け薬食発第 0216002 号厚生労働省医薬食品局長通知 以下 旧通知 という ) 等により実施してきたところです 先般
Microsoft Word - 【発送版】記載整備通知
 薬食機参発 0929 第 1 号 平成 26 年 9 月 29 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の承認書又は認証書の記載整備について 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業が登録制に移行されること等に伴い
薬食機参発 0929 第 1 号 平成 26 年 9 月 29 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の承認書又は認証書の記載整備について 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業が登録制に移行されること等に伴い
Microsoft Word - (発出)マル製通知案
 薬食機参発 1119 第 7 号 薬食監麻発 1119 第 12 号 平成 26 年 11 月 19 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 厚生労働省医薬食品局監視指導 麻薬対策課長 ( 公印省略 ) 医療機器及び体外診断用医薬品の製造所の変更又は追加に係る手続 の迅速化について 医療機器及び体外診断用医薬品の製造所の変更に係る手続きの迅速化については
薬食機参発 1119 第 7 号 薬食監麻発 1119 第 12 号 平成 26 年 11 月 19 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 厚生労働省医薬食品局監視指導 麻薬対策課長 ( 公印省略 ) 医療機器及び体外診断用医薬品の製造所の変更又は追加に係る手続 の迅速化について 医療機器及び体外診断用医薬品の製造所の変更に係る手続きの迅速化については
前項に規定する事項のうち当該被験薬の治験薬概要書から予測できないもの に改め 同項を同条第三項とし 同条第一項の次に次の一項を加える 2治験依頼者は 被験薬について法第八十条の二第六項に規定する事項を知ったときは その発現症例一覧等を当該被験薬ごとに 当該被験薬について初めて治験の計画を届け出た日等
 厚生労働省令第二十四号薬事法(昭和三十五年法律第百四十五号)第十四条第三項(同条第九項及び同法第十九条の二第五項において準用する場合を含む ) 第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む ) 第八十条の二第一項 第四項及び第五項並びに第八十二条の規定に基づき 医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十年二月二十九日厚生労働大臣舛添要一医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令医薬品の臨床試験の実施の基準に関する省令(平成九年厚生省令第二十八号)の一部を次のように改正する
厚生労働省令第二十四号薬事法(昭和三十五年法律第百四十五号)第十四条第三項(同条第九項及び同法第十九条の二第五項において準用する場合を含む ) 第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む ) 第八十条の二第一項 第四項及び第五項並びに第八十二条の規定に基づき 医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十年二月二十九日厚生労働大臣舛添要一医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令医薬品の臨床試験の実施の基準に関する省令(平成九年厚生省令第二十八号)の一部を次のように改正する
法律 出典 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年 8 月 10 日法律第 145 号 ) 政令 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行令 ( 昭和 36 年 1 月 26 日政令第 11 号 ) 省令 医薬品 医療機器等の品質
 医療機器クラス分類表 ( 平成 30 年 10 月 19 日現在 ) 香川県健康福祉部薬務感染症対策課薬事指導グループ 法律 出典 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年 8 月 10 日法律第 145 号 ) 政令 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行令 ( 昭和 36 年 1 月 26 日政令第 11 号 ) 省令 医薬品
医療機器クラス分類表 ( 平成 30 年 10 月 19 日現在 ) 香川県健康福祉部薬務感染症対策課薬事指導グループ 法律 出典 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年 8 月 10 日法律第 145 号 ) 政令 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行令 ( 昭和 36 年 1 月 26 日政令第 11 号 ) 省令 医薬品
医療機器プログラムの取扱いに関する Q&A について ( その 2) ( 別紙 ) 用いた略語 改正法 : 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 ) 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行令
 事務連絡平成 27 年 9 月 30 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局医療機器 再生医療等製品担当参事官室 厚生労働省医薬食品局監視指導 麻薬対策課 医療機器プログラムの取扱いに関する Q&A について ( その 2) 医療機器プログラムの取扱いについては 医療機器プログラムの取扱いについて ( 平成 26 年 11 月 21 日付け薬食機参発 1121 第
事務連絡平成 27 年 9 月 30 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局医療機器 再生医療等製品担当参事官室 厚生労働省医薬食品局監視指導 麻薬対策課 医療機器プログラムの取扱いに関する Q&A について ( その 2) 医療機器プログラムの取扱いについては 医療機器プログラムの取扱いについて ( 平成 26 年 11 月 21 日付け薬食機参発 1121 第
PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1
 薬生発 07 31 第 4 号 平成 29 年 7 月 31 日 各都道府県知事殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則の一部を改正する省令 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令の一部を改正する省令 及び 医療機器の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令
薬生発 07 31 第 4 号 平成 29 年 7 月 31 日 各都道府県知事殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則の一部を改正する省令 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令の一部を改正する省令 及び 医療機器の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令
< F2D CFA90B6984A93AD8FC897DF91E632368D868169>
 厚生労働省令第二十六号薬事法(昭和三十五年法律第百四十五号)第十二条の二第二号並びに第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む )の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令及び医薬品の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十五年三月十一日厚生労働大臣田村憲久医薬品
厚生労働省令第二十六号薬事法(昭和三十五年法律第百四十五号)第十二条の二第二号並びに第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む )の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令及び医薬品の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十五年三月十一日厚生労働大臣田村憲久医薬品
Microsoft PowerPoint - ⑨140925,30日薬連講習会(後発RMP)930.ppt [互換モード]
![Microsoft PowerPoint - ⑨140925,30日薬連講習会(後発RMP)930.ppt [互換モード] Microsoft PowerPoint - ⑨140925,30日薬連講習会(後発RMP)930.ppt [互換モード]](/thumbs/101/151698947.jpg) 後発医薬品 RMP について 厚生労働省医薬食品局安全対策課磯﨑正季子 1 後発医薬品への RMP の適用 平成 24 年 4 月 11 日薬食安発 0411 第 1 号 薬食審査発 0411 第 2 号安全対策課長 審査管理課長連名通知 医薬品リスク管理計画指針について 適用範囲医療用医薬品 ( 新医薬品 バイオ後続品 後発医薬品 ) 策定検討の時点 承認申請時 新医薬品 バイオ後続品後発医薬品
後発医薬品 RMP について 厚生労働省医薬食品局安全対策課磯﨑正季子 1 後発医薬品への RMP の適用 平成 24 年 4 月 11 日薬食安発 0411 第 1 号 薬食審査発 0411 第 2 号安全対策課長 審査管理課長連名通知 医薬品リスク管理計画指針について 適用範囲医療用医薬品 ( 新医薬品 バイオ後続品 後発医薬品 ) 策定検討の時点 承認申請時 新医薬品 バイオ後続品後発医薬品
薬事法における病院及び医師に対する主な規制について 特定生物由来製品に係る説明 ( 法第 68 条の 7 平成 14 年改正 ) 特定生物由来製品の特性を踏まえ 製剤のリスクとベネフィットについて患者に説明を行い 理解を得るように努めることを これを取り扱う医師等の医療関係者に義務づけたもの ( 特
 薬事法における病院及び医師に対する主な規制について 情報の提供等 ( 法第 77 条の 3 第 2 項及び第 3 項 第 2 項 : 昭和 54 年改正 第 3 項 : 平成 6 年改正 ) 医薬品の製造販売業者等が行う医薬品又は医療機器の適正な使用のために必要な情報の収集に協力するよう努めることを また 医薬品及び医療機器の適正な使用を確保するため 医薬品の製造販売業者等から提供される情報の活用その他必要な情報の収集
薬事法における病院及び医師に対する主な規制について 情報の提供等 ( 法第 77 条の 3 第 2 項及び第 3 項 第 2 項 : 昭和 54 年改正 第 3 項 : 平成 6 年改正 ) 医薬品の製造販売業者等が行う医薬品又は医療機器の適正な使用のために必要な情報の収集に協力するよう努めることを また 医薬品及び医療機器の適正な使用を確保するため 医薬品の製造販売業者等から提供される情報の活用その他必要な情報の収集
る として 平成 20 年 12 月に公表された 規制改革推進のための第 3 次答申 において 医療機器開発の円滑化の観点から 薬事法の適用範囲の明確化を図るためのガイドラインを作成すべきであると提言したところである 今般 薬事法の適用に関する判断の透明性 予見可能性の向上を図るため 臨床研究におい
 都道府県知事 各保健所設置市長殿 特別区長 薬食発 0331 第 7 号 平成 22 年 3 月 31 日 厚生労働省医薬食品局長 臨床研究において用いられる未承認医療機器の提供等に係る 薬事法の適用について 薬事法 ( 昭和 35 年法律第 145 号 ) は 医療機器について品質 有効性及び安全性の確保がなされた製品のみが流通するよう種々の規制を設けているが 薬事法第 14 条第 1 項の承認を受けていない医療機器
都道府県知事 各保健所設置市長殿 特別区長 薬食発 0331 第 7 号 平成 22 年 3 月 31 日 厚生労働省医薬食品局長 臨床研究において用いられる未承認医療機器の提供等に係る 薬事法の適用について 薬事法 ( 昭和 35 年法律第 145 号 ) は 医療機器について品質 有効性及び安全性の確保がなされた製品のみが流通するよう種々の規制を設けているが 薬事法第 14 条第 1 項の承認を受けていない医療機器
改正薬事法の施行に伴う製造販売の承認を要しない医薬品等の取扱い等について
 薬食審査発第 0331015 号平成 17 年 3 月 31 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 改正薬事法の施行に伴う製造販売の承認を要しない医薬品等の取扱い等について 薬事法及び採血及び供血あっせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 薬事法等一部改正法 という ) による改正後の薬事法 ( 昭和 35 年法律第 145
薬食審査発第 0331015 号平成 17 年 3 月 31 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 改正薬事法の施行に伴う製造販売の承認を要しない医薬品等の取扱い等について 薬事法及び採血及び供血あっせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 薬事法等一部改正法 という ) による改正後の薬事法 ( 昭和 35 年法律第 145
PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1
 PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1 項第 1 号に定める医療機器リスク管理計画書をもって 承認申請資料のうち臨床試験の試験成績に関する資料又はこれに代替するものとして厚生労働大臣が認める資料の一部に代えることができることとしたこと
PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1 項第 1 号に定める医療機器リスク管理計画書をもって 承認申請資料のうち臨床試験の試験成績に関する資料又はこれに代替するものとして厚生労働大臣が認める資料の一部に代えることができることとしたこと
はじめて医療機器を製造販売または製造される方へ
 を製造 ( 輸入 ) 販売するには 国内で必要な許可等について を製造販売 製造 ( 輸入 ) するためには 医薬品 等の品質 有効性及び安全性の確保等に関する法律 ( 以下 薬機法という ) の許可等 ( 製造販売業許可 製造業登録 ) が必要になります 製品を市場に出荷するために必要な許可 販売する製品に対して最終責製造販売業任を持ち 自社の名前で市場へ出荷する この許可では製造することはできません
を製造 ( 輸入 ) 販売するには 国内で必要な許可等について を製造販売 製造 ( 輸入 ) するためには 医薬品 等の品質 有効性及び安全性の確保等に関する法律 ( 以下 薬機法という ) の許可等 ( 製造販売業許可 製造業登録 ) が必要になります 製品を市場に出荷するために必要な許可 販売する製品に対して最終責製造販売業任を持ち 自社の名前で市場へ出荷する この許可では製造することはできません
3 治験実施計画書目的 当該治験について 治験実施計画書が手順書に従い適切に作成及び改訂されていることを確認する 次の事項を調べる (1) 治験実施計画書の記載項目 ( 再生医療等製品 GCP 省令第 7 条第 1 項に規定する項目 ) (2) 治験実施計画書の作成 改訂の手順と日付 (3) 治験計
 別添 10 再生医療等製品 GCP 省令チェックリスト Ⅰ 治験依頼者 ( 受託機関を含む ) 用 1 組織及び体制目的 治験の依頼及び管理に当たって 再生医療等製品 GCP 省令に沿った業務を行うために適切にして十分な人材を有し かつ 組織及び体制が確立していることを確認する 1 治験依頼者の組織 ( 当該被験機器の開発組織を含む ) と再生医療等製品 G CP 省令に係わる組織との関係 2 治験の依頼及び管理の業務に従事する者の氏名
別添 10 再生医療等製品 GCP 省令チェックリスト Ⅰ 治験依頼者 ( 受託機関を含む ) 用 1 組織及び体制目的 治験の依頼及び管理に当たって 再生医療等製品 GCP 省令に沿った業務を行うために適切にして十分な人材を有し かつ 組織及び体制が確立していることを確認する 1 治験依頼者の組織 ( 当該被験機器の開発組織を含む ) と再生医療等製品 G CP 省令に係わる組織との関係 2 治験の依頼及び管理の業務に従事する者の氏名
スライド 1
 薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
ともに 申請者が承認審査のスケジュールに沿って法令上求められる製造体制を整備することや承認後円滑に医療現場に提供するための対応が十分になされることで 更なる迅速な実用化を促すものである この制度では 原則として新規原理 新規作用機序等により 生命に重大な影響がある重篤な疾患等に対して 極めて高い有効
 ともに 申請者が承認審査のスケジュールに沿って法令上求められる製造体制を整備することや承認後円滑に医療現場に提供するための対応が十分になされることで 更なる迅速な実用化を促すものである この制度では 原則として新規原理 新規作用機序等により 生命に重大な影響がある重篤な疾患等に対して 極めて高い有効性が期待される医療機器 体外診断用医薬品 再生医療等製品を指定することとする また 本制度では PMDA
ともに 申請者が承認審査のスケジュールに沿って法令上求められる製造体制を整備することや承認後円滑に医療現場に提供するための対応が十分になされることで 更なる迅速な実用化を促すものである この制度では 原則として新規原理 新規作用機序等により 生命に重大な影響がある重篤な疾患等に対して 極めて高い有効性が期待される医療機器 体外診断用医薬品 再生医療等製品を指定することとする また 本制度では PMDA
<4D F736F F D E34208EA18CB18EE891B182AB977697CC C8E8DB782B591D682A688CB978A>
 Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
konbi
 薬生薬審発 0915 第 1 号薬生機審発 0915 第 1 号薬生安発 0915 第 3 号薬生監麻発 0915 第 3 号平成 28 年 9 月 15 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) 厚生労働省医薬
薬生薬審発 0915 第 1 号薬生機審発 0915 第 1 号薬生安発 0915 第 3 号薬生監麻発 0915 第 3 号平成 28 年 9 月 15 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) 厚生労働省医薬
< F2D819B955C8EA692CA926D DC58F4994AD8F6F>
 薬食監麻発第 0331008 号平成 17 年 3 月 31 日 各都道府県衛生主管部 ( 局 ) 長 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 一部改正法 という ) 第 2 条の規定による改正後の薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 及び関係政省令等の規定に基づく医薬品 医薬部外品 化粧品及び医療機器 (
薬食監麻発第 0331008 号平成 17 年 3 月 31 日 各都道府県衛生主管部 ( 局 ) 長 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 96 号 以下 一部改正法 という ) 第 2 条の規定による改正後の薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 及び関係政省令等の規定に基づく医薬品 医薬部外品 化粧品及び医療機器 (
<4D F736F F D2089FC92F994ED8CB18ED295E58F5782CC82BD82DF82CC8FEE95F192F18B9F977697CC5F A2E646F63>
 治験に係わる被験者募集のための情報提供要領 < 改訂版 > 平成 20 年 11 月 日本製薬工業協会 医薬品評価委員会 はじめに 厚生省 ( 現厚生労働省 ) 治験を円滑に推進するための検討会 の最終報告書を受け 平成 11 年 6 月 30 日医薬監第 65 号にて厚生省医薬安全局監視指導課 ( 現医薬局監視指導 麻薬対策課 ) より 治験に係る被験者募集の情報提供の取扱いについて が通知された
治験に係わる被験者募集のための情報提供要領 < 改訂版 > 平成 20 年 11 月 日本製薬工業協会 医薬品評価委員会 はじめに 厚生省 ( 現厚生労働省 ) 治験を円滑に推進するための検討会 の最終報告書を受け 平成 11 年 6 月 30 日医薬監第 65 号にて厚生省医薬安全局監視指導課 ( 現医薬局監視指導 麻薬対策課 ) より 治験に係る被験者募集の情報提供の取扱いについて が通知された
受付後 持参又は郵送等の報告方法によらず 医薬品医療機器総合機構 ( 以下 機構 という ) 審査マネジメント部審査企画課から別紙 1 不具合等報告送付整理票 により郵送にて連絡される また 第二報以降については 機構が付与した識別番号を記載して報告すること イ平成 26 年 6 月 30 日以前に
 薬機審マ発第 0606001 号平成 26 年 6 月 6 日 ( 別記 ) 殿 独立行政法人医薬品医療機器総合機構審査マネジメント部長 治験不具合等報告に関する取扱いについて 医療機器の治験中の不具合及び有害事象の報告 ( 以下 治験不具合等報告 という ) については 平成 19 年 3 月 30 日付け薬食発第 0330001 号厚生労働省医薬食品局長通知 独立行政法人医薬品医療機器総合機構に対する機械器具等に係る治験不具合等報告について
薬機審マ発第 0606001 号平成 26 年 6 月 6 日 ( 別記 ) 殿 独立行政法人医薬品医療機器総合機構審査マネジメント部長 治験不具合等報告に関する取扱いについて 医療機器の治験中の不具合及び有害事象の報告 ( 以下 治験不具合等報告 という ) については 平成 19 年 3 月 30 日付け薬食発第 0330001 号厚生労働省医薬食品局長通知 独立行政法人医薬品医療機器総合機構に対する機械器具等に係る治験不具合等報告について
医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など ) 医薬品候補物質のスクリーニン
 特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
Taro-再製造単回使用医療機器基準
 厚生労働省告示第二百六十一号医薬品医療機器等の品質有効性及び安全性の確保等に関する法律 ( 昭和三十五年法律第百四十 五号 ) 第四十二条第二項の規定に基づき再製造単回使用医療機器基準を次のように定め平成二十 九年七月三十一日から適用す る平成二十九年七月三十一日厚生労働大臣塩崎恭久再製造単回使用医療機器基準第 1 定義 1 再生部品 とは 医療機関において使用された単回使用の医療機器の全部又は一部であって
厚生労働省告示第二百六十一号医薬品医療機器等の品質有効性及び安全性の確保等に関する法律 ( 昭和三十五年法律第百四十 五号 ) 第四十二条第二項の規定に基づき再製造単回使用医療機器基準を次のように定め平成二十 九年七月三十一日から適用す る平成二十九年七月三十一日厚生労働大臣塩崎恭久再製造単回使用医療機器基準第 1 定義 1 再生部品 とは 医療機関において使用された単回使用の医療機器の全部又は一部であって
じ ) その他の処方せん医薬品又は高度管理医療機器の製造販売に係る業務の責任者との密接な連携を図らせること ( 安全確保業務に係る組織及び職員 ) 第四条第一種製造販売業者は 次に掲げる要件を満たす安全確保業務の統括に係る部門 ( 以下この章において 安全管理統括部門 という ) を置かなければなら
 厚生労働省令第百三十五号薬事法 ( 昭和三十五年法律第百四十五号 ) 第十二条の二第二号の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令を次のように定める 平成十六年九月二十二日厚生労働大臣坂口力 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令目次第一章総則 ( 第一条第二条 ) 第一種製造販売業者の製造販売後安全管理の基準
厚生労働省令第百三十五号薬事法 ( 昭和三十五年法律第百四十五号 ) 第十二条の二第二号の規定に基づき 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令を次のように定める 平成十六年九月二十二日厚生労働大臣坂口力 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令目次第一章総則 ( 第一条第二条 ) 第一種製造販売業者の製造販売後安全管理の基準
標準業務手順 目次
 浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
都道府県医師会医療安全担当理事殿 ( 法安 56) 平成 27 年 8 月 5 日 日本医師会常任理事今村定臣 酵素電極法を用いた血糖測定に使用する医療機器及び体外診断用医薬品に係る 使用上の注意 の改訂について グルコース分析装置 自己検査用グルコース測定器及び自動分析装置等並びに血液検査用グルコ
 都道府県医師会医療安全担当理事殿 ( 法安 56) 平成 27 年 8 月 5 日 日本医師会常任理事今村定臣 酵素電極法を用いた血糖測定に使用する医療機器及び体外診断用医薬品に係る 使用上の注意 の改訂について グルコース分析装置 自己検査用グルコース測定器及び自動分析装置等並びに血液検査用グルコースキット及び自己検査用グルコースキット ( 測定項目として血糖値を有する医療機器または体外診断用医薬品
都道府県医師会医療安全担当理事殿 ( 法安 56) 平成 27 年 8 月 5 日 日本医師会常任理事今村定臣 酵素電極法を用いた血糖測定に使用する医療機器及び体外診断用医薬品に係る 使用上の注意 の改訂について グルコース分析装置 自己検査用グルコース測定器及び自動分析装置等並びに血液検査用グルコースキット及び自己検査用グルコースキット ( 測定項目として血糖値を有する医療機器または体外診断用医薬品
薬食機発 0131 第 1 号平成 25 年 1 月 31 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課医療機器審査管理室長 薬事法に基づく登録認証機関の基準改正に伴う留意事項について ( その 2) 薬事法 ( 昭和 35 年法律第 145 号 以下 法 という )
 薬食機発 0131 第 1 号平成 25 年 1 月 31 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課医療機器審査管理室長 薬事法に基づく登録認証機関の基準改正に伴う留意事項について ( その 2) 薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 23 条の 2 第 1 項の登録認証機関の登録申請等の取扱いについては 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律等の施行に関する適合性認証機関の登録申請等について
薬食機発 0131 第 1 号平成 25 年 1 月 31 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課医療機器審査管理室長 薬事法に基づく登録認証機関の基準改正に伴う留意事項について ( その 2) 薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 23 条の 2 第 1 項の登録認証機関の登録申請等の取扱いについては 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律等の施行に関する適合性認証機関の登録申請等について
静岡県立静岡がんセンター臨床研究事務局の業務手順書
 治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 6.0 平成 20 年 1 月 28
治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 6.0 平成 20 年 1 月 28
国立仙台病院受託研究取扱規程
 独立行政法人国立病院機構仙台医療センター受託研究取扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構仙台医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程の定めるところによる 2 契約 経理及び書式等については 原則として独立行政法人国立病院機構
独立行政法人国立病院機構仙台医療センター受託研究取扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構仙台医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程の定めるところによる 2 契約 経理及び書式等については 原則として独立行政法人国立病院機構
薬生発 0926 第 5 号 平成 29 年 9 月 26 日 都道府県知事 各保健所設置市長殿 特別区長 厚生労働省医薬 生活衛生局長 ( 公印省略 ) コンタクトレンズの適正使用に関する情報提供等の徹底について コンタクトレンズ ( カラーコンタクトレンズを含む ) の販売に関しては これまで
 薬生発 0926 第 5 号 平成 29 年 9 月 26 日 都道府県知事 各保健所設置市長殿 特別区長 厚生労働省医薬 生活衛生局長 ( 公印省略 ) コンタクトレンズの適正使用に関する情報提供等の徹底について コンタクトレンズ ( カラーコンタクトレンズを含む ) の販売に関しては これまで コンタクトレンズの適正使用に関する情報提供等の徹底について ( 平成 24 年 7 月 18 日付け薬食発
薬生発 0926 第 5 号 平成 29 年 9 月 26 日 都道府県知事 各保健所設置市長殿 特別区長 厚生労働省医薬 生活衛生局長 ( 公印省略 ) コンタクトレンズの適正使用に関する情報提供等の徹底について コンタクトレンズ ( カラーコンタクトレンズを含む ) の販売に関しては これまで コンタクトレンズの適正使用に関する情報提供等の徹底について ( 平成 24 年 7 月 18 日付け薬食発
Microsoft Word _正当理由通知(薬局医薬品) (反映)
 薬食発 0318 第 4 号 平成 26 年 3 月 18 日 都道府県知事 各保健所設置市長殿 特別区長 厚生労働省医薬食品局長 ( 公印省略 ) 薬局医薬品の取扱いについて 薬事法及び薬剤師法の一部を改正する法律 ( 平成 25 年法律第 103 号 以下 改正法 という ) については 薬事法及び薬剤師法の一部を改正する法律の施行期日を定める政令 ( 平成 26 年政令第 24 号 ) により
薬食発 0318 第 4 号 平成 26 年 3 月 18 日 都道府県知事 各保健所設置市長殿 特別区長 厚生労働省医薬食品局長 ( 公印省略 ) 薬局医薬品の取扱いについて 薬事法及び薬剤師法の一部を改正する法律 ( 平成 25 年法律第 103 号 以下 改正法 という ) については 薬事法及び薬剤師法の一部を改正する法律の施行期日を定める政令 ( 平成 26 年政令第 24 号 ) により
通知(一括更新手続き)
 薬食審査発 0330 第 6 号 平成 27 年 3 月 30 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) 化粧品製造販売届書の届出先の都道府県が変更になる場合等の取扱いについて 化粧品製造販売届書の取扱いについては 改正薬事法の施行に伴う製造販売の承認を要しない医薬品等の取扱い等について ( 平成 17 年 3 月 31 日付け薬食審査発第 0331015
薬食審査発 0330 第 6 号 平成 27 年 3 月 30 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) 化粧品製造販売届書の届出先の都道府県が変更になる場合等の取扱いについて 化粧品製造販売届書の取扱いについては 改正薬事法の施行に伴う製造販売の承認を要しない医薬品等の取扱い等について ( 平成 17 年 3 月 31 日付け薬食審査発第 0331015
北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下
 北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下 モニタリング という ) 監査の受け入れ 並びに試験審査委員会( 治験審査委員会が兼ねる 以下 治験審査委員会
北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下 モニタリング という ) 監査の受け入れ 並びに試験審査委員会( 治験審査委員会が兼ねる 以下 治験審査委員会
<945F96F B3816A2E786264>
 Q-14 食品衛生法 ( 昭和 22 年法律第 233 号 ) とは 1 食品衛生法について 食品衛生法とは食品の安全性の確保のために公衆衛生の見地から必要な規制その他の措置を講ずることにより 飲食に起因する衛生上の危害の発生を防止し もつて国民の健康の保護を図ることを目的として 食品の規格等の設定 検査の実施 健康を損なうおそれのある食品の販売の禁止などの事項を規定しています 適用範囲食品衛生法の中で
Q-14 食品衛生法 ( 昭和 22 年法律第 233 号 ) とは 1 食品衛生法について 食品衛生法とは食品の安全性の確保のために公衆衛生の見地から必要な規制その他の措置を講ずることにより 飲食に起因する衛生上の危害の発生を防止し もつて国民の健康の保護を図ることを目的として 食品の規格等の設定 検査の実施 健康を損なうおそれのある食品の販売の禁止などの事項を規定しています 適用範囲食品衛生法の中で
( 委員会の業務 ) 第 4 条委員会は その責務の遂行のために以下の最新資料を病院長から入手する なお あらかじめ 自ら治験を実施する者 委員会及び病院長の合意が得られている場合においては GCP 省令第 26 条の6 第 2 項に関する通知に限り 自ら治験を実施する者から入手することができる ま
 秋田大学医学部附属病院医師主導治験における治験審査委員会規程 第 1 章医師主導治験審査委員会 ( 目的と適用範囲 ) 第 1 条本規程は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 医薬品の臨床試験の実施の基準に関する省令( 平成 9 年 3 月 27 日厚生省令第 28 号 )( 以下 GCP 省令 という ) 並びにGCP 省令に関連する通知書等に基づいて
秋田大学医学部附属病院医師主導治験における治験審査委員会規程 第 1 章医師主導治験審査委員会 ( 目的と適用範囲 ) 第 1 条本規程は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 医薬品の臨床試験の実施の基準に関する省令( 平成 9 年 3 月 27 日厚生省令第 28 号 )( 以下 GCP 省令 という ) 並びにGCP 省令に関連する通知書等に基づいて
本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シ
 医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
先進医療の実績報告要領 Ⅰ 実績報告の実施について (1) 実績報告の目的先進医療の実施状況を把握し 保険導入等に係る検討のための基礎資料とすることを目的とするものである (2) 実績報告の対象医療機関平成 30 年 6 月 30 日現在において 先進医療を実施している医療機関平成 30 年 3 月
 先進医療の実績報告要領 Ⅰ 実績報告の実施について (1) 実績報告の目的先進医療の実施状況を把握し 保険導入等に係る検討のための基礎資料とすることを目的とするものである (2) 実績報告の対象医療機関平成 30 年 6 月 30 日現在において 先進医療を実施している医療機関平成 30 年 3 月 31 日現在において 先進医療を実施している医療機関 ( 保険導入等分 ) 先進医療 A 告示番号
先進医療の実績報告要領 Ⅰ 実績報告の実施について (1) 実績報告の目的先進医療の実施状況を把握し 保険導入等に係る検討のための基礎資料とすることを目的とするものである (2) 実績報告の対象医療機関平成 30 年 6 月 30 日現在において 先進医療を実施している医療機関平成 30 年 3 月 31 日現在において 先進医療を実施している医療機関 ( 保険導入等分 ) 先進医療 A 告示番号
査を実施し 必要に応じ適切な措置を講ずること (2) 本品の警告 効能 効果 性能 用法 用量及び使用方法は以下のとお りであるので 特段の留意をお願いすること なお その他の使用上の注意については 添付文書を参照されたいこと 警告 1 本品投与後に重篤な有害事象の発現が認められていること 及び本品
 薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
し 自ら治験を実施する者が実施した治験において発生した副作用等については 規制当局へ報告する必要があることに留意すること なお この注意事項は 被験薬に係る副作用等情報を実施医療機関の長に通知するよう 自ら治験を実施する者に義務付けている医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年厚生
 薬食審査発 0701 第 21 号 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) 自ら治験を実施した者による治験副作用等報告について 自ら治験を実施した者による治験副作用等報告の取扱いについては 独立行政法人医薬品医療機器総合機構に対する治験副作用等報告について ( 平成 16 年 3 月 30 日付け薬食発第 0330001
薬食審査発 0701 第 21 号 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) 自ら治験を実施した者による治験副作用等報告について 自ら治験を実施した者による治験副作用等報告の取扱いについては 独立行政法人医薬品医療機器総合機構に対する治験副作用等報告について ( 平成 16 年 3 月 30 日付け薬食発第 0330001
Microsoft Word - 2-① 補償ガイドライン平成27年版(本文)Ver3.1.1.do
 1. 総則 被験者の健康被害補償に関するガイドライン Ver. 3 Ver. 3. 1 Ver. 3. 1.1 : 2 0 1 5 ( 平成 2 7 ) 年 8 月 1 8 日 : 2 0 1 5 ( 平成 2 7 ) 年 1 2 月 2 1 日 : 2 0 1 6 ( 平成 2 8 ) 年 1 2 月 2 0 日 1-1 本ガイドラインは 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年厚生省令第
1. 総則 被験者の健康被害補償に関するガイドライン Ver. 3 Ver. 3. 1 Ver. 3. 1.1 : 2 0 1 5 ( 平成 2 7 ) 年 8 月 1 8 日 : 2 0 1 5 ( 平成 2 7 ) 年 1 2 月 2 1 日 : 2 0 1 6 ( 平成 2 8 ) 年 1 2 月 2 0 日 1-1 本ガイドラインは 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年厚生省令第
< F2D8E9197BF A836F815B2E6A7464>
 ( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
本手順書で使用する用語の定義 用語電子的記録書面電子的記録利用システム実務担当者原データ治験関連文書サイボウズサイボウズメッセージ 定義人の知覚では認識できない, 電子式等の方法で記録され, コンピュータで処理される記録紙媒体による資料治験依頼者, 実施医療機関の長, 治験責任医師並びに治験審査委員
 ( 第 1 版 :2015 年 7 月 1 日 ) 本手順書で使用する用語の定義 用語電子的記録書面電子的記録利用システム実務担当者原データ治験関連文書サイボウズサイボウズメッセージ 定義人の知覚では認識できない, 電子式等の方法で記録され, コンピュータで処理される記録紙媒体による資料治験依頼者, 実施医療機関の長, 治験責任医師並びに治験審査委員会の間での電子的記録の作成, 交付, 受領及び保存に用いるシステム規定や文書等で責任者の行うべき業務の権限を与えられ,
( 第 1 版 :2015 年 7 月 1 日 ) 本手順書で使用する用語の定義 用語電子的記録書面電子的記録利用システム実務担当者原データ治験関連文書サイボウズサイボウズメッセージ 定義人の知覚では認識できない, 電子式等の方法で記録され, コンピュータで処理される記録紙媒体による資料治験依頼者, 実施医療機関の長, 治験責任医師並びに治験審査委員会の間での電子的記録の作成, 交付, 受領及び保存に用いるシステム規定や文書等で責任者の行うべき業務の権限を与えられ,
Microsoft PowerPoint - 運用 [互換モード]
![Microsoft PowerPoint - 運用 [互換モード] Microsoft PowerPoint - 運用 [互換モード]](/thumbs/91/105850431.jpg) 押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
301226更新 (薬局)平成29 年度に実施した個別指導指摘事項(溶け込み)
 平成 29 年度に実施した個別指導において保険薬局に改善を求めた主な指摘事項 東海北陸厚生局 目次 Ⅰ 調剤全般に関する事項 1 処方せんの取扱い 1 2 処方内容に関する薬学的確認 1 3 調剤 1 4 調剤済処方せんの取扱い 1 5 調剤録等の取扱い 2 Ⅱ 調剤技術料に関する事項 1 調剤料 2 2 一包化加算 2 3 自家製剤加算 2 Ⅲ 薬剤管理料に関する事項 1 薬剤服用歴管理指導料 2
平成 29 年度に実施した個別指導において保険薬局に改善を求めた主な指摘事項 東海北陸厚生局 目次 Ⅰ 調剤全般に関する事項 1 処方せんの取扱い 1 2 処方内容に関する薬学的確認 1 3 調剤 1 4 調剤済処方せんの取扱い 1 5 調剤録等の取扱い 2 Ⅱ 調剤技術料に関する事項 1 調剤料 2 2 一包化加算 2 3 自家製剤加算 2 Ⅲ 薬剤管理料に関する事項 1 薬剤服用歴管理指導料 2
<4D F736F F F696E74202D EA98CC8935F8C9F B8DEC977095F18D902E B8CDD8AB B83685D>
 製造販売後安全管理業務における現状 ノバルティス社やファイザー社等で 安全管理情報 ( 副作用等 ) の処理や国報告に問題があったことが判明 安全管理情報の処理と副作用報告その 2 ( 副作用報告に関する内容を中心に ) 当県でも GQP GVP フォローアップ調査で安全管理情報が適切に処理されているかを重点的に確認 副作用報告漏れや安全管理情報の処理が適切でない事例が見られた GVP 省令の内容について説明
製造販売後安全管理業務における現状 ノバルティス社やファイザー社等で 安全管理情報 ( 副作用等 ) の処理や国報告に問題があったことが判明 安全管理情報の処理と副作用報告その 2 ( 副作用報告に関する内容を中心に ) 当県でも GQP GVP フォローアップ調査で安全管理情報が適切に処理されているかを重点的に確認 副作用報告漏れや安全管理情報の処理が適切でない事例が見られた GVP 省令の内容について説明
国立病院機構大阪医療センター受託研究取扱細則
 国立病院機構大阪医療センター 受託研究取扱細則 ( 主旨 ) 第 1 条国立病院機構大阪医療センターにおける受託研究の取扱いに関しては 国立病院機構大阪医療センター受託研究取扱規程 ( 以下 規程 という ) 及び他に定めるもののほか 規程第 1 条第 2 項に規定するこの細則の定めるところによる ( 総則 ) 第 2 条研究責任者は 原則として医長職相当以上とする ただし 副作用報告及び感染症報告を受託研究として実施する場合
国立病院機構大阪医療センター 受託研究取扱細則 ( 主旨 ) 第 1 条国立病院機構大阪医療センターにおける受託研究の取扱いに関しては 国立病院機構大阪医療センター受託研究取扱規程 ( 以下 規程 という ) 及び他に定めるもののほか 規程第 1 条第 2 項に規定するこの細則の定めるところによる ( 総則 ) 第 2 条研究責任者は 原則として医長職相当以上とする ただし 副作用報告及び感染症報告を受託研究として実施する場合
Microsoft Word - 局長通知(新旧対照表).docx
 医薬品等適正広告基準について 新旧対照表 ( 昭和 55 年 10 月 9 日薬発第 1339 号各都道府県知事あて厚生省薬務局長通知改正平成 14 年 3 月 28 日医薬発第 0328009 号厚生労働省医薬局長通知 ) 現行改定案 第 1 ( 目的 ) この基準は 医薬品 医薬部外品 化粧品及び医療用具 ( 以下 医薬品等 という ) の広告が虚偽 誇大にわたらないようにするとともにその適正を図ることを目的とする
医薬品等適正広告基準について 新旧対照表 ( 昭和 55 年 10 月 9 日薬発第 1339 号各都道府県知事あて厚生省薬務局長通知改正平成 14 年 3 月 28 日医薬発第 0328009 号厚生労働省医薬局長通知 ) 現行改定案 第 1 ( 目的 ) この基準は 医薬品 医薬部外品 化粧品及び医療用具 ( 以下 医薬品等 という ) の広告が虚偽 誇大にわたらないようにするとともにその適正を図ることを目的とする
Microsoft Word - 表紙 雛形(保険者入り)高齢者支援課180320
 老高発 0330 第 4 号 平成 30 年 3 月 30 日 都道府県 各指定都市民生主管部 ( 局 ) 長殿 中核市 厚生労働省老健局高齢者支援課長 ( 公印省略 ) 有料老人ホーム情報提供制度実施要領について 地域包括ケアシステムの強化のための介護保険法等の一部を改正する法律 ( 平成 29 年法律第 52 号 ) による改正後の老人福祉法 ( 昭和 38 年法律第 133 号 ) 第 29
老高発 0330 第 4 号 平成 30 年 3 月 30 日 都道府県 各指定都市民生主管部 ( 局 ) 長殿 中核市 厚生労働省老健局高齢者支援課長 ( 公印省略 ) 有料老人ホーム情報提供制度実施要領について 地域包括ケアシステムの強化のための介護保険法等の一部を改正する法律 ( 平成 29 年法律第 52 号 ) による改正後の老人福祉法 ( 昭和 38 年法律第 133 号 ) 第 29
薬食審査発 0318 第 1 号薬食監麻発 0318 第 6 号平成 22 年 3 月 18 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 厚生労働省医薬食品局監視指導 麻薬対策課長 改正法施行に伴う経過措置等終了にあたっての対応について 薬事法及び採血及び供血あつせ
 薬食審査発 0318 第 1 号薬食監麻発 0318 第 6 号平成 22 年 3 月 18 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 厚生労働省医薬食品局監視指導 麻薬対策課長 改正法施行に伴う経過措置等終了にあたっての対応について 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 9 6 号 以下 改正法 という ) の施行及び改正法による改正後の薬事法
薬食審査発 0318 第 1 号薬食監麻発 0318 第 6 号平成 22 年 3 月 18 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 厚生労働省医薬食品局監視指導 麻薬対策課長 改正法施行に伴う経過措置等終了にあたっての対応について 薬事法及び採血及び供血あつせん業取締法の一部を改正する法律 ( 平成 14 年法律第 9 6 号 以下 改正法 という ) の施行及び改正法による改正後の薬事法
<4D F736F F D208EA18CB182C98AD682B782E995578F808BC696B18EE88F878F E38E748EE593B1816A E7B8D732E646F637
 治験に関する標準業務手順書 ( 医師主導治験 ) 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医師主導治験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 (
治験に関する標準業務手順書 ( 医師主導治験 ) 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医師主導治験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 (
<4D F736F F D EF8E9197BF5F92E88AFA95F18D CC97AF88D38E968D805F E646F63>
 部会資料 定期報告を含む副作用報告等の規制改正の留意事項 2009 年 4 月 日本製薬工業協会医薬品評価委員会臨床評価部会 PMS 部会電子化情報部会 目 次 1 定期報告を含む副作用報告等関連規制改正の経緯及びポイント... 5 2 規制当局への定期報告に関する留意事項と補足... 7 2-1 個別症例報告に市販後副作用等報告を活用できる一変治験... 7 2-2 定期報告の対象となる副作用等症例...
部会資料 定期報告を含む副作用報告等の規制改正の留意事項 2009 年 4 月 日本製薬工業協会医薬品評価委員会臨床評価部会 PMS 部会電子化情報部会 目 次 1 定期報告を含む副作用報告等関連規制改正の経緯及びポイント... 5 2 規制当局への定期報告に関する留意事項と補足... 7 2-1 個別症例報告に市販後副作用等報告を活用できる一変治験... 7 2-2 定期報告の対象となる副作用等症例...
法改正の目的 1 Ⅰ 医療機器等の特性を踏まえた規制の構築 1. 医療機器等の製造販売業及び製造業の章の新設 2. 体外診断用医薬品の製造販売業の新設 3. 医療機器等の製造業の登録制への移行 4. プログラムの位置付けの明確化 5. QMS 調査の見直し 6. 認証制度に関する見直し 7. 医療機
 医薬品医療機器等法の概要について ~ 医療機器等 ( ) を中心に ~ 東京都健康安全研究センター広域監視部医療機器監視課 ( ) 医療機器等 : 医療機器及び体外診断用医薬品 1 薬事法から医薬品医療機器等法へ 薬事法が 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 に改正されました 以下 医薬品医療機器等法 とします 2-1 - 法改正の目的 1 Ⅰ 医療機器等の特性を踏まえた規制の構築
医薬品医療機器等法の概要について ~ 医療機器等 ( ) を中心に ~ 東京都健康安全研究センター広域監視部医療機器監視課 ( ) 医療機器等 : 医療機器及び体外診断用医薬品 1 薬事法から医薬品医療機器等法へ 薬事法が 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 に改正されました 以下 医薬品医療機器等法 とします 2-1 - 法改正の目的 1 Ⅰ 医療機器等の特性を踏まえた規制の構築
GVP省令
 医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令 ( ) 発簡日平成 16 年 9 月 22 日発簡番号省令第 135 号情報種別省令 目次 第 1 章総則 ( 第 1 条 - 第 2 条 ) 第 2 章 第一種製造販売業者の製造販売後安全管理の基準 ( 第 3 条 - 第 12 条 ) 第 3 章 第二種製造販売業者の製造販売後安全管理の基準 ( 第 13 条 - 第
医薬品 医薬部外品 化粧品及び医療機器の製造販売後安全管理の基準に関する省令 ( ) 発簡日平成 16 年 9 月 22 日発簡番号省令第 135 号情報種別省令 目次 第 1 章総則 ( 第 1 条 - 第 2 条 ) 第 2 章 第一種製造販売業者の製造販売後安全管理の基準 ( 第 3 条 - 第 12 条 ) 第 3 章 第二種製造販売業者の製造販売後安全管理の基準 ( 第 13 条 - 第
平成14年8月 日
 平成 30 年 11 月 15 日福祉保健局 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 に基づく行政処分 ( 回収命令 ) について 都は本日 以下の事業者に対し 医薬品 医療機器等の品質 有効性及び安全性の確保 等に関する法律 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 70 条第 1 項の 規定に基づく 回収命令 を行ったので お知らせします 1 対象事業者氏名ピュアハートキングス株式会社
平成 30 年 11 月 15 日福祉保健局 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 に基づく行政処分 ( 回収命令 ) について 都は本日 以下の事業者に対し 医薬品 医療機器等の品質 有効性及び安全性の確保 等に関する法律 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 70 条第 1 項の 規定に基づく 回収命令 を行ったので お知らせします 1 対象事業者氏名ピュアハートキングス株式会社
静岡県立静岡がんセンター臨床研究事務局の業務手順書
 治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 1 目次 1. 目的と適用範囲...
治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 1 目次 1. 目的と適用範囲...
一について第一に 感染症の予防及び感染症の患者に対する医療に関する法律(平成十年法律第百十四号 以下 感染症法 という )第十二条の規定に基づき 後天性免疫不全症候群(以下 エイズという )の患者及びその病原体を保有している者であって無症状のもの(以下 HIV感染者 という )(以下 エイズの患者等
 平成十一年八月十日受領答弁第三七号衆議院議員家西悟君提出血液製剤による感染被害の救済に関する質問に対し 別紙答弁書を送付する 内閣衆質一四五第三七号平成十一年八月十日衆議院議長伊宗一郎殿内閣総理大臣小渕恵三 一について第一に 感染症の予防及び感染症の患者に対する医療に関する法律(平成十年法律第百十四号 以下 感染症法 という )第十二条の規定に基づき 後天性免疫不全症候群(以下 エイズという )の患者及びその病原体を保有している者であって無症状のもの(以下
平成十一年八月十日受領答弁第三七号衆議院議員家西悟君提出血液製剤による感染被害の救済に関する質問に対し 別紙答弁書を送付する 内閣衆質一四五第三七号平成十一年八月十日衆議院議長伊宗一郎殿内閣総理大臣小渕恵三 一について第一に 感染症の予防及び感染症の患者に対する医療に関する法律(平成十年法律第百十四号 以下 感染症法 という )第十二条の規定に基づき 後天性免疫不全症候群(以下 エイズという )の患者及びその病原体を保有している者であって無症状のもの(以下
医師主導治験取扱要覧
 15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
を追加する (2) 実施要領通知の報告様式別紙 1 医薬品安全性情報報告書 及び同報告様式別紙 2 医療機器安全性情報報告書 を別添のとおり変更する
 薬食発 0311 第 1 号平成 25 年 3 月 11 日 各都道府県知事殿 厚生労働省医薬食品局長 医薬品 医療機器等安全性情報報告制度 の報告における電子メールの活用について 薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 77 条の 4 の 2 第 2 項の規定に基づく 医療機関等からの医薬品又は医療機器についての副作用 感染症及び不具合報告 ( 以下 副作用等報告
薬食発 0311 第 1 号平成 25 年 3 月 11 日 各都道府県知事殿 厚生労働省医薬食品局長 医薬品 医療機器等安全性情報報告制度 の報告における電子メールの活用について 薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 77 条の 4 の 2 第 2 項の規定に基づく 医療機関等からの医薬品又は医療機器についての副作用 感染症及び不具合報告 ( 以下 副作用等報告
○大阪府建設業法施行細則
 大阪府建設業法施行細則昭和四十七年八月十四日大阪府規則第六十九号大阪府建設業法施行細則をここに公布する 大阪府建設業法施行細則大阪府建設業法施行細則 ( 昭和三十六年大阪府規則第七十一号 ) の全部を改正する ( 趣旨 ) 第一条この規則は 建設業法施行令 ( 昭和三十一年政令第二百七十三号 以下 政令 という ) 及び建設業法施行規則 ( 昭和二十四年建設省令第十四号 以下 省令 という ) に定めるもののほか
大阪府建設業法施行細則昭和四十七年八月十四日大阪府規則第六十九号大阪府建設業法施行細則をここに公布する 大阪府建設業法施行細則大阪府建設業法施行細則 ( 昭和三十六年大阪府規則第七十一号 ) の全部を改正する ( 趣旨 ) 第一条この規則は 建設業法施行令 ( 昭和三十一年政令第二百七十三号 以下 政令 という ) 及び建設業法施行規則 ( 昭和二十四年建設省令第十四号 以下 省令 という ) に定めるもののほか
実施医療機関治験審査委員会標準的業務手順書
 実施医療機関治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令 という
実施医療機関治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令 という
ICH Q4B Annex12
 薬食審査発 0321 第 1 号平成 2 5 年 3 月 21 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) ICHQ4B ガイドラインに基づく事項別付属文書 ( エンドトキシン試験法 ) について 今般 日米 EU 医薬品規制調和国際会議 (ICH) において ICHQ4B ガイドライン ( 平成 21 年 5 月 26 日付け薬食審査発第 0526001
薬食審査発 0321 第 1 号平成 2 5 年 3 月 21 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) ICHQ4B ガイドラインに基づく事項別付属文書 ( エンドトキシン試験法 ) について 今般 日米 EU 医薬品規制調和国際会議 (ICH) において ICHQ4B ガイドライン ( 平成 21 年 5 月 26 日付け薬食審査発第 0526001
Microsoft Word - 分権_課長通知(平成30年10月17日付薬生薬審発1017第2号)_修正
 薬生薬審発 1017 第 2 号 平成 30 年 10 月 17 日 各 地方厚生局長都道府県知事保健所設置市長特別区長 殿 厚生労働省医薬 生活衛生局 医薬品審査管理課長 ( 公印省略 ) 地域の自主性及び自立性を高めるための改革の推進を図るための関係法律の整 備に関する法律の施行による毒物及び劇物取締法における毒物又は劇物の原体 の製造業又は輸入業の登録等に係る事務 権限の委譲等について 地域の自主性及び自立性を高めるための改革の推進を図るための関係法律の整備に関する法律
薬生薬審発 1017 第 2 号 平成 30 年 10 月 17 日 各 地方厚生局長都道府県知事保健所設置市長特別区長 殿 厚生労働省医薬 生活衛生局 医薬品審査管理課長 ( 公印省略 ) 地域の自主性及び自立性を高めるための改革の推進を図るための関係法律の整 備に関する法律の施行による毒物及び劇物取締法における毒物又は劇物の原体 の製造業又は輸入業の登録等に係る事務 権限の委譲等について 地域の自主性及び自立性を高めるための改革の推進を図るための関係法律の整備に関する法律
薬局を利用するために必要な情報の掲示 ( 薬事法第 9 条の 4) 次の事項について 掲示板等により 薬局内に掲示 しなければなりません また 第 3 については 特定販売を行うことについての広告をする場合 ホームページ等に表示しなければなりません < 具体例 > 第 1 薬局の管理及び運営に関する
 薬局を利用するために必要な情報の掲示 ( 薬事法第 9 条の 4) 次の事項について 掲示板等により 薬局内に掲示 しなければなりません また 第 3 については 特定販売を行うことについての広告をする場合 ホームページ等に表示しなければなりません < 具体例 > 第 1 薬局の管理及び運営に関する事項 1 許可の区分の別薬局 開設者氏名 株式会社 開設者の氏名又は名称その 薬局の名称 薬局 店 2
薬局を利用するために必要な情報の掲示 ( 薬事法第 9 条の 4) 次の事項について 掲示板等により 薬局内に掲示 しなければなりません また 第 3 については 特定販売を行うことについての広告をする場合 ホームページ等に表示しなければなりません < 具体例 > 第 1 薬局の管理及び運営に関する事項 1 許可の区分の別薬局 開設者氏名 株式会社 開設者の氏名又は名称その 薬局の名称 薬局 店 2
改正後第 2 章通関業 第 1 節許可 新旧対照表 別紙 3 通関業法基本通達( 昭和 47 年 3 月 1 日蔵関第 105 号 ) ( 注 ) 下線を付した箇所が改正部分である 改正前第 2 章通関業第 1 節許可 3-8 削除 ( 譲渡 相続 合併又は分割の場合における通関業の許可の効果 )
 第 2 章通関業 第 1 節許可 第 2 章通関業第 1 節許可 3-8 削除 ( 譲渡 相続 合併又は分割の場合における通関業の許可の効果 ) 3-8 通関業について譲渡 相続 合併又は分割が行われた場合において 当該譲渡 相続 合併又は分割後 通関業を営もうとする者についての通関業の許可の要否の判定については 次による なお 当該譲渡等により通関業の許可が消滅した者については 法第 12 条第
第 2 章通関業 第 1 節許可 第 2 章通関業第 1 節許可 3-8 削除 ( 譲渡 相続 合併又は分割の場合における通関業の許可の効果 ) 3-8 通関業について譲渡 相続 合併又は分割が行われた場合において 当該譲渡 相続 合併又は分割後 通関業を営もうとする者についての通関業の許可の要否の判定については 次による なお 当該譲渡等により通関業の許可が消滅した者については 法第 12 条第
法人及び地方独立行政法人法 ( 平成 15 年法律第 118 号 ) 第 2 条第 1 項に規定する地方独立行政法人ホ医療法 ( 昭和 23 年法律第 205 号 ) 第 1 条の 2 第 2 項に規定する医療提供施設又は獣医療法 ( 平成 4 年法律第 46 号 ) 第 2 条第 2 項に規定する
 石川県薬物の濫用の防止に関する条例施行規則 ( 平成 26 年石川県規則第 30 号 :H26.10.6 公布 ) ( 趣旨 ) 第 1 条この規則は 石川県薬物の濫用の防止に関する条例 ( 平成 26 年石川県条例第 38 号 以下 条例 という ) の施行に関し必要な事項を定めるものとする ( 知事監視製品の販売等の届出等 ) 第 2 条条例第 12 条第 1 項の規定による届出は 別記様式第
石川県薬物の濫用の防止に関する条例施行規則 ( 平成 26 年石川県規則第 30 号 :H26.10.6 公布 ) ( 趣旨 ) 第 1 条この規則は 石川県薬物の濫用の防止に関する条例 ( 平成 26 年石川県条例第 38 号 以下 条例 という ) の施行に関し必要な事項を定めるものとする ( 知事監視製品の販売等の届出等 ) 第 2 条条例第 12 条第 1 項の規定による届出は 別記様式第
00 事務連絡案
 事務連絡 平成 30 年 10 月 30 日 都道府県知事 各保健所設置市 特別区 衛生検査所業務担当部 ( 局 ) 御中 厚生労働省医政局地域医療計画課 医療関連サービス室 衛生検査所において新たに作成する標準作業書及び台帳の参考例について 医療法等の一部を改正する法律 ( 平成 29 年法律第 57 号 以下 改正法 という ) の一部の規定が平成 30 年 12 月 1 日に施行されることに伴い
事務連絡 平成 30 年 10 月 30 日 都道府県知事 各保健所設置市 特別区 衛生検査所業務担当部 ( 局 ) 御中 厚生労働省医政局地域医療計画課 医療関連サービス室 衛生検査所において新たに作成する標準作業書及び台帳の参考例について 医療法等の一部を改正する法律 ( 平成 29 年法律第 57 号 以下 改正法 という ) の一部の規定が平成 30 年 12 月 1 日に施行されることに伴い
ICH-GCPとJ-GCPとの比較表
 参考資料 10 我が国の GCP と ICH-GCP の主な 1 治験の契約に関する規定 1-1 契約者に関する規定 1-2 実施医療機関の長との契約を規定したことに伴う規定 2 治験審査委員会 (IRB) に関する規定 2-1 IRB の設置に関する規定 2-2 IRB への審議依頼に関する規定 1/11 1. 治験の契約に関する規定 1-1. 契約者に関する規定 ICH-GCP 1.17( 用語の定義
参考資料 10 我が国の GCP と ICH-GCP の主な 1 治験の契約に関する規定 1-1 契約者に関する規定 1-2 実施医療機関の長との契約を規定したことに伴う規定 2 治験審査委員会 (IRB) に関する規定 2-1 IRB の設置に関する規定 2-2 IRB への審議依頼に関する規定 1/11 1. 治験の契約に関する規定 1-1. 契約者に関する規定 ICH-GCP 1.17( 用語の定義
治 験 実 施 標 準 業 務 手 順 書
 治験審査委員会標準業務手順書 < 企業治験 > 横浜労災病院 目 次 第 1 章治験審査委員会 2 目的と適用範囲 2 治験審査委員会の責務 2 治験審査委員会の設置及び構成 2 治験審査委員会の業務 3 治験審査委員会の運営 5 第 2 章治験審査委員会事務局 6 治験審査委員会事務局の設置と業務 6 第 3 章記録の保存と公開 7 記録の保存責任者 7 記録の保存期間 7 記録の公開 8 1 第
治験審査委員会標準業務手順書 < 企業治験 > 横浜労災病院 目 次 第 1 章治験審査委員会 2 目的と適用範囲 2 治験審査委員会の責務 2 治験審査委員会の設置及び構成 2 治験審査委員会の業務 3 治験審査委員会の運営 5 第 2 章治験審査委員会事務局 6 治験審査委員会事務局の設置と業務 6 第 3 章記録の保存と公開 7 記録の保存責任者 7 記録の保存期間 7 記録の公開 8 1 第
製造販売後調査事務手続き等 について
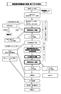 製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
医療用医薬品の市販直後調査の実施方法等について 平成 18 年 3 月 24 日付 : 厚生労働省医薬食品局安全対策課長 ( 薬食安発第号 号 ) 医療用医薬品の市販直後調査に関する Q&A について 平成 18 年 3 月 24 日付 : 厚生労働省医薬食品局安全対策課 ( 事務連
 医療用医薬品の市販直後調査の実施方法等について 平成 18 年 3 月 24 日付 : 厚生労働省医薬食品局安全対策課長 ( 薬食安発第号 0324001 号 ) 医療用医薬品の市販直後調査に関する Q&A について 平成 18 年 3 月 24 日付 : 厚生労働省医薬食品局安全対策課 ( 事務連絡 ) 医療用医薬品の全例調査方式による使用成績調査及び市販直後調査に関する Q&A について 平成
医療用医薬品の市販直後調査の実施方法等について 平成 18 年 3 月 24 日付 : 厚生労働省医薬食品局安全対策課長 ( 薬食安発第号 0324001 号 ) 医療用医薬品の市販直後調査に関する Q&A について 平成 18 年 3 月 24 日付 : 厚生労働省医薬食品局安全対策課 ( 事務連絡 ) 医療用医薬品の全例調査方式による使用成績調査及び市販直後調査に関する Q&A について 平成
事業者が行うべき措置については 匿名加工情報の作成に携わる者 ( 以下 作成従事者 という ) を限定するなどの社内規定の策定 作成従事者等の監督体制の整備 個人情報から削除した事項及び加工方法に関する情報へのアクセス制御 不正アクセス対策等を行うことが考えられるが 規定ぶりについて今後具体的に検討
 資料 2 匿名加工情報に関する委員会規則等の方向性について 1. 委員会規則の趣旨匿名加工情報は 個人情報を加工して 特定の個人を識別することができず かつ 作成の元となった個人情報を復元することができないようにすることで 個人情報の取扱いにおいて目的外利用 ( 第 16 条 ) や第三者提供 ( 第 23 条第 1 項 ) を行うに際して求められる本人の同意を不要とするなど その取扱いについて個人情報の取扱いに関する義務よりも緩やかな一定の規律が設けられるものである
資料 2 匿名加工情報に関する委員会規則等の方向性について 1. 委員会規則の趣旨匿名加工情報は 個人情報を加工して 特定の個人を識別することができず かつ 作成の元となった個人情報を復元することができないようにすることで 個人情報の取扱いにおいて目的外利用 ( 第 16 条 ) や第三者提供 ( 第 23 条第 1 項 ) を行うに際して求められる本人の同意を不要とするなど その取扱いについて個人情報の取扱いに関する義務よりも緩やかな一定の規律が設けられるものである
GVPの基礎
 京都府健康福祉部薬務課 平成 29 年 3 月 8 日 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令 (GVP 省令 ) GVP 省令 第一章 ( 総則 ) 第二章 ( 第一種製販の製造販売後安全管理の基準 ) 第三章 ( 第二種製販の製造販売後安全管理の基準 ) 第四章 ( 第三種製販の製造販売後安全管理の基準 ) 第五章 ( 雑則 ) 第一種 ~
京都府健康福祉部薬務課 平成 29 年 3 月 8 日 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令 (GVP 省令 ) GVP 省令 第一章 ( 総則 ) 第二章 ( 第一種製販の製造販売後安全管理の基準 ) 第三章 ( 第二種製販の製造販売後安全管理の基準 ) 第四章 ( 第三種製販の製造販売後安全管理の基準 ) 第五章 ( 雑則 ) 第一種 ~
Microsoft Word - 【発出版2】製造所取扱いに関するQ&A -
 薬食機参発 1020 第 4 号 平成 26 年 10 月 20 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いに関する質疑応答集 (Q&A) について 医療機器及び体外診断用医薬品の製造業の登録の範囲等については 医療機器及び体外診断用医薬品の製造業の取扱いについて
薬食機参発 1020 第 4 号 平成 26 年 10 月 20 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いに関する質疑応答集 (Q&A) について 医療機器及び体外診断用医薬品の製造業の登録の範囲等については 医療機器及び体外診断用医薬品の製造業の取扱いについて
Microsoft Word - (課×県・指定)【頭紙】「精神障害者保健福祉手帳の診断書の記入に当たって留意すべき事項について」等の一部改正について.rtf
 ( 別添 3) 精神科病院に入院する時の告知等に係る書面及び入退院の届出等について ( 平成 12 年 3 月 30 日障精第 22 号厚生省大臣官房障害保健福祉部精神保健福祉課長通知 ) 新旧対照表 ( 変更点は下線部 ) 改正後現行 障精第 2 2 号平成 12 年 3 月 30 日一部改正障精発第 0325001 号平成 17 年 3 月 25 日一部改正障精発第 0929005 号平成 18
( 別添 3) 精神科病院に入院する時の告知等に係る書面及び入退院の届出等について ( 平成 12 年 3 月 30 日障精第 22 号厚生省大臣官房障害保健福祉部精神保健福祉課長通知 ) 新旧対照表 ( 変更点は下線部 ) 改正後現行 障精第 2 2 号平成 12 年 3 月 30 日一部改正障精発第 0325001 号平成 17 年 3 月 25 日一部改正障精発第 0929005 号平成 18
一太郎 11/10/9/8 文書
 薬食審査発 0515 第 9 号 平成 25 年 5 月 15 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) 自ら治験を実施した者による治験副作用等報告について 自ら治験を実施した者による治験副作用等報告の取扱いについては 平成 16 年 3 月 30 日付薬食発第 0330001 号厚生労働省医薬食品局長通知 独立行政法人 医薬品医療機器総合機構に対する治験副作用等報告について
薬食審査発 0515 第 9 号 平成 25 年 5 月 15 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) 自ら治験を実施した者による治験副作用等報告について 自ら治験を実施した者による治験副作用等報告の取扱いについては 平成 16 年 3 月 30 日付薬食発第 0330001 号厚生労働省医薬食品局長通知 独立行政法人 医薬品医療機器総合機構に対する治験副作用等報告について
<4D F736F F D208EA18CB182C98AD682B782E995578F808BC696B18EE88F878F E7B8D732E646F6378>
 治験に関する標準業務手順書 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医薬品及び医療機器の臨床試験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和
治験に関する標準業務手順書 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医薬品及び医療機器の臨床試験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和
Ⅲ-3 試用医薬品に関する基準 平成 10 年 1 月 20 日公正取引委員会届出改定平成 13 年 3 月 19 日公正取引委員会届出改定平成 16 年 5 月 25 日公正取引委員会届出改定平成 17 年 3 月 29 日公正取引委員会届出改定平成 26 年 6 月 16 日公正取引委員会 消費
 Ⅲ-3 試用医薬品に関する基準 平成 10 年 1 月 20 日公正取引委員会届出改定平成 13 年 3 月 19 日公正取引委員会届出改定平成 16 年 5 月 25 日公正取引委員会届出改定平成 17 年 3 月 29 日公正取引委員会届出改定平成 26 年 6 月 16 日公正取引委員会 消費者庁長官届出 本基準は規約第 5 条第 3 号 施行規則第 2 条 ( 試用医薬品提供基準 ) に基づくものである
Ⅲ-3 試用医薬品に関する基準 平成 10 年 1 月 20 日公正取引委員会届出改定平成 13 年 3 月 19 日公正取引委員会届出改定平成 16 年 5 月 25 日公正取引委員会届出改定平成 17 年 3 月 29 日公正取引委員会届出改定平成 26 年 6 月 16 日公正取引委員会 消費者庁長官届出 本基準は規約第 5 条第 3 号 施行規則第 2 条 ( 試用医薬品提供基準 ) に基づくものである
目次 第 1 章治験審査委員会... 3 ( 目的と適用範囲 )... 3 ( 治験審査委員会の責務 )... 3 ( 治験審査委員会の設置及び構成 )... 3 ( 治験審査委員会の業務 )... 4 ( 治験審査委員会の運営 )... 6 第 2 章治験審査委員会事務局... 8 ( 治験審査委
 治験審査委員会標準業務手順書 < 医師主導治験 > 横浜労災病院 目次 第 1 章治験審査委員会... 3 ( 目的と適用範囲 )... 3 ( 治験審査委員会の責務 )... 3 ( 治験審査委員会の設置及び構成 )... 3 ( 治験審査委員会の業務 )... 4 ( 治験審査委員会の運営 )... 6 第 2 章治験審査委員会事務局... 8 ( 治験審査委員会事務局の設置と業務 )... 8
治験審査委員会標準業務手順書 < 医師主導治験 > 横浜労災病院 目次 第 1 章治験審査委員会... 3 ( 目的と適用範囲 )... 3 ( 治験審査委員会の責務 )... 3 ( 治験審査委員会の設置及び構成 )... 3 ( 治験審査委員会の業務 )... 4 ( 治験審査委員会の運営 )... 6 第 2 章治験審査委員会事務局... 8 ( 治験審査委員会事務局の設置と業務 )... 8
規程書
 独立行政法人国立病院機構栃木医療センター 受託研究取扱規程 平成 25 年 4 月 1 日 独立行政法人国立病院機構栃木医療センター受託研究取 扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構栃木医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程定めるところによる
独立行政法人国立病院機構栃木医療センター 受託研究取扱規程 平成 25 年 4 月 1 日 独立行政法人国立病院機構栃木医療センター受託研究取 扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構栃木医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程定めるところによる
実施医療機関治験審査委員会標準的業務手順書
 地方独立行政法人静岡市立静岡病院 治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 及び医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器
地方独立行政法人静岡市立静岡病院 治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 及び医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器
長崎大学病院治験審査委員会内規 平成 21 年 4 月 1 日 病院内規第 3 号 ( 趣旨 ) 第 1 条この内規は, 長崎大学病院における医薬品の臨床試験の実施に関する内規 ( 以下 治験内規 という ) 第 4 条第 2 項, 長崎大学病院における医療機器の臨床試験の実施に関する内規 ( 以下
 長崎大学病院治験審査委員会内規 平成 21 年 4 月 1 日 病院内規第 3 号 ( 趣旨 ) 第 1 条この内規は, 長崎大学病院における医薬品の臨床試験の実施に関する内規 ( 以下 治験内規 という ) 第 4 条第 2 項, 長崎大学病院における医療機器の臨床試験の実施に関する内規 ( 以下 医療機器治験内規 という ) 第 4 条第 2 項及び長崎大学病院における再生医療等製品の臨床試験の実施に関する内規
長崎大学病院治験審査委員会内規 平成 21 年 4 月 1 日 病院内規第 3 号 ( 趣旨 ) 第 1 条この内規は, 長崎大学病院における医薬品の臨床試験の実施に関する内規 ( 以下 治験内規 という ) 第 4 条第 2 項, 長崎大学病院における医療機器の臨床試験の実施に関する内規 ( 以下 医療機器治験内規 という ) 第 4 条第 2 項及び長崎大学病院における再生医療等製品の臨床試験の実施に関する内規
2 改正法による改正後の医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 以下 法 という ) において 新たに 再生医療等製品 が定義され ( 法第 2 条第 9 項 ) 再生医療等製品についての副作用等の報告義務が規定されたため ( 法第 68
 薬食発 1002 第 20 号 平成 26 年 10 月 2 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医薬品等の副作用等の報告について 薬事法等の一部を改正する法律及び薬事法等の一部を改正する法律の施行に伴う関係政令の整備等及び経過措置に関する政令の施行に伴う関係省令の整備等に関する省令 ( 平成 26 年厚生労働省令第 87 号 以下 改正省令 という ) が 平成 26
薬食発 1002 第 20 号 平成 26 年 10 月 2 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医薬品等の副作用等の報告について 薬事法等の一部を改正する法律及び薬事法等の一部を改正する法律の施行に伴う関係政令の整備等及び経過措置に関する政令の施行に伴う関係省令の整備等に関する省令 ( 平成 26 年厚生労働省令第 87 号 以下 改正省令 という ) が 平成 26
なお,PMDA メディナビでパスワードを設定済の方は, 共通のパスワードとなります (4) 登録完了 ( 図 2 ステップ 3) なお, 登録後, ログイン時は (1) で表示される画面で, ログイン画面へ をクリックし, メー ルアドレス及びパスワードを入力してください 図 1 PMDA メディナ
 2 マイ医薬品集作成サービス について 独立行政法人医薬品医療機器総合機構 (PMDA) では,PMDAメディナビ( 医薬品医療機器情報配信サービス ) にご登録いただいている方がご利用いただける登録 利用無料の追加機能として, マイ医薬品作成サービス を提供しています あらかじめ情報が必要な医薬品を登録しておけば, 添付文書情報等の最新情報を一覧で管理 閲覧することができる大変便利なサービスです
2 マイ医薬品集作成サービス について 独立行政法人医薬品医療機器総合機構 (PMDA) では,PMDAメディナビ( 医薬品医療機器情報配信サービス ) にご登録いただいている方がご利用いただける登録 利用無料の追加機能として, マイ医薬品作成サービス を提供しています あらかじめ情報が必要な医薬品を登録しておけば, 添付文書情報等の最新情報を一覧で管理 閲覧することができる大変便利なサービスです
神戸市立医療センター西市民病院治験審査委員会業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関
 神戸市立医療センター西市民病院治験審査委員会 標準業務手順書 目次 第 1 章治験審査委員会 目的と適用範囲 1 治験審査委員会の責務 1 治験審査委員会の設置及び構成 1 治験審査委員会の業務 2 治験審査委員会の運営 4 第 2 章治験審査委員会事務局治験審査委員会事務局の業務 6 第 3 章記録の保存記録の保存責任者 6 記録の保存期間 6 手順書の改訂 7 第 4 章情報公開会議の記録等の公表
神戸市立医療センター西市民病院治験審査委員会 標準業務手順書 目次 第 1 章治験審査委員会 目的と適用範囲 1 治験審査委員会の責務 1 治験審査委員会の設置及び構成 1 治験審査委員会の業務 2 治験審査委員会の運営 4 第 2 章治験審査委員会事務局治験審査委員会事務局の業務 6 第 3 章記録の保存記録の保存責任者 6 記録の保存期間 6 手順書の改訂 7 第 4 章情報公開会議の記録等の公表
鑑-H リンゼス錠他 留意事項通知の一部改正等について
 日医発第 617 号 ( 保 154) 平成 30 年 8 月 29 日 都道府県医師会長殿 日本医師会長横倉義武 医薬品医療機器等法上の効能 効果等の変更に伴う留意事項の一部改正等について 平成 30 年 8 月 21 日付け保医発 0821 第 1 号厚生労働省保険局医療課長通知により 添付資料の通り保険適用上の取扱いに関する留意事項が一部改正されましたのでお知らせ申し上げます 今回の改正は 同日付けで添付資料の医薬品の効能
日医発第 617 号 ( 保 154) 平成 30 年 8 月 29 日 都道府県医師会長殿 日本医師会長横倉義武 医薬品医療機器等法上の効能 効果等の変更に伴う留意事項の一部改正等について 平成 30 年 8 月 21 日付け保医発 0821 第 1 号厚生労働省保険局医療課長通知により 添付資料の通り保険適用上の取扱いに関する留意事項が一部改正されましたのでお知らせ申し上げます 今回の改正は 同日付けで添付資料の医薬品の効能
実施医療機関治験審査委員会標準的業務手順書
 静岡市立清水病院治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令 という
静岡市立清水病院治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器 GCP 省令 という
●薬事法等の一部を改正する法律案
 第一八三回 閣第七三号 薬事法等の一部を改正する法律案 ( 薬事法の一部改正 ) 第一条薬事法 ( 昭和三十五年法律第百四十五号 ) の一部を次のように改正する 題名を次のように改める 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 目次中 第一条 第二条 を 第一条 - 第二条 に 医薬品等の製造販売業 を 医薬品 医薬部外品及び化粧品の製造販売業 に 第四章の二登録認証機関 (
第一八三回 閣第七三号 薬事法等の一部を改正する法律案 ( 薬事法の一部改正 ) 第一条薬事法 ( 昭和三十五年法律第百四十五号 ) の一部を次のように改正する 題名を次のように改める 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 目次中 第一条 第二条 を 第一条 - 第二条 に 医薬品等の製造販売業 を 医薬品 医薬部外品及び化粧品の製造販売業 に 第四章の二登録認証機関 (
( 別添 2) ( 別添 2) 平成 14 年 9 月 27 日保発第 号の別添 2 組合管掌健康保険一括適用取扱要領 組合管掌健康保険一括適用取扱要領 ( 準則 ) 第 1 健康保険法 ( 以下 法 という ) 第 34 条第 1 項の規定による厚生労働大臣の承認 ( 以下 一括適
 ( 別添 1) 新 ( 別添 1) 健康保険 厚生年金保険一括適用承認基準 健康保険一括適用承認基準 健康保険法第 34 条第 1 項又は厚生年金保険法第 8 条の 2 の規定による厚生労働大 臣の承認 ( 以下 一括適用の承認 という ) は 次の各項に定める基準に適合する適 用事業所について行うものとする 健康保険法第 34 条の規定による厚生労働大臣の承認 ( 以下 一括適用の承認 と いう
( 別添 1) 新 ( 別添 1) 健康保険 厚生年金保険一括適用承認基準 健康保険一括適用承認基準 健康保険法第 34 条第 1 項又は厚生年金保険法第 8 条の 2 の規定による厚生労働大 臣の承認 ( 以下 一括適用の承認 という ) は 次の各項に定める基準に適合する適 用事業所について行うものとする 健康保険法第 34 条の規定による厚生労働大臣の承認 ( 以下 一括適用の承認 と いう
Microsoft PowerPoint - 3. 規格改正時の扱い R1_3
 JIS 改正対応 認証基準で引 する規格改正時の対応について 平成 28 年 11 月 14 日 一般社団法人日本画像医療システム工業会 法規 安全部会部会長古川浩 1 認証における規格の扱い 2 認証基準への適合要求について 指定高度管理医療機器等の製造販売の認証第 23 条の 2 の 23 厚生労働大臣が基準を定めて指定する高度管理医療機器 管理医療機器又管理医療機器又は体外診断用医薬品 ( 以下
JIS 改正対応 認証基準で引 する規格改正時の対応について 平成 28 年 11 月 14 日 一般社団法人日本画像医療システム工業会 法規 安全部会部会長古川浩 1 認証における規格の扱い 2 認証基準への適合要求について 指定高度管理医療機器等の製造販売の認証第 23 条の 2 の 23 厚生労働大臣が基準を定めて指定する高度管理医療機器 管理医療機器又管理医療機器又は体外診断用医薬品 ( 以下
