第16回医療機器レギュラトリーサイエンス研究会
|
|
|
- あつとし かつま
- 7 years ago
- Views:
Transcription
1 第 16 回医療機器レギュラトリーサイエンス研究会 再生医療等製品の開発と産業化にかかる課題 国立成育医療研究センター 梅澤明弘 1
2 ES 細胞をつくる 国立成育医療研究センター もみじの家 研究所 病院 運営棟
3 役に立つお薬 化成品 解熱薬 ステロイド バイオ薬 ホルモン抗体ワクチン再生医療製品
4 上市された再生医療等製品 軟骨表皮骨髄間質骨格筋
5 ES 細胞と ips 細胞は兄弟 ES 細胞 胚性幹細胞 Embryonic Stem Cells ips 細胞 人工多能性幹細胞 induced Pluripotent Stem Cells
6 国立成育医療研究センターにて ES 細胞をつくる
7 ES 細胞 ( 胚性幹細胞 ) エバンス先生 2007 年ノーベル医学生理学賞
8 ES 細胞 ( 胚性幹細胞 ) 無限に増える どんな細胞にもなれる
9 ES 細胞を用いた再生医療
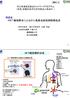
10 小児難病に対する ES 細胞を用いた再生医療尿素サイクル異常症アンモニアを肝臓で代謝できない へその緒を通じて投与し 肝臓へ
11 11 Products cell (hepatocyte) haes (ESC-drived) LB (ipsc-derived) HepaStem (stromal cell)
12 12 haes 原料 phaes-wcb 治験薬 HAES 50 μm
13 13 全体計画 - 治験届提出まで - A) 高アンモニア血症を生じる尿素サイクル異常症に対する治験 a. 治療プロトコールの作成 b. 医師主導治験 B) 品質管理 C) 効力裏付試験 D) 非臨床安全性試験 E) 投与方法の標準化と教育訓練 F) バンクの維持 管理
14 14 臨床試験 適応案 重症高アンモニア血症を生じる先天代謝異常症の患者で 低体重 ( 体重 6kg 以下 ) 循環器疾患等合併症 ドナー不在 などの理由により 即時的な肝臓移植手術は困難であるが 将来肝臓移植手術が可能と考えられる場合で 食事療法 薬物治療 血液浄化療法等 通常の医療による血中アンモニア値の制御が困難で このままでは重篤な不可逆的脳障害を起こすと考えられる症例
15 Treatment protocol (design) Diagnosis Injection haes Liver transplantation Birth Portal vein Best care Injection of hesc-derived hepatocytes into portal vein or umbilical vein
16 haes 投与 Cell injection from portal vein 16
17 治験 17
18 臨床利用のための新規 ES 細胞の樹立とストック作製に関する研究 18 最新の国際動向もふまえ ガイドラインをまとめる 新規にES 細胞の樹立及びストック作製 広く社会に公開し 社会的な合意を形成する
19 我が国のヒト ES 細胞株 ヒト ES 細胞株の名称樹立機関の名称樹立完了報告書の提出日 1 KhES-1 京都大学再生医科学研究所平成 15 年 8 月 8 日 KhES-2 KhES-3 KhES-4 KhES-5 SEES1 SEES2 SEES3 同上同上独立行政法人国立成育医療研究センター研究所 平成 15 年 11 月 28 日 平成 20 年 12 月 5 日 平成 22 年 11 月 5 日 SEES4 同上平成 23 年 12 月 5 日 SEES5 SEES6 SEES7 同上 平成 25 年 1 月 29 日 1 ES 樹立 分配指針 17 条に基づく国への提出日 19
20 弊所パイプライン上の製品 ES 細胞由来 肝細胞 間質細胞 軟骨 開発品 治験薬 開発品 20
21 Origin of mesenchymal stromal cells ⅰ) Bone marrow ⅱ) Fat ⅲ) Fetus ⅳ) Menstrual blood ⅴ) Endometrium ⅵ) Umbilical cord ⅶ) Placenta ⅷ) Amnion ⅸ) Embryonic stem cell ⅹ) ips cell
22 Origin of knst Stromal cells = 間質細胞 kanshitsu knst Umezawa, A., et al.. Mol. Cell. Biol. 11: , 1991
23 Target diseases for cell-based therapy using knst Spinal cord injury Cerebral infarction Lysosomal storage disease Scarless wound healing Ischemic limb Cardiovascular disease Duchenne muscular dystrophy
24 Toluidine Blue 24
25 Toluidine Blue 25
26 ヒト ES 細胞の取扱いに関する制度 新制度 基礎的研究 臨床研究 治験 医療 樹立手続 & 樹立の倫理 ES 樹立 分配指針 樹立指針 (H26 年 11 月 25 日 ) 品質 安全性 利用手続 & 利用の倫理 分配使用指針 (H26 年 11 月 25 日 ) 再生医療等安全性確保法 (H26 年 11 月 25 日 ) 医薬品医療機器等法 ( 改正薬事法 ) 再生医療等安全性確保法 文科省厚労省文科 厚労両省共管 予防 診断及び治療のみを目的としたもの ( 文部科学省 ) 26
27 ヒト ES 細胞の主な流れと適用される手続き 基礎的研究利用のみの場合 再生医療等安全性確保法の適用を受ける場合 医薬品医療機器等法の適用を受ける場合 樹立指針分配 使用指針 樹立機関分配機関使用機関 加工 ES のみ 樹立機関細胞培養加工施設 使用機関細胞培養加工施設 細胞培養加工施設 樹立機関 使用機関 ( 治験依頼者 or 製造販売業 ) 治験依頼者 or 製造販売業 使用機関 再生医療等提供機関 医療機関 基礎的研究機関 再生医療等安全確保法 医薬品医療機器等法 : ヒト ES 細胞の流れ : ヒト ES 細胞由来の分化細胞の流れ 27
28 CMC Development Clinical Study Approval Non- Clinical Study Phase 1 Phase 2 Phase 3 Post- Approve l Target product Profile Establishment of Design Quality and Product Quality by CMC study Process Validation Control Strategy Control Strategy Control Strategy Quality Attributes Process Parameters CQA CPP Control Strategy Consistency Equivalency Knowledge Management/Quality Risk Management GMP for Investigational Product GCTP
29 Establishment of Commercial Manufacturing Stage Research and Development Transfer Commercial Manufacturing Knowledge management and Techical Transfer Activity Knowledge Management in Research &/or Development Division Investigational products Production (Pilot &/or Commercial Scale) Technical Transfer Control Strategy PV Knowledge Knowledge Management in Manufacturing Plant Control Strategy Commercial Batches Manufacturing Approach of Evaluation Manufacturing Process Design Development Manufacturing Process Improvement Verification Process of Investigational product Validation Analytical method, Computer Systems, Sterility assurance Manufacturing Process Verification Manufacturing Process Process Monitoring Validation Qualification of Equipment Process Validation/Verification Change Control Revalidation Consistency of Process and Product Quality
30 GMP for Investigational products Management & Supervision System (Release, Deviation, Change Control, Self-inspection, Training/Education, Complaint, Recall) Quality Control System (Laboratory system) Supplier Management System Product Quality Review Validation / Verification Manufacturing Control System (operation performance of process, Sterility assurance, Product quality monitoring) Facility & Equipment System (qualification, calibration, maintenance) Document Management System (Product master file, specification, statement, SOPs, record) Reflecting product marketing authorization documents Quality Risk Management / Knowledge Management
31 国立成育医療研究センターが提供する再生医療製品 ES 細胞由来 肝細胞 治験薬 間質細胞 開発品 軟骨製品 開発品
32 病気の克服に向けて 医療従事者 患者 AMED 病 気 産業界 行政 研究者
を行った 2.iPS 細胞の由来の探索 3.MEF および TTF 以外の細胞からの ips 細胞誘導 4.Fbx15 以外の遺伝子発現を指標とした ips 細胞の樹立 ips 細胞はこれまでのところレトロウイルスを用いた場合しか樹立できていない また 4 因子を導入した線維芽細胞の中で ips 細
 平成 19 年度実績報告 免疫難病 感染症等の先進医療技術 平成 15 年度採択研究代表者 山中伸弥 京都大学物質 - 細胞統合システム拠点 / 再生医科学研究所 教授 真に臨床応用できる多能性幹細胞の樹立 1. 研究実施の概要 胚性幹 (ES) 細胞は受精後間もない胚から樹立する幹細胞であり 様々な細胞へと分化する多能性を維持したまま 長期かつ大量に培養することが可能であることから 脊髄損傷 若年性糖尿病
平成 19 年度実績報告 免疫難病 感染症等の先進医療技術 平成 15 年度採択研究代表者 山中伸弥 京都大学物質 - 細胞統合システム拠点 / 再生医科学研究所 教授 真に臨床応用できる多能性幹細胞の樹立 1. 研究実施の概要 胚性幹 (ES) 細胞は受精後間もない胚から樹立する幹細胞であり 様々な細胞へと分化する多能性を維持したまま 長期かつ大量に培養することが可能であることから 脊髄損傷 若年性糖尿病
スライド 1
 平成 25 年度 GMP 事例研究会 プロセスバリデーション / 継続的工程確認の今後の方向性 独立行政法人医薬品医療機器総合機構品質管理部調査専門員 原賢太郎 ( 平成 25 年 9 月 17 日 ( 火 ) 東京会場 ) 大野勝人 ( 平成 25 年 9 月 20 日 ( 金 ) 大阪会場 ) 1 目次 1 はじめに 2 バリデーション基準の改訂の背景 3 基本的な考え方 4 製品ライフサイクルを通した管理
平成 25 年度 GMP 事例研究会 プロセスバリデーション / 継続的工程確認の今後の方向性 独立行政法人医薬品医療機器総合機構品質管理部調査専門員 原賢太郎 ( 平成 25 年 9 月 17 日 ( 火 ) 東京会場 ) 大野勝人 ( 平成 25 年 9 月 20 日 ( 金 ) 大阪会場 ) 1 目次 1 はじめに 2 バリデーション基準の改訂の背景 3 基本的な考え方 4 製品ライフサイクルを通した管理
Microsoft Word - 【プレスリリース・J】毛包再生非臨床 説明文 最終版.docx
 2018 年 6 月 4 日 毛包器官再生医療に向けた非臨床試験開始について 株式会社オーガンテクノロジーズ ( 代表取締役 : 杉村泰宏以下 オーガンテクノロジーズ ) 並びに国立研究開発法人理化学研究所 ( 理事長 : 松本紘以下 理研 ) は 再生医療分野である 毛包器官再生による脱毛症の治療 に向けた臨床研究の前段階である非臨床試験を開始することといたしましたのでお知らせいたします 1. 脱毛症とその治療
2018 年 6 月 4 日 毛包器官再生医療に向けた非臨床試験開始について 株式会社オーガンテクノロジーズ ( 代表取締役 : 杉村泰宏以下 オーガンテクノロジーズ ) 並びに国立研究開発法人理化学研究所 ( 理事長 : 松本紘以下 理研 ) は 再生医療分野である 毛包器官再生による脱毛症の治療 に向けた臨床研究の前段階である非臨床試験を開始することといたしましたのでお知らせいたします 1. 脱毛症とその治療
査を実施し 必要に応じ適切な措置を講ずること (2) 本品の警告 効能 効果 性能 用法 用量及び使用方法は以下のとお りであるので 特段の留意をお願いすること なお その他の使用上の注意については 添付文書を参照されたいこと 警告 1 本品投与後に重篤な有害事象の発現が認められていること 及び本品
 薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
マスターバッチ本文
 Masterbatches Technical Information 1 3 7 9 11 13 15 17 19 21 23 25 27 29 31 32 33 35 40 41 42 43 45 47 48 49 51 52 53 55 57 58 58 58 58 59 61 63 64 65 66 1 masterbatches 2 masterbatches 3 masterbatches
Masterbatches Technical Information 1 3 7 9 11 13 15 17 19 21 23 25 27 29 31 32 33 35 40 41 42 43 45 47 48 49 51 52 53 55 57 58 58 58 58 59 61 63 64 65 66 1 masterbatches 2 masterbatches 3 masterbatches
01 再生医療新法関係参考資料(法正局後)
 再生医療とは 再生医療 再生医療等安全確保法案について資料 4- 再生医療とは 病気やけがで機能不全になった組織 臓器を再生させる医療であり 創薬のための再生医療技術の応用にも期待されている 医療 ES 細胞 ( 胚性幹細胞 ) 受精卵から作製された細胞 倫理面の課題あり 創薬 ヒト ips 細胞等から目的とするヒトの細胞を作製し 薬物の安全性等を確認 受精卵 ES 細胞 目 ヒト ips 細胞 筋肉
再生医療とは 再生医療 再生医療等安全確保法案について資料 4- 再生医療とは 病気やけがで機能不全になった組織 臓器を再生させる医療であり 創薬のための再生医療技術の応用にも期待されている 医療 ES 細胞 ( 胚性幹細胞 ) 受精卵から作製された細胞 倫理面の課題あり 創薬 ヒト ips 細胞等から目的とするヒトの細胞を作製し 薬物の安全性等を確認 受精卵 ES 細胞 目 ヒト ips 細胞 筋肉
JIS Z 9001:1998JIS Z 9002:1998 ISO/IEC 17025ISO/IEC Guide 25
 JIS Q 17025 IDT, ISO/IEC 17025 IT JIS Z 9001:1998JIS Z 9002:1998 ISO/IEC 17025ISO/IEC Guide 25 JIS Q 17025 IDT, ISO/IEC 17025 IT IT JIS Q 17025ISO/IEC 17025 (2) JIS Z 9358 ISO/IEC Guide 58 (3) testing
JIS Q 17025 IDT, ISO/IEC 17025 IT JIS Z 9001:1998JIS Z 9002:1998 ISO/IEC 17025ISO/IEC Guide 25 JIS Q 17025 IDT, ISO/IEC 17025 IT IT JIS Q 17025ISO/IEC 17025 (2) JIS Z 9358 ISO/IEC Guide 58 (3) testing
臨床評価とは何か ( 独 ) 医薬品医療機器総合機構医療機器審査第一部方眞美
 臨床評価とは何か ( 独 ) 医薬品医療機器総合機構医療機器審査第一部方眞美 本日の Agenda 1. 臨床評価とは 2. 医療機器の特性を踏まえた有効性 安全性評価 3. 各国の規制の違い 4. 臨床評価報告書について 5. 臨床評価報告書の概念 6. 臨床研究と治験の違いは? 7. 文献評価の問題点 8. 治験活性化にむけて 臨床評価 とは そのものの有効性と安全性をヒトで評価すること 自己認証の欧州から出てきた概念
臨床評価とは何か ( 独 ) 医薬品医療機器総合機構医療機器審査第一部方眞美 本日の Agenda 1. 臨床評価とは 2. 医療機器の特性を踏まえた有効性 安全性評価 3. 各国の規制の違い 4. 臨床評価報告書について 5. 臨床評価報告書の概念 6. 臨床研究と治験の違いは? 7. 文献評価の問題点 8. 治験活性化にむけて 臨床評価 とは そのものの有効性と安全性をヒトで評価すること 自己認証の欧州から出てきた概念
untitled
 - 1 - - 2 - - 3 - - 4 - - 5 - - 6 - - 7 - - 8 - - 9 - ..... - 10 - - 11 - - 12 - - 13 - - 14 - - 15 - - 16 - -- - 17 - - 18 - - 19 - - 20 - - 21 - - 22 - - 23 - - 24 - - 25 - - 26 - - 27 - - 28 - - 29
- 1 - - 2 - - 3 - - 4 - - 5 - - 6 - - 7 - - 8 - - 9 - ..... - 10 - - 11 - - 12 - - 13 - - 14 - - 15 - - 16 - -- - 17 - - 18 - - 19 - - 20 - - 21 - - 22 - - 23 - - 24 - - 25 - - 26 - - 27 - - 28 - - 29
研究成果報告書
 様式 C-19 科学研究費助成事業 ( 科学研究費補助金 ) 研究成果報告書 研究成果の概要 ( 和文 ): 平成 24 年 5 月 15 日現在 機関番号 :32612 研究種目 : 基盤研究 (C) 研究期間 :2009~2011 課題番号 :21592265 研究課題名 ( 和文 ) 再生に向けたヒト人工多能性幹細胞を用いた網膜変性疾患の病態解明 研究課題名 ( 英文 ) AnanlysisoftheretinaldegenerativediseasesusingiPScells
様式 C-19 科学研究費助成事業 ( 科学研究費補助金 ) 研究成果報告書 研究成果の概要 ( 和文 ): 平成 24 年 5 月 15 日現在 機関番号 :32612 研究種目 : 基盤研究 (C) 研究期間 :2009~2011 課題番号 :21592265 研究課題名 ( 和文 ) 再生に向けたヒト人工多能性幹細胞を用いた網膜変性疾患の病態解明 研究課題名 ( 英文 ) AnanlysisoftheretinaldegenerativediseasesusingiPScells
スライド 1
 新技術で分離した ヒト骨質由来微小幹細胞の医療応用 薗田精昭 関西医科大学大学院医学研究科先端医療学専攻修復医療応用系幹細胞生物学 2001 背景 (1): 微小幹細胞とは Journal of Cellular Biochemistry 80;455-460(2001) 微小幹細胞に関する最初の報告生体の組織内に非常に小さな spore-like stem cell が存在することが初めて報告された
新技術で分離した ヒト骨質由来微小幹細胞の医療応用 薗田精昭 関西医科大学大学院医学研究科先端医療学専攻修復医療応用系幹細胞生物学 2001 背景 (1): 微小幹細胞とは Journal of Cellular Biochemistry 80;455-460(2001) 微小幹細胞に関する最初の報告生体の組織内に非常に小さな spore-like stem cell が存在することが初めて報告された
PowerPoint プレゼンテーション
 自己紹介 Self-introduction 岡山大学理学部線虫 C. elegans の骨格筋の発生 京都大学大学院医学研究科心筋肥大の転写機構 ES/iPS 細胞の心筋分化 国立循環器病研究センター動脈硬化の発生機序 ( 平滑筋 ) ミネソタ大学幹細胞研究所骨格筋幹細胞の増殖 分化 信州大学農学部 / バイオメディカル研究所 分子細胞機能学研究室 (C101) TEL : 0265-77-1426(
自己紹介 Self-introduction 岡山大学理学部線虫 C. elegans の骨格筋の発生 京都大学大学院医学研究科心筋肥大の転写機構 ES/iPS 細胞の心筋分化 国立循環器病研究センター動脈硬化の発生機序 ( 平滑筋 ) ミネソタ大学幹細胞研究所骨格筋幹細胞の増殖 分化 信州大学農学部 / バイオメディカル研究所 分子細胞機能学研究室 (C101) TEL : 0265-77-1426(
PT51_p69_77.indd
 臨床講座 特発性血小板減少性紫斑病 ITP の登場によりその危険性は下がりました また これまで 1 ヘリコバクター ピロリの除菌療法 治療の中心はステロイドであり 糖尿病 不眠症 胃炎 ヘリコバクター ピロリ ピロリ菌 は 胃炎や胃 十二指 満月様顔貌と肥満などに悩む患者が多かったのですが 腸潰瘍に深く関わっています ピロリ菌除菌療法により約 受容体作動薬によりステロイドの減量 6 割の患者で 血小板数が
臨床講座 特発性血小板減少性紫斑病 ITP の登場によりその危険性は下がりました また これまで 1 ヘリコバクター ピロリの除菌療法 治療の中心はステロイドであり 糖尿病 不眠症 胃炎 ヘリコバクター ピロリ ピロリ菌 は 胃炎や胃 十二指 満月様顔貌と肥満などに悩む患者が多かったのですが 腸潰瘍に深く関わっています ピロリ菌除菌療法により約 受容体作動薬によりステロイドの減量 6 割の患者で 血小板数が
制度から見る薬剤師の役割
 平成 27 年 7 月 23 日第 32 回 ICH 即時報告会全電通労働会館 ( 全電通ホール ) ICH Q12: Technical and Regulatory Considerations for Pharmaceutical Product Lifecycle Management 医薬品医療機器総合機構 再生医療製品等審査部 岸岡康博 1 本日の内容 本トピックの目的 リスボン会議後から福岡会議までの活動
平成 27 年 7 月 23 日第 32 回 ICH 即時報告会全電通労働会館 ( 全電通ホール ) ICH Q12: Technical and Regulatory Considerations for Pharmaceutical Product Lifecycle Management 医薬品医療機器総合機構 再生医療製品等審査部 岸岡康博 1 本日の内容 本トピックの目的 リスボン会議後から福岡会議までの活動
<4D F736F F F696E74202D2097D58FB08E8E8CB1838F815B834E F197D58FB E96D8816A66696E616C CF68A4A2E >
 再生医療等製品の非臨床安全性評価の考え方 ex vivo 遺伝子治療を中心に 独立行政法人医薬品医療機器総合機構 (PMDA) 再生医療製品等審査部 真木一茂 様式 1-B 第 24 回日本遺伝子細胞治療学会学術集会 CO I 開示 発表者名 : 真木一茂 演題発表に関連し 開示すべき CO I 関係にある企業などはありません 2 1 本日の話 1.Ex vivo 遺伝子治療について 2. 治験開始に必要な非臨床試験
再生医療等製品の非臨床安全性評価の考え方 ex vivo 遺伝子治療を中心に 独立行政法人医薬品医療機器総合機構 (PMDA) 再生医療製品等審査部 真木一茂 様式 1-B 第 24 回日本遺伝子細胞治療学会学術集会 CO I 開示 発表者名 : 真木一茂 演題発表に関連し 開示すべき CO I 関係にある企業などはありません 2 1 本日の話 1.Ex vivo 遺伝子治療について 2. 治験開始に必要な非臨床試験
2017 年 12 月 15 日 報道機関各位 国立大学法人東北大学大学院医学系研究科国立大学法人九州大学生体防御医学研究所国立研究開発法人日本医療研究開発機構 ヒト胎盤幹細胞の樹立に世界で初めて成功 - 生殖医療 再生医療への貢献が期待 - 研究のポイント 注 胎盤幹細胞 (TS 細胞 ) 1 は
 2017 年 12 月 15 日 報道機関各位 国立大学法人東北大学大学院医学系研究科国立大学法人九州大学生体防御医学研究所国立研究開発法人日本医療研究開発機構 ヒト胎盤幹細胞の樹立に世界で初めて成功 - 生殖医療 再生医療への貢献が期待 - 研究のポイント 注 胎盤幹細胞 (TS 細胞 ) 1 は 自己複製能と胎盤の細胞に分化する能力を持った胎盤由来の特殊な細胞である 本研究において ヒト胎盤の細胞
2017 年 12 月 15 日 報道機関各位 国立大学法人東北大学大学院医学系研究科国立大学法人九州大学生体防御医学研究所国立研究開発法人日本医療研究開発機構 ヒト胎盤幹細胞の樹立に世界で初めて成功 - 生殖医療 再生医療への貢献が期待 - 研究のポイント 注 胎盤幹細胞 (TS 細胞 ) 1 は 自己複製能と胎盤の細胞に分化する能力を持った胎盤由来の特殊な細胞である 本研究において ヒト胎盤の細胞
ALDEFLUOR® 造血幹細胞/造血前駆細胞の新しい同定試薬
 ALDEFLUOR Immunophenotyping ALDEFLUOR Primitive Mature or ALDH Aldehyde Dehydrogenase(ALDH) ALDH Stemness ALDH Primitive Mature ALDEFLUOR Intracellular enzymatic assay ALDEFLUOR BAAA ALDH BAA ALDH BAA
ALDEFLUOR Immunophenotyping ALDEFLUOR Primitive Mature or ALDH Aldehyde Dehydrogenase(ALDH) ALDH Stemness ALDH Primitive Mature ALDEFLUOR Intracellular enzymatic assay ALDEFLUOR BAAA ALDH BAA ALDH BAA
PowerPoint プレゼンテーション
 研究開発課題名難病 希少疾患の医薬品開発におけるクリニカルイノベーションネットワーク構想の推進を目指した疾患登録システム ( 患者レジストリ ) の構築 研究開発代表者 国立研究開発法人国立精神 神経医療研究センター 資料 2-3 トランスレーショナルメディカルセンター 臨床研究支援室長 発表内容 本研究の目標 実施体制 Remudy の実績と課題 目指すもの 疾患登録システム レジストリの信頼性について
研究開発課題名難病 希少疾患の医薬品開発におけるクリニカルイノベーションネットワーク構想の推進を目指した疾患登録システム ( 患者レジストリ ) の構築 研究開発代表者 国立研究開発法人国立精神 神経医療研究センター 資料 2-3 トランスレーショナルメディカルセンター 臨床研究支援室長 発表内容 本研究の目標 実施体制 Remudy の実績と課題 目指すもの 疾患登録システム レジストリの信頼性について
( 参考資料 1) US-FDA のシステム (6 システム ) 査察の枠組みについて Page 2 of 5 pages (STRATEGY: 戦略 ) C. A Scheme of Systems for the Manufacture of Drugs/Drug Products 原薬 / 医
 ( 参考資料 1) US-FDA のシステム (6 システム ) 査察の枠組みについて Page 1 of 5 pages 2017.09. 20 ( 参考資料 1) US-FDA のシステム (6 システム ) 査察の枠組みについて ファルマ ソリューションズ この文書は 米国 FDA が医薬品製造所の GMP 査察を行う場合の査察官用のマニュアルである COMPLIANCE PROGRAM GUIDANCE
( 参考資料 1) US-FDA のシステム (6 システム ) 査察の枠組みについて Page 1 of 5 pages 2017.09. 20 ( 参考資料 1) US-FDA のシステム (6 システム ) 査察の枠組みについて ファルマ ソリューションズ この文書は 米国 FDA が医薬品製造所の GMP 査察を行う場合の査察官用のマニュアルである COMPLIANCE PROGRAM GUIDANCE
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 <その他分野 ( 消化器官用薬 解毒剤 その他 )> 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号
 資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
Microsoft PowerPoint - 資料3-8_(B理研・古関)拠点B理研古関120613
 再生医療実現拠点ネットワークプログラム 疾患 組織別実用化研究拠点 ( 拠点 B) 資料 3-8 課題名 : NKT 細胞再生によるがん免疫治療技術開発拠点 研究代表者 : 理化学研究所古関明彦分担研究機関 : 千葉大学慶應義塾大学国立病院機構 1 NKT 細胞標的治療の抗腫瘍効果 B16 マウスメラノーマ細胞 agalcer/dcs (3 x 10 6 ) 7d 14d NKT 細胞標的治療 agalcer/dcs
再生医療実現拠点ネットワークプログラム 疾患 組織別実用化研究拠点 ( 拠点 B) 資料 3-8 課題名 : NKT 細胞再生によるがん免疫治療技術開発拠点 研究代表者 : 理化学研究所古関明彦分担研究機関 : 千葉大学慶應義塾大学国立病院機構 1 NKT 細胞標的治療の抗腫瘍効果 B16 マウスメラノーマ細胞 agalcer/dcs (3 x 10 6 ) 7d 14d NKT 細胞標的治療 agalcer/dcs
テルモ株式会社事業戦略説明会 THERAPEUTIC SYSTEMS & CELL PROCESSING MARK FLOWER GLOBAL MARKETING December 5, 2011
 テルモ株式会社事業戦略説明会 THERAPEUTIC SYSTEMS & CELL PROCESSING MARK FLOWER GLOBAL MARKETING December 5, 2011 再生医療 細胞治療 細胞処理 再生医療は 急速に進化している学際的な医療分野です 生物学 化学 物理学などの様々な基礎学術が 細胞治療の領域において 素材 デバイス 治療戦略に応用されています 再生医療
テルモ株式会社事業戦略説明会 THERAPEUTIC SYSTEMS & CELL PROCESSING MARK FLOWER GLOBAL MARKETING December 5, 2011 再生医療 細胞治療 細胞処理 再生医療は 急速に進化している学際的な医療分野です 生物学 化学 物理学などの様々な基礎学術が 細胞治療の領域において 素材 デバイス 治療戦略に応用されています 再生医療
 identity outreach aggressive casework assessment accountability action system accessibility advocacy medical model enabling medical social work intergroup work intervention intake integration informal
identity outreach aggressive casework assessment accountability action system accessibility advocacy medical model enabling medical social work intergroup work intervention intake integration informal
2-工業会活動.indd
 平 成 27 年 12 月 第 744 号 1.はじめに IAQG 2015 10 19 22 IAQG 2 4 38 2. 会 議 概 要 1 9100 2016 9100 CD Coordination Draft 545 APAQG 88 199 9100 IAQG9100 2016 4 2 9104-3 9104-3 2016 3 JAQG 9 3 JAQG 4 IAQG IAQG 3. 各
平 成 27 年 12 月 第 744 号 1.はじめに IAQG 2015 10 19 22 IAQG 2 4 38 2. 会 議 概 要 1 9100 2016 9100 CD Coordination Draft 545 APAQG 88 199 9100 IAQG9100 2016 4 2 9104-3 9104-3 2016 3 JAQG 9 3 JAQG 4 IAQG IAQG 3. 各
<4D F736F F D20322E CA48B8690AC89CA5B90B688E38CA E525D>
 PRESS RELEASE(2017/07/18) 九州大学広報室 819-0395 福岡市西区元岡 744 TEL:092-802-2130 FAX:092-802-2139 MAIL:[email protected] URL:http://www.kyushu-u.ac.jp 造血幹細胞の過剰鉄が血液産生を阻害する仕組みを解明 骨髄異形成症候群の新たな治療法開発に期待 - 九州大学生体防御医学研究所の中山敬一主幹教授
PRESS RELEASE(2017/07/18) 九州大学広報室 819-0395 福岡市西区元岡 744 TEL:092-802-2130 FAX:092-802-2139 MAIL:[email protected] URL:http://www.kyushu-u.ac.jp 造血幹細胞の過剰鉄が血液産生を阻害する仕組みを解明 骨髄異形成症候群の新たな治療法開発に期待 - 九州大学生体防御医学研究所の中山敬一主幹教授
STAP現象の検証の実施について
 STAP 現象の検証の実施について 実験総括責任者 : 独立行政法人理化学研究所発生 再生科学総合研究センター特別顧問 ( 相澤研究ユニット研究ユニットリーダー兼務 ) 相澤慎一 研究実施責任者 : 独立行政法人理化学研究所発生 再生科学総合研究センター多能性幹細胞研究プロジェクトプロジェクトリーダー丹羽仁史 2014 年 4 月 7 日 独立行政法人理化学研究所 1 検証実験の目的 STAP 現象が存在するか否かを一から検証する
STAP 現象の検証の実施について 実験総括責任者 : 独立行政法人理化学研究所発生 再生科学総合研究センター特別顧問 ( 相澤研究ユニット研究ユニットリーダー兼務 ) 相澤慎一 研究実施責任者 : 独立行政法人理化学研究所発生 再生科学総合研究センター多能性幹細胞研究プロジェクトプロジェクトリーダー丹羽仁史 2014 年 4 月 7 日 独立行政法人理化学研究所 1 検証実験の目的 STAP 現象が存在するか否かを一から検証する
ヒト脂肪組織由来幹細胞における外因性脂肪酸結合タンパク (FABP)4 FABP 5 の影響 糖尿病 肥満の病態解明と脂肪幹細胞再生治療への可能性 ポイント 脂肪幹細胞の脂肪分化誘導に伴い FABP4( 脂肪細胞型 ) FABP5( 表皮型 ) が発現亢進し 分泌されることを確認しました トランスク
 平成 28 年 12 月 19 日 ヒト脂肪組織由来幹細胞における外因性脂肪酸結合タンパク (FABP)4 FABP 5 の影響 糖尿病 肥満の病態解明と脂肪幹細胞再生治療への可能性 名古屋大学大学院医学系研究科 ( 研究科長 髙橋雅英 ) 泌尿器科学分野の山本徳則 ( やまもととくのり ) 准教授 後藤百万 ( ごとうももかず ) 教授と札幌医科大学内分泌内科の古橋眞人 ( ふるはしまさと ) 講師
平成 28 年 12 月 19 日 ヒト脂肪組織由来幹細胞における外因性脂肪酸結合タンパク (FABP)4 FABP 5 の影響 糖尿病 肥満の病態解明と脂肪幹細胞再生治療への可能性 名古屋大学大学院医学系研究科 ( 研究科長 髙橋雅英 ) 泌尿器科学分野の山本徳則 ( やまもととくのり ) 准教授 後藤百万 ( ごとうももかず ) 教授と札幌医科大学内分泌内科の古橋眞人 ( ふるはしまさと ) 講師
Agenda Benefit/Risk Assessmentとは Life-Cycleを通したBenefit/Risk Assessment 開発段階 市販後 2
 Benefit/Risk Balance の向上に向けて - 非臨床から臨床へ 臨床から非臨床へ ( 独 ) 医薬品医療機器総合機構 佐藤淳子 第 35 回日本臨床薬理学会学術総会 2014.12.5. 松山非臨床と臨床のクロストークによる副作用リスクに対する科学的なアプローチ 1 Agenda Benefit/Risk Assessmentとは Life-Cycleを通したBenefit/Risk
Benefit/Risk Balance の向上に向けて - 非臨床から臨床へ 臨床から非臨床へ ( 独 ) 医薬品医療機器総合機構 佐藤淳子 第 35 回日本臨床薬理学会学術総会 2014.12.5. 松山非臨床と臨床のクロストークによる副作用リスクに対する科学的なアプローチ 1 Agenda Benefit/Risk Assessmentとは Life-Cycleを通したBenefit/Risk
学報_台紙20まで
 M 平成23年度 科学研究費補助金の決定 研究推進課 平成23年度科学研究費補助金 文部科学省 独 日本学術振興会 が決定しま した 新学術領域研究及び若手研究 スタートアップ 等を除く平成23年5月6日 現在の状況は表のとおりです 来年度に向け より積極的な申請をよろしくお願いします 奈 良 県 立 医 科 大 学 学 報 12 採択件数 金額 H23年度 145件 H22年度比
M 平成23年度 科学研究費補助金の決定 研究推進課 平成23年度科学研究費補助金 文部科学省 独 日本学術振興会 が決定しま した 新学術領域研究及び若手研究 スタートアップ 等を除く平成23年5月6日 現在の状況は表のとおりです 来年度に向け より積極的な申請をよろしくお願いします 奈 良 県 立 医 科 大 学 学 報 12 採択件数 金額 H23年度 145件 H22年度比
PowerPoint プレゼンテーション
 背景 クリニカル イノベーション ネットワーク (CIN) の背景と概要 資料 3 新しい医薬品 医療機器等の開発に当たっては 世界的にコストが高騰している 特に 医薬品にあっては タフツ大学の試算によると 1 新薬当たり $2,558 million( 約 3,000 億円 ) 要するといわれている (Nov. 18, 2014, Tufts Center for the Study of Drug
背景 クリニカル イノベーション ネットワーク (CIN) の背景と概要 資料 3 新しい医薬品 医療機器等の開発に当たっては 世界的にコストが高騰している 特に 医薬品にあっては タフツ大学の試算によると 1 新薬当たり $2,558 million( 約 3,000 億円 ) 要するといわれている (Nov. 18, 2014, Tufts Center for the Study of Drug
in vivo
 Title 第 288 回 東 京 歯 科 大 学 学 会 ( 総 会 ) Journal 歯 科 学 報, 109(4): 405-443 URL http://hdl.handle.net/10130/1668 Right Posted at the Institutional Resources for Unique Colle Available from http://ir.tdc.ac.jp/
Title 第 288 回 東 京 歯 科 大 学 学 会 ( 総 会 ) Journal 歯 科 学 報, 109(4): 405-443 URL http://hdl.handle.net/10130/1668 Right Posted at the Institutional Resources for Unique Colle Available from http://ir.tdc.ac.jp/
公募情報 平成 28 年度日本医療研究開発機構 (AMED) 成育疾患克服等総合研究事業 ( 平成 28 年度 ) 公募について 平成 27 年 12 月 1 日 信濃町地区研究者各位 信濃町キャンパス学術研究支援課 公募情報 平成 28 年度日本医療研究開発機構 (AMED) 成育疾患克服等総合研
 公募情報 平成 28 年度日本医療研究開発機構 (AMED) 成育疾患克服等総合研究事業 ( 平成 28 年度 ) 公募について 平成 27 年 12 月 1 日 信濃町地区研究者各位 信濃町キャンパス学術研究支援課 公募情報 平成 28 年度日本医療研究開発機構 (AMED) 成育疾患克服等総合研究事業 ( 平成 28 年度 ) 公募について 11 月 27 日付で平成 28 年度 成育疾患克服等総合研究事業
公募情報 平成 28 年度日本医療研究開発機構 (AMED) 成育疾患克服等総合研究事業 ( 平成 28 年度 ) 公募について 平成 27 年 12 月 1 日 信濃町地区研究者各位 信濃町キャンパス学術研究支援課 公募情報 平成 28 年度日本医療研究開発機構 (AMED) 成育疾患克服等総合研究事業 ( 平成 28 年度 ) 公募について 11 月 27 日付で平成 28 年度 成育疾患克服等総合研究事業
< F2D8E9197BF A836F815B2E6A7464>
 ( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
PowerPoint
 2011 12 6PTC Live TechForum TOKYO [email protected] 1/ 52 1949 12 16 1,874 ( ) 1 9,457 3 1,315 ( ) 38,318 123,165 ( ) 2011 3 31 Gr. Gr. Gr. Gr. Gr. PF 2/ 52 1 2 3 4PMT 5 Integrity 6 7 8 1/2 3/ 52 OEM
2011 12 6PTC Live TechForum TOKYO [email protected] 1/ 52 1949 12 16 1,874 ( ) 1 9,457 3 1,315 ( ) 38,318 123,165 ( ) 2011 3 31 Gr. Gr. Gr. Gr. Gr. PF 2/ 52 1 2 3 4PMT 5 Integrity 6 7 8 1/2 3/ 52 OEM
はじめに この 成人 T 細胞白血病リンパ腫 (ATLL) の治療日記 は を服用される患者さんが 服用状況 体調の変化 検査結果の経過などを記録するための冊子です は 催奇形性があり サリドマイドの同類薬です は 胎児 ( お腹の赤ちゃん ) に障害を起こす可能性があります 生まれてくる赤ちゃんに
 を服用される方へ 成人 T 細胞白血病リンパ腫 (ATLL) の治療日記 使用開始日年月日 ( 冊目 ) はじめに この 成人 T 細胞白血病リンパ腫 (ATLL) の治療日記 は を服用される患者さんが 服用状況 体調の変化 検査結果の経過などを記録するための冊子です は 催奇形性があり サリドマイドの同類薬です は 胎児 ( お腹の赤ちゃん ) に障害を起こす可能性があります 生まれてくる赤ちゃんに被害を及ぼすことがないよう
を服用される方へ 成人 T 細胞白血病リンパ腫 (ATLL) の治療日記 使用開始日年月日 ( 冊目 ) はじめに この 成人 T 細胞白血病リンパ腫 (ATLL) の治療日記 は を服用される患者さんが 服用状況 体調の変化 検査結果の経過などを記録するための冊子です は 催奇形性があり サリドマイドの同類薬です は 胎児 ( お腹の赤ちゃん ) に障害を起こす可能性があります 生まれてくる赤ちゃんに被害を及ぼすことがないよう
LHHBAA+ArialMT Adobe Identity 0
 13ヲ ヲオヲァヲャヲ ヲアヲゥヲイ ヲウヲァヲイ ヲェヲエヲ ヲ ヲアヲュヲァヲイヲ ヲクヲイ (ヲウヲ ヲエヲカヲッヲイ 6メ2ヲ ヲエヲウヲ ヲアヲッ) 30965 2009-12-23 ICS: 93.040 1 71 71 71 7 1 71 7 1501-03-05-02-01:2009 1 71 71 71 71 71 71 71 7 TEXNIKH 1 71 71 71 71 71
13ヲ ヲオヲァヲャヲ ヲアヲゥヲイ ヲウヲァヲイ ヲェヲエヲ ヲ ヲアヲュヲァヲイヲ ヲクヲイ (ヲウヲ ヲエヲカヲッヲイ 6メ2ヲ ヲエヲウヲ ヲアヲッ) 30965 2009-12-23 ICS: 93.040 1 71 71 71 7 1 71 7 1501-03-05-02-01:2009 1 71 71 71 71 71 71 71 7 TEXNIKH 1 71 71 71 71 71
おことわり 本発表は演者の個人的見解を示すものであり PMDA 及び ICH Q12 EWG の公式な見解ではないことにご留意ください 2
 第 18 回医薬品品質フォーラム ICH Q12: Technical and Regulatory Considerations for Pharmaceutical Product Lifecycle Management 医薬品医療機器総合機構新薬審査第四部八木聡美 1 おことわり 本発表は演者の個人的見解を示すものであり PMDA 及び ICH Q12 EWG の公式な見解ではないことにご留意ください
第 18 回医薬品品質フォーラム ICH Q12: Technical and Regulatory Considerations for Pharmaceutical Product Lifecycle Management 医薬品医療機器総合機構新薬審査第四部八木聡美 1 おことわり 本発表は演者の個人的見解を示すものであり PMDA 及び ICH Q12 EWG の公式な見解ではないことにご留意ください
 外来化学療法を受けるがん患者のケアプログラム試案の作成 患者の困難や苦悩とニーズに焦点を当てて 1 2 2 Abstract A purpose of this study is to develop the tentative care program of cancer out-patients undergoing chemotherapy. We did the literature reviews
外来化学療法を受けるがん患者のケアプログラム試案の作成 患者の困難や苦悩とニーズに焦点を当てて 1 2 2 Abstract A purpose of this study is to develop the tentative care program of cancer out-patients undergoing chemotherapy. We did the literature reviews
スライド 1
 ライフサイクルプロセスに関する国際標準とソフトウェアファクトリ ISO/IEC 15288, ISO/IEC 12207, INCOSE Handbook and IEEE Std 1517 松本吉弘 工学博士 ; IEEE Life Fellow 京都高度技術研究所 All Rights Reserved Yoshihiro Matsumoto; 2007 1 対象とした国際標準 IEEE Std
ライフサイクルプロセスに関する国際標準とソフトウェアファクトリ ISO/IEC 15288, ISO/IEC 12207, INCOSE Handbook and IEEE Std 1517 松本吉弘 工学博士 ; IEEE Life Fellow 京都高度技術研究所 All Rights Reserved Yoshihiro Matsumoto; 2007 1 対象とした国際標準 IEEE Std
本日の内容 1. 施行通知の改定について 2.QbD 適用品目と通常申請品目の調査の違い 3. 調査及び相談業務からの事例 4. QbD 申請にあたっての留意事項 2 2
 QbD 申請と通常申請された品目の GMP 適合性調査の違いについて What is the difference of GMP compliance inspection and traditional approach products 独立行政法人医薬品医療機器総合機構品質管理部 Pharmaceuticals and Medical Devices Agency Office of GMP/QMS
QbD 申請と通常申請された品目の GMP 適合性調査の違いについて What is the difference of GMP compliance inspection and traditional approach products 独立行政法人医薬品医療機器総合機構品質管理部 Pharmaceuticals and Medical Devices Agency Office of GMP/QMS
CROCO について
 CROCO について CROCO とは コース 正式名称 Clinical Research Online Professional Certification Program at Osaka University といい 大阪大学医学部附属病院が提供する 臨床研究に関する教育の e-learning サイトです 臨床研究を実施する研究者 専門職の方 倫理審査委員会の委員 事務局の方を対象に 臨床研究に必要な情報
CROCO について CROCO とは コース 正式名称 Clinical Research Online Professional Certification Program at Osaka University といい 大阪大学医学部附属病院が提供する 臨床研究に関する教育の e-learning サイトです 臨床研究を実施する研究者 専門職の方 倫理審査委員会の委員 事務局の方を対象に 臨床研究に必要な情報
骨髄異形成症候群に対する 同種造血幹細胞移植の現状と課題
 第 36 回造血幹細胞移植委員会 (H25.2.4) 資料 5 第 36 回厚生科学審議会疾病対策部会造血幹細胞移植委員会 日本造血細胞移植学会 (JSHCT) 移植医療の現場からの提言 日本造血細胞移植学会理事長 岡本真一郎 我が国における非血縁者間造血幹細胞移植数 2000 1800 1600 1400 1200 1000 800 600 400 200 非血縁者間骨髄移植非血縁者間臍帯血移植
第 36 回造血幹細胞移植委員会 (H25.2.4) 資料 5 第 36 回厚生科学審議会疾病対策部会造血幹細胞移植委員会 日本造血細胞移植学会 (JSHCT) 移植医療の現場からの提言 日本造血細胞移植学会理事長 岡本真一郎 我が国における非血縁者間造血幹細胞移植数 2000 1800 1600 1400 1200 1000 800 600 400 200 非血縁者間骨髄移植非血縁者間臍帯血移植
骨の再生を促進する複合多孔質足場材料を開発
 同時発表 : 筑波研究学園都市記者会 ( 資料配布 ) 文部科学記者会 ( 資料配布 ) 科学記者会 ( 資料配布 ) 厚生労働記者会 ( 資料配布 ) 骨の再生を促進する複合多孔質足場材料を開発 ~ 生体内の細胞微小環境を模倣し 骨再生能力を向上 ~ 平成 24 年 6 月 6 日独立行政法人物質 材料研究機構独立行政法人理化学研究所独立行政法人国立成育医療研究センター 1. 独立行政法人物質 材料研究機構
同時発表 : 筑波研究学園都市記者会 ( 資料配布 ) 文部科学記者会 ( 資料配布 ) 科学記者会 ( 資料配布 ) 厚生労働記者会 ( 資料配布 ) 骨の再生を促進する複合多孔質足場材料を開発 ~ 生体内の細胞微小環境を模倣し 骨再生能力を向上 ~ 平成 24 年 6 月 6 日独立行政法人物質 材料研究機構独立行政法人理化学研究所独立行政法人国立成育医療研究センター 1. 独立行政法人物質 材料研究機構
表紙1
 Graduate School of Engineering Nagasaki Institute of Applied Science Graduate School of Engineering Nagasaki Institute of Applied Science Institute for Innovative Science and Technology Doctoral Program
Graduate School of Engineering Nagasaki Institute of Applied Science Graduate School of Engineering Nagasaki Institute of Applied Science Institute for Innovative Science and Technology Doctoral Program
IFAC International Auditing Practice Committee Issued by the International Federation of Accountants
 IFAC International Auditing Practice Committee Issued by the International Federation of Accountants Accounting estimate Accounting system Adverse opinion Agreed-upon procedures engagement Analytical
IFAC International Auditing Practice Committee Issued by the International Federation of Accountants Accounting estimate Accounting system Adverse opinion Agreed-upon procedures engagement Analytical
PowerPoint プレゼンテーション
 RBM シンポジウム 2016 年 3 月 31 日 ICH-E6(ICH-GCP) の動向 改訂のインパクト 日本製薬工業協会医薬品評価委員会臨床評価部会 ( ヤンセンファーマ株式会社 ) 松下敏 本日の発表 ICH-E6(R2) Step 2b 文書の状況 我々製薬企業への影響 今後のJPMAの対応 まとめ 本日は 治験依頼者としての立場 ( 視点 ) として 影響等を検討して報告します そのため
RBM シンポジウム 2016 年 3 月 31 日 ICH-E6(ICH-GCP) の動向 改訂のインパクト 日本製薬工業協会医薬品評価委員会臨床評価部会 ( ヤンセンファーマ株式会社 ) 松下敏 本日の発表 ICH-E6(R2) Step 2b 文書の状況 我々製薬企業への影響 今後のJPMAの対応 まとめ 本日は 治験依頼者としての立場 ( 視点 ) として 影響等を検討して報告します そのため
ISO
 ISO ISO ISO(International Standardization Organization) 135 ISO CD(Committee Draft) DIS(Draft for International Standard) FDIS(Final DIS) ISO ISO23500 2004.01.13 ANSI/AAMI RD52 2004.04.13 6 2004.08.09
ISO ISO ISO(International Standardization Organization) 135 ISO CD(Committee Draft) DIS(Draft for International Standard) FDIS(Final DIS) ISO ISO23500 2004.01.13 ANSI/AAMI RD52 2004.04.13 6 2004.08.09
Hitachi Field Matching Hitachi Recruiting My Page Hit
 01 02 03 Hitachi Field Matching 008 010 020 026 030 036 038 040 046 050 052 062 064 066 Hitachi Recruiting My Page 068 070 072 074 076 080 082 002 Hitachi Field Navigator Hitachi Field Navigator 003 BUSINESS
01 02 03 Hitachi Field Matching 008 010 020 026 030 036 038 040 046 050 052 062 064 066 Hitachi Recruiting My Page 068 070 072 074 076 080 082 002 Hitachi Field Navigator Hitachi Field Navigator 003 BUSINESS
佐賀県肺がん地域連携パス様式 1 ( 臨床情報台帳 1) 患者様情報 氏名 性別 男性 女性 生年月日 住所 M T S H 西暦 電話番号 年月日 ( ) - 氏名 ( キーパーソンに ) 続柄居住地電話番号備考 ( ) - 家族構成 ( ) - ( ) - ( ) - ( ) - 担当医情報 医
 佐賀県肺がん地域連携パス様式 1 ( 臨床情報台帳 1) 患者様情報 氏名 性別 男性 女性 生 住所 M T S H 西暦 電話番号 氏名 ( キーパーソンに ) 続柄居住地電話番号備考 家族構成 情報 医療機関名 診療科 住所 電話番号 紹介医 計画策定病院 (A) 連携医療機関 (B) 疾患情報 組織型 遺伝子変異 臨床病期 病理病期 サイズ 手術 有 無 手術日 手術時年齢 手術 有 無 手術日
佐賀県肺がん地域連携パス様式 1 ( 臨床情報台帳 1) 患者様情報 氏名 性別 男性 女性 生 住所 M T S H 西暦 電話番号 氏名 ( キーパーソンに ) 続柄居住地電話番号備考 家族構成 情報 医療機関名 診療科 住所 電話番号 紹介医 計画策定病院 (A) 連携医療機関 (B) 疾患情報 組織型 遺伝子変異 臨床病期 病理病期 サイズ 手術 有 無 手術日 手術時年齢 手術 有 無 手術日



