ナトレル ブレスト インプラント ナトレル 410 ブレスト インプラント 使用成績調査中間報告 2017 年 5 月 アラガン ジャパン株式会社
|
|
|
- しょうぶ むこやま
- 4 years ago
- Views:
Transcription
1 ナトレル ブレスト インプラント ナトレル 410 ブレスト インプラント 使用成績調査中間報告 2017 年 5 月 アラガン ジャパン株式会社
2
3 はじめに ナトレル ブレスト インプラント及びナトレル 410 ブレスト インプラント ( 以下 本製品 ) は 乳房再建術あるいは乳房増大術において 乳房の形状を修復または形成するために適用部位に埋入されるゲル充填人工乳房です 本邦においては 平成 24 年に 乳房再建術において 腫瘍または外傷により切除された または胸部の発育 形成異常等により適切に成長しなかった乳房の形状を修復または形成する また 乳房増大術において適切なバストサイズを達成する を効能 効果として ナトレル ブレスト インプラントが再審査期間 ( 平成 24 年 9 月 28 日 ~ 平成 27 年 9 月 27 日 ) で承認され 同年 7 月から販売開始 その後 平成 25 年にナトレル 410 ブレスト インプラントが再審査期間 ( 平成 25 年 10 月 11 日 ~ 平成 27 年 9 月 27 日 ) で承認され 平成 26 年 1 月から販売が開始されました アラガン ジャパン株式会社では使用成績調査を CRO( 株式会社アスクレップ ) を通じ実施しています この度 使用成績調査中間報告のデータをまとめましたのでご報告いたします 本製品の適正使用の一助になれば幸いに存じます 1 使用成績調査 1.1 実施状況本製品の使用実態下における安全性 有効性及び適正使用状況について 乳房再建術 ( 乳房の形状の修復または形成 ) または乳房増大術に本製品が使用された患者を対象として情報を収集 評価することを目的として 使用成績調査を継続中である 使用成績調査期間は平成 25 年 7 月から平成 38 年 10 月で 登録症例数として可能な限り 3,000 例 安全性最低評価症例数として 乳房再建術及び乳房増大術それぞれ 300 例を収集することを目的とし 施術後 10 年に亘り追跡調査を実施する予定である 本調査は 医療機器の製造販売後の調査及び試験の実施の基準に関する省令 ( 平成 16 年 12 月 20 日 厚生労働省令第 171 号 以下 GPSP 省令 という ) を遵守し 実施している なお 本製品の再審査期間はナトレル R ブレスト インプラント [ ラウンド型 ( 以下 RR)] が平成 24 年 9 月 28 日 ~ 平成 27 年 9 月 27 日 ナトレル R 410 ブレスト インプラント [ アナトミカル型 ( 以下 410)] が平成 25 年 10 月 11 日 ~ 平成 27 年 9 月 27 日であり 平成 27 年 12 月 24 日に再審査申請資料を提出している 1
4 1.2 症例構成平成 28 年 9 月 27 日までに 50 施設から 2,938 例の調査票を回収した 内訳は RR が 30 施設 168 例 410 が 50 施設 2,775 例であった このうち 31 例を除く 2,907 例 (RR:166 例 410:2,746 例 ) を安全性解析対象症例とし さらに 8 例を除く 2,899 例 (RR:166 例 410:2,738 例 ) を有効性解析対象症例とした ( 図 1) なお 1 症例に 2 製品使用されることもあることから 有効性については製品ごとの集計を行っている 調査票が回収された製品数は 50 施設 3,190 製品であり RR が 174 製品 410 が 3,016 製品であった このうち 9 製品を除く 3,148 製品 (RR:172 製品 410: 2,976 製品 ) を有効性解析対象製品数とした 調査票回収症例数 2938 例 RR 168 例 例 調査票回収施設数 50 施設 RR 30 施設 施設 安全性解析対象症例数 2907 例 RR 166 例 例 安全性解析除外症例 *1 1 プロトコール違反症例 30 例 2 安全性評価不能症例 1 例 3 再調査不能症例 0 例 合計 31 例 有効性解析除外症例 1 安全性除外条件に合致し有害事象あり 8 例 2 最終有効性評価がすべて未記載 0 例 合計 8 例 有効性解析対象症例数 2899 例 RR 166 例 例 *1: 有害事象が発現している症例は除外していない 図 1 症例構成図 2
5 1.3 安全性 患者背景要因別の不具合 医療機器による副作用の発現症例率 患者背景要因別の不具合 医療機器による副作用の発現症例率安全性解析対象症例 2,907 例 (RR:166 例 410:2,746 例 ) の性別は 男性が 2 例 女性が 2,905 例であった 年齢は 40~49 歳が 1,309 例で最も多かった 基礎疾患 合併症として乳癌を有していた症例は 2,885 例であり 未分化大細胞型リンパ腫 ( 以下 ALCL) を有していた症例はなかった ( 表 1) 不具合 医療機器による副作用は 2,907 例中 130 例に発現し 副作用発現症例率は 4.47% であった また RR では 166 例中 9 例に副作用が発現し 副作用発現症例率は 5.42% 410 では 2,746 例中 121 例に副作用が発現し 副作用発現症例率は 4.41% であった 患者背景要因が不具合 医療機器による副作用の発現に及ぼす影響について検討した結果 いずれの要因においても統計学的な有意差は認められなかった 3
6 表 1 患者背景要因別の不具合 医療機器による副作用の発現症例率 ( 安全性解析対象例 )(1/4) 患者背景要因 症例数 不具合 副作用の発現した症例数 不具合 副作用の発現した症例率 検定結果 (1)Fisher の直接確率 (2)χ 2 検定 安全性解析対象例数性別年齢身長体重基礎疾患 合併症乳癌乳癌以外の癌未分化大細胞型リンパ腫結合組織疾患 / 自己免疫疾患神経系疾患その他既往歴特記すべき体質 過敏性素因施術箇所インプラントの使用目的初回挿入 / 二次修正の区分 男 (1) p= 女 ~29 歳 (2) p= ~39 歳 ~49 歳 ~59 歳 歳以上 不明 未記載 cm 未満 (2) p= cm 以上 ~160cm 未満 cm 以上 ~170cm 未満 cm 以上 不明 未記載 kg 未満 (2) p= kg 以上 ~50kg 未満 kg 以上 ~60kg 未満 kg 以上 不明 未記載 無 (1) p= 有 無 (1) p= 有 無 (1) p= 有 無 有 無 (1) p= 有 無 (1) p= 有 無 (1) p= 有 無 (1) p= 有 無 (1) p= 有 右乳房 左乳房 再建術 豊胸術 初回挿入 二次修正
7 表 1 患者背景要因別の不具合 医療機器による副作用の発現症例率 ( 安全性解析対象例 )(2/4) 患者背景要因 症例数 不具合 副作用の発現した症例数 不具合 副作用の発現した症例率 検定結果 (1)Fisher の直接確率 (2)χ 2 検定 乳房再建手術に関する情報 初回挿入に関する情報 二次修正に関する情報 安全性解析対象例数 乳腺切除術式 腋窩リンパ節郭清の有無 放射線照射の有無 併用療法 ( 補助療法 ) の有無 再建の時期 組織拡張器使用の有無 併施した皮弁の内容 皮膚切開部位 インプラントの挿入部位 乳腺切除術式 腋窩リンパ節郭清の有無 放射線照射の有無 併用療法 ( 補助療法 ) の有無 再建の時期 組織拡張器使用の有無 併施した皮弁の内容 温存術 全摘術 ( 皮下乳腺全摘出術を含む ) なし あり 不明 未記載 なし あり 不明 未記載 なし 化学療法 ホルモン療法 トラスツズマブ その他 不明 未記載 同時再建 二期再建 なし あり 皮弁 筋皮弁 遊離皮弁 なし 瘢痕部位 腋窩 乳輪 乳房下溝 その他 皮下 乳腺下 胸筋下 皮弁 筋皮弁下 温存術 全摘術 ( 皮下乳腺全摘出術を含む ) なし あり 不明 未記載 なし あり 不明 未記載 なし 化学療法 ホルモン療法 トラスツズマブ 不明 未記載 同時再建 二期再建 なし あり 皮弁 筋皮弁 遊離皮弁 なし
8 表 1 患者背景要因別の不具合 医療機器による副作用の発現症例率 ( 安全性解析対象例 )(3/4) 患者背景要因 症例数 不具合 副作用の発現した症例数 不具合 副作用の発現した症例率 検定結果 (1)Fisher の直接確率 (2)χ 2 検定 乳房再建手術に関する情報 二次修正に関する情報 二次修正における挿入済みインプラント情報 安全性解析対象例数 皮膚切開部位 インプラントの挿入部位 前回挿入されたインプラントの二次修正の理由 メーカー名 表面の種類 形 内容物又は構造 容量 挿入期間 瘢痕部位 腋窩 乳輪 乳房下溝 皮下 乳腺下 胸筋下 皮弁 筋皮弁下 その他 破損 被膜拘縮 変形 感染 露出 その他の合併症 患者希望 Inamed Mentor PIP Eurosilicon Arion Sebbin Nagor Novamedical Silimed その他 不明 未記載 スムース テクスチャード ラウンド型 アナトミカル型 シリコンジェル 軟 硬 生理食塩水 ハイドロジェル ダブルルーメン 不明 未記載 cc 未満 cc 以上 ~150cc 未満 cc 以上 不明 未記載 年未満 年以上 ~5 年未満 年以上 ~10 年未満 年以上 不明 未記載
9 表 1 患者背景要因別の不具合 医療機器による副作用の発現症例率 ( 安全性解析対象例 )(4/4) 患者背景要因 症例数 不具合 副作用の発現した症例数 不具合 副作用の発現した症例率 検定結果 (1)Fisher の直接確率 (2)χ 2 検定 乳房増大手術に関する情報 初回挿入に関する情報 二次修正に関する情報 二次修正における挿入済みインプラント情報 安全性解析対象例数 皮膚切開部位 インプラントの挿入部位 皮膚切開部位 インプラントの挿入部位 前回挿入されたインプラントの二次修正の理由 メーカー名 表面の種類 形 内容物又は構造 容量 挿入期間 腋窩 乳輪 乳房下溝 乳腺下 胸筋下 筋膜下 腋窩 乳輪 乳房下溝 乳腺下 胸筋下 筋膜下 破損 被膜拘縮 変形 感染 露出 その他の合併症 患者希望 Inamed Mentor PIP Eurosilicon Arion Sebbin Nagor Novamedical Silimed スムース テクスチャード ラウンド型 アナトミカル型 シリコンジェル 軟 硬 生理食塩水 ハイドロジェル ダブルルーメン cc 未満 cc 以上 ~150cc 未満 cc 以上 年未満 年以上 ~5 年未満 年以上 ~10 年未満 年以上
10 1.3.2 調査終了症例調査終了症例の一覧を表 2 に示した 当該調査単位期間終了までに 24 例 (RR:6 例 410:18 例 ) が調査を終了した 調査終了までの期間は 7~670 日であり 24 例中 18 例が 1 年以内であった 調査終了理由は 患者の協力が得られない ( 来院せず含む ) が 7 例 死亡及び転院が各 2 例 その他 ( インプラント抜去 ) が 13 例であった 副作用を発現した症例は 9 例であり これらのうち 感染 術後創合併症及び感染 医療機器位置異常の 3 例が重篤であり いずれも本製品との因果関係は関連性があるかもしれないと判断された 転帰は 感染 医療機器位置異常の 2 例は本製品を抜去後 軽快している 8
11 感染重篤 可能性あるかもしれない 未回復既知 14 皮膚しわ非重篤否定できる軽快既知感染重篤否定できる回復既知 右乳房 再建術 初回挿入 有 有 無 無 99 その他 有 有 医療機器位置異常 非重篤 可能性大 軽快 既知 右乳房 再建術 二次修正 有 有 無 無 25 その他 有 有 感染 非重篤 確実 軽快 既知 左乳房 再建術 初回挿入 有 有 無 無 320 その他 無 無 左乳房 再建術 初回挿入 有 有 無 無 322 その他 有 無 医療機器使用法過誤 非重篤 否定できる 軽快 既知 右乳房 再建術 初回挿入 有 有 無 無 316 その他 有 有 医療機器破損 非重篤 可能性あるかもしれない 軽快 既知 左乳房 再建術 初回挿入 有 有 無 無 42 その他 有 有 感染 重篤 可能性あるかもしれない 軽快 既知 右乳房 再建術 初回挿入 有 有 無 無 305 転院 無 無 右乳房 再建術 初回挿入 有 有 無 無 110 死亡 有 無 再発乳癌 重篤 否定できる 死亡 既知 右乳房 再建術 初回挿入 有 有 無 無 80 その他 有 有 医療機器位置異常 重篤 可能性あるかもしれない 軽快 既知 右乳房 再建術 初回挿入 有 有 無 有 36 その他 有 無 皮下組織膿瘍 重篤 否定できる 回復 未知 RR 右乳房 再建術 初回挿入 有 有 無 無 149 患者の協力が得られない ( 来院せず含む ) 無 無 性別 : 全例女性有害事象は ICH 国際医薬用語集 (MedDRA/J)Ver19.0 に基づき分類その他 : インプラント抜去 表 2 調査終了症例一覧 No. 年齢製品施術箇所 インプラントの使用目的 初回挿入 / 二次修正の区分 基礎疾患 合併症 未分化大 有無 乳癌有無 細胞型リンパ腫有無 既往歴有無 追跡調査終了日までの期間 ( 日 ) 追跡調査終了理由 基本語 (PT) 重篤度 1 56 RR 左乳房 再建術 初回挿入 有 有 無 無 172 その他 無 無 左乳房 再建術 初回挿入 有 有 無 有 495 患者の協力が得られない ( 来院せず含む ) 無 無 左乳房 豊胸術 初回挿入 有 有 無 有 256 その他 有 有 医療機器使用法過誤 非重篤 確実 回復 既知 右乳房 再建術 初回挿入 有 有 無 無 344 その他 有 無 医療機器使用法過誤 非重篤 否定できる 回復 既知 /410 右乳房 / 左乳房 再建術 / 再建術 初回挿入 / 初回挿入 有 有 無 無 46 死亡 有 無 自殺既遂 重篤 否定できる 死亡 既知 右乳房 再建術 初回挿入 有 有 無 有 7 患者の協力が得られない ( 来院せず含む ) 無 無 7 29 RR 左乳房 再建術 初回挿入 有 有 無 無 670 患者の協力が得られない ( 来院せず含む ) 無 無 8 49 RR 左乳房 再建術 初回挿入 有 有 無 無 395 患者の協力が得られない ( 来院せず含む ) 無 無 9 46 RR 右乳房 再建術 初回挿入 有 有 無 無 497 転院 有 有 疼痛 非重篤 可能性あるかもしれない 不明 既知 左乳房 再建術 初回挿入 有 有 無 無 465 患者の協力が得られない ( 来院せず含む ) 無 無 左乳房 再建術 初回挿入 有 有 無 無 148 その他 有 有 術後創合併症 重篤 可能性あるかもしれない 未回復 既知 有害事象有無 副作用有無 有害事象 本製品との因果関係 転帰 既知未知 12 非重篤可能性大回復既知 右乳房 再建術 初回挿入 有 有 無 無 33 患者の協力が得られない ( 来院せず含む ) 無 無 RR 右乳房 再建術 初回挿入 有 有 無 有 435 その他 有 有 乳房インプラント関連被膜拘縮 9
12 1.3.3 不具合 感染症の発現状況当該調査単位期間終了までの不具合 感染症の発現症例率は 4.47%(130/2,907 例 ) 発現件数は 147 件であった 主な不具合 感染症 (10 件以上 ) は 漿液腫 29 件 (1.00%) 乳房インプラント関連被膜拘縮 21 件 (0.72%) 皮膚しわ 18 件 (0.62%) 疼痛 17 件 (0.58%) 医療機器位置異常 13 件 (0.45%) であった ( 表 3) 表 3 不具合 感染症の発現状況 時 期 調査施設数 50 調査症例数 2907 不具合等の発現症例数 130 不具合等の発現件数 147 不具合等の発現症例率 4.47% 不具合等の種類不具合等の種類別発現症例 ( 件数 ) 率 (%) 感染症および寄生虫症 9 (0.31) 感染 9 (0.31) 良性 悪性および詳細不明の新生物 ( 嚢胞およびポリープを含む ) 1 (0.03) 再発乳癌 1 (0.03) 精神障害 1 (0.03) 錯覚 1 (0.03) 血管障害 7 (0.24) 血腫 7 (0.24) 皮膚および皮下組織障害 30 (1.03) 紅斑 7 (0.24) * 発疹 2 (0.07) 皮膚壊死 3 (0.10) 皮膚しわ 18 (0.62) 一般 全身障害および投与部位の状態 48 (1.65) 壊死 1 (0.03) 疼痛 17 (0.58) 発熱 1 (0.03) 腫脹 1 (0.03) 炎症 8 (0.28) 乳房インプラント関連被膜拘縮 21 (0.72) 傷害 中毒および処置合併症 33 (1.14) 移植手術における合併症 3 (0.10) 漿液腫 29 (1.00) 術後創合併症 1 (0.03) 製品の問題 17 (0.58) 医療機器破損 2 (0.07) 医療機器位置異常 13 (0.45) 医療機器使用法過誤 2 (0.07) *: 使用上の注意から予測できない不具合 感染症不具合等は ICH 国際医薬用語集 (MedDRA/J)Ver19.0 に基づき分類 使用成績調査の累計 10
13 1.3.4 重篤な有害事象当該調査単位期間終了までの重篤な有害事象の発現症例率は 1.14%(33/2,907 例 ) 発現件数は 38 件であった その内訳 (2 件以上 ) は 再発乳癌が 10 件 (0.34%) 感染が 8 件 (0.28%) 医療機器位置異常が 5 件 (0.17%) 乳房インプラント関連被膜拘縮が 3 件 (0.10%) 炎症及び医療機器使用法過誤が各 2 件 (0.07%) であった これらのうち感染 7 件 医療機器位置異常 4 件 乳房インプラント関連被膜拘縮 3 件 炎症 2 件 再発乳癌 1 件は 本製品との因果関係が否定されなかった ( 表 4) 時 期 表 4 重篤な有害事象 調査施設数 50 調査症例数 2907 発現症例数 33 発現件数 38 発現症例率 1.14% 有害事象の種類 感染症および寄生虫症 8 (0.28) 感染 * 皮下組織膿瘍 良性 悪性および詳細不明の新生物 ( 嚢胞およびポリープを含む ) 乳癌 再発乳癌 悪性新生物 8 1 (0.28) (0.03) 12 (0.41) 1 10 [9] 1 (0.03) (0.34) (0.03) 精神障害 1 (0.03) 自殺既遂 1 (0.03) 一般 全身障害および投与部位の状態 5 (0.17) 疼痛 1 (0.03) 炎症 2 (0.07) 乳房インプラント関連被膜拘縮 3 (0.10) 傷害 中毒および処置合併症 2 (0.07) * 処置後出血 1 (0.03) 術後創合併症 1 (0.03) 外科および内科処置 1 (0.03) * 腫瘍切除 累計 有害事象の種類別発現症例 ( 件数 ) 率 (%) 1 (0.03) 製品の問題 7 (0.24) 5 医療機器位置異常 2 医療機器使用法過誤 [2] *: 使用上の注意から予測できない有害事象 [ ] は因果関係が否定された症例数 ( 件数 ) 有害事象は ICH 国際医薬用語集 (MedDRA/J)Ver19.0 に基づき分類 (0.17) (0.07) ALCL( 未分化大細胞型リンパ腫 ) 発現状況 本邦では 当該調査単位期間 ( 平成 27 年 9 月 28 日 ~ 平成 28 年 9 月 27 日 ) に ALCL を発現した 症例は収集されていない 11
14 1.4 有効性 医師及び患者の満足度評価患者背景要因別の最終の医師及び患者の満足度評価において 有効率の定義として 満足 及び やや満足 を有効 それ以外を無効として有効製品率を検討した 有効性解析対象症例 2,899 例中 (RR:166 例 410:2,738 例 ) 有効性解析対象製品は 3,148 製品 (RR:172 製品 410:2,976 製品 ) であった 医師の満足度評価における有効製品率は 84.12%(2,648/3,148 製品 ) その内訳は RR が 73.84% (127/172 製品 ) 410 が 84.71%(2,521/2,976 製品 ) であった また 今回から患者の満足度評価についても検討した 患者の満足度評価における有効製品率は 85.64%(2,696/3,148 製品 ) その内訳は RR が 78.49%(135/172 製品 ) 410 が 86.06%(2,561/2,976 製品 ) であった 本製品の有効製品率については 医師及び患者の満足度評価はほぼ一致していた 1.5 まとめナトレル R ブレスト インプラント (RR) 及びナトレル R 410 ブレスト インプラント (410) の安全性 有効性及び適正使用状況について 使用成績調査中間報告 ( 実施期間 : 平成 25 年 7 月 ~ 平成 38 年 10 月 施術後 10 年に亘り追跡調査 ) として検討した 安全性 : 安全性解析対象症例 2,907 例 (RR:166 例 410:2,746 例 ) 中 不具合 副作用を発現した症例率は 4.47%(130/2,907 例 ) であり その内訳は RR が 5.42%(9/166 例 ) 及び 410 が 4.41%(121/2,746 例 ) であった また 長期使用においても同様の結果であった なお 重篤な有害事象の発現症例率は 1.14% 発現件数は 38 件 (33/2,907 例 ) であった 調査終了症例は 24 例 (RR:6 例 410:18 例 ) であり 24 例中 18 例が 1 年以内に調査を終了 調査終了理由の内訳は 患者の協力が得られない ( 来院せず含む ) が 7 例 死亡及び転院が各 2 例 その他 ( インプラント抜去 ) が 13 例であった 有効性 : 医師の満足度評価における有効製品率は 84.12%(2,648/3,148 製品 ) 患者の満足度評価における有効製品率は 85.64%(2,696/3,148 製品 ) であり 本製品の有効製品率については 医師及び患者の満足度評価はほぼ一致していた 結論 : 安全性に関してはこれまでと同様の傾向であり 問題となるような新たな知見は認められなかった 有効性に関しては医師及び患者の満足度評価はほぼ一致していた 12
ヒアルロン酸ナトリウム架橋体製剤 特定使用成績調査
 ヒアルロン酸ナトリウム架橋体製剤 ( サイビスクディスポ 関節注 2mL) 特定使用成績調査 (J-STEP/EL) 謹啓時下ますますご清祥のこととお喜び申し上げます 平素より格別のご高配を賜り 厚く御礼申し上げます さて ヒアルロン酸ナトリウム架橋体製剤 ( サイビスクディスポ 関節注 2mL) は 保存的非薬物治療及び経口薬物治療が十分奏功しない疼痛を有する変形性膝関節症の患者を対象に 本剤の製造販売後の使用実態下における複数回使用を含めた安全性及び有効性について確認することを目的として
ヒアルロン酸ナトリウム架橋体製剤 ( サイビスクディスポ 関節注 2mL) 特定使用成績調査 (J-STEP/EL) 謹啓時下ますますご清祥のこととお喜び申し上げます 平素より格別のご高配を賜り 厚く御礼申し上げます さて ヒアルロン酸ナトリウム架橋体製剤 ( サイビスクディスポ 関節注 2mL) は 保存的非薬物治療及び経口薬物治療が十分奏功しない疼痛を有する変形性膝関節症の患者を対象に 本剤の製造販売後の使用実態下における複数回使用を含めた安全性及び有効性について確認することを目的として
薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リ
 薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リスク管理計画の実施状況及び得られた結果の評価に関する報告の様式 提出等の取扱いについては 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について
薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リスク管理計画の実施状況及び得られた結果の評価に関する報告の様式 提出等の取扱いについては 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について
Microsoft PowerPoint - 印刷用 K-net dr身原(2014).pptx
 もっと知りたい乳房再建術 広島市民病院形成外科 身原弘哉 ( 注 : 症例写真は削除しています ) 昨年 10 月から人工乳房 ( シリコンインプラント ) による乳房再建が一部保険適応となり 今年 1 月よりさらに適応が拡大されました 保険適応となったことにより 全国的にインプラントによる乳房再建の割合が増加するものと思われます 本日はこの人工乳房による乳房再建について 本乳房る乳房再建 当院における工夫点を交えて説明します
もっと知りたい乳房再建術 広島市民病院形成外科 身原弘哉 ( 注 : 症例写真は削除しています ) 昨年 10 月から人工乳房 ( シリコンインプラント ) による乳房再建が一部保険適応となり 今年 1 月よりさらに適応が拡大されました 保険適応となったことにより 全国的にインプラントによる乳房再建の割合が増加するものと思われます 本日はこの人工乳房による乳房再建について 本乳房る乳房再建 当院における工夫点を交えて説明します
症例報告書の記入における注意点 1 必須ではない項目 データ 斜線を引くこと 未取得 / 未測定の項目 2 血圧平均値 小数点以下は切り捨てとする 3 治験薬服薬状況 前回来院 今回来院までの服薬状況を記載する服薬無しの場合は 1 日投与量を 0 錠 とし 0 錠となった日付を特定すること < 演習
 ABC-123 臨床試験進行または再発胃癌患者に対するプラセボを対照薬とした無作為化二重盲検比較試験症例報告書 治験実施計画書番号 P123-31-V01 被験者識別コード 割付番号 治験実施医療機関名 ご自分の医療機関 お名前を記載して下さい 症例報告書記載者名 症例報告書記載者名 治験責任医師 ( 署名又は記名 押印 ) 治験責任医師記載内容確認完了日 印 2 0 年 月 日 1 症例報告書の記入における注意点
ABC-123 臨床試験進行または再発胃癌患者に対するプラセボを対照薬とした無作為化二重盲検比較試験症例報告書 治験実施計画書番号 P123-31-V01 被験者識別コード 割付番号 治験実施医療機関名 ご自分の医療機関 お名前を記載して下さい 症例報告書記載者名 症例報告書記載者名 治験責任医師 ( 署名又は記名 押印 ) 治験責任医師記載内容確認完了日 印 2 0 年 月 日 1 症例報告書の記入における注意点
スライド 1
 岡山済生会総合病院 乳房再建術パンフレット 1. はじめに 1 2. 今回はじめて手術を受けられる方へ 2 3. 以前に乳がん手術を受けた方へ 3 4. 乳房再建術について 4 5. 退院後の生活について 11 岡山済生会総合病院 形成外科乳腺外科 本パンフレットは 岡山大学乳がん治療 再建センターのご協力を頂いて作成しております 表紙写真 Wikipedia より引用 (Shawn Lipowsk
岡山済生会総合病院 乳房再建術パンフレット 1. はじめに 1 2. 今回はじめて手術を受けられる方へ 2 3. 以前に乳がん手術を受けた方へ 3 4. 乳房再建術について 4 5. 退院後の生活について 11 岡山済生会総合病院 形成外科乳腺外科 本パンフレットは 岡山大学乳がん治療 再建センターのご協力を頂いて作成しております 表紙写真 Wikipedia より引用 (Shawn Lipowsk
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠 50mg 医薬品リスク管理計画書 (RMP) の概要 有効成分 タペンタ 錠 100mg 製造販売業者 ヤンセンファーマ株式会社 薬効分類 821 提出年月 平成 30 年
 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
レクタブル 2 mg 注腸フォーム 14 回に係る医薬品リスク管理計画書 (RMP) の概要 販売名 レクタブル 2 mg 注腸フ 有効成分 ブデソニド ォーム14 回 製造販売業者 EA ファーマ株式会社 薬効分類 提出年月 平成 29 年 10 月 1.1. 安全性検討事項 重要な特
 レクタブル 2mg 注腸フォーム 14 回 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はEAファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません EA ファーマ株式会社 レクタブル 2 mg 注腸フォーム 14 回に係る医薬品リスク管理計画書 (RMP) の概要 販売名 レクタブル 2 mg 注腸フ 有効成分 ブデソニド ォーム14
レクタブル 2mg 注腸フォーム 14 回 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はEAファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません EA ファーマ株式会社 レクタブル 2 mg 注腸フォーム 14 回に係る医薬品リスク管理計画書 (RMP) の概要 販売名 レクタブル 2 mg 注腸フ 有効成分 ブデソニド ォーム14
 乳がんの疑いがある といわれたあなたへ 乳がんの疑いがあるといわれ 気が動転しているのではないでしょうか これからの人生がどうなるのか 心配でいっぱいかもしれません 乳がんは 比較的治癒率の高いがんで 新しい治療も開発されています 乳房を温存したり 再建したり 女性らしい体を保つ治療法もあります 納得のいく治療を受けるために 今 あなたができること まずは正確な情報を集めましょう もっと 知ってほしい
乳がんの疑いがある といわれたあなたへ 乳がんの疑いがあるといわれ 気が動転しているのではないでしょうか これからの人生がどうなるのか 心配でいっぱいかもしれません 乳がんは 比較的治癒率の高いがんで 新しい治療も開発されています 乳房を温存したり 再建したり 女性らしい体を保つ治療法もあります 納得のいく治療を受けるために 今 あなたができること まずは正確な情報を集めましょう もっと 知ってほしい
重篤な副作用は 自然流産の 1 例 1 件であった 本症例は 本剤服用後も性交があり どの時点での妊娠か判断できず 本剤と自然流産との関連は評価できないと考えた 非重篤な副作用のうち 使用上の注意から予測できない副作用は 腹部膨満及び月経困難症各 2 件 腹部不快感 口内炎 ざ瘡 尿臭異常 月経障害
 再審査報告書 販 売 名ノルレボ錠 0.75 mg 有 効 成 分 名レボノルゲストレル 申 請 者 名あすか製薬株式会社 承 認 の 緊急避妊 効 能 効 果 承 認 の 用 法 用 量 承 認 年 月 日平成 23 年 2 月 23 日 再 審 査 期 間 4 年 備 考 平成 28 年 5 月 13 日 医薬品医療機器総合機構 性交後 72 時間以内にレボノルゲストレルとして 1.5 mg を
再審査報告書 販 売 名ノルレボ錠 0.75 mg 有 効 成 分 名レボノルゲストレル 申 請 者 名あすか製薬株式会社 承 認 の 緊急避妊 効 能 効 果 承 認 の 用 法 用 量 承 認 年 月 日平成 23 年 2 月 23 日 再 審 査 期 間 4 年 備 考 平成 28 年 5 月 13 日 医薬品医療機器総合機構 性交後 72 時間以内にレボノルゲストレルとして 1.5 mg を
医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年
![医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年 医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年](/thumbs/91/107149459.jpg) 事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム 製造販売業者 EA ファーマ株式会社 薬効分類 提出年月 平成 30 年 10 月 1.1. 安全
 モビコール配合内用剤 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はEAファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません EA ファーマ株式会社 モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム
モビコール配合内用剤 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はEAファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません EA ファーマ株式会社 モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム
日本医薬品安全性学会 COI 開示 筆頭発表者 : 加藤祐太 演題発表に関連し 開示すべき COI 関連の企業などはありません
 医薬品副作用データベース (JADER) を用いた市販後の副作用発現状況の検討 加藤祐太 1)2) 岸達生 3) 高松昭司 2) 白石正 4) 1) 山形大学医学部医薬品医療機器評価学講座 2) 医薬品医療機器総合機構安全第二部 3) 医薬品医療機器総合機構信頼性保証部 4) 山形大学医学部附属病院薬剤部 日本医薬品安全性学会 COI 開示 筆頭発表者 : 加藤祐太 演題発表に関連し 開示すべき COI
医薬品副作用データベース (JADER) を用いた市販後の副作用発現状況の検討 加藤祐太 1)2) 岸達生 3) 高松昭司 2) 白石正 4) 1) 山形大学医学部医薬品医療機器評価学講座 2) 医薬品医療機器総合機構安全第二部 3) 医薬品医療機器総合機構信頼性保証部 4) 山形大学医学部附属病院薬剤部 日本医薬品安全性学会 COI 開示 筆頭発表者 : 加藤祐太 演題発表に関連し 開示すべき COI
佐賀県肺がん地域連携パス様式 1 ( 臨床情報台帳 1) 患者様情報 氏名 性別 男性 女性 生年月日 住所 M T S H 西暦 電話番号 年月日 ( ) - 氏名 ( キーパーソンに ) 続柄居住地電話番号備考 ( ) - 家族構成 ( ) - ( ) - ( ) - ( ) - 担当医情報 医
 佐賀県肺がん地域連携パス様式 1 ( 臨床情報台帳 1) 患者様情報 氏名 性別 男性 女性 生 住所 M T S H 西暦 電話番号 氏名 ( キーパーソンに ) 続柄居住地電話番号備考 家族構成 情報 医療機関名 診療科 住所 電話番号 紹介医 計画策定病院 (A) 連携医療機関 (B) 疾患情報 組織型 遺伝子変異 臨床病期 病理病期 サイズ 手術 有 無 手術日 手術時年齢 手術 有 無 手術日
佐賀県肺がん地域連携パス様式 1 ( 臨床情報台帳 1) 患者様情報 氏名 性別 男性 女性 生 住所 M T S H 西暦 電話番号 氏名 ( キーパーソンに ) 続柄居住地電話番号備考 家族構成 情報 医療機関名 診療科 住所 電話番号 紹介医 計画策定病院 (A) 連携医療機関 (B) 疾患情報 組織型 遺伝子変異 臨床病期 病理病期 サイズ 手術 有 無 手術日 手術時年齢 手術 有 無 手術日
【押印あり】日本医学会宛
 別紙 再生医療等製品患者登録システムへの参加協力のお願い 患者登録システムの目的 患者登録システムは 再生医療等製品の市販後の使用状況や患者予後等のデータを収集し 迅速な安全対策や新たな製品開発等を通じて 医療の向上に役立てることを目的としています 患者登録システムは 製品毎に構築 運用されます この患者登録システムは 一般的には レジストリ と呼ばれることもあります 構築形態例 患者登録システムの対象
別紙 再生医療等製品患者登録システムへの参加協力のお願い 患者登録システムの目的 患者登録システムは 再生医療等製品の市販後の使用状況や患者予後等のデータを収集し 迅速な安全対策や新たな製品開発等を通じて 医療の向上に役立てることを目的としています 患者登録システムは 製品毎に構築 運用されます この患者登録システムは 一般的には レジストリ と呼ばれることもあります 構築形態例 患者登録システムの対象
1)表紙14年v0
 NHO µ 医師が治療により回復が期待できないと判断する 終末期 であると医療チームおよび本人 家族が判断する 患者の意志表明は明確であるか? いいえ はい 意思は文書化されているか? はい 患者には判断能力があるか? 医療チームと患者家族で治療方針を相談する 患者の意思を推量できる場合には それを尊重する はい はい 患者の意思を再確認する はい 合意が得られたか? はい いいえ 倫理委員会などで議論する
NHO µ 医師が治療により回復が期待できないと判断する 終末期 であると医療チームおよび本人 家族が判断する 患者の意志表明は明確であるか? いいえ はい 意思は文書化されているか? はい 患者には判断能力があるか? 医療チームと患者家族で治療方針を相談する 患者の意思を推量できる場合には それを尊重する はい はい 患者の意思を再確認する はい 合意が得られたか? はい いいえ 倫理委員会などで議論する
第2次JMARI報告書
 3 肝胆管系または膵臓の悪性腫瘍 6 5 4 3 2 症例数 : 3 平均在院日数 ( 加重平均 : 29.7 最長入院日数 : 579 変動係数 : 1.134 標準偏差 : 33.5423 症例数 : 155 平均在院日数 ( 加重平均 : 42.8 最長在院日数 : 465 変動係数 : 1.11 標準偏差 : 47.94 症例数 : 平均在院日数 ( 加重平均 : 39.5 最短入院日数 :
3 肝胆管系または膵臓の悪性腫瘍 6 5 4 3 2 症例数 : 3 平均在院日数 ( 加重平均 : 29.7 最長入院日数 : 579 変動係数 : 1.134 標準偏差 : 33.5423 症例数 : 155 平均在院日数 ( 加重平均 : 42.8 最長在院日数 : 465 変動係数 : 1.11 標準偏差 : 47.94 症例数 : 平均在院日数 ( 加重平均 : 39.5 最短入院日数 :
Microsoft Word - LIA RMP_概要ver2.docx
 リアルダ錠 1200mg に係る 医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任は持田製薬株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません 持田製薬株式会社 リアルダ錠 1200mg に係る医薬品リスク管理計画書 (RMP) の概要 販売名リアルダ錠 1200mg 有効成分メサラジン 製造販売業者持田製薬株式会社薬効分類 872399 提出年月
リアルダ錠 1200mg に係る 医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任は持田製薬株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません 持田製薬株式会社 リアルダ錠 1200mg に係る医薬品リスク管理計画書 (RMP) の概要 販売名リアルダ錠 1200mg 有効成分メサラジン 製造販売業者持田製薬株式会社薬効分類 872399 提出年月
査を実施し 必要に応じ適切な措置を講ずること (2) 本品の警告 効能 効果 性能 用法 用量及び使用方法は以下のとお りであるので 特段の留意をお願いすること なお その他の使用上の注意については 添付文書を参照されたいこと 警告 1 本品投与後に重篤な有害事象の発現が認められていること 及び本品
 薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
改訂後改訂前 << 効能 効果に関連する使用上の注意 >> 関節リウマチ 1. 過去の治療において 少なくとも1 剤の抗リウマチ薬 ( 生物製剤を除く ) 等による適切な治療を行っても 疾患に起因する明らかな症状が残る場合に投与すること 2. 本剤とアバタセプト ( 遺伝子組換え ) の併用は行わな
 - 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 警告 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ ヒト型抗ヒト TNFα モノクローナル抗体製剤 ( 一般名 : ゴリムマブ ( 遺伝子組換え )) 2017 年 4 月 製造販売元ヤンセンファーマ株式会社発売元田辺三菱製薬株式会社 この度 標記製品 ( 以下 本剤 ) シンポニー 皮下注 50mg シリンジ ( 一般名 :
- 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 警告 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ ヒト型抗ヒト TNFα モノクローナル抗体製剤 ( 一般名 : ゴリムマブ ( 遺伝子組換え )) 2017 年 4 月 製造販売元ヤンセンファーマ株式会社発売元田辺三菱製薬株式会社 この度 標記製品 ( 以下 本剤 ) シンポニー 皮下注 50mg シリンジ ( 一般名 :
PowerPoint プレゼンテーション
 第 21 回京都乳癌コンセンサス会議 テーマ HER2 陰性再発乳癌の抗がん薬治療 アンケート集計結果 1 回答いただいた御施設 (50 音順 ) 大阪赤十字病院 大津赤十字病院 加藤乳腺クリニック 関西医科大学附属枚方病院 菅典道クリニック 京都医療センター 京都市立病院 京都第一赤十字病院 京都大学医学部附属病院 倉敷中央病院 公立八鹿病院 沢井記念乳腺クリニック 滋賀県立成人病センター 静岡県立がんセンター
第 21 回京都乳癌コンセンサス会議 テーマ HER2 陰性再発乳癌の抗がん薬治療 アンケート集計結果 1 回答いただいた御施設 (50 音順 ) 大阪赤十字病院 大津赤十字病院 加藤乳腺クリニック 関西医科大学附属枚方病院 菅典道クリニック 京都医療センター 京都市立病院 京都第一赤十字病院 京都大学医学部附属病院 倉敷中央病院 公立八鹿病院 沢井記念乳腺クリニック 滋賀県立成人病センター 静岡県立がんセンター
婦人科63巻6号/FUJ07‐01(報告) M
 図 1 調査前年 1 年間の ART 実施周期数別施設数 図 4 ART 治療周期数別自己注射の導入施設数と導入率 図 2 自己注射の導入施設数と導入率 図 5 施設の自己注射の使用目的 図 3 導入していない理由 図 6 製剤種類別自己注射の導入施設数と施設率 図 7 リコンビナント FSH を自己注射された症例の治療成績は, 通院による注射症例と比較し, 差があるか 図 10 リコンビナント FSH
図 1 調査前年 1 年間の ART 実施周期数別施設数 図 4 ART 治療周期数別自己注射の導入施設数と導入率 図 2 自己注射の導入施設数と導入率 図 5 施設の自己注射の使用目的 図 3 導入していない理由 図 6 製剤種類別自己注射の導入施設数と施設率 図 7 リコンビナント FSH を自己注射された症例の治療成績は, 通院による注射症例と比較し, 差があるか 図 10 リコンビナント FSH
 エムプリシティ点滴静注用 300 mg エムプリシティ点滴静注用 400 mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はブリストル マイヤーズスクイブ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ブリストル マイヤーズスクイブ株式会社 医薬品リスク管理計画書 平成 29 年 10 月 16 日 独立行政法人医薬品医療機器総合機構理事長殿
エムプリシティ点滴静注用 300 mg エムプリシティ点滴静注用 400 mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はブリストル マイヤーズスクイブ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ブリストル マイヤーズスクイブ株式会社 医薬品リスク管理計画書 平成 29 年 10 月 16 日 独立行政法人医薬品医療機器総合機構理事長殿
医療事故防止対策に関するワーキング・グループにおいて、下記の点につき協議検討する
 大阪府立病院機構医療事故公表基準 1 公表の目的この基準は 府立 5 病院における医療事故の公表に関する取り扱いについて必要な事項を定めるものとする 病院職員は 次に掲げる公表の意義を正しく認識し 医療事故防止に努めるものとする (1) 病院職員が事故原因の分析や再発防止への取組みなどの情報を共有化し 医療における安全管理の徹底を図るため 自発的に医療事故を公表していくことが求められていること (2)
大阪府立病院機構医療事故公表基準 1 公表の目的この基準は 府立 5 病院における医療事故の公表に関する取り扱いについて必要な事項を定めるものとする 病院職員は 次に掲げる公表の意義を正しく認識し 医療事故防止に努めるものとする (1) 病院職員が事故原因の分析や再発防止への取組みなどの情報を共有化し 医療における安全管理の徹底を図るため 自発的に医療事故を公表していくことが求められていること (2)
< A815B B83578D E9197BF5F906697C38B40945C F92F18B9F91CC90A72E786C73>
 がんに対する診療機能 各領域の専門医に加え 認定看護師 専門 認定薬剤師等とともにチーム医療を展開しており 標準的かつ良質 適切な医療の提供に努め 又 他の医療機関との連携を推進しております. 肺がん 当該疾患の診療を担当している 医師数 当該疾患を専門としてい 腫瘍内科 4 4 2 腫瘍外科 ( 外科 ) 5 4 3 腫瘍放射線科 実績実績実績 開胸 治療の実施 (: 実施可 / : 実施不可 )
がんに対する診療機能 各領域の専門医に加え 認定看護師 専門 認定薬剤師等とともにチーム医療を展開しており 標準的かつ良質 適切な医療の提供に努め 又 他の医療機関との連携を推進しております. 肺がん 当該疾患の診療を担当している 医師数 当該疾患を専門としてい 腫瘍内科 4 4 2 腫瘍外科 ( 外科 ) 5 4 3 腫瘍放射線科 実績実績実績 開胸 治療の実施 (: 実施可 / : 実施不可 )
医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など ) 医薬品候補物質のスクリーニン
 特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
菌種 報告年 株数 MIC(μg/mL) Range MIC50 MIC > ( 幾何平均 ) C.tropicalis >
 生物学的同等性試験におけるイトリゾール カプセル 50 のロット間での統計学 的有意差が本剤の有効性及び安全性に与える影響について イトリゾール カプセル 50 は,1993 年に内臓真菌症 ( 深在性真菌症 ), 深在性皮膚真菌症及び表在性皮膚真菌症を適応症として承認され, その後,1999 年に爪白癬等の適応を追加,2004 年及び 2006 年にはそれぞれ爪白癬のパルス療法および注射剤からの切り替えとしての新用法
生物学的同等性試験におけるイトリゾール カプセル 50 のロット間での統計学 的有意差が本剤の有効性及び安全性に与える影響について イトリゾール カプセル 50 は,1993 年に内臓真菌症 ( 深在性真菌症 ), 深在性皮膚真菌症及び表在性皮膚真菌症を適応症として承認され, その後,1999 年に爪白癬等の適応を追加,2004 年及び 2006 年にはそれぞれ爪白癬のパルス療法および注射剤からの切り替えとしての新用法
記 第 1 再審査資料の構成及び作成上の注意事項再審査資料の構成及び作成上の注意事項は次のとおりとすること また 再審査申請書の写し及び平成 10 年 12 月 1 日付け医薬審第 1058 号厚生省医薬安全局審査管理課長通知 新医薬品等の申請資料の信頼性の基準の遵守について により添付することとし
 薬生薬審発 1128 第 2 号 平成 29 年 11 月 28 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) 新医療用医薬品の再審査申請に際し添付すべき資料について 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 第 14 条の4 第 4 項に基づく新医療用医薬品の再審査申請に際し添付すべき資料
薬生薬審発 1128 第 2 号 平成 29 年 11 月 28 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) 新医療用医薬品の再審査申請に際し添付すべき資料について 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 第 14 条の4 第 4 項に基づく新医療用医薬品の再審査申請に際し添付すべき資料
形成外科って何? 整形外科と同じ??? 美容外科のこと??? 形成外科とは 身体に生じた組織の異常や変形 欠損 あるいは整容的な不満足に対して あらゆる手法や特殊な技術を駆使し 機能のみならず形態的にもより正常に より美しくすることによって みなさまの生活の質 "Quality of Life" の
 形成外科とは ~ 乳がん治療との関わり ~ 独立行政法人国立病院機構岡山医療センター形成外科医師高田温行 形成外科って何? 整形外科と同じ??? 美容外科のこと??? 形成外科とは 身体に生じた組織の異常や変形 欠損 あるいは整容的な不満足に対して あらゆる手法や特殊な技術を駆使し 機能のみならず形態的にもより正常に より美しくすることによって みなさまの生活の質 "Quality of Life"
形成外科とは ~ 乳がん治療との関わり ~ 独立行政法人国立病院機構岡山医療センター形成外科医師高田温行 形成外科って何? 整形外科と同じ??? 美容外科のこと??? 形成外科とは 身体に生じた組織の異常や変形 欠損 あるいは整容的な不満足に対して あらゆる手法や特殊な技術を駆使し 機能のみならず形態的にもより正常に より美しくすることによって みなさまの生活の質 "Quality of Life"
Microsoft Word - 奈良県GQP-GVPガイドライン doc
 三. 安全確保措置の実施に関する手順 1. 目的安全確保措置の実施に関する手順の目的を記載する < 記載例 > 本手順は GVP 省令の第 9 条に基づき 安全確保措置の実施を適正かつ円滑に行うために必要な手順を定めるものである 2. 適用範囲安全確保措置の実施に関する手順の適用範囲を記載する < 記載例 > 本手順書は 二. 安全管理情報の検討及びその結果に基づく安全確保措置の立案に関する手順 で立案された安全確保措置の決定
三. 安全確保措置の実施に関する手順 1. 目的安全確保措置の実施に関する手順の目的を記載する < 記載例 > 本手順は GVP 省令の第 9 条に基づき 安全確保措置の実施を適正かつ円滑に行うために必要な手順を定めるものである 2. 適用範囲安全確保措置の実施に関する手順の適用範囲を記載する < 記載例 > 本手順書は 二. 安全管理情報の検討及びその結果に基づく安全確保措置の立案に関する手順 で立案された安全確保措置の決定
がん登録実務について
 平成 28 年度東京都がん登録説明会資料 2-1 がん登録届出実務について (1) 1. 届出対象 2. 届出候補見つけ出し 3. 診断日 4. 届出票の作成例示 東京都地域がん登録室 1 1. 届出対象 1 原発部位で届出 2 入院 外来を問わず 当該腫瘍に対して 自施設を初診し 診断あるいは治療の対象 ( 経過観察を含む ) となった腫瘍を届出 3 届出対象となった腫瘍を 1 腫瘍 1 届出の形で届出
平成 28 年度東京都がん登録説明会資料 2-1 がん登録届出実務について (1) 1. 届出対象 2. 届出候補見つけ出し 3. 診断日 4. 届出票の作成例示 東京都地域がん登録室 1 1. 届出対象 1 原発部位で届出 2 入院 外来を問わず 当該腫瘍に対して 自施設を初診し 診断あるいは治療の対象 ( 経過観察を含む ) となった腫瘍を届出 3 届出対象となった腫瘍を 1 腫瘍 1 届出の形で届出
<4D F736F F D B A814089FC92F982CC82A8926D82E782B95F E31328C8E5F5F E646F63>
 - 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ 抗悪性腫瘍剤 ( ブルトン型チロシンキナーゼ阻害剤 ) ( 一般名 : イブルチニブ ) 2016 年 12 月 この度 抗悪性腫瘍剤 イムブルビカ カプセル 140 mg ( 以下標記製品 ) につきまして 再発又は難治性のマントル細胞リンパ腫 の効能追加承認を取得したことに伴い
- 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ 抗悪性腫瘍剤 ( ブルトン型チロシンキナーゼ阻害剤 ) ( 一般名 : イブルチニブ ) 2016 年 12 月 この度 抗悪性腫瘍剤 イムブルビカ カプセル 140 mg ( 以下標記製品 ) につきまして 再発又は難治性のマントル細胞リンパ腫 の効能追加承認を取得したことに伴い
スライド 1
 1/5 PMDA からの医薬品適正使用のお願い ( 独 ) 医薬品医療機器総合機構 No.6 2012 年 1 月 ラミクタール錠 ( ラモトリギン ) の重篤皮膚障害と用法 用量遵守 早期発見について ラミクタール錠は 用法 用量 を遵守せず投与した場合に皮膚障害の発現率が高くなることが示されている ( 表 1 参照 ) ため 用法 用量 を遵守することが平成 20 年 10 月の承認時より注意喚起されています
1/5 PMDA からの医薬品適正使用のお願い ( 独 ) 医薬品医療機器総合機構 No.6 2012 年 1 月 ラミクタール錠 ( ラモトリギン ) の重篤皮膚障害と用法 用量遵守 早期発見について ラミクタール錠は 用法 用量 を遵守せず投与した場合に皮膚障害の発現率が高くなることが示されている ( 表 1 参照 ) ため 用法 用量 を遵守することが平成 20 年 10 月の承認時より注意喚起されています
三重大学医学部附属病院臨床研究開発センター
 治験及び臨床研究における 有害事象対応マニュアル Ver 1.0 三重大学医学部附属病院 臨床研究開発センター TEL : 059-231-5246 ( 内線 :5223 6530) FAX : 059-231-5247 目次 1. 有害事象の定義... 1 2. 重篤な有害事象の定義... 1 3. 予期しない重篤な有害事象の定義... 1 4. 有害事象発生時の対応 ( 全ての有害事象 )...
治験及び臨床研究における 有害事象対応マニュアル Ver 1.0 三重大学医学部附属病院 臨床研究開発センター TEL : 059-231-5246 ( 内線 :5223 6530) FAX : 059-231-5247 目次 1. 有害事象の定義... 1 2. 重篤な有害事象の定義... 1 3. 予期しない重篤な有害事象の定義... 1 4. 有害事象発生時の対応 ( 全ての有害事象 )...
販売名 : アドバンテージ ( 承認番号 : 22300BZX ) 別紙 改訂箇所を _ 下線で示しております < 新記載第 5 版 > 適切な項目へ記載した < 旧記載第 4 版 > 警告 1. 適応対象 ( 患者 ) 以下の患者には TVT 術を実施する際のリスクと利点を慎重に検討
 平成 28 年 6 月 医療機関各位 ボストン サイエンティフィックジャパン株式会社 アドバンテージ オブトリクス Ⅱ 添付文書改訂のお知らせ 謹啓貴院におかれましては ますますご清祥のこととお喜び申し上げます この度 弊社が製造販売致しました尿失禁治療テープ アドバンテージ 及び オブトリクス Ⅱ の添付文書を改訂致しましたので その内容についてお知らせ申し上げます 当該製品をご使用の先生方におかれましては
平成 28 年 6 月 医療機関各位 ボストン サイエンティフィックジャパン株式会社 アドバンテージ オブトリクス Ⅱ 添付文書改訂のお知らせ 謹啓貴院におかれましては ますますご清祥のこととお喜び申し上げます この度 弊社が製造販売致しました尿失禁治療テープ アドバンテージ 及び オブトリクス Ⅱ の添付文書を改訂致しましたので その内容についてお知らせ申し上げます 当該製品をご使用の先生方におかれましては
h29c04
 総数 第 1 位第 2 位第 3 位第 4 位第 5 位 総数 悪性新生物 25,916 心疾患 14,133 肺炎 7,239 脳血管疾患 5,782 老衰 4,483 ( 29.8) ( 16.2) ( 8.3) ( 6.6) ( 5.1) PAGE - 1 0 歳 先天奇形 変形及び染色体異 38 胎児及び新生児の出血性障害 10 周産期に特異的な呼吸障害及 9 不慮の事故 9 妊娠期間及び胎児発育に関連
総数 第 1 位第 2 位第 3 位第 4 位第 5 位 総数 悪性新生物 25,916 心疾患 14,133 肺炎 7,239 脳血管疾患 5,782 老衰 4,483 ( 29.8) ( 16.2) ( 8.3) ( 6.6) ( 5.1) PAGE - 1 0 歳 先天奇形 変形及び染色体異 38 胎児及び新生児の出血性障害 10 周産期に特異的な呼吸障害及 9 不慮の事故 9 妊娠期間及び胎児発育に関連
を追加する (2) 実施要領通知の報告様式別紙 1 医薬品安全性情報報告書 及び同報告様式別紙 2 医療機器安全性情報報告書 を別添のとおり変更する
 薬食発 0311 第 1 号平成 25 年 3 月 11 日 各都道府県知事殿 厚生労働省医薬食品局長 医薬品 医療機器等安全性情報報告制度 の報告における電子メールの活用について 薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 77 条の 4 の 2 第 2 項の規定に基づく 医療機関等からの医薬品又は医療機器についての副作用 感染症及び不具合報告 ( 以下 副作用等報告
薬食発 0311 第 1 号平成 25 年 3 月 11 日 各都道府県知事殿 厚生労働省医薬食品局長 医薬品 医療機器等安全性情報報告制度 の報告における電子メールの活用について 薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 77 条の 4 の 2 第 2 項の規定に基づく 医療機関等からの医薬品又は医療機器についての副作用 感染症及び不具合報告 ( 以下 副作用等報告
ケブザラ皮下注 150mg/200mg シリンジ ケブザラ皮下注 150mg/200mg オートインジェクターに係る医薬品リスク管理計画書 (RMP) の概要 販売名 製造販売業者 1 ケブザラ皮下注 150mg シリンジ 2 ケブザラ皮下注 200mg シリンジ 3 ケブザラ皮下注 150mg オ
 ケブザラ皮下注 150mgシリンジケブザラ皮下注 200mgシリンジケブザラ皮下注 150mgオートインジェクターケブザラ皮下注 200mgオートインジェクターに係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はサノフィ株式会社にあります 当該情報を適正使用以外の営利目的で利用することはできません サノフィ株式会社 ケブザラ皮下注 150mg/200mg シリンジ
ケブザラ皮下注 150mgシリンジケブザラ皮下注 200mgシリンジケブザラ皮下注 150mgオートインジェクターケブザラ皮下注 200mgオートインジェクターに係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はサノフィ株式会社にあります 当該情報を適正使用以外の営利目的で利用することはできません サノフィ株式会社 ケブザラ皮下注 150mg/200mg シリンジ
医師主導治験取扱要覧
 9. 安全性情報の取扱いに関する手順書 1. 目的及び適用範囲 本手順書は 安全性情報の取扱いに係る用語の定義を定め 当該治験に関与する者が 安全性情報を適 切に取扱うための手順その他必要な事項を定めるものである 2. 用語の定義等 2.1. 用語の定義 2.1.1. 治験責任医師等 本手順書は 自ら治験を実施する者を 治験責任医師 と記載し また 治験責任医師及び治験分担医師 を併せて 治験責任医師等
9. 安全性情報の取扱いに関する手順書 1. 目的及び適用範囲 本手順書は 安全性情報の取扱いに係る用語の定義を定め 当該治験に関与する者が 安全性情報を適 切に取扱うための手順その他必要な事項を定めるものである 2. 用語の定義等 2.1. 用語の定義 2.1.1. 治験責任医師等 本手順書は 自ら治験を実施する者を 治験責任医師 と記載し また 治験責任医師及び治験分担医師 を併せて 治験責任医師等
untitled
 1 2 有害事象とは何ですか? 有害事象 (Adverse Event) 治験薬又は製造販売後臨床試験薬を投与された被験者に生じたすべての好ましくない又は意図しない疾病又はその徴候をいう 当該治験薬又は当該製造販売後臨床試験薬との因果関係の有無は問わない 副作用とは何ですか? 副作用 (Adverse Drug Reaction) 治験薬 ( 対象薬として用いられる市販薬を除く ) については以下のとおり
1 2 有害事象とは何ですか? 有害事象 (Adverse Event) 治験薬又は製造販売後臨床試験薬を投与された被験者に生じたすべての好ましくない又は意図しない疾病又はその徴候をいう 当該治験薬又は当該製造販売後臨床試験薬との因果関係の有無は問わない 副作用とは何ですか? 副作用 (Adverse Drug Reaction) 治験薬 ( 対象薬として用いられる市販薬を除く ) については以下のとおり
シダキュアスギ舌下錠 2,000JAU 5,000JAU に係る医薬品リスク管理計画書 (RMP) の概要 販売名 シダキュアスギ舌下錠 2,000JAU,5,000JAU 有効成分 スギ花粉エキス原末 承認取得者名 鳥居薬品株式会社 薬効分類 提出年月 平成 30 年 8 月 1.1.
 シダキュアスギ舌下錠 2,000JAU シダキュアスギ舌下錠 5,000JAU に係る医薬品リスク管理計画書 本資料に記載された情報に関する権利及び内容についての責任は 鳥居薬品株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません 鳥居薬品株式会社 1 シダキュアスギ舌下錠 2,000JAU 5,000JAU に係る医薬品リスク管理計画書 (RMP) の概要 販売名 シダキュアスギ舌下錠
シダキュアスギ舌下錠 2,000JAU シダキュアスギ舌下錠 5,000JAU に係る医薬品リスク管理計画書 本資料に記載された情報に関する権利及び内容についての責任は 鳥居薬品株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません 鳥居薬品株式会社 1 シダキュアスギ舌下錠 2,000JAU 5,000JAU に係る医薬品リスク管理計画書 (RMP) の概要 販売名 シダキュアスギ舌下錠
ケブザラ皮下注 150mg/200mg シリンジに係る医薬品リスク管理計画書 (RMP) の概要 販売名 1 ケブザラ皮下注 150mg シリンジ 2 ケブザラ皮下注 200mg シリンジ 有効成分 サリルマブ ( 遺伝子組換え ) 製造販売業者 サノフィ株式会社 薬効分類 399 提出年月 平成
 ケブザラ皮下注 150mgシリンジケブザラ皮下注 200mgシリンジに係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はサノフィ株式会社にあります 当該情報を適正使用以外の営利目的で利用することはできません サノフィ株式会社 ケブザラ皮下注 150mg/200mg シリンジに係る医薬品リスク管理計画書 (RMP) の概要 販売名 1 ケブザラ皮下注 150mg シリンジ
ケブザラ皮下注 150mgシリンジケブザラ皮下注 200mgシリンジに係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はサノフィ株式会社にあります 当該情報を適正使用以外の営利目的で利用することはできません サノフィ株式会社 ケブザラ皮下注 150mg/200mg シリンジに係る医薬品リスク管理計画書 (RMP) の概要 販売名 1 ケブザラ皮下注 150mg シリンジ
頭頚部がん1部[ ].indd
![頭頚部がん1部[ ].indd 頭頚部がん1部[ ].indd](/thumbs/92/108881798.jpg) 1 1 がん化学療法を始める前に がん化学療法を行うときは, その目的を伝え なぜ, 化学療法を行うか について患者の理解と同意を得ること ( インフォームド コンセント ) が必要である. 病理組織, 病期が決定したら治療計画を立てるが, がん化学療法を治療計画に含める場合は以下の場合である. 切除可能であるが, 何らかの理由で手術を行わない場合. これには, 導入として行う場合と放射線療法との併用で化学療法を施行する場合がある.
1 1 がん化学療法を始める前に がん化学療法を行うときは, その目的を伝え なぜ, 化学療法を行うか について患者の理解と同意を得ること ( インフォームド コンセント ) が必要である. 病理組織, 病期が決定したら治療計画を立てるが, がん化学療法を治療計画に含める場合は以下の場合である. 切除可能であるが, 何らかの理由で手術を行わない場合. これには, 導入として行う場合と放射線療法との併用で化学療法を施行する場合がある.
別添 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について < 半年ごとの定期報告の受け付け> Q1 平成 26 年 6 月 30 日までの間は 治験依頼者 ( 自ら治験を実施する者を除く ) が提出する副作用等症例の定期報告は なお従前の例によることができる とあるが 平成 26 年
 事務連絡 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局審査管理課 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 第 273 条第 3 項に基づく治験副作用等定期報告については 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について ( 平成 24 年
事務連絡 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局審査管理課 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 第 273 条第 3 項に基づく治験副作用等定期報告については 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について ( 平成 24 年
2. 転移するのですか? 悪性ですか? 移行上皮癌は 悪性の腫瘍です 通常はゆっくりと膀胱の内部で進行しますが リンパ節や肺 骨などにも転移します 特に リンパ節転移はよく見られますので 膀胱だけでなく リンパ節の検査も行うことが重要です また 移行上皮癌の細胞は尿中に浮遊していますので 診断材料や
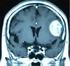 動物の腫瘍インフォメーション シート 4 犬の膀胱腫瘍 膀胱腫瘍とは 膀胱内貼りの粘膜から発生する腫瘍で 血尿などを起こします 犬の膀胱腫瘍のうちの多くは 移行上皮癌 ( いこうじょうひがん ) とよばれる悪性腫瘍ですが 良性の腫瘍や 慢性の膀胱炎によるポリープなどもみられることがあります 良性のものは 基本的には手術で切除すれば完治可能です ここでは 主に悪性の移行上皮癌について 検査法や治療オプションをご説明します
動物の腫瘍インフォメーション シート 4 犬の膀胱腫瘍 膀胱腫瘍とは 膀胱内貼りの粘膜から発生する腫瘍で 血尿などを起こします 犬の膀胱腫瘍のうちの多くは 移行上皮癌 ( いこうじょうひがん ) とよばれる悪性腫瘍ですが 良性の腫瘍や 慢性の膀胱炎によるポリープなどもみられることがあります 良性のものは 基本的には手術で切除すれば完治可能です ここでは 主に悪性の移行上皮癌について 検査法や治療オプションをご説明します
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 <その他分野 ( 消化器官用薬 解毒剤 その他 )> 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号
 資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
1. はじめに ステージティーエスワンこの文書は Stage Ⅲ 治癒切除胃癌症例における TS-1 術後補助化学療法の予後 予測因子および副作用発現の危険因子についての探索的研究 (JACCRO GC-07AR) という臨床研究について説明したものです この文書と私の説明のな かで わかりにくいと
 StageⅢ 治癒切除胃癌症例における TS-1 術後補助化学療法の 予後予測因子および副作用発現の危険因子についての 探索的研究 (JACCRO GC-07AR) についてのご説明 説明 同意文書 作成日 :2014 年 5 月 27 日 施設名 : 東京医科大学八王子医療センター 1. はじめに ステージティーエスワンこの文書は Stage Ⅲ 治癒切除胃癌症例における TS-1 術後補助化学療法の予後
StageⅢ 治癒切除胃癌症例における TS-1 術後補助化学療法の 予後予測因子および副作用発現の危険因子についての 探索的研究 (JACCRO GC-07AR) についてのご説明 説明 同意文書 作成日 :2014 年 5 月 27 日 施設名 : 東京医科大学八王子医療センター 1. はじめに ステージティーエスワンこの文書は Stage Ⅲ 治癒切除胃癌症例における TS-1 術後補助化学療法の予後
副作用収集状況 市販直後調査期間中 (2011 年 4 月 11 日 ~2011 年 10 月 31 日 ) に収集された副作用は 200 例 258 件でした そのうち 重篤な副作用は 8 例 14 件でした 副作用の内訳を表 1 に示します 重篤な副作用は 高カルシウム血症 3 件 意識変容状態
 医師 薬剤師の先生方へ 2012 年 1 月 中外製薬株式会社 安全管理責任者 エディロール R カプセル 0.5µg 0.75µg 市販直後調査結果のご報告 市販直後調査期間 :2011 年 4 月 11 日 ~2011 年 10 月 31 日 謹啓 先生方におかれましては ますますご清祥のこととお慶び申し上げます 平素は格別のご高配を賜り 厚く御礼申し上げます エディロール カプセル 0.5µg
医師 薬剤師の先生方へ 2012 年 1 月 中外製薬株式会社 安全管理責任者 エディロール R カプセル 0.5µg 0.75µg 市販直後調査結果のご報告 市販直後調査期間 :2011 年 4 月 11 日 ~2011 年 10 月 31 日 謹啓 先生方におかれましては ますますご清祥のこととお慶び申し上げます 平素は格別のご高配を賜り 厚く御礼申し上げます エディロール カプセル 0.5µg
10038 W36-1 ワークショップ 36 関節リウマチの病因 病態 2 4 月 27 日 ( 金 ) 15:10-16:10 1 第 5 会場ホール棟 5 階 ホール B5(2) P2-203 ポスタービューイング 2 多発性筋炎 皮膚筋炎 2 4 月 27 日 ( 金 ) 12:4
 10001 P1-089 ポスタービューイング 1 関節リウマチの治療 :DMARDs NSAIDs 4 月 26 日 ( 木 ) 13:20-14:40 - ポスター 展示会場ホール E B2 階 ホール E 10002 P2-041 ポスタービューイング 2 関節リウマチの治療評価と予測 2 4 月 27 日 ( 金 ) 12:40-14:00 - ポスター 展示会場ホール E B2 階 ホール
10001 P1-089 ポスタービューイング 1 関節リウマチの治療 :DMARDs NSAIDs 4 月 26 日 ( 木 ) 13:20-14:40 - ポスター 展示会場ホール E B2 階 ホール E 10002 P2-041 ポスタービューイング 2 関節リウマチの治療評価と予測 2 4 月 27 日 ( 金 ) 12:40-14:00 - ポスター 展示会場ホール E B2 階 ホール
‡BUNITE_Studyƒv?ƒgƒR??−iFinal_Ver_−j _docx
 調査実施計画書 経口糖尿病治療薬 ( インクレチン関連薬関連薬を含む ) 投与に関する実態調査研究 UNITE Study (Use of a New and Innovative Therapy for diabetes: Evaluation study) 社団法人日本糖尿病協会 第 1.0 版 2010 年 3 月作成 目次 1. 研究の概要 1 2. はじめに 3 3. 調査の目的 3 4.
調査実施計画書 経口糖尿病治療薬 ( インクレチン関連薬関連薬を含む ) 投与に関する実態調査研究 UNITE Study (Use of a New and Innovative Therapy for diabetes: Evaluation study) 社団法人日本糖尿病協会 第 1.0 版 2010 年 3 月作成 目次 1. 研究の概要 1 2. はじめに 3 3. 調査の目的 3 4.
Microsoft Word - DatRetPTC_R3.4SoC_sep2012 Japanese.doc
 Release 3.3 から 3.4 への主な変更点 MedDRA データ検索及び提示 : 考慮事項公表版 3.4 (MedDRA バージョン 15.1 対応 ) 2012 年 10 月 1 日 以下に MedDRA データ検索及び提示 : 考慮事項 のリリース 3.3 から 3.4 への間での変更点を示す 文書全体における変更点 全般的なスペル 句読点 文字の間隔 図表番号およびフォーマットのエラーの修正
Release 3.3 から 3.4 への主な変更点 MedDRA データ検索及び提示 : 考慮事項公表版 3.4 (MedDRA バージョン 15.1 対応 ) 2012 年 10 月 1 日 以下に MedDRA データ検索及び提示 : 考慮事項 のリリース 3.3 から 3.4 への間での変更点を示す 文書全体における変更点 全般的なスペル 句読点 文字の間隔 図表番号およびフォーマットのエラーの修正
乳癌かな?!と思ったら
 乳癌かな?! と思ったら 東京高輪病院外科谷本芽弘理 乳癌といえば 北斗昌さん 小林麻央さん 乳癌はなぜ悲劇的なイメージか 40~50 代女性に多い 仕事 子育てに忙しい女ざかり!! 年齢階級別乳癌罹患率の推移 資料 : 独立行政法人国立がん研究センターがん対策情報センター 本日の目標 敵を知る 乳癌について知る 早期発見を目指す 乳癌かな?! ときの対応法を知る 診断から治療の流れを知る 乳癌を受け入れて早期に治療を始める心の準備を!!
乳癌かな?! と思ったら 東京高輪病院外科谷本芽弘理 乳癌といえば 北斗昌さん 小林麻央さん 乳癌はなぜ悲劇的なイメージか 40~50 代女性に多い 仕事 子育てに忙しい女ざかり!! 年齢階級別乳癌罹患率の推移 資料 : 独立行政法人国立がん研究センターがん対策情報センター 本日の目標 敵を知る 乳癌について知る 早期発見を目指す 乳癌かな?! ときの対応法を知る 診断から治療の流れを知る 乳癌を受け入れて早期に治療を始める心の準備を!!
1. 医薬品リスク管理計画を策定の上 適切に実施すること 2. 国内での治験症例が極めて限られていることから 製造販売後 一定数の症例に係るデータが集積されるまでの間は 全 症例を対象に使用成績調査を実施することにより 本剤使用患者の背景情報を把握するとともに 本剤の安全性及び有効性に関するデータを
 薬生薬審発 0525 第 3 号薬生安発 0525 第 1 号平成 30 年 5 月 25 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) トファシチニブクエン酸塩製剤の使用に当たっての留意事項について トファシチニブクエン酸塩製剤 ( 販売名 : ゼルヤンツ錠
薬生薬審発 0525 第 3 号薬生安発 0525 第 1 号平成 30 年 5 月 25 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) トファシチニブクエン酸塩製剤の使用に当たっての留意事項について トファシチニブクエン酸塩製剤 ( 販売名 : ゼルヤンツ錠
販売名 再審査報告書 1 ゴナールエフ皮下注用 75 2 ゴナールエフ皮下注用 ゴナールエフ皮下注ペン ゴナールエフ皮下注ペン ゴナールエフ皮下注ペン 900 有 効 成 分 名 ホリトロピンアルファ ( 遺伝子組換え ) 申 請 者 名 メルクセローノ株式会社
 販売名 再審査報告書 1 ゴナールエフ皮下注用 75 2 ゴナールエフ皮下注用 150 3 ゴナールエフ皮下注ペン 300 4 ゴナールエフ皮下注ペン 450 5 ゴナールエフ皮下注ペン 900 有 効 成 分 名 ホリトロピンアルファ ( 遺伝子組換え ) 申 請 者 名 メルクセローノ株式会社 承 認 の 効 能 効 果 承 認 の 用 法 用 量 平成 29 年 2 月 17 日医薬品医療機器総合機構
販売名 再審査報告書 1 ゴナールエフ皮下注用 75 2 ゴナールエフ皮下注用 150 3 ゴナールエフ皮下注ペン 300 4 ゴナールエフ皮下注ペン 450 5 ゴナールエフ皮下注ペン 900 有 効 成 分 名 ホリトロピンアルファ ( 遺伝子組換え ) 申 請 者 名 メルクセローノ株式会社 承 認 の 効 能 効 果 承 認 の 用 法 用 量 平成 29 年 2 月 17 日医薬品医療機器総合機構
販売名 有効成分名 再審査報告書 1 レキップ CR 錠 2 mg 2 レキップ CR 錠 8 mg ロピニロール塩酸塩 平成 29 年 9 月 26 日医薬品医療機器総合機構 申請者名グラクソ スミスクライン株式会社 承認の効能 効果承認の用法 用量承認年月日再審査期間 パーキンソン病 通常 成人
 販売名 有効成分名 再審査報告書 1 レキップ CR 錠 2 mg 2 レキップ CR 錠 8 mg ロピニロール塩酸塩 平成 29 年 9 月 26 日医薬品医療機器総合機構 申請者名グラクソ スミスクライン株式会社 承認の効能 効果承認の用法 用量承認年月日再審査期間 パーキンソン病 通常 成人にはロピニロールとして 1 日 1 回 2 mg から始め 2 週目に 4 mg/ 日とする 以後経過観察しながら
販売名 有効成分名 再審査報告書 1 レキップ CR 錠 2 mg 2 レキップ CR 錠 8 mg ロピニロール塩酸塩 平成 29 年 9 月 26 日医薬品医療機器総合機構 申請者名グラクソ スミスクライン株式会社 承認の効能 効果承認の用法 用量承認年月日再審査期間 パーキンソン病 通常 成人にはロピニロールとして 1 日 1 回 2 mg から始め 2 週目に 4 mg/ 日とする 以後経過観察しながら
< E082AA82F1936F985E8F578C768C8B89CA816989FC92F994C5816A2E786C73>
 院内がん登録集計 登録対象 28( 平成 2) 年 1 月 1 日より 12 月 31 日までの 1 年間に当院で診断された悪性新生物の件数です 登録対象は新規の診断症例または他院で診断された初診症例であり 入院患者および外来患者を対象としています 1 腫瘍 1 登録の原則に基づき同一患者に別のがん腫と判断されるがんが生じた場合には腫瘍毎の登録 ( 複数登録 ) となります
院内がん登録集計 登録対象 28( 平成 2) 年 1 月 1 日より 12 月 31 日までの 1 年間に当院で診断された悪性新生物の件数です 登録対象は新規の診断症例または他院で診断された初診症例であり 入院患者および外来患者を対象としています 1 腫瘍 1 登録の原則に基づき同一患者に別のがん腫と判断されるがんが生じた場合には腫瘍毎の登録 ( 複数登録 ) となります
性黒色腫は本邦に比べてかなり高く たとえばオーストラリアでは悪性黒色腫の発生率は日本の 100 倍といわれており 親戚に一人は悪性黒色腫がいるくらい身近な癌といわれています このあと皮膚癌の中でも比較的発生頻度の高い基底細胞癌 有棘細胞癌 ボーエン病 悪性黒色腫について本邦の統計データを詳しく紹介し
 2012 年 12 月 6 日放送 第 111 回日本皮膚科学会総会 5 教育講演 20-1 皮膚腫瘍の最新疫学データ 筑波大学大学院皮膚科 講師藤澤康弘 はじめに皮膚癌は国立がん研究センターがとりまとめている全国集計データでも年々増加の一途をたどっており なかでも高齢者の患者の増加が目立ちます 日常の皮膚科診療でも遭遇する機会が今後も増え続けることから その発生状況を知っておくことは役に立つと思います
2012 年 12 月 6 日放送 第 111 回日本皮膚科学会総会 5 教育講演 20-1 皮膚腫瘍の最新疫学データ 筑波大学大学院皮膚科 講師藤澤康弘 はじめに皮膚癌は国立がん研究センターがとりまとめている全国集計データでも年々増加の一途をたどっており なかでも高齢者の患者の増加が目立ちます 日常の皮膚科診療でも遭遇する機会が今後も増え続けることから その発生状況を知っておくことは役に立つと思います
院内がん登録における発見経緯 来院経路 発見経緯がん発見のきっかけとなったもの 例 ) ; を受けた ; 職場の健康診断または人間ドックを受けた 他疾患で経過観察中 ; 別の病気で受診中に偶然 がん を発見した ; 解剖により がん が見つかった 来院経路 がん と診断された時に その受診をするきっ
 15 年 12 月時点 院内がん登録統計 (13 年 ) 登録対象 当院で診断された または治療された がん 当院で がん と判明した場合や他施設から がん の治療のためにされた場合に登録 診断された時点で登録を行うため 治療実績 手術件数などとは件数が異なります 例 )A さんは X 医院で胃がんと診断され 治療のために当院に来院された 胃がん を登録 1 腫瘍 1 登録 1 人が複数の部位に がん
15 年 12 月時点 院内がん登録統計 (13 年 ) 登録対象 当院で診断された または治療された がん 当院で がん と判明した場合や他施設から がん の治療のためにされた場合に登録 診断された時点で登録を行うため 治療実績 手術件数などとは件数が異なります 例 )A さんは X 医院で胃がんと診断され 治療のために当院に来院された 胃がん を登録 1 腫瘍 1 登録 1 人が複数の部位に がん
33 NCCN Guidelines Version NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines ) (NCCN 腫瘍学臨床診療ガイドライン ) 非ホジキンリンパ腫 2015 年第 2 版 NCCN.or
 33 NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines ) (NCCN 腫瘍学臨床診療ガイドライン ) 2015 年第 2 版 NCCN.org NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines ) (NCCN 腫瘍学臨床診療ガイドライン ) の Lugano
33 NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines ) (NCCN 腫瘍学臨床診療ガイドライン ) 2015 年第 2 版 NCCN.org NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines ) (NCCN 腫瘍学臨床診療ガイドライン ) の Lugano
PowerPoint プレゼンテーション
 口腔がんについて 熊本県の現状と当科の取り組みについて 熊本大学大学院生命科学研究部歯科口腔外科学分野 熊本大学医学部附属病院歯科口腔外科 中山秀樹 講演の内容 1. 口腔がんの特徴 2. 熊本大学における口腔がんの現状 3. 口腔がんの早期発見へ向けた取り組み 口腔粘膜疾患鑑別システムの紹介 4. 進行口腔がんに対する当科での治療 手術 抗がん剤併用の放射線治療など 講演の内容 1. 口腔がんの特徴
口腔がんについて 熊本県の現状と当科の取り組みについて 熊本大学大学院生命科学研究部歯科口腔外科学分野 熊本大学医学部附属病院歯科口腔外科 中山秀樹 講演の内容 1. 口腔がんの特徴 2. 熊本大学における口腔がんの現状 3. 口腔がんの早期発見へ向けた取り組み 口腔粘膜疾患鑑別システムの紹介 4. 進行口腔がんに対する当科での治療 手術 抗がん剤併用の放射線治療など 講演の内容 1. 口腔がんの特徴
 一般名 : オファツムマブ ( 遺伝子組換え ) 製剤 はじめに ( 適正使用に関するお願い )4 治療スケジュール6 投与に際しての注意事項 7 7 8 8 9 1 1 11 12 13 14 15 重大な副作用とその対策 18 18 28 32 34 36 4 42 44 45 参考資料 5 付録 55 55 55 64 3 1 はじめに4 はじめ 5 に1 2 治療スケジュール6 対象患者の選択インフォームドコンセント投与準備
一般名 : オファツムマブ ( 遺伝子組換え ) 製剤 はじめに ( 適正使用に関するお願い )4 治療スケジュール6 投与に際しての注意事項 7 7 8 8 9 1 1 11 12 13 14 15 重大な副作用とその対策 18 18 28 32 34 36 4 42 44 45 参考資料 5 付録 55 55 55 64 3 1 はじめに4 はじめ 5 に1 2 治療スケジュール6 対象患者の選択インフォームドコンセント投与準備
14栄養・食事アセスメント(2)
 14 5. 栄養 食事アセスメント 2 ④成果 アウトカム outcome の予測 合併症 死亡 5. 栄養 食事 アセスメント 2 率 ケア必要度 平均在院日数などの成果が予測出来 るかどうか 疾患別に検討されている 一般病棟の高 齢患者では総蛋白質 血清アルブミン リンパ球数と 1. 栄養状態の評価 判定の定義と目標 術後合併症併発 一般病棟内科疾患患者ではアルブミ ① 栄養状態の評価 判定 栄養状態が過剰あるいは欠乏
14 5. 栄養 食事アセスメント 2 ④成果 アウトカム outcome の予測 合併症 死亡 5. 栄養 食事 アセスメント 2 率 ケア必要度 平均在院日数などの成果が予測出来 るかどうか 疾患別に検討されている 一般病棟の高 齢患者では総蛋白質 血清アルブミン リンパ球数と 1. 栄養状態の評価 判定の定義と目標 術後合併症併発 一般病棟内科疾患患者ではアルブミ ① 栄養状態の評価 判定 栄養状態が過剰あるいは欠乏
Microsoft PowerPoint - komatsu 2
 Surgical Alternatives to Hysterectomy in the Management of Leiomyomas 子宮摘出術に代わる子宮筋腫の外科的選択肢 ACOG PRACTICE BULLETIN 2000 M6 31 番小松未生 子宮筋腫 女性の骨盤内腫瘍で最も頻度が高い 大部分は無症状 治療は子宮摘出術が一般的 挙児希望 子宮温存希望の女性も多い 治療法の選択肢は増えているが
Surgical Alternatives to Hysterectomy in the Management of Leiomyomas 子宮摘出術に代わる子宮筋腫の外科的選択肢 ACOG PRACTICE BULLETIN 2000 M6 31 番小松未生 子宮筋腫 女性の骨盤内腫瘍で最も頻度が高い 大部分は無症状 治療は子宮摘出術が一般的 挙児希望 子宮温存希望の女性も多い 治療法の選択肢は増えているが
 χ 嶋 寺 伸 一 図 図 初発年齢 歳未満の乳児期発症例が最も多く しだ いに減少した 嵌頓時月齢 嵌頓は2 か月以下の2 例に発生し うち8 例に緊急手術が行われた その月齢は生後 か月に小さな peak を 8か月に大きな peak を認め 乳児期においてほぼ二峰性 のグラフを示した 表2 図2 嵌頓に関わる因子の検討 性別 男 女 患側 R L B 初発年齢 か月 手術時年齢 か月 手術時体重
χ 嶋 寺 伸 一 図 図 初発年齢 歳未満の乳児期発症例が最も多く しだ いに減少した 嵌頓時月齢 嵌頓は2 か月以下の2 例に発生し うち8 例に緊急手術が行われた その月齢は生後 か月に小さな peak を 8か月に大きな peak を認め 乳児期においてほぼ二峰性 のグラフを示した 表2 図2 嵌頓に関わる因子の検討 性別 男 女 患側 R L B 初発年齢 か月 手術時年齢 か月 手術時体重
審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果
![審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果 審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果](/thumbs/92/108604766.jpg) 審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
5. 乳がん 当該疾患の診療を担当している診療科名と 専門 乳房切除 乳房温存 乳房再建 冷凍凝固摘出術 1 乳腺 内分泌外科 ( 外科 ) 形成外科 2 2 あり あり なし あり なし なし あり なし なし あり なし なし 6. 脳腫瘍 当該疾患の診療を担当している診療科名と 専
 がんに対する診療機能 各領域の専門医に加え 認定看護師 専門 認定薬剤師等とともにチーム医療を展開しており 標準的かつ良質 適切な医療の提供に努め 又 他の医療機関との連携を推進しております 平成 29 年 9 月 1 日現在 1. 肺がん 当該疾患の診療を担当している診療科名と 専門 1 腫瘍外科 ( 外科 ) 6 3 開胸 胸腔鏡下 定位 ありありなしなしなしなし なしなしなしありなしなし 2.
がんに対する診療機能 各領域の専門医に加え 認定看護師 専門 認定薬剤師等とともにチーム医療を展開しており 標準的かつ良質 適切な医療の提供に努め 又 他の医療機関との連携を推進しております 平成 29 年 9 月 1 日現在 1. 肺がん 当該疾患の診療を担当している診療科名と 専門 1 腫瘍外科 ( 外科 ) 6 3 開胸 胸腔鏡下 定位 ありありなしなしなしなし なしなしなしありなしなし 2.
モニタリング計画書・報告書
 0 ... 2... 2... 2... 3 4.1.... 3 4.1.1.... 3 4.1.2.... 4 4.1.3.... 4 4.1.4.... 5 4.2.... 5 4.3.... 6 4.4.... 6... 6 5.1.... 6 5.1.1.... 7 5.1.2.... 8 5.1.3.... 9 5.1.4.... 9 5.2.... 15 5.2.1.... 15 5.2.2....
0 ... 2... 2... 2... 3 4.1.... 3 4.1.1.... 3 4.1.2.... 4 4.1.3.... 4 4.1.4.... 5 4.2.... 5 4.3.... 6 4.4.... 6... 6 5.1.... 6 5.1.1.... 7 5.1.2.... 8 5.1.3.... 9 5.1.4.... 9 5.2.... 15 5.2.1.... 15 5.2.2....
桜町病院対応病名小分類別 診療科別 手術数 (2017/04/ /03/31) D12 D39 Ⅳ G64 女性生殖器の性状不詳又は不明の新生物 D48 その他及び部位不明の性状不詳又は不明の新生物 Ⅲ 総数 構成比 (%) 該当無し Ⅰ 感染症及び寄生虫症 Ⅱ 新生物 C54 子宮体部
 D12 D39 Ⅳ G64 女性生殖器の性状不詳又は不明の新生物 D48 その他及び部位不明の性状不詳又は不明の新生物 Ⅲ 総数 構成比 (%) 該当無し Ⅰ 感染症及び寄生虫症 Ⅱ 新生物 C54 子宮体部の悪性新生物 結腸 直腸 肛門及び肛門管の良性新生物 D25 子宮平滑筋腫 D27 卵巣の良性新生物 血液及び造血器の疾患並びに免疫機構の障害 内分泌 栄養及び代謝疾患 Ⅴ 精神及び行動の障害
D12 D39 Ⅳ G64 女性生殖器の性状不詳又は不明の新生物 D48 その他及び部位不明の性状不詳又は不明の新生物 Ⅲ 総数 構成比 (%) 該当無し Ⅰ 感染症及び寄生虫症 Ⅱ 新生物 C54 子宮体部の悪性新生物 結腸 直腸 肛門及び肛門管の良性新生物 D25 子宮平滑筋腫 D27 卵巣の良性新生物 血液及び造血器の疾患並びに免疫機構の障害 内分泌 栄養及び代謝疾患 Ⅴ 精神及び行動の障害
糖尿病経口薬 QOL 研究会研究 1 症例報告書 新規 2 型糖尿病患者に対する経口糖尿病薬クラス別の治療効果と QOL の相関についての臨床試験 施設名医師氏名割付群記入年月日 症例登録番号 / 被験者識別コード / 1/12
 症例報告書 新規 2 型糖尿病患者に対する経口糖尿病薬クラス別の治療効果と QOL の相関についての臨床試験 施設名医師氏名割付群記入年月日 症例登録番号 / 被験者識別コード / 1/12 患者背景同意取得時から試験開始までの状況について記入 性別 男 女 年齢生年月日 歳 西暦年月日 身長. cm 体重. kg 腹囲. cm 糖尿病罹病期間 西暦年月 ~ 現在 喫煙 合併症 あり なし飲酒 あり
症例報告書 新規 2 型糖尿病患者に対する経口糖尿病薬クラス別の治療効果と QOL の相関についての臨床試験 施設名医師氏名割付群記入年月日 症例登録番号 / 被験者識別コード / 1/12 患者背景同意取得時から試験開始までの状況について記入 性別 男 女 年齢生年月日 歳 西暦年月日 身長. cm 体重. kg 腹囲. cm 糖尿病罹病期間 西暦年月 ~ 現在 喫煙 合併症 あり なし飲酒 あり
現況解析2 [081027].indd
![現況解析2 [081027].indd 現況解析2 [081027].indd](/thumbs/91/105571151.jpg) ビタミン D 製剤使用量と予後 はじめに 2005 年末調査の現況報告において 透析前血清カルシウム濃度 透析前血清リン濃度が望ましい値の範囲内にあった週 3 回の血液透析患者のみを対象に 各種リン吸着薬そしてビタミンD 製剤と生命予後との関係を報告した この報告では ビタミンD 製剤の使用の有無と生命予後との関係が解析されたのみであった そこで 今回の解析では 各種ビタミンD 製剤の使用量と予後との関係を解析した
ビタミン D 製剤使用量と予後 はじめに 2005 年末調査の現況報告において 透析前血清カルシウム濃度 透析前血清リン濃度が望ましい値の範囲内にあった週 3 回の血液透析患者のみを対象に 各種リン吸着薬そしてビタミンD 製剤と生命予後との関係を報告した この報告では ビタミンD 製剤の使用の有無と生命予後との関係が解析されたのみであった そこで 今回の解析では 各種ビタミンD 製剤の使用量と予後との関係を解析した
70 頭頸部放射線療法 放射線化学療法
 頭頸部放射線療法 放射線化学療法の患者への歯科治療 口腔ケア (1) 総論 1) 頭頸部の放射線 化学放射線療法の特徴 2) 頭頸部がん放射線療法による口腔への影響 3) 頭頸部放射線療法における歯科の役割 (2) 放射線治療による口腔合併症 ( 有害事象 ) と対処 1) 局所療法と急性 晩期障害 2) 口腔粘膜炎 3) 口腔乾燥症 4) 歯性感染症 カンジダ性口内炎 5) 味覚異常 6) 放射線性骨髄炎
頭頸部放射線療法 放射線化学療法の患者への歯科治療 口腔ケア (1) 総論 1) 頭頸部の放射線 化学放射線療法の特徴 2) 頭頸部がん放射線療法による口腔への影響 3) 頭頸部放射線療法における歯科の役割 (2) 放射線治療による口腔合併症 ( 有害事象 ) と対処 1) 局所療法と急性 晩期障害 2) 口腔粘膜炎 3) 口腔乾燥症 4) 歯性感染症 カンジダ性口内炎 5) 味覚異常 6) 放射線性骨髄炎
1 対象 1( 重複回答あり 大腸がん検診全国集計成績 件数 1. 地域検診 職域検診 無回答 3 合計 518
 大腸がん検診実態調査 の 集計成績 1 対象 1( 重複回答あり 大腸がん検診全国集計成績 件数 1. 地域検診 204 2. 職域検診 193 3. 118 無回答 3 合計 518 2 実施方法 ( 重複回答あり 大腸がん検診全国集計成績 件数 1. 便潜血検査 147 2. 便潜血検査 + 問診 139 3. 33 直接の場合 ( 重複回答あり ) 1. 全大腸内視鏡 29 2. 注腸 3 3.S
大腸がん検診実態調査 の 集計成績 1 対象 1( 重複回答あり 大腸がん検診全国集計成績 件数 1. 地域検診 204 2. 職域検診 193 3. 118 無回答 3 合計 518 2 実施方法 ( 重複回答あり 大腸がん検診全国集計成績 件数 1. 便潜血検査 147 2. 便潜血検査 + 問診 139 3. 33 直接の場合 ( 重複回答あり ) 1. 全大腸内視鏡 29 2. 注腸 3 3.S
葉酸とビタミンQ&A_201607改訂_ indd
 L FO AT E VI TAMI NB12 医療関係者用 葉酸 とビタミンB ビタミンB12 アリムタ投与に際して 警告 1 本剤を含むがん化学療法に際しては 緊急時に十分対応できる医療施設において がん化学療 法に十分な知識 経験を持つ医師のもとで 本剤の投与が適切と判断される症例についてのみ投 与すること 適応患者の選択にあたっては 各併用薬剤の添付文書を参照して十分注意すること また 治療開始に先立ち
L FO AT E VI TAMI NB12 医療関係者用 葉酸 とビタミンB ビタミンB12 アリムタ投与に際して 警告 1 本剤を含むがん化学療法に際しては 緊急時に十分対応できる医療施設において がん化学療 法に十分な知識 経験を持つ医師のもとで 本剤の投与が適切と判断される症例についてのみ投 与すること 適応患者の選択にあたっては 各併用薬剤の添付文書を参照して十分注意すること また 治療開始に先立ち
要望番号 ;Ⅱ-286 未承認薬 適応外薬の要望 ( 別添様式 ) 1. 要望内容に関連する事項 要望者 ( 該当するものにチェックする ) 学会 ( 学会名 ; 特定非営利活動法人日本臨床腫瘍学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 優先順位 33 位 ( 全 33 要望
 未承認薬 適応外薬の要望 ( 別添様式 ) 1. 要望内容に関連する事項 要望者 ( 該当するものにチェックする ) 学会 ( 学会名 ; 特定非営利活動法人日本臨床腫瘍学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 優先順位 33 位 ( 全 33 要望中 ) 要望する医薬品 成 分 名 ( 一般名 ) 販 売 名 会 社 名 国内関連学会 ロペラミドロペミンヤンセンファーマ株式会社
未承認薬 適応外薬の要望 ( 別添様式 ) 1. 要望内容に関連する事項 要望者 ( 該当するものにチェックする ) 学会 ( 学会名 ; 特定非営利活動法人日本臨床腫瘍学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 優先順位 33 位 ( 全 33 要望中 ) 要望する医薬品 成 分 名 ( 一般名 ) 販 売 名 会 社 名 国内関連学会 ロペラミドロペミンヤンセンファーマ株式会社
(別添様式)
 未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名 要望された医薬品 ユーシービージャパン株式会社要望番号 Ⅱ-254.2 成分名 Lacosamide ( 一般名 ) Vimpat 販売名 未承認薬 適応 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) 未承認薬 適応外薬 他の抗てんかん薬で十分な効果が認められないてんかん患者の部分発作
未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名 要望された医薬品 ユーシービージャパン株式会社要望番号 Ⅱ-254.2 成分名 Lacosamide ( 一般名 ) Vimpat 販売名 未承認薬 適応 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) 未承認薬 適応外薬 他の抗てんかん薬で十分な効果が認められないてんかん患者の部分発作
< E082AA82F1936F985E8F578C768C8B89CA816989FC92F994C5816A2E786C73>
 院内がん登録集計 登録対象 27( 平成 19) 年 1 月 1 日より 12 月 31 日までの 1 年間に当院で診断された悪性新生物の件数です 登録対象は新規の診断症例または他院で診断された初診症例であり 入院患者を対象としています 1 腫瘍 1 登録の原則に基づき同一患者に別のがん腫と判断されるがんが生じた場合には腫瘍毎の登録 ( 複数登録 ) となります 登録項目の内容院内がん登録を行うにあたって
院内がん登録集計 登録対象 27( 平成 19) 年 1 月 1 日より 12 月 31 日までの 1 年間に当院で診断された悪性新生物の件数です 登録対象は新規の診断症例または他院で診断された初診症例であり 入院患者を対象としています 1 腫瘍 1 登録の原則に基づき同一患者に別のがん腫と判断されるがんが生じた場合には腫瘍毎の登録 ( 複数登録 ) となります 登録項目の内容院内がん登録を行うにあたって
5. 死亡 (1) 死因順位の推移 ( 人口 10 万対 ) 順位年次 佐世保市長崎県全国 死因率死因率死因率 24 悪性新生物 悪性新生物 悪性新生物 悪性新生物 悪性新生物 悪性新生物 位 26 悪性新生物 350
 5. 死亡 () 死因順位の推移 ( 人口 0 万対 ) 順位年次 佐世保市長崎県全国 死因率死因率死因率 24 悪性新生物 328.4 悪性新生物 337.0 悪性新生物 286.6 25 悪性新生物 377.8 悪性新生物 354. 悪性新生物 290.3 位 26 悪性新生物 350.3 悪性新生物 355.7 悪性新生物 290.3 27 悪性新生物 332.4 悪性新生物 35. 悪性新生物
5. 死亡 () 死因順位の推移 ( 人口 0 万対 ) 順位年次 佐世保市長崎県全国 死因率死因率死因率 24 悪性新生物 328.4 悪性新生物 337.0 悪性新生物 286.6 25 悪性新生物 377.8 悪性新生物 354. 悪性新生物 290.3 位 26 悪性新生物 350.3 悪性新生物 355.7 悪性新生物 290.3 27 悪性新生物 332.4 悪性新生物 35. 悪性新生物
<4D F736F F D2089BB8A7797C C B B835888E790AC8C7689E6>
 2012 年 4 月更新作成者 : 宇根底亜希子 化学療法看護エキスパートナース育成計画 1. 目的江南厚生病院に通院あるいは入院しているがん患者に質の高いケアを提供できるようになるために 看護師が化学療法分野の知識や技術を習得することを目的とする 2. 対象者 1 ) レベル Ⅱ 以上で各分野の知識と技術習得を希望する者 2 ) 期間中 80% 以上参加できる者 3. 教育期間 時間間 1 年間の継続教育とする
2012 年 4 月更新作成者 : 宇根底亜希子 化学療法看護エキスパートナース育成計画 1. 目的江南厚生病院に通院あるいは入院しているがん患者に質の高いケアを提供できるようになるために 看護師が化学療法分野の知識や技術を習得することを目的とする 2. 対象者 1 ) レベル Ⅱ 以上で各分野の知識と技術習得を希望する者 2 ) 期間中 80% 以上参加できる者 3. 教育期間 時間間 1 年間の継続教育とする
目次 C O N T E N T S 1 下痢等の胃腸障害 下痢について 3 下痢の副作用発現状況 3 最高用量別の下痢の副作用発現状況 3 下痢の程度 4 下痢の発現時期 4 下痢の回復時期 5 下痢による投与中止時期 下痢以外の胃腸障害について 6 下痢以外の胃腸障害の副
 目次 C O N T E N T S 1 下痢等の胃腸障害 3 1.1 下痢について 3 下痢の副作用発現状況 3 最高用量別の下痢の副作用発現状況 3 下痢の程度 4 下痢の発現時期 4 下痢の回復時期 5 下痢による投与中止時期 5 1.2 下痢以外の胃腸障害について 6 下痢以外の胃腸障害の副作用発現状況 6 胃腸障害に関連する重篤な副作用発現症例 6 1.3 消化性潰瘍, 炎症性腸疾患等の胃腸疾患のある患者さんにおける安全性について
目次 C O N T E N T S 1 下痢等の胃腸障害 3 1.1 下痢について 3 下痢の副作用発現状況 3 最高用量別の下痢の副作用発現状況 3 下痢の程度 4 下痢の発現時期 4 下痢の回復時期 5 下痢による投与中止時期 5 1.2 下痢以外の胃腸障害について 6 下痢以外の胃腸障害の副作用発現状況 6 胃腸障害に関連する重篤な副作用発現症例 6 1.3 消化性潰瘍, 炎症性腸疾患等の胃腸疾患のある患者さんにおける安全性について
た 18 歳以上の AD/HD 患者を対象に 日本人を含むアジア人によるプラセボ対照二重盲検比較試験及びその長期継続投与試験が現在実施されており 本剤の製造販売者によれば これらの試験成績に基づき 本剤の成人期 AD/HD 患者への追加適応に関する承認事項一部変更承認申請が行われる予定とされている
 ( 別添 1) 平成 22 年 6 月 3 日薬事 食品衛生審議会医薬品第一部会資料 ( 抜粋 ) ストラテラカプセル 5mg 他の小児期 AD/HD 患者の成人期への 継続使用について 平成 22 年 6 月 3 日 医薬食品局審査管理課 1. 背景ストラテラカプセル 5mg 同 10mg 同 25mg( 以下 本剤 という ) は 小児期における注意欠陥 / 多動性障害 (AD/HD) の効能
( 別添 1) 平成 22 年 6 月 3 日薬事 食品衛生審議会医薬品第一部会資料 ( 抜粋 ) ストラテラカプセル 5mg 他の小児期 AD/HD 患者の成人期への 継続使用について 平成 22 年 6 月 3 日 医薬食品局審査管理課 1. 背景ストラテラカプセル 5mg 同 10mg 同 25mg( 以下 本剤 という ) は 小児期における注意欠陥 / 多動性障害 (AD/HD) の効能
を優先する場合もあります レントゲン検査や細胞診は 麻酔をかけずに実施でき 検査結果も当日わかりますので 初診時に実施しますが 組織生検は麻酔が必要なことと 検査結果が出るまで数日を要すること 骨腫瘍の場合には正確性に欠けることなどから 治療方針の決定に必要がない場合には省略されることも多い検査です
 動物の腫瘍インフォメーション シート 5 犬の骨肉腫 骨肉腫 とは 犬の骨から発生する悪性腫瘍の一種です 犬の骨にみられる腫瘍には 骨肉腫の他にもいくつかの種類がありますが ここでは 最もよくみられる骨肉腫について 診断方法や治療の選択肢をご説明します ご希望にあった治療法を選択していただく際に参考にしていただければ幸いです 1. 骨のがんかもしれないと診断されました どのような病気が考えられますか?
動物の腫瘍インフォメーション シート 5 犬の骨肉腫 骨肉腫 とは 犬の骨から発生する悪性腫瘍の一種です 犬の骨にみられる腫瘍には 骨肉腫の他にもいくつかの種類がありますが ここでは 最もよくみられる骨肉腫について 診断方法や治療の選択肢をご説明します ご希望にあった治療法を選択していただく際に参考にしていただければ幸いです 1. 骨のがんかもしれないと診断されました どのような病気が考えられますか?
<4D F736F F F696E74202D2088F38DFC B2D6E FA8ECB90FC8EA197C C93E0292E B8CDD8AB B83685D>
 乳癌の放射線治療 放射線治療科竹内有樹 K-net 2014.5.15 15 本日の内容 1 乳癌における放射線治療の役割 2 放射線治療の実際 3 当院での放射線治療 1 乳癌における放射線治療の役割 乳房温存術後の局所再発予防 乳癌局所治療の変遷 乳房温存術と放射線治療併用率の増加 本邦の乳がん手術術式の変遷 乳房温存療法における放射線治療併用率 乳房温存療法 ( 手術 + 放射線 ) の適応
乳癌の放射線治療 放射線治療科竹内有樹 K-net 2014.5.15 15 本日の内容 1 乳癌における放射線治療の役割 2 放射線治療の実際 3 当院での放射線治療 1 乳癌における放射線治療の役割 乳房温存術後の局所再発予防 乳癌局所治療の変遷 乳房温存術と放射線治療併用率の増加 本邦の乳がん手術術式の変遷 乳房温存療法における放射線治療併用率 乳房温存療法 ( 手術 + 放射線 ) の適応
3. 安全性本治験において治験薬が投与された 48 例中 1 例 (14 件 ) に有害事象が認められた いずれの有害事象も治験薬との関連性は あり と判定されたが いずれも軽度 で処置の必要はなく 追跡検査で回復を確認した また 死亡 その他の重篤な有害事象が認められなか ったことから 安全性に問
 フェキソフェナジン塩酸塩錠 6mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにフェキソフェナジン塩酸塩は 第二世代抗ヒスタミン薬の一つであり 抗原抗体反応に伴って起こる肥満細胞からのヒスタミンなどのケミカルメディエーターの遊離を抑制すると共に ヒスタミンの H1 作用に拮抗することにより アレルギー症状を緩和する 今回 フェキソフェナジン塩酸塩錠 6mg
フェキソフェナジン塩酸塩錠 6mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにフェキソフェナジン塩酸塩は 第二世代抗ヒスタミン薬の一つであり 抗原抗体反応に伴って起こる肥満細胞からのヒスタミンなどのケミカルメディエーターの遊離を抑制すると共に ヒスタミンの H1 作用に拮抗することにより アレルギー症状を緩和する 今回 フェキソフェナジン塩酸塩錠 6mg
Microsoft Word - SMART-C_manual_v2.doc
 SMART-C Ver.2 運用マニュアル SMART-C Ver.2 目次 : 画面構成 1 画面の基本的動作 1 画面一覧 ログイン画面 2 症例一覧画面 5 患者基本データ画面 6 投与量詳細 8 投与前データ 11 投与中 4 週 ~ 投与中 48 週 ~ 投与終了時 ~ 投与終了後 24 週 13 有害事象 15 併用薬 17 SMART-C Ver.2 画面構成 ログ イン 症例一覧画面
SMART-C Ver.2 運用マニュアル SMART-C Ver.2 目次 : 画面構成 1 画面の基本的動作 1 画面一覧 ログイン画面 2 症例一覧画面 5 患者基本データ画面 6 投与量詳細 8 投与前データ 11 投与中 4 週 ~ 投与中 48 週 ~ 投与終了時 ~ 投与終了後 24 週 13 有害事象 15 併用薬 17 SMART-C Ver.2 画面構成 ログ イン 症例一覧画面
Microsoft PowerPoint - 【資料3】届出マニュアル改訂について
 国立がん研究センターがん対策情報センター National Cancer Center Center for Cancer Control and Information Services 全国がん登録届出マニュアル 2016 2017 改訂版の発行について 国立研究開発法人国立がん研究センター がん対策情報センターがん登録センター 柴田亜希子 1 国立がん研究センターがん対策情報センター National
国立がん研究センターがん対策情報センター National Cancer Center Center for Cancer Control and Information Services 全国がん登録届出マニュアル 2016 2017 改訂版の発行について 国立研究開発法人国立がん研究センター がん対策情報センターがん登録センター 柴田亜希子 1 国立がん研究センターがん対策情報センター National
(2) 傷病分類別ア入院患者入院患者を傷病分類別にみると 多い順に Ⅴ 精神及び行動の障害 千人 Ⅸ 循環器系の疾患 千人 Ⅱ 新生物 千人となっている 病院では Ⅴ 精神及び行動の障害 千人 Ⅸ 循環器系の疾患 千人 Ⅱ 新生物 147.
 結果の概要 1 推計患者数 調査日に全国 ( 宮城県の石巻医療圏 気仙沼医療圏及び福島県を除く ) の医療施設で受療した推計患者数は 入院 1,341.0 千人 外来 7,260.5 千人である (1) 施設の種類 性 年齢階級別 入院 1,341.0 千人について 施設の種類別にみると 病院 1,290.1 千人 一般診療所 50.9 千人 性別にみると 男 613.6 千人 女 727.5 千人
結果の概要 1 推計患者数 調査日に全国 ( 宮城県の石巻医療圏 気仙沼医療圏及び福島県を除く ) の医療施設で受療した推計患者数は 入院 1,341.0 千人 外来 7,260.5 千人である (1) 施設の種類 性 年齢階級別 入院 1,341.0 千人について 施設の種類別にみると 病院 1,290.1 千人 一般診療所 50.9 千人 性別にみると 男 613.6 千人 女 727.5 千人
再審査報告書 販売名 平成 29 年 11 月 8 日 医薬品医療機器総合機構 1 ネスプ注射液 10µg/1mL プラシリンジ 同注射液 15µg/1mL プラシリンジ 同注射液 20µg/1mL プラシリンジ 同注射液 30µg/1mL プラシリンジ 同注射液 40µg/1mL プラシリンジ 同
 再審査報告書 販売名 平成 29 年 11 月 8 日 医薬品医療機器総合機構 1 ネスプ注射液 10µg/1mL プラシリンジ 同注射液 15µg/1mL プラシリンジ 同注射液 20µg/1mL プラシリンジ 同注射液 30µg/1mL プラシリンジ 同注射液 40µg/1mL プラシリンジ 同注射液 60µg/0.6mL プラシリンジ 同注射液 120µg/0.6mL プラシリンジ 同注射液
再審査報告書 販売名 平成 29 年 11 月 8 日 医薬品医療機器総合機構 1 ネスプ注射液 10µg/1mL プラシリンジ 同注射液 15µg/1mL プラシリンジ 同注射液 20µg/1mL プラシリンジ 同注射液 30µg/1mL プラシリンジ 同注射液 40µg/1mL プラシリンジ 同注射液 60µg/0.6mL プラシリンジ 同注射液 120µg/0.6mL プラシリンジ 同注射液
CIN 推進拠点事業概要 事業名 補助事業課題 採択課題名 事業代表者 事業担当者 補助事業予定期間 クリニカル イノベーション ネットワーク推進支援事業 クリニカル イノベーション ネットワーク (CIN) の推進拠点 CIN 構想の加速 推進を目指したレジストリ情報統合拠点の構築 国立国際医療研
 クリニカル イノベーション ネットワーク推進支援事業 CIN 構想の加速 推進を目指したレジストリ情報統合拠点の構築 事業代表者国立研究開発法人国立国際医療研究センター理事長國土典宏 資料 1-2 資料内容 事業の概要 国内の患者レジストリ等の状況 (1 次調査中間報告 ) CIN 推進拠点事業概要 事業名 補助事業課題 採択課題名 事業代表者 事業担当者 補助事業予定期間 クリニカル イノベーション
クリニカル イノベーション ネットワーク推進支援事業 CIN 構想の加速 推進を目指したレジストリ情報統合拠点の構築 事業代表者国立研究開発法人国立国際医療研究センター理事長國土典宏 資料 1-2 資料内容 事業の概要 国内の患者レジストリ等の状況 (1 次調査中間報告 ) CIN 推進拠点事業概要 事業名 補助事業課題 採択課題名 事業代表者 事業担当者 補助事業予定期間 クリニカル イノベーション
1)~ 2) 3) 近位筋脱力 CK(CPK) 高値 炎症を伴わない筋線維の壊死 抗 HMG-CoA 還元酵素 (HMGCR) 抗体陽性等を特徴とする免疫性壊死性ミオパチーがあらわれ 投与中止後も持続する例が報告されているので 患者の状態を十分に観察すること なお 免疫抑制剤投与により改善がみられた
 適正使用に欠かせない情報です 必ずお読みください 使用上の注意 改訂のお知らせ 注 1) 処方箋医薬品 ATORVASTATIN TABLETS AMALUET COMBINATION TABLETS 注 1) 処方箋医薬品 PRAVASTATIN SODIUM TABLETS 注 1) 注意 - 医師等の処方箋により使用すること PITAVASTATIN CALCIUM TABLETS 2016
適正使用に欠かせない情報です 必ずお読みください 使用上の注意 改訂のお知らせ 注 1) 処方箋医薬品 ATORVASTATIN TABLETS AMALUET COMBINATION TABLETS 注 1) 処方箋医薬品 PRAVASTATIN SODIUM TABLETS 注 1) 注意 - 医師等の処方箋により使用すること PITAVASTATIN CALCIUM TABLETS 2016
また リハビリテーションの種類別では 理学療法はいずれの医療圏でも 60% 以上が実施したが 作業療法 言語療法は実施状況に医療圏による差があった 病型別では 脳梗塞の合計(59.9%) 脳内出血 (51.7%) が3 日以内にリハビリテーションを開始した (6) 発症時の合併症や生活習慣 高血圧を
 栃木県脳卒中発症登録 5 ヵ年の状況 資料 2 1 趣旨栃木県では平成 10 年度から脳卒中発症登録事業として 県内約 30 の医療機関における脳卒中の発症状況を登録し 発症の危険因子や基礎疾患の状況 病型等の発症動向の把握に取り組んでいる 医療機関から保健環境センターに登録されるデータは年間約 4,200 件であり これまでに約 8 万件のデータが同センターに蓄積されている 今回 蓄積データのうち
栃木県脳卒中発症登録 5 ヵ年の状況 資料 2 1 趣旨栃木県では平成 10 年度から脳卒中発症登録事業として 県内約 30 の医療機関における脳卒中の発症状況を登録し 発症の危険因子や基礎疾患の状況 病型等の発症動向の把握に取り組んでいる 医療機関から保健環境センターに登録されるデータは年間約 4,200 件であり これまでに約 8 万件のデータが同センターに蓄積されている 今回 蓄積データのうち
p 13
 p 12 p 13 p 14 p 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 10. 安全性 (1) 副作用 ( 臨床検査値異常を含む ) 総症例 1030 例中 副作用が報告されたのは 519 例 (50.4%) でした 主な症状は鼓腸 197 例 (19.1%) 下痢 188 例 (18.3%) 腹部膨満
p 12 p 13 p 14 p 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 10. 安全性 (1) 副作用 ( 臨床検査値異常を含む ) 総症例 1030 例中 副作用が報告されたのは 519 例 (50.4%) でした 主な症状は鼓腸 197 例 (19.1%) 下痢 188 例 (18.3%) 腹部膨満
老人保健研究報告書(介護保険〜).indd
 平成 28 年度老人保健事業推進費等補助金 ( 老人保健健康増進等事業分 ) 事業 介護保険サービスの質の評価に資する 利用者の状態把握に関する調査研究事業 報告書 学校法人産業医科大学 平成 29 年 3 月 平成 28 年度老人保健事業推進費等補助金 ( 老人保健健康増進等事業分 ) 事業 介護保険サービスの質の評価に資する利用者の状態把握に関する調査研究事業 報告書 事業実施者 : 学校法人産業医科大学
平成 28 年度老人保健事業推進費等補助金 ( 老人保健健康増進等事業分 ) 事業 介護保険サービスの質の評価に資する 利用者の状態把握に関する調査研究事業 報告書 学校法人産業医科大学 平成 29 年 3 月 平成 28 年度老人保健事業推進費等補助金 ( 老人保健健康増進等事業分 ) 事業 介護保険サービスの質の評価に資する利用者の状態把握に関する調査研究事業 報告書 事業実施者 : 学校法人産業医科大学
「手術看護を知り術前・術後の看護につなげる」
 周術期看護エキスパートナース育成計画 作成者 : 高橋育代 1. 目的江南厚生病院に通院あるいは入院している手術を受ける患者に質の高いケアを提供できるようになるために 看護師が周術期看護分野の知識や技術を習得することを目的とする 2. 対象者 1) レベル Ⅱ 以上で手術看護分野の知識と技術習得を希望する者 2) 期間中 80% 以上参加できる者 3. 教育期間 時間 1 年間の継続教育とする 10
周術期看護エキスパートナース育成計画 作成者 : 高橋育代 1. 目的江南厚生病院に通院あるいは入院している手術を受ける患者に質の高いケアを提供できるようになるために 看護師が周術期看護分野の知識や技術を習得することを目的とする 2. 対象者 1) レベル Ⅱ 以上で手術看護分野の知識と技術習得を希望する者 2) 期間中 80% 以上参加できる者 3. 教育期間 時間 1 年間の継続教育とする 10
もくじ 第 1 章 乳房再建手術 とは 4 乳房再建手術 の方法にはどんな種類がありますか 乳房再建手術 はいつどのように いますか 第 2 章自分のからだの組織を使う 乳房再建手術 自分のからだの組織を使う 乳房再建手術 とはどういうものですか手術を受ける前に知っておきたいこと 手術 入院期間と費
 乳がん手術後に もういちど乳房を取り戻す 乳房再建手術 HandBook 監修 : 乳腺外科形成外科 昭和大学病院ブレストセンター 中村清吾埼玉医科大学総合医療センター形成外科 美容外科教授三鍋俊春 もくじ 第 1 章 乳房再建手術 とは 4 乳房再建手術 の方法にはどんな種類がありますか 乳房再建手術 はいつどのように いますか 第 2 章自分のからだの組織を使う 乳房再建手術 自分のからだの組織を使う
乳がん手術後に もういちど乳房を取り戻す 乳房再建手術 HandBook 監修 : 乳腺外科形成外科 昭和大学病院ブレストセンター 中村清吾埼玉医科大学総合医療センター形成外科 美容外科教授三鍋俊春 もくじ 第 1 章 乳房再建手術 とは 4 乳房再建手術 の方法にはどんな種類がありますか 乳房再建手術 はいつどのように いますか 第 2 章自分のからだの組織を使う 乳房再建手術 自分のからだの組織を使う
平成 28 年 10 月 17 日 平成 28 年度の認定看護師教育基準カリキュラムから排尿自立指導料の所定の研修として認めら れることとなりました 平成 28 年度研修生から 排泄自立指導料 算定要件 施設基準を満たすことができます 下部尿路機能障害を有する患者に対して 病棟でのケアや多職種チーム
 平成 28 年 10 月 17 日 平成 28 年度の認定看護師教育基準カリキュラムから排尿自立指導料の所定の研修として認めら れることとなりました 平成 28 年度研修生から 排泄自立指導料 算定要件 施設基準を満たすことができます 下部尿路機能障害を有する患者に対して 病棟でのケアや多職種チームの介入による下部尿路機能の回復のための包括的排尿ケアについて評価する ( 新 ) 排尿自立指導料 [
平成 28 年 10 月 17 日 平成 28 年度の認定看護師教育基準カリキュラムから排尿自立指導料の所定の研修として認めら れることとなりました 平成 28 年度研修生から 排泄自立指導料 算定要件 施設基準を満たすことができます 下部尿路機能障害を有する患者に対して 病棟でのケアや多職種チームの介入による下部尿路機能の回復のための包括的排尿ケアについて評価する ( 新 ) 排尿自立指導料 [
本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シ
 医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
PowerPoint プレゼンテーション
 平成 25 年 5 月 18 日健康セミナー 乳がんの治療について NTT 東日本札幌病院外科 小西和哉 1 本日の内容 検診 診断 治療方針 治療の実際 進行度 薬剤感受性 内分泌受容体 HER2 タンパク がん罹患率 2 日本人女性 16 人に 1 人が乳癌 欧米女性 8 人に 1 人が乳癌 がん生存率 3 乳がん罹患率 4 乳がんの危険因子 5 肥満 閉経後は発生リスクを高めます 既往歴 (
平成 25 年 5 月 18 日健康セミナー 乳がんの治療について NTT 東日本札幌病院外科 小西和哉 1 本日の内容 検診 診断 治療方針 治療の実際 進行度 薬剤感受性 内分泌受容体 HER2 タンパク がん罹患率 2 日本人女性 16 人に 1 人が乳癌 欧米女性 8 人に 1 人が乳癌 がん生存率 3 乳がん罹患率 4 乳がんの危険因子 5 肥満 閉経後は発生リスクを高めます 既往歴 (
Microsoft Word - program.doc
 1. 研修プログラムの特色 北海道医療大学歯科医師臨床研修プログラム 患者および家族とのより良い人間関係を築き 全人的な視点から得られた医療情報を理解し それに基づいた総合治療計画を立案する 歯科疾患予防および治療における基本的技能を身につけるとともに 自ら行なった処置の経過を観察 評価し 診断と治療に常にフィードバックする態度 習慣を身につける 2. 臨床研修の目標 ( 到達目標 ) 臨床研修の目標の概要歯科医師臨床研修の目標は
1. 研修プログラムの特色 北海道医療大学歯科医師臨床研修プログラム 患者および家族とのより良い人間関係を築き 全人的な視点から得られた医療情報を理解し それに基づいた総合治療計画を立案する 歯科疾患予防および治療における基本的技能を身につけるとともに 自ら行なった処置の経過を観察 評価し 診断と治療に常にフィードバックする態度 習慣を身につける 2. 臨床研修の目標 ( 到達目標 ) 臨床研修の目標の概要歯科医師臨床研修の目標は


