はじめに 平成 21(2009) 年 5 月 1 日に倫理委員会 薬物治験審査委員会の皆様に利益相反マネジメントの実施を依頼してより 7 年が経ちました この間 国などによる各種倫理指針の改訂をはじめ 日本医学会や日本学術会議などによるガイドラインの発行など 利益相反マネジメントを取り巻く状況は 日
|
|
|
- らむ ほがり
- 5 years ago
- Views:
Transcription
1 臨床研究の利益相反マネジメントガイドライン 平成 28(2016) 年 4 月 1 日 利益相反マネジメント委員会 0
2 はじめに 平成 21(2009) 年 5 月 1 日に倫理委員会 薬物治験審査委員会の皆様に利益相反マネジメントの実施を依頼してより 7 年が経ちました この間 国などによる各種倫理指針の改訂をはじめ 日本医学会や日本学術会議などによるガイドラインの発行など 利益相反マネジメントを取り巻く状況は 日々変化しております これらの変化に対応するため 平成 22(2010) 年 5 月 17 日に発行した 臨床研究の利益相反マネジメントについて ~ 各委員会担当者用資料 ~ を新たにガイドラインとして改訂することといたしました このガイドラインを参考に 今後も利益相反マネジメントにご協力いただきたく よろしくお願い申し上げます 利益相反マネジメント委員会 委員長山下精彦 1
3 目次 1. 利益相反マネジメントを行う際の守秘義務 研究に係る利益相反状況申告書 の確認事項 各委員会による確認事項 利益相反事項があった場合の具体的なマネジメント方法 (1) 同意説明文書への記載例 (2) 研究計画の変更 (3) 参考資料について 利益相反マネジメント委員会への回付 各委員会による審議後の対応 臨床研究に関する利益相反マネジメントの Q&A
4 1. 利益相反マネジメントを行う際の守秘義務 研究者から提出される 研究に係る利益相反状況申告書 には 個人的収入など 個人情報が多数含まれています 申告書の内容は 提出された研究についての審議にのみ使用し その情報は一切漏らさないでください 利益相反マネジメントに関与する教職員及び各委員会の委員には守秘義務が課せられていますので十分ご注意ください 学校法人日本医科大学利益相反マネジメント規程 ( 守秘義務 ) 第 22 条 COI 委員会の関係者 利益相反アドバイザー 事務局員及びその他の関係者は 第 16 条に基づく教職員等の自己申告の内容及び COI 委員会の審議の内容等 職務上知り得た一切の情報について その秘密を守らなければならない 3
5 2. 研究に係る利益相反状況申告書 の確認事項 (1) 倫理委員会 薬物治験審査委員会 ( 以下 各委員会 ) に研究を申請する研究者に対し 研究に係る利益相反状況申告書 ( 以下 申告書 ) を 研究の申請書と共に提出するよう指導してください (2) 申告書を受領した各委員会の事務局担当者は 以下の点に注意して 記 載漏れや記載の間違いがないか 確認してください a. 研究課題名 研究課題名が 各委員会へ申請した研究の課題名と同一か? b. 研究参加者の確認研究申請書に記載された研究者と 申告書に記載された研究者が一致しているか? 学外の研究分担者を記載する必要はありません 人を対象とする医学系研究に関する倫理指針 が施行されたことにより 侵襲 ( 軽微な侵襲を除く ) を伴う研究であって介入を行うものを実施する場合には モニタリング及び必要に応じて監査を実施しなければなりません 学内の研究者がモニタリングや監査を行う場合には 申告書に記載があるか確認してください c. 研究の種別企業治験もしくは企業治験以外のいずれかが選択されているか? 治験とは 医薬品もしくは医療機器の製造販売承認申請を目的とした第 Ⅰ~Ⅲ 相の臨床試験及び製造販売後臨床試験 ( 第 Ⅳ 相 ) をいいます 治験は 医薬品の臨床試験の実施の基準に関する省令 (GCP: 4
6 Good Clinical Practice) に従って行います 治験以外の研究は 人を対象とする医学系研究に関する倫理指針 など 各種の倫理指針等に沿って行います d. 研究体制どのような体制で研究を実施するのか 研究体制が選択されているか? 多施設共同研究 医師主導研究 が選択されている場合は 代表施設名や代表施設での状況が記載されているかも確認してください その他 が選択されている場合は 詳細が記載されているかも確認してください e. 研究の資金源 ( 予定含む ) 研究の資金源が正確に記載されているか? ヘルシンキ宣言 及び 人を対象とする医学系研究に関する倫理指針 において 研究の資金源を研究計画書 患者 ( 被験者 ) への同意説明文書に記載することを定めています そのため 申告書にも研究の資金源について正確に記載するよう求めてください i. 企業等 治験以外の共同研究や受託研究等により企業から研究費が提供されている場合は 企業名と金額が記載されているか 確認してください 企業等と共同研究 受託研究を行う際は 大学 ( 法人 ) もしくは病院として契約を締結する必要があることを研究者に通知してください 治験以外の研究については 各所属の庶務課が窓口となり 手続きを行います 5
7 ii. 助成金 助成金によっては 企業が別の名称の財団を設立し 出資している場合があるため 助成元の背景 ( 設立趣旨やスポンサー等 ) がわかるような資料の提出を求めてください iii. 保険診療の範囲内 特別に研究費を使用せず 保険診療の範囲内で研究を行う場合は 保険診療の欄が選択されているか 確認してください 多施設共同研究の場合は 保険診療の範囲内の研究であっても 検体やケースカードの送付など 様々な費用が発生することが想定されるため これらの費用が発生する場合には 保険診療の範囲内 ではなく その他 の欄を選択し 誰がその費用を支出するのか 記載を求めてください iv. その他 その他 が選択されている場合は 詳細が記載されているか 確認してください 外部から資金提供を受けず 所属の研究助成費 ( 医局費等 ) 等で行う場合は その他 の欄に記載されているか 確認してください f. 研究に伴う医薬品 機器の提供研究に伴う医薬品 機器の提供を受けるか受けないか いずれかが選択されているか? 研究に使用する薬剤 研究機器などを無償で提供を受ける場合は 提供元の名称と価格の概算が記載されているか 確認してください 研究に使用する薬剤 研究機器などを割引等の範囲を超えて通常よ 6
8 り安く提供を受ける場合は 提供元の名称と優遇価格が記載されているか 確認してください 薬剤の提供を受ける場合は 共同研究契約等の契約の範囲内での提供か Material Transfer Agreement(MTA) を締結した上での提供か 確認してください 研究機器の提供を受ける場合は 資材課の手続きが必要です これらの手続きを行っているか もしくは行う予定であるか 確認してください 薬剤や研究機器などの物品の提供ではなく 抗体作製や血液検査の実施といったサービスの提供を受ける場合は その他の欄にサービスの内容が記載されているか 確認してください サービスの提供を受けている場合は 共同研究契約等の契約の範囲内での提供か 何らかの契約を締結した上でのサービスの提供か 確認してください 研究費等で通常の手続きを経て 購入や賃借する場合は 外部からの提供には該当しません g. 研究の対象となる医薬品 医療機器の製造販売企業名本研究の対象となる医薬品 医療機器の製造販売企業名が記載されているか? 各委員会に提出された医療用医薬品や医療機器の添付文書の製造販売企業名が記載されているか 確認してください 手術手技の研究やコホート研究など 医薬品や医療機器を研究対象としない研究の場合には 該当なし など 該当する企業がないことが明確になっているか 確認してください 研究対象となる医薬品や医療機器の製造販売企業だけでなく 比較対象となる医薬品や医療機器の製造販売企業名も記載されているか 7
9 確認してください 本研究のために使用するものの 研究対象とはならない医薬品や医 療機器の製造販売企業名を記載する必要はありません h. 利益相反 (COI) に関する事項治験依頼者または申告書に記載された企業と研究代表者 研究分担者等が所属する部署との産学連携活動の実施状況について 有 もしくは 無 のいずれかが選択されているか? 有 が選択されていた場合は 治験依頼者または申告書に記載された企業との産学連携活動内容が記載されているか 確認してください 研究代表者は 研究に直接関与するものだけではなく 研究に関連する全ての産学連携活動内容を申告する必要があります i. 研究代表者とその家族の利益相反に関する事項について (1)-(4) の全ての欄の 有 もしくは 無 のいずれかが選択さ れているか? j. 学内分担研究者等の利益相反に関する事項について 有 もしくは 無 のいずれかが選択されているか? 研究代表者が学内研究分担者等全員に聞き取り調査を行います 有 が選択されていた場合は 該当者自身が記載をした別紙様式 3( 研究分担者等用 ) があるかを確認してください (3) 申告書には 個人情報が含まれるため その取扱い については 十分注意してください 8
10 3. 各委員会による確認事項 利益相反には 実際に弊害が生じていなくとも 弊害が生じているかのごとく見られる状況が含まれるため 各委員会は 研究に関連する利益相反事項がある場合には 客観性 公平性が保たれていることが十分に説明されているか 確認してください (1) 本法人内ルールの遵守 本法人には 以下のようなルールがあります これらのルールが遵守されて いるか 確認してください a. 企業等との共同研究 受託研究の契約は 大学 ( 法人 ) もしくは病院が締結する b. MTA は 研究者個人が責任を持って締結し 研究マテリアルの受入れ 管理を行う c. 研究機器の受入れは 各所属資材課を通じて行う d. 研究に関するサービスの提供など 研究に関して企業等から何らかの利便の提供を受ける場合は 大学 ( 法人 ) もしくは病院が契約を締結する e. 研究費の受入れは大学 ( 法人 ) もしくは病院が行う ( 研究者個人が謝金等を受け取る研究は認められない ) (2) 各委員会は 以下の点を確認したうえで 利益相反に関する審議を行っ てください a. 研究体制 利益相反事項がある研究者が研究の客観性 公平性に疑いをもたれかね ないような役割を担っていないか? 9
11 客観性 公平性を損なうという印象を社会に与えることがないよう にどのような研究体制になっているのか 確認してください b. 研究資金源研究計画書や同意説明文書等に記載されているか? 企業等から資金の提供を受ける場合 契約の締結が必要になります 各委員会での承認後に契約を締結することになりますので 契約書の案が添付されているのか 確認してください 添付されていない場合は 添付を求めてください c. 研究に伴う医薬品 機器の提供研究計画書や同意説明文書等に記載されているか? 外部から研究に伴う医薬品 機器の提供がある場合は 必ず記載を求めると共に 学内手続きを行う必要があります d. 治験依頼者または申告書に記載された企業との関係研究計画書や同意説明文書等に開示されているか? 研究者や研究者の所属する部署との利益相反に関する事項がすべて 研究計画書や同意説明文書等に開示されているか 確認してください 研究者や研究者の所属する部署との利益相反に関する事項をどのように管理しているのか その対策についても記載があることを確認してください 治験依頼者または申告書に記載された企業が 研究データの集計 保管 統計解析 解釈に関して 影響力を行使できる状態になっていないか 確認してください 治験依頼者または申告書に記載された企業と締結する契約書の内容 10
12 が研究計画書と異なっていないか 確認してください 企業との契約において 企業側にデータや研究成果 研究成果に基づく知的財産を提供することが義務付けられている場合は 企業がデータの解釈等に影響を与える余地のない状況になっていることを確認すると共に 企業側に提供されることが研究計画書にも記載されているか確認してください e. 外部への情報公開研究結果の良し悪しにかかわらず 必ず公表することになっているか? 研究結果の学会発表や論文発表の決定に関して 資金提供者や企業が影響力を行使することは認められません 介入を伴う研究の場合 研究開始前に外部データベースに登録するなど 透明性を保つための措置がなされているか 確認してください 11
13 4. 利益相反事項があった場合の具体的なマネジメント方法 (1) 同意説明文書への記載例研究計画書や患者 ( 被験者 ) への同意説明文書には 資金源 起こりうる利害の衝突 研究者の関連組織との関わり について記載する必要があります 同意説明文書への記載例を参考に 研究者に対して指導してください また 利益相反 という文言を同意説明文書に記載する場合は 利益相反 という言葉自体の意味が 説明されているか 確認してください 例 1: 利益相反とは利益相反とは 外部との利益関係により 教育 研究に従事する者としての社会的責任と 外部との関係によって得る利益とが衝突 相反するため 大学の研究者として必要な 公正な姿勢 が損なわれる または損なわれるのではないかと第三者から疑われることを言います 利益相反は法的に何ら問題がない場合にも発生する状況であるため 日本医科大学においては 臨床研究を実施する際には 研究者に利益相反状況の申告を義務付け 大学として利益相反を適切に管理しています 例 2: 企業から研究費を得ている場合本研究は ABC 製薬の研究資金を用いて実施するものです しかし 本研究は 日本医科大学の 研究代表者 が責任を持って行っており 研究計画の立案 実施 集計 保管 統計解析 解釈に関して ABC 製薬は一切関与しません また 本研究を行うことについては 日本医科大学 委員会に申請し 倫理的に問題がなく 公正な研究を行うことができると判断を受けたうえで実施しています 例 3: 企業と一緒に研究を行っている場合 本研究は ABC 製薬との共同研究です 研究実施のために ABC 製薬から 12
14 資金提供を受けていますが 本研究は 日本医科大学の 研究代表者 が責任を持って行うものであり 本研究を行うことについては 日本医科大学 委員会に申請し 倫理的に問題がなく 公正な研究を行うことができると判断を受けたうえで実施しています 例 4: 所属する部署に寄付金等がある場合本研究は 科の研究費により行います 当科は 本研究に用いる医薬品 ( 医薬品名 ) を製造販売する ABC 製薬株式会社から寄付金を受けていますが 本研究に関係するものではありません 本研究は 日本医科大学の 研究代表者 が責任を持って行っており 研究計画の立案 実施 集計 保管 統計解析 解釈に関して ABC 製薬は一切関与しません また 本研究を行うことについては 日本医科大学 委員会に申請し 倫理的に問題がなく 公正な研究を行うことができると判断を受けたうえで実施しています 例 5: 試薬 医療機器等何らかの物品 技術的サービス ( 分析の実施や抗体の作製などのサービス ) 提供を無償もしくは安価に受けている場合本研究は 科の研究費により行います 本研究に用いる医薬品 ( 医薬品名 ) については 製造販売する ABC 製薬株式会社から無償で提供を受けています 本研究は 日本医科大学の 研究代表者 が責任を持って行っており 研究計画の立案 実施 集計 保管 統計解析 解釈に関して ABC 製薬は一切関与しません また 本研究を行うことについては 日本医科大学 委員会に申請し 倫理的に問題がなく 公正な研究を行うことができると判断を受けたうえで実施しています 例 6: 研究者等が個人的に収入を得ている場合この臨床研究に使用する医薬品の一つ ( 医薬品名 ) は ABC 株式会社のものを使用します 研究 ( 代表 参加 ) 医師の ( 医師名 ) は ABC 株式会社主催の講演会等で講演をしていますが 本研究計画の立案 実施 集計 保管 統計解 13
15 析 解釈に関して ABC 製薬は一切関与しません また 本研究を行うことについては 日本医科大学 委員会に申請し 倫理的に問題がなく 公正な研究を行うことができると判断を受けたうえで実施しています 例 7: 企業等が出資する NPO 法人等が研究の主体となり 研究を行う場合この臨床研究は ABC 株式会社の資金により NPO 法人 が主体となり 全国の複数の医療機関で行われています NPO 法人 は~ 記載例: がん患者を対象とした多施設共同による質の高いがん臨床研究 臨床研究を企画立案し 実施する研究者を支援し その研究成果をもってがん治療の進歩 及び発展に寄与し 人類の福祉に貢献することを目的とする組織であり その趣旨に賛同する会員からの会費及び企業からの寄付金等によって運営されています この臨床研究は 資金提供側の意見によって研究結果が左右されることはなく 研究結果は どのような結果であっても公表されます この臨床研究については NPO 法人 の倫理委員会で 患者さんを対象とした臨床研究として 医学的に適切であり 患者さんの権利 健康が守られていることが審査され承認を受けています また 日本医科大学での臨床研究は 日本医科大学の 研究代表者 が責任をもって行うものであり この臨床研究を行うことについては日本医科大学 委員会に申請し 倫理的に問題がなく 公正な研究を行うことができると判断を受けたうえで実施しています 例 8: 研究代表施設が企業から研究費を得て行う研究に参加する場合この臨床研究は ABC 株式会社と研究代表施設の 大学が共同研究契約を締結のうえ ABC 株式会社から資金提供を受け 全国の複数の医療機関で行われています 日本医科大学は 研究費の提供は受けず 保険診療の範囲内で 研究に協力しています ABC 株式会社は薬剤に関する情報提供を本研究グループに対して行いますが 本研究計画の立案 実施 集計 保管 統計解析 解釈には関与せず 研究代表施設の倫理委員会で患者さんを対象とした臨床研究とし 14
16 て 医学的に適切であり 患者さんの権利 健康が守られていることが審査され承認を受けています また 日本医科大学での臨床研究は 日本医科大学の 研究代表者 が責任をもって行うものであり この臨床研究を行うことについては日本医科大学 委員会に申請し 倫理的に問題がなく 公正な研究を行うことができると判断を受けたうえで実施しています 例 9: 公的研究費を得て研究を実施する場合この臨床研究は 平成 年度 の研究助成を得て実施します ( 助成番号 ) 本研究を行うことについては 日本医科大学 委員会に申請し 倫理的に問題がなく 公正な研究を行うことができると判断を受けたうえで実施しています 15
17 (2) 研究計画の変更治験依頼者または申告書に記載された企業から多額な個人的利益を得ている研究者が参加している場合 社会からみて その研究自体に バイアスがかかっているのではないかと疑われる可能性があります 一方で その研究者が参加しなければ 研究を実施できない場合も考えられます そのため 研究計画では 治験依頼者または申告書に記載された企業から多額な個人的利益を得ている研究者が参加したとしても 研究の客観性 公平性を損なうようなことがない研究であることを示す必要があります 研究の客観性 公平性が保たれていることの説明が不十分である場合には 研究計画の変更を求めてください 参考 : 薬事 食品衛生審議会薬事分科会申し合わせ ( 平成 20 年 3 月 24 日 ) ( 審議不参加の基準 ) 1) 委員等本人又は家族が 申告対象期間中に審議品目の製造販売業者又は競合企業からの寄附金 契約金等の受取 ( 又は割当て 以下同じ ) 実績があり それぞれの個別企業からの受取額が 申告対象期間中で年度あたり 500 万円を超える年度がある場合は 当該委員等は 当該審議品目についての審議又は議決が行われている間 部会等の審議会場から退室する ( 議決不参加の基準 ) 2) 委員等本人又は家族が 申告対象期間中に審議品目の製造販売業者又は競合企業から寄附金 契約金等の受取実績があり それぞれの個別企業からの受取額が 申告対象期間中いずれも年度あたり500 万円以下の場合は 当該委員等は 部会等へ出席し 意見を述べることができるが 当該審議品目についての議決には加わらない ただし 寄附金 契約金等が 申告対象期間中いずれも年度あたり50 万円以下の場合は 議決にも加わることができる 16
18 (3) 参考資料 利益相反マネジメントを行う上で 様々な資料が出されています 次の資料を参考にして 利益相反マネジメントを実施してください 国立研究開発法人日本医療研究開発機構平成 28 年 3 月 17 日研究活動における利益相反の管理に関する規則 u.pdf 厚生労働科学研究における利益相反 (Conflict of Interest:COI) の管理に関する指針 ( 平成 27 年 4 月 1 日一部改正 ) kouseikagakuka/150407sisin.pdf 日本医学会平成 27 年 3 月一部改定 医学研究の COI マネージメントに関するガイドライン 国立大学附属病院長会議平成 26 年 9 月改定 企業等からの資金提供状況の公表に関するガイドライン 日本学術会議平成 26 年 3 月 27 日 我が国の研究者主導臨床試験に係る問題点と今後の対応策 17
19 全国医学部長病院長会議平成 26 年 2 月 24 日改訂 医系大学 研究機関 病院の COI( 利益相反 ) マネージメントガイドライン 日本学術会議平成 25 年 12 月 20 日 臨床研究にかかる利益相反 (COI) マネージメントの意義と透明性確保について 国立大学附属病院長会議平成 25 年 9 月 19 日 臨床研究の信頼性確保と利益相反の管理に関する緊急対策 日本製薬工業協会平成 23 年 3 月 2 日 企業活動と医療機関等の関係の透明性ガイドライン 18
20 5. 利益相反マネジメント委員会への回付 (1) 利益相反マネジメント委員会による審議が相当という場合は 事務局を経由して 審議に関連する次の書類を利益相反マネジメント委員会に回付してください a. 各委員会に提出された申請書の写し b. 研究に係る利益相反状況申告書 ( 別紙様式 3) の写し c. 利益相反マネジメント委員会への回付依頼書 ( 任意書式 ) (2) 提出された書類をもとに 利益相反マネジメント委員会で審議します (3) 利益相反マネジメント委員会での審議結果を回付元の各委員会に通知し ます (4) 各委員会では 利益相反マネジメント委員会での審議結果を参考に 申 請された研究について 最終的な判断を行い 申請者に対して審議結果を 通知してください (5) 各委員会は 利益相反事項を含む審議結果を COI 自己申告書送付一覧 に記載し 利益相反マネジメント委員会に報告してください 19
21 6. 各委員会による審議後の対応 (1) 各委員会事務局において 利益相反事項を含む審議結果を COI 自己申 告書送付一覧 に記載し 研究に係る利益相反状況申告書 ( 別紙様式 3) の写しと共に 利益相反マネジメント委員会事務局に送付してください (2) 申告書には 個人情報が多数含まれるため 保管の際は 十分注意して ください 20
22 日本医科大学 委員会 COI 自己申告書送付一覧 ( 第 回平成 年 月 日 ) 区分審査番号申請部署申請者課題名研究期間審査結果 COI に関する事項 年月日 ~ 年月日 年月日 ~ 年月日 年月日 ~ 年月日 年月日 ~ 年月日 年月日 ~ 年月日 年月日 ~ 年月日 年月日 ~ 年月日 区分欄には 治験の場合は 治 自主研究の場合は 自 と記載をお願いします 21
23 記載例 日本医科大学 委員会 COI 自己申告書送付一覧 ( 第 52 回平成 21 年 11 月 19 日 ) 区分審査番号申請部署申請者課題名研究期間審査結果 COI に関する事項 自 科日医太郎 を用いた 疾患への治療 H21 年 12 月 1 日 ~ H24 年 11 月 30 日 ( 予定 ) 承認 同意説明文書への記載を確認 自 科武蔵杉子 症候群におけるマーカー探索 H21 年 12 月 1 日 ~ H22 年 11 月 30 日 条件付き承認 11/26 承認 同意説明文書への記載を指導し 変更後承 認 自 科多摩永男ヒト脂肪由来幹細胞の研究使用について H21 年 12 月 1 日 ~ H22 年 11 月 30 日 承認 COI に関する事項なし 治 科千葉北斗 を対象としたプラセボ対照 二重 盲検 無作為化並行群間比較による探索 試験 ( 第 Ⅱ 相 ) H21 年 12 月 1 日 ~ H22 年 11 月 30 日 承認 治験調整医師としての個人収入は 一般的 範囲内で問題ないと判断 申請通り承認 自 科日獣花子 症の新規診断方法について H21 年 12 月 1 日 ~ H22 年 11 月 30 日 COI 委員会に回付 条件付き承認 11/26 承認 COI 委員会での審議結果を通知し 研究計 画一部変更後承認 年月日 ~ 年月日 区分欄には 治験の場合は 治 自主研究の場合は 自 と記載をお願いします 22
24 7. 臨床研究に関する利益相反マネジメントの Q&A Q1. なぜ各委員会が利益相反マネジメントを行わなければならないのです か? A1. 人を対象とする医学系研究に関する倫理指針において 倫理審査委員会の役割 責務として 倫理的観点及び科学的観点から 研究機関及び研究者等の利益相反に関する情報も含めて中立的かつ公正に審査を行う ことが定められているためです また 医薬品の臨床試験の実施の基準に関する省令 のガイダンスについて でも 治験審査委員会の責務 ( 第 32 条 ) の2(6) のその他治験審査委員会が必要と認める資料の例として 企業との連携がある場合 利益相反に関する資料等 が挙げられています Q2. 臨床研究の利益相反をマネジメントする際に一番重要なことは何です か? A2. 患者 ( 被験者 ) さんが不当な不利益を被らないようにマネジメントすることが一番重要です 臨床研究においては 人間の尊厳及び人権を守らなければなりません 臨床研究の質及び透明性の確保を基本として 科学的な客観性を保証するようにマネジメントを行ってください 23
25 Q3. 研究者が提出した自己申告書に 虚偽の内容が記載されていたために 適切な利益相反マネジメントを行うことできず 問題になった場合は どうすればよいのですか? A3. 各委員会は 研究者が提出した自己申告書をもとに審議を行う機関であり その内容について調査を行う機関ではありません そのため 基本的に提出を受けた自己申告書の内容について 審議を行うことを原則としています 各委員会において 研究者が提出した自己申告書をもとに適切な利益相反マネジメントを行っていたのであれば 各委員会の責任ではなく 虚偽の内容を申告した研究者自身の責任となります 虚偽の申告を行った研究者自身が 自らの責任において 説明責任を負うことになります Q4. 公正な研究を行うために 利益相反事項のある研究者には研究への参 加を取りやめること もしくは研究への参加形態の変更を求めなけれ ばなりませんか? A4. 研究者が自らの専門領域で特殊な治療に関する臨床研究を行う場合 その研究者でなくてはできない研究が多数あります この研究ができなくなっては 生命科学の進歩にとって 大きな損失になります そのため 利益相反問題となりかねないような利益相反事項を抱える研究者が参加する場合には 研究の客観性 公平性を損なうような研究計画でないことを確認するとともに 定期的に各委員会への報告を求めたり 第三者による監査を義務付けたりするなど 公正な研究が実施できるよう 検討し 対応してください 24
26 平成 28(2016) 年 4 月 1 日 学校法人日本医科大学 利益相反マネジメント委員会 第二版発行 問合せ先 利益相反マネジメント委員会事務局 nms-tlo@nms.ac.jp 電話 : FAX:
平成 28 年 4 月版 別紙様式 3 研究に係る利益相反状況申告書 Q&A Q1. 学内研究分担者等の氏名 Q1-1 Q1-2 Q1-3 Q1-4 質問学外の研究分担者名を記載しなくてもよいのですか? 学内研究分担者等 というのは どのような人をいうのですか? モニタリング 監査とはどのようなもの
 別紙様式 3 研究に係る利益相反状況申告書 Q&A Q1. 学内研究分担者等の氏名 Q1-1 Q1-2 Q1-3 Q1-4 質問学外の研究分担者名を記載しなくてもよいのですか? 学内研究分担者等 というのは どのような人をいうのですか? モニタリング 監査とはどのようなものですか? 欄が足りない場合はどうすればよいですか? 回答記載する必要はありません ただし その研究者が本学において研究を実施する場合には記載してください
別紙様式 3 研究に係る利益相反状況申告書 Q&A Q1. 学内研究分担者等の氏名 Q1-1 Q1-2 Q1-3 Q1-4 質問学外の研究分担者名を記載しなくてもよいのですか? 学内研究分担者等 というのは どのような人をいうのですか? モニタリング 監査とはどのようなものですか? 欄が足りない場合はどうすればよいですか? 回答記載する必要はありません ただし その研究者が本学において研究を実施する場合には記載してください
特定臨床研究に関する手順書
 学校法人日本医科大学における特定臨床研究に関する手順書 ( 新規申請分 ) 1. 目的 本手順書は 学校法人日本医科大学における特定臨床研究に関する規程 ( 以下 規程 という ) を円滑に運用するために 本法人における手順を示すものである 2. 用語の定義 2.1 全般本手順書において使用する用語は 規程において使用する用語の例によるものとする 2.2 付属所属長規程第 5 条第 2 項により 理事長は実施医療機関の管理者の権限を次に定める付属所属長に委任しているため
学校法人日本医科大学における特定臨床研究に関する手順書 ( 新規申請分 ) 1. 目的 本手順書は 学校法人日本医科大学における特定臨床研究に関する規程 ( 以下 規程 という ) を円滑に運用するために 本法人における手順を示すものである 2. 用語の定義 2.1 全般本手順書において使用する用語は 規程において使用する用語の例によるものとする 2.2 付属所属長規程第 5 条第 2 項により 理事長は実施医療機関の管理者の権限を次に定める付属所属長に委任しているため
(2) 利益相反についての事務局勉強会 ( 平成 20 年 8 月 25 日 ~8 月 27 日 ) 利益相反に関する業務を知的財産 ベンチャー育成 (TLO) センターで行うのにあたり 利益相反マネジメント委員会の学外委員である弁護士 2 名から 利益相反に関する基礎的な事項についてレクチャーを受
 利益相反マネジメント委員会 1. 構成員について平成 20 年 4 月 1 日に 学校法人日本医科大学に利益相反マネジメント委員会を設置し 日本医科大学及び日本獣医生命科学大学の利益相反問題については 法人としてマネジメントを行っていくものとして 下記のメンバーで本委員会が発足した 委員長 : 隈崎達夫 ( 学校法人日本医科大学常務理事 ) 副委員長 : 鎌田隆 ( 弁護士 学校法人日本医科大学理事
利益相反マネジメント委員会 1. 構成員について平成 20 年 4 月 1 日に 学校法人日本医科大学に利益相反マネジメント委員会を設置し 日本医科大学及び日本獣医生命科学大学の利益相反問題については 法人としてマネジメントを行っていくものとして 下記のメンバーで本委員会が発足した 委員長 : 隈崎達夫 ( 学校法人日本医科大学常務理事 ) 副委員長 : 鎌田隆 ( 弁護士 学校法人日本医科大学理事
07案3団体あて臨床研究法COI通知
 様式 A 利益相反管理基準 ver.3.0 日付所属機関立場氏名利用基準 研究課題 : 基準 1 基準 2 研究責任医師は 次に掲げる事項について 研究計画書及び説明文書に記載し 研究結果の公表時に開示すること 研究責任医師以外の者が研究成果を公表する場合も 同様に開示すること 1 規則第 21 条第 1 項第 1 号に規定する関与 ( 研究に対する関与 ) として 次に掲げる関与が有る場合には その内容ア医薬品等製造販売業者
様式 A 利益相反管理基準 ver.3.0 日付所属機関立場氏名利用基準 研究課題 : 基準 1 基準 2 研究責任医師は 次に掲げる事項について 研究計画書及び説明文書に記載し 研究結果の公表時に開示すること 研究責任医師以外の者が研究成果を公表する場合も 同様に開示すること 1 規則第 21 条第 1 項第 1 号に規定する関与 ( 研究に対する関与 ) として 次に掲げる関与が有る場合には その内容ア医薬品等製造販売業者
日本医療情報学会
 医療情報学研究の利益相反 (COI) に関する指針 The Guidelines Concerning Conflict of Interest in Medical Information Research 一般社団法人日本医療情報学会 はじめに一般社団法人日本医療情報学会 ( 以下 日本医療情報学会という ) は 医療情報学に関する研究 教育 技術向上 その他社会応用の推進のために 会員相互の交流を図り
医療情報学研究の利益相反 (COI) に関する指針 The Guidelines Concerning Conflict of Interest in Medical Information Research 一般社団法人日本医療情報学会 はじめに一般社団法人日本医療情報学会 ( 以下 日本医療情報学会という ) は 医療情報学に関する研究 教育 技術向上 その他社会応用の推進のために 会員相互の交流を図り
する 研究実施施設の環境 ( プライバシーの保護状態 ) について記載する < 実施方法 > どのような手順で研究を実施するのかを具体的に記載する アンケート等を用いる場合は 事前にそれらに要する時間を測定し 調査による患者への負担の度合いがわかるように記載する 調査手順で担当が複数名いる場合には
 参考 : 様式 2( 記載例 ) ( 研究責任者 ) ( 本会倫理審査委員会 ) 西暦年月日 研究計画書 ( 第版 ) 公益社団法人富山県薬剤師会倫理審査委員会委員長様 計画者 ( 研究責任者 ) 所属 : 職名 : 氏名 : 印 1. 研究の名称 : 2. 研究の実施体制 研究責任者名所属職名役割及び責任 薬局管理薬剤師 研究分担者名 所属 職名 役割及び責任 薬局 薬剤師 病院 科 病院薬剤部
参考 : 様式 2( 記載例 ) ( 研究責任者 ) ( 本会倫理審査委員会 ) 西暦年月日 研究計画書 ( 第版 ) 公益社団法人富山県薬剤師会倫理審査委員会委員長様 計画者 ( 研究責任者 ) 所属 : 職名 : 氏名 : 印 1. 研究の名称 : 2. 研究の実施体制 研究責任者名所属職名役割及び責任 薬局管理薬剤師 研究分担者名 所属 職名 役割及び責任 薬局 薬剤師 病院 科 病院薬剤部
<4D F736F F D A835E838A F8B7982D18AC48DB85F20534F A68CEB8E9A E9A8F4390B38DCF2
 自治医科大学人を対象とした医学系研究に関するモニタリング及び監査の標準業務手順書 ver.1.0(2015 年 5 月 15 日 ) 1. 目的等 1) 目的 (1) 本手順書は 自治医科大学の教職員が 人を対象とする医学系研究に関する倫理指針 ( 平成 26 年文部科学省 厚生労働省告示第 3 号 ) 及び指針告示に伴う通知ならびにガイダンス ( 以下 指針 指針告示に伴う通知及びガイダンスを合わせて
自治医科大学人を対象とした医学系研究に関するモニタリング及び監査の標準業務手順書 ver.1.0(2015 年 5 月 15 日 ) 1. 目的等 1) 目的 (1) 本手順書は 自治医科大学の教職員が 人を対象とする医学系研究に関する倫理指針 ( 平成 26 年文部科学省 厚生労働省告示第 3 号 ) 及び指針告示に伴う通知ならびにガイダンス ( 以下 指針 指針告示に伴う通知及びガイダンスを合わせて
標準業務手順 目次
 浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
医師主導治験取扱要覧
 15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
同意説明文書(見本)
 同意説明文書 患者さんへ 膠原病の皮膚症状と血管障害の関連性について に関する研究の説明 これは臨床研究への参加についての説明文書です 本臨床研究についてわかりやすく説明しますので 内容を十分ご理解されたうえで 参加するかどうか患者さんご自身の意思でお決め下さい また ご不明な点などがございましたら遠慮なくご質問下さい 臨床研究代表者群馬大学大学院医学系研究科皮膚科学講師茂木精一郎 臨床研究責任医師群馬大学大学院医学系研究科皮膚科学講師茂木精一郎
同意説明文書 患者さんへ 膠原病の皮膚症状と血管障害の関連性について に関する研究の説明 これは臨床研究への参加についての説明文書です 本臨床研究についてわかりやすく説明しますので 内容を十分ご理解されたうえで 参加するかどうか患者さんご自身の意思でお決め下さい また ご不明な点などがございましたら遠慮なくご質問下さい 臨床研究代表者群馬大学大学院医学系研究科皮膚科学講師茂木精一郎 臨床研究責任医師群馬大学大学院医学系研究科皮膚科学講師茂木精一郎
手順書03
 杏林大学医学部倫理委員会 人を対象とする医学系研究に関する業務手順書 ➂ 研究計画書の作成等に関する手続等 1 はじめに本手順書は 杏林大学医学部倫理委員会規程に基づき 杏林大学医学部及び医学部付属病院の専任教職員が行う人を対象とした医学系研究について 医の倫理に関するヘルシンキ宣言の趣旨に添い 人を対象とする医学系研究に関する倫理指針及び その他関連通知に基づいて適正かつ円滑に行われるよう これらの研究等に係る必要な手順を定めるものである
杏林大学医学部倫理委員会 人を対象とする医学系研究に関する業務手順書 ➂ 研究計画書の作成等に関する手続等 1 はじめに本手順書は 杏林大学医学部倫理委員会規程に基づき 杏林大学医学部及び医学部付属病院の専任教職員が行う人を対象とした医学系研究について 医の倫理に関するヘルシンキ宣言の趣旨に添い 人を対象とする医学系研究に関する倫理指針及び その他関連通知に基づいて適正かつ円滑に行われるよう これらの研究等に係る必要な手順を定めるものである
(6) 企業等から一定額以上の物品を購入し 又は役務の提供を受ける行為 (7) 外部から利益相反の弊害が生ずるかのように見られることが懸念される行為 2 第 4 条に規定する COI 委員会は 教職員等以外の者による前項各号の行為を利益相反マネジメントの対象に加えることができる 第 2 章組織 (
 学校法人日本医科大学利益相反マネジメント規程 第 1 章総則 ( 目的 ) 第 1 条この規程は 学校法人日本医科大学 ( 以下 本法人 という ) が本法人利益相反マネジメントポリシー ( 平成 18 年 12 月 1 日制定 ) の精神に則り 教職員等の産学官連携活動等に伴って生ずる利益相反問題に適切に対処 ( マネジメント ) することにより 本法人及び教職員等の社会的信用及び名誉を保持することを目的とする
学校法人日本医科大学利益相反マネジメント規程 第 1 章総則 ( 目的 ) 第 1 条この規程は 学校法人日本医科大学 ( 以下 本法人 という ) が本法人利益相反マネジメントポリシー ( 平成 18 年 12 月 1 日制定 ) の精神に則り 教職員等の産学官連携活動等に伴って生ずる利益相反問題に適切に対処 ( マネジメント ) することにより 本法人及び教職員等の社会的信用及び名誉を保持することを目的とする
国立病院機構大阪医療センター受託研究取扱細則
 国立病院機構大阪医療センター 受託研究取扱細則 ( 主旨 ) 第 1 条国立病院機構大阪医療センターにおける受託研究の取扱いに関しては 国立病院機構大阪医療センター受託研究取扱規程 ( 以下 規程 という ) 及び他に定めるもののほか 規程第 1 条第 2 項に規定するこの細則の定めるところによる ( 総則 ) 第 2 条研究責任者は 原則として医長職相当以上とする ただし 副作用報告及び感染症報告を受託研究として実施する場合
国立病院機構大阪医療センター 受託研究取扱細則 ( 主旨 ) 第 1 条国立病院機構大阪医療センターにおける受託研究の取扱いに関しては 国立病院機構大阪医療センター受託研究取扱規程 ( 以下 規程 という ) 及び他に定めるもののほか 規程第 1 条第 2 項に規定するこの細則の定めるところによる ( 総則 ) 第 2 条研究責任者は 原則として医長職相当以上とする ただし 副作用報告及び感染症報告を受託研究として実施する場合
(3) 倫理学 法律学の専門家等 本法人に所属しない人文 社会科学の有識者若干名 (4) 一般の立場から意見を述べることができる者若干名 (5) 分子生物学 細胞生物学 遺伝学 臨床薬理学 病理学等の専門家若しくは遺伝子治療等臨床研究の対象となる疾患に係る臨床医として 日本医科大学長が推薦した者若干
 学校法人日本医科大学中央倫理委員会規程 ( 平成 28 年 1 月 1 日規程第 3 号 ) ( 目的 ) 第 1 条この規程は 医の倫理に関するヘルシンキ宣言の趣旨を尊重し 人を対象とする医学系研究に関する倫理指針 ヒトゲノム 遺伝子解析研究に関する倫理指針 遺伝子治療臨床研究に関する指針 ヒト受精胚の作成を行う生殖補助医療研究に関する倫理指針 等 国等が示した関係法令及び関係指針 ( 以下すべて併せて
学校法人日本医科大学中央倫理委員会規程 ( 平成 28 年 1 月 1 日規程第 3 号 ) ( 目的 ) 第 1 条この規程は 医の倫理に関するヘルシンキ宣言の趣旨を尊重し 人を対象とする医学系研究に関する倫理指針 ヒトゲノム 遺伝子解析研究に関する倫理指針 遺伝子治療臨床研究に関する指針 ヒト受精胚の作成を行う生殖補助医療研究に関する倫理指針 等 国等が示した関係法令及び関係指針 ( 以下すべて併せて
岩手医科大学医学部及び附属病院における人を対象とする医学系研究に係るモニタリング及び監査の実施に関する標準業務手順書 岩手医科大学医学部及び附属病院における 人を対象とする医学系研究に係る モニタリング及び監査の実施に関する標準業務手順書 岩手医科大学 第 1.0 版平成 29 年 10 月 1 日
 岩手医科大学医学部及び附属病院における 人を対象とする医学系研究に係る モニタリング及び監査の実施に関する標準業務手順書 岩手医科大学 第 1.0 版平成 29 年 10 月 1 日施行 目次 1. 目的...1 2. 研究機関の長の責務...1 3. 研究責任者の責務...1 4. モニタリング担当者の責務...1 5. 監査担当者の責務...2 6. 多施設共同研究におけるモニタリング及び監査の実施について...2
岩手医科大学医学部及び附属病院における 人を対象とする医学系研究に係る モニタリング及び監査の実施に関する標準業務手順書 岩手医科大学 第 1.0 版平成 29 年 10 月 1 日施行 目次 1. 目的...1 2. 研究機関の長の責務...1 3. 研究責任者の責務...1 4. モニタリング担当者の責務...1 5. 監査担当者の責務...2 6. 多施設共同研究におけるモニタリング及び監査の実施について...2
1. はじめに ステージティーエスワンこの文書は Stage Ⅲ 治癒切除胃癌症例における TS-1 術後補助化学療法の予後 予測因子および副作用発現の危険因子についての探索的研究 (JACCRO GC-07AR) という臨床研究について説明したものです この文書と私の説明のな かで わかりにくいと
 StageⅢ 治癒切除胃癌症例における TS-1 術後補助化学療法の 予後予測因子および副作用発現の危険因子についての 探索的研究 (JACCRO GC-07AR) についてのご説明 説明 同意文書 作成日 :2014 年 5 月 27 日 施設名 : 東京医科大学八王子医療センター 1. はじめに ステージティーエスワンこの文書は Stage Ⅲ 治癒切除胃癌症例における TS-1 術後補助化学療法の予後
StageⅢ 治癒切除胃癌症例における TS-1 術後補助化学療法の 予後予測因子および副作用発現の危険因子についての 探索的研究 (JACCRO GC-07AR) についてのご説明 説明 同意文書 作成日 :2014 年 5 月 27 日 施設名 : 東京医科大学八王子医療センター 1. はじめに ステージティーエスワンこの文書は Stage Ⅲ 治癒切除胃癌症例における TS-1 術後補助化学療法の予後
北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下
 北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下 モニタリング という ) 監査の受け入れ 並びに試験審査委員会( 治験審査委員会が兼ねる 以下 治験審査委員会
北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下 モニタリング という ) 監査の受け入れ 並びに試験審査委員会( 治験審査委員会が兼ねる 以下 治験審査委員会
<4D F736F F D208EA18CB182C98AD682B782E995578F808BC696B18EE88F878F E38E748EE593B1816A E7B8D732E646F637
 治験に関する標準業務手順書 ( 医師主導治験 ) 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医師主導治験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 (
治験に関する標準業務手順書 ( 医師主導治験 ) 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 趣旨 ) 第 1 条本手順書は 公益財団法人大原記念倉敷中央医療機構倉敷中央病院 ( 以下 本院 という ) において医師主導治験 ( 以下 治験 という ) を行う場合の取扱について必要な事項を定めるものである 2 本手順書は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 (
個人としての利益相反マネジメントの運用指針 平成 30 年 7 月 9 日 利益相反マネジメント委員会決定 個人としての利益相反を適切に管理するため 以下の運用指針を定め実施することとする 1. 利益相反マネジメントの対象事象国立大学法人岡山大学利益相反マネジメント規程第 3 条に規定される行為につ
 個人としての利益相反マネジメントの運用指針 平成 30 年 7 月 9 日 利益相反マネジメント委員会決定 個人としての利益相反を適切に管理するため 以下の運用指針を定め実施することとする 1. 利益相反マネジメントの対象事象国立大学法人岡山大学利益相反マネジメント規程第 3 条に規定される行為について 次に掲げるものを対象とする (1) 国立大学法人岡山大学職員兼業規程により承認を得て行う兼業 1
個人としての利益相反マネジメントの運用指針 平成 30 年 7 月 9 日 利益相反マネジメント委員会決定 個人としての利益相反を適切に管理するため 以下の運用指針を定め実施することとする 1. 利益相反マネジメントの対象事象国立大学法人岡山大学利益相反マネジメント規程第 3 条に規定される行為について 次に掲げるものを対象とする (1) 国立大学法人岡山大学職員兼業規程により承認を得て行う兼業 1
【押印あり】日本医学会宛
 別紙 再生医療等製品患者登録システムへの参加協力のお願い 患者登録システムの目的 患者登録システムは 再生医療等製品の市販後の使用状況や患者予後等のデータを収集し 迅速な安全対策や新たな製品開発等を通じて 医療の向上に役立てることを目的としています 患者登録システムは 製品毎に構築 運用されます この患者登録システムは 一般的には レジストリ と呼ばれることもあります 構築形態例 患者登録システムの対象
別紙 再生医療等製品患者登録システムへの参加協力のお願い 患者登録システムの目的 患者登録システムは 再生医療等製品の市販後の使用状況や患者予後等のデータを収集し 迅速な安全対策や新たな製品開発等を通じて 医療の向上に役立てることを目的としています 患者登録システムは 製品毎に構築 運用されます この患者登録システムは 一般的には レジストリ と呼ばれることもあります 構築形態例 患者登録システムの対象
愛知県立大学利益相反マネージメント規程
 愛知県立大学利益相反マネージメント規程 ( 目的 ) 第 1 条本規程は 愛知県立大学の教職員等 ( 客員共同研究員を含む ) が産学連携活動を含む社会貢献活動を行う際に生じるおそれのある利益相反 の弊害に適切に対応するため 利益相反関係の透明性を確保するとともに その適切な管理を行うことを目的とする ( 適用範囲 ) 第 2 条この規程は 本学の教職員 学部及び大学院の学生等に適用する ( 利益相反の定義
愛知県立大学利益相反マネージメント規程 ( 目的 ) 第 1 条本規程は 愛知県立大学の教職員等 ( 客員共同研究員を含む ) が産学連携活動を含む社会貢献活動を行う際に生じるおそれのある利益相反 の弊害に適切に対応するため 利益相反関係の透明性を確保するとともに その適切な管理を行うことを目的とする ( 適用範囲 ) 第 2 条この規程は 本学の教職員 学部及び大学院の学生等に適用する ( 利益相反の定義
埼玉医科大学倫理委員会
 全国大腸癌肝転移登録事業および登録情報に基づく研究 研究計画書 研究責任者 埼玉医科大学総合医療センター消化管 一般外科 石橋敬一郎 Version 1.0 2017 年 10 月 31 日 0 1. 研究の名称 全国大腸癌肝転移登録事業および登録情報に基づく研究 2. 研究組織について研究代表者 : 大腸癌研究会大腸癌肝転移データベース合同委員会委員長高橋慶一がん 感染症センター都立駒込病院外科副委員長山本雅一東京女子医科大学消化器外科研究事務局
全国大腸癌肝転移登録事業および登録情報に基づく研究 研究計画書 研究責任者 埼玉医科大学総合医療センター消化管 一般外科 石橋敬一郎 Version 1.0 2017 年 10 月 31 日 0 1. 研究の名称 全国大腸癌肝転移登録事業および登録情報に基づく研究 2. 研究組織について研究代表者 : 大腸癌研究会大腸癌肝転移データベース合同委員会委員長高橋慶一がん 感染症センター都立駒込病院外科副委員長山本雅一東京女子医科大学消化器外科研究事務局
eRequest - Frequently Asked Questions
 2018 年度 UCBJ 研究支援申請方法 1. 趣旨 ユーシービージャパン株式会社 ( 以下 UCBJ ) は 革新的な医薬品を開発し 患者の皆様の治療に貢献するとともに 医学 薬学領域の学術研究活動を支援いたします UCBJ は 2017 年から研究支援の公募を開始いたしました 患者の皆様にとって有益な治療につながる革新的で独創性のある研究に対して 研究支援金 ( 以下 支援金 ) の拠出をもって支援いたします
2018 年度 UCBJ 研究支援申請方法 1. 趣旨 ユーシービージャパン株式会社 ( 以下 UCBJ ) は 革新的な医薬品を開発し 患者の皆様の治療に貢献するとともに 医学 薬学領域の学術研究活動を支援いたします UCBJ は 2017 年から研究支援の公募を開始いたしました 患者の皆様にとって有益な治療につながる革新的で独創性のある研究に対して 研究支援金 ( 以下 支援金 ) の拠出をもって支援いたします
CROCO について
 CROCO について CROCO とは コース 正式名称 Clinical Research Online Professional Certification Program at Osaka University といい 大阪大学医学部附属病院が提供する 臨床研究に関する教育の e-learning サイトです 臨床研究を実施する研究者 専門職の方 倫理審査委員会の委員 事務局の方を対象に 臨床研究に必要な情報
CROCO について CROCO とは コース 正式名称 Clinical Research Online Professional Certification Program at Osaka University といい 大阪大学医学部附属病院が提供する 臨床研究に関する教育の e-learning サイトです 臨床研究を実施する研究者 専門職の方 倫理審査委員会の委員 事務局の方を対象に 臨床研究に必要な情報
I. 目的人間を対象とする医学研究の倫理的原則については すでに ヘルシンキ宣言 や 臨床研究の倫理指針 ( 厚生労働省告示第 255 号 2008 年度改訂 ) において述べられているが 被験者の人権 生命を守り 安全に実施することに格別な配慮が求められる 本学会は その活動において社会的責任と高
 日本アルコール アディクション医学会 臨床研究の利益相反に関する指針 日本アルコール アディクション医学会は臨床医学 基礎医学 社会医学その他関係分野の協力のもとに アルコール及び薬物 行動の依存 アディクションに関する研究の進歩並びに知識の普及 情報の提供等をはかり もって学術 文化の発展に寄与することを目的として活動している 事業内容は 学術集会を開催 ( 市民公開講座 日本医師会認定産業医研修会
日本アルコール アディクション医学会 臨床研究の利益相反に関する指針 日本アルコール アディクション医学会は臨床医学 基礎医学 社会医学その他関係分野の協力のもとに アルコール及び薬物 行動の依存 アディクションに関する研究の進歩並びに知識の普及 情報の提供等をはかり もって学術 文化の発展に寄与することを目的として活動している 事業内容は 学術集会を開催 ( 市民公開講座 日本医師会認定産業医研修会
9 中止基準 ( 研究対象者の中止 研究全体の中止について ) 10 研究対象者への研究実施後の医療提供に関する対応 通常の診療を超える医療行為 を伴う研究を実施した場合 研究実施後において 研究対象者が研究の結果より得られた利用可能な最善の予防 診断及び治療が受けられるように努めること 11 研究
 倫理審査書類 ( 研究計画書 ) チェックシート 研究計画書には 原則として以下の項目を含めてください 申請時 提出は不要です 2017.5.2 1 研究の名称 ( 標題 ) 2 研究の実施体制 ( 研究組織 ) 多施設共同研究の場合 共同研究機関の研究者名 役割も詳細に記載 3 研究の背景及び意義 研究を実施する意義 必要性に関して 文献等を用いて研究の 科学的合理性の根拠 と 本研究で得られる成果
倫理審査書類 ( 研究計画書 ) チェックシート 研究計画書には 原則として以下の項目を含めてください 申請時 提出は不要です 2017.5.2 1 研究の名称 ( 標題 ) 2 研究の実施体制 ( 研究組織 ) 多施設共同研究の場合 共同研究機関の研究者名 役割も詳細に記載 3 研究の背景及び意義 研究を実施する意義 必要性に関して 文献等を用いて研究の 科学的合理性の根拠 と 本研究で得られる成果
Microsoft Word - H _概要_.doc
 平成 25 年 5 月独立行政法人国立病院機構西新潟中央病院倫理審査委員会 ( 受託研究 ) 議事要旨 開催日時 開催場所 出席委員名は別紙のとおり 治験及び製造販売後臨床試験に関する調査審議事項 審議事項 治験等の実施に関する研究 継続 部分発作を有する小児てんかん患者を対象とした TRI476(Oxcarbazepine) 第 Ⅱ/Ⅲ 相試験被験薬 :TRI476(Oxcarbazepine)
平成 25 年 5 月独立行政法人国立病院機構西新潟中央病院倫理審査委員会 ( 受託研究 ) 議事要旨 開催日時 開催場所 出席委員名は別紙のとおり 治験及び製造販売後臨床試験に関する調査審議事項 審議事項 治験等の実施に関する研究 継続 部分発作を有する小児てんかん患者を対象とした TRI476(Oxcarbazepine) 第 Ⅱ/Ⅲ 相試験被験薬 :TRI476(Oxcarbazepine)
12_モニタリングの実施に関する手順書
 12_ モニタリングの実施に関する手順書 静岡県立大学大学院薬食生命科学総合学府薬学研究院薬食研究推進センター版数 :1.0 版作成年月日 :2014 月 8 月 1 日 ( 最終確定 :2015 年 1 月 14 日 ) 1. 目的と適用範囲 本手順書は 当該研究において モニターが モニタリングを適切に実施するための手順 その他必要な事項を定めるものである 2. 実施体制及び責務 2.1 研究責任者の責務研究責任者は
12_ モニタリングの実施に関する手順書 静岡県立大学大学院薬食生命科学総合学府薬学研究院薬食研究推進センター版数 :1.0 版作成年月日 :2014 月 8 月 1 日 ( 最終確定 :2015 年 1 月 14 日 ) 1. 目的と適用範囲 本手順書は 当該研究において モニターが モニタリングを適切に実施するための手順 その他必要な事項を定めるものである 2. 実施体制及び責務 2.1 研究責任者の責務研究責任者は
ICH-GCPとJ-GCPとの比較表
 参考資料 10 我が国の GCP と ICH-GCP の主な 1 治験の契約に関する規定 1-1 契約者に関する規定 1-2 実施医療機関の長との契約を規定したことに伴う規定 2 治験審査委員会 (IRB) に関する規定 2-1 IRB の設置に関する規定 2-2 IRB への審議依頼に関する規定 1/11 1. 治験の契約に関する規定 1-1. 契約者に関する規定 ICH-GCP 1.17( 用語の定義
参考資料 10 我が国の GCP と ICH-GCP の主な 1 治験の契約に関する規定 1-1 契約者に関する規定 1-2 実施医療機関の長との契約を規定したことに伴う規定 2 治験審査委員会 (IRB) に関する規定 2-1 IRB の設置に関する規定 2-2 IRB への審議依頼に関する規定 1/11 1. 治験の契約に関する規定 1-1. 契約者に関する規定 ICH-GCP 1.17( 用語の定義
群馬大学人を対象とする医学系研究倫理審査委員会 _ 情報公開 通知文書 人を対象とする医学系研究についての 情報公開文書 研究課題名 : がんサバイバーの出産の実際調査 はじめに近年 がん治療の進歩によりがん治療後に長期間生存できる いわゆる若年のがんサバイバーが増加しています これらのがんサバイバ
 人を対象とする医学系研究についての 情報公開文書 研究課題名 : がんサバイバーの出産の実際調査 はじめに近年 がん治療の進歩によりがん治療後に長期間生存できる いわゆる若年のがんサバイバーが増加しています これらのがんサバイバーにおいて生命の質の維持 向上は重要な問題で 中でもがん治療による妊孕性 ( 将来の妊娠の可能性 ) への影響は人生を左右する大きな問題と考えられますが 我が国においては がん患者の妊孕性温存治療に対する一定の指針がないのが現状です
人を対象とする医学系研究についての 情報公開文書 研究課題名 : がんサバイバーの出産の実際調査 はじめに近年 がん治療の進歩によりがん治療後に長期間生存できる いわゆる若年のがんサバイバーが増加しています これらのがんサバイバーにおいて生命の質の維持 向上は重要な問題で 中でもがん治療による妊孕性 ( 将来の妊娠の可能性 ) への影響は人生を左右する大きな問題と考えられますが 我が国においては がん患者の妊孕性温存治療に対する一定の指針がないのが現状です
山形県立中央病院治験審査委員会業務手順書
 山形県立中央病院治験審査委員会業務手順書 第 1 目的この手順書は山形県立中央病院医薬品等臨床試験受託研究取扱要綱 ( 以下 取扱要綱 という ) に基づいて山形県立中央病院治験審査委員会 ( 以下 本委員会 という ) の運用方法を定め それに基づく業務手順書を示すものである なお 製造販売後臨床試験においては 以下 治験 とあるのを 製造販売後臨床試験 と読み替えるものとする 第 2 本委員会の責務本委員会は全ての被験者の人権の保護
山形県立中央病院治験審査委員会業務手順書 第 1 目的この手順書は山形県立中央病院医薬品等臨床試験受託研究取扱要綱 ( 以下 取扱要綱 という ) に基づいて山形県立中央病院治験審査委員会 ( 以下 本委員会 という ) の運用方法を定め それに基づく業務手順書を示すものである なお 製造販売後臨床試験においては 以下 治験 とあるのを 製造販売後臨床試験 と読み替えるものとする 第 2 本委員会の責務本委員会は全ての被験者の人権の保護
<4D F736F F D20819B8CA48B868C7689E68F D A8CA9967B5F E646F63>
 研究計画書 本委員会ではゲノム解析研究を審査対象としている 臨床試験などは対象とならないため, 試験計画 ではない 以下, 計画書では 研究 を使用する 委員には, 医学の専門外の方もいます 研究計画は専門外の者にも理解しやすいように, 平易な表現で分かり易く記載する 研究課題名 : 1. 提供者を選ぶ方針 申請者氏名 ( 所属 職名 ): 合理的に選択していることが分かる具体的な方法を記載する 提供者が疾病や薬剤反応性異常を有する場合等にあっては,
研究計画書 本委員会ではゲノム解析研究を審査対象としている 臨床試験などは対象とならないため, 試験計画 ではない 以下, 計画書では 研究 を使用する 委員には, 医学の専門外の方もいます 研究計画は専門外の者にも理解しやすいように, 平易な表現で分かり易く記載する 研究課題名 : 1. 提供者を選ぶ方針 申請者氏名 ( 所属 職名 ): 合理的に選択していることが分かる具体的な方法を記載する 提供者が疾病や薬剤反応性異常を有する場合等にあっては,
Microsoft Word - H _概要_.doc
 平成 25 年 2 月独立行政法人国立病院機構西新潟中央病院倫理審査委員会 ( 受託研究 ) 議事要旨 開催日時 開催場所 出席委員名は別紙のとおり 治験及び製造販売後臨床試験に関する調査審議事項 審議事項 治験等の実施に関する研究 継続 ME2080 の Dravet 症候群患者を対象とした一般臨床試験 ( 第 Ⅲ 相 ) (Protocol No:STP-1) 被験薬 :ME2080(Stiripentol)
平成 25 年 2 月独立行政法人国立病院機構西新潟中央病院倫理審査委員会 ( 受託研究 ) 議事要旨 開催日時 開催場所 出席委員名は別紙のとおり 治験及び製造販売後臨床試験に関する調査審議事項 審議事項 治験等の実施に関する研究 継続 ME2080 の Dravet 症候群患者を対象とした一般臨床試験 ( 第 Ⅲ 相 ) (Protocol No:STP-1) 被験薬 :ME2080(Stiripentol)
( 委員以外の者の出席 ) 第 5 条委員長は 必要に応じ当該研究に必要な知見及び専門知識を持つ教員 産業医または看護師等を委員会の同意を得て出席させ 意見を聴くことができる ただし 上記の者の出席が困難な場合は 委員長又は委員長が指名した者が口頭等で意見を聴取し 委員会で報告することができる (
 一関工業高等専門学校における人を対象とする研究倫理審査委員会規則 ( 平成 28 年 6 月 9 日制定 ) ( 設置 ) 第 1 条一関工業高等専門学校 ( 以下 本校 という ) に, 人を対象とする研究における研究倫理について審査するため, 人を対象とする研究倫理審査委員会 ( 以下 委員会 という ) を置く ( 目的 ) 第 2 条委員会は, 本校における人を対象とする研究が, 独立行政法人国立高等専門学校機構における研究者等の行動規範
一関工業高等専門学校における人を対象とする研究倫理審査委員会規則 ( 平成 28 年 6 月 9 日制定 ) ( 設置 ) 第 1 条一関工業高等専門学校 ( 以下 本校 という ) に, 人を対象とする研究における研究倫理について審査するため, 人を対象とする研究倫理審査委員会 ( 以下 委員会 という ) を置く ( 目的 ) 第 2 条委員会は, 本校における人を対象とする研究が, 独立行政法人国立高等専門学校機構における研究者等の行動規範
ただし 対象となることを希望されないご連絡が 2016 年 5 月 31 日以降にな った場合には 研究に使用される可能性があることをご了承ください 研究期間 研究を行う期間は医学部長承認日より 2019 年 3 月 31 日までです 研究に用いる試料 情報の項目群馬大学医学部附属病院産科婦人科で行
 人を対象とする医学系研究についての 情報公開文書 研究課題名 : 予定帝王切開における脊椎麻酔による血圧変動と出生後の児への影響についての検討 はじめに現在 日本のほとんどの施設の標準的な麻酔方法は脊椎麻酔であり 当院でも帝王切開に対する標準的な麻酔方法を脊椎麻酔としています 脊椎麻酔では全身麻酔と比較し児への麻酔の影響が少ないとされていますが 麻酔導入後のお母さんの血圧低下を認めることが多く その際に赤ちゃんへどのような影響があるかは明らかにされていません
人を対象とする医学系研究についての 情報公開文書 研究課題名 : 予定帝王切開における脊椎麻酔による血圧変動と出生後の児への影響についての検討 はじめに現在 日本のほとんどの施設の標準的な麻酔方法は脊椎麻酔であり 当院でも帝王切開に対する標準的な麻酔方法を脊椎麻酔としています 脊椎麻酔では全身麻酔と比較し児への麻酔の影響が少ないとされていますが 麻酔導入後のお母さんの血圧低下を認めることが多く その際に赤ちゃんへどのような影響があるかは明らかにされていません
での教育的講演や市民に対して公開講座などを行う場合は, その社会的影 響が大きいことから演者には特段の指針遵守の義務がある Ⅲ. 利益相反開示の対象者 利益相反状態が生じる可能性がある以下の対象者に本指針が適用される 1 学術集会などにおける発表の筆頭演者 共同演者 2 学会誌, 刊行物における論文
 利益相反に関する指針 序文 日本渡航医学会は, 渡航医学に興味を持つ医師, 歯科医師, 看護師, 薬剤 師などが集う学際的学会であり, 渡航医学の進歩, 発展, 普及に貢献して いる 学術集会や学会誌などで発表される研究においては, 新規の医薬品や医療 機器, 技術を用いた臨床研究も多く, 産学連携による研究や開発が行われ る場合が少なくない このような産学連携による臨床研究は医学の進歩の ために必要ではあるが,
利益相反に関する指針 序文 日本渡航医学会は, 渡航医学に興味を持つ医師, 歯科医師, 看護師, 薬剤 師などが集う学際的学会であり, 渡航医学の進歩, 発展, 普及に貢献して いる 学術集会や学会誌などで発表される研究においては, 新規の医薬品や医療 機器, 技術を用いた臨床研究も多く, 産学連携による研究や開発が行われ る場合が少なくない このような産学連携による臨床研究は医学の進歩の ために必要ではあるが,
料 情報の提供に関する記録 を作成する方法 ( 作成する時期 記録の媒体 作成する研究者等の氏名 別に作成する書類による代用の有無等 ) 及び保管する方法 ( 場所 第 12 の1⑴の解説 5に規定する提供元の機関における義務 8 個人情報等の取扱い ( 匿名化する場合にはその方法等を含む ) 9
 北里研究所病院研究倫理委員会研究申請時確認シート ( 補助資料 ) 20170425 Ver.2.0 < 研究計画書の確認 > 記載項目 1 研究の名称 2 研究の実施体制 ( 研究機関の名称及び研究者等の氏名を含む ) 3 研究の目的及び意義 4 研究の方法及び期間 5 研究対象者の選定方針 6 研究の科学的合理性の根拠 7インフォームド コンセントを受ける手続等 ( インフォームド コンセントを受ける場合には
北里研究所病院研究倫理委員会研究申請時確認シート ( 補助資料 ) 20170425 Ver.2.0 < 研究計画書の確認 > 記載項目 1 研究の名称 2 研究の実施体制 ( 研究機関の名称及び研究者等の氏名を含む ) 3 研究の目的及び意義 4 研究の方法及び期間 5 研究対象者の選定方針 6 研究の科学的合理性の根拠 7インフォームド コンセントを受ける手続等 ( インフォームド コンセントを受ける場合には
治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会
 治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会 第 1 条 ( 目的 ) 1. 本手順書は 新光会治験審査委員会 ( 以下 委員会という ) において 医薬品及び医療機器 ( 以下 医薬品等という ) の治験の調査審議を実施するに当たり 薬事法 ( 昭和 35 年 8 月 10 日法律第 145 号 ) に基づく 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3
治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会 第 1 条 ( 目的 ) 1. 本手順書は 新光会治験審査委員会 ( 以下 委員会という ) において 医薬品及び医療機器 ( 以下 医薬品等という ) の治験の調査審議を実施するに当たり 薬事法 ( 昭和 35 年 8 月 10 日法律第 145 号 ) に基づく 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3
<4D F736F F D208BA6312D CF689768ED C93FA967B8AE189C888E389EF82C982A882AF82E A94BD82CC8AC7979D82C98AD682B782E98B4B92F62E646F63>
 公益社団法人日本眼科医会における利益相反の管理に関する規程 ( 目的 ) 第 条この規程は 厚生労働科学研究における利益相反 (Conflict Of Interest;COI) の管理に関する指針 ( 平成 0 年 3 月 3 日科発第 03300 号 厚生科学課長決定以下 利益相反管理指針 という ) に基づき 公益社団法人日本眼科医会 ( 以下 本会 という ) において研究等を実施する研究者の利益相反
公益社団法人日本眼科医会における利益相反の管理に関する規程 ( 目的 ) 第 条この規程は 厚生労働科学研究における利益相反 (Conflict Of Interest;COI) の管理に関する指針 ( 平成 0 年 3 月 3 日科発第 03300 号 厚生科学課長決定以下 利益相反管理指針 という ) に基づき 公益社団法人日本眼科医会 ( 以下 本会 という ) において研究等を実施する研究者の利益相反
(目的)
 計画書作成時留意点 計画書は医療関係者以外の方からも審査されます 医療関係者以外の方がみて理解でき るように配慮してください また 各項目は簡潔に記載してください 項目の幅は自由 に広げていただいて結構です 多くの研究は患者様に参加を求めるわけですから あくまで自由意思で参加する環境を 作ることが倫理性を評価するうえで大切になります 研究参加者に加わる危害をいかに 減らすか 最小限にしたときの研究参加者の受ける侵襲と研究から得られる社会的効果
計画書作成時留意点 計画書は医療関係者以外の方からも審査されます 医療関係者以外の方がみて理解でき るように配慮してください また 各項目は簡潔に記載してください 項目の幅は自由 に広げていただいて結構です 多くの研究は患者様に参加を求めるわけですから あくまで自由意思で参加する環境を 作ることが倫理性を評価するうえで大切になります 研究参加者に加わる危害をいかに 減らすか 最小限にしたときの研究参加者の受ける侵襲と研究から得られる社会的効果
日本医科大学付属第二病院治験標準業務手順書
 日本医科大学武蔵小杉病院 薬物治験審査委員会標準業務手順書 日本医科大学武蔵小杉病院 治験管理事務局 設定 :1998.4.1 改訂 :2005.9.1 :2006.4.1 :2010.7.1 :2012.9.1 :2014.1.1 :2015.12.1 :2016.3.1 :2018.10.1-1 - 日本医科大学武蔵小杉病院薬物治験審査委員会標準業務手順書 目次第 1 章薬物治験審査委員会 3
日本医科大学武蔵小杉病院 薬物治験審査委員会標準業務手順書 日本医科大学武蔵小杉病院 治験管理事務局 設定 :1998.4.1 改訂 :2005.9.1 :2006.4.1 :2010.7.1 :2012.9.1 :2014.1.1 :2015.12.1 :2016.3.1 :2018.10.1-1 - 日本医科大学武蔵小杉病院薬物治験審査委員会標準業務手順書 目次第 1 章薬物治験審査委員会 3
本手順書で使用する用語の定義 用語電子的記録書面電子的記録利用システム実務担当者原データ治験関連文書サイボウズサイボウズメッセージ 定義人の知覚では認識できない, 電子式等の方法で記録され, コンピュータで処理される記録紙媒体による資料治験依頼者, 実施医療機関の長, 治験責任医師並びに治験審査委員
 ( 第 1 版 :2015 年 7 月 1 日 ) 本手順書で使用する用語の定義 用語電子的記録書面電子的記録利用システム実務担当者原データ治験関連文書サイボウズサイボウズメッセージ 定義人の知覚では認識できない, 電子式等の方法で記録され, コンピュータで処理される記録紙媒体による資料治験依頼者, 実施医療機関の長, 治験責任医師並びに治験審査委員会の間での電子的記録の作成, 交付, 受領及び保存に用いるシステム規定や文書等で責任者の行うべき業務の権限を与えられ,
( 第 1 版 :2015 年 7 月 1 日 ) 本手順書で使用する用語の定義 用語電子的記録書面電子的記録利用システム実務担当者原データ治験関連文書サイボウズサイボウズメッセージ 定義人の知覚では認識できない, 電子式等の方法で記録され, コンピュータで処理される記録紙媒体による資料治験依頼者, 実施医療機関の長, 治験責任医師並びに治験審査委員会の間での電子的記録の作成, 交付, 受領及び保存に用いるシステム規定や文書等で責任者の行うべき業務の権限を与えられ,
前項に規定する事項のうち当該被験薬の治験薬概要書から予測できないもの に改め 同項を同条第三項とし 同条第一項の次に次の一項を加える 2治験依頼者は 被験薬について法第八十条の二第六項に規定する事項を知ったときは その発現症例一覧等を当該被験薬ごとに 当該被験薬について初めて治験の計画を届け出た日等
 厚生労働省令第二十四号薬事法(昭和三十五年法律第百四十五号)第十四条第三項(同条第九項及び同法第十九条の二第五項において準用する場合を含む ) 第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む ) 第八十条の二第一項 第四項及び第五項並びに第八十二条の規定に基づき 医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十年二月二十九日厚生労働大臣舛添要一医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令医薬品の臨床試験の実施の基準に関する省令(平成九年厚生省令第二十八号)の一部を次のように改正する
厚生労働省令第二十四号薬事法(昭和三十五年法律第百四十五号)第十四条第三項(同条第九項及び同法第十九条の二第五項において準用する場合を含む ) 第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む ) 第八十条の二第一項 第四項及び第五項並びに第八十二条の規定に基づき 医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十年二月二十九日厚生労働大臣舛添要一医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令医薬品の臨床試験の実施の基準に関する省令(平成九年厚生省令第二十八号)の一部を次のように改正する
目次 第 1 章治験審査委員会... 3 ( 目的と適用範囲 )... 3 ( 治験審査委員会の責務 )... 3 ( 治験審査委員会の設置及び構成 )... 3 ( 治験審査委員会の業務 )... 4 ( 治験審査委員会の運営 )... 6 第 2 章治験審査委員会事務局... 8 ( 治験審査委
 治験審査委員会標準業務手順書 < 医師主導治験 > 横浜労災病院 目次 第 1 章治験審査委員会... 3 ( 目的と適用範囲 )... 3 ( 治験審査委員会の責務 )... 3 ( 治験審査委員会の設置及び構成 )... 3 ( 治験審査委員会の業務 )... 4 ( 治験審査委員会の運営 )... 6 第 2 章治験審査委員会事務局... 8 ( 治験審査委員会事務局の設置と業務 )... 8
治験審査委員会標準業務手順書 < 医師主導治験 > 横浜労災病院 目次 第 1 章治験審査委員会... 3 ( 目的と適用範囲 )... 3 ( 治験審査委員会の責務 )... 3 ( 治験審査委員会の設置及び構成 )... 3 ( 治験審査委員会の業務 )... 4 ( 治験審査委員会の運営 )... 6 第 2 章治験審査委員会事務局... 8 ( 治験審査委員会事務局の設置と業務 )... 8
目 次 1. はじめに 企業等からの資金提供状況の公表に関するガイドラインの策定にあたって 2. 企業等からの資金提供状況に関する公表の現状 3. 企業等からの資金提供状況の公表のガイドライン (1) ガイドラインの対象 (2) 公表内容 (3) 公表期間 公表時期 (4) 資金受入状況等の把握方法
 企業等からの資金提供状況の公表に関するガイドライン 平成 26 年 6 月 ( 平成 26 年 9 月改定 ) ( 平成 27 年 6 月改定 ) ( 平成 28 年 6 月改定 ) 国立大学附属病院長会議 目 次 1. はじめに 企業等からの資金提供状況の公表に関するガイドラインの策定にあたって 2. 企業等からの資金提供状況に関する公表の現状 3. 企業等からの資金提供状況の公表のガイドライン
企業等からの資金提供状況の公表に関するガイドライン 平成 26 年 6 月 ( 平成 26 年 9 月改定 ) ( 平成 27 年 6 月改定 ) ( 平成 28 年 6 月改定 ) 国立大学附属病院長会議 目 次 1. はじめに 企業等からの資金提供状況の公表に関するガイドラインの策定にあたって 2. 企業等からの資金提供状況に関する公表の現状 3. 企業等からの資金提供状況の公表のガイドライン
Microsoft PowerPoint - 運用 [互換モード]
![Microsoft PowerPoint - 運用 [互換モード] Microsoft PowerPoint - 運用 [互換モード]](/thumbs/91/105850431.jpg) 押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
個人情報保護方針の例
 個人情報の取扱いについて シミックヘルスケア株式会社個人情報保護管理責任者 シミックヘルスケア株式会社 ( 以下 当社 といいます ) は お客様 お取引先様 従業員の方々の個人情報について 個人情報保護方針 ( プライバシー ポリシー ) に従い適正な管理を行うとともに 個人情報の保護に努めます 具体的には 以下の内容に従って個人情報の取り扱いを行います 1. 個人情報取扱事業者の名称シミックヘルスケア株式会社
個人情報の取扱いについて シミックヘルスケア株式会社個人情報保護管理責任者 シミックヘルスケア株式会社 ( 以下 当社 といいます ) は お客様 お取引先様 従業員の方々の個人情報について 個人情報保護方針 ( プライバシー ポリシー ) に従い適正な管理を行うとともに 個人情報の保護に努めます 具体的には 以下の内容に従って個人情報の取り扱いを行います 1. 個人情報取扱事業者の名称シミックヘルスケア株式会社
JCROA自主ガイドライン第4版案 GCP監査WG改訂案及び意見
 受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
宮城県立がんセンター受託研究業務手順書
 平成 26 年 4 月 1 日一部改正使用成績調査 特定使用成績調査編 本編は 薬事法第 14 条の 4 及び第 14 条の 6 に基づく医薬品及び医療機器の再審査 再評価申請の際に提出すべき資料の収集のために行われる製造販売後調査 ( 使用成績調査及び特定使用成績調査 )( 以下 使用成績調査等 ) に適用するものとする 本編は 薬事法第 14 条の 4 第 4 項 薬事法第 14 条の 6 第
平成 26 年 4 月 1 日一部改正使用成績調査 特定使用成績調査編 本編は 薬事法第 14 条の 4 及び第 14 条の 6 に基づく医薬品及び医療機器の再審査 再評価申請の際に提出すべき資料の収集のために行われる製造販売後調査 ( 使用成績調査及び特定使用成績調査 )( 以下 使用成績調査等 ) に適用するものとする 本編は 薬事法第 14 条の 4 第 4 項 薬事法第 14 条の 6 第
倫理委員会審査手順書
 昭和大学歯科病院 臨床研究申請手順書 昭和大学歯科病院 臨床試験支援室 2015 年 4 月 1 日 平成 27 年 4 月から 人を対象とする医学系研究に関する倫理指針 が施行され 臨床研究を行う場合 被験者を保護し その尊厳及び人権を尊重しつつ 一層の適正な推進を図ることが求められております 昭和大学歯科病院臨床試験審査委員会においても改正された指針に適合した運用を行いますので 下記の申請手順を確認し
昭和大学歯科病院 臨床研究申請手順書 昭和大学歯科病院 臨床試験支援室 2015 年 4 月 1 日 平成 27 年 4 月から 人を対象とする医学系研究に関する倫理指針 が施行され 臨床研究を行う場合 被験者を保護し その尊厳及び人権を尊重しつつ 一層の適正な推進を図ることが求められております 昭和大学歯科病院臨床試験審査委員会においても改正された指針に適合した運用を行いますので 下記の申請手順を確認し
治 験 実 施 標 準 業 務 手 順 書
 治験審査委員会標準業務手順書 < 企業治験 > 横浜労災病院 目 次 第 1 章治験審査委員会 2 目的と適用範囲 2 治験審査委員会の責務 2 治験審査委員会の設置及び構成 2 治験審査委員会の業務 3 治験審査委員会の運営 5 第 2 章治験審査委員会事務局 6 治験審査委員会事務局の設置と業務 6 第 3 章記録の保存と公開 7 記録の保存責任者 7 記録の保存期間 7 記録の公開 8 1 第
治験審査委員会標準業務手順書 < 企業治験 > 横浜労災病院 目 次 第 1 章治験審査委員会 2 目的と適用範囲 2 治験審査委員会の責務 2 治験審査委員会の設置及び構成 2 治験審査委員会の業務 3 治験審査委員会の運営 5 第 2 章治験審査委員会事務局 6 治験審査委員会事務局の設置と業務 6 第 3 章記録の保存と公開 7 記録の保存責任者 7 記録の保存期間 7 記録の公開 8 1 第
委員会記載 資料番号
 研究実施計画書記載要項 (2016 年 4 月 1 日改訂 ) 各項目について 該当する青字記載の事項に留意の上 計画書を作成し てください 下線部は記載不足が多い箇所ですので 該当する場合 記 載時に特にご留意ください 1. 課題名 : 2. 研究の意義 ( 背景 ) と目的 : 今まで何がわかっていて何がわかっていないのか 何を明らかにしようとするのか それによって何が得られるのか 3. 研究の方法
研究実施計画書記載要項 (2016 年 4 月 1 日改訂 ) 各項目について 該当する青字記載の事項に留意の上 計画書を作成し てください 下線部は記載不足が多い箇所ですので 該当する場合 記 載時に特にご留意ください 1. 課題名 : 2. 研究の意義 ( 背景 ) と目的 : 今まで何がわかっていて何がわかっていないのか 何を明らかにしようとするのか それによって何が得られるのか 3. 研究の方法
( 委員会の業務 ) 第 4 条委員会は その責務の遂行のために以下の最新資料を病院長から入手する なお あらかじめ 自ら治験を実施する者 委員会及び病院長の合意が得られている場合においては GCP 省令第 26 条の6 第 2 項に関する通知に限り 自ら治験を実施する者から入手することができる ま
 秋田大学医学部附属病院医師主導治験における治験審査委員会規程 第 1 章医師主導治験審査委員会 ( 目的と適用範囲 ) 第 1 条本規程は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 医薬品の臨床試験の実施の基準に関する省令( 平成 9 年 3 月 27 日厚生省令第 28 号 )( 以下 GCP 省令 という ) 並びにGCP 省令に関連する通知書等に基づいて
秋田大学医学部附属病院医師主導治験における治験審査委員会規程 第 1 章医師主導治験審査委員会 ( 目的と適用範囲 ) 第 1 条本規程は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 医薬品の臨床試験の実施の基準に関する省令( 平成 9 年 3 月 27 日厚生省令第 28 号 )( 以下 GCP 省令 という ) 並びにGCP 省令に関連する通知書等に基づいて
臨床研究に関する研修会1
 臨床研究に関する研修会 Ⅱ 長崎大学病院臨床研究センター 平成 27 年 9 月 24 日 倫理委員会申請時の注意点 臨床研究センター 副センター長福島千鶴 e-learning の受講 研究を申請する研究者及び 研究分担者は 申請前に必ず e-learning を受講して下さい CITI JAPAN プロジェクト ( 医学研究者標準コース ) 所属関係なし 研究責任者は研究分担者の受講状況を確認の上
臨床研究に関する研修会 Ⅱ 長崎大学病院臨床研究センター 平成 27 年 9 月 24 日 倫理委員会申請時の注意点 臨床研究センター 副センター長福島千鶴 e-learning の受講 研究を申請する研究者及び 研究分担者は 申請前に必ず e-learning を受講して下さい CITI JAPAN プロジェクト ( 医学研究者標準コース ) 所属関係なし 研究責任者は研究分担者の受講状況を確認の上
役職員が権利者又は発明者である知的財産権の保有をいう 第 2 章利益相反マネージメントの体制第 1 節利益相反マネージメント委員会 ( 設置 ) 第 3 条研究所に 利益相反マネージメント委員会 ( 以下 利益相反委員会 という ) を置く ( 任務 ) 第 4 条利益相反委員会は 次に掲げる事項に
 国立研究開発法人産業技術総合研究所利益相反マネージメント実施規程 制定平成 17 年 10 月 1 日 17 規程第 68 号 最終改正平成 29 年 3 月 30 日 28 規程第 84 号一部改正 目次第 1 章総則 ( 第 1 条 第 2 条 ) 第 2 章利益相反マネージメントの体制第 1 節利益相反マネージメント委員会 ( 第 3 条 - 第 8 条 ) 第 2 節利益相反マネージメント
国立研究開発法人産業技術総合研究所利益相反マネージメント実施規程 制定平成 17 年 10 月 1 日 17 規程第 68 号 最終改正平成 29 年 3 月 30 日 28 規程第 84 号一部改正 目次第 1 章総則 ( 第 1 条 第 2 条 ) 第 2 章利益相反マネージメントの体制第 1 節利益相反マネージメント委員会 ( 第 3 条 - 第 8 条 ) 第 2 節利益相反マネージメント
Microsoft Word - 案1-1 臨床研究法COI通知
 医政研発 0302 第 号 平成 30 年 3 月 2 日 都道府県 各保健所設置市 特別区 衛生主管部 ( 局 ) 長殿 厚生労働省医政局研究開発振興課長 ( 公印省略 ) 臨床研究法における臨床研究の利益相反管理について 今般 臨床研究法施行規則 ( 平成 30 年厚生労働省令第 7 号 以下 規則 という ) が平成 30 年 2 月 28 日付けで公布され 臨床研究法 ( 平成 29 年法律第
医政研発 0302 第 号 平成 30 年 3 月 2 日 都道府県 各保健所設置市 特別区 衛生主管部 ( 局 ) 長殿 厚生労働省医政局研究開発振興課長 ( 公印省略 ) 臨床研究法における臨床研究の利益相反管理について 今般 臨床研究法施行規則 ( 平成 30 年厚生労働省令第 7 号 以下 規則 という ) が平成 30 年 2 月 28 日付けで公布され 臨床研究法 ( 平成 29 年法律第
<4D F736F F D208CC2906C8FEE95F182CC8EE688B582C982C282A282C E646F6378>
 個人情報の取扱いについて 株式会社ヘルスクリック個人情報保護管理責任者 株式会社ヘルスクリック ( 以下 当社 といいます ) は お客様 お取引先様 従業員の方々の個人情報について 個人情報保護方針 ( プライバシー ポリシー ) に従い適正な管理を行うとともに 個人情報の保護に努めます 具体的には 以下の内容に従って個人情報の取り扱いを行います 1. 個人情報取扱事業者の名称株式会社ヘルスクリック
個人情報の取扱いについて 株式会社ヘルスクリック個人情報保護管理責任者 株式会社ヘルスクリック ( 以下 当社 といいます ) は お客様 お取引先様 従業員の方々の個人情報について 個人情報保護方針 ( プライバシー ポリシー ) に従い適正な管理を行うとともに 個人情報の保護に努めます 具体的には 以下の内容に従って個人情報の取り扱いを行います 1. 個人情報取扱事業者の名称株式会社ヘルスクリック
利益相反(Conflict of Interest : COI)に関するQ&A (案)
 一般社団法人日本体外循環技術医学会 利益相反 (Conflict of Interest : COI) に関する Q & A 一般社団法人日本体外循環技術医学会 ( 本法人 ) 会員の多くは 所属施設で臨床研究を実施し それによって得られた成果を本法人の学術集会などで発表されます 研究の実施と発表という2つのステップそれぞれの利益相反 (COI) に該当する項目について 所属施設だけでなく 本法人にもその内容を開示することが求められています
一般社団法人日本体外循環技術医学会 利益相反 (Conflict of Interest : COI) に関する Q & A 一般社団法人日本体外循環技術医学会 ( 本法人 ) 会員の多くは 所属施設で臨床研究を実施し それによって得られた成果を本法人の学術集会などで発表されます 研究の実施と発表という2つのステップそれぞれの利益相反 (COI) に該当する項目について 所属施設だけでなく 本法人にもその内容を開示することが求められています
文書管理番号
 プライバシーマーク付与適格性審査実施規程 1. 一般 1.1 適用範囲この規程は プライバシーマーク付与の適格性に関する審査 ( 以下 付与適格性審査 という ) を行うプライバシーマーク指定審査機関 ( 以下 審査機関 という ) が その審査業務を遂行する際に遵守すべき事項を定める 1.2 用語この基準で用いる用語は 特段の定めがない限り プライバシーマーク制度基本綱領 プライバシーマーク指定審査機関指定基準
プライバシーマーク付与適格性審査実施規程 1. 一般 1.1 適用範囲この規程は プライバシーマーク付与の適格性に関する審査 ( 以下 付与適格性審査 という ) を行うプライバシーマーク指定審査機関 ( 以下 審査機関 という ) が その審査業務を遂行する際に遵守すべき事項を定める 1.2 用語この基準で用いる用語は 特段の定めがない限り プライバシーマーク制度基本綱領 プライバシーマーク指定審査機関指定基準
< F2D8E9197BF A836F815B2E6A7464>
 ( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
資料1:「生命倫理に関する研究機関における検討について」(赤林先生資料)
 資料 1 命倫理に関する研究機関における検討について 東京 学医学部医療倫理学分野 林朗 次 医学系研究における法令 指針等 機関の の役割 倫理審査委員会の役割 倫理審査委員会の構成 研究実施にあたっての検討の流れ 医学系研究における法令 指針等 医学系研究に関する法律 医薬品医療機器等法 (2015 年改訂 ) 治験 再 医療等安全性確保法 (2013 年 ) 再 医療研究 医学系研究に関する基本的な指針
資料 1 命倫理に関する研究機関における検討について 東京 学医学部医療倫理学分野 林朗 次 医学系研究における法令 指針等 機関の の役割 倫理審査委員会の役割 倫理審査委員会の構成 研究実施にあたっての検討の流れ 医学系研究における法令 指針等 医学系研究に関する法律 医薬品医療機器等法 (2015 年改訂 ) 治験 再 医療等安全性確保法 (2013 年 ) 再 医療研究 医学系研究に関する基本的な指針
( 様式 1-1) 日本専門医機構認定形成外科専門医資格更新申請書 20 年月日フリガナ 氏 名 生年月日年月日 所属施設 ( 病院 医院 ) 名 勤務先住所 連絡先 ( 電話 : - - ) ( FAX : - - ) アドレス 1: アドレス 2: 専門医登録番号 - 医籍登録番号
 形成外科領域専門医更新様式等一覧 様式 1-1 日本専門医機構認定形成外科専門医資格更新申請書 1-2 単位集計表 様式 2 勤務実態の自己申告書 様式 3 形成外科診療実績記録 ( 過去 5 年間 ) 様式 4 手術症例一覧表 (4-1~4-5) 様式 5 症例一覧表 (5-1~5-5) 様式 6-1 専門医共通講習受講実績記録 6-2 専門医共通講習受講証明書類貼付台紙 様式 7 形成外科領域講習受講実績記録
形成外科領域専門医更新様式等一覧 様式 1-1 日本専門医機構認定形成外科専門医資格更新申請書 1-2 単位集計表 様式 2 勤務実態の自己申告書 様式 3 形成外科診療実績記録 ( 過去 5 年間 ) 様式 4 手術症例一覧表 (4-1~4-5) 様式 5 症例一覧表 (5-1~5-5) 様式 6-1 専門医共通講習受講実績記録 6-2 専門医共通講習受講証明書類貼付台紙 様式 7 形成外科領域講習受講実績記録
医薬品医療機器総合機構における専門協議等の実施に関する達 新旧対照表 改正後 1.~3.( 略 ) 1.~3.( 略 ) 現行 4. 専門委員が申請資料作成等関与者等である場合の取扱い (1)~(4) ( 略 ) 4. 専門委員が申請資料作成等関与者等である場合の取扱い (1) ~(4) ( 略 )
 資料 4-2 厚生労働省薬事分科会審議参加規程等の見直しに伴う医薬品医療機器総合機構における専門協議等の実施に関する達の改正等について 1. 趣旨 PMDA においては 医薬品 医療機器等の承認審査等の業務の実施に際し 臨床業務等に従事する外部専門家から意見を伺う専門協議等を実施している 専門協議等における利益相反に関する取扱いについては 医薬品医療機器総合機構における専門協議等の実施に関する達 (
資料 4-2 厚生労働省薬事分科会審議参加規程等の見直しに伴う医薬品医療機器総合機構における専門協議等の実施に関する達の改正等について 1. 趣旨 PMDA においては 医薬品 医療機器等の承認審査等の業務の実施に際し 臨床業務等に従事する外部専門家から意見を伺う専門協議等を実施している 専門協議等における利益相反に関する取扱いについては 医薬品医療機器総合機構における専門協議等の実施に関する達 (
臨床研究に参加される研究対象者の方へ 皮膚症状を呈する膠原病における炎症性サイトカインの病態への関与について に関する研究の説明 これは臨床研究への参加についての説明文書です 本臨床研究についてわかりやすく説明しますので 内容を十分ご理解されたうえで 参加するかどうか患者さんご自身の意思でお決め下さ
 臨床研究に参加される研究対象者の方へ 皮膚症状を呈する膠原病における炎症性サイトカインの病態への関与について に関する研究の説明 これは臨床研究への参加についての説明文書です 本臨床研究についてわかりやすく説明しますので 内容を十分ご理解されたうえで 参加するかどうか患者さんご自身の意思でお決め下さい また ご不明な点などがございましたら遠慮なくご質問下さい 臨床研究代表者群馬大学大学院医学系研究科皮膚科学茂木精一郎臨床研究責任医師群馬大学大学院医学系研究科皮膚科学茂木精一郎
臨床研究に参加される研究対象者の方へ 皮膚症状を呈する膠原病における炎症性サイトカインの病態への関与について に関する研究の説明 これは臨床研究への参加についての説明文書です 本臨床研究についてわかりやすく説明しますので 内容を十分ご理解されたうえで 参加するかどうか患者さんご自身の意思でお決め下さい また ご不明な点などがございましたら遠慮なくご質問下さい 臨床研究代表者群馬大学大学院医学系研究科皮膚科学茂木精一郎臨床研究責任医師群馬大学大学院医学系研究科皮膚科学茂木精一郎
大学病院治験受託手順書
 千葉大学医学部附属病院治験審査委員会運営手順書 第 1 条目的本手順書は 千葉大学医学部附属病院各種委員会規程の定めるところにより 千葉大学医学部附属病院治験審査委員会 ( 以下 委員会 という ) の運営方法を定め 医薬品等の治験 製造販売後調査および臨床試験等に関わる業務手順を示すものである 第 2 条委員会の責務 1 本委員会は 千葉大学医学部附属病院 ( 以下 本院 という ) において 治験及び製造販売後臨床試験
千葉大学医学部附属病院治験審査委員会運営手順書 第 1 条目的本手順書は 千葉大学医学部附属病院各種委員会規程の定めるところにより 千葉大学医学部附属病院治験審査委員会 ( 以下 委員会 という ) の運営方法を定め 医薬品等の治験 製造販売後調査および臨床試験等に関わる業務手順を示すものである 第 2 条委員会の責務 1 本委員会は 千葉大学医学部附属病院 ( 以下 本院 という ) において 治験及び製造販売後臨床試験
Ⅲ 第 43 期監査報告書等 監査報告書 私たち監事は 平成 27 年 9 月 1 日から平成 28 年 8 月 31 日までの第 43 期事業年度にお ける理事の職務の執行を監査いたしました その方法及び結果につき以下のとおり報告い たします 1. 監査の方法及びその内容私たち監事は 理事及び使用
 監査報告書 私たち監事は 平成 27 年 9 月 1 日から平成 28 年 8 月 31 日までの第 43 期事業年度にお ける理事の職務の執行を監査いたしました その方法及び結果につき以下のとおり報告い たします 1. 監査の方法及びその内容私たち監事は 理事及び使用人と意思疎通を図り 情報の収集及び監査の環境の整備に努めるとともに 理事会その他重要な会議に出席し 理事及び使用人等からその職務の執行状況について報告を受け
監査報告書 私たち監事は 平成 27 年 9 月 1 日から平成 28 年 8 月 31 日までの第 43 期事業年度にお ける理事の職務の執行を監査いたしました その方法及び結果につき以下のとおり報告い たします 1. 監査の方法及びその内容私たち監事は 理事及び使用人と意思疎通を図り 情報の収集及び監査の環境の整備に努めるとともに 理事会その他重要な会議に出席し 理事及び使用人等からその職務の執行状況について報告を受け
( 様式第 6) 病院の管理及び運営に関する諸記録の閲覧方法に関する書類 病院の管理及び運営に関する諸記録の閲覧方法 計画 現状の別 1. 計画 2. 現状 閲 覧 責 任 者 氏 名 閲 覧 担 当 者 氏 名 閲覧の求めに応じる場所 閲覧の手続の概要 ( 注 ) 既に医療法施行規則第 9 条の
 ( 様式第 6) 病院の管理及び運営に関する諸記録の閲覧方法に関する書類 病院の管理及び運営に関する諸記録の閲覧方法 計画 現状の別 1. 計画 2. 現状 閲 覧 責 任 者 氏 名 閲 覧 担 当 者 氏 名 閲覧の求めに応じる場所 閲覧の手続の概要 ( 注 ) 既に医療法施行規則第 9 条の 20 第 5 号の規定に合致する方法により記録を閲覧させている病院は現状について その他の病院は計画について記載することとし
( 様式第 6) 病院の管理及び運営に関する諸記録の閲覧方法に関する書類 病院の管理及び運営に関する諸記録の閲覧方法 計画 現状の別 1. 計画 2. 現状 閲 覧 責 任 者 氏 名 閲 覧 担 当 者 氏 名 閲覧の求めに応じる場所 閲覧の手続の概要 ( 注 ) 既に医療法施行規則第 9 条の 20 第 5 号の規定に合致する方法により記録を閲覧させている病院は現状について その他の病院は計画について記載することとし
中医協総 医薬品及び医療機器の費用対効果評価に関する取扱いについて 1 既収載品に係る費用対効果評価の手続き (1) 対象品目の指定中央社会保険医療協議会の定める以下の選定基準に基づき 費用対効果評価専門部会において指定 公表されたものとする 次の全ての要件を満たす品
 中医協総 - 5 2 8. 2. 1 0 医薬品及び医療機器の費用対効果評価に関する取扱いについて 1 既収載品に係る費用対効果評価の手続き (1) 対象品目の指定中央社会保険医療協議会の定める以下の選定基準に基づき 費用対効果評価専門部会において指定 公表されたものとする 次の全ての要件を満たす品目を対象とする なお 2においてイのⅰ イのⅱ ロのⅰ 及びロのⅱは それぞれ1 品目が該当するものとし
中医協総 - 5 2 8. 2. 1 0 医薬品及び医療機器の費用対効果評価に関する取扱いについて 1 既収載品に係る費用対効果評価の手続き (1) 対象品目の指定中央社会保険医療協議会の定める以下の選定基準に基づき 費用対効果評価専門部会において指定 公表されたものとする 次の全ての要件を満たす品目を対象とする なお 2においてイのⅰ イのⅱ ロのⅰ 及びロのⅱは それぞれ1 品目が該当するものとし
untitled
 1 2 重要ポイント 臨床試験研究費 ( 治験薬管理費を含む ) は 試験デザイン 治験薬投与期間 検査項目数などの治験内容に基づき 各ポイントの合計により算出されます 以下について 事前に治験依頼者と協議し 契約書を締結する必要があります 各金額 支払い時期 支払方法 被験者負担軽減費 保険外併用療養費支給対象外費の適用範囲等併せて 各部門や他科へ研究費の配分がある場合 追加請求が発生しないよう契約締結までに確認が必要です
1 2 重要ポイント 臨床試験研究費 ( 治験薬管理費を含む ) は 試験デザイン 治験薬投与期間 検査項目数などの治験内容に基づき 各ポイントの合計により算出されます 以下について 事前に治験依頼者と協議し 契約書を締結する必要があります 各金額 支払い時期 支払方法 被験者負担軽減費 保険外併用療養費支給対象外費の適用範囲等併せて 各部門や他科へ研究費の配分がある場合 追加請求が発生しないよう契約締結までに確認が必要です
製造販売後調査事務手続き等 について
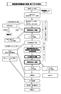 製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
国立仙台病院受託研究取扱規程
 独立行政法人国立病院機構仙台医療センター受託研究取扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構仙台医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程の定めるところによる 2 契約 経理及び書式等については 原則として独立行政法人国立病院機構
独立行政法人国立病院機構仙台医療センター受託研究取扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構仙台医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程の定めるところによる 2 契約 経理及び書式等については 原則として独立行政法人国立病院機構
<4D F736F F D E34208EA18CB18EE891B182AB977697CC C8E8DB782B591D682A688CB978A>
 Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
医学系研究の COI( 利益相反 ) に関する指針 一般社団法人日本脳神経外科学会 COI 委員会 I. 指針策定の目的医学系研究においては産学連携による研究 開発が行われる 日本では大学などの学術機関において国家予算による研究費は米国等に比して少なく 研究費の約 50% を民間企業に依存している
 医学系研究の COI( 利益相反 ) に関する指針 一般社団法人日本脳神経外科学会 COI 委員会 I. 指針策定の目的医学系研究においては産学連携による研究 開発が行われる 日本では大学などの学術機関において国家予算による研究費は米国等に比して少なく 研究費の約 50% を民間企業に依存している すなわち 本邦においては産学連携による医学系研究は医学の進歩のために不可欠できわめて重要な役割を担っている
医学系研究の COI( 利益相反 ) に関する指針 一般社団法人日本脳神経外科学会 COI 委員会 I. 指針策定の目的医学系研究においては産学連携による研究 開発が行われる 日本では大学などの学術機関において国家予算による研究費は米国等に比して少なく 研究費の約 50% を民間企業に依存している すなわち 本邦においては産学連携による医学系研究は医学の進歩のために不可欠できわめて重要な役割を担っている
長崎大学病院治験審査委員会内規 平成 21 年 4 月 1 日 病院内規第 3 号 ( 趣旨 ) 第 1 条この内規は, 長崎大学病院における医薬品の臨床試験の実施に関する内規 ( 以下 治験内規 という ) 第 4 条第 2 項, 長崎大学病院における医療機器の臨床試験の実施に関する内規 ( 以下
 長崎大学病院治験審査委員会内規 平成 21 年 4 月 1 日 病院内規第 3 号 ( 趣旨 ) 第 1 条この内規は, 長崎大学病院における医薬品の臨床試験の実施に関する内規 ( 以下 治験内規 という ) 第 4 条第 2 項, 長崎大学病院における医療機器の臨床試験の実施に関する内規 ( 以下 医療機器治験内規 という ) 第 4 条第 2 項及び長崎大学病院における再生医療等製品の臨床試験の実施に関する内規
長崎大学病院治験審査委員会内規 平成 21 年 4 月 1 日 病院内規第 3 号 ( 趣旨 ) 第 1 条この内規は, 長崎大学病院における医薬品の臨床試験の実施に関する内規 ( 以下 治験内規 という ) 第 4 条第 2 項, 長崎大学病院における医療機器の臨床試験の実施に関する内規 ( 以下 医療機器治験内規 という ) 第 4 条第 2 項及び長崎大学病院における再生医療等製品の臨床試験の実施に関する内規
1. 一般社団法人日本脳神経外科学会が行う学術総会および支部学術集会及びこれに関係したセミナーや講演会などにおける発表 2. 一般社団法人日本脳神経外科学会の機関誌 Neurologia medico-chirurgicaにおける論文発表をする者 (COI に関する自己申告書の提出が必要とされる基準
 医学系研究の COI( 利益相反 ) に関する細則 一般社団法人日本脳神経外科学会 COI 委員会 ( 目的 ) 第 1 条この細則は 一般社団法人日本脳神経外科学会が 医学系研究の COI( 利益相反 ) に関する指針 ( 以下 本指針 と略す ) を対象者に遵守させるにあたり 本指針の具体的な運用方法を示すことを目的とする (COI に関する自己申告 ) 第 2 条以下の対象者は過去 3 年間のCOIの有無を明らかにする義務がある
医学系研究の COI( 利益相反 ) に関する細則 一般社団法人日本脳神経外科学会 COI 委員会 ( 目的 ) 第 1 条この細則は 一般社団法人日本脳神経外科学会が 医学系研究の COI( 利益相反 ) に関する指針 ( 以下 本指針 と略す ) を対象者に遵守させるにあたり 本指針の具体的な運用方法を示すことを目的とする (COI に関する自己申告 ) 第 2 条以下の対象者は過去 3 年間のCOIの有無を明らかにする義務がある
14個人情報の取扱いに関する規程
 個人情報の取扱いに関する規程 第 1 条 ( 目的 ) 第 1 章総則 この規程は 東レ福祉会 ( 以下 本会 という ) における福祉事業に係わる個人情報の適法かつ適正な取扱いの確保に関する基本的事項を定めることにより 個人の権利 利益を保護することを目的とする 第 2 条 ( 定義 ) この規程における各用語の定義は 個人情報の保護に関する法律 ( 以下 個人情報保護法 という ) および個人情報保護委員会の個人情報保護に関するガイドラインによるものとする
個人情報の取扱いに関する規程 第 1 条 ( 目的 ) 第 1 章総則 この規程は 東レ福祉会 ( 以下 本会 という ) における福祉事業に係わる個人情報の適法かつ適正な取扱いの確保に関する基本的事項を定めることにより 個人の権利 利益を保護することを目的とする 第 2 条 ( 定義 ) この規程における各用語の定義は 個人情報の保護に関する法律 ( 以下 個人情報保護法 という ) および個人情報保護委員会の個人情報保護に関するガイドラインによるものとする
臨床試験(治験)実施の手続き
 製造販売後調査実施の手続き はじめに 本書は 昭和大学藤が丘病院における製造販売後調査実施の手続き方法等について記載したものです 本書内のは当院が提供する書類を示し は審査等に必要な書類を示しております 調査内容により提出書類 資料に変更が生じる場合があります 詳細は支援室にご確認ください 申請する書類および資料は 事前に E-mail に添付して支援室にお送りください 内容の確認をし ご連絡させて頂きます
製造販売後調査実施の手続き はじめに 本書は 昭和大学藤が丘病院における製造販売後調査実施の手続き方法等について記載したものです 本書内のは当院が提供する書類を示し は審査等に必要な書類を示しております 調査内容により提出書類 資料に変更が生じる場合があります 詳細は支援室にご確認ください 申請する書類および資料は 事前に E-mail に添付して支援室にお送りください 内容の確認をし ご連絡させて頂きます
<93648EA593498B4C985E82C98AD682B782E E838A F E315F C668DDA95AA292E786C7378>
 1 実施医療機関の長等の承諾 電磁的記録として扱う治験関連文書 ( 範囲 ) の承諾 SOP 等 施設の正式文書の記載 実施医療機関の長からの確認 実務担当者からの確認 電磁的記録の交付 受領手段の承諾 SOP 等 施設の正式文書の記載 実施医療機関の長からの確認 実務担当者からの確認 ( 版 :2013 年 9 月 1 日 ver2.0) 2 3 電磁的記録として扱う治験関連文書 電磁的記録の交付
1 実施医療機関の長等の承諾 電磁的記録として扱う治験関連文書 ( 範囲 ) の承諾 SOP 等 施設の正式文書の記載 実施医療機関の長からの確認 実務担当者からの確認 電磁的記録の交付 受領手段の承諾 SOP 等 施設の正式文書の記載 実施医療機関の長からの確認 実務担当者からの確認 ( 版 :2013 年 9 月 1 日 ver2.0) 2 3 電磁的記録として扱う治験関連文書 電磁的記録の交付
個人データの安全管理に係る基本方針
 個人情報保護宣言 ( プライバシーポリシー ) 一般社団法人日本投資顧問業協会 一般社団法人日本投資顧問業協会 ( 以下 協会 といいます ) は 個人情報の重要性を認識し これを保護することを法的 社会的責務と考えています 協会が事業活動を行うにあたり 個人情報を保護することを事業運営上の最重要事項の一つと位置づけ 個人情報の保護に関する法律 および 行政手続における特定の個人を識別するための番号の利用等に関する法律
個人情報保護宣言 ( プライバシーポリシー ) 一般社団法人日本投資顧問業協会 一般社団法人日本投資顧問業協会 ( 以下 協会 といいます ) は 個人情報の重要性を認識し これを保護することを法的 社会的責務と考えています 協会が事業活動を行うにあたり 個人情報を保護することを事業運営上の最重要事項の一つと位置づけ 個人情報の保護に関する法律 および 行政手続における特定の個人を識別するための番号の利用等に関する法律
Microsoft Word - *Xpert Flu検討 患者用説明書 修正.docx
 患者さんへ 自主臨床研究 全自動遺伝子解析装置におけるインフルエンザ試薬の性 能評価 についてのご説明 札幌医科大学附属病院 作成年月日 :2019 年 1 月 25 日 第 3 版 1 1. はじめに 臨床研究により新しい治療法を確立することは大学病院の使命であり 患者さんのご協力により成し遂げることができるものです 今回参加をお願いする臨床研究は 自主臨床研究 と呼ばれるもので 実際の診療に携わる医師が医学的必要性
患者さんへ 自主臨床研究 全自動遺伝子解析装置におけるインフルエンザ試薬の性 能評価 についてのご説明 札幌医科大学附属病院 作成年月日 :2019 年 1 月 25 日 第 3 版 1 1. はじめに 臨床研究により新しい治療法を確立することは大学病院の使命であり 患者さんのご協力により成し遂げることができるものです 今回参加をお願いする臨床研究は 自主臨床研究 と呼ばれるもので 実際の診療に携わる医師が医学的必要性
個人情報の取り扱いについて 公益財団法人岩手県予防医学協会 個人情報保護管理責任者常務理事 公益財団法人岩手県予防医学協会 ( 以下 協会 という ) は 健康診断等で取得した個人情報 を協会の個人情報保護基本規程に従って適正に管理し 以下のとおりお取り扱いさせていただき ますので 個人情報の提供
 個人情報の取り扱いについて 公益財団法人岩手県予防医学協会 個人情報保護管理責任者常務理事 公益財団法人岩手県予防医学協会 ( 以下 協会 という ) は 健康診断等で取得した個人情報 を協会の個人情報保護基本規程に従って適正に管理し 以下のとおりお取り扱いさせていただき ますので 個人情報の提供 利用について同意をお願い致します 1. 個人情報の利用目的 (1) 健康診断等 ( 各種健康診断 人間ドック
個人情報の取り扱いについて 公益財団法人岩手県予防医学協会 個人情報保護管理責任者常務理事 公益財団法人岩手県予防医学協会 ( 以下 協会 という ) は 健康診断等で取得した個人情報 を協会の個人情報保護基本規程に従って適正に管理し 以下のとおりお取り扱いさせていただき ますので 個人情報の提供 利用について同意をお願い致します 1. 個人情報の利用目的 (1) 健康診断等 ( 各種健康診断 人間ドック
実施医療機関治験審査委員会標準的業務手順書
 地方独立行政法人静岡市立静岡病院 治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 及び医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器
地方独立行政法人静岡市立静岡病院 治験審査委員会標準業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3 月 27 日 厚生省令第 28 号 )( 以下 GCP 省令 という ) 及び医療機器の臨床試験の実施の基準に関する省令 ( 平成 17 年 3 月 23 日 厚生労働省令第 36 号 )( 以下 医療機器
目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2
 免疫アレルギー疾患等実用化研究事業 ( 移植医療技術開発研究分野 ) 2019 年度 1 次公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 戦略推進部 難病研究課 2018 年 11 月 1 目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2 1. はじめに
免疫アレルギー疾患等実用化研究事業 ( 移植医療技術開発研究分野 ) 2019 年度 1 次公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 戦略推進部 難病研究課 2018 年 11 月 1 目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2 1. はじめに
個人情報保護に関する規定 ( 規定第 98 号 ) 第 1 章 総則 ( 目的 ) 第 1 条学校法人トヨタ学園および豊田工業大学 ( 以下, 総称して本学という ) は, 個人情報の保護に関する法律 ( 平成 15 年法律第 57 号, 以下, 法律という ) に定める個人情報取り扱い事業者 (
 個人情報保護に関する規定 ( 規定第 98 号 ) 第 1 章 総則 ( 目的 ) 第 1 条学校法人トヨタ学園および豊田工業大学 ( 以下, 総称して本学という ) は, 個人情報の保護に関する法律 ( 平成 15 年法律第 57 号, 以下, 法律という ) に定める個人情報取り扱い事業者 ( 以下, 取り扱い事業者という ) として, 本学が入手 保管 管理する個人情報 ( 以下, 個人情報という
個人情報保護に関する規定 ( 規定第 98 号 ) 第 1 章 総則 ( 目的 ) 第 1 条学校法人トヨタ学園および豊田工業大学 ( 以下, 総称して本学という ) は, 個人情報の保護に関する法律 ( 平成 15 年法律第 57 号, 以下, 法律という ) に定める個人情報取り扱い事業者 ( 以下, 取り扱い事業者という ) として, 本学が入手 保管 管理する個人情報 ( 以下, 個人情報という
恩賜第 42 回社会福祉法人財団済生会中央治験審査委員会 会議の記録の概要 開催日時 平成 28 年 1 月 13 日 ( 水 )15:30~17:17 開催場所 出席委員名 東京都港区三田 三田国際ビル 21 階 社会福祉法人 恩賜財団済生会本部事務局中会議室 豊島
 恩賜第 42 回社会福祉法人財団済生会中央治験審査委員会 会議の記録の概要 開催日時 平成 28 年 1 月 13 日 ( 水 )15:30~17:17 開催場所 出席委員名 108-0073 東京都港区三田 1-4-28 三田国際ビル 21 階 社会福祉法人 恩賜財団済生会本部事務局中会議室 豊島聰 ( 出席 ) 委員長林茂樹 ( 出席 ) 副委員長 市場みすゞ ( 出席 ) 漆原尚巳 ( 出席
恩賜第 42 回社会福祉法人財団済生会中央治験審査委員会 会議の記録の概要 開催日時 平成 28 年 1 月 13 日 ( 水 )15:30~17:17 開催場所 出席委員名 108-0073 東京都港区三田 1-4-28 三田国際ビル 21 階 社会福祉法人 恩賜財団済生会本部事務局中会議室 豊島聰 ( 出席 ) 委員長林茂樹 ( 出席 ) 副委員長 市場みすゞ ( 出席 ) 漆原尚巳 ( 出席
臨床研究に関する標準業務手順書
 臨床研究に関する標準業務手順書 2018/04/01 第 15 版 改定履歴 日付 版 改定理由 改定箇所 内容 2010/02/06 1 新規制定 2010/04/14 2 COI 関連手順の明確化 フローチャートに COI に関する手順の追記 2010/08/19 3 様式 必要書類の追加 COI 関連様式の追記 安全性に関する報告の手順および様式 ( 様式 11) の追加 委託研究に関する手順
臨床研究に関する標準業務手順書 2018/04/01 第 15 版 改定履歴 日付 版 改定理由 改定箇所 内容 2010/02/06 1 新規制定 2010/04/14 2 COI 関連手順の明確化 フローチャートに COI に関する手順の追記 2010/08/19 3 様式 必要書類の追加 COI 関連様式の追記 安全性に関する報告の手順および様式 ( 様式 11) の追加 委託研究に関する手順
<4D F736F F D20362D318EA18CB190528DB888CF88F589EF8BC696B18EE88F878F912E646F63>
 独立行政法人国立病院機構敦賀医療センターにおける企業主導治験に係る治験審査委員会業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は当院における 受託研究取扱規程 及び 企業主導治験に係る標準業務手順書 に基づいて 企業主導治験に係る標準業務手順書第 12 条第 1 項の規定により院内に設置された治験審査委員会の運営に関する手続き及び記録の保存方法等を定めるものである
独立行政法人国立病院機構敦賀医療センターにおける企業主導治験に係る治験審査委員会業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は当院における 受託研究取扱規程 及び 企業主導治験に係る標準業務手順書 に基づいて 企業主導治験に係る標準業務手順書第 12 条第 1 項の規定により院内に設置された治験審査委員会の運営に関する手続き及び記録の保存方法等を定めるものである
個人情報の保護に関する
 個人情報の保護に関する規則 第 1 章総則 ( 目的 ) 第 1 条早稲田大学 ( 以下 大学 という ) は 個人情報の保護が人格の尊厳に由来する基本的要請であることを深く認識し この規則によって 大学が保有する個人情報の取扱いに関する基本事項を定め もって個人情報の収集 管理および利用に関する大学の責務を明らかにするとともに 個人情報の主体である学生 教職員等に 自己に関する個人情報の開示ならびに訂正および削除の請求権を保障することによって
個人情報の保護に関する規則 第 1 章総則 ( 目的 ) 第 1 条早稲田大学 ( 以下 大学 という ) は 個人情報の保護が人格の尊厳に由来する基本的要請であることを深く認識し この規則によって 大学が保有する個人情報の取扱いに関する基本事項を定め もって個人情報の収集 管理および利用に関する大学の責務を明らかにするとともに 個人情報の主体である学生 教職員等に 自己に関する個人情報の開示ならびに訂正および削除の請求権を保障することによって
共同事業体協定書ひな形 ( 名称 ) 第 1 条この機関は 共同事業体 ( 以下 機関 という ) と称する ここでいう 機関 は 応募要領の参加資格に示した共同事業体のことであるが 協定書等において必ず 共同事業体 という名称を用いなければならない ということはない ( 目的 ) 第 2 条機関は
 共同事業体協定書ひな形 ( 名称 ) 第 1 条この機関は 共同事業体 ( 以下 機関 という ) と称する ここでいう 機関 は 応募要領の参加資格に示した共同事業体のことであるが 協定書等において必ず 共同事業体 という名称を用いなければならない ということはない ( 目的 ) 第 2 条機関は 知 の集積による産学連携推進事業のうち研究開発プラットフォーム運営等委託事業 ( 以下 委託事業 という
共同事業体協定書ひな形 ( 名称 ) 第 1 条この機関は 共同事業体 ( 以下 機関 という ) と称する ここでいう 機関 は 応募要領の参加資格に示した共同事業体のことであるが 協定書等において必ず 共同事業体 という名称を用いなければならない ということはない ( 目的 ) 第 2 条機関は 知 の集積による産学連携推進事業のうち研究開発プラットフォーム運営等委託事業 ( 以下 委託事業 という
京都府立医科大学附属病院
 治験費用の取扱に関する手順書 京都府立医科大学附属病院 第 1 版平成 21 年 11 月 16 日 第 2 版平成 23 年 3 月 16 日 第 3 版平成 25 年 2 月 1 日 1. 目的 本手順書は 京都府立医科大学附属病院治験実施取扱規定の定めるところにより 治験 費用の取り扱いに関する運用方法を定め それに基づく業務手順を示すものである 2. 治験に係る経費の範囲 (1) 治験経費
治験費用の取扱に関する手順書 京都府立医科大学附属病院 第 1 版平成 21 年 11 月 16 日 第 2 版平成 23 年 3 月 16 日 第 3 版平成 25 年 2 月 1 日 1. 目的 本手順書は 京都府立医科大学附属病院治験実施取扱規定の定めるところにより 治験 費用の取り扱いに関する運用方法を定め それに基づく業務手順を示すものである 2. 治験に係る経費の範囲 (1) 治験経費
2 改善命令 1への対応 TIB 審査会は ファーマコビジランス部門が委員長および事務局を務め 営業部門から独立した組織として運営しており 更に 2014 年 4 月より 審査体制の強化を目指し 法的観点から法務部員を メディカルサイエンスの立場からメディカルアフェアーズ部員 ( 医師 ) を委員に
 2015 年 7 月 10 日 武田薬品工業株式会社 厚生労働省発薬食 0612 第 7 号に係る改善命令に対する改善計画 弊社は 2014 年 3 月以降 医療関係者向けの広告資材に関する審査 管理体制を強化してまいりましたが 今般の改善命令を受け 再発防止のため 下記のとおり新たな改善策を実施いたします なお 改善策の実施状況につきましては 今後 定期的に厚生労働省医薬食品局監視指導 麻薬対策課までご報告いたしますとともに
2015 年 7 月 10 日 武田薬品工業株式会社 厚生労働省発薬食 0612 第 7 号に係る改善命令に対する改善計画 弊社は 2014 年 3 月以降 医療関係者向けの広告資材に関する審査 管理体制を強化してまいりましたが 今般の改善命令を受け 再発防止のため 下記のとおり新たな改善策を実施いたします なお 改善策の実施状況につきましては 今後 定期的に厚生労働省医薬食品局監視指導 麻薬対策課までご報告いたしますとともに
血液 尿を用いたライソゾーム病のスクリーニング検査法の検討 に関する説明書 一般財団法人脳神経疾患研究所先端医療研究センター 所属長衞藤義勝 この説明書は 血液 尿を用いたライソゾーム病のスクリーニング検査法の検討 の内容について説明したものです この研究についてご理解 ご賛同いただける場合は, 被
 血液 尿を用いたライソゾーム病のスクリーニング検査法の検討 に関する説明書 一般財団法人脳神経疾患研究所先端医療研究センター 所属長衞藤義勝 この説明書は 血液 尿を用いたライソゾーム病のスクリーニング検査法の検討 の内容について説明したものです この研究についてご理解 ご賛同いただける場合は, 被験者 ( 研究の対象者 ) として研究にご参加くださいますようお願い申し上げます この研究に参加されない場合でも,
血液 尿を用いたライソゾーム病のスクリーニング検査法の検討 に関する説明書 一般財団法人脳神経疾患研究所先端医療研究センター 所属長衞藤義勝 この説明書は 血液 尿を用いたライソゾーム病のスクリーニング検査法の検討 の内容について説明したものです この研究についてご理解 ご賛同いただける場合は, 被験者 ( 研究の対象者 ) として研究にご参加くださいますようお願い申し上げます この研究に参加されない場合でも,
再発小児 B 前駆細胞性急性リンパ性白血病におけるキメラ遺伝子の探索 ( この研究は 小児白血病リンパ腫研究グループ (JPLSG)ALL-B12 治療研究の付随研究として行われます ) 研究機関名及び研究責任者氏名 この研究が行われる研究機関と研究責任者は次に示す通りです 研究代表者眞田昌国立病院
 < 小児 B 前駆細胞性急性リンパ性白血病に対する 多施設共同臨床試験 (ALL-B12 研究 ) に参加された方へ > 研究課題 再発小児 B 前駆細胞性急性リンパ性白血病におけるキメラ遺伝子の探索 への保存検体の使用について 日本小児白血病リンパ腫研究グループ (JPLSG) が行っております小児 B 前駆細胞性急性リンパ性白血病に対する多施設共同臨床試験 (ALL-B12 研究 ) に参加された患者さんの中で検体提供への同意を文書で頂いている方につきましては
< 小児 B 前駆細胞性急性リンパ性白血病に対する 多施設共同臨床試験 (ALL-B12 研究 ) に参加された方へ > 研究課題 再発小児 B 前駆細胞性急性リンパ性白血病におけるキメラ遺伝子の探索 への保存検体の使用について 日本小児白血病リンパ腫研究グループ (JPLSG) が行っております小児 B 前駆細胞性急性リンパ性白血病に対する多施設共同臨床試験 (ALL-B12 研究 ) に参加された患者さんの中で検体提供への同意を文書で頂いている方につきましては
Ⅲ 治験に係る直接費用と間接費用 ( 但し 治験検討会議出席に係る旅費については 下記 Ⅳにて記載する ) 1. 算出方法 (1) 治験に係る経費設定( 表 1) に従い費用を算出する 2. 覚書の作成と請求方法 (1) 治験契約の際 病院長と治験依頼者は 治験契約書 ( 別記様式第 12 号第 3
 治験費用に関する手順書 ( 改訂第 5 版 ) Ⅰ 目的 本手順書は 当院で実施される治験費用の事務手続き方法を定めたものである Ⅱ 治験に係る経費の範囲 1. 治験に係る直接費用 間接費用 及び治験検討会議出席に係る指導料 ( 表 1) (1) 直接費用 1) 研究費 2) 治験検討会議出席に係る旅費 3) 治験審査委員会外部委員の講師指導 4) 治験に関し雇用したアルバイト賃金及び備品費 5)
治験費用に関する手順書 ( 改訂第 5 版 ) Ⅰ 目的 本手順書は 当院で実施される治験費用の事務手続き方法を定めたものである Ⅱ 治験に係る経費の範囲 1. 治験に係る直接費用 間接費用 及び治験検討会議出席に係る指導料 ( 表 1) (1) 直接費用 1) 研究費 2) 治験検討会議出席に係る旅費 3) 治験審査委員会外部委員の講師指導 4) 治験に関し雇用したアルバイト賃金及び備品費 5)
制定 : 平成 24 年 5 月 30 日平成 23 年度第 4 回理事会決議施行 : 平成 24 年 6 月 1 日 個人情報管理規程 ( 定款第 65 条第 2 項 ) 制定平成 24 年 5 月 30 日 ( 目的 ) 第 1 条この規程は 定款第 66 条第 2 項の規定に基づき 公益社団法
 制定 : 平成 24 年 5 月 30 日平成 23 年度第 4 回理事会決議施行 : 平成 24 年 6 月 1 日 個人情報管理規程 ( 定款第 65 条第 2 項 ) 制定平成 24 年 5 月 30 日 ( 目的 ) 第 1 条この規程は 定款第 66 条第 2 項の規定に基づき 公益社団法人岐阜県山林協会 ( 以下 この法人 という ) が定める 個人情報保護に関する基本方針 に従い 個人情報の適正な取扱いに関してこの法人の役職員が遵守すべき事項を定め
制定 : 平成 24 年 5 月 30 日平成 23 年度第 4 回理事会決議施行 : 平成 24 年 6 月 1 日 個人情報管理規程 ( 定款第 65 条第 2 項 ) 制定平成 24 年 5 月 30 日 ( 目的 ) 第 1 条この規程は 定款第 66 条第 2 項の規定に基づき 公益社団法人岐阜県山林協会 ( 以下 この法人 という ) が定める 個人情報保護に関する基本方針 に従い 個人情報の適正な取扱いに関してこの法人の役職員が遵守すべき事項を定め
3 治験実施計画書目的 当該治験について 治験実施計画書が手順書に従い適切に作成及び改訂されていることを確認する 次の事項を調べる (1) 治験実施計画書の記載項目 ( 再生医療等製品 GCP 省令第 7 条第 1 項に規定する項目 ) (2) 治験実施計画書の作成 改訂の手順と日付 (3) 治験計
 別添 10 再生医療等製品 GCP 省令チェックリスト Ⅰ 治験依頼者 ( 受託機関を含む ) 用 1 組織及び体制目的 治験の依頼及び管理に当たって 再生医療等製品 GCP 省令に沿った業務を行うために適切にして十分な人材を有し かつ 組織及び体制が確立していることを確認する 1 治験依頼者の組織 ( 当該被験機器の開発組織を含む ) と再生医療等製品 G CP 省令に係わる組織との関係 2 治験の依頼及び管理の業務に従事する者の氏名
別添 10 再生医療等製品 GCP 省令チェックリスト Ⅰ 治験依頼者 ( 受託機関を含む ) 用 1 組織及び体制目的 治験の依頼及び管理に当たって 再生医療等製品 GCP 省令に沿った業務を行うために適切にして十分な人材を有し かつ 組織及び体制が確立していることを確認する 1 治験依頼者の組織 ( 当該被験機器の開発組織を含む ) と再生医療等製品 G CP 省令に係わる組織との関係 2 治験の依頼及び管理の業務に従事する者の氏名
学校法人金沢工業大学個人情報の保護に関する規則
 学校法人金沢工業大学個人情報の保護に関する規則 ( 平成 22 年 12 月 1 日施行 ) 改正平成 27 年 12 月 1 日 第 1 章総則 ( 目的 ) 第 1 条この規則は 学校法人金沢工業大学 ( 以下 本法人 という ) における個人情報の取得 利用 保管 その他の取扱いについて必要な事項を定めることにより 個人情報の適切な保護に資することを目的とする ( 定義 ) 第 2 条この規則において
学校法人金沢工業大学個人情報の保護に関する規則 ( 平成 22 年 12 月 1 日施行 ) 改正平成 27 年 12 月 1 日 第 1 章総則 ( 目的 ) 第 1 条この規則は 学校法人金沢工業大学 ( 以下 本法人 という ) における個人情報の取得 利用 保管 その他の取扱いについて必要な事項を定めることにより 個人情報の適切な保護に資することを目的とする ( 定義 ) 第 2 条この規則において
4 研修について考慮する事項 1. 研修の対象者 a. 職種横断的な研修か 限定した職種への研修か b. 部署 部門を横断する研修か 部署及び部門別か c. 職種別の研修か 2. 研修内容とプログラム a. 研修の企画においては 対象者や研修内容に応じて開催時刻を考慮する b. 全員への周知が必要な
 新井病院 医療安全管理者の業務指針 新井病院医療安全管理者業務指針 1. はじめに医療機関の管理者は 自ら安全管理体制を確保するとともに 医療安全管理者を配置するにあたっては 必要な権限を委譲し また 必要な資源を付与して その活動を推進することで医療機関内の安全管理につとめなければならない 2. 医療安全管理者の位置づけ医療安全管理者とは 病院管理者 ( 病院長 ) の任命を受け 安全管理のために必要な権限の委譲と
新井病院 医療安全管理者の業務指針 新井病院医療安全管理者業務指針 1. はじめに医療機関の管理者は 自ら安全管理体制を確保するとともに 医療安全管理者を配置するにあたっては 必要な権限を委譲し また 必要な資源を付与して その活動を推進することで医療機関内の安全管理につとめなければならない 2. 医療安全管理者の位置づけ医療安全管理者とは 病院管理者 ( 病院長 ) の任命を受け 安全管理のために必要な権限の委譲と
<4D F736F F D208CC2906C8FEE95F182C98AD682B782E98AEE967B95FB906A93992E646F63>
 個人情報に関する基本情報 社会福祉法人東京雄心会 ( 以下 法人 という ) は 利用者等の個人情報を適切に取り扱うことは 介護サービスに携わるものの重大な責務と考えます 法人が保有する利用者等の個人情報に関し適性かつ適切な取り扱いに努力するとともに 広く社会からの信頼を得るために 自主的なルールおよび体制を確立し 個人情報に関連する法令その他関係法令及び厚生労働省のガイドラインを遵守し 個人情報の保護を図ることを目的とします
個人情報に関する基本情報 社会福祉法人東京雄心会 ( 以下 法人 という ) は 利用者等の個人情報を適切に取り扱うことは 介護サービスに携わるものの重大な責務と考えます 法人が保有する利用者等の個人情報に関し適性かつ適切な取り扱いに努力するとともに 広く社会からの信頼を得るために 自主的なルールおよび体制を確立し 個人情報に関連する法令その他関係法令及び厚生労働省のガイドラインを遵守し 個人情報の保護を図ることを目的とします
る として 平成 20 年 12 月に公表された 規制改革推進のための第 3 次答申 において 医療機器開発の円滑化の観点から 薬事法の適用範囲の明確化を図るためのガイドラインを作成すべきであると提言したところである 今般 薬事法の適用に関する判断の透明性 予見可能性の向上を図るため 臨床研究におい
 都道府県知事 各保健所設置市長殿 特別区長 薬食発 0331 第 7 号 平成 22 年 3 月 31 日 厚生労働省医薬食品局長 臨床研究において用いられる未承認医療機器の提供等に係る 薬事法の適用について 薬事法 ( 昭和 35 年法律第 145 号 ) は 医療機器について品質 有効性及び安全性の確保がなされた製品のみが流通するよう種々の規制を設けているが 薬事法第 14 条第 1 項の承認を受けていない医療機器
都道府県知事 各保健所設置市長殿 特別区長 薬食発 0331 第 7 号 平成 22 年 3 月 31 日 厚生労働省医薬食品局長 臨床研究において用いられる未承認医療機器の提供等に係る 薬事法の適用について 薬事法 ( 昭和 35 年法律第 145 号 ) は 医療機器について品質 有効性及び安全性の確保がなされた製品のみが流通するよう種々の規制を設けているが 薬事法第 14 条第 1 項の承認を受けていない医療機器
