肺炎マイコプラズマ (Mycoplasma pneumoniae)検査・診断マニュアル
|
|
|
- さやな ねぎたや
- 7 years ago
- Views:
Transcription
1 肺炎マイコプラズマ Mycoplasma pneumoniae 検査マニュアル 平成 23 年 9 月 1
2 目次 1. Mycoplasma pneumoniae によって起こる疾患 3 2. 検査に関する一般的な注意 4 1) 検査材料の採取 4 2) 検査材料の輸送 5 3) 検査の進め方 5 4) 検査結果による確定診断 3. 検査方法 6 8 1) 培養法 M. pneumoniae の分離法 2) 抗体検査法 8 18 3) 抗原検査法 21 4) 遺伝子検出法 PCR 法 LAMP 法 22 4. その他 27 参考情報1 薬剤耐性菌 27 参考情報2 M. pneumoniae の遺伝子型別 33 参考情報3 アルギニン添加 Hayflick 変法液体培地 参考情報4 届出基準 5. 文献 6. 執筆者 40 42 43 45 2
3 1. Mycoplasma pneumoniae によって起こる疾患 M. pneumoniae は Mollicutes 綱 M ycoplasma 属の細菌であり 分類学的に はグラム陽性菌に近い 細胞壁を全くもたず 増殖にはコレステロールや多 くの栄養素を要求する しかし 純培養が可能であり ゲノムサイズの小ささ 約 800kb から自己増殖が可能な最小クラスの細菌の一つとされている G+C 含量は 40% 形態は細長い形をしている M. pneumoniae によって起こる主な疾患は 気管支炎と肺炎である 原発性 異型肺炎の がマイコプラズマ肺炎であり 市中肺炎としての頻度 も高い 患者は若年齢層に多いが すべての年齢層で発生する 秋冬期に多い 傾向はあるが 年間を通して発生し 家族内や学校での集団発生がしばしば 見られる 潜伏期間は1 3週間程度である かつて日本では4年ごとにマ イコプラズマ肺炎の大流行が見られ オリンピック肺炎 と呼ばれたことも あったが 現在は 4 年の流行周期は見られなくなっている 症状は風邪に似 た感冒症状 発熱で 乾いた咳が長く続くのが特徴である 胸部 X 線検査で は すりガラス様の淡い陰影が認められる マイコプラズマ肺炎は他の細菌 性肺炎に比べれば症状が軽度なことが多い しかし様々な合併症をおこすこ ともあり まれに重篤な臨床経過をみることもある 合併症としては発疹 溶 血性貧血 関節炎 中耳炎 髄膜脳炎 末梢神経障害 心外膜炎 収縮性心膜炎 などがある 中枢神経系合併症を併発した場合は重症となることもある ま た 回復期以降にアレルギー性紫斑病や血小板減少性紫斑病なども見られる ことがある M. pneumoniae 感染は ギラン バレー症候群やスティーブン ス ジョンソン症候群を引き起こすことがあるとの報告もある 肺炎症状回 復後は M. pneumoniae 体内から比較的すみやかに消失すると考えられてい るが 気管内に数ヶ月間 また 低ガンマグロブリン血症の患者では数年間留 まった例も報告されている M. pneumoniae がヒトに肺炎を起こす仕組みは 完全には明らかにされて いないが M. pneumoniae が気道粘膜に接着して増殖し 細胞に傷害を与える ことと 菌体成分によって免疫細胞が刺激を受け 炎症反応を引き起こすこ とが主な原因だと考えられている 近年 M. pneumoniae が百日咳毒素と構造 が似た毒素を持つことが明らかになり Community Acquired Respiratory Distress Syndrome toxin (CARDS 毒素)と呼ばれている 研究が行われて 3
4 いるが どの程度病原性に関与しているかはよくわかっていない 4
5 2. 検査に関する一般的注意 M. pneumoniae は BSL2 の病原体であり 臨床検体および菌の取り扱い は P2 実験室の安全キャビネット内で行う 患者検体 汚染した器材 培養 液等は 使用後 オートクレーブあるいは消毒液で滅菌 消毒処理し しか るべき廃棄を行う 1 検査材料の採取 M. pneumoniae 感染症の診断に使われる臨床材料は 主として 咽頭ス ワブと血清 血液 である 鼻咽頭スワブからも咽頭スワブと同様に検 出を行うことができる 合併症の症状がある場合などは病変部の体液 胸水 髄液 細胞組織などを検査することもある 咽頭スワブ検体の採取 取り扱い法 採取時は以下の点に留意するよう 医師に依頼する 木軸以外の滅菌綿棒で咽頭の後壁を強くこすりとるようにする M. pneumoniae は咽頭の粘膜細胞に付着しているので 粘膜細胞がたく さん綿棒でこすりとられるようにする 咽頭スワブは M. pneumoniae 分離用培地に直ちに入れ 37 で培養 を開始するか 検査機関へ速やかに輸送する 医療機関で一時保管する 場合は 輸送培地に入れた状態で冷凍保管し できるだけ早く検査機関 に輸送する 一晩程度の保管であれは 輸送培地に入れた状態で室温に 置いてよい 4 の冷蔵庫には入れないほうがよい 遺伝子検出法のみを目的とし 菌の分離培養を行わない場合は スワ ブが多少乾燥してしまってもかまわないが できるだけ早く検査を実 施するようにする その他の検体の採取 取り扱い法 M. pneumoniae の分離培養を目的とする全て臨床検体は 下記の点に 留意する 遺伝子検出法のみで分離培養を目的としない場合でも M. pneumoniae の DNA の分解 消失をできるだけ防ぐため下記に準じた取 5
6 り扱いをする 血清診断用の血清は一般的な方法で取り扱う M. pneumoniae をはじめとするマイコプラズマ属の菌は 乾燥に弱 いので検体が乾かないようにする 低温にも弱いため 4 の冷蔵 庫には長時間保存しない 一晩程度保管する場合は室温でよい 長期間 安定的に保管ができるのは 80 での冷凍保存のみで 20 の保存では生菌数が徐々に低下する 凍結 融解の繰り返し も好ましくない 2 検査材料の輸送 臨床材料を輸送する場合は 感染症法に基づき 感染性物質の輸送 規則に関するガイダンス WHO 等による適正な梱包を行い ゆ うパックで輸送する 咽頭スワブならびに鼻咽頭スワブは輸送培地 に入れ 胸水 細胞組織 髄液はそのまま ドライアイスにて冷凍して 輸送する ドライアイスを用いることができない場合には 冷蔵輸送 よりも常温で速やかに輸送したほうがよい 肺炎マイコプラズマ疑いの臨床分離株を輸送する場合は 菌の増 殖が認められる液体培地や寒天培地を上述の通り適正に梱包し ゆ うパックで常温輸送する 輸送培地 輸送培地として 後述の培地 Hayflick 変法液体培地 を使用す るが 検体中の他の菌の増殖抑制を目的としてアンピシリンを 200μg/ml の濃度で添加する また 輸送用培地として BD 社の Universal Viral Transport for Viruses, Chlamydiae, Mycoplasmas and Ureaplasmas も利用できる この培地は滅菌済みのスワブ採取棒とセ ットになって個装されており 常温で保存が可能である 感染研にお ける使用経験では Hayflick 変法液体培地とのあいだに大きな性能の 違いはない 医療機関などでは輸送培地の調製 準備ができない場 合が多いので 検査機関から提供するようにする 3 検査の進め方 6
7 検査を行うにあたり 培養法と遺伝子検出法を同時に行う場合は 検体を分割し 一方を培養法 もう一方からは 遺伝子検出法用の鋳型 DNA 抽出を行う 以下に検体種類別の検査手順を示す 咽頭スワブ 鼻咽頭スワブ 培養法か遺伝子検出法 あるいはこの両方を試す スワブの入って いた輸送培地は 最初に 0.45μm のメンブランフィルターで濾過する と 他の菌の影響を少なくすることができる M. pneumoniae は 0.45μm のメンブランフィルターを通過する また 必要に応じ遠心 濃縮する 念のためフィルターを濾過した検体と濾過しない検体の両 方について検査を行う 菌量が少ない検体ではフィルター濾過が逆 効果なことがあるため 遺伝子検出法のみを目的とした乾燥スワブの場合には 送付された スワブに 500μl の生理食塩水を加え 綿球をよく洗った後 生理食塩 水を回収し ゲノム DNA を抽出する 血清 血液 抗体検査法を行う PA 法は必ず行い 他の抗体検査法は補助的に 行う PA 法にはセロディア-MYCO II 富士レビオ 株 などのキ ットが利用できる 胸水 髄液 細胞組織などの検体 培養法と遺伝子検出法の両方を行う 4 検査結果による確定診断 臨床的に肺炎症状を呈し 胸部 X 線像に特有の陰影がみられる症例 で 下記のいずれかの検査結果が得られた場合 マイコプラズマ肺炎 と確定診断される 1 培養法により M. pneumoniae が分離同定されたとき 2 抗体検査法の受身凝集反応 PA によって ペア血清で 4 倍 7
8 以上の抗体価上昇 単一血清では 320 倍以上の抗体価が見 られた場合 または 補体結合反応 CF によってペア血 清で 4 倍以上の抗体価上昇 単一血清では 64 倍以上の抗体 価がみられた場合 3 遺伝子検出法で M. pneumoniae の DNA が検出された場合 また M. pneumoniae に感染していても症状が軽く 肺炎には至らな い上気道炎症例もあるので 胸部 X 線像の陰影が無くても M. pneumoniae の存在 あるいは明らかな抗体上昇認めた場合は M. pneumoniae 感染によるものと診断できる 参考資料 4 には感染症発生動向調査における定点医療機関からの 届出基準を記載した 8
9 3 検査方法 1 培養法 M. pneumoniae の分離法 M. pneumoniae の分離培養による検出は もっとも確定的な実験室 診断法だが M. pneumoniae の培養検査は時間がかかるため 早期診断 法にはならない しかし M. pneumoniae の分離が期待できる臨床材料 については できるだけ培養法を実施すべきである ①基本培地の調製法 ブドウ糖添加 Hayflick 変法液体培地 PPLO 液体培地 1 リットルあたりの組成 マイコプラズマ基礎培地 PPLO ブロス ブドウ糖 21 g 5g (0.5%) フェノールレッド 20 mg (0.002%) 蒸留水 750 ml 上記を高圧蒸気滅菌し 約 50 以下に冷えたら 無菌的に以下の ものを加える ウマ血清 55 で 30 分間加熱済 25 % 新鮮酵母エキス 150 ml (15 %) 100 ml (10 %) ペニシリン G 100 万単位 2.5 % 酢酸タリウム溶液 10 ml PPLO Broth w/o CV, Difco , Becton Dickinson 毒性があるので 取り扱いに注意する ウマ血清 25 % 新鮮酵母エキスについては 後述の 培地の添加 物について を参照 酢酸タリウム溶液は 他の雑菌が増殖するのを 防ぐために加えるもので 添加は必須ではない ペニシリン G はア ンピシリン 終濃度 50μg/ml に置き換えることも可能 培地は凍結可能な密閉チューブに約 3 ml ずつ無菌的に分注し 20 以下で保存する 凍結状態では数年間安定 解凍後は よく撹 9
10 拌して使用する Hayflick 変法寒天培地 PPLO 寒天平板培地 1 リットルあたりの組成 PPLO 寒天培地 35 g 蒸留水 750 ml 上記を高圧蒸気滅菌し 約 50 以下に冷えたら 無菌的に以下の ものを加える ウマ血清 55 で 30 分間加熱済 25 % 新鮮酵母エキス 150 ml (15 %) 100 ml (10 %) ペニシリン G 100 万単位 PPLO Agar, Difco , Becton Dickinson 上記組成を混合後 シャーレに流して寒天平板を作製する 培養中 の培地の乾燥を防ぐため 培地層を 4-5mm の程度の厚さにする ピペ ット等を使用して等量の培地をシャーレに注ぐと培地の厚さが均一 になり 直径 9 cm のシャーレだと約 25ml 程度 実体顕微鏡での 観察が容易になる 寒天平板作製後はビニール袋に入れて 4 で保存 する 一般的な細菌用寒天は マイコプラズマ発育阻害成分を含む場 合があるので マイコプラズマ用の寒天平板の調製には通常用いな い ペニシリン G はアンピシリン 終濃度 50μg/ml に置き換える ことも可能 M. pneumoniae 用選択培地 メチレンブルー含有二層培地 臨床検体からの M. pneumoniae の分離には メチレンブルーを添加 した選択培地を用いる 上記の Hayflick 変法液体培地に 終濃度 0.001%のメチレンブルーを加えて調製する メチレンブルーはヒトの 口腔内に常在する M. pneumoniae 以外のマイコプラズマの増殖を抑制 するはたらきがある 栓のできる小試験管に PPLO 寒天培地 1 ml を 10
11 入れて固めた後 メチレンブルー含有培地を 2 ml を重層して二層培 地とする この培地では液層と寒天層の境界の酸化還元電位が M. pneumoniae の増殖に適し 分離率が向上するとされている 二層培地 の有効使用期間は 作製後 冷蔵保存で2週間程度である 図1 図1 二層培地 Hayflick 変法液体培地は ph 指示薬として添加したフェノールレッ ドによって赤色だが M. pneumoniae が増殖すると ph が低下し黄色に 変色する 選択培地用にメチレンブルーを添加すると Hayflick 変法 培地は茶色がかった色になる これに M. pneumoniae が増殖すると緑 黄色になる 図2 図2 メチレンブルーの有無による Hayflick 変法培地の色調変化の例 11
12 培地の添加物について 25 % 新鮮酵母エキス 研究室で継代された M. pneumoniae は 新鮮酵母エキスの代わりに 市販の酵母エキス粉末を使用しても増殖する しかし 臨床検体から の分離培養の場合 市販の酵母エキス粉末を使用した培地では 分離 率が低下する このため 新鮮酵母エキスを調製するのが望ましい 自 家調製が煩雑であれば 市販の新鮮酵母エキスを使用しても構わない 以下に調整法を記載する 必要な試薬 器具 滅菌済フラスコ 2リットル容量 1個 3リットルフラスコに 1.5 リットル蒸留水を入れ滅菌したもの 1個 ニッテンドライイースト 500 g 1缶 日本甜菜糖株式会社 Nippon Beet Sugar MFG. Co. Ltd 鍋 コンロ 3N NaOH 溶液 滅菌済遠心チューブ 8000 x g に耐えるもの 高速遠心機 8000 x g 回転可能な機種 保存用滅菌済容器 細胞培養用 25 cm2 フラスコや 50ml チューブ 等 調製法 鍋に湯を沸騰させ 1.5 リットル蒸留水入りフラスコを湯煎し 充 分に加熱する ニッテンドライイースト 500 g を 1.5 リットル蒸留水 に加える 数回に分けて加え フラスコを湯から持ち上げ撹拌する 加熱しながら約 20 分間 熱水抽出を行う この間 3 4 分毎にフラ スコを持ち上げ強く撹拌する フラスコごと水で急冷する これ以後の操作は 無菌的に行う 抽出液を滅菌済遠心チューブに分注し 4 にて xg で 20 分間遠心する 上清を 再度 新しい滅菌済遠心チューブに入れ 同 じ条件で遠心する その上清を滅菌済フラスコに集める NaOH 溶液 12
13 で ph を 7.6 に調整する 50ml 滅菌チューブに小分けし 20 で凍結保存する 解凍後はシリンジタイプの 0.45μm フィルターで濾過してから使用 する 液中の浮遊物によってフィルターが目詰まりをおこすことがあ るので その場合はフィルターを複数個使用する 濾過しにくい場合 は大きな孔径のフィルターや滅菌濾紙で前濾過してもよい 馬血清 Gibco 社などから市販されているウマ血清を 55 で 30 分間 加熱 処理してから使用する マイコプラズマは増殖にコレステロールを 要求する このため コレステロール供給源として 培地に動物血清を 添加する必要がある 一般にウマ血清がこの用途に用いられているが ウマ血清はロットによって M. pneumoniae の発育阻害因子が多く含 まれることがあるので これを不活化するために加熱処理をする ② 検体の培養と観察 ア 初代培養 咽頭拭い綿棒絞り液 0.2 ml を二層培地 または通常の液体培地 に 0.1 ml を PPLO 寒天平板培地に接種し 37 で培養する 二層培地および液体培地は通常のインキュベーターで培養する 炭酸ガスがあると培地の ph に影響し 色調変化の判断がしにくい ため 寒天平板培地は 5% 炭酸ガスインキュベータ 5% 炭酸ガスを含む 窒素内で培養すると増殖が良い 5% 炭酸ガスインキュベータ等がな い場合は 寒天表面の乾燥を防ぐためビニール袋に入れて 37 で好 気培養する ビニール袋内に 精製水でしめらせたペーパータオルを 2 3枚入れておくと乾燥を防ぐ効果がある 液体培地に M. pneumoniae が増殖すると液層が緑黄色に変化する メチレンブルーを添加しない液体培地では黄色に変色する 検体中の菌数が少なかったり 分離菌の性質によっては 増殖に 2 3 週間程度要することもある 変色した培地液体層の一部を後述する方法で 80 に凍結保存す 13
14 る 注 M. pneumoniae が増殖しても培地はほとんど濁らないが 細かい 粒子状の浮遊物や 沈殿状が見えることがある これは菌があつまっ てかたまりになっているものである マイクロコロニー 短期間 1 3 日間 で培地が変色したり 液層に濃い濁りが生じた場合は マイコプラズマ以外の咽頭内細菌の増殖が考えられる このような場 合 M. pneumoniae 増殖の判定は不可能となる 雑菌の増殖はかなりの 頻度 3 10 で起こる イ 寒天平板培地への移植とコロニー観察 培地の液層が変色しただけでは M. pneumoniae が増殖したのか明 らかではないので 変色した液層を PPLO 寒天平板培地に移植して コロニーを形成させてみる必要がある 変色した培地液層を滅菌生理食塩液または Hayflick 変法液体培地 で に段階希釈し 各希釈液 10 μl を PPLO 寒天平板シャーレ にスポット接種して培養する 1 枚のシャーレを 4 6 区画に分割し てスポットできる PPLO 寒天平板培地に接種した検体は 培養開始5日後頃から観察 を開始する マイコプラズマのコロニーは微小 0.1mm 程度 なので 観察には 倍率程度の実体顕微鏡が必要である 寒天平板を観 察し マイコプラズマ に特徴的な目玉焼き状 コロニーを探す 図 3 図3 マイコプラズマの目玉 焼き状コロニー マイコプラズマのコロニーが目玉焼き状になるのは コロニーの中 14
15 央部が寒天層に入り込んでいるためであり コロニーが小さいうちは 目玉焼き形状を呈さない M. pneumoniae の場合は 寒天平板培地表面 の状態にもよるが 他のマイコプラズマ種のコロニーよりも目玉焼き の形状が目立たないこともある ウ コロニー染色 形状の観察だけで マイコプラズマのコロニーであるか確信を持て ない場合は Dienes の染色液でコロニーを染色して観察する Dienes の染色液 メチレンブルー 2.5 g アズール 1.25 g II マルトース 10 g 炭酸ナトリウム 0.25 g 安息香酸 0.25 g 精製水 100 ml 上記染色液をコロニーの生じた寒天平板にかけ 数分後に観察する マイコプラズマのコロニーは 青色に染まる ヘモフィルス属以外の 細菌のコロニーは染まらない 染色したコロニーは 継代や純化に用 いない エ コロニーの純化 寒天平板上のコロニーを純化する必要がある場合は 先の細いピペ ット 注射針 滅菌済みつまようじなどでコロニーをひろう マイコプ ラズマのコロニーは寒天に入りこんでいるので寒天ごと切り出すよ うにして取る コロニーは 2 3ml の Hayflick 変法液体培地に接種して 培養する 菌が増殖したら培養液を 25 ゲージの注射針に数回通す さ らに 0.45μm のメンブランフィルターを通過させ 適当に段階希釈し た後 PPLO 寒天培地にまいてコロニーを形成させる そこから再び コロニーを拾い 純化されるまで同じ操作を繰り返す この方法は フィルタークローニング法と呼ばれている 15
16 ③ M. pneumoniae の同定法 培養法により検出されたマイコプラズマが M. pneumoniae であるか の確認は 以下のような同定法を用いる ア コロニーへの赤血球付着能試験 M. pneumoniae のコロニーには赤血球が付着する性質がある 咽頭 から分離される他のマイコプラズマ種のコロニーには この性質はな いので 分離菌が M. pneumoniae であると確認する一つの目安になる M. genitalium のコロニーも赤血球が付着する性質をもつが 咽頭か ら分離されることはまれである M. genitalium は非淋菌性尿道炎の原 因菌として おもに泌尿 生殖器から分離される 赤血球付着試験の方法 ヒツジ保存血を PBS で 100 倍に希釈する これをマイコプラズマ のコロニーが形成されているシャーレに 約7 ml 加え 37 で3 0分 1時間静置する 希釈血液を捨てた後 シャーレに残っている 血液を PBS で2 3回洗い流す 実体顕微鏡でコロニーに赤血球が 付着しているかを観察する 図4. 赤血球が付着した M.pneumoniae のコロニー 小さな点に 見えるのが赤血球 イ ブドウ糖代謝性 アルギニン非代謝性であることを確認する ブ ド ウ 糖 添 加 Hayflick 変 法 液 体 培 地 あ る い は ア ル ギ ニ ン 添 加 16
17 Hayflick 変法液体培地での増殖を調べる 参考情報3を参照 ウ 抗 M. pneumoniae 血 清 を 用 い た 代 謝 阻 害 試 験 Metabolic inhibition test などで確認する 血清検査法の項を参照 エ M. pneumoniae に対して特異的な PCR 法 17 で確認する 後述の PCR 法を使用する 遺伝子検査法の項を参照 ④ M. pneumoniae 菌株の保存法 液体培地のまま保存する場合 液体培地で培養したマイコプラズマは そのまま凍結保存用のチュ ーブにいれ 80 以下に保存する 保護剤を添加する際には グリセ ロール ジメチルスルホキシド(DMSO)などを添加して保存する 下に 示すような 2 倍保存液と 培養液を 1 : 1 に混合し 細胞凍結用のチュ ーブに分注して 80 フリーザーあるいは液体窒素中に保存する 長 期保存の際は 数年ごとに定期的な継代培養を行うことが望ましい 2 倍保存液 PPLO broth w/o CV 培養液作製時の 2 倍濃度にする グリセロール 10% 高圧蒸気滅菌後 室温保存可 凍結乾燥して保存する場合 凍結乾燥の際の保護剤としては 12 スクロース 10% 脱脂乳なども 推奨されている 凍結乾燥菌は 4 以下の保存が望ましい 菌株保存時の注意点 ア M. pneumoniae の液体培養では 菌は培地中に浮遊もしているが かなりの量が培養容器の内壁 特に底面 に付着している 継代 保 存するときには培養容器の内壁面の付着菌をピペットやスクレイパ ーなどでこすり取るようにする 培地に浮遊している菌のみ採取して 継代を繰り返すと 細胞接着能を失った変異体の割合が増えてくるこ 17
18 とがある 細胞接着能をもつ もとの性質を保持した菌株を保存維持 するために注意する イ 図5に示すように M. pneumoniae は増殖によって培地の ph が低 下しだすと生菌数が減少しやすい このため培地が黄色変化してから 時間が経過したものは保存に適さない そのような場合は 植え継い で再培養した方が良い 分離株ごとに増殖カーブは異なるため 培養 日数よりも培地色調変化を増殖と保存時期の目安とする 培地の黄 色変化後は 1 2 日以内に保存するようにする 図5 M. pneumoniae 増殖と培地 ph 変化の関連図 18
19 2 抗体検査法 マイコプラズマ肺炎の確定診断の多くは 抗体検査法によって行われて いる M. pneumoniae の抗体検査法として おもに以下の方法があげられ る 受身凝集反応 PA 補体結合反応 CF イムノカード IC ELISA 法 EIA 間接蛍光抗体法 IFA 寒冷凝集反応 代謝阻止抗体 MI この中で比較的広く用いられているのは 受身凝集反応 PA と 補体結合反応 CF である 簡便さから イムノカードも使われるよ うになってきている 抗体検査法は 患者の抗体価が上昇しているこ とが前提なので 早期診断にはなりにくい しかし IgM 抗体を検出す る方法なら ある程度の早期診断も期待できる 受身凝集反応 PA M. pneumoniae 抗原を粒子表面に結合させておき そこに血清を加 えたときの粒子の凝集を見ることで 血清中の抗マイコプラズマ抗体 の有無を判定する 粒子に赤血球を用いた古典的な方法は間接赤血球 凝集反応 (IHA) とよばれる 抗原の吸着を促進するためにタンニン酸 やホルマリン 塩化クロムなどで処理をした赤血球の表面に抗原を吸 着させて行う しかし 赤血球を用いた凝集反応では非特異的な凝集 が起こることがある このため 現在では凝集体としてラテックス粒 子 ゼラチン粒子などがよく用いられる 市販品として富士レビオ 株 からセロディア-MYCO II が出ている 色素で着色したゼラチ ン粒子を使用したキットであり 判定までの時間は 3 時間程度である 海外で市販されているキットでは IgM と IgG を同時に または別々 に検出する物もある 海外のキットについては文献 4 を参照 19
20 補体結合反応 CF 感作赤血球に補体が結合すると溶血が起こるが 抗原と抗体の結合 物が存在すると それに補体が結合して消費されるために溶血が起こ らなくなる CF 法では 抗原と抗体の結合物による補体の消費量を指 標として判定を行う 反応抗原は膜糖脂質とされ 血清中の IgG クラ スの抗体を測定する ペア血清で 4 倍以上の上昇を陽性とするが 単 一血清で判定するには 64 倍以上の抗体価が必要である 抗体価が上 昇するまで発症後 2 週間以上を要するため 本法での早期診断は困難 である 市販の試薬として 以下の試薬が入手可能である 肺炎マイコプラズマ CF試薬 生研 として CF 抗原 CF 抗血清 x 32 倍の陽性血清 ならびに 正常抗原 デンカ生研 イムノカード IC 迅 速 に 臨 床 検 査 を 行 う た め の カ ー ド 型 の 製 品 Meridian Diagnostics, Immuno Card Mycoplasma Test で 日本ではイムノカー ド マイコプラズマ抗体の名称で 株 ティーエフビーから販売され ている カード型のキットに患者血清や血漿を加え 抗 M. pneumonia 抗体の存在を酵素抗体法で検出する仕組みになっている 検体と試薬 を入れれば 5 分程度で結果が得られるため 臨床の現場でも簡単に検 査が行える利点がある IgM 抗体を検出するように作られており 発 病の初期にも診断が行えるとされている しかし 簡便な迅速キット であるため 検出感度や特異性にやや問題があるとの報告もある 文 献 正確さを期すにはペア血清の検査が望ましい 株式会社テイエフビー ELISA 法 ELISA 法は 高感度 特異的で汎用性があり 定量的な結果が得られ る利点もある マイコプラズマ肺炎診断の抗体検査に応用する場合は M. pneumoniae の菌体成分 粗精製又は精製菌体成分 を抗原とする 20
21 方法が用いられる 菌体の超音波破砕液などを未精製で抗原に用いる と患者以外の人の血清でもかなりの反応が起こり バックグランドが 高くなる この場合 抗 M. pneumoniae 抗血清用いてサンドイッチ ELISA を行えばバックグラウンドを低く抑えることができる 精製抗 原を使用する場合は P1 細胞接着タンパク質などがあげられる また 合成ペプチドや 遺伝子組換えによって生産した M. pneumoniae のタ ンパク質を抗原として使用することもできる 海外では ELISA 法に基づく診断キットも複数販売されている 文 献 4 参照 間接蛍光抗体法 IFA 固定した M. pneumoniae の抗原に 患者の血清を反応させて 血清 中に M. pneumoniae に対する抗体が存在するかを調べる 通常 培地 に沈めたカバーグラス上に M. pneumoniae を増殖させ メタノール 酢酸などで固定し 患者血清と反応させる 反応後カバーグラスを洗 浄し M. pneumoniae 抗原に結合してカバーガラス上に残っている抗 体を 蛍光標識した抗ヒト Ig 抗体で検出する 観察には蛍光顕微鏡を 用いる 操作がやや煩雑で 蛍光像の観察と判定にも習熟を要するが M. pneumoniae 抗体の存在を直接検出する有効な方法である 寒冷凝集反応 寒冷凝集反応とは 低温 4 で O 型 Rh(-) の赤血球が凝集する 反応で 赤血球の I 抗原に対する IgM 抗体によって起こる マイコプ ラズマ肺炎ではこの抗体の上昇が見られるため 寒冷凝集反応が診断 の指標となりうる 通常 マイコプラズマ肺炎発症後 1 2 週間で寒冷 凝集反応がみられるが 陽性になるのは マイコプラズマ肺炎の約 であるとされる 寒冷凝集反応は 他の細菌やウイルス感染症 自己免疫疾患 血液の疾患によっても見られ マイコプラズマ肺炎に 特異的ではない 現在はマイコプラズマ肺炎の検査法としてほとんど 使用されない 21
22 代謝阻止抗体 MI M. pneumoniae 感染患者の血清中には M. pneumoniae の増殖を阻止 す る 抗 体 MI 抗 体 が 産 生 さ れ て い る 患 者 の 血 清 に M. pneumoniae の増殖を阻害する活性が見られれば M. pneumoniae の感 染が疑われる 参考 抗原検査法 抗体検査法による早期診断には限界があるが もし M. pneumoniae の菌体成分を高感度 特異的に検出する抗原検査法があれば 有効な 早期診断が可能になると考えられる しかし M. pneumoniae の抗原検 査はこれまでいくつか方法が報告されているが 特異性と感度が十分 ではなく 有効な方法はいまだに普及していない 過去に海外で イム ノクロマト法にもとづいた M. pneumoniae 簡易抗原検査キットが実 用化されたが 日本では市販されず どの程度有用であったのかは不 明である 現状で利用が考えられる抗原検査法は 直接蛍光抗体法 DFA で 蛍光標識した抗 M. pneumoniae モノクローナル抗体で マ イコプラズマ肺炎患者の咽頭ぬぐい液中に存在する M. pneumoniae を免疫染色して顕微鏡観察する方法である 蛍光顕微鏡での観察や判 定に多少の習熟を要するが 早期診断法として有用であるとの報告も ある 5 マイコプラズマ肺炎の早期診断を意図するなら 現時点では遺伝子 検出検査法を使用するのが最も信頼性が高い 22
23 4 遺伝子検出検査法 現在 M. pneumoniae の遺伝子検出検査法としては ① PCR 法 か ② LAMP 法を用いるのが一般的である ① PCR 法 PCR 法は比較的簡便に行うことができ 検出感度も培養法より高い PCR による M. pneumoniae DNA の検出は 現在 マイコプラズマ肺炎の 早期診断法として最も有効な方法であると考えられる しかし PCR は しばしば擬陽性による誤判定も起こすので注意を要する PCR 法は すでに多くの方法が報告されているが M. pneumoniae の細 胞接着タンパク質 P1 の遺伝子 p1 遺伝子 の配列を検出ターゲットと したものが多い 臨床材料から直接検出を行う場合は 検出感度を上げ るため nested PCR が用いられる ここでは nested PCR による p1 遺伝子 検出法の例を示す PCR 法の実験操作 鋳型 DNA の調製 検体のからの DNA の調製は M. pneumoniae DNA の分解を防ぐため にも 採取後できるだけ速やかに行うのが好ましい 方法は 一般的な DNA 抽出操作を行えばよいが 次のような簡便な方法でもよい 1. 咽頭スワブや体液中から鋳型 DNA の調製 1 2 ml の咽頭拭い液や 体液 髄液 組織液など を卓上遠心機で 遠心し x g 10 分間 上清をのぞく 沈渣に 0.1 Triton-X100 を含む TE buffer 10mM Tris-HCl, 1mM EDTA, ph 8.0 を 50 μl 加え 懸濁する 95 で 5 分間加熱した後 鋳型 DNA として使用する さらに プロテイナーゼK を終濃度 1 µg/ml になるように加え 55 で 15 分間処理すると DNA の収率が上がる場合があるが プロテイナ ーゼKを使用した場合は フェノール抽出 エタノール沈殿でプロテイ ナーゼKを失活 除去する必要がある 咽頭スワブや体液からの DNA の抽出は QIAGEN 社の QIAamp DNA Mini Kit などのようなキットで も簡便に行うことができる 23
24 2. 細胞組織からの鋳型 DNA の抽出 患者の細胞組織などから PCR で M. pneumoniae の検出を試みること もある この場合の検体処理法も DNA を抽出するための方法であれ ばどのような方法を用いてもかまわないが QIAGEN 社などのキット 製品を使用すれば簡便に行うことができる PCR 反応 使用プライマー p1 遺伝子検出用プライマー 1st PCR 用プライマー ADH2F: 5 -GGC AGT GGC AGT CAA CAA ACC ACG TAT-3 ADH2R: 5 -GAA CTT AGC GCC AGC AAC TGC CAT-3 2nd PCR 用プライマー ADH/3F : 5 -GAA CCG AAG CGG CTT TGA CCG CAT -3 ADH/3R: 5 -GTT GAC CAT GCC TGA GAA CAG TAA -3 これらのプライマーを使用した場合 1st PCR では 1451 bp 2nd PCR で は 1324 bp の PCR 産物が生成する 注 ここに示したプライマーは一例であり M. pneumoniae の検出用の プライマー配列は数多く報告されている 参考情報2 M. pneumoniae の遺伝子型別 の2 項にも p1 遺伝子を検出する nested PCR 用のプラ イマーを記した 24
25 PCR 反応液組成 1st 2nd PCR 共通 鋳型 DNA 10ng 1μg 5μl dntp 溶液 各1.25 mm 16μl プライマー F 10 pmol/ml 2μl プライマー R 10 pmol/ml 2μl Taq DNA ポリメラーゼ 1 U/μl 2μl MgCl2 25 mmol/l 8μl 10倍緩衝液* 10μl 滅菌精製水 55μl 100μl *10 倍緩衝液は市販の PCR 酵素製品に付属のものを利用 上記の反応液を混合して下記の条件で PCR を行う 現在は あら かじめ混合された PCR 用の酵素試薬も市販されており タカラバイ オの Premix Taq EX など このような試薬を用いれば 反応液に鋳 型 DNA とプライマーを加えるだけなので簡便で再現性も良い PCR 反応を行う場合には必ず 陰性対照と陽性対照を置かな くてはならない 陽性対照用には あらかじめ M. pneumoniae の菌 体又は DNA を希釈して PCR が陽性になるような低濃度のサンプ ルを調製しておく これを小分け冷凍保存しておき 検査時に使用す る PCR 反応条件 1st, 2nd PCR 共通 94 1分 94 1分 55 1分 72 1分 サイクル 5分 1st PCR が終了したら 0.8%のアガロースゲル電気泳動によって 25
26 DNA の増幅が起こっているかを確認する 特異的な増幅が起こって いたら陽性と判断し 増幅が起こっていない場合は 1st PCR の反応液 1 数 μl を鋳型として 2nd PCR 反応を行う アガロースゲル電気泳動による分析と判定 PCR 終了後 反応液 5 10μl を 0.8 アガロースゲルで電気泳動し エチジウムブロマイド溶液 0.5μg/ml で染色した後 UV トランス イルミネーターを使用して観察する PCR によって特異的な DNA の 増幅がおこっていれば陽性と判定する 増幅が見られない場合や 不 明瞭なスメアになっている場合は陰性 検出限界以下 と判定する 26
27 ② LAMP (loop mediated isothermal amplification method) 法 LAMP 法 は 栄 研 化 学 に よ り 開 発 さ れ た 遺 伝 子 検 出 法 で 簡便で検出感度が高い方法である 実 験室内のコンタミネーションで擬陽性を示すこともあるので 反応後 のチューブは決して実験室で開けないなど作業環境と手技に注意が 必要である 肺炎マイコプラズマ用の LAMP キットが栄研化学より発売されて いるので これを使用する 必要な試薬 器具 LAMP 試薬 Loopamp マイコプラズマ P 検出試薬キット (栄研化学株式会社) マスターミックス調製用滅菌チューブ ピペット 滅菌チップ Loopamp 反応チューブ 氷 微量簡易遠心機 Loopamp リアルタイム濁度測定装置 リアルタイム濁度測定装置を使わない場合 Loopamp 蛍光 目視検出試薬 栄研化学株式会社 ヒートブロック 試験手順 DNA サンプルは 95 で 5 分加熱ののち 氷上で急冷したのちに鋳 型として用いる 汚染による擬陽性を防ぐため 予め UV を照射した安全キャビネ ットやクリーンベンチの中で手袋を装着し作業を行う 反応時には必ず陽性対照と陰性対照を用いること 27
28 4. その他 参考情報1 薬剤耐性菌 M. pneumoniae 感染症には β ラクタム系薬剤は無効であり 通常はエリス ロマイシン ジョサマイシン等のマクロライド系あるいはテトラサイクリン ミノサイクリン等のテトラサイクリン系薬剤が治療に使用される 一方 最近 一部の患者からマクロライド系薬剤に耐性を示す M. pneumoniae が分離され るようになった 耐性菌は 通常 23S rrna 遺伝子ドメイン V 領域に点変異を 起こしており 変異部位によって各マクロライド系薬剤に対する耐性度も少 しずつ異なっている 文献 8 今後 このような耐性菌による感染の拡大を 防止する観点から M. pneumoniae 分離株の薬剤感受性を調べ 耐性菌の動向 を把握していく必要がある M. pneumoniae の薬剤感受性試験法には定まったものがなく その確立お よび標準化が急務と思われるが 以下に神奈川県衛生研究所で現在実施して いる微量液体培地希釈法による感受性試験法について記述する 1 薬剤感受性試験 1 培地 培養法の項に記した Hayflick 変法培地を使用する 2 菌液の調製 液体培地で十分に増殖させた M. pneumoniae の新鮮培養液を新た な液体培地を用いて希釈し CFU / ml としたものを使用する 3 感受性試験 ① 液体培地で 2 ないしは 4 倍階段希釈した薬剤希釈液 100μl を 96 穴マイクロプレート(滅菌済)の各ウェルに分注する ② M. pneumoniae 希釈液 100μl をマイクロプレートの各ウェルに分 注する ③ 対照として 薬剤を含まない培地 200μl 培地対照 および薬剤 28
29 を含まない培地 100 μl に M. pneumoniae 希釈液 100μl を分注した対 照ウェルを用意する M. pneumoniae 対照 ④ マイクロプレートをミキサーで十分混釈し 乾燥を防ぐために 湿潤箱 精製水で湿らせたペーパータオルなどを入れたタッパー 容器など に入れ 37 で好気培養する ⑤ マイクロプレートを毎日 2 回 朝と晩 観察し M. pneumoniae 対照ウェルが完全に黄変した時に 培地対照ウェルと変わらない色 調 橙色 を呈するウェルの薬剤濃度を最小発育阻止濃度 MIC; μg / ml とする 感受性試験実施上の注意事項 ① 培地 ph は MIC 値に影響を与える ph の範囲で エリスロマイシンの MIC 値 は酸性側で高く テトラサイクリンはアルカリ側で高い 感受性用培地の最適 ph については今後の検討課題であるが 感受性試験を実施する際には常に一定にして おく必要がある ② M. pneumoniae 菌数も MIC 値に影響するが CFU/ml であればバラツキは小 さい ③ MIC の判定において M. pneumoniae 対照ウェルが完全に黄変した時に判定する MIC をイニシャル MIC その後数日間培養し M. pneumoniae の増殖が停止した時 に判定するものをファイナル MIC とする場合もある しかし エリスロマイシンや テトラサイクリンのように静菌的に作用する抗生物質では判定後における培養で MIC が変動し ファイナル MIC の判定に戸惑うことがある 従って 当所ではイニ シャル MIC を感受性値として採用している ④ M. pneumoniae の薬剤感受性試験には ここで記載した微量液体培地希釈法以外に 寒天培地希釈法も利用されているが 当所では 感受性用培地の調整や感受性試験 の操作が容易であること等の理由から 上記方法を採用している 両者において測 定された MIC に大差はないとする報告もあるが 今後 感受性試験法の標準化を進 める上で検討すべき課題と考えられる 29
30 2 マクロライド耐性 M. pneumoniae の遺伝子解析 上述のように マクロライド耐性 M. pneumoniae は 23S rrna 遺伝子ド メインⅤ領域に点変異を起こしていることが明らかにされており 既知 の変異については PCR-RFLP 法 (文献 15) やリアルタイム PCR (文献 16 17) で迅速に検出することが可能である 更に 上記の遺伝子領域を塩 基配列解析することにより 未知の変異の検出が可能となる 以下に こ れらの耐性遺伝子解析法について記載する 1) PCR-RFLP 法による遺伝子変異の検出 PCR-RFLP 法 (文献 15)を用いて M. pneumoniae の 23S rrna 遺伝子ド メ イ ン Ⅴ 領 域 の A2063C 2063 位 の adenine が cytosine に 置 換 A2063G A2064G C2617G の変異を調べることができる これらの変異 を含む遺伝子塩基配列を Nested PCR で増幅し 増幅産物を制限酵素で 処理後 その切断パターンを電気泳動により確認する ① サンプル DNA の調整 a) クローニング後の M. pneumoniae の液体培養液 0.5ml をマイ クロチューブにとる b) 15,000rpm 20 分間冷却遠心する c) 上清を捨て 沈査に 20μ lの TE 緩衝液を加えて撹拌する d) アルミブロックヒーターで 99 5 分間処理する e) 加熱後 氷水中で冷却する 又は冷凍庫に保存する ② Nested PCR a) First PCR 23S rrna 遺伝子ドメイン V 領域の変異部位を含 む 927bp の塩基配列を増幅 プライマー 1 (MN23SDVF) 5 - GCAGTGAAGAACGAGGGG (MN23SDVR) 5 - GTCCTCGCTTCGGTCCTCTCG -3 ( ) 30
31 反応液組成 2 PCR Solution Premix Taq 25μ l 蒸留水 17μ l プライマー 1 (MN23SDVF 10μM) 3μ l プライマー 2 (MN23SDVR 10μM) 3μ l サンプル DNA 2μ l 計 50μ l P CR 反応条件 94 2分 秒 55 1分 分 72 5分 30 サイクル First PCR の増幅産物 927bp を Second PCR に使用し 23S rrna の あるいは 2617 位を含む塩基配列を増幅する b) Second PCR 位を含む 210bp の塩基配列を増幅 プライマー 1( MN23SF1937): 5 -ACTATAACGGTCCTAAGGTA (MN23SR2128): 5 -ACCTATTCTCTACATGATAA 反応液組成 2 PCR Solution Premix Taq 25μ l 蒸留水 17μ l プライマー 1 (MN23SF μM) 3μ l プライマー 2 (MN23SR μM) 3μ l サンプル DNA 2μ l 計 50μ l 31
32 PCR 反応条件 94 2分 秒 55 1分 分 72 5分 30 サイクル c) Second PCR 位を含む 108bp の塩基配列を増幅 プライマー 1(MN23SF2577): 5 -TACGTGAGTTGGGTTCAAA-3 ( ) 2(MN23SR2664): (M23SDVR プライマーと同配列) 5 -GTCCTCGCTTCGGTCCTCTCG-3 ( ) 32
33 反応液組成 2 PCR Solution Premix Taq 25μ l 蒸留水 17μ l プライマー 1 (MN23SF μM) 3μ l プライマー 2 (MN23SR μM) 3μ l サンプル DNA 2μ l 計 50μ l PCR 反応条件 94 2分 秒 55 1分 分 72 5分 30 サイクル ③制限酵素処理 a) BceAI BbsI 及び BsaI による処理 上記 b)の Second PCR 産物を用い A2063C 及び A2063G の検出 をするため BceAI (1U/PCR 産物 1μl) 及び BbsI (5U/PCR 産物 1μl) で 37 2 時 間 50 分 処 理 し A2064G の 検 出 に は BsaI 1U/PCR 産物 1μl で 50 2 時間 50 分処理する b) BsmFI による処理 33
34 上記 c)の Second PCR 産物を用い C2617G の検出をするため に BsmFI (2U/PCR 産物 1μl)を用い 37 2 時間 50 分処理する ④アガロースゲル電気泳動 制限酵素で処理した PCR 産物及び制限酵素非処理の産物を 15 グラジュエントポリアクリルアミドゲルあるいは 4 Nusive3:1 アガ ロースゲルを用いて電気泳動し それぞれの泳動パターンを比較し て変異の確認を行う 通常は アガロースゲルによる電気泳動パター ンで充分に変異の確認は可能である 2) 23S rrna ドメイン V 塩基配列解析方法 塩基配列解析法は煩雑ではあるが 位点変異の迅 速かつ確実な検出が可能で 現在 PCR-RFLP 法で確認できない A2064C も検出可能である 更に 薬剤感受性試験でマクロライド耐 性を示すにもかかわらず上記 PCR-RFLP 法で点変異が検出できない M. pneumoniae 臨床分離株については 塩基配列解析でしか変異を確 認できない しかし この方法によりこれまでに報告のない他の部位 に変異が検出されても 薬剤感受性試験を実施して耐性との関連性 を証明する必要がある ① サンプル DNA の調整と PCR サンプル DNA の調整は上記 PCR-RFLP 法と同様に行い 塩 基配列解析に用いる PCR 増幅産物も 上記 PCR-RFLP 法にお ける First PCR と同様に行い作成する ② PCR 産 物 927bp に つ い て DNA の 精 製 を MiniElute PCR purification kit (Qiagen)等で行う 方法はキット解説書に従う ③ BigDye Terminater V3.1 cycle sequencing kit(applied Biosystems) を用い ABI Prism3100 genetic analyzer (Applied Biosystems)で解 する プライマーは PCR-RFLP 法で使用したものと同様のものを用 い る 2063,2064 位 の 変 異 確 認 の 場 合 は MN23SDVF MN23SDVR MN23SF1973 を用いる PCR 産物の 34
35 DNA 塩基配列は BLAST を用いて M. pneumonie M129 株の塩基配列 (accession no.x68422)と比較する 35
36 参考情報2 M. pneumoniae の遺伝子型別 M. pneumoniae にはⅠ型菌とⅡ型菌の 2 つの型があることが明らかに なっている Ⅰ型菌とⅡ型菌はp 1 遺伝子の塩基配列に違いが見られ こ れを調べることによって区別することができる 文献 6 7 Ⅰ型菌と Ⅱ型菌の病原性の違いや流行との関連はよくわかっていないが 過去の 国内分離菌の型別調査では 下図のように数年から 10 年程度の間隔でⅠ 型菌とⅡ型菌が出現を繰り返している 下図の上の矢印は 過去に日本で 大きなマイコプラズマ肺炎の流行が見られた年である 図6 国内 M. pneumoniae 分離株の遺伝子型別調査 文献 13 検査によって M. pneumoniae が分離できた場合 分離菌の型別を行えば 出現菌型の地域差や発生状況との関連で興味が持たれる 分離菌が得ら れている場合は 型別は比較的簡単に行えるので 以下に 方法を記す 36
37 1 M. pneumoniae の遺伝子型別法 PCR-RFLP 法 M. pneumoniae の遺伝子型別は PCR-RFLP 法が簡便で正確ある M. pneumoniae の p1 遺伝子 P1 タンパク質の遺伝子 には Ⅰ型菌とⅡ型菌 で塩基配列が異なる部位が2カ所存在する RepMP2/3 領域と RepMP4 領域 この部分を PCR で増幅し塩基配列の違いを制限酵素の切断パタ ーンで区別する プライマー ADH1 と ADH2 は RepMP4 領域を増幅するのに用い ADH3 と ADH4 は RepMP2/3 領域を増幅するのに用いる どちらの部位 の分析を行ってもⅠ型菌とⅡ型菌は区別できる ただし 近年はそれぞれ の菌型の亜種も見つかってきており このような亜種では RepMP4 と RepMP2/3 領域の両方を分析しないと 区別できない場合がある 使用プライマーセット 1 RepMP4 領域用 ADH1 : CTGCCTTGTCCAAGTCCACT ADH2 : AACCTTGTCGGGAAGAGCTG 使用プライマーセット 2 RepMP2/3 領域用 ADH3 : CGAGTTTGCTGCTAACGAGT ADH4 : CTTGACTGATACCTGTGCGG PCR 反応条件 94 1分 94 1分 55 1分 分 分 30 サイクル M. pneumoniae 分離株の DNA を鋳型として上記の条件で PCR を行う と いずれの場合も約 2.5 kb の PCR 産物が得られる この PCR 産物を制 限酵素 HaeIII で消化した後 2 アガロースゲル電気泳動で分析し 泳動 パターンを比較して型別を行う 37
38 M 1 図7 サイズマーカー 100 bp ラダー I 型菌 2 II 型菌 3 II 型亜種菌 IIa 型 M. pneumoniae の p1 遺伝子型別結果 PCR-RFLP 法 詳しいバンドのサイズは次ページの付表も参照 上記は レーン 1 が I 型菌 レーン2が II 型菌の分析結果である まれに レーン3 ADH3-ADH4 プライマー使用 のように I 型菌 II 型菌とは RFLP パターンが異なる株が見つかることがある この写真の場合は IIa 型 最近は中国の分離菌の中にも新型の亜種が見つかってきており 文献 14 今後 日本で新しい菌型が出現してくることも予想される 既知のものと異なる RFLP パターンを示す株が発見された場合は p1 遺 38
39 伝の塩基配列分析などを行い 論文やデータベース登録などの形で報告 しておく価値がありますので 分析のための技術情報が必要な場合は 感 染研までご連絡下さい 39
40 付表 M. pneumoniae の p1 遺伝子にもとづいた型別 PCR 産物の HaeIII 処理で 以下のサイズの断片が生じる プライマー ADH1-ADH2 プライマー ADH3-ADH4 I型 I型 II 型 II' 型 II 型 II' 型 単位 bp 2 Nested PCR によって高検出感度化した M. pneumoniae の遺伝子型別法 上述の PCR-RFLP 法による M. pneumoniae の遺伝子型別法では p1 遺 伝子の比較的長い領域を PCR で増幅するため 鋳型 DNA の品質が悪い と PCR がうまくかからないことがある このため M. pneumoniae がか なり多く存在している臨床検体であっても 分離培養なしで直接 遺伝 子型別を行うことはできない例が多かった この PCR-RFLP 法を Nested PCR 化することによって M. pneumoniae の検出と型別の両方が行える になった この方法を用いるときには陽性対照としてⅠ型菌 Ⅱ型菌 Ⅱ型亜種 菌のゲノム DNA を準備し 陰性対照もおくこと 陽性対照用の DNA が 必要な場合は 感染研にお問い合わせ下さい 40
41 1st PCR 反応 1st PCR では前述の ADH1 と ADH4 プライマーを用いて p1 遺伝子 のほぼ全体を増幅する 1st PCR プライマー ADH1 : CTGCCTTGTCCAAGTCCACT ADH4 : CTTGACTGATACCTGTGCGG PCR 反応液組成 1st PCR 鋳型 DNA 10ng 1μg 5μl プライマー F 10 pmol/μl 2μl プライマー R 10 pmol/μl 2μl EX Taq DNA ポリメラーゼ premix 25μl 滅菌精製水 16μl 50μl 1st PCR 反応条件 秒 秒 秒 72 4分 分 30 サイクル M. pneumoniae 分離株または臨床検体由来のゲノム DNA を鋳型とし た場合 上記の条件で PCR を行うと 約 4 kb の PCR 産物が得られる 増幅産物は 0.8% アガロースゲル電気泳動で PCR 産物を確認するが 鋳型の量が少ないと 1st PCR ではバンドが確認できないこともある 2nd PCR 反応 1st PCR の産物を鋳型に RepMP4 領域と RepMP2/3 領域を増幅す る 2 組の PCR を行う 41
42 使用プライマーセット 1 RepMP4 領域用 ADH1a: AAGTCCACTTGGATTCTCATCCTCACCGCC ADH2a: GGAAGAGCTGCTAACAATTCCGGATTGAGA 使用プライマーセット 2 RepMP2/3 領域用 ADH3a: GCTAACGAGTACGAGCGCTTTAACCAGAAG ADH4a: ACCTGTGCGGTTAATGATTTCCTTAAAGACA PCR 反応液組成 2nd PCR 鋳型 DNA 10ng 1μg 5μl プライマー F 10 pmol/μl 2μl プライマー R 10 pmol/μl 2μl EX Taq DNA ポリメラーゼ premix 25μl 滅菌精製水 16μl 50μl 2nd PCR 反応条件 秒 秒 秒 72 2分 分 18 サイクル 1st PCR 産物を鋳型として上記の条件で PCR を行うと それぞれ 約 2.5 kb の PCR 産物が得られる 0.8% アガロースゲルで PCR 産物 2 μl を電気泳動し結果を確認する この Nested PCR 法を検出法として用いる場合は をここで特異的 なバンドが確認できたものは M. pneumoniae 陽性とする HaeIII を用いた RFLP 型別 2nd PCR 産物 RepMP4 RepMP2/3 領域それぞれ を Hae III で消 化し 断片を 2%アガロースゲルで電気泳動する 制限酵素処理後の 42
43 電気泳動泳動結果は 既出の図7の型別結果の写真と同様になる 厳密には Nested PCR-RFLP 法では用いているプライマー部位が原 法の PCR-RFLP 法の位置と少し異なるため 前出の付表のサイズと は バンドのサイズがわずかに異なっている しかし この差は電気 泳動では区別できない 43
44 参考情報3 アルギニン添加 Hayflick 変法液体培地 PPLO 液体培地 1 リットルあたりの組成 マイコプラズマ基礎培地 PPLO ブロス アルギニン 21 g 5 g (0.5%) フェノールレッド 20 mg (0.002%) 蒸留水 750 ml アルギニン培地は 滅菌前に 1N HCl で ph を中性 微酸性に調製し 濃いオレンジ色にしておく 菌増殖によりピンク色に色調変化するた め 培養前に培地の色が赤いと判別しづらいため 上記を高圧蒸気滅菌し 血清が凝固しない温度 約 50 以下に冷 えたら 無菌的に以下のものを加える ウマ血清 55 で 30 分間加熱済 150 ml (15 %) 25 % 新鮮酵母エキス 100 ml (10 %) ペニシリン G 100 万単位 2.5 % 酢酸タリウム溶液 10 ml PPLO Broth w/o CV, Difco , Becton Dickinson クリスタルバイ オレット無添加 毒性があるので 取り扱いに注意 必須ではない ペニシリン G はアンピシリン 終濃度 50μg/ml に置き換えることも 可能 Mycoplasma 属菌の代謝性をみるには ブドウ糖添加 PPLO 液体培地な らびにアルギニン添加 PPLO 液体培地の 2 種類の培地に検体や菌コロニ ーを接種し 37 好気条件で培養する 何も接種しない培地のみの陰性 対照も一緒に培養し 色調変化を比較観察する 例えば M. pneumoniae は グルコースのみを代謝するので 増殖するとブドウ糖添加培地のほうが 強く黄変する アルギニン添加培地も黄変する M. orale は アルギニ ンのみを代謝するので アルギニン添加培地のほうがより強いピンク色 44
45 に変わる ブドウ糖添加培地もピンク色に変化してくる M. fermentans や M. penetrans は ブドウ糖 アルギニンの両方を代謝するため ブドウ糖 添加培地は強く黄変 アルギニン添加培地は強いピンク色になる 図8 代謝性の異なるマイコプラズマ培養時の培地の色調変化 M. pneumoniae はブドウ糖添加 M. orale はアルギニン添加 培地で培養した 補足 ヒト臨床検体からは M. pneumoniae 以外に下記のマイコプラ ズマ種が分離されることがある それぞれが主に分離される部位とそ れらの代謝性を示す 種名 主に分離される部位 代謝性 赤血球付着性 気道 ブドウ糖 口腔 アルギニン 無し M. salivarium 口腔 アルギニン 無し M. fermentans 口腔等 M. hominis 泌尿器 アルギニン 無し 泌尿器 ブドウ糖 有り 両方 有り ブドウ糖 有り ブドウ糖 無し M. pneumoniae M. orale M. genitalium M. penetrans M. amphoriforme 両方 気道 泌尿器 気道 Acholeplasma laidlawii 45 有り 無し
46 参考情報4 マイコプラズマ肺炎届出基準 マイコプラズマ肺炎は感染症法上 五類感染症 定点把握感染症 に分類 されている 国内の感染症動向調査の定点として指定されている医療機関か らは 以下の基準をみたした場合に届け出が提出される マイコプラズマ肺 炎 1 定義 Mycoplasma pneumoniae の感染によって発症する肺炎である 2 臨床的特徴 好発年齢は 6 12歳の小児であり 小児では発生頻度の高い感染症の一 つである 潜伏期は2 3週間とされ 飛沫で感染する 異型肺炎像を呈する こと が多い 頑固な咳嗽と発熱を主症状に発病し 中耳炎 胸膜炎 心筋炎 髄 膜炎などの合併症を併発する症例も報告されている 3 届出基準 ア 患者 確定例 指定届出機関の管理者は 当該指定届出機関の医師が 2 の臨床的特 徴を有する者を診察した結果 症状や所見からマイコプラズマ肺炎が疑わ れ かつ 4 により マイコプラズマ肺炎患者と診断した場合には 法 第14条第2項の規定による届出を週単位で 翌週の月曜日に届け出なけ ればならない イ 感染症死亡者の死体 指定届出機関の管理者は 当該指定届出機関の医師が 2 の臨床的特 徴を有する死体を検案した結果 症状や所見から マイコプラズマ肺炎が疑 われ か つ 4 により マイコプラズマ肺炎により死亡したと判断した 場合には 法第14条第2項の規定による届出を週単位で 翌週の月曜日に 届け出なければな らない 4 届出のために必要な検査所見 検査方法 分離 同定による病原体の検出 PCR法又はLAMP法による病原体の遺伝子の検出 検査材料 気道から採取 された検体 抗体の検出 血清 ペア血清による抗体陽転又は抗体価の有意の上昇 又は単一 血清で間接血球凝集抗体価320倍以上 補体結合抗体価64 倍以上 ゼラチン粒子凝集抗体価320倍以上 若しくはIg M抗体の検出 迅速診断キット 46
47 47
48 5 文献 1. 尾形学監修 輿水馨 清水高正 山本孝史編集 マイコプラズマとその実 験法 1988 近代出版 2. 佐々木正吾編 マイコプラズマ図説 1980 東海大学出版会 3. 佐々木正吾 尾形学 中村昌弘編 マイコプラズマ 1974 講談社サイエン テイフィック 4. Waites, K. B., Bébéar, C. M., Robertson, J. A., Talkington, D. F. and Kenny, G. E. : Laboratory diagnosis of mycoplasmal infections in Cumitech-Cumulatie techniques and procedures in clinical microbiology, edited by Nolte, F. S. 2001, ASM press, Washington, DC, U.S.A. 5. 田澤節子 岩澤篤郎 中村良子 Mycoplasma, 臨床と微生物, 2001, Kenri T, Taniguchi R, Sasaki Y et al. : Identification of a new variable sequence in the P1 cytadhesin gene of Mycoplasma pneumoniae: evidence for the generation of antigenic variation by DNA recombination between repetitive sequences. Infect Immun 67 : , Dorigo-Zetsma JW, Wilbrink B, Dankert J et al. : Mycoplasma pneumoniae P1 Type 1- and Type 2-Specific Sequences within the P1 Cytadhesin Gene of Individual Strains. Infect Immun 69 : , Okazaki N, Narita M, Yamada S, Izumikawa K, Umetsu M, Kenri T, Sasaki Y, Arakawa Y, Sasaki T.: Characteristics of macrolide-resistant Mycoplasma pneumoniae strains isolated from patients and induced with erythromycin in vitro. Microbiol Immunol 45 : ,
49 9. 成田 光生 富樫 武弘: 小児マイコプラズマ感染 症診断における迅速診 断キットの有用性. 感染症学雑誌 77(5) : Matthias F.C.Beersma, et al : Evaluation of 12 Commercial Tests and the Complement Fixation Test for Mycoplasma pneumoniae- Specific Immunoglobulin G (IgG) and IgM Antibodies, with PCR Used as the Gold Standard. J. Clin. Microbiol. 43: , Thacker, W. L., and D. F. Talkington. Analysis of complement fixation and commercial enzyme immunoassays for detection of antibodies to Mycoplasma pneumoniae in human serum. Clin. Diagn. Lab. Immunol. 7: , 加藤彰一 半定量解析によるイムノカードマイコプラズマ抗体キット の有用性の評価. 小児感染免疫 Kenri T, Okazaki N, Yamazaki T, Narita M, Izumikawa K, Matsuoka M, Suzuki S, Horino A, Sasaki T. Genotyping analysis of Mycoplasma pneumoniae clinical strains in Japan between 1995 and 2005: type shift phenomenon of M. pneumoniae clinical strains. J. Med. Microbiol. 57: , Zhao F, Cao B, Li J, Song S, Tao X, Yin Y, He L, Zhang J. Sequence analysis of the p1 adhesin gene of Mycoplasma pneumoniae in clinical isolates collected in Beijing in 2008 to J. Clin. Microbiol. 49: , Matsuoka M. et al :Characterization and molecular analysis of macrolideresistant Mycoplasma pneumoniae clinical isolates obtained in Japan. Antimicrob. Agents Chemother. 48: , Morozumi M, et al.:acute Respiratory Diseases Study Group. Increased macrolide resistance of Mycoplasma pneumoniae in pediatric patients with community-acquired pneumonia. Antimicrob. Agents Chemother. 52:348-49
50 50, Peuchant O,et al.: Increased macrolide resistance of Mycoplasma pneumoniae in France directly detected in clinical specimens by real-time PCR and melting curve analysis. J Antimicrob Chemother. 64(1):
51 6 執筆者 神奈川県衛生研究所 微生物部 大屋日登美 国立感染症研究所 細菌第二部 第二室 堀野敦子 見理 剛 佐々木 裕子 問い合わせ先 神奈川県衛生研究所 神奈川県茅ヶ崎下町屋 国立感染症研究所 細菌第二部 東京都武蔵村山市学園
肺炎マ検出マニュアル2011改訂版_
 Mycoplasma pneumoniae 23 9 1 1. Mycoplasma pneumoniae 2. 1) 2) 3) 4) 3. 1) M. pneumoniae 2) 3) 4) PCR LAMP 4. M. pneumoniae Hayflick 5. 6. 2 Mycoplasma pneumoniae M. pneumoniae Mollicutes ycoplasma 800kb
Mycoplasma pneumoniae 23 9 1 1. Mycoplasma pneumoniae 2. 1) 2) 3) 4) 3. 1) M. pneumoniae 2) 3) 4) PCR LAMP 4. M. pneumoniae Hayflick 5. 6. 2 Mycoplasma pneumoniae M. pneumoniae Mollicutes ycoplasma 800kb
DNA/RNA調製法 実験ガイド
 DNA/RNA 調製法実験ガイド PCR の鋳型となる DNA を調製するにはいくつかの方法があり 検体の種類や実験目的に応じて適切な方法を選択します この文書では これらの方法について実際の操作方法を具体的に解説します また RNA 調製の際の注意事項や RNA 調製用のキット等をご紹介します - 目次 - 1 実験に必要なもの 2 コロニーからの DNA 調製 3 増菌培養液からの DNA 調製
DNA/RNA 調製法実験ガイド PCR の鋳型となる DNA を調製するにはいくつかの方法があり 検体の種類や実験目的に応じて適切な方法を選択します この文書では これらの方法について実際の操作方法を具体的に解説します また RNA 調製の際の注意事項や RNA 調製用のキット等をご紹介します - 目次 - 1 実験に必要なもの 2 コロニーからの DNA 調製 3 増菌培養液からの DNA 調製
■リアルタイムPCR実践編
 リアルタイム PCR 実践編 - SYBR Green I によるリアルタイム RT-PCR - 1. プライマー設計 (1)Perfect Real Time サポートシステムを利用し 設計済みのものを購入する ヒト マウス ラットの RefSeq 配列の大部分については Perfect Real Time サポートシステムが利用できます 目的の遺伝子を検索して購入してください (2) カスタム設計サービスを利用する
リアルタイム PCR 実践編 - SYBR Green I によるリアルタイム RT-PCR - 1. プライマー設計 (1)Perfect Real Time サポートシステムを利用し 設計済みのものを購入する ヒト マウス ラットの RefSeq 配列の大部分については Perfect Real Time サポートシステムが利用できます 目的の遺伝子を検索して購入してください (2) カスタム設計サービスを利用する
豚丹毒 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 23 年 2 月 8 日 ( 告示第 358 号 ) 新規追加 1 定義シードロット規格に適合した豚丹毒菌の培養菌液を不活化し アルミニウムゲルアジュバントを添加したワクチンである 2 製法 2.1 製造用株 名称豚丹
 豚丹毒 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 23 年 2 月 8 日 ( 告示第 358 号 ) 新規追加 1 定義シードロット規格に適合した豚丹毒菌の培養菌液を不活化し アルミニウムゲルアジュバントを添加したワクチンである 2 製法 2.1 製造用株 2.1.1 名称豚丹毒菌多摩 96 株 ( 血清型 2 型 ) 又はこれと同等と認められた株 2.1.2 性状感受性豚に接種すると
豚丹毒 ( アジュバント加 ) 不活化ワクチン ( シード ) 平成 23 年 2 月 8 日 ( 告示第 358 号 ) 新規追加 1 定義シードロット規格に適合した豚丹毒菌の培養菌液を不活化し アルミニウムゲルアジュバントを添加したワクチンである 2 製法 2.1 製造用株 2.1.1 名称豚丹毒菌多摩 96 株 ( 血清型 2 型 ) 又はこれと同等と認められた株 2.1.2 性状感受性豚に接種すると
耐性菌届出基準
 37 ペニシリン耐性肺炎球菌感染症 (1) 定義ペニシリン G に対して耐性を示す肺炎球菌による感染症である (2) 臨床的特徴小児及び成人の化膿性髄膜炎や中耳炎で検出されるが その他 副鼻腔炎 心内膜炎 心嚢炎 腹膜炎 関節炎 まれには尿路生殖器感染から菌血症を引き起こすこともある 指定届出機関の管理者は 当該指定届出機関の医師が (2) の臨床的特徴を有する者を診察した結果 症状や所見からペニシリン耐性肺炎球菌感染症が疑われ
37 ペニシリン耐性肺炎球菌感染症 (1) 定義ペニシリン G に対して耐性を示す肺炎球菌による感染症である (2) 臨床的特徴小児及び成人の化膿性髄膜炎や中耳炎で検出されるが その他 副鼻腔炎 心内膜炎 心嚢炎 腹膜炎 関節炎 まれには尿路生殖器感染から菌血症を引き起こすこともある 指定届出機関の管理者は 当該指定届出機関の医師が (2) の臨床的特徴を有する者を診察した結果 症状や所見からペニシリン耐性肺炎球菌感染症が疑われ
Taro-SV02500b.jtd
 牛大腸菌性下痢症 (K99 保有全菌体 FY 保有全菌体 31A 保有全菌体 O78 全菌体 )( アジュバント加 ) 不活化ワクチン 平成 21 年 11 月 12 日 ( 告示第 1569 号 ) 一部改正 1 定義線毛抗原 K99 FY 及び 31A を保有する大腸菌並びに O78 の大腸菌の培養菌液を不活化したものを混合し アルミニウムゲルアジュバントを添加したワクチンである 2 製法 2.1
牛大腸菌性下痢症 (K99 保有全菌体 FY 保有全菌体 31A 保有全菌体 O78 全菌体 )( アジュバント加 ) 不活化ワクチン 平成 21 年 11 月 12 日 ( 告示第 1569 号 ) 一部改正 1 定義線毛抗原 K99 FY 及び 31A を保有する大腸菌並びに O78 の大腸菌の培養菌液を不活化したものを混合し アルミニウムゲルアジュバントを添加したワクチンである 2 製法 2.1
遺伝子検査の基礎知識
 リアルタイム PCR( インターカレーター法 ) 実験ガイドこの文書では インターカレーター法 (TB Green 検出 ) によるリアルタイム PCR について 蛍光検出の原理や実験操作の流れなどを解説します 実際の実験操作の詳細については 各製品の取扱説明書をご参照ください - 目次 - 1 蛍光検出の原理 2 実験に必要なもの 3 実験操作法 4 結果の解析 1 1 蛍光検出の原理 インターカレーターによる蛍光検出の原理
リアルタイム PCR( インターカレーター法 ) 実験ガイドこの文書では インターカレーター法 (TB Green 検出 ) によるリアルタイム PCR について 蛍光検出の原理や実験操作の流れなどを解説します 実際の実験操作の詳細については 各製品の取扱説明書をご参照ください - 目次 - 1 蛍光検出の原理 2 実験に必要なもの 3 実験操作法 4 結果の解析 1 1 蛍光検出の原理 インターカレーターによる蛍光検出の原理
Microsoft Word - FMB_Text(PCR) _ver3.doc
 2.PCR 法による DNA の増幅 現代の分子生物学において その進歩に最も貢献した実験法の1つが PCR(Polymerase chain reaction) 法である PCR 法は極めて微量の DNA サンプルから特定の DNA 断片を短時間に大量に増幅することができる方法であり 多大な時間と労力を要した遺伝子クローニングを過去のものとしてしまった また その操作の簡便さから 現在では基礎研究のみならず臨床遺伝子診断から食品衛生検査
2.PCR 法による DNA の増幅 現代の分子生物学において その進歩に最も貢献した実験法の1つが PCR(Polymerase chain reaction) 法である PCR 法は極めて微量の DNA サンプルから特定の DNA 断片を短時間に大量に増幅することができる方法であり 多大な時間と労力を要した遺伝子クローニングを過去のものとしてしまった また その操作の簡便さから 現在では基礎研究のみならず臨床遺伝子診断から食品衛生検査
プロトコール集 ( 研究用試薬 ) < 目次 > 免疫組織染色手順 ( 前処理なし ) p2 免疫組織染色手順 ( マイクロウェーブ前処理 ) p3 免疫組織染色手順 ( オートクレーブ前処理 ) p4 免疫組織染色手順 ( トリプシン前処理 ) p5 免疫組織染色手順 ( ギ酸処理 ) p6 免疫
 < 目次 > 免疫組織染色手順 ( 前処理なし ) p2 免疫組織染色手順 ( マイクロウェーブ前処理 ) p3 免疫組織染色手順 ( オートクレーブ前処理 ) p4 免疫組織染色手順 ( トリプシン前処理 ) p5 免疫組織染色手順 ( ギ酸処理 ) p6 免疫組織染色手順 ( ギ酸処理後 マイクロウェーブまたはオートクレーブ処理 )p7 抗原ペプチドによる抗体吸収試験 p8 ウエスタン ブロッティング
< 目次 > 免疫組織染色手順 ( 前処理なし ) p2 免疫組織染色手順 ( マイクロウェーブ前処理 ) p3 免疫組織染色手順 ( オートクレーブ前処理 ) p4 免疫組織染色手順 ( トリプシン前処理 ) p5 免疫組織染色手順 ( ギ酸処理 ) p6 免疫組織染色手順 ( ギ酸処理後 マイクロウェーブまたはオートクレーブ処理 )p7 抗原ペプチドによる抗体吸収試験 p8 ウエスタン ブロッティング
BKL Kit (Blunting Kination Ligation Kit)
 製品コード 6126/6127 BKL Kit (Blunting Kination Ligation Kit) 説明書 PCR 産物を平滑末端ベクターにクローニングする場合 使用するポリメラーゼ酵素の種類により 3' 末端に余分に付加された塩基を除去し さらに 5' 末端をリン酸化する必要があります 本製品は これらの一連の反応を簡便に短時間に行うためのキットです PCR 産物の末端平滑化とリン酸化を同時に行うことにより
製品コード 6126/6127 BKL Kit (Blunting Kination Ligation Kit) 説明書 PCR 産物を平滑末端ベクターにクローニングする場合 使用するポリメラーゼ酵素の種類により 3' 末端に余分に付加された塩基を除去し さらに 5' 末端をリン酸化する必要があります 本製品は これらの一連の反応を簡便に短時間に行うためのキットです PCR 産物の末端平滑化とリン酸化を同時に行うことにより
別紙 1 新型インフルエンザ (1) 定義新型インフルエンザウイルスの感染による感染症である (2) 臨床的特徴咳 鼻汁又は咽頭痛等の気道の炎症に伴う症状に加えて 高熱 (38 以上 ) 熱感 全身倦怠感などがみられる また 消化器症状 ( 下痢 嘔吐 ) を伴うこともある なお 国際的連携のもとに
 別紙 1 新型インフルエンザ (1) 定義新型インフルエンザウイルスの感染による感染症である (2) 臨床的特徴咳 鼻汁又は咽頭痛等の気道の炎症に伴う症状に加えて 高熱 (38 以上 ) 熱感 全身倦怠感などがみられる また 消化器症状 ( 下痢 嘔吐 ) を伴うこともある なお 国際的連携のもとに最新の知見を集約し 変更される可能性がある (3) 届出基準ア患者 ( 確定例 ) 患者 ( 確定例
別紙 1 新型インフルエンザ (1) 定義新型インフルエンザウイルスの感染による感染症である (2) 臨床的特徴咳 鼻汁又は咽頭痛等の気道の炎症に伴う症状に加えて 高熱 (38 以上 ) 熱感 全身倦怠感などがみられる また 消化器症状 ( 下痢 嘔吐 ) を伴うこともある なお 国際的連携のもとに最新の知見を集約し 変更される可能性がある (3) 届出基準ア患者 ( 確定例 ) 患者 ( 確定例
ISOSPIN Blood & Plasma DNA
 血液 血清 血しょうからの DNA 抽出キット ISOSPIN Blood & Plasma DNA マニュアル ( 第 2 版 ) Code No. 312-08131 NIPPON GENE CO., LTD. I 製品説明 ISOSPIN Blood & Plasma DNA( アイソスピンブラッド & プラズマ DNA) は 血液 血清 血しょうから DNAを抽出するためのキットです 本キットは
血液 血清 血しょうからの DNA 抽出キット ISOSPIN Blood & Plasma DNA マニュアル ( 第 2 版 ) Code No. 312-08131 NIPPON GENE CO., LTD. I 製品説明 ISOSPIN Blood & Plasma DNA( アイソスピンブラッド & プラズマ DNA) は 血液 血清 血しょうから DNAを抽出するためのキットです 本キットは
Microsoft Word - 【要旨】_かぜ症候群の原因ウイルス
 かぜ症候群の原因ウイルス ~ サフォードウイルスもそのひとつ?~ 新潟県保健環境科学研究所ウイルス科主任研究員広川智香 1 はじめにかぜ症候群とは, 鼻やのど, 気管支や肺に急性の炎症をきたす疾患の総称で, その原因となる病原体は 80~90% がウイルスといわれています 主な原因ウイルスとしてはライノウイルス, コロナウイルス, パラインフルエンザウイルス,RS ウイルス, インフルエンザウイルスなどがあげられます
かぜ症候群の原因ウイルス ~ サフォードウイルスもそのひとつ?~ 新潟県保健環境科学研究所ウイルス科主任研究員広川智香 1 はじめにかぜ症候群とは, 鼻やのど, 気管支や肺に急性の炎症をきたす疾患の総称で, その原因となる病原体は 80~90% がウイルスといわれています 主な原因ウイルスとしてはライノウイルス, コロナウイルス, パラインフルエンザウイルス,RS ウイルス, インフルエンザウイルスなどがあげられます
パナテスト ラットβ2マイクログロブリン
 研究用試薬 2014 年 4 月作成 EIA 法ラット β 2 マイクログロブリン測定キット PRH111 パナテスト A シリーズラット β 2- マイクロク ロフ リン 1. はじめに β 2 - マイクログロブリンは, 血液, 尿, および体液中に存在し, ヒトでは腎糸球体障害, 自己免疫疾患, 悪性腫瘍, 肝疾患などによって血中濃度が変化するといわれています. また,β 2 - マイクログロブリンの尿中濃度は,
研究用試薬 2014 年 4 月作成 EIA 法ラット β 2 マイクログロブリン測定キット PRH111 パナテスト A シリーズラット β 2- マイクロク ロフ リン 1. はじめに β 2 - マイクログロブリンは, 血液, 尿, および体液中に存在し, ヒトでは腎糸球体障害, 自己免疫疾患, 悪性腫瘍, 肝疾患などによって血中濃度が変化するといわれています. また,β 2 - マイクログロブリンの尿中濃度は,
遺伝子検査の基礎知識
 遺伝子検査の準備と注意事項 PCR はわずか 1 分子の鋳型 DNA でも検出可能であるため 反応液調製時に鋳型となりうる核酸等が混入しないように細心の注意が必要です この文書では 正確な遺伝子検査を行うために必要な実験器具類やコンタミネーション防止のための注意事項について解説します - 目次 - 1 実験環境の整備 2 必要な実験器具と装置 1 実験環境の整備 コンタミネーションの原因 PCR は非常に高感度な検出法であるため
遺伝子検査の準備と注意事項 PCR はわずか 1 分子の鋳型 DNA でも検出可能であるため 反応液調製時に鋳型となりうる核酸等が混入しないように細心の注意が必要です この文書では 正確な遺伝子検査を行うために必要な実験器具類やコンタミネーション防止のための注意事項について解説します - 目次 - 1 実験環境の整備 2 必要な実験器具と装置 1 実験環境の整備 コンタミネーションの原因 PCR は非常に高感度な検出法であるため
1-4. 免疫抗体染色 抗体とは何かリンパ球 (B 細胞 ) が作る物質 特定の ( タンパク質 ) 分子に結合する 体の中に侵入してきた病原菌や毒素に結合して 破壊したり 無毒化したりする作用を持っている 例 : 抗血清馬などに蛇毒を注射し 蛇毒に対する抗体を作らせたもの マムシなどの毒蛇にかまれ
 1. 血液細胞の免疫蛍光染色とフローサイトメトリー解析 1-1. フローサイトメトリー ( Flow Cytometory ) とは細胞浮遊液をフローセル内を高速で流し 個々の細胞の形質等についてレーザー光を用いて解析する研究手法 フローサイトメーター( Flow Cytometer ) フローサイトメトリーにおいて使用する細胞解析用の装置今回は BD Accuri C6 を使用する 1-2. フローサイトメーターで何ができるか?
1. 血液細胞の免疫蛍光染色とフローサイトメトリー解析 1-1. フローサイトメトリー ( Flow Cytometory ) とは細胞浮遊液をフローセル内を高速で流し 個々の細胞の形質等についてレーザー光を用いて解析する研究手法 フローサイトメーター( Flow Cytometer ) フローサイトメトリーにおいて使用する細胞解析用の装置今回は BD Accuri C6 を使用する 1-2. フローサイトメーターで何ができるか?
医療機関における診断のための検査ガイドライン
 医療機関における診断のための検査ガイドライン 新型インフルエンザ専門家会議 平成 19 年 3 月 26 日 153 154 ウイルス輸送培地 医療機関における診断のための検査 事前準備臨床検体の採取検体の輸送 地方衛生研究所において PBS 等を用いた培地を作成 ウイルス輸送培地の供給 地方衛生研究所より 感染症指定医療機関等へ分配供給 ウイルス輸送培地の保管 医療機関において 4 又は -20
医療機関における診断のための検査ガイドライン 新型インフルエンザ専門家会議 平成 19 年 3 月 26 日 153 154 ウイルス輸送培地 医療機関における診断のための検査 事前準備臨床検体の採取検体の輸送 地方衛生研究所において PBS 等を用いた培地を作成 ウイルス輸送培地の供給 地方衛生研究所より 感染症指定医療機関等へ分配供給 ウイルス輸送培地の保管 医療機関において 4 又は -20
組織からのゲノム DNA 抽出キット Tissue Genomic DNA Extraction Mini Kit 目次基本データ 3 キットの内容 3 重要事項 4 操作 4 サンプル別プロトコール 7 トラブルシューティング 9 * 本製品は研究用です *
 組織からのゲノム DNA 抽出キット Tissue Genomic DNA Extraction Mini Kit 目次基本データ 3 キットの内容 3 重要事項 4 操作 4 サンプル別プロトコール 7 トラブルシューティング 9 * 本製品は研究用です * 2 本キットは動物の組織からトータル DNA を迅速に効率よく抽出するようにデザインされています また 細菌 固定組織 酵母用のプロトコールも用意しています
組織からのゲノム DNA 抽出キット Tissue Genomic DNA Extraction Mini Kit 目次基本データ 3 キットの内容 3 重要事項 4 操作 4 サンプル別プロトコール 7 トラブルシューティング 9 * 本製品は研究用です * 2 本キットは動物の組織からトータル DNA を迅速に効率よく抽出するようにデザインされています また 細菌 固定組織 酵母用のプロトコールも用意しています
医薬品タンパク質は 安全性の面からヒト型が常識です ではなぜ 肌につける化粧品用コラーゲンは ヒト型でなくても良いのでしょうか? アレルギーは皮膚から 最近の学説では 皮膚から侵入したアレルゲンが 食物アレルギー アトピー性皮膚炎 喘息 アレルギー性鼻炎などのアレルギー症状を引き起こすきっかけになる
 化粧品用コラーゲンの原料 現在は 魚由来が中心 かつては ウシの皮膚由来がほとんど BSE 等病原体混入の危険 人に感染する病原体をもたない アレルギーの問題は未解決 ( むしろ問題は大きくなったかもしれない ) アレルギーを引き起こす可能性 医薬品タンパク質は 安全性の面からヒト型が常識です ではなぜ 肌につける化粧品用コラーゲンは ヒト型でなくても良いのでしょうか? アレルギーは皮膚から 最近の学説では
化粧品用コラーゲンの原料 現在は 魚由来が中心 かつては ウシの皮膚由来がほとんど BSE 等病原体混入の危険 人に感染する病原体をもたない アレルギーの問題は未解決 ( むしろ問題は大きくなったかもしれない ) アレルギーを引き起こす可能性 医薬品タンパク質は 安全性の面からヒト型が常識です ではなぜ 肌につける化粧品用コラーゲンは ヒト型でなくても良いのでしょうか? アレルギーは皮膚から 最近の学説では
イルスが存在しており このウイルスの存在を確認することが診断につながります ウ イルス性発疹症 についての詳細は他稿を参照していただき 今回は 局所感染疾患 と 腫瘍性疾患 のウイルス感染検査と読み方について解説します 皮膚病変におけるウイルス感染検査 ( 図 2, 表 ) 表 皮膚病変におけるウイ
 2012 年 12 月 13 日放送 第 111 回日本皮膚科学会総会 6 教育講演 26-3 皮膚病変におけるウイルス感染検査と読み方 川崎医科大学皮膚科 講師山本剛伸 はじめにウイルス性皮膚疾患は 臨床症状から視診のみで診断がつく例もありますが ウイルス感染検査が必要となる症例も日常多く遭遇します ウイルス感染検査法は多種類存在し それぞれに利点 欠点があります 今回は それぞれのウイルス感染検査について
2012 年 12 月 13 日放送 第 111 回日本皮膚科学会総会 6 教育講演 26-3 皮膚病変におけるウイルス感染検査と読み方 川崎医科大学皮膚科 講師山本剛伸 はじめにウイルス性皮膚疾患は 臨床症状から視診のみで診断がつく例もありますが ウイルス感染検査が必要となる症例も日常多く遭遇します ウイルス感染検査法は多種類存在し それぞれに利点 欠点があります 今回は それぞれのウイルス感染検査について
Bacterial 16S rDNA PCR Kit
 研究用 Bacterial 16S rdna PCR Kit 説明書 v201802da 微生物の同定は 形態的特徴 生理 生化学的性状 化学分類学的性状などを利用して行われますが これらの方法では同定までに時間を要します また 同定が困難な場合や正しい結果が得られない場合もあります 近年 微生物同定にも分子生物学を利用した方法が採用されるようになり 微生物の持つ DNA を対象として解析を行う方法が活用されています
研究用 Bacterial 16S rdna PCR Kit 説明書 v201802da 微生物の同定は 形態的特徴 生理 生化学的性状 化学分類学的性状などを利用して行われますが これらの方法では同定までに時間を要します また 同定が困難な場合や正しい結果が得られない場合もあります 近年 微生物同定にも分子生物学を利用した方法が採用されるようになり 微生物の持つ DNA を対象として解析を行う方法が活用されています
ノーウオ―クウイルスのPCR法
 厚生労働科学研究新型インフルエンザ等新興 再興感染症研究事業 現在 国内で分離 同定できないウイルス性出血熱等の診断等の対応方法に関する研究 班より SFTS ウイルス検査マニュアル 平成 25 年 3 月 13 日 RT-PCR 法により SFTS ウイルス核蛋白質 (NP) 遺伝子を特異的に検出 同定する検査法を解説する 本法は 1 本の反応チューブ内で逆転写反応 遺伝子増幅を連続的に行い SFTS
厚生労働科学研究新型インフルエンザ等新興 再興感染症研究事業 現在 国内で分離 同定できないウイルス性出血熱等の診断等の対応方法に関する研究 班より SFTS ウイルス検査マニュアル 平成 25 年 3 月 13 日 RT-PCR 法により SFTS ウイルス核蛋白質 (NP) 遺伝子を特異的に検出 同定する検査法を解説する 本法は 1 本の反応チューブ内で逆転写反応 遺伝子増幅を連続的に行い SFTS
 The clinical characteristics of Mycoplasma pneumoniae pneumonia in children younger than 6 years old Nobue Takeda1,2),Tomomichi Kurosaki1),Naruhiko Ishiwada2),Yoichi Kohno2) 1)Department of Pediatrics,Chiba
The clinical characteristics of Mycoplasma pneumoniae pneumonia in children younger than 6 years old Nobue Takeda1,2),Tomomichi Kurosaki1),Naruhiko Ishiwada2),Yoichi Kohno2) 1)Department of Pediatrics,Chiba
大学院博士課程共通科目ベーシックプログラム
 平成 30 年度医科学専攻共通科目 共通基礎科目実習 ( 旧コア実習 ) 概要 1 ). 大学院生が所属する教育研究分野における実習により単位認定可能な実習項目 ( コア実習項目 ) 1. 組換え DNA 技術実習 2. 生体物質の調製と解析実習 3. 薬理学実習 4. ウイルス学実習 5. 免疫学実習 6. 顕微鏡試料作成法実習 7. ゲノム医学実習 8. 共焦点レーザー顕微鏡実習 2 ). 実習を担当する教育研究分野においてのみ単位認定可能な実習項目
平成 30 年度医科学専攻共通科目 共通基礎科目実習 ( 旧コア実習 ) 概要 1 ). 大学院生が所属する教育研究分野における実習により単位認定可能な実習項目 ( コア実習項目 ) 1. 組換え DNA 技術実習 2. 生体物質の調製と解析実習 3. 薬理学実習 4. ウイルス学実習 5. 免疫学実習 6. 顕微鏡試料作成法実習 7. ゲノム医学実習 8. 共焦点レーザー顕微鏡実習 2 ). 実習を担当する教育研究分野においてのみ単位認定可能な実習項目
一次サンプル採取マニュアル PM 共通 0001 Department of Clinical Laboratory, Kyoto University Hospital その他の検体検査 >> 8C. 遺伝子関連検査受託終了項目 23th May EGFR 遺伝子変異検
 Department of Clinical Laboratory, Kyoto University Hospital 6459 8. その他の検体検査 >> 8C. 遺伝子関連検査受託終了項目 23th May. 2017 EGFR 遺伝子変異検査 ( 院内測定 ) c-erbb/egfr [tissues] 基本情報 8C051 c-erbb/egfr JLAC10 診療報酬 分析物 識別材料測定法
Department of Clinical Laboratory, Kyoto University Hospital 6459 8. その他の検体検査 >> 8C. 遺伝子関連検査受託終了項目 23th May. 2017 EGFR 遺伝子変異検査 ( 院内測定 ) c-erbb/egfr [tissues] 基本情報 8C051 c-erbb/egfr JLAC10 診療報酬 分析物 識別材料測定法
Microsoft Word - H30eqa麻疹風疹実施手順書(案)v13日付記載.docx
 平成 30 年度外部精度管理事業 課題 1 麻疹 風疹 実施手順書 ( ウイルスの核酸検出検査 ) 1) 検体を受け取りましたら 外部精度管理事業ホームページ (https://www.niid.go.jp/niid/ja/reference/eqa.html) にてお手続きください 2) 検体到着後 各チューブのスピンダウンを行ってから 500 マイクロリットルの Nuclease-free water
平成 30 年度外部精度管理事業 課題 1 麻疹 風疹 実施手順書 ( ウイルスの核酸検出検査 ) 1) 検体を受け取りましたら 外部精度管理事業ホームページ (https://www.niid.go.jp/niid/ja/reference/eqa.html) にてお手続きください 2) 検体到着後 各チューブのスピンダウンを行ってから 500 マイクロリットルの Nuclease-free water
ChIP Reagents マニュアル
 ChIP Reagents ~ クロマチン免疫沈降 (ChIP) 法用ストック溶液セット ~ マニュアル ( 第 1 版 ) Code No. 318-07131 NIPPON GENE CO., LTD. 目次 Ⅰ 製品説明 1 Ⅱ セット内容 1 Ⅲ 保存 2 Ⅳ 使用上の注意 2 Ⅴ 使用例 2 < 本品以外に必要な試薬 機器など> 2 1) 磁気ビーズと一次抗体の反応 3 2)-1 細胞の調製
ChIP Reagents ~ クロマチン免疫沈降 (ChIP) 法用ストック溶液セット ~ マニュアル ( 第 1 版 ) Code No. 318-07131 NIPPON GENE CO., LTD. 目次 Ⅰ 製品説明 1 Ⅱ セット内容 1 Ⅲ 保存 2 Ⅳ 使用上の注意 2 Ⅴ 使用例 2 < 本品以外に必要な試薬 機器など> 2 1) 磁気ビーズと一次抗体の反応 3 2)-1 細胞の調製
よる感染症は これまでは多くの有効な抗菌薬がありましたが ESBL 産生菌による場合はカルバペネム系薬でないと治療困難という状況になっています CLSI 標準法さて このような薬剤耐性菌を患者検体から検出するには 微生物検査という臨床検査が不可欠です 微生物検査は 患者検体から感染症の原因となる起炎
 2014 年 7 月 9 日放送 薬剤耐性菌の動向と最近の CLSI 標準法の変更点 順天堂大学 臨床検査部係長 三澤 成毅 薬剤耐性菌の動向まず 薬剤耐性菌の動向についてお話しします 薬剤耐性菌の歴史は 1940 年代に抗菌薬の第一号としてペニシリンが臨床応用された頃から始まったと言えます 以来 新しい抗菌薬の開発 導入と これに対する薬剤耐性菌の出現が繰り返され 今日に至っています 薬剤耐性菌の近年の特徴は
2014 年 7 月 9 日放送 薬剤耐性菌の動向と最近の CLSI 標準法の変更点 順天堂大学 臨床検査部係長 三澤 成毅 薬剤耐性菌の動向まず 薬剤耐性菌の動向についてお話しします 薬剤耐性菌の歴史は 1940 年代に抗菌薬の第一号としてペニシリンが臨床応用された頃から始まったと言えます 以来 新しい抗菌薬の開発 導入と これに対する薬剤耐性菌の出現が繰り返され 今日に至っています 薬剤耐性菌の近年の特徴は
PanaceaGel ゲル内細胞の観察 解析方法 1. ゲル内細胞の免疫染色 蛍光観察の方法 以下の 1-1, 1-2 に関して ゲルをスパーテルなどで取り出す際は 4% パラホルムアルデヒドで固定してから行うとゲルを比較的簡単に ( 壊さずに ) 取り出すことが可能です セルカルチャーインサートを
 1. ゲル内細胞の免疫染色 蛍光観察の方法 以下の 1-1, 1-2 に関して ゲルをスパーテルなどで取り出す際は 4% パラホルムアルデヒドで固定してから行うとゲルを比較的簡単に ( 壊さずに ) 取り出すことが可能です セルカルチャーインサートを用いた培養ではインサート底面をメス等で切り取ることで またウェルプレートを用いた培養ではピペットの水流でゲル ( 固定後 ) を底面から浮かすことで 回収しやすくなります
1. ゲル内細胞の免疫染色 蛍光観察の方法 以下の 1-1, 1-2 に関して ゲルをスパーテルなどで取り出す際は 4% パラホルムアルデヒドで固定してから行うとゲルを比較的簡単に ( 壊さずに ) 取り出すことが可能です セルカルチャーインサートを用いた培養ではインサート底面をメス等で切り取ることで またウェルプレートを用いた培養ではピペットの水流でゲル ( 固定後 ) を底面から浮かすことで 回収しやすくなります
31608 要旨 ルミノール発光 3513 後藤唯花 3612 熊﨑なつみ 3617 新野彩乃 3619 鈴木梨那 私たちは ルミノール反応で起こる化学発光が強い光で長時間続く条件について興味をもち 研究を行った まず触媒の濃度に着目し 1~9% の値で実験を行ったところ触媒濃度が低いほど強い光で長
 31608 要旨 ルミノール発光 3513 後藤唯花 3612 熊﨑なつみ 3617 新野彩乃 3619 鈴木梨那 私たちは ルミノール反応で起こる化学発光が強い光で長時間続く条件について興味をもち 研究を行った まず触媒の濃度に着目し 1~9% の値で実験を行ったところ触媒濃度が低いほど強い光で長時間発光した 次にルミノール溶液の液温に着目し 0 ~60 にて実験を行ったところ 温度が低いほど強く発光した
31608 要旨 ルミノール発光 3513 後藤唯花 3612 熊﨑なつみ 3617 新野彩乃 3619 鈴木梨那 私たちは ルミノール反応で起こる化学発光が強い光で長時間続く条件について興味をもち 研究を行った まず触媒の濃度に着目し 1~9% の値で実験を行ったところ触媒濃度が低いほど強い光で長時間発光した 次にルミノール溶液の液温に着目し 0 ~60 にて実験を行ったところ 温度が低いほど強く発光した
無細胞タンパク質合成試薬キット Transdirect insect cell
 発現プラスミドの構築 1. インサート DNA の調製開始コドンは出来るだけ 5'UTR に近い位置に挿入して下さい 経験的に ptd1 の EcoRV/KpnI サイトへのライゲーション効率が最も高いことを確認しています 本プロトコルに従うと インサートサイズにも依りますが 90% 以上のコロニーがインサートの挿入されたクローンとして得られます 可能な限り EcoRV/KpnI サイトへ挿入されるお奨めします
発現プラスミドの構築 1. インサート DNA の調製開始コドンは出来るだけ 5'UTR に近い位置に挿入して下さい 経験的に ptd1 の EcoRV/KpnI サイトへのライゲーション効率が最も高いことを確認しています 本プロトコルに従うと インサートサイズにも依りますが 90% 以上のコロニーがインサートの挿入されたクローンとして得られます 可能な限り EcoRV/KpnI サイトへ挿入されるお奨めします
鳥インフルエンザA(H7N9)ウイルス検出マニュアル(第2版)公開用
 鳥インフルエンザ A(H7N9) ウイルス 検出マニュアル ( 第 2 版 ) 1 目次 1 臨床検体またはウイルス培養液からの RNA の抽出 ( 参考 ) ---------- 3 2 リアルタイム RT-PCR(TaqMan Probe 法 ) による鳥インフルエンザ A(H7N9) ウイルスの検出方法 ---------- 4 3 Conventional RT-PCR 法よる鳥インフルエンザ
鳥インフルエンザ A(H7N9) ウイルス 検出マニュアル ( 第 2 版 ) 1 目次 1 臨床検体またはウイルス培養液からの RNA の抽出 ( 参考 ) ---------- 3 2 リアルタイム RT-PCR(TaqMan Probe 法 ) による鳥インフルエンザ A(H7N9) ウイルスの検出方法 ---------- 4 3 Conventional RT-PCR 法よる鳥インフルエンザ
Cytotoxicity LDH Assay Kit-WST
 ytotoxicity L ssay Kit-WST はじめに 本説明書は ytotoxicity L ssay Kit-WST を用いた抗体依存性細胞傷害測定用 (ntibody-dependent cellmediated cytotoxicity: ) です 本製品のキット内容や Working Solution の調製方法に関して 製品添付の取扱い説明書も合わせてご覧ください 正確な測定のために
ytotoxicity L ssay Kit-WST はじめに 本説明書は ytotoxicity L ssay Kit-WST を用いた抗体依存性細胞傷害測定用 (ntibody-dependent cellmediated cytotoxicity: ) です 本製品のキット内容や Working Solution の調製方法に関して 製品添付の取扱い説明書も合わせてご覧ください 正確な測定のために
2017 年 8 月 9 日放送 結核診療における QFT-3G と T-SPOT 日本赤十字社長崎原爆諫早病院副院長福島喜代康はじめに 2015 年の本邦の新登録結核患者は 18,820 人で 前年より 1,335 人減少しました 新登録結核患者数も人口 10 万対 14.4 と減少傾向にあります
 2017 年 8 月 9 日放送 結核診療における QFT-3G と T-SPOT 日本赤十字社長崎原爆諫早病院副院長福島喜代康はじめに 2015 年の本邦の新登録結核患者は 18,820 人で 前年より 1,335 人減少しました 新登録結核患者数も人口 10 万対 14.4 と減少傾向にありますが 本邦の結核では高齢者結核が多いのが特徴です 結核診療における主な検査法を示します ( 図 1) 従来の細菌学的な抗酸菌の塗抹
2017 年 8 月 9 日放送 結核診療における QFT-3G と T-SPOT 日本赤十字社長崎原爆諫早病院副院長福島喜代康はじめに 2015 年の本邦の新登録結核患者は 18,820 人で 前年より 1,335 人減少しました 新登録結核患者数も人口 10 万対 14.4 と減少傾向にありますが 本邦の結核では高齢者結核が多いのが特徴です 結核診療における主な検査法を示します ( 図 1) 従来の細菌学的な抗酸菌の塗抹
検体採取 患者の検査前準備 検体採取のタイミング 5. 免疫学的検査 >> 5G. 自己免疫関連検査 >> 5G010. 記号 添加物 ( キャップ色等 ) 採取材料 採取量 測定材料 F 凝固促進剤 + 血清分離剤 ( 青 細 ) 血液 3 ml 血清 H 凝固促進剤 + 血清分離剤 ( ピンク
 5. 免疫学的検査 >> 5G. 自己免疫関連検査 >> 5G010. anti nuclear antibody 連絡先 : 3764 基本情報 分析物 5G010 JLAC10 診療報酬 識別材料 023 血清 測定法 162 蛍光抗体法 (FAT) 結果識別 第 2 章 特掲診療料 D014 5 抗核抗体 ( 蛍光抗体法 ) 半定量 105 点 第 3 部 検査 第 1 節 検体検査料 第 1
5. 免疫学的検査 >> 5G. 自己免疫関連検査 >> 5G010. anti nuclear antibody 連絡先 : 3764 基本情報 分析物 5G010 JLAC10 診療報酬 識別材料 023 血清 測定法 162 蛍光抗体法 (FAT) 結果識別 第 2 章 特掲診療料 D014 5 抗核抗体 ( 蛍光抗体法 ) 半定量 105 点 第 3 部 検査 第 1 節 検体検査料 第 1
Bacterial 16S rDNA PCR Kit
 研究用 Bacterial 16S rdna PCR Kit 説明書 v201307da 微生物の同定は 形態的特徴 生理 生化学的性状 化学分類学的性状などを利用して行われますが これらの方法では同定までに時間を要します また 同定が困難な場合や正しい結果が得られない場合もあります 近年 微生物同定にも分子生物学を利用した方法が採用されるようになり 微生物の持つ DNA を対象として解析を行う方法が活用されています
研究用 Bacterial 16S rdna PCR Kit 説明書 v201307da 微生物の同定は 形態的特徴 生理 生化学的性状 化学分類学的性状などを利用して行われますが これらの方法では同定までに時間を要します また 同定が困難な場合や正しい結果が得られない場合もあります 近年 微生物同定にも分子生物学を利用した方法が採用されるようになり 微生物の持つ DNA を対象として解析を行う方法が活用されています
本日の内容 HbA1c 測定方法別原理と特徴 HPLC 法 免疫法 酵素法 原理差による測定値の乖離要因
 HbA1c 測定系について ~ 原理と特徴 ~ 一般社団法人日本臨床検査薬協会 技術運営委員会副委員長 安部正義 本日の内容 HbA1c 測定方法別原理と特徴 HPLC 法 免疫法 酵素法 原理差による測定値の乖離要因 HPLC 法 HPLC 法原理 高速液体クロマトグラフィー 混合物の分析法の一つ 固体または液体の固定相 ( 吸着剤 ) 中で 液体または気体の移動相 ( 展開剤 ) に試料を加えて移動させ
HbA1c 測定系について ~ 原理と特徴 ~ 一般社団法人日本臨床検査薬協会 技術運営委員会副委員長 安部正義 本日の内容 HbA1c 測定方法別原理と特徴 HPLC 法 免疫法 酵素法 原理差による測定値の乖離要因 HPLC 法 HPLC 法原理 高速液体クロマトグラフィー 混合物の分析法の一つ 固体または液体の固定相 ( 吸着剤 ) 中で 液体または気体の移動相 ( 展開剤 ) に試料を加えて移動させ
緑膿菌 Pseudomonas aeruginosa グラム陰性桿菌 ブドウ糖非発酵 緑色色素産生 水まわりなど生活環境中に広く常在 腸内に常在する人も30%くらい ペニシリンやセファゾリンなどの第一世代セフェム 薬に自然耐性 テトラサイクリン系やマクロライド系抗生物質など の抗菌薬にも耐性を示す傾
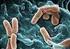 2 緑膿菌 Pseudomonas aeruginosa グラム陰性桿菌 ブドウ糖非発酵 緑色色素産生 水まわりなど生活環境中に広く常在 腸内に常在する人も30%くらい ペニシリンやセファゾリンなどの第一世代セフェム 薬に自然耐性 テトラサイクリン系やマクロライド系抗生物質など の抗菌薬にも耐性を示す傾向が強い 多剤耐性緑膿菌は5類感染症定点把握疾患 赤痢菌属 グラム陰性通性嫌気性桿菌 腸内細菌科
2 緑膿菌 Pseudomonas aeruginosa グラム陰性桿菌 ブドウ糖非発酵 緑色色素産生 水まわりなど生活環境中に広く常在 腸内に常在する人も30%くらい ペニシリンやセファゾリンなどの第一世代セフェム 薬に自然耐性 テトラサイクリン系やマクロライド系抗生物質など の抗菌薬にも耐性を示す傾向が強い 多剤耐性緑膿菌は5類感染症定点把握疾患 赤痢菌属 グラム陰性通性嫌気性桿菌 腸内細菌科
リアルタイムPCRの基礎知識
 1. リアルタイム PCR の用途リアルタイム PCR 法は 遺伝子発現解析の他に SNPs タイピング 遺伝子組み換え食品の検査 ウイルスや病原菌の検出 導入遺伝子のコピー数の解析などさまざまな用途に応用されている 遺伝子発現解析のような定量解析は まさにリアルタイム PCR の得意とするところであるが プラス / マイナス判定だけの定性的な解析にもその威力を発揮する これは リアルタイム PCR
1. リアルタイム PCR の用途リアルタイム PCR 法は 遺伝子発現解析の他に SNPs タイピング 遺伝子組み換え食品の検査 ウイルスや病原菌の検出 導入遺伝子のコピー数の解析などさまざまな用途に応用されている 遺伝子発現解析のような定量解析は まさにリアルタイム PCR の得意とするところであるが プラス / マイナス判定だけの定性的な解析にもその威力を発揮する これは リアルタイム PCR
pdf0_1ページ目
 平成 年 月 日 担 当 課 衛生環境研究所 ( 担当者 ) ( 高田 梁川 ) 電話 -- 鳥取県感染症流行情報 第 [ 平成 年 月 7 日 ( 月 ) ~ 月 日 ( 日 祝 ) ] 疾 病 名 東 部 中 部 西 部 イ ン フ ル エ ン ザ 〇 感 染 性 胃 腸 炎 〇 〇 〇 水 痘 ( 水 ぼ う そ う ) 流行性耳下腺炎 ( おたふくかぜ ) 手 足 口 病 〇 〇 〇 ヘ ル
平成 年 月 日 担 当 課 衛生環境研究所 ( 担当者 ) ( 高田 梁川 ) 電話 -- 鳥取県感染症流行情報 第 [ 平成 年 月 7 日 ( 月 ) ~ 月 日 ( 日 祝 ) ] 疾 病 名 東 部 中 部 西 部 イ ン フ ル エ ン ザ 〇 感 染 性 胃 腸 炎 〇 〇 〇 水 痘 ( 水 ぼ う そ う ) 流行性耳下腺炎 ( おたふくかぜ ) 手 足 口 病 〇 〇 〇 ヘ ル
培養細胞からの Total RNA 抽出の手順 接着細胞のプロトコル 1. プレート ( またはウエル ) より培地を除き PBSでの洗浄を行う 2. トリプシン処理を行い 全量を1.5ml 遠心チューブに移す スクレイパーを使って 細胞を掻き集める方法も有用です 3. 低速遠心 ( 例 300 g
 Maxwell RSC simplyrna Cells / Tissue Kit ( カタログ番号 AS1340/AS1390) 簡易マニュアル 注意 : キットを受け取りましたら 1-Thioglycerolを取り出し キット箱は室温で保存してください 取り出した1-Thioglycerolは2~10 で保存してください ご用意いただくもの 細胞 組織の両方の場合で共通 ボルテックスミキサー ピペットマン
Maxwell RSC simplyrna Cells / Tissue Kit ( カタログ番号 AS1340/AS1390) 簡易マニュアル 注意 : キットを受け取りましたら 1-Thioglycerolを取り出し キット箱は室温で保存してください 取り出した1-Thioglycerolは2~10 で保存してください ご用意いただくもの 細胞 組織の両方の場合で共通 ボルテックスミキサー ピペットマン
研究成果報告書
 様式 C-19 科学研究費補助金研究成果報告書 平成 21 年 5 月 13 日現在 研究種目 : 若手研究 (B) 研究期間 :2007~2008 課題番号 :19791396 研究課題名 ( 和文 ) デンタルユニット給水系バイオフィルムの実験モデルの確立と関連遺伝子の解析研究課題名 ( 英文 ) Establishment of in vitro biofilm model and analysis
様式 C-19 科学研究費補助金研究成果報告書 平成 21 年 5 月 13 日現在 研究種目 : 若手研究 (B) 研究期間 :2007~2008 課題番号 :19791396 研究課題名 ( 和文 ) デンタルユニット給水系バイオフィルムの実験モデルの確立と関連遺伝子の解析研究課題名 ( 英文 ) Establishment of in vitro biofilm model and analysis
PrimeSTAR® Mutagenesis Basal Kit
 PrimeSTAR Mutagenesis Basal Kit 説明書 v201107da 目次 I. キットの内容...3 II. 保存...3 III. 本システムの原理...3 IV. プライマー設計について...5 V. 操作...8 VI. 実験例...10 VII. トラブルシューティング...13 VIII. 関連製品...13 IX. 注意...13 2 PrimeSTAR Mutagenesis
PrimeSTAR Mutagenesis Basal Kit 説明書 v201107da 目次 I. キットの内容...3 II. 保存...3 III. 本システムの原理...3 IV. プライマー設計について...5 V. 操作...8 VI. 実験例...10 VII. トラブルシューティング...13 VIII. 関連製品...13 IX. 注意...13 2 PrimeSTAR Mutagenesis
目 次 1. はじめに 1 2. 組成および性状 2 3. 効能 効果 2 4. 特徴 2 5. 使用方法 2 6. 即時効果 持続効果および累積効果 3 7. 抗菌スペクトル 5 サラヤ株式会社スクラビイン S4% 液製品情報 2/ PDF
 サラヤ株式会社スクラビイン S4% 液製品情報 1/8 52-0198-01-4PDF 目 次 1. はじめに 1 2. 組成および性状 2 3. 効能 効果 2 4. 特徴 2 5. 使用方法 2 6. 即時効果 持続効果および累積効果 3 7. 抗菌スペクトル 5 サラヤ株式会社スクラビイン S4% 液製品情報 2/8 52-0198-01-4PDF 1. はじめに 医療関連感染の原因となる微生物の多くは
サラヤ株式会社スクラビイン S4% 液製品情報 1/8 52-0198-01-4PDF 目 次 1. はじめに 1 2. 組成および性状 2 3. 効能 効果 2 4. 特徴 2 5. 使用方法 2 6. 即時効果 持続効果および累積効果 3 7. 抗菌スペクトル 5 サラヤ株式会社スクラビイン S4% 液製品情報 2/8 52-0198-01-4PDF 1. はじめに 医療関連感染の原因となる微生物の多くは
Western BLoT Rapid Detect
 研究用 Western BLoT Rapid Detect 説明書 v201212 Western BLoT Rapid Detect は 標識二次抗体の代わりに独自の IgG Detector(HRP labeled) を利用して一次抗体を検出するウェスタンブロッティング専用の検出試薬キットです 本製品を利用することで 標識二次抗体を用いて検出する従来法ではできなかった迅速検出 高感度検出 シグナルの増強
研究用 Western BLoT Rapid Detect 説明書 v201212 Western BLoT Rapid Detect は 標識二次抗体の代わりに独自の IgG Detector(HRP labeled) を利用して一次抗体を検出するウェスタンブロッティング専用の検出試薬キットです 本製品を利用することで 標識二次抗体を用いて検出する従来法ではできなかった迅速検出 高感度検出 シグナルの増強
テイカ製薬株式会社 社内資料
 テイカ製薬株式会社社内資料 アレルギー性結膜炎治療剤トラニラスト点眼液.5% TS TRANILAST Ophthalmic Solution.5% TS 生物学的同等性に関する資料 発売元 : 興和株式会社 製造販売元 : テイカ製薬株式会社 9 年 月作成 TSTR5BE9 ラット及びモルモットアレルギー性結膜炎モデルにおける生物学的同等性試験 Ⅰ. 試験の目的トラニラスト点眼液.5% TS および標準製剤の生物学的同等性をラット受動感作アレルギー性結膜炎モデル及びモルモット能動感作アレルギー性結膜炎モデルを用い薬力学的に検討した
テイカ製薬株式会社社内資料 アレルギー性結膜炎治療剤トラニラスト点眼液.5% TS TRANILAST Ophthalmic Solution.5% TS 生物学的同等性に関する資料 発売元 : 興和株式会社 製造販売元 : テイカ製薬株式会社 9 年 月作成 TSTR5BE9 ラット及びモルモットアレルギー性結膜炎モデルにおける生物学的同等性試験 Ⅰ. 試験の目的トラニラスト点眼液.5% TS および標準製剤の生物学的同等性をラット受動感作アレルギー性結膜炎モデル及びモルモット能動感作アレルギー性結膜炎モデルを用い薬力学的に検討した
Title
 不規則抗体検査の解説 福島県立総合衛生学院 教務部臨床検査学科 安田広康 SLIDE 1 不規則抗体同定のプロセス (1) 不規則抗体スクリーニング (Sc) 可能性の高い抗体の推定 * 否定できない抗体の推定反応態度 *1 消去法 * - 日臨技 輸血 移植検査技術教本 - *1 陽性の Sc 赤血球 1) 反応パターン ) 反応温度 ) 凝集の強さ * 陰性の Sc 赤血球 1) 量的効果 *
不規則抗体検査の解説 福島県立総合衛生学院 教務部臨床検査学科 安田広康 SLIDE 1 不規則抗体同定のプロセス (1) 不規則抗体スクリーニング (Sc) 可能性の高い抗体の推定 * 否定できない抗体の推定反応態度 *1 消去法 * - 日臨技 輸血 移植検査技術教本 - *1 陽性の Sc 赤血球 1) 反応パターン ) 反応温度 ) 凝集の強さ * 陰性の Sc 赤血球 1) 量的効果 *
MLPA 法 Q&A 集
 MLPA 法 Q&A 集 目次 1. MLPA 法の導入 Q1. 導入にあたり 何が必要になりますか? Q2. 実験にはどのようなサンプルが必要でしょうか? Q3. サンプルDNAはどれくらい用意すれば良いですか? Q4. キャピラリーシーケンサが自施設に無い場合でも実験はできますか? Q5. FFPE 検体でも実験はできますか? 2. 実験のセットアップ Q1. 実験において重要なポイントはありますか?
MLPA 法 Q&A 集 目次 1. MLPA 法の導入 Q1. 導入にあたり 何が必要になりますか? Q2. 実験にはどのようなサンプルが必要でしょうか? Q3. サンプルDNAはどれくらい用意すれば良いですか? Q4. キャピラリーシーケンサが自施設に無い場合でも実験はできますか? Q5. FFPE 検体でも実験はできますか? 2. 実験のセットアップ Q1. 実験において重要なポイントはありますか?
手順 ) 1) プライマーの設計 発注変異導入部位がプライマーのほぼ中央になるようにする 可能であれば 制限酵素サイトができるようにすると確認が容易になる プライマーは 25-45mer で TM 値が 78 以上になるようにする Tm= (%GC)-675/N-%mismatch
 Mutagenesis 目的 ) 既存の遺伝子に PCR を利用して変異を導入する 1 点変異導入方法 ) Quik Change Site-Directed Mutagenesis Kit(Stratagene) のプロトコールを流用 http://www.stratagene.com/products/showproduct.aspx?pid=131 Kit 中では DNA polymerase
Mutagenesis 目的 ) 既存の遺伝子に PCR を利用して変異を導入する 1 点変異導入方法 ) Quik Change Site-Directed Mutagenesis Kit(Stratagene) のプロトコールを流用 http://www.stratagene.com/products/showproduct.aspx?pid=131 Kit 中では DNA polymerase
2017 年 2 月 27 日 Myco Finder バリデーションデータ 日水製薬株式会社 研究部
 2017 年 2 月 27 日 Myco Finder バリデーションデータ 日水製薬株式会社 研究部 1. 概要 マイコプラズマ遺伝子検出キット (Myco Finder) の性能を評価するために 下記ふたつの情報を参 考にバリデーションデータを取得した 1. 第十七改正日本薬局方 ( 平成 28 年 3 月 7 日厚生労働省告示 64 号 ) 参考情報 バイオテクノロジー応用医薬品 / 生物起源由来医薬品の製造に用いる細胞基材に対するマイコ
2017 年 2 月 27 日 Myco Finder バリデーションデータ 日水製薬株式会社 研究部 1. 概要 マイコプラズマ遺伝子検出キット (Myco Finder) の性能を評価するために 下記ふたつの情報を参 考にバリデーションデータを取得した 1. 第十七改正日本薬局方 ( 平成 28 年 3 月 7 日厚生労働省告示 64 号 ) 参考情報 バイオテクノロジー応用医薬品 / 生物起源由来医薬品の製造に用いる細胞基材に対するマイコ
Gen とるくん™(酵母用)High Recovery
 研究用 Gen とるくん ( 酵母用 ) High Recovery 説明書 v201510da Gen とるくん ( 酵母用 )High Recovery は 細胞壁分解酵素による酵母菌体処理と塩析による DNA 精製の組み合わせにより 効率良く酵母ゲノム DNA を抽出 精製するためのキットです 本キットを用いた酵母ゲノム DNA 調製操作は 遠心による酵母菌体の回収 GenTLE Yeast
研究用 Gen とるくん ( 酵母用 ) High Recovery 説明書 v201510da Gen とるくん ( 酵母用 )High Recovery は 細胞壁分解酵素による酵母菌体処理と塩析による DNA 精製の組み合わせにより 効率良く酵母ゲノム DNA を抽出 精製するためのキットです 本キットを用いた酵母ゲノム DNA 調製操作は 遠心による酵母菌体の回収 GenTLE Yeast
5
 QCWS 参考プロトコル 抗 HLA 抗体検査 (ICFA) 2019 年度版 作成者日本組織適合性学会認定制度委員会ワーキンググループ抗 HLA 抗体 WG 制定 改訂履歴 版数 制定日 施行日 制定理由 作成責任者 初版 日本組織適合性学会が開催する QCWS での HLA 検査を実施する際に用いる QCWS 参考プロトコルとして制定した WG 版数 改訂日 施行日 改訂理由 改訂内容 改訂責任者
QCWS 参考プロトコル 抗 HLA 抗体検査 (ICFA) 2019 年度版 作成者日本組織適合性学会認定制度委員会ワーキンググループ抗 HLA 抗体 WG 制定 改訂履歴 版数 制定日 施行日 制定理由 作成責任者 初版 日本組織適合性学会が開催する QCWS での HLA 検査を実施する際に用いる QCWS 参考プロトコルとして制定した WG 版数 改訂日 施行日 改訂理由 改訂内容 改訂責任者
1 2
 1 2 ECO 3 4 5 6 7 8 全てのゾーンには 新規納入からメンテナンスに至るまで お客様をサポートします 抗菌が要求されます 一般清潔区域 病院内全てのゾーンで生活環境を汚染する菌類からの汚染防止対策として 抗菌フィルター をお勧めします 高度清潔区域 清 潔 区 域 準清潔区域 ① 細菌類 ② 真菌類 酵母類 製 作 ご 提 案 銀 ゼ オライトの 抗 菌 抗 カ ビ の メ カ ニ
1 2 ECO 3 4 5 6 7 8 全てのゾーンには 新規納入からメンテナンスに至るまで お客様をサポートします 抗菌が要求されます 一般清潔区域 病院内全てのゾーンで生活環境を汚染する菌類からの汚染防止対策として 抗菌フィルター をお勧めします 高度清潔区域 清 潔 区 域 準清潔区域 ① 細菌類 ② 真菌類 酵母類 製 作 ご 提 案 銀 ゼ オライトの 抗 菌 抗 カ ビ の メ カ ニ
埼玉県調査研究成績報告書 ( 家畜保健衛生業績発表集録 ) 第 55 報 ( 平成 25 年度 ) 11 牛呼吸器病由来 Mannheimia haemolytica 株の性状調査 および同定法に関する一考察 中央家畜保健衛生所 荒井理恵 Ⅰ はじめに Mannheimia haemolytica
 11 牛呼吸器病由来 Mannheimia haemolytica 株の性状調査 および同定法に関する一考察 中央家畜保健衛生所 荒井理恵 Ⅰ はじめに Mannheimia haemolytica は牛呼吸器病の主要な原因菌であり 時に成牛の死亡も引き起こすことから重要視される病原体である 本菌はパスツレラ科に属するグラム陰性短桿菌であり 莢膜の抗原性により 現在 12 種類の血清型に分類されている
11 牛呼吸器病由来 Mannheimia haemolytica 株の性状調査 および同定法に関する一考察 中央家畜保健衛生所 荒井理恵 Ⅰ はじめに Mannheimia haemolytica は牛呼吸器病の主要な原因菌であり 時に成牛の死亡も引き起こすことから重要視される病原体である 本菌はパスツレラ科に属するグラム陰性短桿菌であり 莢膜の抗原性により 現在 12 種類の血清型に分類されている
検査項目情報 水痘. 帯状ヘルペスウイルス抗体 IgG [EIA] [ 髄液 ] varicella-zoster virus, viral antibody IgG 連絡先 : 3764 基本情報 ( 標準コード (JLAC10) ) 基本情報 ( 診療報酬 ) 標準コード (JLAC10) 5F
![検査項目情報 水痘. 帯状ヘルペスウイルス抗体 IgG [EIA] [ 髄液 ] varicella-zoster virus, viral antibody IgG 連絡先 : 3764 基本情報 ( 標準コード (JLAC10) ) 基本情報 ( 診療報酬 ) 標準コード (JLAC10) 5F 検査項目情報 水痘. 帯状ヘルペスウイルス抗体 IgG [EIA] [ 髄液 ] varicella-zoster virus, viral antibody IgG 連絡先 : 3764 基本情報 ( 標準コード (JLAC10) ) 基本情報 ( 診療報酬 ) 標準コード (JLAC10) 5F](/thumbs/99/142875588.jpg) varicella-zoster virus, viral antibody IgG 連絡先 : 3764 基本情報 ( 標準コード (JLAC10) ) 基本情報 ( 診療報酬 ) 標準コード (JLAC10) 5F193 分析物 水痘. 帯状ヘルペスウイルス 診療報酬 特掲診療料 >> 検査 >> 検体検査料 >> 検体検査実施料 >> ( 免疫学的検査 ) D012 D012 38 381 グロブリンクラス別ウイルス抗体価
varicella-zoster virus, viral antibody IgG 連絡先 : 3764 基本情報 ( 標準コード (JLAC10) ) 基本情報 ( 診療報酬 ) 標準コード (JLAC10) 5F193 分析物 水痘. 帯状ヘルペスウイルス 診療報酬 特掲診療料 >> 検査 >> 検体検査料 >> 検体検査実施料 >> ( 免疫学的検査 ) D012 D012 38 381 グロブリンクラス別ウイルス抗体価
(Microsoft Word - \202\205\202\2232-1HP.doc)
 イーズ NO.002(15 年 8 月発行 ) 日本薬局方 微生物限度試験法微生物限度試験法の実際 監修 : 国立衛生試験所三瀬勝利 前号では微生物限度試験法について 全体的な解説を行ったが 本号では生菌数試験 大腸菌 サルモネラ 緑膿菌 黄色ブドウ球菌の試験項目ごとに それぞれ実際の試験の流れを図解してみた 試験を行う際に役立てて頂ければ幸いである また無菌試験法についても補冊として添付したので参照されたい
イーズ NO.002(15 年 8 月発行 ) 日本薬局方 微生物限度試験法微生物限度試験法の実際 監修 : 国立衛生試験所三瀬勝利 前号では微生物限度試験法について 全体的な解説を行ったが 本号では生菌数試験 大腸菌 サルモネラ 緑膿菌 黄色ブドウ球菌の試験項目ごとに それぞれ実際の試験の流れを図解してみた 試験を行う際に役立てて頂ければ幸いである また無菌試験法についても補冊として添付したので参照されたい
MightyAmp™ DNA Polymerase Ver.3
 研究用 MightyAmp DNA Polymerase Ver.3 説明書 v201805da MightyAmp DNA Polymerase は 究極の反応性を追求して開発された PCR 酵素であり 通常の PCR 酵素では増幅が困難な PCR 阻害物質を多く含むクルードな生体粗抽出液を用いる場合にも その強力な増幅能により良好な反応性を示します MightyAmp DNA Polymerase
研究用 MightyAmp DNA Polymerase Ver.3 説明書 v201805da MightyAmp DNA Polymerase は 究極の反応性を追求して開発された PCR 酵素であり 通常の PCR 酵素では増幅が困難な PCR 阻害物質を多く含むクルードな生体粗抽出液を用いる場合にも その強力な増幅能により良好な反応性を示します MightyAmp DNA Polymerase
検体採取 患者の検査前準備 検体採取のタイミング 記号 添加物 ( キャップ色等 ) 採取材料 採取量 測定材料 F 凝固促進剤 + 血清分離剤 ( 青 細 ) 血液 3 ml 血清 H 凝固促進剤 + 血清分離剤 ( ピンク ) 血液 6 ml 血清 I 凝固促進剤 + 血清分離剤 ( 茶色 )
 toxoplasma gondii antibody-igg 連絡先 : 3764 基本情報 分析物 5E156 JLAC10 診療報酬 識別材料 023 血清 測定法 052 化学 生物発光イムノアッセイ (CLEIA) 結果識別 第 2 章 特掲診療料 D012 14 トキソプラズマ抗体 第 3 部 検査 第 1 節 検体検査料 第 1 款 検体検査実施料 ( 免疫学的検査 ) 93 点 加算等
toxoplasma gondii antibody-igg 連絡先 : 3764 基本情報 分析物 5E156 JLAC10 診療報酬 識別材料 023 血清 測定法 052 化学 生物発光イムノアッセイ (CLEIA) 結果識別 第 2 章 特掲診療料 D012 14 トキソプラズマ抗体 第 3 部 検査 第 1 節 検体検査料 第 1 款 検体検査実施料 ( 免疫学的検査 ) 93 点 加算等
Pyrobest ® DNA Polymerase
 Pyrobest DNA Polymerase 説明書 v201102da 対活Pyrobest DNA Polymerase は Pyrococcus sp. 由来の 3' 5' exonuclease 活性 (proof reading 活性 ) を有する耐熱性 α 型 DNA ポリメラーゼです α 型 DNA ポリメラーゼは Pol I 型ポリメラーゼ (Taq DNA ポリメラーゼなど )
Pyrobest DNA Polymerase 説明書 v201102da 対活Pyrobest DNA Polymerase は Pyrococcus sp. 由来の 3' 5' exonuclease 活性 (proof reading 活性 ) を有する耐熱性 α 型 DNA ポリメラーゼです α 型 DNA ポリメラーゼは Pol I 型ポリメラーゼ (Taq DNA ポリメラーゼなど )
Microsoft Word - 届出基準
 第 4 三類感染症 1 コレラ (1) 定義コレラ毒素 (CT) 産生性コレラ菌 (Vibrio cholerae O1) 又は V. cholerae O139 による急性感染性腸炎である (2) 臨床的特徴潜伏期間は数時間から 5 日 通常 1 日前後である 近年のエルトールコレラは軽症の水様性下痢や軟で経過することが多いが まれに 米のとぎ汁 様の臭のない水様を 1 日数リットルから数十リットルも排泄し
第 4 三類感染症 1 コレラ (1) 定義コレラ毒素 (CT) 産生性コレラ菌 (Vibrio cholerae O1) 又は V. cholerae O139 による急性感染性腸炎である (2) 臨床的特徴潜伏期間は数時間から 5 日 通常 1 日前後である 近年のエルトールコレラは軽症の水様性下痢や軟で経過することが多いが まれに 米のとぎ汁 様の臭のない水様を 1 日数リットルから数十リットルも排泄し
