Microsoft Word - ランソプラゾール.doc
|
|
|
- ほのか みょうだに
- 9 years ago
- Views:
Transcription
1 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意改訂のお知らせ 平成 23 年 5 月 処方せん医薬品処方せん医薬品処方せん医薬品処方せん医薬品 プロトンポンプ インヒビターランソラールカプセル 15 ランソラールカプセル 30 ランソプラゾールカプセルランソプラゾール OD 錠 15mg 日医工 ランソプラゾール OD 錠 30mg 日医工 ランソプラゾール口腔内崩壊錠製造販売元日医工株式会社富山市総曲輪 1 丁目 6 番 21 この度上記製品につきまして 使用上の注意 の一部を改訂 ( 下線部分 ) いたしましたので, お知らせ申し上げます なお, 改訂添付文書を封入した製品がお手元に届くまでには若干の日数が必要ですので, 今後のご使用に際しましては下記内容をご高覧くださいますようお願い申し上げます < 改訂内容 > ( : 自主改訂 ) ランソラールカプセル 15/ ランソラールカプセル 30 改訂後 現 行 (: 現行どおり (2) その他の副作用胃潰瘍, 十二指腸潰瘍, 吻合部潰瘍, 逆流性食道炎,Zollinger-Ellison 症候群, 非びらん性胃食道逆流症の場合頻度不明 過敏症注発疹, そう痒, 多形紅斑 炎, 舌炎, 大腸炎 (collagenous colitis 等注を含む ) その他発熱, 総コレステロール上昇, 尿酸上昇, 女性 化乳房注, 浮腫, 倦怠感, 舌 口唇のしびれ感, 四肢のしびれ感, 筋肉痛, 脱毛, かすみ目, 脱力感, 関節痛, 低ナトリウム血症注 1: このような場合には投与を中止すること 注 3: 下痢が継続する場合,collagenous colitis 等が発現している可能性があるため, 速やかに本剤の投与を中止すること 腸管粘膜に縦走潰瘍, びらん, 易出血等の異常を認めることがあるので, 下血, 血便が認められる場合には, 適切な処置を行うこと ヘリコバクター ピロリの除菌の補助の場合 : 現行どおり (: 略 (2) その他の副作用胃潰瘍, 十二指腸潰瘍, 吻合部潰瘍, 逆流性食道炎,Zollinger-Ellison 症候群, 非びらん性胃食道逆流症の場合頻度不明 過敏症注発疹, そう痒 炎, 舌炎, 大腸炎注 その他発熱, 総コレステロール上昇, 尿酸上昇, 女性化乳房注, 浮腫, 倦怠感, 舌 口唇のしびれ感, 四肢のしびれ感, 筋肉痛, 脱毛, かすみ目, 脱力感, 関節痛注 1: このような場合には投与を中止すること 注 3: 下痢が継続する場合, 内視鏡検査では腸管粘膜に異常を認めないが, 組織学的に大腸粘膜下に膠原線維束の肥厚や炎症細胞の浸潤を伴う大腸炎が発現している可能性があるため, 速やかに本剤の投与を中止すること ヘリコバクター ピロリの除菌の補助の場合 : 略 1
2 改訂後現行 (~(7): 現行どおり (8) 海外における複数の観察研究で, プロトンポンプインヒビターによる治療において骨粗鬆症に伴う股関節骨折, 手関節骨折, 脊椎骨折のリスク増加が報告されている 特に, 高用量及び長期間 (1 年以上 ) の治療を受けた患者で, 骨折のリスクが増加した (~(7): 略 ランソプラゾール OD 錠 15mg/30mg 日医工 改訂後 現 行 (: 現行どおり (2) その他の副作用胃潰瘍, 十二指腸潰瘍, 吻合部潰瘍, 逆流性食道炎,Zollinger-Ellison 症候群の場合頻度不明 過敏症注発疹, そう痒, 多形紅斑 炎, 舌炎, 大腸炎 (collagenous colitis 等注を含む ) その他発熱, 総コレステロール上昇, 尿酸上昇, 女性化乳房注, 浮腫, 倦怠感, 舌 口唇のしびれ感, 四肢のしびれ感, 筋肉痛, 脱毛, かすみ目, 脱力感, 関節痛, 低ナトリウム血症注 1: このような場合には投与を中止すること 注 3: 下痢が継続する場合,collagenous colitis 等が発現している可能性があるため, 速やかに本剤の投与を中止すること 腸管粘膜に縦走潰瘍, びらん, 易出血等の異常を認めることがあるので, 下血, 血便が認められる場合には, 適切な処置を行うこと ヘリコバクター ピロリの除菌の補助の場合 : 現行どおり (: 略 (2) その他の副作用胃潰瘍, 十二指腸潰瘍, 吻合部潰瘍, 逆流性食道炎,Zollinger-Ellison 症候群の場合頻度不明 過敏症注発疹, そう痒 炎, 舌炎, 大腸炎注 その他発熱, 総コレステロール上昇, 尿酸上昇, 女性化乳房注, 浮腫, 倦怠感, 舌 口唇のしびれ感, 四肢のしびれ感, 筋肉痛, 脱毛, かすみ目, 脱力感, 関節痛注 1: このような場合には投与を中止すること 注 3: 下痢が継続する場合, 内視鏡検査では腸管粘膜に異常を認めないが, 組織学的に大腸粘膜下に膠原線維束の肥厚や炎症細胞の浸潤を伴う大腸炎が発現している可能性があるため, 速やかに本剤の投与を中止すること ヘリコバクター ピロリの除菌の補助の場合 : 略 (~(6): 現行どおり (7) 海外における複数の観察研究で, プロトンポンプインヒビターによる治療において骨粗鬆症に伴う股関節骨折, 手関節骨折, 脊椎骨折のリスク増加が報告されている 特に, 高用量及び長期間 (1 年以上 ) の治療を受けた患者で, 骨折のリスクが増加した (~(6): 略 * 改訂内容につきましては,DSU No.200(2011 年 6 月発行 ) に掲載の予定です < 改訂理由 > ランソプラゾール製剤との因果関係が否定できない副作用発現症例の集積により, その他の副作用 の項に 多形紅斑, 低ナトリウム血症 を追記いたしました 本剤投与中の collagenous colitis( 膠原性大腸炎 ) の発現については, 従来より その他の副作用 の 大腸炎 の記載により注意喚起を行って参りましたが, 注意すべき所見 症状を追記し, より一層の注意喚起を行うことといたしました 米国 FDA におけるプロトンポンプインヒビター使用に伴う骨折リスク増加に関する措置結果に基づき, 重大な基本的注意 の項に股関節, 手関節, 脊椎の骨折リスク増加の可能性について追記し, 注意喚起を行うことといたしました 2
3 < 改訂後の使用上の注意全文 > ランソラールカプセル 15 禁忌 ( 次の患者には投与しないこと ) 1. 本剤の成分に対する過敏症の既往歴のある患者 2. アタザナビル硫酸塩を投与中の患者 ( 相互作用 の項参照 ) < 効能 効果に関連する使用上の注意 > ヘリコバクター ピロリの除菌の補助の場合 1. 進行期胃 MALT リンパ腫に対するヘリコバクター ピロリ除菌治療の有効性は確立していない 2. 特発性血小板減少性紫斑病に対しては, ガイドライン等を参照し, ヘリコバクター ピロリ除菌治療が適切と判断される症例にのみ除菌治療を行うこと 3. 早期胃癌に対する内視鏡的治療後胃以外には, ヘリコバクター ピロリ除菌治療による胃癌の発症抑制に対する有効性は確立していない < 用法 用量に関連する使用上の注意 > 逆流性食道炎の維持療法において,1 日 1 回 30mg の投与は,1 日 1 回 15mg 投与中に再発した例など 15mg では効果が不十分な場合に限る 使用上の注意 1. 慎重投与 ( 次の患者には慎重に投与すること ) ( 薬物過敏症の既往歴のある患者 (2) 障害のある患者 [ 本剤の代謝, 排泄が遅延することがある ] ( 高齢者 ( 高齢者への投与 の項参照) 2. 重要な基本的注意 ( 治療にあたっては経過を十分に観察し, 病状に応じ治療上必要最小限の使用にとどめること (2) 胃潰瘍, 十二指腸潰瘍, 吻合部潰瘍に使用する場合は, 長期の使用経験は十分でないので, 維持療法には用いないことが望ましい ( 逆流性食道炎の維持療法については, 再発 再燃を繰り返す患者に対し投与することとし, 本来維持療法の必要のない患者に投与することのないよう留意すること また,1 日 1 回 30mg 又は 15mg の投与により寛解状態が長期にわたり継続する症例で, 減量又は投与中止により再発するおそれがないと判断される場合は 1 日 1 回 15mg に減量又は中止すること なお, 維持療法中は定期的に内視鏡検査を実施するなど観察を十分に行うことが望ましい (4) 非びらん性胃食道逆流症の治療については, 投与開始 2 週間後を目安として効果を確認し, 症状の改善傾向が認められない場合には, 酸逆流以外の原因が考えられるため他の適切な治療への変更を考慮すること ( その他の注意 の項参照) (5) 非びらん性胃食道逆流症の治療については, 問診により胸やけ, 呑酸等の酸逆流症状が繰り返しみられること (1 週間あたり 2 日以上 ) を確認のうえ投与すること なお, 本剤の投与が胃癌, 食道癌等の悪性腫瘍及び他の消化器疾患による症状を隠蔽することがあるので, 内視鏡検査等によりこれらの疾患でないことを確認すること (6) 本剤をヘリコバクター ピロリの除菌の補助に用いる際には, 除菌治療に用いられる他の薬剤の添付文書に記載されている禁忌, 慎重投与, 重大な副作用等の使用上の注意を必ず確認すること 3. 相互作用本剤は主として薬物代謝酵素 CYP2C19 又は CYP3A4 で代謝される また, 本剤の胃酸分泌抑制作用により, 併用薬剤の吸収を促進又は抑制することがある ( 併用禁忌 ( 併用しないこと ) 薬剤名等臨床症状 措置方法機序 危険因子 アタザナビル硫酸塩 ( レイアタッツ ) アタザナビル硫酸塩の作用を減弱するおそれがある 本剤の胃酸分泌抑制作用によりアタザナビル硫酸塩の溶解性が低下し, アタザナビルの血中濃度が低下することがある (2) 併用注意 ( 併用に注意すること ) 薬剤名等 臨床症状 措置方法 機序 危険因子 テオフィリン テオフィリンの血中濃度が低下することがある 本剤が薬物代謝酵素を誘導し, テオフィリンの代謝を促進することが考えられている タクロリムス水和物 タクロリムスの血中濃度が上昇することがある 本剤が薬物代謝酵素におけるタクロリムスの代謝を競合的に阻害するためと考えられている 3 薬剤名等 臨床症状 措置方法 機序 危険因子 これらの薬剤の作用 を増強する可能性が ある ジゴキシンメチルジゴキシン イトラコナゾールゲフィチニブ フェニトインジアゼパム これらの薬剤の作用を減弱する可能性がある 本剤の胃酸分泌抑制作用によりジゴキシンの加水分解が抑制され, ジゴキシンの血中濃度が上昇する可能性がある 本剤の胃酸分泌抑制作用によりこれらの薬剤の血中濃度が低下する可能性がある これらの薬剤の代謝, 排泄が遅延することが類薬 ( オメプラゾール ) で報告されている ( 重大な副作用 ( 頻度不明 ) アナフィラキシー反応, ショックアナフィラキシー反応 ( 全身発疹, 顔面浮腫, 呼吸困難等 ) があらわれることがあり, ショックを起こした例もあるので, 観察を十分に行い, 異常が認められた場合には投与を中止し, 適切な処置を行うこと 2) 汎血球減少, 無顆粒球症, 溶血性貧血, 顆粒球減少, 血小板減少, 貧血汎血球減少, 無顆粒球症, 溶血性貧血, 顆粒球減少, 血小板減少, 貧血があらわれることがあるので, 観察を十分に行い, 異常が認められた場合には投与を中止するなど適切な処置を行うこと 重篤な機能障害黄疸,AST(GOT),ALT(GPT) の上昇等を伴う重篤な機能障害があらわれることがあるので, 観察を十分に行い, 異常が認められた場合には投与を中止し, 適切な処置を行うこと 4) 中毒性表皮壊死融解症, 皮膚粘膜眼症候群中毒性表皮壊死融解症 (Toxic Epidermal Necrolysis: TEN), 皮膚粘膜眼症候群 (Stevens-Johnson 症候群 ) があらわれることがあるので, 観察を十分に行い, 異常が認められた場合には投与を中止し, 適切な処置を行うこと 5) 偽膜性大腸炎等の血便を伴う重篤な大腸炎ヘリコバクター ピロリの除菌に用いるアモキシシリン水和物, クラリスロマイシンでは, 偽膜性大腸炎等の血便を伴う重篤な大腸炎があらわれることがあるので, 腹痛, 頻回の下痢があらわれた場合には直ちに投与を中止するなど適切な処置を行うこと 6) 間質性肺炎間質性肺炎があらわれることがあるので, 発熱, 咳嗽, 呼吸困難, 肺音の異常 ( 捻髪音 ) 等があらわれた場合には, 速やかに胸部 X 線等の検査を実施し, 本剤の投与を中止し, 副腎皮質ホルモン剤の投与等の適切な処置を行うこと 7) 間質性腎炎間質性腎炎があらわれ, 急性腎不全に至ることもあるので, 腎機能検査値 (BUN, クレアチニン上昇等 ) に注意し, 異常が認められた場合には投与を中止し, 適切な処置を行うこと (2) その他の副作用胃潰瘍, 十二指腸潰瘍, 吻合部潰瘍, 逆流性食道炎, Zollinger-Ellison 症候群, 非びらん性胃食道逆流症の場合頻度不明注 過敏症発疹, そう痒, 多形紅斑 臓 AST(GOT) 上昇,ALT(GPT) 上昇,Al-P 上昇,LDH 上昇,γ-GTP 上昇 血液好酸球増多 食欲不振, 腹痛, カンジダ症, 味覚異常, 口内炎, 舌炎, 大腸炎 (collagenous colitis 等注 を含む ) 精神神経系頭痛, 眠気, うつ状態, 不眠, めまい, 振戦その他発熱, 総コレステロール上昇, 尿酸上昇, 女性化乳房注, 浮腫, 倦怠感, 舌 口唇のしびれ感, 四肢のしびれ感, 筋肉痛, 脱毛, かすみ目, 脱力感, 関節痛, 低ナトリウム血症注 1: このような場合には投与を中止すること 注 2: 観察を十分に行い, 異常が認められた場合には投与を中止するなど適切な処置を行うこと 注 3: 下痢が継続する場合,collagenous colitis 等が発現している可能性があるため, 速やかに本剤の投与を中止すること 腸管粘膜に縦走潰瘍, びらん, 易出血等の異常を認めることがあるので, 下血, 血便が認められる場合には, 適切な処置を行うこと
4 ヘリコバクター ピロリの除菌の補助の場合 頻度不明 消化器 軟便, 下痢, 味覚異常, 腹部膨満感, 悪心, 嘔吐, 腹痛, 便 秘, 口内炎, 舌炎, 口渇, 胸やけ, 胃食道逆流, 食欲不振 臓 AST(GOT) 上昇,ALT(GPT) 上昇,Al-P 上昇,LDH 上昇,γ-GTP 上昇, ビリルビン上昇 血 液 好中球減少, 好酸球増多, 白血球増多, 貧血, 血小板減少 注 過敏症 発疹, そう痒 精神神経系 頭痛, 眠気, めまい, 不眠, しびれ感, うつ状態 その他 トリグリセライド上昇, 尿酸上昇, 総コレステロール上昇 低下, 尿蛋白陽性, 尿糖陽性, 倦怠感 注 1: このような場合には投与を中止すること 注 2: 観察を十分に行い, 異常が認められた場合には投与を中止するなど 適切な処置を行うこと なお, 外国で行われた試験で認められている副作用 ( 頻度 1% 以上 ) は次のとおりである 消化器 下痢, 味覚異常, 悪心, 嘔吐, 口内炎, 腹痛, 排便回数増加 臓 AST(GOT) 上昇,ALT(GPT) 上昇 過敏症 発疹 精神神経系 頭痛, めまい 5. 高齢者への投与一般に高齢者では酸分泌能は低下しており, その他生理機能の低下もあるので, 低用量から投与を開始するなど慎重に投与すること 6. 妊婦, 産婦, 授乳婦等への投与 ( 妊婦又は妊娠している可能性のある婦人には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること [ 動物試験 ( ラット ) において胎児血漿中濃度は母動物の血漿中濃度より高いことが認められている また, ウサギ ( 経口 30mg /kg/ 日 ) で胎児死亡率の増加が認められている なお, ラットにランソプラゾール (50mg/kg/ 日 ), アモキシシリン水和物 (500mg/kg/ 日 ) 及びクラリスロマイシン (160mg /kg/ 日 ) を併用投与した試験で, 母動物での毒性の増強とともに胎児の発育抑制の増強が認められている ] (2) 授乳中の婦人への投与は避けることが望ましいが, やむを得ず投与する場合は, 授乳を避けさせること [ 動物試験 ( ラット ) で母乳中へ移行することが報告されている ] 7. 小児等への投与小児に対する安全性は確立していない ( 使用経験が少ない ) 8. 適用上の注意薬剤交付時 :PTP 包装の薬剤は PTP シートから取り出して服用するよう指導すること (PTP シートの誤飲により, 硬い鋭角部が食道粘膜へ刺入し, 更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することが報告されている ) ( 類薬 ( オメプラゾール ) で, 視力障害が発現したとの報告がある (2) ラットに 52 週間強制経口投与した試験で,50mg/kg/ 日群 ( 臨床用量の約 100 倍 ) において 1 例に良性の精巣間細胞腫が認められている さらに,24 ヵ月間強制経口投与した試験で,15mg/kg/ 日以上の群において良性の精巣間細胞腫の発生増加が, また,5mg/kg/ 日以上の群において胃のカルチノイド腫瘍が認められており, 加えて, 雌ラットの 15mg/kg/ 日以上及び雄ラットの 50mg/kg/ 日以上の群において網膜萎縮の発生頻度の増加が認められている 精巣間細胞腫及び網膜萎縮については, マウスのがん原性試験, イヌ, サルの毒性試験では認められず, ラットに特有な変化と考えられる ( ラットにランソプラゾール (15mg/kg/ 日以上 ), アモキシシリン水和物 (2000mg/kg/ 日 ) を 4 週間併用経口投与した試験, 及びイヌにランソプラゾール (100mg/kg/ 日 ), アモキシシリン水和物 (500mg/kg/ 日 ), クラリスロマイシン (25mg/kg/ 日 ) を 4 週間併用経口投与した試験で, アモキシシリン水和物を単独あるいは併用投与した動物に結晶尿が認められているが, 結晶はアモキシシリン水和物が排尿後に析出したものであり, 体内で析出したものではないことが確認されている (4) 本剤の投与が胃癌による症状を隠蔽することがあるので, 悪性でないことを確認のうえ投与すること (5) 長期投与における安全性は確立していない ( 本邦においては長期投与の経験は十分でない ) (6) 非びらん性胃食道逆流症の治療において, 食道内酸逆流の高リスクである中高齢者, 肥満者, 裂孔ヘルニア所見ありのいずれにも該当しない場合には本剤の治療効果が得られにくいことが臨床試験により示されている (7) ヘリコバクター ピロリの除菌判定上の注意 : ランソプラゾール等のプロトンポンプインヒビターやアモキシシリン水和物, クラリスロマイシン等の抗生物質及びメトロニダゾールの服用中や投与終了直後では, 13 C- 尿素呼気試験の判定結果が偽陰性になる可能性があるため, 13 C- 尿素呼気試験による除菌判定を行う場合には, これらの薬剤の投与終了後 4 週以降の時点で実施することが望ましい (8) 海外における複数の観察研究で, プロトンポンプインヒビターによる治療において骨粗鬆症に伴う股関節骨折, 手関節骨折, 脊椎骨折のリスク増加が報告されている 特に, 高用量及び長期間 (1 年以上 ) の治療を受けた患者で, 骨折のリスクが増加した : 自主改訂 4
5 ランソラールカプセル 30, ランソプラゾール OD 錠 15mg 日医工 / ランソプラゾール OD 錠 30mg 日医工 禁忌 ( 次の患者には投与しないこと ) 1. 本剤の成分に対する過敏症の既往歴のある患者 2. アタザナビル硫酸塩を投与中の患者 ( 相互作用 の項参照 ) < 効能 効果に関連する使用上の注意 > ヘリコバクター ピロリの除菌の補助の場合 1. 進行期胃 MALT リンパ腫に対するヘリコバクター ピロリ除菌治療の有効性は確立していない 2. 特発性血小板減少性紫斑病に対しては, ガイドライン等を参照し, ヘリコバクター ピロリ除菌治療が適切と判断される症例にのみ除菌治療を行うこと 3. 早期胃癌に対する内視鏡的治療後胃以外には, ヘリコバクター ピロリ除菌治療による胃癌の発症抑制に対する有効性は確立していない < 用法 用量に関連する使用上の注意 > ( 逆流性食道炎の維持療法において,1 日 1 回 30mg の投与は, 1 日 1 回 15mg 投与中に再発した例など 15mg では効果が不十分な場合に限る ランソプラゾール OD 錠 15mg/30mg 日医工 のみ (2) 本剤は口腔内で崩壊するが, 口腔の粘膜から吸収されることはないため, 唾液又は水で飲み込むこと ( 適用上の注意 の項参照) 使用上の注意 1. 慎重投与 ( 次の患者には慎重に投与すること ) ( 薬物過敏症の既往歴のある患者 (2) 障害のある患者 [ 本剤の代謝, 排泄が遅延することがある ] ( 高齢者 ( 高齢者への投与 の項参照) 2. 重要な基本的注意 ( 治療にあたっては経過を十分に観察し, 病状に応じ治療上必要最小限の使用にとどめること (2) 胃潰瘍, 十二指腸潰瘍, 吻合部潰瘍に使用する場合は, 長期の使用経験は十分でないので, 維持療法には用いないことが望ましい ( 逆流性食道炎の維持療法については, 再発 再燃を繰り返す患者に対し投与することとし, 本来維持療法の必要のない患者に投与することのないよう留意すること また,1 日 1 回 30mg 又は 15mg の投与により寛解状態が長期にわたり継続する症例で, 減量又は投与中止により再発するおそれがないと判断される場合は 1 日 1 回 15mg に減量又は中止すること なお, 維持療法中は定期的に内視鏡検査を実施するなど観察を十分に行うことが望ましい (4) 本剤をヘリコバクター ピロリの除菌の補助に用いる際には, 除菌治療に用いられる他の薬剤の添付文書に記載されている禁忌, 慎重投与, 重大な副作用等の使用上の注意を必ず確認すること 3. 相互作用本剤は主として薬物代謝酵素 CYP2C19 又は CYP3A4 で代謝される また, 本剤の胃酸分泌抑制作用により, 併用薬剤の吸収を促進又は抑制することがある ( 併用禁忌 ( 併用しないこと ) 薬剤名等臨床症状 措置方法機序 危険因子 アタザナビル硫酸塩 ( レイアタッツ ) アタザナビル硫酸塩の作用を減弱するおそれがある 本剤の胃酸分泌抑制作用によりアタザナビル硫酸塩の溶解性が低下し, アタザナビルの血中濃度が低下することがある (2) 併用注意 ( 併用に注意すること ) 薬剤名等 臨床症状 措置方法 機序 危険因子 テオフィリン テオフィリンの血中濃度が低下することがある 本剤が薬物代謝酵素を誘導し, テオフィリンの代謝を促進することが考えられている タクロリムス水和物 ジゴキシンメチルジゴキシン イトラコナゾールゲフィチニブ フェニトインジアゼパム タクロリムスの血中濃度が上昇することがある これらの薬剤の作用を増強する可能性がある 本剤が薬物代謝酵素におけるタクロリムスの代謝を競合的に阻害するためと考えられている 本剤の胃酸分泌抑制作用によりジゴキシンの加水分解が抑制され, ジゴキシンの血中濃度が上昇する可能性がある これらの薬剤の作用本剤の胃酸分泌抑制作用にを減弱する可能性がよりこれらの薬剤の血中濃ある 度が低下する可能性がある これらの薬剤の代謝, 排泄が遅延することが類薬 ( オメプラゾール ) で報告されている 4. 副作用本剤は使用成績調査等の副作用発現頻度が明確となる調査を実 施していない ( 重大な副作用 ( 頻度不明 ) アナフィラキシー反応, ショックアナフィラキシー反応 ( 全身発疹, 顔面浮腫, 呼吸困難等 ) があらわれることがあり, ショックを起こした例もあるので, 観察を十分に行い, 異常が認められた場合には投与を中止し, 適切な処置を行うこと 2) 汎血球減少, 無顆粒球症, 溶血性貧血, 顆粒球減少, 血小板減少, 貧血汎血球減少, 無顆粒球症, 溶血性貧血, 顆粒球減少, 血小板減少, 貧血があらわれることがあるので, 観察を十分に行い, 異常が認められた場合には投与を中止するなど適切な処置を行うこと 重篤な機能障害黄疸,AST(GOT),ALT(GPT) の上昇等を伴う重篤な機能障害があらわれることがあるので, 観察を十分に行い, 異常が認められた場合には投与を中止し, 適切な処置を行うこと 4) 中毒性表皮壊死融解症, 皮膚粘膜眼症候群中毒性表皮壊死融解症 (Toxic Epidermal Necrolysis: TEN), 皮膚粘膜眼症候群 (Stevens-Johnson 症候群 ) があらわれることがあるので, 観察を十分に行い, 異常が認められた場合には投与を中止し, 適切な処置を行うこと 5) 偽膜性大腸炎等の血便を伴う重篤な大腸炎ヘリコバクター ピロリの除菌に用いるアモキシシリン水和物, クラリスロマイシンでは, 偽膜性大腸炎等の血便を伴う重篤な大腸炎があらわれることがあるので, 腹痛, 頻回の下痢があらわれた場合には直ちに投与を中止するなど適切な処置を行うこと 6) 間質性肺炎間質性肺炎があらわれることがあるので, 発熱, 咳嗽, 呼吸困難, 肺音の異常 ( 捻髪音 ) 等があらわれた場合には, 速やかに胸部 X 線等の検査を実施し, 本剤の投与を中止し, 副腎皮質ホルモン剤の投与等の適切な処置を行うこと 7) 間質性腎炎間質性腎炎があらわれ, 急性腎不全に至ることもあるので, 腎機能検査値 (BUN, クレアチニン上昇等 ) に注意し, 異常が認められた場合には投与を中止し, 適切な処置を行うこと (2) その他の副作用胃潰瘍, 十二指腸潰瘍, 吻合部潰瘍, 逆流性食道炎, Zollinger-Ellison 症候群の場合頻度不明注 過敏症発疹, そう痒, 多形紅斑 臓 AST(GOT) 上昇,ALT(GPT) 上昇,Al-P 上昇,LDH 上昇,γ-GTP 上昇 血 液 好酸球増多 消化器 便秘, 下痢, 口渇, 腹部膨満感, 悪心, 嘔吐, 食欲不振, 腹痛, カンジダ症, 味覚異常, 口内炎, 舌炎, 大腸炎 (collagenous colitis 等注 を含む ) 精神神経系 頭痛, 眠気, うつ状態, 不眠, めまい, 振戦 その他 発熱, 総コレステロール上昇, 尿酸上昇, 女性化乳房注, 浮 腫, 倦怠感, 舌 口唇のしびれ感, 四肢のしびれ感, 筋肉痛, 脱毛, かすみ目, 脱力感, 関節痛, 低ナトリウム血症 注 1: このような場合には投与を中止すること 注 2: 観察を十分に行い, 異常が認められた場合には投与を中止するなど 適切な処置を行うこと 注 3: 下痢が継続する場合,collagenous colitis 等が発現している可能性が あるため, 速やかに本剤の投与を中止すること 腸管粘膜に縦走潰瘍, びらん, 易出血等の異常を認めることがあるので, 下血, 血便が認め られる場合には, 適切な処置を行うこと ヘリコバクター ピロリの除菌の補助の場合 頻度不明 消化器 軟便, 下痢, 味覚異常, 腹部膨満感, 悪心, 嘔吐, 腹痛, 便 秘, 口内炎, 舌炎, 口渇, 胸やけ, 胃食道逆流, 食欲不振 臓 AST(GOT) 上昇,ALT(GPT) 上昇,Al-P 上昇,LDH 上昇,γ-GTP 上昇, ビリルビン上昇 血 液 好中球減少, 好酸球増多, 白血球増多, 貧血, 血小板減少 注 過敏症 発疹, そう痒 精神神経系 頭痛, 眠気, めまい, 不眠, しびれ感, うつ状態 その他 トリグリセライド上昇, 尿酸上昇, 総コレステロール上昇 低下, 尿蛋白陽性, 尿糖陽性, 倦怠感 注 1: このような場合には投与を中止すること 注 2: 観察を十分に行い, 異常が認められた場合には投与を中止するなど 適切な処置を行うこと 5
6 なお, 外国で行われた試験で認められている副作用 ( 頻度 1% 以上 ) は次のとおりである 消化器 下痢, 味覚異常, 悪心, 嘔吐, 口内炎, 腹痛, 排便回数増加 臓 AST(GOT) 上昇,ALT(GPT) 上昇 過敏症 発疹 精神神経系 頭痛, めまい 5. 高齢者への投与一般に高齢者では酸分泌能は低下しており, その他生理機能の低下もあるので, 低用量から投与を開始するなど慎重に投与すること 6. 妊婦, 産婦, 授乳婦等への投与 ( 妊婦又は妊娠している可能性のある婦人には治療上の有益性が危険性を上回ると判断される場合にのみ投与すること [ 動物試験 ( ラット ) において胎児血漿中濃度は母動物の血漿中濃度より高いことが認められている また, ウサギ ( 経口 30mg /kg/ 日 ) で胎児死亡率の増加が認められている なお, ラットにランソプラゾール (50mg/kg/ 日 ), アモキシシリン水和物 (500mg/kg/ 日 ) 及びクラリスロマイシン (160mg /kg/ 日 ) を併用投与した試験で, 母動物での毒性の増強とともに胎児の発育抑制の増強が認められている ] (2) 授乳中の婦人への投与は避けることが望ましいが, やむを得ず投与する場合は, 授乳を避けさせること [ 動物試験 ( ラット ) で母乳中へ移行することが報告されている ] 7. 小児等への投与小児に対する安全性は確立していない ( 使用経験が少ない ) 8. 適用上の注意 ( 薬剤交付時 PTP 包装の薬剤は PTP シートから取り出して服用するよう指導すること (PTP シートの誤飲により, 硬い鋭角部が食道粘膜へ刺入し, 更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することが報告されている ) ランソプラゾール OD 錠 15mg/30mg 日医工 のみ (2) 服用時本剤は舌の上にのせ唾液を浸潤させ舌で軽くつぶし, 崩壊後唾液のみで服用可能である また, 水で服用することもできる ( 類薬 ( オメプラゾール ) で, 視力障害が発現したとの報告がある (2) ラットに 52 週間強制経口投与した試験で,50mg/kg/ 日群 ( 臨床用量の約 100 倍 ) において 1 例に良性の精巣間細胞腫が認められている さらに,24 ヵ月間強制経口投与した試験で,15mg/kg/ 日以上の群において良性の精巣間細胞腫の発生増加が, また,5mg/kg/ 日以上の群において胃のカルチノイド腫瘍が認められており, 加えて, 雌ラットの 15mg/kg/ 日以上及び雄ラットの 50mg/kg/ 日以上の群において網膜萎縮の発生頻度の増加が認められている 精巣間細胞腫及び網膜萎縮については, マウスのがん原性試験, イヌ, サルの毒性試験では認められず, ラットに特有な変化と考えられる ( ラットにランソプラゾール (15mg/kg/ 日以上 ), アモキシシリン水和物 (2000mg/kg/ 日 ) を 4 週間併用経口投与した試験, 及びイヌにランソプラゾール (100mg/kg/ 日 ), アモキシシリン水和物 (500mg/kg/ 日 ), クラリスロマイシン (25mg/kg/ 日 ) を 4 週間併用経口投与した試験で, アモキシシリン水和物を単独あるいは併用投与した動物に結晶尿が認められているが, 結晶はアモキシシリン水和物が排尿後に析出したものであり, 体内で析出したものではないことが確認されている (4) 本剤の投与が胃癌による症状を隠蔽することがあるので, 悪性でないことを確認のうえ投与すること (5) 長期投与における安全性は確立していない ( 本邦においては長期投与の経験は十分でない ) (6) ヘリコバクター ピロリの除菌判定上の注意 : ランソプラゾール等のプロトンポンプインヒビターやアモキシシリン水和物, クラリスロマイシン等の抗生物質及びメトロニダゾールの服用中や投与終了直後では,13C- 尿素呼気試験の判定結果が偽陰性になる可能性があるため,13C- 尿素呼気試験による除菌判定を行う場合には, これらの薬剤の投与終了後 4 週以降の時点で実施することが望ましい (7) 海外における複数の観察研究で, プロトンポンプインヒビターによる治療において骨粗鬆症に伴う股関節骨折, 手関節骨折, 脊椎骨折のリスク増加が報告されている 特に, 高用量及び長期間 (1 年以上 ) の治療を受けた患者で, 骨折のリスクが増加した : 自主改訂 ランソラール A 6
<4D F736F F D2082A8926D82E782B995B68F E834E838D838A E3132>
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能 効果 用法 用量 使用上の注意 改訂のお知らせ 2013 年 12 月 東和薬品株式会社 このたび 平成 25 年 8 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 25 年 11 月 29 日付にて 下記の内容で承認されました また 使用上の注意 を改訂致しましたので 併せてお知らせ申し上げます
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能 効果 用法 用量 使用上の注意 改訂のお知らせ 2013 年 12 月 東和薬品株式会社 このたび 平成 25 年 8 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 25 年 11 月 29 日付にて 下記の内容で承認されました また 使用上の注意 を改訂致しましたので 併せてお知らせ申し上げます
1)~ 2) 3) 近位筋脱力 CK(CPK) 高値 炎症を伴わない筋線維の壊死 抗 HMG-CoA 還元酵素 (HMGCR) 抗体陽性等を特徴とする免疫性壊死性ミオパチーがあらわれ 投与中止後も持続する例が報告されているので 患者の状態を十分に観察すること なお 免疫抑制剤投与により改善がみられた
 適正使用に欠かせない情報です 必ずお読みください 使用上の注意 改訂のお知らせ 注 1) 処方箋医薬品 ATORVASTATIN TABLETS AMALUET COMBINATION TABLETS 注 1) 処方箋医薬品 PRAVASTATIN SODIUM TABLETS 注 1) 注意 - 医師等の処方箋により使用すること PITAVASTATIN CALCIUM TABLETS 2016
適正使用に欠かせない情報です 必ずお読みください 使用上の注意 改訂のお知らせ 注 1) 処方箋医薬品 ATORVASTATIN TABLETS AMALUET COMBINATION TABLETS 注 1) 処方箋医薬品 PRAVASTATIN SODIUM TABLETS 注 1) 注意 - 医師等の処方箋により使用すること PITAVASTATIN CALCIUM TABLETS 2016
D961H は AstraZeneca R&D Mӧlndal( スウェーデン ) において開発された オメプラゾールの一方の光学異性体 (S- 体 ) のみを含有するプロトンポンプ阻害剤である ネキシウム (D961H の日本における販売名 ) 錠 20 mg 及び 40 mg は を対象として
 第 2 部 CTD の概要 一般名 : エソメプラゾールマグネシウム水和物 版番号 : 2.2 緒言 ネキシウム カプセル ネキシウム 懸濁用顆粒分包 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています D961H は AstraZeneca R&D Mӧlndal( スウェーデン ) において開発された オメプラゾールの一方の光学異性体
第 2 部 CTD の概要 一般名 : エソメプラゾールマグネシウム水和物 版番号 : 2.2 緒言 ネキシウム カプセル ネキシウム 懸濁用顆粒分包 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています D961H は AstraZeneca R&D Mӧlndal( スウェーデン ) において開発された オメプラゾールの一方の光学異性体
<4D F736F F D B A814089FC92F982CC82A8926D82E782B95F E31328C8E5F5F E646F63>
 - 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ 抗悪性腫瘍剤 ( ブルトン型チロシンキナーゼ阻害剤 ) ( 一般名 : イブルチニブ ) 2016 年 12 月 この度 抗悪性腫瘍剤 イムブルビカ カプセル 140 mg ( 以下標記製品 ) につきまして 再発又は難治性のマントル細胞リンパ腫 の効能追加承認を取得したことに伴い
- 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ 抗悪性腫瘍剤 ( ブルトン型チロシンキナーゼ阻害剤 ) ( 一般名 : イブルチニブ ) 2016 年 12 月 この度 抗悪性腫瘍剤 イムブルビカ カプセル 140 mg ( 以下標記製品 ) につきまして 再発又は難治性のマントル細胞リンパ腫 の効能追加承認を取得したことに伴い
Microsoft Word - sa_niflec_ doc
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能又は効果 用法及び用量 使用上の注意改訂のお知らせ 経口腸管洗浄剤 発売 2009 年 4 月 製造販売 この度 経口腸管洗浄剤ニフレック 内用において 効能又は効果 用法及び用量 の追加承認を取得したことに伴い 添付文書を以下のとおり改訂致しましたのでご案内申し上げます 今後のご使用につきましては 下記内容をご参照下さいますようお願い申し上げます
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能又は効果 用法及び用量 使用上の注意改訂のお知らせ 経口腸管洗浄剤 発売 2009 年 4 月 製造販売 この度 経口腸管洗浄剤ニフレック 内用において 効能又は効果 用法及び用量 の追加承認を取得したことに伴い 添付文書を以下のとおり改訂致しましたのでご案内申し上げます 今後のご使用につきましては 下記内容をご参照下さいますようお願い申し上げます
Ⅰ. 改訂内容 ( 部変更 ) ペルサンチン 錠 12.5 改 訂 後 改 訂 前 (1) 本剤投与中の患者に本薬の注射剤を追加投与した場合, 本剤の作用が増強され, 副作用が発現するおそれがあるので, 併用しないこと ( 過量投与 の項参照) 本剤投与中の患者に本薬の注射剤を追加投与した場合, 本
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意 改訂のお知らせ 2006 年 1 月日本ベーリンガーインゲルハイム株式会社 注 ) 処方せん医薬品 ( ジピリダモール製剤 ) = 登録商標注 ) 注意 - 医師等の処方せんにより使用すること 謹啓時下ますますご清祥のこととお慶び申し上げます 平素は弊社製品につきましてご愛顧を賜り厚く御礼申し上げます さて, この度, 自主改訂によりペルサンチン
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意 改訂のお知らせ 2006 年 1 月日本ベーリンガーインゲルハイム株式会社 注 ) 処方せん医薬品 ( ジピリダモール製剤 ) = 登録商標注 ) 注意 - 医師等の処方せんにより使用すること 謹啓時下ますますご清祥のこととお慶び申し上げます 平素は弊社製品につきましてご愛顧を賜り厚く御礼申し上げます さて, この度, 自主改訂によりペルサンチン
葉酸とビタミンQ&A_201607改訂_ indd
 L FO AT E VI TAMI NB12 医療関係者用 葉酸 とビタミンB ビタミンB12 アリムタ投与に際して 警告 1 本剤を含むがん化学療法に際しては 緊急時に十分対応できる医療施設において がん化学療 法に十分な知識 経験を持つ医師のもとで 本剤の投与が適切と判断される症例についてのみ投 与すること 適応患者の選択にあたっては 各併用薬剤の添付文書を参照して十分注意すること また 治療開始に先立ち
L FO AT E VI TAMI NB12 医療関係者用 葉酸 とビタミンB ビタミンB12 アリムタ投与に際して 警告 1 本剤を含むがん化学療法に際しては 緊急時に十分対応できる医療施設において がん化学療 法に十分な知識 経験を持つ医師のもとで 本剤の投与が適切と判断される症例についてのみ投 与すること 適応患者の選択にあたっては 各併用薬剤の添付文書を参照して十分注意すること また 治療開始に先立ち
 医薬品の使用上の注意の改訂について ( 平成 14 年 6 月 5 日 ) ( 医薬安発第 0605002 号 ) ( 各都道府県衛生主管部 ( 局 ) 長あて厚生労働省医薬局安全対策課長通知 ) 医薬品の安全対策については 日頃よりご尽力いただいているところでありますが 今般 別添のとおり日本製薬団体連合会安全性委員会委員長あて通知及び連絡したので ご承知願います 医薬品の使用上の注意の改訂について
医薬品の使用上の注意の改訂について ( 平成 14 年 6 月 5 日 ) ( 医薬安発第 0605002 号 ) ( 各都道府県衛生主管部 ( 局 ) 長あて厚生労働省医薬局安全対策課長通知 ) 医薬品の安全対策については 日頃よりご尽力いただいているところでありますが 今般 別添のとおり日本製薬団体連合会安全性委員会委員長あて通知及び連絡したので ご承知願います 医薬品の使用上の注意の改訂について
パリエット錠5mg、パリエット錠10mg、パリエット錠20mg
 医薬品の適正使用に欠かせない情報です 必ずお読みください 用法 用量 使用上の注意改訂のお知らせ 処方箋医薬品注意 - 医師等の処方箋により使用すること 2017 年 9-11 月 このたび 標記製品の用法 用量 使用上の注意を下記のとおり改訂致しました ( 用法 用量の改訂は 錠 5mg 錠 10mg のみ ) 今後のご使用に際しましては 下記内容をご参照頂き 本書を適正使用情報としてご活用頂きますようお願い申し上げます
医薬品の適正使用に欠かせない情報です 必ずお読みください 用法 用量 使用上の注意改訂のお知らせ 処方箋医薬品注意 - 医師等の処方箋により使用すること 2017 年 9-11 月 このたび 標記製品の用法 用量 使用上の注意を下記のとおり改訂致しました ( 用法 用量の改訂は 錠 5mg 錠 10mg のみ ) 今後のご使用に際しましては 下記内容をご参照頂き 本書を適正使用情報としてご活用頂きますようお願い申し上げます
医薬品の適正使用に欠かせない情報です
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意 改訂のお知らせ 劇薬 処方せん医薬品 ( 注意 - 医師等の処方せんにより使用すること ) 高血圧症 狭心症治療剤持続性 Ca 拮抗剤日本薬局方アムロジピンベシル酸塩錠アムロジピン錠 2.5mg フソー アムロジピン錠 5mg フソー アムロジピン錠 10mg フソー 日本薬局方アムロジピンベシル酸塩口腔内崩壊錠アムロジピン OD
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意 改訂のお知らせ 劇薬 処方せん医薬品 ( 注意 - 医師等の処方せんにより使用すること ) 高血圧症 狭心症治療剤持続性 Ca 拮抗剤日本薬局方アムロジピンベシル酸塩錠アムロジピン錠 2.5mg フソー アムロジピン錠 5mg フソー アムロジピン錠 10mg フソー 日本薬局方アムロジピンベシル酸塩口腔内崩壊錠アムロジピン OD
減量・コース投与期間短縮の基準
 用法 用量 通常 成人には初回投与量 (1 回量 ) を体表面積に合せて次の基準量とし 朝食後および夕食後の 1 日 2 回 28 日間連日経口投与し その後 14 日間休薬する これを 1 クールとして投与を繰り返す ただし 本剤の投与によると判断される臨床検査値異常 ( 血液検査 肝 腎機能検査 ) および消化器症状が発現せず 安全性に問題がない場合には休薬を短縮できるが その場合でも少なくとも
用法 用量 通常 成人には初回投与量 (1 回量 ) を体表面積に合せて次の基準量とし 朝食後および夕食後の 1 日 2 回 28 日間連日経口投与し その後 14 日間休薬する これを 1 クールとして投与を繰り返す ただし 本剤の投与によると判断される臨床検査値異常 ( 血液検査 肝 腎機能検査 ) および消化器症状が発現せず 安全性に問題がない場合には休薬を短縮できるが その場合でも少なくとも
p 13
 p 12 p 13 p 14 p 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 10. 安全性 (1) 副作用 ( 臨床検査値異常を含む ) 総症例 1030 例中 副作用が報告されたのは 519 例 (50.4%) でした 主な症状は鼓腸 197 例 (19.1%) 下痢 188 例 (18.3%) 腹部膨満
p 12 p 13 p 14 p 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 10. 安全性 (1) 副作用 ( 臨床検査値異常を含む ) 総症例 1030 例中 副作用が報告されたのは 519 例 (50.4%) でした 主な症状は鼓腸 197 例 (19.1%) 下痢 188 例 (18.3%) 腹部膨満
スライド 1
 1/5 PMDA からの医薬品適正使用のお願い ( 独 ) 医薬品医療機器総合機構 No.6 2012 年 1 月 ラミクタール錠 ( ラモトリギン ) の重篤皮膚障害と用法 用量遵守 早期発見について ラミクタール錠は 用法 用量 を遵守せず投与した場合に皮膚障害の発現率が高くなることが示されている ( 表 1 参照 ) ため 用法 用量 を遵守することが平成 20 年 10 月の承認時より注意喚起されています
1/5 PMDA からの医薬品適正使用のお願い ( 独 ) 医薬品医療機器総合機構 No.6 2012 年 1 月 ラミクタール錠 ( ラモトリギン ) の重篤皮膚障害と用法 用量遵守 早期発見について ラミクタール錠は 用法 用量 を遵守せず投与した場合に皮膚障害の発現率が高くなることが示されている ( 表 1 参照 ) ため 用法 用量 を遵守することが平成 20 年 10 月の承認時より注意喚起されています
< F2D C D838A8BDB92CA926D2E6A7464>
 保医発 0221 第 31 号平成 25 年 2 月 21 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 ヘリコバクター ピロリ感染の診断及び治療に関する取扱いについて の一部改正について 今般 ヘリコバクター ピロリ感染の診断及び治療に使用する医薬品の効能
保医発 0221 第 31 号平成 25 年 2 月 21 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 ヘリコバクター ピロリ感染の診断及び治療に関する取扱いについて の一部改正について 今般 ヘリコバクター ピロリ感染の診断及び治療に使用する医薬品の効能
Drug Infomation
 PPI と 今日のお話 H2 ブロッカーの特徴 何のために処方していますか? 胃酸分泌抑制薬 ( 特に PPI ) について 薬剤部医薬品情報課 松本早苗 2016 年 10 月 21 日救急部カンファレンス 胃酸分泌抑制薬 ( 特に PPI) の落とし穴 (*_*;) ストレスや敗血症による潰瘍予防の適正使用 NST の立場から PPI と H2 ブロッカーの比較 PPI と H2 ブロッカーの特徴
PPI と 今日のお話 H2 ブロッカーの特徴 何のために処方していますか? 胃酸分泌抑制薬 ( 特に PPI ) について 薬剤部医薬品情報課 松本早苗 2016 年 10 月 21 日救急部カンファレンス 胃酸分泌抑制薬 ( 特に PPI) の落とし穴 (*_*;) ストレスや敗血症による潰瘍予防の適正使用 NST の立場から PPI と H2 ブロッカーの比較 PPI と H2 ブロッカーの特徴
5_使用上の注意(37薬効)Web作業用.indd
 34 ビタミン主薬製剤 1 ビタミン A 主薬製剤 使用上の注意と記載条件 1. 次の人は服用前に医師又は薬剤師に相談することあ医師の治療を受けている人 い妊娠 3 ヵ月以内の妊婦, 妊娠していると思われる人又は妊娠を希望する人 ( 妊娠 3 ヵ月前から妊娠 3 ヵ月までの間にビタミン A を 1 日 10,000 国際単位以上摂取した妊婦から生まれた児に先天異常の割合が上昇したとの報告がある )
34 ビタミン主薬製剤 1 ビタミン A 主薬製剤 使用上の注意と記載条件 1. 次の人は服用前に医師又は薬剤師に相談することあ医師の治療を受けている人 い妊娠 3 ヵ月以内の妊婦, 妊娠していると思われる人又は妊娠を希望する人 ( 妊娠 3 ヵ月前から妊娠 3 ヵ月までの間にビタミン A を 1 日 10,000 国際単位以上摂取した妊婦から生まれた児に先天異常の割合が上昇したとの報告がある )
150800247.indd
 ヘリコバクター ピロリ ピロリ菌 感染症について 消化器内科 藤澤 聖 1983 年に胃の粘膜からピロリ菌が発見されて以来様々な研究がなされ ピロリ菌と胃の関係や 種々の病気との関連について明らかになってきました ピロリ菌が胃に感染すると長い年月をかけて 萎縮性胃炎 腸上皮化生という状態を惹き起こし そこから大部分の胃癌が発生すると言われてい ます また胃潰瘍 十二指腸潰瘍や胃 MALT リンパ腫など胃腸疾患のみならず
ヘリコバクター ピロリ ピロリ菌 感染症について 消化器内科 藤澤 聖 1983 年に胃の粘膜からピロリ菌が発見されて以来様々な研究がなされ ピロリ菌と胃の関係や 種々の病気との関連について明らかになってきました ピロリ菌が胃に感染すると長い年月をかけて 萎縮性胃炎 腸上皮化生という状態を惹き起こし そこから大部分の胃癌が発生すると言われてい ます また胃潰瘍 十二指腸潰瘍や胃 MALT リンパ腫など胃腸疾患のみならず
食欲不振 全身倦怠感 皮膚や白目が黄色くなる [ 肝機能障害 黄疸 ] 尿量減少 全身のむくみ 倦怠感 [ 急性腎不全 ] 激しい上腹部の痛み 腰背部の痛み 吐き気 [ 急性膵炎 ] 発熱 から咳 呼吸困難 [ 間質性肺炎 ] 排便の停止 腹痛 腹部膨満感 [ 腸閉塞 ] 手足の筋肉の痛み こわばり
![食欲不振 全身倦怠感 皮膚や白目が黄色くなる [ 肝機能障害 黄疸 ] 尿量減少 全身のむくみ 倦怠感 [ 急性腎不全 ] 激しい上腹部の痛み 腰背部の痛み 吐き気 [ 急性膵炎 ] 発熱 から咳 呼吸困難 [ 間質性肺炎 ] 排便の停止 腹痛 腹部膨満感 [ 腸閉塞 ] 手足の筋肉の痛み こわばり 食欲不振 全身倦怠感 皮膚や白目が黄色くなる [ 肝機能障害 黄疸 ] 尿量減少 全身のむくみ 倦怠感 [ 急性腎不全 ] 激しい上腹部の痛み 腰背部の痛み 吐き気 [ 急性膵炎 ] 発熱 から咳 呼吸困難 [ 間質性肺炎 ] 排便の停止 腹痛 腹部膨満感 [ 腸閉塞 ] 手足の筋肉の痛み こわばり](/thumbs/91/105740782.jpg) くすりのしおり内服剤 2013 年 11 月作成薬には効果 ( ベネフィット ) だけでなく副作用 ( リスク ) があります 副作用をなるべく抑え 効果を最大限に引き出すことが大切です そのために この薬を使用される患者さんの理解と協力が必要です 商品名 : グラクティブ錠 12.5mg 主成分 : シタグリプチンリン酸塩水和物 (Sitagliptin phosphate hydrate) 剤形
くすりのしおり内服剤 2013 年 11 月作成薬には効果 ( ベネフィット ) だけでなく副作用 ( リスク ) があります 副作用をなるべく抑え 効果を最大限に引き出すことが大切です そのために この薬を使用される患者さんの理解と協力が必要です 商品名 : グラクティブ錠 12.5mg 主成分 : シタグリプチンリン酸塩水和物 (Sitagliptin phosphate hydrate) 剤形
したことによると考えられています 4. ピロリ菌の検査法ピロリ菌の検査法にはいくつかの種類があり 内視鏡を使うものとそうでないものに大きく分けられます 前者は 内視鏡を使って胃の組織を採取し それを材料にしてピロリ菌の有無を調べます 胃粘膜組織を顕微鏡で見てピロリ菌を探す方法 ( 鏡検法 ) 先に述
 ピロリ菌のはなし ( 上 ) 大阪掖済会病院部長 消化器内科佐藤博之 1. はじめにピロリ菌という言葉を聞いたことがある方も多いと思います ピロリ菌はヒトの胃の中に住む細菌で 胃潰瘍や十二指腸潰瘍に深く関わっていることが明らかにされています 22 年前に発見されてから研究が精力的に進められ 以後 胃潰瘍や十二指腸潰瘍の治療法が大きく様変わりすることになりました 我が国では 2000 年 11 月に胃潰瘍
ピロリ菌のはなし ( 上 ) 大阪掖済会病院部長 消化器内科佐藤博之 1. はじめにピロリ菌という言葉を聞いたことがある方も多いと思います ピロリ菌はヒトの胃の中に住む細菌で 胃潰瘍や十二指腸潰瘍に深く関わっていることが明らかにされています 22 年前に発見されてから研究が精力的に進められ 以後 胃潰瘍や十二指腸潰瘍の治療法が大きく様変わりすることになりました 我が国では 2000 年 11 月に胃潰瘍
使用上の注意 1. 慎重投与 ( 次の患者には慎重に投与すること ) 1 2X X 重要な基本的注意 1TNF 2TNF TNF 3 X - CT X 4TNFB HBsHBcHBs B B B B 5 6TNF 7 8dsDNA d
 2015 5 7 201410 28 TNF 阻害薬 TNFFab シムジア 皮下注 200mg シリンジ Cimzia 200mg Syringe for S.C. Injection セルトリズマブペゴル ( 遺伝子組換え ) 製剤 873999 22400AMX01488000 20132 20133 20155 20079 警告 1. 2. 1 2 X - CT 3. TNF 4. 1 禁忌
2015 5 7 201410 28 TNF 阻害薬 TNFFab シムジア 皮下注 200mg シリンジ Cimzia 200mg Syringe for S.C. Injection セルトリズマブペゴル ( 遺伝子組換え ) 製剤 873999 22400AMX01488000 20132 20133 20155 20079 警告 1. 2. 1 2 X - CT 3. TNF 4. 1 禁忌
Microsoft PowerPoint - __________________________ ppt
 日本ヘリコバクター学会のガイドラインについて教えて下さい ピロリ菌を除菌すると胃癌の予防になるのですか? 2009 年 1 月 日本ヘリコバクター学会よりピロリ菌除菌に関するガイドラインが発表されました それによるとピロリ菌に感染している人はすべて除菌を受けることを強く勧められています (%) 12 8 内視鏡治療後の別の胃癌の発生率 除菌しない場合 : 4.1 %/ 年 除菌できた場合 :1.4
日本ヘリコバクター学会のガイドラインについて教えて下さい ピロリ菌を除菌すると胃癌の予防になるのですか? 2009 年 1 月 日本ヘリコバクター学会よりピロリ菌除菌に関するガイドラインが発表されました それによるとピロリ菌に感染している人はすべて除菌を受けることを強く勧められています (%) 12 8 内視鏡治療後の別の胃癌の発生率 除菌しない場合 : 4.1 %/ 年 除菌できた場合 :1.4
タケキャブ錠 10 mg 他に係る医薬品リスク管理計画書 (RMP) の概要 ( 別紙様式 ) 販売名 タケキャブ錠 10 mg 同 20 mg 有効成分 ボノプラザンフマル酸塩 製造販売業者 武田薬品工業株式会社 薬効分類 提出年月 2018 年 4 月 1.1. 安全性検討事項 重要
 タケキャブ錠 10 mg タケキャブ錠 20 mg に係る 医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任は 武田薬品工業株式会社に帰属するものであり 当該情報を適正使用以外の営利目的に利用することはできません 武田薬品工業株式会社 タケキャブ錠 10 mg 他に係る医薬品リスク管理計画書 (RMP) の概要 ( 別紙様式 ) 販売名 タケキャブ錠 10 mg 同 20 mg
タケキャブ錠 10 mg タケキャブ錠 20 mg に係る 医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任は 武田薬品工業株式会社に帰属するものであり 当該情報を適正使用以外の営利目的に利用することはできません 武田薬品工業株式会社 タケキャブ錠 10 mg 他に係る医薬品リスク管理計画書 (RMP) の概要 ( 別紙様式 ) 販売名 タケキャブ錠 10 mg 同 20 mg
モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム 製造販売業者 EA ファーマ株式会社 薬効分類 提出年月 平成 30 年 10 月 1.1. 安全
 モビコール配合内用剤 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はEAファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません EA ファーマ株式会社 モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム
モビコール配合内用剤 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はEAファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません EA ファーマ株式会社 モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム
スライド 1
 薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
厚生労働省告示024号/平成22年1月22日告示/平成22年1月22日施行
 厚生労働省告示第 206 号 / 平成 30 年 4 月 17 日告示 / 平成 30 年 4 月 18 日施行 区分商品名規格単位会社名成分名効能 効果用法 用量規制等備考 内用薬レキサルティ 1mg1 錠大塚製薬ブレクスピプ統合失調症 通常 にはブレクスピプラゾールとして 1 日 1 回 1mg から投与を開始した後 劇 錠 1mg ラゾール 4 日以上の間隔をあけて増量し 1 日 1 回 2mg
厚生労働省告示第 206 号 / 平成 30 年 4 月 17 日告示 / 平成 30 年 4 月 18 日施行 区分商品名規格単位会社名成分名効能 効果用法 用量規制等備考 内用薬レキサルティ 1mg1 錠大塚製薬ブレクスピプ統合失調症 通常 にはブレクスピプラゾールとして 1 日 1 回 1mg から投与を開始した後 劇 錠 1mg ラゾール 4 日以上の間隔をあけて増量し 1 日 1 回 2mg
使用上の注意改訂のお知らせ スピーゲル
 医薬品の適正使用に欠かせない情報です 必ずお読みください 使用上の注意改訂のお知らせ このたび制酸剤スピーゲルにつきまして 使用上の注意を下記のとおり改訂いたしましたので お知らせ申し上げます 平成 20 年 9 月 記 スピーゲル ( メタケイ酸アルミン酸マグネシウム ) 1. 改訂箇所下記の下線部のとおり [ 相互作用 ] の 併用注意 を改訂し [ その他の注意 ] を新設しました 2. 改訂内容
医薬品の適正使用に欠かせない情報です 必ずお読みください 使用上の注意改訂のお知らせ このたび制酸剤スピーゲルにつきまして 使用上の注意を下記のとおり改訂いたしましたので お知らせ申し上げます 平成 20 年 9 月 記 スピーゲル ( メタケイ酸アルミン酸マグネシウム ) 1. 改訂箇所下記の下線部のとおり [ 相互作用 ] の 併用注意 を改訂し [ その他の注意 ] を新設しました 2. 改訂内容
添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示され
 添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示されます 検索条件設定時の注意 検索はテキスト文章 (SGML 又は XML) が対象となっており 画像及び
添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示されます 検索条件設定時の注意 検索はテキスト文章 (SGML 又は XML) が対象となっており 画像及び
ハイゼントラ20%皮下注1g/5mL・2g/10mL・4g/20mL
 CSL19-158 医薬品の適正使用に欠かせない情報です 必ずお読みください 効能又は効果 用法及び用量 使用上の注意改訂のお知らせ 2019 年 3 月血漿分画製剤 ( 皮下注用人免疫グロブリン製剤 ) この度 標記製品の製造販売承認事項の一部変更が承認されました それに伴い 効能又は効果 用法及び用量 及び 使用上の注意 等を改訂いたしましたので お知らせいたします 改訂添付文書を封入した製品がお手元に届くまでには若干の日時を要しますので
CSL19-158 医薬品の適正使用に欠かせない情報です 必ずお読みください 効能又は効果 用法及び用量 使用上の注意改訂のお知らせ 2019 年 3 月血漿分画製剤 ( 皮下注用人免疫グロブリン製剤 ) この度 標記製品の製造販売承認事項の一部変更が承認されました それに伴い 効能又は効果 用法及び用量 及び 使用上の注意 等を改訂いたしましたので お知らせいたします 改訂添付文書を封入した製品がお手元に届くまでには若干の日時を要しますので
160223メトトレキサート1_4.indd
 使用上の注意改訂のお知らせ 2016 年 3 月 田辺三菱製薬株式会社 このたび 標記製品につきまして 使用上の注意 を改訂しましたのでお知らせ致します 今後のご使用に際しましては 下記内容をご参照下さいますようお願い致します 改訂概要 改訂項目改訂内容 副作用 ( その他の副作用 ) 悪寒を追記し 先発医薬品の記載順に合わせて記載整備しました -1- 使用上の注意 の改訂内容 (3~6 頁に改訂後の
使用上の注意改訂のお知らせ 2016 年 3 月 田辺三菱製薬株式会社 このたび 標記製品につきまして 使用上の注意 を改訂しましたのでお知らせ致します 今後のご使用に際しましては 下記内容をご参照下さいますようお願い致します 改訂概要 改訂項目改訂内容 副作用 ( その他の副作用 ) 悪寒を追記し 先発医薬品の記載順に合わせて記載整備しました -1- 使用上の注意 の改訂内容 (3~6 頁に改訂後の
ネキシウムカプセル10mg/ネキシウムカプセル20mg
 NEX-9.0 **2016 年 2 月改訂 ( 第 9 版 ) * 2015 年 1 月改訂 処方箋医薬品 : 注意 - 医師等の処方箋により使用すること 貯法 : 室温保存使用期限 : ケース等に表示 プロトンポンプ インヒビター エソメプラゾールマグネシウム水和物カプセル 日本標準商品分類番号 872329 10mg 20mg 承認番号 22300AMX00598 22300AMX00599
NEX-9.0 **2016 年 2 月改訂 ( 第 9 版 ) * 2015 年 1 月改訂 処方箋医薬品 : 注意 - 医師等の処方箋により使用すること 貯法 : 室温保存使用期限 : ケース等に表示 プロトンポンプ インヒビター エソメプラゾールマグネシウム水和物カプセル 日本標準商品分類番号 872329 10mg 20mg 承認番号 22300AMX00598 22300AMX00599
オメプラール錠10/オメプラール錠20
 OMP-19.1 **2015 年 1 月改訂 ( 第 26 版 ) * 2014 年 7 月改訂 処方箋医薬品 : 注意 - 医師等の処方箋により使用すること 貯法 : 室温保存使用期限 : ケース等に表示 日本薬局方 プロトンポンプ インヒビター オメプラゾール腸溶錠 日本標準商品分類番号 872329 オメプラール錠 10 オメプラール錠 20 承認番号 21200AMZ00641 21300AMZ00054
OMP-19.1 **2015 年 1 月改訂 ( 第 26 版 ) * 2014 年 7 月改訂 処方箋医薬品 : 注意 - 医師等の処方箋により使用すること 貯法 : 室温保存使用期限 : ケース等に表示 日本薬局方 プロトンポンプ インヒビター オメプラゾール腸溶錠 日本標準商品分類番号 872329 オメプラール錠 10 オメプラール錠 20 承認番号 21200AMZ00641 21300AMZ00054
ネキシウムに係る医薬品リスク管理計画書 (RMP) の概要 販売名 ネキシウム カプセル 10 mg 20mg ネキシウム 懸濁用顆粒分包 10mg 20mg 有効成分 エソメプラゾールマグネシウム水和物 製造販売業者アストラゼネカ株式会社薬効分類 提出年月 平成 30 年 10 月
 ネキシウム カプセル 10 mg ネキシウム カプセル 20 mg ネキシウム 懸濁用顆粒分包 10 mg ネキシウム 懸濁用顆粒分包 20 mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はアストラゼネカ株式会社に帰属するものであり 当該情報を適正使用以外の営利目的に利用することはできません アストラゼネカ株式会社 ネキシウムに係る医薬品リスク管理計画書 (RMP)
ネキシウム カプセル 10 mg ネキシウム カプセル 20 mg ネキシウム 懸濁用顆粒分包 10 mg ネキシウム 懸濁用顆粒分包 20 mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はアストラゼネカ株式会社に帰属するものであり 当該情報を適正使用以外の営利目的に利用することはできません アストラゼネカ株式会社 ネキシウムに係る医薬品リスク管理計画書 (RMP)
扶桑薬品工業 再審査結果のお知らせ 無水エタノール注
 医薬品の適正使用に欠かせない情報です 必ずお読みください 再審査結果 使用上の注意改訂のお知らせ 経皮的エタノール注入療法用剤 処方せん医薬品 ( 注意 医師等の処方せんにより使用すること ) 無水エタノール注 フソー このたび経皮的エタノール注入療法用剤無水エタノール注 フソー につきまして 薬事法第 14 条の 4 第 3 項の規定による再審査が終了し 再審査結果が通知されました その結果 効能
医薬品の適正使用に欠かせない情報です 必ずお読みください 再審査結果 使用上の注意改訂のお知らせ 経皮的エタノール注入療法用剤 処方せん医薬品 ( 注意 医師等の処方せんにより使用すること ) 無水エタノール注 フソー このたび経皮的エタノール注入療法用剤無水エタノール注 フソー につきまして 薬事法第 14 条の 4 第 3 項の規定による再審査が終了し 再審査結果が通知されました その結果 効能
ラベプラゾールナトリウム錠20 ㎎「日医工」
 患者向医薬品ガイド 2017 年 12 月更新 ラベプラゾールナトリウム錠 20 mg 日医工 この薬は? 販売名 一般名 含有量 (1 錠中 ) ラベプラゾールナトリウム錠 20 mg 日医工 Rabeprazole Na Tablets 20mg ラベプラゾールナトリウム Rabeprazole Sodium 20mg 患者向医薬品ガイドについて 患者向医薬品ガイドは 患者の皆様や家族の方などに
患者向医薬品ガイド 2017 年 12 月更新 ラベプラゾールナトリウム錠 20 mg 日医工 この薬は? 販売名 一般名 含有量 (1 錠中 ) ラベプラゾールナトリウム錠 20 mg 日医工 Rabeprazole Na Tablets 20mg ラベプラゾールナトリウム Rabeprazole Sodium 20mg 患者向医薬品ガイドについて 患者向医薬品ガイドは 患者の皆様や家族の方などに
<4D F736F F D2089BB8A7797C C B B835888E790AC8C7689E6>
 2012 年 4 月更新作成者 : 宇根底亜希子 化学療法看護エキスパートナース育成計画 1. 目的江南厚生病院に通院あるいは入院しているがん患者に質の高いケアを提供できるようになるために 看護師が化学療法分野の知識や技術を習得することを目的とする 2. 対象者 1 ) レベル Ⅱ 以上で各分野の知識と技術習得を希望する者 2 ) 期間中 80% 以上参加できる者 3. 教育期間 時間間 1 年間の継続教育とする
2012 年 4 月更新作成者 : 宇根底亜希子 化学療法看護エキスパートナース育成計画 1. 目的江南厚生病院に通院あるいは入院しているがん患者に質の高いケアを提供できるようになるために 看護師が化学療法分野の知識や技術を習得することを目的とする 2. 対象者 1 ) レベル Ⅱ 以上で各分野の知識と技術習得を希望する者 2 ) 期間中 80% 以上参加できる者 3. 教育期間 時間間 1 年間の継続教育とする
医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能
 医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 1 2 3 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能 ) ( 医薬品の名称のみで検索する場合 34 の項目は未選択 未入力で可 ) 検索結果で表示したい文書を選択
医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 1 2 3 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能 ) ( 医薬品の名称のみで検索する場合 34 の項目は未選択 未入力で可 ) 検索結果で表示したい文書を選択
スライド 1
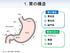 1. 胃の構造 胃の構造 胃底部 胃底部 胃体部 幽門部 胃液の成分ペプシン胃酸粘液 1. 胃の構造 胃の構造と役割 噴門胃底部胃体部幽門部 粘液を分泌胃酸 ( 塩酸 ) ペプシンを分泌胃酸 ( 塩酸 ) ペプシンを分泌ガストリンを血液中に分泌 ペプシン 胃酸 粘液 タンパク質を分解 病原菌の殺菌やペプシノーゲンの活性化 ペプシンや胃酸から胃粘膜を保護 1. 復習 胃の構造と役割 噴門 胃底部 胃体部
1. 胃の構造 胃の構造 胃底部 胃底部 胃体部 幽門部 胃液の成分ペプシン胃酸粘液 1. 胃の構造 胃の構造と役割 噴門胃底部胃体部幽門部 粘液を分泌胃酸 ( 塩酸 ) ペプシンを分泌胃酸 ( 塩酸 ) ペプシンを分泌ガストリンを血液中に分泌 ペプシン 胃酸 粘液 タンパク質を分解 病原菌の殺菌やペプシノーゲンの活性化 ペプシンや胃酸から胃粘膜を保護 1. 復習 胃の構造と役割 噴門 胃底部 胃体部
用法・用量DB
 データベース データベースの概要 医療用医薬品の添付文書に記載されているに関するデータベースです 処方薬の適正な投与量 ( 上限 下限 ) や投与日数 ( 上限 下限 ) などのチェック および患者さんへの服薬指導にご利用いただくことが可能です 本データベースは 医療用医薬品の添付文書に記載されているの情報を網羅しています データベースの特徴 年齢や体重 体表面積 適応病名 投与経路 療法毎にデータを作成しているため
データベース データベースの概要 医療用医薬品の添付文書に記載されているに関するデータベースです 処方薬の適正な投与量 ( 上限 下限 ) や投与日数 ( 上限 下限 ) などのチェック および患者さんへの服薬指導にご利用いただくことが可能です 本データベースは 医療用医薬品の添付文書に記載されているの情報を網羅しています データベースの特徴 年齢や体重 体表面積 適応病名 投与経路 療法毎にデータを作成しているため
より詳細な情報を望まれる場合は 担当の医師または薬剤師におたずねください また 患者向医薬品ガイド 医療専門家向けの 添付文書情報 が医薬品医療機器総合機構のホームページに掲載されています
 くすりのしおり内服剤 2014 年 6 月作成薬には効果 ( ベネフィット ) だけでなく副作用 ( リスク ) があります 副作用をなるべく抑え 効果を最大限に引き出すことが大切です そのために この薬を使用される患者さんの理解と協力が必要です 商品名 : バルサルタン錠 20mg AA 主成分 : バルサルタン (Valsartan) 剤形 : 淡黄色の錠剤 直径約 7.2mm 厚さ約 3.1mm
くすりのしおり内服剤 2014 年 6 月作成薬には効果 ( ベネフィット ) だけでなく副作用 ( リスク ) があります 副作用をなるべく抑え 効果を最大限に引き出すことが大切です そのために この薬を使用される患者さんの理解と協力が必要です 商品名 : バルサルタン錠 20mg AA 主成分 : バルサルタン (Valsartan) 剤形 : 淡黄色の錠剤 直径約 7.2mm 厚さ約 3.1mm
ネキシウムカプセル10mg/ネキシウムカプセル20mg
 NEX-10.0 **2018 年 1 月改訂 ( 第 10 版 ) * 2016 年 2 月改訂 処方箋医薬品 : 注意 - 医師等の処方箋により使用すること 貯法 : 室温保存使用期限 : ケース等に表示 プロトンポンプ インヒビター エソメプラゾールマグネシウム水和物カプセル 日本標準商品分類番号 872329 10mg 20mg 承認番号 22300AMX00598 22300AMX00599
NEX-10.0 **2018 年 1 月改訂 ( 第 10 版 ) * 2016 年 2 月改訂 処方箋医薬品 : 注意 - 医師等の処方箋により使用すること 貯法 : 室温保存使用期限 : ケース等に表示 プロトンポンプ インヒビター エソメプラゾールマグネシウム水和物カプセル 日本標準商品分類番号 872329 10mg 20mg 承認番号 22300AMX00598 22300AMX00599
タフィンラーカプセル50mg/75mg、メキニスト錠0.5mg/2mg 添付文書改訂のお知らせ
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 添付文書改訂のお知らせ 製造販売 2018 年 7 月 このたび 標記製品の効能又は効果の一部変更承認に伴い 添付文書の記載内容を改訂いたしましたのでお知らせいたします 今後のご使用に際しましてご参照下さいますようお願い申し上げます 効能又は効果 ( タフィンラーカプセル メキニスト錠共通 ) 改訂後 (2018 年 7 月改訂 ) 効能又は効果
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 添付文書改訂のお知らせ 製造販売 2018 年 7 月 このたび 標記製品の効能又は効果の一部変更承認に伴い 添付文書の記載内容を改訂いたしましたのでお知らせいたします 今後のご使用に際しましてご参照下さいますようお願い申し上げます 効能又は効果 ( タフィンラーカプセル メキニスト錠共通 ) 改訂後 (2018 年 7 月改訂 ) 効能又は効果
第 2 部 CTD の概要 一般名 : エソメプラゾールマグネシウム水和物 版番号 : 緒言 ネキシウム カプセル ネキシウム 懸濁用顆粒分包 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています
 第 2 部 CTD の概要 一般名 : エソメプラゾールマグネシウム水和物 版番号 : 2.6.1 緒言 ネキシウム カプセル ネキシウム 懸濁用顆粒分包 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています 2.6.1 緒言一般名 : エソメプラゾールマグネシウム水和物 目次 頁 目次... 2 略語及び専門用語一覧表...
第 2 部 CTD の概要 一般名 : エソメプラゾールマグネシウム水和物 版番号 : 2.6.1 緒言 ネキシウム カプセル ネキシウム 懸濁用顆粒分包 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています 2.6.1 緒言一般名 : エソメプラゾールマグネシウム水和物 目次 頁 目次... 2 略語及び専門用語一覧表...