フィニバックス点滴静注用・キット
|
|
|
- あきみ とどろき
- 4 years ago
- Views:
Transcription
1 **2013 年 3 月改訂 ( 第 13 版, 薬食安通知等に基づく使用上の注意の項の改訂 ) *2012 年 5 月改訂貯法 : 室温保存 ( 取扱い上の注意 の項参照) 使用期限 : 外箱等に表示 ( 使用期間 3 年 ) カルバペネム系抗生物質製剤処方せん医薬品注 1) 日本標準商品分類番号 点滴静注用 0.25g 点滴静注用 0.5g キット点滴静注用 承認番号 22300AMX AMX AMX00577 薬価収載 2011 年 11 月 2011 年 9 月 2011 年 11 月 販売開始 2005 年 9 月 2011 年 11 月 2006 年 6 月 効能追加 2012 年 5 月 2012 年 5 月 2012 年 5 月 国際誕生 2005 年 7 月 2005 年 7 月 2005 年 7 月 注射用ドリペネム水和物 禁忌 ( 次の患者には投与しないこと ) 1. 本剤の成分によるショックの既往歴のある患者 2. バルプロ酸ナトリウムを投与中の患者 [ てんかんの発作が再発するおそれがある ( 相互作用 の項参照)] 原則禁忌 ( 次の患者には投与しないことを原則とするが, 特に必要とする場合には慎重に投与すること ) 本剤の成分に対し過敏症の既往歴のある患者 1. 組成 販売名 成分 含量 2. 性状 販売名 性状 剤形 ph 浸透圧比 に対する比 フィニバックス点滴静注用 0.25g 1 瓶中ドリペネム水和物 0.25g( 力価 ) フィニバックス点滴静注用 0.25g 白色 ~ 微黄褐白色の結晶性の粉末である ( 注射剤 ) 4.5~6.0 10mg( 力価 )/ml 水溶液 約 1 2.5mg( 力価 )/ml 組成 性状 フィニバックス点滴静注用 0.5g 1 瓶中ドリペネム水和物 0.5g( 力価 ) フィニバックス点滴静注用 0.5g フィニバックスキット点滴静注用 0.25g 1 キット中ドリペネム水和物 0.25g( 力価 ) フィニバックスキット点滴静注用 0.25g 白色 ~ 微黄褐白色の白色 ~ 微黄褐白色の結結晶性の粉末である 晶性の粉末である ( 注 ( 注射剤 ) 射剤 ) 4.5~6.0 10mg( 力価 )/ml 水溶液 約 1 5mg( 力価 )/ml 4.5~ mg( 力価 )/ml 約 1 2.5mg( 力価 )/ml 1 キット中添付溶解液 - - 日局 100mL キット :1 つのプラスチック容器に隔壁を設けて, 上室に薬剤, 下室に溶解液を充てんした注射剤 効能 効果 * < 適応菌種 > ドリペネムに感性のブドウ球菌属, レンサ球菌属, 肺炎球菌, 腸球菌属 ( エンテロコッカス フェシウムを除く ), モラクセラ ( ブランハメラ ) カタラーリス, 大腸菌, シトロバクター属, クレブシエラ属, エンテロバクター属, セラチア属, プロテウス属, モルガネラ モルガニー, プロビデンシア属, インフルエンザ菌, 緑膿菌, アシネトバクター属, ペプトストレプトコッカス属, バクテロイデス属, プレボテラ属 < 適応症 > 敗血症, 感染性心内膜炎 深在性皮膚感染症, リンパ管 リンパ節炎 外傷 熱傷及び手術創等の二次感染 骨髄炎, 関節炎 咽頭 喉頭炎, 扁桃炎 ( 扁桃周囲炎, 扁桃周囲膿瘍を含む ) 肺炎, 肺膿瘍, 膿胸, 慢性呼吸器病変の二次感染 複雑性膀胱炎, 腎盂腎炎, 前立腺炎 ( 急性症, 慢性症 ), 精巣上体炎 ( 副睾丸炎 ) 腹膜炎, 腹腔内膿瘍 胆嚢炎, 胆管炎, 肝膿瘍 子宮内感染, 子宮付属器炎, 子宮旁結合織炎 化膿性髄膜炎 眼窩感染, 角膜炎 ( 角膜潰瘍を含む ), 眼内炎 ( 全眼球炎を含む ) 中耳炎 顎骨周辺の蜂巣炎, 顎炎 用法 用量 * 通常, 成人にはドリペネムとして 1 回 0.25g( 力価 ) を1 日 2 回又は 3 回,30 分以上かけて点滴静注する なお, 年齢 症状に応じて適宜増減するが, 重症 難治性感染症には,1 回 0.5g( 力価 ) を1 日 3 回投与し, 増量が必要と判断される場合に限り 1 回量として 1.0g( 力価 ),1 日量として 3.0g( 力価 ) まで投与できる 通常, 小児にはドリペネムとして 1 回 20mg( 力価 )/kgを1 日 3 回, 30 分以上かけて点滴静注する なお, 年齢 症状に応じて適宜増減するが, 重症 難治性感染症には,1 回 40mg( 力価 )/kg まで増量することができる ただし, 投与量の上限は 1 回 1.0g( 力価 ) までとする < 用法 用量に関連する使用上の注意 > 1. 注射液の調製方法 (1) フィニバックス点滴静注用 0.25g( 力価 )10mL 容量瓶, フィニバックス点滴静注用 0.5g( 力価 )20mL 容量瓶通常, 100mL を用いて, よく振盪して溶解する 注射用水は溶液が等張とならないため使用しないこと また, L-システイン及び L-シスチンを含むアミノ酸製剤と配合すると, 著しく力価が低下するので, 配合しないこと (2) フィニバックスキット点滴静注用 0.25g( 力価 ) 溶解液 ( 日局 ) 部分を手で押して隔壁を開通させ, 更に溶解液部分を繰り返し押して薬剤を完全に溶解する ( 詳しい溶解方法については, キット製品の外袋及びカバーシートに記載の溶解操作方法を参照のこと ) 2. 高度の腎障害のある患者では, 投与量を減らすか, 投与間隔をあけるなど患者の状態を十分に観察し, 慎重に投与すること 腎機能障害患者への投与に際しては, 下表を目安に投与量を調節すること [ 慎重投与 及び 薬物動態 の項参照] 注 1) 注意 - 医師等の処方せんにより使用すること (1)
2 フィニバックス点滴静注用 キット (2) 腎機能正常者の 1 日投与量に対応する Ccr 別の 1 日投与量の目安 Ccr 腎機能正常者 (70 Ccr) の1 日投与量に対応する 1 日投与量 ( 力価 ) (ml/min) 0.25g 2 回 0.25g 3 回 0.5g 3 回 1.0g 3 回 50 Ccr< g 2 回 0.25g 2~3 回 0.5g 2~3 回 1.0g 2 回 1 30 Ccr< g 2 回 0.25g 3 回又は 0.5g 2 回 0.5g 3 回 Ccr< g 2 回 g 3 回 2 Ccr: クレアチニンクリアランス 1:1.0g 3 回投与は避けることが望ましい 2: 低体重患者では安全性に留意し, 慎重に投与すること 3. 本剤の使用にあたっては, 耐性菌の発現等を防ぐため, 原則として感受性を確認し, 疾病の治療上必要な最小限の期間の投与にとどめること 4. 本剤の使用に際しては, 投与開始後 3 日を目安として更に継続投与が必要か判定し, 投与中止又はより適切な他剤に切り替えるべきか検討を行うこと 使用上の注意 **,* 1. 慎重投与 ( 次の患者には慎重に投与すること ) (1) ドリペネムに関する注意 1) カルバペネム系, ペニシリン系又はセフェム系抗生物質に対し過敏症の既往歴のある患者 2) 本人又は両親, 兄弟に気管支喘息, 発疹, 蕁麻疹等のアレルギー症状を起こしやすい体質を有する患者 3) 高度の腎障害のある患者 [ 血中からの消失が遅延する また, 痙攣, 意識障害等の中枢神経症状が起こりやすい ( 用法 用量に関連する使用上の注意, 重大な副作用 及び 薬物動態 の項参照 )] 4) 肝障害のある患者 [ 肝障害が悪化するおそれがある ] 5) 経口摂取の不良な患者又は非経口栄養の患者, 全身状態の悪い患者 [ ビタミン K 欠乏症状があらわれることがあるので観察を十分に行うこと ] 6) 高齢者 [ 高齢者への投与 の項参照] 7) てんかんの既往歴あるいは中枢神経障害を有する患者 [ 痙攣, 意識障害等の中枢神経症状が起こりやすい ( 重大な副作用 の項参照 )] (2) に関する注意 1) 心臓, 循環器系機能障害のある患者 [ ナトリウムの負荷及び循環血液量を増すことから心臓に負担をかけ, 症状が悪化するおそれがある ] 2) 腎障害のある患者 [ 水分, 塩化ナトリウムの過剰投与に陥りやすく, 症状が悪化するおそれがある ] 2. 重要な基本的注意 (1) 本剤によるショック, アナフィラキシーの発生を確実に予知できる方法がないので, 次の措置をとること 1) 事前に既往歴等について十分な問診を行うこと なお, 抗生物質等によるアレルギー歴は必ず確認すること 2) 投与に際しては, 必ずショック等に対する救急処置のとれる準備をしておくこと 3) 投与開始から投与終了後まで, 患者を安静の状態に保たせ, 十分な観察を行うこと 特に, 投与開始直後は注意深く観察すること (2) 発疹等の副作用の発現には特に注意し, 症状が発現した時には, 他剤に切り替えるなど適切な処置を講じること なお, 継続使用にあたっても, 引き続き副作用症状に注意すること 3. 相互作用併用禁忌 ( 併用しないこと ) 薬剤名等臨床症状 措置方法機序 危険因子バルプロ酸ナトリウムバルプロ酸の血中濃度が低下機序は不明デパケン, バレリン, し, てんかんの発作が再発すハイセレニン等るおそれがある 4. 副作用 < 成人 > 承認時における安全性評価対象例 835 例中, 副作用は 37 例 (4.4%) に認められた 主なものは, 下痢 6 例 (0.7%), 発疹 5 例 (0.6%) であった また, 臨床検査値の異常変動は, 検査を実施した安全性評価対象例 818 例中,195 例 (23.8%) に認められた 主なものは,ALT(GPT) 上昇 102 例 /806 例 (12.7%),AST(GOT) 上昇 78 例 /807 例 (9.7%) であった 重症 難治性感染症患者を対象とした 1 回 1.0g( 力価 )1 日 3 回投与による臨床試験の安全性評価対象例 101 例中, 臨床検査値異常を含む副作用は 42 例 (41.6%) に認められた 主なものは,ALT(GPT) 上昇 14 例 (13.9%),AST(GOT) 上昇 13 例 (12.9%),γ-GTP 上昇 9 例 (8.9%), 下痢 9 例 (8.9%),Al- P 上昇 7 例 (6.9%) であった < 小児 > 承認時における安全性評価対象例 107 例中, 臨床検査値異常を含む副作用は 30 例 (28.0%) に認められた 主なものは, 下痢 14 例 (13.1%), 血小板増多 6 例 (5.6%),ALT(GPT) 上昇 6 例 (5.6%) であった (1) 重大な副作用 1) ショック, アナフィラキシー ( 頻度不明 ): ショック, アナフィラキシーを起こすことがあるので, 観察を十分に行い, 不快感, 口内異常感, 喘鳴, 眩暈, 便意, 耳鳴, 発汗等があらわれた場合には投与を中止し, 適切な処置を行うこと 2) 偽膜性大腸炎 (0.1~1%): 偽膜性大腸炎等の血便を伴う重篤な大腸炎があらわれることがあるので, 腹痛, 頻回の下痢があらわれた場合には直ちに投与を中止するなど適切な処置を行うこと 3) 肝機能障害, 黄疸 ( 頻度不明 ): 肝機能障害, 黄疸があらわれることがあるので, 定期的に検査を行うなど観察を十分に行い, 異常が認められた場合には投与を中止し, 適切な処置を行うこと 4) 急性腎不全 ( 頻度不明 ): 急性腎不全等の重篤な腎障害があらわれることがあるので, 定期的に検査を行うなど観察を十分に行い, 異常が認められた場合には投与を中止し, 適切な処置を行うこと 5) 汎血球減少症, 無顆粒球症, 白血球減少, 血小板減少 ( 頻度不明 ): 汎血球減少症, 無顆粒球症, 白血球減少, 血小板減少があらわれることがあるので, 定期的に血液検査を行うなど観察を十分に行い, 異常が認められた場合には投与を中止し, 適切な処置を行うこと 6) 中毒性表皮壊死融解症 (Toxic Epidermal Necrolysis:TEN), 皮膚粘膜眼症候群 (Stevens-Johnson 症候群 )( 頻度不明 ): 中毒性表皮壊死融解症, 皮膚粘膜眼症候群があらわれることがあるので, 観察を十分に行い, 異常が認められた場合には投与を中止し, 適切な処置を行うこと 7) 間質性肺炎 ( 頻度不明 ): 間質性肺炎があらわれることがあるので, 観察を十分に行い, 発熱, 咳嗽, 呼吸困難等の異常が認められた場合には速やかに胸部 X 線検査等を実施し, 間質性肺炎が疑われる場合には投与を中止し, 副腎皮質ホルモン剤の投与等の適切な処置を行うこと 8) 痙攣, 意識障害 ( 頻度不明 ): 痙攣, 意識障害等の中枢神経症状があらわれることがあるので, 観察を十分に行い, このような症状があらわれた場合には直ちに投与を中止し, 適切な処置を行うこと 特に腎障害や, 脳血管障害等の中枢神経障害のある患者に起こりやすいので, 投与する場合には注意すること (2) 重大な副作用 ( 類薬 ) 1) 溶血性貧血 : 他のカルバペネム系抗生物質で, 溶血性貧血があらわれることが報告されているので, 定期的に血液検査を行うなど観察を十分に行い, 異常が認められた場合には投与を中止し, 適切な処置を行うこと (2)
3 フィニバックス点滴静注用 キット (3) 2) 肺好酸球増加症 (PIE 症候群 ): 他のカルバペネム系抗生物質で, 発熱, 咳嗽, 呼吸困難, 胸部 X 線異常, 好酸球増多等を伴う肺好酸球増加症 (PIE 症候群 ) があらわれることが報告されているので, 観察を十分に行い, 異常が認められた場合には投与を中止し, 適切な処置を行うこと 3) 血栓性静脈炎 : 他のカルバペネム系抗生物質で, 血栓性静脈炎があらわれることが報告されているので, 観察を十分に行い, 異常が認められた場合には投与を中止し, 適切な処置を行うこと (3) その他の副作用次のような副作用があらわれた場合には, 必要に応じて, 減量又は投与を中止するなど適切な処置を行うこと 種類 \ 頻度 5% 以上 0.5~5% 未満 0.5% 未満頻度不明発疹そう痒, 発熱, 過敏症注 1 発赤, 蕁麻疹 血液 肝臓 腎臓 消化器 顆粒球減少, 貧血 ( 赤血球減血小板増多, 少, ヘモグロビ好酸球増多ン減少, ヘマトクリット減少 ), 血小板減少, 好塩基球増多 AST(GOT) 上 LDH 上昇,Al- 昇, A L T P 上昇,γ- (GPT) 上昇 GTP 上昇,LAP 上昇, ビリルビン上昇 下痢 BUN 上昇 嘔気, 嘔吐, 胃不快感, 腹痛 血清クレアチニン上昇 食欲不振 精神神経系 しびれ感, 振戦 菌交代症 口内炎 カンジダ症 ビタミン欠乏症 その他 血清カリウム上昇 頭痛, 倦怠感, ほてり, 注射部位血管痛 注 1: 症状があらわれた場合には投与を中止すること ビタミン K 欠乏症状 ( 低プロトロンビン血症, 出血傾向等 ), ビタミン B 群欠乏症状 ( 舌炎, 口内炎, 食欲不振, 神経炎等 ) 電解質異常 ( 血清カリウム, 血清ナトリウム, 血清クロール ) 5. 高齢者への投与 (1) 本剤は腎排泄型の薬剤であり, 高齢者では一般に生理機能が低下していることが多いので, 用量並びに投与間隔に留意するなど患者の状態を観察しながら慎重に投与すること (2) 高齢者では, ビタミン K 欠乏による出血傾向があらわれることがある 6. 妊婦, 産婦, 授乳婦等への投与 (1) 妊婦又は妊娠している可能性のある婦人には, 治療上の有益性が危険性を上回ると判断される場合にのみ投与すること [ 妊娠中の投与に関する安全性は確立していない ] (2) 投与中は授乳を避けさせること [ 動物試験 ( ラット ) で母乳中へ移行することが報告されている ] 7. 小児等への投与低出生体重児, 新生児に対する安全性は確立していない [ 使用経験がない ] 8. 臨床検査結果に及ぼす影響 (1) テステープ反応を除くベネディクト試薬, フェーリング試薬, クリニテストによる尿糖検査では偽陽性を呈することがあるので注意すること (2) 直接クームス試験陽性を呈することがあるので注意すること (3) ウロビリノーゲン検査では偽陽性を呈することがあるので注意 すること 9. 適用上の注意 (1) 投与経路 : 本剤は点滴静脈内注射にのみ使用すること (2) 調製方法 : 通常, 100mL を用いて, よく振盪して溶解する 注射用水は溶液が等張とならないため使用しないこと また,L-システイン及び L-シスチンを含むアミノ酸製剤と配合すると, 著しく力価が低下するので, 配合しないこと (3) 調製時 1) 調製後は速やかに使用すること なお, やむを得ず保存を必要とする場合でも日局に溶解した場合, 室温保存では 8 時間以内に, 冷蔵庫保存では 24 時間以内に使用すること ( 取扱い上の注意 の項参照) 2) キット製品の場合は残液は決して使用しないこと 薬物動態 * 1. 血漿中濃度 (1) 健康成人健康成人男性各 6 例に 0.25g( 力価 ),0.5g( 力価 ) 及び 1.0g ( 力価 ) を 30 分かけて単回点滴静注したときの血漿中濃度及び薬物動態パラメータを図 1 表 1 に示す 反復投与での体内動態は単回投与時とほとんど変わらなかった 1) 投与量 g( 力価 ) n 表 1 薬物動態パラメータ Cmax AUC0-12 T1/2(β) (hr) ± ± ± ± ± ± ± ± ±0.09 ( 測定法 :bioassay)(mean±s.d.) (2) 小児患者小児患者 (2 ヵ月 ~13 歳 )99 例に 20mg( 力価 )/kg 体重 25kg 以上は 0.5g( 力価 ) を 30 分以上かけて点滴静注したときの血漿中濃度 (190 ポイント ) を図 2 に示す また, 母集団薬物動態解析結果に基づいて推定した薬物曝露量を表 2 に示す 2) (3)
4 フィニバックス点滴静注用 キット (4) 表 2 小児における薬物曝露量推定値注 1 (1 日 3 回投与 ) 投与量注 2 mg( 力価 )/kg n Cmax 1 日あたりの AUC ± ±23.1 注 1:NONMEM ぢを用いて推定注 2: 体重 25kg 以上は 0.5g( 力価 ) (mean±s.d.) (3) 高齢者健康高齢者 (66~69 歳 )6 例に 0.25g( 力価 ) を 30 分かけて単回点滴静注したとき, 高齢者では非高齢者に比べて血中からの消失が遅延する傾向が認められるものの,Cmax に有意な差はみられなかった 3) 表 3 薬物動態パラメータ 投与量 g( 力価 ) n Cmax AUC0-24 T1/2(β) (hr) 高齢者 ± ± ±0.19 非高齢者 ± ±3.48 注 ±0.08 注 1:AUC0-12 ( 測定法 :bioassay)(mean±s.d.) (4) 腎機能障害患者 1) 腎機能障害患者 12 例に 0.25g( 力価 ) を 30 分かけて単回点滴静注したとき, 腎機能の低下に伴い, 血中からの消失が遅延する傾向が認められた 4) Ccr (ml/min) n 表 4 薬物動態パラメータ Cmax AUC0-24 T1/2(β) (hr) 50 Ccr< ± ± ± Ccr< ± ± ±0.32 Ccr< Ccr: クレアチニンクリアランス ( 測定法 :bioassay,hplc)(mean±s.d.) 2) 健康成人, 腎機能障害患者及び健康高齢者の 92 例から得られた 921 ポイントの血漿中濃度について, 母集団薬物動態解析を行った 本剤の薬物動態に対する影響因子として, 腎機能障害の程度 (Ccr) の影響が大きく,Ccr に応じた投与量の調節が必要であると考えられた 5) Ccr 別の 1 日投与量ごとの曝露量 (1 日あたりの AUC) を表 5 に示す また,Ccr に応じた投与量の調節は, 用法 用量に関連する使用上の注意 の Ccr 別の 1 日投与量の目安を参考にすること 表 5 Ccr 別の 1 日投与量ごとの 1 日あたりの AUC( 定常状態 ) 注 1 Ccr (ml/min) 105 Ccr 70 Ccr < Ccr <70 30 Ccr <50 Ccr< g 2 回 34.7 ( ) 41.3 ( ) 58.2 ( ) 82.9 ( ) 145 ( ) 1 日投与量ごとの 1 日あたりの AUC 0.25g 3 回 52.3 ( ) 62.2 ( ) 87.5 ( ) 124 ( ) 215 ( ) 0.5g 2 回 0.5g 3 回 1.0g 2 回 1.0g 3 回 69.4 ( ) 82.7 ( ) 117 ( ) 166 ( ) 293 ( ) 104 ( ) 124 ( ) 175 ( ) 250 ( ) 433 ( ) 139 ( ) 165 ( ) 233 ( ) 332 ( ) 587 ( ) 209 ( ) 250 ( ) 349 ( ) 498 ( ) 872 ( ) Ccr: クレアチニンクリアランス注 1: 中央値 (90% 予測範囲 ), 母集団薬物動態解析パラメータ (NONMEM ぢを用いて推定 ) によるシミュレーション結果 (5) 血液透析患者血液透析患者 6 例に 0.5g( 力価 ) を 1 時間かけて単回点滴静注したときの血漿中濃度を図 3 に示す 点滴開始 2 時間後から 4 時間かけて透析することにより血液透析未実施の場合と比較し て AUC は 43% に低下した 6) ( 外国人によるデータ ) 2. 分布皮膚組織, 関節液, 滑膜, 海綿骨, 皮質骨, 喀痰, 前立腺組織, 胆汁, 胆嚢, 腹腔内滲出液, 子宮 子宮付属器, 骨盤死腔液, 前房水, 中耳粘膜, 口蓋扁桃, 中耳分泌物, 歯肉, 嚢胞, 髄液への移行が認められた 7),8) ( 参考 ) 乳汁中移行授乳ラットに [ 14 C]-ドリペネム 20mg( 力価 )/kg を静脈内投与したときの乳汁中放射能濃度は投与 30 分後に最高濃度に達したが, 血漿中放射能濃度の約 1/6 であった 9) 3. 代謝 排泄 (1) 主として糸球体ろ過及び尿細管分泌により腎から尿中に排泄される 健康成人男性 6 例に 0.25g( 力価 ),0.5g( 力価 ) 及び 1.0g( 力価 ) を単回点滴静注したときの尿中排泄率は, 投与量に関係なく,24 時間までに未変化体として約 75%,βラクタム環が開裂したジカルボン酸体 ( 主代謝物 ) を含めると約 90% であった 1) (2) ヒト腎デヒドロペプチダーゼ-I に安定性を示す 10) 4. その他血清蛋白結合率 :0.5g( 力価 )1 日 2 回反復投与試験において限外ろ過法にて測定した血清蛋白結合率は約 9% であった 1) 臨床成績 * 1. 成人承認時における臨床試験での有効性評価対象例は 734 例であり, 有効率は 93.2%(684 例 ) であった 11) 表 6 臨床成績 疾患名 有効例数 / 有効性評価対象例数 有効率 (%) 敗血症, 感染性心内膜炎 11/ 深在性皮膚感染症, リンパ管 リンパ節炎 19/ 外科領域感染症外傷 熱傷及び手術創等の二次感染 20/ 整形外科領域感染症 骨髄炎, 関節炎 6/6 - 呼吸器感染症 咽頭 喉頭炎, 扁桃炎 ( 扁桃周囲炎, 扁桃周囲膿瘍を含む ), 肺炎, 肺膿瘍, 膿胸, 慢性呼吸器病変の二次感染 299/ 尿路感染症複雑性膀胱炎, 腎盂腎炎, 前立腺炎 ( 急性症, 慢性症 ), 精巣上体炎 ( 副睾丸炎 ) 198/ 腹腔内感染症 腹膜炎, 腹腔内膿瘍 33/ 肝 胆道感染症 胆嚢炎, 胆管炎, 肝膿瘍 22/ 産婦人科領域感染症子宮内感染, 子宮付属器炎, 子宮旁結合織炎 32/ (4)
5 フィニバックス点滴静注用 キット (5) 眼科領域感染症 疾患名 眼窩感染, 角膜炎 ( 角膜潰瘍を含む ), 眼内炎 ( 全眼球炎を含む ) 有効例数 / 有効性評価対象例数 有効率 (%) 15/ 耳鼻科領域感染症中耳炎 5/6 - 歯科 口腔外科領域顎骨周辺の蜂巣炎, 顎炎 24/ 感染症 重症 難治性感染症患者を対象とした 1 回 1.0g( 力価 )1 日 3 回投与による臨床試験で登録された 101 例のうち, 本剤 1 回 1.0g( 力価 )1 日 3 回投与が必要となる重症 難治性感染症患者で, かつ本剤単独での有効性評価が可能な症例を選択した結果, 有効性評価対象例は 73 例となり, 有効率は 75.3%(55 例 ) であった 12),13) 表 7 臨床成績 1 回 1.0g( 力価 )1 日 3 回投与 疾患名 有効例数 / 有効性評価対象例数 有効率 (%) 敗血症 27/ 肺炎 15/ 腹膜炎, 腹腔内膿瘍 12/ 手術創の二次感染 1/1-2. 小児承認時における臨床試験での有効性評価対象例は 100 例であり, 有効率は 97.0%(97 例 ) であった 7),14) 表 8 臨床成績 敗血症 疾患名 リンパ管 リンパ節炎呼吸器感染症咽頭 喉頭炎, 扁桃炎 ( 扁桃周囲炎, 扁桃周囲膿瘍を含む ), 肺炎 有効例数 / 有効性評価対象例数 有効率 (%) 5/5-2/2-61/ 尿路感染症 腎盂腎炎 11/ 化膿性髄膜炎 6/6 注 1 - 耳鼻科領域感染症 中耳炎 8/8 - 歯科 口腔外科領域顎骨周辺の蜂巣炎感染症 4/5 - 注 1: 本剤単剤での評価が可能であった症例は 6 例中 2 例であり, 他の 4 例はセフェム系抗生物質との併用療法での評価症例である 薬効薬理 1. 薬理作用好気性のグラム陽性菌, グラム陰性菌及び嫌気性菌に対して, 幅広い抗菌スペクトルを有し, 特に緑膿菌に対しては既存のカルバペネム系抗生物質に比べ強い抗菌力を有する 15) 2. 作用機序細菌の細胞壁合成酵素であるペニシリン結合蛋白 (PBP) に結合し, 細菌の細胞壁合成阻害により抗菌作用を発揮し, その作用は殺菌的である 黄色ブドウ球菌では PBP1 に, 緑膿菌では PBP2,3 に, 大腸菌では PBP2 に高い結合親和性を示した 15) 有効成分に関する理化学的知見 一般的名称 : ドリペネム水和物 (JAN) Doripenem Hydrate 略号 :DRPM 化学名 :(+)-(4R,5S,6S)-6-[(1R)-1-Hydroxyethyl]-4-methyl-7- oxo-3-[[(3s,5s)-5-[(sulfamoylamino)methyl]-3- pyrrolidinyl]thio]-1-azabicyclo[3.2.0]hept-2-ene-2- carboxylic acid monohydrate 分子式 :C15H24N4O6S2 H2O 分子量 : 化学構造式 : 性状 : 白色 ~ 微黄褐白色の結晶性の粉末である 水にやや溶けにくく, メタノールに溶けにくく, エタノール (99.5) にほとんど溶けない 融点 : 明確な融点を示さない (140 以上で徐々に着色する ) 分配係数 :0.002[1-オクタノール/ 水 ] 取扱い上の注意 1. キット製品では, 下記の点に注意すること (1) 製品の品質を保持するため, 本品を包んでいる外袋は使用時まで開封しないこと (2) 次の場合には使用しないこと 1) 外袋が破損しているときや溶解液が漏出しているとき 2) 隔壁の開通前に薬剤が溶解しているとき 3) 薬剤が変色しているときや, 薬剤溶解前に溶解液が着色しているとき (3) 容器の液目盛りはおよその目安として使用すること 2. 溶解時の安定性 0.25g 製剤 1 瓶及び 1 キットを 100mL に溶解したときの含量を表 9 に示す 表 9 溶解時の安定性 本剤 配合量 保存条件 含量注 1 (%) 8 時間保存後 24 時間保存後 瓶製品 mL 5 遮光 キット製品 mL 5 遮光 注 1: 初期値に対する残存率 (%) で表示, 測定法 ;HPLC 3. 主な輸液製剤との配合変化 0.25g 製剤 1 瓶を主な輸液製剤に溶解したときの含量を表 10 に示す 16) 表 10 主な輸液製剤との配合変化 輸液製剤 含量注 1 (%) 名称 配合量 8 時間保存後 24 時間保存後 5% ブドウ糖注射液 100mL EL-3 号輸液 500mL KN1 号輸液 500mL KN3 号輸液 500mL アクチット注 500mL ヴィーン D 注 500mL キリット注 5% 300mL ソリタ-T1 号輸液 500mL ソリタ-T3 号輸液 500mL フィジオゾール 3 号輸液 500mL ハルトマン液 ph:8- HD 500mL ラクテック G 輸液 500mL ポタコール R 輸液 500mL 注 1: 初期値に対する残存率 (%) で表示, 測定法 ;HPLC 保存条件 :25 包装 フィニバックス点滴静注用 0.25g:10 瓶 (10mL 容量瓶 ) フィニバックス点滴静注用 0.5g:10 瓶 (20mL 容量瓶 ) フィニバックスキット点滴静注用 0.25g:10 キット (5)
6 フィニバックス点滴静注用 キット (6) 主要文献 * 文献請求番号 1) 中島光好ほか : 日本化学療法学会雑誌,2005,53(S-1), ) 社内資料 ( 小児患者における薬物動態 ) ) 中島光好ほか : 日本化学療法学会雑誌,2005,53(S-1), ) 上原慎也ほか : 日本化学療法学会雑誌,2005,53(S-1), ) 社内資料 ( 母集団薬物動態解析 ) ) 社内資料 ( 血液透析患者における薬物動態 ) ) 社内資料 ( 国内第 3 相試験 ( 化膿性髄膜炎 )) ) 塩野義製薬集計 ; 荒田次郎ほか : 日本化学療法学会雑誌, 2005,53(S-1), を含む 10 文献 9) 社内資料 ( ラットにおける乳汁移行性 ) ) 山野佳則ほか : 日本化学療法学会雑誌,2005,53(S-1), ) 塩野義製薬集計 ; 齊藤厚ほか : 日本化学療法学会雑誌,2005,53 (S-1), を含む 17 文献 12) 社内資料 ( 国内第 3 相試験 ( 高用量 血液内科 )) ) 社内資料 ( 国内第 3 相試験 ( 高用量 血液内科以外 )) ) 社内資料 ( 国内第 3 相試験 ( 一般感染症 )) ) 藤村亨滋ほか : 日本化学療法学会雑誌,2005,53(S-1), ) 社内資料 ( フィニバックスの配合変化表 ) 文献請求先 主要文献に記載の社内資料につきましても下記にご請求ください 塩野義製薬株式会社医薬情報センター 大阪市中央区道修町 3 丁目 1 番 8 号電話 FAX 製造販売元 FBX 17 DA (6) ぢ : 登録商標
フィニバックス点滴静注用・キット
 **2018 年 5 月改訂 ( 第 15 版, 使用上の注意の項等の自主改訂 ) *2017 年 6 月改訂貯法 : 室温保存 ( 取扱い上の注意 の項参照) 使用期限 : 外箱等に表示 ( 使用期間 3 年 ) カルバペネム系抗生物質製剤処方箋医薬品注 1) 日本標準商品分類番号 876139 点滴静注用 0.25g 点滴静注用 0.5g キット点滴静注用 承認番号 22300AMX00576
**2018 年 5 月改訂 ( 第 15 版, 使用上の注意の項等の自主改訂 ) *2017 年 6 月改訂貯法 : 室温保存 ( 取扱い上の注意 の項参照) 使用期限 : 外箱等に表示 ( 使用期間 3 年 ) カルバペネム系抗生物質製剤処方箋医薬品注 1) 日本標準商品分類番号 876139 点滴静注用 0.25g 点滴静注用 0.5g キット点滴静注用 承認番号 22300AMX00576
改訂の理由及び調査の結果直近 3 年度の国内副作用症例の集積状況 転帰死亡症例 国内症例が集積したことから専門委員の意見も踏まえた調査の結果 改訂することが適切と判断した 低カルニチン血症関連症例 16 例 死亡 0 例
 ピボキシル基を有する抗菌薬の 使用上の注意 の改訂について 成分名該当商品名効能 効果改訂の概要 成分名該当商品名 ( 承認取得者 ) 1セフカペンピボキシ 1フロモックス小児用細粒 100mg 同錠ル塩酸塩水和物 75mg 同錠 100mg( 塩野義製薬株式 2セフジトレンピボキ会社 ) 他シル 2メイアクト MS 小児用細粒 10% 同 3セフテラムピボキシ MS 錠 100mg(Meiji Seika
ピボキシル基を有する抗菌薬の 使用上の注意 の改訂について 成分名該当商品名効能 効果改訂の概要 成分名該当商品名 ( 承認取得者 ) 1セフカペンピボキシ 1フロモックス小児用細粒 100mg 同錠ル塩酸塩水和物 75mg 同錠 100mg( 塩野義製薬株式 2セフジトレンピボキ会社 ) 他シル 2メイアクト MS 小児用細粒 10% 同 3セフテラムピボキシ MS 錠 100mg(Meiji Seika
使用上の注意の改訂理由 副作用( その他の副作用 ) 妊婦, 産婦, 授乳婦等への投与 臨床検査結果に及ぼす影響 の項の改訂について ( 薬生安通知によらない改訂 ) 先発医薬品の改訂に伴い 同様の改訂を行い注意をお願いすることとしました ここでお知らせした内容は 田辺製薬販売株式会社ホームページ
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意改訂のお知らせ 2016 年 1 月 田辺製薬販売株式会社 製造販売元田辺三菱製薬株式会社 このたび 標記製品につきまして 使用上の注意 を改訂しましたのでお知らせ致します 今後のご使用に際しましては 下記内容をご参照下さいますようお願い致します 改訂概要 改訂項目 副作用 ( その他の副作用 ) 改訂内容 コリンエステラーゼ低下
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意改訂のお知らせ 2016 年 1 月 田辺製薬販売株式会社 製造販売元田辺三菱製薬株式会社 このたび 標記製品につきまして 使用上の注意 を改訂しましたのでお知らせ致します 今後のご使用に際しましては 下記内容をご参照下さいますようお願い致します 改訂概要 改訂項目 副作用 ( その他の副作用 ) 改訂内容 コリンエステラーゼ低下
改訂の理由及び調査の結果直近 3 年度の国内副作用症例の集積状況 転帰死亡症例 アモキシシリン水和物及びクラブラン酸カリウム アモキシシリン水和物の国内症例が集積したことから 専門委員の意見も踏まえた調査の結果 改訂することが適切と判断した 血小板減少関連症例 1 アモキシシリン水和物 3 例 (
 アモキシシリン水和物含有製剤の 使用上の注意 の改訂について 成分名該当商品名効能 効果改訂の概要 成分名該当商品名 ( 承認取得者 ) 1 アモキシシリン水和物 1 サワシリンカプセル 125 同カプセ 2 クラブラン酸カリウル 250 同細粒 10% 同錠 250( アム アモキシシリン水ステラス製薬株式会社 ) パセト和物シンカプセル 125 同カプセル 3 ランソプラゾール ア 250 同細粒
アモキシシリン水和物含有製剤の 使用上の注意 の改訂について 成分名該当商品名効能 効果改訂の概要 成分名該当商品名 ( 承認取得者 ) 1 アモキシシリン水和物 1 サワシリンカプセル 125 同カプセ 2 クラブラン酸カリウル 250 同細粒 10% 同錠 250( アム アモキシシリン水ステラス製薬株式会社 ) パセト和物シンカプセル 125 同カプセル 3 ランソプラゾール ア 250 同細粒
(Microsoft PowerPoint - \201iweb\214\374\201j2009_11 \222\307\225\342\225i\224\255\224\204\210\304\223\340.PPT)
 平成 21 年 11 月 13 日 Drug Information 平成 21 年 11 月度追補品販売のごのご案内 謹啓時下ますますご清栄のこととお慶び申し上げます 平素は 格別のご高配を賜り 厚く御礼申し上げます さて この度平成 21 年 11 月 13 日付官報にて アムロジピン OD 錠 2.5mg 5mg KRM サルポグレラートサルポグレラート塩酸塩錠 50mg 100mg KRM
平成 21 年 11 月 13 日 Drug Information 平成 21 年 11 月度追補品販売のごのご案内 謹啓時下ますますご清栄のこととお慶び申し上げます 平素は 格別のご高配を賜り 厚く御礼申し上げます さて この度平成 21 年 11 月 13 日付官報にて アムロジピン OD 錠 2.5mg 5mg KRM サルポグレラートサルポグレラート塩酸塩錠 50mg 100mg KRM
審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7
![審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7 審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7](/thumbs/92/110490968.jpg) 審査報告書 平成 26 年 1 月 6 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [
審査報告書 平成 26 年 1 月 6 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [
使用上の注意 1. 慎重投与 ( 次の患者には慎重に投与すること ) 1 2X X 重要な基本的注意 1TNF 2TNF TNF 3 X - CT X 4TNFB HBsHBcHBs B B B B 5 6TNF 7 8dsDNA d
 2015 5 7 201410 28 TNF 阻害薬 TNFFab シムジア 皮下注 200mg シリンジ Cimzia 200mg Syringe for S.C. Injection セルトリズマブペゴル ( 遺伝子組換え ) 製剤 873999 22400AMX01488000 20132 20133 20155 20079 警告 1. 2. 1 2 X - CT 3. TNF 4. 1 禁忌
2015 5 7 201410 28 TNF 阻害薬 TNFFab シムジア 皮下注 200mg シリンジ Cimzia 200mg Syringe for S.C. Injection セルトリズマブペゴル ( 遺伝子組換え ) 製剤 873999 22400AMX01488000 20132 20133 20155 20079 警告 1. 2. 1 2 X - CT 3. TNF 4. 1 禁忌
「ガスメット錠10mg・20mg」「ガスメットD錠10mg・20mg」使用上の注意改訂のお知らせ
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意改訂のお知らせ H2 受容体拮抗剤 このたび H2 受容体拮抗剤ガスメット錠 10mg ガスメット錠 20mg 及びガスメット D 錠 10mg ガスメット D 錠 20mg につきまして 自主改訂に基づき 使用上の注意を下記のとおり改訂致しましたので お知らせ申し上げます 平成 25 年 8 月 記 ガスメット錠 10mg ガスメット錠
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意改訂のお知らせ H2 受容体拮抗剤 このたび H2 受容体拮抗剤ガスメット錠 10mg ガスメット錠 20mg 及びガスメット D 錠 10mg ガスメット D 錠 20mg につきまして 自主改訂に基づき 使用上の注意を下記のとおり改訂致しましたので お知らせ申し上げます 平成 25 年 8 月 記 ガスメット錠 10mg ガスメット錠
ィニバックス点滴静注用 0.25 g 同キット点滴静注用 0.25 g に変更された ( 平成 23 年 6 月 7 日 ) 注 2) 新規有効成分含有医薬品の再審査期間について に係る通知 ( 平成 19 年 4 月 1 日付け薬食発第 号 ) に基づき 0.25 g 製剤の再審査
 再審査報告書 平成 29 年 10 月 23 日医薬品医療機器総合機構 販 売 1) 名注 フィニバックス点滴静注用 0.25 g 同点滴静注用 0.5 g 同キット点滴静注用 0.25 g 有 効 成 分 名 ドリペネム水和物 申 請 者 名 塩野義製薬株式会社 承認の効能 効果 承認の用法 用量 承認年月日承認事項一部変更承認年月日 再審査期間 1. 8 年注 2) 備考 < 適応菌種 > ドリペネムに感性のブドウ球菌属
再審査報告書 平成 29 年 10 月 23 日医薬品医療機器総合機構 販 売 1) 名注 フィニバックス点滴静注用 0.25 g 同点滴静注用 0.5 g 同キット点滴静注用 0.25 g 有 効 成 分 名 ドリペネム水和物 申 請 者 名 塩野義製薬株式会社 承認の効能 効果 承認の用法 用量 承認年月日承認事項一部変更承認年月日 再審査期間 1. 8 年注 2) 備考 < 適応菌種 > ドリペネムに感性のブドウ球菌属
葉酸とビタミンQ&A_201607改訂_ indd
 L FO AT E VI TAMI NB12 医療関係者用 葉酸 とビタミンB ビタミンB12 アリムタ投与に際して 警告 1 本剤を含むがん化学療法に際しては 緊急時に十分対応できる医療施設において がん化学療 法に十分な知識 経験を持つ医師のもとで 本剤の投与が適切と判断される症例についてのみ投 与すること 適応患者の選択にあたっては 各併用薬剤の添付文書を参照して十分注意すること また 治療開始に先立ち
L FO AT E VI TAMI NB12 医療関係者用 葉酸 とビタミンB ビタミンB12 アリムタ投与に際して 警告 1 本剤を含むがん化学療法に際しては 緊急時に十分対応できる医療施設において がん化学療 法に十分な知識 経験を持つ医師のもとで 本剤の投与が適切と判断される症例についてのみ投 与すること 適応患者の選択にあたっては 各併用薬剤の添付文書を参照して十分注意すること また 治療開始に先立ち
<4D F736F F D B A814089FC92F982CC82A8926D82E782B95F E31328C8E5F5F E646F63>
 - 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ 抗悪性腫瘍剤 ( ブルトン型チロシンキナーゼ阻害剤 ) ( 一般名 : イブルチニブ ) 2016 年 12 月 この度 抗悪性腫瘍剤 イムブルビカ カプセル 140 mg ( 以下標記製品 ) につきまして 再発又は難治性のマントル細胞リンパ腫 の効能追加承認を取得したことに伴い
- 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ 抗悪性腫瘍剤 ( ブルトン型チロシンキナーゼ阻害剤 ) ( 一般名 : イブルチニブ ) 2016 年 12 月 この度 抗悪性腫瘍剤 イムブルビカ カプセル 140 mg ( 以下標記製品 ) につきまして 再発又は難治性のマントル細胞リンパ腫 の効能追加承認を取得したことに伴い
<4D F736F F D2082A8926D82E782B995B68F A A E5F89968FF E372E646F63>
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意改訂のお知らせ 2011 年 7 月 東和薬品株式会社 このたび 標記製品の 使用上の注意 を改訂いたしましたのでお知らせ申し上げます なお 改訂添付文書を封入した製品がお手元に届くまでには日数を要する場合がございますので 今後のご使用に際しましては 下記内容にご留意くださいますようお願い申し上げます 1. 改訂内容 改訂後 ( 下線部改訂
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意改訂のお知らせ 2011 年 7 月 東和薬品株式会社 このたび 標記製品の 使用上の注意 を改訂いたしましたのでお知らせ申し上げます なお 改訂添付文書を封入した製品がお手元に届くまでには日数を要する場合がございますので 今後のご使用に際しましては 下記内容にご留意くださいますようお願い申し上げます 1. 改訂内容 改訂後 ( 下線部改訂
クラリチンドライシロップ 1% クラリチン錠 10mg クラリチンレディタブ錠 10mg 第 1 部申請書等行政情報及び添付文書に関する情報 (7) 同種同効品一覧 シェリング プラウ株式会社
 クラリチンドライシロップ 1% クラリチン錠 10mg クラリチンレディタブ錠 10mg 第 1 部申請書等行政情報及び添付文書に関する情報 (7) 同種同効品一覧 シェリング プラウ株式会社 Loratadine Section 1.7 Listing of Similar drugs 表 1.7-1 同種同効品一覧 ( ロラタジン, 塩酸オロパタジン )(1 of 5) ロラタジン塩酸オロパタジンクラリチン
クラリチンドライシロップ 1% クラリチン錠 10mg クラリチンレディタブ錠 10mg 第 1 部申請書等行政情報及び添付文書に関する情報 (7) 同種同効品一覧 シェリング プラウ株式会社 Loratadine Section 1.7 Listing of Similar drugs 表 1.7-1 同種同効品一覧 ( ロラタジン, 塩酸オロパタジン )(1 of 5) ロラタジン塩酸オロパタジンクラリチン
<4D F736F F D2082A8926D82E782B995B68F C D815B838B43505F4F E31302E646F63>
 医薬品の適正使用に欠かせない情報です 必ずお読みください 効能 効果 用法 用量 追加に伴う 使用上の注意 改訂のお知らせ 2010 年 11 月 東和薬品株式会社 このたび 平成 22 年 6 月に承認事項一部変更承認申請をしていました弊社製品のランソプラゾールカプセル15mg/30mg トーワ ランソプラゾールOD 錠 15mg/30mg トーワ の 効能 効果 用法 用量 追加が平成 22 年
医薬品の適正使用に欠かせない情報です 必ずお読みください 効能 効果 用法 用量 追加に伴う 使用上の注意 改訂のお知らせ 2010 年 11 月 東和薬品株式会社 このたび 平成 22 年 6 月に承認事項一部変更承認申請をしていました弊社製品のランソプラゾールカプセル15mg/30mg トーワ ランソプラゾールOD 錠 15mg/30mg トーワ の 効能 効果 用法 用量 追加が平成 22 年
 資料 3-3 資料 3-7 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 ( 案 ) < 小児 WG> 目次 < > 医療上の必要性の基準に該当すると考えられた品目 本邦における適応外薬アモキシシリン水和物 ( 要望番号 ;34) 1 アンピシリンナトリウム ( 要望番号 ;43) 7 医療上の必要性の高い未承認薬 適応外薬検討会議 医療上の必要性に係る基準 への該当性の評価
資料 3-3 資料 3-7 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 ( 案 ) < 小児 WG> 目次 < > 医療上の必要性の基準に該当すると考えられた品目 本邦における適応外薬アモキシシリン水和物 ( 要望番号 ;34) 1 アンピシリンナトリウム ( 要望番号 ;43) 7 医療上の必要性の高い未承認薬 適応外薬検討会議 医療上の必要性に係る基準 への該当性の評価
減量・コース投与期間短縮の基準
 用法 用量 通常 成人には初回投与量 (1 回量 ) を体表面積に合せて次の基準量とし 朝食後および夕食後の 1 日 2 回 28 日間連日経口投与し その後 14 日間休薬する これを 1 クールとして投与を繰り返す ただし 本剤の投与によると判断される臨床検査値異常 ( 血液検査 肝 腎機能検査 ) および消化器症状が発現せず 安全性に問題がない場合には休薬を短縮できるが その場合でも少なくとも
用法 用量 通常 成人には初回投与量 (1 回量 ) を体表面積に合せて次の基準量とし 朝食後および夕食後の 1 日 2 回 28 日間連日経口投与し その後 14 日間休薬する これを 1 クールとして投与を繰り返す ただし 本剤の投与によると判断される臨床検査値異常 ( 血液検査 肝 腎機能検査 ) および消化器症状が発現せず 安全性に問題がない場合には休薬を短縮できるが その場合でも少なくとも
開発の経緯 セフタジジムは Cephalosporium acremonium 又は Cephalosporium salmosynnematum の培養によって得られる抗生物質の誘導体で第三世代のセファロスポリンである セフェム母核の 7 位には 他の誘導体で知られているアミノチアゾリル基にカルボ
 a Novartis company 開発の経緯 セフタジジムは Cephalosporium acremonium 又は Cephalosporium salmosynnematum の培養によって得られる抗生物質の誘導体で第三世代のセファロスポリンである セフェム母核の 7 位には 他の誘導体で知られているアミノチアゾリル基にカルボキシプロピルオキシイミノ基を 3 位にはピリジンを導入することにより緑膿菌に対する抵抗力を強化している
a Novartis company 開発の経緯 セフタジジムは Cephalosporium acremonium 又は Cephalosporium salmosynnematum の培養によって得られる抗生物質の誘導体で第三世代のセファロスポリンである セフェム母核の 7 位には 他の誘導体で知られているアミノチアゾリル基にカルボキシプロピルオキシイミノ基を 3 位にはピリジンを導入することにより緑膿菌に対する抵抗力を強化している
耐性菌届出基準
 37 ペニシリン耐性肺炎球菌感染症 (1) 定義ペニシリン G に対して耐性を示す肺炎球菌による感染症である (2) 臨床的特徴小児及び成人の化膿性髄膜炎や中耳炎で検出されるが その他 副鼻腔炎 心内膜炎 心嚢炎 腹膜炎 関節炎 まれには尿路生殖器感染から菌血症を引き起こすこともある 指定届出機関の管理者は 当該指定届出機関の医師が (2) の臨床的特徴を有する者を診察した結果 症状や所見からペニシリン耐性肺炎球菌感染症が疑われ
37 ペニシリン耐性肺炎球菌感染症 (1) 定義ペニシリン G に対して耐性を示す肺炎球菌による感染症である (2) 臨床的特徴小児及び成人の化膿性髄膜炎や中耳炎で検出されるが その他 副鼻腔炎 心内膜炎 心嚢炎 腹膜炎 関節炎 まれには尿路生殖器感染から菌血症を引き起こすこともある 指定届出機関の管理者は 当該指定届出機関の医師が (2) の臨床的特徴を有する者を診察した結果 症状や所見からペニシリン耐性肺炎球菌感染症が疑われ
< F2D A8CF6926D905C90BF82C98C5782E98EE688B5>
 保医発 1031 第 6 号平成 23 年 10 月 31 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 公知申請に係る事前評価が終了した医薬品の保険上の取扱いについて 本年 10 月 31 日開催の薬事 食品衛生審議会医薬品第二部会において
保医発 1031 第 6 号平成 23 年 10 月 31 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 公知申請に係る事前評価が終了した医薬品の保険上の取扱いについて 本年 10 月 31 日開催の薬事 食品衛生審議会医薬品第二部会において
ラピアクタ点滴静注液バッグ・バイアル
 **2016 年 4 月改訂 ( 第 7 版, 薬生安通知等に基づく使用上の注意の項の改訂 ) *2013 年 7 月改訂貯法 : 室温保存使用期限 : 外箱等に表示抗インフルエンザウイルス剤処方箋医薬品注 1) 日本標準商品分類番号 87625 バッグ バイアル 承認番号 22300AMX01152 22300AMX01151 薬価収載 2012 年 6 月 2012 年 6 月 販売開始 2010
**2016 年 4 月改訂 ( 第 7 版, 薬生安通知等に基づく使用上の注意の項の改訂 ) *2013 年 7 月改訂貯法 : 室温保存使用期限 : 外箱等に表示抗インフルエンザウイルス剤処方箋医薬品注 1) 日本標準商品分類番号 87625 バッグ バイアル 承認番号 22300AMX01152 22300AMX01151 薬価収載 2012 年 6 月 2012 年 6 月 販売開始 2010
スライド 1
 1/5 PMDA からの医薬品適正使用のお願い ( 独 ) 医薬品医療機器総合機構 No.6 2012 年 1 月 ラミクタール錠 ( ラモトリギン ) の重篤皮膚障害と用法 用量遵守 早期発見について ラミクタール錠は 用法 用量 を遵守せず投与した場合に皮膚障害の発現率が高くなることが示されている ( 表 1 参照 ) ため 用法 用量 を遵守することが平成 20 年 10 月の承認時より注意喚起されています
1/5 PMDA からの医薬品適正使用のお願い ( 独 ) 医薬品医療機器総合機構 No.6 2012 年 1 月 ラミクタール錠 ( ラモトリギン ) の重篤皮膚障害と用法 用量遵守 早期発見について ラミクタール錠は 用法 用量 を遵守せず投与した場合に皮膚障害の発現率が高くなることが示されている ( 表 1 参照 ) ため 用法 用量 を遵守することが平成 20 年 10 月の承認時より注意喚起されています
 医薬品の使用上の注意の改訂について ( 平成 14 年 6 月 5 日 ) ( 医薬安発第 0605002 号 ) ( 各都道府県衛生主管部 ( 局 ) 長あて厚生労働省医薬局安全対策課長通知 ) 医薬品の安全対策については 日頃よりご尽力いただいているところでありますが 今般 別添のとおり日本製薬団体連合会安全性委員会委員長あて通知及び連絡したので ご承知願います 医薬品の使用上の注意の改訂について
医薬品の使用上の注意の改訂について ( 平成 14 年 6 月 5 日 ) ( 医薬安発第 0605002 号 ) ( 各都道府県衛生主管部 ( 局 ) 長あて厚生労働省医薬局安全対策課長通知 ) 医薬品の安全対策については 日頃よりご尽力いただいているところでありますが 今般 別添のとおり日本製薬団体連合会安全性委員会委員長あて通知及び連絡したので ご承知願います 医薬品の使用上の注意の改訂について
添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示され
 添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示されます 検索条件設定時の注意 検索はテキスト文章 (SGML 又は XML) が対象となっており 画像及び
添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示されます 検索条件設定時の注意 検索はテキスト文章 (SGML 又は XML) が対象となっており 画像及び
Microsoft Word - LIA RMP_概要ver2.docx
 リアルダ錠 1200mg に係る 医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任は持田製薬株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません 持田製薬株式会社 リアルダ錠 1200mg に係る医薬品リスク管理計画書 (RMP) の概要 販売名リアルダ錠 1200mg 有効成分メサラジン 製造販売業者持田製薬株式会社薬効分類 872399 提出年月
リアルダ錠 1200mg に係る 医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任は持田製薬株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません 持田製薬株式会社 リアルダ錠 1200mg に係る医薬品リスク管理計画書 (RMP) の概要 販売名リアルダ錠 1200mg 有効成分メサラジン 製造販売業者持田製薬株式会社薬効分類 872399 提出年月
Ⅰ. 改訂内容 ( 部変更 ) ペルサンチン 錠 12.5 改 訂 後 改 訂 前 (1) 本剤投与中の患者に本薬の注射剤を追加投与した場合, 本剤の作用が増強され, 副作用が発現するおそれがあるので, 併用しないこと ( 過量投与 の項参照) 本剤投与中の患者に本薬の注射剤を追加投与した場合, 本
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意 改訂のお知らせ 2006 年 1 月日本ベーリンガーインゲルハイム株式会社 注 ) 処方せん医薬品 ( ジピリダモール製剤 ) = 登録商標注 ) 注意 - 医師等の処方せんにより使用すること 謹啓時下ますますご清祥のこととお慶び申し上げます 平素は弊社製品につきましてご愛顧を賜り厚く御礼申し上げます さて, この度, 自主改訂によりペルサンチン
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意 改訂のお知らせ 2006 年 1 月日本ベーリンガーインゲルハイム株式会社 注 ) 処方せん医薬品 ( ジピリダモール製剤 ) = 登録商標注 ) 注意 - 医師等の処方せんにより使用すること 謹啓時下ますますご清祥のこととお慶び申し上げます 平素は弊社製品につきましてご愛顧を賜り厚く御礼申し上げます さて, この度, 自主改訂によりペルサンチン
1)~ 2) 3) 近位筋脱力 CK(CPK) 高値 炎症を伴わない筋線維の壊死 抗 HMG-CoA 還元酵素 (HMGCR) 抗体陽性等を特徴とする免疫性壊死性ミオパチーがあらわれ 投与中止後も持続する例が報告されているので 患者の状態を十分に観察すること なお 免疫抑制剤投与により改善がみられた
 適正使用に欠かせない情報です 必ずお読みください 使用上の注意 改訂のお知らせ 注 1) 処方箋医薬品 ATORVASTATIN TABLETS AMALUET COMBINATION TABLETS 注 1) 処方箋医薬品 PRAVASTATIN SODIUM TABLETS 注 1) 注意 - 医師等の処方箋により使用すること PITAVASTATIN CALCIUM TABLETS 2016
適正使用に欠かせない情報です 必ずお読みください 使用上の注意 改訂のお知らせ 注 1) 処方箋医薬品 ATORVASTATIN TABLETS AMALUET COMBINATION TABLETS 注 1) 処方箋医薬品 PRAVASTATIN SODIUM TABLETS 注 1) 注意 - 医師等の処方箋により使用すること PITAVASTATIN CALCIUM TABLETS 2016
Microsoft Word - sa_niflec_ doc
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能又は効果 用法及び用量 使用上の注意改訂のお知らせ 経口腸管洗浄剤 発売 2009 年 4 月 製造販売 この度 経口腸管洗浄剤ニフレック 内用において 効能又は効果 用法及び用量 の追加承認を取得したことに伴い 添付文書を以下のとおり改訂致しましたのでご案内申し上げます 今後のご使用につきましては 下記内容をご参照下さいますようお願い申し上げます
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能又は効果 用法及び用量 使用上の注意改訂のお知らせ 経口腸管洗浄剤 発売 2009 年 4 月 製造販売 この度 経口腸管洗浄剤ニフレック 内用において 効能又は効果 用法及び用量 の追加承認を取得したことに伴い 添付文書を以下のとおり改訂致しましたのでご案内申し上げます 今後のご使用につきましては 下記内容をご参照下さいますようお願い申し上げます
<4D F736F F D2082A8926D82E782B995B68F E834E838D838A E3132>
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能 効果 用法 用量 使用上の注意 改訂のお知らせ 2013 年 12 月 東和薬品株式会社 このたび 平成 25 年 8 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 25 年 11 月 29 日付にて 下記の内容で承認されました また 使用上の注意 を改訂致しましたので 併せてお知らせ申し上げます
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能 効果 用法 用量 使用上の注意 改訂のお知らせ 2013 年 12 月 東和薬品株式会社 このたび 平成 25 年 8 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 25 年 11 月 29 日付にて 下記の内容で承認されました また 使用上の注意 を改訂致しましたので 併せてお知らせ申し上げます
ファロム錠150mg、ファロム錠200mg患者向医薬品ガイド
 患者向医薬品ガイド 2018 年 7 月更新 ファロム錠 150mg ファロム錠 200mg この薬は? 販売名 一般名 含有量 (1 錠中 ) ファロム錠 150mg ファロム錠 200mg Farom Tablets 150mg Farom Tablets 200mg ファロペネムナトリウム水和物 Faropenem Sodium Hydrate 150.0mg( 力価 ) 200.0mg( 力価
患者向医薬品ガイド 2018 年 7 月更新 ファロム錠 150mg ファロム錠 200mg この薬は? 販売名 一般名 含有量 (1 錠中 ) ファロム錠 150mg ファロム錠 200mg Farom Tablets 150mg Farom Tablets 200mg ファロペネムナトリウム水和物 Faropenem Sodium Hydrate 150.0mg( 力価 ) 200.0mg( 力価
Microsoft Word エリンダシン使注意.doc
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意改訂のお知らせ エルカトニン製剤 劇薬 指定医薬品 処方せん医薬品 ( 注意 - 医師等の処方せんにより使用すること ) エリンダシン注 10 単位 エリンダシン注 20 単位 エリンダシン注 このたび エルカトニン製剤エリンダシン注 10 単位 エリンダシン注 20 単位及びエリンダシン注 [ 東菱薬品工業 製造販売 ] につきまして
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意改訂のお知らせ エルカトニン製剤 劇薬 指定医薬品 処方せん医薬品 ( 注意 - 医師等の処方せんにより使用すること ) エリンダシン注 10 単位 エリンダシン注 20 単位 エリンダシン注 このたび エルカトニン製剤エリンダシン注 10 単位 エリンダシン注 20 単位及びエリンダシン注 [ 東菱薬品工業 製造販売 ] につきまして
スライド 0
 Drug Safety Information 使用上の注意の改訂指示 年月日 2013 年 7 月 9 日 販売名 ( 承認取得者 ) インヴェガ錠 3mg 同錠 6mg 同錠 9mg( ヤンセンファーマ ) 成分名 パリペリドン 効能 効果 統合失調症 改訂の概要 類薬 ( リスペリドン ) における重大な副作用 の項に記載のある 麻痺性イレウス を削除し 重大な副作用 の項に 麻痺性イレ ウス
Drug Safety Information 使用上の注意の改訂指示 年月日 2013 年 7 月 9 日 販売名 ( 承認取得者 ) インヴェガ錠 3mg 同錠 6mg 同錠 9mg( ヤンセンファーマ ) 成分名 パリペリドン 効能 効果 統合失調症 改訂の概要 類薬 ( リスペリドン ) における重大な副作用 の項に記載のある 麻痺性イレウス を削除し 重大な副作用 の項に 麻痺性イレ ウス
アシクリル・アシクリルバッグ(アイロム)使用上の注意改訂のお知らせ_120913
 御得意様各位 2012 年 10 月 - 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 使用上の注意改訂のお知らせ 抗ウイルス化学療法剤 注射用アシクロビル 製造販売元アイロム製薬株式会社神奈川県厚木市旭町四丁目 18 番 29 号 謹啓時下益々ご清祥のこととお慶び申し上げます 平素は格別のご高配を賜り厚くお礼申し上げます さて この度 抗ウイルス化学療法剤 アシクリル点滴静注用 250mg
御得意様各位 2012 年 10 月 - 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 使用上の注意改訂のお知らせ 抗ウイルス化学療法剤 注射用アシクロビル 製造販売元アイロム製薬株式会社神奈川県厚木市旭町四丁目 18 番 29 号 謹啓時下益々ご清祥のこととお慶び申し上げます 平素は格別のご高配を賜り厚くお礼申し上げます さて この度 抗ウイルス化学療法剤 アシクリル点滴静注用 250mg
用法 用量 発作性夜間ヘモグロビン尿症における溶血抑制 mg mg mg mg kg 30kg 40kg 20kg 30kg 10kg 20kg 5kg 10kg 1900mg mg mg mg
 C EculizumabGenetical Recombination AMX 警告 1 2 禁忌 ( 次の患者には投与しないこと ) 1 2 組成 性状 ml mg mg mg mg mg ph ph mgml 効能 効果 発作性夜間ヘモグロビン尿症における溶血抑制 < 効能 効果に関連する使用上の注意 > 共通 1C5 C5b-9 b 発作性夜間ヘモグロビン尿症における溶血抑制 1 2 3 4
C EculizumabGenetical Recombination AMX 警告 1 2 禁忌 ( 次の患者には投与しないこと ) 1 2 組成 性状 ml mg mg mg mg mg ph ph mgml 効能 効果 発作性夜間ヘモグロビン尿症における溶血抑制 < 効能 効果に関連する使用上の注意 > 共通 1C5 C5b-9 b 発作性夜間ヘモグロビン尿症における溶血抑制 1 2 3 4
<4D F736F F D2082A8926D82E782B995B68F D815B838B8FF E31312E646F63>
 医薬品の適正使用に欠かせない情報です 必ずお読みください 効能 効果 用法 用量 追加に伴う 使用上の注意 改訂のお知らせ 2010 年 11 月 東和薬品株式会社 このたび 平成 22 年 6 月に承認事項一部変更承認申請をしていました弊社製品のオメプラゾール錠 トーワ 10mg/20mgの 効能 効果 用法 用量 追加が平成 22 年 11 月 15 日付にて 下記の内容で承認されました また承認に伴い
医薬品の適正使用に欠かせない情報です 必ずお読みください 効能 効果 用法 用量 追加に伴う 使用上の注意 改訂のお知らせ 2010 年 11 月 東和薬品株式会社 このたび 平成 22 年 6 月に承認事項一部変更承認申請をしていました弊社製品のオメプラゾール錠 トーワ 10mg/20mgの 効能 効果 用法 用量 追加が平成 22 年 11 月 15 日付にて 下記の内容で承認されました また承認に伴い
5_使用上の注意(37薬効)Web作業用.indd
 34 ビタミン主薬製剤 1 ビタミン A 主薬製剤 使用上の注意と記載条件 1. 次の人は服用前に医師又は薬剤師に相談することあ医師の治療を受けている人 い妊娠 3 ヵ月以内の妊婦, 妊娠していると思われる人又は妊娠を希望する人 ( 妊娠 3 ヵ月前から妊娠 3 ヵ月までの間にビタミン A を 1 日 10,000 国際単位以上摂取した妊婦から生まれた児に先天異常の割合が上昇したとの報告がある )
34 ビタミン主薬製剤 1 ビタミン A 主薬製剤 使用上の注意と記載条件 1. 次の人は服用前に医師又は薬剤師に相談することあ医師の治療を受けている人 い妊娠 3 ヵ月以内の妊婦, 妊娠していると思われる人又は妊娠を希望する人 ( 妊娠 3 ヵ月前から妊娠 3 ヵ月までの間にビタミン A を 1 日 10,000 国際単位以上摂取した妊婦から生まれた児に先天異常の割合が上昇したとの報告がある )
Microsoft Word - JAID_JSC 2014 正誤表_ 原稿
 JAID/JSC 感染症治療ガイド 2014 表 記載にりがありましたので, 下記のように追加 訂させていただきます 2016 年 9 月 JAID/JSC 感染症治療ガイド ガイドライン作成委員会 P106 Ⅶ 呼吸器感染症,A-2 院内肺炎 3 Definitive Therapy P. aeruginosa 多剤耐性の場合 CL:5mg/kg 1 回ローディング その 24 時間後に以下の維持用量を開始する
JAID/JSC 感染症治療ガイド 2014 表 記載にりがありましたので, 下記のように追加 訂させていただきます 2016 年 9 月 JAID/JSC 感染症治療ガイド ガイドライン作成委員会 P106 Ⅶ 呼吸器感染症,A-2 院内肺炎 3 Definitive Therapy P. aeruginosa 多剤耐性の場合 CL:5mg/kg 1 回ローディング その 24 時間後に以下の維持用量を開始する
ファロム錠150mg、ファロム錠200mg患者向医薬品ガイド
 患者向医薬品ガイド 2019 年 4 月更新 ファロム錠 150mg ファロム錠 200mg この薬は? 販売名 一般名 含有量 (1 錠中 ) ファロム錠 150mg ファロム錠 200mg Farom Tablets 150mg Farom Tablets 200mg ファロペネムナトリウム水和物 Faropenem Sodium Hydrate 150.0mg( 力価 ) 200.0mg( 力価
患者向医薬品ガイド 2019 年 4 月更新 ファロム錠 150mg ファロム錠 200mg この薬は? 販売名 一般名 含有量 (1 錠中 ) ファロム錠 150mg ファロム錠 200mg Farom Tablets 150mg Farom Tablets 200mg ファロペネムナトリウム水和物 Faropenem Sodium Hydrate 150.0mg( 力価 ) 200.0mg( 力価
改訂後 適応症 表在性皮膚感染症 深在性皮膚感染症 リンパ管 リンパ節炎 慢性膿皮症 ざ瘡 ( 化膿性炎症を伴うもの ) 外傷 熱傷及び手術創等の二次感染 乳腺炎 肛門周囲膿瘍 咽頭 喉頭炎 扁桃炎 ( 扁桃周囲炎 扁桃周囲膿瘍を含む ) 急性気管支炎 肺炎 慢性呼吸器病変の二次感染 膀胱炎 腎盂腎
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能 効果 用法 用量 の追加及び 使用上の注意 改訂のお知らせ 2016 年 1 月製造販売元大原薬品工業株式会社お問い合わせ先 : 安全管理部 TEL : 03-6740-7701 FAX : 03-6740-7703 注 1) 注意 医師等の処方箋により使用すること この度 弊社製品 レボフロキサシン錠 250mg 500mg オーハラ
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能 効果 用法 用量 の追加及び 使用上の注意 改訂のお知らせ 2016 年 1 月製造販売元大原薬品工業株式会社お問い合わせ先 : 安全管理部 TEL : 03-6740-7701 FAX : 03-6740-7703 注 1) 注意 医師等の処方箋により使用すること この度 弊社製品 レボフロキサシン錠 250mg 500mg オーハラ
メイアクトMS小児用細粒10%
 2018 年 3 月改訂 ( 第 8 版 ) *2015 年 10 月改訂 日本標準商品分類番号 876132 遮光 室温保存 ( 取扱貯法い上の注意 の項参照 ) 使用期限外箱に最終年月表示 経口用セフェム系抗生物質製剤処方箋医薬品注 1) 承認番号 22000AMX02180000 薬価収載 2008 年 12 月 販売開始 2009 年 1 月 効能追加 2009 年 11 月 禁忌 ( 次の患者には投与しないこと
2018 年 3 月改訂 ( 第 8 版 ) *2015 年 10 月改訂 日本標準商品分類番号 876132 遮光 室温保存 ( 取扱貯法い上の注意 の項参照 ) 使用期限外箱に最終年月表示 経口用セフェム系抗生物質製剤処方箋医薬品注 1) 承認番号 22000AMX02180000 薬価収載 2008 年 12 月 販売開始 2009 年 1 月 効能追加 2009 年 11 月 禁忌 ( 次の患者には投与しないこと
抗菌薬の殺菌作用抗菌薬の殺菌作用には濃度依存性と時間依存性の 2 種類があり 抗菌薬の効果および用法 用量の設定に大きな影響を与えます 濃度依存性タイプでは 濃度を高めると濃度依存的に殺菌作用を示します 濃度依存性タイプの抗菌薬としては キノロン系薬やアミノ配糖体系薬が挙げられます 一方 時間依存性
 2012 年 1 月 4 日放送 抗菌薬の PK-PD 愛知医科大学大学院感染制御学教授三鴨廣繁抗菌薬の PK-PD とは薬物動態を解析することにより抗菌薬の有効性と安全性を評価する考え方は アミノ配糖体系薬などの副作用を回避するための薬物血中濃度モニタリング (TDM) の分野で発達してきました 近年では 耐性菌の増加 コンプロマイズド ホストの増加 新規抗菌薬の開発の停滞などもあり 現存の抗菌薬をいかに科学的に使用するかが重要な課題となっており
2012 年 1 月 4 日放送 抗菌薬の PK-PD 愛知医科大学大学院感染制御学教授三鴨廣繁抗菌薬の PK-PD とは薬物動態を解析することにより抗菌薬の有効性と安全性を評価する考え方は アミノ配糖体系薬などの副作用を回避するための薬物血中濃度モニタリング (TDM) の分野で発達してきました 近年では 耐性菌の増加 コンプロマイズド ホストの増加 新規抗菌薬の開発の停滞などもあり 現存の抗菌薬をいかに科学的に使用するかが重要な課題となっており
開発の経緯 ゲムシタビン点滴静注用 200mg 1g サンド は 後発医薬品として開発を企画し 規格及び試験方法を設定 加速試験を行い 平成 22 年 1 月に製造販売承認を取得した ( 薬食発第 号 ( 平成 17 年 3 月 31 日 ) に基づき承認申請 ) 製品の特徴及び有用
 a Novartis company 開発の経緯 ゲムシタビン点滴静注用 200mg 1g サンド は 後発医薬品として開発を企画し 規格及び試験方法を設定 加速試験を行い 平成 22 年 1 月に製造販売承認を取得した ( 薬食発第 0331015 号 ( 平成 17 年 3 月 31 日 ) に基づき承認申請 ) 製品の特徴及び有用性 ゲムシタビンは代謝拮抗剤である ヌクレオシド能動輸送体を介して細胞内に入り
a Novartis company 開発の経緯 ゲムシタビン点滴静注用 200mg 1g サンド は 後発医薬品として開発を企画し 規格及び試験方法を設定 加速試験を行い 平成 22 年 1 月に製造販売承認を取得した ( 薬食発第 0331015 号 ( 平成 17 年 3 月 31 日 ) に基づき承認申請 ) 製品の特徴及び有用性 ゲムシタビンは代謝拮抗剤である ヌクレオシド能動輸送体を介して細胞内に入り
スライド 0
 Drug Safety Information 使用上の注意の改訂指示 年月日 2013 年 1 月 8 日 販売名 ( 承認取得者 ) スーテントカプセル 12.5mg( ファイザー ) 一般名 スニチニブリンゴ酸塩 効能 効果イマチニブ抵抗性の消化管間質腫瘍根治切除不能又は転移性の腎細胞癌膵神経内分泌腫瘍 改訂の概要 重大な副作用 の項に 皮膚粘膜眼症候群 (Stevens-Johnson 症候群
Drug Safety Information 使用上の注意の改訂指示 年月日 2013 年 1 月 8 日 販売名 ( 承認取得者 ) スーテントカプセル 12.5mg( ファイザー ) 一般名 スニチニブリンゴ酸塩 効能 効果イマチニブ抵抗性の消化管間質腫瘍根治切除不能又は転移性の腎細胞癌膵神経内分泌腫瘍 改訂の概要 重大な副作用 の項に 皮膚粘膜眼症候群 (Stevens-Johnson 症候群
モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム 製造販売業者 EA ファーマ株式会社 薬効分類 提出年月 平成 30 年 10 月 1.1. 安全
 モビコール配合内用剤 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はEAファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません EA ファーマ株式会社 モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム
モビコール配合内用剤 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はEAファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません EA ファーマ株式会社 モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム
割合が10% 前後となっています 新生児期以降は 4-5ヶ月頃から頻度が増加します ( 図 1) 原因菌に関しては 本邦ではインフルエンザ菌が原因となる頻度がもっとも高く 50% 以上を占めています 次いで肺炎球菌が20~30% と多く インフルエンザ菌と肺炎球菌で 原因菌の80% 近くを占めていま
 2012 年 6 月 13 日放送 小児科領域の重症感染症 慶應義塾大学感染制御センター教授岩田敏はじめに小児科領域の重症感染症としては 脳炎 髄膜炎 敗血症 菌血症 肺炎 膿胸 心筋炎 好中球減少時の感染症などがあげられます これらの疾患は 抗微生物薬の進歩した今日においても 難治性であったり予後が不良であったりすることから そのマネジメントには苦労するところであります 本日はこれらの疾患のうち
2012 年 6 月 13 日放送 小児科領域の重症感染症 慶應義塾大学感染制御センター教授岩田敏はじめに小児科領域の重症感染症としては 脳炎 髄膜炎 敗血症 菌血症 肺炎 膿胸 心筋炎 好中球減少時の感染症などがあげられます これらの疾患は 抗微生物薬の進歩した今日においても 難治性であったり予後が不良であったりすることから そのマネジメントには苦労するところであります 本日はこれらの疾患のうち
医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能
 医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 1 2 3 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能 ) ( 医薬品の名称のみで検索する場合 34 の項目は未選択 未入力で可 ) 検索結果で表示したい文書を選択
医薬品の添付文書等を調べる場合 最後に 検索 をクリック ( 下部の 検索 ボタンでも可 ) 特定の文書 ( 添付文書以外の文書 ) の記載内容から調べる場合 検索 をクリック ( 下部の 検索 ボタンでも可 ) 最後に 1 2 3 調べたい医薬品の名称を入力 ( 名称の一部のみの入力でも検索可能 ) ( 医薬品の名称のみで検索する場合 34 の項目は未選択 未入力で可 ) 検索結果で表示したい文書を選択
< アシクリル点滴静注用 250mg> 改訂後 1. 慎重投与 ( 次の患者には慎重に投与すること (1 腎障害のある患者 [ 用法 用量に関連する使用上の注意 及び 重要な基本的注意 の項参照 ] (2 肝障害のある患者 [ 肝障害が増悪するおそれがある ] (3 高齢者 [ 用法 用量に関連する
![< アシクリル点滴静注用 250mg> 改訂後 1. 慎重投与 ( 次の患者には慎重に投与すること (1 腎障害のある患者 [ 用法 用量に関連する使用上の注意 及び 重要な基本的注意 の項参照 ] (2 肝障害のある患者 [ 肝障害が増悪するおそれがある ] (3 高齢者 [ 用法 用量に関連する < アシクリル点滴静注用 250mg> 改訂後 1. 慎重投与 ( 次の患者には慎重に投与すること (1 腎障害のある患者 [ 用法 用量に関連する使用上の注意 及び 重要な基本的注意 の項参照 ] (2 肝障害のある患者 [ 肝障害が増悪するおそれがある ] (3 高齢者 [ 用法 用量に関連する](/thumbs/91/105674588.jpg) - 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 の変更及び使用上の注意改訂のお知らせ 2010 年 7 月 処方せん医薬品 ( 注意 医師等の処方せんにより使用すること 抗ウイルス化学療法剤 アシクロビル製剤 アシクロビル製剤 製造販売元アイロム製薬株式会社神奈川県厚木市旭町四丁目 18 番 29 号 販売元扶桑薬品工業株式会社大阪市城東区森之宮二丁目 3 番
- 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 の変更及び使用上の注意改訂のお知らせ 2010 年 7 月 処方せん医薬品 ( 注意 医師等の処方せんにより使用すること 抗ウイルス化学療法剤 アシクロビル製剤 アシクロビル製剤 製造販売元アイロム製薬株式会社神奈川県厚木市旭町四丁目 18 番 29 号 販売元扶桑薬品工業株式会社大阪市城東区森之宮二丁目 3 番
2012 年 1 月 25 日放送 歯性感染症における経口抗菌薬療法 東海大学外科学系口腔外科教授金子明寛 今回は歯性感染症における経口抗菌薬療法と題し歯性感染症からの分離菌および薬 剤感受性を元に歯性感染症の第一選択薬についてお話し致します 抗菌化学療法のポイント歯性感染症原因菌は嫌気性菌および好
 2012 年 1 月 25 日放送 歯性感染症における経口抗菌薬療法 東海大学外科学系口腔外科教授金子明寛 今回は歯性感染症における経口抗菌薬療法と題し歯性感染症からの分離菌および薬 剤感受性を元に歯性感染症の第一選択薬についてお話し致します 抗菌化学療法のポイント歯性感染症原因菌は嫌気性菌および好気性菌の複数菌感染症です 嫌気性菌の占める割合が 高くおよそ 2:1 の頻度で検出されます 嫌気性菌では
2012 年 1 月 25 日放送 歯性感染症における経口抗菌薬療法 東海大学外科学系口腔外科教授金子明寛 今回は歯性感染症における経口抗菌薬療法と題し歯性感染症からの分離菌および薬 剤感受性を元に歯性感染症の第一選択薬についてお話し致します 抗菌化学療法のポイント歯性感染症原因菌は嫌気性菌および好気性菌の複数菌感染症です 嫌気性菌の占める割合が 高くおよそ 2:1 の頻度で検出されます 嫌気性菌では
改訂後 ( 下線 : 追加記載 ) 改訂前 ( 下線 : 削除 ) 使用上の注意 1) 腎障害のある患者 [ 高い血中濃度が持続するおそれがある ]( 用法 用量に関連する使用上の注意 の項参照 ) 2)~ 4) 現行のとおり テオフィリン リトナビル 中枢神経抑制剤アルコール ( 飲酒 ) ピルシ
 2)~ 4) 現行のとおり テオフィリン リトナビル 中枢神経抑制剤アルコール ( 飲酒 ) ピルシ 改訂後 ( 下線 : 追加記載 ) 改訂前 ( 下線 : 削除 ) 使用上の注意 1) 腎障害のある患者 [ 高い血中濃度が持続するおそれがある ]( 用法 用量に関連する使用上の注意 の項参照 ) 2)~ 4) 現行のとおり テオフィリン リトナビル 中枢神経抑制剤アルコール ( 飲酒 ) ピルシ](/thumbs/93/111540608.jpg) 適正使用に欠かせない情報です 必ずお読みください 使用上の注意 改訂のお知らせ 持続性選択 H 1 受容体拮抗 アレルギー性疾患治療剤 注 ) 処方せん医薬品 CETIRIZINE HYDROCHLORIDE TABLETS 2011 年 7 月 注 ) 注意 医師等の処方せんにより使用すること このたび 当社の持続性選択 H 1 受容体拮抗 アレルギー性疾患治療剤 セチリジン塩酸塩錠 5mg NP
適正使用に欠かせない情報です 必ずお読みください 使用上の注意 改訂のお知らせ 持続性選択 H 1 受容体拮抗 アレルギー性疾患治療剤 注 ) 処方せん医薬品 CETIRIZINE HYDROCHLORIDE TABLETS 2011 年 7 月 注 ) 注意 医師等の処方せんにより使用すること このたび 当社の持続性選択 H 1 受容体拮抗 アレルギー性疾患治療剤 セチリジン塩酸塩錠 5mg NP
シプロフロキサシン錠 100mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを
 シプロフロキサシン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを有し 上気道感染症 尿路感染症 皮膚感染症などに有効なニューキノロン系の合成抗菌剤である シプロキサン 錠
シプロフロキサシン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを有し 上気道感染症 尿路感染症 皮膚感染症などに有効なニューキノロン系の合成抗菌剤である シプロキサン 錠
ハイゼントラ20%皮下注1g/5mL・2g/10mL・4g/20mL
 CSL19-158 医薬品の適正使用に欠かせない情報です 必ずお読みください 効能又は効果 用法及び用量 使用上の注意改訂のお知らせ 2019 年 3 月血漿分画製剤 ( 皮下注用人免疫グロブリン製剤 ) この度 標記製品の製造販売承認事項の一部変更が承認されました それに伴い 効能又は効果 用法及び用量 及び 使用上の注意 等を改訂いたしましたので お知らせいたします 改訂添付文書を封入した製品がお手元に届くまでには若干の日時を要しますので
CSL19-158 医薬品の適正使用に欠かせない情報です 必ずお読みください 効能又は効果 用法及び用量 使用上の注意改訂のお知らせ 2019 年 3 月血漿分画製剤 ( 皮下注用人免疫グロブリン製剤 ) この度 標記製品の製造販売承認事項の一部変更が承認されました それに伴い 効能又は効果 用法及び用量 及び 使用上の注意 等を改訂いたしましたので お知らせいたします 改訂添付文書を封入した製品がお手元に届くまでには若干の日時を要しますので
緑膿菌 Pseudomonas aeruginosa グラム陰性桿菌 ブドウ糖非発酵 緑色色素産生 水まわりなど生活環境中に広く常在 腸内に常在する人も30%くらい ペニシリンやセファゾリンなどの第一世代セフェム 薬に自然耐性 テトラサイクリン系やマクロライド系抗生物質など の抗菌薬にも耐性を示す傾
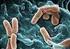 2 緑膿菌 Pseudomonas aeruginosa グラム陰性桿菌 ブドウ糖非発酵 緑色色素産生 水まわりなど生活環境中に広く常在 腸内に常在する人も30%くらい ペニシリンやセファゾリンなどの第一世代セフェム 薬に自然耐性 テトラサイクリン系やマクロライド系抗生物質など の抗菌薬にも耐性を示す傾向が強い 多剤耐性緑膿菌は5類感染症定点把握疾患 赤痢菌属 グラム陰性通性嫌気性桿菌 腸内細菌科
2 緑膿菌 Pseudomonas aeruginosa グラム陰性桿菌 ブドウ糖非発酵 緑色色素産生 水まわりなど生活環境中に広く常在 腸内に常在する人も30%くらい ペニシリンやセファゾリンなどの第一世代セフェム 薬に自然耐性 テトラサイクリン系やマクロライド系抗生物質など の抗菌薬にも耐性を示す傾向が強い 多剤耐性緑膿菌は5類感染症定点把握疾患 赤痢菌属 グラム陰性通性嫌気性桿菌 腸内細菌科
2.7.3(5 群 ) 呼吸器感染症臨床的有効性グレースビット 錠 細粒 表 (5 群 )-3 疾患別陰性化率 疾患名 陰性化被験者数 / 陰性化率 (%) (95%CI)(%) a) 肺炎 全体 91/ (89.0, 98.6) 細菌性肺炎 73/ (86
 2.7.3(5 群 ) 呼吸器感染症臨床的有効性グレースビット 錠 細粒 表 2.7.3.3.2(5 群 )-2 原因菌別臨床効果 原因菌 肺炎 慢性呼吸器病変の二次感染 急性上気道感染症群 5 群合計 単独菌 83 82(98.8) 67 61(91.0) 14 14(100) 164 157(95.7) 複数菌 (2 種 ) 14 14(100) 7 7(100) 2 2 23 23(100)
2.7.3(5 群 ) 呼吸器感染症臨床的有効性グレースビット 錠 細粒 表 2.7.3.3.2(5 群 )-2 原因菌別臨床効果 原因菌 肺炎 慢性呼吸器病変の二次感染 急性上気道感染症群 5 群合計 単独菌 83 82(98.8) 67 61(91.0) 14 14(100) 164 157(95.7) 複数菌 (2 種 ) 14 14(100) 7 7(100) 2 2 23 23(100)
スライド 1
 薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
Microsoft Word - セピドナリン静注用1gIF2.DOC
 2007 年 9 月改訂 ( 第 2 版 ) 日本標準商品分類番号 :876132 医薬品インタビューフォーム日本病院薬剤師会の IF 記載要領 (1998 年 9 月 ) に準拠して作成 セフェム系抗生物質製剤 指定医薬品処方せん医薬品 日本薬局方注射用セフォチアム塩酸塩セピドナリン 静注用 1g SEPIDNARIN 剤形注射剤 ( 用時溶解 ) 規格 含量 一般名 製造 輸入承認年月日薬価基準収載
2007 年 9 月改訂 ( 第 2 版 ) 日本標準商品分類番号 :876132 医薬品インタビューフォーム日本病院薬剤師会の IF 記載要領 (1998 年 9 月 ) に準拠して作成 セフェム系抗生物質製剤 指定医薬品処方せん医薬品 日本薬局方注射用セフォチアム塩酸塩セピドナリン 静注用 1g SEPIDNARIN 剤形注射剤 ( 用時溶解 ) 規格 含量 一般名 製造 輸入承認年月日薬価基準収載
ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル
 ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル 1mg は 1 カプセル中ロペラミド塩酸塩 1 mg を含有し消化管から吸収されて作用を発現する このことから
ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル 1mg は 1 カプセル中ロペラミド塩酸塩 1 mg を含有し消化管から吸収されて作用を発現する このことから
改訂後改訂前 << 効能 効果に関連する使用上の注意 >> 関節リウマチ 1. 過去の治療において 少なくとも1 剤の抗リウマチ薬 ( 生物製剤を除く ) 等による適切な治療を行っても 疾患に起因する明らかな症状が残る場合に投与すること 2. 本剤とアバタセプト ( 遺伝子組換え ) の併用は行わな
 - 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 警告 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ ヒト型抗ヒト TNFα モノクローナル抗体製剤 ( 一般名 : ゴリムマブ ( 遺伝子組換え )) 2017 年 4 月 製造販売元ヤンセンファーマ株式会社発売元田辺三菱製薬株式会社 この度 標記製品 ( 以下 本剤 ) シンポニー 皮下注 50mg シリンジ ( 一般名 :
- 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 警告 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ ヒト型抗ヒト TNFα モノクローナル抗体製剤 ( 一般名 : ゴリムマブ ( 遺伝子組換え )) 2017 年 4 月 製造販売元ヤンセンファーマ株式会社発売元田辺三菱製薬株式会社 この度 標記製品 ( 以下 本剤 ) シンポニー 皮下注 50mg シリンジ ( 一般名 :
オキサゾリジノン系合成抗菌剤リネゾリド点滴静注液 リネゾリド注射液 配合変化表リネゾリド点滴静注液 組成 性状 1. 組成 本剤は 1 バッグ中 (300mL) に次の成分を含有 有効成分 添加物 リネゾリド 600mg ブドウ糖 g クエン酸ナトリウム水和物 クエン酸水和物 ph 調節
 263 170 263 配合変化表 2018 年 11 月作成 オキサゾリジノン系合成抗菌剤 リネゾリド点滴静注液 リネゾリド注射液 製造販売元 : オキサゾリジノン系合成抗菌剤リネゾリド点滴静注液 リネゾリド注射液 配合変化表リネゾリド点滴静注液 組成 性状 1. 組成 本剤は 1 バッグ中 (300mL) に次の成分を含有 有効成分 添加物 リネゾリド 600mg ブドウ糖 13.702g クエン酸ナトリウム水和物
263 170 263 配合変化表 2018 年 11 月作成 オキサゾリジノン系合成抗菌剤 リネゾリド点滴静注液 リネゾリド注射液 製造販売元 : オキサゾリジノン系合成抗菌剤リネゾリド点滴静注液 リネゾリド注射液 配合変化表リネゾリド点滴静注液 組成 性状 1. 組成 本剤は 1 バッグ中 (300mL) に次の成分を含有 有効成分 添加物 リネゾリド 600mg ブドウ糖 13.702g クエン酸ナトリウム水和物
110607セチリジン5-1.indd
 使用上の注意改訂のお知らせ 2011 年 7 月田辺製薬販売株式会社 製造販売元田辺三菱製薬株式会社 このたび, 標記製品につきまして, 使用上の注意 を改訂しましたのでお知らせ致します 今後のご使用に際しましてご留意下さいますようお願い致します 今後とも弊社製品のご使用にあたって副作用 感染症等をご経験の際には, 弊社 MR までできるだけ速やかにご連絡下さいますようお願い申し上げます なお, このたびの改訂添付文書を封入した製品をお届けするには若干の日時を要しますので,
使用上の注意改訂のお知らせ 2011 年 7 月田辺製薬販売株式会社 製造販売元田辺三菱製薬株式会社 このたび, 標記製品につきまして, 使用上の注意 を改訂しましたのでお知らせ致します 今後のご使用に際しましてご留意下さいますようお願い致します 今後とも弊社製品のご使用にあたって副作用 感染症等をご経験の際には, 弊社 MR までできるだけ速やかにご連絡下さいますようお願い申し上げます なお, このたびの改訂添付文書を封入した製品をお届けするには若干の日時を要しますので,
(2) 健康成人の血漿中濃度 ( 反復経口投与 ) 9) 健康成人男子にスイニー 200mgを1 日 2 回 ( 朝夕食直前 ) 7 日間反復経口投与したとき 血漿中アナグリプチン濃度は投与 2 日目には定常状態に達した 投与 7 日目における C max 及びAUC 0-72hの累積係数はそれぞれ
 1. 血漿中濃度 (1) 健康成人の血漿中濃度 ( 単回経口投与 ) 8) 健康成人男子にスイニー 100mg 又は200mgを空腹時に単回経口投与したときの血漿中アナグリプチン濃度は 投与後約 1~ 2 時間で C maxに達した後 二相性の消失を示し t 1/2αは約 2 時間 t 1/2βは約 6 時間であった C max 及びAUC0- は投与量の増加に伴って増加した 血漿中アナグリプチン濃度推移
1. 血漿中濃度 (1) 健康成人の血漿中濃度 ( 単回経口投与 ) 8) 健康成人男子にスイニー 100mg 又は200mgを空腹時に単回経口投与したときの血漿中アナグリプチン濃度は 投与後約 1~ 2 時間で C maxに達した後 二相性の消失を示し t 1/2αは約 2 時間 t 1/2βは約 6 時間であった C max 及びAUC0- は投与量の増加に伴って増加した 血漿中アナグリプチン濃度推移
<4D F736F F D E5F836F D F934890C3928D E B81768AB38ED28CFC88E396F B A2E646F63>
 患者向医薬品ガイド 2017 年 7 月作成 塩酸バンコマイシン点滴静注用 0.5g HK この薬は? 販売名 一般名 含有量 (1 バイアル中 ) 塩酸バンコマイシン点滴静注用 0.5g HK Vancomycin for Injection 0.5 HK バンコマイシン塩酸塩 Vancomycin Hydrochloride バンコマイシン塩酸塩 0.5g( 力価 ) 患者向医薬品ガイドについて
患者向医薬品ガイド 2017 年 7 月作成 塩酸バンコマイシン点滴静注用 0.5g HK この薬は? 販売名 一般名 含有量 (1 バイアル中 ) 塩酸バンコマイシン点滴静注用 0.5g HK Vancomycin for Injection 0.5 HK バンコマイシン塩酸塩 Vancomycin Hydrochloride バンコマイシン塩酸塩 0.5g( 力価 ) 患者向医薬品ガイドについて
査を実施し 必要に応じ適切な措置を講ずること (2) 本品の警告 効能 効果 性能 用法 用量及び使用方法は以下のとお りであるので 特段の留意をお願いすること なお その他の使用上の注意については 添付文書を参照されたいこと 警告 1 本品投与後に重篤な有害事象の発現が認められていること 及び本品
 薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
Microsoft Word - 茬çfl�宛玺0618第1å‘·_æŠ¥èŒ¬é•£å®łã†¦é•ıç�¥ï¼‹ã…¡ã…‹ã…łã…«ã…�ㅳ;.doc
 薬生安発 0 6 1 8 第 1 号 令和元年 6 月 1 8 日 日本製薬団体連合会 安全性委員会委員長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 使用上の注意 の改訂について 令和元年度第 3 回薬事 食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会 ( 令和元年 5 月 31 日開催 ) における審議結果等を踏まえ 医薬品の 使用上の注意 の改訂が必要と考えますので 下記のとおり必要な措置を講ずるよう関係業者に対し周知徹底方お願い申し上げます
薬生安発 0 6 1 8 第 1 号 令和元年 6 月 1 8 日 日本製薬団体連合会 安全性委員会委員長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 使用上の注意 の改訂について 令和元年度第 3 回薬事 食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会 ( 令和元年 5 月 31 日開催 ) における審議結果等を踏まえ 医薬品の 使用上の注意 の改訂が必要と考えますので 下記のとおり必要な措置を講ずるよう関係業者に対し周知徹底方お願い申し上げます
<4D F736F F D208F64835C815B90C3928D E A8D8795CF89BB955C5F E3389FC92F95F2E646F63>
 薬効分類循環器官用薬の そ他の類剤 NS 配合変化表 ( 日本薬局方炭酸水素ナトリウム注射液 ) 日新製薬株式会社 1. 変動 NS (10mL) に 0.1mol/L 塩酸あるいは 0.1mol/L 水酸化ナトリウム液を加え ( 各々の最大添加量は 10mL) 変動及び変化を観察した NS 中 : 炭酸水素ナトリウム 1.4g 含有 規格 :7.0~8.5 : 4 5 6 7 8 9 10 11
薬効分類循環器官用薬の そ他の類剤 NS 配合変化表 ( 日本薬局方炭酸水素ナトリウム注射液 ) 日新製薬株式会社 1. 変動 NS (10mL) に 0.1mol/L 塩酸あるいは 0.1mol/L 水酸化ナトリウム液を加え ( 各々の最大添加量は 10mL) 変動及び変化を観察した NS 中 : 炭酸水素ナトリウム 1.4g 含有 規格 :7.0~8.5 : 4 5 6 7 8 9 10 11
別紙 成分名 該当商品名 ( 承認取得者 ) 効能 効果 アリセプト錠 3mg 同錠 5mg 同錠 10mg 同細粒 0.5% 同 D 錠 3mg 同 D ドネペジル塩酸塩ピルシカイニド塩酸塩水和物 ( 経口剤 ) ベプリジル塩酸塩水和物プロパフェノン塩酸塩ベラプロストナトリウム 錠 5mg 同 D
 自動車運転等に係る注意に関する 使用上の注意 の改訂について 成分名 該当商品名 別紙参照 成分名該当商品名 ( 承認取得者 ) 別紙参照 効能 効果 別紙参照 改訂の概要改訂の理由及び調査の結果直近 3 年度の国内副作用症例の集積状況 転帰死亡症例 重要な基本的注意 の項に自動車運転等に関する注意喚起を追記する 医薬品等の普及 安全に関する行政評価 監視結果に基づく勧告( 平成 25 年 3 月
自動車運転等に係る注意に関する 使用上の注意 の改訂について 成分名 該当商品名 別紙参照 成分名該当商品名 ( 承認取得者 ) 別紙参照 効能 効果 別紙参照 改訂の概要改訂の理由及び調査の結果直近 3 年度の国内副作用症例の集積状況 転帰死亡症例 重要な基本的注意 の項に自動車運転等に関する注意喚起を追記する 医薬品等の普及 安全に関する行政評価 監視結果に基づく勧告( 平成 25 年 3 月
1. 医薬品リスク管理計画を策定の上 適切に実施すること 2. 国内での治験症例が極めて限られていることから 製造販売後 一定数の症例に係るデータが集積されるまでの間は 全 症例を対象に使用成績調査を実施することにより 本剤使用患者の背景情報を把握するとともに 本剤の安全性及び有効性に関するデータを
 薬生薬審発 0525 第 3 号薬生安発 0525 第 1 号平成 30 年 5 月 25 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) トファシチニブクエン酸塩製剤の使用に当たっての留意事項について トファシチニブクエン酸塩製剤 ( 販売名 : ゼルヤンツ錠
薬生薬審発 0525 第 3 号薬生安発 0525 第 1 号平成 30 年 5 月 25 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) トファシチニブクエン酸塩製剤の使用に当たっての留意事項について トファシチニブクエン酸塩製剤 ( 販売名 : ゼルヤンツ錠
- 医薬品の適正使用に欠かせない情報です 必ずお読みください - 効能又は効果 用法及び用量の一部変更 使用上の注意改訂のお知らせ 平成 23 年 5 月 劇薬 処方せん医薬品 ( 注意 - 医師等の処方せんにより使用すること ) エタンブトール製剤 エタンブトール塩酸塩錠 このたび 標記製品の 効
 - 医薬品の適正使用に欠かせない情報です 必ずお読みください - 効能又は効果 用法及び用量の一部変更 使用上の注意改訂のお知らせ 平成 23 年 5 月 劇薬 処方せん医薬品 ( 注意 - 医師等の処方せんにより使用すること ) エタンブトール製剤 エタンブトール塩酸塩錠 このたび 標記製品の 効能又は効果 及び 用法及び用量 の一部変更が平成 23 年 5 月 20 日付にて 承認されました それに伴い
- 医薬品の適正使用に欠かせない情報です 必ずお読みください - 効能又は効果 用法及び用量の一部変更 使用上の注意改訂のお知らせ 平成 23 年 5 月 劇薬 処方せん医薬品 ( 注意 - 医師等の処方せんにより使用すること ) エタンブトール製剤 エタンブトール塩酸塩錠 このたび 標記製品の 効能又は効果 及び 用法及び用量 の一部変更が平成 23 年 5 月 20 日付にて 承認されました それに伴い
食欲不振 全身倦怠感 皮膚や白目が黄色くなる [ 肝機能障害 黄疸 ] 尿量減少 全身のむくみ 倦怠感 [ 急性腎不全 ] 激しい上腹部の痛み 腰背部の痛み 吐き気 [ 急性膵炎 ] 発熱 から咳 呼吸困難 [ 間質性肺炎 ] 排便の停止 腹痛 腹部膨満感 [ 腸閉塞 ] 手足の筋肉の痛み こわばり
![食欲不振 全身倦怠感 皮膚や白目が黄色くなる [ 肝機能障害 黄疸 ] 尿量減少 全身のむくみ 倦怠感 [ 急性腎不全 ] 激しい上腹部の痛み 腰背部の痛み 吐き気 [ 急性膵炎 ] 発熱 から咳 呼吸困難 [ 間質性肺炎 ] 排便の停止 腹痛 腹部膨満感 [ 腸閉塞 ] 手足の筋肉の痛み こわばり 食欲不振 全身倦怠感 皮膚や白目が黄色くなる [ 肝機能障害 黄疸 ] 尿量減少 全身のむくみ 倦怠感 [ 急性腎不全 ] 激しい上腹部の痛み 腰背部の痛み 吐き気 [ 急性膵炎 ] 発熱 から咳 呼吸困難 [ 間質性肺炎 ] 排便の停止 腹痛 腹部膨満感 [ 腸閉塞 ] 手足の筋肉の痛み こわばり](/thumbs/91/105740782.jpg) くすりのしおり内服剤 2013 年 11 月作成薬には効果 ( ベネフィット ) だけでなく副作用 ( リスク ) があります 副作用をなるべく抑え 効果を最大限に引き出すことが大切です そのために この薬を使用される患者さんの理解と協力が必要です 商品名 : グラクティブ錠 12.5mg 主成分 : シタグリプチンリン酸塩水和物 (Sitagliptin phosphate hydrate) 剤形
くすりのしおり内服剤 2013 年 11 月作成薬には効果 ( ベネフィット ) だけでなく副作用 ( リスク ) があります 副作用をなるべく抑え 効果を最大限に引き出すことが大切です そのために この薬を使用される患者さんの理解と協力が必要です 商品名 : グラクティブ錠 12.5mg 主成分 : シタグリプチンリン酸塩水和物 (Sitagliptin phosphate hydrate) 剤形
膿疱性乾癬の効能追加 ( 承認事項の 部変更承認 ) に伴う改訂 改訂内容 ( 該当部のみ抜粋 ) 警告 1.~3. 4. 関節リウマチ患者では, 本剤の治療を行う前に, 少なくとも 1 剤の抗リウマチ薬等の使用を十分勘案すること. また, 本剤についての十分な知識とリウマチ治療の経験をもつ医師が使
 - 医薬品の適正使 に かせない情報です 必ずお読みください - 添付文書改訂のお知らせ 注 ) 物由来製品 劇薬 処 箋医薬品 2018 年 3-4 月 この度 新たな効能として膿疱性乾癬が承認され (20mg 製剤を除く ) これに伴い添付文書 ( 効能 効果 用法 用量 使用上の注意 等 ) を改訂致しました 今後のご使用に際しましては 以下の内容をご参照くださいますようお願い申し上げます なお
- 医薬品の適正使 に かせない情報です 必ずお読みください - 添付文書改訂のお知らせ 注 ) 物由来製品 劇薬 処 箋医薬品 2018 年 3-4 月 この度 新たな効能として膿疱性乾癬が承認され (20mg 製剤を除く ) これに伴い添付文書 ( 効能 効果 用法 用量 使用上の注意 等 ) を改訂致しました 今後のご使用に際しましては 以下の内容をご参照くださいますようお願い申し上げます なお
用法 用量に関連する使用上の注意 1) 本剤の使用にあたっては 耐性菌の発現等を防ぐため 原則として感受性を確認し 疾病の治療上必要な最小限の期間の投与にとどめること 2) 高度の腎障害のある患者には 投与量を減らすか 投与間隔をあけて投与するなど慎重に投与すること [ 慎重投与 の項参照 ] 3)
![用法 用量に関連する使用上の注意 1) 本剤の使用にあたっては 耐性菌の発現等を防ぐため 原則として感受性を確認し 疾病の治療上必要な最小限の期間の投与にとどめること 2) 高度の腎障害のある患者には 投与量を減らすか 投与間隔をあけて投与するなど慎重に投与すること [ 慎重投与 の項参照 ] 3) 用法 用量に関連する使用上の注意 1) 本剤の使用にあたっては 耐性菌の発現等を防ぐため 原則として感受性を確認し 疾病の治療上必要な最小限の期間の投与にとどめること 2) 高度の腎障害のある患者には 投与量を減らすか 投与間隔をあけて投与するなど慎重に投与すること [ 慎重投与 の項参照 ] 3)](/thumbs/91/104694910.jpg) 2018 年 7 月改訂 ( 第 23 版 ) 2017 年 10 月改訂貯法 : 室温保存 ( 湿気を避けること ) 使用期限 : 包装に表示の期限内に使用すること 合成ペニシリン製剤 処方箋医薬品 日本薬局方アモキシシリンカプセル PASC3 日本標準商品分類番号 876131 PASETOCIN Capsules 注意 - 医師等の処方箋により使用すること 125mgカプセル 250mgカプセル
2018 年 7 月改訂 ( 第 23 版 ) 2017 年 10 月改訂貯法 : 室温保存 ( 湿気を避けること ) 使用期限 : 包装に表示の期限内に使用すること 合成ペニシリン製剤 処方箋医薬品 日本薬局方アモキシシリンカプセル PASC3 日本標準商品分類番号 876131 PASETOCIN Capsules 注意 - 医師等の処方箋により使用すること 125mgカプセル 250mgカプセル
<4D F736F F D2082A8926D82E782B995B68F D815B838B4E618FF931306D E3131>
 医薬品の適正使用に欠かせない情報です 必ずお読みください 効能 効果 用法 用量 追加及び 使用上の注意 改訂のお知らせ 2012 年 11 月 東和薬品株式会社 このたび 平成 24 年 5 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 24 年 11 月 19 日付にて 下記の内容で承認されました また 使用上の注意 の項も改訂致しましたので 併せてお知らせ申し上げます
医薬品の適正使用に欠かせない情報です 必ずお読みください 効能 効果 用法 用量 追加及び 使用上の注意 改訂のお知らせ 2012 年 11 月 東和薬品株式会社 このたび 平成 24 年 5 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 24 年 11 月 19 日付にて 下記の内容で承認されました また 使用上の注意 の項も改訂致しましたので 併せてお知らせ申し上げます
情報提供の例
 163 セレギリン塩酸塩 ( 神経 8) 標榜薬効 ( 薬効コード ) 抗パーキンソン剤 (116) 平成 23 年 9 月 26 日新規 平成 28 年 9 月 14 日 追記 成分名セレギリン塩酸塩 内服薬 主な製品名エフピー OD 錠 他後発品あり 承認されている効能 効果次の疾患に対するレボドパ含有製剤との併用療法パーキンソン病 ( 過去のレボドパ含有製剤治療において 十分な効果が得られていないもの
163 セレギリン塩酸塩 ( 神経 8) 標榜薬効 ( 薬効コード ) 抗パーキンソン剤 (116) 平成 23 年 9 月 26 日新規 平成 28 年 9 月 14 日 追記 成分名セレギリン塩酸塩 内服薬 主な製品名エフピー OD 錠 他後発品あり 承認されている効能 効果次の疾患に対するレボドパ含有製剤との併用療法パーキンソン病 ( 過去のレボドパ含有製剤治療において 十分な効果が得られていないもの
「 」 説明および同意書
 EDP( エトポシド + ドキソルビシン + シスプラチン ) 療法 説明および同意書 四国がんセンター泌尿器科 患者氏名 ( ) さん 御本人さんのみへの説明でよろしいですか? ( 同席者の氏名をすべて記載 ) ( ( はい ) ) < 病名 > 副腎がん 転移部位 ( ) < 治療 > EDP 療法 (E: エトポシド D: ドキソルビシン P: シスプラチン ) < 治療開始予定日 > 平成
EDP( エトポシド + ドキソルビシン + シスプラチン ) 療法 説明および同意書 四国がんセンター泌尿器科 患者氏名 ( ) さん 御本人さんのみへの説明でよろしいですか? ( 同席者の氏名をすべて記載 ) ( ( はい ) ) < 病名 > 副腎がん 転移部位 ( ) < 治療 > EDP 療法 (E: エトポシド D: ドキソルビシン P: シスプラチン ) < 治療開始予定日 > 平成
より詳細な情報を望まれる場合は 担当の医師または薬剤師におたずねください また 患者向医薬品ガイド 医療専門家向けの 添付文書情報 が医薬品医療機器総合機構のホームページに掲載されています
 くすりのしおり内服剤 2014 年 6 月作成薬には効果 ( ベネフィット ) だけでなく副作用 ( リスク ) があります 副作用をなるべく抑え 効果を最大限に引き出すことが大切です そのために この薬を使用される患者さんの理解と協力が必要です 商品名 : バルサルタン錠 20mg AA 主成分 : バルサルタン (Valsartan) 剤形 : 淡黄色の錠剤 直径約 7.2mm 厚さ約 3.1mm
くすりのしおり内服剤 2014 年 6 月作成薬には効果 ( ベネフィット ) だけでなく副作用 ( リスク ) があります 副作用をなるべく抑え 効果を最大限に引き出すことが大切です そのために この薬を使用される患者さんの理解と協力が必要です 商品名 : バルサルタン錠 20mg AA 主成分 : バルサルタン (Valsartan) 剤形 : 淡黄色の錠剤 直径約 7.2mm 厚さ約 3.1mm
ヒアルロン酸ナトリウム架橋体製剤 特定使用成績調査
 ヒアルロン酸ナトリウム架橋体製剤 ( サイビスクディスポ 関節注 2mL) 特定使用成績調査 (J-STEP/EL) 謹啓時下ますますご清祥のこととお喜び申し上げます 平素より格別のご高配を賜り 厚く御礼申し上げます さて ヒアルロン酸ナトリウム架橋体製剤 ( サイビスクディスポ 関節注 2mL) は 保存的非薬物治療及び経口薬物治療が十分奏功しない疼痛を有する変形性膝関節症の患者を対象に 本剤の製造販売後の使用実態下における複数回使用を含めた安全性及び有効性について確認することを目的として
ヒアルロン酸ナトリウム架橋体製剤 ( サイビスクディスポ 関節注 2mL) 特定使用成績調査 (J-STEP/EL) 謹啓時下ますますご清祥のこととお喜び申し上げます 平素より格別のご高配を賜り 厚く御礼申し上げます さて ヒアルロン酸ナトリウム架橋体製剤 ( サイビスクディスポ 関節注 2mL) は 保存的非薬物治療及び経口薬物治療が十分奏功しない疼痛を有する変形性膝関節症の患者を対象に 本剤の製造販売後の使用実態下における複数回使用を含めた安全性及び有効性について確認することを目的として
DRAFT#9 2011
 報道関係各位 2019 年 1 月 8 日 ユーシービージャパン株式会社 抗てんかん剤 ビムパット ドライシロップ 10% 及び ビムパット 点滴静注 200mg 製造販売承認のお知らせ ユーシービージャパン株式会社 ( 本社 : 東京都新宿区 代表取締役社長 : 菊池加奈子 以下 ユーシービージャパン また ユーシービーグループを総称して以下 ユーシービー ) は本日 抗てんかん剤 ビムパット ドライシロップ
報道関係各位 2019 年 1 月 8 日 ユーシービージャパン株式会社 抗てんかん剤 ビムパット ドライシロップ 10% 及び ビムパット 点滴静注 200mg 製造販売承認のお知らせ ユーシービージャパン株式会社 ( 本社 : 東京都新宿区 代表取締役社長 : 菊池加奈子 以下 ユーシービージャパン また ユーシービーグループを総称して以下 ユーシービー ) は本日 抗てんかん剤 ビムパット ドライシロップ
腎薬ニュース第 5 号 (2007 年 6 月 ;2012 年 1 月加筆修正 ) 熊本大学薬学部臨床薬理学分野平田純生 添付文書どおり腎機能に基づいた投与量にしても起こるアシクロビル中毒の原因は? 1. アシクロビル中毒の症状は? 慢性腎臓病 (CKD) 患者に頻発するアシクロビル バラシクロビル
 腎薬ニュース第 5 号 (2007 年 6 月 ;2012 年 1 月加筆修正 ) 熊本大学薬学部臨床薬理学分野平田純生 添付文書どおり腎機能に基づいた投与量にしても起こるアシクロビル中毒の原因は? 1. アシクロビル中毒の症状は? 慢性腎臓病 (CKD) 患者に頻発するアシクロビル バラシクロビル中毒の特徴は呂律困難 振戦 幻視 幻聴 昏迷 昏睡などの症状を伴う意識障害が代表的です 腎不全で精神神経症状や痙攣を起こす薬物は
腎薬ニュース第 5 号 (2007 年 6 月 ;2012 年 1 月加筆修正 ) 熊本大学薬学部臨床薬理学分野平田純生 添付文書どおり腎機能に基づいた投与量にしても起こるアシクロビル中毒の原因は? 1. アシクロビル中毒の症状は? 慢性腎臓病 (CKD) 患者に頻発するアシクロビル バラシクロビル中毒の特徴は呂律困難 振戦 幻視 幻聴 昏迷 昏睡などの症状を伴う意識障害が代表的です 腎不全で精神神経症状や痙攣を起こす薬物は
<4D F736F F D D A616C5F208E FE382CC928D88D389F090E08F915F A E A2E646F63>
 市販直後調査平成 22 年 12 月 ~ 平成 23 年 6 月 2010 年 12 月作成 - 医薬品の適正使用に欠かせない情報です 必ずお読みください - 新医薬品の 使用上の注意 の解説 持続性選択 H1 受容体拮抗 アレルギー性疾患治療剤 処方せん医薬品 ( 注意 - 医師等の処方せんにより使用すること ) 禁忌 ( 次の患者には投与しないこと ) (1) 本剤の成分又はピペラジン誘導体 (
市販直後調査平成 22 年 12 月 ~ 平成 23 年 6 月 2010 年 12 月作成 - 医薬品の適正使用に欠かせない情報です 必ずお読みください - 新医薬品の 使用上の注意 の解説 持続性選択 H1 受容体拮抗 アレルギー性疾患治療剤 処方せん医薬品 ( 注意 - 医師等の処方せんにより使用すること ) 禁忌 ( 次の患者には投与しないこと ) (1) 本剤の成分又はピペラジン誘導体 (
デベルザ錠20mg 適正使用のお願い
 2014 年 3 月作成薬価基準未収載 - 医薬品の適正使用に欠かせない情報です 使用前に必ずお読みください - 適正使用のお願い 処方せん医薬品 : 注意 - 医師等の処方せんにより使用すること 製造販売元 販売元 適応となる患者さんとデベルザ錠の使い方 本剤を投与する前に 以下のことを確認してください 2 型糖尿病の患者さんですか 本剤の効能 効果は 2 型糖尿病 です 1 型糖尿病の患者さんは
2014 年 3 月作成薬価基準未収載 - 医薬品の適正使用に欠かせない情報です 使用前に必ずお読みください - 適正使用のお願い 処方せん医薬品 : 注意 - 医師等の処方せんにより使用すること 製造販売元 販売元 適応となる患者さんとデベルザ錠の使い方 本剤を投与する前に 以下のことを確認してください 2 型糖尿病の患者さんですか 本剤の効能 効果は 2 型糖尿病 です 1 型糖尿病の患者さんは
社内資料 ph 変動試験 セファゾリン Na 注射用 1g NP 2014 年 6 月ニプロ株式会社 セファゾリン Na 注射用 1g NP の ph 変動試験 1. 試験目的セファゾリン Na 注射用 1g NP は セファゾリンナトリウムを有効成分とするセファロスポリン系抗生物質製剤である 今回
 社内資料 ph 変動試験 セファゾリン Na 注射用 1g NP 2014 年 6 月ニプロ株式会社 セファゾリン Na 注射用 1g NP 配合変化試験 ~ph 変動試験 ~ 1/2 社内資料 ph 変動試験 セファゾリン Na 注射用 1g NP 2014 年 6 月ニプロ株式会社 セファゾリン Na 注射用 1g NP の ph 変動試験 1. 試験目的セファゾリン Na 注射用 1g NP
社内資料 ph 変動試験 セファゾリン Na 注射用 1g NP 2014 年 6 月ニプロ株式会社 セファゾリン Na 注射用 1g NP 配合変化試験 ~ph 変動試験 ~ 1/2 社内資料 ph 変動試験 セファゾリン Na 注射用 1g NP 2014 年 6 月ニプロ株式会社 セファゾリン Na 注射用 1g NP の ph 変動試験 1. 試験目的セファゾリン Na 注射用 1g NP
扶桑薬品工業 再審査結果のお知らせ 無水エタノール注
 医薬品の適正使用に欠かせない情報です 必ずお読みください 再審査結果 使用上の注意改訂のお知らせ 経皮的エタノール注入療法用剤 処方せん医薬品 ( 注意 医師等の処方せんにより使用すること ) 無水エタノール注 フソー このたび経皮的エタノール注入療法用剤無水エタノール注 フソー につきまして 薬事法第 14 条の 4 第 3 項の規定による再審査が終了し 再審査結果が通知されました その結果 効能
医薬品の適正使用に欠かせない情報です 必ずお読みください 再審査結果 使用上の注意改訂のお知らせ 経皮的エタノール注入療法用剤 処方せん医薬品 ( 注意 医師等の処方せんにより使用すること ) 無水エタノール注 フソー このたび経皮的エタノール注入療法用剤無水エタノール注 フソー につきまして 薬事法第 14 条の 4 第 3 項の規定による再審査が終了し 再審査結果が通知されました その結果 効能
使用上の注意 1. 慎重投与 ( 次の患者には慎重に投与すること ) 1) セフェム系抗生物質に対し過敏症の既往歴のある患者 2) 本人又は両親 兄弟に気管支喘息 発疹 蕁麻疹等のアレルギー症状を起こしやすい体質を有する患者 3) 高度の腎障害のある患者 [ 高い血中濃度が持続することがある ] 4
![使用上の注意 1. 慎重投与 ( 次の患者には慎重に投与すること ) 1) セフェム系抗生物質に対し過敏症の既往歴のある患者 2) 本人又は両親 兄弟に気管支喘息 発疹 蕁麻疹等のアレルギー症状を起こしやすい体質を有する患者 3) 高度の腎障害のある患者 [ 高い血中濃度が持続することがある ] 4 使用上の注意 1. 慎重投与 ( 次の患者には慎重に投与すること ) 1) セフェム系抗生物質に対し過敏症の既往歴のある患者 2) 本人又は両親 兄弟に気管支喘息 発疹 蕁麻疹等のアレルギー症状を起こしやすい体質を有する患者 3) 高度の腎障害のある患者 [ 高い血中濃度が持続することがある ] 4](/thumbs/91/105360333.jpg) 2017 年 10 月改訂 ( 第 21 版 ) 2017 年 9 月改訂貯法 : 室温保存 ( 湿気を避けること ) 使用期限 : 包装に表示の期限内に使用すること 合成ペニシリン製剤 処方箋医薬品 PAST2 日本標準商品分類番号 876131 PASETOCIN Tablets 250 アモキシシリン水和物錠 注意 - 医師等の処方箋により使用すること 承認番号薬価収載販売開始再審査結果再評価結果効能追加
2017 年 10 月改訂 ( 第 21 版 ) 2017 年 9 月改訂貯法 : 室温保存 ( 湿気を避けること ) 使用期限 : 包装に表示の期限内に使用すること 合成ペニシリン製剤 処方箋医薬品 PAST2 日本標準商品分類番号 876131 PASETOCIN Tablets 250 アモキシシリン水和物錠 注意 - 医師等の処方箋により使用すること 承認番号薬価収載販売開始再審査結果再評価結果効能追加
アビガン錠 200mg に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 アビガン錠 200mg 有効成分 ファビピラビル 製造販売業者 富士フイルム富山化学株式会社 薬効分類 提出年月 平成 30 年 10 月 1.1. 安全性検討事項 重要な特定されたリスク 頁 重要な潜在
 アビガン錠 200mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任は, 富士フイルム富山化学株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません 富士フイルム富山化学株式会社 アビガン錠 200mg に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 アビガン錠 200mg 有効成分 ファビピラビル 製造販売業者 富士フイルム富山化学株式会社
アビガン錠 200mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任は, 富士フイルム富山化学株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません 富士フイルム富山化学株式会社 アビガン錠 200mg に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 アビガン錠 200mg 有効成分 ファビピラビル 製造販売業者 富士フイルム富山化学株式会社
<4D F736F F D A CC82A082C4817A88E396F CC934B899E8A4F8E C98C5782E995DB8CAF906697C38FE382CC8EE688B582A282C
 保医発 0316 第 1 号 平成 24 年 3 月 16 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 厚生労働省保険局歯科医療管理官 医薬品の適応外使用に係る保険診療上の取扱いについて 保険診療における医薬品の取扱いについては 厚生労働大臣が承認した効能又は効果
保医発 0316 第 1 号 平成 24 年 3 月 16 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 厚生労働省保険局歯科医療管理官 医薬品の適応外使用に係る保険診療上の取扱いについて 保険診療における医薬品の取扱いについては 厚生労働大臣が承認した効能又は効果
p 13
 p 12 p 13 p 14 p 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 10. 安全性 (1) 副作用 ( 臨床検査値異常を含む ) 総症例 1030 例中 副作用が報告されたのは 519 例 (50.4%) でした 主な症状は鼓腸 197 例 (19.1%) 下痢 188 例 (18.3%) 腹部膨満
p 12 p 13 p 14 p 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 10. 安全性 (1) 副作用 ( 臨床検査値異常を含む ) 総症例 1030 例中 副作用が報告されたのは 519 例 (50.4%) でした 主な症状は鼓腸 197 例 (19.1%) 下痢 188 例 (18.3%) 腹部膨満
<4D F736F F D FC8D65816A58797A616C F8E FE382CC928D88D389F090E08F E328B6C82DF816A2E646F6378>
 市販直後調査平成 26 年 4 月 ~ 平成 26 年 10 月 2014 年 4 月作成 - 医薬品の適正使用に欠かせない情報です 必ずお読みください - 新医薬品の 使用上の注意 の解説 持続性選択 H 1 受容体拮抗 アレルギー性疾患治療剤 処方せん医薬品 ( 注意 - 医師等の処方せんにより使用すること ) レボセチリジン塩酸塩シロップ 禁忌 ( 次の患者には投与しないこと ) (1) 本剤の成分又はピペラジン誘導体
市販直後調査平成 26 年 4 月 ~ 平成 26 年 10 月 2014 年 4 月作成 - 医薬品の適正使用に欠かせない情報です 必ずお読みください - 新医薬品の 使用上の注意 の解説 持続性選択 H 1 受容体拮抗 アレルギー性疾患治療剤 処方せん医薬品 ( 注意 - 医師等の処方せんにより使用すること ) レボセチリジン塩酸塩シロップ 禁忌 ( 次の患者には投与しないこと ) (1) 本剤の成分又はピペラジン誘導体
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠 50mg 医薬品リスク管理計画書 (RMP) の概要 有効成分 タペンタ 錠 100mg 製造販売業者 ヤンセンファーマ株式会社 薬効分類 821 提出年月 平成 30 年
 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
2017 年 9 月 画像診断部 中央放射線科 造影剤投与マニュアル ver 2.0 本マニュアルは ESUR 造影剤ガイドライン version 9.0(ESUR: 欧州泌尿生殖器放射線学会 ) などを参照し 前マニュアルを改訂して作成した ( 前マニュアル作成 2014 年 3 月 今回の改訂
 2017 年 9 月 画像診断部 中央放射線科 造影剤投与マニュアル ver 2.0 本マニュアルは ESUR 造影剤ガイドライン version 9.0(ESUR: 欧州泌尿生殖器放射線学会 ) などを参照し 前マニュアルを改訂して作成した ( 前マニュアル作成 2014 年 3 月 今回の改訂 2017 年 8 月 ) 新たなエビデンスの報告や運用上困難な場合は適宜変更を加える 1. 造影剤アレルギーの既往を有する患者への対応
2017 年 9 月 画像診断部 中央放射線科 造影剤投与マニュアル ver 2.0 本マニュアルは ESUR 造影剤ガイドライン version 9.0(ESUR: 欧州泌尿生殖器放射線学会 ) などを参照し 前マニュアルを改訂して作成した ( 前マニュアル作成 2014 年 3 月 今回の改訂 2017 年 8 月 ) 新たなエビデンスの報告や運用上困難な場合は適宜変更を加える 1. 造影剤アレルギーの既往を有する患者への対応
2012 年 7 月 18 日放送 嫌気性菌感染症 愛知医科大学大学院感染制御学教授 三鴨廣繁 嫌気性菌とは嫌気性菌とは 酸素分子のない環境で生活をしている細菌です 偏性嫌気性菌と通性嫌気性菌があります 偏性嫌気性菌とは 酸素分子 20% を含む環境 すなわち大気中では全く発育しない細菌のことで 通
 2012 年 7 月 18 日放送 嫌気性菌感染症 愛知医科大学大学院感染制御学教授 三鴨廣繁 嫌気性菌とは嫌気性菌とは 酸素分子のない環境で生活をしている細菌です 偏性嫌気性菌と通性嫌気性菌があります 偏性嫌気性菌とは 酸素分子 20% を含む環境 すなわち大気中では全く発育しない細菌のことで 通性嫌気性菌とは 酸素に抵抗性を獲得したため大気中でもある程度増殖できるようになった細菌で 大腸菌や黄色ブドウ球菌などがこれに属します
2012 年 7 月 18 日放送 嫌気性菌感染症 愛知医科大学大学院感染制御学教授 三鴨廣繁 嫌気性菌とは嫌気性菌とは 酸素分子のない環境で生活をしている細菌です 偏性嫌気性菌と通性嫌気性菌があります 偏性嫌気性菌とは 酸素分子 20% を含む環境 すなわち大気中では全く発育しない細菌のことで 通性嫌気性菌とは 酸素に抵抗性を獲得したため大気中でもある程度増殖できるようになった細菌で 大腸菌や黄色ブドウ球菌などがこれに属します
160223メトトレキサート1_4.indd
 使用上の注意改訂のお知らせ 2016 年 3 月 田辺三菱製薬株式会社 このたび 標記製品につきまして 使用上の注意 を改訂しましたのでお知らせ致します 今後のご使用に際しましては 下記内容をご参照下さいますようお願い致します 改訂概要 改訂項目改訂内容 副作用 ( その他の副作用 ) 悪寒を追記し 先発医薬品の記載順に合わせて記載整備しました -1- 使用上の注意 の改訂内容 (3~6 頁に改訂後の
使用上の注意改訂のお知らせ 2016 年 3 月 田辺三菱製薬株式会社 このたび 標記製品につきまして 使用上の注意 を改訂しましたのでお知らせ致します 今後のご使用に際しましては 下記内容をご参照下さいますようお願い致します 改訂概要 改訂項目改訂内容 副作用 ( その他の副作用 ) 悪寒を追記し 先発医薬品の記載順に合わせて記載整備しました -1- 使用上の注意 の改訂内容 (3~6 頁に改訂後の
Epilepsy2015
 Key Concepts 1. 患者個々の治療のゴールをできるだけ早く設定 てんかんの薬物治療 薬物治療学 小川竜一 か または他の抗てんかん薬へ切り替える 第一 選択薬とは異なる作用機序の薬物 3. 年齢や合併症 服薬コンプライアンスなどの基本 情報も抗てんかん薬の選択に影響 2. 抗てんかん薬の投与が中止できる患者も存在する 決定する必要がある 50%~70%は単剤で管理でき る 2 慢性の脳の病気
Key Concepts 1. 患者個々の治療のゴールをできるだけ早く設定 てんかんの薬物治療 薬物治療学 小川竜一 か または他の抗てんかん薬へ切り替える 第一 選択薬とは異なる作用機序の薬物 3. 年齢や合併症 服薬コンプライアンスなどの基本 情報も抗てんかん薬の選択に影響 2. 抗てんかん薬の投与が中止できる患者も存在する 決定する必要がある 50%~70%は単剤で管理でき る 2 慢性の脳の病気
患者向け医薬品ガイド
 患者向医薬品ガイド 2013 年 6 月作成 この薬は? 販売名一般名含有量 (1バイアル中) Evoltra 20mg I.V. Infusion クロファラビン Clofarabine 20mg 患者向医薬品ガイドについて 患者向医薬品ガイドは 患者の皆様や家族の方などに 医療用医薬品の正しい理解と 重大な副作用の早期発見などに役立てていただくために作成したものです したがって この医薬品を使用するときに特に知っていただきたいことを
患者向医薬品ガイド 2013 年 6 月作成 この薬は? 販売名一般名含有量 (1バイアル中) Evoltra 20mg I.V. Infusion クロファラビン Clofarabine 20mg 患者向医薬品ガイドについて 患者向医薬品ガイドは 患者の皆様や家族の方などに 医療用医薬品の正しい理解と 重大な副作用の早期発見などに役立てていただくために作成したものです したがって この医薬品を使用するときに特に知っていただきたいことを
名称未設定
 健感発 00 第 1 号 令和元年 月 日 都道府県知事 各保健所設置市長 特別区長 殿 厚生労働省健康局結核感染課長 ( 公印省略 元号を改める政令の施行に伴う通知様式の改正について 元号を改める政令 ( 平成 31 年政令第 13 号 が平成 31 年 月 1 日に公布され 同年 月 1 日から施行されたことに伴い 健康局結核感染課関係の通知等において示している様式については 平成 を 令和 に変更する等
健感発 00 第 1 号 令和元年 月 日 都道府県知事 各保健所設置市長 特別区長 殿 厚生労働省健康局結核感染課長 ( 公印省略 元号を改める政令の施行に伴う通知様式の改正について 元号を改める政令 ( 平成 31 年政令第 13 号 が平成 31 年 月 1 日に公布され 同年 月 1 日から施行されたことに伴い 健康局結核感染課関係の通知等において示している様式については 平成 を 令和 に変更する等
禁忌を含む使用上の注意 等は DI 頁をご参照ください 臨床成績 本剤での臨床試験は実施していませんが 本剤を溶解したものはセファメジン注射用 筋注用と同一のものなので セファメジン注射用 筋注用の成績を以下に示します 比較試験 ( 呼吸器感染症 尿路感染症 ) 及び一般臨床試験 ( 静注 点滴静注
 日本標準商品分類番号 8763 薬価基準収載 処方箋医薬品 ( 注意 医師等の処方箋により使用すること ) 禁忌( 次の患者には投与しないこと ) () 本剤の成分によるショックの既往歴のある患者 () 筋注用 0.5g 0.5gのみ該当 リドカイン等のアニリド系局所麻酔剤に対し 過敏症の既往歴のある患者 [ 添付の溶解液はリドカインを含有している ] 原則禁忌( 次の患者には投与しないことを原則とするが
日本標準商品分類番号 8763 薬価基準収載 処方箋医薬品 ( 注意 医師等の処方箋により使用すること ) 禁忌( 次の患者には投与しないこと ) () 本剤の成分によるショックの既往歴のある患者 () 筋注用 0.5g 0.5gのみ該当 リドカイン等のアニリド系局所麻酔剤に対し 過敏症の既往歴のある患者 [ 添付の溶解液はリドカインを含有している ] 原則禁忌( 次の患者には投与しないことを原則とするが
緒言
 CERA 2.2 緒言 Page 1 ミルセラ注シリンジ25 μg ミルセラ注シリンジ50 μg ミルセラ注シリンジ75 μg ミルセラ注シリンジ100 μg ミルセラ注シリンジ150 μg ミルセラ注シリンジ200 μg ミルセラ注シリンジ250 μg [ 腎性貧血 ] 第 2 部 CTD の概要 ( サマリー ) 2.2 緒言 中外製薬株式会社 CERA 2.2 緒言 Page 2 目次頁 2.2
CERA 2.2 緒言 Page 1 ミルセラ注シリンジ25 μg ミルセラ注シリンジ50 μg ミルセラ注シリンジ75 μg ミルセラ注シリンジ100 μg ミルセラ注シリンジ150 μg ミルセラ注シリンジ200 μg ミルセラ注シリンジ250 μg [ 腎性貧血 ] 第 2 部 CTD の概要 ( サマリー ) 2.2 緒言 中外製薬株式会社 CERA 2.2 緒言 Page 2 目次頁 2.2
Microsoft Word - オーソ_201302_Final.docx
 医薬品の適正使用に欠かせない情報です 必ずお読みください H24-11 平成 25 年 2 月 / ( ノルエチステロン エチニルエストラジオール錠 ) 使用上の注意改訂のご案内 製造販売元ヤンセンファーマ株式会社 / 発売元持田製薬株式会社 この度 オーソ 777-21 錠 / オーソ M-21 錠の 使用上の注意 を改訂致しましたので ご案内申し上げます 今後のご使用に際しましては 下記内容にご留意くださいますようお願い致します
医薬品の適正使用に欠かせない情報です 必ずお読みください H24-11 平成 25 年 2 月 / ( ノルエチステロン エチニルエストラジオール錠 ) 使用上の注意改訂のご案内 製造販売元ヤンセンファーマ株式会社 / 発売元持田製薬株式会社 この度 オーソ 777-21 錠 / オーソ M-21 錠の 使用上の注意 を改訂致しましたので ご案内申し上げます 今後のご使用に際しましては 下記内容にご留意くださいますようお願い致します
日本医薬品安全性学会 COI 開示 筆頭発表者 : 加藤祐太 演題発表に関連し 開示すべき COI 関連の企業などはありません
 医薬品副作用データベース (JADER) を用いた市販後の副作用発現状況の検討 加藤祐太 1)2) 岸達生 3) 高松昭司 2) 白石正 4) 1) 山形大学医学部医薬品医療機器評価学講座 2) 医薬品医療機器総合機構安全第二部 3) 医薬品医療機器総合機構信頼性保証部 4) 山形大学医学部附属病院薬剤部 日本医薬品安全性学会 COI 開示 筆頭発表者 : 加藤祐太 演題発表に関連し 開示すべき COI
医薬品副作用データベース (JADER) を用いた市販後の副作用発現状況の検討 加藤祐太 1)2) 岸達生 3) 高松昭司 2) 白石正 4) 1) 山形大学医学部医薬品医療機器評価学講座 2) 医薬品医療機器総合機構安全第二部 3) 医薬品医療機器総合機構信頼性保証部 4) 山形大学医学部附属病院薬剤部 日本医薬品安全性学会 COI 開示 筆頭発表者 : 加藤祐太 演題発表に関連し 開示すべき COI
シプロフロキサシン
 シプロフロキサシン点滴静注液 300mg DK の 配合変化試験 大興製薬株式会社 共和薬品工業株式会社 作成年月日 :2010.12.22 CPFX-D-8( 1 シプロフロキサシン点滴静注液 300mg DK の配合変化試験 1. 試験目的シプロフロキサシン点滴静注液 300mg DK は 有効成分としてシプロフロキサシンを 300mg 含有するニューキノロン系注射用抗菌剤である 今回 本製剤について各輸液及び注射剤における配合変化試験を実施し
シプロフロキサシン点滴静注液 300mg DK の 配合変化試験 大興製薬株式会社 共和薬品工業株式会社 作成年月日 :2010.12.22 CPFX-D-8( 1 シプロフロキサシン点滴静注液 300mg DK の配合変化試験 1. 試験目的シプロフロキサシン点滴静注液 300mg DK は 有効成分としてシプロフロキサシンを 300mg 含有するニューキノロン系注射用抗菌剤である 今回 本製剤について各輸液及び注射剤における配合変化試験を実施し
改訂後 改訂前 使用上の注意 3. 副作用 (1) 重大な副作用 ( 頻度不明 ) 下記の重大な副作用があらわれることがあるので 観察を十分に行い 異常が認められた場合には投与を中止し 適切な処置を行うこと ₁) 現行通り ₂) 中毒性表皮壊死融解症 (Toxic Epidermal Necroly
 医薬品の適正使用に欠かせない情報です 必ずお読みください 使用上の注意改訂のお知らせ 広範囲経口抗菌製剤 レボフロキサシン水和物製剤 処方せん医薬品 : 注意 医師等の処方せんにより使用すること 製造販売元 2010 年 10 月 このたび 標記製品の 使用上の注意 の一部を改訂いたしましたので ご連絡申し上げます 本剤につきましては 既にご案内をさせて頂きましたとおり 厚生労働省告示第 76 号
医薬品の適正使用に欠かせない情報です 必ずお読みください 使用上の注意改訂のお知らせ 広範囲経口抗菌製剤 レボフロキサシン水和物製剤 処方せん医薬品 : 注意 医師等の処方せんにより使用すること 製造販売元 2010 年 10 月 このたび 標記製品の 使用上の注意 の一部を改訂いたしましたので ご連絡申し上げます 本剤につきましては 既にご案内をさせて頂きましたとおり 厚生労働省告示第 76 号
2006 年 3 月 3 日放送 抗菌薬の適正使用 市立堺病院薬剤科科長 阿南節子 薬剤師は 抗菌薬投与計画の作成のためにパラメータを熟知すべき 最初の抗菌薬であるペニシリンが 実質的に広く使用されるようになったのは第二次世界大戦後のことです それまで致死的な状況であった黄色ブドウ球菌による感染症に
 2006 年 3 月 3 日放送 抗菌薬の適正使用 市立堺病院薬剤科科長 阿南節子 薬剤師は 抗菌薬投与計画の作成のためにパラメータを熟知すべき 最初の抗菌薬であるペニシリンが 実質的に広く使用されるようになったのは第二次世界大戦後のことです それまで致死的な状況であった黄色ブドウ球菌による感染症に対して ペニシリンは劇的な効果を発揮しました しかし その後ペニシリンが広範囲に使用されたことによって
2006 年 3 月 3 日放送 抗菌薬の適正使用 市立堺病院薬剤科科長 阿南節子 薬剤師は 抗菌薬投与計画の作成のためにパラメータを熟知すべき 最初の抗菌薬であるペニシリンが 実質的に広く使用されるようになったのは第二次世界大戦後のことです それまで致死的な状況であった黄色ブドウ球菌による感染症に対して ペニシリンは劇的な効果を発揮しました しかし その後ペニシリンが広範囲に使用されたことによって
リクスビス使用上の注意解説_ pdf
 2017 年 1 月作成 ( 第 3 版 ) 医薬品の適正使用に欠かせない情報です 使用前に必ずお読みください 新医薬品の の解説 生物由来製品 ) 処方箋医薬品注 遺伝子組換え血液凝固第 Ⅸ 因子製剤 ノナコグガンマ ( 遺伝子組換え ) 製造販売元 ( 輸入元 ) バクスアルタ株式会社東京都港区虎ノ門一丁目 23 番 1 号 注 ) 注意 医師等の処方箋により使用すること はじめに リクスビス静注用
2017 年 1 月作成 ( 第 3 版 ) 医薬品の適正使用に欠かせない情報です 使用前に必ずお読みください 新医薬品の の解説 生物由来製品 ) 処方箋医薬品注 遺伝子組換え血液凝固第 Ⅸ 因子製剤 ノナコグガンマ ( 遺伝子組換え ) 製造販売元 ( 輸入元 ) バクスアルタ株式会社東京都港区虎ノ門一丁目 23 番 1 号 注 ) 注意 医師等の処方箋により使用すること はじめに リクスビス静注用
