メキニスト錠 0.5mg メキニスト錠 2mg 製造販売承認申請書添付資料 第 2 部 ( モジュール 2)CTD の概要 ( サマリー ) 2.6. 非臨床試験の概要文及び概要表 緒言 薬理試験の概要文 薬理試験概要表 ノバルティスファーマ株式会社
|
|
|
- つかさ いざわ
- 4 years ago
- Views:
Transcription
1 メキニスト錠 0.5mg メキニスト錠 2mg 製造販売承認申請書添付資料 第 2 部 ( モジュール 2)CTD の概要 ( サマリー ) 2.6. 非臨床試験の概要文及び概要表 緒言 薬理試験の概要文 薬理試験概要表 ノバルティスファーマ株式会社
2 非臨床概要薬理試験の目次 項目 - 頁 緒言 p 薬理試験の概要文 p まとめ p 効力を裏付ける試験 p 副次的薬理試験 p 安全性薬理試験 p 薬力学的薬物相互作用試験 p 考察及び結論 p 薬理試験の概要文 ( タフィンラー / メキニスト併用 ) p まとめ p 効力を裏付ける試験 p 副次的薬理試験 p 安全性薬理試験 p 薬力学的薬物相互作用試験 p 考察及び結論 p 図表 p 参考文献 p 薬理試験概要表 p 薬理試験 : 一覧表 p 効力を裏付ける試験 p 副次的薬理試験 p 安全性薬理試験 p 薬力学的薬物相互作用試験 p 薬理試験概要表 ( タフィンラー / メキニスト併用 ) p 薬理試験 : 一覧表 p 効力を裏付ける試験 p 副次的薬理試験 p 安全性薬理試験 p 薬力学的薬物相互作用試験 p. 8
3 及び の略号等一覧 略語 ( 略称 ) 内容 ANCOVA Analysis of covariance ATP アデノシン三リン酸 CDK サイクリン依存性キナーゼ cdna 相補的 DNA CI コンビネーションインデックス Cmax 最高血漿中濃度 CR Complete response DAPI 4',6-diamidino-2-phenylindole DMSO ジメチルスルホキシド DNA デオキシリボ核酸 ECG 心電図 ELISA Enzyme-linked immunosorbent assay EOHSA Excess over highest single agent ERK Extracellular signal-regulated kinase GAP GTPase activating proteins GDP グアノシン二リン酸 GEF Guanosine-nucleotide exchange factor GLP 医薬品の安全性に関する非臨床試験の実施の基準 GTP グアノシン三リン酸 HEK293 Human embryonic kidney 293 herg Human ether-a-go-go related gene HPMC ヒドロキシプロピルメチルセルロース HUVEC ヒト臍帯静脈血管内皮細胞 IC50 50% 阻害濃度 IFN インターフェロン IL インターロイキン IP 腹腔内投与 IP-10 Interferon-γ-inducing protein 10 Ki 阻害定数 Km ミカエリス定数 LC-MS/MS 液体クロマトグラフィー質量分析法 LPS リポポリサッカライド MAPK Mitogen-activated protein kinase MEK Mitogen-activated extracellular signal-regulated kinase mrna メッセンジャー RNA PARP Poly (ADP-ribose) polymerase PBMC 末梢血単核細胞 PDGF 血小板由来増殖因子 PI3K Phosphatidylinositol-3 kinase PMA Phorbol 12-myristate 13-acetate P-MEK 活性型 MEK ppt Percentage points PR Partial response PTEN Phosphatase and tensin homolog deleted on chromosome 10 RB Retinoblastoma Apr :16:10
4 及び の略号等一覧 ( つづき ) 略語 ( 略称 ) 内容 RNA リボ核酸 SDラット Sprague Dawleyラット SDS-PAGE ドデシル硫酸ナトリウム-ポリアクリルアミドゲル電気泳動 S6P S6リボソーム蛋白質 sirna small interfering RNA TGI 腫瘍増殖抑制率 Tp-e 貫壁性再分極相のばらつき TNF-α 腫瘍壊死因子 -α U-MEK 不活性型 MEK Apr :16:10
5 緒言トラメチニブジメチルスルホキシド付加物 (GSK B 図 ) は 強力かつ選択的な MEK 阻害薬である 悪性黒色腫では BRAF V600 変異が高頻度でみられ 本変異により MAPKシグナル伝達経路が恒常的に活性化することから RAFの下流に存在する MEKを阻害する GSK B の BRAF V600 変異を有する悪性黒色腫に対する有効性が期待される GSK Bは in vitro において MEK1/2 を阻害し ERKリン酸化を阻害することにより 各種腫瘍細胞株に対して増殖抑制作用を示した また BRAF V600E 変異を有するヒト悪性黒色腫細胞株を移植したマウスにおいて 腫瘍増殖を抑制した 今回 BRAF V600 遺伝子変異を有する悪性黒色腫 を効能 効果として承認申請を行った 図 トラメチニブジメチルスルホキシド付加物 (GSK B) の構造式 BRAF V600 遺伝子変異を有する悪性黒色腫 における申請用法 用量は以下のとおりで ある 用法 用量 通常 成人にはトラメチニブとして 2 mg を 1 日 1 回経口投与する Apr :14: p. 1
6 薬理試験の概要文 まとめトラメチニブジメチルスルホキシド付加物 (GSK B) は 強力かつ選択的な MEK 阻害薬である 今回申請する BRAF V600 遺伝子変異を有する悪性黒色腫 に対する効力を裏付ける試験として in vitro における MEK 阻害作用 各種キナーゼに及ぼす影響 BRAF V600 遺伝子変異陽性 ( 以下 BRAF V600 変異陽性 ) の悪性黒色腫を含む各種ヒト腫瘍由来細胞株に対する増殖抑制作用及び ERKリン酸化阻害作用 細胞周期に及ぼす影響 アポトーシス誘導作用 耐性獲得メカニズム 代謝物の薬理活性並びにサロゲートマーカーに関する試験 in vivo における BRAF V600 変異陽性のヒト悪性黒色腫由来細胞株を用いたマウス異種移植モデルでの試験及びサロゲートマーカーに関する試験の成績を示した また 副次的薬理試験として 各種受容体 チャネル 酵素及びキナーゼに及ぼす影響に関する試験成績を示した 更に 安全性薬理試験として 中枢神経系 心血管系及び呼吸系に対する影響を検討した試験の成績を示した なお 試験には主に GSK Bを 一部の試験には GSK A( 遊離塩基 ) を使用した 投与量及び濃度はすべて遊離塩基に換算して記載した 効力を裏付ける試験 In vitro 試験 MEK 阻害作用 GSK B は不活性型の U-MEK1 及び U-MEK2 の活性化 ( キナーゼ活性の発現 ) を阻害し IC50 はそれぞれ 0.7 及び 0.9 nm であった U-MEK1 のキナーゼ活性の発現に必要な Ser218 及び Ser222 のリン酸化のうち GSK B は Ser218 のリン酸化を阻害したが Ser222のリン酸化には影響を及ぼさなかった U-MEK1 に対する結合動態パラメータ (k(off)) から GSK A の解離は ATP 非競合的なアロステリック阻害薬である PD と比較して極めて遅いことが示された また GSK Bは活性型の P- MEK1 及び P-MEK2 活性 (ERKをリン酸化するキナーゼ活性) を阻害し IC50はそれぞれ 13.2 及び 10.7 nm であった P-MEK1 に対する阻害様式は ATP との非競合的阻害であった GSK Bは PD と P-MEK1 の結合部位において 競合的に結合を阻害した GSK Bの MEK1/2 以外の各種キナーゼ (43 及び 171 種類のパネル ) に対する阻害作用は弱く MEK1/2 と最も相同性の高い MEK5 のリン酸化に対しても阻害作用を示さなかったことから MEK1/2 に対する高い選択性が示された 腫瘍細胞増殖抑制作用計 320 種類 (CellTiterGlo アッセイ及び核を 4',6-diamidino-2-phenylindole(DAPI) 染色し リアルタイムイメージ法で解析した細胞株数の合計 ) のヒト腫瘍細胞株パネルを用いた網羅的解析において BRAF 変異陽性細胞株の 88% 及び RAS 変異陽性細胞株の 72% の細胞株が GSK Bに高い感受性を示した 一方 野生型 BRAF 及び RASを有する細胞株では 28% の細胞株だけが高い感受性を示した また 218 種類のヒト腫瘍細胞株パネル ( 固形癌 p. 1
7 由来 ) を用いた網羅的解析においても BRAF 及び RAS 変異陽性細胞株の 80% を超える細胞株が GSK Bに対して高い感受性を示した 一方 野性型 BRAF 及び RAS を有する細胞株では 高い感受性を示した細胞株は 40% 未満であった また 組織別では 特に 悪性黒色腫 膵臓癌及び結腸癌由来の 80% を超える細胞株が GSK Bに対して高い感受性を示した ERKリン酸化レベルと GSK Bに対する感受性との間に完全な関連性は認められなかったが 21 株中 ERKリン酸化 (Thr202/Tyr204) レベルの高い 5 株のうち 4 株は GSK Bに感受性を示した その他の 16 株については ERKリン酸化 (Thr202/Tyr204) レベルと GSK Bに対する感受性との間に関連性は認められなかった また DUSP6(ERKを不活性化させる働きを有している )mrnaを発現している細胞株の多くは GSK Bに対して高い感受性を示し DUSP6 mrna を発現していない細胞株の多くは GSK Bに対する感受性が低かった BRAF V600 変異陽性の 17 種類のヒト悪性黒色腫細胞株のうち 14 種類の細胞株は GSK B に対して高い感受性を示し 増殖抑制作用の IC50 は 0.3~9.5 nmであった BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株に対する GSK Bの増殖抑制作用の可逆性を検討した結果 増殖抑制作用はウォッシュアウトすることにより減弱することが示された BRAF V600E 又は V600K 変異陽性のヒト悪性黒色腫由来のそれぞれ A375P F11 又は YUSIT1 細胞株を高濃度の GSK (BRAF 阻害薬 ) 存在下で 1 週間以上培養し その中から単離した GSK に対して耐性を獲得した耐性細胞クローンでは NRAS 又は MEK1 あるいはその両方に変異 (NRAS:Q61K 及び A146T 変異 MEK1:K59 の欠失 ( インフレーム変異 ;K59del) 又は P387Sのミスセンス変異 ) が検出された これらの耐性細胞クローンは GSK B に対する感受性も 1/200 未満 ~ 約 1/3に低下した 細胞周期に及ぼす影響及びアポトーシス誘導作用 BRAF V600E 変異陽性のヒト結腸直腸癌由来 HT29 細胞株において GSK A は MEK 及び ERKのリン酸化レベルを低下させ 細胞周期抑制因子である p15 及び p27 蛋白レベルの増加並びに細胞周期促進因子である c-myc サイクリン A D1 及び D2 蛋白レベルの低下を誘導した また サイクリン E CDK2 CDK4 及び retinoblastoma(rb) の蛋白レベルをわずかに低下させ 細胞周期の停止にかかわる RBリン酸化レベルを低下させた ヒト結腸直腸癌由来 HT29 及び Colo205 細胞株 (BRAF V600E 変異陽性 ) において GSK A は G0/G1 期のピークを増加させ細胞周期の停止を誘導した後 サブ G1 分画 (DNAの断片化を検出) を増加させた また GSK Aはカスパーゼ 3 7 及び 9 並びに PARP の切断 ( 活性化 ) を誘導し カスパーゼの活性化は サブ G1 分画の増加と関連していた GSK Bに対する獲得耐性に関する検討 KRAS 変異陽性のヒト結腸直腸癌由来 HCT116 細胞株を高濃度の GSK Bで 2 週間以上曝露し GSK B に耐性を獲得した HCT116(212-Res) 細胞株に対する GSK Bの増殖抑制作用の IC50 は 3.3 μmであり 親細胞株 (HCT116 細胞株 ) に対す p. 2
8 る IC50(2 nm) と比較して感受性は 1/1650 に低下した HCT116(212-Res) 細胞株から単離した GSK B 耐性細胞クローンの遺伝子配列解析を行った結果 MEK2 における L119P のアミノ酸置換を起こす単一点突然変異がみられた GSK B 耐性細胞クローン ( クローン 4) に non-silencing small interfering RNA(siRNA) を処理しても GSK Bに対する耐性は維持されたままであったが (IC50=2565 nm) MEK2 をノックダウンさせる sirna を導入することにより GSK Bに対する感受性は回復した (IC50=72 nm) 代謝物の薬理活性ヒトでの主な血漿中代謝物は GSK (M5: 脱アセチル体 ) 及び GSK A (M7:M5 の酸化体 ) である M5の in vitro における U-MEK1 の活性化 ( キナーゼ活性の発現 ) に対する阻害作用 P-MEK1 活性 (ERKをリン酸化する活性) に対する阻害作用 BRAF V600E 変異陽性のヒト悪性黒色腫由来 SK-MEL-28 細胞株における ERKリン酸化阻害作用及び増殖抑制作用は GSK B と同程度であった また M7 の P-MEK1 活性に対する阻害作用の IC50 は 73 nmであり 阻害活性は未変化体 (GSK B:IC50= 7.0 nm) の約 1/10と弱かった サロゲートマーカーの検討 GSK Bは phorbol 12-myristate 13-acetate(PMA) 刺激ヒト PBMC における ERKリン酸化を濃度依存的に阻害した 同様にイヌ及びラットの PBMC(PMA 刺激 ) においても ERKリン酸化を阻害し IC50はヒト及びラットは同程度であり イヌではヒトと比較して低値であった In vivo 試験 ERKリン酸化阻害作用 GSK B(0.1~3 mg/kg 単回 ~14 日間経口投与 ) は BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマウス異種移植モデルの腫瘍組織において ERK のリン酸化を用量依存的に阻害することが示された また ERKリン酸化阻害作用の持続がみられた 8 時間後の血中未変化体濃度は 100 nmを超えており 作用がみられなかった 24 時間後では 100 nmを下回っていた 更に GSK B の ERKリン酸化阻害作用は 14 日間経口投与しても 減弱しないことが示された p27 蛋白レベル増加作用 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマウス異種移植モデルにおいて GSK Bは 3 mg/kg の 1 日 1 回 7 日間経口投与により 腫瘍組織において G1 期停止のマーカーである p27 蛋白レベルを増加させた p. 3
9 腫瘍増殖抑制作用 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマウス異種移植モデルにおいて GSK Bは 1 及び 3 mg/kg の 1 日 1 回 14 日間経口投与により 腫瘍増殖を有意に抑制した サロゲートマーカーの検討 GSK B を経口投与したマウスから単離した PBMC の ERK リン酸化レベルは 用 量 (0.03~3 mg/kg) に依存して低下した 副次的薬理試験 23 種類の各種受容体及びチャネル並びに 7 種類の各種酵素に対し GSK A は 10 μmで 50% を超える阻害作用を示さなかった 各種キナーゼ (43 及び 171 種類のパネル ) に及ぼす影響を検討した結果 GSK A 及び GSK B は 10 μmで 50% を超える阻害作用を示さなかった GSK B は増殖因子非存在下の HUVEC( 正常細胞 ) の細胞数に影響を及ぼさなかった (IC50=10000 nm) 安全性薬理試験雄 SDラットにおいて GSK Bの 100 mg/kg の単回経口投与により 体重増加の抑制 自発運動量の減少 腹臥位 眼瞼下垂 下痢 立毛及び散瞳が認められた 覚醒雄 SDラットにおいて GSK Bの 及び mg/kg( 及び 1 mg/m 2 ) の単回経口投与により mg/kgで軽度で一過性の体温低下 ( 最大で 0.8 C 投与 1 時間後 ) がみられた 換気機能及び気道抵抗に影響は認められなかった GSK Bは herg cdna を導入した HEK293 細胞において hergチャネルテール電流を抑制し IC25 IC50 及び IC75はそれぞれ 及び 5.30 μm( 及び ng/ml) であった ウサギ左心室ウェッジ標本において GSK Bは 及び 30 μm( 約 及び ng/ml) の濃度で (18450 ng/mlは溶解限界濃度 ) QT 間隔に影響を及ぼさなかった GSK B は 10 及び 30 μmで等尺性収縮力をそれぞれ 16.3 及び 64.8% 低下させ 30 μmで Tp-e 間隔を約 26% 短縮させた 麻酔雄ビーグル犬において ( 非 GLP 試験 ) GSK Aは 1 mg/kg の静脈内投与 (10 分間持続投与 ) により心電図パラメータ 血圧及び心拍数に影響を及ぼさなかった 血漿中 GSK 濃度は投与開始 10 分後まで増加し 最高血漿中 GSK 濃度は 2.5 μm ( 約 1500 ng/ml) であった 覚醒雄ビーグル犬において (GLP 試験 ) GSK Bは 及び mg/kg( 及び 1.5 mg/m 2 ) の単回経口投与により 動脈圧 心拍数 ECG パラメータ ( 波形異常 不整脈及び間隔 ) 及び体温に影響を及ぼさなかった p. 4
10 薬力学的薬物相互作用試験臨床において併用される GSK との併用による薬理作用を検討した in vitro 及び in vivo の試験成績は CTD 併用パートの 2.6.2( タフィンラー / メキニスト併用 ) に記載した 効力を裏付ける試験 RAS/RAF/MEK/ERK(MAPK) 経路は 正常細胞及び種々のがん細胞の分化 増殖おいて重要なシグナル伝達経路である ( 図 ) RAFには 3 種類 (A B 及び C) のサブタイプが知られており 2 量体を形成して下流の MEKへシグナルを伝達させるが 種々のがんにおいて BRAFの変異が高頻度に認められており 外国人では悪性黒色腫の 60%[Davies, 2002] 甲状腺癌の 30~50% 大腸癌の 5~20% 卵巣癌の約 30% が変異型 BRAFを有することが報告されている [Wellbrock, 2004] これまでにがんに関連する BRAF 遺伝子変異の多くは BRAFの構造変化をもたらし 下流シグナルである MEK-ERK 経路を異常に活性化する 中でも約 90% と最も頻度の高い変異は Exon15 の T1799 塩基置換型の点突然変異であり キナーゼドメイン内に位置する 600 番目のアミノ酸であるバリン (V600) が主にグルタミン酸 アスパラギン酸又はリジンに変異している (V600E D 又は K)[Wan, 2004; Wellbrock, 2004; Bello, 2013] V600 変異を有する BRAFは野生型と比較して高い活性を持つことが報告されており [Wan, 2004] RAS の活性化に関係なく恒常的に MEK/ERKを活性化してがん細胞の増殖を促進すると考えられている MEK/ERKの恒常的な活性化は サイクリン D1 等の細胞周期促進因子のアップレギュレーション及び p27 等の細胞周期抑制因子のダウンレギュレーションを誘導し アポトーシス関連因子の機能を調節することにより 悪性黒色腫の増殖を促進させると考えられていることから [Bello, 2013] BRAFの下流に存在する MEKは BRAF V600 変異陽性のがんに対する分子標的薬の重要な標的になると考えられる [Nissan, 2011] 今回申請する適応症である悪性黒色腫の日本人患者での BRAF V600 遺伝子変異陽性の割合は外国人患者 (60%) と比べて低い ( 約 20~30%) ことが報告されているが 外国人と同様に日本人でも V600E 及び V600Kの 2 種類の変異が悪性黒色腫における BRAF 遺伝子変異の大部分を占めると考えられる [Sasaki, 2004; Ashida, 2012] ことから 選択的 MEK 阻害薬である GSK B は BRAF V600 変異陽性の悪性黒色腫に対する治療薬としての可能性を有している p. 5
11 増殖因子が受容体に結合すると 受容体のチロシン残基がリン酸化され その後 活性化シグナルが RAS /RAF/MEK/ERK へと伝達される GSK の標的である RAF は RAS によって活性化 ( リン酸化 ) された後 MEK をリン酸化して活性化させる GSK B の標的である MEK は RAF によってリン酸化された後 ERK をリン酸化する GDP:guanosine diphosphate ( グアノシン二リン酸 ) GTP:guanosine triphosphate ( グアノシン三リン酸 ) GAP:GTPase activating proteins GEF:guanine-nucleotide exchange factor 図 増殖因子受容体を介した細胞内シグナル伝達 (MAPK 経路 ) Data source: [Alcala, 2012] の Figure In vitro 試験 In vitro 試験において 主に GSK B の MEKに対する阻害作用及び阻害様式並びに BRAF V600E 変異陽性を含む各種ヒト腫瘍細胞株及びヒト悪性黒色腫由来 GSK 耐性細胞クローンに対する増殖抑制作用を検討した また GSK B に対する耐性獲得メカニズム 代謝物の薬理活性及びサロゲートマーカーについて検討した MEK 阻害作用 U-MEK1 並びに U-MEK2 は RAFにより それぞれ Ser218 及び Ser222 残基並びに Ser222 及び Ser226 残基がリン酸化され 活性化 ( キナーゼ活性の発現 ) される (P-MEK) [Roskoski, 2012] その後 P-MEKは ERK1/2 のスレオニン及びセリン残基をリン酸化する ( 図 ) p. 6
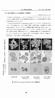
12 そこで GSK B の MEK 阻害作用を検討する目的で BRAF による U-MEK1/2 の活 性化に対する阻害作用 ( ) 及び P-MEK1/2 活性 (ERK1/2 をリン酸化する活性 ) に対する阻害作用 ( ) を検討した U-MEK (unphosphoryalted-mek): 不活性型 MEK P-MEK (phosphoryalted-mek): リン酸化 MEK ( 活性型 ) 図 RAF/MEK/ERK 経路 BRAF による U-MEK1/2の活性化に対する阻害作用方法本試験系の模式図を図 に示す (UH2008/00021/00) U-MEK1(0.3 nm) 又は U- MEK2(0.6 nm) に各種濃度の GSK B を添加し 室温で 40 分間インキュベートした その後 変異型 BRAF(V600E 変異陽性 )(20 nm) 及び ATP(30 μm) を添加して 10 分間反応させ GSK Bに結合していない U-MEKをリン酸化した (P-MEK1/2) この反応液中に不活性型 ERK2(4 μm) [γ 33 P]-ATP(30 μm;0.08 μci/μl) 及び SB590885R (BRAF 阻害薬 400 nm) を添加し P-MEK1 は 90 分間 P-MEK2 は 120 分間反応させて ERK2 をリン酸化した ERK2 に取り込まれた [γ 33 P]-ATP の放射活性を測定し GSK Bに結合していない U-MEK1/2 由来の P-MEK1/2 による ERK2 リン酸化活性を測定し BRAF V600E による U-MEKの活性化 ( キナーゼ活性の発現 ) に対する阻害作用を検討した p. 7
13 1:U-MEK1 に GSK B を処理 2:U-MEK1 をリン酸化させるために変異型 BRAF (V600E 変異陽性 ) 及び ATP を添加 (GSK B が結合していない U-MEK はリン酸化されるが 結合している U-MEK はリン酸化されない ) 3: 選択的 BRAF 阻害薬である SB590885R を添加して BRAF の活性を阻害し 反応を停止させる 4: 不活性型 ERK2 (kinase dead K52R マウス ERK2) 及び ATP を添加し 生成された P-MEK1 の活性 (ERK をリン酸化するキナーゼ活性 ) を ERK リン酸化レベルから評価 (GSK B が結合していない U-MEK はリン酸化 (P-MEK) され それに続き ERK がリン酸化されるが GSK B が結合している U-MEK は リン酸化されないため P-MEK による ERK のリン酸化が起こらないという原理を利用 ) 図には U-MEK1 の活性化に対する阻害作用を検討した試験系を示したが U-MEK2 についても同様の試験系で検討を行った 結果 図 Data source: UH2008/00021/00 の Figure 4 (A) U-MEK に対する阻害作用を検討した試験系 GSK B は U-MEK1 及び U-MEK2 の活性化を阻害し IC50 はそれぞれ 0.7 及び 0.9 nm であった ( 表 ) 表 U-MEK に対する阻害作用 酵素 IC50 (nm) n U-MEK U-MEK Data source: UH2008/00021/00の Table U-MEK1の Ser218 及び Ser222のリン酸化へ及ぼす影響 U-MEK1 のキナーゼ活性の発現には Ser218 及び Ser222 のリン酸化が必要であることが報告されている [Yan, 1994] 本試験では GSK Bが U-MEK1 の Ser218 及び Ser222 をリン酸化させるか否かを検討した 方法 U-MEK1(30 nm) 及び GSK B(75 nm) を室温で 40 分間プレインキュベートし 変異型 BRAF(V600E 変異陽性 )(20 nm) 及び ATP(30 μm) を添加して更に室温で 1 時 p. 8
14 間インキュベートした (UH2008/00021/00) SDS-PAGE 用緩衝液を添加して反応を停止させ SDS-PAGE により MEK1 のバンドを分離した後 mass spectrometry 法により U-MEK1 のリン酸化部位及びレベルを解析し Ser218 及び Ser222のリン酸化率を算出した 結果 GSK B(75 nm) は変異型 BRAF V600Eによる U-MEK1 の Ser218のリン酸化を阻害したが Ser222 のリン酸化を阻害しなかった ( 表 ) 表 U-MEK1 の Ser218 及び Ser222 のリン酸化に及ぼす影響 試験群 Ser218のリン酸化率 (%) Ser222のリン酸化率 (%) U-MEK1 (BRAF V600E 非添加 ) 0 0 U-MEK1+BRAF V600E U-MEK1+BRAF V600E+GSK B (75 nm) 3 92 Data source: UH2008/00021/00 の Table U-MEK1に対する結合動態パラメータ PD は ATP 非競合的なアロステリック MEK 阻害薬である [Akinleye, 2013] GSK A の U-MEK1 に対する結合動態を PD と比較検討した 方法 U-MEK1 を含む反応用緩衝液中に GSK A( 及び 63 nm) 又は PD ( 及び 250 nm) を添加し 25 C で 60(association phase) 及び 180 (dissociation phase) 秒間反応させ 結合動態パラメータを Biacore S51ソフトウェアを用いて解析した (UH2008/00046/00) 結果 GSK A 及び PD の U-MEK1 に対する結合動態パラメータを表 に示す k(off) のデータから GSK A の解離は PD と比較して極めて遅いことが示された 表 U-MEK1 に対する結合動態パラメータ 被験物質 K D (M) k(on) (1/Ms) k(off) (1/s) GSK A PD 各パラメータの値は 2 回の試験の平均値 K D : 解離定数 k(on): 結合速度 k(off): 解離速度 Data source: UH2008/00046/00 の Table P-MEK1/2 活性に対する阻害作用方法本試験系の模式図を図 に示す (UH2008/00021/00) P-MEK1(0.5 nm) 又は P- MEK2(0.5 nm) 不活性型 ERK2(1 μm) ATP(40 μm) 及び [γ 33 P]-ATP(0.6 μci) を含む反応用緩衝液に各種濃度の GSK B を添加し 室温で 40 分間反応させた 45 分間放置した後 ERK2 に取り込まれた [γ 33 P]-ATP の放射活性を測定することにより P-MEK p. 9
15 及び P-MEK2 による ERK2 のリン酸化反応を測定した GSK B の P-MEK1/2 活性 (ERK をリン酸化する活性 ) に対する阻害作用を ERK2 のリン酸化レベルを指標として評 価した 図には P-MEK1 活性 (ERK をリン酸化する活性 ) に対する阻害作用を検討した試験系を示したが P-MEK2 活性についても同様の試験系で検討を行った 結果 図 P-MEK 活性に対する阻害作用を検討した試験系 Data source: UH2008/00021/00 の Figure 1 (A) GSK B は P-MEK1 及び P-MEK2 活性を阻害し IC50 はそれぞれ 13.2 及び 10.7 nm であった ( 表 ) まとめ 表 P-MEK 活性に対する阻害作用 酵素 IC50 (nm) n P-MEK P-MEK Data source: UH2008/00021/00の Table 1 GSK B は U-MEK1/2( 不活性型 ) の活性化 ( キナーゼ活性の発現 ) を阻害し U- MEK1 のキナーゼ活性の発現に必要な Ser218 及び Ser222 のリン酸化のうち Ser218 のリン 酸化を阻害したが Ser222 のリン酸化には影響を及ぼさなかった U-MEK1 に対する結合動 態パラメータ (k(off)) から GSK A の解離は ATP 非競合的なアロステリック阻害 薬である PD と比較して極めて遅いことが示された また GSK B は P- MEK1/2( 活性化 MEK) 活性 (ERK をリン酸化するキナーゼ活性 ) も阻害することが示さ れた ( 図 ) p. 10
16 U-MEK: 不活性型 MEK P-MEK: 活性型 MEK 図 GSK B の U-MEK 及び P-MEK 阻害作用の模式図 P-MEK1に対する阻害様式方法 P-MEK1 に対する阻害作用を と同様の方法で検討し 不活性化 ERK 濃度を一定 (1 μm) とし ATP 及び GSK Bの濃度を変動させて反応させ ATP 濃度 - 反応速度曲線 ミカエリスメンテンの数式及び各種数式モデル (competitive non-competitive mixed 及び uncompetitive モデル ) により阻害様式を解析し Ki 及び K m, ATP を算出した (UH2008/00021/00) 結果 ATP 濃度 - 反応速度曲線 ミカエリスメンテンの数式及び各種数式モデルから GSK Bの P-MEK1 に対する阻害様式は ATP との非競合的 (non-competitive) であることが示された ( 図 ) K m, ATP は 4.3 μmであり Ki は 11.6 nm であった p. 11
17 縦軸 :P-MEK1 反応速度 横軸 :ATP 濃度図 P-MEK1に対する ATP との阻害様式 Data source: UH2008/00021/00の Figure P-MEK1における PD との競合様式 GSK Bの P-MEK1 に対する阻害様式の検討において ATP との非競合的阻害であることが示されていることから ( ) 本試験では P-MEK1 における結合部位が GSK B 及び PD で同一であるか否かを明らかにする目的で 両被験物質の競合様式を検討した 方法 GSK B 及び PD の二次元濃度マトリクスを調製し P-MEK1 に対する阻害作用を と同様の方法で検討した (UH2008/00021/00) PD との競合様式は Yonetani-Theorellの数式により解析した 結果 1/Velocity( 反応速度 ) 及び PD 濃度をプロットしたデータは ( 図 ) 相互排他的結合を解析する Yonetani-Theorellモデルの数式にフィットしたことから GSK B 及び PD は P-MEK1 の結合部位において 相互排他的に競合的に阻害することが示された p. 12
18 縦軸 :1/ 反応速度 横軸 :GSK A:PD 濃度 図 Data source: UH2008/00021/00 の Figure 3 P-MEK1 における PD との競合様式 各種キナーゼに及ぼす影響 ( 選択性 ) キナーゼパネルにおける検討方法 GSK A 又は B(10 μm) の各種キナーゼパネル (43 種類 ) に対する阻害活性を fluorescence polarizationアッセイ LEADseeker scintillation proximityアッセイ IMAP technology fluorescence depolarizationアッセイ又は time resolved-fluorescence resonance energy transferアッセイにより測定した (UH2008/00021/00) また 171 種類のキナーゼパネルを用いて GSK A(10 μm) のキナーゼ阻害活性を測定した (UH2008/00047/00) 結果 GSK A 又は Bは 10 μm で 43 種類のキナーゼに対して 50% を超える阻害作用を示さなかった (IC50>10 μm) また GSK Aは 10 μm で 171 種類のキナーゼに対して 50% を超える阻害作用を示さなかった (IC50>10 μm) MEK5に及ぼす影響 MEK5 は MEK1/2 とキナーゼドメインで 85% 以上 ATP 結合部位では 98% 以上の相同性を有する (UH2007/00097/02) GSK Bの MEK5 活性 (ERK5 をリン酸化する活性 ) に対する阻害作用を ERK5 のリン酸化レベルを指標として評価し ERK1/2 リン酸化に及ぼす影響と比較した 方法マウス胎児皮膚由来 NIH3T3 細胞株に GSK B(1 μm) を 37 C で 1 時間処理した その後 MEK5 経路を刺激するために マウス組換え血小板由来増殖因子 (PDGF)-BB を p. 13
19 37 C で 5 分間処理した 細胞株を溶解後 perk5(thr218/tyr220) 抗体及び perk1/2 (Thr202/Tyr204) 抗体を用いてリン酸化 ERK5 及びリン酸化 ERK1/2 をウエスタンブロット法により検出した 比較対照物質として PD の MEK5 及び MEK1/2 に及ぼす影響も同様に検討した 結果 ERK5 は PDGF-BB で刺激された MEK5 によりリン酸化されることが示された ( 図 ) GSK Bは ERK5 のリン酸化レベルを変化させなかったことから ( 図 ) MEK5 に対して影響を及ぼさないことが示された 一方 GSK Bは ERK1/2 のリン酸化を阻害したことから ( 図 ) 本試験系においても MEK1/2 に対して阻害作用を有することが確認された 比較対照物質である PD も GSK Bと同様に ERK1/2 のリン酸化を阻害したが ERK5 のリン酸化レベルに対しては影響を及ぼさなかった ( 図 ) PDGF BB: 血小板由来増殖因子 -BB PD :MEK 阻害薬図 NIH3T3 細胞株における MEK5 及び MEK1/2に及ぼす影響 Data source: UH2007/00097/02の Figure 11 まとめ GSK Bの P-MEK1 に対する阻害様式は ATP との非競合的であり GSK B は P-MEK1 の結合部位において ATP 非競合的なアロステリック阻害薬である PD の結合を競合的に阻害した GSK Bは MEK1/2 以外の各種キナーゼ (43 及び 171 種類のパネル ) に対してほとんど阻害作用を示さず MEK1/2 と最も相同性の高い MEK5 の ERK5 リン酸化活性に対しても阻害作用を示さなかったことから MEK1/2 に対する高い選択性が示された p. 14
20 腫瘍細胞増殖抑制作用 各種ヒト腫瘍細胞株における BRAF 及び RAS の変異と GSK B に対する感受性との関連の網羅的解析 ( 試験 1) 方法 BRAFあるいは RAS 変異陽性又は野生型 BRAF/RAS を有する各種ヒト腫瘍細胞株パネル ( 計 320 種類 ; 後述の 2つの測定方法での合計 ) に GSK B(0.014 nm~7.3 μm) を添加して 72 時間培養した (UH2007/00097/02) CellTitierGloアッセイ又は核を DAPI 染色し リアルタイムイメージ法で解析することにより生細胞数を計測し 各細胞株の GSK Bに対する感受性を検討した 本試験における GSK B に対する感受性の程度は IC50 を指標に 高感受性 (IC50<50 nm 又は殺細胞作用を示した場合 ) 及び低感受性 (IC50>50 nm 又は高濃度で処理したときに無処理のときと比較して 50% 超まで増殖可能な場合 ) と定義し 検討したいずれの濃度でも影響を受けなかった場合は感受性なしと定義した 結果計 320 種類のヒト腫瘍細胞株パネルを用いた網羅的解析において BRAF 変異陽性細胞株の 88% 及び RAS 変異陽性細胞株の 72% の細胞株が GSK Bに対して高い感受性を示した ( 図 ) 一方 野生型 BRAF 及び RASを有する細胞株では 28% の細胞株だけが高い感受性を示した ( 図 ) p. 15
21 縦軸 : 細胞株の割合 (%) B-raf:BRAF 変異陽性の細胞株 ras:ras 変異陽性の細胞株 WT ras/raf: 野生型 RAS 及び RAF を有する細胞株 sensitive: 高感受性 (IC50<50 nm 又は殺細胞作用を示した場合 ) less-sensitive: 低感受性 (IC50>50 nm 又は高濃度で処理したときに無処理のときと比較して 50% 超まで増殖可能な場合 ) non-sensitive: 感受性なし ( 検討したいずれの濃度でも影響を受けなかった場合 ) IC50:50% 増殖阻害濃度 図 Data source: UH2007/00097/02 の Figure 5 各種ヒト腫瘍細胞株における BRAF 及び RAS の変異と GSK B に対する感受性との関連 各種ヒト腫瘍細胞株における ERKリン酸化レベルと GSK Bに対する感受性との関連性 の試験において GSK B に対して感受性あり ( 高あるいは低感受性 ) 又は感受性なしとされた細胞株を用いて 細胞内 ERKリン酸化レベルと GSK B に対する感受性との関連性を検討した 方法 BRAFあるいは RAS 変異陽性又は野生型 BRAF/RAS を有する各種ヒト腫瘍細胞株を溶解し ERK1/2 perk(tyr204) 又は perk(thr202/tyr204) 抗体を用いてウエスタンブロット法によりリン酸化 ERKを検出した (UH2007/00097/02) 各細胞株におけるリン酸化 ERKのウエスタンブロットのバンドを近赤外蛍光法により検出し 蛍光強度を Odyssey reader TM により定量化した 定量化した ERKリン酸化レベルの高い順から 25% の細胞株を高いと判断した p. 16
22 結果 21 株中 ERKリン酸化 (Thr202/Tyr204) レベルの高い 5 株 (Lovo:RAS 変異陽性 ; ヒト結腸直腸癌由来 SHP77:RAS 変異陽性 ; ヒト肺癌由来 SK-MEL-2:RAS 変異陽性 ; ヒト悪性黒色腫由来 SK-MEL-28:BRAF 変異陽性 ; ヒト悪性黒色腫由来及び A172: 野生型 BRAF/RAS; ヒト神経膠芽腫由来 ) のうち 4 株 (Lovo SK-MEL-2 SK-MEL-28 及び A172) は GSK Bに感受性を示した ( 図 ) その他の 16 株については ERKリン酸化 (Thr202/Tyr204) レベルと GSK Bに対する感受性との間に関連性は認められなかった S: 感受性あり R: 感受性なし R:Ras mut:ras 変異陽性の細胞株 B:BRAF mut:braf 変異陽性の細胞株 W:wt/wt: 野生型 BRAF 及び RAS を有する細胞株矢印は ERK リン酸化 (Thr202/Tyr204) レベルが 高い と定義した 5 株を示す 図 ヒト腫瘍細胞株における ERK リン酸化 (Thr202/Tyr204) レベルと Data source: UH2007/00097/02 の Figure 8 GSK B に対する感受性との関連性 p. 17
23 各種ヒト腫瘍細胞株における BRAF 及び RAS の変異と GSK B に対する感受性との関連の網羅的解析 ( 試験 2) 方法 BRAFあるいは RAS 変異陽性又は野生型 BRAF/RAS を有する 218 種類の各種ヒト腫瘍細胞株パネル ( 固形癌由来 ) に GSK B(0.16 nm~5 μm) を添加して 72 時間培養した (2014N205857_00) 核を DAPI 染色し生細胞数を計測し GSK Bの増殖抑制作用を検討した 本試験における GSK B に対する感受性の程度は IC50を指標に 高感受性 (IC50<50 nm) 中程度の感受性(IC50=50~1000 nm) と定義し IC50>1000 nmの細胞株は感受性なしと定義した 結果 218 種類のヒト腫瘍細胞株パネル ( 固形癌由来 ) を用いた網羅的解析において BRAF 及び RAS 変異陽性細胞株の 80% を超える細胞株が GSK Bに対して高い感受性を示した ( 図 ) 一方 野性型 BRAF 及び RASを有する細胞株では 高い感受性を示した細胞株は 40% 未満であった また 組織別では 特に 悪性黒色腫 膵臓癌及び結腸癌由来の 80% を超える細胞株が GSK Bに対して高い感受性を示した ( 図 ) 縦軸 : 細胞株数 RAS:RAS 変異陽性の細胞株 BRAF:BRAF 変異陽性の細胞株 Wild Type: 野生型 RAS 及び RAF を有する細胞株 Sensitive: 高感受性 Intermediate: 中程度の感受性 Resistant: 抵抗性 ( 感受性なし ) GI50:50% 増殖阻害濃度 図 各種ヒト腫瘍細胞株 ( 固形癌由来 ) における BRAF 及び RAS の変異と GSK B に対する感受性との関連 Data source: 2014N205857_00の Figure 1A p. 18
24 縦軸 : 細胞株数 Sensitive: 高感受性 Intermediate: 中程度の感受性 Resistant: 抵抗性 ( 感受性なし ) GI50:50% 増殖抑制濃度 bladder: 膀胱癌 breast: 乳癌 colon: 結腸癌 glioma: 神経膠腫 head&neck: 頭頸部癌 kidney: 腎癌 liver: 肝臓癌 lung: 肺癌 ovary: 卵巣癌 pancreas: 膵臓癌 sarcoma: 肉腫 melanoma: 悪性黒色腫 図 各種ヒト腫瘍細胞株 ( 固形癌由来 ) の GSK B に対する感受性及び由来組織との関連 Data source: 2014N205857_00の Figure 1B 各種ヒト腫瘍細胞株における DUSP6 mrnaレベルと GSK Bに対する感受性との関連性 DUSP6はホスファターゼの 1 種であり RAF/RAS/MEK/ERK 経路の活性化によりアップレギュレーションされることが知られ [Furukawa, 2008] ERKを脱リン酸化させ 不活性化させる働きを有している [Caunt, 2013] ERKは MEKの基質であり DUSP6 発現レベルは GSK Bに対する感受性に影響を及ぼす可能性が考えられることから の試験で用いた 218 種類のヒト腫瘍細胞株における DUSP6 mrna レベルと GSK B に対する感受性との関連性を検討した 方法 218 種類の各種ヒト腫瘍細胞株 ( 固形癌由来 ) を溶解し DUSP6 mrnaレベルをマイクロアレイ法により測定し MAS5アルゴリズム (Affymetrix) を用いてデータを正規化した (2014N205857_00) 本試験における DUSP6 mrna の発現に関しては MAS5 アルゴリズムを用いて正規化した値が 100 超を発現あり 100 未満を発現なしと定義した p. 19
25 また 229 種類のヒト腫瘍細胞株 * の DUSP6 mrna 発現レベルと GSK B に対する感受性の試験成績から これらの間の関連性について統計学的検討を行った GSK B に対する感受性の有無 ( 感受性あり (IC50<50 nm) 又は感受性なし (IC50>1000 nm)) 並びに DUSP6の mrna 発現の有無 ( 発現あり (MAS5>100) 及び発現なし (MAS5< 100)) に従って細胞を 4つのカテゴリー ( 真の陽性 (DUSP6 mrna の発現あり及び GSK Bに対して感受性あり ) 偽陽性(DUSP6 mrnaの発現あり及び GSK Bに対して感受性なし ) 及び偽陰性 (DUSP6 mrna の発現なし及び GSK Bに対して感受性あり ) 及び真の陰性 (DUSP6 mrnaの発現なし及び GSK Bに対して感受性なし ) に分類し それぞれに属する細胞株数から DUSP6 の mrna 発現の有無と感受性との関連を以下のように解析した Sensitivity: 真の陽性 /( 真の陽性 + 偽陰性 ) 100 Specificity: 真の陽性 /( 真の陽性 + 偽陽性 ) 100 p 値 :Fisher s exact test(two-tailed) により算出 *: DUSP6 mrna レベルと GSK Bに対する感受性との関連性についての試験はヒト腫瘍細胞株における BRAF 及び RAS の変異と GSK B に対する感受性との関連の網羅的解析 ( ) の一環として実施し この網羅的解析には当初 229 種類のヒト腫瘍細胞株を用いた しかし そのうち 11 種類の細胞株では BRAF 及び RASの変異の情報が得られなかったため これらの 11 種類の細胞株を除く 218 種類の細胞株を用いて一連の試験を実施し その結果を 及び に示した DUSP6の mrna 発現の有無と感受性との関連を検討した統計学的解析に関しては BRAF 及び RASの変異の情報は必ずしも必要でなかったことから 当初本試験に用いた 229 種類のヒト腫瘍細胞株のすべてを対象に実施した 結果 218 種類の各種ヒト腫瘍細胞株において DUSP6 mrna を発現している細胞株の多くは GSK Bに対して高い感受性を示したが DUSP6 mrnaを発現していない細胞株の多くは GSK B に対する感受性が低かった ( 図 ) また 229 種類の細胞株を対象とした統計学的解析において DUSP6 mrna 発現の有無と GSK B に対する感受性との間に有意な相関性が認められた (sensitivity:79% specificity:82% p=0.0027) p. 20
26 縦軸 : 細胞株数 S: 高感受性 I: 中程度の感受性 R: 抵抗性 ( 感受性なし ) GI50:50% 増殖抑制濃度 MAS5>100:DUSP6 mrna の発現あり MAS5<100:DUSP6 mrna の発現なし 図 ヒト腫瘍細胞株 ( 固形癌由来 ) における DUSP6 mrnaレベルと GSK Bに対する感受性との関連性 Data source: 2014N205857_00の Figure 5A BRAF V600 変異陽性のヒト悪性黒色腫細胞株に対する増殖抑制作用 BRAFの下流に存在する MEKは BRAF V600 遺伝子変異を有する腫瘍に対する分子標的薬の重要な標的となると考えられる [Nissan, 2011] 各種ヒト腫瘍細胞株のパネルを用いた検討において GSK Bは BRAF 変異陽性の細胞株の増殖を抑制することが示されている ( 及び ) 今回申請する適応症である悪性黒色腫は BRAF 遺伝子変異の頻度が高く その変異の 90% 以上が V600E 変異である [Nissan, 2011] ことから GSK Bの BRAF V600 変異陽性のヒト悪性黒色腫細胞株に対する増殖抑制作用を検討した 方法 BRAF 変異陽性 (V600E V600K 又は V600D) のヒト悪性黒色腫細胞株 (17 種類 ) に GSK B(0.05 nm~1 μm) を添加して 72 時間培養した (2011N116395_00) CellTiterGloアッセイにより生細胞数を計測し 細胞増殖抑制作用の IC50を算出した 結果 BRAF V600 変異陽性の 17 種類のヒト悪性黒色腫細胞株のうち 14 種類の細胞株は GSK Bに対して高い感受性を示し 増殖抑制作用の IC50は 0.3~9.5 nmであった ( 表 ) GSK B に対して高い感受性を示した 14 種類の細胞株 (IC50は 0.3~9.5 nm) と比較して IGR-1 細胞株の感受性は低く (IC50=62.3 nm) SK-MEL-3 及び A2058 細胞株は感受性を示さなかった (>1000 nm)( 表 ) p. 21
27 表 BRAF V600 変異陽性のヒト悪性黒色腫細胞株に対する増殖抑制作用 # 細胞株 BRAF 遺伝子変異の種類 PTEN の種類 IC50 (nm) UACC-257 V600V/E 野生型 SK-MEL-1 V600V/E 野生型 COLO-829 V600V/E 欠失 A101D V600V/E 欠失 SK-MEL-24 V600V/E 欠失 SK-MEL-5 V600V/E 野生型 SK-MEL-3 V600V/E 野生型 > 1000 A2058 a V600V/E 欠失 > 1000 SK-MEL-28 b V600E T167A 変異型 UACC-62 V600E 欠失 A375P F11 V600E 野生型 WW165 V600V/K 野生型 IGR-1 c V600V/K 野生型 YUMAC V600K 野生型 YULAC V600K 野生型 YUSIT1 V600K 野生型 WM-115 V600V/D 欠失 平均値 ± 標準偏差 (n=4~11) #:retinoblastoma (RB) gene 1 サイクリン依存性キナーゼ (CDK) 4 MEK1 又は MEK2 遺伝子に関する遺伝子変異の有無を検討した a:mek1 P124S, RB1 Q93* 変異陽性 b:cdk4 R24C 変異陽性 c:mek2 E66_K68del 変異陽性 Data source: 2011N116395_00 の Table BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株に対する増殖抑制作用の可逆性 BRAF V600E 変異陽性のヒト悪性黒色腫細胞株に対する GSK B の増殖抑制作用の可逆性を検討した 方法 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株に GSK B( 及び 3000 nm) を添加し 3 時間又は 1あるいは 2 日間培養した (UH2007/00097/02) GSK Bを除去 ( ウォッシュアウト :1~4 日間 ) し 培養液を交換し 培養液交換直後 及び 4 日後 (day 0~4) に CellTiterGlo アッセイにより生細胞数を計測した 結果各種濃度の GSK Bを 3 時間又は 1あるいは 2 日間培養し いずれも 1~4 日間のウォッシュアウト期間を設けて GSK B の A375P F11 細胞株に対する増殖抑制作用の可逆性を検討した結果 高濃度である 1000 及び 3000 nmを除き 増殖抑制作用はウォッシュアウトすることにより減弱することが示された ( 図 ) p. 22
28 d0: ウォッシュアウト直後 d1: ウォッシュアウト翌日 d2: ウォッシュアウト 2 日後 d3: ウォッシュアウト 3 日後 d4: ウォッシュアウト 4 日後 GSK B を 3 時間処理 ( 上段 ) 1 日間処理 ( 下段左 ) 2 日間処理 ( 下段右 ) 縦軸 : ウォッシュアウト直後の生細胞数に対する各濃度での生細胞数の割合 図 まとめ BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株に対する増 Data source: UH2007/00097/02 の Figure 10 殖抑制作用の可逆性 計 320 種類並びに 218 種類のヒト腫瘍細胞株パネルを用いた網羅的検討において それぞ れ BRAF 変異陽性細胞株の 88% 及び RAS 変異陽性細胞株の 72% の細胞株並びに BRAF 及び RAS 変異陽性細胞株の 80% を超える細胞株が GSK B に高い感受性を示した 一方 野生型 BRAF 及び RAS を有する細胞株では それぞれ 28% 及び 40% 未満の細胞株だけが高 い感受性を示した 組織別では 特に 悪性黒色腫 膵臓癌及び結腸癌由来の 80% を超える 細胞株が GSK B に対して高い感受性を示した ERK リン酸化レベルと GSK B に対する感受性との間に完全な関連性は認められな かったが 21 株中 ERK リン酸化 (Thr202/Tyr204) レベルの高い上位 25% の 5 株のうち 4 株 は GSK B に感受性を示した また DUSP6(ERK を不活性化させる働きを有してい る )mrna を発現している細胞株の多くは GSK B に対して高い感受性を示し DUSP6 mrna を発現していない細胞株の多くは GSK B に対する感受性が低かった BRAF V600 変異を有する 17 種類のヒト悪性黒色腫細胞株のうち 14 種類の細胞株は GSK B に対して高い感受性を示し 増殖抑制作用の IC50 は 0.3~9.5 nm であった GSK B のヒト悪性黒色腫由来 A375P F11 細胞株に対する増殖抑制作用の可逆性を検 討した結果 増殖抑制作用は GSK B をウォッシュアウトした後に減弱した p. 23
29 ヒト悪性黒色腫由来 GSK 耐性細胞クローンに対する増殖抑制作用臨床において RAF 阻害剤の使用による耐性腫瘍の出現が報告されていることから [Alcala, 2012; Lito, 2013] BRAF V600 変異陽性の 2 種類のヒト悪性黒色腫由来細胞株 (BRAF V600E 変異陽性の A375P F11 細胞株及び BRAF V600K 変異陽性の YUSIT1 細胞株 ) を高濃度の GSK (BRAF 阻害薬 ) で 1 週間以上処理して耐性細胞株を誘導し その細胞クローンを単離し GSK B の GSK 耐性細胞クローンの増殖に対する抑制作用を検討した A375P F11 細胞株より単離した耐性細胞クローンでの検討方法 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株に GSK を 1.2 又は 1.6 μmの濃度まで増加させて曝露することにより耐性を誘導した単一細胞クローン (9 株 ) を限界希釈法により単離した後 これらの RAS RAF MEK PIK3CA 及び PTEN 遺伝子における変異の有無を確認した (2011N116394_00) GSK 耐性細胞クローンを GSK (0.5~10000 nm) 及び GSK B(0.05 ~1000 nm) 存在下で 72 時間培養した後 CellTiterGloアッセイにより生細胞数を計測し 増殖抑制作用の IC50 を算出した 結果 GSK に耐性を獲得した細胞クローン (IC50>10000 nm) は GSK Bに対する感受性も 1/200 未満 ~ 約 1/12(IC50=62~>1000 nm) に低下した ( 表 ) 耐性細胞クローンでは NRAS 又は MEK1 あるいはその両方に変異 (NRAS:Q61K 及び A146T 変異 MEK1:K59 の欠失 ( インフレーム変異 ;K59del) 又は P387S のミスセンス変異 ) が検出されたが KRAS HRAS ARAF CRAF PTEN 及び PIK3CAに変異はみられなかった p. 24
30 表 A375P F11 細胞株由来 GSK 耐性細胞クローンに対する 増殖抑制作用 細胞株 獲得変異 IC50 (nm) NRAS MEK1 GSK GSK B A375P F11 ( 親細胞株 ) 野生型 野生型 R5-3 A146T 野生型 > R8-1 A146T 野生型 > R8-3 A146T 野生型 > R6-3 A146T P387S > R5-5 Q61K P387S > R6-2 Q61K P387S > R6-4 Q61K, A146T P387S >10000 >900 12R5-1 WT K59del >10000 > R5-5 WT K59del >10000 >900 平均値 ± 標準偏差 (n 3) Data source: 2011N116394_00の Table YUSIT1 細胞株より単離した耐性細胞クローンでの検討方法 BRAF V600K 変異陽性のヒト悪性黒色腫由来 YUSIT1 細胞株に 0.1 μmの GSK を曝露することにより耐性を誘導した単一細胞クローンを限界希釈法により単離した後 これらの RAS RAF MEK PIK3CA 及び PTEN 遺伝子における変異の有無を確認した (2011N116394_00) また CellTiterGloアッセイにより生細胞数を計測し 増殖抑制作用の IC50 を算出した 結果 GSK に耐性を獲得した細胞クローン (GSK に対する感受性は親細胞株の 1/35 以下 ) は GSK Bに対する感受性も約 1/7~1/3(IC50=2.3~5.0 nm) に低下した ( 表 ) p. 25
31 細胞株 表 YUSIT1 細胞株由来 GSK 耐性細胞クローン NRAS 獲得変異 に対する増殖抑制作用 GSK IC50 (nm) GSK B YUSIT1 ( 親細胞株 ) 野性型 YUSIT1-B11 Q61K YUSIT1-B29 ND YUSIT1-B27 Q61K YUSIT1-B10 Q61K YUSIT1-B31 Q61K YUSIT1-B25 Q61K YUSIT1-B24 Q61K > YUSIT1-B4 Q61K > YUSIT1-B5 Q61K > YUSIT1-B14 Q61K > YUSIT1-B7 Q61K > YUSIT1-B6 Q61K > 平均値 ± 標準偏差 (n 3) ND: 実施せず 親細胞株は BRAF V600K 変異及び MEK2 E27K 変異陽性 Data source: 2011N116394_00の Table 2 まとめ BRAF V600E 又は V600K 変異陽性ヒト悪性黒色腫由来のそれぞれ A375P F11 又は YUSIT1 細胞株を高濃度の GSK 存在下で 1 週間以上培養し GSK に対して耐性を獲得した単一細胞クローンを単離した それらの耐性細胞クローンでは NRAS 又は MEK1 あるいはその両方に変異 (NRAS:Q61K 及び A146T 変異 MEK1:K59 の欠失 ( インフレーム変異 ;K59del) 又は P387S のミスセンス変異 ) が検出された これらの耐性細胞クローンは GSK Bに対する感受性も 1/200 未満 ~ 約 1/3 に低下していた 細胞周期に及ぼす影響 MEK-ERK 経路は細胞周期を調節する各因子の発現を調節しており MEK-ERK 経路が阻害されると 細胞周期抑制因子である p15 及び p27 の発現が増加し 細胞周期促進因子であるサイクリン A D1 及び E の発現が低下する [Yamaguchi, 2011] その結果 細胞周期抑制因子である retinoblastoma(rb) 蛋白の活性化 ( リン酸化の抑制 ) 及び細胞周期促進因子の機能抑制が誘導され 細胞周期は G1 期で停止すると考えられている [Yamaguchi, 2011; Dick, 2013] そこで GSK A の細胞周期に関連する因子 ( サイクリン A D1 D2 及び E 並びに CDK2 CDK4 CDK6 p15 p18 p27 p53 p57 c-myc 及び RB) に及ぼす影響を検討した 方法 BRAF V600E 変異陽性のヒト結腸直腸癌由来 HT29 細胞株に GSK A(10 nm) を添加し 15 分間又は あるいは 72 時間培養した (UH2008/00045/00) サイクリン A D1 D2 及び E 並びに CDK2 CDK4 CDK6 p15 p18 p27 p53 p57 c- Myc RB MEK 及び ERKの蛋白レベル また RB MEK 及び ERKのリン酸化レベルをウエスタンブロット法により測定した p. 26
32 結果ヒト結腸直腸癌由来 HT29 細胞株において ERKリン酸化レベルは GSK Aの添加 15 分後に低下し MEKリン酸化レベルは 1 時間後に低下した GSK Aの添加 2 時間後に c-myc 蛋白レベル並びに 4 時間後にサイクリン D1 及び D2 蛋白レベルが低下し 16 時間後に p15 及び p27 蛋白レベルが増加し サイクリン A 蛋白レベルが低下した また 16 時間後には RB のリン酸化レベルが低下し 24 時間後にサイクリン E CDK2 CDK4 及び RB の蛋白レベルがわずかに低下した MEK ERK p53 p18 p57 及び CDK6 の蛋白レベルには変化は認められなかった アポトーシス誘導作用 MEK-ERK 経路はアポトーシスの誘導に関与していると考えられている [Santarpia, 2012] そこで GSK A のアポトーシス誘導作用を検討した 方法 BRAF V600E 変異陽性のヒト結腸直腸癌由来 HT29 並びに Colo205 細胞株をそれぞれ 10 及び 100 nm 並びに 1 及び 10 nm の GSK A 存在下で 又は 4 日間培養した (UH2008/00045/00) Propidium iodideで細胞内 DNA を染色し アポトーシスのマーカーであるサブ G1 分画 (DNA の断片化を検出 ) をフローサイトメトリーにより測定した また ウエスタンブロット法によりアポトーシスのマーカーであるカスパーゼ 3 7 及び 9 並びに PARP の切断 ( 活性化 ) を検討した 結果 GSK Aはいずれの細胞株においても培養 1 日目に G0/G1 期のピークを増加させ 細胞周期の停止を誘導した その後 G0/G1 期のピークは減少し HT29 細胞株では 100 nm で Colo205 細胞株では 10 nmでサブ G1 分画が出現し 培養 3 及び 4 日目にその増加が認められた また GSK A はカスパーゼ 3 7 及び 9 並びに PARP の切断 ( 活性化 ) を誘導した GSK Aによるカスパーゼの活性化は サブ G1 分画の増加が誘導される濃度で認められ 時間経過も一致していた まとめヒト結腸直腸癌由来 HT29 細胞株において GSK A は MEK 及び ERKのリン酸化レベルを低下させ 細胞周期抑制因子である p15 及び p27 蛋白レベルの増加並びに細胞周期促進因子である c-myc 並びにサイクリン A D1 及び D2 蛋白レベルの低下を誘導した また サイクリン E CDK2 CDK4 及び RB の蛋白レベルをわずかに低下させ 細胞周期の停止にかかわる RBリン酸化レベルを低下させた ヒト結腸直腸癌由来 HT29 及び Colo205 細胞株において GSK Aは G0/G1 期のピークを増加させ細胞周期の停止を誘導した後 サブ G1 分画 (DNA の断片化を検出 ) を増加させた また GSK Aはカスパーゼ 3 7 及び 9 並びに PARP の切断 ( 活性化 ) を誘導し カスパーゼの活性化は サブ G1 分画の増加と関連していた p. 27
33 獲得耐性に関する検討アロステリック MEK 阻害薬の耐性獲得メカニズムは報告されていないため KRAS 変異陽性のヒト結腸直腸癌由来 HCT116 細胞株を高濃度の GSK B で 2 週間以上処理して耐性細胞クローンを単離し 耐性化にかかわる要因について検討した 耐性細胞クローンの遺伝子配列解析 GSK B に対する耐性メカニズムを解明する一環として 耐性を示す細胞クローンの遺伝子配列解析を行った 方法 KRAS 変異陽性であり ミスマッチ修復機構を欠損しているヒト結腸直腸癌由来 HCT116 細胞株を数週間かけて GSK Bの濃度を 100 nm~1 μmまで段階的に増加させながら処理し 高濃度である 1 μm でも増殖可能な GSK B 耐性の細胞集団である HCT116 (212-Res) 細胞株を単離した (UH2008/00029/00) その後 限界希釈法により耐性細胞クローン (4 種類 ) を単離した GSK B に対する耐性の獲得を確認するために HCT116(212-Res) 細胞株に GSK Bを添加して 72 時間培養した後 CellTiterGlo アッセイにより生細胞数を計測し 親細胞株 (HCT116 細胞株 ) に対する感受性と比較した また 耐性細胞クローンの 1 種類 ( クローン 4) について ERKリン酸化レベルをウエスタンブロット法により測定し 親細胞株と比較した 耐性化にかかわる要因を検討するために 耐性細胞クローンの MEK1 MEK2 ERK1 及び ERK2 遺伝子の配列解析を行った 結果 GSK B に耐性を獲得した HCT116(212-Res) 細胞株に対する GSK B の増殖抑制作用の IC50 は 3.3 μm であり 親細胞株に対する IC50(2 nm) と比較して感受性は 1/1650に低下した HCT116(212-Res) 細胞株は PD325901に対しても耐性を示した (IC50 >10 μm) また 耐性細胞クローン( クローン 4) に対して GSK B は ERKリン酸化阻害作用を示さなかった GSK B 耐性細胞クローンの配列解析を行った結果 MEK2 における L119P のアミノ酸置換を起こす単一点突然変異がみられたが MEK1 及び ERK1/2 にアミノ酸変異は認められなかった ( 表 ) p. 28
34 表 GSK B に耐性を示す HCT116(212Res) 細胞株から単離した耐性 細胞クローンにおける遺伝子及びアミノ酸変異 遺伝子サンプル塩基対変異アミノ酸変異 MEK1 MEK2 ERK1 ERK2 Data source: UH2008/00029/00 の Table 1 HCT116 親細胞株 変異なし 変異なし 耐性細胞クローン 1, 3, 4, 5 変異なし 変異なし HCT116 親細胞株 C192C/T サイレント 耐性細胞クローン 1, 3, 4, 5 T356T/C L119P HCT116 親細胞株 G156G/A サイレント 耐性細胞クローン 1, 3, 4, 5 G156G/A サイレント HCT116 親細胞株 変異なし 変異なし 耐性細胞クローン 1, 3, 4, 5 変異なし 変異なし MEK2 RNA 干渉による検討 GSK B に対する耐性化にかかわる要因を解明するために MEK2 における単一点突然変異により耐性を獲得した耐性細胞クローン ( ) に対する MEK2 ノックダウンの影響を検討した 方法 GSK B 耐性細胞クローン ( クローン 4) に MEK2 sirna(100 nm) 又はコントロールとして non-silencing sirnaをトランスフェクトした (UH2008/00029/00) トランスフェクトの 24 時間後に CellTiterGlo アッセイにより生細胞数を測定した 結果 GSK B 耐性細胞クローン ( クローン 4) に non-silencing sirnaを導入しても GSK Bに対する耐性を維持していたが (IC50=2565 nm) MEK2 をノックダウンさせる sirnaを導入することにより GSK Bに対する感受性は回復した (IC50= 72 nm) まとめ HCT116 細胞株を高濃度の GSK B で 2 週間以上曝露し GSK Bに耐性を獲得した HCT116(212-Res) 細胞株に対する GSK B の増殖抑制作用の IC50 は 3.3 μm であり 親細胞株に対する IC50(2 nm) と比較して感受性は 1/1650 に低下した HCT116 (212-Res) 細胞株は PD325901に対しても耐性を示した (IC50>10 μm) GSK B 耐性細胞クローンの遺伝子配列解析を行った結果 MEK2 における L119P のアミノ酸置換を起こす単一点突然変異がみられた MEK2 のノックダウンにより GSK B 耐性細胞クローン ( クローン 4)(IC50=2565 nm) の GSK Bに対する感受性は回復した 代謝物の薬理活性 GSK B のヒトでの主な血漿中代謝物は GSK (M5: 脱アセチル体 ) 及び GSK A(M7:M5の酸化体 ) である ( 及び :2012N134931_00) M5 の in vitro における薬理活性を評価するため MEK 阻害作用並びに BRAF V600E 変異陽性 SK-MEL-28 細胞株における ERKリン酸化阻害作用及び細胞増殖抑制作用を検討し 未変化 p. 29
35 体 (GSK B) の作用と比較した また M7 の in vitro における P-MEK1 活性に対す る阻害作用を検討し M5 及び未変化体の作用と比較した M5の薬理活性方法 MEK 阻害作用 GSK B 又は M5の U-MEK1 の活性化 ( キナーゼ活性の発現 ) 及び P-MEK1 活性 (ERKをリン酸化する活性) に対する阻害作用を それぞれ 及び と同様の方法で検討した (2012N139081_00) ERK 阻害作用 BRAF V600E 変異陽性のヒト悪性黒色腫由来 SK-MEL-28 細胞株を一連の濃度の GSK B 又は M5で 1 時間処理した 細胞を洗浄後 リン酸化 ERKに対する抗体を用いたウエスタンブロット法により ERKリン酸化レベルを測定した 細胞増殖抑制作用 SK-MEL-28 細胞株を nm~7.3 μm の GSK B 又は M5 存在下で 72 時間培養し CellTiterGloアッセイにより生細胞数を測定した 結果 M5の U-MEK1 の活性化に対する阻害作用の IC50(1.01 nm) は GSK Bの IC50 (0.72 nm) の 1.4 倍であった ( 表 ) また M5の P-MEK1 活性に対する阻害作用の IC50(34.55 nm) は GSK Bの IC50(14.10 nm) の 2.5 倍であったことから ( 表 ) M5 の MEK 阻害作用は GSK B と同程度であることが示された 同様に M5の SK-MEL-28 細胞株における ERKリン酸化阻害作用の IC50(2.0 nm) は GSK Bの IC50(1.6 nm) の 1.3 倍であり M5 の細胞増殖抑制作用の IC50(1.7 nm) は GSK Bの IC50(0.9 nm) の 1.9 倍であったことから ( 表 ) M5の ERK リン酸化阻害作用及び細胞増殖抑制作用も GSK B と同程度であることが示された 表 代謝物 M5 の薬理活性 被験物質 全長キナーゼにおける検討 U-MEK1 活性化阻害作用 P-MEK1 活性阻害作用 IC50 (nm) SK-MEL-28 細胞株における検討 ERK リン酸化阻害作用 細胞増殖抑制作用 GSK B (21) (24) (2) (4) M (2) (2) (2) (2) 平均値 ± 標準偏差 括弧内の数値は例数 Data source: 2012N139081_00の Table M7の薬理活性方法 GSK B M5 又は M7の P-MEK1 活性 (ERKをリン酸化する活性) に対する阻害作用を と同様の方法で検討した (2012N148387_00) p. 30
36 結果 M7の P-MEK1 活性に対する阻害作用の IC50は 73 nm であり 阻害活性は未変化体 (GSK B;IC50=7.0 nm) の約 1/10と弱かった ( 表 ) なお M5の P- MEK1 活性に対する阻害作用の IC50 は 9.0 nm であり 未変化体の活性と同程度であった ( 表 ) 表 代謝物 M7 の薬理活性 被験物質 P-MEK1 活性阻害作用 :IC50 (nm) GSK B ( 未変化体 ) M M 平均値 ± 標準偏差 (n=2) Data source: 2012N148387_00の Table 1 まとめヒトでの主な代謝物である M5 及び M7の in vitro における薬理活性を GSK Bと比較した M5 の U-MEK1 の活性化 ( キナーゼ活性の発現 ) 及び P-MEK1 活性 (ERKをリン酸化する活性 ) に対する阻害作用 並びにヒト悪性黒色腫由来 SK-MEL-28 細胞株における ERKリン酸化阻害作用及び増殖抑制作用は いずれも GSK B と同程度であった 一方 M7 の P-MEK 活性に対する阻害作用は GSK B の約 1/10 と弱かった ラット イヌ及びヒト末梢血単核細胞を用いた in vitro におけるサロゲートマーカーの検討 GSK B の薬理活性を評価するサロゲートマーカーとして 末梢血単核細胞 (PBMC) における ERKリン酸化レベルが利用できるか否かを in vitro において検討した 方法ラット イヌ及びヒトの血液に GSK B(0.13 nm~2.5 μm) を添加した後 PMA (1 μm) で 30 分間 (37 C) 刺激した (UH2008/00030/00) その後 PBMC を単離し ERKリン酸化レベルを ELISA 法により測定した 結果 GSK B は PMA 刺激ヒト PBMC における ERKリン酸化を濃度依存的に阻害し その IC50は 及び 24.5 nmであった ( 表 ) PMA 刺激イヌ PBMCにおける GSK B の ERKリン酸化阻害作用の IC50 はヒトの 1/3 未満であり ヒト PBMC と比較して有意に低かった 一方 PMA 刺激ラット PBMC における GSK Bの IC50はヒトと同程度であった p. 31
37 表 動物種 ラット イヌ及びヒト PBMC における ERK リン酸化阻害作用 IC50 (nm) 試験 1 試験 2 ヒト イヌ * - ラット 平均値 ± 標準偏差 (n=2~4) -: 実施せず *:p<0.05 vs ヒト PBMC (t- 検定 ) Data source: UH2008/00030/00の Table 1 及び 2 まとめ GSK Bは PMA 刺激ヒト イヌ及びラット PBMC における ERKリン酸化を濃度依存的に阻害した 阻害作用の IC50はヒト及びラットでは同程度であり イヌではヒトと比較して低値であった In vivo 試験 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマウス異種移植モデルにおける検討 ERKリン酸化阻害作用 ( 単回経口投与による作用持続時間 ) 方法 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株の懸濁液を雌無胸腺ヌードマウス (CD1 nu/nu) の皮下に移植し 腫瘍を 1~4 週間増殖 ( 腫瘍塊の体積は 120~ 450 mm 3 ) させた後 GSK B(1 又は 3 mg/kg) を単回経口投与した (UH2008/00051/03) 投与 又は 48 時間後に腫瘍組織を採取し ERK 及びリン酸化 ERK 量をウエスタンブロット法により測定し 総 ERK 量に対するリン酸化 ERK 量の比を算出した また 腫瘍組織採取時に採血し LC-MS/MS 法により血中 GSK 濃度を測定した 結果 GSK Bは 1 mg/kg の経口投与により投与 4 時間後から腫瘍組織において ERKリン酸化阻害作用を示し 阻害作用は 8 時間後まで持続したが 24 時間後では作用が減弱する傾向がみられた ( 図 ) 3 mg/kg では投与 2 時間後から ERKリン酸化阻害作用が認められ 阻害作用は 8 時間後まで持続したが 24 時間後では阻害作用は認められなかった ( 図 ) また 3 mg/kg では 1 mg/kg と比較してより強い阻害作用がみられた ( 図 ) GSK B の 1 及び 3 mg/kg を単回経口投与したとき 作用の持続がみられた 8 時間 (480 分 ) 後の血中 GSK 濃度は 100 nm を超えており 作用がみられなかった 24 時間 (1440 分 ) 後では 100 nmを下回っていた ( 図 ) p. 32
38 図 平均値 ± 標準偏差 (n=4) 縦軸 : 総 ERK 量に対するリン酸化 ERK 量の比 Vehicle: 媒体 (0.5% HPMC-0.1% Tween 80 溶液 ) BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマ ウス異種移植モデルにおける ERK リン酸化阻害作用 Data source: UH2008/00051/03 の Figure 1 平均値 (n=4) 図 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマウス異種移植モデルにおける単回投与後の血中 GSK 濃度推移 Data source: UH2008/00051/03 の Figure p. 33
39 ERKリン酸化阻害作用 ( 単回経口投与による用量反応性及び 4 日間経口投与 ) 方法 と同様の方法で腫瘍を増殖させた後 GSK Bの あるいは 3 mg/kg を単回又は 3 mg/kg を 1 日 1 回 4 日間経口投与した (UH2008/00051/03) 1 又は 4 日目の投与 4 時間後に腫瘍組織を採取し ERK 及びリン酸化 ERK 量を ELISA 法により測定し 総 ERK 量に対するリン酸化 ERK 量の割合を算出した 結果 GSK Bは 1 及び 3 mg/kg の単回経口投与並びに 3 mg/kgの 4 日間経口投与により 媒体投与と比較して総 ERK 量に対するリン酸化 ERK 量の比を有意に低下させた ( 図 ) 4 日間経口投与したときの ERKリン酸化阻害作用は 単回経口投与したときと比較してより強い傾向がみられた ( 図 ) 図 平均値 ± 標準偏差 (n=3) **:p<0.01 vs 媒体群 (t- 検定 ) 縦軸 : 総 ERK 量に対するリン酸化 ERK 量の割合 0 ( 媒体 ):0.5% HPMC-0.1% Tween 80 溶液 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマ ウス異種移植モデルにおける単回及び 4 日間経口投与後の Data source: UH2008/00051/03 の Figure 10 ERK リン酸化阻害作用 ERKリン酸化阻害作用 ( 単回並びに 7 及び 14 日間経口投与 ) 方法 と同様の方法で腫瘍を増殖させた後 GSK B(3 mg/kg) を単回又は 1 日 1 回 7あるいは 14 日間経口投与した (UH2008/00051/03) 1 7 又は 14 日目の投与 4 時間後に腫瘍組織を採取し ERK 及びリン酸化 ERK 量を ELISA 法により測定し 総 ERK 量に対するリン酸化 ERK 量の割合を算出した 結果 GSK Bは 3 mg/kg の単回並びに 1 日 1 回 7 及び 14 日間経口投与により 総 ERK 量に対するリン酸化 ERK 量の比を低下させた ( 図 ) また 14 日間経口投与にお p. 34
40 いても 単回経口投与と同程度の ERK リン酸化阻害作用がみられ 阻害作用は減弱しない ことが示された ( 図 ) 図 平均値 ± 標準偏差 (n=3) GSK B の用量 :3 mg/kg Vehicle: 媒体 (0.5% HPMC-0.1% Tween 80 溶液 ) 縦軸 : 総 ERK 量に対するリン酸化 ERK 量の割合 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマ ウス異種移植モデルにおける単回並びに 7 及び 14 日間経口投与後の Data source: UH2008/00051/03 の Figure 3 ERK リン酸化阻害作用 p27 蛋白レベル増加作用 p27は細胞周期抑制因子であり 細胞周期を G1 期で停止させることが知られている [Khattar, 2010] また MAPK 及び PI3K 経路のいずれも p27 の発現調節に関与していることが報告されている [Khattar, 2010] そこで BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマウス異種移植モデルの腫瘍組織において GSK Bの p27 蛋白レベルに及ぼす影響を検討した 方法 と同様の方法で腫瘍を増殖させた後 GSK Bの 3 mg/kg を 1 日 1 回 7 日間経口投与し 投与 4 時間後に腫瘍組織を採取し ウエスタンブロット法により p27 蛋白を検出した (UH2008/00051/03) 結果 GSK B は 3 mg/kg の 1 日 1 回 7 日間経口投与により G1 期停止のマーカーである p27 蛋白レベルを増加させた ( 図 ) p. 35
41 図 GSK B の 3 mg/kg を 1 日 1 回 7 日間経口投与し 最終投与の 4 時間後に測定 Tumor#1~3: 各群 n=3 Vehicle: 媒体 (0.5% HPMC-0.1% Tween 80 溶液 ) 上図 : マウス抗 p27 抗体 下図 : ウサギ抗 p27 抗体を用いて検討 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いた マウス異種移植モデルの腫瘍組織における p27(g1 期停止のマーカー ) Data source: UH2008/00051/03 の Figure 5 蛋白レベル増加作用 腫瘍増殖抑制作用方法 と同様の方法で腫瘍を増殖させた後 GSK Bの 1 3 又は 10 mg/kg を 1 日 1 回 14 日間経口投与した (UH2008/00051/03) 比較対照薬として ノギテカンの 10 mg/kgを 4 日間隔で 4 回腹腔内投与した 腫瘍の長径と短径を週 2 回測定し 腫瘍体積 ( 長径 短径 2 0.5) を算出した 本薬の投与 13 日目に 媒体群に対する腫瘍増殖抑制率を算出した 最終測定時の腫瘍体積について ANCOVA 検定法及び Stepdown Bonferroni 検定法により 媒体群との間で統計解析を行った 腫瘍の完全退縮は個々の腫瘍体積が 13 mm 3 未満の場合と定義し 部分的退縮は個々の腫瘍体積が投与開始時の 50% 程度の場合と定義した 結果 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマウス異種移植モデルにおいて GSK Bの 1 mg/kg を 1 日 1 回 14 日間経口投与することにより 7 例中 1 例で部分的退縮が認められ 抑制率は 49.6% であり 統計学的有意差が認められた ( 図 表 ) 3 mg/kg では 7 例中 1 例で完全退縮が 2 例で部分的退縮が認められ 抑制率は 77.8% であり 統計学的有意差が認められた ( 図 表 ) 10 mg/kg を 1 日 1 回 14 日間経口投与したときには忍容性が認められなかった ノギテカンは 10 mg/kgの 4 日間隔 4 回腹腔内投与により 腫瘍の退縮が全例にみられた ( 図 ) p. 36
42 縦軸 : 腫瘍体積中央値 (mm 3 ) 横軸 : 腫瘍移植後の日数平均値 (n=7) qd:1 日 1 回投与 CR: 完全退縮 PR: 部分的退縮 Topotecan: ノギテカン Vehicle: 媒体 (0.5% HPMC-0.1% Tween 80 溶液 ) 10 mg/kg の 1 日 1 回 14 日間経口投与は忍容性を示さず 図 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマ ウス異種移植モデルにおける腫瘍増殖抑制作用 ( 腫瘍体積中央値 ) Data source: UH2008/00051/03 の Figure 13 表 群 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマ ウス異種移植モデルにおける腫瘍増殖抑制作用 ( 腫瘍増殖抑制率 ) 腫瘍体積中央値 (mm 3 ) 腫瘍増殖抑制率 (%) ANCOVA p 値 Stepdown Bonferroni p 値 CR/PR (7 例中 ) 媒体 GSK B 1 mg/kg 1 日 1 回 14 日間経口投与 PR GSK B 3 mg/kg 1 日 1 回 14 日間経口投与 < CR/2PR GSK B 10 mg/kg 1 日 1 回 14 日間経口投与 忍容性なし ノギテカン 10 mg/kg 4 日間隔 4 回腹腔内投与 CR/1PR 腫瘍増殖抑制率は 投与 13 日目の腫瘍体積から算出した p 値は p<0.05 を有意差ありと判断した CR: 完全退縮 PR: 部分的退縮 -: 該当せず又は実施せず Data source: UH2008/00051/03 の Table 4 まとめ V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマウス異種移植モデルの 腫瘍組織において GSK B は ERK のリン酸化を用量依存的に阻害し ERK リン酸化 p. 37
43 阻害作用が持続していた 8 時間後の血中 GSK 濃度は 100 nm を超えており 作用が認められなかった 24 時間後では 100 nmを下回っていた GSK Bの ERKリン酸化阻害作用は 14 日間経口投与においても 減弱しなかった また GSK B は 3 mg/kg の 1 日 1 回 7 日間経口投与により 腫瘍組織において G1 期停止のマーカーである p27 蛋白レベルを増加させた 更に GSK Bは 1 及び 3 mg/kg の 1 日 1 回 14 日間経口投与により 腫瘍増殖を有意に抑制した サロゲートマーカーの検討 PBMCにおける ERKリン酸化阻害作用が GSK B の薬理活性を評価するためのサロゲートマーカーとして利用できるか否かを in vivo において評価するため GSK B を経口投与したマウスから PBMC を単離して ERKリン酸化阻害作用を検討した 方法雌無胸腺ヌードマウス (CD1 nu/nu) に GSK B( 及び 3 mg/kg) を単回経口投与し 4 時間後に採血した その後 と同様の方法で PBMC を単離し PMA(20 μm) で 30 分間刺激した後 ERK 及びリン酸化 ERK 量を ELISA 法により測定し 総 ERK 量に対するリン酸化 ERK 量の比を算出した (UH2008/00030/00) 結果 GSK B(0.03~3 mg/kg) を経口投与したマウスから単離した PBMCにおける総 ERK 量に対するリン酸化 ERK 量の比は GSK Bの用量に依存して低下した ( 図 ) 平均値 ± 標準偏差 (n=3) Unstim: 刺激なし Stim:PMA で刺激縦軸 : 総 ERK 量に対するリン酸化 ERK 量の比 図 GSK B を投与したマウスから単離した PBMC における Data source: UH2008/00030/00 の Figure 3 ERK リン酸化阻害作用 p. 38
44 まとめ GSK B を投与したマウスから単離した PBMC の ERK リン酸化レベルは GSK B の用量に依存して低下した 副次的薬理試験 各種受容体 チャネル 酵素及びキナーゼに及ぼす影響 23 種類の各種受容体及びチャネル並びに 7 種類の各種酵素に及ぼす GSK A の影響を検討した (CD2007/01300/00) GSK A は 10 μmで 50% を超える阻害作用を示さなかった (IC50>10 μm) 各種キナーゼに及ぼす影響 ( 選択性 ) の項 ( ) に記載したとおり 43 種類の各種キナーゼ (UH2008/0021/00) 及び 171 種類の各種キナーゼ (UH2008/00047/00) に及ぼす影響をパネル法により検討した結果 GSK A 及び GSK Bは 10 μmで 50% を超える阻害作用を示さなかった (IC50>10 μm) 正常ヒト臍帯静脈血管内皮細胞 (HUVEC) の増殖に及ぼす影響方法 HUVECを GSK B(0.014 nm~7.3 μm) 存在下で 72 時間培養し CellTiterGlo アッセイにより生細胞数を測定し 増殖抑制作用の IC50 を算出した (UH2007/00097/02) なお HUVEC に対する影響は 増殖因子非存在下及び存在下の条件下で検討した 結果 GSK B は増殖因子非存在下において HUVECの細胞数に影響を及ぼさなかった (IC50=10000 nm) 一方 増殖因子存在下では 増殖抑制作用を示した(IC50=4 nm) 安全性薬理試験 中枢神経系に及ぼす影響雄 SDラット (4 匹 ) に GSK Bの 100 mg/kg を単回経口投与し Irwin 試験の変法により投与 及び 24 時間後の一般状態及び行動を評価した (CD2007/01303/00) 100 mg/kg で体重増加の抑制がみられた ( 体重増加は媒体群の 1/3) また 自発運動量の減少 ( 投与 2 及び 24 時間後 ) 腹臥位( 投与 2 及び 3 時間後 ) 眼瞼下垂( 投与 3 4 及び 24 時間後 ) 下痢( 投与 4~24 時間後 ) 立毛( 投与 24 時間後 ) 及び散瞳 ( 投与 24 時間後 ) が認められた 呼吸系に及ぼす影響覚醒雄 SDラット (4 匹 ラテン方格クロスオーバー法 ) に GSK Bの 及び mg/kg( 及び 1 mg/m 2 ) を単回経口投与し 換気機能 ( 一回換気量 呼吸数及び分時換気量 ) 気道抵抗( 総肺抵抗 ) 及び体温を投与 5 日後まで測定した (CD2007/00963/00) p. 39
45 0.125 mg/kg で軽度で一過性の体温低下 ( 最大 0.8 C 投与 1 時間後 ) がみられた 換気機 能及び気道抵抗に影響は認められなかった 心血管系に及ぼす影響 herg アッセイ GSK Bは herg cdna を導入した HEK293 細胞 (n=5) において hergチャネルテール電流を抑制し IC25 IC50 及び IC75はそれぞれ 及び 5.30 μm( 及び ng/ml) であった (FD2007/00151/00) ウサギ左心室ウェッジ標本を用いた試験雌ウサギ左心室ウェッジ標本 (n=4) において 及び 30 μm( 約 及び ng/ml) の濃度で (18450 ng/mlは溶解限界濃度 ) GSK B の QT 間隔及び Tp-e 間隔への影響並びに早期後脱分極の誘発の可能性を評価した (UH2007/00108/00) GSK Bは QT 間隔に影響を及ぼさなかった GSK Bは 10 及び 30 μmで等尺性収縮力をそれぞれ 16.3 及び 64.8% 低下させ いずれも有意差がみられた (t- 検定 ) また 30 μmで Tp-e 間隔を約 26% 短縮させ 有意差がみられた (t- 検定 ) イヌにおける in vivo 試験 静脈内投与 ( 非 GLP 試験 ) 麻酔雄ビーグル犬 (3 匹 クロスオーバー法 ) において GSK A の 1 mg/kg (20 mg/m 2 ) を静脈内投与 (10 分間持続投与 ) し 心電図パラメータ (PR 間隔 QRS 幅 RR 間隔 QT 間隔及び QTc 間隔 ) 血圧及び心拍数に及ぼす影響を検討した (CD2007/01301/00) 投与前 投与 及び 30 分後にこれらの評価項目並びに血漿中 GSK 濃度を測定した GSK Aは心電図パラメータ 血圧及び心拍数に影響を及ぼさなかった 血漿中 GSK 濃度は投与開始 10 分後まで増加し 最高血漿中 GSK 濃度は 2.5 μm ( 約 1500 ng/ml) であった 経口投与 (GLP 試験 ) 覚醒雄ビーグル犬 (4 匹 ラテン方格クロスオーバー変法 ) に GSK Bの 及び mg/kg( 及び 1.5 mg/m 2 ) を単回経口投与し テレメトリー法により動脈圧 心拍数 体温及び ECG 間隔を投与 5 日後まで測定した (CD2007/00962/00) GSK B は動脈圧 心拍数 ECG パラメータ ( 波形異常 不整脈及び間隔 ) 及び体温に影響を及ぼさなかった p. 40
46 薬力学的薬物相互作用試験臨床において併用される GSK との併用による薬理作用を検討した in vitro 及び in vivo の試験成績は CTD 併用パートの 2.6.2( タフィンラー / メキニスト併用 ) に記載した 考察及び結論 効力を裏付ける試験 In vitro 試験 MEK 阻害作用 GSK Bは U-MEK1/2 の活性化 ( キナーゼ活性の発現 ) を阻害した U-MEK1 の活性化 (MEK1 のキナーゼ活性の発現 ) には MEK1 の Ser218 及び Ser222 の 2ヵ所のリン酸化が必要であることが報告されている [Yan, 1994] GSK B は変異型 BRAF V600E の存在下で MEK1 の Ser218のリン酸化を阻害したが Ser222 のリン酸化には影響を及ぼさなかったことから GSK B の MEK 阻害作用の発現には MEK1 の Ser218 のリン酸化阻害作用が重要であると考えられる また GSK Bは P-MEK1/2 活性 (ERKをリン酸化する活性 ) を阻害し P-MEK1 に対する阻害様式は ATP との非競合的阻害であった GSK Bは ATP 非競合的なアロステリック阻害薬である PD と P-MEK1 の結合部位において 相互排他的に競合的に結合を阻害することが示された このことから PD と同様に GSK Bは ATP 非競合的なアロステリック阻害薬であると考えられた GSK Bは MEK1/2 を阻害したのに対して 43 及び 171 種類の各種キナーゼ ( パネル ) に対する阻害作用は弱く (IC50の比較で>758 倍 ) MEK1/2 と最も相同性の高い MEK5 のリン酸化に対しても阻害作用を示さなかったことから MEK1/2 に対する高い選択性が示された これらの結果から GSK B は U-MEKの活性化 ( キナーゼ活性の発現 ) 及び P-MEK 活性 (ERKをリン酸化する活性) の両方を阻害する強力かつ選択的な MEK1/2 阻害薬であり ATP 非競合的なアロステリック阻害薬として作用することが示された 腫瘍細胞増殖抑制作用計 320 種類 (CellTiterGlo アッセイ及び DAPI 染色法による検討で用いた細胞株数の合計 ) のヒト腫瘍細胞株パネルを用いた網羅的検討において BRAF 変異陽性細胞株の 88% 及び RAS 変異陽性細胞株の 72% の細胞株が GSK Bに対して高い感受性を示した 一方 野生型 BRAF 及び RAS を有する細胞株では 28% の細胞株だけが高い感受性を示した また 218 種類のヒト腫瘍細胞株パネル ( 固形癌由来 ) を用いた網羅的解析においても BRAF 及び RAS 変異陽性細胞株の 80% を超える細胞株が GSK Bに対して高い感受性を示した 一方 野性型 BRAF 及び RAS を有する細胞株では 高い感受性を示した細胞株は 40% 未満であった また 組織別では 特に 悪性黒色腫 膵臓癌及び結腸癌由来の 80% を超える細胞株が GSK B に対して高い感受性を示した 21 株中 ERKリン酸化 (Thr202/Tyr204) レベルの高い上位 25% の 5 株のうち 4 株は GSK Bに感受性を示した このことから ベースラインの ERKリン酸化レベルが非 p. 41
47 常に高い細胞株は GSK Bに対する感受性を有する可能性が考えられるが その他の 16 株での ERKリン酸化レベルと感受性との関連性は明らかではなかったことから 効果予測因子としての有用性は高くはないと考えられる また DUSP6(ERKを不活性化させる働きを有している )mrna レベルが高い細胞株の多くは GSK Bに対して高い感受性を示し DUSP6 mrnaレベルが低い細胞株の多くは GSK B に対する感受性が低かった これらの試験成績から RAF 及び RAS 変異の有無並びに ERKリン酸化レベル及び DUSP6 mrna レベルは GSK B の効果予測因子となる可能性が示された BRAF V600 変異陽性の 17 種類のヒト悪性黒色腫細胞株のうち 14 種類の細胞株は GSK Bに対して高い感受性を示し 増殖抑制作用の IC50は 0.3~9.5 nmであった In vitro における薬効発現濃度 ( 標的濃度 ) に関して の試験で検討した細胞株のうち 4 種類の代表的な BRAF V600E 変異陽性のヒト悪性黒色腫細胞株に対する GSK Bの増殖抑制作用の IC50 を この 4 種類のうちの 1 種類である SK-MEL-3 細胞株における ERKリン酸化阻害作用に対する高濃度ヒト血清の影響 ( ヒト蛋白結合の影響 ) を考慮した係数 (11.9) を用いて補正し GSK B の薬効発現濃度 ( 標的濃度 ) を算出したところ その値は ng/ml(15.00 nm) であることが示された ( 表 ) [2012N139008_00] 表 BRAF V600E 変異陽性のヒト悪性黒色腫細胞株に対する増殖抑制作用及び ヒト蛋白結合を考慮した補正により算出した薬効発現濃度 ( 標的濃度 ) 細胞株 由来組織 BRAF 変異 IC50 (nm) A375 悪性黒色腫 V600E 1.25 A375 悪性黒色腫 V600E 1.22 SK-MEL-28 悪性黒色腫 V600E 1.46 SK-MEL-28 悪性黒色腫 V600E 1.68 SK-MEL-3 悪性黒色腫 V600E SK-MEL-3 悪性黒色腫 V600E MALME3M 悪性黒色腫 V600E 1.39 MALME3M 悪性黒色腫 V600E 1.28 平均値 1.26 ERK リン酸化阻害アッセイにおけるヒト蛋白結合を考慮した補正係数 11.9 薬効発現濃度 (nm) 薬効発現濃度 (ng/ml) Data source: [2012N139008_00] の Table 1 これらの成績から GSK Bは BRAF V600 変異陽性のヒト悪性黒色腫細胞株の増殖を抑制することが示された 一方 BRAF V600 変異陽性であっても 17 種類のうち 3 種類の細胞株が GSK B に対して感受性を示さなかった ( ) 当該試験ではヒト悪性黒色腫由来細胞株の RB CDK4 PTEN 及び MEK1/2 の遺伝子変異の有無を調べ その変異の有無が GSK B に対する感受性に及ぼす影響について検討した (2011N116395_00) その結果 GSK Bに対して非感受性であった 3 株のうち 2 株では MEK1 又は MEK2 に変異を有していたことから MEK 変異が GSK B の感受性に影響を与えた可能性が考えられる CDK4 及び PTENに関しては 変異と感受性との間に関連性は認められなかった p. 42
48 GSK B のヒト悪性黒色腫由来 A375P F11 細胞株に対する増殖抑制作用の可逆性を検討した結果 高濃度である 1000 及び 3000 nmを除き 増殖抑制作用はウォッシュアウトすることにより減弱することが示された このことから 持続的な増殖抑制作用を発現させるためには GSK B の持続的な曝露が必要であることが示唆された BRAF V600 変異陽性の 2 種類のヒト悪性黒色腫由来細胞株 (A375P F11 細胞株 (V600E) 及び YUSIT1 細胞株 (V600K)) を高濃度の GSK で 1 週間以上培養して耐性細胞クローンを単離し (IC nm) これらの GSK 耐性細胞クローンに対する GSK Bに対する感受性を検討した結果 1/200 未満 ~ 約 1/3 以下に低下していた GSK 耐性細胞クローンでは NRASあるいは MEK1 又はその両方に変異 (NRAS: Q61K 及び A146T 変異 MEK1:K59 の欠失 ( インフレーム変異 ;K59del) 又は P387S のミスセンス変異 ) が検出されたが KRAS HRAS ARAF CRAF PTEN 及び PIK3CA に変異はみられなかった なお これらの耐性細胞クローンに GSK 及び GSK B を併用して BRAF 及び MEK1/2 の両方を阻害すると 感受性が回復することが示されている ( タフィンラー / メキニスト併用 ) 細胞周期に及ぼす影響及びアポトーシス誘導作用 BRAF V600E 変異陽性のヒト結腸直腸癌由来 HT29 細胞株において GSK A は MEK 及び ERKのリン酸化レベルを低下させ 細胞周期抑制因子である p15 及び p27 蛋白レベルの増加並びに細胞周期促進因子である c-myc 並びにサイクリン A D1 及び D2 蛋白レベルの低下を誘導した また サイクリン E CDK2 CDK4 及び RB の蛋白レベルをわずかに低下させ 細胞周期の停止にかかわる RB リン酸化レベルを低下させた ヒト結腸直腸癌由来 HT29 及び Colo205 細胞株 (BRAF V600E 変異陽性 ) において GSK Aは G0/G1 期のピークを増加させ細胞周期の停止を誘導した後 サブ G1 分画 (DNAの断片化を検出) を増加させた また GSK Aはカスパーゼ 3 7 及び 9 並びに PARP の切断 ( 活性化 ) を誘導し カスパーゼの活性化は サブ G1 分画の増加と関連していた これらのことから GSK Aのアポトーシス誘導作用は G0/G1 期停止後のカスパーゼの活性化と関連しており GSK Aの細胞増殖抑制作用には アポトーシス誘導作用が関与していると考えられる GSK Bに対する獲得耐性発現メカニズム KRAS 変異陽性のヒト結腸直腸癌由来 HCT116 細胞株を高濃度の GSK Bで 2 週間以上処理して耐性細胞株 (HCT116(212-Res); 感受性は 1/1650に低下 ) を単離し また この耐性細胞株から耐性細胞クローンを単離して耐性化にかかわる遺伝子変異について検討した なお この耐性細胞株は他のアロステリック MEK 阻害薬である PD に対しても耐性を示した ( 感受性は 1/909 未満に低下 )(UH2008/00029/00) GSK B 耐性細胞クローンの遺伝子配列解析を行った結果 MEK2 における L119P のアミノ酸置換を起こす単一点突然変異が認められた sirnaを用いて MEK2 をノックダウンさせることにより 耐性細胞クローンの GSK Bに対する感受性は回復することから GSK Bに対する耐性発現メカニズムには MEK2 における L119P の単一点突然変異が関与していること p. 43
49 が示された 他の MEK 阻害薬である PD の耐性にも MEK1 遺伝子の L115P の変異が関与していることが報告されており L115 は PD の結合ポケット内に存在していることが示唆されていることから [Delaney, 2002] GSK Bに対する耐性の発現にも結合部位における MEKの変異が深く関与している可能性が考えられる なお GSK B 等の MEK 阻害薬を患者に投与したときに MEK2 における L119P の変異が患者から検出された報告はない 代謝物の薬理活性ヒトでの主な血漿中代謝物は GSK (M5: 脱アセチル体 ) 及び GSK A (M7:M5 の酸化体 ) である ( 及び :2012N134931_00) M5 の in vitro における U-MEK1 の活性化 ( キナーゼ活性の発現 ) に対する阻害作用 P-MEK1 活性 (ERKをリン酸化する活性 ) に対する阻害作用 BRAF V600E 変異陽性のヒト悪性黒色腫由来 SK- MEL-28 細胞株における ERKリン酸化阻害作用及び増殖抑制作用は GSK B と同程度であった また M7の P-MEK1 活性に対する阻害作用の IC50 は 73 nmであり 阻害活性は未変化体 (GSK B:IC50=7.0 nm) の約 1/10と弱かった ヒトにおける M5 及び M7の薬理活性はそれぞれ同程度及び約 1/10 であったが それぞれの血漿中濃度はいずれも未変化体の約 1/7 以下であることから ( :2012N134931_00) GSK Bの薬効における M5 及び M7の寄与の程度は低いと考えられる In vivo 試験 ERKリン酸化阻害作用 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマウス異種移植モデルにおいて GSK Bは 1 及び 3 mg/kg の単回経口投与により 腫瘍組織における ERKリン酸化を阻害した GSK Bの 3 mg/kg では 投与 2 時間後から ERKリン酸化阻害作用が認められ 阻害作用は 8 時間後まで持続した ERKリン酸化阻害作用の持続がみられた 8 時間後の血中 GSK 濃度は 100 nm を超えており 作用がみられなかった 24 時間後では 100 nm を下回っていた これらの結果から 血中 GSK 濃度が 100 nmを超えたときに ERKリン酸化阻害作用が発現すると考えられた 反復経口投与の検討では GSK Bは 3 mg/kg を 1 日 1 回 4 7 又は 14 日間経口投与することにより ERKリン酸化を阻害した このことから GSK B による ERKリン酸化阻害作用は反復投与しても減弱しないことが示された p27 蛋白レベル増加作用 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマウス異種移植モデルにおいて GSK Bは 3 mg/kg を 1 日 1 回 7 日間経口投与することにより G1 期停止のマーカーである p27 蛋白レベルを増加させ 細胞周期を G1 期で停止させることが示唆された 本試験成績は in vitro 試験成績 ( ) と一致しており GSK A 及び GSK Bは MEKを阻害し p27 及びサイクリン D1 等の細胞周期調節因子の発現を p. 44
50 調節し RB の機能を阻害して細胞周期を G1 期で停止させ カスパーゼ 3 等の活性化を誘 導してアポトーシスを誘導することが示唆された 腫瘍増殖抑制作用 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株を用いたマウス異種移植モデルにおいて GSK Bは 1 及び 3 mg/kg の 1 日 1 回 14 日間経口投与により 腫瘍増殖を有意に抑制した 腫瘍増殖抑制作用を示した用量は 同モデルで ERKリン酸化阻害作用 (1 及び 3 mg/kg) 及び p27 蛋白レベル増加作用 (3 mg/kg) を示した用量と同程度であったことから GSK B は ERKのリン酸化を阻害し 細胞周期を停止させることにより腫瘍増殖を抑制したと考えられる このような in vivo における用量依存的な腫瘍増殖抑制作用は BRAF V600E 変異陽性のヒト結腸直腸癌由来 HT-29 及び Colo205 細胞株並びに KRAS 変異陽性のヒト結腸直腸癌由来 HCT116 細胞株を用いたマウス異種移植モデルでも認められた (UH2008/0051/02) ことから in vitro 試験の成績と同様に GSK Bは組織の由来にかかわらず BRAF V600 変異陽性及び KRAS 変異陽性の腫瘍の増殖を抑制する可能性が考えられる ヒト血漿中 GSK 濃度及びマウス異種移植モデルにおける薬効発現濃度の比較マウスにおける in vivo 試験において 血中 GSK 濃度が 100 nm(61.5 ng/ml) を超えたときに十分な ERKリン酸化阻害作用を発現し ( ) 腫瘍増殖抑制作用は ERKリン酸化阻害作用により発現することが示唆されている BRAF V600 変異陽性固形癌の日本人患者に予定臨床用量である 2 mg を 1 日 1 回 15 日間経口投与したときの定常状態における血漿中 GSK 濃度 ( トラフ濃度 ) は約 11.7 ng/mlであり ( ; MEK 試験 ) 乖離は大きくないことから GSK Bは予定臨床用量において効果を発現すると考えられる サロゲートマーカーの検討 GSK Bは in vitro において PMA 刺激ヒト イヌ及びラット PBMCにおける ERK リン酸化を濃度依存的に阻害し ( ) GSK B を経口投与したマウスから単離した PBMC における ERK リン酸化レベルは 用量 (0.03~3 mg/kg) に依存して低下した GSK Bは BRAF V600E 変異陽性のヒト悪性黒色腫由来細胞株 A375P F11 を用いたマウス異種移植モデルで腫瘍増殖抑制作用を示した用量 (1 及び 3 mg/kg) で PBMC における ERK 阻害作用を示したことから 臨床において血液サンプル中の PBMCの ERKリン酸化レベルは GSK Bの MEK 阻害作用を評価するサロゲートマーカーとして有用であると考えられる 副次的薬理試験各種受容体 チャネル 酵素及びキナーゼに及ぼす影響 23 種類の各種受容体及びチャネル並びに 7 種類の各種酵素に及ぼす GSK A の影響を検討した GSK A は 10 μm で 50% を超える阻害作用を示さなかった また 各種 p. 45
51 キナーゼ (43 及び 171 種類のパネル ) に及ぼす影響を検討した結果 GSK A 及び GSK B は 10 μm で 50% を超える阻害作用を示さなかった これらの結果から GSK B は選択的な MEK 阻害薬であることが示された HUVECの増殖に及ぼす影響増殖因子存在下及び非存在下での HUVECの増殖に及ぼす GSK Bの影響を検討したところ GSK Bは増殖因子非存在下の HUVEC( 正常細胞 ) の細胞数に影響を及ぼさず (IC50=10000 nm) 増殖因子存在下の HUVECの増殖を抑制した (IC50=4 nm) 増殖因子非存在下と存在下での IC50 は 2500 倍の乖離がみられたことから GSK B は正常細胞の増殖には影響を及ぼさないが血管内皮細胞増殖因子等によって増殖が促進している細胞に対しては増殖抑制作用を示すと考えられた また BRAF V600 変異を有するヒト腫瘍細胞株に対する増殖抑制作用の IC50 は 0.3~ 9.5 nmであり ( ) 正常細胞の増殖に及ぼす影響の代表として検討した増殖因子非存在下の HUVEC に対する IC50(10000 nm) と比較すると 1053~33333 倍の乖離がみられたことから 高い腫瘍選択性を有することが示唆された 安全性薬理試験雄 SDラットに GSK B の 100 mg/kg を単回経口投与することにより 体重増加の抑制 ( 体重増加は媒体群の 1/3) 自発運動量の減少( 投与 2 及び 24 時間後 ) 腹臥位( 投与 2 及び 3 時間後 ) 眼瞼下垂( 投与 3 4 及び 24 時間後 ) 下痢( 投与 4~24 時間後 ) 立毛 ( 投与 24 時間後 ) 及び散瞳 ( 投与 24 時間後 ) が認められた 影響が認められた用量である 100 mg/kg は予定臨床用量である 2 mg を体重 50 kg の患者に投与した場合の 2500 倍に相当することから 臨床において GSK B が中枢神経系に対する重篤な副作用を誘発する可能性は低いと考えられる 雄 SDラットにおいて GSK Bの 及び mg/kg( 及び 1 mg/m 2 ) の単回経口投与により mg/kg で軽度で一過性の体温低下 ( 最大 0.8 C 投与 1 時間後 ) がみられた 雄ラットに GSK Bの mg/kg を単回経口投与したときの血漿中 GSK 濃度は 5.48 ng/mlであり ( ) 日本人患者に GSK Bの予定臨床用量である 2 mg を 1 日 1 回 15 日間経口投与 (n=5) したときの Cmax(25.5 ng/ml; 表 ) よりも低く イヌの 10 日間経口投与の毒性試験において mg/kg/ 日で体温低下がみられているが ( ) 安全性薬理試験では軽度で一過性の影響であったことから臨床において重篤な中枢性の副作用を誘発する可能性は低いと考えられる また mg/kg を単回経口投与したときに 換気機能及び気道抵抗には影響は認められなかったことから GSK Bが臨床において呼吸系に影響を及ぼす可能性は低いと考えられた GSK Bは herg cdna を導入した HEK293 細胞において hergチャネルテール電流を抑制し IC25 IC50 及び IC75はそれぞれ 及び 5.30 μm( 及び ng/ml) であった p. 46
52 ウサギ左心室ウェッジ標本において GSK Bは 30 μm( 約 ng/ml; 溶解限界濃度 ) までの濃度で QT 間隔に影響を及ぼさなかった GSK Bは 10 及び 30 μmで等尺性収縮力をそれぞれ 16.3 及び 64.8% 低下させ 30 μmで Tp-e 間隔を約 26% 短縮させた 麻酔雄ビーグル犬において GSK A は 1 mg/kg の静脈内投与 (10 分間持続投与 ) により心電図パラメータ 血圧及び心拍数に影響を及ぼさなかった 血漿中 GSK 濃度は投与終了時 ( 投与開始 10 分後 ) に最高濃度の 2.5 μm( 約 1500 ng/ml) に達した 覚醒雄ビーグル犬において GSK Bは 及び mg/kg の単回経口投与により 動脈圧 心拍数 ECG パラメータ ( 波形異常 不整脈及び間隔 ) 及び体温に影響を及ぼさなかった 心血管系への影響を検討した試験において in vitro の電気生理学的試験である hergアッセイでは IC50=1.54 μm(947.7 ng/ml) で阻害作用がみられ ウサギ左心室ウェッジ標本を用いた試験では 10 μm 以上で影響が認められた これらの影響がみられた 1.54 μm (947.7 ng/ml) 及び 10 μm(6154 ng/ml) は日本人患者に GSK B の予定臨床用量である 2 mg を 1 日 1 回 15 日間経口投与 (n=5) したときの Cmax(25.5 ng/ml)( 表 ) 及びヒトにおける血漿蛋白結合率 (97.4%; ) から推定される非結合型 GSK 濃度である 0.66 ng/mlの 1400 倍超であると推定されることから ヒトで QT 延長を含む心臓の伝導異常を誘発する可能性は低いと考えられた また イヌの in vivo 試験では 最高血漿中 GSK 濃度が 2.5 μm( 約 1500 ng/ml) に達する 1 mg/kg の静脈内投与 (10 分間持続投与 ) でも影響は認められなかった このイヌにおける最高血漿中 GSK 濃度である 2.5 μm( 約 1500 ng/ml) は日本人患者に予定臨床用量である 2 mg を 1 日 1 回経口投与したときの Cmax(25.5 ng/ml)( 表 ) の約 60 倍であった 一方 イヌの in vivo 試験では影響は認められなかったが 臨床試験において観察された左室駆出率低下 ( ) のメカニズムを検討するための毒性試験において左室機能 ( 心拍出量 1 回拍出量 駆出率 左室内腔面積変化率及び左室内径短縮率 ) の低下がみられた ( ) 薬力学的薬物相互作用試験 臨床において併用される GSK との併用による薬理作用に関しては CTD 併用パ ートの 2.6.2(2.6.2 タフィンラー / メキニスト併用 ) に記載した 結論 GSK Bは MEK1/2 に対する選択的阻害薬であり BRAF V600E 遺伝子変異を有する悪性黒色腫に対して増殖抑制作用を発現することから BRAF V600 遺伝子変異を有する悪性黒色腫 に対する治療薬として期待される 参考文献 Akinleye A, Furqan M, Mukhi N, et al. MEK and the inhibitors: from bench to bedside. J Hematol Oncol. 2013;6:27(1-11) p. 47
53 Alcala AM, Flaherty KT. BRAF inhibitors for the treatment of metastatic melanoma: clinical trials and mechanisms of resistance. Clin Cancer Res. 2012;18:33-9. Ashida A, Uhara H, Kiniwa Y, et al. Assessment of BRAF and KIT mutations in Japanese melanoma patients. J Dermatol Sci. 2012;66: Bello DM, Ariyan CE, Carvajal RD. Melanoma mutagenesis and aberrant cell signaling. Cancer Control. 2013;20: Caunt CJ, Keyse SM. Dual-specificity MAP kinase phosphatases (MKPs): shaping the outcome of MAP kinase signalling. FEBS J. 2013;280: Davies H, Bignell GR, Cox C, et al. Mutations of the BRAF gene in human cancer. Nature. 2002;417: Delaney AM, Printen JA, Chen H, et al. Identification of a novel mitogen-activated protein kinase kinase activation domain recognized by the inhibitor PD Mol Cell Biol. 2002;22: Dick FA, Rubin SM. Molecular mechanisms underlying RB protein function. Nat Rev Mol Cell Biol. 2013;14: Furukawa T, Tanji E, Xu S, et al. Feedback regulation of DUSP6 transcription responding to MAPK1 via ETS2 in human cells. Biochem Biophys Res Commun. 2008;377: GlaxoSmithKline Document Number 2012N139008_00 Study ID 2012N139008_00. Estimating the minimum biologically active target concentration of GSK B for in vivo activity in sensitive BRAF mutant lines (melanoma and CRC). Report Date 10-May Khattar E, Kumar V. Mitogenic regulation of p27 Kip1 gene is mediated by AP-1 transcription factors. J Biol Chem. 2010;285: Lito P, Rosen N, Solit DB. Tumor adaptation and resistance to RAF inhibitors. Nat Med. 2013;19: Nissan MH, Solit DB. The SWOT of BRAF inhibition in melanoma: RAF inhibitors, MEK inhibitors or both?. Curr Oncol Rep. 2011;13: Roskoski R Jr. MEK1/2 dual-specificity protein kinases: structure and regulation. Biochem Biophys Res Commun. 2012;417:5-10. Santarpia L, Lippman SL, El-Naggar AK. Targeting the mitogen-activated protein kinase RAS-RAF signaling pathway in cancer therapy. Expert Opin Ther Targets. 2012;16: p. 48
54 Sasaki Y, Niu C, Makino R, et al. BRAF point mutations in primary melanoma show different prevalences by subtype. J Invest Dermatol. 2004;123: Wan PTC, Garnett MJ, Roe SM, et al. Mechanism of activation of the RAF-ERK signaling pathway by oncogenic mutations of B-RAF. Cell. 2004;116: Wellbrock C, Karasarides M, Marais R. The RAF proteins take centre stage. Nat Rev Mol Cell Biol. 2004;5: Yamaguchi T, Kakefuda R, Tajima N, et al. Antitumor activities of JTP (GSK ), a novel MEK1/2 inhibitor, on colorectal cancer cell lines in vitro and in vivo. Int J Oncol. 2011;39: Yan M, Templeton DJ. Identification of 2 serine residues of MEK-1 that are differentially phosphorylated during activation by raf and MEK kinase. J Biol Chem. 1994;269: p. 49
55 薬理試験の概要文 ( タフィンラー / メキニスト併用 ) まとめ GSK 及び GSK Bの併用療法に関連する in vitro 及び in vivo の効力を裏付ける試験成績について以下に示した また 臨床試験において GSK を投与した一部の患者でみられた発熱の機序を検討するため 安全性薬理試験のフォローアップ試験として サイトカイン遊離に及ぼす影響を検討するための in vitro 試験を実施しており ( タフィンラー CTD ) その試験成績のうち GSK 及び 3 種類の代謝物並びに GSK Bを併用処理したときの成績を記載した なお 試験には GSK A( 遊離塩基 ) 及び GSK B( ジメチルスルホキシド付加物 ) を使用した 投与量及び濃度はすべて遊離塩基に換算して記載した 効力を裏付ける試験 In vitro 試験 GSK 及び GSK Bのいずれに対しても感受性を示す BRAF V600E V600K 又は V600D 変異陽性のヒト悪性黒色腫由来細胞株を GSK 及び GSK B 存在下で培養したときに 14 株中 13 株で併用効果が認められた 一方 両被験物質の単独処理に対して感受性を示さなかった 2 株では 併用処理しても増殖抑制作用に変化はみられなかった GSK に対する耐性を獲得した BRAF V600E 変異陽性のヒト悪性黒色腫由来の細胞クローンを GSK 及び GSK B の併用下で培養すると 検討したすべての耐性細胞クローンにおいて併用効果が認められた 耐性細胞クローンを GSK で単独処理しても ERKリン酸化レベル並びにサイクリン D1 及び p27 蛋白レベルに変化はみられなかったが GSK 及び GSK Bの併用処理では ERKのリン酸化が阻害され G1 期停止のマーカーとなるサイクリン D1 蛋白レベルの低下及び p27 蛋白レベルの増加が認められた また GSK に対する耐性を獲得した BRAF V600K 変異陽性のヒト悪性黒色腫由来の細胞クローンにおいても 検討したすべての耐性細胞クローンにおいて併用効果が認められた ヒト悪性黒色腫由来細胞株及び GSK 耐性細胞クローンのいずれにおいても 両被験物質併用によるアポトーシスの誘導への併用効果はみられなかった In vivo 試験 BRAF V600E 変異陽性のヒト悪性黒色腫由来細胞株を用いたマウス異種移植モデルにおいて GSK 及び GSK Bの併用効果を様々な投与方法及び投与期間で投与して検討した ( 試験 1~7) その結果 GSK 及び GSK B を最大効果発現用量未満の用量で最長 90 日間併用投与することにより 腫瘍増殖抑制作用は単独投与に比べて増強され 作用がより長期間持続した 生存について検討した試験では GSK の 30 及び 100 mg/kg 並びに GSK Bの 1 mg/kg の各単独投与群と媒体群の生存曲線との間に有意差がみられた 各単独投与群では試験終了までに 10 例中 2~5 例が死亡したのに対し いずれの併用投与群も試験終了時点まで全例が生存し 媒体群と各併用群の生存曲線の間に p. 50
56 有意差がみられた 試験 1~7 のいずれの試験においても 併用投与の忍容性は良好であっ た 安全性薬理試験臨床試験において GSK 及び GSK B を併用投与することにより発熱の発現頻度の増加がみられたことから 発熱の機序を検討するためのフォローアップ試験の一環として ヒト PBMC 又は血液を GSK 及び 3 種類の代謝物並びに GSK Bを併用処理したときのサイトカイン遊離量又は血漿中サイトカイン濃度に及ぼす影響を in vitro で検討した その結果 GSK 及び 3 種類の代謝物並びに GSK Bは それぞれを単独処理したときと同様にいずれの組合わせの併用処理においても 発熱に関連すると考えられる 9 種類のサイトカイン (IFNα IFNγ IP-10 IL-1β IL-6 IL-8 IL-10 IL-12p70 及び TNF-α) の遊離を促進させなかった 効力を裏付ける試験 RAF 阻害薬は効果発現が早く 高い奏効率を示すことから BRAF V600E 変異陽性の転移性悪性黒色腫患者の治療を著しく進歩させた [Chapman, 2011] しかし 治療開始の 1 年以内に RAF 阻害薬に対する耐性腫瘍が出現し 効果が減弱することが報告されている [Lito, 2013; Alcala, 2012; Sullivan, 2013] RAF 阻害薬に対する耐性発現機序の一つとして MAPK 経路の再活性化が関与していると考えられている ( 図 )[Alcala, 2012] BRAF V600 変異陽性の悪性黒色腫に対して最初に承認されたベムラフェニブ及びそのアナログである PLX4720 に対して耐性を獲得した腫瘍細胞では MAPK 経路において RAFの上流に存在する NRAS 又は下流に存在する MEK1 の二次的活性化変異 あるいは CRAF 及び COTの過剰発現を介した再活性化がみられることが報告されている [Nazarian, 2010; Alcala, 2012; Emery, 2009] また インスリン様増殖因子 -1 受容体 (IGF-1R) 及び血小板由来増殖因子受容体 (PDGFR) 等の RAF 上流の受容体チロシンキナーゼ (RTK) の活性化も報告されている [Alcala, 2012] BRAF V600 変異陽性のヒト腫瘍細胞株を高濃度の GSK で 1 週間以上処理して耐性細胞クローンを単離し 耐性化にかかわる遺伝子変異及び耐性細胞クローンにおける細胞内シグナル伝達の変化について検討した試験成績もこれらの知見を支持しており NRAS 及び MEK1 の変異による MAPK 経路の再活性化が GSK に対する耐性獲得機序に関与していると考えられた ( タフィンラー CTD ) 以上より RAF 阻害薬及び MEK 阻害薬を併用投与して BRAF/MEKを同時に阻害することで 以下の可能性が考えられる 1. MAPK 経路を介した増殖シグナルをより確実に抑制することにより BRAF V600 変異陽性の腫瘍細胞に対する増殖抑制作用が増強される 2. 耐性発現機序の一つと考えられている MAPK 経路の再活性化を抑制し 耐性の発現を遅延させる p. 51
57 以下に RAF 阻害薬である GSK 及び MEK1/2 阻害薬である GSK B を併用 投与したときの腫瘍増殖抑制作用に関する試験成績を示した PDGFR-β: 血小板由来増殖因子受容体 -β IGF-1R: インスリン様増殖因子 -1 受容体 RTK: 受容体型チロシンキナーゼ GTP:guanosine triphosphate ( グアノシン三リン酸 ) 図 Data source: [Alcala, 2012] の Figure 2 BRAF V600 変異陽性の悪性黒色腫細胞における RAF 阻害薬に対する耐性発現機序 In vitro 試験 (GSK 及び GSK B の併用効果 ) BRAF V600 変異陽性のヒト悪性黒色腫由来細胞株及び GSK 耐性細胞クローンの 増殖に対する GSK 及び GSK B の併用効果について検討した p. 52
58 BRAF V600 変異陽性ヒト悪性黒色腫由来細胞株の増殖に及ぼす影響 細胞増殖抑制作用方法 BRAF V600 変異陽性 (V600E V600K 又は V600D) の 17 種類のヒト悪性黒色腫由来細胞株に GSK 又は GSK Bの単独 あるいは GSK 及び GSK Bの併用 ( モル濃度比 10:1) 処理の条件下で 72 時間培養した CellTiterGloアッセイにより生細胞数を計測し 併用処理したときの細胞増殖抑制作用を単独処理した場合と比較した (2011N116395_00) 併用効果は 以下の 2 種類の独立した解析方法により評価した コンビネーションインデックス (CI) 法 :Chou&Talalayの方法[Chou, 1984] により CIを算出し CI<0.9( 相乗効果 ) 0.9~1.1( 相加効果 ) 及び>1.1( 拮抗作用 ) と定義した 相加又は相乗効果がみられた場合に 併用効果ありと判断した Excess Over Highest Single Agent(EOHSA) 解析 : 併用によりどの程度細胞増殖抑制作用が増強したのかを定量した ( 併用処理及び単独処理 (GSK 又は GSK Bの効果の高かった方 ) 時の反応率の差を percentage points(ppt) で表した )[Liu, 2011] 単独での作用と比較して作用の増強がみられた ( プラスの ppt が得られた ) 場合に 併用効果ありと判断した 結果 BRAF V600E 変異陽性のヒト悪性黒色腫由来細胞株 11 株のうち GSK 及び GSK Bのいずれに対しても感受性を示した 9 株すべてに対して両被験物質の併用効果が認められた (CI 法 : 相乗的な増殖抑制作用 (CI=0.40~0.87) EOHSA 解析 : 細胞増殖抑制作用が増強 (EOHSA=14.1~25.4 ppt))( 表 ) 一方 GSK 又は GSK Bのいずれに対しても感受性を示さなかった SK-MEL-3 及び A2058 細胞株に対しては 併用効果は認められなかった BRAF V600K 変異陽性のヒト悪性黒色腫由来細胞株のうち GSK 及び GSK Bのいずれに対しても感受性を示した 4 株中 3 株では併用効果が認められた (CI 法 : 相加効果又は中程度の相乗効果 (CI=0.83~0.91)) EOHSA 解析 : 細胞増殖抑制作用が増強 (EOHSA=16.5~29.6 ppt)) 一方 残りの 1 株 (WW165) に対しては併用により CI 法での評価においてわずかではあるが各被験物質の単独処理に比べて細胞増殖抑制作用が減弱した (CI=1.18) また GSK に耐性 (IC50は>10000 nm) 及び GSK Bに低感受性 (IC50=45.4 nm) であった IGR-1 細胞株に対しては 併用により増殖抑制作用が増強した (EOHSA=10.2 ppt)(gsk 単独処理時の IC50が算出できなかったため CI 法では評価できず ) BRAF V600D 変異陽性のヒト悪性黒色腫由来 WM-115 細胞株に対しても GSK 及び GSK Bの併用効果が認められた (CI 法 : 相乗効果 (CI=0.64) EOHSA 解析 : 細胞増殖抑制作用が増強 (EOHSA=13.7 ppt)) p. 53
59 表 腫瘍細胞株 # BRAF V600 変異陽性のヒト悪性黒色腫由来細胞株に対する増殖抑制作用 BRAF アミノ酸変異 (GSK 及び GSK B の併用効果 ) IC50 (nm) GSK GSK B 併用 CI EOHSA (ppt) UACC ± ± ± ± ± 9.5 SK-MEL-1 18 ± ± ± ± ± 4.0 COLO ± ± ± ± ± 4.5 A101D V600E 33 ± ± ± ± ± 1.5 SK-MEL-24 ( ヘテロ変異体 ) 78 ± ± ± ± ± 0.6 SK-MEL ± ± ± ± ± 5.3 SK-MEL-3 >10000 >1000 >10000 NA NA A2058 a >10000 >1000 >10000 NA NA SK-MEL-28 b V600E UACC ± ± ± ± ± 3.9 ( ホモ変異体 ) A375P F WW165 V600K IGR-1 c ( ヘテロ変異体 ) > NA 10.2 YUMAC V600K YULAC ( ホモ変異体 ) YUSIT WM-115 V600D ( ヘテロ変異体 ) 41 ± ± ± ± ± 4.1 平均値 ± 標準偏差 (n=4~8) ただし SK-MEL-28 WW165 IGR-1 YUMAC YULAC 及び YUSIT1 細胞株 (n=2) 並びに A375P F11 細胞株 (n 2) については平均値を示す :GSK 及び GSK B を 10:1 のモル濃度比で併用したときの GSK 成分の IC50 NA: 単独処理時の IC50 が検討した濃度範囲外であったため CI は算出できず a:mek1 P124S, RB1 Q93* 変異陽性 b:cdk4 R24C 変異陽性 c:mek2 E66_K68del 変異陽性 Data source: 2011N116395_00 の Table アポトーシス誘導作用方法 で細胞増殖抑制作用を検討したヒト悪性黒色腫由来細胞株 17 株のうち BRAF V600E 変異陽性の 7 株及び V600K 変異陽性の 1 株 (GSK 及び GSK B に対して感受性株 6 株及び非感受性株 2 株 ) に GSK 又は GSK Bの単独 あるいは GSK 及び GSK Bの併用 ( モル濃度比 10:1) 処理の条件下で 24 時間培養した後 CaspaseGloアッセイによりアポトーシス誘導の指標となるカスパーゼ 3 及び 7 活性を測定した (2011N116395_00) 結果両被験物質に感受性を示した V600E 又は V600K 変異陽性のヒト悪性黒色腫由来細胞株 6 株中 1 株 (BRAF V600E 変異陽性の SK-MEL-1 細胞株 ) では両被験物質をそれぞれ単独処理したときに また 他の 1 株 (BRAF V600K 変異陽性の YUMAC 細胞株 ) では GSK Bを単独処理したときにアポトーシスの誘導がみられた ( それぞれの細胞株におけるカスパーゼ 3 及び 7 活性は媒体群と比較して約 5 及び 3 倍 ) それ以外の 4 株 (UACC-257 A101D UACC-62 及び A375P F11 細胞株 ) 及び両被験物質に対して非感受性の 2 株 (SK-MEL-3 及び A2058 細胞株 ) ではいずれの被験物質によってもアポトーシスの誘導はみられなかった 上述の 8 株を GSK 及び GSK B で併用処理しても それぞれを単独処理した場合と比較してアポトーシス誘導作用の増強はみられなかった p. 54
60 BRAF V600E 変異陽性ヒト悪性黒色腫由来 A375P F11 細胞株より単離した GSK 耐性細胞クローンに対する併用効果 BRAF V600E 変異陽性のヒト悪性黒色腫由来 A375P F11 細胞株 ( 親細胞株 ) 及び A375P F11 細胞株を高濃度の GSK で 1 週間以上培養して得た GSK 耐性細胞クローンを GSK 及び GSK B で処理し 細胞増殖抑制作用 細胞内シグナル伝達経路に及ぼす影響及びアポトーシス誘導作用に対する併用効果について検討した 細胞増殖抑制作用方法 GSK 耐性細胞クローンの増殖に対する GSK Bの単独及び GSK との併用効果を検討するために 高濃度の GSK での 1 週間以上の培養により GSK に対して耐性を獲得した 9 種類のサブクローン ( タフィンラー CTD 及びメキニスト CTD ) に GSK 又は GSK Bの単独 あるいは GSK 及び GSK Bの併用 ( モル濃度比 10:1) 処理の条件下で 72 時間培養し と同様の方法で増殖抑制作用の IC50 CI 及び EOHSAを算出し A375P F11 細胞株 ( 親細胞株 ) に対する作用と比較した (2011N116394_00) 結果 A375P F11 細胞株 ( 親細胞株 ) では各被験物質の単独処理により濃度依存的に細胞増殖が抑制され GSK 及び GSK B で併用処理すると 併用効果が認められた (CI 法 : 相乗的な増殖抑制作用 (CI=0.49) EOHSA 解析 : 細胞増殖抑制作用が増強 (EOHSA =19 ppt))( 表 ) GSK 耐性細胞クローン (GSK の IC50>10000 nm) を GSK 及び GSK Bで併用処理したときの GSK の IC50 は 178~392 nmであり いずれの耐性細胞クローンにおいても単独処理時と比較して IC50 は低下した ( 表 ) GSK Bに対しても感受性を示さなかった 3 種類の耐性細胞クローンを含む 9 種類すべての耐性細胞クローンに対して併用効果を EOHSA 解析で評価したところ GSK の細胞増殖抑制作用は単独処理したときに比べて高く 細胞増殖抑制作用は併用処理によって増強された (EOHSA=19~>50 ppts)( 耐性細胞クローンでは GSK 単独処理時の IC50 が算出できなかったため CI 法では評価できず ) p. 55
61 表 細胞株 A375P F11 細胞株より単離した耐性細胞クローンにおける GSK 及び GSK B の併用効果 ( 増殖抑制作用 ) 獲得変異 IC50 (nm) NRAS MEK1 GSK GSK B 併用 a CI EOHSA (ppt) A375P F11 ( 親細胞株 ) # WT WT 28 ± 16 5 ± 3 7 ± ± ± 1 12R5-3 A146T WT > ± ± 70 NA 28 ± 5 12R8-1 A146T WT > ± ± 136 NA 29 ± 8 12R8-3 A146T WT > ± ± 182 NA 27 ± 1 16R6-3 A146T P387S > ± ± 123 NA 36 ± 9 16R5-5 # Q61K P387S > ± ± 72 NA 36 ± 3 16R6-2 Q61K P387S > ± ± 57 NA 28 ± 8 16R6-4 # Q61K, A146T P387S >10000 > ± 169 NA >50 12R5-1 WT K59del >10000 > ± 149 NA 19 ± 1 12R5-5 # WT K59del >10000 > ± 101 NA 46 ± 12 平均値 ± 標準偏差 (n= 3) NA: 単独処理時の IC50 が検討した濃度範囲外であったため CI は算出できず a:gsk 及び GSK B を 10:1 のモル濃度比で併用したときの GSK 成分の IC50 #: シグナル伝達に及ぼす影響についても検討 ( 図 ) Data source: 2011N116394_00 の Table 細胞内シグナル伝達に及ぼす影響方法 A375P F11 細胞株 ( 親細胞株 ) 及び 3 種類の耐性細胞クローン (16R5-5:NRAS Q61K 変異及び MEK1 P387S 変異陽性 GSK B に対する感受性も 1/20 以下に低下 16R6-4: NRAS Q61K A146T 変異及び MEK1 P387S 変異陽性 GSK Bに対しても耐性 12R5-5:MEK1 K59del 変異陽性 GSK Bに対しても耐性 ) を GSK ( 又は 1000 nm) 及び GSK B(10 又は 30 nm) の単独又はそれらの併用で 24 時間培養した後 ウエスタンブロット法により MEK ERK S6リボソーム蛋白質 (S6P) 及び AKT(T308) のリン酸化レベル並びにサイクリン D1 及び p27 蛋白レベルを測定した (2011N116394_00) 結果 A375P F11 細胞株 ( 親細胞株 ) では ERK 及び S6P のリン酸化阻害 G1 期停止のマーカーとなるサイクリン D1 蛋白レベルの低下及び p27 蛋白レベルの増加がみられた ( 図 の左上 ) 3 種類の耐性細胞クローン (NRAS 又は MEK1 変異陽性であり GSK B に対しても感受性が低下あるいは耐性を示す ) のいずれにおいても GSK は単独処理では ERK 及び S6P リン酸化並びにサイクリン D1 及び p27 蛋白レベルに影響を及ぼさなかった ( 図 の右上及び下段 ) 一方 いずれの耐性細胞クローンに対しても 両被験物質は併用により GSK B の単独処理と比較して ERKリン酸化阻害作用を増強し G1 期停止のマーカーとなるサイクリン D1 蛋白レベルの低下及び p27 蛋白レベルの増加がみられた また AKT のリン酸化をわずかに阻害した しかし 併用しても S6Pのリン酸化に対してはわずかに阻害するか又はまったく阻害作用を示さなかった p. 56
62 A375:A375P F11 細胞株 GSK212:GSK B ( レーン 5 及び 9が GSK Bの単独処理に該当 ) 図 A375P F11 細胞株より単離した耐性細胞クローンにおける GSK 及び GSK Bの併用効果 ( 細胞内シグナル伝達に及ぼす影響 ) Data source: 2011N116394_00の Figure アポトーシス誘導作用方法 A375P F11 細胞株 ( 親細胞株 ) 及び耐性細胞クローンを GSK 又は GSK B の単独 あるいは GSK 及び GSK Bの併用 ( モル濃度比 10:1) 処理の条件下で 24 時間培養した後 と同様の方法でカスパーゼ 3/7 活性を測定した (2011N116394_00) 結果親細胞株及び耐性細胞クローンのいずれにおいても 各被験物質は単独及び併用処理のいずれでもアポトーシスを誘導しなかった BRAF V600K 変異陽性ヒト悪性黒色腫由来 YUSIT1 細胞株より単離した GSK 耐性細胞クローンに対する併用効果方法 BRAF V600K 変異陽性ヒト悪性黒色腫由来 YUSIT1 細胞株及び YUSIT1 細胞株を高濃度の GSK で 1 週間以上培養して得た GSK 耐性細胞クローンの増殖に対する GSK 及び GSK B の併用効果を と同様の方法で検討し 増殖抑制作用の IC50 CI 及び EOHSA を算出した (2011N116394_00) p. 57
1. Caov-3 細胞株 A2780 細胞株においてシスプラチン単剤 シスプラチンとトポテカン併用添加での殺細胞効果を MTS assay を用い検討した 2. Caov-3 細胞株においてシスプラチンによって誘導される Akt の活性化に対し トポテカンが影響するか否かを調べるために シスプラチ
 ( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 朝日通雄 恒遠啓示 副査副査 瀧内比呂也谷川允彦 副査 勝岡洋治 主論文題名 Topotecan as a molecular targeting agent which blocks the Akt and VEGF cascade in platinum-resistant ovarian cancers ( 白金製剤耐性卵巣癌における
( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 朝日通雄 恒遠啓示 副査副査 瀧内比呂也谷川允彦 副査 勝岡洋治 主論文題名 Topotecan as a molecular targeting agent which blocks the Akt and VEGF cascade in platinum-resistant ovarian cancers ( 白金製剤耐性卵巣癌における
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社
 オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
るが AML 細胞における Notch シグナルの正確な役割はまだわかっていない mtor シグナル伝達系も白血病細胞の増殖に関与しており Palomero らのグループが Notch と mtor のクロストークについて報告している その報告によると 活性型 Notch が HES1 の発現を誘導
 学位論文の内容の要旨 論文提出者氏名 奥橋佑基 論文審査担当者 主査三浦修副査水谷修紀 清水重臣 論文題目 NOTCH knockdown affects the proliferation and mtor signaling of leukemia cells ( 論文内容の要旨 ) < 要旨 > 目的 : sirna を用いた NOTCH1 と NOTCH2 の遺伝子発現の抑制の 白血病細胞の細胞増殖と下流のシグナル伝達系に対する効果を解析した
学位論文の内容の要旨 論文提出者氏名 奥橋佑基 論文審査担当者 主査三浦修副査水谷修紀 清水重臣 論文題目 NOTCH knockdown affects the proliferation and mtor signaling of leukemia cells ( 論文内容の要旨 ) < 要旨 > 目的 : sirna を用いた NOTCH1 と NOTCH2 の遺伝子発現の抑制の 白血病細胞の細胞増殖と下流のシグナル伝達系に対する効果を解析した
Microsoft Word - FHA_13FD0159_Y.doc
 1 要約 Pin1 inhibitor PiB prevents tumor progression by inactivating NF-κB in a HCC xenograft mouse model (HCC 皮下移植マウスモデルにおいて Pin1 インヒビターである PiB は NF-κB 活性を低下させることにより腫瘍進展を抑制する ) 千葉大学大学院医学薬学府先端医学薬学専攻 ( 主任
1 要約 Pin1 inhibitor PiB prevents tumor progression by inactivating NF-κB in a HCC xenograft mouse model (HCC 皮下移植マウスモデルにおいて Pin1 インヒビターである PiB は NF-κB 活性を低下させることにより腫瘍進展を抑制する ) 千葉大学大学院医学薬学府先端医学薬学専攻 ( 主任
グルコースは膵 β 細胞内に糖輸送担体を介して取り込まれて代謝され A T P が産生される その結果 A T P 感受性 K チャンネルの閉鎖 細胞膜の脱分極 電位依存性 Caチャンネルの開口 細胞内 Ca 2+ 濃度の上昇が起こり インスリンが分泌される これをインスリン分泌の惹起経路と呼ぶ イ
 薬効薬理 1. 作用機序 アナグリプチンはジペプチジルペプチダーゼ -4(DPP-4) の競合的かつ可逆的な選択的阻害剤である インクレチンであるグルカゴン様ペプチド-1(GL P-1) 及びグルコース依存性インスリン分泌刺激ポリペプチド (GI P) は グルコース依存的なインスリン分泌促進作用やグルカゴン分泌抑制作用等 ( 主にGLP-1の作用 ) を有するが 24) DPP-4により分解されて活性を失う
薬効薬理 1. 作用機序 アナグリプチンはジペプチジルペプチダーゼ -4(DPP-4) の競合的かつ可逆的な選択的阻害剤である インクレチンであるグルカゴン様ペプチド-1(GL P-1) 及びグルコース依存性インスリン分泌刺激ポリペプチド (GI P) は グルコース依存的なインスリン分泌促進作用やグルカゴン分泌抑制作用等 ( 主にGLP-1の作用 ) を有するが 24) DPP-4により分解されて活性を失う
日本標準商品分類番号 カリジノゲナーゼの血管新生抑制作用 カリジノゲナーゼは強力な血管拡張物質であるキニンを遊離することにより 高血圧や末梢循環障害の治療に広く用いられてきた 最近では 糖尿病モデルラットにおいて増加する眼内液中 VEGF 濃度を低下させることにより 血管透過性を抑制す
 日本標準商品分類番号 872491 カリジノゲナーゼの血管新生抑制作用 カリジノゲナーゼは強力な血管拡張物質であるキニンを遊離することにより 高血圧や末梢循環障害の治療に広く用いられてきた 最近では 糖尿病モデルラットにおいて増加する眼内液中 VEGF 濃度を低下させることにより 血管透過性を抑制することが示されたが 血管新生に対するカリジノゲナーゼの影響を評価した報告はない そこで今回 網膜血管新生に対するカリジノゲナーゼの役割を同定するため
日本標準商品分類番号 872491 カリジノゲナーゼの血管新生抑制作用 カリジノゲナーゼは強力な血管拡張物質であるキニンを遊離することにより 高血圧や末梢循環障害の治療に広く用いられてきた 最近では 糖尿病モデルラットにおいて増加する眼内液中 VEGF 濃度を低下させることにより 血管透過性を抑制することが示されたが 血管新生に対するカリジノゲナーゼの影響を評価した報告はない そこで今回 網膜血管新生に対するカリジノゲナーゼの役割を同定するため
関係があると報告もされており 卵巣明細胞腺癌において PI3K 経路は非常に重要であると考えられる PI3K 経路が活性化すると mtor ならびに HIF-1αが活性化することが知られている HIF-1αは様々な癌種における薬理学的な標的の一つであるが 卵巣癌においても同様である そこで 本研究で
 ( 様式甲 5) 氏 名 髙井雅聡 ( ふりがな ) ( たかいまさあき ) 学 位 の 種 類 博士 ( 医学 ) 学位授与番号 甲 第 号 学位審査年月日 平成 27 年 7 月 8 日 学位授与の要件 学位規則第 4 条第 1 項該当 Crosstalk between PI3K and Ras pathways via 学位論文題名 Protein Phosphatase 2A in human
( 様式甲 5) 氏 名 髙井雅聡 ( ふりがな ) ( たかいまさあき ) 学 位 の 種 類 博士 ( 医学 ) 学位授与番号 甲 第 号 学位審査年月日 平成 27 年 7 月 8 日 学位授与の要件 学位規則第 4 条第 1 項該当 Crosstalk between PI3K and Ras pathways via 学位論文題名 Protein Phosphatase 2A in human
Microsoft Word - 第14回定例会_金納様_final.doc
 クロスオーバー実験のデザインと解析 - テレメトリー法による QT/QTc 試験の実データを用いた検討 - I. テレメトリー法による QT/QTc 試験について 1) イヌを用いたテレメトリー QT/QTc 試験の実際 金納明宏 薬理統計グループ安全性薬理チーム 要約 : 医薬品開発の非臨床試験で, 安全性薬理試験の QT/QTc 延長を評価する in vivo テレメトリー試験は, ヒトでの不整脈発現を評価する上で非常に重要な試験である.
クロスオーバー実験のデザインと解析 - テレメトリー法による QT/QTc 試験の実データを用いた検討 - I. テレメトリー法による QT/QTc 試験について 1) イヌを用いたテレメトリー QT/QTc 試験の実際 金納明宏 薬理統計グループ安全性薬理チーム 要約 : 医薬品開発の非臨床試験で, 安全性薬理試験の QT/QTc 延長を評価する in vivo テレメトリー試験は, ヒトでの不整脈発現を評価する上で非常に重要な試験である.
報道発表資料 2006 年 4 月 13 日 独立行政法人理化学研究所 抗ウイルス免疫発動機構の解明 - 免疫 アレルギー制御のための新たな標的分子を発見 - ポイント 異物センサー TLR のシグナル伝達機構を解析 インターフェロン産生に必須な分子 IKK アルファ を発見 免疫 アレルギーの有効
 60 秒でわかるプレスリリース 2006 年 4 月 13 日 独立行政法人理化学研究所 抗ウイルス免疫発動機構の解明 - 免疫 アレルギー制御のための新たな標的分子を発見 - がんやウイルスなど身体を蝕む病原体から身を守る物質として インターフェロン が注目されています このインターフェロンのことは ご存知の方も多いと思いますが 私たちが生まれながらに持っている免疫をつかさどる物質です 免疫細胞の情報の交換やウイルス感染に強い防御を示す役割を担っています
60 秒でわかるプレスリリース 2006 年 4 月 13 日 独立行政法人理化学研究所 抗ウイルス免疫発動機構の解明 - 免疫 アレルギー制御のための新たな標的分子を発見 - がんやウイルスなど身体を蝕む病原体から身を守る物質として インターフェロン が注目されています このインターフェロンのことは ご存知の方も多いと思いますが 私たちが生まれながらに持っている免疫をつかさどる物質です 免疫細胞の情報の交換やウイルス感染に強い防御を示す役割を担っています
ータについては Table 3 に示した 両製剤とも投与後血漿中ロスバスタチン濃度が上昇し 試験製剤で 4.7±.7 時間 標準製剤で 4.6±1. 時間に Tmaxに達した また Cmaxは試験製剤で 6.3±3.13 標準製剤で 6.8±2.49 であった AUCt は試験製剤で 62.24±2
 ロスバスタチン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロスバスタチンは HMG-CoA 還元酵素を競合的に阻害することにより HMG-CoA のメバロン酸への変更を減少させ コレステロール生合成における早期の律速段階を抑制する高コレステロール血症治療剤である 今回 ロスバスタチン錠 mg TCK とクレストール 錠 mg の生物学的同等性を検討するため
ロスバスタチン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロスバスタチンは HMG-CoA 還元酵素を競合的に阻害することにより HMG-CoA のメバロン酸への変更を減少させ コレステロール生合成における早期の律速段階を抑制する高コレステロール血症治療剤である 今回 ロスバスタチン錠 mg TCK とクレストール 錠 mg の生物学的同等性を検討するため
学位論文の内容の要旨 論文提出者氏名 小川憲人 論文審査担当者 主査田中真二 副査北川昌伸 渡邉守 論文題目 Clinical significance of platelet derived growth factor -C and -D in gastric cancer ( 論文内容の要旨 )
 学位論文の内容の要旨 論文提出者氏名 小川憲人 論文審査担当者 主査田中真二 副査北川昌伸 渡邉守 論文題目 Clinical significance of platelet derived growth factor -C and -D in gastric cancer ( 論文内容の要旨 ) < 要旨 > platelet derived growth factor (PDGF 血小板由来成長因子)-C,
学位論文の内容の要旨 論文提出者氏名 小川憲人 論文審査担当者 主査田中真二 副査北川昌伸 渡邉守 論文題目 Clinical significance of platelet derived growth factor -C and -D in gastric cancer ( 論文内容の要旨 ) < 要旨 > platelet derived growth factor (PDGF 血小板由来成長因子)-C,
ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル
 ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル 1mg は 1 カプセル中ロペラミド塩酸塩 1 mg を含有し消化管から吸収されて作用を発現する このことから
ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル 1mg は 1 カプセル中ロペラミド塩酸塩 1 mg を含有し消化管から吸収されて作用を発現する このことから
大学院博士課程共通科目ベーシックプログラム
 平成 30 年度医科学専攻共通科目 共通基礎科目実習 ( 旧コア実習 ) 概要 1 ). 大学院生が所属する教育研究分野における実習により単位認定可能な実習項目 ( コア実習項目 ) 1. 組換え DNA 技術実習 2. 生体物質の調製と解析実習 3. 薬理学実習 4. ウイルス学実習 5. 免疫学実習 6. 顕微鏡試料作成法実習 7. ゲノム医学実習 8. 共焦点レーザー顕微鏡実習 2 ). 実習を担当する教育研究分野においてのみ単位認定可能な実習項目
平成 30 年度医科学専攻共通科目 共通基礎科目実習 ( 旧コア実習 ) 概要 1 ). 大学院生が所属する教育研究分野における実習により単位認定可能な実習項目 ( コア実習項目 ) 1. 組換え DNA 技術実習 2. 生体物質の調製と解析実習 3. 薬理学実習 4. ウイルス学実習 5. 免疫学実習 6. 顕微鏡試料作成法実習 7. ゲノム医学実習 8. 共焦点レーザー顕微鏡実習 2 ). 実習を担当する教育研究分野においてのみ単位認定可能な実習項目
ソラフェニブ 薬理試験の概要文 効力を裏付ける試験 in vitro 試験ソラフェニブは当初, 生化学的検討により C-RAF 阻害物質の構造 - 活性相関を評価する過程で発見された新規化合物である ソラフェニブの活性について in vitro で行っ
 2.6.2.2 効力を裏付ける試験 2.6.2.2.1 in vitro 試験は当初, 生化学的検討により C-RAF 阻害物質の構造 - 活性相関を評価する過程で発見された新規化合物である の活性について in vitro で行った試験の結果を, 表 2.6.2-1 にまとめた 以下に, 表に示した各試験の方法の概略について記載する キナーゼ阻害活性 RAF (C-RAF, B-RAF 及び V0E
2.6.2.2 効力を裏付ける試験 2.6.2.2.1 in vitro 試験は当初, 生化学的検討により C-RAF 阻害物質の構造 - 活性相関を評価する過程で発見された新規化合物である の活性について in vitro で行った試験の結果を, 表 2.6.2-1 にまとめた 以下に, 表に示した各試験の方法の概略について記載する キナーゼ阻害活性 RAF (C-RAF, B-RAF 及び V0E
3. 安全性本治験において治験薬が投与された 48 例中 1 例 (14 件 ) に有害事象が認められた いずれの有害事象も治験薬との関連性は あり と判定されたが いずれも軽度 で処置の必要はなく 追跡検査で回復を確認した また 死亡 その他の重篤な有害事象が認められなか ったことから 安全性に問
 フェキソフェナジン塩酸塩錠 6mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにフェキソフェナジン塩酸塩は 第二世代抗ヒスタミン薬の一つであり 抗原抗体反応に伴って起こる肥満細胞からのヒスタミンなどのケミカルメディエーターの遊離を抑制すると共に ヒスタミンの H1 作用に拮抗することにより アレルギー症状を緩和する 今回 フェキソフェナジン塩酸塩錠 6mg
フェキソフェナジン塩酸塩錠 6mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにフェキソフェナジン塩酸塩は 第二世代抗ヒスタミン薬の一つであり 抗原抗体反応に伴って起こる肥満細胞からのヒスタミンなどのケミカルメディエーターの遊離を抑制すると共に ヒスタミンの H1 作用に拮抗することにより アレルギー症状を緩和する 今回 フェキソフェナジン塩酸塩錠 6mg
ピルシカイニド塩酸塩カプセル 50mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにピルジカイニド塩酸塩水和物は Vaughan Williams らの分類のクラスⅠCに属し 心筋の Na チャンネル抑制作用により抗不整脈作用を示す また 消化管から速やかに
 ピルシカイニド塩酸塩カプセル 50mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにピルジカイニド塩酸塩水和物は Vaughan Williams らの分類のクラスⅠCに属し 心筋の Na チャンネル抑制作用により抗不整脈作用を示す また 消化管から速やかに吸収され 体内でもほとんど代謝を受けない頻脈性不整脈 ( 心室性 ) に優れた有効性をもつ不整脈治療剤である
ピルシカイニド塩酸塩カプセル 50mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにピルジカイニド塩酸塩水和物は Vaughan Williams らの分類のクラスⅠCに属し 心筋の Na チャンネル抑制作用により抗不整脈作用を示す また 消化管から速やかに吸収され 体内でもほとんど代謝を受けない頻脈性不整脈 ( 心室性 ) に優れた有効性をもつ不整脈治療剤である
前立腺癌は男性特有の癌で 米国においては癌死亡者数の第 2 位 ( 約 20%) を占めてい ます 日本でも前立腺癌の罹患率 死亡者数は急激に上昇しており 現在は重篤な男性悪性腫瘍疾患の1つとなって図 1 います 図 1 初期段階の前立腺癌は男性ホルモン ( アンドロゲン ) に反応し増殖します そ
 再発した前立腺癌の増殖を制御する新たな分子メカニズムの発見乳癌治療薬が効果的 発表者筑波大学先端領域学際研究センター教授柳澤純 (junny@agbi.tsukuba.ac.jp TEL: 029-853-7320) ポイント 女性ホルモンが制御する新たな前立腺癌の増殖 細胞死メカニズムを発見 女性ホルモン及び女性ホルモン抑制剤は ERβ 及び KLF5 を通じ FOXO1 の発現量を変化することで前立腺癌の増殖
再発した前立腺癌の増殖を制御する新たな分子メカニズムの発見乳癌治療薬が効果的 発表者筑波大学先端領域学際研究センター教授柳澤純 (junny@agbi.tsukuba.ac.jp TEL: 029-853-7320) ポイント 女性ホルモンが制御する新たな前立腺癌の増殖 細胞死メカニズムを発見 女性ホルモン及び女性ホルモン抑制剤は ERβ 及び KLF5 を通じ FOXO1 の発現量を変化することで前立腺癌の増殖
( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 教授 大道正英 髙橋優子 副査副査 教授教授 岡 田 仁 克 辻 求 副査 教授 瀧内比呂也 主論文題名 Versican G1 and G3 domains are upregulated and latent trans
 ( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 大道正英 髙橋優子 副査副査 岡 田 仁 克 辻 求 副査 瀧内比呂也 主論文題名 Versican G1 and G3 domains are upregulated and latent transforming growth factor- binding protein-4 is downregulated in breast
( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 大道正英 髙橋優子 副査副査 岡 田 仁 克 辻 求 副査 瀧内比呂也 主論文題名 Versican G1 and G3 domains are upregulated and latent transforming growth factor- binding protein-4 is downregulated in breast
シプロフロキサシン錠 100mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを
 シプロフロキサシン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを有し 上気道感染症 尿路感染症 皮膚感染症などに有効なニューキノロン系の合成抗菌剤である シプロキサン 錠
シプロフロキサシン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを有し 上気道感染症 尿路感染症 皮膚感染症などに有効なニューキノロン系の合成抗菌剤である シプロキサン 錠
あった AUCtはで ± ng hr/ml で ± ng hr/ml であった 2. バイオアベイラビリティの比較およびの薬物動態パラメータにおける分散分析の結果を Table 4 に示した また 得られた AUCtおよび Cmaxについてとの対数値
 モンテルカストチュアブル錠 5mg TCK の生物学的同等性試験 ( 口中溶解後 水なし投与 ) バイオアベイラビリティの比較 辰巳化学株式会社 はじめにモンテルカストナトリウムは アレルギーのメディエーターの 1 つであるロイコトリエン (LT) の受容体の内 cyslt1 受容体を遮断する抗アレルギー薬である 今回 モンテルカストチュアブル錠 5mg TCK とキプレス チュアブル錠 5mg の生物学的同等性を検討するため
モンテルカストチュアブル錠 5mg TCK の生物学的同等性試験 ( 口中溶解後 水なし投与 ) バイオアベイラビリティの比較 辰巳化学株式会社 はじめにモンテルカストナトリウムは アレルギーのメディエーターの 1 つであるロイコトリエン (LT) の受容体の内 cyslt1 受容体を遮断する抗アレルギー薬である 今回 モンテルカストチュアブル錠 5mg TCK とキプレス チュアブル錠 5mg の生物学的同等性を検討するため
テイカ製薬株式会社 社内資料
 テイカ製薬株式会社社内資料 アレルギー性結膜炎治療剤トラニラスト点眼液.5% TS TRANILAST Ophthalmic Solution.5% TS 生物学的同等性に関する資料 発売元 : 興和株式会社 製造販売元 : テイカ製薬株式会社 9 年 月作成 TSTR5BE9 ラット及びモルモットアレルギー性結膜炎モデルにおける生物学的同等性試験 Ⅰ. 試験の目的トラニラスト点眼液.5% TS および標準製剤の生物学的同等性をラット受動感作アレルギー性結膜炎モデル及びモルモット能動感作アレルギー性結膜炎モデルを用い薬力学的に検討した
テイカ製薬株式会社社内資料 アレルギー性結膜炎治療剤トラニラスト点眼液.5% TS TRANILAST Ophthalmic Solution.5% TS 生物学的同等性に関する資料 発売元 : 興和株式会社 製造販売元 : テイカ製薬株式会社 9 年 月作成 TSTR5BE9 ラット及びモルモットアレルギー性結膜炎モデルにおける生物学的同等性試験 Ⅰ. 試験の目的トラニラスト点眼液.5% TS および標準製剤の生物学的同等性をラット受動感作アレルギー性結膜炎モデル及びモルモット能動感作アレルギー性結膜炎モデルを用い薬力学的に検討した
 ,...~,.'~ 表 2.6.2.2-26 試験管内 PAE 菌株薬剤 MIC (µg/ml) PAE (h) 1 MIC 4 MIC STFX 0.025 0.92 2.35 S. aureus FDA 209-P LVFX 0.20 0.68 2.68 CPFX 0.20 1.05 1.59 SPFX 0.10 0.35 1.07 STFX 0.025 2.33 1.14 E. coli KL-16
,...~,.'~ 表 2.6.2.2-26 試験管内 PAE 菌株薬剤 MIC (µg/ml) PAE (h) 1 MIC 4 MIC STFX 0.025 0.92 2.35 S. aureus FDA 209-P LVFX 0.20 0.68 2.68 CPFX 0.20 1.05 1.59 SPFX 0.10 0.35 1.07 STFX 0.025 2.33 1.14 E. coli KL-16
論文題目 腸管分化に関わるmiRNAの探索とその発現制御解析
 論文題目 腸管分化に関わる microrna の探索とその発現制御解析 氏名日野公洋 1. 序論 microrna(mirna) とは細胞内在性の 21 塩基程度の機能性 RNA のことであり 部分的相補的な塩基認識を介して標的 RNA の翻訳抑制や不安定化を引き起こすことが知られている mirna は細胞分化や増殖 ガン化やアポトーシスなどに関与していることが報告されており これら以外にも様々な細胞諸現象に関与していると考えられている
論文題目 腸管分化に関わる microrna の探索とその発現制御解析 氏名日野公洋 1. 序論 microrna(mirna) とは細胞内在性の 21 塩基程度の機能性 RNA のことであり 部分的相補的な塩基認識を介して標的 RNA の翻訳抑制や不安定化を引き起こすことが知られている mirna は細胞分化や増殖 ガン化やアポトーシスなどに関与していることが報告されており これら以外にも様々な細胞諸現象に関与していると考えられている
Microsoft Word - 第14回定例会_平田様_final .doc
 クロスオーバー実験のデザインと解析 - テレメトリー法によ る QT/QTc 試験の実データを用いた検討 - II. クロスオーバー実験の統計解析 4) 有意差検定と信頼区間方式の解析の比較 平田篤由 薬理統計グループ安全性薬理チーム 要約 : ヒトの QT/QTc 評価試験における判断基準は,QTc 間隔の 95% 信頼区間の上限が 10ms を越えるかどうかである. 一方, 非臨床試験のイヌを用いたテレメトリー
クロスオーバー実験のデザインと解析 - テレメトリー法によ る QT/QTc 試験の実データを用いた検討 - II. クロスオーバー実験の統計解析 4) 有意差検定と信頼区間方式の解析の比較 平田篤由 薬理統計グループ安全性薬理チーム 要約 : ヒトの QT/QTc 評価試験における判断基準は,QTc 間隔の 95% 信頼区間の上限が 10ms を越えるかどうかである. 一方, 非臨床試験のイヌを用いたテレメトリー
Page 2 略語一覧表 略語 英語名 和名 ATP adenosine triphosphate アデノシン三リン酸 APD 50 action potential duration at 50% 50% 活動電位持続時間 repolarization APD 90 action potentia
 Page 1 タルセバ錠 25, 100, 150 mg ( エルロチニブ塩酸塩 ) 第 2 部資料概要 2.6.3 薬理試験概要表 中外製薬株式会社 Page 2 略語一覧表 略語 英語名 和名 ATP adenosine triphosphate アデノシン三リン酸 APD 50 action potential duration at 50% 50% 活動電位持続時間 repolarization
Page 1 タルセバ錠 25, 100, 150 mg ( エルロチニブ塩酸塩 ) 第 2 部資料概要 2.6.3 薬理試験概要表 中外製薬株式会社 Page 2 略語一覧表 略語 英語名 和名 ATP adenosine triphosphate アデノシン三リン酸 APD 50 action potential duration at 50% 50% 活動電位持続時間 repolarization
使用上の注意 1. 慎重投与 ( 次の患者には慎重に投与すること ) 1 2X X 重要な基本的注意 1TNF 2TNF TNF 3 X - CT X 4TNFB HBsHBcHBs B B B B 5 6TNF 7 8dsDNA d
 2015 5 7 201410 28 TNF 阻害薬 TNFFab シムジア 皮下注 200mg シリンジ Cimzia 200mg Syringe for S.C. Injection セルトリズマブペゴル ( 遺伝子組換え ) 製剤 873999 22400AMX01488000 20132 20133 20155 20079 警告 1. 2. 1 2 X - CT 3. TNF 4. 1 禁忌
2015 5 7 201410 28 TNF 阻害薬 TNFFab シムジア 皮下注 200mg シリンジ Cimzia 200mg Syringe for S.C. Injection セルトリズマブペゴル ( 遺伝子組換え ) 製剤 873999 22400AMX01488000 20132 20133 20155 20079 警告 1. 2. 1 2 X - CT 3. TNF 4. 1 禁忌
結果 この CRE サイトには転写因子 c-jun, ATF2 が結合することが明らかになった また これら の転写因子は炎症性サイトカイン TNFα で刺激したヒト正常肝細胞でも活性化し YTHDC2 の転写 に寄与していることが示唆された ( 参考論文 (A), 1; Tanabe et al.
 氏名 ( 本籍 ) 田辺敦 ( 神奈川県 ) 学位の種類博士 ( 学術 ) 学位記番号学位授与年月日学位授与の要件学位論文題名 甲第 64 号平成 28 年 3 月 15 日学位規則第 3 条第 2 項該当 RNA ヘリカーゼ YTHDC2 の転写制御機構と癌転移における YTHDC2 の 役割についての解析 論文審査委員 ( 主査 ) 佐原弘益 ( 副査 ) 村上賢 滝沢達也 代田欣二 論文内容の要旨
氏名 ( 本籍 ) 田辺敦 ( 神奈川県 ) 学位の種類博士 ( 学術 ) 学位記番号学位授与年月日学位授与の要件学位論文題名 甲第 64 号平成 28 年 3 月 15 日学位規則第 3 条第 2 項該当 RNA ヘリカーゼ YTHDC2 の転写制御機構と癌転移における YTHDC2 の 役割についての解析 論文審査委員 ( 主査 ) 佐原弘益 ( 副査 ) 村上賢 滝沢達也 代田欣二 論文内容の要旨
Microsoft PowerPoint - 2_(廣瀬宗孝).ppt
 TrkA を標的とした疼痛と腫瘍増殖 に効果のあるペプチド 福井大学医学部 器官制御医学講座麻酔 蘇生学領域 准教授 廣瀬宗孝 1 研究背景 癌による痛みはWHOの指針に沿って治療すれば 8 割の患者さんで痛みが取れ 残りの内 1 割は痛みの専門医の治療を受ければ痛みが取れる しかし最後の1 割は QOLを良好に保ったまま痛み治療を行うことは困難であるのが現状である TrkAは神経成長因子 (NGF)
TrkA を標的とした疼痛と腫瘍増殖 に効果のあるペプチド 福井大学医学部 器官制御医学講座麻酔 蘇生学領域 准教授 廣瀬宗孝 1 研究背景 癌による痛みはWHOの指針に沿って治療すれば 8 割の患者さんで痛みが取れ 残りの内 1 割は痛みの専門医の治療を受ければ痛みが取れる しかし最後の1 割は QOLを良好に保ったまま痛み治療を行うことは困難であるのが現状である TrkAは神経成長因子 (NGF)
記載データ一覧 品目名 製造販売業者 BE 品質再評価 1 マグミット錠 250mg 協和化学工業 2 酸化マグネシウム錠 250mg TX みらいファーマ 3 酸化マグネシウム錠 250mg モチダ 持田製薬販売 # 4 酸化マグネシウム錠 250mg マイラン マイラン製薬 # 5 酸化マグネシ
 医療用医薬品最新品質情報集 ( ブルーブック ) 2017.7.7 初版 有効成分 酸化マグネシウム 品目名 ( 製造販売業者 ) 1 マグミット錠 250mg 協和化学工業 後発医薬品 2 酸化マグネシウム錠 250mg TX みらいファーマ 3 酸化マグネシウム錠 250mg モチダ 持田製薬販売 4 酸化マグネシウム錠 250mg マイラン マイラン製薬 5 酸化マグネシウム錠 250mg ケンエー
医療用医薬品最新品質情報集 ( ブルーブック ) 2017.7.7 初版 有効成分 酸化マグネシウム 品目名 ( 製造販売業者 ) 1 マグミット錠 250mg 協和化学工業 後発医薬品 2 酸化マグネシウム錠 250mg TX みらいファーマ 3 酸化マグネシウム錠 250mg モチダ 持田製薬販売 4 酸化マグネシウム錠 250mg マイラン マイラン製薬 5 酸化マグネシウム錠 250mg ケンエー
解禁日時 :2019 年 2 月 4 日 ( 月 ) 午後 7 時 ( 日本時間 ) プレス通知資料 ( 研究成果 ) 報道関係各位 2019 年 2 月 1 日 国立大学法人東京医科歯科大学 国立研究開発法人日本医療研究開発機構 IL13Rα2 が血管新生を介して悪性黒色腫 ( メラノーマ ) を
 解禁日時 :2019 年 2 月 4 日 ( 月 ) 午後 7 時 ( 日本時間 ) プレス通知資料 ( 研究成果 ) 報道関係各位 2019 年 2 月 1 日 国立大学法人東京医科歯科大学 国立研究開発法人日本医療研究開発機構 IL13Rα2 が血管新生を介して悪性黒色腫 ( メラノーマ ) を進展させるしくみを解明 難治がんである悪性黒色腫の新規分子標的治療法の開発に期待 ポイント 難治がんの一つである悪性黒色腫
解禁日時 :2019 年 2 月 4 日 ( 月 ) 午後 7 時 ( 日本時間 ) プレス通知資料 ( 研究成果 ) 報道関係各位 2019 年 2 月 1 日 国立大学法人東京医科歯科大学 国立研究開発法人日本医療研究開発機構 IL13Rα2 が血管新生を介して悪性黒色腫 ( メラノーマ ) を進展させるしくみを解明 難治がんである悪性黒色腫の新規分子標的治療法の開発に期待 ポイント 難治がんの一つである悪性黒色腫
博士の学位論文審査結果の要旨
 博士の学位論文審査結果の要旨 申請者氏名 稲荷均 横浜市立大学大学院医学研究科外科治療学 審査員 主査横浜市立大学大学院医学研究科教授矢尾正祐 副査横浜市立大学大学院医学研究科講師成井一隆 副査横浜市立大学大学院医学研究科講師仙石徹 学位論文 : 転移性乳癌における EZH2 発現の臨床的意義 Expression of enhancer of zeste homolog 2 correlates
博士の学位論文審査結果の要旨 申請者氏名 稲荷均 横浜市立大学大学院医学研究科外科治療学 審査員 主査横浜市立大学大学院医学研究科教授矢尾正祐 副査横浜市立大学大学院医学研究科講師成井一隆 副査横浜市立大学大学院医学研究科講師仙石徹 学位論文 : 転移性乳癌における EZH2 発現の臨床的意義 Expression of enhancer of zeste homolog 2 correlates
られる 糖尿病を合併した高血圧の治療の薬物治療の第一選択薬はアンジオテンシン変換酵素 (ACE) 阻害薬とアンジオテンシン II 受容体拮抗薬 (ARB) である このクラスの薬剤は単なる降圧効果のみならず 様々な臓器保護作用を有しているが ACE 阻害薬や ARB のプラセボ比較試験で糖尿病の新規
 論文の内容の要旨 論文題目アンジオテンシン受容体拮抗薬テルミサルタンの メタボリックシンドロームに対する効果の検討 指導教員門脇孝教授 東京大学大学院医学系研究科 平成 19 年 4 月入学 医学博士課程 内科学専攻 氏名廣瀬理沙 要旨 背景 目的 わが国の死因の第二位と第三位を占める心筋梗塞や脳梗塞などの心血管疾患を引き起こす基盤となる病態として 過剰なエネルギー摂取と運動不足などの生活習慣により内臓脂肪が蓄積する内臓脂肪型肥満を中心に
論文の内容の要旨 論文題目アンジオテンシン受容体拮抗薬テルミサルタンの メタボリックシンドロームに対する効果の検討 指導教員門脇孝教授 東京大学大学院医学系研究科 平成 19 年 4 月入学 医学博士課程 内科学専攻 氏名廣瀬理沙 要旨 背景 目的 わが国の死因の第二位と第三位を占める心筋梗塞や脳梗塞などの心血管疾患を引き起こす基盤となる病態として 過剰なエネルギー摂取と運動不足などの生活習慣により内臓脂肪が蓄積する内臓脂肪型肥満を中心に
抗菌薬の殺菌作用抗菌薬の殺菌作用には濃度依存性と時間依存性の 2 種類があり 抗菌薬の効果および用法 用量の設定に大きな影響を与えます 濃度依存性タイプでは 濃度を高めると濃度依存的に殺菌作用を示します 濃度依存性タイプの抗菌薬としては キノロン系薬やアミノ配糖体系薬が挙げられます 一方 時間依存性
 2012 年 1 月 4 日放送 抗菌薬の PK-PD 愛知医科大学大学院感染制御学教授三鴨廣繁抗菌薬の PK-PD とは薬物動態を解析することにより抗菌薬の有効性と安全性を評価する考え方は アミノ配糖体系薬などの副作用を回避するための薬物血中濃度モニタリング (TDM) の分野で発達してきました 近年では 耐性菌の増加 コンプロマイズド ホストの増加 新規抗菌薬の開発の停滞などもあり 現存の抗菌薬をいかに科学的に使用するかが重要な課題となっており
2012 年 1 月 4 日放送 抗菌薬の PK-PD 愛知医科大学大学院感染制御学教授三鴨廣繁抗菌薬の PK-PD とは薬物動態を解析することにより抗菌薬の有効性と安全性を評価する考え方は アミノ配糖体系薬などの副作用を回避するための薬物血中濃度モニタリング (TDM) の分野で発達してきました 近年では 耐性菌の増加 コンプロマイズド ホストの増加 新規抗菌薬の開発の停滞などもあり 現存の抗菌薬をいかに科学的に使用するかが重要な課題となっており
く 細胞傷害活性の無い CD4 + ヘルパー T 細胞が必須と判明した 吉田らは 1988 年 C57BL/6 マウスが腹腔内に移植した BALB/c マウス由来の Meth A 腫瘍細胞 (CTL 耐性細胞株 ) を拒絶すること 1991 年 同種異系移植によって誘導されるマクロファージ (AIM
 ( 様式甲 5) 氏 名 山名秀典 ( ふりがな ) ( やまなひでのり ) 学 位 の 種 類 博士 ( 医学 ) 学位授与番号 甲 第 号 学位審査年月日 平成 26 年 7 月 30 日 学位授与の要件 学位規則第 4 条第 1 項該当 Down-regulated expression of 学位論文題名 monocyte/macrophage major histocompatibility
( 様式甲 5) 氏 名 山名秀典 ( ふりがな ) ( やまなひでのり ) 学 位 の 種 類 博士 ( 医学 ) 学位授与番号 甲 第 号 学位審査年月日 平成 26 年 7 月 30 日 学位授与の要件 学位規則第 4 条第 1 項該当 Down-regulated expression of 学位論文題名 monocyte/macrophage major histocompatibility
ルリコナゾールルコナック爪外用液 5% CTD 第 2 部 ( モジュール2): CTDの概要 ( サマリー ) 2.6 非臨床試験の概要文及び概要表 緒言 佐藤製薬株式会社
 ルコナック爪外用液 5% CTD 第 2 部 ( モジュール2): CTDの概要 ( サマリー ) 2.6.1 緒言 佐藤製薬株式会社 略号一覧表 略号 英語 日本語 本剤 - SKN-08 外用液剤 目 次 2.6.1 緒言... 1 2.6.1 緒言 ((-)-(E)-[(4R)-4-(2,4-dichlorophenyl)-1,3-dithiolan-2-ylidene] (1H-imidazol-1-yl)
ルコナック爪外用液 5% CTD 第 2 部 ( モジュール2): CTDの概要 ( サマリー ) 2.6.1 緒言 佐藤製薬株式会社 略号一覧表 略号 英語 日本語 本剤 - SKN-08 外用液剤 目 次 2.6.1 緒言... 1 2.6.1 緒言 ((-)-(E)-[(4R)-4-(2,4-dichlorophenyl)-1,3-dithiolan-2-ylidene] (1H-imidazol-1-yl)
( 続紙 1 ) 京都大学 博士 ( 薬学 ) 氏名 大西正俊 論文題目 出血性脳障害におけるミクログリアおよびMAPキナーゼ経路の役割に関する研究 ( 論文内容の要旨 ) 脳内出血は 高血圧などの原因により脳血管が破綻し 脳実質へ出血した病態をいう 漏出する血液中の種々の因子の中でも 血液凝固に関
 Title 出血性脳障害におけるミクログリアおよびMAPキナーゼ経路の役割に関する研究 ( Abstract_ 要旨 ) Author(s) 大西, 正俊 Citation Kyoto University ( 京都大学 ) Issue Date 2010-03-23 URL http://hdl.handle.net/2433/120523 Right Type Thesis or Dissertation
Title 出血性脳障害におけるミクログリアおよびMAPキナーゼ経路の役割に関する研究 ( Abstract_ 要旨 ) Author(s) 大西, 正俊 Citation Kyoto University ( 京都大学 ) Issue Date 2010-03-23 URL http://hdl.handle.net/2433/120523 Right Type Thesis or Dissertation
の活性化が背景となるヒト悪性腫瘍の治療薬開発につながる 図4 研究である 研究内容 私たちは図3に示すようなyeast two hybrid 法を用いて AKT分子に結合する細胞内分子のスクリーニングを行った この結果 これまで機能の分からなかったプロトオンコジン TCL1がAKTと結合し多量体を形
 AKT活性を抑制するペプチ ド阻害剤の開発 野口 昌幸 北海道大学遺伝子病制御研究所 教授 広村 信 北海道大学遺伝子病制御研究所 ポスドク 岡田 太 北海道大学遺伝子病制御研究所 助手 柳舘 拓也 株式会社ラボ 研究員 ナーゼAKTに結合するタンパク分子を検索し これまで機能の 分からなかったプロトオンコジンTCL1がAKTと結合し AKT の活性化を促す AKT活性補助因子 であることを見い出し
AKT活性を抑制するペプチ ド阻害剤の開発 野口 昌幸 北海道大学遺伝子病制御研究所 教授 広村 信 北海道大学遺伝子病制御研究所 ポスドク 岡田 太 北海道大学遺伝子病制御研究所 助手 柳舘 拓也 株式会社ラボ 研究員 ナーゼAKTに結合するタンパク分子を検索し これまで機能の 分からなかったプロトオンコジンTCL1がAKTと結合し AKT の活性化を促す AKT活性補助因子 であることを見い出し
子として同定され 前立腺癌をはじめとした癌細胞や不死化細胞で著しい発現低下が認められ 癌抑制遺伝子として発見された Dkk-3 は前立腺癌以外にも膵臓癌 乳癌 子宮内膜癌 大腸癌 脳腫瘍 子宮頸癌など様々な癌で発現が低下し 癌抑制遺伝子としてアポトーシス促進的に働くと考えられている 先行研究では ヒ
 学位論文の内容の要旨 論文提出者氏名 髙田愛子 論文審査担当者 主査北川昌伸副査山岡昇司 清水重臣 論文題目 Dkk-3 induces apoptosis through mitochondrial and Fas death receptor pathways in human mucinous ovarian cancer cells ( 論文内容の要旨 ) < 要旨 > Wnt シグナルの阻害因子
学位論文の内容の要旨 論文提出者氏名 髙田愛子 論文審査担当者 主査北川昌伸副査山岡昇司 清水重臣 論文題目 Dkk-3 induces apoptosis through mitochondrial and Fas death receptor pathways in human mucinous ovarian cancer cells ( 論文内容の要旨 ) < 要旨 > Wnt シグナルの阻害因子
( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 教授 森脇真一 井上善博 副査副査 教授教授 東 治 人 上 田 晃 一 副査 教授 朝日通雄 主論文題名 Transgene number-dependent, gene expression rate-independe
 ( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 森脇真一 井上善博 副査副査 東 治 人 上 田 晃 一 副査 朝日通雄 主論文題名 Transgene number-dependent, gene expression rate-independent rejection of D d -, K d -, or D d K d -transgened mouse skin
( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 森脇真一 井上善博 副査副査 東 治 人 上 田 晃 一 副査 朝日通雄 主論文題名 Transgene number-dependent, gene expression rate-independent rejection of D d -, K d -, or D d K d -transgened mouse skin
( 図 ) IP3 と IRBIT( アービット ) が IP3 受容体に競合して結合する様子
 60 秒でわかるプレスリリース 2006 年 6 月 23 日 独立行政法人理化学研究所 独立行政法人科学技術振興機構 細胞内のカルシウムチャネルに情報伝達を邪魔する 偽結合体 を発見 - IP3 受容体に IP3 と競合して結合するタンパク質 アービット の機能を解明 - 細胞分裂 細胞死 受精 発生など 私たちの生の営みそのものに関わる情報伝達は 細胞内のカルシウムイオンの放出によって行われています
60 秒でわかるプレスリリース 2006 年 6 月 23 日 独立行政法人理化学研究所 独立行政法人科学技術振興機構 細胞内のカルシウムチャネルに情報伝達を邪魔する 偽結合体 を発見 - IP3 受容体に IP3 と競合して結合するタンパク質 アービット の機能を解明 - 細胞分裂 細胞死 受精 発生など 私たちの生の営みそのものに関わる情報伝達は 細胞内のカルシウムイオンの放出によって行われています
抑制することが知られている 今回はヒト子宮内膜におけるコレステロール硫酸のプロテ アーゼ活性に対する効果を検討することとした コレステロール硫酸の着床期特異的な発現の機序を解明するために 合成酵素であるコ レステロール硫酸基転移酵素 (SULT2B1b) に着目した ヒト子宮内膜は排卵後 脱落膜 化
 論文の内容の要旨 論文題目 着床期ヒト子宮内膜におけるコレステロール硫酸の発現調節機序及び機能の解析 指導教員武谷雄二教授 東京大学大学院医学系研究科 平成 15 年 4 月入学 医学博士課程 生殖 発達 加齢医学専攻 清末美奈子 緒言 着床とは 受精卵が分割し形成された胚盤胞が子宮内膜上皮へ接着 貫通し 子 宮内膜間質を浸潤して絨毛構造を形成するまでの一連の現象をいう 胚盤胞から分化した トロフォブラストが浸潤していく過程で
論文の内容の要旨 論文題目 着床期ヒト子宮内膜におけるコレステロール硫酸の発現調節機序及び機能の解析 指導教員武谷雄二教授 東京大学大学院医学系研究科 平成 15 年 4 月入学 医学博士課程 生殖 発達 加齢医学専攻 清末美奈子 緒言 着床とは 受精卵が分割し形成された胚盤胞が子宮内膜上皮へ接着 貫通し 子 宮内膜間質を浸潤して絨毛構造を形成するまでの一連の現象をいう 胚盤胞から分化した トロフォブラストが浸潤していく過程で
-119-
 -119- - 日中医学協会助成事業 - 前立腺がんの造骨性骨転移のメカニズム解明 研究者氏名中国所属機関日本研究機関指導責任者共同研究者 王麗楊中国医科大学大阪大学歯学研究科教授米田俊之相野誠 要旨 近年日本の男性において急増している前立腺がんは死亡率の第 2 位にランクされている 80% 以上の前立腺癌は造骨性の骨転移を示し 患者の QOL および生存期間を著しく低下させる 前立腺がん発生のメカニズムには未だ不明な点が多く
-119- - 日中医学協会助成事業 - 前立腺がんの造骨性骨転移のメカニズム解明 研究者氏名中国所属機関日本研究機関指導責任者共同研究者 王麗楊中国医科大学大阪大学歯学研究科教授米田俊之相野誠 要旨 近年日本の男性において急増している前立腺がんは死亡率の第 2 位にランクされている 80% 以上の前立腺癌は造骨性の骨転移を示し 患者の QOL および生存期間を著しく低下させる 前立腺がん発生のメカニズムには未だ不明な点が多く
資料4-4 木酢液の検討状況について
 資料 4-4 木酢液の検討状況について 木酢液の薬効 薬害 安全性等に係る検討に関し 第 6 回及び第 8 回合同 会合において 以下のとおり整理された 安全性 薬効 薬害に係る試験の実施 ( 論点 ) 第 6 回合同会合において検討した結果 変異原性試験 ( 復帰突然変異原性試験 ) の結果について指摘があった また 1) 木酢液 に含まれるホルムアルデヒドについては IARC( 国際ガン研究機関
資料 4-4 木酢液の検討状況について 木酢液の薬効 薬害 安全性等に係る検討に関し 第 6 回及び第 8 回合同 会合において 以下のとおり整理された 安全性 薬効 薬害に係る試験の実施 ( 論点 ) 第 6 回合同会合において検討した結果 変異原性試験 ( 復帰突然変異原性試験 ) の結果について指摘があった また 1) 木酢液 に含まれるホルムアルデヒドについては IARC( 国際ガン研究機関
脳組織傷害時におけるミクログリア形態変化および機能 Title変化に関する培養脳組織切片を用いた研究 ( Abstract_ 要旨 ) Author(s) 岡村, 敏行 Citation Kyoto University ( 京都大学 ) Issue Date URL http
 脳組織傷害時におけるミクログリア形態変化および機能 Title変化に関する培養脳組織切片を用いた研究 ( Abstract_ 要旨 ) Author(s) 岡村, 敏行 Citation Kyoto University ( 京都大学 ) Issue Date 2009-03-23 URL http://hdl.handle.net/2433/124054 Right Type Thesis or
脳組織傷害時におけるミクログリア形態変化および機能 Title変化に関する培養脳組織切片を用いた研究 ( Abstract_ 要旨 ) Author(s) 岡村, 敏行 Citation Kyoto University ( 京都大学 ) Issue Date 2009-03-23 URL http://hdl.handle.net/2433/124054 Right Type Thesis or
センシンレンのエタノール抽出液による白血病細胞株での抗腫瘍効果の検討
 Evaluation of anti-tumor activity with the treatment of ethanol extract from Andrographis Paniculata in leukemic cell lines Hidehiko Akiyama 1), Kazuharu Suzuki 2), Toshiyuki Taniguchi 2) and Itsuro Katsuda
Evaluation of anti-tumor activity with the treatment of ethanol extract from Andrographis Paniculata in leukemic cell lines Hidehiko Akiyama 1), Kazuharu Suzuki 2), Toshiyuki Taniguchi 2) and Itsuro Katsuda
研究目的 1. 電波ばく露による免疫細胞への影響に関する研究 我々の体には 恒常性を保つために 生体内に侵入した異物を生体外に排除する 免疫と呼ばれる防御システムが存在する 免疫力の低下は感染を引き起こしやすくなり 健康を損ないやすくなる そこで 2 10W/kgのSARで電波ばく露を行い 免疫細胞
 資料 - 生電 6-3 免疫細胞及び神経膠細胞を対象としたマイクロ波照射影響に関する実験評価 京都大学首都大学東京 宮越順二 成田英二郎 櫻井智徳多氣昌生 鈴木敏久 日 : 平成 23 年 7 月 22 日 ( 金 ) 場所 : 総務省第 1 特別会議室 研究目的 1. 電波ばく露による免疫細胞への影響に関する研究 我々の体には 恒常性を保つために 生体内に侵入した異物を生体外に排除する 免疫と呼ばれる防御システムが存在する
資料 - 生電 6-3 免疫細胞及び神経膠細胞を対象としたマイクロ波照射影響に関する実験評価 京都大学首都大学東京 宮越順二 成田英二郎 櫻井智徳多氣昌生 鈴木敏久 日 : 平成 23 年 7 月 22 日 ( 金 ) 場所 : 総務省第 1 特別会議室 研究目的 1. 電波ばく露による免疫細胞への影響に関する研究 我々の体には 恒常性を保つために 生体内に侵入した異物を生体外に排除する 免疫と呼ばれる防御システムが存在する
パナテスト ラットβ2マイクログロブリン
 研究用試薬 2014 年 4 月作成 EIA 法ラット β 2 マイクログロブリン測定キット PRH111 パナテスト A シリーズラット β 2- マイクロク ロフ リン 1. はじめに β 2 - マイクログロブリンは, 血液, 尿, および体液中に存在し, ヒトでは腎糸球体障害, 自己免疫疾患, 悪性腫瘍, 肝疾患などによって血中濃度が変化するといわれています. また,β 2 - マイクログロブリンの尿中濃度は,
研究用試薬 2014 年 4 月作成 EIA 法ラット β 2 マイクログロブリン測定キット PRH111 パナテスト A シリーズラット β 2- マイクロク ロフ リン 1. はじめに β 2 - マイクログロブリンは, 血液, 尿, および体液中に存在し, ヒトでは腎糸球体障害, 自己免疫疾患, 悪性腫瘍, 肝疾患などによって血中濃度が変化するといわれています. また,β 2 - マイクログロブリンの尿中濃度は,
D961H は AstraZeneca R&D Mӧlndal( スウェーデン ) において開発された オメプラゾールの一方の光学異性体 (S- 体 ) のみを含有するプロトンポンプ阻害剤である ネキシウム (D961H の日本における販売名 ) 錠 20 mg 及び 40 mg は を対象として
 第 2 部 CTD の概要 一般名 : エソメプラゾールマグネシウム水和物 版番号 : 2.2 緒言 ネキシウム カプセル ネキシウム 懸濁用顆粒分包 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています D961H は AstraZeneca R&D Mӧlndal( スウェーデン ) において開発された オメプラゾールの一方の光学異性体
第 2 部 CTD の概要 一般名 : エソメプラゾールマグネシウム水和物 版番号 : 2.2 緒言 ネキシウム カプセル ネキシウム 懸濁用顆粒分包 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています D961H は AstraZeneca R&D Mӧlndal( スウェーデン ) において開発された オメプラゾールの一方の光学異性体
PowerPoint プレゼンテーション
 多能性幹細胞を利用した毒性の判定方法 教授 森田隆 准教授 吉田佳世 ( 大阪市立大学大学院医学研究科遺伝子制御学 ) これまでの問題点 化学物質の人体および環境に及ぼす影響については 迅速にその評価を行うことが社会的に要請されている 一方 マウスやラットなど動物を用いた実験は必要ではあるが 動物愛護や費用 時間的な問題がある そこで 哺乳動物細胞を用いたリスク評価系の開発が望まれる 我々は DNA
多能性幹細胞を利用した毒性の判定方法 教授 森田隆 准教授 吉田佳世 ( 大阪市立大学大学院医学研究科遺伝子制御学 ) これまでの問題点 化学物質の人体および環境に及ぼす影響については 迅速にその評価を行うことが社会的に要請されている 一方 マウスやラットなど動物を用いた実験は必要ではあるが 動物愛護や費用 時間的な問題がある そこで 哺乳動物細胞を用いたリスク評価系の開発が望まれる 我々は DNA
Untitled
 上原記念生命科学財団研究報告集, 26 (2012) 75. 哺乳類のゴルジ体ストレス応答の分子機構の解明 吉田秀郎 Key words: ゴルジ体, 小胞体, 転写, ストレス応答, 細胞小器官 兵庫県立大学大学院生命理学研究科生体物質化学 Ⅱ 講座 緒言細胞内には様々な細胞小器官が存在して細胞の機能を分担しているが, その存在量は細胞の需要に応じて厳密に制御されており, 必要な時に必要な細胞小器官が必要な量だけ増強される.
上原記念生命科学財団研究報告集, 26 (2012) 75. 哺乳類のゴルジ体ストレス応答の分子機構の解明 吉田秀郎 Key words: ゴルジ体, 小胞体, 転写, ストレス応答, 細胞小器官 兵庫県立大学大学院生命理学研究科生体物質化学 Ⅱ 講座 緒言細胞内には様々な細胞小器官が存在して細胞の機能を分担しているが, その存在量は細胞の需要に応じて厳密に制御されており, 必要な時に必要な細胞小器官が必要な量だけ増強される.
犬の糖尿病は治療に一生涯のインスリン投与を必要とする ヒトでは 1 型に分類されている糖尿病である しかし ヒトでは肥満が原因となり 相対的にインスリン作用が不足する 2 型糖尿病が主体であり 犬とヒトとでは糖尿病発症メカニズムが大きく異なっていると考えられている そこで 本研究ではインスリン抵抗性
 犬におけるインスリン抵抗性と糖尿病発症に関する メタボローム研究 (Metabolome study on canine insulin resistance and diabetes onset) 学位論文の内容の要約 獣医生命科学研究科獣医学専攻博士課程平成 24 年入学 野澤聡司 ( 指導教員 : 田﨑弘之 ) 犬の糖尿病は治療に一生涯のインスリン投与を必要とする ヒトでは 1 型に分類されている糖尿病である
犬におけるインスリン抵抗性と糖尿病発症に関する メタボローム研究 (Metabolome study on canine insulin resistance and diabetes onset) 学位論文の内容の要約 獣医生命科学研究科獣医学専攻博士課程平成 24 年入学 野澤聡司 ( 指導教員 : 田﨑弘之 ) 犬の糖尿病は治療に一生涯のインスリン投与を必要とする ヒトでは 1 型に分類されている糖尿病である
学位論文の内容の要旨 論文提出者氏名 松尾祐介 論文審査担当者 主査淺原弘嗣 副査関矢一郎 金井正美 論文題目 Local fibroblast proliferation but not influx is responsible for synovial hyperplasia in a mur
 学位論文の内容の要旨 論文提出者氏名 松尾祐介 論文審査担当者 主査淺原弘嗣 副査関矢一郎 金井正美 論文題目 Local fibroblast proliferation but not influx is responsible for synovial hyperplasia in a murine model of rheumatoid arthritis ( 論文内容の要旨 ) < 要旨
学位論文の内容の要旨 論文提出者氏名 松尾祐介 論文審査担当者 主査淺原弘嗣 副査関矢一郎 金井正美 論文題目 Local fibroblast proliferation but not influx is responsible for synovial hyperplasia in a murine model of rheumatoid arthritis ( 論文内容の要旨 ) < 要旨
Aug :35:42
 Aug 24 2012 16:35:42 非臨床概要薬理試験の目次 項目 - 頁 2.6.1. 緒言... ~xr1i 2.6.1 - p. 1 2.6.2. 薬理試験の概要文... ~xr2i 2.6.2 - p. 1 2.6.2.1. まとめ... ~xr3i 2.6.2 - p. 1 2.6.2.2. 効力を裏付ける試験... ~xr4i 2.6.2 - p. 2 2.6.2.2.1. In
Aug 24 2012 16:35:42 非臨床概要薬理試験の目次 項目 - 頁 2.6.1. 緒言... ~xr1i 2.6.1 - p. 1 2.6.2. 薬理試験の概要文... ~xr2i 2.6.2 - p. 1 2.6.2.1. まとめ... ~xr3i 2.6.2 - p. 1 2.6.2.2. 効力を裏付ける試験... ~xr4i 2.6.2 - p. 2 2.6.2.2.1. In
PowerPoint プレゼンテーション
 パーキンソン病患者の認知 障害を正常化する薬 帯広畜産大学獣医学研究部門基礎獣医学分野教授石井利明 背景 ~ パーキンソン病 (PD) とは ~ PD の概要 (10 万人に 100 人の割合で発症 ) アルツハイマー病に次いで多い進行性神経変性疾患 発症の原因は不明 黒質線条体ドパミン (DA) 神経の傷害 PD の症状 1 運動症状 安静時振戦 : ふるえ 固縮 : 筋肉のこわばり 無動 : 動作が遅くなる
パーキンソン病患者の認知 障害を正常化する薬 帯広畜産大学獣医学研究部門基礎獣医学分野教授石井利明 背景 ~ パーキンソン病 (PD) とは ~ PD の概要 (10 万人に 100 人の割合で発症 ) アルツハイマー病に次いで多い進行性神経変性疾患 発症の原因は不明 黒質線条体ドパミン (DA) 神経の傷害 PD の症状 1 運動症状 安静時振戦 : ふるえ 固縮 : 筋肉のこわばり 無動 : 動作が遅くなる
ルグリセロールと脂肪酸に分解され吸収される それらは腸上皮細胞に吸収されたのちに再び中性脂肪へと生合成されカイロミクロンとなる DGAT1 は腸管で脂質の再合成 吸収に関与していることから DGAT1 KO マウスで認められているフェノタイプが腸 DGAT1 欠如に由来していることが考えられる 実際
 学位論文の内容の要旨 論文提出者氏名 津田直人 論文審査担当者 主査下門顕太郎副査吉田雅幸横関博雄 論文題目 Intestine-Targeted DGAT1 Inhibition Improves Obesity and Insulin Resistance without Skin Aberrations in Mice ( 論文内容の要旨 ) < 要旨 > Diacylglycerol O-acyltransferase
学位論文の内容の要旨 論文提出者氏名 津田直人 論文審査担当者 主査下門顕太郎副査吉田雅幸横関博雄 論文題目 Intestine-Targeted DGAT1 Inhibition Improves Obesity and Insulin Resistance without Skin Aberrations in Mice ( 論文内容の要旨 ) < 要旨 > Diacylglycerol O-acyltransferase
( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 教授 花房俊昭 宮村昌利 副査副査 教授教授 朝 日 通 雄 勝 間 田 敬 弘 副査 教授 森田大 主論文題名 Effects of Acarbose on the Acceleration of Postprandial
 ( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 花房俊昭 宮村昌利 副査副査 朝 日 通 雄 勝 間 田 敬 弘 副査 森田大 主論文題名 Effects of Acarbose on the Acceleration of Postprandial Hyperglycemia-Induced Pathological Changes Induced by Intermittent
( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 花房俊昭 宮村昌利 副査副査 朝 日 通 雄 勝 間 田 敬 弘 副査 森田大 主論文題名 Effects of Acarbose on the Acceleration of Postprandial Hyperglycemia-Induced Pathological Changes Induced by Intermittent
トリアムシノロンアセトニド マキュエイド硝子体内注用 40mg 医薬品製造販売承認事項一部変更承認申請書 添付資料 CTD 第 2 部 ( 資料概要 ) 2.6 非臨床試験の概要文及び概要表 薬物動態試験の概要文 わかもと製薬株式会社 1
 トリアムシノロンアセトニド マキュエイド硝子体内注用 40mg 医薬品製造販売承認事項一部変更承認申請書 添付資料 CTD 第 2 部 ( 資料概要 ) 2.6 非臨床試験の概要文及び概要表 2.6.4 薬物動態試験の概要文 わかもと製薬株式会社 1 2.6.4 薬物動態試験の概要文マキュエイド硝子体内注用 目次 2.6.4 薬物動態試験の概要文... 4 2.6.4.1 まとめ... 4 2.6.4.2
トリアムシノロンアセトニド マキュエイド硝子体内注用 40mg 医薬品製造販売承認事項一部変更承認申請書 添付資料 CTD 第 2 部 ( 資料概要 ) 2.6 非臨床試験の概要文及び概要表 2.6.4 薬物動態試験の概要文 わかもと製薬株式会社 1 2.6.4 薬物動態試験の概要文マキュエイド硝子体内注用 目次 2.6.4 薬物動態試験の概要文... 4 2.6.4.1 まとめ... 4 2.6.4.2
Folia Pharmacol. Jpn mg/14 ml mg/ ml Genentech, Inc. Genentech HER human epidermal growth factor receptor type HER - HER HER HER HER
 Folia Pharmacol. Jpn. 143 420 mg/14 ml 1 2 3 4 mg/ ml Genentech, Inc. Genentech HER human epidermal growth factor receptor type HER - HER HER HER HER HER KPL- HER BO HER CLEOPATRA HER HER 1. HER HER EGFR
Folia Pharmacol. Jpn. 143 420 mg/14 ml 1 2 3 4 mg/ ml Genentech, Inc. Genentech HER human epidermal growth factor receptor type HER - HER HER HER HER HER KPL- HER BO HER CLEOPATRA HER HER 1. HER HER EGFR
微小粒子状物質曝露影響調査報告書
 (7)PM 2.5 抽出物が高血圧ラットの呼吸 循環機能に及ぼす影響に関する研究 要旨大気環境中の浮遊粒子状物質の吸入により 呼吸器系のみならず心臓血管系に対するリスクが高まることが指摘されているが十分に明らかにされてはいない そこで 心臓血管系の病態モデルとして自然発症高血圧ラット (SHR:Spontaneous Hypertensive Rat) を用いて 抽出物及び 抽出物の影響について気管内投与を行い検討した
(7)PM 2.5 抽出物が高血圧ラットの呼吸 循環機能に及ぼす影響に関する研究 要旨大気環境中の浮遊粒子状物質の吸入により 呼吸器系のみならず心臓血管系に対するリスクが高まることが指摘されているが十分に明らかにされてはいない そこで 心臓血管系の病態モデルとして自然発症高血圧ラット (SHR:Spontaneous Hypertensive Rat) を用いて 抽出物及び 抽出物の影響について気管内投与を行い検討した
一次サンプル採取マニュアル PM 共通 0001 Department of Clinical Laboratory, Kyoto University Hospital その他の検体検査 >> 8C. 遺伝子関連検査受託終了項目 23th May EGFR 遺伝子変異検
 Department of Clinical Laboratory, Kyoto University Hospital 6459 8. その他の検体検査 >> 8C. 遺伝子関連検査受託終了項目 23th May. 2017 EGFR 遺伝子変異検査 ( 院内測定 ) c-erbb/egfr [tissues] 基本情報 8C051 c-erbb/egfr JLAC10 診療報酬 分析物 識別材料測定法
Department of Clinical Laboratory, Kyoto University Hospital 6459 8. その他の検体検査 >> 8C. 遺伝子関連検査受託終了項目 23th May. 2017 EGFR 遺伝子変異検査 ( 院内測定 ) c-erbb/egfr [tissues] 基本情報 8C051 c-erbb/egfr JLAC10 診療報酬 分析物 識別材料測定法
図 B 細胞受容体を介した NF-κB 活性化モデル
 60 秒でわかるプレスリリース 2007 年 12 月 17 日 独立行政法人理化学研究所 免疫の要 NF-κB の活性化シグナルを増幅する機構を発見 - リン酸化酵素 IKK が正のフィーッドバックを担当 - 身体に病原菌などの異物 ( 抗原 ) が侵入すると 誰にでも備わっている免疫システムが働いて 異物を認識し 排除するために さまざまな反応を起こします その一つに 免疫細胞である B 細胞が
60 秒でわかるプレスリリース 2007 年 12 月 17 日 独立行政法人理化学研究所 免疫の要 NF-κB の活性化シグナルを増幅する機構を発見 - リン酸化酵素 IKK が正のフィーッドバックを担当 - 身体に病原菌などの異物 ( 抗原 ) が侵入すると 誰にでも備わっている免疫システムが働いて 異物を認識し 排除するために さまざまな反応を起こします その一つに 免疫細胞である B 細胞が
新規遺伝子ARIAによる血管新生調節機構の解明
 [PRESS RELEASE] No.KPUnews290004 2018 年 1 月 24 日神戸薬科大学企画 広報課 脂肪細胞のインスリンシグナルを調節し 糖尿病 メタボリック症候群の発症を予防 する新規分子の発見 日本人男性の約 30% 女性の約 20% は肥満に該当し 肥満はまさに国民病です 内臓脂肪の蓄積はインスリン抵抗性を引き起こし 糖尿病 メタボリック症候群の発症に繋がります 糖尿病
[PRESS RELEASE] No.KPUnews290004 2018 年 1 月 24 日神戸薬科大学企画 広報課 脂肪細胞のインスリンシグナルを調節し 糖尿病 メタボリック症候群の発症を予防 する新規分子の発見 日本人男性の約 30% 女性の約 20% は肥満に該当し 肥満はまさに国民病です 内臓脂肪の蓄積はインスリン抵抗性を引き起こし 糖尿病 メタボリック症候群の発症に繋がります 糖尿病
の基軸となるのは 4 種の eif2αキナーゼ (HRI, PKR, または ) の活性化, eif2αのリン酸化及び転写因子 の発現誘導である ( 図 1). によってアミノ酸代謝やタンパク質の折りたたみ, レドックス代謝等に関わるストレス関連遺伝子の転写が促進され, それらの働きによって細胞はス
 活性型がん遺伝子 による ストレス適応応答制御機構の解明と治療への応用 Regulation Mechanisms of Stress Response by Oncogenic 平成 26 年度入学永澤生久子 (Nagasawa, Ikuko) 指導教員冨田章弘 がんの発生はがん遺伝子の変化の集積に起因し, 活性型がん遺伝子による細胞増殖シグナルの異常な活性化は現在のがん治療において重要な治療標的である.
活性型がん遺伝子 による ストレス適応応答制御機構の解明と治療への応用 Regulation Mechanisms of Stress Response by Oncogenic 平成 26 年度入学永澤生久子 (Nagasawa, Ikuko) 指導教員冨田章弘 がんの発生はがん遺伝子の変化の集積に起因し, 活性型がん遺伝子による細胞増殖シグナルの異常な活性化は現在のがん治療において重要な治療標的である.
平成14年度研究報告
 平成 14 年度研究報告 研究テーマ 多嚢胞性卵巣発症に関する遺伝性素因の解析 - PCO の解析 - 北海道大学大学院医学研究科 助手菅原照夫 現所属 : 北海道大学大学院医学研究科 医学部連携研究センター サマリー 多嚢胞性卵巣 (PCO) は生殖可能年齢の婦人の 5 10% に発症する内分泌疾患である 臨床症状は 月経不順 多毛 肥満 排卵障害が主な特徴であり 難治性の不妊症の主な原因である
平成 14 年度研究報告 研究テーマ 多嚢胞性卵巣発症に関する遺伝性素因の解析 - PCO の解析 - 北海道大学大学院医学研究科 助手菅原照夫 現所属 : 北海道大学大学院医学研究科 医学部連携研究センター サマリー 多嚢胞性卵巣 (PCO) は生殖可能年齢の婦人の 5 10% に発症する内分泌疾患である 臨床症状は 月経不順 多毛 肥満 排卵障害が主な特徴であり 難治性の不妊症の主な原因である
Taro-kv12250.jtd
 ニューカッスル病 マレック病 ( ニューカッスル病ウイルス由来 F 蛋白遺伝子導入マレック病ウイルス 1 型 ) 凍結生ワクチン 平成 22 年 8 月 12 日 ( 告示第 2288 号 ) 新規追加 ニューカッスル病ウイルスのF 蛋白をコードする遺伝子を弱毒マレック病ウイルス (1 型 ) に挿入して得られた組換え体ウイルスを培養細胞で増殖させて得た感染細胞浮遊液を凍結したワクチンである 1 小分製品の試験
ニューカッスル病 マレック病 ( ニューカッスル病ウイルス由来 F 蛋白遺伝子導入マレック病ウイルス 1 型 ) 凍結生ワクチン 平成 22 年 8 月 12 日 ( 告示第 2288 号 ) 新規追加 ニューカッスル病ウイルスのF 蛋白をコードする遺伝子を弱毒マレック病ウイルス (1 型 ) に挿入して得られた組換え体ウイルスを培養細胞で増殖させて得た感染細胞浮遊液を凍結したワクチンである 1 小分製品の試験
新規 P2X4 受容体アンタゴニスト NCP-916 の鎮痛作用と薬物動態に関する検討 ( 分野名 : ライフイノベーション分野 ) ( 学籍番号 )3PS1333S ( 氏名 ) 小川亨 序論 神経障害性疼痛とは, 体性感覚神経系の損傷や疾患によって引き起こされる痛みと定義され, 自発痛やアロディ
 九州大学学術情報リポジトリ Kyushu University Institutional Repository 新規 P2X4 受容体アンタゴニスト NCP-916 の鎮痛作用と薬物動態に関する検討 小川, 亨 http://hdl.handle.net/2324/178378 出版情報 : 九州大学, 216, 博士 ( 創薬科学 ), 課程博士バージョン : 権利関係 : やむを得ない事由により本文ファイル非公開
九州大学学術情報リポジトリ Kyushu University Institutional Repository 新規 P2X4 受容体アンタゴニスト NCP-916 の鎮痛作用と薬物動態に関する検討 小川, 亨 http://hdl.handle.net/2324/178378 出版情報 : 九州大学, 216, 博士 ( 創薬科学 ), 課程博士バージョン : 権利関係 : やむを得ない事由により本文ファイル非公開
<4D F736F F D B82C982C282A282C482512E646F63>
 サンプル条件および固定化分子の選択 Biacoreの実験ではセンサーチップに固定化する分子をリガンド それに対して結合を測定する分子をアナライトと呼びます いずれの分子をリガンドとし アナライトとするかは 実験系を構築する上で重要です 以下にサンプルに適したリガンド アナライトの設計方法やサンプルの必要条件などをご紹介します アナライト リガンド センサーチップ (1) タンパク質リガンドとしてもアナライトとしても用いることができます
サンプル条件および固定化分子の選択 Biacoreの実験ではセンサーチップに固定化する分子をリガンド それに対して結合を測定する分子をアナライトと呼びます いずれの分子をリガンドとし アナライトとするかは 実験系を構築する上で重要です 以下にサンプルに適したリガンド アナライトの設計方法やサンプルの必要条件などをご紹介します アナライト リガンド センサーチップ (1) タンパク質リガンドとしてもアナライトとしても用いることができます
RNA Poly IC D-IPS-1 概要 自然免疫による病原体成分の認識は炎症反応の誘導や 獲得免疫の成立に重要な役割を果たす生体防御機構です 今回 私達はウイルス RNA を模倣する合成二本鎖 RNA アナログの Poly I:C を用いて 自然免疫応答メカニズムの解析を行いました その結果
 RNA Poly IC D-IPS-1 概要 自然免疫による病原体成分の認識は炎症反応の誘導や 獲得免疫の成立に重要な役割を果たす生体防御機構です 今回 私達はウイルス RNA を模倣する合成二本鎖 RNA アナログの Poly I:C を用いて 自然免疫応答メカニズムの解析を行いました その結果 Poly I:C により一部の樹状細胞にネクローシス様の細胞死が誘導されること さらにこの細胞死がシグナル伝達経路の活性化により制御されていることが分かりました
RNA Poly IC D-IPS-1 概要 自然免疫による病原体成分の認識は炎症反応の誘導や 獲得免疫の成立に重要な役割を果たす生体防御機構です 今回 私達はウイルス RNA を模倣する合成二本鎖 RNA アナログの Poly I:C を用いて 自然免疫応答メカニズムの解析を行いました その結果 Poly I:C により一部の樹状細胞にネクローシス様の細胞死が誘導されること さらにこの細胞死がシグナル伝達経路の活性化により制御されていることが分かりました
学位論文の内容の要旨 論文提出者氏名 佐藤雄哉 論文審査担当者 主査田中真二 副査三宅智 明石巧 論文題目 Relationship between expression of IGFBP7 and clinicopathological variables in gastric cancer (
 学位論文の内容の要旨 論文提出者氏名 佐藤雄哉 論文審査担当者 主査田中真二 副査三宅智 明石巧 論文題目 Relationship between expression of IGFBP7 and clinicopathological variables in gastric cancer ( 論文内容の要旨 ) < 要旨 > Insulin-like growth factor ( 以下 IGF)
学位論文の内容の要旨 論文提出者氏名 佐藤雄哉 論文審査担当者 主査田中真二 副査三宅智 明石巧 論文題目 Relationship between expression of IGFBP7 and clinicopathological variables in gastric cancer ( 論文内容の要旨 ) < 要旨 > Insulin-like growth factor ( 以下 IGF)
学位論文の要約
 学位論文内容の要約 愛知学院大学 甲第 678 号論文提出者土屋範果 論文題目 骨芽細胞におけるずり応力誘発性 細胞内 Ca 2+ 濃度上昇へのグルタミン酸の関与 No. 1 愛知学院大学 Ⅰ. 緒言 矯正歯科治療時には機械刺激により骨リモデリングが誘発される 機械 刺激が骨リモデリングや骨量の制御因子の一つであることはよく知られて いるが 骨関連細胞が機械刺激を感受する分子機構は十分に明らかにされ
学位論文内容の要約 愛知学院大学 甲第 678 号論文提出者土屋範果 論文題目 骨芽細胞におけるずり応力誘発性 細胞内 Ca 2+ 濃度上昇へのグルタミン酸の関与 No. 1 愛知学院大学 Ⅰ. 緒言 矯正歯科治療時には機械刺激により骨リモデリングが誘発される 機械 刺激が骨リモデリングや骨量の制御因子の一つであることはよく知られて いるが 骨関連細胞が機械刺激を感受する分子機構は十分に明らかにされ
アミヴィッド静注 CTD 第 2 部 2.1 第 2 部から第 5 部の目次 富士フイルム RI ファーマ株式会社
 CTD 第 2 部 富士フイルム RI ファーマ株式会社 ( 空白ページ ) 2 第 2 部 ( モジュール 2): CTD の概要 ( サマリー ) ---------------------------------------------- 第 2 巻 2.2 緒言 2.3 品質に関する概括資料緒言 2.3.S 原薬 (AV-105, ) 2.3.S 原薬 ( フロルベタピル ( 18 F),
CTD 第 2 部 富士フイルム RI ファーマ株式会社 ( 空白ページ ) 2 第 2 部 ( モジュール 2): CTD の概要 ( サマリー ) ---------------------------------------------- 第 2 巻 2.2 緒言 2.3 品質に関する概括資料緒言 2.3.S 原薬 (AV-105, ) 2.3.S 原薬 ( フロルベタピル ( 18 F),
法医学問題「想定問答」(記者会見後:平成15年 月 日)
 平成 28 年 5 月 26 日 肺がんに対する新たな分子標的治療を発見! 本研究成果のポイント 肺がんのうち 5% 程度を占める KRAS( 1) 遺伝子変異肺がんは, 上皮間葉移行 ( 2) 状態により上皮系と間葉系の 2 種類に分類される KRAS 遺伝子変異を有する肺がんに対し現在臨床試験中の MEK 阻害薬は, 投与後に細胞表面受容体を活性化することにより効果が減弱され, 活性化される細胞表面受容体は上皮間葉移行状態により異なる
平成 28 年 5 月 26 日 肺がんに対する新たな分子標的治療を発見! 本研究成果のポイント 肺がんのうち 5% 程度を占める KRAS( 1) 遺伝子変異肺がんは, 上皮間葉移行 ( 2) 状態により上皮系と間葉系の 2 種類に分類される KRAS 遺伝子変異を有する肺がんに対し現在臨床試験中の MEK 阻害薬は, 投与後に細胞表面受容体を活性化することにより効果が減弱され, 活性化される細胞表面受容体は上皮間葉移行状態により異なる
Untitled
 上原記念生命科学財団研究報告集, 25 (2011) 86. 線虫 C. elegans およびマウスをモデル動物とした体細胞レベルで生じる性差の解析 井上英樹 Key words: 性差, ストレス応答,DMRT 立命館大学生命科学部生命医科学科 緒言性差は雌雄の性に分かれた動物にみられ, 生殖能力の違いだけでなく形態, 行動などそれぞれの性の間でみられる様々な差異と定義される. 性差は, 形態や行動だけでなく疾患の発症リスクの男女差といった生理的なレベルの差異も含まれる.
上原記念生命科学財団研究報告集, 25 (2011) 86. 線虫 C. elegans およびマウスをモデル動物とした体細胞レベルで生じる性差の解析 井上英樹 Key words: 性差, ストレス応答,DMRT 立命館大学生命科学部生命医科学科 緒言性差は雌雄の性に分かれた動物にみられ, 生殖能力の違いだけでなく形態, 行動などそれぞれの性の間でみられる様々な差異と定義される. 性差は, 形態や行動だけでなく疾患の発症リスクの男女差といった生理的なレベルの差異も含まれる.
能性を示した < 方法 > M-CSF RANKL VEGF-C Ds-Red それぞれの全長 cdnaを レトロウイルスを用いてHeLa 細胞に遺伝子導入した これによりM-CSFとDs-Redを発現するHeLa 細胞 (HeLa-M) RANKLと Ds-Redを発現するHeLa 細胞 (HeL
 学位論文の内容の要旨 論文提出者氏名 秦野雄 論文審査担当者 主査竹田秀副査北川昌伸 山口朗 論文題目 Tumor associated osteoclast-like giant cells promote tumor growth and lymphangiogenesis by secreting vascular endothelial growth factor-c ( 論文内容の要旨 )
学位論文の内容の要旨 論文提出者氏名 秦野雄 論文審査担当者 主査竹田秀副査北川昌伸 山口朗 論文題目 Tumor associated osteoclast-like giant cells promote tumor growth and lymphangiogenesis by secreting vascular endothelial growth factor-c ( 論文内容の要旨 )
本日の内容 HbA1c 測定方法別原理と特徴 HPLC 法 免疫法 酵素法 原理差による測定値の乖離要因
 HbA1c 測定系について ~ 原理と特徴 ~ 一般社団法人日本臨床検査薬協会 技術運営委員会副委員長 安部正義 本日の内容 HbA1c 測定方法別原理と特徴 HPLC 法 免疫法 酵素法 原理差による測定値の乖離要因 HPLC 法 HPLC 法原理 高速液体クロマトグラフィー 混合物の分析法の一つ 固体または液体の固定相 ( 吸着剤 ) 中で 液体または気体の移動相 ( 展開剤 ) に試料を加えて移動させ
HbA1c 測定系について ~ 原理と特徴 ~ 一般社団法人日本臨床検査薬協会 技術運営委員会副委員長 安部正義 本日の内容 HbA1c 測定方法別原理と特徴 HPLC 法 免疫法 酵素法 原理差による測定値の乖離要因 HPLC 法 HPLC 法原理 高速液体クロマトグラフィー 混合物の分析法の一つ 固体または液体の固定相 ( 吸着剤 ) 中で 液体または気体の移動相 ( 展開剤 ) に試料を加えて移動させ
Peroxisome Proliferator-Activated Receptor a (PPARa)アゴニストの薬理作用メカニズムの解明
 インスリンによる脂肪細胞の数とサイズの制御機構の解明 Clarification of Regulatory Mechanisms for Determining Number and Size of Adipocytes by Insulin 平成 25 年度論文博士申請者 指導教員 伊藤実 (Ito, Minoru) 本島清人 肥満は糖尿病 脂質異常症 高血圧 動脈硬化症などの生活習慣病の基盤となるリスクファクターである
インスリンによる脂肪細胞の数とサイズの制御機構の解明 Clarification of Regulatory Mechanisms for Determining Number and Size of Adipocytes by Insulin 平成 25 年度論文博士申請者 指導教員 伊藤実 (Ito, Minoru) 本島清人 肥満は糖尿病 脂質異常症 高血圧 動脈硬化症などの生活習慣病の基盤となるリスクファクターである
今後の展開現在でも 自己免疫疾患の発症機構については不明な点が多くあります 今回の発見により 今後自己免疫疾患の発症機構の理解が大きく前進すると共に 今まで見過ごされてきたイントロン残存の重要性が 生体反応の様々な局面で明らかにされることが期待されます 図 1 Jmjd6 欠損型の胸腺をヌードマウス
 PRESS RELEASE(2015/11/05) 九州大学広報室 819-0395 福岡市西区元岡 744 TEL:092-802-2130 FAX:092-802-2139 MAIL:koho@jimu.kyushu-u.ac.jp URL:http://www.kyushu-u.ac.jp 免疫細胞が自分自身を攻撃しないために必要な新たな仕組みを発見 - 自己免疫疾患の発症機構の解明に期待 -
PRESS RELEASE(2015/11/05) 九州大学広報室 819-0395 福岡市西区元岡 744 TEL:092-802-2130 FAX:092-802-2139 MAIL:koho@jimu.kyushu-u.ac.jp URL:http://www.kyushu-u.ac.jp 免疫細胞が自分自身を攻撃しないために必要な新たな仕組みを発見 - 自己免疫疾患の発症機構の解明に期待 -
PowerPoint プレゼンテーション
 酵素 : タンパク質の触媒 タンパク質 Protein 酵素 Enzyme 触媒 Catalyst 触媒 Cataylst: 特定の化学反応の反応速度を速める物質 自身は反応の前後で変化しない 酵素 Enzyme: タンパク質の触媒 触媒作用を持つタンパク質 第 3 回 : タンパク質はアミノ酸からなるポリペプチドである 第 4 回 : タンパク質は様々な立体構造を持つ 第 5 回 : タンパク質の立体構造と酵素活性の関係
酵素 : タンパク質の触媒 タンパク質 Protein 酵素 Enzyme 触媒 Catalyst 触媒 Cataylst: 特定の化学反応の反応速度を速める物質 自身は反応の前後で変化しない 酵素 Enzyme: タンパク質の触媒 触媒作用を持つタンパク質 第 3 回 : タンパク質はアミノ酸からなるポリペプチドである 第 4 回 : タンパク質は様々な立体構造を持つ 第 5 回 : タンパク質の立体構造と酵素活性の関係
Microsoft PowerPoint - agonist
 図説薬理学 Pictured Pharmacology アゴニストとアンタゴニストの関係 宮崎大学農学部獣医薬理学講座伊藤勝昭 禁 : 無断転載 Copyright: Katsuaki Ito Veterinary Pharmacology University of Miyazaki このファイルは学生が講義で聞いた内容を正確に より深く理解するために作られたもので 教科書の補助資料です ファイルの内容の無断転載を防ぐため
図説薬理学 Pictured Pharmacology アゴニストとアンタゴニストの関係 宮崎大学農学部獣医薬理学講座伊藤勝昭 禁 : 無断転載 Copyright: Katsuaki Ito Veterinary Pharmacology University of Miyazaki このファイルは学生が講義で聞いた内容を正確に より深く理解するために作られたもので 教科書の補助資料です ファイルの内容の無断転載を防ぐため
<4D F736F F D F4390B38CE3816A90528DB88C8B89CA2E646F63>
 学位論文の内容の要旨 論文提出者氏名 論文審査担当者 論文題目 主査 荒川真一 御給美沙 副査木下淳博横山三紀 Thrombospondin-1 Production is Enhanced by Porphyromonas gingivalis Lipopolysaccharide in THP-1 Cells ( 論文の内容の要旨 ) < 要旨 > 歯周炎はグラム陰性嫌気性細菌によって引き起こされる慢性炎症性疾患であり
学位論文の内容の要旨 論文提出者氏名 論文審査担当者 論文題目 主査 荒川真一 御給美沙 副査木下淳博横山三紀 Thrombospondin-1 Production is Enhanced by Porphyromonas gingivalis Lipopolysaccharide in THP-1 Cells ( 論文の内容の要旨 ) < 要旨 > 歯周炎はグラム陰性嫌気性細菌によって引き起こされる慢性炎症性疾患であり
緒言
 CERA 2.2 緒言 Page 1 ミルセラ注シリンジ25 μg ミルセラ注シリンジ50 μg ミルセラ注シリンジ75 μg ミルセラ注シリンジ100 μg ミルセラ注シリンジ150 μg ミルセラ注シリンジ200 μg ミルセラ注シリンジ250 μg [ 腎性貧血 ] 第 2 部 CTD の概要 ( サマリー ) 2.2 緒言 中外製薬株式会社 CERA 2.2 緒言 Page 2 目次頁 2.2
CERA 2.2 緒言 Page 1 ミルセラ注シリンジ25 μg ミルセラ注シリンジ50 μg ミルセラ注シリンジ75 μg ミルセラ注シリンジ100 μg ミルセラ注シリンジ150 μg ミルセラ注シリンジ200 μg ミルセラ注シリンジ250 μg [ 腎性貧血 ] 第 2 部 CTD の概要 ( サマリー ) 2.2 緒言 中外製薬株式会社 CERA 2.2 緒言 Page 2 目次頁 2.2
上原記念生命科学財団研究報告集, 31 (2017)
 上原記念生命科学財団研究報告集, 31 (2017) 172. 骨肉腫の転移巣形成機序の解明と治療標的の探索 三輪真嗣 * 金沢大学大学院医薬保健学総合研究科先進運動器医療創成講座 Key words: 骨肉腫, 新規治療,GSK-3β 緒言骨肉腫は 10~20 代に好発する悪性骨腫瘍であり その発生頻度は 1~2 人 /100 万人といわれている 化学療法の導入前は患肢切断術が基本であったが長期生存は
上原記念生命科学財団研究報告集, 31 (2017) 172. 骨肉腫の転移巣形成機序の解明と治療標的の探索 三輪真嗣 * 金沢大学大学院医薬保健学総合研究科先進運動器医療創成講座 Key words: 骨肉腫, 新規治療,GSK-3β 緒言骨肉腫は 10~20 代に好発する悪性骨腫瘍であり その発生頻度は 1~2 人 /100 万人といわれている 化学療法の導入前は患肢切断術が基本であったが長期生存は
Wnt3 positively and negatively regu Title differentiation of human periodonta Author(s) 吉澤, 佑世 Journal, (): - URL Rig
 Wnt3 positively and negatively regu Title differentiation of human periodonta Author(s) 吉澤, 佑世 Journal, (): - URL http://hdl.handle.net/10130/3408 Right Posted at the Institutional Resources for Unique
Wnt3 positively and negatively regu Title differentiation of human periodonta Author(s) 吉澤, 佑世 Journal, (): - URL http://hdl.handle.net/10130/3408 Right Posted at the Institutional Resources for Unique
上原記念生命科学財団研究報告集, 30 (2016)
 上原記念生命科学財団研究報告集, 30 (2016) 147. オートファジーと細胞死を制御する癌抑制遺伝子の発見 難波卓司 高知大学教育研究部総合科学系複合領域科学部門 Key words: 小胞体ストレス, オートファジー,BAP31 緒言多くの固形癌や転移した癌は低栄養環境に置かれ 増殖を行うにはその環境に適応する必要がある そのため 癌細胞の低栄養環境への適応の阻害は新たな抗癌剤のターゲットとして有望であると考えられている
上原記念生命科学財団研究報告集, 30 (2016) 147. オートファジーと細胞死を制御する癌抑制遺伝子の発見 難波卓司 高知大学教育研究部総合科学系複合領域科学部門 Key words: 小胞体ストレス, オートファジー,BAP31 緒言多くの固形癌や転移した癌は低栄養環境に置かれ 増殖を行うにはその環境に適応する必要がある そのため 癌細胞の低栄養環境への適応の阻害は新たな抗癌剤のターゲットとして有望であると考えられている
Untitled
 上原記念生命科学財団研究報告集, 23(2009) 149. サルエイズウイルスのヒトへの感染伝播を規定する宿主制御因子の解明 武内寛明 Key words: エイズウイルス, 異種間感染, 感染症, 人畜共通感染症, 新興感染症 東京大学医科学研究所感染症国際研究センター微生物学分野 緒言ヒト後天性免疫不全症候群 ( ヒトエイズ ) は, ヒト免疫不全ウイルス (HIV) によって引き起こされる慢性持続感染症である.
上原記念生命科学財団研究報告集, 23(2009) 149. サルエイズウイルスのヒトへの感染伝播を規定する宿主制御因子の解明 武内寛明 Key words: エイズウイルス, 異種間感染, 感染症, 人畜共通感染症, 新興感染症 東京大学医科学研究所感染症国際研究センター微生物学分野 緒言ヒト後天性免疫不全症候群 ( ヒトエイズ ) は, ヒト免疫不全ウイルス (HIV) によって引き起こされる慢性持続感染症である.
医療用医薬品最新品質情報集 ( ブルーブック ) 初版有効成分リトドリン塩酸塩 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 (25 ) 1) 溶解度 (37 ) 1 ウテロン錠 5mg サンド 2
 医療用医薬品最新品質情報集 ( ブルーブック ) 2018.7.13 初版有効成分リトドリン塩酸塩 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 (25 ) 1) 溶解度 (37 ) 1 ウテロン錠 5mg サンド 2 塩酸リトドリン錠 5mg YD 陽進堂 3 リトドリン錠 5mg PP ポーラファルマ 4 ルテオニン錠
医療用医薬品最新品質情報集 ( ブルーブック ) 2018.7.13 初版有効成分リトドリン塩酸塩 品目名 ( 製造販売業者 ) 後発医薬品 品目名 ( 製造販売業者 ) 先発医薬品 効能 効果用法 用量添加物 1) 解離定数 (25 ) 1) 溶解度 (37 ) 1 ウテロン錠 5mg サンド 2 塩酸リトドリン錠 5mg YD 陽進堂 3 リトドリン錠 5mg PP ポーラファルマ 4 ルテオニン錠
学位論文内容の要旨 Abstract Background This study was aimed to evaluate the expression of T-LAK cell originated protein kinase (TOPK) in the cultured glioma ce
 はやしともひで 氏名林智秀 学位の種類博士 ( 医学 ) 学位記番号 富生命博甲第 92 号 学位授与年月日 平成 29 年 9 月 28 日 専攻名認知 情動脳科学専攻 学位授与の要件 富山大学学位規則第 3 条第 3 項該当 学位論文題目 Impact of T-LAK cell originated protein kinase (TOPK) expression on outcome in
はやしともひで 氏名林智秀 学位の種類博士 ( 医学 ) 学位記番号 富生命博甲第 92 号 学位授与年月日 平成 29 年 9 月 28 日 専攻名認知 情動脳科学専攻 学位授与の要件 富山大学学位規則第 3 条第 3 項該当 学位論文題目 Impact of T-LAK cell originated protein kinase (TOPK) expression on outcome in
Untitled
 上原記念生命科学財団研究報告集, 23(2009) 71. 間葉系細胞へ分化する能力を有するグリオーマ細胞の characterization と組織内局在 岩下寿秀 Key words: グリオーマ, 間葉系細胞,side population * 愛知医科大学医学部病理学講座 緒言腫瘍組織はヘテロな細胞集団であり,at random に増殖していると考えられてきたが, 最近の研究結果から腫瘍組織にも正常の組織と同様のヒエラルキーが存在する可能性が示唆されている.
上原記念生命科学財団研究報告集, 23(2009) 71. 間葉系細胞へ分化する能力を有するグリオーマ細胞の characterization と組織内局在 岩下寿秀 Key words: グリオーマ, 間葉系細胞,side population * 愛知医科大学医学部病理学講座 緒言腫瘍組織はヘテロな細胞集団であり,at random に増殖していると考えられてきたが, 最近の研究結果から腫瘍組織にも正常の組織と同様のヒエラルキーが存在する可能性が示唆されている.
一般薬理試験及び毒性試験 2. 毒性試験 (1) 単回投与毒性試験 ( マウス イヌ サル ) 33) 動物種 投与経路 投与量 (mg/kg) 概略の致死量 (mg/kg) マウス 経口 2000 雌雄 :>2000 腹腔内 300 雌雄 :300 経口 750 雌雄 :>750 腹腔内 500
 枢神経系影響なし心血管系一般薬理試験及び毒性試験 1. 一般薬理試験 32) 試験項目 動物種 ( 性 動物数 ) 投与経路投与量主な結果 評価中一般状態 体温及び自発運動量に及ぼす作用 (Irwin 法 ) ( 雄 4 ) 30 100 300mg/kg herg 電流に及ぼす作用 ( ホールセルパッチクランプ法 ) herg 発現ヒト胎児腎細胞株 HEK293 in vitro 4 20 100μmol/L
枢神経系影響なし心血管系一般薬理試験及び毒性試験 1. 一般薬理試験 32) 試験項目 動物種 ( 性 動物数 ) 投与経路投与量主な結果 評価中一般状態 体温及び自発運動量に及ぼす作用 (Irwin 法 ) ( 雄 4 ) 30 100 300mg/kg herg 電流に及ぼす作用 ( ホールセルパッチクランプ法 ) herg 発現ヒト胎児腎細胞株 HEK293 in vitro 4 20 100μmol/L
生理学 1章 生理学の基礎 1-1. 細胞の主要な構成成分はどれか 1 タンパク質 2 ビタミン 3 無機塩類 4 ATP 第5回 按マ指 (1279) 1-2. 細胞膜の構成成分はどれか 1 無機りん酸 2 リボ核酸 3 りん脂質 4 乳酸 第6回 鍼灸 (1734) E L 1-3. 細胞膜につ
 の基礎 1-1. 細胞の主要な構成成分はどれか 1 タンパク質 2 ビタミン 3 無機塩類 4 ATP 第5回 (1279) 1-2. 細胞膜の構成成分はどれか 1 無機りん酸 2 リボ核酸 3 りん脂質 4 乳酸 第6回 (1734) 1-3. 細胞膜について正しい記述はどれか 1 糖脂質分子が規則正しく配列している 2 イオンに対して選択的な透過性をもつ 3 タンパク質分子の二重層膜からなる 4
の基礎 1-1. 細胞の主要な構成成分はどれか 1 タンパク質 2 ビタミン 3 無機塩類 4 ATP 第5回 (1279) 1-2. 細胞膜の構成成分はどれか 1 無機りん酸 2 リボ核酸 3 りん脂質 4 乳酸 第6回 (1734) 1-3. 細胞膜について正しい記述はどれか 1 糖脂質分子が規則正しく配列している 2 イオンに対して選択的な透過性をもつ 3 タンパク質分子の二重層膜からなる 4
PowerPoint プレゼンテーション
 細胞の情報伝達 (1) 何を学習するか細胞が環境からシグナル ( 刺激 ) を受けて 細胞の状態が変化するときに 細胞内でどのような現象が起きているか を知る分子の大変複雑な連続反応であるので 反応の最初の段階を中心に見ていく ( 共通の現象が多いから ; 疾患の治療の標的となる分子が多い ) これを知るために (2) リガンドの拡散様式 ( 図 16-3) リガンドを発現する細胞とこれを受け取る細胞との
細胞の情報伝達 (1) 何を学習するか細胞が環境からシグナル ( 刺激 ) を受けて 細胞の状態が変化するときに 細胞内でどのような現象が起きているか を知る分子の大変複雑な連続反応であるので 反応の最初の段階を中心に見ていく ( 共通の現象が多いから ; 疾患の治療の標的となる分子が多い ) これを知るために (2) リガンドの拡散様式 ( 図 16-3) リガンドを発現する細胞とこれを受け取る細胞との
cover
 旭川医科大学研究フォーラム (2016.3) 16:42-45. 平成 25 26 年度 独創性のある生命科学研究 個別研究課題 24) 脂肪組織由来幹細胞を用いた低浸襲細胞治療に関する研究 岡久美子 24) 脂肪組織由来幹細胞を用いた低侵襲細胞治療に関する研究研究代表者岡久美子 研究目的 細胞治療は骨再建 再生を低侵襲 効率的に行うために有用である 近年 脂肪組織に含まれる体性幹細胞 (Adiposederivedstem
旭川医科大学研究フォーラム (2016.3) 16:42-45. 平成 25 26 年度 独創性のある生命科学研究 個別研究課題 24) 脂肪組織由来幹細胞を用いた低浸襲細胞治療に関する研究 岡久美子 24) 脂肪組織由来幹細胞を用いた低侵襲細胞治療に関する研究研究代表者岡久美子 研究目的 細胞治療は骨再建 再生を低侵襲 効率的に行うために有用である 近年 脂肪組織に含まれる体性幹細胞 (Adiposederivedstem
Untitled
 上原記念生命科学財団研究報告集, 24(2010) 164. 消化器癌におけるエピジェネティックな microrna 異常の解析 鈴木拓 Key words: 胃癌, 大腸癌,microRNA, DNA メチル化, 癌抑制遺伝子 札幌医科大学医学部内科学第一講座 緒言 microrna( 以下 mirna) は 18 ~ 22 塩基程度の短い non-coding RNA であり, 分化 増殖 アポトーシスなど細胞内の様々なプロセスに重要な役割を担っている
上原記念生命科学財団研究報告集, 24(2010) 164. 消化器癌におけるエピジェネティックな microrna 異常の解析 鈴木拓 Key words: 胃癌, 大腸癌,microRNA, DNA メチル化, 癌抑制遺伝子 札幌医科大学医学部内科学第一講座 緒言 microrna( 以下 mirna) は 18 ~ 22 塩基程度の短い non-coding RNA であり, 分化 増殖 アポトーシスなど細胞内の様々なプロセスに重要な役割を担っている
ん細胞の標的分子の遺伝子に高い頻度で変異が起きています その結果 標的分子の特定のアミノ酸が別のアミノ酸へと置き換わることで分子標的療法剤の標的分子への結合が阻害されて がん細胞が薬剤耐性を獲得します この病態を克服するためには 標的分子に遺伝子変異を持つモデル細胞を樹立して そのモデル細胞系を用い
 プレスリリース 平成 30 年 7 月 6 日 各報道機関御中 国立大学法人山梨大学 CRISPR/Cas9 によるゲノム編集技術を用いた 白血病細胞への分子標的療法剤に対する耐性遺伝子変異の導入 新規治療薬を開発するためのモデル細胞系の樹立方法の確立 - 山梨大学医学部小児科学講座の玉井望雅と犬飼岳史准教授らの研究グループは 筑波大学および大阪大学との共同研究で CRISPR/Cas9 によるゲノム編集技術を用いて白血病細胞株に薬剤耐性の遺伝子変異を導入することに世界で初めて成功しました
プレスリリース 平成 30 年 7 月 6 日 各報道機関御中 国立大学法人山梨大学 CRISPR/Cas9 によるゲノム編集技術を用いた 白血病細胞への分子標的療法剤に対する耐性遺伝子変異の導入 新規治療薬を開発するためのモデル細胞系の樹立方法の確立 - 山梨大学医学部小児科学講座の玉井望雅と犬飼岳史准教授らの研究グループは 筑波大学および大阪大学との共同研究で CRISPR/Cas9 によるゲノム編集技術を用いて白血病細胞株に薬剤耐性の遺伝子変異を導入することに世界で初めて成功しました
生物学に関する実験例 - 生化学 / 医療に関する実験例 ラジオアッセイ法によるホルモン測定 [ 目的 ] 本実習では, 放射免疫測定 (Radioimmunoassay,RIA) 法による血中インスリンとイムノラジオメトリックアッセイ ( 免疫放射定測定 Immunoradiometric ass
![生物学に関する実験例 - 生化学 / 医療に関する実験例 ラジオアッセイ法によるホルモン測定 [ 目的 ] 本実習では, 放射免疫測定 (Radioimmunoassay,RIA) 法による血中インスリンとイムノラジオメトリックアッセイ ( 免疫放射定測定 Immunoradiometric ass 生物学に関する実験例 - 生化学 / 医療に関する実験例 ラジオアッセイ法によるホルモン測定 [ 目的 ] 本実習では, 放射免疫測定 (Radioimmunoassay,RIA) 法による血中インスリンとイムノラジオメトリックアッセイ ( 免疫放射定測定 Immunoradiometric ass](/thumbs/104/163903931.jpg) 生物学に関する実験例 - 生化学 / 医療に関する実験例 ラジオアッセイ法によるホルモン測定 [ 目的 ] 本実習では, 放射免疫測定 (Radioimmunoassay,RIA) 法による血中インスリンとイムノラジオメトリックアッセイ ( 免疫放射定測定 Immunoradiometric assay, IRMA) 法による血清中のレニンを定量を通して 今日用いられている種々のインビトロ検査法の原理並びに両者の違い等を理解する
生物学に関する実験例 - 生化学 / 医療に関する実験例 ラジオアッセイ法によるホルモン測定 [ 目的 ] 本実習では, 放射免疫測定 (Radioimmunoassay,RIA) 法による血中インスリンとイムノラジオメトリックアッセイ ( 免疫放射定測定 Immunoradiometric assay, IRMA) 法による血清中のレニンを定量を通して 今日用いられている種々のインビトロ検査法の原理並びに両者の違い等を理解する
[PDF] 蛍光タンパク質FRETプローブを用いたアポトーシスのタイムラプス解析
![[PDF] 蛍光タンパク質FRETプローブを用いたアポトーシスのタイムラプス解析 [PDF] 蛍光タンパク質FRETプローブを用いたアポトーシスのタイムラプス解析](/thumbs/94/118065377.jpg) ApplicationNote Vol. BioStation ID Time-Lapse Analysis of Apototic Cells by FRET-based indicator 蛍光タンパク質 FRET プローブを用いたアポトーシスのタイムラプス解析 サンプル提供 : 理化学研究所脳科学研究センター宮脇敦先生 はじめに Fluorescence Resonance Energy Transfer
ApplicationNote Vol. BioStation ID Time-Lapse Analysis of Apototic Cells by FRET-based indicator 蛍光タンパク質 FRET プローブを用いたアポトーシスのタイムラプス解析 サンプル提供 : 理化学研究所脳科学研究センター宮脇敦先生 はじめに Fluorescence Resonance Energy Transfer
<4D F736F F F696E74202D2097D58FB08E8E8CB1838F815B834E F197D58FB E96D8816A66696E616C CF68A4A2E >
 再生医療等製品の非臨床安全性評価の考え方 ex vivo 遺伝子治療を中心に 独立行政法人医薬品医療機器総合機構 (PMDA) 再生医療製品等審査部 真木一茂 様式 1-B 第 24 回日本遺伝子細胞治療学会学術集会 CO I 開示 発表者名 : 真木一茂 演題発表に関連し 開示すべき CO I 関係にある企業などはありません 2 1 本日の話 1.Ex vivo 遺伝子治療について 2. 治験開始に必要な非臨床試験
再生医療等製品の非臨床安全性評価の考え方 ex vivo 遺伝子治療を中心に 独立行政法人医薬品医療機器総合機構 (PMDA) 再生医療製品等審査部 真木一茂 様式 1-B 第 24 回日本遺伝子細胞治療学会学術集会 CO I 開示 発表者名 : 真木一茂 演題発表に関連し 開示すべき CO I 関係にある企業などはありません 2 1 本日の話 1.Ex vivo 遺伝子治療について 2. 治験開始に必要な非臨床試験
ASC は 8 週齢 ICR メスマウスの皮下脂肪組織をコラゲナーゼ処理後 遠心分離で得たペレットとして単離し BMSC は同じマウスの大腿骨からフラッシュアウトにより獲得した 10%FBS 1% 抗生剤を含む DMEM にて それぞれ培養を行った FACS Passage 2 (P2) の ASC
 学位論文の内容の要旨 論文提出者氏名 山本麻衣子 論文審査担当者 主査 : 井関祥子副査 : 柴田俊一 青木和広 Osteogenic Potential of Mouse Adipose-Derived Stem Cells Sorted 論文題目 for CD90 and CD105 in Vitro ( 論文の内容の要旨 ) < 緒言 > 脂肪組織は皮下の浅層に存在するため 採取が低侵襲で容易であり
学位論文の内容の要旨 論文提出者氏名 山本麻衣子 論文審査担当者 主査 : 井関祥子副査 : 柴田俊一 青木和広 Osteogenic Potential of Mouse Adipose-Derived Stem Cells Sorted 論文題目 for CD90 and CD105 in Vitro ( 論文の内容の要旨 ) < 緒言 > 脂肪組織は皮下の浅層に存在するため 採取が低侵襲で容易であり
平成 28 年 12 月 12 日 癌の転移の一種である胃癌腹膜播種 ( ふくまくはしゅ ) に特異的な新しい標的分子 synaptotagmin 8 の発見 ~ 革新的な分子標的治療薬とそのコンパニオン診断薬開発へ ~ 名古屋大学大学院医学系研究科 ( 研究科長 髙橋雅英 ) 消化器外科学の小寺泰
 平成 28 年 12 月 12 日 癌の転移の一種である胃癌腹膜播種 ( ふくまくはしゅ ) に特異的な新しい標的分子 synaptotagmin 8 の発見 ~ 革新的な分子標的治療薬とそのコンパニオン診断薬開発へ ~ 名古屋大学大学院医学系研究科 ( 研究科長 髙橋雅英 ) 消化器外科学の小寺泰弘 ( こでらやすひろ ) 教授 神田光郎 ( かんだみつろう ) 助教の研究グループは ほぼ全ての既知の遺伝子とその選択的スプライシング産物を対象とした
平成 28 年 12 月 12 日 癌の転移の一種である胃癌腹膜播種 ( ふくまくはしゅ ) に特異的な新しい標的分子 synaptotagmin 8 の発見 ~ 革新的な分子標的治療薬とそのコンパニオン診断薬開発へ ~ 名古屋大学大学院医学系研究科 ( 研究科長 髙橋雅英 ) 消化器外科学の小寺泰弘 ( こでらやすひろ ) 教授 神田光郎 ( かんだみつろう ) 助教の研究グループは ほぼ全ての既知の遺伝子とその選択的スプライシング産物を対象とした

 測定した また Scrは酵素法にて測定し その参考基 r =0.575 p
測定した また Scrは酵素法にて測定し その参考基 r =0.575 p