スライド 1
|
|
|
- ときな たなせ
- 7 years ago
- Views:
Transcription
1 資料 7-3 治験の効率化を目指した医療機関と依頼者の共有プロセス - 施設選定から Site initiation- 欧州製薬団体連合会技術委員会臨床部会 青野寛之, 越智由貴子 ( アストラゼネカ株式会社 ), 原輝文, 西山逸夫 ( グラクソ スミスクライン株式会社 ), 廣瀬隆 ( サノフィ アベンティス株式会社 ), 山地宏和 ( 日本ベーリンガーインゲルハイム株式会社 ), 桜井丙午 ( ノバルティスファーマ株式会社 ), 大土井久暁 ( ノボノルディスクファーマ株式会社 ), 辻本朋美 ( バイエル薬品株式会社 ), 眞下秀樹 ( ユーシービージャパン株式会社 )
2 目的 欧州製薬団体連合会 (EFPIA) 臨床部会では, 国際的に競争力のある治験環境を実現するために, 2003 年より治験環境調査を行い, 治験の効率化のためにこれまで種々の提言を行ってきた. 今回, 施設選定の情報収集からSite initiation* までの期間短縮及び効率化を目指して, 依頼者と医療機関の共有プロセスを作成した. * 医療機関に治験薬 資材を搬入して 被験者のリクルートが開始できるようになる日
3 背景 欧州製薬団体連合会 (EFPIA) 臨床部会の治験環境調査 (2008 年 ) によると, 初回訪問から契約までの訪問回数は平均値 5.2 回, 最大値 27 回, 最低値 1 回であった ( 図 1). 訪問回数に影響すると考えられる項目の集計結果 ( 抜粋 ) は以下の通りであった. 1.IRB 審議資料等の送付一部は持参が必要 : 11%, 認められていない :3.1% 2. IRB 出席 54.4% 3. 契約までに面会した訪問先 5 部署以上 :31.3% 4. 治験事務局の院内書類 ( 履歴書など ) の一元管理ある程度行なってくれた :26.9%, あまり行ってくれなかった :11.3%, 全く行ってくれなかった :5.9%
4 大学B大学C大学B大学C 病学A病院院AB病院病院B病院C図 1. 初回訪問から契約締結までの訪問回数 国公立大学 私立大学 ( 回数 ) ( 回数 ) 大平均値 :6.9 最大値 :27 最小値 :2 平均値 :9.0 最大値 :22 最小値 :2 3 回 3 回 ( 回数 ) 学A国立病院公立病院大 平均値 :5.6 最大値 :20 最小値 :1 0 ( 回数 ) 平均値 :6.1 最大値 :25 最小値 : 回 3 回 5 0 病 院CA 0 初回訪問から契約締結までの訪問回数 (EFPIA 環境調査 2008)( プロトコール毎 )
5 医療機関における効率化の取組みの実例 ( 各医療機関共通の取組み ) 1. 治験関連業務窓口を治験事務局で一本化 2. 医師の履歴書の一元管理 3. ,Telによる対応, 郵送による書類の授受 4. ヒアリング時に全関係部門について一括で協議 決定 第 29 回日本臨床薬理学会治験環境改善への取り組みの現状とその課題 2-P-014
6 方法 施設選定の情報収集から Site initiation までの流れを, 医療機関への訪問が必須である項目 ( 治験責任医師及び施設の選定など ) と訪問以外の方法 ( 郵送, 電話, 等 ) で対応可能な項目に分け, 医療機関と依頼者が実施する項目と手順を特定した共有プロセスを作成した. さらに, 一部の医療機関の協力を得て, 医療機関からみた本プロセスの評価を実施した.
7 医療機関と依頼者の共有プロセス の作成ポイント 新たな取り組み 事前アンケート 依頼前から実務的打ち合わせの開始 ( ヒアリング兼実務担当者打合せ ) ヒアリング準備シートを利用する 医療機関側 事務局 依頼者との橋渡し 院内のすり合わせ, 取りまとめ 各関係者の面会のアポイント調整 依頼者からの確認事項, 要請に関してメールや電話により対応 CV( 履歴書 ) や FD( ファイナンシャルディスクロージャー ) の全員分の 収集に協力 依頼者標準版 ( 症例ファイル等 ) の使用の推奨, 施設版が必要な場合は施設側で作成 依頼者側 試験概要, プロトコールなど実務的な手順の早期確定, 提示 ヒアリングまでに症例ファイル / ワークシート標準版を作成 メールや電話により医療機関側に必要十分な情報を逐次交換
8 共有プロセスの評価方法 1. 共有プロセスの説明と意見聴取 8 施設と 1SMO を対象として本プロセスについて説明を行い, 実施可能性や検討が必要なポイントについて意見聴取を行った. 2. パイロット試験の実施 4 施設を対象とし, 共有プロセスに基づきパイロット試験を実施した. 問題点並びに改善点を CRA 及び医療機関の双方で評価した. 4 施設のトライアル開始時の状況 A 病院 : 訪問 2 から共有プロセスで実施した. B 病院 : 事前アンケートから共有プロセスで実施した. 但し, 同じプロジェクトの別の試験が継続中であった. C 病院 : 訪問 2 から共有プロセスで実施した. D 病院 : 秘密保持契約書およびアンケート回収のみ完了していたが, それ以降は共有プロセスで実施した.
9 医療機関と依頼者の共有プロセス - 施設選定から Site initiation(1)- 事前情報収集とアポイント取得 依頼者 医療機関 事前アンケート 機密保持同意書の送付 / 回収 SOP 等の入手 訪問要否決定 事前アンケート 機密保持同意書の回答 / 返送 SOP 等の提供 選定調査アポイント調整 訪問 1: 施設 責任医師選定調査 治験説明 医療機関, 責任医師の要件調査 - 実施上の問題点や契約上の疑問点に関する協議 - 組入れ症例数の協議など
10 医療機関と依頼者の共有プロセス - 施設選定から Site initiation(2)- 治験届および依頼手続き準備 依頼者 依頼可否報告 同意説明文書作成依頼 ヒアリング準備 ( ヒアリングシート ) プロトコール等の合意 医療機関 同意説明文書作成 ヒアリング準備 ( ヒアリングシート ) ヒアリングの日程調整 プロトコール等の合意 訪問 2: ヒアリング ( 第 1 回実務担当者打合せ ) プロトコール等説明 責任医師が関与するプロセスについて打ち合わせ 他の関係者との打ち合わせ ( ヒアリングシートを活用 )
11 医療機関と依頼者の共有プロセス - 施設選定から Site initiation(3)- 実務業務フローの確定と依頼契約手続き 依頼者 医療機関 依頼書, 審議資料の提出 / 結果入手 ヒアリング時未確定事項のフォローアップ 治験資材, 機器の納入 IVRS アカウント設定 IRB による審議, 結果通知 ヒアリング時未確定事項のフォローアップ 治験資材, 機器の受領, テスト完了 FD( 全員分 ), 施設基準値の提供 EDC web Training スタートアップミーティングの日程調整 訪問 3: スタートアップミーティング 治験薬の搬入 スタートアップミーティング ( 事務局が司会, 院内フローは CRC が説明. 試験内容及び治験薬概要は依頼者が説明.)
12 結果 1. 共有プロセスの説明と意見聴取 8 施設 1SMO において, 共有プロセスに沿った試験実施可能との回答を得た. 一部, 検討が必要な点が挙げられたが, 双方で調整しながら進めることで問題は回避可能と考えられた. 問題なく実施 できる点 基本的な業務 プロセスに関しては, 院内手順と同様 事前アンケートへは対応可能. 情報開示により回答の精度向上が期待される 施設選定項目はwebに掲載している. 追加質問の回答は適時アップデート ヒアリングは, 治験事務局で院内の参加者および日程調整可能 実施上の要検討点 ( 回答件数 ) 治験責任医師 (PI) 選定時 ( 訪問 1) では治験分担医師の確認は困難 (3) Financial Disclosure は書式が依頼者毎で異なり 個人情報にあたるため事務局対応は困難 (2) IRB 当日に依頼者側担当者の院内待機が必要 (2) ヒアリング ( 訪問 2) 時の項目が多いので 別途 PI に協議を希望 (1) ヒアリング時点では担当 CRC は未定 (1) 訪問回数を限定すると, メール, 電話の対応で訪問以上に手間が増える可能性がある (2) 依頼者のプロトコールが確定しているかが鍵 (3)
13 2. パイロット試験の実施 (1) 4 施設について共有プロセスに基づきパイロット試験を実施した. (1) プロセス通りに出来なかった項目 B 病院 ヒアリングシートが時間不足で準備できなかった. 事前アンケート調査で患者数について, 責任医師との打合せが必要であった. 施設 責任医師調査訪問とヒアリングが同日になった. プロトコール合意書の入手がヒアリング終了後になった. C 病院 試験の性質上, 医師以外の評価者のトレーニング, 認定作業があるため, そのために訪問が増えた. 試験の性質上, 医師, 薬剤師,CRC 及び CRA を盲検, 非盲検と二手に分けるため一度の打合せでは, 問題点や疑問の解決には至らず, ヒアリング後に更に 1 回打合せを実施した. 会社手順でスタートアップミーティング前に必須文書の確認が必要なため, 訪問が 1 回増えた. 事務局としての CV,FD の入手については, 医師数も多いこともあり, 対応できなかった. このため CRA が各医師に事前了解を得た上で, 医局秘書に全医師の CV を取りまとめていただき事務局に提出した.
14 2. パイロット試験の実施 (2) (2) アンケート回答 A 病院 不確定要素があまりに多い状態で面談をスタートすると依頼者で未確定のことが多く, その後の電話やメール等でのやりとりが膨大で負担となる. 依頼者側も事前準備をしておいてもらわないとスムーズには行かない. プロトコルに明示されていない内容についても, ある程度明確になるよう確認しておいてもらえると, 医療機関への確認すべき内容, こちらで調整が必要な事項等について煩雑にならないのかもしれない. B 病院 訪問回数が少ない分 1 回の時間が多くなるのは仕方ないと思う. あらかじめプロセスの内容が項目ごとに文書化されていることで, スケジュールや事前の準備に役立ったと思う. C 病院 最近では病院側の治験契約書中の一部の文言修正を要望してくる依頼者が増えてきている. 病院側としてはなるべくこの要望に副えるよう, 関連部署と調整を図りたいが, それにはある程度時間を要するので, 契約段階での交渉となると治験の開始に影響を与えてしまう. 依頼者固有の要望がある場合は, 依頼前の段階でこの辺りの要望事項について協議を始めることが出来れば時間の短縮につながると思う. D 病院 当院の場合は通常より, メール等で対応可能なことは来院することは求めていません. どうしても来院したいという場合にはあえてお断りはしておりません. 今回のプロセス内容については特に問題点を感じることはありません.
15 考察 国際共同治験では被験者の登録が競合的であり, 日本が諸外国と同様またはこれを上回るパフォーマンスを示すためには各施設における早期症例登録開始が重要な要因となる. 本共有プロセスは, 症例登録開始までに必要とされる医療機関および依頼者双方の業務分担を明確にすることで, 施設選定から Site initiation を効率化することができる. 共有プロセスに対する意見聴取の結果,8 施設 1SMO より本プロセスへの賛同が得られた. 施設毎に検討が必要な項目がいくつか挙げられたものの, これらを医療機関 依頼者にて双方調整することによりプロセスの大幅な変更がなく実施可能と考えられ, 本プロセスが医療機関側からみても実現可能なものであると思われた.
16 今回, パイロット試験の十分な実施 評価には至らなかったが, データの蓄積およびフィードバックを行い, より適切なプロセスへとアップデートするとともに, より多くの医療機関と本プロセスを共有していきたい. 今後はさらなる治験の効率化のために, 医療機関と連携して治験実施中及び終了時のプロセスについても検討していきたい. 謝辞 以下の医療機関等の治験事務局の先生方には, 共有プロセスの実施について ご対応ならびに貴重なご意見を頂戴いたしましたことに深謝申し上げます. ( 順不同 ) 福島県立医科大学, 国立精神 神経医療研究センター,NHO 山形病院,NHO 東京医療センター, NHO 水戸医療センター, NHO 大阪医療センター,NHO 四国がんセンター, 大阪市立大学, 未来医療研究センター
治験事務局標準業務マニュアル
 治験申請等に関する手順書 Ⅰ) 新規治験の申請 1. 実施体制 治験事務局院内スタッフが SMO との提携し 事務局を運営する なお SMO の費用は院内費用とは別に算定するため 別途相談とする CRC 院内スタッフを用いる場合 SMO を利用する場合 どちらの選択も可能とする 2. ヒアリング (a) 予約に際しての条件 プロトコールが固定され 責任医師との合意が文書で得られた時点で予約は可能とする
治験申請等に関する手順書 Ⅰ) 新規治験の申請 1. 実施体制 治験事務局院内スタッフが SMO との提携し 事務局を運営する なお SMO の費用は院内費用とは別に算定するため 別途相談とする CRC 院内スタッフを用いる場合 SMO を利用する場合 どちらの選択も可能とする 2. ヒアリング (a) 予約に際しての条件 プロトコールが固定され 責任医師との合意が文書で得られた時点で予約は可能とする
臨床試験(治験)の手続きについて
 臨床試験 ( 治験 製造販売後臨床試験 ) の手続きについて 本書は 昭和大学横浜市北部病院における臨床試験 ( 治験 製造販売後臨床試験 ) の手続き等に関して記したものです 始める前にご一読下さい なお 下記手続きにおいて必要書類を提出される場合は臨床試験支援室 ( 連絡先 :10 ページ参照 ) までご連絡下さい - 試験依頼前 - 関係書類の入手 当院の臨床試験 ( 治験 製造販売後臨床試験
臨床試験 ( 治験 製造販売後臨床試験 ) の手続きについて 本書は 昭和大学横浜市北部病院における臨床試験 ( 治験 製造販売後臨床試験 ) の手続き等に関して記したものです 始める前にご一読下さい なお 下記手続きにおいて必要書類を提出される場合は臨床試験支援室 ( 連絡先 :10 ページ参照 ) までご連絡下さい - 試験依頼前 - 関係書類の入手 当院の臨床試験 ( 治験 製造販売後臨床試験
医師主導治験取扱要覧
 15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
<4D F736F F D E34208EA18CB18EE891B182AB977697CC C8E8DB782B591D682A688CB978A>
 Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
Ver.2018.4 治験手続き要領 医療法人渓仁会手稲渓仁会病院治験事務局 治験の手続き要領は以下の通りとする 製造販売後臨床試験も以下に準じる 1. 治験審査委員会 (IRB) 開催日 書類提出期限 IRB 開催日は原則 毎月第 1 水曜日です 手続き書類の提出期限は IRB 開催日の 3 週間前です 開催予定日は手稲渓仁会病院治験管理センターホームページ ( 以下 HP) の 治験依頼者の方へ
Microsoft PowerPoint - 運用 [互換モード]
![Microsoft PowerPoint - 運用 [互換モード] Microsoft PowerPoint - 運用 [互換モード]](/thumbs/91/105850431.jpg) 押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
押印省略 電子申請に伴う 統一書式の運用について 独立行政法人国立病院機構東京医療センター 2012.11.1 Ver.1.0 東京医療センターにおける 書式運用基本方針 東京医療センターの書式運用基本方針 1 東京医療センター 企業主導治験に係る標準業務手順書より抜粋 第 6 章治験事務局の設置及び業務第 23 条 ( 略 ) 3 治験事務局は 院長の指示により 次の業務を行う ( 略 ) (4)
内容 1. はじめに 大規模治験ネットワーク登録医療機関への支援内容 治験実施医療機関情報の登録と公開 登録の条件 事前確認 大規模治験ネットワーク への登録方法 登録の手順 登録でき
 大規模治験ネットワーク 登録マニュアル Ver1.1 2013/4/1 公益社団法人日本医師会治験促進センター 0 内容 1. はじめに... 2 2. 大規模治験ネットワーク登録医療機関への支援内容... 2 3. 治験実施医療機関情報の登録と公開... 3 4. 登録の条件... 4 5. 事前確認... 5 6. 大規模治験ネットワーク への登録方法... 6 6-1 登録の手順... 6 6-2
大規模治験ネットワーク 登録マニュアル Ver1.1 2013/4/1 公益社団法人日本医師会治験促進センター 0 内容 1. はじめに... 2 2. 大規模治験ネットワーク登録医療機関への支援内容... 2 3. 治験実施医療機関情報の登録と公開... 3 4. 登録の条件... 4 5. 事前確認... 5 6. 大規模治験ネットワーク への登録方法... 6 6-1 登録の手順... 6 6-2
12_モニタリングの実施に関する手順書
 12_ モニタリングの実施に関する手順書 静岡県立大学大学院薬食生命科学総合学府薬学研究院薬食研究推進センター版数 :1.0 版作成年月日 :2014 月 8 月 1 日 ( 最終確定 :2015 年 1 月 14 日 ) 1. 目的と適用範囲 本手順書は 当該研究において モニターが モニタリングを適切に実施するための手順 その他必要な事項を定めるものである 2. 実施体制及び責務 2.1 研究責任者の責務研究責任者は
12_ モニタリングの実施に関する手順書 静岡県立大学大学院薬食生命科学総合学府薬学研究院薬食研究推進センター版数 :1.0 版作成年月日 :2014 月 8 月 1 日 ( 最終確定 :2015 年 1 月 14 日 ) 1. 目的と適用範囲 本手順書は 当該研究において モニターが モニタリングを適切に実施するための手順 その他必要な事項を定めるものである 2. 実施体制及び責務 2.1 研究責任者の責務研究責任者は
治験実施に必要な手続きについて (HP 用 ) 治験 製造販売後臨床試験 聖マリアンナ医科大学病院治験管理室 聖マリアンナ医科大学病院治験管理室 2011 年 10 月作成 2013 年 1 月改訂 2014 年 4 月改訂 2018 年 4 月改定 2018 年 5 月改定 Ⅰ. 治験審査委員会
 治験実施に必要な手続きについて (HP 用 ) 治験 製造販売後臨床試験 2011 年 10 月作成 2013 年 1 月改訂 2014 年 4 月改訂 2018 年 4 月改定 2018 年 5 月改定 Ⅰ. 治験審査委員会 (IRB) と連絡先 治験審査委員会名称 治験審査委員会設置者 聖マリアンナ医科大学附属病院等治験審査委員会 St. Marianna University Group Institutional
治験実施に必要な手続きについて (HP 用 ) 治験 製造販売後臨床試験 2011 年 10 月作成 2013 年 1 月改訂 2014 年 4 月改訂 2018 年 4 月改定 2018 年 5 月改定 Ⅰ. 治験審査委員会 (IRB) と連絡先 治験審査委員会名称 治験審査委員会設置者 聖マリアンナ医科大学附属病院等治験審査委員会 St. Marianna University Group Institutional
臨床試験(治験)実施の手続き
 製造販売後調査実施の手続き はじめに 本書は 昭和大学藤が丘病院における製造販売後調査実施の手続き方法等について記載したものです 本書内のは当院が提供する書類を示し は審査等に必要な書類を示しております 調査内容により提出書類 資料に変更が生じる場合があります 詳細は支援室にご確認ください 申請する書類および資料は 事前に E-mail に添付して支援室にお送りください 内容の確認をし ご連絡させて頂きます
製造販売後調査実施の手続き はじめに 本書は 昭和大学藤が丘病院における製造販売後調査実施の手続き方法等について記載したものです 本書内のは当院が提供する書類を示し は審査等に必要な書類を示しております 調査内容により提出書類 資料に変更が生じる場合があります 詳細は支援室にご確認ください 申請する書類および資料は 事前に E-mail に添付して支援室にお送りください 内容の確認をし ご連絡させて頂きます
製造販売後調査事務手続き等 について
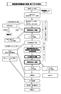 製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
市場調査における有害事象報告の実態について
 市場調査における有害事象報告の実態について メディカル調査研究グループ代表幹事仁司与志矢 2018.6.22 @ ファルマミーティング例会 12 年間で意識が大きく変わりました 12 年前に初めて 市場調査時の AE 報告 についてファルマミーティング例会にて紹介 当時は 海外で騒いでいる 対岸の火事 だった この時のメッセージは これが日本で始まったらまともな調査はできなくなる という問題提起 12
市場調査における有害事象報告の実態について メディカル調査研究グループ代表幹事仁司与志矢 2018.6.22 @ ファルマミーティング例会 12 年間で意識が大きく変わりました 12 年前に初めて 市場調査時の AE 報告 についてファルマミーティング例会にて紹介 当時は 海外で騒いでいる 対岸の火事 だった この時のメッセージは これが日本で始まったらまともな調査はできなくなる という問題提起 12
弊社の紹介 創業 :2002 年 社員数 :110 名 (2014 年 10 月現在 ) 業務内容 : CRC 業務 ( 治験 臨床研究 医師主導治験 その他調査 ) 治験事務局 IRB 事務局運営支援業務 医師主導治験調整事務局支援業務 医療機関体制整備支援業務 GCP 教育 CRC 教育 CRA
 カット ドゥ スクエア (CtDoS2) の 事例紹介 ~ 治験依頼者 - 実施医療機関 -IRB の三者間で CtDoS2 を活用してみて ~ 株式会社新日本科学臨床薬理研究所九州エリア支援部鹿児島支援室サイトマネジメントチーム黒木沙織 1 弊社の紹介 創業 :2002 年 社員数 :110 名 (2014 年 10 月現在 ) 業務内容 : CRC 業務 ( 治験 臨床研究 医師主導治験 その他調査
カット ドゥ スクエア (CtDoS2) の 事例紹介 ~ 治験依頼者 - 実施医療機関 -IRB の三者間で CtDoS2 を活用してみて ~ 株式会社新日本科学臨床薬理研究所九州エリア支援部鹿児島支援室サイトマネジメントチーム黒木沙織 1 弊社の紹介 創業 :2002 年 社員数 :110 名 (2014 年 10 月現在 ) 業務内容 : CRC 業務 ( 治験 臨床研究 医師主導治験 その他調査
<4D F736F F F696E74202D208EA18CB B90B389BB8DEC8BC694C F E B93C782DD8EE682E890EA97705D205B8CDD8AB
 治験等適正化作業班における 検討 独立行政法人国立病院機構本部伊藤澄信 第 6 回治験中核病院 拠点医療機関等協議会 本日の内容 設置の経緯等について 主な検討内容について 今後の課題について その他 1 設置の経緯 (1) 1. 設置の背景 新たな治験活性化 5 カ年計画の中間見直しに関する検討会 報告の 重点的取組事項 ( アクションプラン ) の進捗 において 今後 取組みをより加速かつ強化すべき課題
治験等適正化作業班における 検討 独立行政法人国立病院機構本部伊藤澄信 第 6 回治験中核病院 拠点医療機関等協議会 本日の内容 設置の経緯等について 主な検討内容について 今後の課題について その他 1 設置の経緯 (1) 1. 設置の背景 新たな治験活性化 5 カ年計画の中間見直しに関する検討会 報告の 重点的取組事項 ( アクションプラン ) の進捗 において 今後 取組みをより加速かつ強化すべき課題
< F2D8E9197BF A836F815B2E6A7464>
 ( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
4 研修について考慮する事項 1. 研修の対象者 a. 職種横断的な研修か 限定した職種への研修か b. 部署 部門を横断する研修か 部署及び部門別か c. 職種別の研修か 2. 研修内容とプログラム a. 研修の企画においては 対象者や研修内容に応じて開催時刻を考慮する b. 全員への周知が必要な
 新井病院 医療安全管理者の業務指針 新井病院医療安全管理者業務指針 1. はじめに医療機関の管理者は 自ら安全管理体制を確保するとともに 医療安全管理者を配置するにあたっては 必要な権限を委譲し また 必要な資源を付与して その活動を推進することで医療機関内の安全管理につとめなければならない 2. 医療安全管理者の位置づけ医療安全管理者とは 病院管理者 ( 病院長 ) の任命を受け 安全管理のために必要な権限の委譲と
新井病院 医療安全管理者の業務指針 新井病院医療安全管理者業務指針 1. はじめに医療機関の管理者は 自ら安全管理体制を確保するとともに 医療安全管理者を配置するにあたっては 必要な権限を委譲し また 必要な資源を付与して その活動を推進することで医療機関内の安全管理につとめなければならない 2. 医療安全管理者の位置づけ医療安全管理者とは 病院管理者 ( 病院長 ) の任命を受け 安全管理のために必要な権限の委譲と
Project Goals
 平成 23 年度治験推進地域連絡会議 治験推進に向けた欧州製薬団体連合会 (EFPIA) の取り組み 欧州製薬団体連合会 (EFPIA) 技術委員会臨床部会 本日の内容 日本の治験環境の変化と現状 治験等の効率化に関する今後の期待 EFPIA臨床部会の取り組み On/Off-site Monitoringの普及 ALCOAの普及 合同モニター研修 2 3 日本の治験環境の変化と現状 - 新 G C
平成 23 年度治験推進地域連絡会議 治験推進に向けた欧州製薬団体連合会 (EFPIA) の取り組み 欧州製薬団体連合会 (EFPIA) 技術委員会臨床部会 本日の内容 日本の治験環境の変化と現状 治験等の効率化に関する今後の期待 EFPIA臨床部会の取り組み On/Off-site Monitoringの普及 ALCOAの普及 合同モニター研修 2 3 日本の治験環境の変化と現状 - 新 G C
4.7.4 プロセスのインプットおよびアウトプット (1) プロセスへのインプット情報 インプット情報 作成者 承認者 備 考 1 開発に関するお客様から お客様 - の提示資料 2 開発に関する当社収集資 リーダ - 料 3 プロジェクト計画 完了報 リーダ マネージャ 告書 ( 暫定計画 ) 4
 サンプル : プロジェクト管理規定 4.7 プロジェクト立ち上げ 4.7.1 目的 本プロセスはリーダ主導で プロジェクト体制の確立とプロジェクト内容 分担 業務指示 プロジェクト目標 担当者別プロジェクト目標を開発メンバに周知徹底することによって 組織としての意識統一を図るとともに開発プロセスをスムーズに立ち上げることを目的とする 4.7.2 このプロセスにかかわる人物の役割と責務 部門 略記 参加
サンプル : プロジェクト管理規定 4.7 プロジェクト立ち上げ 4.7.1 目的 本プロセスはリーダ主導で プロジェクト体制の確立とプロジェクト内容 分担 業務指示 プロジェクト目標 担当者別プロジェクト目標を開発メンバに周知徹底することによって 組織としての意識統一を図るとともに開発プロセスをスムーズに立ち上げることを目的とする 4.7.2 このプロセスにかかわる人物の役割と責務 部門 略記 参加
Microsoft Word - H _概要_.doc
 平成 25 年 2 月独立行政法人国立病院機構西新潟中央病院倫理審査委員会 ( 受託研究 ) 議事要旨 開催日時 開催場所 出席委員名は別紙のとおり 治験及び製造販売後臨床試験に関する調査審議事項 審議事項 治験等の実施に関する研究 継続 ME2080 の Dravet 症候群患者を対象とした一般臨床試験 ( 第 Ⅲ 相 ) (Protocol No:STP-1) 被験薬 :ME2080(Stiripentol)
平成 25 年 2 月独立行政法人国立病院機構西新潟中央病院倫理審査委員会 ( 受託研究 ) 議事要旨 開催日時 開催場所 出席委員名は別紙のとおり 治験及び製造販売後臨床試験に関する調査審議事項 審議事項 治験等の実施に関する研究 継続 ME2080 の Dravet 症候群患者を対象とした一般臨床試験 ( 第 Ⅲ 相 ) (Protocol No:STP-1) 被験薬 :ME2080(Stiripentol)
標準業務手順 目次
 浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
京都府立医科大学附属病院
 治験費用の取扱に関する手順書 京都府立医科大学附属病院 第 1 版平成 21 年 11 月 16 日 第 2 版平成 23 年 3 月 16 日 第 3 版平成 25 年 2 月 1 日 1. 目的 本手順書は 京都府立医科大学附属病院治験実施取扱規定の定めるところにより 治験 費用の取り扱いに関する運用方法を定め それに基づく業務手順を示すものである 2. 治験に係る経費の範囲 (1) 治験経費
治験費用の取扱に関する手順書 京都府立医科大学附属病院 第 1 版平成 21 年 11 月 16 日 第 2 版平成 23 年 3 月 16 日 第 3 版平成 25 年 2 月 1 日 1. 目的 本手順書は 京都府立医科大学附属病院治験実施取扱規定の定めるところにより 治験 費用の取り扱いに関する運用方法を定め それに基づく業務手順を示すものである 2. 治験に係る経費の範囲 (1) 治験経費
静岡県立静岡がんセンター臨床研究事務局の業務手順書
 治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 6.0 平成 20 年 1 月 28
治験薬管理者の業務手順書 更新履歴 版 承認日 承認者 1.0 平成 15 年 3 月 14 日 施行 経営戦略会議 2.0 平成 15 年 4 月 15 日 改正 経営戦略会議 3.0 平成 16 年 3 月 31 日 改正 経営戦略会議 4.0 平成 17 年 6 月 20 日 改正 経営戦略会議 5.0 平成 18 年 3 月 10 日 改正 経営戦略会議 6.0 平成 20 年 1 月 28
山形県立中央病院治験審査委員会業務手順書
 山形県立中央病院治験審査委員会業務手順書 第 1 目的この手順書は山形県立中央病院医薬品等臨床試験受託研究取扱要綱 ( 以下 取扱要綱 という ) に基づいて山形県立中央病院治験審査委員会 ( 以下 本委員会 という ) の運用方法を定め それに基づく業務手順書を示すものである なお 製造販売後臨床試験においては 以下 治験 とあるのを 製造販売後臨床試験 と読み替えるものとする 第 2 本委員会の責務本委員会は全ての被験者の人権の保護
山形県立中央病院治験審査委員会業務手順書 第 1 目的この手順書は山形県立中央病院医薬品等臨床試験受託研究取扱要綱 ( 以下 取扱要綱 という ) に基づいて山形県立中央病院治験審査委員会 ( 以下 本委員会 という ) の運用方法を定め それに基づく業務手順書を示すものである なお 製造販売後臨床試験においては 以下 治験 とあるのを 製造販売後臨床試験 と読み替えるものとする 第 2 本委員会の責務本委員会は全ての被験者の人権の保護
社会通信教育に関する実態調査 報告書
 平成 22 年度文部科学省委託調査 社会通信教育に関する調査研究 社会通信教育に関する実態調査 報告書 平成 23 年 3 月 株式会社日本能率協会総合研究所 目次 I 調査の概要... 1 1 調査目的... 1 2 調査内容... 1 (1) 社会通信教育の実施団体に対する調査... 1 (2) 社会通信教育の受講者への調査... 2 (3) 社会通信教育の利用企業への調査... 2 3 調査の流れ...
平成 22 年度文部科学省委託調査 社会通信教育に関する調査研究 社会通信教育に関する実態調査 報告書 平成 23 年 3 月 株式会社日本能率協会総合研究所 目次 I 調査の概要... 1 1 調査目的... 1 2 調査内容... 1 (1) 社会通信教育の実施団体に対する調査... 1 (2) 社会通信教育の受講者への調査... 2 (3) 社会通信教育の利用企業への調査... 2 3 調査の流れ...
臨床研究に関する標準業務手順書
 臨床研究に関する標準業務手順書 2018/04/01 第 15 版 改定履歴 日付 版 改定理由 改定箇所 内容 2010/02/06 1 新規制定 2010/04/14 2 COI 関連手順の明確化 フローチャートに COI に関する手順の追記 2010/08/19 3 様式 必要書類の追加 COI 関連様式の追記 安全性に関する報告の手順および様式 ( 様式 11) の追加 委託研究に関する手順
臨床研究に関する標準業務手順書 2018/04/01 第 15 版 改定履歴 日付 版 改定理由 改定箇所 内容 2010/02/06 1 新規制定 2010/04/14 2 COI 関連手順の明確化 フローチャートに COI に関する手順の追記 2010/08/19 3 様式 必要書類の追加 COI 関連様式の追記 安全性に関する報告の手順および様式 ( 様式 11) の追加 委託研究に関する手順
症候性サーベイランス実施 手順書 インフルエンザ様症候性サーベイランス 編 平成 28 年 5 月 26 日 群馬県感染症対策連絡協議会 ICN 分科会サーベイランスチーム作成
 症候性サーベイランス実施 手順書 インフルエンザ様症候性サーベイランス 編 平成 28 年 5 月 26 日 群馬県感染症対策連絡協議会 ICN 分科会サーベイランスチーム作成 目次 1. はじめに 2. インフルエンザ様症候性サーベイランスについて 1) 目的 2) 対象施設 3. サーベイランスの進め方 1) 開始の決定 2) 対象者 実施場所の選定 3) データの収集 4) データの集計 分析
症候性サーベイランス実施 手順書 インフルエンザ様症候性サーベイランス 編 平成 28 年 5 月 26 日 群馬県感染症対策連絡協議会 ICN 分科会サーベイランスチーム作成 目次 1. はじめに 2. インフルエンザ様症候性サーベイランスについて 1) 目的 2) 対象施設 3. サーベイランスの進め方 1) 開始の決定 2) 対象者 実施場所の選定 3) データの収集 4) データの集計 分析
JCROA自主ガイドライン第4版案 GCP監査WG改訂案及び意見
 受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
UMIN INDICE Lower level data communication protocol for CDISC ODM規約
 UMIN INDICE Lower level data communication protocol for CDISC ODM 規約 API Ver2.7 用 UMIN INDICE システムに臨床研究データを CDISC ODM 形式で電子的に送付する場合の ODM 下層レベルのデータ交換規約 UMIN センター 2013/05/16 目次 1 概要...- 2-1.1 UMIN センター...-
UMIN INDICE Lower level data communication protocol for CDISC ODM 規約 API Ver2.7 用 UMIN INDICE システムに臨床研究データを CDISC ODM 形式で電子的に送付する場合の ODM 下層レベルのデータ交換規約 UMIN センター 2013/05/16 目次 1 概要...- 2-1.1 UMIN センター...-
13.1 ログイン ID の変更 ログイン ID を変更する手順について説明します 画面 操作概要 トップ (1) グローバルメニュー ログイン ID の変更 を選択 ログイン ID の変更 (2) ログイン ID を変更 ログイン ID の変更 (3) ログイン ID の変更を完了 2
 13 その他編 操作の概要 ログイン ID の変更 ログイン ID を変更することができます 13.1 ログイン ID の変更 パスワードの変更 パスワードを変更することができます 13.2 パスワードの変更 秘密の質問の変更 秘密の質問を変更することができます 13.3 秘密の質問の変更 メール送受信設定の変更 メール送受信設定を変更することができます 13.4 メール送受信設定の変更 処理結果一覧
13 その他編 操作の概要 ログイン ID の変更 ログイン ID を変更することができます 13.1 ログイン ID の変更 パスワードの変更 パスワードを変更することができます 13.2 パスワードの変更 秘密の質問の変更 秘密の質問を変更することができます 13.3 秘密の質問の変更 メール送受信設定の変更 メール送受信設定を変更することができます 13.4 メール送受信設定の変更 処理結果一覧
1. のれんを資産として認識し その後の期間にわたり償却するという要求事項を設けるべきであることに同意するか 同意する場合 次のどの理由で償却を支持するのか (a) 取得日時点で存在しているのれんは 時の経過に応じて消費され 自己創設のれんに置き換わる したがって のれんは 企業を取得するコストの一
 ディスカッション ペーパー のれんはなお償却しなくてよいか のれんの会計処理及び開示 に対する意見 平成 26 年 9 月 30 日 日本公認会計士協会 日本公認会計士協会は 企業会計基準委員会 (ASBJ) 欧州財務報告諮問グループ (EFRAG) 及びイタリアの会計基準設定主体 (OIC) のリサーチ グループによるリサーチ活動に敬意を表すとともに ディスカッション ペーパー のれんはなお償却しなくてよいか
ディスカッション ペーパー のれんはなお償却しなくてよいか のれんの会計処理及び開示 に対する意見 平成 26 年 9 月 30 日 日本公認会計士協会 日本公認会計士協会は 企業会計基準委員会 (ASBJ) 欧州財務報告諮問グループ (EFRAG) 及びイタリアの会計基準設定主体 (OIC) のリサーチ グループによるリサーチ活動に敬意を表すとともに ディスカッション ペーパー のれんはなお償却しなくてよいか
平成 30 年度救急業務のあり方に関する検討会報告書の概要 消防庁救急企画室 はじめに 消防庁救急企画室では 高齢化を背景として救急需要が増大する中 救急車の適正利用の推進や救急業務の円滑な実施と質の向上等 救急業務を安定的かつ持続的に提供し救命率の向上を図ることを目的に 平成 30 年度救急業務の
 平成 30 年度救急業務のあり方に関する検討会報告書の概要 消防庁救急企画室 はじめに 消防庁救急企画室では 高齢化を背景として救急需要が増大する中 救急車の適正利用の推進や救急業務の円滑な実施と質の向上等 救急業務を安定的かつ持続的に提供し救命率の向上を図ることを目的に 平成 30 年度救急業務のあり方に関する検討会 ( 座長 : 山本保博一般財団法人救急振興財団会長 ) を開催しました 検討会では
平成 30 年度救急業務のあり方に関する検討会報告書の概要 消防庁救急企画室 はじめに 消防庁救急企画室では 高齢化を背景として救急需要が増大する中 救急車の適正利用の推進や救急業務の円滑な実施と質の向上等 救急業務を安定的かつ持続的に提供し救命率の向上を図ることを目的に 平成 30 年度救急業務のあり方に関する検討会 ( 座長 : 山本保博一般財団法人救急振興財団会長 ) を開催しました 検討会では
Microsoft PowerPoint - CocoroClover_紹介資料(VirtualShowroom用)
 ストレスチェックサービス CocoroClover のご紹介 目次 1. ストレスチェック制度の概要 ------------------------- 2 2. サービスの概要 ------------------------------------- 4 3. サービスの特徴 ------------------------------------- 5 4. 導入のメリット -------------------------------------
ストレスチェックサービス CocoroClover のご紹介 目次 1. ストレスチェック制度の概要 ------------------------- 2 2. サービスの概要 ------------------------------------- 4 3. サービスの特徴 ------------------------------------- 5 4. 導入のメリット -------------------------------------
Microsoft PowerPoint - 矢庭第3日(第6章ケアマネジメントのプロセス)
 介護支援専門員実務研修 3 日目 13:45~15:45 第 6 章 ケアマネジメントのプロセス 1 本科目の目的と修得目標 目的 ケアマネジメントプロセスの全体像を理解する 修得目標 1. ケアマネジメントプロセスの構成と流れについて説明 できる 2. 各プロセスの意義について説明できる 3. 各プロセスの目的について説明できる 4. 各プロセスの関連性を述べることができる 5. ケアマネジメントプロセスの全体像について説明できる
介護支援専門員実務研修 3 日目 13:45~15:45 第 6 章 ケアマネジメントのプロセス 1 本科目の目的と修得目標 目的 ケアマネジメントプロセスの全体像を理解する 修得目標 1. ケアマネジメントプロセスの構成と流れについて説明 できる 2. 各プロセスの意義について説明できる 3. 各プロセスの目的について説明できる 4. 各プロセスの関連性を述べることができる 5. ケアマネジメントプロセスの全体像について説明できる
)各 職場復帰前 受入方針の検討 () 主治医等による 職場復帰可能 との判断 主治医又はにより 職員の職場復帰が可能となる時期が近いとの判断がなされる ( 職員本人に職場復帰医師があることが前提 ) 職員は健康管理に対して 主治医からの診断書を提出する 健康管理は 職員の職場復帰の時期 勤務内容
 職場復帰支援の流れ図 職員(家族)(保主健治師医)等 )各 療養期間中 () 職員からの診断書の提出 職員本人から主治医に対して 診断書に長期療養を必要とする旨のほか 必要な療養期間 ( 見込み ) を明記するよう依頼する 主治医から職員本人に対して 診断書が発行される 職員から健康管理に対して 診断書を提出する () 受入方針検討前までの情報収集, 健康管理は 職員の同意のもとに主治医と連携をとり
職場復帰支援の流れ図 職員(家族)(保主健治師医)等 )各 療養期間中 () 職員からの診断書の提出 職員本人から主治医に対して 診断書に長期療養を必要とする旨のほか 必要な療養期間 ( 見込み ) を明記するよう依頼する 主治医から職員本人に対して 診断書が発行される 職員から健康管理に対して 診断書を提出する () 受入方針検討前までの情報収集, 健康管理は 職員の同意のもとに主治医と連携をとり
<4D F736F F D208CC2906C8FEE95F182CC8EE688B582C982C282A282C E646F6378>
 個人情報の取扱いについて 株式会社ヘルスクリック個人情報保護管理責任者 株式会社ヘルスクリック ( 以下 当社 といいます ) は お客様 お取引先様 従業員の方々の個人情報について 個人情報保護方針 ( プライバシー ポリシー ) に従い適正な管理を行うとともに 個人情報の保護に努めます 具体的には 以下の内容に従って個人情報の取り扱いを行います 1. 個人情報取扱事業者の名称株式会社ヘルスクリック
個人情報の取扱いについて 株式会社ヘルスクリック個人情報保護管理責任者 株式会社ヘルスクリック ( 以下 当社 といいます ) は お客様 お取引先様 従業員の方々の個人情報について 個人情報保護方針 ( プライバシー ポリシー ) に従い適正な管理を行うとともに 個人情報の保護に努めます 具体的には 以下の内容に従って個人情報の取り扱いを行います 1. 個人情報取扱事業者の名称株式会社ヘルスクリック
恩賜第 42 回社会福祉法人財団済生会中央治験審査委員会 会議の記録の概要 開催日時 平成 28 年 1 月 13 日 ( 水 )15:30~17:17 開催場所 出席委員名 東京都港区三田 三田国際ビル 21 階 社会福祉法人 恩賜財団済生会本部事務局中会議室 豊島
 恩賜第 42 回社会福祉法人財団済生会中央治験審査委員会 会議の記録の概要 開催日時 平成 28 年 1 月 13 日 ( 水 )15:30~17:17 開催場所 出席委員名 108-0073 東京都港区三田 1-4-28 三田国際ビル 21 階 社会福祉法人 恩賜財団済生会本部事務局中会議室 豊島聰 ( 出席 ) 委員長林茂樹 ( 出席 ) 副委員長 市場みすゞ ( 出席 ) 漆原尚巳 ( 出席
恩賜第 42 回社会福祉法人財団済生会中央治験審査委員会 会議の記録の概要 開催日時 平成 28 年 1 月 13 日 ( 水 )15:30~17:17 開催場所 出席委員名 108-0073 東京都港区三田 1-4-28 三田国際ビル 21 階 社会福祉法人 恩賜財団済生会本部事務局中会議室 豊島聰 ( 出席 ) 委員長林茂樹 ( 出席 ) 副委員長 市場みすゞ ( 出席 ) 漆原尚巳 ( 出席
国際共同治験における役割分担 -治験依頼者へのアンケートをもとに-
 部会資料 国際共同治験における役割分担 - 治験依頼者へのアンケートをもとに - 年 月 日本製薬工業協会 医薬品評価委員会臨床評価部会 目次 はじめに... 国際共同治験における業務... アンケート方法... 4 アンケート結果まとめ... 4. 調査対象医療機関背景... 6 4. 医療機関と治験依頼者の役割分担... 6 4. 医療機関の治験実施体制... 8 4.4 英語の配布文書の位置付け...
部会資料 国際共同治験における役割分担 - 治験依頼者へのアンケートをもとに - 年 月 日本製薬工業協会 医薬品評価委員会臨床評価部会 目次 はじめに... 国際共同治験における業務... アンケート方法... 4 アンケート結果まとめ... 4. 調査対象医療機関背景... 6 4. 医療機関と治験依頼者の役割分担... 6 4. 医療機関の治験実施体制... 8 4.4 英語の配布文書の位置付け...
ISO19011の概要について
 3 技術資料 3-1 ISO19011 の概要について 従来の環境マネジメントシステムの監査の指針であった ISO14010 ISO14011 ISO1401 2 が改正 統合され 2002 年 10 月に ISO19011 として発行されました この指針は 単に審査登録機関における審査の原則であるばかりでなく 環境マネジメントシステムの第二者監査 ( 取引先等利害関係対象の審査 ) や内部監査に適用できる有効な指針です
3 技術資料 3-1 ISO19011 の概要について 従来の環境マネジメントシステムの監査の指針であった ISO14010 ISO14011 ISO1401 2 が改正 統合され 2002 年 10 月に ISO19011 として発行されました この指針は 単に審査登録機関における審査の原則であるばかりでなく 環境マネジメントシステムの第二者監査 ( 取引先等利害関係対象の審査 ) や内部監査に適用できる有効な指針です
治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会
 治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会 第 1 条 ( 目的 ) 1. 本手順書は 新光会治験審査委員会 ( 以下 委員会という ) において 医薬品及び医療機器 ( 以下 医薬品等という ) の治験の調査審議を実施するに当たり 薬事法 ( 昭和 35 年 8 月 10 日法律第 145 号 ) に基づく 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3
治験審査委員会手順書 平成 27 年 10 月 1 日 医療法人新光会 第 1 条 ( 目的 ) 1. 本手順書は 新光会治験審査委員会 ( 以下 委員会という ) において 医薬品及び医療機器 ( 以下 医薬品等という ) の治験の調査審議を実施するに当たり 薬事法 ( 昭和 35 年 8 月 10 日法律第 145 号 ) に基づく 医薬品の臨床試験の実施の基準に関する省令 ( 平成 9 年 3
スライド 1
 背景 目的 スライド 1 治験に係わる当事者の手作業 紙作業の労働集約的業務 On-Site で行うモニタリング業務の非効率性は 治験コスト削減 スピード短縮のための大きな障壁となっている GCP 運用通知第 21 条 < 第 2 項 >2 では 中央モニタリングに関する手順書 ( 必須文書 23.1 1) ) に基づく Off-Site でのモニタリングを許容している 昨年 欧米では時をほぼ同じくしてReflection
背景 目的 スライド 1 治験に係わる当事者の手作業 紙作業の労働集約的業務 On-Site で行うモニタリング業務の非効率性は 治験コスト削減 スピード短縮のための大きな障壁となっている GCP 運用通知第 21 条 < 第 2 項 >2 では 中央モニタリングに関する手順書 ( 必須文書 23.1 1) ) に基づく Off-Site でのモニタリングを許容している 昨年 欧米では時をほぼ同じくしてReflection
エンカレッジオンラインのご利用について 動作環境 : Internet Explorer 9 以上 Firefox 最新版 Google Chrome 最新版 Safari 最新版 その他注意事項 : ご不明な点や不具合のご報告はお手数ですがこちらまでご連絡ください エンカレッジ事務局 電話番号 :
 運用管理者向けご利用マニュアル 2017 年 12 月 26 日版 エンカレッジオンラインのご利用について 動作環境 : Internet Explorer 9 以上 Firefox 最新版 Google Chrome 最新版 Safari 最新版 その他注意事項 : ご不明な点や不具合のご報告はお手数ですがこちらまでご連絡ください エンカレッジ事務局 電話番号 :03-3342-5175 メールアドレス
運用管理者向けご利用マニュアル 2017 年 12 月 26 日版 エンカレッジオンラインのご利用について 動作環境 : Internet Explorer 9 以上 Firefox 最新版 Google Chrome 最新版 Safari 最新版 その他注意事項 : ご不明な点や不具合のご報告はお手数ですがこちらまでご連絡ください エンカレッジ事務局 電話番号 :03-3342-5175 メールアドレス
修正履歴 版数 修正日 修正内容 章 V /6/24 初版作成 V /6/30 イベント番号一式画面変更 全般 V /5/ 年 2 月機能追加部分反映 全般 2
 操作マニュアル 一般社団法人福島県医療福祉情報ネットワーク協議会 Ver 1.3 2016 年 6 月 5 日 1 修正履歴 版数 修正日 修正内容 章 V1.0 2015/6/24 初版作成 V1.1 2015/6/30 イベント番号一式画面変更 全般 V1.2 2016/5/16 2016 年 2 月機能追加部分反映 全般 2 遠隔カンファレンス 目次 1. ログイン画面 2. ホーム画面 3.
操作マニュアル 一般社団法人福島県医療福祉情報ネットワーク協議会 Ver 1.3 2016 年 6 月 5 日 1 修正履歴 版数 修正日 修正内容 章 V1.0 2015/6/24 初版作成 V1.1 2015/6/30 イベント番号一式画面変更 全般 V1.2 2016/5/16 2016 年 2 月機能追加部分反映 全般 2 遠隔カンファレンス 目次 1. ログイン画面 2. ホーム画面 3.
