|
|
|
- もえり ひらみね
- 7 years ago
- Views:
Transcription
1 Clinical Practice Guidelines for the Management of Pain, Agitation, and Delirium in Adult Patients in the Intensive Care Unit Juliana Barr, MD, FCCM; Gilles L. Fraser, PharmD, FCCM; Kathleen Puntillo, RN, PhD, FAAN, FCCM; E. Wesley Ely, MD, MPH, FACP, FCCM; Céline Gélinas, RN, PhD; Joseph F. Dasta, MSc, FCCM, FCCP; Judy E. Davidson, DNP, RN; John W. Devlin, PharmD, FCCM, FCCP; John P. Kress, MD; Aaron M. Joffe, DO; Douglas B. Coursin, MD; Daniel L. Herr, MD, MS, FCCM; Avery Tung, MD; Bryce R. H. Robinson, MD, FACS; Dorrie K. Fontaine, PhD, RN, FAAN; Michael A. Ramsay, MD; Richard R. Riker, MD, FCCM; Curtis N. Sessler, MD, FCCP, FCCM; Brenda Pun, MSN, RN, ACNP; Yoanna Skrobik, MD, FRCP; Roman Jaeschke, MD Critical Care Medicine 2013; 41(1):
2
3 成人 ICU 患者の疼痛 不穏およびせん妄の管理に関する臨床ガイドライン Clinical Practice Guidelines for the Management of Pain, Agitation, and Delirium in Adult Patients in the Intensive Care Unit Juliana Barr, MD, FCCM 1 ; Gilles L. Fraser, PharmD, FCCM 2 ; Kathleen Puntillo, RN, PhD, FAAN, FCCM 3 ; E. Wesley Ely, MD, MPH, FACP, FCCM 4 ; Céline Gélinas, RN, PhD 5 ; Joseph F. Dasta, MSc, FCCM, FCCP 6 ; Judy E. Davidson, DNP, RN 7 ; John W. Devlin, PharmD, FCCM, FCCP 8 ; John P. Kress, MD 9 ; Aaron M. Joffe, DO 10 ; Douglas B. Coursin, MD 11 ; Daniel L. Herr, MD, MS, FCCM 12 ; Avery Tung, MD 13 ; Bryce R. H. Robinson, MD, FACS 14 ; Dorrie K. Fontaine, PhD, RN, FAAN 15 ; Michael A. Ramsay, MD 16 ; Richard R. Riker, MD, FCCM 17 ; Curtis N. Sessler, MD, FCCP, FCCM 18 ; Brenda Pun, MSN, RN, ACNP 19 ; Yoanna Skrobik, MD, FRCP 20 ; Roman Jaeschke, MD 21 1 VA Palo Alto Health Care System, Palo Alto, CA, and Stanford University School of Medicine, Stanford, CA. 2 Tufts University School of Medicine, Maine Medical Center, Portland, ME. 3 Department of Physiological Nursing, University of California, San Francisco, CA. 4 VA-GRECC (Geriatric Research Education Clinical Center) for the VA Tennessee Valley Healthcare System, Vanderbilt University Medical Center, Nashville, TN. 5 Ingram School of Nursing, McGill University and Centre for Nursing Research/ Lady Davis Institute, Jewish General Hospital, Montreal, QC, Canada. 6 The Ohio State University, College of Pharmacy, Columbus, OH, and The University of Texas, College of Pharmacy, Austin, TX. 7 Scripps Clinical Center, Scripps Health, La Jolla, CA. 8 Department of Pharmacy Practice, Northeastern University Special and Scientific Staff, Division of Pulmonary, Critical Care, and Sleep Medicine, Tufts University of Medicine, Boston, MA. 9 Department of Medicine, Section of Pulmonary and Critical Care, University of Chicago, Chicago, IL. 10 Department of Anesthesiology and Pain Medicine, University of Washington/Harborview Medical Center, Seattle, WA. 11 Departments of Anesthesiology and Internal Medicine, University of Wisconsin School of Medicine and Public Health, Madison, WI. 12 Shock Trauma Center, Division of Trauma Critical Care Medicine, University of Maryland, Baltimore, MD. 13 Department of Anesthesia and Critical Care, University of Chicago, Chicago, IL. 14 Department of Surgery, Division of Trauma and Critical Care, University of Cincinnati, Cincinnati, OH. 15 University of Virginia, School of Nursing, Charlottesville, VA. 16 Baylor University Medical Center, Dallas, TX. 17 Tufts University School of Medicine, Maine Medical Center, Portland, ME. 18 Department of Internal Medicine, Virginia Commonwealth University Heath System, Richmond, VA. 19 Department of Allergy, Pulmonary, and Critical Care Medicine, Vanderbilt University Medical Center, Nashville, TN. 20 Université de Montréal, Montréal, Canada. 21 Departments of Medicine and Clinical Epidemiology and Biostatistics, St. Joseph s Hospital and McMaster University, Hamilton, Ontario, Canada. Supplemental digital content is available for this article. Direct URL citations appear in the printed text and are provided in the HTML and PDF versions of this on the journal s Web site ( To minimize the perception of bias in these Guidelines, individual Task Force members with a significant conflict of interest on a particular topic were recused from grading the literature, writing evidence summaries, and developing specific statements and recommendations on that topic. Final decisions regarding strength of evidence and strength of recommendations for all questions were voted on anonymously by all Task Force members. Voting distributions for all statements and recommendations can be found on line at We refer readers to the Methods Section of these Guidelines for more details. Supporting Organizations: American College of Critical Care Medicine (ACCM) in conjunction with Society of Critical Care Medicine (SCCM) and American Society of Health-System Pharmacists (ASHP). Mr. Dasta has consultancies with Hospira, Axel Rx, Cadence Pharmaceuticals, and Pacira Pharmaceuticals and has received honoraria/speaking fees from the France Foundation (speakers bureau CME program) sponsored by Hospira. Dr. Devlin has received honoraria/speaking fees, consultancies, and grants from Hospira. Dr. Ely has received honoraria/speaking fees from GSK and Hospira; and has received grants from Hospira, Pfizer, and Aspect. Dr. Herr has received honoraria/speaking fees from Hospira. Dr. Kress has received honorar ia/speaking fees from Hospira; and has received a grant from Hospira (unrestricted research). Ms. Pun has received honoraria/ speaking fees from Hospira. Dr. Ramsay has received honoraria/speaking fees from Hospira and Masimo; and has received a grant from Masimo. Dr. Riker has consultancies with Masimo; and has received honoraria/speaking fees from Orion. Dr. Sessler has received honoraria/speaking fees from Hospira and consulting fees from Massimo. The remaining authors have not disclosed any potential conflicts of interest. These guidelines have been reviewed and endorsed by the American College of Chest Physicians and the American Association for Respiratory Care; are supported by the American Association for Respiratory Care; and have been reviewed by the New Zealand Intensive Care Society. For information regarding this article, [email protected] The American College of Critical Care Medicine (ACCM), which honors individuals for their achievements and contributions to multidisciplinary critical care medicine, is the consultative body of the Society of Critical Care Medicine (SCCM) that possesses recognized expertise in the practice of critical care. The College has developed administrative guidelines and clinical practice parameters for the critical care practitioner. New guidelines and practice parameters are continually developed, and current ones are systematically reviewed and revised. Copyright 2013 by the Society of Critical Care Medicine DOI: /CCM.0b013e b72 Critical Care Medicine 1
4 Barr et al 目的 :2002 年に Critical Care Medicine 誌に公表された 成人重症患者に対する鎮静 鎮痛薬の使用に関する臨床ガイドライン を改訂する 方法 :American College of Critical Care Medicine( 米国クリティカルケア医学会 :ACCM) は ガイドラインの作成ならびに成人重症患者の疼痛 不穏と鎮静およびせん妄の管理とアウトカムに関する専門知識をもつ専門家 20 名を招集し 多施設共同による集学的な作業部会を立ち上げた 4 つの分科会からなるこの作業部会は 面談や電話 テレビ会議 電子上でのコミュニケーションを通じて 6 年にわたり共同作業を進めた 各分科会は 臨床現場で直面する疑問 ( クリニカル クエスチョン ) を提示し Grading of Recommendations Assessment, Development and Evaluation( 推奨度の検討 開発 評価 :GRADE) システム ( を用いて文献のレビュー 評価および要約を行い クリニカル クエスチョンに対するステートメント ( 記述的なもの ) および推奨事項 ( 実行可能なもの ) を作成する責任を担った 専門の図書館員の支援を受け データベースソフトウェア Refworks を用いて 8 つの臨床に関連した検索エンジンから 成人 ICU 患者の疼痛と鎮痛 不穏と鎮静 せん妄および臨床的アウトカムに関する 19,000 件を超える文献の Web データベースを構築した また 計量心理学的解析を行い 疼痛 不穏 / 鎮静およびせん妄の各種評価ツールを比較検討した 作業部会のメンバー全員が各ステートメントおよび推奨事項の裏付けとなる文献のレビューを実施し 各分科会にフィードバックを行った すべてのステートメントおよび推奨事項に対する合意の形成には Nominal Group Technique 法および Delphi 変法を用い 作業部会のメンバー全員が E-Survey( com) を通じて匿名投票を行い 投票は 2010 年 12 月に終了した この終了時点からガイドラインの公表までの期間に発表された関連研究については 本文中で言及している 各ステートメントおよび推奨事項に対するエビデンスの質を 高い (A) 中等度 (B) または低い / 非常に低い (C) のいずれかに格付けした 推奨事項に対しては推奨度を 強い (1) または弱い (2) に格付けし その介入法に肯定的な推奨事項には + の記号を 否定的な推奨事項には - の記号を付した 推奨度が強い場合 ( 肯定的であっても否定的であっても ) その介入法による有益な影響が有害な影響 ( リスク 負荷 費用 ) を明らかに上回る または上回らないことを意味しており 推奨事項はいずれも ~ を推奨する という表現で記述している 推奨度が弱い場合 ( 肯定的であっても否定的であっても ) 有益な影響と有害な影響のバランスの不明確性を意味しており 推奨事項はいずれも ~ を提案する という表現で記述している 十分なエビデンスがない場合や合意形成に至らなかった場合 推奨しなかった ( 推奨度 0) エビデンスがない場合に 専門家の意見に基づく合意を根拠として用いなかった なお 作業部会のメンバーが関連研究の共著者である場合 利益相反の問題は一貫した方法に従って扱うこととし 本ガイドラインの作成にあたり医療業界からの助成は受けなかった 結論 : 本ガイドラインは 重症患者に対する疼痛 不穏およびせん妄の予防および治療のためのエビデンスに基づく総合的な患者中心型プロトコルを作成する上でロードマップとなるものである (Crit Care Med 2013; 41: ) キーワード : 不穏 鎮痛 救急医療 せん妄 エビデンスに基づく医療 GRADE ガイドライン 集中治療 アウトカム 疼痛 プロトコル 鎮静 ステートメントおよび推奨事項 1. 疼痛と鎮痛 a. 疼痛の発現 i. 内科 外科および外傷部門の成人 ICU 患者は 安静時も通常の ICU ケアにおいても日常的に疼痛を感じている (B) ii. 心臓血管外科術後の成人患者では 疼痛が認められることが一般的であるが 十分に治療されていない 女性の方が男性よりも心臓血管外科術後の疼痛を強く感じる (B) iii. 成人 ICU 患者では 一般的に処置に伴う疼痛が認められる (B) b. 疼痛の評価 i. すべての成人 ICU 患者に対して 定期的に疼痛のモニタリングを行うことを推奨する (+ 1B) ii. 内科 術後管理および外傷 ( 脳損傷を除く ) の成人 ICU 患者のうち 疼痛の自己申告は不能であるが 運動機能が障害されておら ず 行動が観察可能である者に疼痛のモニタリングを行う上で Behavioral Pain Scale (BPS) および Critical-Care Pain Observation Tool(CPOT) は最も妥当かつ信頼性のある行動学的疼痛スケールである これらの評価スケールを他の ICU 患者の集団で使用する場合およびフランス語や英語以外の言語に翻訳する場合は さらなる妥当性の検証試験が必要である (B) iii. 成人 ICU 患者における疼痛の評価をバイタルサイン ( またはバイタルサインを含む観察的疼痛スケール ) のみで実施することを提案しない (- 2C) iv. ただし これらの患者でさらに詳細な疼痛評価を開始すべきかどうかを判断する目的では バイタルサインを用いてもよいと提案する (+ 2C) c. 疼痛の治療 i. 成人 ICU 患者で胸腔チューブを抜去する場 2 January 2013 Volume 41 Number 1
5 Special Article 合は 疼痛緩和のために先行して鎮痛薬の投与および / または非薬物療法の介入 ( リラクセーションなど ) を行うことを推奨する (+ 1C) ii. 成人 ICU 患者でその他の侵襲的処置や疼痛を伴う可能性のある処置を行う場合も 疼痛緩和のために先行して鎮痛薬の投与および / または非薬物療法の介入を行うことを提案する (+ 2C) iii. 重症患者の非神経障害性疼痛に対する治療では 第一選択薬としてオピオイドの静脈内投与を検討することを推奨する (+ 1C) iv. 現在利用可能な静脈内投与におけるオピオイドは 同程度の目標鎮痛レベルを設定して用量調節を行えば いずれも有効性は同等である (C) v. オピオイドを減量する ( あるいはオピオイドの静脈内投与の必要性をなくす ) ため またオピオイド投与に伴う副作用を抑制するために 非オピオイド性鎮痛薬を検討することを提案する (+ 2C) vi. 神経障害性疼痛に対する治療では オピオイドの静脈内投与に加えてガバペンチンまたはカルバマゼピンの経腸投与を検討することを推奨する (+ 1A) vii. 腹部大動脈瘤手術を施行した患者における術後鎮痛では 胸部硬膜外麻酔 / 鎮痛を検討することを推奨する (+ 1B) viii. 腹部大動脈瘤の手術を施行した患者における術後鎮痛法として非経口オピオイドよりも腰椎硬膜外へのオピオイド投与を優先的に使用することに関して この患者集団でオピオイドの硬膜外投与が非経口オピオイドを凌ぐベネフィットはないため 推奨しない (0 A) ix. 胸腔内手術または非血管系腹部手術を施行した患者における胸部硬膜外鎮痛の使用に関して これらの患者でこの鎮痛薬投与法に関するエビデンスは不十分で一貫性がないため 推奨しない (0 B) x. 外傷性肋骨骨折患者では 胸部硬膜外鎮痛を検討することを提案する (+ 2B) xi. 内科の ICU 患者において全身性鎮痛よりも脳脊髄幹 / 局所鎮痛を優先することに関して この患者集団でのエビデンスがないた め 推奨しない (0 エビデンスなし) 2. 不穏と鎮静 a. 鎮静深度と臨床的アウトカム i. 成人 ICU 患者では 浅い鎮静レベルを維持すると 臨床的アウトカムが改善する ( 人工呼吸器装着期間の短縮 ICU 在室期間の短縮など )(B) ii. 浅い鎮静レベルを維持すると 生理的ストレス反応は大きくなるが 心筋虚血の発生率上昇とは関連しない (B) iii. これらの患者における鎮静深度と心理的ストレスの関係は不明である (C) iv. 成人 ICU 患者では 臨床的に禁忌でない限り 深い鎮静レベルよりも浅い鎮静レベルを維持するように鎮静薬の用量調節を行うことを推奨する (+ 1B) b. 鎮静深度および脳機能のモニタリング i.richmond Agitation-Sedation Scale(RASS) および Sedation-Agitation Scale(SAS) は 成人 ICU 患者の鎮静の質および深度を評価する上で最も妥当かつ信頼性のある鎮静評価ツールである (B) ii. 昏睡状態になく 麻痺が認められない成人重症患者に鎮静深度のモニタリングを行う場合 脳機能に関する客観的指標 ( 聴覚誘発電位 [AEP] Bispectral Index[BIS] Narcotrend Index[NI] Patient State Index[PSI] state entropy[se] など ) は主観的なスコア化された鎮静評価の代替として不適当であるため これらの指標を第一モニタリング手法として用いることを推奨しない (- 1B) iii. 筋弛緩薬を使用している成人 ICU 患者では主観的な鎮静評価が困難な場合があるため 主観的な鎮静評価法とともに脳機能に関する客観的指標 (AEP BIS NI PSI SE など ) を補助的に用いることを提案する (+ 2B) iv. 発作の既往またはその疑いがある成人 ICU 患者に非けいれん性発作の活動性のモニタリングを行う場合 あるいは頭蓋内圧上昇が認められる成人 ICU 患者に burst suppression に達する電位抑制作用のある薬剤の用量調節を行う場合は 脳波 (EEG) 測定法を用いることを推奨する (+ 1A) c. 鎮静薬の選択 i. 人工呼吸中の成人 ICU 患者に鎮静薬を使用 Critical Care Medicine 3
6 Barr et al する場合は 臨床的アウトカムを改善させるためにベンゾジアゼピン系薬 ( ミダゾラムまたはロラゼパム ) よりも非ベンゾジアゼピン系薬 ( プロポフォールまたはデクスメデトミジン ) を優先的に使用することを提案する (+ 2B) 3. せん妄 a. せん妄に伴うアウトカム i. 成人 ICU 患者では せん妄は死亡率の増加に関連する (A) ii. 成人 ICU 患者では せん妄は ICU 在室期間および入院期間の延長に関連する (A) iii. 成人 ICU 患者では せん妄は ICU 退室後の認知機能障害の発生に関連する (B) b. せん妄の検出およびモニタリング i. 成人 ICU 患者に対して 定期的にせん妄のモニタリングを行うことを推奨する (+ 1B) ii.confusion Assessment Method for the ICU (CAM-ICU) および Intensive Care Delirium Screening Checklist(ICDSC) は 成人 ICU 患者にせん妄のモニタリングを行う上で最も妥当かつ信頼性のあるツールである (A) iii. 臨床現場において 成人 ICU 患者に対し定期的なせん妄のモニタリングは実行可能である (B) c. せん妄の危険因子 i. 以下の 4 つのベースライン危険因子は ICU でのせん妄の発現に対して有意かつ正の相関を示す : 既存の認知症 高血圧および / またはアルコール依存症の既往歴 入院時点で重症度の高い疾患 (B) ii.icu 患者において 昏睡はせん妄の発現に関連する独立した危険因子である (B) iii. 成人 ICU 患者におけるオピオイドの使用とせん妄の発現の関連性については データが一貫していない (B) iv. 成人 ICU 患者において ベンゾジアゼピン系薬の使用はせん妄の発現に関連する危険因子である可能性がある (B) v. 成人 ICU 患者におけるプロポフォールの使用とせん妄の発現の関連性については データが不十分であり 評価できない (C) vi. せん妄の発現リスクがある人工呼吸中の成人 ICU 患者に鎮静薬を使用する場合は ベンゾジアゼピン系薬よりもデクスメデトミ ジンを使用した方がせん妄の発現率が低い可能性がある (B) d. せん妄の予防 i. 成人 ICU 患者では せん妄の発現抑制と期間短縮のために 可能な限り早期モビライゼーションを促すことを推奨する (+ 1B) ii. 成人 ICU 患者における薬物療法によるせん妄予防プロトコルの使用は これらの患者でこのプロトコルによるせん妄の発現率の低下または期間短縮を示す有力なデータがないため 推奨しない (0 C) iii. 成人 ICU 患者における非薬物療法と薬物療法の併用によるせん妄予防プロトコルの使用は これらの患者でこのプロトコルによるせん妄の発現率の低下を示すものはないため 推奨しない (0 C) iv. 成人 ICU 患者において せん妄予防の目的でのハロペリドールまたは非定型抗精神病薬投与は提案しない (- 2C) v. 成人 ICU 患者において せん妄予防を目的としたデクスメデトミジンの使用は これらの患者での有効性を示す有力なエビデンスがないため 推奨しない (0 C) e. せん妄の治療 i. 成人 ICU 患者において ハロペリドールがせん妄の期間を短縮するという公表されたエビデンスはない ( エビデンスなし ) ii. 成人 ICU 患者において 非定型抗精神病薬はせん妄の期間を短縮するかもしれない (C) iii.icu 患者において せん妄期間の短縮の目的ではリバスチグミン投与を推奨しない (- 1B) iv. トルサード ド ポアンツ (torsades de pointes) の著明なリスクがある患者 ( ベースライン時に QTc 間隔延長が認められる患者 QTc 間隔延長を起こすことが知られている薬剤を投与中の患者 これら不整脈の既往歴がある患者など ) に対して 抗精神病薬を使用することを提案しない (- 2C) v. アルコールまたはベンゾジアゼピン系薬の離脱症状とは無関係のせん妄を呈する成人 ICU 患者に対して せん妄の期間を短縮するために鎮静薬を使用する場合は ベンゾジアゼピン系薬の投与よりもデクスメデトミジンの静脈内持続投与を行うことを提案する (+ 2B) 4 January 2013 Volume 41 Number 1
7 Special Article 4.ICU のアウトカムを改善させるための疼痛 不穏およびせん妄の管理戦略 a. 人工呼吸中の成人 ICU 患者に対して 鎮静を毎日中断するか 目標鎮静レベルを浅く設定するかのどちらかを日常的に行うことを推奨する (+ 1B) b. 人工呼吸中の成人 ICU 患者に対して 鎮痛優先の鎮静 (analgesia-first sedation) を行うことを提案する (+ 2B) c. 成人 ICU 患者に対して 光 音をコントロールするための方策を取る 患者ケアを一括して行う 睡眠サイクルを障害しないように夜間の刺激を減らすなど環境を最適に整えることにより 睡眠を促すことを推奨する (+ 1C) d. 人工呼吸中の成人 ICU 患者において 睡眠を促すための特定の換気モードの使用に関して そのような介入の有効性を示すエビデンスが不十分なため 推奨しない (0 エビデンスなし) e. 成人 ICU 患者の疼痛 不穏およびせん妄の管理に関するガイドラインまたはプロトコルの使用を促すために 医療従事者への教育 印刷および / または電子化されたプロトコルやオーダー票 および適切な ICU 回診チェックリストを用いることを含む学際的な ICU チームアプローチを推奨する (+ 1B) 前版の 成人重症患者に対する鎮静 鎮痛薬の使用に関する臨床ガイドライン が公表されて以降 ICU 入室患者の身体的および精神的な快適さに関して われわれの知識は著しく進歩している (1) ICU 患者の疼痛 鎮静 不穏およびせん妄を評価するための妥当かつ信頼性のある臨床評価ツールが開発されたことにより 臨床医にとっては より適切な患者管理と 非薬物療法および薬物療法による介入のアウトカムの評価が可能になった (2,3) また ICU 患者の疼痛 不穏およびせん妄 (pain, agitation, and delirium:pad) の治療に一般的に使用される薬剤の臨床薬理学に関する知識が深まったことにより これらの薬剤へ長期間さらされることによる短期および長期のアウトカムを予測できるようになった (4-6) これらの薬剤の投与法や用量調節の方法が 薬剤の選択と同じように患者アウトカムに影響を及ぼすということもわかった (7-16) ほとんどの ICU 患者では 浅い鎮静レベルを維持しながら患者の快適さを実現する安全かつ有効な戦略を用いることで 臨床的アウトカムが改善する (9-13,16-20) 重症患者の疼痛 不穏 不安およびせん妄を取り除こうとすることは 末梢器官の十分な血流と機能を維持しながら心肺機能の安定を維持するといった 他の臨床上の管理目標と対立してしまうことがある (21,22) また さまざまな エビデンスに基づく バンドルや臨床アルゴリズムが増えており 管理目標はさらに複雑になる可能性がある また その一部は規制当局や保険支払機関によって広く採用されている (23-30) さらに 世界の地域によって文化や哲学 実践基準 人材および資源の確保の面に非常に大きな違いがあるため エビデンスに基づく診療の普及は難しい課題である (31-36) 今回の改訂版ガイドラインの目的は 成人 ICU 患者の臨床的アウトカムを改善するために PAD に対する最良の管理法を推奨することであり われわれは 公表された関連エビデンスについて 客観性および透明性を確保しながら厳格かつバイアスのない評価を行った これらのエビデンスを基に ICU 患者 患者家族 介護者および保険支払機関 規制当局の価値観や選好性ならびに重要な ICU 臨床的アウトカムとのバランスを考慮して 臨床において適用可能なステートメントおよび推奨事項を作成した 本ガイドラインの適用範囲は 内科 外科および外傷部門の成人 ICU 挿管および非挿管患者に対する PAD の短期および長期管理である 処置に対する鎮痛および鎮静については簡単にしか言及されていないが これについては 意識下鎮静に関する American Society of Anesthesiologists のガイドラインに詳述されている (37) なお 小児 ICU 患者における鎮痛および鎮静については 現在 American College of Critical Care Medicine( 米国クリティカルケア医学会 :ACCM) がガイドラインを別途 作成中である 本ガイドラインでは PAD モニタリングツールの計量心理学的側面に重点を置いており ICU 患者における PAD の管理法として 薬物療法および非薬物療法の両方について言及した また 重症患者におけるせん妄の発現過程に関するわれわれの理解が深まったことを反映して せん妄の予防 診断および治療にも重点を置いた 本ガイドラインは 臨床医が重症患者の PAD をより総合的に管理できるよう支援する意図で作成されたものであり 臨床医は 個々の患者のケアニーズや各地域における医療制度下で利用可能な資源の状況に合わせて本ガイドラインを利用すべきである なお 本ガイドラインは規定的なものではなく 絶対的に遵守すべきものでもない Critical Care Medicine 5
8 Barr et al a 表 1. エビデンスの質に影響を及ぼす因子 エビデンスレベル エビデンス の質 エビデンスのタイプ 定義 A 高い 質の高い RCT 推定される効果への確信は 今後研究が実施されてもおそら く変わらない B 中等度 重大な欠点のある RCT( ダウング レード ) b または質の高い OS( アッ プグレード ) c 今後の研究が 推定される効果への確信に重大な影響を及ぼす可能性があり 推定が変わるかもしれない C 低い OS 今後の研究が 推定される効果への確信に重大な影響を及ぼ す可能性が非常に高く 推定が変わる可能性がある RCT = ランダム化比較試験 OS = 観察研究 a Guyatt らの文献 (40) より引用 b 重大な欠点のある RCT:1) 試験デザインに欠点がある ( 計画 実施面のバイアス ) 2) 結果が一貫していない 3) エビデンスが間接的である 4) 結果の正確度が低い 5) 報告バイアスの可能性が高い c 質の高い OS:1) 治療効果が大きい 2) 用量反応性を示すエビデンスがある 3) すべての考え得るバイアスがみかけ上の治療効果を低くするものである 方法 PAD の管理に関して専門知識を有する専門家 20 名からなる ACCM の集学的な作業部会は 2002 年に公表された 成人重症患者に対する鎮静 鎮痛薬の使用に関する臨床ガイドライン (1) の改訂の責任を担った この作業部会の分科会に 疼痛と鎮痛 不穏と鎮静 せん妄および ICU アウトカムという 4 つのサブテーマがそれぞれ割り当てられた 各分科会は 臨床現場で直面する疑問 ( クリニカル クエスチョン ) およびアウトカム項目を提示し 文献の検索 レビューおよび評価を行い クリニカル クエスチョンに対するステートメントおよび推奨事項を作成し 担当のガイドラインセクションの草案をまとめた 文献のレビュー作業を円滑に進めるために 分科会は関連キーワードの総合リストを作成し 専門の図書館員 (C.K. University of Cincinnati) がそのキーワードリストを展開 整理した 具体的には 対応する Medical Subject Heading(MeSH) 用語のリスト ( 補足デジタルコンテンツ 1 A590) を作成し 臨床に関連したデータベースを検索し ソフトウェア Refworks (Bethesda MD) を用いて パスワード保護がかかった Web データベースを構築した すべての文献検索は 8 つのデータベース (PubMed MEDLINE Cochrane Database of Systematic Reviews Cochrane Central Register of Controlled Trials CINAHL Scopus ISI Web of Science International Pharmaceutical Abstracts) から行った 検索条件は 対象が成人 (> 18 歳 ) で 1999 年 12 月 (2002 年版ガイドラインの検索対象期間の終了時 ) から 2010 年 12 月までの期間に公表された ( または印刷中 ) 英語で書かれた文献とし 患者数が 30 例未満の研究 論説 叙述形式のレビュー 症例報告 動物試験 in vitro 試験および Letters to the Editor は除外した なお これ以降は 2 週間毎の頻度で自動検索を継続し 2012 年 7 月までの関連文献を本ガイドラインに盛り込んだが 2010 年 12 月以降に公表された研究は エビデンス評価および投票のプロセスを経ていない また 2002 年版ガイドラインの参考文献も Refworks データベースに含め 1999 年 12 月以前に公表された文献の絞り込み検索も必要に応じて行い 最終的には 19,000 件を超える文献を含めた 臨床現場でのエビデンスの質および推奨事項の推奨度を格付けするための構造化システムである Grading of Recommendations Assessment, Development and Evaluation( 推奨度の検討 開発 評価 :GRADE)( を用いて 今回の 2012 年版ガイドラインにおけるステートメントおよび推奨事項を作成した (38-40) 分科会は GRADE ワーキンググループのメンバー (R.J. D.C. H.S. G.G.) との共同作業を進め すべてのクリニカル クエスチョンを 記述的 な言葉または 実行可能な 言葉のどちらかで表現した 実行可能なクエスチョンについては 集団 (Population) 介入(Intervention) 比較(Comparison) アウトカム (Outcomes) の形式で構造化し 各介入法の臨床的アウトカムを 臨床判断における重要性の観点から 重大 重要 または 非重要 のいずれかに分類した 重大および重要なアウトカムについてのみエビデンスの評価を行い 重大なアウトカムについてのみ推奨事項を作成した グループ評価を円滑に進めるために 分科会のメンバーは データベースを検索して関連文献を特定し その PDF をアップロードした メンバー 2 名がそれぞ 6 January 2013 Volume 41 Number 1
9 Special Article a 表 2. 推奨度に影響を及ぼす因子 検討項目 エビデンスの質 有益な影響と有害な影響のバランスの不明確性 価値観および選好性に関する不明確性または多様性 その介入法を用いることが資源活用の点で賢明であるか否かの不明確性 推奨度への影響 エビデンスの質が低ければ 強い推奨となる可能性が低くなり 逆に高ければ 強い推奨となる可能性が高くなる リスクとベネフィットのバランスの不明確性が高ければ 強い推奨となる可能性が低くなり 逆に低ければ 強い推奨となる可能性が高くなる 価値観および選好性に関する多様性が大きければ 強い推奨となる可能性が低くなり 逆に小さければ 強い推奨となる可能性が高くなる その介入法の総費用が高ければ 強い推奨となる可能性が低くなり 逆に低ければ 強い推奨となる可能性が高くなる a Guyatt らの文献 (40) より引用 れ独立して 各研究の結果を要約した GRADE エビデンスプロファイルを作成し エビデンスの質を評価した 研究のデザインと特性の両方に基づいて エビデンスの質を高い ( レベル A) 中等度( レベル B) または低い / 非常に低い ( レベル C) のいずれかに評価することとし 研究特性によってはエビデンスの質を格上げまたは格下げできるようにした ( 表 1) 特定のアウトカムに関して複数の研究で異なる結果が得られており そのトピックについて公表された系統的レビューがない場合は GRADE ワーキンググループのメンバー (R.J.) が関連文献のメタアナリシスを実施した 各分科会はメンバー全体で各クエスチョンのエビデンスプロファイルの評価を行い Nominal Group Technique 法を用いて 総合的なエビデンスの質 ( 記述的および実行可能なクエスチョンの両方 ) および推奨度 ( 実行可能なクエスチョンのみ ) を決定し 他の作業部会メンバーによる評価を受けるためにエビデンスサマリーの草案を作成した すべての重大なアウトカムに関して エビデンスの質とリスク / ベネフィットに基づき 推奨事項に対する推奨度を強い (1) または弱い (2) のどちらかに評価し その介入法に肯定的な推奨事項には + の記号を 否定的な推奨事項には - の記号を付した( 表 2)(41,42) エビデンスがない場合や分科会のメンバー間で合意形成に至らなかった場合 推奨しない (0) とした 推奨事項の裏付けとなるエビデンスがない場合に 専門家の意見のみに基づく合意を根拠として用いなかった 推奨度が強い場合 その介入法に肯定的 (+ 1) であっても否定的 (- 1) であっても その介入法によるベネフィットがリスクを明らかに上回る ( または上回らない ) と作業部会のメンバーの大多数が判断したことを意味しており 患者および医療従事者は 選択できるのであれば 大多数がこれを実行する ( または実行しない ) ことを選択するだろうということである 推奨度が弱い場合 その介入法に肯定的 (+ 2) であっても否定的 (- 2) であっても その介入法によるベネフィットがリスクを上回る ( または上回らない ) 可能性が高いということであるが エビデンスの質が低い あるいはリスクとベネフィットのバランスが拮抗してほとんど相殺されるという理由により 作業部会のメンバーはこのリスクとベネフィットのバランスを確信できないことを意味している すなわち この情報に基づいて 患者および医療従事者の大多数がこれを実行する ( あるいは実行しない ) ことを選択するかもしれないが 別の選択をする者も少なくないだろうということである (40,43,44) 本ガイドライン全体を通じて 推奨度の強い推奨事項はいずれも ~を推奨する という表現で記述し 推奨度の弱い推奨事項はいずれも ~を提案する という表現で記述する すべてのステートメントおよび推奨事項に関する合意の形成には Delphi 変法で匿名投票方式を用いた (41,45) 作業部会のメンバーは 分科会が作成した GRADE エビデンスサマリーとステートメントおよび推奨事項を評価し オンライン電子調査ツールである E-Survey( Scottsdale AZ) を通じて 匿名による投票およびコメントのフィードバックを行った 各クエスチョンのエビデンスレベルに関する合意の基準は 過半数 (> 50%) の票を得ることとした 推奨事項の推奨度に関する合意の基準は 以下のとおりとした : その介入法 ( またはそれに対抗する介入法 ) に肯定的な推奨事項に対して 肯定票が作業部会メンバー全票の 50% 以上で 反対票が 20% 未満であることとし この基準に満たない場合は 推奨しない こととした 推奨度を 弱い ではなく 強い に格付けするための基準は 強い推奨に対する票が全票の 70% 以上であることとし そうでない場合は弱い Critical Care Medicine 7
10 Barr et al 推奨と評価した この合意形成法は GRADE ワーキンググループが提唱し 2008 年敗血症ガイドライン委員会がガイドライン推奨事項の作成における公平性 透明性および匿名性を確保するために採用しているものである (46,47) 投票結果とコメントを要約して 作業部会のメンバー全員に配布し 各メンバーが確認した 1 回目の投票で合意が形成されなかった場合 さらに議論を重ね 2 回目 3 回目の投票を行った すべてのクエスチョンに関する投票は 2010 年 12 月までに終了した 作業部会のメンバーによる各ステートメントおよび推奨事項に対する最終投票の集計結果およびコメントについては 補足デジタルコンテンツ 2( links.lww.com/ccm/a591) に要約を示す 作業部会のメンバーは 義務付けされた年 1 回の利益相反に関する申告を行った 重大な潜在的利益相反 ( 論文の共著者など ) がある者は それに関連するクエスチョンについて エビデンスの評価や格付けならびに分科会によるエビデンスステートメントおよび推奨事項の作成の過程から外れた すべてのクエスチョンのエビデンスレベルおよび推奨度の最終決定の過程において 作業部会のメンバー全員が匿名投票を行った 本ガイドラインの作成にあたり 医療業界からの助成や支援は受けなかった 計量心理学的解析本ガイドラインには 明瞭なコミュニケーションができない成人重症患者における 1) 疼痛の検出および評価 2) 鎮静深度および不穏度の評価 ならびに 3) せん妄の検出のためのさまざまなベッドサイド行動学的評価ツールの使用に関するステートメントおよび推奨事項が盛り込まれている これまでのところ ICU 患者におけるこれらのツールの使用に関して 計量心理学的特性 ( 信頼性および妥当性 ) および実施可能性を比較したデータは公表されていない 評価スケールの信頼性とは そのスケールを用いて疼痛 鎮静またはせん妄のスコアを時間的に ( 再テスト信頼性 ) あるいは評価者間で ( 評価者間信頼性 ) 再現する際の総合的な正確度を指す (48) 妥当性とは そのテストまたはスケールを用いた評価の結果から導かれる結論の妥当性を指す ( 例えば せん妄評価ツールが本当にせん妄を検出しているか?)(49) 具体的な妥当性検証方法として 内容的妥当性 基準関連妥当性および弁別的妥当性の検証がある 評価ツールを ある状況下の特定の集団に特定の目的で用いるとき その信頼性および妥当性の両方を示すことができる (48,49) 実施可 能性とは 臨床医がそのスケールを臨床現場 (ICU など ) に適用する際の容易さである 作業部会は 成人 ICU 患者に用いられている行動学的疼痛スケールについて 計量心理学的特性の評価および比較を行い その解析結果を既報のデータと比較した (50) 鎮静スケールおよびせん妄スケールについては 妥当性の検証方法が疼痛スケールとは異なっており 計量心理学的特性の評価や比較を行うための同様のスコア化法がなかった そこで作業部会は 計量心理学的評価の専門家 (D.S. C.J. C.W.) の助言を受けて 鎮静スケールおよびせん妄スケールの評価および比較を行うための同様のスコア化法を開発した (48) 疼痛 鎮静およびせん妄のスケールの計量心理学的特性を 1) 項目選択および内容的妥当性の検証 2) 信頼性 3) 妥当性 4) 実施可能性 5) 実施の意義または実施による患者アウトカムへの影響に基づいて評価すると 未調整スコアの範囲は 疼痛スケールで 0 ~ 25 鎮静スケールで 0 ~ 18 せん妄スケールで 0 ~ 21 であった これらのスケール間にあるスコアの意義の差を解消して結果を容易に解釈できるように 各特性項目に対してスコアの重み付けを行い 3 スケールとも総重み付けスコアの範囲が 0 ~ 20 になるようにした この詳細については 補足デジタルコンテンツ 3 ( に要約を記す 各スケールの計量心理学的特性は 重み付けスコアが 15 ~ 20 であれば極めて良好 12 ~ 14.9 であれば中等度と評価し 10 ~ 11.9 の場合は 妥当性の追加検証試験を要するという条件付きで許容可能 0 ~ 9.9 の場合は 十分なデータが報告されていない / 許容不能と評価した 計量心理学的特性の評価が中等度または極めて良好 ( すなわち 重み付けスコアが 12 以上 ) のスケールは 成人 ICU 患者で使用する上で十分な妥当性および信頼性があると判断した また 各スケールに関するエビデンスの質についても 計量心理学的解析用に一部改変した GRADE システムと同様の分類を用いて評価した すべての研究の評価およびすべてのスケールのスコア化は 2 名の評価者がそれぞれ独立して行った 疼痛と鎮痛 ICU 患者における疼痛の発現.International Association for the Study of Pain は 疼痛を 実質的または潜在的な組織損傷に伴う あるいはそのような損傷に関して表現される不快な感覚体験および感情体験 と定義している (51) この定義が示すように 疼痛とは主観的なものであり それを感じている者が報告して初めて 8 January 2013 Volume 41 Number 1
11 Special Article 存在する おそらく ほとんどの重症患者が ICU 在室期間中に疼痛を感じ (52) 疼痛がストレスの大きな原因と考えている (53-56) しかしながら 意識レベルの変化や 人工呼吸器の使用 あるいは高用量の鎮静薬または筋弛緩薬の使用により 疼痛を ( 言葉でも他の合図でも ) 自己申告することができない重症患者は多いと思われる (57) それでも 患者の疼痛を正確に評価することは 有効な疼痛治療を行うための大前提である International Association for the Study of Pain も述べているように 言葉によるコミュニケーションができないからといって その患者が疼痛を感じ 適切な疼痛緩和治療を必要としている可能性を否定することはできない (58) したがって 臨床医はコミュニケーション能力が損なわれた患者用に開発された評価法を用いて 患者の疼痛を正確に検出できなければならない このような患者の場合 運動機能が障害されていない限り 患者の行動学的反応を疼痛の代替指標として考えるべきである (59) 成人重症患者における疼痛の検出 定量および管理は重要課題であり これらの課題に対して 20 年以上にわたり研究が行われている (60) それにもかかわらず 内科および外科のどちらの ICU 患者においても 著明な疼痛の発現率は依然として 50% 以上である (61,62) 安静時の疼痛 (61) や 外科手術 外傷 熱傷あるいは癌に関連する疼痛に加え 患者は処置に伴う疼痛も感じる (63-70) このことは Agency for Health Care Policy and Research が 20 年前に公表した急性疼痛管理に関する最初の臨床ガイドラインでも強調されている (71) 処置に伴う疼痛は非常に一般的であり 処置に伴う疼痛に対して十分な治療が行われないことは 多くの ICU 患者にとって依然として大きな問題である (68) ICU 患者において 緩和されない疼痛の生理的および心理的な悪影響は重大で 長期にわたって持続する 昔から ICU 患者にとって疼痛は最大の悩みであり 十分な睡眠がとれない主要原因である (72) 最近では ICU 退室後の病棟入院患者を対象とした研究において ICU 在室期間中 患者の 82%( 患者数 75 例 ) が気管内チューブに関連する疼痛または不快感があったと記憶しており (56) 77%( 患者数 93 例 ) が中等度 ~ 重度の疼痛を感じていたと記憶している (73) ことが明らかにされている また 心臓血管外科手術患者の 82%( 患者数 120 例 ) が ICU 退室後 1 週間の時点で ICU 在室期間中の最大の心的外傷的な記憶を疼痛と回答したが 退室後 6 ヵ月時点でも 38% が ICU で の最大の心的外傷的な記憶として疼痛を記憶していた (74) Granja ら (75) の報告では ICU 退室後 6 ヵ月時点で 患者の 17%( 患者数 313 例 ) が重度の疼痛を感じていたと記憶しており 18% で心的外傷後ストレス障害 (PTSD) の発現リスクが高かったことが認められている Schelling ら (25) は 急性呼吸窮迫症候群のため ICU で治療を受けた 80 例を対象に 質問票を用いた長期追跡研究 ( 追跡期間中央値 4 年 ) を実施しており 正常データを示す対照群に比べて ICU 在室期間中の疼痛およびその他の心的外傷的状況を記憶している内科および外科患者では 慢性疼痛の発現率 (38%) および PTSD 症状の発現率 (27%) が高く 健康関連 QOL が低かった (21%) ことが認められている 疼痛により誘導されるストレス反応は ICU 患者に有害な影響を与えることがある 血中カテコラミン値が上昇すると 細動脈収縮が誘発され 組織灌流が障害され 組織酸素分圧が低下する可能性がある (76) 疼痛により誘導される他の反応としては 高血糖 脂肪分解および基質蛋白を生じる筋破壊の原因となる代謝亢進の可能性がある (77) さらに 蛋白の代謝刺激と低酸素血症によって 創治癒過程が障害され 創感染のリスクが上昇する 疼痛は 免疫系の重要な機能であるナチュラルキラー細胞活性を抑制し (78,79) 細胞傷害性 T 細胞数を減少させ 好中球の食作用活性を低下させる (80) 急性疼痛は 消耗性の慢性持続性疼痛 特に神経障害性疼痛の発現に関連する最も重要な危険因子である可能性がある (81) 成人 ICU 患者における緩和されない急性疼痛は非常に一般的であり 決して無害であることはなく 短期的にも長期的にも影響がある これらの患者の疼痛を適切に検出および治療することに 特別な注意を払わなければならない ICU 患者における疼痛の評価. 重症患者における疼痛の治療は 臨床医が再現性のある疼痛評価を行えるかどうか また 疼痛治療として行った介入法の適切性を判断するために患者のモニタリングを経時的に行えるかどうかにかかっている 患者からの疼痛の自己申告が ゴールドスタンダード であり 臨床医は まず患者に疼痛の自己評価をさせることを常に考えるべきである Chanques ら (82) は 100 例を超える ICU 患者を対象に 5 種類の疼痛強度評価スケールの評価を行っており このうち 0 ~ 10 点の視覚的に拡大した水平方向の数値評価スケールが最も妥当性および実施可能性の高いスケールであると認めている しかしながら 疼痛の自己申告が不能な重症患者の場合は Critical Care Medicine 9
12 Barr et al 表 3. 麻薬性鎮痛薬の薬理学 (1,128,440,472) 等鎮痛用量 (mg) 麻薬性鎮痛薬 IV PO 作用発現 (IV) 消失半減期 持続投与後消失半減期 代謝経路 フェンタニル 0.1 N/A 1~2 分 2~4 時間 200 分 (6 時間持続注入後 ) 300 分 (12 時間持続注入後 ) a N- 脱アルキル化 CYP3A4/5 基質 hydromorphone ~15 分 2~3 時間 N/A グルクロン酸化 モルヒネ ~10 分 3~4 時間 N/A グルクロン酸化 メタドン N/A c N/A c 1~3 日 15 ~ 60 時間 N/A N- 脱メチル化 CYP3A4/5 2D6 2B6 1A2 基質 レミフェンタニル N/A N/A 1~3 分 3~10 分 3~4 分 血漿エステラーゼによる 加水分解 PO = 経口 IV = 静脈内 N/A = 該当なし IBW = 理想体重 a 12 時間以降の場合および末梢器官機能障害がある場合 持続投与後消失半減期は予測できない上昇を示す b 投与間隔を延長した場合には 1 回の投与量の増量が必要になる可能性がある 例えば hydromorphone の場合は 3 時間毎に 0.5 mg IV 投与 モルヒ ネの場合は 3 ~ 4 時間毎に 4 ~ 8 mg IV 投与 c 等鎮痛用量表はメタドンの作用が過小評価となっている可能性がある モルヒネまたは hydromorphone の用量が高くなるにつれて モルヒネまたは hydromorphone からメタドンへの換算比が高くなる ( すなわち メタドンの作用が高くなる ) 経口メタドンと非経口メタドンの鎮痛作用の比は 2:1 であるが その信頼区間は広い d QTc は 心電図における QT 間隔 ( 補正済み ) である 妥当性 信頼性および実施可能性が確認された構造化ツールを用いて 患者の疼痛評価を行わなければならない (83) ICU 患者の疼痛は 効率的かつ再現性のある方法で 定期的に反復して評価することが重要である 客観的な疼痛指標はないが 疼痛指標として主に患者行動に注目した妥当かつ信頼性のある臨床上の疼痛評価ツールは存在している 行動学的疼痛評価ツールに関するレビューはこれまでにも公表されているが ツールの開発 妥当性の検証および ICU 患者への適用可能性についての最新の考察が必要である (50,84) 各種疼痛スケールの項目選択の手順および計量心理学的特性 ( 妥当性および信頼性 ) に関する詳細な系統的レビューがあれば 臨床医は疼痛スケールを選定しやすくなり ICU 患者での使用が標準化されてくると思われる 最近の研究から 行動学的疼痛スケールを使用すれば ICU における疼痛管理および臨床的アウトカムの改善 ( 鎮痛薬および鎮静薬の適正使用 人工呼吸器装着期間の短縮 ICU 在室期間の短縮など ) を達成できることが示されている (2,3,85) 疼痛の治療. フェンタニル hydromorphone メタドン モルヒネ レミフェンタニルなどのオピオイドは 重症患者の疼痛管理に使用する主要薬剤である ( 表 3)(62) 個々の患者でどの薬剤および投与レジメンが最適であるかは 薬剤の薬物動態および薬力学的特性を含むさまざまな因子によって決まってくる (52) Meperidine については 神経毒性の可能性があることから ICU 患者では徐々に使用されなくなっている (52) オピオイド必要量を減量するために 他の種類の鎮痛薬や疼痛調節系への作用薬 例えば 局所麻酔薬 ( ブピバカインなど ) 非ステロイド性抗炎症薬(ketorolac イブプロフェンなど ) アセトアミノフェン( 静脈内 ) 鎮痙薬などを鎮痛補助薬として用いることができる ( 表 4) しかしながら これらの薬剤を疼痛管理において単独投与した場合の安全性プロファイルおよび有効性に関して 重症患者を対象とした十分な検討は行われていない 非 ICU 患者を対象とした研究結果から導かれた薬物療法の指針を 重症患者には適用できない可能性がある (52) アセトアミノフェン( 静脈内 ) は 米国での使用が最近承認された薬剤であり 大手術または心臓血管外科術後の ICU 患者における術後疼痛に対して オピオイドと併用した場合に安全かつ有効であることが示されている (80,86-89) オピオイドのみでは十分な治療が困難な神経障害性疼痛には 消化管吸収能および消化管運動能が十分に維持されている ICU 患者であれば ガバペンチンおよびカルバマゼピンの経 10 January 2013 Volume 41 Number 1
13 Special Article 表 3( 続き ) 活性代謝物間欠投与法 IV 注入速度副作用およびその他の情報 なし なし 6- および 3- グルクロニド代謝物 0.5 ~ 1 時間毎に 0.35 ~ 0.5 μg/kg IV 投与 1 ~ 2 時間毎に b 0.2 ~ 0.6 mg IV 投与 1 ~ 2 時間毎に b 2 ~ 4mg IV 投与 0.7 ~ 10 μg/kg/ 時モルヒネに比べて低血圧が発現する可能性が低い 肝機能障害症例で蓄積性を示す 0.5 ~ 3 mg/ 時モルヒネ / フェンタニルに耐性を示す患者での選択肢となる 肝 / 腎機能障害症例で蓄積性を示す 2 ~ 30 mg/ 時肝 / 腎機能障害症例で蓄積性を示す ヒスタミン遊離作用がある N- 脱メチル化誘導体 IV/PO:6 ~ 12 時間毎に 10 ~ 40 mg 投与 IV:8 ~ 12 時間毎に 2.5 ~ 10 mg 投与 推奨しない オピオイド必要量の増加が認められる場合に 耐性発現を遅延させるために使用できる 麻薬性鎮痛薬の使用歴がない患者では 薬物動態および薬力学的特性を予測できない QTc d のモニタリングを行うこと なし N/A 負荷用量 :1.5 μg/kg IV 維持用量 : μg/kg/ 時 IV 肝 / 腎不全に伴う蓄積性はない 体重が IBW の 130% を超える場合は IBW を用いて用量を決定すること 腸投与による治療が可能である (90,91) 鎮痛薬の投与方法も 治療において検討すべきことの 1 つである 間欠静脈内投与法と持続静脈内投与法のいずれを選択すべきかは 薬剤の薬物動態 疼痛の頻度および重症度 患者の精神状態などによって決まってくると思われる (92) オピオイドおよびその他の治療薬の経腸投与は 消化管吸収能および消化管運動能が十分に維持されている患者に限定するべきである 特定の外科手術後の術後鎮痛には 局所または脳脊髄幹 ( 脊髄内または硬膜外 ) 鎮痛も行われることがある (93,94) 疼痛管理に音楽療法 リラクセーションなどの非薬物療法の介入法を補助的に用いると オピオイドを減量するとともに 鎮痛効果が高まる可能性がある これらの介入法は 低コストで 実施が容易であり 安全である ICU 患者の疼痛管理では複数の介入法を組み合わせて用いることが推奨されているが ICU 患者における非薬物療法の介入法の有効性に関する研究は少数しか公表されていない (52,95) 成人 ICU 患者では 入室時の診断に関係なく 疼痛が一般的にみられ 疼痛によって患者が ICU ケア ( 早期のモビライゼーション 人工呼吸器離脱など ) に参加することが困難になる場合もある したがって 臨床医は患者の疼痛を頻繁に再評価し 不十分または過 剰な鎮痛による後遺症の可能性を避けるよう鎮痛レベルを慎重に調節するべきである すべての重症患者に対し 患者の自己申告に基づいて あるいは系統的に適用される行動学的指標を用いて 定期的に再現性のある疼痛評価を行うべきである 疼痛が重度になるまで待つことなく 早期に検出し 治療を開始することで 疼痛の管理を行いやすくなる (52) 疼痛と鎮痛 : クエスチョン ステートメント 推奨事項 1. 疼痛の発現 a. クエスチョン : 成人 ICU 患者は ICU で処置に伴う疼痛以外の疼痛を感じるか? そうである場合 その疼痛にはどのような事象や状況が関係しているか?( 記述的なクエスチョン ) 回答 : 内科 外科および外傷部門の成人 ICU 患者は 安静時も通常の ICU ケアにおいても日常的に疼痛を感じている (B) 心臓血管外科術後の成人患者では 疼痛が認められることが一般的であるが 十分に治療されていない 女性の方が男性よりも心臓血管外科術後の疼痛を強く感じる (B) 根拠 : 内科 外科および外傷部門の ICU 患者は 安静時でも著明な疼痛を経験する (61,63,73) したがって 部門にかかわらず すべての成 Critical Care Medicine 11
14 Barr et al 表 4. 非麻薬性鎮痛薬の薬理学 (1,91,132,440) 非麻薬性鎮痛薬 ( 投与経路 ) 作用発現消失半減期代謝経路活性代謝物 ケタミン (IV) 30~40 秒 2~3 時間 N- 脱メチル化ノルケタミン アセトアミノフェン (PO) アセトアミノフェン (PR) 30~60 分 ( 変動あり ) 2~4 時間グルクロン酸化 スルホン化なし アセトアミノフェン (IV) 5~10 分 2 時間グルクロン酸化 スルホン化なし Ketorolac a (IM/IV) 10 分 2.4 ~ 8.6 時間水酸化 抱合 / 腎排泄なし イブプロフェン (IV) N/A 2.2 ~ 2.4 時間酸化なし イブプロフェン (PO) 25 分 1.8 ~ 2.5 時間酸化なし ガバペンチン (PO) N/A 5~7 時間腎排泄なし カルバマゼピン即放性製剤 (PO) 4~5 時間 初回投与時 25 ~ 65 時間 以降 12 ~ 17 時間 酸化 なし PO = 経口 PR = 経直腸 IM 筋注 IV = 静脈内 N/A = 該当なし a 年齢 65 歳超または体重 50 kg 未満の患者の場合 6 時間毎に 15 mg IV/IM 投与 ; 最大用量 60 mg/ 日 5 日間 人 ICU 患者で疼痛の評価を行うべきである 安静時の疼痛は 重大な臨床症候群として扱うべきである 心臓血管外科手術患者では 外科手術 咳嗽 呼吸ケアの処置および体動に伴う疼痛が依然として高頻度にみられるが これに対して十分に治療されていない 女性の方が男性よりも心臓血管外科術後の疼痛を強く感じる (73,96-98) したがって 心臓血管外科手術患者では疼痛を評価し 治療を行わなければならない 特に女性での発現に注意を払いつつ 患者の疼痛状態に応じて 個別に疼痛管理を行うべきである (97) b. クエスチョン : 成人 ICU 患者が処置時に経験する疼痛とは?( 記述的なクエスチョン ) 回答 : 成人 ICU 患者では 一般的に処置に伴う疼痛が認められる (B) 根拠 : 成人 ICU 患者において 胸腔チューブの抜去や創ケアなどの非外科的処置に伴う疼痛は高頻度にみられる (68,99) 疼痛レベルは一般的に中等度であり (68) 処置前の疼痛レベルや鎮痛薬の投与により異なってくる (100) 処 置前に鎮痛薬の投与が行われている患者は 25% 未満である (68) 処置に伴う疼痛は年齢によって異なり (64,66) 非白人の方が白人よりも強く感じる (64,66,68) 非外科患者および外科患者における処置に伴う疼痛の違いは 処置によって異なる (64,66) 血行動態の変化は 処置に伴う疼痛の指標としては妥当でない (99) 得られている情報から 先行的な鎮痛薬の投与にはベネフィットがあることが示唆されているが 先行的な介入を行わない場合の処置に伴う疼痛のリスクについては不明である 2. 疼痛の評価 a. クエスチョン : 成人 ICU 患者では疼痛の評価を定期的に行うべきか?( 実行可能なクエスチョン ) 回答 : すべての成人 ICU 患者に対して 定期的に疼痛のモニタリングを行うことを推奨する (+ 1B) 根拠 : 成人 ICU 患者では 疼痛の評価を定期的に行うことで臨床的アウトカムが改善する 疼痛の評価を 特にプロトコルに従って実施した場合に 鎮痛薬使用量の有意な削減 ICU 在室 12 January 2013 Volume 41 Number 1
15 Special Article 表 4( 続き ) 投与法 初期負荷時の用量 0.1 ~ 0.5 mg/kg IV 以降 0.05 ~ 0.4 mg/kg/ 時 4 ~ 6 時間毎に 325 ~ 1,000 mg 投与 最大用量 4 g/ 日 副作用およびその他の情報 急性オピオイド耐性の発現を減弱させる 幻覚およびその他の精神的混乱が発現する可能性がある 著明な肝機能障害を有する患者では禁忌となる可能性がある 4 時間毎に 650 mg IV 投与 ~ 6 時間毎に 1,000 mg IV 投与 最大用量 4 g/ 日 初回 30 mg IM / IV 投与 以降 6 時間毎に 15 ~ 30 mg IM / IV 投与 最長 5 日間 最大用量 = 120 mg/ 日 5 日間 6 時間毎に 30 分以上かけて 400 ~ 800 mg IV 注入 最大用量 = 3.2 g/ 日 以下に該当する場合 非ステロイド性抗炎症薬の使用を避ける : 腎機能障害 消化管出血 血小板異常 アンジオテンシン変換酵素阻害薬の併用 うっ血性心不全 肝硬変 喘息 冠動脈バイパス手術施行患者における周術期疼痛の治療では禁忌である 以下に該当する場合 非ステロイド性抗炎症薬の使用を避ける : 腎機能障害 消化管出血 血小板異常 アンジオテンシン変換酵素阻害薬の併用 うっ血性心不全 肝硬変 喘息 冠動脈バイパス手術施行患者における周術期疼痛の治療では禁忌である 4 時間毎に 400 mg PO 投与 最大用量 = 2.4 g/ 日 開始用量 = 1 日 3 回各 100 mg PO 維持用量 = 900 ~ 3,600 mg/ 日を 3 回に分けて投与 開始用量 = 1 日 2 回各 50 ~ 100 mg PO 維持用量 = 4 ~ 6 時間毎に 100 ~ 200 mg 投与 最大用量 = 1,200 mg/ 日 副作用 :( 高頻度の副作用 ) 鎮静 錯乱 めまい 運動失調 腎不全患者では用量調節を行うこと 急な中止に伴い 薬剤離脱症状 発作が発現する 副作用 :( 高頻度の副作用 ) 眼振 めまい 複視 立ちくらみ 倦怠感 ;( 稀な副作用 ) 再生不良性貧血 無顆粒球症 HLA-B1502 遺伝子を保有する患者では Stevens-Johnson 症候群または中毒性表皮壊死症が発現する さまざまな薬剤との間で肝酵素誘導による薬物相互作用が生じる 期間の有意な短縮および人工呼吸器装着期間の有意な短縮が認められている (3,62) 適切な治療を行う上で 疼痛の評価は 特に総合的な疼痛管理プロトコルの一環として必要不可欠である エビデンスの質は中等度であるが すべての ICU 患者で定期的に疼痛の評価を行うことによるベネフィットが これによるリスクを著しく上回るため これを強く推奨することが適切と考える b. クエスチョン : 疼痛の自己申告が不能な成人重症患者において 最も妥当かつ信頼性のある行動学的疼痛指標とは?( 記述的なクエスチョン ) 回答 : 内科 術後管理および外傷 ( 脳損傷を除く ) の成人 ICU 患者のうち 疼痛の自己申告は不能であるが 運動機能が障害されておらず 行動が観察可能である者に疼痛のモニタリングを行う上で Behavioral Pain Scale(BPS) および Critical-Care Pain Observation Tool(CPOT) は最も妥当かつ信頼性のある行動学的疼痛スケールである これらの評価スケールを他の ICU 患者の集団で使用する場合およびフランス語や英 語以外の言語に翻訳する場合は さらなる妥当性の検証試験が必要である (B) 根拠 : 次の 6 種類の行動学的疼痛スケールについて解析を行った :BPS BPS-Non-Intubated (BPS-NI) CPOT Non-Verbal Pain Scale(NVPS; 初版 [NVPS-I] および改訂版 [NVPS-R] の両方 ) Pain Behavioral Assessment Tool(PBAT) Pain Assessment, Intervention, and Notation (PAIN) アルゴリズム 表 5にこれらのスケールの計量心理学的スコアを示す 多少の欠点のあるデータではあるが 観察研究から 内科 術後管理および外傷部門の ICU 患者において BPS( 総スコアの範囲 :3 ~ 12) および CPOT ( 総スコアの範囲 :0 ~ 8) の計量心理学的特性が 評価者間信頼性 ( ) 弁別的妥当性 (101,102,104,107,109,110) および基準関連妥当性 ( ,109,110) の点で良好であるとの一貫したエビデンスが得られている 侵襲的処置を受けた術後成人 ICU 患者において スコア> 2 をカットオフ値として CPOT を用いた場合 著明な疼痛の予測における感度は 86% Critical Care Medicine 13
16 Barr et al 表 5. 疼痛スケールの計量心理学的スコア 疼痛スケール スコア化を行った計量心理学的特性項目 Critical Care Pain Observation Tool BPS BPS- Non-intubated Nonverbal Pain Scale a Pain Behavioral Assessment Tool Pain Assessment and Intervention Notation 項目選択に関する記述 内容的妥当性の検証 欠点の提示 内部一貫性 Ⅰ=1/Rev=2 0 0 評価者間信頼性 研究者チーム以外の者による評価者間信頼性の検証 評価者間信頼性が低いか一貫性がない場合の評価者内信頼性の検証 N/A Ⅰ=N/A /Rev=0 0 0 検証における被験者総数 基準関連妥当性の検証 : ゴールドスタンダード との相関性 基準関連妥当性の検証 : 感度 基準関連妥当性の検証 : 特異度 弁別的妥当性の検証 実施可能性 使用法の記述 臨床現場におけるスケールの使用意義 総スコア ( 範囲 :0 ~ 25) Ⅰ=11/Rev= 重み付けスコア b ( 範囲 :0 ~ 20) Ⅰ=9.2/Rev= 計量心理学的エビデンスの質 ( 重み付けスコアに基づく ) M M L VL L VL BPS = Behavioral Pain Scale Ⅰ= 初版 Rev = 改訂版 M = 中等度 L = 低い VL = 極めて低い N/A = 該当なし a Nonverbal Pain Scale にはⅠと Rev の 2 種類がある b 重み付けスコア ( 範囲 :0 ~ 20):15 ~ 20 の場合は計量心理学的特性が極めて良好 12 ~ 14.9 の場合は良好 (M) 10 ~ 11.9 の場合は許容可能であるが 追加検証試験を要する (L) 10 未満の場合は計量心理学的特性に関する十分なデータが報告されていない / 計量心理学的特性は許容不能 (VL) 特異度は 78% であった (111,112) この研究者らは BPS についても同様に 言葉によるコミュニケーションができない成人 ICU 患者における安静時と比べた侵襲的処置時の記述統計量に基づいて カットオフ値 (> 5) を提唱している (62) CPOT および BPS は 標準化された短期間の講習によって 問題なく ICU に導入することができ (2,85) これらを標準的に使用すれば より適切な疼痛管理が可能となり ICU 患者の臨床的アウトカムが改善する (2,3,85) BPS-NI は BPS を非挿管 ICU 患者用に改変したものであるが (113) これまでにまだ 30 例の 患者群でしか検証が行われていないため BPS- NI の計量心理学的特性を裏付けるには追加の研究が必要である NVPS(114) NVPS-R(115) PBAT(116) および PAIN(117) についても 計量心理学的特性を検討するためのさらなる研究が必要である c. クエスチョン : 成人 ICU 患者における疼痛の評価にバイタルサインを使用するべきか?( 実行可能なクエスチョン ) 回答 : 成人 ICU 患者における疼痛の評価をバイタルサイン ( またはバイタルサインを含む観察的疼痛スケール ) のみで実施することを提案し 14 January 2013 Volume 41 Number 1
17 Special Article ない (- 2C) ただし これらの患者でさらに詳細な疼痛評価を開始すべきかどうかを判断する目的では バイタルサインを用いてもよいと提案する (+ 2C) 根拠 : 内科 術後管理および外傷部門の ICU 患者における疼痛評価を目的としたバイタルサインの使用の妥当性に関して エビデンスは重大な欠点のある観察研究から得られたものであり 研究間で一貫していない 疼痛を伴う処置を受けた重症患者でバイタルサインが上昇する傾向があるとしても そのような上昇は疼痛の予測因子としては信頼性がない (66,101,105,107,110) バイタルサインは侵襲的および非侵襲的処置時とも上昇するという報告 (109) と非侵襲的処置時には安定しているという報告 (99) がある バイタルサインは 患者による疼痛の自己申告結果 (105,110) および行動学的疼痛スコア (101,107) のいずれにも相関していない ただし バイタルサインは疼痛 苦痛またはその他の因子により変化する可能性があるため これらの患者でさらに詳細な疼痛評価を行うべきかどうかの判断基準にはなり得ると考えられる (118) 3. 疼痛の治療 a. クエスチョン : 成人 ICU 患者において 処置に伴う疼痛に対して先行的に治療を行うべきか? ( 実行可能なクエスチョン ) 回答 : 成人 ICU 患者で胸腔チューブを抜去する場合は 疼痛緩和のために先行して鎮痛薬の投与および / または非薬物療法の介入 ( リラクセーションなど ) を行うことを推奨する (+ 1C) 成人 ICU 患者でその他の侵襲的処置や疼痛を伴う可能性のある処置を行う場合も 疼痛緩和のために先行して鎮痛薬の投与および / または非薬物療法の介入を行うことを提案する (+ 2C) 根拠 : 胸腔チューブの抜去を行う患者では 抜去の前に疼痛に対して薬物療法および非薬物療法を行うことを われわれは強く推奨する 胸腔チューブの抜去前に モルヒネの静脈内投与に加えてリラクセーション (119) 局所 valdecoxib(120) sufentanil( 静脈内 ) またはフェンタニル (121) の投与を受けた患者では 疼痛スコアが有意に低かった これらの研究によると 有益な影響の方が有害な影響より大きい その他の疼痛を伴う処置の場合も 大多数 の ICU 患者は処置前に疼痛に対する先行的な非薬物療法および / または薬物療法を受けることを望んでいると考えるのが妥当である b. クエスチョン : 成人 ICU 患者の疼痛緩和に使用すべき薬剤の種類は?( 実行可能なクエスチョン ) 回答 : 重症患者の非神経障害性疼痛に対する治療では 第一選択薬としてオピオイドの静脈内投与を検討することを推奨する (+ 1C) 現在利用可能な静脈内投与におけるオピオイドは 同程度の目標鎮痛レベルを設定して用量調節を行えば いずれも有効性は同等である (C) 神経障害性疼痛に対する治療では オピオイドの静脈内投与に加えて ガバペンチンまたはカルバマゼピンの経腸投与を検討することを推奨する (+ 1A) オピオイドを減量する( あるいはオピオイドの静脈内投与の必要性をなくす ) ため またオピオイド投与に伴う副作用を抑制するために 非オピオイド性鎮痛薬を検討することを提案する (+ 2C) 根拠 : 非神経障害性疼痛については 疼痛強度を下げるためにオピオイド主体のレジメンの使用を支持するエビデンスが得られている (87,90,91, ) 薬剤の価格や資源活用の問題は別として いずれのオピオイドも 同程度の目標鎮痛レベルを設定して用量調節を行えば 静脈内投与した場合の鎮痛効果は同程度のようであり 臨床的アウトカム ( 人工呼吸器装着期間 ICU 在室期間など ) も同様である 非神経障害性疼痛の場合 オピオイドに加えて アセトアミノフェンの静脈内投与 (87) シクロオキシゲナーゼ阻害薬の経口 静脈内または経直腸投与 (122,123,135) ケタミン静脈内投与 (132,137) など 非オピオイドを用いることができる 非オピオイドを用いることで オピオイドの総投与量が減少し オピオイド投与に伴う副作用の発現率と重症度が低下する可能性もある 神経障害性疼痛については 人工呼吸中の患者の場合 オピオイド単独を静脈内投与するよりも オピオイドの静脈内投与に加えてガバペンチンまたはカルバマゼピンを経口投与することで より高い疼痛緩和効果が得られる (90,91) オピオイドと非オピオイドの直接比較データがないため 特に ICU 患者における非オピオイド性鎮痛薬の作用について結論を導くことができない Critical Care Medicine 15
18 Barr et al c. クエスチョン : 胸部または腹部外科手術を受けた あるいは外傷性肋骨骨折を負った成人重傷患者 ( 人工呼吸中および人工呼吸器を装着していない ICU 患者の両方を含む ) の疼痛緩和において 鎮痛薬の投与法 ( 脳脊髄幹または非経口 ) はどれが推奨されるか?( 実行可能なクエスチョン ) 回答 : 腹部大動脈手術を施行した患者における術後鎮痛では 胸部硬膜外麻酔 / 鎮痛を検討することを推奨する (+ 1B) 腹部大動脈瘤の手術を施行した患者における術後鎮痛法として非経口オピオイドよりも腰椎硬膜外へのオピオイド投与を優先的に使用することに関して この患者集団でオピオイドの硬膜外投与が非経口オピオイドを凌ぐベネフィットはないため 推奨しない (0 A) 胸腔内手術または非血管系腹部手術を施行した患者における胸部硬膜外鎮痛の使用に関して これらの患者でこの鎮痛薬投与法に関するエビデンスは不十分で一貫性がないため 推奨しない (0 B) 外傷性肋骨骨折患者では 胸部硬膜外鎮痛を検討することを提案する (+ 2B) 内科の ICU 患者において全身性鎮痛よりも脳脊髄幹 / 局所鎮痛を優先することに関して この患者集団でのエビデンスがないため 推奨しない (0 エビデンスなし) 根拠 : 質の高いエビデンスにより 腹部大動脈手術を施行した患者において 硬膜外カテーテルを術前に留置していれば 胸部硬膜外麻酔 / 鎮痛は非経口オピオイド単独よりも疼痛緩和に優れることが示されている これらの患者における胸部硬膜外麻酔 / 鎮痛の稀な合併症は 術後心不全 感染症および呼吸不全である (138,139) 質の高いエビデンスにより これらの患者において 腰椎硬膜外オピオイドに非経口オピオイドを凌ぐベネフィットはないことが示されている ( ) 胸腔内手術または非血管系腹部手術を施行した患者における胸部硬膜外鎮痛の使用については 研究デザインにいくつかの欠点があるため 推奨することができない ( ) 肋骨骨折患者では 硬膜外鎮痛により 特に咳嗽発現時または深呼吸時の疼痛コントロールが改善し 肺炎の発現率が低下するが 低血圧のリスクが上昇する (150,151) 内科 ICU 患者における脳脊髄幹 / 局所鎮痛の使用については これを支持するエビデンスがない 不穏と鎮静鎮静の適応. 重症患者において 不穏および不安は高頻度に発現し 有害な臨床的アウトカムを伴う ( ) ICU 患者では 不穏および不穏による悪影響に対する治療として 鎮静薬が一般的に投与されている (157) 疼痛 せん妄 低酸素血症 低血糖 低血圧 アルコールおよびその他の薬物の離脱症状といった 不穏の基礎にある原因を速やかに検出し それに対して速やかに治療を行うことが重要である 鎮静薬を投与する前に 患者の快適さを維持する 十分な鎮痛薬を投与する 頻繁に見当識を回復させる 正常な睡眠パターンが保たれるように環境を最適に整えるといった 不安および不穏を抑制するための措置を試みるべきである 鎮静薬の用量調節を行い 浅い鎮静 ( 患者は覚醒可能で 単純な指示に意識的に従うことができる ) または深い鎮静 ( 患者は疼痛刺激に反応しない ) を維持することができる 複数の研究から 成人 ICU 患者では 持続的な深い鎮静には悪影響があり 浅い鎮静レベルを維持することにはベネフィットがあることが示されている (10,14,15,20,158) 鎮静スケールの使用 鎮静薬使用量の減量のためにデザインされた鎮静プロトコルの使用 および非ベンゾジアゼピン系薬の使用は ICU 患者のアウトカムの改善に関連しており これらの使用により 人工呼吸器装着期間の短縮 ICU 在室期間の短縮 入院期間の短縮 ならびにせん妄および長期認知機能障害の発現率の低下が認められている (7-10,12,13,18,19, ) 鎮静薬の臨床薬理学. 従来 ICU 患者の鎮静には ベンゾジアゼピン系薬 ( ミダゾラムまたはロラゼパム ) およびプロポフォールが一般的に使用されている 2002 年版ガイドラインでは ミダゾラムは短期の鎮静にのみ推奨され ロラゼパムは長期の鎮静に プロポフォールは間欠的な覚醒が必要な患者に推奨された (1) 臨床現場における鎮静管理の状況について調べた最近の調査によると ミダゾラムおよびプロポフォールは依然として ICU 患者の鎮静に使用される主要薬剤であるが ICU におけるロラゼパムの使用頻度は低下しており 稀にバルビツール酸系薬 ジアゼパムおよびケタミンが使用されている (62, ) デクスメデトミジンは 2002 年版ガイドラインの完成直前に米国で承認されたが 今では ICU 患者の鎮静管理に広く使用されるようになっている ( ) ICU 患者に処方されている鎮静薬の臨床薬理学については 表 6 に要約を示す 16 January 2013 Volume 41 Number 1
19 Special Article 表 6. 鎮静薬の臨床薬理学 (1) 薬剤 IV 負荷投与後の作用発現 消失半減期 活性 代謝物 負荷用量 (IV) 維持用量 (IV) 副作用 ミダゾラム 2~5 分 3~11 時間あり a ロラゼパム 15~20 分 8~15 時間なし 数分間かけて 0.01 ~ 0.05 mg/kg 0.02~0.04 mg/kg ( 2 mg) 0.02 ~ 0.1 mg/kg/ 時呼吸抑制 低血圧 必要に応じて 2 ~ 6 時間毎に 0.02 ~ 0.06 mg/kg あるいは 0.01~0.1 mg/kg/ 時 ( 10 mg/ 時 ) ジアゼパム 2~5 分 20~ 120 時間 あり a 5 ~ 10 mg 必要に応じて 0.5~6 時間毎に 0.03 ~ 0.1 mg/kg 呼吸抑制 低血圧 プロピレングリコール関連アシドーシス 腎毒性 e 呼吸抑制 低血圧 静脈炎 プロポフォール 1~2 分 短期投与時 : 3 ~ 12 時間 ; 長期投与時 : 50 ± 18.6 時間 なし 5 分間かけて b 5 μg/kg/ 分 5 ~ 50 μg/kg/ 分注射時疼痛 f 低血圧 呼吸抑制 高トリグリセリド血症 膵炎 アレルギー反応 プロポフォール注入症候群 プロポフォールによる深い鎮静では 浅い鎮静の場合に比べて覚醒が著明に遅延する デクスメデトミジン d 5 ~10 分 1.8 ~ 3.1 時間なし 10 分間かけて 0.2 ~ 0.7 μg/kg/ 時 1 μg/kg c 徐脈 低血圧 負荷投与に伴う高血圧 気道反射消失 IV = 静脈内 a 特に腎不全患者では 活性代謝物により鎮静作用が延長する b プロポフォールの IV 負荷投与は 低血圧が発現する可能性が低い患者でのみ行う c 血行動態が不安定の患者ではデクスメデトミジン IV 負荷投与をしない d デクスメデトミジンの維持用量は 忍容性に応じて 1.5 μg/kg/ 時まで増量してもよい e 静脈炎は ジアゼパムを末梢静脈投与した場合に生じる f 注射部位の疼痛は 一般的にプロポフォールを末梢静脈投与した場合に生じる ベンゾジアゼピン系薬. ベンゾジアゼピンは 脳内のγアミノ酪酸 A(GABA A ) ニューロン受容体を活性化する 抗不安作用 健忘作用 鎮静作用 催眠作用および鎮痙作用があるが 鎮痛作用はない (169,170) 健忘作用は鎮静作用の範囲を逸脱するものである (171) ロラゼパムはミダゾラムより作用が強く ミダゾラムはジアゼパムより作用が強い ミダゾラムおよびジアゼパムは ロラゼパムより脂溶性が高いため ロラゼパムよりも鎮静作用の発現が速やかで 分布容積が大きい 高齢患者は ベンゾジアゼピンの鎮静作用に対する感受性が有意に高い (171) ベンゾジアゼピンは呼吸抑制および全身性低血圧を誘発する可能性があり 心肺機能抑制作用のある他の薬剤 特にオピオイドと併用投与した場合にその傾向が強くなる (172) ベースライン時に呼吸不全および/ または循環動態不安定が認められる重症患者では ベンゾジアゼピン誘発性の心肺機能不安定が発現する可能性が高い (172) 長期投与に伴い ベンゾジアゼピン耐性が発現する ベンゾジアゼピンはいずれも肝臓で代謝される ベ ンゾジアゼピンのクリアランスは 肝機能障害やその他の肝疾患を有する患者および高齢患者で低下し チトクローム P450 酵素系および / または肝臓におけるグルクロン酸抱合を阻害する他の薬剤と併用した場合も低下する ( ) 腎不全患者でも ロラゼパムの消失半減期および臨床作用持続時間の延長がみられる (176,177) ミダゾラムおよびジアゼパムの活性代謝物は 長期投与に伴い 特に腎機能障害のある患者で蓄積される可能性がある (178) ベンゾジアゼピンのクリアランスは年齢とともに低下する (175,179,180) ベンゾジアゼピン系薬による鎮静からの覚醒は ベンゾジアゼピン系薬の長期投与 ( 末梢組織の飽和による ) 加齢 肝機能障害あるいは腎機能障害により遅延する可能性がある (171,175,181) ロラゼパムは ミダゾラムに比べて作用が強く 消失が遅いため ロラゼパムによる短期 (1 ~ 2 日 ) の鎮静からの覚醒はミダゾラムの場合より遅延する可能性がある しかしながら ICU 患者を対象としたこれらの薬剤の持続投与に関する比較研究によると ロラゼパムを用いた場合よりもミダゾラムを用いた場合の方が鎮静からの覚醒 Critical Care Medicine 17
20 Barr et al 時間は長く バラツキも大きい (171,175, ) ジアゼパムは 末梢組織の飽和と 腎機能障害のある患者で蓄積する活性代謝物の存在により 作用の持続時間が長い (185) ロラゼパムの非経口製剤には 希釈剤としてプロピレングリコールが含まれているが ICU 患者ではこれが毒性を誘発する可能性がある ( ) プロピレングリコール毒性は 代謝性アシドーシスおよび急性腎損傷として生じる 重症患者ではこれらの病態が頻繁に生じるため ロラゼパムの投与に関連している可能性は見過ごされるかもしれない 当初 非常に高い用量で持続注入した場合 (15 ~ 25 mg/ 時 ) にのみ蓄積が認められると考えられていたが 現在得られているエビデンスによると 1 日総静脈内投与量が 1 mg/kg と少なくても プロピレングリコール毒性が生じる可能性がある (191) 信頼性のあるスクリーニング 観察ツールとして 血清浸透圧較差が使用されており 浸透圧較差 > 10 ~ 12 mosm/l という閾値は ロラゼパムの投与に伴いプロピレングリコールの著明な蓄積が生じる患者の特定に有用な可能性がある (187,191) プロポフォール. プロポフォールは 中枢神経系にある複数の受容体 (GABA A 受容体 グリシン受容体 ニコチン受容体および M 1 ムスカリン受容体を含む ) に結合して神経伝達を阻害する静脈内投与の鎮静薬である ( ) プロポフォールには鎮静作用 催眠作用 抗不安作用 健忘作用 制吐作用および鎮痙作用があるが 鎮痛作用はない (195,196) ICU 患者において 浅い鎮静レベルでのプロポフォールの健忘作用はベンゾジアゼピン系薬の作用より小さい (197) プロポフォールは脂溶性が高く 血液脳関門を速やかに通過するため 鎮静の作用が速やかに発現する 脂溶性が高いことから 末梢組織への再分布も速やかである このように再分布が速やかであるのに加え 肝および肝外クリアランスが高いため プロポフォールの短期投与では 投与後の作用の消失も速やかである 鎮静作用の持続時間が短いことから プロポフォールは神経学的評価のために頻繁な覚醒が必要な患者で有用と考えられ 毎日鎮静中断のプロトコルも実践しやすいと考えられる (183,198,199) しかしながら プロポフォールの長期投与では 末梢組織の飽和が生じ 覚醒が遅延する可能性がある (198) プロポフォールは 用量依存的な呼吸抑制および全身性血管拡張による低血圧を誘発する これらの作用は プロポフォールを他の鎮静薬やオピオイドと併用 した場合に特に強く発現する可能性がある ベースライン時に呼吸不全および / または循環動態不安定が認められる患者では プロポフォールの投与に伴う心肺機能不安定が発現する可能性が高い その他の副作用として 高トリグリセリド血症 急性膵炎およびミオクローヌスが挙げられる ( ) プロポフォールは 卵レシチンおよび大豆油を含有する 10% 脂質乳濁液中に溶解しているため 卵または大豆へのアレルギーがある患者ではアレルギー反応が誘発される可能性がある プロポフォールの一部のジェネリック医薬品には亜硫酸塩保存料が含まれており これもアレルギー反応を誘発する可能性がある (196) プロポフォールの投与に伴い 稀にプロポフォール注入症候群 (PRIS) が発現することがある その徴候および症状はさまざまであるが 例えば 経時的悪化を示す代謝性アシドーシス 高トリグリセリド血症 昇圧薬の必要量増加を伴う低血圧 不整脈などがみられる 急性腎損傷 高カリウム血症 横紋筋融解症および肝機能障害も PRIS 症例で時々報告されている (205,206) PRIS のメカニズムについては ミトコンドリア機能障害 脂肪酸酸化障害 炭水化物代謝の脂肪基質への転換およびプロポフォール代謝物の蓄積が可能性として考えられる (207) 通常 PRIS はプロポフォールを高用量 (> 70 μg/kg/ 分 ) で長期投与した場合に発現するが 低用量注入時にも発現する可能性がある (208,209) プロポフォールの注入に伴う PRIS の発現率は約 1% である (210) PRIS による死亡率は高く ( 最高 33%) 注入の中止後でも死亡の可能性がある (202) PRIS は臨床像が多様で 特異性のある診断法がなく 発現が稀であるため 生命を脅かす可能性のあるこの病態の検出は難しい PRIS を早期に認識し 疑われる場合はプロポフォールを早期に中止することが極めて重要である 時期が遅れると PRIS 患者の管理は対症的な治療となる デクスメデトミジン. デクスメデトミジンは選択的 α 2 受容体作動薬であり 鎮静作用 鎮痛薬 / オピオイドの節減効果および交感神経遮断作用があるが 鎮痙作用はない (211,212) デクスメデトミジンの鎮静パターンは 他の鎮静薬とは大きく異なる デクスメデトミジンで鎮静された患者は 覚醒および対話が比較的容易で 呼吸抑制はほとんどみられない (213,214) デクスメデトミジンの静脈内投与開始後 15 分以内に鎮静作用が発現し 1 時間以内に鎮静効果がピークとなる (167,215) デクスメデトミジンを静脈内に初期負荷投与すると 鎮静作用の発現が早まる可能性があ 18 January 2013 Volume 41 Number 1
21 Special Article るが 重症患者では血行動態不安定となる可能性が高くなる (216) デクスメデトミジンは速やかに末梢組織に再分布し 肝臓で代謝される (217) 肝機能が正常な患者の場合 消失半減期は約 3 時間である (215) 重度肝機能障害のある患者では デクスメデトミジンの消失が障害されるため 覚醒が遅延する可能性があり デクスメデトミジンの投与量を減量させる必要性がある (218) デクスメデトミジンは 米国において最大用量 0.7 μg/kg/ 時 ( 処置時の鎮静では 1.0 μg/kg/ 時 ) で ICU 患者の短期鎮静 (< 24 時間 ) に承認されているのみであるが 複数の研究から さらに高用量 ( 最高 1.5 μg/kg/ 時 ) で 24 時間以上 ( 最長 28 日 ) 注入する場合も デクスメデトミジンは安全かつ有効であることが確認されている (216, ) 最も一般的に認められるデクスメデトミジンの副作用は 低血圧および徐脈である (223) 静脈内への負荷投与は 低血圧または高血圧を誘発する可能性がある (215,224) デクスメデトミジンは呼吸ドライブに大きな影響を及ぼさないことから 米国では 非挿管 ICU 患者での使用が承認されている唯一の鎮静薬となっており 抜管後 必要に応じて注入を継続することができる ( ) しかしながら デクスメデトミジンは中咽頭筋の緊張低下を誘発する可能性があり 非挿管患者ではこれによって気道閉塞が生じる可能性があるため これらの患者では低換気および低酸素血症の両方について持続的な呼吸のモニタリングが必要である (225) デクスメデトミジンのオピオイド節減効果により 重症患者におけるオピオイド必要量は減少する可能性がある (219,220,224,228) デクスメデトミジンの鎮痛作用機序については意見が分かれている (229) α 2 受容体は脊髄背部および上位中枢に局在するが 脊髄以外の経路によるデクスメデトミジンの鎮痛作用も報告されている (230) 最近の研究によると デクスメデトミジンが投与された ICU 患者では ミダゾラムで鎮静された患者に比べてせん妄の発現率が低い可能性がある (220) 不穏と鎮静 : クエスチョン ステートメント 推奨事項 1. 鎮静深度と臨床的アウトカムクエスチョン : 成人 ICU 患者の鎮静レベルを浅く維持するべきか? ( 実行可能なクエスチョン ) 回答 : 成人 ICU 患者では 浅い鎮静レベルを維持すると 臨床的アウトカムが改善する ( 人工呼吸器装着期間の短縮 ICU 在室期間の短縮など )(B) 浅い鎮静レベルを維持すると 生理的ストレス反応は大きくなるが 心筋虚血の発生率上昇とは関連しな い (B) これらの患者における鎮静深度と心理的ストレスの関係は不明である (C) 成人 ICU 患者では 臨床的に禁忌でない限り 深い鎮静レベルよりも浅い鎮静レベルを維持するように鎮静薬の用量調節を行うことを推奨する (+ 1B) 根拠 :13 件の研究において ICU 患者における鎮静深度と臨床的アウトカム ( 人工呼吸器装着期間 ICU 在室期間 生理的ストレスの指標 ICU 退室後心理的ストレスの評価を含む ) の直接的な関係について検討が行われている (10,14,15,20,158, ) このうち 5 件の研究で 深い鎮静レベルの場合に人工呼吸器装着期間および ICU 在室期間の延長が認められた (10,14,15,20,158) また 3 件の研究で 浅い鎮静レベルの場合に生理的ストレスの増大の所見として カテコラミン濃度の上昇および / または酸素消費量の上昇が認められたが (232,235,236) 別の 1 件では認められなかった (233) これらの患者において 生理的ストレスのマーカーの上昇と臨床的アウトカム ( 心筋虚血など ) の間に明確な関係が認められなかったことから この変化の臨床的意義は不明である ( ) 4 件の研究において 鎮静深度と ICU 退室後心理的ストレスの関係について検討が行われた (20,231,237,238) このうち 1 件で 毎日鎮静中断のプロトコルを実践しても 心理的な有害アウトカムは誘導されないことが示され (231) 別の 1 件でも 鎮静レベルが浅い患者において 心理的な有害事象の発現率は低かった (20) 3 件目の研究では 鎮静レベルが深いほど記憶再生の率が低かったが 妄想記憶と浅いレベルの鎮静は相関しないことが認められた (238) 一方 4 件目の研究では 覚醒時間とストレスを伴う ICU 記憶の再生との間に関連性が認められた (237) ICU での鎮静深度と ICU 退室後の心理的ストレスの関係に関するエビデンスの総合的な質は低く これらの研究結果は一貫していない すなわち ICU 患者で浅い鎮静レベルを維持することに関して 総合的なベネフィットがリスクを上回っているように思われる 2. 鎮静深度および脳機能のモニタリング a. 鎮静スケールクエスチョン : 人工呼吸中の成人 ICU 患者において鎮静の深度および質を評価する上で 最も妥当かつ信頼性のある主観的鎮静スケールはどれか?( 記述的なクエスチョン ) Critical Care Medicine 19
22 Barr et al 表 7. 鎮静スケールの計量心理学的スコア 鎮静スケール スコア化を行った計量心理学的特性項目 Observer s Assessment of Alertness/Sedation Scale Ramsay Sedation Scale New Sheffield Sedation Scale Sedation Intensive Care Score 項目選択に関する記述 内容的妥当性の検証 欠点の提示 評価者間信頼性 研究者チーム以外の者による評価者間信頼性の検証 評価者間信頼性が低いか一貫性がない場合の評価者内信頼性の検証 NA 0 NA NA 検証における被験者総数 基準関連妥当性の検証 弁別的妥当性の検証 実施可能性 使用法の記述 臨床現場におけるスケールの使用意義 総スコア ( 範囲 :0 ~ 18) 重み付けスコア a ( 範囲 :0 ~ 20) 計量心理学的エビデンスの質 ( 重み付けスコアに基づく ) VL VL VL L VG = 極めて良好 M = 中等度 L = 低い VL = 極めて低い N/A = 該当なし a 重み付けスコア ( 範囲 :0 ~ 20):15 ~ 20 の場合は計量心理学的特性が極めて良好 (VG) 12 ~ 14.9 の場合は良好 (M) 10 ~ 11.9 の場合は許容可能であるが 追加検証試験を要する (L) 10 未満の場合は計量心理学的特性に関する十分なデータが報告されていない / 計量心理学的特性は許容不能 (VL) 回答 :Richmond Agitation-Sedation Scale(RASS) および Sedation-Agitation Scale(SAS) は 成人 ICU 患者の鎮静の質および深度を評価する上で最も妥当かつ信頼性のある鎮静評価ツールである (B) 根拠 : 成人 ICU 患者における鎮静深度および不穏のモニタリングに使用できる数種類の主観的鎮静スケールが開発されており これらの計量心理学的特性に関するデータは十分に報告されている しかしながら 評価が行われた特性項目の総合的な範囲やエビデンスの質はスケール間で大きく異なっている われわれは 成人 ICU 患者における鎮静の深度および質の評価用に開発されている以下の 10 種類の主観的鎮静スケールについて 計量心理学的特性データを評価した :1)Observer s Assessment of Alertness/Sedation Scale(OAA/S) 2)Ramsay Sedation Scale(Ramsay) 3)New Sheffield Sedation Scale(Sheffield) 4)Sedation Intensive Care Score(SEDIC) 5)Motor Activity Assessment Scale(MAAS) 6)Adaptation to the Intensive Care Environment(ATICE) 7) Minnesota Sedation Assessment Tool(MSAT) 8) Vancouver Interaction and Calmness Scale(VICS) 9)SAS 10)RASS 総患者数 2,805 例の 27 件の研究について評価を行った (2, ) このうち 26 件は観察研究であり 残りの 1 件では 事前にスコア化された患者鎮静レベルのビデオに対する盲検ランダム化法による評価が行われた (253) 10 種類すべての鎮静スケールの計量心理学的特性については 表 7に要約を示す RASS および SAS は 計量心理学的スコア ( すなわち 評価者間信頼性 収束的または弁別的妥当性 ) が最も高く 検証における被験者数も十分であった 両スケールとも ICU 臨床医を含む評価者による評価において 評価者 20 January 2013 Volume 41 Number 1
23 Special Article 表 7( 続き ) 鎮静スケール Motor Activity Assessment Scale Adaptation to the Intensive Care Environment Minnesota Sedation Assessment Tool Vancouver Interaction and Calmness Scale Sedation- Agitation Scale Richmond Agitation- Sedation Scale NA NA NA NA NA NA L M M M VG VG 間信頼性が高く (240,262,263) さまざまな臨床状況で鎮静レベル間の弁別が可能であった (246,250,258,261) これらのスケールによる鎮静スコアと脳波 (EEG) または Bispectral Index(BIS) 値の間には 中等度 ~ 高度の相関性が認められた (244,246,258) さらに RASS については 鎮静薬の投与に対する目標鎮静深度が常に一致しており このスケールの実施可能性が示された (2,246,254) ATICE MSAT および VICS は 計量心理学的エビデンスの質は良好であったが 一部の計量心理学的特性 ( 収束的妥当性 弁別的妥当性など ) の評価が行われていなかった (242,243,249,259, 260) MAAS SEDIC Sheffield Ramsay および OAA/S については エビデンスの質が低く ICU 患者における鎮静の深度と質を評価する上での信頼性および妥当性について 追加研究や計量心理学的特性の検証が必要である (239,241,242,245, , ,255,261, 262,264) 要約すると 各鎮静スケールの計量心理学的特性を比較評価した結果 重症患者で使用する場合に最も妥当かつ信頼性のあるスケールは RASS および SAS であり ATICE MSAT および VICS の妥当性および信頼性は中等度であった 残りのスケールについては 重症患者での鎮静深度の評価における信頼性および妥当性を詳細に評価する追加研究が必要である b. 神経学的モニタリング i. クエスチョン : 昏睡状態になく 筋弛緩薬を使用していない成人 ICU 患者において 鎮静深度の評価に脳機能に関する客観的指標 ( 聴覚誘発電位 [AEP] Bispectral Index[BIS] Narcotrend Index[NI] Patient State Index [PSI] state entropy[se] など ) を使用するべきか?( 実行可能なクエスチョン ) Critical Care Medicine 21
24 Barr et al 回答 : 昏睡状態になく 麻痺が認められない成人重症患者に鎮静深度のモニタリングを行う場合 脳機能に関する客観的指標 (AEP BIS NI PSI SE など ) は主観的なスコア化された鎮静評価の代替として不適当であるため これらの指標を第一モニタリング手法として用いることを推奨しない (- 1B) ii. クエスチョン : 筋弛緩薬を使用している成人 ICU 患者において 鎮静深度の評価に脳機能に関する客観的指標 (AEP BIS NI PSI または SE) を使用するべきか?( 実行可能なクエスチョン ) 回答 : 筋弛緩薬を使用している成人 ICU 患者では主観的な鎮静評価が困難な場合があるため 主観的な鎮静評価法とともに脳機能に関する客観的指標 (AEP BIS NI PSI SE など ) を補助的に用いることを提案する (+ 2B) iii. クエスチョン : 発作の既往またはその疑いがある成人 ICU 患者において 非けいれん性発作の活動性を検出しようとする場合 あるいは burst suppression に達するために電位抑制作用のある薬剤の用量調節を行う場合に EEG 測定法を使用するべきか?( 実行可能なクエスチョン ) 回答 : 発作の既往またはその疑いがある成人 ICU 患者に非けいれん性発作の活動性のモニタリングを行う場合 あるいは頭蓋内圧上昇が認められる成人 ICU 患者に burst suppression に達する電位抑制作用のある薬剤の用量調節を行う場合は EEG 測定法を用いることを推奨する (+ 1A) 根拠 : われわれは 成人 ICU 患者を対象に鎮静の客観的指標とスコア化された鎮静評価を比較した 18 件の研究について評価を行った (244,248,258, ) 検討が行われた客観的指標は EEG の未処理パラメータおよび処理パラメータと AEP であり EEG の処理パラメータ ( 未処理 EEG 信号を特定のアルゴリズムにより特定の指数に変換したもの ) は BIS Bispectral Index XP (BIS-XP SE) NI および PSI であった 総合的に エビデンスは一貫していなかった 質が中等度の 15 件の研究では 重症患者において AEP または EEG 信号の処理パラメー タ (BIS NI SE および PSI を含む ) に基づく鎮静の客観的指標は 主観的鎮静評価の補助手段として有用な可能性が示された (244,248,258,266,267, ,276, ) しかしながら これらの研究のほとんどで 検討対象の客観的指標と鎮静スコアの相関に対して筋電図信号が負の影響を及ぼすことが報告された 質が中等度の別の 5 件では 鎮静深度の評価における客観的指標の使用に スコア化された主観的評価を超えるベネフィットはないことが示された ( ,277,284) ほとんどの研究において これらの客観的指標は深い鎮静と浅い鎮静の判別が可能なだけで 指標値と特定の鎮静スコアとの間の相関は乏しく 指標値は筋電図信号のアーチファクトにより負の影響を受けることが確認された 複数の研究から 発作既往があるか発作リスク ( 外傷性脳損傷 脳内出血 脳血管障害 原因不明の意識レベル低下が認められる患者など ) がある ICU 患者において 持続的な EEG 測定は非けいれん性発作の活動性の検出に有用であることが示されている (275,281) 持続的 EEG 測定は 頭蓋内圧上昇が認められる重症患者に burst suppression に達する電位抑制作用のある薬剤の用量調節を行う場合にも有用な可能性がある (275,281) 3. 鎮静薬の選択クエスチョン : 人工呼吸中の成人 ICU 患者の鎮静には ベンゾジアゼピン系薬ではなく非ベンゾジアゼピン系薬を使用するべきか?( 実行可能なクエスチョン ) 回答 : 人工呼吸中の成人 ICU 患者に鎮静薬を使用する場合は 臨床的アウトカムを改善させるためにベンゾジアゼピン系薬 ( ミダゾラムまたはロラゼパム ) よりも非ベンゾジアゼピン系薬 ( プロポフォールまたはデクスメデトミジン ) を優先的に使用することを提案する (+ 2B) 根拠 : 一般的に ICU 患者に使用する鎮静薬は 1) 各患者における適応および鎮静目標 2) 該当する患者集団における薬剤の臨床薬理学 ( 作用の発現および消失 副作用プロファイルを含む ) ならびに 3) その鎮静薬 22 January 2013 Volume 41 Number 1
25 Special Article の使用に伴う総費用に基づいて選択するべきである ICU 患者を対象とした鎮静薬の影響に関するアウトカム研究は 主としてベンゾジアゼピン系薬 ( ミダゾラムまたはロラゼパム ) と非ベンゾジアゼピン系薬 ( プロポフォールまたはデクスメデトミジン ) を比較したものである われわれが文献レビューを行った時点で 鎮静にプロポフォールが使用された ICU 患者とデクスメデトミジンが使用された ICU 患者の臨床的アウトカムを比較した研究は 質の低い 2 件が公表されているのみであった (285,286) 鎮静にケタミンまたはその他の鎮静薬が使用された ICU 患者の臨床的アウトカムを比較 した研究はない われわれが評価を行った複数の研究から ベンゾジアゼピン系薬による鎮静レジメンを持続的に用いると 人工呼吸器装着期間の延長 ICU 在室期間の延長 せん妄の発現など 有害な臨床的アウトカムを伴うことが示唆されている (29,183,220, ) ただし このような結果が一貫して報告されているわけでもなかった (197,222,285, ) われわれは 鎮静にベンゾジアゼピン系薬 ( ミダゾラムまたはロラゼパム ) が使用された ICU 患者と非ベンゾジアゼピン系薬 ( プロポフォールまたはデクスメデトミジン ) が使用された ICU 患者の臨床的アウトカムを比較した総患者数 1,551 例の 13 件の研究につい ベンゾジアゼピン系薬 非ベンゾジアゼピン系薬 試験または 試験サブグループ 平均 SD 患者数 平均 SD 患者数 重み 平均差 IV 投与 変量効果モデル 95% CI 平均差 IV 投与 変量効果モデル 95% CI Hall 時間以上 M/P SD Hall ~ 72 時間 M/P SD Pandharipande 2007 L/D IQR Carson 2006 L/P IQR Hall 時間未満 M/P SD Riker 2009 M/D SD 中央値 Searle 1997 M/P SD Huey-Ling 2008 M/P SD % 0.68 [-4.66 ~ 6.02] % [-4.83 ~ 4.27] % 1.50 [-1.86 ~ 4.86] % 2.10 [-0.44 ~ 4.64] % [-2.31 ~ 1.37] % 1.70 [0.55 ~ 2.85] % 0.20 [-0.84 ~ 1.24] % 0.30 [-0.27 ~ 0.87] 総合 (95% CI) % 0.57 [0.03 ~ 1.10] 異質性 :Tau 2 = 0.08;Chi 2 = 8.03 df = 7(p = 0.33) I 2 = 13% 総合効果の検定 :Z = 2.08(p = 0.04) ベンゾジアゼピン系薬の方が優れている 非ベンゾジアゼピン系薬の方が優れている 図 1. ベンゾジアゼピン系薬による鎮静と非ベンゾジアゼピン系薬による鎮静を比較した試験のうち 質が中等度 ~ 高い試験を対象とした ICU 在室期間に関するメタアナリシス CI = 信頼区間 IQR = 四分位数範囲 L/D = ロラゼパム vs. デクスメデトミジン L/P = ロラゼパム vs. プロポフォール M/P = ミダゾラム vs. プロポフォール M/D = ミダゾラム vs. デクスメデトミジン SD = 標準偏差 IV = 静脈内 Critical Care Medicine 23
26 Barr et al て評価を行ったが ICU 在室期間に関して一貫した差は認められなかった (183,197,220,222,285,286, ) しかしながら 質が中等度 ~ 高い 6 件の研究を対象にメタアナリシスを行った結果 鎮静にベンゾジアゼピン系薬が使用された患者では 非ベンゾジアゼピン系薬が使用された患者に比べて ICU 在室期間が約 0.5 日延長する可能性が示唆された (p = 0.04)( 図 1) (183,197,220,222,292, ) 人工呼吸器装着期間については 鎮静にベンゾジアゼピン系薬を使用した場合に延長することが 限られたデータから示唆されている (183,220,292,298) ベンゾジアゼピン系薬による鎮静患者と非ベンゾジアゼピン系薬による鎮静患者の間で死亡率に明確な差は認められなかった (220,222,285,295) ベンゾジアゼピン系薬による鎮静が ICU ケア費用に及ぼす影響について 6 件の研究で評価が行われている (194,222,286,294,299,300) このうち 1 件の研究においてのみ 鎮静にベンゾジアゼピン系薬 ( ミダゾラム注入 ) を用いた場合に デクスメデトミジンと比較して ICU ケア費用の増大が認められた (300) 鎮静にプロポフォールが使用された ICU 患者とミダゾラムまたはロラゼパムが使用された ICU 患者のアウトカムを比較した研究について評価を行ったところ 一部のアウトカム研究で プロポフォールの使用に伴い人工呼吸器装着期間が短縮する可能性が示されたが この影響は患者集団によって異なり (183,197,291,292, ) 必ずしも ICU 在室期間の短縮につながるわけではなかった プロポフォールによる鎮静患者とベンゾジアゼピン系薬による鎮静患者の間で自己抜管の発生率に明確な差は認められなかった (183) ある系統的レビューでは プロポフォールと他の鎮静薬の間で ICU 患者の臨床的アウトカムを比較した 16 件のランダム化比較試験の評価が行われた (291) これらの試験のうちプロポフォールとミダゾラムの比較試験のみを対象としたメタアナリシスにおいて 死亡率に差は認められず 人工呼吸器装着期間はプロポフォール投与患者でわずかに短縮したが ICU 在室期間に差は認められなかった 鎮静にプロポフォールとベンゾジアゼピン系薬のどちらを用いるかについてとせん妄の発現との関連性は明確でなく これに関係する研究としては 鎮静にプロポフォールが使用された ICU 患者とベンゾジアゼピン系薬が使用された ICU 患者の間でせん妄の発現率を比較した 2 件が公表されているのみである (285,286) 両研究とも 患者はプロポフォール ミダゾラムまたはデクスメデトミジ ンのいずれかの群にランダム化され プロポフォール群およびミダゾラム群の間でせん妄の発現率は同程度であることが示されたが エビデンスの質は低かった われわれは 鎮静にデクスメデトミジンが使用された ICU 患者とベンゾジアゼピン系薬 ( ミダゾラムまたはロラゼパム ) が使用された ICU 患者のアウトカムを比較した 5 件の研究について評価を行った (220,222,285,286,293) 人工呼吸器装着期間については この評価を行った 4 件中 3 件で群間差は認められなかった (222,285,286) しかしながら 最大規模の研究において 人工呼吸器離脱までの期間が デクスメデトミジン群 (3.7 日 ) ではミダゾラム群 (5.6 日 ) に比べて有意に短縮することが確認された (220) ベンゾジアゼピン系薬群に比べて デクスメデトミジン群での自己抜管の発生率の低下は認められなかった (222) ICU 在室期間については 5 件中 4 件で群間差は認められなかった (220,222,285,286) Maximizing Efficacy of Targeted Sedation and Reducing Neurological Dysfunction 試験のサブグループ解析を含む 5 件の研究において 鎮静にデクスメデトミジンが使用された患者とベンゾジアゼピン系薬が使用された患者の間でせん妄の発現に関する比較が行われ (220,222,285,286,298) せん妄の発現率 有病率およびせん妄が発症していない日数が報告された 質の高い研究は 1 件のみであったが (220) 5 件中 3 件において デクスメデトミジンの方が優れるという結果が確認された (286,288,300) 敗血症患者のみを対象としたサブグループ解析では デクスメデトミジンの方がロラゼパムよりも優れることが示されている (298) 1 件では ベンゾジアゼピン系薬の使用とせん妄の発現は関連しないことが認められた (222) 質が非常に低い 1 件では デクスメデトミジン群でせん妄発現率の上昇が示唆されたが この研究方法には せん妄評価が不正確などの重大な欠点があった (285) ガイドライン作業部会が投票を終えて推奨事項を作成した後に ICU での鎮静薬としてデクスメデトミジンとミダゾラムまたはプロポフォールを比較した 2 件の質の高いランダム化二重盲検比較試験の結果が公表され (301) 関連アウトカムとして人工呼吸器装着期間 ICU 在室期間および入院期間が報告された ミダゾラム群で人工呼吸器装着期間の延長が認められたが これ以外に群間差は認められなかった これらの結果は われわれが実施した既報データの解析結果と一致しており われわれが解析結果に基づいて作成したベンゾジアゼピン系薬による鎮静と非ベンゾジアゼピン 24 January 2013 Volume 41 Number 1
27 Special Article 系薬による鎮静に関する推奨事項に矛盾していない 要約すると 現在得られている文献から 鎮静にベンゾジアゼピン系薬を使用した場合と非ベンゾジアゼピン系薬を使用した場合の間で アウトカムにわずかな差があると考えられる われわれが実施した 質が中等度 ~ 高い研究のメタアナリシスによると 鎮静にベンゾジアゼピン系薬を使用した場合に ICU 在室期間が延長する 質が中等度 ~ 高いデータに基づくと 人工呼吸器装着期間の短縮という点で プロポフォールはロラゼパムより優れており (183) デクスメデトミジンはミダゾラムより優れている (220) ベンゾジアゼピン系薬の相対的なせん妄誘発作用の臨床的意義は不明であるが 質の高い 1 件の研究において ベンゾジアゼピン系薬の方がデクスメデトミジンよりもリスクが高いことが示されている (220) せん妄の予防および治療に関するその他の推奨事項は 本ガイドラインのせん妄のセクションに盛り込まれている 患者の ICU 退室が効率的に行われている医療機関では ICU の資源消費抑制の点でデクスメデトミジンの方がミダゾラムよりも有利な可能性がある (300) ICU 患者の鎮静には ベンゾジアゼピン系薬よりプロポフォールまたはデクスメデトミジンを使用した方が有利なようであるが ICU 患者における不穏の管理 特に不安 発作およびアルコール / ベンゾジアゼピン系薬の離脱症状の治療においては ベンゾジアゼピン系薬はやはり重要な薬剤である また 深い鎮静や健忘が必要な場合 あるいは他の鎮静薬の使用量を低減するために併用療法が必要な場合も ベンゾジアゼピン系薬は重要である (166,302) せん妄 ICU 患者におけるせん妄に関する疫学. せん妄は 脳機能障害が急性に発現し これに伴ってベースライン精神状態の変化や変動 注意障害 および思考の混乱または意識レベルの変化がみられる症候群である ( ) 主な特徴は 1) 意識レベルの低下 ( 周囲環境の認識における清明度の低下 ) と 注意の集中 持続または移動の能力の低下 および 2) 認知の変化 ( 記憶欠損 失見当識 言語障害 ) または知覚障害 ( 幻覚 妄想 ) の発現である (310) せん妄患者では幻覚または妄想のどちらかがみられるという誤解が多いが これらの症状はどちらもせん妄の診断の必要条件ではない せん妄患者でよくみられるその他の症状は 睡眠障害 精神運動異常および情緒障害 ( 恐怖 不安 怒り うつ 無感情 多幸症 ) である せん妄患者は 不穏 を示す場合 ( 過活動型せん妄 ) 落ち着きがあり倦怠感を示す場合 ( 低活動型せん妄 ) あるいはこれら 2 つのタイプを交互に示す場合がある 過活動型せん妄では幻覚および妄想がよくみられるが 低活動型せん妄では錯乱および鎮静がよくみられるため ICU 患者では誤診されることが多い 重症患者におけるせん妄は 今や重要な公衆衛生問題として認識されており 人工呼吸中の成人 ICU 患者の最高 80% でみられ その費用は米国単独で年間 40 ~ 160 億ドルに上る ( ) この 10 年の間に ICU 患者のせん妄に関する研究は非常に広範囲に行われるようになったが ( ) 重症患者のせん妄の基礎にある病態生理学はまだ十分に解明されていない ( ) ICU 患者アウトカムに対するせん妄の影響.ICU 患者において 急性脳機能障害の発現を特徴とするせん妄は 死亡リスクの上昇 入院期間の延長 費用の増大 認知症様状態に一致する長期認知機能障害リスクの上昇といった 有害な臨床的アウトカムに関連する独立した重要な予測因子である (313, ) ICU チームの医療習慣によって せん妄の発現率やせん妄による影響の大きさは変わってくる (220,222, ) 集中治療の専門家は せん妄のどの側面について予測 予防 検出あるいは治療が可能かを解明しようとしている ICU 患者におけるせん妄の予防 検出および治療. せん妄は 疾患誘発性の症候群である場合があるため ( 例えば 重症敗血症における臓器機能障害 ) せん妄の発現と重症度を抑制し せん妄期間を短縮するには原因に対する迅速な管理が極めて重要である 医原性因子 ( 鎮静薬およびオピオイドへの曝露など ) や環境的因子 ( 長時間の身体的拘束または不動など ) も ICU 患者のせん妄に寄与する可能性がある ICU 患者では 特定および回避可能な危険因子について評価を行うべきであり 治療介入を行う際は 個々の患者でその介入がせん妄を誘発あるいは悪化させる可能性を評価するべきである せん妄の予防戦略は 非薬物療法 ( 早期のモビライゼーションなど ) によるアプローチ 薬物療法によるアプローチ およびこれらの併用によるアプローチに分類される 妥当かつ信頼性のあるせん妄評価ツールを用いて重症患者のせん妄をモニタリングすることで 臨床医はせん妄を速やかに検出し 速やかに治療を開始することができ その結果として患者アウトカムを改善できる可能性がある せん妄が発現した患者では せん妄の重症度を低下 Critical Care Medicine 25
28 Barr et al させ せん妄期間を短縮するために さまざまな薬剤が投与されることが多い ICU 患者のせん妄の管理における抗精神病薬については 十分な統計学的検出力を備えた二重盲検ランダム化プラセボ対照試験による有効性および安全性の証明がなされていないが さまざまな国際ガイドラインによってその使用が推奨されており ( ) 集中治療専門医のほとんどが せん妄患者の治療に抗精神病薬を使用している (164) 前版のガイドラインにおいて せん妄の治療にハロペリドールを使用するという推奨事項は 症例集積研究のデータしか得られていなかったため レベル C に格付けされた このようなデータは今回の改訂版ではエビデンスの基準を満たしておらず 前版の作成以降も 成人 ICU 患者のせん妄の治療におけるハロペリドールの安全性および有効性に関して プロスペクティブ試験による検証はなされていない 同様に この患者集団における他の抗精神病薬の使用に関するデータも乏しい 最近 せん妄の治療における抗精神病薬の使用に関する Cochrane Review が公表されたが ICU 患者における抗精神病薬の使用は検討の対象外であった (340) 非 ICU 患者で得られたハロペリドールの使用に関するデータで ICU 患者集団に適用できる可能性のある頑健なデータはない ハロペリドールを含む抗精神病薬全般について ICU 患者のせん妄の治療に使用する場合の安全性および有効性を判断するには さらに研究が必要である 薬物および / またはアルコールの離脱によるせん妄. ICU 在室期間中 重症患者は 薬物またはアルコールの離脱に関連するタイプのせん妄を発現する可能性がある 通常 そのようなせん妄は過活動型である 離脱症状は 1) 患者が慢性的に使用していた違法薬物または処方薬 2) 定期的な ICU ケアの一環として投与された鎮静薬またはオピオイド あるいは 3) 慢性的なエタノール (ETOH) 摂取の急な中止によって生じる 薬物およびアルコール離脱症状の病態生理学 診断および治療に関する完全なレビューは本ガイドラインの対象外である 詳細については 他の臨床ガイドラインを参照されたい ( ) 高用量オピオイドまたは鎮静薬が長期間使用されている患者では 薬剤への生理的依存が生じる可能性があり 急な中止によって薬剤離脱症状が出現する可能性がある (344) 急性オピオイド離脱の徴候および症状は 発汗 立毛 散瞳 流涙 鼻漏 嘔吐 下痢 腹部けいれん 頻脈 高血圧 発熱 頻呼吸 あくび 不穏状態 易刺激性 筋肉痛 疼痛感受性の上昇 不 安などである 症状は オピオイドの投与中止後 12 時間以内に発現する可能性があるが オピオイド拮抗薬 ナロキソン あるいは nalbuphine などの作動性と拮抗性を併せ持つ薬剤の投与により発現時期が早まる可能性もある (345,346) ICU 患者でベンゾジアゼピン系薬の使用期間が長くなると 投与を急に中止した際に 不安 不穏 振戦 頭痛 発汗 不眠 悪心 嘔吐 ミオクローヌス 筋けいれん 過活動型せん妄や 場合によっては発作などの離脱症状が発現する可能性がある (344) ベンゾジアゼピン系薬の長期曝露後に その鎮静作用をベンゾジアゼピン受容体拮抗薬のフルマゼニルで中和すると ベンゾジアゼピン離脱症状が誘発される可能性がある (347,348) デクスメデトミジンが最長 7 日間投与された成人 ICU 患者で デクスメデトミジンの投与中止後 24 ~ 48 時間以内に離脱症状が発現しており 最も多く認められた症状は悪心 嘔吐および不穏であった (349) ICU 患者におけるデクスメデトミジンおよびミダゾラムによる鎮静の影響をプロスペクティブに比較した過去最大の研究では 投与中止後の離脱症状の発現率がミダゾラム群で 8.2% であったのに対して デクスメデトミジン群では 4.9% であった (p = 0.25)(220) 重症患者におけるオピオイドおよび鎮静薬の離脱の徴候 症状は 見過ごされたり アルコールや違法薬物の離脱といった他の原因によるものと判断されたりする可能性がある 成人 ICU 患者におけるオピオイドおよび鎮静薬の使用に伴う薬剤離脱症状の病態生理学および発現率に関して 過去 10 年間で研究はわずかしか公表されていない ほとんどの研究がレトロスペクティブ研究であり さまざまな鎮静薬および鎮痛薬が投与された患者を対象としていることから これらの患者における薬剤離脱症状の具体的な発現率や危険因子を明らかにすることは困難である (344,350) 1 件の小規模なプロスペクティブ研究において ミダゾラムまたはプロポフォールとの併用で sufentanil の注入が行われた成人 ICU 患者で 注入中止後の離脱の徴候および症状について評価が行われた (351) 鎮静期間は sufentanil / ミダゾラム群が 7.7 日 sufentanil / プロポフォール群が 3.5 日であった 離脱症状の発現率は ミダゾラム群 (35%) の方がプロポフォール群 (28%) よりも高かった ICU 患者におけるオピオイドまたは鎮静薬の離脱症状の予防または治療に関する具体的な推奨事項はないが オピオイドおよび / または鎮静薬を長期間投与した場合は 薬剤離脱症状のリスクを軽減するために 数日間かけて漸減中止するべきである 26 January 2013 Volume 41 Number 1
29 Special Article ETOH 依存は入院患者全体の 15 ~ 20% で認められる (352) 特に外科および外傷部門において ETOH 依存が認められる入院患者の 8 ~ 31% で 入院期間中に神経機能障害および自律神経障害の徴候および症状を伴うアルコール離脱症候群 (AWS) が発現する ( ) AWS の症状は 軽度のものもあれば 生命を脅かすものもある (356) AWS を発現した入院患者のうち 最高 15% の患者で全身性強直間代発作が発現し 5% の患者で中枢神経系興奮 ( 不穏 せん妄 発作 ) と hyperadrenergic 症状 ( 高血圧 頻脈 不整脈 ) が組み合わさった生命を脅かす病態の振戦せん妄 (DT) が発現する (357) 重度の AWS を発現した ICU 患者では せん妄が持続するために 人工呼吸器装着期間が延長し ICU 在室期間が延長する可能性がある ( ) ICU 患者では 過去の ETOH 依存が過小評価されることが多いため AWS または DT のリスクがある患者を検出するのが困難である AWS や DT のスクリーニングツールは まだ集中治療現場での十分な検証がなされていない アルコール離脱によるせん妄をその他の原因によるせん妄と判別するのは難しいかもしれない ICU 患者の AWS 症状に対しては 具体的に不穏 精神病および自律神経活動亢進を標的とした薬剤を必要に応じて投与するという症状に基づく治療を行うことで AWS の重症度が低下し AWS 期間が短縮し 薬剤の必要量が減少する (358) ベンゾジアゼピン系薬がアルコール離脱症状に対する治療の中心とされているが その有効性および安全性については明確ではない (320) これまでのところ 重度 AWS 症状の治療におけるデクスメデトミジンとベンゾジアゼピン系薬の安全性および有効性を比較した研究は公表されていない ICU 患者における AWS によるせん妄の診断および管理は 依然として難しい課題である 集中治療現場におけるアルコール離脱症状評価ツールの使用 アルコール離脱症状の予防 および治療の妥当性に関する議論については 本ガイドラインの対象外である せん妄 : クエスチョン ステートメント 推奨事項 1.ICU 患者におけるせん妄に伴うアウトカムクエスチョン : 成人 ICU 患者におけるせん妄に伴うアウトカムは?( 記述的なクエスチョン ) 回答 : 成人 ICU 患者では せん妄は死亡率の増加 (A) ICU 在室期間および入院期間の延長 (A) ICU 退室後の認知機能障害の発生 (B) に関連する 根拠 : 多数のプロスペクティブコホート研究により せん妄を発現した患者は ICU 在室期間中およ び ICU 退室後とも 有害アウトカムを伴うリスクが高いことが示されている このリスクは 既存の併存疾患 疾患重症度 年齢および単に関連しているだけと考えられる他の共変量とは独立している 11 件のプロスペクティブコホート研究において ICU 在室期間中のせん妄の発現状況と 次のさまざまな時点における死亡率との関係が検討された :ICU 退室時 (5 件 ) 病院退院時(4 件 ) 30 日後 (1 件 ) 3 ヵ月後 (1 件 ) 6 ヵ月後 (3 件 ) および 12 ヵ月後 (1 件 )(318,319,321,322, ) せん妄の発現状況は すべての研究で ICU 在室期間中に 1 日以上持続したか否かによって分類され 3 件の研究では せん妄の期間と死亡率の関係についても検討が行われた (320,321,366) 15 件のうち エビデンスの質の高い 3 件を含む 11 件の研究で せん妄は死亡に関連する独立した予測因子であることが示された (320,321,366) せん妄の期間 ( 昏睡について調整 一部の研究では精神賦活薬への曝露についても調整 ) は 6 ヵ月後および 12 ヵ月後の死亡率と有意に関連した 2 件のコホート研究では せん妄期間が 1 日延長する毎に死亡リスクが一貫して 10% 上昇することが示された ( 共変量について調整し せん妄を時間依存共変量として処理した解析 ) (320,321) 9 件のプロスペクティブコホート研究において ICU における 1 日以上のせん妄と ICU 在室期間および / または入院期間 ならびに人工呼吸器装着期間との関係が検討された (318,319,322, 323,360,361,363,364,367) せん妄は 人工呼吸器装着期間 (360,363,364,367) および ICU 在室期間 (318,319,364,367) に関連する独立した予測因子であることが それぞれ 4 件の研究で示された これらのエンドポイントは immortal time バイアス すなわち 治療への曝露あるいは独立変数の状態 ( この場合 せん妄の有無 ) が実際のエンドポイント発生までの期間 ( この場合 人工呼吸器装着期間または ICU 在室期間 ) に日によって変化しうる場合に生じるバイアスの影響を受けるリスクが特に高い (368) したがって 入院期間に関しても 9 件の研究のうち immortal time バイアスの影響を調整した質の高い 3 件 (318,322,368) を含む 7 件 (318,319,322,323,361,364,367) の研究において せん妄に予測因子としての強い関連性が認められたことは重要である 2 件のプロスペクティブコホート研究において ICU 在室期間中のせん妄とその後 Critical Care Medicine 27
30 Barr et al 表 8. せん妄モニタリングツールの計量心理学的スコア せん妄モニタリングツール スコア化を行った計量心理学的特性項目 Confusion Assessment Method for the ICU Intensive Care Delirium Screening Checklist Cognitive Test for Delirium Nursing Delirium Screening Scale Delirium Detection Score 項目選択に関する記述 内容的妥当性の検証 欠点の提示 評価者間信頼性 研究者チーム以外の者による評価者間信頼性の検証 評価者間信頼性が低いか一貫性がない場合の評価者内信頼性の検証 NA NA NA NA 0 検証における被験者総数 基準関連妥当性の検証 : 感度 基準関連妥当性の検証 : 特異度 予測妥当性の検証 実施可能性 使用法の記述 臨床現場におけるスケールの使用意義 総スコア ( 範囲 :0 ~ 19 または 21) 18/19 14/19 14/19 11/19 9/21 重み付けスコア a ( 範囲 :0 ~ 20) 計量心理学的エビデンスの質 ( 重み付けスコアに基づく ) VG VG M M VL VG = 極めて良好 M = 中等度 L = 低い VL = 極めて低い N/A = 該当なし a 重み付けスコア ( 範囲 :0 ~ 20):15 ~ 20 の場合は計量心理学的特性が極めて良好 (VG) 12 ~ 14.9 の場合は良好 (M) 10 ~ 11.9 の場合は許容可能であるが 追加検証試験を要する (L) 10 未満の場合は計量心理学的特性に関する十分なデータが報告されていない / 計量心理学的特性は許容不能 (VL) の認知機能障害の関係が検討された 質が中等度の 1 件では ICU 在室期間中に 1 日以上のせん妄が認められた場合に 退院時における認知機能障害の発現率が高くなるという関連性が報告された (322) 質が中等度の最近のプロスペクティブコホート研究では ICU におけるせん妄期間の延長に伴い 3 ヵ月後および 12 ヵ月後における認知機能障害の発現率に有意な上昇が認められた (324) 2. せん妄の検出およびモニタリング a. クエスチョン :ICU 患者では 客観的ベッドサイドせん妄評価ツールを用いて定期的にせん妄のモニタリングを行うべきか?( 実行可能なクエスチョン ) 回答 : 成人 ICU 患者に対して 定期的にせん妄のモニタリングを行うことを推奨する (+ 1B) 根拠 : 人工呼吸中の ICU 患者 (14,220,222,308, 360,369,370) および人工呼吸器を装着していない ICU 患者 (309,359, ) のどちらにおいても せん妄の発現は一般的である ICU 患者のせん妄は過活動型よりも低活動型であることが多いため ICU の医療従事者はしばしば患者のせん妄の存在を過小評価する (372,380) せん妄は ICU の挿管患者および非挿管患者のどちらでも妥当かつ信頼性のあるツールを用いて検出することができる ほとんどの研究において 介護者が妥当かつ信頼性のあるせん妄評価ツールを用いた結果 せん妄の検出率が改善し (367) これによって恐怖や失見当識の認められる患者を安心させることができた (381) せん妄のモニタリングを行う根拠は以下のとおりである :1) 情報が与えられた中等度 ~ 高リスク患者のほとんどが せん妄のモニタリングを受けることを 28 January 2013 Volume 41 Number 1
31 Special Article 希望している 2) せん妄と重大なアウトカムとの関連性に関する質の高いコホートデータから モニタリングを行わない場合はせん妄が 見過ごされる率 が高いことが示されている 3) 本ガイドラインで推奨されている評価ツールを用いた ICU せん妄モニタリングプログラムがすでに問題なく導入されており 大規模に実践されている 4) ほとんどの ICU で 方針決定者はせん妄評価を質の高い日常的なケアの一環として採用することができる (254,372,374,382,383) われわれは 中等度のエビデンスに基づき せん妄のリスクが中等度 ~ 高い ICU 患者 ( ベースライン時にアルコール依存症 認知機能障害または高血圧の既往歴を有する患者 重症敗血症またはショック患者 人工呼吸中の患者 非経口鎮静薬およびオピオイドが投与されている患者など ) では 看護のシフト毎に 1 回以上の頻度で 妥当かつ信頼性のあるせん妄評価ツールを用いてせん妄の発現状況を定期的にモニタリングすることを強く推奨する b. クエスチョン : 内科および外科の人工呼吸中の ICU 患者および人工呼吸器を装着していない ICU 患者において 妥当性および信頼性について最も強力なエビデンスが得られているせん妄モニタリング用の評価ツールは?( 記述的なクエスチョン ) 回答 :Confusion Assessment Method for the ICU (CAM-ICU) および Intensive Care Delirium Screening Checklist(ICDSC) は 成人 ICU 患者にせん妄のモニタリングを行う上で最も妥当かつ信頼性のあるツールである (A) 根拠 :Cognitive Test for Delirium(CTD) CAM-ICU Delirium Detection Score(DDS) ICDSC Nursing Delirium Screening Scale(Nu- DESC) の 5 種類のせん妄モニタリングツールについて ICU 患者で使用する場合の特性を評価した これらの計量心理学的特性を表 8に示す CAM-ICU(308,359, , ) および ICDSC(309,371) は いずれも計量心理学的特性 ( 妥当性および信頼性 ) が極めて良好であり 明確に ICU 患者 ( 人工呼吸中の患者および人工呼吸器を装着していない患者の両方 ) 用にデザインされたものである これらのツールは 20 を超える言語に翻訳されており 現在 世界各地で使用されている (315) CAM-ICU および ICDSC は ICU 看護師および集中治療専門医を評 価者とした検証において 高い評価者間信頼性を示している (308,309,373) また American Psychiatric Association のせん妄基準を対照とした検証では いずれも高い感度および特異度を示した (319,359,379) CAM-ICU または ICDSC により検出されるせん妄の予測因子としての妥当性検証では ICU 在室期間および入院期間の延長 (318,319,322,323,360,361,363,364,367) 死亡リスクの上昇 (318,319,321,322, ) などの臨床的アウトカムとの関連性が認められた われわれが実施した文献レビューに基づくと CAM-ICU および ICDSC は ICU 患者においてせん妄を検出する上で いずれも妥当かつ信頼性および実施可能性のあるツールである (254,309) CTD( ) および Nu-DESC (379) については われわれの解析において 重み付け計量心理学的スコア 12 以上という基準には達していたが 研究者チーム以外の者による評価者間信頼性 臨床的実施可能性などのいくつかの計量心理学的特性に関して検証が行われていなかった DDS(347) については 重症患者におけるせん妄モニタリングツールとして 総合的な妥当性 信頼性および実施可能性を適切に評価するには さらなる計量心理学的検証が必要である われわれが 2010 年にせん妄モニタリングツールに関する文献のレビューおよび解析を終了した後に せん妄評価ツールを臨床現場で使用した際の感度 特異度および信頼性を解析した研究が数件公表された ( ) 5 種類の ICU せん妄スクリーニングツールに関するメタアナリシスによると われわれの勧告に矛盾することなく CAM-ICU および ICDSC はせん妄の検出における感度および特異度が最も高いツールであった (392) CAM-ICU と ICDSC の比較研究を対象とした別のメタアナリシスにおいても これらのツールはともに感度および特異度が高いことが示された (393) 臨床現場における多様な各 ICU 患者集団でのせん妄モニタリングツールの性能を評価するには さらに研究が必要である (391,394) c. クエスチョン : 臨床現場において 定期的なせん妄のモニタリングの導入は可能か?( 記述的なクエスチョン ) 回答 : 臨床現場において 成人 ICU 患者に対し Critical Care Medicine 29
32 Barr et al 定期的なせん妄のモニタリングは実行可能である (B) 根拠 : 中等度のエビデンスから 臨床現場において せん妄の定期的なモニタリングは実行可能であることが示されている さまざまな医療機関において計 2,000 例を超える患者を対象とした多数の導入研究が行われており これらの研究におけるせん妄モニタリングの遵守率は 90% を超えていた 推奨されるせん妄モニタリングツールのいくつかを用いたモニタリングにおいて 臨床現場の ICU 看護師および医師と基準となる熟練評価者との間で高い評価者間信頼性が示された (254,372,374,382,383) このように ICU におけるせん妄モニタリングの導入が可能であることは研究によって示されているが 医師に積極的な取り組みの姿勢がないことは大きな障壁となる (395) この問題を克服するには 人的な要因や ICU の医療習慣を変えることに焦点を当てた戦略が必要である (316) 最近 ( このクエスチョンに関するエビデンスの格付け終了後 ) せん妄モニタリングの導入に関する研究がさらに 1 件公表され 500 例を超える ICU 患者 ( 内科 外科および心臓部門 ) および 600 名を超える ICU 看護師が参加した 3 年にわたるこの研究からも 臨床現場におけるせん妄の定期的なモニタリングは実行可能であるという結論が支持された (394) 3. せん妄の危険因子 a. クエスチョン :ICU でのせん妄の発現に相関しているベースライン危険因子は?( 記述的なクエスチョン ) 回答 : 以下の 4 つのベースライン危険因子は ICU でのせん妄の発現に対して有意かつ正の相関を示す : 既存の認知症 高血圧および / またはアルコール依存症の既往歴 入院時点で重症度の高い疾患 (B) 根拠 : 以下のベースライン危険因子について 2 件以上の多変量解析で有意性が示されている : 既存の認知症 (329,375,396) ベースライン時における高血圧の既往歴 (318,397) アルコール依存症 (1 日当たり 2 ~ 3 単位以上の摂取 )(318,396) 入院時点で重症度の高い疾患 (318,328,329,398) 年齢については 非 ICU 患者でせん妄に関連する最も有意な危険因子の 1 つであることが確認されているが ICU 患者 の場合 有意性が認められた研究は 2 件のみで (328,398) 4 件の研究では有意性が認められなかった (318,375,396,399) ICU 患者における年齢とせん妄の発現との関連性を明確にするには さらに研究が必要である b. クエスチョン : 昏睡は ICU におけるせん妄の発現に関連する危険因子か?( 記述的なクエスチョン ) 回答 :ICU 患者において 昏睡はせん妄の発現に関連する独立した危険因子である ICU 患者における昏睡の各タイプ ( 薬剤誘発性昏睡 器質的昏睡 神経学的昏睡 内科的な昏睡 ) とせん妄との関連性を明らかにするには さらに研究が必要である (B) 根拠 : 数件の報告から 昏睡は ICU 患者におけるせん妄に関連する独立した危険因子であることが示されている (318,399) このうち 1 件では 内科的な昏睡 ( 原発性神経学的疾患による昏睡 ) 鎮静薬誘発性昏睡および多因子性昏睡 ( 内科的疾患および鎮静薬の両方に起因する昏睡 ) の 3 つのカテゴリーに昏睡の分類が行われた (318) この研究において 鎮静薬誘発性昏睡および多因子性昏睡はせん妄の発現に対して有意な関連を示したが 内科的な昏睡は関連を示さなかった (318) c. クエスチョン : 成人 ICU 患者におけるせん妄の発現に関連している ICU 治療関連 ( 後天的 ) 危険因子 ( オピオイド ベンゾジアゼピン系薬 プロポフォール デクスメデトミジン ) は?( 記述的なクエスチョン ) 回答 : 成人 ICU 患者におけるオピオイドの使用とせん妄の発現の関連性については データが一貫していない (B) 成人 ICU 患者において ベンゾジアゼピン系薬の使用はせん妄の発現に関連する危険因子である可能性がある (B) 成人 ICU 患者におけるプロポフォールの使用とせん妄の発現の関連性については データが不十分であり 評価できない (C) せん妄の発現リスクがある人工呼吸中の成人 ICU 患者に鎮静薬を使用する場合は ベンゾジアゼピン系薬よりもデクスメデトミジンを使用した方がせん妄の発現率が低い可能性がある (B) 根拠 : オピオイドに関する研究は 研究によってデザインが大きく異なっていた 使用された個々の薬剤について検討しているもの (288,328,397,398) もあれば 1 つの薬剤ク 30 January 2013 Volume 41 Number 1
33 Special Article ラスとしてしか検討していないもの (363) もあり さらに 一部の研究は オピオイドと鎮静薬または他の鎮痛薬を併合して検討していた (318,329,396) また 研究結果にも大きな違いが認められた ほとんどの研究では オピオイドの使用に伴いせん妄のリスクが上昇したか オピオイドとせん妄との関連がなかったことが報告され (288,318,328,329,363, ) 1 件の研究 (400) では 熱傷患者において オピオイドの使用に伴いせん妄のリスクが低下したことが示されている ICU 患者におけるプロポフォールの使用とせん妄のリスクの関係について具体的に検討した質の高い研究は 1 件のみであり この研究において 有意な関連は認められなかった (328) ベンゾジアゼピン系薬については せん妄の危険因子に関する数件の研究において検討が行われている オピオイドの研究と同じく 研究によってデザインに大きな違いがあった 質が中等度の一部の研究では ベンゾジアゼピン系薬の使用とせん妄の発現の間に強い関連が認められたが (288,328) 他の研究では有意な関連が認められなかった (318,363, ) ベンゾジアゼピン系薬による鎮静とデクスメデトミジンによる鎮静を比較した 2 件のランダム化比較試験では デクスメデトミジン群の患者でせん妄の発現率が低い ( 約 20%) ことが確認された (220,298) これらのデータは ベンゾジアゼピン系薬の誘発的な作用やデクスメデトミジンの予防的な作用を示すものではないが ベンゾジアゼピン系薬は ICU におけるせん妄の発現に関する危険因子である可能性が考えられる デクスメデトミジンが ICU 患者におけるせん妄発現リスクを低減するか否かについては 現在研究中である 4. せん妄の予防 a. クエスチョン :ICU において せん妄の発現抑制または期間短縮のために 非薬物療法によるせん妄プロトコルを使用するべきか?( 実行可能なクエスチョン ) 回答 : 成人 ICU 患者では せん妄の発現抑制と期間短縮のために 可能な限り早期モビライゼーションを促すことを推奨する (+ 1B) 根拠 : 重症患者の早期のモビライゼーションは 当初 機能的アウトカムを改善させることを目的とした非薬物療法として検討された しかし ながら 早期のモビライゼーションに関する最初の多施設共同ランダム化比較試験 (326) とその後の導入研究 (401) では せん妄発現率の低下 鎮静深度の抑制 入院期間の短縮 ICU 在室期間の短縮および人工呼吸器非依存日数の増加といった点でも著明な効果が認められた これらの研究から 早期の積極的なモビライゼーションが ICU 患者に悪影響を及ぼす可能性は低いと考えられ 逆に せん妄発現率の低下 せん妄期間の短縮 ICU 在室期間の短縮 入院期間の短縮 および入院費用の削減が実現される可能性があると考えられる さまざまな目標を定めた質の高い非薬物療法プロトコルについて 非 ICU 入院患者で好ましい結果が得られているが (402) そのような多角的介入は ICU での十分な検討がなされていない b. クエスチョン :ICU において せん妄の発現抑制または期間短縮のために 薬物療法によるせん妄予防プロトコルを使用するべきか?( 実行可能なクエスチョン ) 回答 : 成人 ICU 患者における薬物療法によるせん妄予防プロトコルの使用は これらの患者でこのプロトコルによるせん妄の発現率の低下または期間短縮を示す有力なデータがないため 推奨しない (0 C) 根拠 : プロスペクティブ非盲検ランダム化比較試験において 消化管手術後の入院患者を対象として 睡眠覚醒サイクルを維持するための夜間薬物療法レジメンの評価が行われたが このレジメンの集中治療現場における有用性や適用可能性については疑問の余地がある (403) 最近 プロスペクティブプラセボ対照盲検ランダム化試験が公表され 高齢の外科 ICU 患者に対するせん妄予防のための低用量ハロペリドールの予防的投与は有益であることが示された (404) しかしながら これらの患者はそれほど重症ではなく 人工呼吸管理もほとんどの患者で行われていなかった ICU 患者における薬物療法によるせん妄予防プロトコルの使用の安全性および有効性を検討するには さらに研究が必要である c. クエスチョン :ICU において せん妄の発現抑制または期間短縮のために 非薬物療法と薬物療法の併用によるせん妄予防プロトコルを使用するべきか?( 実行可能なクエスチョン ) Critical Care Medicine 31
34 Barr et al 回答 : 成人 ICU 患者における非薬物療法と薬物療法の併用によるせん妄予防プロトコルの使用は これらの患者でこのプロトコルによるせん妄の発現率の低下を示すものはないため 推奨しない (0 C) 根拠 : 介入前後比較研究において ICU 患者の PAD 管理を目的とした集学的プロトコルの効果が評価された このプロトコルに従って管理された患者では せん妄発現率に低下は認められなかったが 亜症候群性せん妄の発現率が低下し 疼痛コントロールが改善し 総 ICU 費用が 15% 削減された (327,405) ICU 患者における亜症候群性せん妄とは ICDSC のスコアが 4 未満の状態であり 亜症候群性せん妄が認められる患者では せん妄が認められない患者に比べて臨床的アウトカムが不良である (319) ICU 患者において 非薬物療法と薬物療法の併用による予防プロトコルが完全なせん妄状態の発現率を低下させるか あるいはせん妄の期間を短縮させるか否かについては さらに研究が必要である d. クエスチョン :ICU 患者において せん妄予防のためにハロペリドールまたは非定型抗精神病薬の予防的投与を行うべきか?( 実行可能なクエスチョン ) 回答 : 成人 ICU 患者において せん妄予防の目的でのハロペリドールまたは非定型抗精神病薬投与は提案しない (- 2C) 根拠 :ICU の一般患者集団に対する抗精神病薬の予防的投与に関して 十分な患者数で有益性を示した あるいは十分な規模の有益性を示した質の高い研究はない 最近公表された質が中等度の研究において ICU に入室した重症度の低い高齢術後患者において 予防的な低用量ハロペリドールの静脈内投与はせん妄の発現率を低下させる可能性があることが示された (404) このデータを重症度の高い多様な ICU 患者集団に適用できるかどうかは不明である デザインは適切であるが統計学的検出力が十分でない多施設共同ランダム化試験において プラセボを対照としてハロペリドールまたは ziprasidone によるせん妄予防の評価が行われたが どちらの薬剤についてもプラセボとの比較で有益性が認められなかった (370) 質が中等度の研究では 心臓血管外科術後の患者において 手術直 後にリスペリドンの単回舌下投与を行うと せん妄の発現率が低下することが示された (406) ICU 患者におけるせん妄予防を目的とした定型および非定型抗精神病薬の安全性および有効性を明確にするには さらに研究が必要である e. クエスチョン :ICU 患者において せん妄予防のためにデクスメデトミジンの予防的投与を行うべきか?( 実行可能なクエスチョン ) 回答 : 成人 ICU 患者において せん妄予防を目的としたデクスメデトミジンの使用は これらの患者での有効性を示すエビデンスがないため 推奨しない (0 C) 根拠 : 循環器 ICU の研究 (306 例 ) において ICU 患者におけるデクスメデトミジンとせん妄予防に関する検討が行われた (407) デクスメデトミジン群では せん妄期間が 2 日であり モルヒネ群の 5 日に対して差が認められたが ( p = 0.03) せん妄の発現率に有意な低下は認められなかった ( それぞれ 9% および 15% p = 0.09) せん妄予防を目的としたデクスメデトミジンの使用については 明確なベネフィットがない上での投与のリスクを考慮して さらなるデータが得られるまで推奨しない 5. せん妄の治療 a. クエスチョン : 成人 ICU 患者において ハロペリドールはせん妄の期間を短縮するか?( 記述的なクエスチョン ) 回答 : 成人 ICU 患者において ハロペリドールがせん妄の期間を短縮するという公表されたエビデンスはない ( エビデンスなし ) b. クエスチョン : 成人 ICU 患者において 非定型抗精神病薬はせん妄の期間を短縮するか?( 記述的なクエスチョン ) 回答 : 成人 ICU 患者において 非定型抗精神病薬はせん妄の期間を短縮するかもしれない (C) 根拠 : 小規模なプロスペクティブランダム化二重盲検プラセボ対照試験 (36 例 ) において せん妄を発現した ICU 患者にクエチアピンを投与した結果 せん妄期間の短縮が認められた (408) この試験では ハロペリドールを投与されているせん妄患者が 12 時間毎にクエチアピン 50 mg またはプラセボを追加投与されるどちらかの群にランダム化された 過去 24 時間以内にハロペリドールが 1 回以上投与されている場合は クエチアピンの用量が 50 mg 増量され 32 January 2013 Volume 41 Number 1
35 Special Article た すべての患者で 必要に応じてハロペリドール 1 ~ 10 mg の 2 時間毎の静脈内投与が可能であったが ハロペリドールの使用に関して群間で有意差はなかった ハロペリドールの単独使用に関する比較データは得られていない 抗精神病薬が重症患者のせん妄の治療において有益であるという仮説について 十分な統計学的検出力を備えた綿密なデザインの多施設共同プラセボ対照試験で検証を行う必要がある c. クエスチョン :ICU 患者におけるせん妄期間を短縮する目的で コリンエステラーゼ阻害薬 ( リバスチグミン ) を使用するべきか?( 実行可能なクエスチョン ) 回答 :ICU 患者において せん妄期間の短縮の目的ではリバスチグミン投与を推奨しない (- 1B) 根拠 : コリンエステラーゼ阻害薬であるリバスチグミンは 高齢認知症患者のせん妄の治療において有益な可能性がある しかしながら 重症患者を対象としたリバスチグミンのプラセボ対照試験は 無益性と有害である可能性により中止された (409) この多施設共同試験は 104 例が組み入れられた段階で リバスチグミン群でせん妄の重症度の上昇およびせん妄期間の延長ならびに死亡率の上昇傾向が認められたことから中止となった 別の研究 ( この推奨事項に関するエビデンスの解析終了後に公表された ) では 待機的心臓手術施行患者 ( 患者数 120 例 > 65 歳 ) において せん妄予防として周術期にリバスチグミンが投与されたが 術後のせん妄発現率に影響は認められなかった (410) d. クエスチョン : トルサード ド ポアンツ (torsades de pointes) のリスクが高い患者では ハロペリドールおよび非定型抗精神病薬の使用を避けるべきか?( 実行可能なクエスチョン ) 回答 :Torsades de pointes の著明なリスクがある患者 ( ベースライン時に QT 間隔延長が認められる患者 QT 間隔延長を起こすことが知られている薬剤を投与中の患者 これら不整脈の既往歴がある患者など ) に対して 抗精神病薬を使用することを提案しない (- 2C) 根拠 :Torsades de pointes は 抗精神病薬の投与に伴う危険な合併症である 初期の症例報告は ハロペリドールの静脈内投与に伴うこの不整脈の発生 (411,412) や QT 間隔延長との 関連性 (413,414) を警告するものであった ただし QT 間隔延長を伴わない torsades de pointes も報告されている (415,416) Torsades de pointes は ziprasidone(417) リスペリドン (418) などの非定型抗精神病薬が投与された患者でも報告されており 最近の報告では このリスクを上昇させる可能性のある薬物相互作用も指摘されている (419) エビデンスの質は低いが この合併症に伴う新たな病態や死亡のリスクは高い e. クエスチョン : 人工呼吸中の成人 ICU 患者において せん妄に対して鎮静薬の静脈内持続投与を行う必要がある場合 せん妄の期間を短縮するにはベンゾジアゼピン系薬よりもデクスメデトミジンを優先的に使用するべきか?( 実行可能なクエスチョン ) 回答 : アルコールまたはベンゾジアゼピン系薬の離脱症状とは無関係のせん妄を呈する成人 ICU 患者において せん妄の期間を短縮するために鎮静薬を使用する場合は ベンゾジアゼピン系薬の投与よりもデクスメデトミジンの静脈内持続投与を行うことを提案する (+ 2B) 根拠 : ベンゾジアゼピン系薬による鎮静とデクスメデトミジンによる鎮静を比較した 2 件のランダム化比較試験において せん妄が認められる患者の割合に関して デクスメデトミジン群で 1 日当たり約 20% の有意な低下が認められた (220,370,420) ベンゾジアゼピン系薬がせん妄のリスクを上昇させたのか あるいはデクスメデトミジンがせん妄のリスクを低下させたのかについては これらのデータから結論を導くことができなかった この問題についてはさらに研究が必要である しかしながら これら 2 件の臨床試験 ( せん妄の発現リスクがある患者が高率に含まれる ) のデータと 観察研究で得られたせん妄の危険因子に関するデータを総合して考えると ベンゾジアゼピン系薬は ICU におけるせん妄の発現に関連する危険因子である可能性がある われわれはこれらの知見に基づき ベンゾジアゼピン系薬またはエタノールの離脱症状とは無関係のせん妄を呈する ICU 患者で鎮静薬を使用する場合は ベンゾジアゼピン系薬よりもデクスメデトミジンの使用を支持する推奨事項を作成した ICU 患者におけるせん妄期間の短縮のためにプロポフォールなどの他 Critical Care Medicine 33
36 Barr et al の非ベンゾジアゼピン系鎮静薬を使用することについては リスクとベネフィットに関する十分なデータがないため 推奨事項を作成できない ICU アウトカムを改善させるための PAD の管理 ICU 患者ケアを最適化するための総合的 PAD 管理プロトコルの使用. われわれが重症患者の PAD を効率的に管理することができれば 費用が削減され ICU アウトカムが改善され ICU ケアへの患者の参加を促すための管理戦略を打ち立てることができる (9-13,16-20) しかしながら 集中治療現場の医療従事者にとって これらのガイドライン推奨事項を実践することは非常に難しい課題である これを成功させる方法の 1 つは エビデンスに基づく各施設独自の総合的 PAD 管理プロトコルを作成し これを導入して 学際的チームアプローチにより PAD の評価 治療および予防を実践することである プロトコルを定めることで エビデンスに基づく 最良の医療習慣 を臨床現場まで普及させ 医療習慣のバラツキをなくし 治療の遅延を回避できるようになる (2,3) さらに プロトコルを用いたアプローチは 患者アウトカムの改善にも大きく寄与し 品質保証作業の指針としても役に立つ (13,327,421,422) これらの利点が認識されているにもかかわらず 総合的 PAD 管理プロトコルの導入の普及は遅れている 米国の ICU のうち PAD 管理プロトコルを導入している ICU はわずか 60% であり 導入している場合もプロトコルの遵守率が低く この状況は患者アウトカムに負の影響を与えている (163,199) 20 年以上前から系統的な疼痛の評価と管理の重要性が強調されてきたにもかかわらず 調査研究からは以下の実態が明らかにされている :1)ICU 患者で疼痛を伴う処置を行う際に 先行して鎮痛薬投与が行われているのはわずか 20% である 2) 疼痛および苦痛は依然として患者のストレスの主要原因である 3) 少なくとも 40% の ICU 患者がなお中等度 ~ 重度の疼痛を報告している (2,60,73,423) 長い間 薬剤誘発性昏睡は 多くの ICU 患者で 人道的観点からの 治療目標とされてきた しかしながら この戦略は死亡リスクを上昇させ 人工呼吸器装着期間および ICU 在室期間を延長させるものであり 長期の神経心理学的機能障害や身体機能の低下を招く可能性がある (75,238,287,318, ) 鎮静薬使用量の削減および最小限の鎮静を促す ICU 鎮静戦略の有益性が公表されているが そのような鎮静 戦略の導入は進んでいない 疼痛および鎮静の定期的な評価 疼痛の管理および最小限の鎮静のための戦略 ( すなわち 毎日鎮静中断あるいはその他の方法による目標鎮静レベルを浅く設定した戦略 ) ならびにせん妄のモニタリングおよび予防の戦略を統合した ICU プロトコルを導入することが 過剰鎮静による合併症を回避する上での最良の戦略であると思われる このようなプロトコルは 臨床看護師と ICU チームの他のメンバーとのコミュニケーションにも役立ち これによって 個々の患者で疼痛および鎮静管理の適切な目標を定め 治療戦略の有効性を評価することが可能になる (3,14,62,259,427,428) 定期的なせん妄のモニタリングによる ICU アウトカムへの影響については厳格な評価が行われていないが せん妄の早期検出によって 患者を安心させることや 原因となっている是正可能な因子を特定し 有効なせん妄治療を行うことが可能になると思われる さらに せん妄の早期検出および早期治療が実現されれば 患者の意識が維持され 場合によっては人工呼吸器離脱トライアルや早期のモビライゼーションの試みの際に患者の協力が得られる可能性もある しかしながら 臨床医との十分な関わりやコミュニケーションが可能な患者でなければ せん妄の評価は困難である 患者をそのような状態に維持するには 最適な疼痛管理と浅い鎮静が極めて重要である 鎮静深度の定義. 重症患者の鎮静レベルを最小限に維持することは明らかに有益であるが 浅い 鎮静と 深い 鎮静の定義に関する明確な合意はない ICU 患者における PAD 管理では 不十分または過剰な治療に伴う短期および長期合併症を回避しながら 一貫して患者の安全および快適さに焦点を当てることを最重要目標とするべきである 従来 ICU における鎮痛および鎮静の目標は 人工呼吸換気を促すこと 患者および介護者の損傷を予防すること ならびに疼痛 不安 不穏およびせん妄に対する不十分な治療による心理的影響および生理的影響を避けることとされてきた 一方で 筋萎縮 筋力低下 肺炎 人工呼吸器依存 血栓塞栓性疾患 神経圧迫 褥瘡 せん妄などの過剰鎮静による合併症を避けることも重要である (11,325,326,429) 浅い鎮静と深い鎮静の厳密な定義があれば 昏睡を誘発することなく患者の快適さをもたらすための鎮静プロトコルを作成し 導入することができる 本ガイドラインの中核をなす原則は次のとおりである :1) 妥当かつ信頼性のある評価ツールを用いて 疼痛 鎮静深度およびせん妄を頻繁にモニタリングする 34 January 2013 Volume 41 Number 1
37 Special Article 2) 疼痛に対して先行的に十分な治療を行う 3) 鎮静薬の投与は必要な場合に限り行う 4) 鎮静薬の用量調節を行い 患者の反応性および意識を 意識的に指示に従うことができるレベル ( 指示に従って 以下の動作のうち 3 つを行えるレベル : 眼を開ける 視線を合わせる 手を握る 舌を出す つま先を動かす ) に維持する (15,16,326) このレベルの反応性および意識は 単に 眠いが覚醒可能 という状態を超えるものであり 患者の自己申告に基づいて疼痛を評価する場合や 人工呼吸器離脱および抜管が可能か否かを評価する場合 せん妄の評価を行う場合 あるいは早期のモビライゼーションの試みを開始する場合には このレベルが必要である 患者が確実に覚醒し 協力的で落ち着いた状態に維持されることを目標に鎮静薬の用量調節を行った方がよいか あるいは毎日の覚醒トライアルを行いながらこれよりも深い鎮静レベルを維持した方がよいかについては まだ明らかではない (16,430) 最終的な解析では どちらの戦略も深い鎮静の発生およびそれに伴うリスクを抑制することが示されている (431) アウトカム : クエスチョン ステートメント 推奨事項 1. 臨床的アウトカムを改善させるための鎮静戦略 a. クエスチョン : 人工呼吸中の成人 ICU 患者では 鎮静を毎日中断するか 目標鎮静レベルを浅く設定するというどちらかのプロトコルに従うべきか?( 実行可能なクエスチョン ) 回答 : 人工呼吸中の成人 ICU 患者に対して 鎮静を毎日中断するか 目標鎮静レベルを浅く設定するかのどちらを日常的に行うことを推奨する (+ 1B) 根拠 : 計 699 例を対象とした 5 件の非盲検ランダム化比較試験において 毎日の鎮静中断に関する評価が行われた (14-16,432,433) 1 件 (432) を除き 対象はいずれも内科 ICU 患者に限定されていた パイロット試験 1 件では 対照群で目標鎮静レベルを浅く設定した戦略が使用された (16) 質の低い 1 件の試験で有害性を示唆する結果が得られたが この試験には試験方法に関する重大な問題があった (433) これらの試験のデータから 毎日の鎮静中断の実施により 人工呼吸器装着期間が短縮し ( あるいは生存者の人工呼吸器非依存日数が増加し ) ICU 在室期間が短縮することが示唆されている もう 1 つの戦略 すなわち 浅い鎮静レベルを維持するプロトコル ( 毎日の鎮静中断を行 わない ) の使用については 計 3,730 例を対象とした 11 件の非盲検試験で評価が行われている これらの試験のデータから この戦略によって人工呼吸器装着期間が短縮する ( あるいは生存者の人工呼吸器非依存日数が増加する ) ことが示唆されている (7-13,18,19,434) プロトコルの使用による ICU 在室期間への影響については データに一貫性がなく 有害な影響を示唆するデータはほとんどなかった (7-13,17-19,327,434) 2 件の試験で相反するデータが得られたのは 対照群の鎮静戦略が介入群の戦略に類似していたためである可能性が高かった (18,19) 患者に対する看護師の比が 1:1 のベッドサイドケアモデルに基づく医療制度や最小限の鎮静を目標としている医療施設では有益性がないかもしれない (435) 毎日の鎮静中断の実施または浅い鎮静レベルを維持するプロトコルの使用による 人工呼吸器関連肺炎 (VAP) せん妄発現率 患者の快適さおよび ICU ケア費用に対する影響については 十分なデータがないため 明確な結論を導くことができない 要約すると 毎日の鎮静中断の実施によって 内科 ICU 患者では臨床的有益性が得られるが アルコール依存症を有する ICU 患者や内科以外の ICU 患者における有益性は不明である 外科 外傷部門 神経内科および神経外科の患者を対象とした試験において この戦略の有効性および安全性を評価する必要がある 深い鎮静を避けるためのプロトコルに基づく管理戦略 (1 時間毎の用量調節など ) についても臨床的に有益であるが 鎮静プロトコルの使用と毎日の鎮静中断の実施を組み合わせた場合に追加的な有益性が得られるか否かは不明である (16) b. クエスチョン : 人工呼吸中の ICU 患者では 鎮痛優先の鎮静 (analgesia-first sedation; すなわち鎮痛鎮静 ) を行うべきか それとも催眠鎮静薬による鎮静を行うべきか?( 実行可能なクエスチョン ) 回答 : 人工呼吸中の成人 ICU 患者に対して 鎮痛優先の鎮静を行うことを提案する (+ 2B) 根拠 : 不穏の主要原因として疼痛および苦痛が高頻度に認められていること また 催眠鎮静薬による標準的な鎮静レジメンによって臨床的アウトカムおよび QOL アウトカムが悪化することを示す報告があることから ほとんどの ICU Critical Care Medicine 35
38 せん妄不穏Barr et al 患者で鎮痛優先の鎮静を行うべきという考え方が支持される 内科および外科 ICU 患者計 630 例を対象とした 4 件の非盲検研究において 鎮痛優先の鎮静戦略の検討が行われた ( ) 質が中等度の 1 件の研究において 鎮痛優先の鎮静により 28 日間中の人工呼吸器非依存期間 が延長し ICU 在室期間が短縮することが示された (439) その他の点に関して 鎮痛優先の鎮静が催眠鎮静薬を用いた鎮静を上回る一貫した利点は認められなかった 最適な鎮痛および鎮静が達成された時間の割合は どちらの戦略の場合も 97% であった (436,438) 1 件の研 A 重症患者の不穏は 十分に治療されていない疼痛 不安 せん妄および / または人工呼吸器不同調が原因となっている可能性がある これらの患者では 疼痛 不穏およびせん妄の検出および治療内容を頻繁に再評価するべきである 臨床的に深い鎮静が必要でない限り 患者がケアに参加できるように 患者を覚醒させ 意識的に指示に従うことができるようにするべきである ガイドラインのステートメント 推奨事項および推奨度の総合的なリストについては カードの裏面を参照すること 評価と治療 ステートメントおよび推奨事項 図 2.A:PAD ガイドライン推奨事項の実践を促すためのポケットカード ( 表側 ) ( 続く ) 痛疼 すべての ICU 患者に対して 定期的に疼痛の評価を行う (1B) コミュニケーションが可能な ICU 患者では 行動学的疼痛スケールによる評価よりも自己申告を優先させる (B) コミュニケーションが不能な ICU 患者では BPS および CPOT が最も妥当かつ信頼性のある行動学的疼痛スケールである (B) 疼痛の評価をバイタルサインのみで実施するべきではないが 補助的に用いてもよい (2C) 胸腔チューブを抜去する場合は 先行して鎮痛薬の投与および / または非薬物療法の介入を行う (1C) その他の処置に伴う疼痛に対しても 先行して鎮痛薬の投与および / または非薬物療法の介入を行うことを提案する (2C) 非神経障害性疼痛に対する治療では 第一選択薬としてオピオイドを使用する (1C) オピオイド必要量を減らすため またオピオイド投与に伴う副作用を抑制するために オピオイドに加えて非オピオイド性鎮痛薬を使用することを提案する (2C) 神経障害性疼痛に対する治療では オピオイドの静脈内投与に加えてガバペンチンまたはカルバマゼピンを投与する (1A) 腹部大動脈手術を施行した患者における術後鎮痛では 胸部硬膜外を用いる (1B) 外傷性肋骨骨折患者では 胸部硬膜外鎮痛を用いることを提案する (2B) すべての ICU 患者に対して 定期的に鎮静の深度および質の評価を行う (1B) RASS および SAS は ICU 患者における鎮静の質および深度を評価する上で最も妥当かつ信頼性のあるツールである (B) 筋弛緩薬を使用している患者では 鎮静のモニタリングに脳機能に関する客観的指標を補助的に用いることを提案する (2B) 発作リスクのある ICU 患者で非けいれん性発作の活動性のモニタリングを行う場合 あるいは頭蓋内圧上昇が認められる ICU 患者に burst suppression に達する電位抑制作用のある薬剤の用量調節を行う場合は EEG 測定法を用いる (1A) 可能な限り目標鎮静レベルを浅く設定し かつ / または鎮静を毎日中断する (1B) ICU 鎮静管理を促進するために 鎮静プロトコルおよびチェックリストを用いる (1B) 人工呼吸中の ICU 患者では 鎮痛優先の鎮静 (analgesia-first sedation) を行うことを提案する (2B) 人工呼吸中の成人 ICU 患者では 鎮静にベンゾジアゼピン系薬 ( ミダゾラムまたはロラゼパム ) よりも非ベンゾジアゼピン系薬 ( プロポフォールまたはデクスメデトミジン ) を使用することを提案する (2B) すべての ICU 患者に対して 定期的にせん妄の評価を行う (1B) CAM-ICU および ICDSC は ICU 患者のせん妄を評価する上で最も妥当かつ信頼性のある評価ツールである (A) せん妄の発現抑制と期間短縮 および機能的アウトカムの改善を図るために 可能な限り ICU 患者の早期モビライゼーションを促す (1B) ICU 患者に対して 光 音をコントロールする 患者ケアを一括して行う 夜間の刺激を減らすなどにより 睡眠を促す (1C) ICU 患者において せん妄期間の短縮の目的ではリバスチグミン投与をしない (1B) トルサード ド ポアンツ (torsades de pointes) のリスクがある患者に対して 抗精神病薬を使用することを提案しない (2B) ETOH / ベンゾジアゼピン系薬の離脱症状とは無関係のせん妄を呈する ICU 患者に対して ベンゾジアゼピン系薬を使用しないことを提案する (2B) Volume 41 Number 1
39 せん妄不穏と鎮静Special Article B PAD ガイドラインの要約 1. ICU 患者は 安静時も ICU ケアにおいても日常的に疼痛を感じている (B) 心臓血管外科術後の患者 特に女性患者における疼痛は十分に治療されていない (B) ICU 患者では 一般的に処置に伴う疼痛が認められる (B) 2. すべての患者に対して 定期的に疼痛の評価を行う (1B) 自己申告は不能であるが 運動機能が障害されていない患者では 疼痛の評価にバイタルサインではなく行動学的疼痛スケールを用いることを提案する (2C) BPS および CPOT が最も妥当かつ信頼性のある行動学的疼痛スケールである (B) バイタルサインは さらに詳細な疼痛評価を開始すべきかどうかを判断する目的でのみ用いる (2C) 3. 非神経障害性疼痛に対しては 第一選択薬としてオピオイドを静脈内投与する (1C) オピオイドの副作用を抑制するために 非オピオイド性鎮痛薬を使用する (1C) 神経障害性疼痛に対しては オピオイドの静脈内投与に加えてガバペンチンまたはカルバマゼピンを使用する (1A) 4. 特に胸腔チューブを抜去する場合 (1C) 処置に伴う疼痛に対して先行して治療を行うことを提案する (2C) 5. 腹部大動脈手術を施行した患者では胸部硬膜外鎮痛を用いる (1B) 外傷性肋骨骨折患者でも胸部硬膜外鎮痛を用いることを提案する (2B) 腹部大動脈瘤の手術を施行した患者における腰椎硬膜外鎮痛の使用に関して (0A) また 胸腔内手術または非血管系腹部手術を施行した患者における胸部硬膜外鎮痛の使用に関して (0B) エビデンスがないため指針を示すことができない 内科の ICU 患者において 局所鎮痛と全身性鎮痛のどちらを使用すべきかに関して エビデンスがないため指針を示すことができない (0) 1. ICU 患者では 浅い鎮静レベルを維持すると臨床的アウトカムが改善する (B) これらの患者では鎮静レベルを浅く維持するべきである (1B) 2. RASS および SAS は 鎮静の質および深度を評価する上で最も妥当かつ信頼性のあるツールである (B) 3. 麻痺が認められない患者では 脳機能に関する指標は 主観的なスコア化された鎮静評価の補助的にのみ用いるべきであるが (1B) 筋弛緩薬を使用している患者では 鎮静深度の第一モニタリング手法として用いることを提案する (2B) 4. 発作リスクのある ICU 患者で非けいれん性発作の活動性のモニタリングを行う場合 あるいは頭蓋内圧上昇が認められる ICU 患者に burst suppression に達する薬剤の用量調節を行う場合は EEG 測定法を用いる (1A) 5. 鎮静を毎日中断するか 浅い鎮静レベルを維持するように鎮静薬の用量調節を行う (1B) 鎮痛優先の鎮静 (analgesia-first sedation) を行うことを提案する (2B) 鎮静にはベンゾジアゼピン系薬よりも非ベンゾジアゼピン系薬を使用することを提案する (2B) ICU 患者における疼痛 鎮静およびせん妄の管理を統合し 促進するために 鎮静プロトコルおよび毎日のチェックリストを用いる (1B) 1. せん妄は死亡率の増加 (A) ICU 在室期間および入院期間の延長 (A) ICU 退室後の認知機能障害の発生 (B) に関連する 2. せん妄の危険因子として以下の因子が挙げられる : 既存の認知症 高血圧 アルコール依存症の既往歴 および入院時点で重症度の高い疾患 (B) 昏睡(B) ベンゾジアゼピン系薬の使用(B) せん妄の発現リスクがある人工呼吸中の成人 ICU 患者に鎮静薬を使用する場合は ベンゾジアゼピン系薬よりもデクスメデトミジンを使用した方がせん妄の発現率が低い (B) 3. ICU 患者のせん妄について定期的にモニタリングを行う (1B) この目的では CAM-ICU および ICDSC が最も妥当かつ信頼性のある評価ツールである (A) 4. せん妄の発現抑制と期間短縮のために 患者の早期モビライゼーションを促す (1B) 5. せん妄予防の目的でのハロペリドールまたは非定型抗精神病薬の予防的投与は提案しない (2C) 6. 成人 ICU 患者に対して 光 音をコントロールするための方策を取る 患者ケアを一括して行う 睡眠サイクルを障害しないように夜間の刺激を減らすなど環境を最適に整えることにより 睡眠を促す (1C) 7. ICU 患者において せん妄期間の短縮の目的ではリバスチグミンを投与しない (1C) 8. ベースライン時に QT 間隔延長が認められる患者 トルサード ド ポアンツ (torsades de pointes) の既往歴がある患者 QT 間隔延長を起こすことが知られている薬剤を投与中の患者では 抗精神病薬を使用することを提案しない (2C) 9. せん妄を呈する ICU 患者に鎮静薬の使用が必要な場合は アルコールまたはベンゾジアゼピン系薬の離脱症状とは無関係のせん妄に対して ベンゾジアゼピン系薬よりもデクスメデトミジンを使用することを提案する (2B) 図 2( 続き ).B: 疼痛 不穏およびせん妄 (PAD) ガイドラインの特定のステートメントおよび推奨事項を要約したポケットカード ( 裏側 ) BPS = Behavioral Pain Scale CPOT = Critical-Care Pain Observation Tool RASS = Richmond Agitation-Sedation Scale SAS = Sedation-Agitation Scale EEG = 脳波 CAM-ICU = Confusion Assessment Method for the ICU ICDSC = Intensive Care Delirium Screening Checklist ETOH エタノール 痛鎮と痛疼= 究において 自己抜管および VAP の発生率に関して鎮痛優先の鎮静による悪影響は認められなかったが この戦略を用いた群で不穏性せん妄の発現率の上昇が認められた (439) せん妄 自己抜管 VAP 死亡および ICU ケア費用に関するデータは十分に得られておらず この戦略の影響について明確な結論を導くことはできない Critical Care Medicinewww.ccmjournal.org 37
40 Barr et al ICU 患者で鎮痛優先の鎮静戦略を用いる場合 特定のオピオイドの使用を支持するような質の高い研究データはほとんどなく (127,134,407) オピオイドの選択においては 薬理学 安全性および費用対効果を考慮するべきである (440) 作用の持続時間が短く かつ用量調節が簡単な鎮痛薬は 神経学的評価が頻繁に行えるため 利点があるかもしれない 鎮痛優先の鎮静のベネフィットは この戦略によって呼吸ドライブが障害される 消化管運動が低下する 経腸栄養の施行が困難になるなどの可能性に対してバランスの取れたものでなければならない (134,441) 鎮痛薬の中止時に疼痛の再発や離脱症状の可能性があることを予想しておくべきである (130) さらに 鎮痛優先の戦略を用いた患者の 18 ~ 70% では 他の従来の鎮静薬の追加投与が必要となる ( ) 鎮痛優先の鎮静に付加的なベネフィットがある可能性が示唆されているが 質が中等度の 1 件の研究 (439) では 看護師を患者に対して 1:1 の比で配備することや患者の 付添人 を置くことが必要とされており また 鎮痛優先の鎮静を従来の GABA に基づく鎮静と具体的に比較した厳格な研究は公表されていないことから この鎮痛優先の鎮静戦略の最終的な役割は不明である 予備的データから 鎮痛優先の鎮静は長期の心理的機能に負の影響を及ぼさないことが示唆されている (442) このデータについて検証を行い せん妄 自己抜管 VAP 死亡 ICU ケア費用などのアウトカムや長期の認知機能に対する鎮痛優先の鎮静の影響についても拡大して検討するべきである これまでの研究ではオピオイドが主要鎮痛薬として投与されているが 重症患者を対象とした今後の研究では オピオイドと非オピオイド性鎮痛薬の併用による複合的な鎮痛法の評価も行うべきである (52) c.icu 患者の睡眠の促進 i. クエスチョン : 成人 ICU 患者では 非薬物療法の介入法を用いて睡眠を促すべきか? ( 実行可能なクエスチョン ) 回答 : 成人 ICU 患者に対して 光 音をコントロールするための方策を取る 患者ケアを一括して行う 睡眠サイクルを障害し ないように夜間の刺激を減らすなど環境を最適に整えることにより 睡眠を促すことを推奨する (+ 1C) 根拠 : ヒトにとって睡眠不足は有害であり ICU 患者では睡眠障害が一般的にみられる (443,444) ICU 患者は 環境的要因 ( 音 光 身体的刺激 ) や レム睡眠の頻度の低下のため 完全な睡眠サイクルがほとんど得られず 何度も覚醒する (443, ) 睡眠不足により組織修復や細胞性免疫機能が障害されるため 治癒反応に影響が出る可能性がある (449) 重症患者では 睡眠不足がせん妄の発現 ( ) および生理的ストレスの増大 (455,456) に寄与している可能性がある この 10 年間において ICU 患者の睡眠科学に進歩はみられなかった 重症患者の睡眠に対する鎮静薬の薬理作用を明らかにした研究はほとんどないことから われわれは ICU 患者に睡眠を促す介入法として 非薬物療法の介入法に注目した 最近公表された 2 件の研究 ( 患者数 > 30 例 プロスペクティブコホート 介入前後比較デザイン ) によると 成人 ICU 患者において 日中および夜間のシフト中に静穏な時間を設け 患者ケアを一括して行うことを実践した結果 睡眠妨害が減少し 観察および患者の自覚のどちらによる評価でも睡眠の促進が認められた (457,458) さらに 別の記述的研究において 人工呼吸中の ICU 患者では 睡眠を妨害されない時間がほとんどないことが確認された (459) われわれは これらの知見から 看護師は患者の睡眠を促すための時間帯を定め その時間帯は日常的 ICU ケア ( 毎日の清拭など ) を避け 消灯し 環境雑音を減らすようにするべきであると考える 計画的な静穏な時間帯を提唱しているこれら 3 件の研究によると ICU において静穏が最も妨害されなかった時間帯は 午前 2 ~ 4 時 (458) 午前 0 ~ 5 時 (457) および午前 3 時前後 (459) である 別の研究において 介護施設患者で得られた間接的なエビデンスとして 高齢入院患者では 日中の光曝露量が夜間の睡眠の 38 January 2013 Volume 41 Number 1
41 予防治療評価予防治療Special Article A B ライアル EEG = 脳波 CAM-ICU = Confusion Assessment Method for the ICU;ICDSC = Intensive Care Delirium Screening Checklist 価評疼痛不穏せん妄 1 シフト当たり 4 回以上および必要に応じて 疼痛の評価を行う 優先的に使用すべき疼痛評価ツール : 自己申告が可能な患者 NRS(0 ~ 10) 自己申告が不能な患者 BPS(3 ~ 12) または CPOT(0 ~ 8) NRS 4 BPS > 5 CPOT 3 の場合 患者は著明な疼痛を感じている 30 分以内に疼痛の治療を行い その後に再評価する 非薬物療法 : リラクセーション療法 薬物療法 : 非神経障害性疼痛 IV オピオイド ± 非オピオイド性鎮痛薬 神経障害性疼痛 ガバペンチンまたはカルバマゼピン + IV オピオイド AAA 修復術後 肋骨骨折 胸部硬膜外 処置前に鎮痛薬の投与および / または非薬物療法 ( リラクセーション療法など ) を行う 疼痛治療を優先し その後 鎮静を行う 1 シフト当たり 4 回以上および必要に応じて 不穏 / 鎮静の評価を行う 優先的に使用すべき鎮静評価ツール : RASS(-5 ~ +4) または SAS(1 ~ 7) NMB 脳機能モニタリングの使用が提案される 不穏 / 鎮静の深度の定義 : 不穏 :RASS = +1 ~+4 または SAS = 5 ~ 7 覚醒して落ち着いている :RASS = 0 または SAS = 4 浅い鎮静 :RASS = -1 ~ -2 または SAS = 3 深い鎮静 :RASS = -3 ~ -5 または SAS = 1 ~ 2 目標鎮静深度または DSI( 目標 : 患者が 不穏がなく意識的に指示に従う ): RASS = -2 ~ 0 SAS = 3 ~ 4 不十分な鎮静 (RASS > 0 SAS > 4) の場合 疼痛の評価 / 治療を行う 必要に応じて鎮静薬を投与する (ETOH またはベンゾジアゼピン系薬の離脱症状が疑われる場合を除き 非ベンゾジアゼピン系薬を優先的に使用 ) 過剰鎮静 (RASS < -2 SAS < 3) の場合 鎮静薬の投与を中断し 目標鎮静レベルに達したら 中断前の 50% の用量で再開する 目標の鎮静レベルが達成されている患者では 禁忌でない限り 毎日の SBT 早期のモビライゼーションと運動を検討する 以下の場合 EEG 測定法を用いる 発作のリスクがある場合 頭蓋内圧上昇のため burst suppression に達するための治療が必要な場合 シフト毎および必要に応じて せん妄の評価を行う 優先的に使用すべきせん妄評価ツール : CAM-ICU( 陽性または陰性 ) ICDSC(0 ~ 8) せん妄状態の定義 : CAM-ICU 陽性 ICDSC 4 必要に応じて疼痛の治療を行う 見当識を回復させる 周囲環境に慣れさせる 必要に応じて患者の眼鏡や補聴器を使用させる せん妄に対する薬物療法 : ETOH またはベンゾジアゼピン系薬の離脱症状が疑われる場合を除き ベンゾジアゼピン系薬を使用しない リバスチグミンを使用しない トルサード ド ポアンツ (torsades de pointes) のリスクが高い場合 抗精神病薬を使用しない せん妄の危険因子を特定する : 認知症 高血圧 ETOH 依存 重症度の高い疾患 昏睡 ベンゾジアゼピン系薬の使用 せん妄のリスクが高い患者ではベンゾジアゼピン系薬を使用しない 早期のモビライゼーションと運動を促す 睡眠を促す ( 光と音をコントロールする 患者ケアを一括して行う 夜間の刺激を減らす ) 適応であれば ベースライン時の抗精神病薬の投与を再開する 疼痛不穏せん妄 疼痛の評価が 1 シフト当たり 4 回以上の頻度で行われた割合 (%) スコア化された ICU 疼痛評価の使用において 現場での経時的な遵守率および実践度の確認 ICU 患者が著明な疼痛 ( すなわち NRS 4 BPS 6 CPOT 3) を感じていた割合 (%) 著明な疼痛の検出後 30 分以内に疼痛治療が開始された割合 (%) 処置前に鎮痛薬の投与および / または非薬物療法が行われた割合 (%) 施設独自の ICU 疼痛管理プロトコルに対する遵守率 (%) 鎮静の評価が 1 シフト当たり 4 回以上の頻度で行われた割合 (%) スコア化された ICU 鎮静評価の使用において 現場での経時的な遵守率および実践度の確認 適切に鎮静された あるいは DSI トライアルで目標鎮静レベルが達成 ( すなわち RASS = -2 ~ 0 SAS = 3 ~ 4) された割合 (%) ICU 患者が不十分な鎮静 (RASS > 0 SAS > 4) の状態にあった割合 (%) ICU 患者が過剰鎮静 ( 非治療的昏睡 RASS < -2 SAS < 3) の状態にあった あるいは DSI トライアルを行えなかった割合 (%) 不十分または過剰な鎮静による SBT 不合格率 (%) 以下の場合に EEG 測定法が用いられた割合 (%): 発作のリスクがある場合 頭蓋内圧上昇のため burst suppression に達するための治療が必要な場合 施設独自の ICU 鎮静 / 不穏管理プロトコルに対する遵守率 (%) せん妄の評価がシフト毎に行われた割合 (%) スコア化された ICU せん妄評価ツールの使用において 現場での経時的な遵守率および実践度の確認 ICU 患者がせん妄 (CAM-ICU 陽性 ICDSC 4) の状態にあった割合 (%) せん妄 (ETOH またはベンゾジアゼピン系薬の離脱症状によるものでない ) が確認されている患者でベンゾジアゼピン系薬が投与された割合 (%) 毎日の理学療法および早期のモビライゼーションが行われた割合 (%) ICU 睡眠促進戦略に対する遵守率 (%) 施設独自の ICU せん妄予防 治療プロトコルに対する遵守率 (%) 図 3.A:ICU での疼痛 不穏およびせん妄 (PAD) ケアバンドル (469) B:ICU での PAD ケアバンドルの評価項目 NRS = 数値評価スケール BPS = Behavioral Pain Scale CPOT = Critical-Care Pain Observation Tool 非薬物療法 = 特に胸腔チューブ抜去時のリラクセーション療法 IV = 静脈内 AAA = 腹部大動脈瘤 NMB = 筋弛緩薬 RASS = Richmond Agitation and Sedation Scale SAS = Sedation- Agitation Scale 脳機能モニタリング = 聴覚誘発電位 (AEP) Bispectral Index(BIS) Narcotrend Index(NI) Patient State Index(PSI) state entropy(se) DSI = 毎日の鎮静中断 ( 自発覚醒トライアル [SAT] ともいう ) ETOH = エタノール 非ベンゾジアゼピン系薬 = プロポフォール ( 挿管患者 / 人工呼吸中の患者で使用 ) デクスメデトミジン ( 挿管患者および非挿管患者で使用 ) SBT = 自発呼吸ト Critical Care Medicinewww.ccmjournal.org 39
42 Barr et al 質および促進に影響を及ぼす可能性があることが示されている (460) これらの結果は ICU 患者集団において検証しなければならない 音や光の悪影響を抑制する上でのアイマスクや耳栓の効果については さらなる研究による裏付けが必要である (461) 重症患者において 高用量の鎮静薬投与および人工呼吸器の装着は睡眠パターンを乱す (459,462) 浅い鎮静レベルを維持することで ICU 患者の睡眠が促されるというエビデンスは得られていない ii. クエスチョン : 人工呼吸中の ICU 患者では 睡眠を促すために特定の換気モードを使用するべきか? ( 実行可能なクエスチョン ) 回答 : 人工呼吸中の成人 ICU 患者において 睡眠を促すための特定の換気モードの使用に関して そのような介入の有効性を示すエビデンスが不十分なため 推奨しない (0 エビデンスなし ) 根拠 :2 件の小規模研究 ( 患者数 <30 例 ) により 人工呼吸中の成人 ICU 患者では 中枢性無呼吸のリスクを低減する換気モードを使用することにより 睡眠の質が改善する可能性があることが示されている (463,464) この結果について 適切にデザインされた大規模なプロスペクティブ試験で検証する必要がある 2.ICU 鎮痛 鎮静 せん妄ガイドラインの導入を促すための戦略クエスチョン : 成人 ICU 患者における鎮静プロトコルおよびガイドラインの実践を促すために 学際的な教育および行動戦略を用いるべきか?( 実行可能なクエスチョン ) 回答 : 成人 ICU 患者の PAD 管理に関するガイドラインまたはプロトコルの使用を促すために 医療従事者への教育 印刷および / または電子化されたプロトコルやオーダー票 および適切な ICU 回診チェックリストを用いることを含む学際的な ICU チームアプローチを推奨する (+ 1B) 根拠 : 総患者数 2,887 例の 12 件の非盲検研究で得られた大部分のデータから ICU 患者の快適さを目的としたプロトコルを導入する際に これに加えて 1 つ以上の戦略を用いることにより 人工呼吸器装着期間が短縮する ( あるいは生存者の人工呼吸器非依存日数が増加する ) ことが示唆されている (7-10,12,13,18,19, ) プロトコルの導入を促すための戦略が ICU 在室期間に及ぼす影響については 総患者数 2,707 例の 11 件の研究でデータが一貫しておらず 有害な影響を示唆するデータはほとんどなかった (7-10,12,13,18,19,159,160,162) 自己抜管の発生率についても この戦略による有害な影響を示すエビデンスはなかった 最後に 患者がそれぞれに定められた目標鎮静レベルに維持された時間あるいは患者または看護師の満足度を指標とした管理に関して これを推奨する十分なデータはなかった 全体的なデータから 戦略 ( 教育 スタッフの補充 電子上でのリマインダーなど ) を用いる主なベネフィットは 人工呼吸器装着期間の短縮であることが示唆されているが 総合的なベネフィットは不明である ICU における総合的鎮静プロトコルの使用状況を改善させるための戦略を用いる上で これに伴うリスクは小さく 費用は最小限である ベッドサイドケアへの推奨事項の適用を促すためのツール本ガイドラインに示したエビデンスと ICU の臨床現場のギャップを埋めることは ICU 臨床医にとって非常に難しい課題である (465,466) これを達成するには多角的な学際的アプローチを用いるのが最良である (4,467) 臨床ガイドラインが支持している推奨事項は 各地域の医療習慣や利用可能な資源の状況に合わせられるべきであり これを雛形として施設独自のプロトコルおよびオーダーセットを作成するべきである 導入を成功させるには 教育による普及 地域オピニオンリーダーの協力 臨床現場でのリマインダー および介護者への実践のフィードバックや 継続的なプロトコルの評価と見直しが必要である (7-10,12,13,18,19, ,468) 電子化したガイドラインを臨床意思決定支援ツールに組み込めば 臨床現場への知見の移行と適用が速やかに行えるようになると考えられる (465,466) われわれはこのような取り組みを支援するために 本ガイドラインの推奨事項を要約したポケットカード ( 図 2) と PAD ケアバンドルの雛形 ( 図 3) を作成した (469) ケアバンドルの使用により ガイドラインの臨床現場への適用が促され VAP カテーテル関連血流感染 敗血症といった ICU における多数の複雑な問題の管理が可能になっている (470,471) ケアバンドルには 患者アウトカムを改善させる可能性が最も高い要素が盛り込まれる 実践しやすく 有益であり しっかりとした科学的および臨床的根拠に基づいており 対象患者集団および医療制度において意義があるといった条 40 January 2013 Volume 41 Number 1
43 Special Article 件に該当する要素が盛り込まれるべきである (31) ケアバンドルの各要素に対する遵守状況については 1 つ以上の患者アウトカムに関連する測定可能な指標を定めて評価するべきである 品質保証データを提示することで 介護者に速やかにフィードバックを行うことができ 短いサイクルで改善を図ることによって バンドルをさらにカスタマイズしていくことができると思われる この PAD ケアバンドルは 統合された戦略によって PAD を系統的に検出 管理することと これらの戦略の有効性を評価することを基本としている ( 図 3) 要約本ガイドラインの目的は 成人 ICU 患者における PAD 管理を最適化するために最良の医療習慣を定めることであり GRADE システムに基づき 公表された関連エビデンスについて 客観性および透明性を確保しながら厳格かつバイアスのない評価を行った上で 本ガイドラインを作成した ステートメントおよび推奨事項の作成では エビデンスの質のみでなく 重要な臨床的アウトカムおよび ICU 利害関係者の価値観と選好性も考慮した われわれは 本ガイドラインが 重症患者に対する総合的な PAD 管理のためのエビデンスに基づく最良の実践プロトコルを作成する上でロードマップになると考えている 謝辞本ガイドラインの作成における Charles P. Kishman, Jr 氏 (MSLS Information Services Librarian; University of Cincinnati Cincinnati OH) の非常に貴重な貢献に対して深謝いたします Kishman 氏は われわれが検索戦略を定め 大規模な Web ガイドラインデータベースを作成 維持する際に助力くださり ガイドラインの参考文献一覧の作成および管理に貢献しました また 本ガイドラインの作成において技術面で助力くださった以下の皆様にも感謝いたします : Christopher D. Stave 氏 (MLS;Lane Medical Library Stanford University School of Medicine Stanford CA); 計量心理学専門家の David Streiner 氏 (PhD; University of Toronto Department of Psychiatry Toronto Ontario カナダ ;McMaster University Department of Clinical Epidemiology and Biostatistics Hamilton Ontario カナダ) Celeste Johnston 氏 (RN DEd;School of Nursing McGill University Montreal Quebec カナダ ) および Carolyn Waltz 氏 (RN PhD FAAN;School of Nursing University of Maryland Baltimore MD);GRADE ワーキンググルー プメンバーの Gordon H. Guyatt 氏 (MD;Departments of Medicine and Clinical Epidemiology and Biostatistics McMaster University Hamilton ON カナダ ) Holger Schunemann 氏 (MD PhD;Department of Clinical Epidemiology & Biostatistics, McMaster University Health Sciences Centre Hamilton ON カ ナダ ) および Deborah Cook 氏 (MD;Department of Medicine Clinical Epidemiology & Biostatistics McMaster University Hamilton ON カナダ ); Patricia Rohr 氏 (Medical Editor;Stanford University School of Medicine Stanford CA);Ina Lee 氏 (PharmD Neuro-ICU clinical pharmacist;university of Washington/Harborview Medical Center Seattle WA); ならびに Kathy Ward 氏および Laura Kolinski 氏 (Society of Critical Care Medicine Mount Prospect IL) REFERENCES 1. Jacobi J, Fraser GL, Coursin DB, et al; Task Force of the American College of Critical Care Medicine (ACCM) of the Society of Critical Care Medicine (SCCM), American Society of Health-System Pharmacists (ASHP), American College of Chest Physicians: Clinical practice guidelines for the sustained use of sedatives and analgesics in the critically ill adult. Crit Care Med 2002; 30: Chanques G, Jaber S, Barbotte E, et al: Impact of systematic evaluation of pain and agitation in an intensive care unit. Crit Care Med 2006; 34: Payen JF, Bosson JL, Chanques G, et al; DOLOREA Investigators: Pain assessment is associated with decreased duration of mechanical ventilation in the intensive care unit: A post Hoc analysis of the DOLOREA study. Anesthesiology 2009; 111: Vasilevskis EE, Ely EW, Speroff T, et al: Reducing iatrogenic risks: ICU-acquired delirium and weakness Crossing the quality chasm. Chest 2010; 138: Riker RR, Fraser GL: Altering intensive care sedation paradigms to improve patient outcomes. Crit Care Clin 2009; 25: , viii 6. Arnold HM, Hollands JM, Skrupky LP, et al: Optimizing sustained use of sedation in mechanically ventilated patients: Focus on safety. Curr Drug Saf 2010; 5: Arabi Y, Haddad S, Hawes R, et al: Changing sedation practices in the intensive care unit Protocol implementation, multifaceted multidisciplinary approach and teamwork. Middle East J Anesthesiol 2007; 19: Arias-Rivera S, Sánchez-Sánchez Mdel M, Santos-Díaz R, et al: Effect of a nursing-implemented sedation protocol on weaning outcome. Crit Care Med 2008; 36: Brattebø G, Hofoss D, Flaatten H, et al: Effect of a scoring system and protocol for sedation on duration of patients need for ventilator support in a surgical intensive care unit. BMJ 2002; 324: Brook AD, Ahrens TS, Schaiff R, et al: Effect of a nursing-implemented sedation protocol on the duration of mechanical ventilation. Crit Care Med 1999; 27: De Jonghe B, Bastuji-Garin S, Fangio P, et al: Sedation algorithm in critically ill patients without acute brain injury. Crit Care Med 2005; 33: Quenot JP, Ladoire S, Devoucoux F, et al: Effect of a nurse-implemented sedation protocol on the incidence of ventilator-associated pneumonia. Crit Care Med 2007; 35: Critical Care Medicine 41
44 Barr et al 13. Robinson BR, Mueller EW, Henson K, et al: An analgesia-deliriumsedation protocol for critically ill trauma patients reduces ventilator days and hospital length of stay. J Trauma 2008; 65: Girard TD, Kress JP, Fuchs BD, et al: Efficacy and safety of a paired sedation and ventilator weaning protocol for mechanically ventilated patients in intensive care (Awakening and Breathing Controlled trial): A randomised controlled trial. Lancet 2008; 371: Kress JP, Pohlman AS, O Connor MF, et al: Daily interruption of sedative infusions in critically ill patients undergoing mechanical ventilation. N Engl J Med 2000; 342: Mehta S, Burry L, Martinez-Motta JC, et al; Canadian Critical Care Trials Group: A randomized trial of daily awakening in critically ill patients managed with a sedation protocol: A pilot trial. Crit Care Med 2008; 36: Adam C, Rosser D, Manji M: Impact of introducing a sedation management guideline in intensive care. Anaesthesia 2006; 61: Bucknall TK, Manias E, Presneill JJ: A randomized trial of protocoldirected sedation management for mechanical ventilation in an Australian intensive care unit. Crit Care Med 2008; 36: Elliott R, McKinley S, Aitken LM, et al: The effect of an algorithmbased sedation guideline on the duration of mechanical ventilation in an Australian intensive care unit. Intensive Care Med 2006; 32: Treggiari MM, Romand JA, Yanez ND, et al: Randomized trial of light versus deep sedation on mental health after critical illness. Crit Care Med 2009; 37: Griffiths RD, Jones C: Seven lessons from 20 years of follow-up of intensive care unit survivors. Curr Opin Crit Care 2007; 13: Milbrandt EB, Angus DC: Bench-to-bedside review: Critical illnessassociated cognitive dysfunction Mechanisms, markers, and emerging therapeutics. Crit Care 2006; 10: Larson MJ, Weaver LK, Hopkins RO: Cognitive sequelae in acute respiratory distress syndrome patients with and without recall of the intensive care unit. J Int Neuropsychol Soc 2007; 13: Jones C, Griffiths RD, Humphris G, et al: Memory, delusions, and the development of acute posttraumatic stress disorder-related symptoms after intensive care. Crit Care Med 2001; 29: Schelling G, Stoll C, Haller M, et al: Health-related quality of life and posttraumatic stress disorder in survivors of the acute respiratory distress syndrome. Crit Care Med 1998; 26: Swaiss IG, Badran I: Discomfort, awareness and recall in the intensive care-still a problem? Middle East J Anesthesiol 2004; 17: Hopkins RO, Weaver LK, Collingridge D, et al: Two-year cognitive, emotional, and quality-of-life outcomes in acute respiratory distress syndrome. Am J Respir Crit Care Med 2005; 171: Jones C, Griffiths RD, Slater T, et al: Significant cognitive dysfunction in non-delirious patients identified during and persisting following critical illness. Intensive Care Med 2006; 32: Jones C, Bäckman C, Capuzzo M, et al: Precipitants of post-traumatic stress disorder following intensive care: A hypothesis generating study of diversity in care. Intensive Care Med 2007; 33: Davydow DS, Gifford JM, Desai SV, et al: Posttraumatic stress disorder in general intensive care unit survivors: A systematic review. Gen Hosp Psychiatry 2008; 30: Rello J, Lode H, Cornaglia G, et al; VAP Care Bundle Contributors: A European care bundle for prevention of ventilator-associated pneumonia. Intensive Care Med 2010; 36: Tufano R, Piazza O, De Robertis E: Guidelines and the medical art. Intensive Care Med 2010; 36: Bellomo R, Stow PJ, Hart GK: Why is there such a difference in outcome between Australian intensive care units and others? Curr Opin Anaesthesiol 2007; 20: Rello J, Lorente C, Bodí M, et al: Why do physicians not follow evidence-based guidelines for preventing ventilator-associated pneumonia? A survey based on the opinions of an international panel of intensivists. Chest 2002; 122: Hicks P, Cooper DJ; The Australian and New Zealand Intensive Care Society (ANZICS) Board and Clinical Trials Group Executive Committee: The Surviving Sepsis Campaign: International guidelines for management of severe sepsis and septic shock: Crit Care Resusc 2008; 10:8 36. Orford NR, Faulkner C, Flintoff W, et al: Implementation and outcomes of a severe sepsis protocol in an Australian tertiary hospital. Crit Care Resusc 2008; 10: American Society of Anesthesiologists Task Force on Sedation and Analgesia by Non-Anesthesiologists: Practice guidelines for sedation and analgesia by non-anesthesiologists. Anesthesiology 2002; 96: Schünemann HJ, Jaeschke R, Cook DJ, et al; ATS Documents Development and Implementation Committee: An official ATS statement: Grading the quality of evidence and strength of recommendations in ATS guidelines and recommendations. Am J Respir Crit Care Med 2006; 174: Guyatt G, Gutterman D, Baumann MH, et al: Grading strength of recommendations and quality of evidence in clinical guidelines: Report from an American college of chest physicians task force. Chest 2006; 129: Guyatt GH, Oxman AD, Vist GE, et al; GRADE Working Group: GRADE: An emerging consensus on rating quality of evidence and strength of recommendations. BMJ 2008; 336: Cross H: Consensus methods: A bridge between clinical reasoning and clinical research? Int J Lepr Other Mycobact Dis 2005; 73: Allen J, Dyas J, Jones M: Building consensus in health care: A guide to using the nominal group technique. Br J Community Nurs 2004; 9: Guyatt GH, Oxman AD, Kunz R, et al; GRADE Working Group: Going from evidence to recommendations. BMJ 2008; 336: Guyatt GH, Oxman AD, Kunz R, et al; GRADE Working Group: What is quality of evidence and why is it important to clinicians? BMJ 2008; 336: McGinnis PQ, Wainwright SF, Hack LM, et al: Use of a Delphi panel to establish consensus for recommended uses of selected balance assessment approaches. Physiother Theory Pract 2010; 26: Jaeschke R, Guyatt GH, Dellinger P, et al; GRADE Working Group: Use of GRADE grid to reach decisions on clinical practice guidelines when consensus is elusive. BMJ 2008; 337:a Dellinger RP, Levy MM, Carlet JM, et al; International Surviving Sepsis Campaign Guidelines Committee; American Association of Critical-Care Nurses; American College of Chest Physicians; American College of Emergency Physicians; Canadian Critical Care Society; European Society of Clinical Microbiology and Infectious Diseases; European Society of Intensive Care Medicine; European Respiratory Society; International Sepsis Forum; Japanese Association for Acute Medicine; Japanese Society of Intensive Care Medicine; Society of Critical Care Medicine; Society of Hospital Medicine; Surgical Infection Society; World Federation of Societies of Intensive and Critical Care Medicine: Surviving Sepsis Campaign: International guidelines for management of severe sepsis and septic shock: Crit Care Med 2008; 36: Streiner DL, Norman GR, Joint Author: Health Measurement Scales: A Practical Guide to Their Development and Use. Fourth Edition. Oxford, Oxford University Press, American Educational Research Association, American Psychological Association, National Council on Measurement in Education, Joint Commission Standards for Educational and Psychological Testing: Standards for Educational and Psychological Testing. Washington, DC, American Educational Research Association, Pudas-Tähkä SM, Axelin A, Aantaa R, et al: Pain assessment tools for unconscious or sedated intensive care patients: A systematic review. J Adv Nurs 2009; 65: January 2013 Volume 41 Number 1
45 Special Article 51. Pain terms: A list with definitions and notes on usage. recommended by the IASP subcommittee on taxonomy. Pain 1979; 6: Erstad BL, Puntillo K, Gilbert HC, et al: Pain management principles in the critically ill. Chest 2009; 135: Ballard KS: Identification of environmental stressors for patients in a surgical intensive care unit. Issues Ment Health Nurs 1981; 3: So HM, Chan DS: Perception of stressors by patients and nurses of critical care units in Hong Kong. Int J Nurs Stud 2004; 41: Hweidi IM: Jordanian patients perception of stressors in critical care units: A questionnaire survey. Int J Nurs Stud 2007; 44: Rotondi AJ, Chelluri L, Sirio C, et al: Patients recollections of stressful experiences while receiving prolonged mechanical ventilation in an intensive care unit. Crit Care Med 2002; 30: Shannon K, Bucknall T: Pain assessment in critical care: What have we learnt from research. Intensive Crit Care Nurs 2003; 19: International association for the study of pain IASP taxonomy. Available at: cfm?section=pain_defi... isplay.cfm&contentid=1728#pain. Accessed October Anand KJ, Craig KD: New perspectives on the definition of pain. Pain 1996; 67:3 6; discussion Puntillo KA: Pain experiences of intensive care unit patients. Heart Lung 1990; 19(5 Pt 1): Chanques G, Sebbane M, Barbotte E, et al: A prospective study of pain at rest: Incidence and characteristics of an unrecognized symptom in surgical and trauma versus medical intensive care unit patients. Anesthesiology 2007; 107: Payen JF, Chanques G, Mantz J, et al: Current practices in sedation and analgesia for mechanically ventilated critically ill patients: A prospective multicenter patient-based study. Anesthesiology 2007; 106: ; quiz Stanik-Hutt JA, Soeken KL, Belcher AE, et al: Pain experiences of traumatically injured patients in a critical care setting. Am J Crit Care 2001; 10: Stotts NA, Puntillo K, Stanik-Hutt J, et al: Does age make a difference in procedural pain perceptions and responses in hospitalized adults? Acute Pain 2007; 9: Stotts NA, Puntillo K, Bonham Morris A, et al: Wound care pain in hospitalized adult patients. Heart Lung 2004; 33: Arroyo-Novoa CM, Figueroa-Ramos MI, Puntillo KA, et al: Pain related to tracheal suctioning in awake acutely and critically ill adults: A descriptive study. Intensive Crit Care Nurs 2008; 24: Puntillo K, Ley SJ: Appropriately timed analgesics control pain due to chest tube removal. Am J Crit Care 2004; 13: ; discussion 302; quiz Puntillo KA, White C, Morris AB, et al: Patients perceptions and responses to procedural pain: Results from Thunder Project II. Am J Crit Care 2001; 10: Puntillo KA: Dimensions of procedural pain and its analgesic management in critically ill surgical patients. Am J Crit Care 1994; 3: Puntillo KA: Effects of interpleural bupivacaine on pleural chest tube removal pain: A randomized controlled trial. Am J Crit Care 1996; 5: Availability of clinical practice guidelines on acute pain management: Operative or medical procedures and trauma and urinary incontinence in adults AHCPR. Fed Regist 1992; 57: Jones J, Hoggart B, Withey J, et al: What the patients say: A study of reactions to an intensive care unit. Intensive Care Med 1979; 5: Gélinas C: Management of pain in cardiac surgery ICU patients: Have we improved over time? Intensive Crit Care Nurs 2007; 23: Schelling G, Richter M, Roozendaal B, et al: Exposure to high stress in the intensive care unit may have negative effects on health-related quality-of-life outcomes after cardiac surgery. Crit Care Med 2003; 31: Granja C, Gomes E, Amaro A, et al; JMIP Study Group: Understanding posttraumatic stress disorder-related symptoms after critical care: The early illness amnesia hypothesis. Crit Care Med 2008; 36: Akça O, Melischek M, Scheck T, et al: Postoperative pain and subcutaneous oxygen tension. Lancet 1999; 354: Hedderich R, Ness TJ: Analgesia for trauma and burns. Crit Care Clin 1999; 15: Beilin B, Shavit Y, Hart J, et al: Effects of anesthesia based on large versus small doses of fentanyl on natural killer cell cytotoxicity in the perioperative period. Anesth Analg 1996; 82: Pollock RE, Lotzová E, Stanford SD: Mechanism of surgical stress impairment of human perioperative natural killer cell cytotoxicity. Arch Surg 1991; 126: Peterson PK, Chao CC, Molitor T, et al: Stress and pathogenesis of infectious disease. Rev Infect Dis 1991; 13: Puntillo KA, Miaskowski C, Summer G: Pain. In: Pathophysiological Phenomena in Nursing: Human Responses to Illness. Third Edition. Carrieri-Kohlman V, Lindsey AM, West CM (Eds). St. Louis, MO, Saunders, 2003, pp Chanques G, Viel E, Constantin JM, et al: The measurement of pain in intensive care unit: Comparison of 5 self-report intensity scales. Pain 2010; 151: Puntillo K, Pasero C, Li D, et al: Evaluation of pain in ICU patients. Chest 2009; 135: Li D, Puntillo K, Miaskowski C: A review of objective pain measures for use with critical care adult patients unable to self-report. J Pain 2008; 9: Arbour C, Gélinas C, Michaud C: Impact of the implementation of the Critical-Care Pain Observation Tool (CPOT) on pain management and clinical outcomes in mechanically ventilated trauma intensive care unit patients: A pilot study. J Trauma Nurs 2011; 18: Darce K: Cadence wins FDA nod to sell IV pain treatment intravenous acetaminophen will be marketed for hospital patients. San Diego Union-Tribune News Nov. 2, Memis D, Inal MT, Kavalci G, et al: Intravenous paracetamol reduced the use of opioids, extubation time, and opioid-related adverse effects after major surgery in intensive care unit. J Crit Care 2010; 25: Pettersson PH, Jakobsson J, Owall A: Intravenous acetaminophen reduced the use of opioids compared with oral administration after coronary artery bypass grafting. J Cardiothorac Vasc Anesth 2005; 19: Candiotti KA, Bergese SD, Viscusi ER, et al: Safety of multipledose intravenous acetaminophen in adult inpatients. Pain Med 2010; 11: Pandey CK, Bose N, Garg G, et al: Gabapentin for the treatment of pain in guillain-barré syndrome: A double-blinded, placebocontrolled, crossover study. Anesth Analg 2002; 95: , table of contents 91. Pandey CK, Raza M, Tripathi M, et al: The comparative evaluation of gabapentin and carbamazepine for pain management in Guillain- Barré syndrome patients in the intensive care unit. Anesth Analg 2005; 101: , table of contents 92. Erstad BL, Chopda S, Esser MJ: Prescribing of analgesics in trauma patients. Am J Ther 1997; 4: Bernards CM, Shen DD, Sterling ES, et al: Epidural, cerebrospinal fluid, and plasma pharmacokinetics of epidural opioids (part 2): Effect of epinephrine. Anesthesiology 2003; 99: Richman JM, Liu SS, Courpas G, et al: Does continuous peripheral nerve block provide superior pain control to opioids? A meta-analysis. Anesth Analg 2006; 102: Cepeda MS, Carr DB, Lau J, et al: Music for pain relief. Cochrane Database Syst Rev 2006;CD Yorke J, Wallis M: Factors affecting the site and intensity of pain experienced by cardiac surgical patients in the critical care unit. Nurs Monogr 2002; 2002:49 55 Critical Care Medicine 43
46 Barr et al 97. Yorke J, Wallis M, McLean B: Patients perceptions of pain management after cardiac surgery in an Australian critical care unit. Heart Lung 2004; 33: Milgrom LB, Brooks JA, Qi R, et al: Pain levels experienced with activities after cardiac surgery. Am J Crit Care 2004; 13: Siffleet J, Young J, Nikoletti S, et al: Patients self-report of procedural pain in the intensive care unit. J Clin Nurs 2007; 16: Puntillo KA, Wild LR, Morris AB, et al: Practices and predictors of analgesic interventions for adults undergoing painful procedures. Am J Crit Care 2002; 11: ; quiz Aïssaoui Y, Zeggwagh AA, Zekraoui A, et al: Validation of a behavioral pain scale in critically ill, sedated, and mechanically ventilated patients. Anesth Analg 2005; 101: Ahlers SJ, van Gulik L, van der Veen AM, et al: Comparison of different pain scoring systems in critically ill patients in a general ICU. Crit Care 2008; 12:R Ahlers SJ, van der Veen AM, van Dijk M, et al: The use of the Behavioral Pain Scale to assess pain in conscious sedated patients. Anesth Analg 2010; 110: Gélinas C, Fillion L, Puntillo KA, et al: Validation of the Critical-Care Pain Observation Tool in adult patients. Am J Crit Care 2006; 15: Gélinas C, Johnston C: Pain assessment in the critically ill ventilated adult: Validation of the Critical-Care Pain Observation Tool and physiologic indicators. Clin J Pain 2007; 23: Marmo L, Fowler S: Pain assessment tool in the critically ill postopen heart surgery patient population. Pain Manag Nurs 2010; 11: Payen JF, Bru O, Bosson JL, et al: Assessing pain in critically ill sedated patients by using a behavioral pain scale. Crit Care Med 2001; 29: Marmo L, Fowler S: Pain assessment tool in the critically ill postopen heart surgery patient population. Pain Manag Nurs 2010; 11: Young J, Siffleet J, Nikoletti S, et al: Use of a Behavioural Pain Scale to assess pain in ventilated, unconscious and/or sedated patients. Intensive Crit Care Nurs 2006; 22: Gélinas C, Arbour C: Behavioral and physiologic indicators during a nociceptive procedure in conscious and unconscious mechanically ventilated adults: Similar or different? J Crit Care 2009; 24:628. e Gélinas C, Fillion L, Puntillo KA: Item selection and content validity of the Critical-Care Pain Observation Tool for non-verbal adults. J Adv Nurs 2009; 65: Gélinas C, Harel F, Fillion L, et al: Sensitivity and specificity of the Critical-Care Pain Observation Tool for the detection of pain in intubated adults after cardiac surgery. J Pain Symptom Manage 2009; 37: Chanques G, Payen JF, Mercier G, et al: Assessing pain in non-intubated critically ill patients unable to self report: An adaptation of the Behavioral Pain Scale. Intensive Care Med 2009; 35: Odhner M, Wegman D, Freeland N, et al: Assessing pain control in nonverbal critically ill adults. Dimens Crit Care Nurs 2003; 22: Kabes AM, Graves JK, Norris J: Further validation of the nonverbal pain scale in intensive care patients. Crit Care Nurse 2009; 29: Puntillo KA, Morris AB, Thompson CL, et al: Pain behaviors observed during six common procedures: Results from Thunder Project II. Crit Care Med 2004; 32: Puntillo KA, Miaskowski C, Kehrle K, et al: Relationship between behavioral and physiological indicators of pain, critical care patients self-reports of pain, and opioid administration. Crit Care Med 1997; 25: Herr K, Coyne PJ, Key T, et al; American Society for Pain Management Nursing: Pain assessment in the nonverbal patient: Position statement with clinical practice recommendations. Pain Manag Nurs 2006; 7: Friesner SA, Curry DM, Moddeman GR: Comparison of two painmanagement strategies during chest tube removal: Relaxation exercise with opioids and opioids alone. Heart Lung 2006; 35: Singh M, Gopinath R: Topical analgesia for chest tube removal in cardiac patients. J Cardiothorac Vasc Anesth 2005; 19: Joshi VS, Chauhan S, Kiran U, et al: Comparison of analgesic efficacy of fentanyl and sufentanil for chest tube removal after cardiac surgery. Ann Card Anaesth 2007; 10: Rapanos T, Murphy P, Szalai JP, et al: Rectal indomethacin reduces postoperative pain and morphine use after cardiac surgery. Can J Anaesth 1999; 46: Hynninen MS, Cheng DC, Hossain I, et al: Non-steroidal anti-inflammatory drugs in treatment of postoperative pain after cardiac surgery. Can J Anaesth 2000; 47: Machata AM, Illievich UM, Gustorff B, et al: Remifentanil for tracheal tube tolerance: A case control study. Anaesthesia 2007; 62: But AK, Erdil F, Yucel A, et al: The effects of single-dose tramadol on post-operative pain and morphine requirements after coronary artery bypass surgery. Acta Anaesthesiol Scand 2007; 51: Krishnan K, Elliot SC, Berridge JC, et al: Remifentanil patientcontrolled analgesia following cardiac surgery. Acta Anaesthesiol Scand 2005; 49: Dahaba AA, Grabner T, Rehak PH, et al: Remifentanil versus morphine analgesia and sedation for mechanically ventilated critically ill patients: A randomized double blind study. Anesthesiology 2004; 101: Karabinis A, Mandragos K, Stergiopoulos S, et al: Safety and efficacy of analgesia-based sedation with remifentanil versus standard hypnotic-based regimens in intensive care unit patients with brain injuries: A randomised, controlled trial [ISRCTN ]. Crit Care 2004; 8:R268 R Chinachoti T, Kessler P, Kirkham A, et al: Remifentanil vs morphine for patients in intensive care unit who need short-term mechanical ventilation. J Med Assoc Thai 2002; 85(Suppl 3):S848 S Soltész S, Biedler A, Silomon M, et al: Recovery after remifentanil and sufentanil for analgesia and sedation of mechanically ventilated patients after trauma or major surgery. Br J Anaesth 2001; 86: Breen D, Wilmer A, Bodenham A, et al: Offset of pharmacodynamic effects and safety of remifentanil in intensive care unit patients with various degrees of renal impairment. Crit Care 2004; 8:R21 R Guillou N, Tanguy M, Seguin P, et al: The effects of small-dose ketamine on morphine consumption in surgical intensive care unit patients after major abdominal surgery. Anesth Analg 2003; 97: Frakes MA, Lord WR, Kociszewski C, et al: Efficacy of fentanyl analgesia for trauma in critical care transport. Am J Emerg Med 2006; 24: Carrer S, Bocchi A, Candini M, et al: Short term analgesia based sedation in the Intensive Care Unit: Morphine vs remifentanil + morphine. Minerva Anestesiol 2007; 73: Maddali MM, Kurian E, Fahr J: Extubation time, hemodynamic stability, and postoperative pain control in patients undergoing coronary artery bypass surgery: An evaluation of fentanyl, remifentanil, and nonsteroidal antiinflammatory drugs with propofol for perioperative and postoperative management. J Clin Anesth 2006; 18: Guggenberger H, Schroeder TH, Vonthein R, et al: Remifentanil or sufentanil for coronary surgery: Comparison of postoperative respiratory impairment. Eur J Anaesthesiol 2006; 23: Schmittner MD, Vajkoczy SL, Horn P, et al: Effects of fentanyl and S(+)-ketamine on cerebral hemodynamics, gastrointestinal motility, and need of vasopressors in patients with intracranial pathologies: A pilot study. J Neurosurg Anesthesiol 2007; 19: Park WY, Thompson JS, Lee KK: Effect of epidural anesthesia and analgesia on perioperative outcome: A randomized, controlled Veterans Affairs cooperative study. Ann Surg 2001; 234: ; discussion January 2013 Volume 41 Number 1
47 Special Article 139. Nishimori M, Ballantyne JC, Low JH: Epidural pain relief versus systemic opioid-based pain relief for abdominal aortic surgery. Cochrane Database Syst Rev 2006; CD Rigg JR, Jamrozik K, Myles PS, et al; MASTER Anaethesia Trial Study Group: Epidural anaesthesia and analgesia and outcome of major surgery: A randomised trial. Lancet 2002; 359: Peyton PJ, Myles PS, Silbert BS, et al: Perioperative epidural analgesia and outcome after major abdominal surgery in high-risk patients. Anesth Analg 2003; 96: Luketich JD, Land SR, Sullivan EA, et al: Thoracic epidural versus intercostal nerve catheter plus patient-controlled analgesia: A randomized study. Ann Thorac Surg 2005; 79: ; discussion Ali M, Winter DC, Hanly AM, et al: Prospective, randomized, controlled trial of thoracic epidural or patient-controlled opiate analgesia on perioperative quality of life. Br J Anaesth 2010; 104: Jottard KJ, van Berlo C, Jeuken L, et al; ERAS Group: Changes in outcome during implementation of a fast-track colonic surgery project in a university-affiliated general teaching hospital: Advantages reached with ERAS (Enhanced Recovery After Surgery project) over a 1-year period. Dig Surg 2008; 25: Rudin A, Flisberg P, Johansson J, et al: Thoracic epidural analgesia or intravenous morphine analgesia after thoracoabdominal esophagectomy: A prospective follow-up of 201 patients. J Cardiothorac Vasc Anesth 2005; 19: Wahlander S, Frumento RJ, Wagener G, et al: A prospective, double-blind, randomized, placebo-controlled study of dexmedetomidine as an adjunct to epidural analgesia after thoracic surgery. J Cardiothorac Vasc Anesth 2005; 19: Turker G, Goren S, Bayram S, et al: Comparison of lumbar epidural tramadol and lumbar epidural morphine for pain relief after thoracotomy: A repeated-dose study. J Cardiothorac Vasc Anesth 2005; 19: Beattie WS, Badner NH, Choi P: Epidural analgesia reduces postoperative myocardial infarction: A meta-analysis. Anesth Analg 2001; 93: Block BM, Liu SS, Rowlingson AJ, et al: Efficacy of postoperative epidural analgesia: A meta-analysis. JAMA 2003; 290: Bulger EM, Edwards T, Klotz P, et al: Epidural analgesia improves outcome after multiple rib fractures. Surgery 2004; 136: Carrier FM, Turgeon AF, Nicole PC, et al: Effect of epidural analgesia in patients with traumatic rib fractures: A systematic review and meta-analysis of randomized controlled trials. Can J Anaesth 2009; 56: Fraser GL, Prato BS, Riker RR, et al: Frequency, severity, and treatment of agitation in young versus elderly patients in the ICU. Pharmacotherapy 2000; 20: Atkins PM, Mion LC, Mendelson W, et al: Characteristics and outcomes of patients who self-extubate from ventilatory support: A case-control study. Chest 1997; 112: Vassal T, Anh NG, Gabillet JM, et al: Prospective evaluation of selfextubations in a medical intensive care unit. Intensive Care Med 1993; 19: Fraser GL, Riker RR, Prato BS, et al: The frequency and cost of patient-initiated device removal in the ICU. Pharmacotherapy 2001; 21: Conti J, Smith D: Haemodynamic responses to extubation after cardiac surgery with and without continued sedation. Br J Anaesth 1998; 80: Cohen D, Horiuchi K, Kemper M, et al: Modulating effects of propofol on metabolic and cardiopulmonary responses to stressful intensive care unit procedures. Crit Care Med 1996; 24: Kollef MH, Levy NT, Ahrens TS, et al: The use of continuous i.v. sedation is associated with prolongation of mechanical ventilation. Chest 1998; 114: Mascia MF, Koch M, Medicis JJ: Pharmacoeconomic impact of rational use guidelines on the provision of analgesia, sedation, and neuromuscular blockade in critical care. Crit Care Med 2000; 28: Marshall J, Finn CA, Theodore AC: Impact of a clinical pharmacist-enforced intensive care unit sedation protocol on duration of mechanical ventilation and hospital stay. Crit Care Med 2008; 36: DuBose JJ, Inaba K, Shiflett A, et al: Measurable outcomes of quality improvement in the trauma intensive care unit: The impact of a daily quality rounding checklist. J Trauma 2008; 64:22 27; discussion Devlin JW, Holbrook AM, Fuller HD: The effect of ICU sedation guidelines and pharmacist interventions on clinical outcomes and drug cost. Ann Pharmacother 1997; 31: Mehta S, McCullagh I, Burry L: Current sedation practices: Lessons learned from international surveys. Crit Care Clin 2009; 25: , vii 164. Patel RP, Gambrell M, Speroff T, et al: Delirium and sedation in the intensive care unit: Survey of behaviors and attitudes of 1384 healthcare professionals. Crit Care Med 2009; 37: Salluh JI, Dal-Pizzol F, Mello PV, et al; Brazilian Research in Intensive Care Network: Delirium recognition and sedation practices in critically ill patients: A survey on the attitudes of 1015 Brazilian critical care physicians. J Crit Care 2009; 24: Wunsch H, Kahn JM, Kramer AA, et al: Use of intravenous infusion sedation among mechanically ventilated patients in the United States. Crit Care Med 2009; 37: Szumita PM, Baroletti SA, Anger KE, et al: Sedation and analgesia in the intensive care unit: Evaluating the role of dexmedetomidine. Am J Health Syst Pharm 2007; 64: Tan JA, Ho KM: Use of dexmedetomidine as a sedative and analgesic agent in critically ill adult patients: A meta-analysis. Intensive Care Med 2010; 36: Young CC, Prielipp RC: Benzodiazepines in the intensive care unit. Crit Care Clin 2001; 17: Greenblatt DJ, Harmatz JS, Shader RI: Clinical pharmacokinetics of anxiolytics and hypnotics in the elderly. Therapeutic considerations (Part I). Clin Pharmacokinet 1991; 21: Barr J, Zomorodi K, Bertaccini EJ, et al: A double-blind, randomized comparison of i.v. lorazepam versus midazolam for sedation of ICU patients via a pharmacologic model. Anesthesiology 2001; 95: Shafer A: Complications of sedation with midazolam in the intensive care unit and a comparison with other sedative regimens. Crit Care Med 1998; 26: Swart EL, Zuideveld KP, de Jongh J, et al: Population pharmacodynamic modelling of lorazepam- and midazolam-induced sedation upon long-term continuous infusion in critically ill patients. Eur J Clin Pharmacol 2006; 62: Swart EL, de Jongh J, Zuideveld KP, et al: Population pharmacokinetics of lorazepam and midazolam and their metabolites in intensive care patients on continuous venovenous hemofiltration. Am J Kidney Dis 2005; 45: Swart EL, Zuideveld KP, de Jongh J, et al: Comparative population pharmacokinetics of lorazepam and midazolam during long-term continuous infusion in critically ill patients. Br J Clin Pharmacol 2004; 57: Greenblatt DJ, von Moltke LL, Ehrenberg BL, et al: Kinetics and dynamics of lorazepam during and after continuous intravenous infusion. Crit Care Med 2000; 28: Greenblatt DJ, Ehrenberg BL, Gunderman J, et al: Kinetic and dynamic study of intravenous lorazepam: Comparison with intravenous diazepam. J Pharmacol Exp Ther 1989; 250: Bauer TM, Ritz R, Haberthür C, et al: Prolonged sedation due to accumulation of conjugated metabolites of midazolam. Lancet 1995; 346: Critical Care Medicine 45
48 Barr et al 179. Greenblatt DJ, Abernethy DR, Locniskar A, et al: Effect of age, gender, and obesity on midazolam kinetics. Anesthesiology 1984; 61: Ochs HR, Greenblatt DJ, Divoll M, et al: Diazepam kinetics in relation to age and sex. Pharmacology 1981; 23: Oldenhof H, de Jong M, Steenhoek A, et al: Clinical pharmacokinetics of midazolam in intensive care patients, a wide interpatient variability? Clin Pharmacol Ther 1988; 43: Pohlman AS, Simpson KP, Hall JB: Continuous intravenous infusions of lorazepam versus midazolam for sedation during mechanical ventilatory support: A prospective, randomized study. Crit Care Med 1994; 22: Carson SS, Kress JP, Rodgers JE, et al: A randomized trial of intermittent lorazepam versus propofol with daily interruption in mechanically ventilated patients. Crit Care Med 2006; 34: Spina SP, Ensom MH: Clinical pharmacokinetic monitoring of midazolam in critically ill patients. Pharmacotherapy 2007; 27: Ariano RE, Kassum DA, Aronson KJ: Comparison of sedative recovery time after midazolam versus diazepam administration. Crit Care Med 1994; 22: Yaucher NE, Fish JT, Smith HW, et al: Propylene glycol-associated renal toxicity from lorazepam infusion. Pharmacotherapy 2003; 23: Barnes BJ, Gerst C, Smith JR, et al: Osmol gap as a surrogate marker for serum propylene glycol concentrations in patients receiving lorazepam for sedation. Pharmacotherapy 2006; 26: Arroliga AC, Shehab N, McCarthy K, et al: Relationship of continuous infusion lorazepam to serum propylene glycol concentration in critically ill adults. Crit Care Med 2004; 32: Reynolds HN, Teiken P, Regan ME, et al: Hyperlactatemia, increased osmolar gap, and renal dysfunction during continuous lorazepam infusion. Crit Care Med 2000; 28: Wilson KC, Farber HW: Propylene glycol accumulation during continuous-infusion lorazepam in critically ill patients. J Intensive Care Med 2008; 23:413; author reply ; author reply Yahwak JA, Riker RR, Fraser GL, et al: Determination of a lorazepam dose threshold for using the osmol gap to monitor for propylene glycol toxicity. Pharmacotherapy 2008; 28: Barr J, Donner A: Optimal intravenous dosing strategies for sedatives and analgesics in the intensive care unit. Crit Care Clin 1995; 11: Barr J: Propofol: A new drug for sedation in the intensive care unit. Int Anesthesiol Clin 1995; 33: Cox CE, Reed SD, Govert JA, et al: Economic evaluation of propofol and lorazepam for critically ill patients undergoing mechanical ventilation. Crit Care Med 2008; 36: McKeage K, Perry CM: Propofol: A review of its use in intensive care sedation of adults. CNS Drugs 2003; 17: Marik PE: Propofol: Therapeutic indications and side-effects. Curr Pharm Des 2004; 10: Weinbroum AA, Halpern P, Rudick V, et al: Midazolam versus propofol for long-term sedation in the ICU: A randomized prospective comparison. Intensive Care Med 1997; 23: Barr J, Egan TD, Sandoval NF, et al: Propofol dosing regimens for ICU sedation based upon an integrated pharmacokinetic-pharmacodynamic model. Anesthesiology 2001; 95: Tanios MA, de Wit M, Epstein SK, et al: Perceived barriers to the use of sedation protocols and daily sedation interruption: A multidisciplinary survey. J Crit Care 2009; 24: Riker RR, Fraser GL: Adverse events associated with sedatives, analgesics, and other drugs that provide patient comfort in the intensive care unit. Pharmacotherapy 2005; 25(5 Pt 2):8S 18S 201. Walder B, Tramèr MR, Seeck M: Seizure-like phenomena and propofol: A systematic review. Neurology 2002; 58: Iyer VN, Hoel R, Rabinstein AA: Propofol infusion syndrome in patients with refractory status epilepticus: An 11-year clinical experience. Crit Care Med 2009; 37: Parviainen I, Uusaro A, Kälviäinen R, et al: Propofol in the treatment of refractory status epilepticus. Intensive Care Med 2006; 32: Voss LJ, Sleigh JW, Barnard JP, et al: The howling cortex: Seizures and general anesthetic drugs. Anesth Analg 2008; 107: Fong JJ, Sylvia L, Ruthazer R, et al: Predictors of mortality in patients with suspected propofol infusion syndrome. Crit Care Med 2008; 36: Diedrich DA, Brown DR: Analytic reviews: Propofol infusion syndrome in the ICU. J Intensive Care Med 2011; 26: Kam PC, Cardone D: Propofol infusion syndrome. Anaesthesia 2007; 62: Merz TM, Regli B, Rothen HU, et al: Propofol infusion syndrome: A fatal case at a low infusion rate. Anesth Analg 2006; 103: Chukwuemeka A, Ko R, Ralph-Edwards A: Short-term low-dose propofol anaesthesia associated with severe metabolic acidosis. Anaesth Intensive Care 2006; 34: Roberts RJ, Barletta JF, Fong JJ, et al: Incidence of propofol-related infusion syndrome in critically ill adults: A prospective, multicenter study. Crit Care 2009; 13:R Khan ZP, Ferguson CN, Jones RM: alpha-2 and imidazoline receptor agonists. Their pharmacology and therapeutic role. Anaesthesia 1999; 54: Bhana N, Goa KL, McClellan KJ: Dexmedetomidine. Drugs 2000; 59: ; discussion Triltsch AE, Welte M, von Homeyer P, et al: Bispectral index-guided sedation with dexmedetomidine in intensive care: A prospective, randomized, double blind, placebo-controlled phase II study. Crit Care Med 2002; 30: Belleville JP, Ward DS, Bloor BC, et al: Effects of intravenous dexmedetomidine in humans. I. Sedation, ventilation, and metabolic rate. Anesthesiology 1992; 77: Venn RM, Karol MD, Grounds RM: Pharmacokinetics of dexmedetomidine infusions for sedation of postoperative patients requiring intensive caret. Br J Anaesth 2002; 88: Dasta JF, Kane-Gill SL, Durtschi AJ: Comparing dexmedetomidine prescribing patterns and safety in the naturalistic setting versus published data. Ann Pharmacother 2004; 38: Dyck JB, Maze M, Haack C, et al: The pharmacokinetics and hemodynamic effects of intravenous and intramuscular dexmedetomidine hydrochloride in adult human volunteers. Anesthesiology 1993; 78: Cunningham FE, Baughman VL, Tonkovich L, et al: Pharmacokinetics of dexmedetomidine (DEX) in patients with hepatic failure (HF). Clin Pharmacol Ther 1999; 65: Venn RM, Grounds RM: Comparison between dexmedetomidine and propofol for sedation in the intensive care unit: Patient and clinician perceptions. Br J Anaesth 2001; 87: Riker RR, Shehabi Y, Bokesch PM, et al; SEDCOM (Safety and Efficacy of Dexmedetomidine Compared With Midazolam) Study Group: Dexmedetomidine vs midazolam for sedation of critically ill patients: A randomized trial. JAMA 2009; 301: Shehabi Y, Ruettimann U, Adamson H, et al: Dexmedetomidine infusion for more than 24 hours in critically ill patients: Sedative and cardiovascular effects. Intensive Care Med 2004; 30: Pandharipande PP, Pun BT, Herr DL, et al: Effect of sedation with dexmedetomidine vs lorazepam on acute brain dysfunction in mechanically ventilated patients: The MENDS randomized controlled trial. JAMA 2007; 298: Gerlach AT, Murphy CV, Dasta JF: An updated focused review of dexmedetomidine in adults. Ann Pharmacother 2009; 43: Venn RM, Bradshaw CJ, Spencer R, et al: Preliminary UK experience of dexmedetomidine, a novel agent for postoperative sedation in the intensive care unit. Anaesthesia 1999; 54: Venn RM, Hell J, Grounds RM: Respiratory effects of dexmedetomidine in the surgical patient requiring intensive care. Crit Care 2000; 4: January 2013 Volume 41 Number 1
49 Special Article 226. Martin E, Ramsay G, Mantz J, et al: The role of the alpha2-adrenoceptor agonist dexmedetomidine in postsurgical sedation in the intensive care unit. J Intensive Care Med 2003; 18: Venn M, Newman J, Grounds M: A phase II study to evaluate the efficacy of dexmedetomidine for sedation in the medical intensive care unit. Intensive Care Med 2003; 29: Elbaradie S, El Mahalawy FH, Solyman AH: Dexmedetomidine vs. propofol for short-term sedation of postoperative mechanically ventilated patients. J Egypt Natl Canc Inst 2004; 16: Panzer O, Moitra V, Sladen RN: Pharmacology of sedative-analgesic agents: Dexmedetomidine, remifentanil, ketamine, volatile anesthetics, and the role of peripheral Mu antagonists. Anesthesiol Clin 2011; 29: , vii 230. Al-Metwalli RR, Mowafi HA, Ismail SA, et al: Effect of intra-articular dexmedetomidine on postoperative analgesia after arthroscopic knee surgery. Br J Anaesth 2008; 101: Kress JP, Gehlbach B, Lacy M, et al: The long-term psychological effects of daily sedative interruption on critically ill patients. Am J Respir Crit Care Med 2003; 168: Kress JP, Vinayak AG, Levitt J, et al: Daily sedative interruption in mechanically ventilated patients at risk for coronary artery disease. Crit Care Med 2007; 35: Hall RI, MacLaren C, Smith MS, et al: Light versus heavy sedation after cardiac surgery: Myocardial ischemia and the stress response. Maritime Heart Centre and Dalhousie University. Anesth Analg 1997; 85: Mangano DT, Siliciano D, Hollenberg M, et al: Postoperative myocardial ischemia. Therapeutic trials using intensive analgesia following surgery. The Study of Perioperative Ischemia (SPI) Research Group. Anesthesiology 1992; 76: Plunkett JJ, Reeves JD, Ngo L, et al: Urine and plasma catecholamine and cortisol concentrations after myocardial revascularization. Modulation by continuous sedation. Multicenter Study of Perioperative Ischemia (McSPI) Research Group, and the Ischemia Research and Education Foundation (IREF). Anesthesiology 1997; 86: Terao Y, Miura K, Saito M, et al: Quantitative analysis of the relationship between sedation and resting energy expenditure in postoperative patients. Crit Care Med 2003; 31: Samuelson KA, Lundberg D, Fridlund B: Stressful experiences in relation to depth of sedation in mechanically ventilated patients. Nurs Crit Care 2007; 12: Samuelson K, Lundberg D, Fridlund B: Memory in relation to depth of sedation in adult mechanically ventilated intensive care patients. Intensive Care Med 2006; 32: Binnekade JM, Vroom MB, de Vos R, et al: The reliability and validity of a new and simple method to measure sedation levels in intensive care patients: A pilot study. Heart Lung 2006; 35: Brandl KM, Langley KA, Riker RR, et al: Confirming the reliability of the Sedation-Agitation Scale administered by ICU nurses without experience in its use. Pharmacotherapy 2001; 21: Chernik DA, Gillings D, Laine H, et al: Validity and reliability of the Observer s Assessment of Alertness/Sedation Scale: Study with intravenous midazolam. J Clin Psychopharmacol 1990; 10: De Jonghe B, Cook D, Griffith L, et al: Adaptation to the Intensive Care Environment (ATICE): Development and validation of a new sedation assessment instrument. Crit Care Med 2003; 31: de Lemos J, Tweeddale M, Chittock D: Measuring quality of sedation in adult mechanically ventilated critically ill patients. the Vancouver Interaction and Calmness Scale. Sedation Focus Group. J Clin Epidemiol 2000; 53: Deogaonkar A, Gupta R, DeGeorgia M, et al: Bispectral Index monitoring correlates with sedation scales in brain-injured patients. Crit Care Med 2004; 32: Devlin JW, Boleski G, Mlynarek M, et al: Motor Activity Assessment Scale: A valid and reliable sedation scale for use with mechanically ventilated patients in an adult surgical intensive care unit. Crit Care Med 1999; 27: Ely EW, Truman B, Shintani A, et al: Monitoring sedation status over time in ICU patients: Reliability and validity of the Richmond Agitation-Sedation Scale (RASS). JAMA 2003; 289: Haberthür C, Lehmann F, Ritz R: Assessment of depth of midazolam sedation using objective parameters. Intensive Care Med 1996; 22: Hernández-Gancedo C, Pestaña D, Peña N, et al: Monitoring sedation in critically ill patients: Bispectral index, Ramsay and observer scales. Eur J Anaesthesiol 2006; 23: Hogg LH, Bobek MB, Mion LC, et al: Interrater reliability of 2 sedation scales in a medical intensive care unit: A preliminary report. Am J Crit Care 2001; 10: Masica AL, Girard TD, Wilkinson GR, et al: Clinical sedation scores as indicators of sedative and analgesic drug exposure in intensive care unit patients. Am J Geriatr Pharmacother 2007; 5: Nassar AP Jr, Neto RCP, de Figueiredo WB, et al: Validity, reliability and applicability of portuguese versions of Sedation-Agitation Scales among critically ill patients. Sao Paulo Medical Journal 2008; 126: Olleveant N, Humphris G, Roe B: A reliability study of the modified new Sheffield Sedation Scale. Nurs Crit Care 1998; 3: Olson D, Lynn M, Thoyre SM, et al: The limited reliability of the Ramsay scale. Neurocrit Care 2007; 7: Pun BT, Gordon SM, Peterson JF, et al: Large-scale implementation of sedation and delirium monitoring in the intensive care unit: A report from two medical centers. Crit Care Med 2005; 33: Ramsay MA, Savege TM, Simpson BR, et al: Controlled sedation with alphaxalone-alphadolone. Br Med J 1974; 2: Rassin M, Sruyah R, Kahalon A, et al: Between the fixed and the changing : Examining and comparing reliability and validity of 3 sedation-agitation measuring scales. Dimens Crit Care Nurs 2007; 26: Riker RR, Fraser GL, Cox PM: Continuous infusion of haloperidol controls agitation in critically ill patients. Crit Care Med 1994; 22: Riker RR, Fraser GL, Simmons LE, et al: Validating the Sedation- Agitation Scale with the Bispectral Index and Visual Analog Scale in adult ICU patients after cardiac surgery. Intensive Care Med 2001; 27: Weinert CR, Calvin AD: Epidemiology of sedation and sedation adequacy for mechanically ventilated patients in a medical and surgical intensive care unit. Crit Care Med 2007; 35: Weinert C, McFarland L: The state of intubated ICU patients: Development of a two-dimensional sedation rating scale for critically ill adults. Chest 2004; 126: Sessler CN, Gosnell MS, Grap MJ, et al: The Richmond Agitation- Sedation Scale: Validity and reliability in adult intensive care unit patients. Am J Respir Crit Care Med 2002; 166: Riker RR, Picard JT, Fraser GL: Prospective evaluation of the Sedation-Agitation Scale for adult critically ill patients. Crit Care Med 1999; 27: Ryder-Lewis MC, Nelson KM: Reliability of the Sedation-Agitation Scale between nurses and doctors. Intensive Crit Care Nurs 2008; 24: Schulte-Tamburen AM, Scheier J, Briegel J, et al: Comparison of five sedation scoring systems by means of auditory evoked potentials. Intensive Care Med 1999; 25: Lu CH, Man KM, Ou-Yang HY, et al: Composite auditory evoked potential index versus bispectral index to estimate the level of sedation in paralyzed critically ill patients: A prospective observational study. Anesth Analg 2008; 107: Lu CH, Ou-Yang HY, Man KM, et al: Relative reliability of the auditory evoked potential and Bispectral Index for monitoring sedation level in surgical intensive care patients. Anaesth Intensive Care 2008; 36: Critical Care Medicine 47
50 Barr et al 267. Arbour R, Waterhouse J, Seckel MA, et al: Correlation between the Sedation-Agitation Scale and the Bispectral Index in ventilated patients in the intensive care unit. Heart Lung 2009; 38: Walsh TS, Ramsay P, Lapinlampi TP, et al: An assessment of the validity of spectral entropy as a measure of sedation state in mechanically ventilated critically ill patients. Intensive Care Med 2008; 34: Haenggi M, Ypparila-Wolters H, Bieri C, et al: Entropy and bispectral index for assessment of sedation, analgesia and the effects of unpleasant stimuli in critically ill patients: An observational study. Crit Care 2008; 12:R Roustan JP, Valette S, Aubas P, et al: Can electroencephalographic analysis be used to determine sedation levels in critically ill patients? Anesth Analg 2005; 101: , table of contents 271. Olson DM, Thoyre SM, Peterson ED, et al: A randomized evaluation of bispectral index-augmented sedation assessment in neurological patients. Neurocrit Care 2009; 11: Weber F, Steinberger M, Ritzka M, et al: Measuring depth of sedation in intensive care patients with the electroencephalographic Narcotrend Index. Eur J Anaesthesiol 2008; 25: Hernández-Gancedo C, Pestaña D, Pérez-Chrzanowska H, et al: Comparing Entropy and the Bispectral index with the Ramsay score in sedated ICU patients. J Clin Monit Comput 2007; 21: Weatherburn C, Endacott R, Tynan P, et al: The impact of bispectral index monitoring on sedation administration in mechanically ventilated patients. Anaesth Intensive Care 2007; 35: Friedman D, Claassen J, Hirsch LJ: Continuous electroencephalogram monitoring in the intensive care unit. Anesth Analg 2009; 109: Consales G, Chelazzi C, Rinaldi S, et al: Bispectral Index compared to Ramsay score for sedation monitoring in intensive care units. Minerva Anestesiol 2006; 72: Tonner PH, Wei C, Bein B, et al: Comparison of two bispectral index algorithms in monitoring sedation in postoperative intensive care patients. Crit Care Med 2005; 33: Adesanya AO, Rosero E, Wyrick C, et al: Assessing the predictive value of the bispectral index vs patient state index on clinical assessment of sedation in postoperative cardiac surgery patients. J Crit Care 2009; 24: Trouiller P, Fangio P, Paugam-Burtz C, et al: Frequency and clinical impact of preserved bispectral index activity during deep sedation in mechanically ventilated ICU patients. Intensive Care Med 2009; 35: Arbour R: Impact of bispectral index monitoring on sedation and outcomes in critically ill adults: A case series. Crit Care Nurs Clin North Am 2006; 18: , xi 281. Riker RR, Fraser GL, Wilkins ML: Comparing the bispectral index and suppression ratio with burst suppression of the electroencephalogram during pentobarbital infusions in adult intensive care patients. Pharmacotherapy 2003; 23: de Wit M, Epstein SK: Administration of sedatives and level of sedation: Comparative evaluation via the Sedation-Agitation Scale and the Bispectral Index. Am J Crit Care 2003; 12: Mondello E, Siliotti R, Noto G, et al: Bispectral Index in ICU: Correlation with Ramsay Score on assessment of sedation level. J Clin Monit Comput 2002; 17: Frenzel D, Greim CA, Sommer C, et al: Is the bispectral index appropriate for monitoring the sedation level of mechanically ventilated surgical ICU patients? Intensive Care Med 2002; 28: Ruokonen E, Parviainen I, Jakob SM, et al; Dexmedetomidine for Continuous Sedation Investigators: Dexmedetomidine versus propofol/midazolam for long-term sedation during mechanical ventilation. Intensive Care Med 2009; 35: Maldonado JR, Wysong A, van der Starre PJ, et al: Dexmedetomidine and the reduction of postoperative delirium after cardiac surgery. Psychosomatics 2009; 50: Samuelson KA, Lundberg D, Fridlund B: Light vs. heavy sedation during mechanical ventilation after oesophagectomy A pilot experimental study focusing on memory. Acta Anaesthesiol Scand 2008; 52: Pandharipande P, Cotton BA, Shintani A, et al: Prevalence and risk factors for development of delirium in surgical and trauma intensive care unit patients. J Trauma 2008; 65: Pandharipande P, Ely EW: Sedative and analgesic medications: Risk factors for delirium and sleep disturbances in the critically ill. Crit Care Clin 2006; 22: , vii 290. Arroliga AC, Thompson BT, Ancukiewicz M, et al; Acute Respiratory Distress Syndrome Network: Use of sedatives, opioids, and neuromuscular blocking agents in patients with acute lung injury and acute respiratory distress syndrome. Crit Care Med 2008; 36: Ho KM, Ng JY: The use of propofol for medium and long-term sedation in critically ill adult patients: A meta-analysis. Intensive Care Med 2008; 34: Fong JJ, Kanji S, Dasta JF, et al: Propofol associated with a shorter duration of mechanical ventilation than scheduled intermittent lorazepam: A database analysis using Project IMPACT. Ann Pharmacother 2007; 41: Esmaoglu A, Ulgey A, Akin A, et al: Comparison between dexmedetomidine and midazolam for sedation of eclampsia patients in the intensive care unit. J Crit Care 2009; 24: Anis AH, Wang XH, Leon H, et al; Propofol Study Group: Economic evaluation of propofol for sedation of patients admitted to intensive care units. Anesthesiology 2002; 96: Hall RI, Sandham D, Cardinal P, et al; Study Investigators: Propofol vs midazolam for ICU sedation: A Canadian multicenter randomized trial. Chest 2001; 119: Huey-Ling L, Chun-Che S, Jen-Jen T, et al: Comparison of the effect of protocol-directed sedation with propofol vs. midazolam by nurses in intensive care: Efficacy, haemodynamic stability and patient satisfaction. J Clin Nurs 2008; 17: Searle NR, Côté S, Taillefer J, et al: Propofol or midazolam for sedation and early extubation following cardiac surgery. Can J Anaesth 1997; 44: Pandharipande PP, Sanders RD, Girard TD, et al; MENDS Investigators: Effect of dexmedetomidine versus lorazepam on outcome in patients with sepsis: An a priori-designed analysis of the MENDS randomized controlled trial. Crit Care 2010; 14:R Barrientos-Vega R, Mar Sánchez-Soria M, Morales-García C, et al: Prolonged sedation of critically ill patients with midazolam or propofol: Impact on weaning and costs. Crit Care Med 1997; 25: Dasta JF, Kane-Gill SL, Pencina M, et al: A cost-minimization analysis of dexmedetomidine compared with midazolam for longterm sedation in the intensive care unit. Crit Care Med 2010; 38: Jakob SM, Ruokonen E, Grounds RM, et al; Dexmedetomidine for Long-Term Sedation Investigators: Dexmedetomidine vs midazolam or propofol for sedation during prolonged mechanical ventilation: Two randomized controlled trials. JAMA 2012; 307: Carrasco G, Cabré L, Sobrepere G, et al: Synergistic sedation with propofol and midazolam in intensive care patients after coronary artery bypass grafting. Crit Care Med 1998; 26: Meagher DJ, Leonard M, Donnelly S, et al: A longitudinal study of motor subtypes in delirium: Relationship with other phenomenology, etiology, medication exposure and prognosis. J Psychosom Res 2011; 71: Gupta N, de Jonghe J, Schieveld J, et al: Delirium phenomenology: What can we learn from the symptoms of delirium? J Psychosom Res 2008; 65: American Psychiatric Association: Delirium, dementia and amnestic and other cognitive disorders. In: Diagnostic and Statistical Manual of Mental Disorders, 4th ed. Washington, DC, American Psychiatric Association, 1994, pp January 2013 Volume 41 Number 1
51 Special Article 306. American Psychiatric Association: Diagnostic and Statistical Manual of Mental Disorders. Washington, DC, American Psychiatric Association, American Psychiatric Association: Practice guideline for the treatment of patients with delirium. Am J Psychiatry 1999; 156: Ely EW, Inouye SK, Bernard GR, et al: Delirium in mechanically ventilated patients: Validity and reliability of the confusion assessment method for the intensive care unit (CAM-ICU). JAMA 2001; 286: Bergeron N, Dubois MJ, Dumont M, et al: Intensive Care Delirium Screening Checklist: Evaluation of a new screening tool. Intensive Care Med 2001; 27: American Psychiatric Association: American Psychiatric Association Practice Guidelines for the Treatment of Psychiatric Disorders. Compendium Arlington, VA, American Psychiatric Association, 2006, pp Changing intensive care to improve life afterward WSJ.com. Available at: html. Accessed November Hospitals fight a form of delirium that often strikes ICU patients The Washington Post. Available at: com/ national/health/hospitals-fight-a-form-of-delirium-that-oftenstrikes- icu-patients/2011/03/23/af518nmd_story.html. Accessed November Milbrandt EB, Deppen S, Harrison PL, et al: Costs associated with delirium in mechanically ventilated patients. Crit Care Med 2004; 32: McNicoll L, Pisani MA, Zhang Y, et al: Delirium in the intensive care unit: Occurrence and clinical course in older patients. J Am Geriatr Soc 2003; 51: Morandi A, Pandharipande P, Trabucchi M, et al: Understanding international differences in terminology for delirium and other types of acute brain dysfunction in critically ill patients. Intensive Care Med 2008; 34: Pun BT, Ely EW: The importance of diagnosing and managing ICU delirium. Chest 2007; 132: Skrobik Y: Delirium prevention and treatment. Crit Care Clin 2009; 25:585 91, x 318. Ouimet S, Kavanagh BP, Gottfried SB, et al: Incidence, risk factors and consequences of ICU delirium. Intensive Care Med 2007; 33: Ouimet S, Riker R, Bergeron N, et al: Subsyndromal delirium in the ICU: Evidence for a disease spectrum. Intensive Care Med 2007; 33: Shehabi Y, Riker RR, Bokesch PM, et al; SEDCOM (Safety and Efficacy of Dexmedetomidine Compared With Midazolam) Study Group: Delirium duration and mortality in lightly sedated, mechanically ventilated intensive care patients. Crit Care Med 2010; 38: Pisani MA, Kong SY, Kasl SV, et al: Days of delirium are associated with 1-year mortality in an older intensive care unit population. Am J Respir Crit Care Med 2009; 180: Ely EW, Shintani A, Truman B, et al: Delirium as a predictor of mortality in mechanically ventilated patients in the intensive care unit. JAMA 2004; 291: Ely EW, Gautam S, Margolin R, et al: The impact of delirium in the intensive care unit on hospital length of stay. Intensive Care Med 2001; 27: Girard TD, Jackson JC, Pandharipande PP, et al: Delirium as a predictor of long-term cognitive impairment in survivors of critical illness. Crit Care Med 2010; 38: Needham DM, Korupolu R, Zanni JM, et al: Early physical medicine and rehabilitation for patients with acute respiratory failure: A quality improvement project. Arch Phys Med Rehabil 2010; 91: Schweickert WD, Pohlman MC, Pohlman AS, et al: Early physical and occupational therapy in mechanically ventilated, critically ill patients: A randomised controlled trial. Lancet 2009; 373: Skrobik Y, Ahern S, Leblanc M, et al: Protocolized intensive care unit management of analgesia, sedation, and delirium improves analgesia and subsyndromal delirium rates. Anesth Analg 2010; 111: Pandharipande P, Shintani A, Peterson J, et al: Lorazepam is an independent risk factor for transitioning to delirium in intensive care unit patients. Anesthesiology 2006; 104: Pisani MA, Murphy TE, Araujo KL, et al: Benzodiazepine and opioid use and the duration of intensive care unit delirium in an older population. Crit Care Med 2009; 37: Martin J, Heymann A, Bäsell K, et al: Evidence and consensusbased German guidelines for the management of analgesia, sedation and delirium in intensive care Short version. Ger Med Sci 2010; 8:Doc Michaud L, Büla C, Berney A, et al: Delirium: Guidelines for general hospitals. Wiadomosci Psychiatryczne 2008; 11: Silva JA, Romera MA, Chamorro C, et al: Sedo-analgesia in neurologically ill patients: Guidelines revisited. Stroke 2008; 39:e67; auhtor reply e Tropea J, Slee JA, Brand CA, et al: Clinical practice guidelines for the management of delirium in older people in Australia. Australas J Ageing 2008; 27: Kessler P, Martin J: [Optimisation of sedation practice in ICU by implementing of S2e Guidelines]. Anasthesiol Intensivmed Notfallmed Schmerzther 2008; 43: Playfor S, Jenkins I, Boyles C, et al; United Kingdom Paediatric Intensive Care Society Sedation; Analgesia and Neuromuscular Blockade Working Group: Consensus guidelines on sedation and analgesia in critically ill children. Intensive Care Med 2006; 32: Potter J, George J; Guideline Development Group: The prevention, diagnosis and management of delirium in older people: Concise guidelines. Clin Med 2006; 6: Truman B, Shintani A, Jackson J, et al: Implementation of the SCCM guidelines for sedation and delirium monitoring in the ICU. Am J Respir Crit Care Med 2003; 167:A American College of Critical Care Medicine of the Society of Critical Care Medicine, American Society of Health-System Pharmacists, American College of Chest Physicians: Clinical practice guidelines for the sustained use of sedatives and analgesics in the critically ill adult. Am J Health Syst Pharm 2002; 59: O Mahony R, Murthy L, Akunne A, et al; Guideline Development Group: Synopsis of the National Institute for Health and Clinical Excellence guideline for prevention of delirium. Ann Intern Med 2011; 154: Lonergan E, Britton AM, Luxenberg J, et al: Antipsychotics for delirium. Cochrane Database Syst Rev 2007; CD Mayo-Smith MF, Beecher LH, Fischer TL, et al; Working Group on the Management of Alcohol Withdrawal Delirium, Practice Guidelines Committee, American Society of Addiction Medicine: Management of alcohol withdrawal delirium. An evidence-based practice guideline. Arch Intern Med 2004; 164: Ashton H: The diagnosis and management of benzodiazepine dependence. Curr Opin Psychiatry 2005; 18: Nicholls L, Bragaw L, Ruetsch C: Opioid dependence treatment and guidelines. J Manag Care Pharm 2010; 16(1 Suppl B):S14 S Cammarano WB, Pittet JF, Weitz S, et al: Acute withdrawal syndrome related to the administration of analgesic and sedative medications in adult intensive care unit patients. Crit Care Med 1998; 26: American Pain Society: Principles of Analgesic Use in the Treatment of Acute Pain and Cancer Pain. Sixth Edition. Glenview, IL, American Pain Society, Preston KL, Bigelow GE, Liebson IA: Antagonist effects of nalbuphine in opioid-dependent human volunteers. J Pharmacol Exp Ther 1989; 248: Critical Care Medicine 49
52 Barr et al 347. Kamijo Y, Masuda T, Nishikawa T, et al: Cardiovascular response and stress reaction to flumazenil injection in patients under infusion with midazolam. Crit Care Med 2000; 28: Breheny FX: Reversal of midazolam sedation with flumazenil. Crit Care Med 1992; 20: Hospira Inc: FDA package insert for dexmedetomidine. Available at: Accessed October Brown C, Albrecht R, Pettit H, et al: Opioid and benzodiazepine withdrawal syndrome in adult burn patients. Am Surg 2000; 66: ; discussion Korak-Leiter M, Likar R, Oher M, et al: Withdrawal following sufentanil/propofol and sufentanil/midazolam. Sedation in surgical ICU patients: Correlation with central nervous parameters and endogenous opioids. Intensive Care Med 2005; 31: Moore RD, Bone LR, Geller G, et al: Prevalence, detection, and treatment of alcoholism in hospitalized patients. JAMA 1989; 261: Foy A, Kay J: The incidence of alcohol-related problems and the risk of alcohol withdrawal in a general hospital population. Drug Alcohol Rev 1995; 14: Spies CD, Neuner B, Neumann T, et al: Intercurrent complications in chronic alcoholic men admitted to the intensive care unit following trauma. Intensive Care Med 1996; 22: Spies CD, Nordmann A, Brummer G, et al: Intensive care unit stay is prolonged in chronic alcoholic men following tumor resection of the upper digestive tract. Acta Anaesthesiol Scand 1996; 40: Bayard M, McIntyre J, Hill KR, et al: Alcohol withdrawal syndrome. Am Fam Physician 2004; 69: Turner RC, Lichstein PR, Peden JG Jr, et al: Alcohol withdrawal syndromes: A review of pathophysiology, clinical presentation, and treatment. J Gen Intern Med 1989; 4: Spies CD, Otter HE, Hüske B, et al: Alcohol withdrawal severity is decreased by symptom-orientated adjusted bolus therapy in the ICU. Intensive Care Med 2003; 29: Lin SM, Liu CY, Wang CH, et al: The impact of delirium on the survival of mechanically ventilated patients. Crit Care Med 2004; 32: Micek ST, Anand NJ, Laible BR, et al: Delirium as detected by the CAM-ICU predicts restraint use among mechanically ventilated medical patients. Crit Care Med 2005; 33: Thomason JW, Shintani A, Peterson JF, et al: Intensive care unit delirium is an independent predictor of longer hospital stay: A prospective analysis of 261 non-ventilated patients. Crit Care 2005; 9:R375 R Norkiene I, Ringaitiene D, Misiuriene I, et al: Incidence and precipitating factors of delirium after coronary artery bypass grafting. Scand Cardiovasc J 2007; 41: Lin SM, Huang CD, Liu CY, et al: Risk factors for the development of early-onset delirium and the subsequent clinical outcome in mechanically ventilated patients. J Crit Care 2008; 23: Lat I, McMillian W, Taylor S, et al: The impact of delirium on clinical outcomes in mechanically ventilated surgical and trauma patients. Crit Care Med 2009; 37: Han JH, Shintani A, Eden S, et al: Delirium in the emergency department: An independent predictor of death within 6 months. Ann Emerg Med 2010; 56: e Ely EW, Dittus R: Reply letter: Pharmacological treatment of delirium in the intensive care unit. JAMA 2004; 292: Spronk PE, Riekerk B, Hofhuis J, et al: Occurrence of delirium is severely underestimated in the ICU during daily care. Intensive Care Med 2009; 35: Shintani AK, Girard TD, Eden SK, et al: Immortal time bias in critical care research: Application of time-varying Cox regression for observational cohort studies. Crit Care Med 2009; 37: Girard TD, Pandharipande PP, Carson SS, et al: Feasibility, efficacy, and safety of antipsychotics for intensive care unit delirium: The MIND randomized, placebo-controlled trial. Crit Care Med 2010; 38: Girard TD, Pandharipande PP, Carson SS, et al; MIND Trial Investigators: Feasibility, efficacy, and safety of antipsychotics for intensive care unit delirium: The MIND randomized, placebo-controlled trial. Crit Care Med 2010; 38: van Eijk MM, van Marum RJ, Klijn IA, et al: Comparison of delirium assessment tools in a mixed intensive care unit. Crit Care Med 2009; 37: Guenther U, Popp J, Koecher L, et al: Validity and reliability of the CAM-ICU Flowsheet to diagnose delirium in surgical ICU patients. J Crit Care 2010; 25: Ely EW, Margolin R, Francis J, et al: Evaluation of delirium in critically ill patients: Validation of the Confusion Assessment Method for the Intensive Care Unit (CAM-ICU). Crit Care Med 2001; 29: Soja SL, Pandharipande PP, Fleming SB, et al: Implementation, reliability testing, and compliance monitoring of the Confusion Assessment Method for the intensive care unit in trauma patients. Intensive Care Med 2008; 34: Pisani MA, Murphy TE, Van Ness PH, et al: Characteristics associated with delirium in older patients in a medical intensive care unit. Arch Intern Med 2007; 167: Roberts B, Rickard CM, Rajbhandari D, et al: Multicentre study of delirium in ICU patients using a simple screening tool. Aust Crit Care 2005; 18:6, 8 9, Balas MC, Deutschman CS, Sullivan-Marx EM, et al: Delirium in older patients in surgical intensive care units. J Nurs Scholarsh 2007; 39: Plaschke K, von Haken R, Scholz M, et al: Comparison of the confusion assessment method for the intensive care unit (CAM-ICU) with the Intensive Care Delirium Screening Checklist (ICDSC) for delirium in critical care patients gives high agreement rate(s). Intensive Care Med 2008; 34: Luetz A, Heymann A, Radtke FM, et al: Different assessment tools for intensive care unit delirium: Which score to use? Crit Care Med 2010; 38: Peterson JF, Pun BT, Dittus RS, et al: Delirium and its motoric subtypes: A study of 614 critically ill patients. J Am Geriatr Soc 2006; 54: Misak C: ICU psychosis and patient autonomy: Some thoughts from the inside. J Med Philos 2005; 30: Riekerk B, Pen EJ, Hofhuis JG, et al: Limitations and practicalities of CAM-ICU implementation, a delirium scoring system, in a Dutch intensive care unit. Intensive Crit Care Nurs 2009; 25: Devlin JW, Fong JJ, Howard EP, et al: Assessment of delirium in the intensive care unit: Nursing practices and perceptions. Am J Crit Care 2008; 17: ; quiz Tobar E, Romero C, Galleguillos T, et al: Confusion Assessment Method for diagnosing delirium in ICU patients: Cultural adaptation and validation of the spanish version. Med Intensiva 2010; 34: Smith HA, Boyd J, Fuchs DC, et al: Diagnosing delirium in critically ill children: Validity and reliability of the Pediatric Confusion Assessment Method for the intensive care unit. Crit Care Med 2011; 39: Hudetz JA, Patterson KM, Byrne AJ, et al: Postoperative delirium is associated with postoperative cognitive dysfunction at one week after cardiac surgery with cardiopulmonary bypass. Psychol Rep 2009; 105(3 Pt 1): Larsson C, Axell AG, Ersson A: Confusion assessment method for the intensive care unit (CAM-ICU): Translation, retranslation and validation into Swedish intensive care settings. Acta Anaesthesiol Scand 2007; 51: Hart RP, Best AM, Sessler CN, et al: Abbreviated cognitive test for delirium. J Psychosom Res 1997; 43: January 2013 Volume 41 Number 1
53 Special Article 389. Hart RP, Levenson JL, Sessler CN, et al: Validation of a cognitive test for delirium in medical ICU patients. Psychosomatics 1996; 37: Kennedy RE, Nakase-Thompson R, Nick TG, et al: Use of the cognitive test for delirium in patients with traumatic brain injury. Psychosomatics 2003; 44: van Eijk MM, van den Boogaard M, van Marum RJ, et al: Routine use of the confusion assessment method for the intensive care unit: A multicenter study. Am J Respir Crit Care Med 2011; 184: Neto AS, Nassar AP Jr, Cardoso SO, et al: Delirium screening in critically ill patients: A systematic review and meta-analysis. Crit Care Med 2012; 40: Gusmao-Flores D, Figueira Salluh JI, Chalhub RA, et al: The confusion assessment method for the intensive care unit (CAM-ICU) and intensive care delirium screening checklist (ICDSC) for the diagnosis of delirium: A systematic review and meta-analysis of clinical studies. Crit Care 2012; 16:R Vasilevskis EE, Morandi A, Boehm L, et al: Delirium and sedation recognition using validated instruments: Reliability of bedside intensive care unit nursing assessments from 2007 to J Am Geriatr Soc 2011; 59(Suppl 2):S249 S Devlin JW, Fong JJ, Fraser GL, et al: Delirium assessment in the critically ill. Intensive Care Med 2007; 33: Van Rompaey B, Elseviers MM, Schuurmans MJ, et al: Risk factors for delirium in intensive care patients: A prospective cohort study. Crit Care 2009; 13:R Dubois MJ, Bergeron N, Dumont M, et al: Delirium in an intensive care unit: A study of risk factors. Intensive Care Med 2001; 27: Pandharipande PP, Morandi A, Adams JR, et al: Plasma tryptophan and tyrosine levels are independent risk factors for delirium in critically ill patients. Intensive Care Med 2009; 35: Ely EW, Girard TD, Shintani AK, et al: Apolipoprotein E4 polymorphism as a genetic predisposition to delirium in critically ill patients. Crit Care Med 2007; 35: Agarwal V, O Neill PJ, Cotton BA, et al: Prevalence and risk factors for development of delirium in burn intensive care unit patients. J Burn Care Res 2010; 31: Needham DM, Korupolu R, Zanni JM, Pradhan P, Colantuoni E, Palmer JB, Brower RG, Fan E: Early physical medicine and rehabilitation for patients with acute respiratory failure: A quality improvement project. Arch Phys Med Rehabil 2010; 91: Inouye SK, Bogardus ST Jr, Charpentier PA, et al: A multicomponent intervention to prevent delirium in hospitalized older patients. N Engl J Med 1999; 340: Aizawa K, Kanai T, Saikawa Y, et al: A novel approach to the prevention of postoperative delirium in the elderly after gastrointestinal surgery. Surg Today 2002; 32: Wang W, Li HL, Wang DX, et al: Haloperidol Prophylaxis Decreases Delirium Incidence in Elderly Patients After Noncardiac Surgery: A randomized controlled trial. Crit Care Med 2011; 40: Awissi DK, Bégin C, Moisan J, et al: I-SAVE study: Impact of sedation, analgesia, and delirium protocols evaluated in the intensive care unit: An economic evaluation. Ann Pharmacother 2012; 46: Prakanrattana U, Prapaitrakool S: Efficacy of risperidone for prevention of postoperative delirium in cardiac surgery. Anaesth Intensive Care 2007; 35: Shehabi Y, Grant P, Wolfenden H, et al: Prevalence of delirium with dexmedetomidine compared with morphine based therapy after cardiac surgery: A randomized controlled trial (DEXmedetomidine COmpared to Morphine-DEXCOM Study). Anesthesiology 2009; 111: Devlin JW, Roberts RJ, Fong JJ, et al: Efficacy and safety of quetiapine in critically ill patients with delirium: A prospective, multicenter, randomized, double-blind, placebo-controlled pilot study. Crit Care Med 2010; 38: van Eijk MM, Roes KC, Honing ML, et al: Effect of rivastigmine as an adjunct to usual care with haloperidol on duration of delirium and mortality in critically ill patients: A multicentre, double-blind, placebo-controlled randomised trial. Lancet 2010; 376: Gamberini M, Bolliger D, Lurati Buse GA, et al: Rivastigmine for the prevention of postoperative delirium in elderly patients undergoing elective cardiac surgery A randomized controlled trial. Crit Care Med 2009; 37: Hunt N, Stern TA: The association between intravenous haloperidol and torsades de pointes. Three cases and a literature review. Psychosomatics 1995; 36: Sharma ND, Rosman HS, Padhi ID, et al: Torsades de pointes associated with intravenous haloperidol in critically ill patients. Am J Cardiol 1998; 81: Metzger E, Friedman R: Prolongation of the corrected QT and torsades de pointes cardiac arrhythmia associated with intravenous haloperidol in the medically ill. J Clin Psychopharmacol 1993; 13: Tisdale JE, Rasty S, Padhi ID, et al: The effect of intravenous haloperidol on QT interval dispersion in critically ill patients: Comparison with QT interval prolongation for assessment of risk of torsades de pointes. J Clin Pharmacol 2001; 41: Perrault LP, Denault AY, Carrier M, et al: Torsades de pointes secondary to intravenous haloperidol after coronary bypass grafting surgery. Can J Anaesth 2000; 47: Tisdale JE, Kovacs R, Mi D, et al: Accuracy of uncorrected versus corrected QT interval for prediction of torsade de pointes associated with intravenous haloperidol. Pharmacotherapy 2007; 27: Heinrich TW, Biblo LA, Schneider J: Torsades de pointes associated with ziprasidone. Psychosomatics 2006; 47: Tei Y, Morita T, Inoue S, et al: Torsades de pointes caused by a small dose of risperidone in a terminally ill cancer patient. Psychosomatics 2004; 45: Pham CP, de Feiter PW, van der Kuy PH, et al: Long QTc interval and torsade de pointes caused by fluconazole. Ann Pharmacother 2006; 40: Pandharipande PP, Girard T, Sanders RD, et al: Comparison of sedation with dexmedetomidine versus lorazepam in septic ICU patients. Critical Care 2008; 12:P Banerjee A, Girard TD, Pandharipande P: The complex interplay between delirium, sedation, and early mobility during critical illness: Applications in the trauma unit. Curr Opin Anaesthesiol 2011; 24: Sessler CN, Pedram S: Protocolized and target-based sedation and analgesia in the ICU. Crit Care Clin 2009; 25: , viii 423. Ethier C, Burry L, Martinez-Motta C, et al; Canadian Critical Care Trials Group: Recall of intensive care unit stay in patients managed with a sedation protocol or a sedation protocol with daily sedative interruption: A pilot study. J Crit Care 2011; 26: Weinert CR, Sprenkle M: Post-ICU consequences of patient wakefulness and sedative exposure during mechanical ventilation. Intensive Care Med 2008; 34: Roberts BL, Rickard CM, Rajbhandari D, et al: Factual memories of ICU: Recall at two years post-discharge and comparison with delirium status during ICU admission A multicentre cohort study. J Clin Nurs 2007; 16: Nelson BJ, Weinert CR, Bury CL, et al: Intensive care unit drug use and subsequent quality of life in acute lung injury patients. Crit Care Med 2000; 28: Shehabi Y, Botha JA, Boyle MS, et al: Sedation and delirium in the intensive care unit: An Australian and New Zealand perspective. Anaesth Intensive Care 2008; 36: Martin J, Franck M, Fischer M, et al: Sedation and analgesia in German intensive care units: How is it done in reality? Results of a patientbased survey of analgesia and sedation. Intensive Care Med 2006; 32: Schweickert WD, Gehlbach BK, Pohlman AS, et al: Daily interruption of sedative infusions and complications of critical illness in mechanically ventilated patients. Crit Care Med 2004; 32: Critical Care Medicine 51
54 Barr et al 430. Mehta S, Burry L, Cook, D, et al: Daily sedation interruption in mechanically ventilated critically ill patients cared for with a sedation protocol: A randomized trial. JAMA 2012 [E-pub ahead of print] 431. Fraser GL, Riker RR: Comfort without coma: Changing sedation practices. Crit Care Med 2007; 35: Anifantaki S, Prinianakis G, Vitsaksaki E, et al: Daily interruption of sedative infusions in an adult medical-surgical intensive care unit: Randomized controlled trial. J Adv Nurs 2009; 65: de Wit M, Gennings C, Jenvey WI, et al: Randomized trial comparing daily interruption of sedation and nursing-implemented sedation algorithm in medical intensive care unit patients. Crit Care 2008; 12:R MacLaren R, Plamondon JM, Ramsay KB, et al: A prospective evaluation of empiric versus protocol-based sedation and analgesia. Pharmacotherapy 2000; 20: O Connor M, Bucknall T, Manias E: International variations in outcomes from sedation protocol research: Where are we at and where do we go from here? Intensive Crit Care Nurs 2010; 26: Breen D, Karabinis A, Malbrain M, et al: Decreased duration of mechanical ventilation when comparing analgesia-based sedation using remifentanil with standard hypnotic-based sedation for up to 10 days in intensive care unit patients: A randomised trial [ISRCTN ]. Crit Care 2005; 9:R200 R Park G, Lane M, Rogers S, et al: A comparison of hypnotic and analgesic based sedation in a general intensive care unit. Br J Anaesth 2007; 98: Rozendaal FW, Spronk PE, Snellen FF, et al; UltiSAFE Investigators: Remifentanil-propofol analgo-sedation shortens duration of ventilation and length of ICU stay compared to a conventional regimen: A centre randomised, cross-over, open-label study in the Netherlands. Intensive Care Med 2009; 35: Strøm T, Martinussen T, Toft P: A protocol of no sedation for critically ill patients receiving mechanical ventilation: A randomised trial. Lancet 2010; 375: Devlin JW, Roberts RJ: Pharmacology of commonly used analgesics and sedatives in the ICU: Benzodiazepines, propofol, and opioids. Crit Care Clin 2009; 25:431 49, vii 441. Nguyen NQ, Chapman MJ, Fraser RJ, et al: The effects of sedation on gastric emptying and intra-gastric meal distribution in critical illness. Intensive Care Med 2008; 34: Strøm T, Stylsvig M, Toft P: Long-term psychological effects of a nosedation protocol in critically ill patients. Crit Care 2011; 15:R Redeker NS: Sleep in acute care settings: An integrative review. J Nurs Scholarsh 2000; 32: Fontana CJ, Pittiglio LI: Sleep deprivation among critical care patients. Crit Care Nurs Q 2010; 33: Lawson N, Thompson K, Saunders G, et al: Sound intensity and noise evaluation in a critical care unit. Am J Crit Care 2010; 19:e88 e98; quiz e Dunn H, Anderson MA, Hill PD: Nighttime lighting in intensive care units. Crit Care Nurse 2010; 30: Tembo AC, Parker V: Factors that impact on sleep in intensive care patients. Intensive Crit Care Nurs 2009; 25: Xie H, Kang J, Mills GH: Clinical review: The impact of noise on patients sleep and the effectiveness of noise reduction strategies in intensive care units. Crit Care 2009; 13: Krachman SL, D Alonzo GE, Criner GJ: Sleep in the intensive care unit. Chest 1995; 107: Sanders RD, Maze M: Contribution of sedative-hypnotic agents to delirium via modulation of the sleep pathway. Can J Anaesth 2011; 58: Weinhouse GL, Schwab RJ, Watson PL, et al: Bench-to-bedside review: Delirium in ICU patients mportance of sleep deprivation. Crit Care 2009; 13: Sanders RD: Hypothesis for the pathophysiology of delirium: Role of baseline brain network connectivity and changes in inhibitory tone. Med Hypotheses 2011; 77: Trompeo AC, Vidi Y, Locane MD, et al: Sleep disturbances in the critically ill patients: Role of delirium and sedative agents. Minerva Anestesiol 2011; 77: Figueroa-Ramos MI, Arroyo-Novoa CM, Lee KA, et al: Sleep and delirium in ICU patients: A review of mechanisms and manifestations. Intensive Care Med 2009; 35: Novaes MA, Knobel E, Bork AM, et al: Stressors in ICU: Perception of the patient, relatives and health care team. Intensive Care Med 1999; 25: Stein-Parbury J, McKinley S: Patients experiences of being in an intensive care unit: A select literature review. Am J Crit Care 2000; 9: Li SY, Wang TJ, Vivienne Wu SF, et al: Efficacy of controlling nighttime noise and activities to improve patients sleep quality in a surgical intensive care unit. J Clin Nurs 2011; 20: Dennis CM, Lee R, Woodard EK, et al: Benefits of quiet time for neuro-intensive care patients. J Neurosci Nurs 2010; 42: Tamburri LM, DiBrienza R, Zozula R, et al: Nocturnal care interactions with patients in critical care units. Am J Crit Care 2004; 13:102 12; quiz Shochat T, Martin J, Marler M, et al: Illumination levels in nursing home patients: Effects on sleep and activity rhythms. J Sleep Res 2000; 9: Gabor JY, Cooper AB, Crombach SA, et al: Contribution of the intensive care unit environment to sleep disruption in mechanically ventilated patients and healthy subjects. Am J Respir Crit Care Med 2003; 167: Cooper AB, Thornley KS, Young GB, et al: Sleep in critically ill patients requiring mechanical ventilation. Chest 2000; 117: Bosma K, Ferreyra G, Ambrogio C, et al: Patient-ventilator interaction and sleep in mechanically ventilated patients: Pressure support versus proportional assist ventilation. Crit Care Med 2007; 35: Parthasarathy S, Tobin MJ: Effect of ventilator mode on sleep quality in critically ill patients. Am J Respir Crit Care Med 2002; 166: Shaneyfelt TM, Centor RM: Reassessment of clinical practice guidelines: Go gently into that good night. JAMA 2009; 301: Clancy CM, Slutsky JR: Guidelines for guidelines: We ve come a long way. Chest 2007; 132: Devlin JW, Tanios MA, Epstein SK: Intensive care unit sedation: Waking up clinicians to the gap between research and practice. Crit Care Med 2006; 34: Brattebø G, Hofoss D, Flaatten H, et al: Effect of a scoring system and protocol for sedation on duration of patients need for ventilator support in a surgical intensive care unit. Qual Saf Health Care 2004;13: Pisani MA, Araujo KL, Van Ness PH, et al: A research algorithm to improve detection of delirium in the intensive care unit. Crit Care 2006; 10:R DePalo VA, McNicoll L, Cornell M, et al: The Rhode Island ICU collaborative: A model for reducing central line-associated bloodstream infection and ventilator-associated pneumonia statewide. Qual Saf Health Care 2010; 19: Castellanos-Ortega A, Suberviola B, García-Astudillo LA, et al: Impact of the Surviving Sepsis Campaign protocols on hospital length of stay and mortality in septic shock patients: Results of a three-year follow-up quasi-experimental study. Crit Care Med 2010; 38: Muellejans B, López A, Cross MH, et al: Remifentanil versus fentanyl for analgesia based sedation to provide patient comfort in the intensive care unit: A randomized, double-blind controlled trial [ISRCTN ]. Crit Care 2004; 8:R1 R January 2013 Volume 41 Number 1
55 Reprinted from an article originally published in English in Critical Care Medicine 2013; 41(1): by Lippincott Williams & Wilkins. Copyright 2013 by the Society of Critical Care Medicine. All rights Reserved. This translation is provided by Springer Japan KK Springer Healthcare Business Unit. Lippincott Williams & Wilkins, a business of Wolters Kluwer Health, the Society of Critical Care Medicine and its affiliates take no responsibility of the accuracy of the translation from the published English original and are not liable for any errors which may occur.
56
要望番号 ;Ⅱ 未承認薬 適応外薬の要望 ( 別添様式 1) 1. 要望内容に関連する事項 要望 者 ( 該当するものにチェックする ) 優先順位 学会 ( 学会名 ; 日本ペインクリニック学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 2 位 ( 全 4 要望中 )
 未承認薬 適応外薬の要望 ( 別添様式 1) 1. 要望内容に関連する事項 要望 者 ( 該当するものにチェックする ) 優先順位 学会 ( 学会名 ; 日本ペインクリニック学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 2 位 ( 全 4 要望中 ) 成分名 ( 一般名 ) 塩酸リドカイン 販売名 0.5%/1%/2% キシロカイン 要望する医薬品要望内容 会社名 国内関連学会
未承認薬 適応外薬の要望 ( 別添様式 1) 1. 要望内容に関連する事項 要望 者 ( 該当するものにチェックする ) 優先順位 学会 ( 学会名 ; 日本ペインクリニック学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 2 位 ( 全 4 要望中 ) 成分名 ( 一般名 ) 塩酸リドカイン 販売名 0.5%/1%/2% キシロカイン 要望する医薬品要望内容 会社名 国内関連学会
ICUにおける 鎮痛・鎮静・せん妄管理
 ICU における 鎮痛 鎮静 せん妄管理 日本大学医学部救急医学系救急集中治療医学分野古川力丸 ( こがわりきまる ) ちんせい の新しいガイドライン出ました 米国集中治療医学会 (SCCM) の鎮静ガイドライン CCM 2002; 30: 119-41 2012 年 SCCM 総会にて内容が発表 ( 流出!?) 2013 年 SCCM 総会に合わせてパブリッシュ Clinnical practice
ICU における 鎮痛 鎮静 せん妄管理 日本大学医学部救急医学系救急集中治療医学分野古川力丸 ( こがわりきまる ) ちんせい の新しいガイドライン出ました 米国集中治療医学会 (SCCM) の鎮静ガイドライン CCM 2002; 30: 119-41 2012 年 SCCM 総会にて内容が発表 ( 流出!?) 2013 年 SCCM 総会に合わせてパブリッシュ Clinnical practice
CQ1: 急性痛風性関節炎の発作 ( 痛風発作 ) に対して第一番目に使用されるお薬 ( 第一選択薬と言います ) としてコルヒチン ステロイド NSAIDs( 消炎鎮痛剤 ) があります しかし どれが最適かについては明らかではないので 検討することが必要と考えられます そこで 急性痛風性関節炎の
 [web 版資料 1 患者意見 1] この度 高尿酸血症 痛風の治療ガイドライン の第 3 回の改訂を行うことになり 鋭意取り組んでおります 診療ガイドライン作成に患者 市民の立場からの参加 ( 関与 ) が重要であることが認識され 診療ガイドライン作成では 患者の価値観 希望の一般的傾向 患者間の多様性を反映させる必要があり 何らかの方法で患者 市民の参加 ( 関与 ) に努めるようになってきております
[web 版資料 1 患者意見 1] この度 高尿酸血症 痛風の治療ガイドライン の第 3 回の改訂を行うことになり 鋭意取り組んでおります 診療ガイドライン作成に患者 市民の立場からの参加 ( 関与 ) が重要であることが認識され 診療ガイドライン作成では 患者の価値観 希望の一般的傾向 患者間の多様性を反映させる必要があり 何らかの方法で患者 市民の参加 ( 関与 ) に努めるようになってきております
スライド 1
 1/5 PMDA からの医薬品適正使用のお願い ( 独 ) 医薬品医療機器総合機構 No.6 2012 年 1 月 ラミクタール錠 ( ラモトリギン ) の重篤皮膚障害と用法 用量遵守 早期発見について ラミクタール錠は 用法 用量 を遵守せず投与した場合に皮膚障害の発現率が高くなることが示されている ( 表 1 参照 ) ため 用法 用量 を遵守することが平成 20 年 10 月の承認時より注意喚起されています
1/5 PMDA からの医薬品適正使用のお願い ( 独 ) 医薬品医療機器総合機構 No.6 2012 年 1 月 ラミクタール錠 ( ラモトリギン ) の重篤皮膚障害と用法 用量遵守 早期発見について ラミクタール錠は 用法 用量 を遵守せず投与した場合に皮膚障害の発現率が高くなることが示されている ( 表 1 参照 ) ため 用法 用量 を遵守することが平成 20 年 10 月の承認時より注意喚起されています
「手術看護を知り術前・術後の看護につなげる」
 2017 年 2 月 1 日 作成者 : 山田さおり 慢性心不全看護エキスパートナース育成コース 1. 目的江南厚生病院に通院あるいは入院している心不全患者に質の高いケアを提供できるようになるために 看護師が慢性心不全看護分野の知識や技術を習得することを目的とする 2. 対象レベルⅡ 以上で各分野の知識と技術習得を希望する者 ( 今年度は院内スタッフを対象にしています ) 期間中 80% 以上参加できる者
2017 年 2 月 1 日 作成者 : 山田さおり 慢性心不全看護エキスパートナース育成コース 1. 目的江南厚生病院に通院あるいは入院している心不全患者に質の高いケアを提供できるようになるために 看護師が慢性心不全看護分野の知識や技術を習得することを目的とする 2. 対象レベルⅡ 以上で各分野の知識と技術習得を希望する者 ( 今年度は院内スタッフを対象にしています ) 期間中 80% 以上参加できる者
抗精神病薬の併用数 単剤化率 主として統合失調症の治療薬である抗精神病薬について 1 処方中の併用数を見たものです 当院の定義 計算方法調査期間内の全ての入院患者さんが服用した抗精神病薬処方について 各処方中における抗精神病薬の併用数を調査しました 調査期間内にある患者さんの処方が複数あった場合 そ
 後発医薬品の使用割合 厚生労働省が策定した 後発医薬品のさらなる使用促進のためのロードマップ に従い 後発品医薬品 ( ジェネリック医薬品 ) 使用の促進に取り組んでいます 当院の定義 計算方法 後発医薬品の数量シェア ( 置換え率 )= 後発医薬品の数量 /( 後発医薬品のある先発医薬品 の数量 + 後発医薬品の数量 参考 厚生労働省ホームページ 後発医薬品の利用促進について http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/kenkou_iryou/iryou/kouhatu-iyaku/
後発医薬品の使用割合 厚生労働省が策定した 後発医薬品のさらなる使用促進のためのロードマップ に従い 後発品医薬品 ( ジェネリック医薬品 ) 使用の促進に取り組んでいます 当院の定義 計算方法 後発医薬品の数量シェア ( 置換え率 )= 後発医薬品の数量 /( 後発医薬品のある先発医薬品 の数量 + 後発医薬品の数量 参考 厚生労働省ホームページ 後発医薬品の利用促進について http://www.mhlw.go.jp/stf/seisakunitsuite/bunya/kenkou_iryou/iryou/kouhatu-iyaku/
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社
 オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 <その他分野 ( 消化器官用薬 解毒剤 その他 )> 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号
 資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
スライド 1
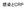 感染と CRP 感染と CRP メニュー 1.Sepsis 1 診断的 価値 Intensive Care Med 2002 2 重症度 3 治療効果 予後判定 判定 Crit Care 2011 Infection 2008 2.ICU Patients 3.VAP Crit Care 2006 Chest 2003 Crit Care Med 2002 Heart & Lung 2011
感染と CRP 感染と CRP メニュー 1.Sepsis 1 診断的 価値 Intensive Care Med 2002 2 重症度 3 治療効果 予後判定 判定 Crit Care 2011 Infection 2008 2.ICU Patients 3.VAP Crit Care 2006 Chest 2003 Crit Care Med 2002 Heart & Lung 2011
PowerPoint プレゼンテーション
 非薬理学的な介入で睡眠とせん妄は改善するのか? m 1/12 はじめに ICU の光や音は睡眠不足の原因である Li SY, Wang TJ, Vivienne Wu SF, Liang SY, Tung HH. Efficacy of controlling night-time noise and activities to improve patients sleep quality in a
非薬理学的な介入で睡眠とせん妄は改善するのか? m 1/12 はじめに ICU の光や音は睡眠不足の原因である Li SY, Wang TJ, Vivienne Wu SF, Liang SY, Tung HH. Efficacy of controlling night-time noise and activities to improve patients sleep quality in a
2015 年 11 月 5 日 乳酸菌発酵果汁飲料の継続摂取がアトピー性皮膚炎症状を改善 株式会社ヤクルト本社 ( 社長根岸孝成 ) では アトピー性皮膚炎患者を対象に 乳酸菌 ラクトバチルスプランタルム YIT 0132 ( 以下 乳酸菌 LP0132) を含む発酵果汁飲料 ( 以下 乳酸菌発酵果
 2015 年 11 月 5 日 乳酸菌発酵果汁飲料の継続摂取がアトピー性皮膚炎症状を改善 株式会社ヤクルト本社 ( 社長根岸孝成 ) では アトピー性皮膚炎患者を対象に 乳酸菌 ラクトバチルスプランタルム YIT 0132 ( 以下 乳酸菌 LP0132) を含む発酵果汁飲料 ( 以下 乳酸菌発酵果汁飲料 ) の飲用試験を実施した結果 アトピー性皮膚炎症状を改善する効果が確認されました なお 本研究成果は
2015 年 11 月 5 日 乳酸菌発酵果汁飲料の継続摂取がアトピー性皮膚炎症状を改善 株式会社ヤクルト本社 ( 社長根岸孝成 ) では アトピー性皮膚炎患者を対象に 乳酸菌 ラクトバチルスプランタルム YIT 0132 ( 以下 乳酸菌 LP0132) を含む発酵果汁飲料 ( 以下 乳酸菌発酵果汁飲料 ) の飲用試験を実施した結果 アトピー性皮膚炎症状を改善する効果が確認されました なお 本研究成果は
3. 安全性本治験において治験薬が投与された 48 例中 1 例 (14 件 ) に有害事象が認められた いずれの有害事象も治験薬との関連性は あり と判定されたが いずれも軽度 で処置の必要はなく 追跡検査で回復を確認した また 死亡 その他の重篤な有害事象が認められなか ったことから 安全性に問
 フェキソフェナジン塩酸塩錠 6mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにフェキソフェナジン塩酸塩は 第二世代抗ヒスタミン薬の一つであり 抗原抗体反応に伴って起こる肥満細胞からのヒスタミンなどのケミカルメディエーターの遊離を抑制すると共に ヒスタミンの H1 作用に拮抗することにより アレルギー症状を緩和する 今回 フェキソフェナジン塩酸塩錠 6mg
フェキソフェナジン塩酸塩錠 6mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにフェキソフェナジン塩酸塩は 第二世代抗ヒスタミン薬の一つであり 抗原抗体反応に伴って起こる肥満細胞からのヒスタミンなどのケミカルメディエーターの遊離を抑制すると共に ヒスタミンの H1 作用に拮抗することにより アレルギー症状を緩和する 今回 フェキソフェナジン塩酸塩錠 6mg
Microsoft Word - ★9. Preop opioid treatment.Schug-EE.docx
 報告書 No. 9 術前にオピオイドを使 している患者の術後疼痛管理 以下の理由で 術前にオピオイドを服 して 術を受ける患者が増えている がんに関連した疼痛 がん性慢性疼痛 ( 例 : 変形性関節症などによるもの ) 急性増悪を繰り返す痛み ( 例 : 鎌状 球症 膵炎 ) 物質使 障害に対するオピオイド維持療法 違法で治療されていない物質使 障害 ( オピオイド鎮痛薬の不適切な使 ) 外科 術や外傷後に
報告書 No. 9 術前にオピオイドを使 している患者の術後疼痛管理 以下の理由で 術前にオピオイドを服 して 術を受ける患者が増えている がんに関連した疼痛 がん性慢性疼痛 ( 例 : 変形性関節症などによるもの ) 急性増悪を繰り返す痛み ( 例 : 鎌状 球症 膵炎 ) 物質使 障害に対するオピオイド維持療法 違法で治療されていない物質使 障害 ( オピオイド鎮痛薬の不適切な使 ) 外科 術や外傷後に
第1回肝炎診療ガイドライン作成委員会議事要旨(案)
 資料 1 C 型慢性肝疾患 ( ゲノタイプ 1 型 2 型 ) に対する治療フローチャート ダクラタスビル + アスナプレビル併用療法 ソホスブビル + リバビリン併用療法 ソホスブビル / レジパスビル併用療法 オムビタスビル / パリタプレビル / リトナビル併用療法 (± リバビリン ) エルバスビル + グラゾプレビル併用療法 ダクラタスビル / アスナプレビル / ベクラブビル 3 剤併用療法による抗ウイルス治療に当たっては
資料 1 C 型慢性肝疾患 ( ゲノタイプ 1 型 2 型 ) に対する治療フローチャート ダクラタスビル + アスナプレビル併用療法 ソホスブビル + リバビリン併用療法 ソホスブビル / レジパスビル併用療法 オムビタスビル / パリタプレビル / リトナビル併用療法 (± リバビリン ) エルバスビル + グラゾプレビル併用療法 ダクラタスビル / アスナプレビル / ベクラブビル 3 剤併用療法による抗ウイルス治療に当たっては
Microsoft PowerPoint - 薬物療法専門薬剤師制度_症例サマリー例_HP掲載用.pptx
 薬物療法専門薬剤師の申請 及び症例サマリーに関する Q&A 注意 : 本 Q&A の番号は独立したものであり 医療薬学会 HP にある 薬物療法専門薬剤師制度の Q&A の番号と関連性はありません 薬物療法専門薬剤師認定制度の目的 幅広い領域の薬物療法 高い水準の知識 技術及び臨床能力を駆使 他の医療従事者と協働して薬物療法を実践 患者に最大限の利益をもたらす 国民の保健 医療 福祉に貢献することを目的
薬物療法専門薬剤師の申請 及び症例サマリーに関する Q&A 注意 : 本 Q&A の番号は独立したものであり 医療薬学会 HP にある 薬物療法専門薬剤師制度の Q&A の番号と関連性はありません 薬物療法専門薬剤師認定制度の目的 幅広い領域の薬物療法 高い水準の知識 技術及び臨床能力を駆使 他の医療従事者と協働して薬物療法を実践 患者に最大限の利益をもたらす 国民の保健 医療 福祉に貢献することを目的
PowerPoint プレゼンテーション
 Palliative care Emphasis program on symptom management and Assessment for Continuous medical Education 呼吸困難 臨床疑問 評価 呼吸困難はどうやって評価したらよいか? 治療 くすりは何を使ったらよいか? ケア 説明 どのように療養の環境を整えたらよいか? メッセージ 呼吸困難は主観的な症状である
Palliative care Emphasis program on symptom management and Assessment for Continuous medical Education 呼吸困難 臨床疑問 評価 呼吸困難はどうやって評価したらよいか? 治療 くすりは何を使ったらよいか? ケア 説明 どのように療養の環境を整えたらよいか? メッセージ 呼吸困難は主観的な症状である
診療ガイドラインのためのGRADEシステム 第3版
 2 1.1 診療ガイドラインとは 1.1-1 診療ガイドラインの定義 診療ガイドライン (clinical practice guideline) i は ヘルスケア関連の診断や治療に焦点を当てた医療介入に関する推奨事項を含む成果物であり 推奨は 医療提供者と医療受給者が最良のヘルスケアに関する決断を支援する声明である 米国医学研究所 (Institute of Medicine: IOM) による診療ガイドラインの定義は以下である
2 1.1 診療ガイドラインとは 1.1-1 診療ガイドラインの定義 診療ガイドライン (clinical practice guideline) i は ヘルスケア関連の診断や治療に焦点を当てた医療介入に関する推奨事項を含む成果物であり 推奨は 医療提供者と医療受給者が最良のヘルスケアに関する決断を支援する声明である 米国医学研究所 (Institute of Medicine: IOM) による診療ガイドラインの定義は以下である
症例報告書の記入における注意点 1 必須ではない項目 データ 斜線を引くこと 未取得 / 未測定の項目 2 血圧平均値 小数点以下は切り捨てとする 3 治験薬服薬状況 前回来院 今回来院までの服薬状況を記載する服薬無しの場合は 1 日投与量を 0 錠 とし 0 錠となった日付を特定すること < 演習
 ABC-123 臨床試験進行または再発胃癌患者に対するプラセボを対照薬とした無作為化二重盲検比較試験症例報告書 治験実施計画書番号 P123-31-V01 被験者識別コード 割付番号 治験実施医療機関名 ご自分の医療機関 お名前を記載して下さい 症例報告書記載者名 症例報告書記載者名 治験責任医師 ( 署名又は記名 押印 ) 治験責任医師記載内容確認完了日 印 2 0 年 月 日 1 症例報告書の記入における注意点
ABC-123 臨床試験進行または再発胃癌患者に対するプラセボを対照薬とした無作為化二重盲検比較試験症例報告書 治験実施計画書番号 P123-31-V01 被験者識別コード 割付番号 治験実施医療機関名 ご自分の医療機関 お名前を記載して下さい 症例報告書記載者名 症例報告書記載者名 治験責任医師 ( 署名又は記名 押印 ) 治験責任医師記載内容確認完了日 印 2 0 年 月 日 1 症例報告書の記入における注意点
PowerPoint プレゼンテーション
 オピオイド / 緩和医療 2012 年 3 月 21 日 主催 : 福岡大学病院腫瘍センター 共催 : 福岡市薬剤師会 福岡地区勤務薬剤師会 緩和医療とは 生命を脅かす疾患に伴う問題に直面する患者と家族に対し 疼痛や身体的 心理社会的 スピリチュアルな問題を 早期から正確に評価し解決することにより 苦痛の予防と軽減を図り 生活の質 (QOL) を向上させるためのアプローチ (WHO, 2002 年
オピオイド / 緩和医療 2012 年 3 月 21 日 主催 : 福岡大学病院腫瘍センター 共催 : 福岡市薬剤師会 福岡地区勤務薬剤師会 緩和医療とは 生命を脅かす疾患に伴う問題に直面する患者と家族に対し 疼痛や身体的 心理社会的 スピリチュアルな問題を 早期から正確に評価し解決することにより 苦痛の予防と軽減を図り 生活の質 (QOL) を向上させるためのアプローチ (WHO, 2002 年
1)~ 2) 3) 近位筋脱力 CK(CPK) 高値 炎症を伴わない筋線維の壊死 抗 HMG-CoA 還元酵素 (HMGCR) 抗体陽性等を特徴とする免疫性壊死性ミオパチーがあらわれ 投与中止後も持続する例が報告されているので 患者の状態を十分に観察すること なお 免疫抑制剤投与により改善がみられた
 適正使用に欠かせない情報です 必ずお読みください 使用上の注意 改訂のお知らせ 注 1) 処方箋医薬品 ATORVASTATIN TABLETS AMALUET COMBINATION TABLETS 注 1) 処方箋医薬品 PRAVASTATIN SODIUM TABLETS 注 1) 注意 - 医師等の処方箋により使用すること PITAVASTATIN CALCIUM TABLETS 2016
適正使用に欠かせない情報です 必ずお読みください 使用上の注意 改訂のお知らせ 注 1) 処方箋医薬品 ATORVASTATIN TABLETS AMALUET COMBINATION TABLETS 注 1) 処方箋医薬品 PRAVASTATIN SODIUM TABLETS 注 1) 注意 - 医師等の処方箋により使用すること PITAVASTATIN CALCIUM TABLETS 2016
( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 教授 花房俊昭 宮村昌利 副査副査 教授教授 朝 日 通 雄 勝 間 田 敬 弘 副査 教授 森田大 主論文題名 Effects of Acarbose on the Acceleration of Postprandial
 ( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 花房俊昭 宮村昌利 副査副査 朝 日 通 雄 勝 間 田 敬 弘 副査 森田大 主論文題名 Effects of Acarbose on the Acceleration of Postprandial Hyperglycemia-Induced Pathological Changes Induced by Intermittent
( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 花房俊昭 宮村昌利 副査副査 朝 日 通 雄 勝 間 田 敬 弘 副査 森田大 主論文題名 Effects of Acarbose on the Acceleration of Postprandial Hyperglycemia-Induced Pathological Changes Induced by Intermittent
抗菌薬の殺菌作用抗菌薬の殺菌作用には濃度依存性と時間依存性の 2 種類があり 抗菌薬の効果および用法 用量の設定に大きな影響を与えます 濃度依存性タイプでは 濃度を高めると濃度依存的に殺菌作用を示します 濃度依存性タイプの抗菌薬としては キノロン系薬やアミノ配糖体系薬が挙げられます 一方 時間依存性
 2012 年 1 月 4 日放送 抗菌薬の PK-PD 愛知医科大学大学院感染制御学教授三鴨廣繁抗菌薬の PK-PD とは薬物動態を解析することにより抗菌薬の有効性と安全性を評価する考え方は アミノ配糖体系薬などの副作用を回避するための薬物血中濃度モニタリング (TDM) の分野で発達してきました 近年では 耐性菌の増加 コンプロマイズド ホストの増加 新規抗菌薬の開発の停滞などもあり 現存の抗菌薬をいかに科学的に使用するかが重要な課題となっており
2012 年 1 月 4 日放送 抗菌薬の PK-PD 愛知医科大学大学院感染制御学教授三鴨廣繁抗菌薬の PK-PD とは薬物動態を解析することにより抗菌薬の有効性と安全性を評価する考え方は アミノ配糖体系薬などの副作用を回避するための薬物血中濃度モニタリング (TDM) の分野で発達してきました 近年では 耐性菌の増加 コンプロマイズド ホストの増加 新規抗菌薬の開発の停滞などもあり 現存の抗菌薬をいかに科学的に使用するかが重要な課題となっており
PowerPoint プレゼンテーション
 鎮静と譫妄の評価 徳島大学病院救急集中治療部 大藤純 集中治療室ストレスが多い 照明 アラーム音 医療機器の雑音医療従事者の会話 チューブ刺激 ICU のストレスの原因 環境因子 騒音 ( アラーム 雑談 ) 照明 (24 時間連続 ) 同じ環境 見慣れない器械 ライン など 医原性因子 全身性炎症反応疼痛 気管チューブ刺激人工呼吸器との不同調低酸素血症心不全 など 非薬物的アプローチ 不穏 譫妄
鎮静と譫妄の評価 徳島大学病院救急集中治療部 大藤純 集中治療室ストレスが多い 照明 アラーム音 医療機器の雑音医療従事者の会話 チューブ刺激 ICU のストレスの原因 環境因子 騒音 ( アラーム 雑談 ) 照明 (24 時間連続 ) 同じ環境 見慣れない器械 ライン など 医原性因子 全身性炎症反応疼痛 気管チューブ刺激人工呼吸器との不同調低酸素血症心不全 など 非薬物的アプローチ 不穏 譫妄
減量・コース投与期間短縮の基準
 用法 用量 通常 成人には初回投与量 (1 回量 ) を体表面積に合せて次の基準量とし 朝食後および夕食後の 1 日 2 回 28 日間連日経口投与し その後 14 日間休薬する これを 1 クールとして投与を繰り返す ただし 本剤の投与によると判断される臨床検査値異常 ( 血液検査 肝 腎機能検査 ) および消化器症状が発現せず 安全性に問題がない場合には休薬を短縮できるが その場合でも少なくとも
用法 用量 通常 成人には初回投与量 (1 回量 ) を体表面積に合せて次の基準量とし 朝食後および夕食後の 1 日 2 回 28 日間連日経口投与し その後 14 日間休薬する これを 1 クールとして投与を繰り返す ただし 本剤の投与によると判断される臨床検査値異常 ( 血液検査 肝 腎機能検査 ) および消化器症状が発現せず 安全性に問題がない場合には休薬を短縮できるが その場合でも少なくとも
未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名要望された医薬品要望内容 CSL ベーリング株式会社要望番号 Ⅱ-175 成分名 (10%) 人免疫グロブリン G ( 一般名 ) プリビジェン (Privigen) 販売名 未承認薬 適応 外薬の分類
 未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名要望された医薬品要望内容 CSL ベーリング株式会社要望番号 Ⅱ-175 成分名 (10%) 人免疫グロブリン G ( 一般名 ) プリビジェン (Privigen) 販売名 未承認薬 適応 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) ( 要望されたについて記載する
未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名要望された医薬品要望内容 CSL ベーリング株式会社要望番号 Ⅱ-175 成分名 (10%) 人免疫グロブリン G ( 一般名 ) プリビジェン (Privigen) 販売名 未承認薬 適応 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) ( 要望されたについて記載する
糖尿病診療における早期からの厳格な血糖コントロールの重要性
 2018 年 12 月 19 日放送 急性胆管炎 胆嚢炎診療ガイドライン 2018 国際医療福祉大学消化器外科教授吉田雅博ガイドラインの作成経過急性胆道感染症 ( 急性胆管炎 急性胆囊炎 ) は急性期に適切な対処が必要であり 特に 急性胆管炎 なかでも重症急性胆管炎では急性期に適切な診療が行われないと早期に死亡に至ることもあります これに対し 2005 年に出版されたガイドライン初版によって世界に向けて診断基準
2018 年 12 月 19 日放送 急性胆管炎 胆嚢炎診療ガイドライン 2018 国際医療福祉大学消化器外科教授吉田雅博ガイドラインの作成経過急性胆道感染症 ( 急性胆管炎 急性胆囊炎 ) は急性期に適切な対処が必要であり 特に 急性胆管炎 なかでも重症急性胆管炎では急性期に適切な診療が行われないと早期に死亡に至ることもあります これに対し 2005 年に出版されたガイドライン初版によって世界に向けて診断基準
P001~017 1-1.indd
 1 クリアランスギャップの理論 透析量の質的管理法 クリアランスギャップ の基礎 はじめに標準化透析量 : Kt /V は, 尿素窒素クリアランス : K(mL/min), 透析時間 : t(min),urea 分布容積 体液量 (ml) から構成される指標であり, 慢性維持透析患者の長期予後規定因子であることが広く認識されている 1-3). しかし, 一方で Kt /V はバスキュラーアクセス (VA)
1 クリアランスギャップの理論 透析量の質的管理法 クリアランスギャップ の基礎 はじめに標準化透析量 : Kt /V は, 尿素窒素クリアランス : K(mL/min), 透析時間 : t(min),urea 分布容積 体液量 (ml) から構成される指標であり, 慢性維持透析患者の長期予後規定因子であることが広く認識されている 1-3). しかし, 一方で Kt /V はバスキュラーアクセス (VA)
<4D F736F F D2089BB8A7797C C B B835888E790AC8C7689E6>
 2012 年 4 月更新作成者 : 宇根底亜希子 化学療法看護エキスパートナース育成計画 1. 目的江南厚生病院に通院あるいは入院しているがん患者に質の高いケアを提供できるようになるために 看護師が化学療法分野の知識や技術を習得することを目的とする 2. 対象者 1 ) レベル Ⅱ 以上で各分野の知識と技術習得を希望する者 2 ) 期間中 80% 以上参加できる者 3. 教育期間 時間間 1 年間の継続教育とする
2012 年 4 月更新作成者 : 宇根底亜希子 化学療法看護エキスパートナース育成計画 1. 目的江南厚生病院に通院あるいは入院しているがん患者に質の高いケアを提供できるようになるために 看護師が化学療法分野の知識や技術を習得することを目的とする 2. 対象者 1 ) レベル Ⅱ 以上で各分野の知識と技術習得を希望する者 2 ) 期間中 80% 以上参加できる者 3. 教育期間 時間間 1 年間の継続教育とする
「手術看護を知り術前・術後の看護につなげる」
 周術期看護エキスパートナース育成計画 作成者 : 高橋育代 1. 目的江南厚生病院に通院あるいは入院している手術を受ける患者に質の高いケアを提供できるようになるために 看護師が周術期看護分野の知識や技術を習得することを目的とする 2. 対象者 1) レベル Ⅱ 以上で手術看護分野の知識と技術習得を希望する者 2) 期間中 80% 以上参加できる者 3. 教育期間 時間 1 年間の継続教育とする 10
周術期看護エキスパートナース育成計画 作成者 : 高橋育代 1. 目的江南厚生病院に通院あるいは入院している手術を受ける患者に質の高いケアを提供できるようになるために 看護師が周術期看護分野の知識や技術を習得することを目的とする 2. 対象者 1) レベル Ⅱ 以上で手術看護分野の知識と技術習得を希望する者 2) 期間中 80% 以上参加できる者 3. 教育期間 時間 1 年間の継続教育とする 10
スライド 1
 薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
臨床試験の実施計画書作成の手引き
 臨床試験実施計画書 汗中乳酸測定システムを用いた 組織酸素代謝評価の検討 聖マリアンナ医科大学救急医学 神奈川県川崎市宮前区菅生 2-16-1 電話 :044-977-8111( 医局内線 3931) 医局 FAX:044-979-1522 責任医師森澤健一郎 [email protected] 臨床試験実施予定期間 : 承認後 ~ 2018 年 6 月 30 日まで 作成日 :2016 年
臨床試験実施計画書 汗中乳酸測定システムを用いた 組織酸素代謝評価の検討 聖マリアンナ医科大学救急医学 神奈川県川崎市宮前区菅生 2-16-1 電話 :044-977-8111( 医局内線 3931) 医局 FAX:044-979-1522 責任医師森澤健一郎 [email protected] 臨床試験実施予定期間 : 承認後 ~ 2018 年 6 月 30 日まで 作成日 :2016 年
認定看護師教育基準カリキュラム
 認定看護師教育基準カリキュラム 分野 : 慢性心不全看護平成 28 年 3 月改正 ( 目的 ) 1. 安定期 増悪期 人生の最終段階にある慢性心不全患者とその家族に対し 熟練した看護技術を用いて水準の高い看護実践ができる能力を育成する 2. 安定期 増悪期 人生の最終段階にある慢性心不全患者とその家族の看護において 看護実践を通して他の看護職者に対して指導ができる能力を育成する 3. 安定期 増悪期
認定看護師教育基準カリキュラム 分野 : 慢性心不全看護平成 28 年 3 月改正 ( 目的 ) 1. 安定期 増悪期 人生の最終段階にある慢性心不全患者とその家族に対し 熟練した看護技術を用いて水準の高い看護実践ができる能力を育成する 2. 安定期 増悪期 人生の最終段階にある慢性心不全患者とその家族の看護において 看護実践を通して他の看護職者に対して指導ができる能力を育成する 3. 安定期 増悪期
当院人工透析室における看護必要度調査 佐藤幸子 木村房子 大館市立総合病院人工透析室 The Evaluation of the Grade of Nursing Requirement in Hemodialysis Patients in Odate Municipal Hospital < 諸
 当院人工透析室における看護必要度調査 佐藤幸子 木村房子 大館市立総合病院人工透析室 The Evaluation of the Grade of Nursing Requirement in Hemodialysis Patients in Odate Municipal Hospital < 諸言 > 近年 透析患者数は毎年 1 万人ずつ増加しているといわれており 2008 年度におけるわが国の透析患者数は
当院人工透析室における看護必要度調査 佐藤幸子 木村房子 大館市立総合病院人工透析室 The Evaluation of the Grade of Nursing Requirement in Hemodialysis Patients in Odate Municipal Hospital < 諸言 > 近年 透析患者数は毎年 1 万人ずつ増加しているといわれており 2008 年度におけるわが国の透析患者数は
日本臨床麻酔学会 vol.30
 842 Vol.30 No.5/Sep. 2010 術後管理における PCA の上手な使い方 PCA ポンプの特徴と使い方 CADD Legacy ( スミスメディカル社 ) * 大友重明 * 笹川智貴 * 国沢卓之 [ 要旨 ] 硬膜外麻酔の代替鎮痛法の一つとして,intravenous patient-controlled analgesia(iv-pca) は非常に有用な手段である. そして,IV-PCA
842 Vol.30 No.5/Sep. 2010 術後管理における PCA の上手な使い方 PCA ポンプの特徴と使い方 CADD Legacy ( スミスメディカル社 ) * 大友重明 * 笹川智貴 * 国沢卓之 [ 要旨 ] 硬膜外麻酔の代替鎮痛法の一つとして,intravenous patient-controlled analgesia(iv-pca) は非常に有用な手段である. そして,IV-PCA
ータについては Table 3 に示した 両製剤とも投与後血漿中ロスバスタチン濃度が上昇し 試験製剤で 4.7±.7 時間 標準製剤で 4.6±1. 時間に Tmaxに達した また Cmaxは試験製剤で 6.3±3.13 標準製剤で 6.8±2.49 であった AUCt は試験製剤で 62.24±2
 ロスバスタチン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロスバスタチンは HMG-CoA 還元酵素を競合的に阻害することにより HMG-CoA のメバロン酸への変更を減少させ コレステロール生合成における早期の律速段階を抑制する高コレステロール血症治療剤である 今回 ロスバスタチン錠 mg TCK とクレストール 錠 mg の生物学的同等性を検討するため
ロスバスタチン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロスバスタチンは HMG-CoA 還元酵素を競合的に阻害することにより HMG-CoA のメバロン酸への変更を減少させ コレステロール生合成における早期の律速段階を抑制する高コレステロール血症治療剤である 今回 ロスバスタチン錠 mg TCK とクレストール 錠 mg の生物学的同等性を検討するため
H29_第40集_大和証券_研究業績_C本文_p indd
 慢性腎臓病 (CKD) における危険因子としての食後高血糖の検討 独立行政法人国立病院機構千葉東病院臨床研究部 糖尿病研究室長関直人 はじめに 1. 研究の背景慢性腎臓病 (CKD) は 動脈硬化 腎機能低下 末期腎不全 心血管イベントなどの危険因子であることが報告されている (1) 一方で食後高血糖もまた 動脈硬化 心血管イベントの危険因子であることが報告されている (2) 食後高血糖の検出には持続血糖モニタリング
慢性腎臓病 (CKD) における危険因子としての食後高血糖の検討 独立行政法人国立病院機構千葉東病院臨床研究部 糖尿病研究室長関直人 はじめに 1. 研究の背景慢性腎臓病 (CKD) は 動脈硬化 腎機能低下 末期腎不全 心血管イベントなどの危険因子であることが報告されている (1) 一方で食後高血糖もまた 動脈硬化 心血管イベントの危険因子であることが報告されている (2) 食後高血糖の検出には持続血糖モニタリング
ピルシカイニド塩酸塩カプセル 50mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにピルジカイニド塩酸塩水和物は Vaughan Williams らの分類のクラスⅠCに属し 心筋の Na チャンネル抑制作用により抗不整脈作用を示す また 消化管から速やかに
 ピルシカイニド塩酸塩カプセル 50mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにピルジカイニド塩酸塩水和物は Vaughan Williams らの分類のクラスⅠCに属し 心筋の Na チャンネル抑制作用により抗不整脈作用を示す また 消化管から速やかに吸収され 体内でもほとんど代謝を受けない頻脈性不整脈 ( 心室性 ) に優れた有効性をもつ不整脈治療剤である
ピルシカイニド塩酸塩カプセル 50mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにピルジカイニド塩酸塩水和物は Vaughan Williams らの分類のクラスⅠCに属し 心筋の Na チャンネル抑制作用により抗不整脈作用を示す また 消化管から速やかに吸収され 体内でもほとんど代謝を受けない頻脈性不整脈 ( 心室性 ) に優れた有効性をもつ不整脈治療剤である
めまい
 Clinical Question 2016 年 12 月 12 日 High-flow nasal cannula oxygen (HFNC: ネーザルハイフロー ) 藤田保健衛生大学救急総合内科作成者 : 新垣大智監修 : 植西憲達 神宮司成弘分野 : 呼吸器テーマ : 治療 ある日の救急外来 症例 :80 歳 女性 病歴 ; 昨日朝から湿性咳嗽と膿性痰あり 夕方から 38 の発熱 今朝から呼吸困難の訴えあり
Clinical Question 2016 年 12 月 12 日 High-flow nasal cannula oxygen (HFNC: ネーザルハイフロー ) 藤田保健衛生大学救急総合内科作成者 : 新垣大智監修 : 植西憲達 神宮司成弘分野 : 呼吸器テーマ : 治療 ある日の救急外来 症例 :80 歳 女性 病歴 ; 昨日朝から湿性咳嗽と膿性痰あり 夕方から 38 の発熱 今朝から呼吸困難の訴えあり
られる 糖尿病を合併した高血圧の治療の薬物治療の第一選択薬はアンジオテンシン変換酵素 (ACE) 阻害薬とアンジオテンシン II 受容体拮抗薬 (ARB) である このクラスの薬剤は単なる降圧効果のみならず 様々な臓器保護作用を有しているが ACE 阻害薬や ARB のプラセボ比較試験で糖尿病の新規
 論文の内容の要旨 論文題目アンジオテンシン受容体拮抗薬テルミサルタンの メタボリックシンドロームに対する効果の検討 指導教員門脇孝教授 東京大学大学院医学系研究科 平成 19 年 4 月入学 医学博士課程 内科学専攻 氏名廣瀬理沙 要旨 背景 目的 わが国の死因の第二位と第三位を占める心筋梗塞や脳梗塞などの心血管疾患を引き起こす基盤となる病態として 過剰なエネルギー摂取と運動不足などの生活習慣により内臓脂肪が蓄積する内臓脂肪型肥満を中心に
論文の内容の要旨 論文題目アンジオテンシン受容体拮抗薬テルミサルタンの メタボリックシンドロームに対する効果の検討 指導教員門脇孝教授 東京大学大学院医学系研究科 平成 19 年 4 月入学 医学博士課程 内科学専攻 氏名廣瀬理沙 要旨 背景 目的 わが国の死因の第二位と第三位を占める心筋梗塞や脳梗塞などの心血管疾患を引き起こす基盤となる病態として 過剰なエネルギー摂取と運動不足などの生活習慣により内臓脂肪が蓄積する内臓脂肪型肥満を中心に
<4D F736F F D204A4F544E D8E8094BB92E88B4C985E8F DCE88C88FE3816A >
 法的脳死判定記録書 (の者に脳死判定を行う場合 ) この記録書では 法的脳死判定を実施しながら 下線部に必要事項を記入し 該当するチェックボックス ( ) に 印を入れること ができます 省令第 5 条第 1 項 脳死判定を受けた者 氏名 住所 性別 生年月日年月日生歳 である 脳死判定を承諾した家族 代表者氏名 住所 脳死判定を受けた者との続柄 脳死判定を受けた者及び家族の意思 ( ア~ウのいずれか
法的脳死判定記録書 (の者に脳死判定を行う場合 ) この記録書では 法的脳死判定を実施しながら 下線部に必要事項を記入し 該当するチェックボックス ( ) に 印を入れること ができます 省令第 5 条第 1 項 脳死判定を受けた者 氏名 住所 性別 生年月日年月日生歳 である 脳死判定を承諾した家族 代表者氏名 住所 脳死判定を受けた者との続柄 脳死判定を受けた者及び家族の意思 ( ア~ウのいずれか
Microsoft Word - ①【修正】B型肝炎 ワクチンにおける副反応の報告基準について
 資料 1 B 型肝炎ワクチンの副反応報告基準について 予防接種法における副反応報告制度について 制度の趣旨副反応報告制度は 予防接種後に生じる種々の身体的反応や副反応が疑われる症状等について情報を収集し ワクチンの安全性について管理 検討を行うことで 広く国民に情報を提供すること及び今後の予防接種行政の推進に資することを目的としている 報告の義務 予防接種法第 12 条 1 項 ( 参考資料 1)
資料 1 B 型肝炎ワクチンの副反応報告基準について 予防接種法における副反応報告制度について 制度の趣旨副反応報告制度は 予防接種後に生じる種々の身体的反応や副反応が疑われる症状等について情報を収集し ワクチンの安全性について管理 検討を行うことで 広く国民に情報を提供すること及び今後の予防接種行政の推進に資することを目的としている 報告の義務 予防接種法第 12 条 1 項 ( 参考資料 1)
というもので これまで十数年にわたって使用されてきたものになります さらに 敗血症 sepsis に中でも臓器障害を伴うものを重症敗血症 severe sepsis 適切な輸液を行っても血圧低下が持続する重症敗血症 severe sepsis を敗血症性ショック septic shock と定義して
 2016 年 8 月 10 日放送 新しい敗血症の定義 慶應義塾大学救急医学教授佐々木淳一はじめに敗血症 英語では sepsis の定義が 2001 年以来 15 年ぶりに大きく改定されました 2016 年 2 月 22 日 第 45 回米国集中治療医学会 (SCCM) において 敗血症および敗血症性ショックの国際コンセンサス定義第 3 版 (Sepsis-3) が発表され 敗血症は 感染症に対する制御不能な宿主反応に起因した生命を脅かす臓器障害
2016 年 8 月 10 日放送 新しい敗血症の定義 慶應義塾大学救急医学教授佐々木淳一はじめに敗血症 英語では sepsis の定義が 2001 年以来 15 年ぶりに大きく改定されました 2016 年 2 月 22 日 第 45 回米国集中治療医学会 (SCCM) において 敗血症および敗血症性ショックの国際コンセンサス定義第 3 版 (Sepsis-3) が発表され 敗血症は 感染症に対する制御不能な宿主反応に起因した生命を脅かす臓器障害
スライド 1
 1. 血液の中に存在する脂質 脂質異常症で重要となる物質トリグリセリド ( 中性脂肪 :TG) 動脈硬化に深く関与する 脂質の種類 トリグリセリド :TG ( 中性脂肪 ) リン脂質 遊離脂肪酸 特徴 細胞の構成成分 ホルモンやビタミン 胆汁酸の原料 動脈硬化の原因となる 体や心臓を動かすエネルギーとして利用 皮下脂肪として貯蔵 動脈硬化の原因となる 細胞膜の構成成分 トリグリセリド ( 中性脂肪
1. 血液の中に存在する脂質 脂質異常症で重要となる物質トリグリセリド ( 中性脂肪 :TG) 動脈硬化に深く関与する 脂質の種類 トリグリセリド :TG ( 中性脂肪 ) リン脂質 遊離脂肪酸 特徴 細胞の構成成分 ホルモンやビタミン 胆汁酸の原料 動脈硬化の原因となる 体や心臓を動かすエネルギーとして利用 皮下脂肪として貯蔵 動脈硬化の原因となる 細胞膜の構成成分 トリグリセリド ( 中性脂肪
Microsoft Word - 博士論文概要.docx
 [ 博士論文概要 ] 平成 25 年度 金多賢 筑波大学大学院人間総合科学研究科 感性認知脳科学専攻 1. 背景と目的映像メディアは, 情報伝達における効果的なメディアの一つでありながら, 容易に感情喚起が可能な媒体である. 誰でも簡単に映像を配信できるメディア社会への変化にともない, 見る人の状態が配慮されていない映像が氾濫することで見る人の不快な感情を生起させる問題が生じている. したがって,
[ 博士論文概要 ] 平成 25 年度 金多賢 筑波大学大学院人間総合科学研究科 感性認知脳科学専攻 1. 背景と目的映像メディアは, 情報伝達における効果的なメディアの一つでありながら, 容易に感情喚起が可能な媒体である. 誰でも簡単に映像を配信できるメディア社会への変化にともない, 見る人の状態が配慮されていない映像が氾濫することで見る人の不快な感情を生起させる問題が生じている. したがって,
博士論文 考え続ける義務感と反復思考の役割に注目した 診断横断的なメタ認知モデルの構築 ( 要約 ) 平成 30 年 3 月 広島大学大学院総合科学研究科 向井秀文
 博士論文 考え続ける義務感と反復思考の役割に注目した 診断横断的なメタ認知モデルの構築 ( 要約 ) 平成 30 年 3 月 広島大学大学院総合科学研究科 向井秀文 目次 はじめに第一章診断横断的なメタ認知モデルに関する研究動向 1. 診断横断的な観点から心理的症状のメカニズムを検討する重要性 2 2. 反復思考 (RNT) 研究の歴史的経緯 4 3. RNT の高まりを予測することが期待されるメタ認知モデル
博士論文 考え続ける義務感と反復思考の役割に注目した 診断横断的なメタ認知モデルの構築 ( 要約 ) 平成 30 年 3 月 広島大学大学院総合科学研究科 向井秀文 目次 はじめに第一章診断横断的なメタ認知モデルに関する研究動向 1. 診断横断的な観点から心理的症状のメカニズムを検討する重要性 2 2. 反復思考 (RNT) 研究の歴史的経緯 4 3. RNT の高まりを予測することが期待されるメタ認知モデル
図 1 緩和ケアチーム情報共有データベースの患者情報画面 1 患者氏名, 生年月日, 性別, 緩和ケアチームへの依頼内容について,2 入退院記録, 3カンファレンス ラウンド実施一覧,4 問題点のリスト,5 介入内容の記録. 図 2 緩和ケアチームカンファレンス ラウンドによる患者評価入力画面 (
 2015; 10(2): 901 5 活動報告 緩和ケアチームデータベースの改良に向けた取り組み 渡邊裕之 1,4), 江藤美和子 2,4) 3,4), 山﨑圭一 1 2 3 4 受付日 2014 年 9 月 10 日 / 改訂日 2015 年 1 月 29 日 / 受理日 2015 年 2 月 3 日 2011 年に, ベルランド総合病院緩和ケアチーム ( 以下,PCT) で構築した PCT 情報共有データベース
2015; 10(2): 901 5 活動報告 緩和ケアチームデータベースの改良に向けた取り組み 渡邊裕之 1,4), 江藤美和子 2,4) 3,4), 山﨑圭一 1 2 3 4 受付日 2014 年 9 月 10 日 / 改訂日 2015 年 1 月 29 日 / 受理日 2015 年 2 月 3 日 2011 年に, ベルランド総合病院緩和ケアチーム ( 以下,PCT) で構築した PCT 情報共有データベース
BA_kanen_QA_zenpan_kani_univers.indd
 その他 B 型肝炎 15% C 型肝炎 68% 41 706 168 66 19 12 肝 には の か 脂肪肝 の で る () という も りま の く い 肝 の肝細胞のなかに 脂肪の く がこ なにたまっ いま 類洞 正常な肝臓 腸管からの栄養や不要物が流れていく 肝細胞 正常な肝臓 脂肪肝の始まり 類洞 腸管からの栄養や不要物が流れていく 類洞 過剰な脂質 糖質の流入 肝細胞 肝細胞のなかに中性脂肪がたまり始める
その他 B 型肝炎 15% C 型肝炎 68% 41 706 168 66 19 12 肝 には の か 脂肪肝 の で る () という も りま の く い 肝 の肝細胞のなかに 脂肪の く がこ なにたまっ いま 類洞 正常な肝臓 腸管からの栄養や不要物が流れていく 肝細胞 正常な肝臓 脂肪肝の始まり 類洞 腸管からの栄養や不要物が流れていく 類洞 過剰な脂質 糖質の流入 肝細胞 肝細胞のなかに中性脂肪がたまり始める
糖尿病経口薬 QOL 研究会研究 1 症例報告書 新規 2 型糖尿病患者に対する経口糖尿病薬クラス別の治療効果と QOL の相関についての臨床試験 施設名医師氏名割付群記入年月日 症例登録番号 / 被験者識別コード / 1/12
 症例報告書 新規 2 型糖尿病患者に対する経口糖尿病薬クラス別の治療効果と QOL の相関についての臨床試験 施設名医師氏名割付群記入年月日 症例登録番号 / 被験者識別コード / 1/12 患者背景同意取得時から試験開始までの状況について記入 性別 男 女 年齢生年月日 歳 西暦年月日 身長. cm 体重. kg 腹囲. cm 糖尿病罹病期間 西暦年月 ~ 現在 喫煙 合併症 あり なし飲酒 あり
症例報告書 新規 2 型糖尿病患者に対する経口糖尿病薬クラス別の治療効果と QOL の相関についての臨床試験 施設名医師氏名割付群記入年月日 症例登録番号 / 被験者識別コード / 1/12 患者背景同意取得時から試験開始までの状況について記入 性別 男 女 年齢生年月日 歳 西暦年月日 身長. cm 体重. kg 腹囲. cm 糖尿病罹病期間 西暦年月 ~ 現在 喫煙 合併症 あり なし飲酒 あり
試験デザイン :n=152 試験開始前に第 VIII 因子製剤による出血時止血療法を受けていた患者群を 以下のい ずれかの群に 2:2:1 でランダム化 A 群 (n=36) (n=35) C 群 (n=18) ヘムライブラ 3 mg/kg を週 1 回 4 週間定期投与し その後 1.5 mg/k
 各位 2018 年 5 月 21 日 ヘムライブラ の 2 本の第 III 相国際共同治験の成績を世界血友病連盟 (WFH)2018 世界大会で発表 中外製薬株式会社 ( 本社 : 東京 代表取締役社長 CEO: 小坂達朗 ) は 血友病 A 治療薬ヘムライブラ [ 一般名 : エミシズマブ ( 遺伝子組換え )] について 第 III 相国際共同治験である HAVEN 3 試験 (NCT02847637)
各位 2018 年 5 月 21 日 ヘムライブラ の 2 本の第 III 相国際共同治験の成績を世界血友病連盟 (WFH)2018 世界大会で発表 中外製薬株式会社 ( 本社 : 東京 代表取締役社長 CEO: 小坂達朗 ) は 血友病 A 治療薬ヘムライブラ [ 一般名 : エミシズマブ ( 遺伝子組換え )] について 第 III 相国際共同治験である HAVEN 3 試験 (NCT02847637)
Epilepsy2015
 Key Concepts 1. 患者個々の治療のゴールをできるだけ早く設定 てんかんの薬物治療 薬物治療学 小川竜一 か または他の抗てんかん薬へ切り替える 第一 選択薬とは異なる作用機序の薬物 3. 年齢や合併症 服薬コンプライアンスなどの基本 情報も抗てんかん薬の選択に影響 2. 抗てんかん薬の投与が中止できる患者も存在する 決定する必要がある 50%~70%は単剤で管理でき る 2 慢性の脳の病気
Key Concepts 1. 患者個々の治療のゴールをできるだけ早く設定 てんかんの薬物治療 薬物治療学 小川竜一 か または他の抗てんかん薬へ切り替える 第一 選択薬とは異なる作用機序の薬物 3. 年齢や合併症 服薬コンプライアンスなどの基本 情報も抗てんかん薬の選択に影響 2. 抗てんかん薬の投与が中止できる患者も存在する 決定する必要がある 50%~70%は単剤で管理でき る 2 慢性の脳の病気
<4D F736F F D2082A8926D82E782B995B68F E834E838D838A E3132>
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能 効果 用法 用量 使用上の注意 改訂のお知らせ 2013 年 12 月 東和薬品株式会社 このたび 平成 25 年 8 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 25 年 11 月 29 日付にて 下記の内容で承認されました また 使用上の注意 を改訂致しましたので 併せてお知らせ申し上げます
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能 効果 用法 用量 使用上の注意 改訂のお知らせ 2013 年 12 月 東和薬品株式会社 このたび 平成 25 年 8 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 25 年 11 月 29 日付にて 下記の内容で承認されました また 使用上の注意 を改訂致しましたので 併せてお知らせ申し上げます
Ⅰ. 改訂内容 ( 部変更 ) ペルサンチン 錠 12.5 改 訂 後 改 訂 前 (1) 本剤投与中の患者に本薬の注射剤を追加投与した場合, 本剤の作用が増強され, 副作用が発現するおそれがあるので, 併用しないこと ( 過量投与 の項参照) 本剤投与中の患者に本薬の注射剤を追加投与した場合, 本
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意 改訂のお知らせ 2006 年 1 月日本ベーリンガーインゲルハイム株式会社 注 ) 処方せん医薬品 ( ジピリダモール製剤 ) = 登録商標注 ) 注意 - 医師等の処方せんにより使用すること 謹啓時下ますますご清祥のこととお慶び申し上げます 平素は弊社製品につきましてご愛顧を賜り厚く御礼申し上げます さて, この度, 自主改訂によりペルサンチン
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意 改訂のお知らせ 2006 年 1 月日本ベーリンガーインゲルハイム株式会社 注 ) 処方せん医薬品 ( ジピリダモール製剤 ) = 登録商標注 ) 注意 - 医師等の処方せんにより使用すること 謹啓時下ますますご清祥のこととお慶び申し上げます 平素は弊社製品につきましてご愛顧を賜り厚く御礼申し上げます さて, この度, 自主改訂によりペルサンチン
ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル
 ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル 1mg は 1 カプセル中ロペラミド塩酸塩 1 mg を含有し消化管から吸収されて作用を発現する このことから
ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル 1mg は 1 カプセル中ロペラミド塩酸塩 1 mg を含有し消化管から吸収されて作用を発現する このことから
Exploring the Art of Vocabulary Learning Strategies: A Closer Look at Japanese EFL University Students A Dissertation Submitted t
 Exploring the Art of Vocabulary Learning Strategies: A Closer Look at Japanese EFL University Students MIZUMOTO, Atsushi Graduate School of Foreign Language Education and Research, Kansai University, Osaka,
Exploring the Art of Vocabulary Learning Strategies: A Closer Look at Japanese EFL University Students MIZUMOTO, Atsushi Graduate School of Foreign Language Education and Research, Kansai University, Osaka,
さらに, そのプロセスの第 2 段階において分類方法が標準化されたことにより, 文書記録, 情報交換, そして栄養ケアの影響を調べる専門能力が大いに強化されたことが認められている 以上の結果から,ADA の標準言語委員会が, 専門職が用いる特別な栄養診断の用語の分類方法を作成するために結成された そ
 アメリカ栄養士会 (ADA) は, 絶えず言い続けているのであるが, 戦略的な計画は栄養士会としての優先的課題であり, それは委員会, ワーキンググループおよび作業部会が栄養士の専門性を向上させるために作成しているツールである 2002 年,ADA 品質管理委員会は, 食物 栄養の専門職の必要性を増大させるADA の戦略的計画を達成させる目的と, 彼らが市場で競争力がつくための援助をするために, 栄養ケアモデル
アメリカ栄養士会 (ADA) は, 絶えず言い続けているのであるが, 戦略的な計画は栄養士会としての優先的課題であり, それは委員会, ワーキンググループおよび作業部会が栄養士の専門性を向上させるために作成しているツールである 2002 年,ADA 品質管理委員会は, 食物 栄養の専門職の必要性を増大させるADA の戦略的計画を達成させる目的と, 彼らが市場で競争力がつくための援助をするために, 栄養ケアモデル
95_財団ニュース.indd
 NO. 95 平成 21 年 7 月 1 日発行 No.95 日本リウマチ財団ニュース 表 1 ACR-EULAR 関節リウマチ診断基準 分類基準 試案 eular 2009, 岡田正人 訳 上を診断とするかはこれから決 score 0 22 34 定され また この項目と点数 0 6 印象も受けるが 時代とともに PIP,MCP,MTP, 手関節 4箇所以上非対称性 4箇所以上対称性 10
NO. 95 平成 21 年 7 月 1 日発行 No.95 日本リウマチ財団ニュース 表 1 ACR-EULAR 関節リウマチ診断基準 分類基準 試案 eular 2009, 岡田正人 訳 上を診断とするかはこれから決 score 0 22 34 定され また この項目と点数 0 6 印象も受けるが 時代とともに PIP,MCP,MTP, 手関節 4箇所以上非対称性 4箇所以上対称性 10
フレイルのみかた
 1フレイルとは? POINT OF STUDY フレイルの概念 高齢期に生理的予備能が低下することでストレスに対する脆弱性が亢進し, 不健康を引き起こしやすい状態は Frailty と表現されており 1), 転倒や日常生活の障害, 要介護の発生, 死亡のリスクを増大させる要因となる. これまでは, 虚弱 や 老衰 などの用語で表現されることが多く, 心身が加齢により老いて衰え, 不可逆的な印象を与えることが懸念されてきた.
1フレイルとは? POINT OF STUDY フレイルの概念 高齢期に生理的予備能が低下することでストレスに対する脆弱性が亢進し, 不健康を引き起こしやすい状態は Frailty と表現されており 1), 転倒や日常生活の障害, 要介護の発生, 死亡のリスクを増大させる要因となる. これまでは, 虚弱 や 老衰 などの用語で表現されることが多く, 心身が加齢により老いて衰え, 不可逆的な印象を与えることが懸念されてきた.
種の評価基準により分類示の包括侵襲性指行為の看護師が行う医行為の範囲に関する基本的な考え方 ( たたき台 ) 指示のレベル : 指示の包括性 (1) 実施する医行為の内容 実施時期について多少の判断は伴うが 指示内容と医行為が1 対 1で対応するもの 指示内容 実施時期ともに個別具体的であるもの 例
 行為の侵襲性(行為の難易度)特定行為について ( 基本的な考え方 ) のイメージ 資料 3-2 特定行為 については 医行為の侵襲性や難易度が高いもの (B1) 医行為を実施するにあたり 詳細な身体所見の把握 実施すべき医行為及びその適時性の判断などが必要であり 実施者に高度な判断能力が求められる ( 判断の難易度が高い ) もの (B2) が想定されるのではないか B1: 特定の医行為 ( 特定行為
行為の侵襲性(行為の難易度)特定行為について ( 基本的な考え方 ) のイメージ 資料 3-2 特定行為 については 医行為の侵襲性や難易度が高いもの (B1) 医行為を実施するにあたり 詳細な身体所見の把握 実施すべき医行為及びその適時性の判断などが必要であり 実施者に高度な判断能力が求められる ( 判断の難易度が高い ) もの (B2) が想定されるのではないか B1: 特定の医行為 ( 特定行為
<4D F736F F D B A814089FC92F982CC82A8926D82E782B95F E31328C8E5F5F E646F63>
 - 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ 抗悪性腫瘍剤 ( ブルトン型チロシンキナーゼ阻害剤 ) ( 一般名 : イブルチニブ ) 2016 年 12 月 この度 抗悪性腫瘍剤 イムブルビカ カプセル 140 mg ( 以下標記製品 ) につきまして 再発又は難治性のマントル細胞リンパ腫 の効能追加承認を取得したことに伴い
- 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ 抗悪性腫瘍剤 ( ブルトン型チロシンキナーゼ阻害剤 ) ( 一般名 : イブルチニブ ) 2016 年 12 月 この度 抗悪性腫瘍剤 イムブルビカ カプセル 140 mg ( 以下標記製品 ) につきまして 再発又は難治性のマントル細胞リンパ腫 の効能追加承認を取得したことに伴い
JICA 事業評価ガイドライン ( 第 2 版 ) 独立行政法人国際協力機構 評価部 2014 年 5 月 1
 JICA 事業評価ガイドライン ( 第 2 版 ) 独立行政法人国際協力機構 評価部 2014 年 5 月 1 JICA 事業評価ガイドライン ( 第 2 版 ) ( 事業評価の目的 ) 1. JICA は 主に 1PDCA(Plan; 事前 Do; 実施 Check; 事後 Action; フィードバック ) サイクルを通じた事業のさらなる改善 及び 2 日本国民及び相手国を含むその他ステークホルダーへの説明責任
JICA 事業評価ガイドライン ( 第 2 版 ) 独立行政法人国際協力機構 評価部 2014 年 5 月 1 JICA 事業評価ガイドライン ( 第 2 版 ) ( 事業評価の目的 ) 1. JICA は 主に 1PDCA(Plan; 事前 Do; 実施 Check; 事後 Action; フィードバック ) サイクルを通じた事業のさらなる改善 及び 2 日本国民及び相手国を含むその他ステークホルダーへの説明責任
 64 は認められなかった 術前に施行したIVIgの効 きた 特に 小児例では血漿交換は肉体的侵襲が 果が明らかでなかったため 2月20日より単純血 大きく Blood Accessも難iしいことから1 IVIg 漿交換を施行した 第1回施行直後より 開瞼3 mmまで可能となり 眼球運動も改善 3回目終了 が推奨されてきている11 12 後より水分経口摂取開始 4回目終了後には人工 呼吸器から離脱が可能となり著明な改善効果を認
64 は認められなかった 術前に施行したIVIgの効 きた 特に 小児例では血漿交換は肉体的侵襲が 果が明らかでなかったため 2月20日より単純血 大きく Blood Accessも難iしいことから1 IVIg 漿交換を施行した 第1回施行直後より 開瞼3 mmまで可能となり 眼球運動も改善 3回目終了 が推奨されてきている11 12 後より水分経口摂取開始 4回目終了後には人工 呼吸器から離脱が可能となり著明な改善効果を認
3) 適切な薬物療法ができる 4) 支持的関係を確立し 個人精神療法を適切に用い 集団精神療法を学ぶ 5) 心理社会的療法 精神科リハビリテーションを行い 早期に地域に復帰させる方法を学ぶ 10. 気分障害 : 2) 病歴を聴取し 精神症状を把握し 病型の把握 診断 鑑別診断ができる 3) 人格特徴
 専門研修プログラム整備基準項目 5 別紙 1 専門技能 ( 診療 検査 診断 処置 手術など ) 1 年目 1 患者及び家族との面接 : 面接によって情報を抽出し診断に結びつけるとともに 良好な治療関係を維持する 2. 診断と治療計画 : 精神 身体症状を的確に把握して診断し 適切な治療を選択するとともに 経過に応じて診断と治療を見直す 3. 疾患の概念と病態の理解 : 疾患の概念および病態を理解し
専門研修プログラム整備基準項目 5 別紙 1 専門技能 ( 診療 検査 診断 処置 手術など ) 1 年目 1 患者及び家族との面接 : 面接によって情報を抽出し診断に結びつけるとともに 良好な治療関係を維持する 2. 診断と治療計画 : 精神 身体症状を的確に把握して診断し 適切な治療を選択するとともに 経過に応じて診断と治療を見直す 3. 疾患の概念と病態の理解 : 疾患の概念および病態を理解し
<4D F736F F F696E74202D AAE90AC94C5817A835F C581698FE39E8A90E690B6816A2E >
 労災疾病等 13 分野医学研究 開発 普及事業 第 2 期 ( 平成 21 年度 ~ 平成 25 年度 ) 分野名 働く女性のためのメディカル ケア 働く女性における介護ストレスに関する研究 - 女性介護離職者の軽減をめざして - 働く女性健康研究センター 主任研究者中部労災病院女性診療科 神経内科部長上條美樹子 研究の目的 現代社会においては女性労働力の確保は経済復興の大きな柱と考えられ 育児休暇制度や勤務形態の工夫など
労災疾病等 13 分野医学研究 開発 普及事業 第 2 期 ( 平成 21 年度 ~ 平成 25 年度 ) 分野名 働く女性のためのメディカル ケア 働く女性における介護ストレスに関する研究 - 女性介護離職者の軽減をめざして - 働く女性健康研究センター 主任研究者中部労災病院女性診療科 神経内科部長上條美樹子 研究の目的 現代社会においては女性労働力の確保は経済復興の大きな柱と考えられ 育児休暇制度や勤務形態の工夫など
葉酸とビタミンQ&A_201607改訂_ indd
 L FO AT E VI TAMI NB12 医療関係者用 葉酸 とビタミンB ビタミンB12 アリムタ投与に際して 警告 1 本剤を含むがん化学療法に際しては 緊急時に十分対応できる医療施設において がん化学療 法に十分な知識 経験を持つ医師のもとで 本剤の投与が適切と判断される症例についてのみ投 与すること 適応患者の選択にあたっては 各併用薬剤の添付文書を参照して十分注意すること また 治療開始に先立ち
L FO AT E VI TAMI NB12 医療関係者用 葉酸 とビタミンB ビタミンB12 アリムタ投与に際して 警告 1 本剤を含むがん化学療法に際しては 緊急時に十分対応できる医療施設において がん化学療 法に十分な知識 経験を持つ医師のもとで 本剤の投与が適切と判断される症例についてのみ投 与すること 適応患者の選択にあたっては 各併用薬剤の添付文書を参照して十分注意すること また 治療開始に先立ち
心房細動1章[ ].indd
![心房細動1章[ ].indd 心房細動1章[ ].indd](/thumbs/91/105546923.jpg) 1 心房細動は, 循環器医のみならず一般臨床医も遭遇することの多い不整脈で, 明らかな基礎疾患を持たない例にも発症し, その有病率は加齢とともに増加する. 動悸などにより QOL が低下するのみならず, しばしば心機能低下, 血栓塞栓症を引き起こす原因となり, 日常診療上最も重要な不整脈のひとつである. 1 [A] 米国の一般人口における心房細動の有病率については,4 つの疫学調査をまとめた Feinberg
1 心房細動は, 循環器医のみならず一般臨床医も遭遇することの多い不整脈で, 明らかな基礎疾患を持たない例にも発症し, その有病率は加齢とともに増加する. 動悸などにより QOL が低下するのみならず, しばしば心機能低下, 血栓塞栓症を引き起こす原因となり, 日常診療上最も重要な不整脈のひとつである. 1 [A] 米国の一般人口における心房細動の有病率については,4 つの疫学調査をまとめた Feinberg
( 様式乙 8) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 教授 米田博 藤原眞也 副査副査 教授教授 黒岩敏彦千原精志郎 副査 教授 佐浦隆一 主論文題名 Anhedonia in Japanese patients with Parkinson s disease ( 日本人パー
 ( 様式乙 8) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 米田博 藤原眞也 副査副査 黒岩敏彦千原精志郎 副査 佐浦隆一 主論文題名 Anhedonia in Japanese patients with Parkinson s disease ( 日本人パーキンソン病患者における幸福感の喪失 ) 学位論文内容の要旨 目的 パーキンソン病 (PD) において 気分障害は非運動症状の中でも重要なものであり
( 様式乙 8) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 米田博 藤原眞也 副査副査 黒岩敏彦千原精志郎 副査 佐浦隆一 主論文題名 Anhedonia in Japanese patients with Parkinson s disease ( 日本人パーキンソン病患者における幸福感の喪失 ) 学位論文内容の要旨 目的 パーキンソン病 (PD) において 気分障害は非運動症状の中でも重要なものであり
10 年相対生存率 全患者 相対生存率 (%) (Period 法 ) Key Point 1
 (ICD10: C81 85, C96 ICD O M: 9590 9729, 9750 9759) 治癒モデルの推定結果が不安定であったため 治癒モデルの結果を示していない 203 10 年相対生存率 全患者 相対生存率 (%) 71 68 50 53 52 45 47 1993 1997 1998 2001 2002 2006 2002 2006 (Period 法 ) 43 38 41 76
(ICD10: C81 85, C96 ICD O M: 9590 9729, 9750 9759) 治癒モデルの推定結果が不安定であったため 治癒モデルの結果を示していない 203 10 年相対生存率 全患者 相対生存率 (%) 71 68 50 53 52 45 47 1993 1997 1998 2001 2002 2006 2002 2006 (Period 法 ) 43 38 41 76
2012 年 2 月 29 日放送 CLSI ブレイクポイント改訂の方向性 東邦大学微生物 感染症学講師石井良和はじめに薬剤感受性試験成績を基に誰でも適切な抗菌薬を選択できるように考案されたのがブレイクポイントです 様々な国の機関がブレイクポイントを提唱しています この中でも 日本化学療法学会やアメ
 2012 年 2 月 29 日放送 CLSI ブレイクポイント改訂の方向性 東邦大学微生物 感染症学講師石井良和はじめに薬剤感受性試験成績を基に誰でも適切な抗菌薬を選択できるように考案されたのがブレイクポイントです 様々な国の機関がブレイクポイントを提唱しています この中でも 日本化学療法学会やアメリカ臨床検査標準委員会 :Clinical and Laboratory Standards Institute
2012 年 2 月 29 日放送 CLSI ブレイクポイント改訂の方向性 東邦大学微生物 感染症学講師石井良和はじめに薬剤感受性試験成績を基に誰でも適切な抗菌薬を選択できるように考案されたのがブレイクポイントです 様々な国の機関がブレイクポイントを提唱しています この中でも 日本化学療法学会やアメリカ臨床検査標準委員会 :Clinical and Laboratory Standards Institute
使用上の注意 1. 慎重投与 ( 次の患者には慎重に投与すること ) 1 2X X 重要な基本的注意 1TNF 2TNF TNF 3 X - CT X 4TNFB HBsHBcHBs B B B B 5 6TNF 7 8dsDNA d
 2015 5 7 201410 28 TNF 阻害薬 TNFFab シムジア 皮下注 200mg シリンジ Cimzia 200mg Syringe for S.C. Injection セルトリズマブペゴル ( 遺伝子組換え ) 製剤 873999 22400AMX01488000 20132 20133 20155 20079 警告 1. 2. 1 2 X - CT 3. TNF 4. 1 禁忌
2015 5 7 201410 28 TNF 阻害薬 TNFFab シムジア 皮下注 200mg シリンジ Cimzia 200mg Syringe for S.C. Injection セルトリズマブペゴル ( 遺伝子組換え ) 製剤 873999 22400AMX01488000 20132 20133 20155 20079 警告 1. 2. 1 2 X - CT 3. TNF 4. 1 禁忌
研修プログラム モデル例
 麻酔科専門医研修プログラム名 NTT 東日本関東病院麻酔科専門医研修プログラム TEL 03-3448-6033 連絡先 FAX 03-3448-6034 e-mail [email protected] 担当者名 松尾綾子 プログラム責任者氏名 河手良一 責任基幹施設 NTT 東日本関東病院 研修プログラム病院群 * 病院群に所属する全施設名をご記入ください 基幹研修施設 関連研修施設 国立成育医療研究センター
麻酔科専門医研修プログラム名 NTT 東日本関東病院麻酔科専門医研修プログラム TEL 03-3448-6033 連絡先 FAX 03-3448-6034 e-mail [email protected] 担当者名 松尾綾子 プログラム責任者氏名 河手良一 責任基幹施設 NTT 東日本関東病院 研修プログラム病院群 * 病院群に所属する全施設名をご記入ください 基幹研修施設 関連研修施設 国立成育医療研究センター
助成研究演題 - 平成 27 年度国内共同研究 (39 歳以下 ) 改良型 STOPP を用いた戦略的ポリファーマシー解消法 木村丈司神戸大学医学部附属病院薬剤部主任 スライド 1 スライド 2 スライド1, 2 ポリファーマシーは 言葉の意味だけを捉えると 薬の数が多いというところで注目されがちで
 助成研究演題 - 平成 27 年度国内共同研究 (39 歳以下 ) 改良型 STOPP を用いた戦略的ポリファーマシー解消法 木村丈司神戸大学医学部附属病院薬剤部主任 スライド 1 スライド 2 スライド1, 2 ポリファーマシーは 言葉の意味だけを捉えると 薬の数が多いというところで注目されがちですけれども それに加えて 潜在的に不適切な処方が含まれていることが問題として取り上げられるようになっています
助成研究演題 - 平成 27 年度国内共同研究 (39 歳以下 ) 改良型 STOPP を用いた戦略的ポリファーマシー解消法 木村丈司神戸大学医学部附属病院薬剤部主任 スライド 1 スライド 2 スライド1, 2 ポリファーマシーは 言葉の意味だけを捉えると 薬の数が多いというところで注目されがちですけれども それに加えて 潜在的に不適切な処方が含まれていることが問題として取り上げられるようになっています
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠 50mg 医薬品リスク管理計画書 (RMP) の概要 有効成分 タペンタ 錠 100mg 製造販売業者 ヤンセンファーマ株式会社 薬効分類 821 提出年月 平成 30 年
 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
ン (LVFX) 耐性で シタフロキサシン (STFX) 耐性は1% 以下です また セフカペン (CFPN) およびセフジニル (CFDN) 耐性は 約 6% と耐性率は低い結果でした K. pneumoniae については 全ての薬剤に耐性はほとんどありませんが 腸球菌に対して 第 3 世代セフ
 2012 年 12 月 5 日放送 尿路感染症 産業医科大学泌尿器科学教授松本哲朗はじめに感染症の分野では 抗菌薬に対する耐性菌の話題が大きな問題点であり 耐性菌を増やさないための感染制御と適正な抗菌薬の使用が必要です 抗菌薬は 使用すれば必ず耐性菌が出現し 増加していきます 新規抗菌薬の開発と耐性菌の増加は 永遠に続く いたちごっこ でしょう しかし 近年 抗菌薬の開発は世界的に鈍化していますので
2012 年 12 月 5 日放送 尿路感染症 産業医科大学泌尿器科学教授松本哲朗はじめに感染症の分野では 抗菌薬に対する耐性菌の話題が大きな問題点であり 耐性菌を増やさないための感染制御と適正な抗菌薬の使用が必要です 抗菌薬は 使用すれば必ず耐性菌が出現し 増加していきます 新規抗菌薬の開発と耐性菌の増加は 永遠に続く いたちごっこ でしょう しかし 近年 抗菌薬の開発は世界的に鈍化していますので
