<4D F736F F D204E6F C825496B3E8F797B18B858FC788F897702E646F63>
|
|
|
- たみじろう やなぎしま
- 4 years ago
- Views:
Transcription
1 引用文献 参考資料 1) Kaufman DW, Kelly JP, Levy M, Shapiro S.: Drug etiology of agranulocytosis: update of the International Agranulocytosis and Aplastic Anemia Study. Pharmacoepidem Drug Safety., 2:S25 (1993) 2) Wadelius M, Stjernberg E, Wiholm BE, et al.: Polymorphisms of NAT2 in relation to sulphasalazine-induced agranulocytosis. Pharmacogenetics., 10:35 (2000) 3) Mosyagin I, Dettling M, Roots I, et al.: Impact of myeloperoxidase and NADPH-oxidase polymorphisms in drug-induced agranulocytosis. J Clin Psychopharmacol., 24:613 (2004) 4) Cooper DS, Goldminz D, Levin A, et al.: Agranulocytosis associated with antithyroid drugs: effects of patient age and drug dose. Ann Intern Med., 98:26 (1983) 5) Tamai H, Takaichi Y, Morita T, et al.: Methimazole-induced agranulocytosis in Japanese patients with Graves disease. Clin Endocrinol., 30:525 (1989) 6) ( 財 ) 日本医薬情報センター編 JAPIC 医療用医薬品集 ) van der Klauw MM, Goudsmit R, Halie MR, et al.: A population-based case-cohort study of drug-associated agranulocytosis. Arch Intern Med.,159:369 (1999) 8) Bennett CI, Davidson CJ, Raishc DW, et al.: Thrombotic thrombocytopenic purpura associated with ticlopidine in the setting of coronary artery stents and stroke prevention. Arch Intern Med., 159:2524 (1999) 9) Andres E, Kurtz JE, Martine-Hunyadi C, et al.: Nonchemotherapy drug-induced agranulocytosis in elderly patients: effects of granulocyte colony-stimulating factor. Am J Med., 112:460 (2002) 10) Willfort A, Lorber C, Kapiotis S, et al.: Treatment of drug-induced agranulocytosis with recombinant granulocyte colony-stimulating factor (rh G-CSF). Ann Hematol., 66:241 (1993) 11) Sinhvi SM, Duchin KL, Willard DA, et al.: Renal handling of captopril: effect of prpbenecid. Clin Pharmacol Ther., 32:182 (1982) 12) Casato M, Pucillo LP, Leoni M, et al.: Granulocytopenia after combined therapy with interferon and angiotensin-converting enzyme inhibitors: Evidence for a synergistic hematologic toxicity. Am J Med., 99:388 (1995) 13) Levy M, Kelly JP, Kaufman DW, et al.: Risk of agranulocytosis and aplastic anemia in relation to history of infectious mononucleosis: a report from the international agranulocytosis and aplastic anemia study. Ann Hematol., 67:187 (1993) 参考資料 1) 森下玲児 内野治人 山岸司久 : 無顆粒球症患者についての全国アンケート調査の集計報告厚生省 ( 当時 ) 特定疾患特発性造血障害調査研究班昭和 54 年 1
2 度研究業績報告書 : (1980) 2) 日本病院薬剤師会編 : 重大な副作用回避のための服薬指導情報集 ( 第 1 集 ) 薬業時報社 (1997) 3) 高橋隆一 : 薬剤による顆粒球減少症の発症の予測に関する研究報告 ( 保健福祉事業報告書 )( 平成 5 年度 ~ 平成 7 年度 ) 2
3 参考 1 薬事法第 77 条の 4 の 2 に基づく副作用報告件数 ( 医薬品別 ) 注意事項 1) 薬事法第 77 条の4の2の規定に基づき報告があったもののうち 報告の多い推定原因医薬品 ( 原則として上位 10 位 ) を列記したもの 注 ) 件数 とは 報告された副作用の延べ数を集計したもの 例えば 1 症例で肝障害及び肺障害が報告された場合には 肝障害 1 件 肺障害 1 件として集計 また 複数の報告があった場合などでは 重複してカウントしている場合があることから 件数がそのまま症例数にあたらないことに留意 2) 薬事法に基づく副作用報告は 医薬品の副作用によるものと疑われる症例を報告するものであるが 医薬品との因果関係が認められないものや情報不足等により評価できないものも幅広く報告されている 3) 報告件数の順位については 各医薬品の販売量が異なること また使用法 使用頻度 併用医薬品 原疾患 合併症等が症例により異なるため 単純に比較できないことに留意すること 4) 副作用名は 用語の統一のため ICH 国際医薬用語集日本語版 (MedDRA/J)ver に収載されている用語 (Preferred Term: 基本語 ) で表示している 年度副作用名医薬品名件数 平成 16 年度 ( 平成 17 年 7 月集計 ) 無顆粒球症 好中球減少症 チアマゾール 59 塩酸チクロピジン 27 ファモチジン 11 サラゾスルファピリジン 10 インターフェロンアルファ-2b 9 プロピルチオウラシル 7 インターフェロンアルファ-2b ( 遺伝子組換え ) 7 アロプリノール 7 塩酸リトドリン 6 塩酸アプリンジン 6 その他 191 合計 340 塩酸イリノテカン 48 塩酸アムルビシン 21 メシル酸イマチニブ 18 ペグインターフェロンアルファ- 2a( 遺伝子組換え ) 12 カルボプラチン 10 ドセタキセル水和物 8 シスプラチン 8 メトトレキサート 7 フルオロウラシル 7 3
4 平成 17 年度 ( 平成 18 年 10 月集計 ) 顆粒球減少症 好中球減少症 無顆粒球症 酒石酸ビノレルビン 6 その他 133 合計 278 チアマゾール 20 カルバマゼピン 5 塩酸チクロピジン 4 ランソプラゾール 4 ファモチジン 4 プロピルチオウラシル 3 バルサルタン 3 テイコプラニン 3 半夏厚朴湯 2 エトポシド 2 その他 63 合計 113 オキサリプラチン 865 塩酸イリノテカン 23 ドセタキセル水和物 21 フルオロウラシル 17 塩酸ドキソルビシン 12 塩酸アムルビシン 10 シスプラチン 10 塩酸エピルビシン 9 ペグインターフェロンアルファ- 2a( 遺伝子組換え ) 8 レボホリナートカルシウム 7 その他 124 合計 1106 チアマゾール 56 塩酸チクロピジン 33 ファモチジン 7 サラゾスルファピリジン 7 ランソプラゾール 6 アロプリノール 6 インターフェロンアルファ-2b 6 ( 遺伝子組み換え ) 塩酸リトドリン 4 メロペネム三水和物 4 プロピルチオウラシル 4 その他 114 合計 247 4
5 顆粒球減少症 塩酸チクロピジン 13 チアマゾール 10 レボフロキサシン 3 ラベプラゾールナトリウム 3 メトトレキサート 3 オメプラゾールナトリウム 3 塩酸リトドリン 2 ランソプラゾール 2 インターフェロンアルファ-2b ( 遺伝子組み換え ) 2 エダラボン 2 その他 67 合計 110 医薬品の販売名 添付文書の内容等を知りたい時は このホームページにリンクしている独立行政法人医薬品医療機器総合機構の医薬品医療機器情報提供ホームページの 添付文書情報 から検索することができます 5
6 参考 2 ICH 国際医薬用語集日本語版 (MedDRA/J)ver における主な関連用語一覧 日米 EU 医薬品規制調和国際会議 (ICH) において検討され 取りまとめられた ICH 国際医薬用語集 (MedDRA) は 医薬品規制等に使用される医学用語( 副作用 効能 使用目的 医学的状態等 ) についての標準化を図ることを目的としたものであり 平成 16 年 3 月 25 日付薬食安発第 号 薬食審査発第 号厚生労働省医薬食品局安全対策課長 審査管理課長通知 ICH 国際医薬用語集日本語版 (MedDRA/J) の使用について により 薬事法に基づく副作用等報告において その使用を推奨しているところである なお 近頃開発され提供が開始されている MedDRA 標準検索式 (SMQ) では SMQ: 白血球減少症 が SMQ: 造血障害による血球減少症 のサブ SMQ として提供されている また SMQ: 無顆粒球症 が独立した SMQ として提供されている これらを用いると MedDRA でコーディングされたデータから包括的に該当する症例を検索することができる 名称 顆粒球減少症 重症顆粒球減少症顆粒球減少症 新生児顆粒球減少症 新生児顆粒球減少症 顆粒球数減少 分葉核球減少顆粒球数減少 無顆粒球症 英語名 Granulocytopenia Granulocytopenia severe Granulocytopenia Granulocytopenia neonatal Granulocytopenia neonatal Granulocyte count decreased Segmented cell decreased Granulocyte count decreased Agranulocytosis 6
7 悪性好中球減少症急性無顆粒球症無顆粒球症無顆粒球性アンギナ 小児遺伝性無顆粒球症 コストマン症候群小児遺伝性無顆粒球症 好中球減少症 好中球減少症好中球減少症増悪慢性好中球減少症 好中球数減少 血中好中球数減少好中球数減少好中球絶対数減少 CSF 好中球数減少 CSF 好中球数減少 好中球減少性感染 好中球減少性感染 好中球減少性大腸炎 好中球減少性大腸炎好中球減少性腸炎 Neutropenia malignant Acute agranulocytosis Agranulocytosis Angina agranulocytic Infantile genetic agranulocytosis Kostmann's syndrome Infantile genetic agranulocytosis Neutropenia Neutropenia Neutropenia aggravated Chronic neutropenia Neutrophil count decreased Blood neutrophil count decreased Neutrophil count decreased Absolute neutrophil count decreased CSF neutrophil count decreased CSF neutrophil count decreased Neutropenic infection Neutropenic infection Neutropenic colitis Neutropenic colitis Neutropenic enterocolitis 7
8 好中球減少性敗血症 好中球減少性敗血症 自己免疫性好中球減少症 自己免疫性好中球減少症 新生児好中球減少症 一過性新生児好中球減少症新生児好中球減少症 特発性好中球減少症 特発性好中球減少症 発熱性好中球減少症 好中球減少性発熱発熱性好中球減少症 Neutropenic sepsis Neutropenic sepsis Autoimmune neutropenia Autoimmune neutropenia Neutropenia neonatal Transient neonatal neutropenia Neutropenia neonatal Idiopathic neutropenia Idiopathic neutropenia Febrile neutropenia Neutropenic fever Febrile neutropenia 8
臨床検査値 G-CSF 白血球数 (/μl) 好中球 (/μl) 投与開始 3 日 投与 14 日目 投与 27 日目 ( 投 中止 1 日後 中止 5 日後 中止 7 日後 白血球数 (/μl)
 臨床検査値 G-CSF 12000 10000 8000 6000 白血球数 (/μl) 好中球 (/μl) 4000 2000 0 投与開始 3 日 投与 14 日目 投与 27 日目 ( 投 1 日後 5 日後 7 日後 白血球数 (/μl) 7200 8300 1100 1100 1100 1400 1700 2700 5900 10200 3600 10800 4600 好中球 (/μl)
臨床検査値 G-CSF 12000 10000 8000 6000 白血球数 (/μl) 好中球 (/μl) 4000 2000 0 投与開始 3 日 投与 14 日目 投与 27 日目 ( 投 1 日後 5 日後 7 日後 白血球数 (/μl) 7200 8300 1100 1100 1100 1400 1700 2700 5900 10200 3600 10800 4600 好中球 (/μl)
<4D F736F F D C825496B3E8F797B18B858FC72E646F63>
 白血球数 1,1/μL と減少を認めたため無顆粒球症を疑い入院 チアマゾールをし メロペネム.5g 2 硫酸イセパマイシン 4 mg のを開始 また G-CSF 1 μg 皮下注を開始 1 日後 : 白血球数 1,1/μL 好中球 % CRP 9.2 mg/dl 2 日後 : 消化管殺菌のため硫酸ポリミキシン B 3 万 IU フルコナゾール 1 mg の内服を開始 4 日後 :CRP 14.53
白血球数 1,1/μL と減少を認めたため無顆粒球症を疑い入院 チアマゾールをし メロペネム.5g 2 硫酸イセパマイシン 4 mg のを開始 また G-CSF 1 μg 皮下注を開始 1 日後 : 白血球数 1,1/μL 好中球 % CRP 9.2 mg/dl 2 日後 : 消化管殺菌のため硫酸ポリミキシン B 3 万 IU フルコナゾール 1 mg の内服を開始 4 日後 :CRP 14.53
Microsoft Word - No2-5無顆粒球症.doc
 重篤副作用疾患別対応マニュアル 無顆粒球症 ( 顆粒球減少症 好中球減少症 ) 平成 19 年 6 月 厚生労働省 本マニュアルの作成に当たっては 学術論文 各種ガイドライン 厚生労働科学研究事業報告書 独立行政法人医薬品医療機器総合機構の保健福祉事業報告書等を参考に 厚生労働省の委託により 関係学会においてマニュアル作成委員会を組織し 社団法人日本病院薬剤師会とともに議論を重ねて作成されたマニュアル案をもとに
重篤副作用疾患別対応マニュアル 無顆粒球症 ( 顆粒球減少症 好中球減少症 ) 平成 19 年 6 月 厚生労働省 本マニュアルの作成に当たっては 学術論文 各種ガイドライン 厚生労働科学研究事業報告書 独立行政法人医薬品医療機器総合機構の保健福祉事業報告書等を参考に 厚生労働省の委託により 関係学会においてマニュアル作成委員会を組織し 社団法人日本病院薬剤師会とともに議論を重ねて作成されたマニュアル案をもとに
6. 引用文献 参考資料 1) 日本臨床腫瘍学会. 腫瘍崩壊症候群 (TLS) 診療ガイダンス. 金原出版 ) Cairo, M. S., et al. Tumour lysis syndrome: new therapeutic strategies and classificat
 6. 引用文献 参考資料 1) 日本臨床腫瘍学会. 腫瘍崩壊症候群 (TLS) 診療ガイダンス. 金原出版. 01. ) Cairo, M. S., et al. Tumour lysis syndrome: new therapeutic strategies and classification. British Journal of Haematology, 17(1), 11, 004. )
6. 引用文献 参考資料 1) 日本臨床腫瘍学会. 腫瘍崩壊症候群 (TLS) 診療ガイダンス. 金原出版. 01. ) Cairo, M. S., et al. Tumour lysis syndrome: new therapeutic strategies and classification. British Journal of Haematology, 17(1), 11, 004. )
Microsoft Word - ARDS引用文献等.doc
 引用文献 参考資料 引用文献 ) Silliman CC, Boshkov LK, Mehdizadehkashi Z, et al : Transfusion-related acute lung injury: epidemiology and a prospective analysis of etiologic factors. Blood. 0: 454-46 (00) ) Kopko PM
引用文献 参考資料 引用文献 ) Silliman CC, Boshkov LK, Mehdizadehkashi Z, et al : Transfusion-related acute lung injury: epidemiology and a prospective analysis of etiologic factors. Blood. 0: 454-46 (00) ) Kopko PM
Microsoft Word - 緑内障④.doc
 7. 引用文献 参考資料 ) 日本緑内障学会緑内障診療ガイドライン作成委員会 : 緑内障診療ガイドライン ( 第 2 版 ). 日眼会誌 :777-84, 2006. 2) Chiou GCY (Ed) : Ophthalmic Toxicology, 2nd Edition. Taylor & Francis, Philadelphia, 999. 3) 北澤克明 ( 監 ) 白土城照 新家眞 山本哲也
7. 引用文献 参考資料 ) 日本緑内障学会緑内障診療ガイドライン作成委員会 : 緑内障診療ガイドライン ( 第 2 版 ). 日眼会誌 :777-84, 2006. 2) Chiou GCY (Ed) : Ophthalmic Toxicology, 2nd Edition. Taylor & Francis, Philadelphia, 999. 3) 北澤克明 ( 監 ) 白土城照 新家眞 山本哲也
7. 引用文献 参考資料 1) Gao Y, Zhao MH.: Drug-induced anti-neutrophil cytoplasmic antibody-associated vasculitis. Nephrology (Carlton). 14:33-41, ) Merk
 7. 引用文献 参考資料 ) Gao Y, Zhao MH.: Drug-induced anti-neutrophil cytoplasmic antibody-associated vasculitis. Nephrology (Carlton). 4:33-4, 009 ) Merkel PA. Drug-induced vasculitis. Rheum Dis Clin North Am.
7. 引用文献 参考資料 ) Gao Y, Zhao MH.: Drug-induced anti-neutrophil cytoplasmic antibody-associated vasculitis. Nephrology (Carlton). 4:33-4, 009 ) Merkel PA. Drug-induced vasculitis. Rheum Dis Clin North Am.
<4D F736F F D208A7B8D9C89F38E EA959489FC90B3816A2E646F6378>
 8. 引用文献 1) Purcell P. Boyd IW.: Bisphosphonate and osteonecrosis of the jaw. Med J Australia 18: 417-418 00 ) Marx RE. Sawatari Y. Fortin M. et al.: Bisphosphonate-Induced Exposed Bone (Osteonecrosis/Osteopetrosis)
8. 引用文献 1) Purcell P. Boyd IW.: Bisphosphonate and osteonecrosis of the jaw. Med J Australia 18: 417-418 00 ) Marx RE. Sawatari Y. Fortin M. et al.: Bisphosphonate-Induced Exposed Bone (Osteonecrosis/Osteopetrosis)
<4D F736F F D2096F295A890AB8CFB93E0898A87412E646F63>
 8. 引用文献 参考資料 1) Ayangco L, Rogers RS III: Oral manifestations of erythema multiforme. Dermatol Clin 1: 195-05 (00) ) Volcheck GW: Clinical evaluation and management of drug hypersensitivity. Immunol Allergy
8. 引用文献 参考資料 1) Ayangco L, Rogers RS III: Oral manifestations of erythema multiforme. Dermatol Clin 1: 195-05 (00) ) Volcheck GW: Clinical evaluation and management of drug hypersensitivity. Immunol Allergy
図 7:AGEP の臨床像 ( 入院時検査所見 ): 白血球 15500/μL( 好中球 86.0% 好酸球 5.0% 単球 3.5% リンパ球 4.5% 異型リンパ球 1%) 赤血球 /μl Hg 14.4g/dL Ht 42.0% 血小板 /μl 血沈 83
 図 7:AGEP の臨床像 ( 入院時検査所見 ): 白血球 5500/μL( 好中球 86.0% 好酸球 5.0% 単球 3.5% リンパ球 4.5% 異型リンパ球 %) 赤血球 474 0 4 /μl Hg 4.4g/dL Ht 4.0% 血小板 0. 0 4 /μl 血沈 83/4 AST 4 IU/L ALT 9 IU/L ALP 05 IU/L LDH 57 IU/L BUN 33.4 mg/dl
図 7:AGEP の臨床像 ( 入院時検査所見 ): 白血球 5500/μL( 好中球 86.0% 好酸球 5.0% 単球 3.5% リンパ球 4.5% 異型リンパ球 %) 赤血球 474 0 4 /μl Hg 4.4g/dL Ht 4.0% 血小板 0. 0 4 /μl 血沈 83/4 AST 4 IU/L ALT 9 IU/L ALP 05 IU/L LDH 57 IU/L BUN 33.4 mg/dl
薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リ
 薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リスク管理計画の実施状況及び得られた結果の評価に関する報告の様式 提出等の取扱いについては 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について
薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リスク管理計画の実施状況及び得られた結果の評価に関する報告の様式 提出等の取扱いについては 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について
Microsoft Word - 奈良県GQP-GVPガイドライン doc
 三. 安全確保措置の実施に関する手順 1. 目的安全確保措置の実施に関する手順の目的を記載する < 記載例 > 本手順は GVP 省令の第 9 条に基づき 安全確保措置の実施を適正かつ円滑に行うために必要な手順を定めるものである 2. 適用範囲安全確保措置の実施に関する手順の適用範囲を記載する < 記載例 > 本手順書は 二. 安全管理情報の検討及びその結果に基づく安全確保措置の立案に関する手順 で立案された安全確保措置の決定
三. 安全確保措置の実施に関する手順 1. 目的安全確保措置の実施に関する手順の目的を記載する < 記載例 > 本手順は GVP 省令の第 9 条に基づき 安全確保措置の実施を適正かつ円滑に行うために必要な手順を定めるものである 2. 適用範囲安全確保措置の実施に関する手順の適用範囲を記載する < 記載例 > 本手順書は 二. 安全管理情報の検討及びその結果に基づく安全確保措置の立案に関する手順 で立案された安全確保措置の決定
症例 2 40 歳代 女性絨毛癌 メトトレキサートによる化学療法中図 2 Grade2 症例 3 40 歳代 女性乳がん術後多臓器転移 パクリタキセルによる外来化学療法中 図 3 症例 4 30 歳代 女性頸管妊娠 メトトレキサートによる化学療法中 図 4-1 図
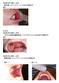 症例 40 歳代 女性絨毛癌 メトトレキサートによる化学療法中図 Grade 症例 40 歳代 女性乳がん術後多臓器転移 パクリタキセルによる外来化学療法中 図 症例 4 0 歳代 女性頸管妊娠 メトトレキサートによる化学療法中 図 4-1 図 4-17 Grade 症例 5 70 歳代 男性盲腸癌腹膜転移 5-FU による外来化学療法中 図 5-1 図 5- Grade4 症例 70 歳代 男性舌癌
症例 40 歳代 女性絨毛癌 メトトレキサートによる化学療法中図 Grade 症例 40 歳代 女性乳がん術後多臓器転移 パクリタキセルによる外来化学療法中 図 症例 4 0 歳代 女性頸管妊娠 メトトレキサートによる化学療法中 図 4-1 図 4-17 Grade 症例 5 70 歳代 男性盲腸癌腹膜転移 5-FU による外来化学療法中 図 5-1 図 5- Grade4 症例 70 歳代 男性舌癌
Microsoft Word - 末梢神経障害③.doc
 7. 引用文献 参考資料 1) 河野豊, 永田博司 : 薬物と神経筋障害診断と治療の進歩 薬物による神経障害末梢神経障害の機序. 日本内科学会誌 96:1585-1590,(007). ) Herskovits S, Schaumburg HH: Neuropathy caused by drugs. Dyck PJ, Thomas PK. eds. Peripheral Neuropathy. 4
7. 引用文献 参考資料 1) 河野豊, 永田博司 : 薬物と神経筋障害診断と治療の進歩 薬物による神経障害末梢神経障害の機序. 日本内科学会誌 96:1585-1590,(007). ) Herskovits S, Schaumburg HH: Neuropathy caused by drugs. Dyck PJ, Thomas PK. eds. Peripheral Neuropathy. 4
入院 3 日目同院皮膚科で SJS と診断され プレドニゾロン 60 mg/ 日 γ- グロブリン 2.5 g/ 日の点滴治療を開始 入院 4 日目家族の希望で当科に転院 ( 現症 ): 顔面 頸部に米粒大までの暗紅色斑が多発 融合し 眼瞼 鼻孔部 口唇粘膜には発赤 びらんを伴っていた 躯幹でも同様
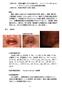 入院 3 日目同院皮膚科で SJS と診断され プレドニゾロン 0 mg/ 日 γ- グロブリン 2. g/ 日の点滴治療を開始 入院 4 日目家族の希望で当科に転院 ( 現症 ): 顔面 頸部に米粒大までの暗紅色斑が多発 融合し 眼瞼 鼻孔部 口唇粘膜には発赤 びらんを伴っていた 躯幹でも同様の暗紅色斑が多発融合し 母指頭大までのびらんと小水疱が集蔟し局面を形成していた 皮膚剥離面積は全体表面積の
入院 3 日目同院皮膚科で SJS と診断され プレドニゾロン 0 mg/ 日 γ- グロブリン 2. g/ 日の点滴治療を開始 入院 4 日目家族の希望で当科に転院 ( 現症 ): 顔面 頸部に米粒大までの暗紅色斑が多発 融合し 眼瞼 鼻孔部 口唇粘膜には発赤 びらんを伴っていた 躯幹でも同様の暗紅色斑が多発融合し 母指頭大までのびらんと小水疱が集蔟し局面を形成していた 皮膚剥離面積は全体表面積の
untitled
 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 20021016 17 18 1018 19 20 21 22 23 24 25 1 11 ICHMedDRA/ J ver. 10.0Preferred Term 26 27 http://www.info.pmda.go.jp/ http://www.pmda.go.jp/index.html ICH MedDRA/Jver.11.1
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 20021016 17 18 1018 19 20 21 22 23 24 25 1 11 ICHMedDRA/ J ver. 10.0Preferred Term 26 27 http://www.info.pmda.go.jp/ http://www.pmda.go.jp/index.html ICH MedDRA/Jver.11.1
特殊病態下感染症における抗菌薬治験の手引き作成委員会報告書(案)
 VOL.51 NO.6 JUNE 2003 JUNE 2003 9) Niederman MS et al: Guidelines for the management of adults with community-acquired pneumonia. Diagnosis, assessment of severity, antimicrobial therapy and prevention.
VOL.51 NO.6 JUNE 2003 JUNE 2003 9) Niederman MS et al: Guidelines for the management of adults with community-acquired pneumonia. Diagnosis, assessment of severity, antimicrobial therapy and prevention.
Rinku General Medical Center
 Rinku General Medical Center 4860 100 1620 Ann Intern Med. 1966; 64: 328 40 CHOP 63 1 83 J Clin Oncol. 1998; 16: 20065-69 Febrile Neutropenia IDSA(Infectious Diseases Society of America) 2002 Guidelines
Rinku General Medical Center 4860 100 1620 Ann Intern Med. 1966; 64: 328 40 CHOP 63 1 83 J Clin Oncol. 1998; 16: 20065-69 Febrile Neutropenia IDSA(Infectious Diseases Society of America) 2002 Guidelines
untitled
 1 2 3 4 5 6 7 8 9 10 11 12 13 µ µ µ 14 15 16 17 1. Fabris P, Betterle C, Floreani A, Greggio NA, de Lazzari F, Naccarato R, Chiaramonte M: Development of type 1 diabetes mellitus during interferon alfa
1 2 3 4 5 6 7 8 9 10 11 12 13 µ µ µ 14 15 16 17 1. Fabris P, Betterle C, Floreani A, Greggio NA, de Lazzari F, Naccarato R, Chiaramonte M: Development of type 1 diabetes mellitus during interferon alfa
参考表 ARONJ を発症するリスクを有する代表的な骨吸収抑制薬 一般名主な商品名効能 効果 注射薬 ゾレドロン酸水和物注射液 (1) パミドロン酸 デノスマブ アレンドロン酸 ゾメタ パミドロン酸二 Na ランマーク ボナロン 高用量 ( 主に悪性腫瘍 ) 悪性腫瘍による高カルシウム血症多発性骨髄
 8. 引用文献 1) 米田俊之, 萩野浩, 他 : 顎骨壊死検討委員会 : 骨吸収抑制薬関連顎骨壊死の病態と管理 : 顎骨壊死検討委員会のポジションペーパー 2016 (https://www.jsoms.or.jp/medical/wp-content/uploads/2015/08/position_pap er2016.pdf) 2) Ruggiero SL, Dodson TB,et al:american
8. 引用文献 1) 米田俊之, 萩野浩, 他 : 顎骨壊死検討委員会 : 骨吸収抑制薬関連顎骨壊死の病態と管理 : 顎骨壊死検討委員会のポジションペーパー 2016 (https://www.jsoms.or.jp/medical/wp-content/uploads/2015/08/position_pap er2016.pdf) 2) Ruggiero SL, Dodson TB,et al:american
2001 2003 2005 2006 2007 2008
 2001 2003 2005 2006 2007 2008 60 etc. http://nosmoke.hp.infoseek.co.jp/yuugaibussitu.htm http://nosmoke.hp.infoseek.co.jp/yuugaibussitu.htm 23.5% 2.8% 2.8% 3.4% 30.3% 9.9% 11.5% 15.8% AAN 65
2001 2003 2005 2006 2007 2008 60 etc. http://nosmoke.hp.infoseek.co.jp/yuugaibussitu.htm http://nosmoke.hp.infoseek.co.jp/yuugaibussitu.htm 23.5% 2.8% 2.8% 3.4% 30.3% 9.9% 11.5% 15.8% AAN 65
別添 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について < 半年ごとの定期報告の受け付け> Q1 平成 26 年 6 月 30 日までの間は 治験依頼者 ( 自ら治験を実施する者を除く ) が提出する副作用等症例の定期報告は なお従前の例によることができる とあるが 平成 26 年
 事務連絡 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局審査管理課 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 第 273 条第 3 項に基づく治験副作用等定期報告については 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について ( 平成 24 年
事務連絡 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局審査管理課 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 第 273 条第 3 項に基づく治験副作用等定期報告については 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について ( 平成 24 年
要望番号 ;Ⅱ-183 未承認薬 適応外薬の要望 ( 別添様式 ) 1. 要望内容に関連する事項 要望者学会 ( 該当する ( 学会名 ; 日本感染症学会 ) ものにチェックする ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 優先順位 1 位 ( 全 8 要望中 ) 要望する医薬品
 未承認薬 適応外薬の要望 ( 別添様式 ) 1. 要望内容に関連する事項 要望者学会 ( 該当する ( 学会名 ; 日本感染症学会 ) ものにチェックする ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 優先順位 1 位 ( 全 8 要望中 ) 要望する医薬品 要望内容 成分名 ( 一般名 ) 販売名 会社名 国内関連学会 未承認薬 適応 外薬の分類 ( 該当するものにチェックする )
未承認薬 適応外薬の要望 ( 別添様式 ) 1. 要望内容に関連する事項 要望者学会 ( 該当する ( 学会名 ; 日本感染症学会 ) ものにチェックする ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 優先順位 1 位 ( 全 8 要望中 ) 要望する医薬品 要望内容 成分名 ( 一般名 ) 販売名 会社名 国内関連学会 未承認薬 適応 外薬の分類 ( 該当するものにチェックする )
貧血
 その他 79 合計 125 平成 17 年度 ( 平成 18 年 10 月集計 ) 赤芽球癆 貧血 溶血性貧血 リン酸フルダラビン 4 バルサルタン 4 塩酸チクロピジン 2 ロサルタンカリウム 2 カンデサルタンシレキセチル 2 ミコフェノール酸モフェチル 2 ホスフルコナゾール 2 フェノバルビタール 2 テオフィリン 2 フェニトイン 2 その他 11 合計 35 ペグインターフェロンアルファ-2
その他 79 合計 125 平成 17 年度 ( 平成 18 年 10 月集計 ) 赤芽球癆 貧血 溶血性貧血 リン酸フルダラビン 4 バルサルタン 4 塩酸チクロピジン 2 ロサルタンカリウム 2 カンデサルタンシレキセチル 2 ミコフェノール酸モフェチル 2 ホスフルコナゾール 2 フェノバルビタール 2 テオフィリン 2 フェニトイン 2 その他 11 合計 35 ペグインターフェロンアルファ-2
10,000 L 30,000 50,000 L 30,000 50,000 L 図 1 白血球増加の主な初期対応 表 1 好中球増加 ( 好中球 >8,000/μL) の疾患 1 CML 2 / G CSF 太字は頻度の高い疾患 32
 白血球増加の初期対応 白血球増加が 30,000~50,000/μL 以上と著明であれば, 白血病の可能性が高い すぐに専門施設 ( ) に紹介しよう ( 図 1) 白血球増加があれば, まず発熱など感染症を疑う症状 所見に注目しよう ( 図 1) 白血球増加があれば, 白血球分画を必ずチェックしよう 成熟好中球 ( 分葉核球や桿状核球 ) 主体の増加なら, 反応性好中球増加として対応しよう ( 図
白血球増加の初期対応 白血球増加が 30,000~50,000/μL 以上と著明であれば, 白血病の可能性が高い すぐに専門施設 ( ) に紹介しよう ( 図 1) 白血球増加があれば, まず発熱など感染症を疑う症状 所見に注目しよう ( 図 1) 白血球増加があれば, 白血球分画を必ずチェックしよう 成熟好中球 ( 分葉核球や桿状核球 ) 主体の増加なら, 反応性好中球増加として対応しよう ( 図
1 見出し1,12ポ,日本語ゴシック,英語Arial,段落後は6ポの設定です
 8. Page1 8. B 1 5) 6) 2099 2370 50 400 mg 19 (1) 1) (a) 78.9% 30/38 4 3 35.7% 5/14 71.4% 10/1485.7% 12/142 1 83.3% 5/63 2 1 1 1 8. Page2 (b) 2099 1897 82.4% 1562/1897 2 84.0% 1298/1545 3 2 80.4% 472/58779.0%
8. Page1 8. B 1 5) 6) 2099 2370 50 400 mg 19 (1) 1) (a) 78.9% 30/38 4 3 35.7% 5/14 71.4% 10/1485.7% 12/142 1 83.3% 5/63 2 1 1 1 8. Page2 (b) 2099 1897 82.4% 1562/1897 2 84.0% 1298/1545 3 2 80.4% 472/58779.0%
要望番号 ;Ⅱ-24 未承認薬 適応外薬の要望 ( 別添様式 ) 1. 要望内容に関連する事項 要望者 ( 該当するものにチェックする ) 学会 ( 学会名 ; 特定非営利活動法人日本臨床腫瘍学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 優先順位 8 位 ( 全 33 要望中
 未承認薬 適応外薬の要望 ( 別添様式 ) 1. 要望内容に関連する事項 要望者 ( 該当するものにチェックする ) 学会 ( 学会名 ; 特定非営利活動法人日本臨床腫瘍学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 優先順位 8 位 ( 全 33 要望中 ) 要望する医薬品 成 分 名 ( 一般名 ) 販 売 名 会 社 名 国内関連学会 amoxicillin-clabulanate
未承認薬 適応外薬の要望 ( 別添様式 ) 1. 要望内容に関連する事項 要望者 ( 該当するものにチェックする ) 学会 ( 学会名 ; 特定非営利活動法人日本臨床腫瘍学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 優先順位 8 位 ( 全 33 要望中 ) 要望する医薬品 成 分 名 ( 一般名 ) 販 売 名 会 社 名 国内関連学会 amoxicillin-clabulanate
いは蛇行状を呈す 数日から数週間の間隔で繰り返し出現する 臨床検査で特徴的な所見はない (3) 中毒性表皮壊死症 (toxic epidermal necrolysis: TEN) 38 以上の発熱が認められる AGEP の経過中に小膿疱が融合し 角層が薄くはがれる所見を呈することがあるが TEN
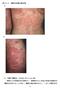 図 6(a,b): 膿疱性乾癬の臨床像 a) b) () 角層下膿疱症 (Sneddon-Wilkinson 病 ) 発熱などの前駆症状は通常なく 間擦部中心に米粒大前後の弛緩性の膿疱を形成することが多い 膿疱は融合傾向を示し しばしば環状ある 5 いは蛇行状を呈す 数日から数週間の間隔で繰り返し出現する 臨床検査で特徴的な所見はない (3) 中毒性表皮壊死症 (toxic epidermal necrolysis:
図 6(a,b): 膿疱性乾癬の臨床像 a) b) () 角層下膿疱症 (Sneddon-Wilkinson 病 ) 発熱などの前駆症状は通常なく 間擦部中心に米粒大前後の弛緩性の膿疱を形成することが多い 膿疱は融合傾向を示し しばしば環状ある 5 いは蛇行状を呈す 数日から数週間の間隔で繰り返し出現する 臨床検査で特徴的な所見はない (3) 中毒性表皮壊死症 (toxic epidermal necrolysis:
Microsoft Word - No2-7血栓症引用.doc
 引用文献 参考資料 引用文献 1) O'Connell KA, et al.: Thromboembolic adverse events after use of recombinant human coagulation factor VIIa. JAMA 295:293-8 (2006) 2) Hashimoto S, et al.: Fatal thromboembolism in acute
引用文献 参考資料 引用文献 1) O'Connell KA, et al.: Thromboembolic adverse events after use of recombinant human coagulation factor VIIa. JAMA 295:293-8 (2006) 2) Hashimoto S, et al.: Fatal thromboembolism in acute
untitled
 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 1 1 1 ICHMedDRA/J ver. 10.0Preferred Term 30 ICH MedDRA/Jver.11.1 EU ICHICH MedDRA 0325001 0325032 ICH MedDRA/J PT LLT MedDRA
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 1 1 1 ICHMedDRA/J ver. 10.0Preferred Term 30 ICH MedDRA/Jver.11.1 EU ICHICH MedDRA 0325001 0325032 ICH MedDRA/J PT LLT MedDRA
Microsoft Word - LIA RMP_概要ver2.docx
 リアルダ錠 1200mg に係る 医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任は持田製薬株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません 持田製薬株式会社 リアルダ錠 1200mg に係る医薬品リスク管理計画書 (RMP) の概要 販売名リアルダ錠 1200mg 有効成分メサラジン 製造販売業者持田製薬株式会社薬効分類 872399 提出年月
リアルダ錠 1200mg に係る 医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任は持田製薬株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません 持田製薬株式会社 リアルダ錠 1200mg に係る医薬品リスク管理計画書 (RMP) の概要 販売名リアルダ錠 1200mg 有効成分メサラジン 製造販売業者持田製薬株式会社薬効分類 872399 提出年月
都道府県医師会医療安全担当理事殿 ( 法安 56) 平成 27 年 8 月 5 日 日本医師会常任理事今村定臣 酵素電極法を用いた血糖測定に使用する医療機器及び体外診断用医薬品に係る 使用上の注意 の改訂について グルコース分析装置 自己検査用グルコース測定器及び自動分析装置等並びに血液検査用グルコ
 都道府県医師会医療安全担当理事殿 ( 法安 56) 平成 27 年 8 月 5 日 日本医師会常任理事今村定臣 酵素電極法を用いた血糖測定に使用する医療機器及び体外診断用医薬品に係る 使用上の注意 の改訂について グルコース分析装置 自己検査用グルコース測定器及び自動分析装置等並びに血液検査用グルコースキット及び自己検査用グルコースキット ( 測定項目として血糖値を有する医療機器または体外診断用医薬品
都道府県医師会医療安全担当理事殿 ( 法安 56) 平成 27 年 8 月 5 日 日本医師会常任理事今村定臣 酵素電極法を用いた血糖測定に使用する医療機器及び体外診断用医薬品に係る 使用上の注意 の改訂について グルコース分析装置 自己検査用グルコース測定器及び自動分析装置等並びに血液検査用グルコースキット及び自己検査用グルコースキット ( 測定項目として血糖値を有する医療機器または体外診断用医薬品
医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年
![医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年 医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年](/thumbs/91/107149459.jpg) 事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
医師主導治験取扱要覧
 9. 安全性情報の取扱いに関する手順書 1. 目的及び適用範囲 本手順書は 安全性情報の取扱いに係る用語の定義を定め 当該治験に関与する者が 安全性情報を適 切に取扱うための手順その他必要な事項を定めるものである 2. 用語の定義等 2.1. 用語の定義 2.1.1. 治験責任医師等 本手順書は 自ら治験を実施する者を 治験責任医師 と記載し また 治験責任医師及び治験分担医師 を併せて 治験責任医師等
9. 安全性情報の取扱いに関する手順書 1. 目的及び適用範囲 本手順書は 安全性情報の取扱いに係る用語の定義を定め 当該治験に関与する者が 安全性情報を適 切に取扱うための手順その他必要な事項を定めるものである 2. 用語の定義等 2.1. 用語の定義 2.1.1. 治験責任医師等 本手順書は 自ら治験を実施する者を 治験責任医師 と記載し また 治験責任医師及び治験分担医師 を併せて 治験責任医師等
<4D F736F F D2082A8926D82E782B995B68F E834E838D838A E3132>
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能 効果 用法 用量 使用上の注意 改訂のお知らせ 2013 年 12 月 東和薬品株式会社 このたび 平成 25 年 8 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 25 年 11 月 29 日付にて 下記の内容で承認されました また 使用上の注意 を改訂致しましたので 併せてお知らせ申し上げます
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能 効果 用法 用量 使用上の注意 改訂のお知らせ 2013 年 12 月 東和薬品株式会社 このたび 平成 25 年 8 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 25 年 11 月 29 日付にて 下記の内容で承認されました また 使用上の注意 を改訂致しましたので 併せてお知らせ申し上げます
 ! 1Munderl P et al. Survival and causes of death, 2 years after Introduction of antiretroviral therapy in Africa. XVI International AIDS Conference, 2006, Abstract THLB0208. 2Walensky RP et al. The
! 1Munderl P et al. Survival and causes of death, 2 years after Introduction of antiretroviral therapy in Africa. XVI International AIDS Conference, 2006, Abstract THLB0208. 2Walensky RP et al. The
<4D F736F F D209A6291A794AD8DEC88F B68CA393992E646F63>
 引用文献 参考資料 引用文献 ) 榊原博樹, 末次勸 : アスピリン喘息呼吸 : 990-00 (993) ) Cowburn AS, Sladek K, Soja J, et al. : Overexpression of leukotriene C4 synthase in bronchial biopsies from patients with aspirin-intolerant asthma.
引用文献 参考資料 引用文献 ) 榊原博樹, 末次勸 : アスピリン喘息呼吸 : 990-00 (993) ) Cowburn AS, Sladek K, Soja J, et al. : Overexpression of leukotriene C4 synthase in bronchial biopsies from patients with aspirin-intolerant asthma.
17)Dumitrescu G, Dahan K, Treton X, Corcos O, Bouhnik Y, Stefanescu C. Nephrotic syndrome after infliximab treatment in a patient with ulcerative coli
 7. 引用文献 参考資料 1)Wooley PH, Griffin J, Panayi GS, Batchelor JR, Welsh KI, Gibson TJ. HLA-DR antigens and toxic reaction to sodium aurothiomalate and D-penicillamine in patients with rheumatoid arthritis.
7. 引用文献 参考資料 1)Wooley PH, Griffin J, Panayi GS, Batchelor JR, Welsh KI, Gibson TJ. HLA-DR antigens and toxic reaction to sodium aurothiomalate and D-penicillamine in patients with rheumatoid arthritis.
ICH Q4B Annex12
 薬食審査発 0321 第 1 号平成 2 5 年 3 月 21 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) ICHQ4B ガイドラインに基づく事項別付属文書 ( エンドトキシン試験法 ) について 今般 日米 EU 医薬品規制調和国際会議 (ICH) において ICHQ4B ガイドライン ( 平成 21 年 5 月 26 日付け薬食審査発第 0526001
薬食審査発 0321 第 1 号平成 2 5 年 3 月 21 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬食品局審査管理課長 ( 公印省略 ) ICHQ4B ガイドラインに基づく事項別付属文書 ( エンドトキシン試験法 ) について 今般 日米 EU 医薬品規制調和国際会議 (ICH) において ICHQ4B ガイドライン ( 平成 21 年 5 月 26 日付け薬食審査発第 0526001
貧血
 薬剤性貧血 英語名 :Anemia 同義語 : 溶血性貧血 メトヘモグロビン血症 赤芽球ろう 鉄芽球性貧血 巨赤芽球性貧血 A. 患者の皆様へ ここでご紹介している副作用は まれなもので 必ず起こるというものではありません ただ 副作用は気づかずに放置していると重くなり健康に影響を及ぼすことがあるので 早めに 気づいて 対処することが大切です そこで より安全な治療を行う上でも 本マニュアルを参考に
薬剤性貧血 英語名 :Anemia 同義語 : 溶血性貧血 メトヘモグロビン血症 赤芽球ろう 鉄芽球性貧血 巨赤芽球性貧血 A. 患者の皆様へ ここでご紹介している副作用は まれなもので 必ず起こるというものではありません ただ 副作用は気づかずに放置していると重くなり健康に影響を及ぼすことがあるので 早めに 気づいて 対処することが大切です そこで より安全な治療を行う上でも 本マニュアルを参考に
アセトアミノフェンお知らせ文書_案_ _ver09.doc
 http://www.maruishi-pharm.co.jp http://www.info.pmda.go.jp http://www.mhlw.go.jp/shingi/other.html 19 3 28 0328001 19 9 28 19 11 30, 分に注意しなければならないため それぞれ 相互作用 の項ならびに 慎重投与 の項に追記致しました 慎重投与 小児等への投与 小児薬物療法検討会議報告書では
http://www.maruishi-pharm.co.jp http://www.info.pmda.go.jp http://www.mhlw.go.jp/shingi/other.html 19 3 28 0328001 19 9 28 19 11 30, 分に注意しなければならないため それぞれ 相互作用 の項ならびに 慎重投与 の項に追記致しました 慎重投与 小児等への投与 小児薬物療法検討会議報告書では
Untitled
 重要な情報が記載されています ので 必ずお読み下さい 平成 29 年 3 月 販売元 製造販売元 使用上使用上の注意注意 改訂改訂のおのお知らせ 拝啓時下 益々ご清栄のこととお慶び申し上げます 平素は弊社製品につきまして格別のお引立てを賜り 厚く御礼申し上げます さて 平成 29 年 3 月 21 日付厚生労働省医薬厚生労働省医薬 生活衛生局安全対策課長通知生活衛生局安全対策課長通知によりにより 標記製品標記製品の
重要な情報が記載されています ので 必ずお読み下さい 平成 29 年 3 月 販売元 製造販売元 使用上使用上の注意注意 改訂改訂のおのお知らせ 拝啓時下 益々ご清栄のこととお慶び申し上げます 平素は弊社製品につきまして格別のお引立てを賜り 厚く御礼申し上げます さて 平成 29 年 3 月 21 日付厚生労働省医薬厚生労働省医薬 生活衛生局安全対策課長通知生活衛生局安全対策課長通知によりにより 標記製品標記製品の
日本医薬品安全性学会 COI 開示 筆頭発表者 : 加藤祐太 演題発表に関連し 開示すべき COI 関連の企業などはありません
 医薬品副作用データベース (JADER) を用いた市販後の副作用発現状況の検討 加藤祐太 1)2) 岸達生 3) 高松昭司 2) 白石正 4) 1) 山形大学医学部医薬品医療機器評価学講座 2) 医薬品医療機器総合機構安全第二部 3) 医薬品医療機器総合機構信頼性保証部 4) 山形大学医学部附属病院薬剤部 日本医薬品安全性学会 COI 開示 筆頭発表者 : 加藤祐太 演題発表に関連し 開示すべき COI
医薬品副作用データベース (JADER) を用いた市販後の副作用発現状況の検討 加藤祐太 1)2) 岸達生 3) 高松昭司 2) 白石正 4) 1) 山形大学医学部医薬品医療機器評価学講座 2) 医薬品医療機器総合機構安全第二部 3) 医薬品医療機器総合機構信頼性保証部 4) 山形大学医学部附属病院薬剤部 日本医薬品安全性学会 COI 開示 筆頭発表者 : 加藤祐太 演題発表に関連し 開示すべき COI
<4D F736F F D20835A838D A83938FC78CF38C515F48508C668DDA94C5816A2E646F63>
 に改善が認められないため 8 月 3 日大学病院精神科に転院となった 転院時 体温 37.3 脈拍 90/ 分であり 意識レベルは JCS でⅠ-3 であった 上下肢 顔輪筋 口輪筋に著明なミオクローヌスを認め B 病院で振戦ととらえられていた症状はミオクローヌスと考えられた また 上半身に著明な発汗を観察し 上肢に中程度の筋強剛も認めた 協調運動障害もあり 自力での歩行は不可能であった 血液検査では
に改善が認められないため 8 月 3 日大学病院精神科に転院となった 転院時 体温 37.3 脈拍 90/ 分であり 意識レベルは JCS でⅠ-3 であった 上下肢 顔輪筋 口輪筋に著明なミオクローヌスを認め B 病院で振戦ととらえられていた症状はミオクローヌスと考えられた また 上半身に著明な発汗を観察し 上肢に中程度の筋強剛も認めた 協調運動障害もあり 自力での歩行は不可能であった 血液検査では
untitled
 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 IFN- IFN- IFN- IL-2 IL-2 IL-2 IFN- 40.0 39.0 38.0 37.0 36.0 2000 1500 1000 500 ml (ml) 12/11 12/12 12/13 12/15 12/17 12/18 12/6 12/12 12/18 12/25 16 17 1 1 1 ICH MedDRA/J
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 IFN- IFN- IFN- IL-2 IL-2 IL-2 IFN- 40.0 39.0 38.0 37.0 36.0 2000 1500 1000 500 ml (ml) 12/11 12/12 12/13 12/15 12/17 12/18 12/6 12/12 12/18 12/25 16 17 1 1 1 ICH MedDRA/J
C/NC : committed/noncommitted
 C/NC : committed/noncommitted 110 time post-icd implant 1) The Cardiac Arrhythmia Suppression Trial (CAST) Investigators Preliminary report : Effect of encainaide and flecainide on mortality in a
C/NC : committed/noncommitted 110 time post-icd implant 1) The Cardiac Arrhythmia Suppression Trial (CAST) Investigators Preliminary report : Effect of encainaide and flecainide on mortality in a
所属役職氏名 : ( 英語 )Professor Yasushi Miyazaki, Department of Hematology, Atomic Bomb Disease and Hibakusha Medicine Unit, Atomic Bomb Disease Institute, N
 ( 報告様式 4) 課題管理番号 16ek0109134h0002 平成 29 年 5 月 26 日 平成 28 年度委託研究開発成果報告書 I. 基本情報 事 業 名 : ( 日本語 ) 難治性疾患実用化研究事業 ( 英語 )Practical Research for Rare/Intractable Diseases 研究 ( 日本語 ) 成人慢性好中球減少症の診療ガイドライン作成に向けた予後追跡調査
( 報告様式 4) 課題管理番号 16ek0109134h0002 平成 29 年 5 月 26 日 平成 28 年度委託研究開発成果報告書 I. 基本情報 事 業 名 : ( 日本語 ) 難治性疾患実用化研究事業 ( 英語 )Practical Research for Rare/Intractable Diseases 研究 ( 日本語 ) 成人慢性好中球減少症の診療ガイドライン作成に向けた予後追跡調査
審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7
![審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7 審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7](/thumbs/92/110490968.jpg) 審査報告書 平成 26 年 1 月 6 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [
審査報告書 平成 26 年 1 月 6 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [
<4D F736F F F696E74202D EA98CC8935F8C9F B8DEC977095F18D902E B8CDD8AB B83685D>
 製造販売後安全管理業務における現状 ノバルティス社やファイザー社等で 安全管理情報 ( 副作用等 ) の処理や国報告に問題があったことが判明 安全管理情報の処理と副作用報告その 2 ( 副作用報告に関する内容を中心に ) 当県でも GQP GVP フォローアップ調査で安全管理情報が適切に処理されているかを重点的に確認 副作用報告漏れや安全管理情報の処理が適切でない事例が見られた GVP 省令の内容について説明
製造販売後安全管理業務における現状 ノバルティス社やファイザー社等で 安全管理情報 ( 副作用等 ) の処理や国報告に問題があったことが判明 安全管理情報の処理と副作用報告その 2 ( 副作用報告に関する内容を中心に ) 当県でも GQP GVP フォローアップ調査で安全管理情報が適切に処理されているかを重点的に確認 副作用報告漏れや安全管理情報の処理が適切でない事例が見られた GVP 省令の内容について説明
を追加する (2) 実施要領通知の報告様式別紙 1 医薬品安全性情報報告書 及び同報告様式別紙 2 医療機器安全性情報報告書 を別添のとおり変更する
 薬食発 0311 第 1 号平成 25 年 3 月 11 日 各都道府県知事殿 厚生労働省医薬食品局長 医薬品 医療機器等安全性情報報告制度 の報告における電子メールの活用について 薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 77 条の 4 の 2 第 2 項の規定に基づく 医療機関等からの医薬品又は医療機器についての副作用 感染症及び不具合報告 ( 以下 副作用等報告
薬食発 0311 第 1 号平成 25 年 3 月 11 日 各都道府県知事殿 厚生労働省医薬食品局長 医薬品 医療機器等安全性情報報告制度 の報告における電子メールの活用について 薬事法 ( 昭和 35 年法律第 145 号 以下 法 という ) 第 77 条の 4 の 2 第 2 項の規定に基づく 医療機関等からの医薬品又は医療機器についての副作用 感染症及び不具合報告 ( 以下 副作用等報告
01_告示(本文)案文_171121
 厚生労働省告示第三百三十八号厚生労働大臣が指定する病院の病棟における療養に要する費用の額の算定方法平成二十年厚生労 ( 働省告示第九十三号第一項第五号及び別表の規定に基づき厚生労働大臣が定める傷病名手術 ) 0 2 処置等及び定義副傷病名及び厚生労働大臣が指定する病院の病棟における療養に要する費用の額の 算定方法第一項第五号の規定に基づき厚生労働大臣が別に定める者の一部を改正する告示を次のよう に定め平成二十九年十一月二十二日から適用する
厚生労働省告示第三百三十八号厚生労働大臣が指定する病院の病棟における療養に要する費用の額の算定方法平成二十年厚生労 ( 働省告示第九十三号第一項第五号及び別表の規定に基づき厚生労働大臣が定める傷病名手術 ) 0 2 処置等及び定義副傷病名及び厚生労働大臣が指定する病院の病棟における療養に要する費用の額の 算定方法第一項第五号の規定に基づき厚生労働大臣が別に定める者の一部を改正する告示を次のよう に定め平成二十九年十一月二十二日から適用する
第 3 章支持 緩和医療 3. 感染症対策 ; 予防接種 FN はじめに高齢者のがん診療においては治療法の選択 化学療法の強度の決定や期待通りの治療効果を得るために感染症対策は重要な因子となる 代表的な感染症である発熱性好中球減少症については臨床腫瘍学会の 発熱性好中球減少症 (FN) 診療ガイドラ
 第 3 章支持 緩和医療 3. 感染症対策 ; 予防接種 FN はじめに高齢者のがん診療においては治療法の選択 化学療法の強度の決定や期待通りの治療効果を得るために感染症対策は重要な因子となる 代表的な感染症である発熱性好中球減少症については臨床腫瘍学会の 発熱性好中球減少症 (FN) 診療ガイドライン改訂第 2 版 が 2017 年 10 月に発表されており ここでは FN が起こった場合の評価
第 3 章支持 緩和医療 3. 感染症対策 ; 予防接種 FN はじめに高齢者のがん診療においては治療法の選択 化学療法の強度の決定や期待通りの治療効果を得るために感染症対策は重要な因子となる 代表的な感染症である発熱性好中球減少症については臨床腫瘍学会の 発熱性好中球減少症 (FN) 診療ガイドライン改訂第 2 版 が 2017 年 10 月に発表されており ここでは FN が起こった場合の評価
審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果
![審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果 審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果](/thumbs/92/108604766.jpg) 審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
保険薬局の登録 ~ クロザリルは CPMS に登録された保険薬局で調剤され 通院患者に渡されることにな っています CPMS 登録にあたり薬局には下記要件が求められます < 要件 1> 1) インターネットが使えること (ecpms(web site) にアクセス可能であること ) 2) 処方元の医
 症例検討会クロザピン ( 商品名 : クロザリル ) について 適応 : 治療抵抗性の統合失調症 ( 他の抗精神病薬で効果が不十分 または副作用により服薬困難な場合など ) に用いられる 作用機序 : クロザピンの詳細な作用機序は不明であるがドーパミン D 2 受容体遮断作用に依存しない中脳辺縁系ドーパミン神経 系に対する選択的抑制が考えられる また クロザピンはミクログリア活性化を抑制し 神経保護作用を有するものと考えられる
症例検討会クロザピン ( 商品名 : クロザリル ) について 適応 : 治療抵抗性の統合失調症 ( 他の抗精神病薬で効果が不十分 または副作用により服薬困難な場合など ) に用いられる 作用機序 : クロザピンの詳細な作用機序は不明であるがドーパミン D 2 受容体遮断作用に依存しない中脳辺縁系ドーパミン神経 系に対する選択的抑制が考えられる また クロザピンはミクログリア活性化を抑制し 神経保護作用を有するものと考えられる
37, 9-14, 2017 : cefcapene piperacillin 3 CT Clostridium difficile CD vancomycin CD 7 Clostridium difficile CD CD associate
 37, 9-14, 2017 : 36 2015 8 6 cefcapene piperacillin 3 CT Clostridium difficile CD vancomycin 20 1983 2016 3 CD 7 Clostridium difficile CD CD associated diarrhea : CDAD CD 1,2 PPI 3 1 36 33 2015 8 6 5 5
37, 9-14, 2017 : 36 2015 8 6 cefcapene piperacillin 3 CT Clostridium difficile CD vancomycin 20 1983 2016 3 CD 7 Clostridium difficile CD CD associated diarrhea : CDAD CD 1,2 PPI 3 1 36 33 2015 8 6 5 5
(事務連絡)公知申請に係る前倒し保険適用通知
 保医発 0425 第 1 号 平成 30 年 4 月 25 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 ( 公印省略 ) 公知申請に係る事前評価が終了した医薬品の保険上の取扱いについて 本日開催の薬事 食品衛生審議会医薬品第二部会において
保医発 0425 第 1 号 平成 30 年 4 月 25 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 ( 公印省略 ) 公知申請に係る事前評価が終了した医薬品の保険上の取扱いについて 本日開催の薬事 食品衛生審議会医薬品第二部会において
8) 引用文献 参考資料 ( 病理検査所見 ) 1. Kaplowitz N and DeLeeve LD. Drug-induced liver disease Marcel Dekker, Inc. NY. USA. (2003) 2. 野本実 青柳豊 : 病理組織学的検討からみた診断と予後推定
 8) 引用文献 参考資料 ( 病理検査所見 ) 1. Kaplowitz N and DeLeeve LD. Drug-induced liver disease Marcel Dekker, Inc. NY. USA. (2003) 2. 野本実 青柳豊 : 病理組織学的検討からみた診断と予後推定. 医学のあゆみ 214: 785-790 (2005) ( 発生機序 ) 3. Kaplowitz
8) 引用文献 参考資料 ( 病理検査所見 ) 1. Kaplowitz N and DeLeeve LD. Drug-induced liver disease Marcel Dekker, Inc. NY. USA. (2003) 2. 野本実 青柳豊 : 病理組織学的検討からみた診断と予後推定. 医学のあゆみ 214: 785-790 (2005) ( 発生機序 ) 3. Kaplowitz
<4D F736F F D B A814089FC92F982CC82A8926D82E782B95F E31328C8E5F5F E646F63>
 - 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ 抗悪性腫瘍剤 ( ブルトン型チロシンキナーゼ阻害剤 ) ( 一般名 : イブルチニブ ) 2016 年 12 月 この度 抗悪性腫瘍剤 イムブルビカ カプセル 140 mg ( 以下標記製品 ) につきまして 再発又は難治性のマントル細胞リンパ腫 の効能追加承認を取得したことに伴い
- 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ 抗悪性腫瘍剤 ( ブルトン型チロシンキナーゼ阻害剤 ) ( 一般名 : イブルチニブ ) 2016 年 12 月 この度 抗悪性腫瘍剤 イムブルビカ カプセル 140 mg ( 以下標記製品 ) につきまして 再発又は難治性のマントル細胞リンパ腫 の効能追加承認を取得したことに伴い
ケブザラ皮下注 150mg/200mg シリンジ ケブザラ皮下注 150mg/200mg オートインジェクターに係る医薬品リスク管理計画書 (RMP) の概要 販売名 製造販売業者 1 ケブザラ皮下注 150mg シリンジ 2 ケブザラ皮下注 200mg シリンジ 3 ケブザラ皮下注 150mg オ
 ケブザラ皮下注 150mgシリンジケブザラ皮下注 200mgシリンジケブザラ皮下注 150mgオートインジェクターケブザラ皮下注 200mgオートインジェクターに係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はサノフィ株式会社にあります 当該情報を適正使用以外の営利目的で利用することはできません サノフィ株式会社 ケブザラ皮下注 150mg/200mg シリンジ
ケブザラ皮下注 150mgシリンジケブザラ皮下注 200mgシリンジケブザラ皮下注 150mgオートインジェクターケブザラ皮下注 200mgオートインジェクターに係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はサノフィ株式会社にあります 当該情報を適正使用以外の営利目的で利用することはできません サノフィ株式会社 ケブザラ皮下注 150mg/200mg シリンジ
改訂の理由及び調査の結果直近 3 年度の国内副作用症例の集積状況 転帰死亡症例 アモキシシリン水和物及びクラブラン酸カリウム アモキシシリン水和物の国内症例が集積したことから 専門委員の意見も踏まえた調査の結果 改訂することが適切と判断した 血小板減少関連症例 1 アモキシシリン水和物 3 例 (
 アモキシシリン水和物含有製剤の 使用上の注意 の改訂について 成分名該当商品名効能 効果改訂の概要 成分名該当商品名 ( 承認取得者 ) 1 アモキシシリン水和物 1 サワシリンカプセル 125 同カプセ 2 クラブラン酸カリウル 250 同細粒 10% 同錠 250( アム アモキシシリン水ステラス製薬株式会社 ) パセト和物シンカプセル 125 同カプセル 3 ランソプラゾール ア 250 同細粒
アモキシシリン水和物含有製剤の 使用上の注意 の改訂について 成分名該当商品名効能 効果改訂の概要 成分名該当商品名 ( 承認取得者 ) 1 アモキシシリン水和物 1 サワシリンカプセル 125 同カプセ 2 クラブラン酸カリウル 250 同細粒 10% 同錠 250( アム アモキシシリン水ステラス製薬株式会社 ) パセト和物シンカプセル 125 同カプセル 3 ランソプラゾール ア 250 同細粒
スライド 1
 1/5 PMDA からの医薬品適正使用のお願い ( 独 ) 医薬品医療機器総合機構 No.6 2012 年 1 月 ラミクタール錠 ( ラモトリギン ) の重篤皮膚障害と用法 用量遵守 早期発見について ラミクタール錠は 用法 用量 を遵守せず投与した場合に皮膚障害の発現率が高くなることが示されている ( 表 1 参照 ) ため 用法 用量 を遵守することが平成 20 年 10 月の承認時より注意喚起されています
1/5 PMDA からの医薬品適正使用のお願い ( 独 ) 医薬品医療機器総合機構 No.6 2012 年 1 月 ラミクタール錠 ( ラモトリギン ) の重篤皮膚障害と用法 用量遵守 早期発見について ラミクタール錠は 用法 用量 を遵守せず投与した場合に皮膚障害の発現率が高くなることが示されている ( 表 1 参照 ) ため 用法 用量 を遵守することが平成 20 年 10 月の承認時より注意喚起されています
慢性膵炎
 - - 121 , g CCK g g - kgkcal kgkcal - g,,, - G.I.Res ; 10 : - ; 13 : - ; 22 : - Meier RF, Beglinger C. Nutrition in pancreatic diseases. Best Pract Res Clin Gastroenterol ; 20 : - Pfutzer RH, Schneider
- - 121 , g CCK g g - kgkcal kgkcal - g,,, - G.I.Res ; 10 : - ; 13 : - ; 22 : - Meier RF, Beglinger C. Nutrition in pancreatic diseases. Best Pract Res Clin Gastroenterol ; 20 : - Pfutzer RH, Schneider
査を実施し 必要に応じ適切な措置を講ずること (2) 本品の警告 効能 効果 性能 用法 用量及び使用方法は以下のとお りであるので 特段の留意をお願いすること なお その他の使用上の注意については 添付文書を参照されたいこと 警告 1 本品投与後に重篤な有害事象の発現が認められていること 及び本品
 薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
Microsoft Word - ①【修正】B型肝炎 ワクチンにおける副反応の報告基準について
 資料 1 B 型肝炎ワクチンの副反応報告基準について 予防接種法における副反応報告制度について 制度の趣旨副反応報告制度は 予防接種後に生じる種々の身体的反応や副反応が疑われる症状等について情報を収集し ワクチンの安全性について管理 検討を行うことで 広く国民に情報を提供すること及び今後の予防接種行政の推進に資することを目的としている 報告の義務 予防接種法第 12 条 1 項 ( 参考資料 1)
資料 1 B 型肝炎ワクチンの副反応報告基準について 予防接種法における副反応報告制度について 制度の趣旨副反応報告制度は 予防接種後に生じる種々の身体的反応や副反応が疑われる症状等について情報を収集し ワクチンの安全性について管理 検討を行うことで 広く国民に情報を提供すること及び今後の予防接種行政の推進に資することを目的としている 報告の義務 予防接種法第 12 条 1 項 ( 参考資料 1)
<4D6963726F736F667420576F7264202D208F64937882CC89BA979F816948508C668DDA94C5816A2E646F6378>
 減 されることが 報 告 されている(ペメトレキセドナトリウムの 添 付 文 書 警 告 欄 もしくは 文 献 9,10) を 参 照 ) メルファランを 前 処 置 として 用 いた 造 血 幹 細 胞 移 植 の 施 行 に 際 しては 腹 部 への 追 加 照 射 を 避 ける 抗 菌 薬 の 長 期 投 与 を 避 ける 等 の 注 意 が 必 要 で ある 11) また 最 近 高 用 量
減 されることが 報 告 されている(ペメトレキセドナトリウムの 添 付 文 書 警 告 欄 もしくは 文 献 9,10) を 参 照 ) メルファランを 前 処 置 として 用 いた 造 血 幹 細 胞 移 植 の 施 行 に 際 しては 腹 部 への 追 加 照 射 を 避 ける 抗 菌 薬 の 長 期 投 与 を 避 ける 等 の 注 意 が 必 要 で ある 11) また 最 近 高 用 量
<4D F736F F D204E6F C82518DC490B C790AB956E8C8C2E646F63>
 重篤副作用疾患別対応マニュアル 再生不良性貧血 ( 汎血球減少症 ) 平成 19 年 6 月 厚生労働省 本マニュアルの作成に当たっては 学術論文 各種ガイドライン 厚生労働科学研究事業報告書 独立行政法人医薬品医療機器総合機構の保健福祉事業報告書等を参考に 厚生労働省の委託により 関係学会においてマニュアル作成委員会を組織し 社団法人日本病院薬剤師会とともに議論を重ねて作成されたマニュアル案をもとに
重篤副作用疾患別対応マニュアル 再生不良性貧血 ( 汎血球減少症 ) 平成 19 年 6 月 厚生労働省 本マニュアルの作成に当たっては 学術論文 各種ガイドライン 厚生労働科学研究事業報告書 独立行政法人医薬品医療機器総合機構の保健福祉事業報告書等を参考に 厚生労働省の委託により 関係学会においてマニュアル作成委員会を組織し 社団法人日本病院薬剤師会とともに議論を重ねて作成されたマニュアル案をもとに
医師主導治験 急性脊髄損傷患者に対する顆粒球コロニー刺激因子を用いたランダム化 プラセボ対照 二重盲検並行群間比較試験第 III 相試験 千葉大学大学院医学研究院整形外科 千葉大学医学部附属病院臨床試験部 1
 医師主導治験 急性脊髄損傷患者に対する顆粒球コロニー刺激因子を用いたランダム化 プラセボ対照 二重盲検並行群間比較試験第 III 相試験 千葉大学大学院医学研究院整形外科 千葉大学医学部附属病院臨床試験部 1 顆粒球コロニー刺激因子 (Granulocyte Colony-Stimulating Factor: G-CSF) 一般名 : フィルグラスチム 調達法 国内企業より無償提供 製造元または供給元の名称協和発酵キリン
医師主導治験 急性脊髄損傷患者に対する顆粒球コロニー刺激因子を用いたランダム化 プラセボ対照 二重盲検並行群間比較試験第 III 相試験 千葉大学大学院医学研究院整形外科 千葉大学医学部附属病院臨床試験部 1 顆粒球コロニー刺激因子 (Granulocyte Colony-Stimulating Factor: G-CSF) 一般名 : フィルグラスチム 調達法 国内企業より無償提供 製造元または供給元の名称協和発酵キリン
<4D F736F F D208D B B835896F2938A975E82CC8D6C82A695FB2E646F63>
 事務連絡平成 21 年 5 月 28 日 都道府県 各 保健所設置市 衛生主管部 ( 局 ) 特別区 感染症対策担当者及び新型インフルエンザ対策担当者殿 厚生労働省新型インフルエンザ対策推進本部事務局 新型インフルエンザの診療等に関する情報 ( 抗インフルエンザ薬の予防投与の考え方等 ) に係る Q&A の送付について 平成 21 年 5 月 3 日付新型インフルエンザ対策推進本部事務連絡 新型インフルエンザの診療等に関する情報
事務連絡平成 21 年 5 月 28 日 都道府県 各 保健所設置市 衛生主管部 ( 局 ) 特別区 感染症対策担当者及び新型インフルエンザ対策担当者殿 厚生労働省新型インフルエンザ対策推進本部事務局 新型インフルエンザの診療等に関する情報 ( 抗インフルエンザ薬の予防投与の考え方等 ) に係る Q&A の送付について 平成 21 年 5 月 3 日付新型インフルエンザ対策推進本部事務連絡 新型インフルエンザの診療等に関する情報
スライド 1
 医薬品副作用報告 中部ろうさい病院薬剤部 2016 年 4 月 1 日 1 中部ろうさい病院副作用報告の書式について 下記ダウンロードページにアクセスしていただき 必要なファイルをダウンロードしてください 書式のファイルは 副作用報告 のリンク先のページに置いてあります ダウンロードページURL http://www.chubuh.johas.go.jp/clinicaltrial/database/
医薬品副作用報告 中部ろうさい病院薬剤部 2016 年 4 月 1 日 1 中部ろうさい病院副作用報告の書式について 下記ダウンロードページにアクセスしていただき 必要なファイルをダウンロードしてください 書式のファイルは 副作用報告 のリンク先のページに置いてあります ダウンロードページURL http://www.chubuh.johas.go.jp/clinicaltrial/database/
Microsoft Word - 難聴(HP掲載版).docx
 8. 遺伝子検査 現在 ミトコンドリア遺伝子 555A G 変異の遺伝子検査は保険適応になっ ていないが 臨床検査の受託検査として外注検査が可能になっている 9. 引用文献 参考資料 ) Usami S, Abe S, Kasai M, Shinkawa H, Moeller B, Kenyon JB, Kimberling WJ. Genetic and clinical features of
8. 遺伝子検査 現在 ミトコンドリア遺伝子 555A G 変異の遺伝子検査は保険適応になっ ていないが 臨床検査の受託検査として外注検査が可能になっている 9. 引用文献 参考資料 ) Usami S, Abe S, Kasai M, Shinkawa H, Moeller B, Kenyon JB, Kimberling WJ. Genetic and clinical features of
審査結果 平成 25 年 9 月 27 日 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 審査結果 ] 平成 25 年 4 月 26 日開
![審査結果 平成 25 年 9 月 27 日 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 審査結果 ] 平成 25 年 4 月 26 日開 審査結果 平成 25 年 9 月 27 日 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 審査結果 ] 平成 25 年 4 月 26 日開](/thumbs/53/31072016.jpg) 審査報告書 平成 25 年 9 月 27 日独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 剤形 含量 ]
審査報告書 平成 25 年 9 月 27 日独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 剤形 含量 ]
ケブザラ皮下注 150mg/200mg シリンジに係る医薬品リスク管理計画書 (RMP) の概要 販売名 1 ケブザラ皮下注 150mg シリンジ 2 ケブザラ皮下注 200mg シリンジ 有効成分 サリルマブ ( 遺伝子組換え ) 製造販売業者 サノフィ株式会社 薬効分類 399 提出年月 平成
 ケブザラ皮下注 150mgシリンジケブザラ皮下注 200mgシリンジに係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はサノフィ株式会社にあります 当該情報を適正使用以外の営利目的で利用することはできません サノフィ株式会社 ケブザラ皮下注 150mg/200mg シリンジに係る医薬品リスク管理計画書 (RMP) の概要 販売名 1 ケブザラ皮下注 150mg シリンジ
ケブザラ皮下注 150mgシリンジケブザラ皮下注 200mgシリンジに係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はサノフィ株式会社にあります 当該情報を適正使用以外の営利目的で利用することはできません サノフィ株式会社 ケブザラ皮下注 150mg/200mg シリンジに係る医薬品リスク管理計画書 (RMP) の概要 販売名 1 ケブザラ皮下注 150mg シリンジ
目次
 第 5 章 医薬品の安全管理情報の提供 伝達 医薬品の製造販売業者は 薬事法の規定により 医薬品の有効性 安全性及び品質等医薬品の適正な使用のために必要な情報を収集し検討するとともに これらの情報を医薬関係者へ提供することが義務づけられている この目的のため 医薬品の製造販売業者は GVP 省令の規定に基づき手順書を作成し これに従って 医薬品の安全管理情報の提供 伝達について総合的な体制の整備に努めている
第 5 章 医薬品の安全管理情報の提供 伝達 医薬品の製造販売業者は 薬事法の規定により 医薬品の有効性 安全性及び品質等医薬品の適正な使用のために必要な情報を収集し検討するとともに これらの情報を医薬関係者へ提供することが義務づけられている この目的のため 医薬品の製造販売業者は GVP 省令の規定に基づき手順書を作成し これに従って 医薬品の安全管理情報の提供 伝達について総合的な体制の整備に努めている
<4D F736F F D204E6F C82558C8C8FAC94C28CB88FAD8FC72E646F63>
 重篤副作用疾患別対応マニュアル 血小板減少症 平成 19 年 6 月 厚生労働省 本マニュアルの作成に当たっては 学術論文 各種ガイドライン 厚生労働科学研究事業報告書 独立行政法人医薬品医療機器総合機構の保健福祉事業報告書等を参考に 厚生労働省の委託により 関係学会においてマニュアル作成委員会を組織し 社団法人日本病院薬剤師会とともに議論を重ねて作成されたマニュアル案をもとに 重篤副作用総合対策検討会で検討され取りまとめられたものである
重篤副作用疾患別対応マニュアル 血小板減少症 平成 19 年 6 月 厚生労働省 本マニュアルの作成に当たっては 学術論文 各種ガイドライン 厚生労働科学研究事業報告書 独立行政法人医薬品医療機器総合機構の保健福祉事業報告書等を参考に 厚生労働省の委託により 関係学会においてマニュアル作成委員会を組織し 社団法人日本病院薬剤師会とともに議論を重ねて作成されたマニュアル案をもとに 重篤副作用総合対策検討会で検討され取りまとめられたものである
Candida albicans In Vitro Diagnostics (13)--D-Glucan Determination Reagents
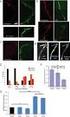 D 012 Candida albicans In Vitro Diagnostics (13)--D-Glucan Determination Reagents DATA : 1 DATA : 2 3 DATA : UNGITEC 1 1 DATA : 20pg/mL 1020pg/mL 10pg/mL (cut off 20pg/mL) 90.2%(37/41) 100%(85/85) 96.8%(122/126)
D 012 Candida albicans In Vitro Diagnostics (13)--D-Glucan Determination Reagents DATA : 1 DATA : 2 3 DATA : UNGITEC 1 1 DATA : 20pg/mL 1020pg/mL 10pg/mL (cut off 20pg/mL) 90.2%(37/41) 100%(85/85) 96.8%(122/126)
用法 用量 発作性夜間ヘモグロビン尿症における溶血抑制 mg mg mg mg kg 30kg 40kg 20kg 30kg 10kg 20kg 5kg 10kg 1900mg mg mg mg
 C EculizumabGenetical Recombination AMX 警告 1 2 禁忌 ( 次の患者には投与しないこと ) 1 2 組成 性状 ml mg mg mg mg mg ph ph mgml 効能 効果 発作性夜間ヘモグロビン尿症における溶血抑制 < 効能 効果に関連する使用上の注意 > 共通 1C5 C5b-9 b 発作性夜間ヘモグロビン尿症における溶血抑制 1 2 3 4
C EculizumabGenetical Recombination AMX 警告 1 2 禁忌 ( 次の患者には投与しないこと ) 1 2 組成 性状 ml mg mg mg mg mg ph ph mgml 効能 効果 発作性夜間ヘモグロビン尿症における溶血抑制 < 効能 効果に関連する使用上の注意 > 共通 1C5 C5b-9 b 発作性夜間ヘモグロビン尿症における溶血抑制 1 2 3 4
Clinical Observation and Etiological Aspect on the Thrombocytopenic Purpura after Rubella Toyoji SODA, Masashi KAWANO, Toshihiko KATO*, and Takeshi SH
 Clinical Observation and Etiological Aspect on the Thrombocytopenic Purpura after Rubella Toyoji SODA, Masashi KAWANO, Toshihiko KATO*, and Takeshi SHIGEMATSU**, Rubella is an acute viral infectious disease
Clinical Observation and Etiological Aspect on the Thrombocytopenic Purpura after Rubella Toyoji SODA, Masashi KAWANO, Toshihiko KATO*, and Takeshi SHIGEMATSU**, Rubella is an acute viral infectious disease
MEDLINE
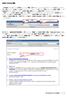 MeSH Database 機能 PubMed では 各データに MeSH( メッシュ ) 用語と呼ばれるコントロールされたキーワードが付与されています 例えば癌のように cancer や tumor などキーワードがいくつか考えられる概念であっても MeSH 用語としては neoplasms の 1 つに決められており MeSH 用語を使用することで的確な検索ができるようになっています 検索フィールドを特に
MeSH Database 機能 PubMed では 各データに MeSH( メッシュ ) 用語と呼ばれるコントロールされたキーワードが付与されています 例えば癌のように cancer や tumor などキーワードがいくつか考えられる概念であっても MeSH 用語としては neoplasms の 1 つに決められており MeSH 用語を使用することで的確な検索ができるようになっています 検索フィールドを特に
薬事法における病院及び医師に対する主な規制について 特定生物由来製品に係る説明 ( 法第 68 条の 7 平成 14 年改正 ) 特定生物由来製品の特性を踏まえ 製剤のリスクとベネフィットについて患者に説明を行い 理解を得るように努めることを これを取り扱う医師等の医療関係者に義務づけたもの ( 特
 薬事法における病院及び医師に対する主な規制について 情報の提供等 ( 法第 77 条の 3 第 2 項及び第 3 項 第 2 項 : 昭和 54 年改正 第 3 項 : 平成 6 年改正 ) 医薬品の製造販売業者等が行う医薬品又は医療機器の適正な使用のために必要な情報の収集に協力するよう努めることを また 医薬品及び医療機器の適正な使用を確保するため 医薬品の製造販売業者等から提供される情報の活用その他必要な情報の収集
薬事法における病院及び医師に対する主な規制について 情報の提供等 ( 法第 77 条の 3 第 2 項及び第 3 項 第 2 項 : 昭和 54 年改正 第 3 項 : 平成 6 年改正 ) 医薬品の製造販売業者等が行う医薬品又は医療機器の適正な使用のために必要な情報の収集に協力するよう努めることを また 医薬品及び医療機器の適正な使用を確保するため 医薬品の製造販売業者等から提供される情報の活用その他必要な情報の収集
Key words: pure red cell anemia, allogeneic bone marrow transplantation.
 Complete Recovery of Hemopoiesis Following Bone Marrow Transplantation in a Patient with Unresponsive Congenital Pure Red Cell Anemia Masami SHIMADA, Hideo MUGISHIMA, Mitsuhiko HARA, Masahiro MISAWA, Hideo
Complete Recovery of Hemopoiesis Following Bone Marrow Transplantation in a Patient with Unresponsive Congenital Pure Red Cell Anemia Masami SHIMADA, Hideo MUGISHIMA, Mitsuhiko HARA, Masahiro MISAWA, Hideo
untitled
 1 2 3 http://www.info.pmda.go.jp/ 4 5 6 7 8 9 10 11 (Quincke s edema) 12 13 梗 疼 () 14 15 J Allergy Clin Immunol 115;S483-S523, 2005 16 17 IgE IgE IgE 18 19 20 21 腿 22 Hydrocortisone 100 200 mg 5 mg/kg
1 2 3 http://www.info.pmda.go.jp/ 4 5 6 7 8 9 10 11 (Quincke s edema) 12 13 梗 疼 () 14 15 J Allergy Clin Immunol 115;S483-S523, 2005 16 17 IgE IgE IgE 18 19 20 21 腿 22 Hydrocortisone 100 200 mg 5 mg/kg
スライド 1
 1 2006 msv 2 2011 3 CT 2011 10mSv 10 40mSv 4 2012 217mSv 5 (CT) 2012 50 60mSv 6 2012 510mSv BRCA25 310 10mSv3% BRCA60-280% 3 5m Sv 1m Sv 12% . http://www.rea.or.jp/ire/pdf/report4.pdf 1.10 20 SMR 1.00
1 2006 msv 2 2011 3 CT 2011 10mSv 10 40mSv 4 2012 217mSv 5 (CT) 2012 50 60mSv 6 2012 510mSv BRCA25 310 10mSv3% BRCA60-280% 3 5m Sv 1m Sv 12% . http://www.rea.or.jp/ire/pdf/report4.pdf 1.10 20 SMR 1.00
 Survey of the Incidence of Dry Cough Caused by ACE Inhibitors MOTOHIRO YAGI*, MIKIO SAITO, MANABU ABE and KATSUJI UNO Pharmacy, Suibarago Hospital õ Received October 24, 1996 Accepted September 3, 1997
Survey of the Incidence of Dry Cough Caused by ACE Inhibitors MOTOHIRO YAGI*, MIKIO SAITO, MANABU ABE and KATSUJI UNO Pharmacy, Suibarago Hospital õ Received October 24, 1996 Accepted September 3, 1997
Microsoft PowerPoint - C-2_武蔵野赤十字病院_Hosoya Discovery Japan 2017配布用.pptx
 Japan Discovery Summit 2017 大規模副作用情報データベースに基づくしゃっくり誘発因子の解析 細谷龍一郎 1,2 植沢芳広 1 野澤 ( 石井 ) 玲子 1 加賀谷肇 1 1 明治薬科大学臨床薬剤学研究室 2 武蔵野赤十字病院薬剤部 しゃっくり ( 吃逆 ) しゃくりは神経反射の一種 横隔膜による吸気運動と声門の閉鎖が同時に発生 特徴的は発生音 ヒック! 英名は Hiccups
Japan Discovery Summit 2017 大規模副作用情報データベースに基づくしゃっくり誘発因子の解析 細谷龍一郎 1,2 植沢芳広 1 野澤 ( 石井 ) 玲子 1 加賀谷肇 1 1 明治薬科大学臨床薬剤学研究室 2 武蔵野赤十字病院薬剤部 しゃっくり ( 吃逆 ) しゃくりは神経反射の一種 横隔膜による吸気運動と声門の閉鎖が同時に発生 特徴的は発生音 ヒック! 英名は Hiccups
<4D F736F F D204A204D484C578D5A897B8CE320979A97F082C882B52093FA967B82CC96F28E968D7390AD D30332E646F63>
 第 5 章 医薬品の安全管理情報の提供 伝達 医薬品の製造販売業者は 薬事法の規定により 医薬品の有効性 安全性及び品質等医薬品の適正な使用のために必要な情報を収集し検討するとともに これらの情報を医薬関係者へ提供することが義務づけられている この目的のため 医薬品の製造販売業者は GVP 省令の規定に基づき手順書を作成し これに従って 医薬品の安全管理情報の提供 伝達について総合的な体制の整備に努めている
第 5 章 医薬品の安全管理情報の提供 伝達 医薬品の製造販売業者は 薬事法の規定により 医薬品の有効性 安全性及び品質等医薬品の適正な使用のために必要な情報を収集し検討するとともに これらの情報を医薬関係者へ提供することが義務づけられている この目的のため 医薬品の製造販売業者は GVP 省令の規定に基づき手順書を作成し これに従って 医薬品の安全管理情報の提供 伝達について総合的な体制の整備に努めている
審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ]
![審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ] 審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ]](/thumbs/91/105024304.jpg) 審査報告書 平成 26 年 2 月 7 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所
審査報告書 平成 26 年 2 月 7 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所
 E Societe de Pathologie Infectieuse de Langue Francaise (, 1991) E Spanish Thoracic Society (1992) E American Thoracic Society (ATS : 1993. ü ù2001 ) E British Thoracic Society (1993, ü è2001 ) E Canadian
E Societe de Pathologie Infectieuse de Langue Francaise (, 1991) E Spanish Thoracic Society (1992) E American Thoracic Society (ATS : 1993. ü ù2001 ) E British Thoracic Society (1993, ü è2001 ) E Canadian
2 有効成分名 添付文書及び審査報告書に基づき記載する 3 品目名 ( 後発医薬品 ) 添付文書及び審査報告書のほか薬価基準収載品目リストにより記載する 複数の品目がある場合は 個別医薬品コード (YJ コード ) 順に番号を振り 記載する ( 複数規格があっても 全規格まとめて YJ コード順とす
 第 18 回ジェネリック医薬品品質情報検討会 参考資料 2 医療用医薬品最新品質情報集 ( ブルーブック ) 作成要領 ( 案 ) 1 対象品目 別途定めるブルーブック作成対象品目に基づく なお 薬価削除経過措置期間中のものは記載対象外とする 2 記載項目 1 作成年月日 2 有効成分名 3 品目名 ( 後発医薬品 ) 4 品目名 ( 先発医薬品 ) 5 効能 効果 6 用法 用量 7 添加物 8
第 18 回ジェネリック医薬品品質情報検討会 参考資料 2 医療用医薬品最新品質情報集 ( ブルーブック ) 作成要領 ( 案 ) 1 対象品目 別途定めるブルーブック作成対象品目に基づく なお 薬価削除経過措置期間中のものは記載対象外とする 2 記載項目 1 作成年月日 2 有効成分名 3 品目名 ( 後発医薬品 ) 4 品目名 ( 先発医薬品 ) 5 効能 効果 6 用法 用量 7 添加物 8
Taro-01_告示(本文)案分
 厚生労働省告示第三百十二号厚生労働大臣が指定する病院の病棟における療養に要する費用の額の算定方法(平成二十年厚生労働省告示第九十三号)第一項第五号及び別表の規定に基づき 厚生労働大臣が定める傷病名 手術19 処置等及び定義副傷病名及び厚生労働大臣が指定する病院の病棟における療養に要する費用の額の算定方法第一項第五号の規定に基づき厚生労働大臣が別に定める者の一部を改正する告示を次のように定め 平成三十年八月二十九日から適用する
厚生労働省告示第三百十二号厚生労働大臣が指定する病院の病棟における療養に要する費用の額の算定方法(平成二十年厚生労働省告示第九十三号)第一項第五号及び別表の規定に基づき 厚生労働大臣が定める傷病名 手術19 処置等及び定義副傷病名及び厚生労働大臣が指定する病院の病棟における療養に要する費用の額の算定方法第一項第五号の規定に基づき厚生労働大臣が別に定める者の一部を改正する告示を次のように定め 平成三十年八月二十九日から適用する
VOL. 21 NO. 2 CHEMOTHERAPY 395
 394 CHEMOTHERAPY MAR. 1973 VOL. 21 NO. 2 CHEMOTHERAPY 395 396 CHEMOTHERAPY MAR. 1973 VOL. 21 NO. 2 CHEMOTHERAPY 397 398 CHEMOTHERAPY MAR. 1973 VOL. 2 1 NO. 2 CHEMOTHERAPY 399 400 CHEMOTHERAPY MAR. 1973
394 CHEMOTHERAPY MAR. 1973 VOL. 21 NO. 2 CHEMOTHERAPY 395 396 CHEMOTHERAPY MAR. 1973 VOL. 21 NO. 2 CHEMOTHERAPY 397 398 CHEMOTHERAPY MAR. 1973 VOL. 2 1 NO. 2 CHEMOTHERAPY 399 400 CHEMOTHERAPY MAR. 1973
Microsoft Word - 日薬連宛抗インフル薬通知(写).doc
 薬生安発 0821 第 1 号 平成 3 0 年 8 月 2 1 日 日本製薬団体連合会 安全性委員会委員長 殿 厚生労働省医薬 生活衛生局医薬安全対策課長 抗インフルエンザウイルス薬の 使用上の注意 の改訂について 平成 30 年度第 1 回薬事 食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会 ( 平成 30 年 5 月 16 日開催 ) 及び平成 30 年度第 4 回薬事 食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会
薬生安発 0821 第 1 号 平成 3 0 年 8 月 2 1 日 日本製薬団体連合会 安全性委員会委員長 殿 厚生労働省医薬 生活衛生局医薬安全対策課長 抗インフルエンザウイルス薬の 使用上の注意 の改訂について 平成 30 年度第 1 回薬事 食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会 ( 平成 30 年 5 月 16 日開催 ) 及び平成 30 年度第 4 回薬事 食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会
過去の医薬品等の健康被害から学ぶもの
 新薬による薬害事件を如何に防ぐか - ソリブジン事件とイレッサ事件から学ぶ - 土井脩 ( 医薬品医療機器レギュラトリーサイエンス財団 ) Pharmaceutical and Medical Device Regulatory Science Society of Japan 2019.01.01 ( レギュラトリーサイエンスエキスパート研修会 薬害教育 ) 研修用教材としてまとめたものであり 公式見解などをまとめたものではありません
新薬による薬害事件を如何に防ぐか - ソリブジン事件とイレッサ事件から学ぶ - 土井脩 ( 医薬品医療機器レギュラトリーサイエンス財団 ) Pharmaceutical and Medical Device Regulatory Science Society of Japan 2019.01.01 ( レギュラトリーサイエンスエキスパート研修会 薬害教育 ) 研修用教材としてまとめたものであり 公式見解などをまとめたものではありません
 CHEMOTHERAPY AUG. 1982 VOL. 30 NO. 8 CHEMOTHERAPY Fig.1 Relation between various-closis of cefazolin and detection rate of organisms in heart blood of dying mice with E. coli and P. aeruginosa infection
CHEMOTHERAPY AUG. 1982 VOL. 30 NO. 8 CHEMOTHERAPY Fig.1 Relation between various-closis of cefazolin and detection rate of organisms in heart blood of dying mice with E. coli and P. aeruginosa infection
本日の内容 1. 未承認対照薬等の取り扱い別添の 4.(3) ウ.( ア ) 2. 対象疾患の悪化等を評価項目にする試験別添の 7.(3) イ.( ア ) 3. 承認取得者以外の治験国内管理人が治験 依頼者となる場合別添の7.(3) オ. 4. 医師主導治験との情報共有別添の7.(3) カ. 5.
 治験の安全性対応シンポジウム 安全性二課長通知の改訂点平成 25 年 5 月 15 日付二課長通知 ( 薬食審査発 0515 第 1 号 薬食安発 0515 第 1 号 ) 2013 年 12 月 16 日 日本製薬工業協会医薬品評価委員会臨床評価部会五十嵐元 山城恭子 1 本日の内容 1. 未承認対照薬等の取り扱い別添の 4.(3) ウ.( ア ) 2. 対象疾患の悪化等を評価項目にする試験別添の
治験の安全性対応シンポジウム 安全性二課長通知の改訂点平成 25 年 5 月 15 日付二課長通知 ( 薬食審査発 0515 第 1 号 薬食安発 0515 第 1 号 ) 2013 年 12 月 16 日 日本製薬工業協会医薬品評価委員会臨床評価部会五十嵐元 山城恭子 1 本日の内容 1. 未承認対照薬等の取り扱い別添の 4.(3) ウ.( ア ) 2. 対象疾患の悪化等を評価項目にする試験別添の
員長及び医薬品医療機器等法登録認証機関協議会代表幹事宛て送付するこ ととしていることを申し添えます 記 1. 基本要件基準第 13 条第 5 項及び第 6 項への適合性確認の基本的な考え方について (1)2023 年 ( 平成 35 年 )2 月 28 日 ( 以下 経過措置期間終了日 という )
 薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
レキサルティに係る医薬品リスク管理計画書 (RMP) の概要 ( 別紙様式 ) レキサルティ錠 1mg 販売名有効成分ブレクスピプラゾールレキサルティ錠 2mg 製造販売業者大塚製薬株式会社薬効分類 安全性検討事項 提出年月 重要な特定されたリスク 平成 30 年 5 月 錐
 レキサルティ錠 1 mgレキサルティ錠 2 mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任は大塚製薬株式会社にありま す 当該製品の適正使用に利用する以外の営利目的に本資料を利用することはできません 大塚製薬株式会社 レキサルティに係る医薬品リスク管理計画書 (RMP) の概要 ( 別紙様式 ) レキサルティ錠 1mg 販売名有効成分ブレクスピプラゾールレキサルティ錠
レキサルティ錠 1 mgレキサルティ錠 2 mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任は大塚製薬株式会社にありま す 当該製品の適正使用に利用する以外の営利目的に本資料を利用することはできません 大塚製薬株式会社 レキサルティに係る医薬品リスク管理計画書 (RMP) の概要 ( 別紙様式 ) レキサルティ錠 1mg 販売名有効成分ブレクスピプラゾールレキサルティ錠
なお,PMDA メディナビでパスワードを設定済の方は, 共通のパスワードとなります (4) 登録完了 ( 図 2 ステップ 3) なお, 登録後, ログイン時は (1) で表示される画面で, ログイン画面へ をクリックし, メー ルアドレス及びパスワードを入力してください 図 1 PMDA メディナ
 2 マイ医薬品集作成サービス について 独立行政法人医薬品医療機器総合機構 (PMDA) では,PMDAメディナビ( 医薬品医療機器情報配信サービス ) にご登録いただいている方がご利用いただける登録 利用無料の追加機能として, マイ医薬品作成サービス を提供しています あらかじめ情報が必要な医薬品を登録しておけば, 添付文書情報等の最新情報を一覧で管理 閲覧することができる大変便利なサービスです
2 マイ医薬品集作成サービス について 独立行政法人医薬品医療機器総合機構 (PMDA) では,PMDAメディナビ( 医薬品医療機器情報配信サービス ) にご登録いただいている方がご利用いただける登録 利用無料の追加機能として, マイ医薬品作成サービス を提供しています あらかじめ情報が必要な医薬品を登録しておけば, 添付文書情報等の最新情報を一覧で管理 閲覧することができる大変便利なサービスです



