細胞骨格を形成するタンパク質
|
|
|
- せせら ちゅうか
- 7 years ago
- Views:
Transcription
1 2 年前期生命活動を担うタンパク質 ( 第 1 回 ) タンパク質の一次構造と高次構造 (p.41-52) 生命活動を担うタンパク質生体の構成成分はいずれも生命にとって重要な機能を果たしている その中でもタンパク質は 重要なだけでなく 非常に多岐にわたる働きを有し 生命活動の仕組みを知る上では その基本的性質から学ぶ必要がある 復習タンパク質とは タンパク質は α-アミノ酸の直鎖状重合体 アミノ基とカルボキシル基がペプチド結合で繋がる アミノ酸数が 100 個以上程度のもの より短いものはペプチドと呼ぶ タンパク質を構成するアミノ酸は 20 種類 タンパク質の性質は 第一にその構成アミノ酸の種類と割合 アミノ酸の配列 そして出来上がったタンパク質にさらに付け加えられる修飾反応が大きく影響する タンパク質の構造と機能タンパク質の機能と構造の間には非常に重要な関連性があり タンパク質が非常に多様な働きを発揮できるのは それに適した形を取ることができるからである タンパク質の立体構造は 1 共有結合で固定された位置関係 2 電気的な相互作用アミノ酸側鎖間の非共有結合的な相互作用 ( 電気的な力 疎水性相互作用 水素結合 ) あるいはアミノ酸側鎖と周囲の水分子などとの相互作用によって 物理化学的に安定な状態を取ろうとすることで形作られる タンパク質が細胞内で合成される途中 そして折り畳みが完了して完全に形が出来るまでの過程では タンパク質の構造が不安定である 種々タンパク質の立体構造を安定化する作用を持つタンパク質分子シャペロンが 正しい立体構造の形成に大きく働いている タンパク質の機能は 酵素 ホルモン 受容体 など多様なものがあるが 基本的に必ず何らかの特定の分子と結合することで その作用を発揮する 分子と分子の結合は その立体構造が鍵と鍵穴のようにフィットすることが基本的な要素である 酵素 基質ホルモン ( サイトカイン ) 受容体抗体 抗原 DNA 結合タンパク質 ( 転写因子 )--- 特定の塩基配列の DNA などの対応関係 1
2 タンパク質の一次構造 (p.41,50) アミノ酸配列のことである アミノ酸配列は 遺伝子 DNA の塩基配列に対応している タンパク質のアミノ酸配列は N- 末端を 1 番目のアミノ酸とし N 末端を左側にする ジスルフィド結合により 分子内あるいは分子間の架橋が起こる 一次構造の類似性相同性 (identity) つのタンパク質の対応する位置に同じアミノ酸ホモロジー (homology: 類似性 )----- 対応する位置に同じまたは類似のアミノ酸 一例としてリゾチーム (lysozyme) の一次構造を調べてみる chicken 1 KVFGRCELAA AMKRHGLDNY RGYSLGNWVC AAKFESNFNT QATNRNTDG-S human 1 KVF-RCELAR TLKRLGMDGY RGISLANWVC LAKWESGYNT RATNYNADGRS 61 TDYGILQINS RWWCNDGR-TP GSRNLCNIPC SALLSSDITA SVNCAKKIVS 61 TDYGILQINS RYWCNDGRKTP GAVNACHLSC SALLQDNIAD AVACAKRVVS 91 -DGNGMNAWVA WRNRCKGT-DV QAWIRGCRL 91 RDPQGIRAWVA WRNRCQNRDV RQYVQGCGV 異なるタンパク質で類似の構造を共有するタンパク群を ファミリー 呼ぶ タンパク質の二次構造 (p.45) タンパク質の部分に見られる規則的な立体構造 αへリックス---- 右巻きらせんポリペプチド鎖内で水素結合 βシート---- 平行 逆平行に並ぶポリペプチド鎖間で水素結合 ペプチド結合は共鳴構造をとり部分的に平面となる タンパク質は短冊をつなげたように折り畳まることができる ペプチド結合部分の平面 β シート α へリックス 2
3 2 年前期生命活動を担うタンパク質 ( 第 1 回 ) 超二次構造二次構造部分が複数組み合わさって より多様な構成を持つ立体構造パターン βαβ 単位 β 屈曲 αα 単位 βバレルギリシャ キー タンパク質の三次構造 (p.48) 一個のタンパク質がとる立体構造( コンフォメーション :conformation) 三次構造を安定化させる要因 1) 水素結合 二次構造を安定化 親水性 2) 共有結合 ( 分子内ジスルフィド結合 ) 3) 疎水性相互作用 4) 静電的相互作用タンパク質に還元剤を作用させてジスルフィド結合を解離させると タンパク質の立体構造が壊される 還元剤を除去すると 三次構造が回復する 酸化還元のほか 加熱 ( 水素結合を壊す ) 尿素などの変性剤( 疎水性相互作用を弱める ) 酸 塩基 (ph の変化により静電的相互作用を変化 ) することによっても立体構造が壊される ドメイン (p.50)---- 一個のタンパク内部に形成される構造的にまとまった領域膜結合ドメイン DNA 結合ドメイン コラーゲン様ドメイン 抗体の可変領域 定常領域 など LDL 受容体 免疫グロブリン (IgG) 膜貫通ドメイン 3
4 タンパク質の四次構造 複数のタンパク質分子が集まって一つの複合体タンパク質を形成している状態 複合体タンパクの個々のポリペプチドをサブユニット (subunit) と呼ぶ 複合体を形成しないタンパク質 ( 単量体 ) は 四次構造を持たないことになるタンパク質の一次 ~ 四次構造まとめタンパク質の構造一次構造 ---- アミノ酸配列二次構造 ---- 特徴的な規則構造三次構造 ---- タンパク質固有の立体構造四次構造 ---- 複数のタンパク質の会合状態ドメイン ---- タンパク質の機能的まとまり部分 タンパク質は 生理的な条件下では 一次構造が決まっていれば特定の高次構造を形成する 遺伝子の DNA 塩基配列が決まれば 完成品のタンパク質の構造も決まる関係になる 遺伝子上の変異が タンパク質の高次構造に大きく影響を与えることもありうる 完成したタンパク質が さらに修飾されることで その性質 構造を変化させていく場合も多い 復習問題 ( 各文の正誤を判定し 誤り部分を直しなさい ) 1. ペプチド結合部分は平面構造を取る 2. 同じ作用を持つタンパク質でも 動物種 ( 生物種 ) が違っているとアミノ酸配列が大きく異なる場合が多い 3. 膜貫通ドメインには親水性アミノ酸が集中している 4. 分子シャペロンとは タンパク質の立体構造の安定化に関わる 5. ある 2 つのタンパク質間の相同性 (%) は それらのホモロジー (%) より高い 6. 加熱処理により タンパク質を安定化している疎水性相互作用が壊される 7. 還元剤処理により タンパク質を安定化しているジスルフィド結合が壊される 8. 界面活性剤処理により タンパク質を安定化している水素結合が壊される 9. 大量の塩により タンパク質を安定化している静電的相互作用が増強される 10. αヘリックスやβシートは アミノ酸側鎖間の水素結合によって安定化されている 11. プロリンは 特にαへリックス構造を乱しやすいアミノ酸である 12. 疎水性アミノ酸の側鎖は タンパク質の内側に集まりやすい 正解 : ( 疎水性 ) ( 低い ) 6. ( 水素結合 ) ( 疎水性相互作用 ) ( 疎水性 ) 11. ( ペプチド主鎖間 ) 12. 4
5 2 年前期生命活動を担うタンパク質 ( 第 2 回 ) 種々のタンパク質とその構造 タンパク質の構成成分から見た区別単純タンパク質 アミノ酸のみからなる( リゾチーム アクチン ヒストンなど ) 複合タンパク質 アミノ酸以外の構成成分を含む糖タンパク質 ( プロテオグリカン グリコホリン イムノグロブリンなど ) リポタンパク質 ( アポリポタンパクBなど (p.139)) 金属タンパク質 ( フェリチン (Fe) アルコールデヒドロゲナーゼ(Zn) など ) ヘムタンパク質 ( ヘモグロビン ミオグロビン シトクロム P450)(p.58) など タンパク質の機能から見た区別タンパク質は酵素以外の機能分子としても 多様な役割を持っている 1 個のタンパク質が 複数の機能を併せ持っている場合もある 構造タンパク質 コラーゲン エラスチン アクチン チューブリン酵素 トリプシン へキソキナーゼ リゾチーム輸送タンパク質 ヘモグロビン Na +,K + -ATPase アポリポタンパクB 受容体 LDL 受容体 アセチルコリン受容体情報伝達に関わるタンパク質 ホルモン 増殖因子 三量体 G タンパク質生体防御に関わるタンパク質 抗体貯蔵タンパク質 フェリチン ミオグロビン ミニ知識酵素の名前 (p.83) *****ase (*** アーゼ *** エース ) 例 ) リパーゼ (lipase = lipid + ase) アルコール脱水素酵素 ( alcohol dehydrogenase = alcohol + de + hydrogen + ase) 血漿タンパク質 ( アルブミン グロブリン フィブリノーゲンなど アルブミン : 代表的な血漿タンパク質 最も含量が多く 肝臓で作られて血液中に分泌される 分子量約 67,000 糖鎖が付加されている 可溶性タンパクであるが 脂肪酸など種々脂溶性低分子物質を結合し 運搬する ( そもそもは 動植物の体液中の可溶性タンパク質の総称 50% 硫安で沈殿しない画分に含まれる 血清アルブミン以外に オボアルブミン ラクトアルブミンなど ) 5
6 細胞膜を隔てた物質輸送に関わるタンパク質 (p ) 細胞膜の内外での物質のやり取り受容体 ある特定の分子を認識し結合するが 膜を通過させない トランスポーター -- 細胞膜内外でイオンや低分子物質を通過させる装置 物質が透過できる間隙を持った構造の膜タンパク質 チャネル 特定の刺激に応じて開閉しイオンを通過させる 細胞膜を隔てた物質の移動 (p.101) 濃度勾配 細胞の内外で物質の濃度が異なること 種々のイオンやグルコースなど 実際に多くの物質は細胞内外で濃度勾配がある 細胞内外のイオン組成 (mm) K + Na + Cl - H CO 3- 蛋白質 Mg 2+ Ca 2+ 細胞内 < 細胞外 受動拡散 濃度勾配に従って 高濃度側から低濃度側に物質が移動 促進拡散 透過する物質が選択的にトランスポーター ( キャリア ) に結合し 拡散過程が促進される 能動輸送 濃度勾配に逆らって 低濃度側から高濃度側に物質が移動 他の物質の濃度差ポテンシャルや ATP が利用される 受動拡散を行う例電位依存性チャネル K + チャネルリガンド依存性チャネル Ca 2+ チャネルアクアポリン 図 1 アクアポリンの模式図 促進拡散を行う例 GLUT 小腸粘膜細胞 膵ラ島 β 細胞などでグルコースを取り込む 細胞外の濃度を反映 GLUT 骨格筋細胞 脂肪細胞などでインスリン刺激時にグルコースを取り込む 細胞外液中の濃度を低下させる 6
7 2 年前期生命活動を担うタンパク質 ( 第 2 回 ) 血漿タンパクの種類と機能 血液中の成分血球 赤血球 白血球 血小板血漿 血液から血球成分を除いた残りの水溶成分血清 血液を凝固させたときに 固形分を除いた残りの水溶成分 ( 血液凝固因子が消失し 血小板から放出された成長因子が含まれる ) 血漿タンパク質タンパク質特徴アルブミン (albumin) 最も量が多い (35-55mg/mL) 肝臓で合成 分泌脂肪酸運搬 脂溶性薬物結合性 γ-グロブリン抗体 形質細胞 (B リンパ球が分化した細胞 ) が合成 分泌抗体は 5 種類 抗原侵入により増加する IgG が最も量が多い (8-18mg/mL) ( グロブリンは 50% 硫安で塩析されるものの総称 ) フィブリノーゲン血液凝固第 Ⅰ 因子 量が多い (2-6mg/mL) 血液凝固反応を受けてフィブリンとなり繊維化するアンチトロンビンⅢ 抗凝固因子 ヘパリンが活性化する ( mg/mL) トランスフェリン Fe イオンの運搬 (2-4mg/mL) セルロプラスミン Cu イオンの運搬 (2-5mg/mL) C 反応性タンパク質 (CRP) 炎症時に急激に増加 肝臓で合成 分泌 脂質成分の輸送体 : リポタンパク質 リポタンパク質の分類 (p155) 比重 直径 主要成分組成 生理作用 キロミクロン < ~ 10000A TG 85% 腸で吸収した脂質を肝臓へ運ぶ VLDL 0.96 ~ ( 超低比重リホ タンハ ク質 ) IDL ~ ( 中間比重リホ タンハ ク質 ) ~ 750 TG 55% 肝臓から末梢組織に脂 A コレステロール 15% 肪酸を運ぶ 220 ~ 300 TG 24% A コレステロール 46% LDL ~ 190 ~ 220 コレステロール 45% ( 低比重リホ タンハ ク質 ) A タンハ ク質 45% LDL が VLDL から形成される過程の中間体肝臓から末梢組織にコレステロールを運ぶ HDL ~ 70 ~ 100 リン脂質 25% 末梢組織から肝臓へコ ( 高比重リホ タンハ ク質 ) 1.21 A タンハ ク質 50% レステロールを運ぶ 7
8 リン脂質 タンパク質 リポタンパク質 (LDL) の模式図 コレステロリルエステル TG 粒子の中心部に疎水性の脂質 ( トリグリセリド エステルのコレステロール ) が集まり その周囲に両親媒性の脂質 ( リン脂質 遊離型のコレステロール) とタンパク質が取り巻いて包んだ形になっている このような粒子全体として 血漿中に分散している コレステロール 復習問題各文の正誤を判定し 誤りの部分は訂正せよ 1. タンパク質には アミノ酸だけでなく金属原子や糖が結合したものもある 2. タンパク質の立体構造と そのタンパク質の機能には関連がある 3. 組織や細胞の骨格 形状を作り維持する役割を持つものを構造タンパク質という 4. アルブミンは コレステロールの運搬を担う血漿タンパク質である 5. ATP のエネルギーを使って物質透過する作用を促進拡散という 6. 細胞内の Na + 濃度や Ca 2+ 濃度は 細胞外に比べて低い 7. トランスポーターは 認識した分子のみを選択的に透過させる 8. アクアポリンは水素イオンを透過させるチャネルである 9. GLUT2 と GLUT4 はどちらも小腸で作用しているグルコース輸送体である 10. アセチルコリン受容体は アセチルコリンの結合により立体構造を変える 11. 血清は血液凝固した血液から得られる水溶成分である 12. ヘパリンの抗凝固作用は アンチトロンビンⅢ の活性化による血液凝固系阻害である 13. 炎症が起こったときに CRP の血漿濃度が著しく上昇する 14. 最も比重の小さい血漿リポタンパク質は LDL( 低比重リポタンパク質 ) である 15. VLDL( 超低比重リポタンパク質 ) の主成分は トリグリセリドである 16. 腸で吸収された脂質は キロミクロンとなって小腸上皮細胞から血中に分泌される 17. LDL は LDL 受容体とともに細胞内に取り込まれる 18. フェリチンは肝臓中で鉄イオンを貯蔵するタンパク質である 正解 : ( 脂肪酸や薬物 ) 5. ( 能動輸送 ) ( 水素 水分子 ) 9. (GLU T4 は筋肉など ) ( カイロミクロン ) ( リンパ管 )
9 2 年前期生命活動を担うタンパク質 ( 第 3 回 ) タンパク質研究法 ( 第 5 章 p ) タンパク質の検出法 定量法タンパク質そのものを目で見ることは難しい 通常は タンパク質は無色 1 分子のタンパク質は 分子量数万程度 (10-19 g 程度 ) 紫外吸収を測定する 簡便 回収できる 試薬と反応させ強い色素を産生させる 汎用されている (BCA 法 B radford 法 ローリー法 ) 試薬と反応させ 蛍光物質を産生させる 高感度 全窒素量を測定する 感度が低い 煩雑 精製 : 純粋なタンパク質を分離する方法 :(p.65) 組織中 細胞内 血液中のタンパク質は 非常に多種多様である これらの生体サンプルは多様なタンパク質の混合物なので その中の特定タンパク質の性質について調べることが困難 できるだけ純度の高い単一のタンパク質を取り出す作業が求められる 沈殿分画法 硫安沈殿 ( 硫安分画 )----- 塩析 PEG( ポリエチレングリコール ) 分画 カラムクロマトグラフィーのまとめ 分離の性質 特徴 例 ゲルろ過 分子量 ( 分子 緩和な条件で タンパク質の変性は少 デキストランゲ の大きさ ) ない ル アガロース サンプルは希釈される ゲル など イオン交換 タンパク質の 緩和な条件で タンパク質の変性は少 DEAE セルロー 荷電 ない ス Q-セファロ 濃縮効果あり ースなど 疎水 ( 逆相 ) 疎水性相互作 分離能が高い ODS など 用 アフィニティ 特異的相互作 抗体と抗原のように 特異的な吸着性 抗体カラム ニ 用 をもつ成分のみを分離できる ッケルカラム 吸着したリガンドを遊離する際に タンパク質の変性が起こる可能性がある レクチンカラムなど 9
10 イオン交換クロマトグラフィー アフィニティクロマトグラフィー 抗体 - 抗原アビジン ( ストレプトアビジン )-ビオチンレクチン- 糖鎖 DNA 鎖 相補的 DNA(RNA) 鎖 ( 例 : オリゴ dt カラム-mRNA 精製 ) プロテイン A- 免疫グロブリン ( IgG) タンパク質の分子量測定 1 SDS-PAGE 法 簡便 精度が高い 2 ゲルろ過カラム法 サンプル回収が可能 多量体に適用可能 精度は低い 3 質量分析法 きわめて高精度 高価な装置が必要 10
11 2 年前期生命活動を担うタンパク質 ( 第 3 回 ) SDS-PAGE 法 (p.67) ガラス板間でアクリルアミドと N,N- メチレンビスアクリルアミドの重合反応を行い 透明のゲルを作成する ゲルは 分子の網目構造をもつので 小さい分子ほど 速やかに泳動されやすい 微量の試料で測定が可能 分離精度が高い 移動度と分子量の対数が相関 75,000 67,000 45,000 25,000 17,800 12,500 アミノ酸配列の決定法 ( p.69) 目的のタンパク質が得られたら そのアミノ酸配列を調べ タンパク質を同定する エドマン分解法質量分析法遺伝子クローニング 11
12 質量分析法 (p.71) ガス化したイオンの分子量 (e/z 値 ) を測定する装置 近年 タンパク質など気化しにくい高分子化合物のイオン化法が開発された 大きい分子量のイオンの高精度分析手法も改良された MALDI-Tof MS: マトリックス支援レーザー脱離イオン飛行時間型大きいタンパク質でも 全体の分子量が推定できる ESI-QTof: エレクトロスプレーイオン化四重極飛行時間型タンパク質を酵素消化し ペプチド断片を解析 アミノ酸配列も解析できる タンパク質の三次元立体構造の解析 (p.70) X 線回折 高分解能 タンパク質の結晶化が必要 NMR 溶液中のタンパク質も解析可能ホモロジー解析 ---- 構造既知のタンパク質と一次構造の特徴を比較してモデルを構築 プロテオーム解析ある試料 ( 細胞 組織 ) 中の多種多様なタンパク質全体を指す 生体内の状態をより良く良く反映した情報と考えられている 近年の技術ではこうした解析が可能になってきた 復習問題 各文の正誤を判定し 誤りの部分は訂正せよ 1. 紫外吸収の測定からタンパク質の量が測定できる 2. タンパク質自体の蛍光を測定することで タンパク質の定量が可能である 3. タンパク質に硫酸アンモニウムなどの塩を大量に加えると 沈殿ができる 4. ゲルろ過クロマトグラフィーで 分子量の大きいタンパク質ほど早く溶出する 5. DEAE セルロースなど陰イオン交換カラムは 酸性タンパク質を吸着し分離する 6. 抗体を結合させたゲルが アフィニティカラムとして利用される 7. mrna の分離精製にゲルろ過カラムクロマトグラフィーが有効である 8. SDS-PAGE では 分子量の小さいタンパク質ほど移動度が大きい 9. フェニルイソチオシナネートが C 末端アミノ酸配列の解析に利用される 10. 二次元 SDS-PAGE では タンパク質を等電点の違いと分子量の違いで詳細に分離する 11. 質量分析は タンパク質の分子量 アミノ酸配列 立体構造が一度に解析可能である 12. ESI とはレーザー光を用いてタンパク質をイオン化する方法である 13. プロテオームとはある生体の多種多様なタンパク質全体の違う混合状態を意味している 正解 : 1. ( 芳香族アミノ酸を含まない場合は ) 2. ( タンパク質は通常無蛍光 ) ( オリゴ dt カラム ) (N 末 ) ( 立体構造は分からない ) 12. (MALDI) 3. 12
13 2 年前期生命活動を担うタンパク質 ( 第 4 回 ) 酵素 ( 第 6 章 ) 酵素とは 生体内の化学反応を司る触媒タンパク質でできている 一部 RNA によるもの ( リボザイム ) もある 基質と結合し 反応中間体を安定化して 活性化エネルギーを下げる 酵素の特徴 (p.84) 1 緩和な条件下で効率的に反応が進む ( 常温 常圧 中性) 2 基質特異性が高い 3 至適温度 至適 ph がある 酵素反応の進み方 (p.81 p.86) 融合適合モデル 加水分解酵素の例エステラーゼ グリコシダーゼ リパーゼなどプロテアーゼ ( ペプチダーゼ) セリンプロテアーゼ----- 活性中心に Ser catalytic triad システインプロテアーゼ----- 活性中心に Cys アスパラギン酸プロテアーゼ----- 活性中心に Asp catalytic diad 亜鉛プロテアーゼ 活性中心に Zn イオン セリン型酵素の例 ( キモトリプシンの活性中心 ) Ser-His-Asp の 3 つのアミノ酸 (catalytic triad) の共同作業で加水分解反応を触媒する 阻害剤 有機リン製剤 ( パラチオン ) DFP など 13
14 酵素の反応速度論 (p.81) 酵素反応速度論 (enzyme kinetics) 酵素反応の性質を的確に評価する方法 反応速度論では 酵素 基質 産物分子の結合と解離の速度を考える E:Enzyme( 酵素分子 ) S:Substrate( 基質分子 ) P:Product( 反応産物分子 ) k: 反応速度定数 v: 反応速度 ( 濃度の変化率 ) k1 k2 k3 E + S ES E + P 酵素の反応速度は 基質濃度で変わる (p.148) 基質濃度の低いとき 基質で飽和しているとき 反応の進行に伴って基質濃度は変化 基質濃度は常に酵素活性に影響を与えている ミカエリス メンテン式 (p.83) 酵素反応の速度 ( 初速度 ) を基質濃度 最大速度 Vmax[S] ES 複合体の解離定数で表した関係式 v = この式から分かること Km + [S] Km 値は v が Vmax の 1/2 のときの基質濃度 [S] Km の場合 速度 v は基質濃度 [S] に比例する Km [S] の場合 速度 v は基質濃度 [S] に関係なく 一定 (Vmax) になる Km の意味 Km 値は v が Vmax の 1/2 のときの基質濃度 ES 複合体の解離定数 ---E と S の親和性を示す Km = Km 値が低いほど 親和性が高い 低濃度の基質でも複合体を形成する Km 値が高いほど 親和性が低く複合体の形成が起こりにくい k 2 +k3 k1 14
15 2 年前期生命活動を担うタンパク質 ( 第 4 回 ) Vmax の意味 最大反応速度 大過剰の基質存在下での反応 複合体を形成していない E が無いような極限状態での反応速度であるから 単位時間に何回酵素が反応できるか 代謝回転数を示す ラインウィーバー バーク プロット 1/[S] と 1/v が比例関係にあることが示される 酵素反応の測定結果から ラインウィーバー バーク プロットのグラフを作成すると Km 値と Vmax とを求めることができる アイソザイム (p.83) 同一の反応を触媒するが タンパク質としては異なる酵素 ( 異なるが類似構造を持つものが多い ) 演習問題 次の各文の正誤を判定し 誤りの部分を直しなさい セリン型プロテアーゼの活性中心には Ser, His, Arg の 3 つのアミノ酸残基がある アスパラギン酸プロテアーゼの活性中心には catalytic triad が存在する 3. 有機リンを主成分とする殺虫剤は エステラーゼを非可逆的に阻害する 4. 酵素による触媒反応速度は 基質濃度に比例する 5. [S] Km の場合 速度 v は基質濃度 [ S] に比例する 6. Km 値が小さいほど 基質と酵素の親和性が高い 7. Km の単位は mol/min である 8. Vmax は基質濃度に応じて変化する 9. Km の小さい酵素は わずかの濃度変化に反応して酵素活性の活性が切り替わる 10. 逆数プロットで表したとき y 切片の値の逆数が Vmax に相当する 11. 乳酸デヒドロゲナーゼには 心筋型と骨格筋型の 2 つのアイソザイムが存在する 12. 基質結合部位を構成するアミノ酸によって基質特異性が決ってくる 正解 : 1. (Arg Asp) 2. (catalytic diad) (vは [S] によって変化 する ) (mo l/l) 8. ( 酵素に固有の値 )
16 補足解説 ミカエリス メンテン式の導出 酵素反応の速度は基質の濃度をあげると増加するが ある程度をこえるとそれ以上は増加しない 酵素の活性中心がすべて反応に関与するときに反応速度は最大となる 酵素が触媒する反応は次のように進むと考えられる + k 1 k 3 + P 1 E + S ES E + P k 2 S ここで E は遊離の酵素 S は基質 (substrate) ES は酵素 - 基質複合体 P は生成物 そして k 1 k 2 k 3 は各段階の反応速度定数を表わす 酵素反応が steady state( 定常状態 ) を保ちながら進行している場合 酵素 - 基質複合体の濃度 [ES] は増減しないから k 1 [ E][S ]= k 2 [ES]+ k 3 [ ES] の関係が保たれている 従って 2 [E]+[S] k = 2 + k 3 = Km [ES] k 1 ES 形成に関わる反応と ES 消費の反応に関わる反応速度比を表しているの右辺の定数を Michaelis は K m と定義した K m は Michaelis 定数と呼ばれ 単位は基質濃度と同じである 酵素の全濃度を [Et] で表わすと [E]=[Et]-[ES] であり 2 式は {[Et]-[ES]}[S] = Km [ES] 両辺に [ES] を掛けて [Et][S]-[ES][S]= K m[es] [ES] を表わす形に変形すると [ Et][S ] 3 [ES]= K m +[S] の関係が得られる つまり酵素 - 基質複合体濃度 [ES] が全酵素濃度 [Et] と基質濃度 [S] の関数で表わされる k3 が極めて小さく 1 式全反応の律速段階であるとすると 逆反応の無視しうる初期の反応速度 VO は V O =k 3 [ES] で表わされるので k 3 [ Et][S] 4 VO = K m +[S] 基質濃度が極めて高いとき 反応速度は最大値で一定となる 即ち酵素がすべて反応に使われている ([ES]=[Et]) ときの最大速度 V max で表わすと V=V max =k 3 [Et] V max[s] 5 V = K m +[S] 5 式は 反応速度は基質濃度のみの関数であることを示している 定数 V max 及び K m は個別の酵素反応ごとに特有のものである 16
17 2 年前期生命活動を担うタンパク質 ( 第 5 回 ) 酵素の活性調節機構 酵素活性の調節 代謝産物量の調節 生体への影響例 ) ぺニシリン系抗菌薬 細菌ぺプチジルトランスフェラーゼを阻害 NSAIDs シクロオキシゲナーゼ(COX-Ⅰ COX-Ⅱ) を阻害スタチン類 HMG-CoA 還元酵素を阻害有機リン製剤 アセチルコリンエステラーゼを阻害 酵素の阻害競合阻害 ( 拮抗阻害 )----- Km が上昇 Vmax 変わらず阻害剤は 基質と同じ部位 ( 活性中心 ) に結合して ES 複合体形成を阻害 非競合阻害 Vmax が低下 Km 変わらず阻害剤は基質と異なる部位に結合し ES 複合体形成 ( 親和性 ) には直接影響しない EI ESI 複合体ができることで 有効な E が減少した状態になる 不競合阻害 Km が低下 かつ Vmax が低下阻害剤は ES 複合体にのみ結合する ES 複合体は P を産生せずに ESI 複合体を形成するのに消費され ES 複合体はできやすくなる 17
18 酵素タンパク質の変化による酵素活性の変化 1) 限定分解による活性化 前駆体タンパク質 ( 不活性型 ) 成熟タンパク質 ( 活性型 ) チモーゲン ( zymogen) タンパク質の部分分解によって活性を発揮する酵素 ( 例 ) トリプシノーゲン トリプシン (p.134) キモトリプシノーゲン キモトリプシン ペプシノーゲン ペプシン 2) リン酸化などの修飾による活性の変化リン酸化 ホスホリラーゼのリン酸化(p ) キナーゼ ( kinase)-----リン酸化酵素ホスファターゼ (phosphatase) 脱リン酸化酵素 アセチル化 ヒストンのアセチル化により ヒストンの塩基性が減弱して DNA がヒストンから離れやすくなる 転写や複製の開始に必要なステップ ヒストンアセチル転移酵素 ( HAT: histone acetytransferase) ヒストン脱アセチル酵素 (HDAC:histone deacetylation complex) ユビキチン化 ユビキチンは アミノ酸 76 個からなるペプチド 細胞内で不要になったタンパク質のリシン残基に結合し プロテアソームにより分解を受ける 変性したタンパク質の細胞内除去機構 ( p.381 ) ADP-リボシル化 細菌毒素による G タンパク質の活性化 アロステリック (allosteric) な調節 (p.83) アロステリック酵素 アロステリック効果による調節を受ける酵素アロステリック効果 ミカエリス メンテンのモデルでは説明できない効果基質濃度の上昇に対してシグモイドカーブを示す ある濃度で急激に反応が増強 アロステリック効果は 作用する因子 ( エフェクター ) が酵素の調節部位に結合し 酵素の立体構造を変化させることに依る 阻害または活性化の作用 酵素の調節部位は 基質結合部位 ( 活性中心 ) とは異なる部位 18
19 アロステリック酵素の一例 : アスパラギン酸カルバモイル転移酵素 (ATC アーゼ ) ATC アーゼはピリミジンヌクレオチド生合成の第一段階の酵素であるが 代謝系の最終産物である CTP により酵素活性が抑制され 一方 ATP により活性化される フィードバック阻害 反応経路の最終産物により 反応全体の律速酵素が阻害される 代謝系全体の速度を調節するしくみになっている 補酵素 (p.84) 酵素活性に タンパク質部分に加えさらに低分子の補因子を必要とするものがある 金属イオン補因子有機低分子補欠分子族 ----タンパク質に強く結合補酵素 可逆的に結合 ビタミンを構成成分とするものが多い NAD + (p.31 図 3.3) 演習問題次の各文の正誤を判定し 誤りの部分を直しなさい 1. 基質以外の因子によって酵素活性が変化することがある 2. 酵素は効率よい触媒なので 逆反応は起こらない 3. チモーゲンとは リン酸化によって活性化される酵素のことである 4. キナーゼとはリン酸化反応を行う酵素である 5. 遺伝子の転写が亢進する際には ヒストンがアセチル化されることが必要である 6. リン酸化されるタンパク質中のアミノ酸残基は セリン チロシン リシンである 7. アロステリック酵素は エフェクター分子の存在下で活性が調節される 8. エフェクター分子はアロステリック酵素の活性中心に結合する 9. 水溶性ビタミンの多くは補酵素の構成成分となっている 10. 補酵素は酵素の安定性に関わり 反応には関わらない 正解 : ( 基質が少なく産物が多いときなど ) 3. ( 限定分解により活性化 ) ( リシン トレオニン ) ( 調節部位 )
20 2 年前期生命活動を担うタンパク質 ( 第 6 回 ) 酵素の臨床診断への応用 酵素の利用法 1. 酵素を利用してある代謝産物を作る古くは発酵 アミノ酸や抗生物質などの生物学的産生基質特異的 立体選択的な反応産物を作る 2. 生体成分の検出 定量被検物質と酵素反応を組み合わせて 紫外 - 可視吸収のある物質に置き換えて容易に検出することができる 3. 生体内の変化を調べる血漿中の酵素活性 ( 酵素量 ) の変動を見ることで 健康状態 疾患の診断に有益な情報が得られる 測定の例 2. 生体成分の定量 例 ) コレステロール ( 血漿総コレステロール ) その他にも グルコース ( 血糖値 ) 遊離脂肪酸などが同様の方法で測定されている 20
21 血漿酵素と臨床診断 検査する酵素 酵素の反応 対応する疾患 乳酸脱水素酵素 (LDH) 乳酸 ピルビン酸 心筋梗塞など心疾患 ( 心型アイソザイム ) クレアチンキナーゼ クレアチン+ATP クレアチンリン酸 + ADP 心筋梗塞 筋肉疾患 ( 心筋アイソザイム CK-MB) アスパラギン酸アミノ転移 Asp + 2-オキソグルタル酸 肝障害 酵素 (AST=GOT) Glu + オキザロ酢酸 心筋梗塞 アラニン酸アミノ転移酵素 Ala + 2-オキソグルタル酸 肝障害 (ALT=GPT) Glu + ピルビン酸 ロイシンアミノペプチダー エキソペプチダーゼ 肝臓 胆道の疾患 ゼ (LAP) アルカリホスファターゼ 様々なリン酸化合物を脱リン 肝臓 胆道の疾患 黄疸 (ALP) 酸化 ( 基質特異性が低い ) γ-グルタミルトランスペ γ-グルタミルペプチドの転移 アルコール性肝障害 プチダーゼ (γ-gtp) アミラーゼ (AMY) でんぷん マルトース 急性膵炎 (P 型 = 膵型アイソザイム ) 演習問題次の各文の正誤を判定し 誤りの部分を直しなさい 1. 酵素活性を測定する際は 長時間かけて測定するよりも 初速度を求めるべきである 2. 補酵素 NADHの紫外吸収の変化を利用して 酵素反応を測定することができる 3. コレステロールオキシダーゼで生成するコレステノンのもつ可視吸収で 血漿中のコレステロール量が測定できる 4. アルカリホスファターゼは 心筋梗塞発症時に血漿中に現れる 5. 心筋のLDHも肝臓のLDHもその性質は同一である 6. 膵臓型アミラーゼが血中に出現するのは 膵炎を起こした組織で破壊された細胞から酵素が血中に漏出するためである 7. 例えばトリプシンなどのタンパク質加水分解酵素の酵素活性測定方法を考えて下さい 正解 : ( 生成する H 2 O 2 を利用して 4-アミノアンチピリンから色素を産生させる ) 4. ( 上の表参照 ) 5. ( アイソザイムは構造が違い Km Vmax などにも違いがある ) 6. 7.( ヒント ) チェックポイント基質として何を使うか?( 既知のタンパク質? ペプチド? 合成基質?) 分解反応で生じたものをどうやって検出するか?( 可視 紫外吸収 蛍光 放射標識 SDS-PAGE 抗体との結合 etc) 21
22 2 年前期生命活動を担うタンパク質 ( 第 7 回 ) タンパク質の翻訳後修飾 分解と品質管理 転写 翻訳しただけでは タンパク質は完成していない その後 タンパク質が完成して機能するまでに何が行われるか? ジスルフィド結合を形成する立体構造 ( 二次構造 三次構造 ) の形成種々アミノ酸側鎖に対する化学修飾 ( 糖鎖付加 アセチル化 リン酸化 脂質付加 ) ペプチドの部分的切除複合体形成 ( 四次構造 ) 膜への結合細胞外への分泌 あるいは特定の細胞内小器官への運搬これらさまざまな過程を経て タンパク質が機能できるようになる これらの過程のうち タンパク質の化学構造を変化させる反応を 翻訳後修飾とよぶ タンパク質立体構造の構築タンパク質のジスルフィド結合 (SS 結合 ) の Cys 残基の組合せは 自然に決ってくる場合もあるが 一旦別の組合せで結合して変性したタンパクを 戻すのは大変 シャペロン(chaperon)---- タンパク質が本来の折りたたみ構造 立体構造を維持するように保護する役目のタンパク質 (p.376) たとえば熱刺激があったとき タンパク質が熱変性する シャペロンが作られる タンパク質の構造維持能力を高め 細胞が死なないようにする特別な刺激の無いときでも 常には働いているシャペロンもある ジスルフィドイソメラーゼ(PDI)---- 誤った SS 結合を切断し 繋ぎ換える酵素 (p.378) 細胞内タンパク質分解機構 プロテアソーム(p.381) 誤った折りたたみ構造のタンパク質を選択的に分解するしくみ ( 不良品の除去 ) 1 構造異常のタンパク質をユビキチン化 ユビキチンは アミノ酸 76 個からなるタンパク質 分解すべきタンパク質のリシン残基のアミノ基に結合する 2 ポリユビキチン化されたタンパク質は プロテアソームによって分解される プロテアソームは ATP 依存的にタンパク分解する酵素複合体 22
23 タンパク質の翻訳後修飾 糖鎖付加(p.52) N- 糖鎖 Asn 残基のアミド末端の N 原子に糖が結合 O- 糖鎖 Ser 残基 Thr 残基の水酸基の O 原子に糖が結合 分泌タンパク質 細胞表面の膜タンパク質のほとんどに糖鎖が付加されている ( 細胞内のタンパク質には糖鎖の付加は稀である ) タンパク質の脂質による修飾と膜への移行 脂質部分が修飾されることによって そのタンパク質は細胞膜の内側に結合する GPI アンカー 23
24 練習問題 次の文の正誤を判定し 誤りがあれば適当な語に直しなさい 1. タンパク質は翻訳により完成し その後で変化を受けることは無い 2. タンパク分子内のジスルフィド結合の位置は 概ね一次構造で決っているが 誤った位置 で生じた結合はジスルフィドイソメラーゼが直している 3. シャペロンは折りたたみ異常が起きたタンパク質を分解する 4. アスパラギンの側鎖に結合する糖鎖を N- 糖鎖と呼ぶ タンパク質の糖鎖修飾は リソソーム内で行われる タンパク質のリン酸化反応は ATP のリン酸が基質タンパク質に転移する 7. 構造異常タンパク質は ユビキチンによる修飾の後 プロテアソームの作用で分解される 8. プロテアソームのタンパク分解作用には ATP のエネルギーは不要である 9. 糖タンパク質の糖鎖部分は細胞の表面に露出している 10. 三量体 G タンパク質は 脂質による修飾を受けている 11. GPI アンカータンパク質は細胞膜の細胞質側に局在する 12. タンパク質のミリスチル化は パルミトイル化と同様に N 末端のアミノ基にアミド結合を 形成する 13. タンパク質修飾に利用されるゲラニルゲラニオールは コレステロール合成系を介して作 られている 正解 : ( 本来の立体構造を維持する役目 分解酵素ではない ) ( ゴルジ体および小胞体 ) (ATP 必要 ) ( 細胞表面に局在 ) 12. ( パルミチル化は C 末付近の Cys にチオエステル結合 )
25 2 年前期生命活動を担うタンパク質 ( 第 8 回 ) タンパク質の細胞内輸送 ( 第 26 章 ) 細胞内小胞の輸送小胞体 ゴルジ体 ゴルジ体 細胞膜 ( エキソサイトーシス : 分泌 ) 細胞膜 エンドソーム ( エンドサイトーシス : 取込み ) クラスリン被覆小胞 (clathlin coated vesicle) 小胞にはタンパク質による裏打ち構造がある 細胞膜の内側を見た走査電顕 エンドサイトーシスした小胞周囲にはタンパク質がコートしている 25
26 糖鎖付加とタンパク質の輸送糖鎖付加はゴルジ体で行われる これは 分泌タンパク質が細胞内輸送される一連の流れの一段階である 1 粗面小胞体のリボソームでタンパク合成 ( : 粗面小胞体リボソームでは 分泌タンパクおよび膜タンパクが合成される 一方 細胞質のリボソームでは細胞内の粗面小胞体滑面小胞体タンパク質が合成される ) 2 合成されつつあるタンパク質が小胞体内腔に入りながら タンパク合成が進む 3 合成されたタンパク質は小胞体膜の一部に包まれ 小胞として小胞体から離れる 4 小胞がゴルジ体に融合し 中身のタンパク質がゴルジ体内腔に入る 5 ゴルジ体でタンパク質の糖鎖付加が行われる 6 修飾されたタンパク質はゴルジ体膜の一部に包まれ 分泌小胞となる 6 分泌小胞は 細胞膜に融合しエキソサイトーシスが起こる ( タンパク質の糖鎖付加は 一部が小胞体で行われるが さらにゴルジ体で進行する ) 分泌タンパク質の輸送シグナル配列 分泌タンパク質がどのようにして膜を通過するのか?(p.386) 翻訳開始 (N 末端 ) から 20 数残基のアミノ酸配列で ある特徴を共有している 疎水性アミノ酸領域と短い極性アミノ酸の領域分泌タンパクおよび膜タンパクにのみ見られる構造 翻訳後修飾の過程で切断されるので 完成したタンパク質には存在しない シグナル配列の一例 H2N-MMSFVSLLLVGILFWATEAEQLTKCEVFQ 下線部は疎水性領域 26
27 タンパク質の核への移行 (p.396) 核膜孔からタンパク質などが行き来する 核移行シグナルを持つタンパク質のみが核内に移行できる (NLS: 塩基性アミノ酸に富む ) 核内へのタンパク質輸送機能を持つタンパク質 インポルチン核外へのタンパク質輸送機能を持つタンパク質 エキソポルチン ( 核移行シグナル 核外移行シグナル部分に結合して 複合体を作って核膜孔を通過する その際 Ran という小型 GTP 結合タンパク質が調節因子として関わる ) 核膜孔の模式図 練習問題次の文の正誤を判定し 誤りがあれば適当な語に直しなさい 1. 小胞体のリボソームと細胞質のリボソームとでは 通常翻訳するタンパク質が異なる 2. 細胞外に分泌されるタンパク質は 細胞質のリボソーム ( ポリソーム ) で合成される 3. 小胞体内に存在するタンパク質は N 末端側にシグナル配列を有している 4. 翻訳されたばかりのタンパク質に結合し タンパク質の変性や凝集を防ぎ 立体構造異常タンパク質を正常に戻すのは SRP の作用である 5. 粗面小胞体のリボソームでのタンパク質合成が行なわれている途中で キモトリプシンが作用してシグナル配列を除去する 6. シグナル配列には疎水性アミノ酸が多い領域がある 7. 全ての分泌タンパク質のシグナル配列は 共通のアミノ酸配列である 8. 分泌タンパク質は小胞体およびゴルジ体で糖鎖付加を受ける 9. 分泌タンパク質はエキソサイトーシスで 細胞外に分泌される 10. 核内外への物質移動は 核膜の変形を伴う小胞輸送で行なわれる 11. インポルチンは 核内から細胞質内へタンパク質を輸送するシャトルタンパク質である 12. Ran は GTP と結合する性質を持つタンパク質である 13. GDP 型の Ran はふたたび核内に輸送される 14. エンドサイトーシスされる小胞はクラスリンタンパク質で包まれている 正解 :1. 2. ( 粗面小胞体 ) 3. ( 翻訳直後はシグナル配列があるが 小胞体内に入るときに切断されている ) 4. ( シャペロン ) 5. ( シグナルペプチダーゼ ) ( アミノ酸配列は一定していない ) ( 核膜孔を通ってタンパク質やmRNA が移動する ) 11. ( エキソポルチン )
28 2 年前期生命活動を担うタンパク質 ( 第 9 回 ) 受容体とリガンド (p.402 p ) 受容体 (receptor)----- 様々な分子と特異的に結合し その刺激を感知する構造体一般的にはタンパク質であるが 一部糖脂質なども受容体の機能を持つものがある リガンド (ligand) 受容体に対して特異的に結合する分子を総称してリガンドと呼ぶ ホルモン 神経伝達物質など生体調節に直接関わる分子のみならず ビタミン リポタンパク質 物質運搬体 隣接する細胞 外来異物 ( ウイルス ) などに対する受容体もある ある細胞応答 組織応答を引き起すリガンドに対しては アゴニスト (agonist: 作用物質 ) アンタゴニスト(antagonist: 非作用物質 ) という個友を用いる場合も多い 主要な受容体の種類細胞膜受容体 受容体タンパク質は 細胞膜上に存在する膜タンパク質である リガンドが結合しても 受容体自身は膜から離れるわけではなく 何らかの反応を引き起こすことで情報を細胞内に伝え 細胞の変化を引き起こす 酵素型受容体 リガンドが結合すると 受容体の一部分の酵素活性が活性になる ( 例 : インスリン受容体 EGF 受容体 ) G タンパク質共役型 (7 回膜貫通型 ) 受容体 リガンドが結合すると 受容体に結合していた三量体 G タンパク質が分離する ( 例 : グルカゴン受容体 アドレナリンβ 受容体 ACh( ムスカリン ) 受容体 ) イオンチャネル型受容体 リガンドが結合すると 受容体が筒状に形を変えて イオンを通過させることが出来る ( 例 :ACh( ニコチン ) 受容体 ) 細胞内取込み型受容体 リガンドが結合すると 受容体が細胞内に丸ごと取り込まれる ( エンドサイトーシス ) ( 例 :LDL 受容体 トランスフェリン受容体 ) 細胞膜脂質とタンパク質のモデル図 28
29 アセチルコリン受容体 インスリン受容体 核内受容体 ( 細胞内受容体 p.406) 受容体タンパク質は 細胞質内または核内に存在している 受容体は 細胞内に侵入してきたリガンドと結合し 形成された複合体が核内に移行する 受容体複合体は DNA の調節部位に結合し 特定の遺伝子の mrna を合成させる転写因子として働く ( 例 : グルココルチコイド受容体 エストロゲン受容体 甲状腺ホルモン受容体 ) 核内受容体はホモ またはヘテロ二量体で作用する 29
30 セカンドメッセンジャー (p.403) 細胞に与えられた刺激が細胞内でどのような変化をもたらすのか? ホルモン オータコイド サイトカインなどの生理活性分子は それぞれ特異的な受容体に結合する 一部の受容体は細胞内にある ( 核内受容体 ) が 多くの刺激分子に対する受容体は細胞膜上にある 生理活性分子が細胞膜上の受容体に結合すると 受容体に結合したリガンド自体は細胞内に入らないのに その細胞では代謝的な変化 形態上の変化 電気的な変化などが引き起こされる リガンドが結合すると 受容体を起点として細胞内に刺激を伝える一連の連鎖的反応 ( 細胞内情報伝達 ) が引き起こされる 細胞膜上の受容体とリガンドの結合に次いで 細胞内に生じて情報を媒介する分子をセカンドメッセンジャーと呼ぶ おもなセカンドメッセンジャー camp( サイクリック AMP) Ca 2+ IP 3 ( イノシトール三リン酸 ) DG( ジアシルグルセロール ) イノシトール -1,4,5- 三リン酸 PIP 2 ( ホスファチジルイノシトール 4,5- 二リン酸 ) DG + IP PLC: ホスホリパーゼ C 3 camp アデニル酸 + シクラーゼ 30
31 復習問題 ( 次の文の正誤を判定し 誤りの部分を直しなさい ) 1. ホルモンは 細胞内に入ることはできない 2. ホルモンなどの細胞活性化分子は それぞれ特異的な受容体と結合する 3. 同じリガンドに対して多数の異なる受容体が存在することがある 4. アセチルコリンムスカリン様受容体は 7 回膜貫通型の受容体である 5. インスリン受容体は ホモ2 量体を形成する酵素型の受容体である 6. セカンドメッセンジャーの camp は ADP の脱リン酸化によって生じる 7. アデニル酸シクラーゼは アデニンをリン酸化して camp を産生する 8. 核内受容体のリガンドは おもに脂溶性ビタミンや脂溶性ホルモンである 9. そもそも生体内に無いはずの物質を認識する受容体も存在する 10. ステロイドホルモンに対する受容体は 細胞表面に存在する 11. インスリンは インスリン受容体に結合した後 細胞質内に取込まれていく 12. アセチルコリン受容体は アセチルコリンの結合により立体構造を変える 正解 : 1. ( 脂溶性のホルモンなどは細胞内に入る ) (α βサブユニットからなるヘテロ4 量体 ) 6. (ATP の脱リン酸化 ) 7. (ATP からピ ロリン酸を遊離する ) ( ウイルス受容体など ) 10. ( 核内受容体 ) 11. ( インスリン受容体は酵素型 )
32 2 年前期生命活動を担うタンパク質 ( 第 10 回 ) 細胞内情報伝達受容体が受けた刺激を伝達するしくみ (p.408) (1) チロシンリン酸化を介する機構 (p.414) インスリン受容体は αサブユニット 2 個 βサブユニット 2 個からなる 4 量体タンパク質である インスリンがαサブユニットに結合すると βサブユニットの立体構造変化を引き起こし βサブユニット上のチロシンキナーゼ部分が活性化し インスリン受容体基質 -1(IRS-1) というタンパク質のチロシン残基をリン酸化する リン酸化された IRS-1 は さらに他のタンパク質を活性化し 連鎖的な細胞内の情報伝達が行われる その結果 GLUT4( グルコース輸送体 ) が細胞質小胞から細胞膜へ移動し グルコースの取込みが上昇することで血糖値が下がる (2) G タンパク質 ( 三量体 G タンパク質 ) を介する機構 (p.416) アドレナリンやグルカゴンに対する受容体は 7つの膜貫通 αへリックスを持つ 三量体 G タンパク質の α γサブユニットは脂質が修飾され膜の内側に結合している 受容体にリガンドが結合すると 受容体と G タンパク質の相互作用で G タンパク質が活性化する 活性化した G タンパク質は 近傍のエフェクタータンパク質に移動し それを活性化する 32
33 a. camp 濃度の上昇を引き起こす グルカゴン エピネフリンなど 図 2 b. IP 3 と Ca 2+ の濃度の上昇を引き起こす------アンギオテンシンⅡ トロンボキサン A 2 など アドレナリンやグルカゴンに対する受容体は Gs タイプの三量体 G を活性化する 一方 アンギオテンシンⅡやトロンボキサン A 2 などの受容体は Gq タイプの三量体 G を活性化する 活性化された Gq は 近傍の膜上にあるリン脂質分解酵素 ホスホリパーゼ C を活性化する ホスホリパーゼ C により セカンドメッセンジャーである IP 3 が産生する IP 3 は 小胞体に結合し 小胞体からの Ca 2+ イオンの遊離を促し Ca 2+ イオン依存性の反応を引き起こす 33
34 G タンパクには作用の異なる 3 種類のタイプがある 受容体のタイプ 情報伝達の様式 受容体の例 Gs タンパク共役型 アデニル酸シクラーゼ活性化 アドレナリンβ 受容体 (camp 濃度の上昇 ) ヒスタミン H 2 受容体グルカゴン受容体 Gi タンパク共役型アデニル酸シクラーゼ抑制アドレナリンα 2 受容体 (camp 濃度の低下 ) ムスカリン M 2 受容体 ドパミン D 2 受容体 Gq タンパク共役型 ホスホリパーゼ C 活性化 アドレナリンα 1 受容体 (IP 3 濃度の上昇 ) ムスカリン M 1 受容体 ヒスタミン H 1 受容体 アンギオテンシンⅡ 受容体 復習問題 ( 次の文の正誤を判定し 誤りの部分を直しなさい ) 1. アデニル酸シクラーゼは Gs タイプの三量体 G タンパク質のよって活性化される 2. 活性化した三量体 G タンパク質は αサブユニットとβγサブユニットに分かれる 3. 細胞内の camp 濃度が上昇すると プロテインキナーゼ A(PKA) が活性化する 4. 細胞内の Ca 2+ 濃度が上昇すると プロテインキナーゼ A(PKA) が活性化する 5. グルカゴン刺激を受けた細胞では ホスホリパーゼ C が活性化する 6. 活性化したホスホリパーゼ C は イノシトール三リン酸 (IP ) を産生する 7. イノシトール三リン酸 (IP 3 ) は プロテインキナーゼ C(PKC) を活性化する 小胞体内は 細胞質内よりも Ca 濃度が高い 9. インスリン受容体は トレオニンキナーゼ活性を持っている 10. 活性化したインスリン受容体は IRS-1 をアセチル化する 11. 受容体タンパク質は 様々な分子と無差別に結合する性質を持っている 12. ニコチン性アセチルコリン受容体は 酵素型受容体の一例である 13. G タンパク質共役型受容体タンパク質は 細胞膜を 7 回貫通する形をとっている 14. ヒスタミン H 1 受容体を刺激すると Gq の活性化を介してホスホリパーゼ C が活性化する 3 正解 : ( プロテインキナーゼ C(PKC)) 5. (PKA) (Ca 2+ を遊離させる ) ( チロシンキナーゼ ) 10. ( リン酸化 ) 11. ( 高い特異性を持つ ) 12. ( イオンチャネル型 )
細胞骨格を形成するタンパク質
 タンパク質に関する練習問題総まとめ 第 1 回タンパク質の一次構造と高次構造 1. ペプチド結合部分は平面構造を取る 2. 分子シャペロンは タンパク質の ( ) をする働きをもつ 3. 動物種が違っても 同じ作用を持つタンパク質は 同一のアミノ酸配列からなる 4. ある 2 つのタンパク質間の相同性 (%) は それらのホモロジー (%) より高い 5. 加熱処理により タンパク質を安定化している
タンパク質に関する練習問題総まとめ 第 1 回タンパク質の一次構造と高次構造 1. ペプチド結合部分は平面構造を取る 2. 分子シャペロンは タンパク質の ( ) をする働きをもつ 3. 動物種が違っても 同じ作用を持つタンパク質は 同一のアミノ酸配列からなる 4. ある 2 つのタンパク質間の相同性 (%) は それらのホモロジー (%) より高い 5. 加熱処理により タンパク質を安定化している
PowerPoint プレゼンテーション
 細胞の情報伝達 (1) 何を学習するか細胞が環境からシグナル ( 刺激 ) を受けて 細胞の状態が変化するときに 細胞内でどのような現象が起きているか を知る分子の大変複雑な連続反応であるので 反応の最初の段階を中心に見ていく ( 共通の現象が多いから ; 疾患の治療の標的となる分子が多い ) これを知るために (2) リガンドの拡散様式 ( 図 16-3) リガンドを発現する細胞とこれを受け取る細胞との
細胞の情報伝達 (1) 何を学習するか細胞が環境からシグナル ( 刺激 ) を受けて 細胞の状態が変化するときに 細胞内でどのような現象が起きているか を知る分子の大変複雑な連続反応であるので 反応の最初の段階を中心に見ていく ( 共通の現象が多いから ; 疾患の治療の標的となる分子が多い ) これを知るために (2) リガンドの拡散様式 ( 図 16-3) リガンドを発現する細胞とこれを受け取る細胞との
PowerPoint プレゼンテーション
 酵素 : タンパク質の触媒 タンパク質 Protein 酵素 Enzyme 触媒 Catalyst 触媒 Cataylst: 特定の化学反応の反応速度を速める物質 自身は反応の前後で変化しない 酵素 Enzyme: タンパク質の触媒 触媒作用を持つタンパク質 第 3 回 : タンパク質はアミノ酸からなるポリペプチドである 第 4 回 : タンパク質は様々な立体構造を持つ 第 5 回 : タンパク質の立体構造と酵素活性の関係
酵素 : タンパク質の触媒 タンパク質 Protein 酵素 Enzyme 触媒 Catalyst 触媒 Cataylst: 特定の化学反応の反応速度を速める物質 自身は反応の前後で変化しない 酵素 Enzyme: タンパク質の触媒 触媒作用を持つタンパク質 第 3 回 : タンパク質はアミノ酸からなるポリペプチドである 第 4 回 : タンパク質は様々な立体構造を持つ 第 5 回 : タンパク質の立体構造と酵素活性の関係
生理学 1章 生理学の基礎 1-1. 細胞の主要な構成成分はどれか 1 タンパク質 2 ビタミン 3 無機塩類 4 ATP 第5回 按マ指 (1279) 1-2. 細胞膜の構成成分はどれか 1 無機りん酸 2 リボ核酸 3 りん脂質 4 乳酸 第6回 鍼灸 (1734) E L 1-3. 細胞膜につ
 の基礎 1-1. 細胞の主要な構成成分はどれか 1 タンパク質 2 ビタミン 3 無機塩類 4 ATP 第5回 (1279) 1-2. 細胞膜の構成成分はどれか 1 無機りん酸 2 リボ核酸 3 りん脂質 4 乳酸 第6回 (1734) 1-3. 細胞膜について正しい記述はどれか 1 糖脂質分子が規則正しく配列している 2 イオンに対して選択的な透過性をもつ 3 タンパク質分子の二重層膜からなる 4
の基礎 1-1. 細胞の主要な構成成分はどれか 1 タンパク質 2 ビタミン 3 無機塩類 4 ATP 第5回 (1279) 1-2. 細胞膜の構成成分はどれか 1 無機りん酸 2 リボ核酸 3 りん脂質 4 乳酸 第6回 (1734) 1-3. 細胞膜について正しい記述はどれか 1 糖脂質分子が規則正しく配列している 2 イオンに対して選択的な透過性をもつ 3 タンパク質分子の二重層膜からなる 4
生物有機化学
 質問への答え 速い 書き込みが追い付かない 空欄を開いたことを言ってほしいなるべくゆっくりやります ただし 生化学をできるだけ網羅し こんなの聞いたことない というところをなるべく残さないようにと思っています 通常の講義よりは速いでしょう 試験では細かいことは聞きません レーザーポインターが見にくい アンカータンパク質の内側 外側とは? 細胞内と細胞外です 動画の場所 Youtube で Harvard
質問への答え 速い 書き込みが追い付かない 空欄を開いたことを言ってほしいなるべくゆっくりやります ただし 生化学をできるだけ網羅し こんなの聞いたことない というところをなるべく残さないようにと思っています 通常の講義よりは速いでしょう 試験では細かいことは聞きません レーザーポインターが見にくい アンカータンパク質の内側 外側とは? 細胞内と細胞外です 動画の場所 Youtube で Harvard
スライド 1
 1. 血液の中に存在する脂質 脂質異常症で重要となる物質トリグリセリド ( 中性脂肪 :TG) 動脈硬化に深く関与する 脂質の種類 トリグリセリド :TG ( 中性脂肪 ) リン脂質 遊離脂肪酸 特徴 細胞の構成成分 ホルモンやビタミン 胆汁酸の原料 動脈硬化の原因となる 体や心臓を動かすエネルギーとして利用 皮下脂肪として貯蔵 動脈硬化の原因となる 細胞膜の構成成分 トリグリセリド ( 中性脂肪
1. 血液の中に存在する脂質 脂質異常症で重要となる物質トリグリセリド ( 中性脂肪 :TG) 動脈硬化に深く関与する 脂質の種類 トリグリセリド :TG ( 中性脂肪 ) リン脂質 遊離脂肪酸 特徴 細胞の構成成分 ホルモンやビタミン 胆汁酸の原料 動脈硬化の原因となる 体や心臓を動かすエネルギーとして利用 皮下脂肪として貯蔵 動脈硬化の原因となる 細胞膜の構成成分 トリグリセリド ( 中性脂肪
第6回 糖新生とグリコーゲン分解
 第 6 回糖新生とグリコーゲン分解 日紫喜光良 基礎生化学講義 2018.5.15 1 主な項目 I. 糖新生と解糖系とで異なる酵素 II. 糖新生とグリコーゲン分解の調節 III. アミノ酸代謝と糖新生の関係 IV. 乳酸 脂質代謝と糖新生の関係 2 糖新生とは グルコースを新たに作るプロセス グルコースが栄養源として必要な臓器にグルコースを供給するため 脳 赤血球 腎髄質 レンズ 角膜 精巣 運動時の筋肉
第 6 回糖新生とグリコーゲン分解 日紫喜光良 基礎生化学講義 2018.5.15 1 主な項目 I. 糖新生と解糖系とで異なる酵素 II. 糖新生とグリコーゲン分解の調節 III. アミノ酸代謝と糖新生の関係 IV. 乳酸 脂質代謝と糖新生の関係 2 糖新生とは グルコースを新たに作るプロセス グルコースが栄養源として必要な臓器にグルコースを供給するため 脳 赤血球 腎髄質 レンズ 角膜 精巣 運動時の筋肉
細胞の構造
 大阪電気通信大学 5/8/18 本日の講義の内容 酵素 教科書 第 4 章 触媒反応とエネルギーの利用 酵素の性質 酵素反応の調節 酵素の種類 触媒の種類 無機物からなる無機触媒と有機物からなる有機触媒がある 触媒反応とエネルギーの利用 1 無機触媒の例 過酸化水素水に二酸化マンガンを入れると過酸化水素水が分解して水と酸素になる 2 有機触媒の例 細胞内に含まれるカタラーゼという酵素を過酸化水素水に加えると
大阪電気通信大学 5/8/18 本日の講義の内容 酵素 教科書 第 4 章 触媒反応とエネルギーの利用 酵素の性質 酵素反応の調節 酵素の種類 触媒の種類 無機物からなる無機触媒と有機物からなる有機触媒がある 触媒反応とエネルギーの利用 1 無機触媒の例 過酸化水素水に二酸化マンガンを入れると過酸化水素水が分解して水と酸素になる 2 有機触媒の例 細胞内に含まれるカタラーゼという酵素を過酸化水素水に加えると
第6回 糖新生とグリコーゲン分解
 第 6 回糖新生とグリコーゲン分解 日紫喜光良 基礎生化学講義 2014.06.3 1 主な項目 I. 糖新生と解糖系とで異なる酵素 II. 糖新生とグリコーゲン分解の調節 III. アミノ酸代謝と糖新生の関係 IV. 乳酸 脂質代謝と糖新生の関係 2 糖新生とは グルコースを新たに作るプロセス グルコースが栄養源として必要な臓器にグルコースを供給するため 脳 赤血球 腎髄質 レンズ 角膜 精巣 運動時の筋肉
第 6 回糖新生とグリコーゲン分解 日紫喜光良 基礎生化学講義 2014.06.3 1 主な項目 I. 糖新生と解糖系とで異なる酵素 II. 糖新生とグリコーゲン分解の調節 III. アミノ酸代謝と糖新生の関係 IV. 乳酸 脂質代謝と糖新生の関係 2 糖新生とは グルコースを新たに作るプロセス グルコースが栄養源として必要な臓器にグルコースを供給するため 脳 赤血球 腎髄質 レンズ 角膜 精巣 運動時の筋肉
タンパク質の合成と 構造 機能 7 章 +24 頁 転写と翻訳リボソーム遺伝子の調節タンパク質の構造弱い結合とタンパク質の機能
 タンパク質の合成と 構造 機能 7 章 +24 頁 転写と翻訳リボソーム遺伝子の調節タンパク質の構造弱い結合とタンパク質の機能 タンパク質の合成 セントラル ドグマによると 遺伝子が持つ情報は タンパク質を合成することで発現 (Expression) される それは 2 段階の反応で進行する DNA 転写 (Transcription) DNA の塩基配列から mrna の塩基配列へ染色体の
タンパク質の合成と 構造 機能 7 章 +24 頁 転写と翻訳リボソーム遺伝子の調節タンパク質の構造弱い結合とタンパク質の機能 タンパク質の合成 セントラル ドグマによると 遺伝子が持つ情報は タンパク質を合成することで発現 (Expression) される それは 2 段階の反応で進行する DNA 転写 (Transcription) DNA の塩基配列から mrna の塩基配列へ染色体の
図 B 細胞受容体を介した NF-κB 活性化モデル
 60 秒でわかるプレスリリース 2007 年 12 月 17 日 独立行政法人理化学研究所 免疫の要 NF-κB の活性化シグナルを増幅する機構を発見 - リン酸化酵素 IKK が正のフィーッドバックを担当 - 身体に病原菌などの異物 ( 抗原 ) が侵入すると 誰にでも備わっている免疫システムが働いて 異物を認識し 排除するために さまざまな反応を起こします その一つに 免疫細胞である B 細胞が
60 秒でわかるプレスリリース 2007 年 12 月 17 日 独立行政法人理化学研究所 免疫の要 NF-κB の活性化シグナルを増幅する機構を発見 - リン酸化酵素 IKK が正のフィーッドバックを担当 - 身体に病原菌などの異物 ( 抗原 ) が侵入すると 誰にでも備わっている免疫システムが働いて 異物を認識し 排除するために さまざまな反応を起こします その一つに 免疫細胞である B 細胞が
スライド 1
 タンパク質 ( 生化学 1) 平成 29 年 4 月 20 日病態生化学分野 分子酵素化学分野教授 山縣和也 生化学 1のスケジュール 4 月 20 日 講義開始 6 月 1 日 中間試験 9 月 25 日 生化学 1 試験 講義日程 内容は一部変更があります 講義資料 ( 山縣 吉澤分 ): 熊本大学病態生化学 で検索 ID: Biochem2 パスワード :76TgFD3Xc 生化学 1 の合否判定は
タンパク質 ( 生化学 1) 平成 29 年 4 月 20 日病態生化学分野 分子酵素化学分野教授 山縣和也 生化学 1のスケジュール 4 月 20 日 講義開始 6 月 1 日 中間試験 9 月 25 日 生化学 1 試験 講義日程 内容は一部変更があります 講義資料 ( 山縣 吉澤分 ): 熊本大学病態生化学 で検索 ID: Biochem2 パスワード :76TgFD3Xc 生化学 1 の合否判定は
スライド 1
 解糖系 (2) 平成 24 年 5 月 7 日生化学 2 ( 病態生化学分野 ) 教授 山縣和也 本日の学習の目標 解糖系の制御機構を理解する 2,3-BPG について理解する 癌と解糖系について理解する エネルギー代謝経路 グリコーゲン グリコーゲン代謝 タンパク質 アミノ酸代謝 トリアシルグリセロール グルコース グルコース 6 リン酸 アミノ酸 脂肪酸 脂質代謝 解糖系 糖新生 β 酸化 乳酸
解糖系 (2) 平成 24 年 5 月 7 日生化学 2 ( 病態生化学分野 ) 教授 山縣和也 本日の学習の目標 解糖系の制御機構を理解する 2,3-BPG について理解する 癌と解糖系について理解する エネルギー代謝経路 グリコーゲン グリコーゲン代謝 タンパク質 アミノ酸代謝 トリアシルグリセロール グルコース グルコース 6 リン酸 アミノ酸 脂肪酸 脂質代謝 解糖系 糖新生 β 酸化 乳酸
ドリル No.6 Class No. Name 6.1 タンパク質と核酸を構成するおもな元素について述べ, 比較しなさい 6.2 糖質と脂質を構成するおもな元素について, 比較しなさい 6.3 リン (P) の生体内での役割について述べなさい 6.4 生物には, 表 1 に記した微量元素の他に, ど
 1 微視的生物学 生化学 1.1 生物を構成する元素 (element) 生物を構成する主要元素の種類と, おもな微量元素とその役割の概略について説明できる 地球上には 100 種類以上の元素があり, そのうち生体を構成する元素の種類は限られていて, 約 20 種類である 主要元素としては水素 (H), 炭素 (C), 窒素 (N), 酸素 (O) の 4 元素で, これらで, 生体を構成するタンパク質や核酸,
1 微視的生物学 生化学 1.1 生物を構成する元素 (element) 生物を構成する主要元素の種類と, おもな微量元素とその役割の概略について説明できる 地球上には 100 種類以上の元素があり, そのうち生体を構成する元素の種類は限られていて, 約 20 種類である 主要元素としては水素 (H), 炭素 (C), 窒素 (N), 酸素 (O) の 4 元素で, これらで, 生体を構成するタンパク質や核酸,
本日の内容 HbA1c 測定方法別原理と特徴 HPLC 法 免疫法 酵素法 原理差による測定値の乖離要因
 HbA1c 測定系について ~ 原理と特徴 ~ 一般社団法人日本臨床検査薬協会 技術運営委員会副委員長 安部正義 本日の内容 HbA1c 測定方法別原理と特徴 HPLC 法 免疫法 酵素法 原理差による測定値の乖離要因 HPLC 法 HPLC 法原理 高速液体クロマトグラフィー 混合物の分析法の一つ 固体または液体の固定相 ( 吸着剤 ) 中で 液体または気体の移動相 ( 展開剤 ) に試料を加えて移動させ
HbA1c 測定系について ~ 原理と特徴 ~ 一般社団法人日本臨床検査薬協会 技術運営委員会副委員長 安部正義 本日の内容 HbA1c 測定方法別原理と特徴 HPLC 法 免疫法 酵素法 原理差による測定値の乖離要因 HPLC 法 HPLC 法原理 高速液体クロマトグラフィー 混合物の分析法の一つ 固体または液体の固定相 ( 吸着剤 ) 中で 液体または気体の移動相 ( 展開剤 ) に試料を加えて移動させ
核内受容体遺伝子の分子生物学
 核内受容体遺伝子の分子生物学 佐賀大学農学部 助教授和田康彦 本講義のねらい 核内受容体を例として脊椎動物における分子生物学的な思考方法を体得する 核内受容体遺伝子を例として脊椎動物における遺伝子解析手法を概観する 脊椎動物における核内受容体遺伝子の役割について理解する ヒトや家畜における核内受容体遺伝子研究の応用について理解する セントラルドグマ ゲノム DNA から相補的な m RNA( メッセンシ
核内受容体遺伝子の分子生物学 佐賀大学農学部 助教授和田康彦 本講義のねらい 核内受容体を例として脊椎動物における分子生物学的な思考方法を体得する 核内受容体遺伝子を例として脊椎動物における遺伝子解析手法を概観する 脊椎動物における核内受容体遺伝子の役割について理解する ヒトや家畜における核内受容体遺伝子研究の応用について理解する セントラルドグマ ゲノム DNA から相補的な m RNA( メッセンシ
スライド 1
 ミトコンドリア電子伝達系 酸化的リン酸化 (2) 平成 24 年 5 月 21 日第 2 生化学 ( 病態生化学分野 ) 教授 山縣和也 本日の学習の目標 電子伝達系を阻害する薬物を理解する ミトコンドリアに NADH を輸送するシャトルについて理解する ATP の産生量について理解する 脱共役タンパク質について理解する 複合体 I III IV を電子が移動するとプロトンが内膜の内側 ( マトリックス側
ミトコンドリア電子伝達系 酸化的リン酸化 (2) 平成 24 年 5 月 21 日第 2 生化学 ( 病態生化学分野 ) 教授 山縣和也 本日の学習の目標 電子伝達系を阻害する薬物を理解する ミトコンドリアに NADH を輸送するシャトルについて理解する ATP の産生量について理解する 脱共役タンパク質について理解する 複合体 I III IV を電子が移動するとプロトンが内膜の内側 ( マトリックス側
酵素
 3 酵素 1. はじめに生体内のほとんどの化学変化は酵素 (enzyme) というタンパク質によって触媒される 近年, タンパク質以外の物質が生体内で触媒作用を発揮する例が見つかっている 例えば, 一部の RNA( リボ核酸 ) には, 触媒作用がある 2. 酵素のはたらき方 (1) 酵素作用のモデル酵素と結びつき変化を受ける物質を基質 (substrate) という 基質は酵素分子の表面の特定の部位
3 酵素 1. はじめに生体内のほとんどの化学変化は酵素 (enzyme) というタンパク質によって触媒される 近年, タンパク質以外の物質が生体内で触媒作用を発揮する例が見つかっている 例えば, 一部の RNA( リボ核酸 ) には, 触媒作用がある 2. 酵素のはたらき方 (1) 酵素作用のモデル酵素と結びつき変化を受ける物質を基質 (substrate) という 基質は酵素分子の表面の特定の部位
報道発表資料 2006 年 8 月 7 日 独立行政法人理化学研究所 国立大学法人大阪大学 栄養素 亜鉛 は免疫のシグナル - 免疫系の活性化に細胞内亜鉛濃度が関与 - ポイント 亜鉛が免疫応答を制御 亜鉛がシグナル伝達分子として作用する 免疫の新領域を開拓独立行政法人理化学研究所 ( 野依良治理事
 60 秒でわかるプレスリリース 2006 年 8 月 7 日 独立行政法人理化学研究所 国立大学法人大阪大学 栄養素 亜鉛 は免疫のシグナル - 免疫系の活性化に細胞内亜鉛濃度が関与 - 私たちの生命維持を行うのに重要な役割を担う微量金属元素の一つとして知られていた 亜鉛 この亜鉛が欠乏すると 味覚障害や成長障害 免疫不全 神経系の異常などをきたします 理研免疫アレルギー科学総合研究センターサイトカイン制御研究グループと大阪大学の研究グループは
60 秒でわかるプレスリリース 2006 年 8 月 7 日 独立行政法人理化学研究所 国立大学法人大阪大学 栄養素 亜鉛 は免疫のシグナル - 免疫系の活性化に細胞内亜鉛濃度が関与 - 私たちの生命維持を行うのに重要な役割を担う微量金属元素の一つとして知られていた 亜鉛 この亜鉛が欠乏すると 味覚障害や成長障害 免疫不全 神経系の異常などをきたします 理研免疫アレルギー科学総合研究センターサイトカイン制御研究グループと大阪大学の研究グループは
報道発表資料 2006 年 4 月 13 日 独立行政法人理化学研究所 抗ウイルス免疫発動機構の解明 - 免疫 アレルギー制御のための新たな標的分子を発見 - ポイント 異物センサー TLR のシグナル伝達機構を解析 インターフェロン産生に必須な分子 IKK アルファ を発見 免疫 アレルギーの有効
 60 秒でわかるプレスリリース 2006 年 4 月 13 日 独立行政法人理化学研究所 抗ウイルス免疫発動機構の解明 - 免疫 アレルギー制御のための新たな標的分子を発見 - がんやウイルスなど身体を蝕む病原体から身を守る物質として インターフェロン が注目されています このインターフェロンのことは ご存知の方も多いと思いますが 私たちが生まれながらに持っている免疫をつかさどる物質です 免疫細胞の情報の交換やウイルス感染に強い防御を示す役割を担っています
60 秒でわかるプレスリリース 2006 年 4 月 13 日 独立行政法人理化学研究所 抗ウイルス免疫発動機構の解明 - 免疫 アレルギー制御のための新たな標的分子を発見 - がんやウイルスなど身体を蝕む病原体から身を守る物質として インターフェロン が注目されています このインターフェロンのことは ご存知の方も多いと思いますが 私たちが生まれながらに持っている免疫をつかさどる物質です 免疫細胞の情報の交換やウイルス感染に強い防御を示す役割を担っています
<4D F736F F D B82C982C282A282C482512E646F63>
 サンプル条件および固定化分子の選択 Biacoreの実験ではセンサーチップに固定化する分子をリガンド それに対して結合を測定する分子をアナライトと呼びます いずれの分子をリガンドとし アナライトとするかは 実験系を構築する上で重要です 以下にサンプルに適したリガンド アナライトの設計方法やサンプルの必要条件などをご紹介します アナライト リガンド センサーチップ (1) タンパク質リガンドとしてもアナライトとしても用いることができます
サンプル条件および固定化分子の選択 Biacoreの実験ではセンサーチップに固定化する分子をリガンド それに対して結合を測定する分子をアナライトと呼びます いずれの分子をリガンドとし アナライトとするかは 実験系を構築する上で重要です 以下にサンプルに適したリガンド アナライトの設計方法やサンプルの必要条件などをご紹介します アナライト リガンド センサーチップ (1) タンパク質リガンドとしてもアナライトとしても用いることができます
1. 背景血小板上の受容体 CLEC-2 と ある種のがん細胞の表面に発現するタンパク質 ポドプラニン やマムシ毒 ロドサイチン が結合すると 血小板が活性化され 血液が凝固します ( 図 1) ポドプラニンは O- 結合型糖鎖が結合した糖タンパク質であり CLEC-2 受容体との結合にはその糖鎖が
 参考資料配布 2014 年 11 月 10 日 独立行政法人理化学研究所 国立大学法人東北大学 血小板上の受容体 CLEC-2 は糖鎖とペプチド鎖の両方を認識 - マムシ毒は糖鎖に依存せず受容体と結合 - 本研究成果のポイント レクチンは糖鎖とのみ結合する というこれまでの考え方を覆す CLEC-2 受容体は同じ領域でマムシ毒とがんに関わる糖タンパク質に結合 糖鎖を模倣したペプチド性薬剤の設計への応用に期待
参考資料配布 2014 年 11 月 10 日 独立行政法人理化学研究所 国立大学法人東北大学 血小板上の受容体 CLEC-2 は糖鎖とペプチド鎖の両方を認識 - マムシ毒は糖鎖に依存せず受容体と結合 - 本研究成果のポイント レクチンは糖鎖とのみ結合する というこれまでの考え方を覆す CLEC-2 受容体は同じ領域でマムシ毒とがんに関わる糖タンパク質に結合 糖鎖を模倣したペプチド性薬剤の設計への応用に期待
Untitled
 上原記念生命科学財団研究報告集, 26 (2012) 75. 哺乳類のゴルジ体ストレス応答の分子機構の解明 吉田秀郎 Key words: ゴルジ体, 小胞体, 転写, ストレス応答, 細胞小器官 兵庫県立大学大学院生命理学研究科生体物質化学 Ⅱ 講座 緒言細胞内には様々な細胞小器官が存在して細胞の機能を分担しているが, その存在量は細胞の需要に応じて厳密に制御されており, 必要な時に必要な細胞小器官が必要な量だけ増強される.
上原記念生命科学財団研究報告集, 26 (2012) 75. 哺乳類のゴルジ体ストレス応答の分子機構の解明 吉田秀郎 Key words: ゴルジ体, 小胞体, 転写, ストレス応答, 細胞小器官 兵庫県立大学大学院生命理学研究科生体物質化学 Ⅱ 講座 緒言細胞内には様々な細胞小器官が存在して細胞の機能を分担しているが, その存在量は細胞の需要に応じて厳密に制御されており, 必要な時に必要な細胞小器官が必要な量だけ増強される.
Microsoft PowerPoint マクロ生物学9
 マクロ生物学 9 生物は様々な化学反応で動いている 大阪大学工学研究科応用生物工学専攻細胞動態学領域 : 福井希一 1 生物の物質的基盤 Deleted based on copyright concern. カープ分子細胞生物学 より 2 8. 生物は様々な化学反応で動い ている 1. 生命の化学的基礎 2. 生命の物理法則 3 1. 生命の化学的基礎 1. 結合 2. 糖 脂質 3. 核酸 4.
マクロ生物学 9 生物は様々な化学反応で動いている 大阪大学工学研究科応用生物工学専攻細胞動態学領域 : 福井希一 1 生物の物質的基盤 Deleted based on copyright concern. カープ分子細胞生物学 より 2 8. 生物は様々な化学反応で動い ている 1. 生命の化学的基礎 2. 生命の物理法則 3 1. 生命の化学的基礎 1. 結合 2. 糖 脂質 3. 核酸 4.
( 図 ) IP3 と IRBIT( アービット ) が IP3 受容体に競合して結合する様子
 60 秒でわかるプレスリリース 2006 年 6 月 23 日 独立行政法人理化学研究所 独立行政法人科学技術振興機構 細胞内のカルシウムチャネルに情報伝達を邪魔する 偽結合体 を発見 - IP3 受容体に IP3 と競合して結合するタンパク質 アービット の機能を解明 - 細胞分裂 細胞死 受精 発生など 私たちの生の営みそのものに関わる情報伝達は 細胞内のカルシウムイオンの放出によって行われています
60 秒でわかるプレスリリース 2006 年 6 月 23 日 独立行政法人理化学研究所 独立行政法人科学技術振興機構 細胞内のカルシウムチャネルに情報伝達を邪魔する 偽結合体 を発見 - IP3 受容体に IP3 と競合して結合するタンパク質 アービット の機能を解明 - 細胞分裂 細胞死 受精 発生など 私たちの生の営みそのものに関わる情報伝達は 細胞内のカルシウムイオンの放出によって行われています
糖鎖の新しい機能を発見:補体系をコントロールして健康な脳神経を維持する
 糖鎖の新しい機能を発見 : 補体系をコントロールして健康な脳神経を維持する ポイント 神経細胞上の糖脂質の糖鎖構造が正常パターンになっていないと 細胞膜の構造や機能が障害されて 外界からのシグナルに対する反応や攻撃に対する防御反応が異常になることが示された 細胞膜のタンパク質や脂質に結合している糖鎖の役割として 補体の活性のコントロールという新規の重要な機能が明らかになった 糖脂質の糖鎖が欠損すると
糖鎖の新しい機能を発見 : 補体系をコントロールして健康な脳神経を維持する ポイント 神経細胞上の糖脂質の糖鎖構造が正常パターンになっていないと 細胞膜の構造や機能が障害されて 外界からのシグナルに対する反応や攻撃に対する防御反応が異常になることが示された 細胞膜のタンパク質や脂質に結合している糖鎖の役割として 補体の活性のコントロールという新規の重要な機能が明らかになった 糖脂質の糖鎖が欠損すると
PowerPoint プレゼンテーション
 アミノ酸代謝 (1) 平成 30 年度 6 月 14 日 1 限病態生化学分野 吉澤達也 アミノ酸代謝 アミノ酸の修飾 食物タンパク質 消化吸収 分解 タンパク質 (20 種類 +α) 遊離アミノ酸 生合成 アミノ酸の生合成 ( 栄養学的非必須アミノ酸 ) 窒素 分解 炭素骨格 非タンパク質性誘導体 ( 神経伝達物質 ホルモン アミノ糖など ) 尿素サイクル 代謝中間体 尿素 糖質 脂質 エネルギー
アミノ酸代謝 (1) 平成 30 年度 6 月 14 日 1 限病態生化学分野 吉澤達也 アミノ酸代謝 アミノ酸の修飾 食物タンパク質 消化吸収 分解 タンパク質 (20 種類 +α) 遊離アミノ酸 生合成 アミノ酸の生合成 ( 栄養学的非必須アミノ酸 ) 窒素 分解 炭素骨格 非タンパク質性誘導体 ( 神経伝達物質 ホルモン アミノ糖など ) 尿素サイクル 代謝中間体 尿素 糖質 脂質 エネルギー
Microsoft PowerPoint - agonist
 図説薬理学 Pictured Pharmacology アゴニストとアンタゴニストの関係 宮崎大学農学部獣医薬理学講座伊藤勝昭 禁 : 無断転載 Copyright: Katsuaki Ito Veterinary Pharmacology University of Miyazaki このファイルは学生が講義で聞いた内容を正確に より深く理解するために作られたもので 教科書の補助資料です ファイルの内容の無断転載を防ぐため
図説薬理学 Pictured Pharmacology アゴニストとアンタゴニストの関係 宮崎大学農学部獣医薬理学講座伊藤勝昭 禁 : 無断転載 Copyright: Katsuaki Ito Veterinary Pharmacology University of Miyazaki このファイルは学生が講義で聞いた内容を正確に より深く理解するために作られたもので 教科書の補助資料です ファイルの内容の無断転載を防ぐため
今後の展開現在でも 自己免疫疾患の発症機構については不明な点が多くあります 今回の発見により 今後自己免疫疾患の発症機構の理解が大きく前進すると共に 今まで見過ごされてきたイントロン残存の重要性が 生体反応の様々な局面で明らかにされることが期待されます 図 1 Jmjd6 欠損型の胸腺をヌードマウス
 PRESS RELEASE(2015/11/05) 九州大学広報室 819-0395 福岡市西区元岡 744 TEL:092-802-2130 FAX:092-802-2139 MAIL:[email protected] URL:http://www.kyushu-u.ac.jp 免疫細胞が自分自身を攻撃しないために必要な新たな仕組みを発見 - 自己免疫疾患の発症機構の解明に期待 -
PRESS RELEASE(2015/11/05) 九州大学広報室 819-0395 福岡市西区元岡 744 TEL:092-802-2130 FAX:092-802-2139 MAIL:[email protected] URL:http://www.kyushu-u.ac.jp 免疫細胞が自分自身を攻撃しないために必要な新たな仕組みを発見 - 自己免疫疾患の発症機構の解明に期待 -
第11回 肝、筋、脳、脂肪組織での代謝の統合
 第 11 回肝 筋 脳 脂肪組織 での代謝の統合 日紫喜光良 基礎生化学講義 2014.7.8 1 講義項目 1 低血糖の結果 対処 原因 2 グルカゴン インスリンの分泌と作用 3 摂食 絶食サイクルと臓器間連携 2 低血糖の症状
第 11 回肝 筋 脳 脂肪組織 での代謝の統合 日紫喜光良 基礎生化学講義 2014.7.8 1 講義項目 1 低血糖の結果 対処 原因 2 グルカゴン インスリンの分泌と作用 3 摂食 絶食サイクルと臓器間連携 2 低血糖の症状
先端生物工学演習Ⅱ 「タンパク質の電気泳動」
 先端生物工学演習 Ⅱ タンパク質の電気泳動 2008 年 10 月 14 日 ( 旧 ) 進化生命システム学塚田幸治 1 話の中身 電気泳動という手法 ( 一般 ) アミノ酸の電荷とタンパク質の電荷 具体的な実験手法について ( 原理 ) Native( ( 構造や機能が破壊されていないタンパク質 ) SDS( ( 変性条件下でのタンパク質 ) 応用例 等電点電気泳動法と二次元電気泳動 非特異的染色法と特異的染色法
先端生物工学演習 Ⅱ タンパク質の電気泳動 2008 年 10 月 14 日 ( 旧 ) 進化生命システム学塚田幸治 1 話の中身 電気泳動という手法 ( 一般 ) アミノ酸の電荷とタンパク質の電荷 具体的な実験手法について ( 原理 ) Native( ( 構造や機能が破壊されていないタンパク質 ) SDS( ( 変性条件下でのタンパク質 ) 応用例 等電点電気泳動法と二次元電気泳動 非特異的染色法と特異的染色法
生物学入門
 第 2 章生命の化学的基礎 生物を構成している元素は 地球上の物質を構成している元素と何ら異なることはない 化学で学んできたこと これから学ぶことが 生物学を理解するための基礎となる 化学の詳しいことは 化学科のおこなう講義や実習に任せることにして ここでは生物学を学ぶために必要な 最低限のことを学ぶことにする 1. 水の性質 生体を構成している分子の中で 割合が一番多いのは 水 である 生体に占める水の割合はおよそ
第 2 章生命の化学的基礎 生物を構成している元素は 地球上の物質を構成している元素と何ら異なることはない 化学で学んできたこと これから学ぶことが 生物学を理解するための基礎となる 化学の詳しいことは 化学科のおこなう講義や実習に任せることにして ここでは生物学を学ぶために必要な 最低限のことを学ぶことにする 1. 水の性質 生体を構成している分子の中で 割合が一番多いのは 水 である 生体に占める水の割合はおよそ
の活性化が背景となるヒト悪性腫瘍の治療薬開発につながる 図4 研究である 研究内容 私たちは図3に示すようなyeast two hybrid 法を用いて AKT分子に結合する細胞内分子のスクリーニングを行った この結果 これまで機能の分からなかったプロトオンコジン TCL1がAKTと結合し多量体を形
 AKT活性を抑制するペプチ ド阻害剤の開発 野口 昌幸 北海道大学遺伝子病制御研究所 教授 広村 信 北海道大学遺伝子病制御研究所 ポスドク 岡田 太 北海道大学遺伝子病制御研究所 助手 柳舘 拓也 株式会社ラボ 研究員 ナーゼAKTに結合するタンパク分子を検索し これまで機能の 分からなかったプロトオンコジンTCL1がAKTと結合し AKT の活性化を促す AKT活性補助因子 であることを見い出し
AKT活性を抑制するペプチ ド阻害剤の開発 野口 昌幸 北海道大学遺伝子病制御研究所 教授 広村 信 北海道大学遺伝子病制御研究所 ポスドク 岡田 太 北海道大学遺伝子病制御研究所 助手 柳舘 拓也 株式会社ラボ 研究員 ナーゼAKTに結合するタンパク分子を検索し これまで機能の 分からなかったプロトオンコジンTCL1がAKTと結合し AKT の活性化を促す AKT活性補助因子 であることを見い出し
Microsoft PowerPoint - DNA1.ppt [互換モード]
![Microsoft PowerPoint - DNA1.ppt [互換モード] Microsoft PowerPoint - DNA1.ppt [互換モード]](/thumbs/94/118241118.jpg) 生物物理化学 タンパク質をコードする遺伝子 (135~) 本 PPT 資料の作成には福岡大学機能生物研究室のホームページを参考にした http://133.100.212.50/~bc1/biochem/index2.htm 1 DA( デオキシリボ核酸 ) の化学的特徴 シャルガフ則とDAのX 線回折像をもとに,DAの構造が予測された (Watson & Crick 1953 年 ) 2 Watson
生物物理化学 タンパク質をコードする遺伝子 (135~) 本 PPT 資料の作成には福岡大学機能生物研究室のホームページを参考にした http://133.100.212.50/~bc1/biochem/index2.htm 1 DA( デオキシリボ核酸 ) の化学的特徴 シャルガフ則とDAのX 線回折像をもとに,DAの構造が予測された (Watson & Crick 1953 年 ) 2 Watson
 60 秒でわかるプレスリリース 2008 年 2 月 19 日 独立行政法人理化学研究所 抗ウイルス反応を増強する重要分子 PDC-TREM を発見 - 形質細胞様樹状細胞が Ⅰ 型インターフェロンの産生を増幅する仕組みが明らかに - インフルエンザの猛威が続いています このインフルエンザの元凶であるインフルエンザウイルスは 獲得した免疫力やウイルスに対するワクチンを見透かすよう変異し続けるため 人類はいまだ発病の恐怖から免れることができません
60 秒でわかるプレスリリース 2008 年 2 月 19 日 独立行政法人理化学研究所 抗ウイルス反応を増強する重要分子 PDC-TREM を発見 - 形質細胞様樹状細胞が Ⅰ 型インターフェロンの産生を増幅する仕組みが明らかに - インフルエンザの猛威が続いています このインフルエンザの元凶であるインフルエンザウイルスは 獲得した免疫力やウイルスに対するワクチンを見透かすよう変異し続けるため 人類はいまだ発病の恐怖から免れることができません
Microsoft PowerPoint - protein1.ppt [互換モード]
![Microsoft PowerPoint - protein1.ppt [互換モード] Microsoft PowerPoint - protein1.ppt [互換モード]](/thumbs/92/108226396.jpg) 生物物理化学 1 セントラルドグマ (central doguma) DA から蛋白質が作られるまでの道筋 フランシス クリックが提唱した 原核生物と真核生物では 若干関与するタンパク質が異なるが 基本的には同じメカニズムで転写 翻訳 タンパク合成が行われる 原核生物 : 核膜が無い ( 構造的に区別出来る核を持たない ) 細胞 ( これを原核細胞という ) から成る生物で 細菌類や藍藻類がこれに属する
生物物理化学 1 セントラルドグマ (central doguma) DA から蛋白質が作られるまでの道筋 フランシス クリックが提唱した 原核生物と真核生物では 若干関与するタンパク質が異なるが 基本的には同じメカニズムで転写 翻訳 タンパク合成が行われる 原核生物 : 核膜が無い ( 構造的に区別出来る核を持たない ) 細胞 ( これを原核細胞という ) から成る生物で 細菌類や藍藻類がこれに属する
報道発表資料 2006 年 6 月 21 日 独立行政法人理化学研究所 アレルギー反応を制御する新たなメカニズムを発見 - 謎の免疫細胞 記憶型 T 細胞 がアレルギー反応に必須 - ポイント アレルギー発症の細胞を可視化する緑色蛍光マウスの開発により解明 分化 発生等で重要なノッチ分子への情報伝達
 60 秒でわかるプレスリリース 2006 年 6 月 21 日 独立行政法人理化学研究所 アレルギー反応を制御する新たなメカニズムを発見 - 謎の免疫細胞 記憶型 T 細胞 がアレルギー反応に必須 - カビが猛威を振るう梅雨の季節 この時期に限って喘息がでるんですよ というあなたは カビ アレルギー アレルギーを引き起こす原因物質は ハウスダストや食べ物 アクセサリなどとさまざまで この季節だけではない
60 秒でわかるプレスリリース 2006 年 6 月 21 日 独立行政法人理化学研究所 アレルギー反応を制御する新たなメカニズムを発見 - 謎の免疫細胞 記憶型 T 細胞 がアレルギー反応に必須 - カビが猛威を振るう梅雨の季節 この時期に限って喘息がでるんですよ というあなたは カビ アレルギー アレルギーを引き起こす原因物質は ハウスダストや食べ物 アクセサリなどとさまざまで この季節だけではない
生物時計の安定性の秘密を解明
 平成 25 年 12 月 13 日 生物時計の安定性の秘密を解明 概要 名古屋大学理学研究科の北山陽子助教 近藤孝男特任教授らの研究グループは 光合 成をおこなうシアノバクテリアの生物時計機構を解析し 時計タンパク質 KaiC が 安定な 24 時 間周期のリズムを形成する分子機構を明らかにしました 生物は, 生物時計 ( 概日時計 ) を利用して様々な生理現象を 時間的に コントロールし 効 率的に生活しています
平成 25 年 12 月 13 日 生物時計の安定性の秘密を解明 概要 名古屋大学理学研究科の北山陽子助教 近藤孝男特任教授らの研究グループは 光合 成をおこなうシアノバクテリアの生物時計機構を解析し 時計タンパク質 KaiC が 安定な 24 時 間周期のリズムを形成する分子機構を明らかにしました 生物は, 生物時計 ( 概日時計 ) を利用して様々な生理現象を 時間的に コントロールし 効 率的に生活しています
2. 看護に必要な栄養と代謝について説明できる 栄養素としての糖質 脂質 蛋白質 核酸 ビタミンなどの性質と役割 およびこれらの栄養素に関連する生命活動について具体例を挙げて説明できる 生体内では常に物質が交代していることを説明できる 代謝とは エネルギーを生み出し 生体成分を作り出す反応であること
 生化学 責任者 コーディネーター 看護専門基礎講座塚本恭正准教授 担当講座 学科 ( 分野 ) 看護専門基礎講座 対象学年 1 期間後期 区分 時間数 講義 22.5 時間 単位数 2 単位 学習方針 ( 講義概要等 ) 生化学反応の場となる細胞と細胞小器官の構造と機能を理解する エネルギー ATP を産生し 生体成分を作り出す代謝反応が生命活動で果たす役割を理解し 代謝反応での酵素の働きを学ぶ からだを構成する蛋白質
生化学 責任者 コーディネーター 看護専門基礎講座塚本恭正准教授 担当講座 学科 ( 分野 ) 看護専門基礎講座 対象学年 1 期間後期 区分 時間数 講義 22.5 時間 単位数 2 単位 学習方針 ( 講義概要等 ) 生化学反応の場となる細胞と細胞小器官の構造と機能を理解する エネルギー ATP を産生し 生体成分を作り出す代謝反応が生命活動で果たす役割を理解し 代謝反応での酵素の働きを学ぶ からだを構成する蛋白質
Slide 1
 転写 1. タンパク合成における RNA の役割酵素誘導 2. RNA ポリメラーゼ鎖型への結合転写開始鎖延長転写終結真核生物の RNA ポリメラーゼ 3. 原核生物における転写制御プロモーターカタボライト ( 異化代謝産物 ) 抑制オペロン 4. 転写後修飾プロセシング RNA ポリメラーゼ ( 鎖型への結合 ) プロモーターに特異的に結合 大腸菌の代表的なプロモーターのセンス鎖の配列 RNA ポリメラーゼ
転写 1. タンパク合成における RNA の役割酵素誘導 2. RNA ポリメラーゼ鎖型への結合転写開始鎖延長転写終結真核生物の RNA ポリメラーゼ 3. 原核生物における転写制御プロモーターカタボライト ( 異化代謝産物 ) 抑制オペロン 4. 転写後修飾プロセシング RNA ポリメラーゼ ( 鎖型への結合 ) プロモーターに特異的に結合 大腸菌の代表的なプロモーターのセンス鎖の配列 RNA ポリメラーゼ
B. モル濃度 速度定数と化学反応の速さ 1.1 段階反応 ( 単純反応 ): + I HI を例に H ヨウ化水素 HI が生成する速さ は,H と I のモル濃度をそれぞれ [ ], [ I ] [ H ] [ I ] に比例することが, 実験により, わかっている したがって, 比例定数を k
![B. モル濃度 速度定数と化学反応の速さ 1.1 段階反応 ( 単純反応 ): + I HI を例に H ヨウ化水素 HI が生成する速さ は,H と I のモル濃度をそれぞれ [ ], [ I ] [ H ] [ I ] に比例することが, 実験により, わかっている したがって, 比例定数を k B. モル濃度 速度定数と化学反応の速さ 1.1 段階反応 ( 単純反応 ): + I HI を例に H ヨウ化水素 HI が生成する速さ は,H と I のモル濃度をそれぞれ [ ], [ I ] [ H ] [ I ] に比例することが, 実験により, わかっている したがって, 比例定数を k](/thumbs/81/83835231.jpg) 反応速度 触媒 速度定数 反応次数について. 化学反応の速さの表し方 速さとは単位時間あたりの変化の大きさである 大きさの値は 0 以上ですから, 速さは 0 以上の値をとる 化学反応の速さは単位時間あたりの物質のモル濃度変化の大きさで表すのが一般的 たとえば, a + bb c (, B, は物質, a, b, c は係数 ) という反応において,, B, それぞれの反応の速さを, B, とし,
反応速度 触媒 速度定数 反応次数について. 化学反応の速さの表し方 速さとは単位時間あたりの変化の大きさである 大きさの値は 0 以上ですから, 速さは 0 以上の値をとる 化学反応の速さは単位時間あたりの物質のモル濃度変化の大きさで表すのが一般的 たとえば, a + bb c (, B, は物質, a, b, c は係数 ) という反応において,, B, それぞれの反応の速さを, B, とし,
生物 第39講~第47講 テキスト
 基礎から分かる生物 興奮の伝導と伝達 1. 興奮の伝導 1 興奮の伝導 興奮が生じると, 興奮が生じた部位と隣接する静止状態の部位の間で電位の差が発生する. この電位差により, 興奮部分から隣接部へと活動電流が流れる. 活動電流が隣接部を興奮させる刺激となり, 隣接部が次々と興奮する. これによって興奮は, 興奮が発生した部位から軸索内を両方向に伝導する. 1 興奮の発生 2 隣接部に活動電流が流れる
基礎から分かる生物 興奮の伝導と伝達 1. 興奮の伝導 1 興奮の伝導 興奮が生じると, 興奮が生じた部位と隣接する静止状態の部位の間で電位の差が発生する. この電位差により, 興奮部分から隣接部へと活動電流が流れる. 活動電流が隣接部を興奮させる刺激となり, 隣接部が次々と興奮する. これによって興奮は, 興奮が発生した部位から軸索内を両方向に伝導する. 1 興奮の発生 2 隣接部に活動電流が流れる
化学物質の分析 > 臨床で用いる分析技術 > 分析技術 > 免疫学的測定法 1 免疫学的測定法 免疫反応を利用して物質を分析する方法として 免疫学的測定法 ( イムノアッセイ ) がある イムノアッセイは 抗体に抗原を認識させる ( 抗原抗体反応を利用する ) ことにより 物質を定量する分析法であり
 1 免疫学的測定法 免疫反応を利用して物質を分析する方法として 免疫学的測定法 ( イムノアッセイ ) がある イムノアッセイは 抗体に抗原を認識させる ( 抗原抗体反応を利用する ) ことにより 物質を定量する分析法であり 多成分一斉解析には不向きであるが 高感度な測定が可能である また 合成医薬品やステロイドホルモンなどの低分子からタンパク質や核酸などの高分子までさまざまな物質の定量に用いられている
1 免疫学的測定法 免疫反応を利用して物質を分析する方法として 免疫学的測定法 ( イムノアッセイ ) がある イムノアッセイは 抗体に抗原を認識させる ( 抗原抗体反応を利用する ) ことにより 物質を定量する分析法であり 多成分一斉解析には不向きであるが 高感度な測定が可能である また 合成医薬品やステロイドホルモンなどの低分子からタンパク質や核酸などの高分子までさまざまな物質の定量に用いられている
グルコースは膵 β 細胞内に糖輸送担体を介して取り込まれて代謝され A T P が産生される その結果 A T P 感受性 K チャンネルの閉鎖 細胞膜の脱分極 電位依存性 Caチャンネルの開口 細胞内 Ca 2+ 濃度の上昇が起こり インスリンが分泌される これをインスリン分泌の惹起経路と呼ぶ イ
 薬効薬理 1. 作用機序 アナグリプチンはジペプチジルペプチダーゼ -4(DPP-4) の競合的かつ可逆的な選択的阻害剤である インクレチンであるグルカゴン様ペプチド-1(GL P-1) 及びグルコース依存性インスリン分泌刺激ポリペプチド (GI P) は グルコース依存的なインスリン分泌促進作用やグルカゴン分泌抑制作用等 ( 主にGLP-1の作用 ) を有するが 24) DPP-4により分解されて活性を失う
薬効薬理 1. 作用機序 アナグリプチンはジペプチジルペプチダーゼ -4(DPP-4) の競合的かつ可逆的な選択的阻害剤である インクレチンであるグルカゴン様ペプチド-1(GL P-1) 及びグルコース依存性インスリン分泌刺激ポリペプチド (GI P) は グルコース依存的なインスリン分泌促進作用やグルカゴン分泌抑制作用等 ( 主にGLP-1の作用 ) を有するが 24) DPP-4により分解されて活性を失う
7. 細胞の情報伝達と物質輸送
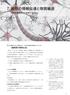 7. 細胞の情報伝達と物質輸送 生物が個体として存在するために 7-1. 細胞はたがいに影響しあい さまざまな情報や物質をやりとりする 細胞間の情報伝達 生物は 光 熱 音 化学物質 磁気など外部環境からの多種多様なシグ ナルに応答 適応する仕組みを備えています 多細胞生物の体内の細胞は周 りの細胞と細胞外液という環境からのシグナルを受け それに応答します 細胞間で情報を交換する方法として下記の 3
7. 細胞の情報伝達と物質輸送 生物が個体として存在するために 7-1. 細胞はたがいに影響しあい さまざまな情報や物質をやりとりする 細胞間の情報伝達 生物は 光 熱 音 化学物質 磁気など外部環境からの多種多様なシグ ナルに応答 適応する仕組みを備えています 多細胞生物の体内の細胞は周 りの細胞と細胞外液という環境からのシグナルを受け それに応答します 細胞間で情報を交換する方法として下記の 3
Microsoft Word - Dr. Abe.doc
 3 ステップ アビジン - ビオチンシステム (SAB 法 ) とポリマー法 慶應義塾大学医学部病理学教室阿部仁 はじめに 免疫組織化学は Coons らが蛍光色素を抗体に標識した蛍光抗体法の技術を確立してから Singers のフェリチン抗体法を経て 1967 年に Nakane と Pierce により標識物質に西洋ワサビペルオキシダーゼ (horseradish peroxidase:hrp)
3 ステップ アビジン - ビオチンシステム (SAB 法 ) とポリマー法 慶應義塾大学医学部病理学教室阿部仁 はじめに 免疫組織化学は Coons らが蛍光色素を抗体に標識した蛍光抗体法の技術を確立してから Singers のフェリチン抗体法を経て 1967 年に Nakane と Pierce により標識物質に西洋ワサビペルオキシダーゼ (horseradish peroxidase:hrp)
平成24年7月x日
 < 概要 > 栄養素の過剰摂取が引き金となり発症する生活習慣病 ( 痛風 動脈硬化や2 型糖尿病など ) は 現代社会における重要な健康問題となっています 近年の研究により 生活習慣病の発症には自然免疫機構を介した炎症の誘導が深く関わることが明らかになってきました 自然免疫機構は 病原性微生物を排除するための感染防御機構としてよく知られていますが 過栄養摂取により生じる代謝物にも反応するために 強い炎症を引き起こして生活習慣病の発症要因になってしまいます
< 概要 > 栄養素の過剰摂取が引き金となり発症する生活習慣病 ( 痛風 動脈硬化や2 型糖尿病など ) は 現代社会における重要な健康問題となっています 近年の研究により 生活習慣病の発症には自然免疫機構を介した炎症の誘導が深く関わることが明らかになってきました 自然免疫機構は 病原性微生物を排除するための感染防御機構としてよく知られていますが 過栄養摂取により生じる代謝物にも反応するために 強い炎症を引き起こして生活習慣病の発症要因になってしまいます
Microsoft PowerPoint - プレゼンテーション1
 A A RNA からタンパク質へ mrna の塩基配列は 遺伝暗号を介してタンパク質のアミノ酸の配列へと翻訳される trna とアミノ酸の結合 RNA 分子は 3 通りの読み枠で翻訳できる trnaは アミノ酸とコドンを結びつけるアダプター分子である (Ψ; プソイドウリジン D; ジヒドロウリジンどちらもウラシルが化学修飾したもの ) アミノアシル trna 合成酵素によって アミノ酸と trna
A A RNA からタンパク質へ mrna の塩基配列は 遺伝暗号を介してタンパク質のアミノ酸の配列へと翻訳される trna とアミノ酸の結合 RNA 分子は 3 通りの読み枠で翻訳できる trnaは アミノ酸とコドンを結びつけるアダプター分子である (Ψ; プソイドウリジン D; ジヒドロウリジンどちらもウラシルが化学修飾したもの ) アミノアシル trna 合成酵素によって アミノ酸と trna
Microsoft PowerPoint - 新技術説明会配付資料rev提出版(後藤)修正.pp
 食品の抗アレルギー活性評価に利用できる マウスモデルの紹介 農研機構食品総合研究所 食品機能研究領域主任研究員 後藤真生 農研機構 は独立行政法人農業 食品産業技術総合研究機構のコミュニケーションネームです 国民の 1/3 はアレルギー症状を自覚している 1 アレルギー症状なし (59.1%) 皮膚 呼吸器 目鼻いずれかのアレルギー症状あり (35.9%) 医療機関に入院 通院中 (58.2%) (
食品の抗アレルギー活性評価に利用できる マウスモデルの紹介 農研機構食品総合研究所 食品機能研究領域主任研究員 後藤真生 農研機構 は独立行政法人農業 食品産業技術総合研究機構のコミュニケーションネームです 国民の 1/3 はアレルギー症状を自覚している 1 アレルギー症状なし (59.1%) 皮膚 呼吸器 目鼻いずれかのアレルギー症状あり (35.9%) 医療機関に入院 通院中 (58.2%) (
論文題目 腸管分化に関わるmiRNAの探索とその発現制御解析
 論文題目 腸管分化に関わる microrna の探索とその発現制御解析 氏名日野公洋 1. 序論 microrna(mirna) とは細胞内在性の 21 塩基程度の機能性 RNA のことであり 部分的相補的な塩基認識を介して標的 RNA の翻訳抑制や不安定化を引き起こすことが知られている mirna は細胞分化や増殖 ガン化やアポトーシスなどに関与していることが報告されており これら以外にも様々な細胞諸現象に関与していると考えられている
論文題目 腸管分化に関わる microrna の探索とその発現制御解析 氏名日野公洋 1. 序論 microrna(mirna) とは細胞内在性の 21 塩基程度の機能性 RNA のことであり 部分的相補的な塩基認識を介して標的 RNA の翻訳抑制や不安定化を引き起こすことが知られている mirna は細胞分化や増殖 ガン化やアポトーシスなどに関与していることが報告されており これら以外にも様々な細胞諸現象に関与していると考えられている
医薬品タンパク質は 安全性の面からヒト型が常識です ではなぜ 肌につける化粧品用コラーゲンは ヒト型でなくても良いのでしょうか? アレルギーは皮膚から 最近の学説では 皮膚から侵入したアレルゲンが 食物アレルギー アトピー性皮膚炎 喘息 アレルギー性鼻炎などのアレルギー症状を引き起こすきっかけになる
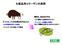 化粧品用コラーゲンの原料 現在は 魚由来が中心 かつては ウシの皮膚由来がほとんど BSE 等病原体混入の危険 人に感染する病原体をもたない アレルギーの問題は未解決 ( むしろ問題は大きくなったかもしれない ) アレルギーを引き起こす可能性 医薬品タンパク質は 安全性の面からヒト型が常識です ではなぜ 肌につける化粧品用コラーゲンは ヒト型でなくても良いのでしょうか? アレルギーは皮膚から 最近の学説では
化粧品用コラーゲンの原料 現在は 魚由来が中心 かつては ウシの皮膚由来がほとんど BSE 等病原体混入の危険 人に感染する病原体をもたない アレルギーの問題は未解決 ( むしろ問題は大きくなったかもしれない ) アレルギーを引き起こす可能性 医薬品タンパク質は 安全性の面からヒト型が常識です ではなぜ 肌につける化粧品用コラーゲンは ヒト型でなくても良いのでしょうか? アレルギーは皮膚から 最近の学説では
1 編 / 生物の特徴 1 章 / 生物の共通性 1 生物の共通性 教科書 p.8 ~ 11 1 生物の特徴 (p.8 ~ 9) 1 地球上のすべての生物には, 次のような共通の特徴がある 生物は,a( 生物は,b( 生物は,c( ) で囲まれた細胞からなっている ) を遺伝情報として用いている )
 1 編 / 生物の特徴 1 章 / 生物の共通性 1 生物の共通性 教科書 p.8 ~ 11 1 生物の特徴 (p.8 ~ 9) 1 地球上のすべての生物には, 次のような共通の特徴がある 生物は,a( 生物は,b( 生物は,c( ) で囲まれた細胞からなっている ) を遺伝情報として用いている ) を利用していろいろな生命活動を行っている 生物は, 形質を子孫に伝える d( ) のしくみをもっている
1 編 / 生物の特徴 1 章 / 生物の共通性 1 生物の共通性 教科書 p.8 ~ 11 1 生物の特徴 (p.8 ~ 9) 1 地球上のすべての生物には, 次のような共通の特徴がある 生物は,a( 生物は,b( 生物は,c( ) で囲まれた細胞からなっている ) を遺伝情報として用いている ) を利用していろいろな生命活動を行っている 生物は, 形質を子孫に伝える d( ) のしくみをもっている
られる 糖尿病を合併した高血圧の治療の薬物治療の第一選択薬はアンジオテンシン変換酵素 (ACE) 阻害薬とアンジオテンシン II 受容体拮抗薬 (ARB) である このクラスの薬剤は単なる降圧効果のみならず 様々な臓器保護作用を有しているが ACE 阻害薬や ARB のプラセボ比較試験で糖尿病の新規
 論文の内容の要旨 論文題目アンジオテンシン受容体拮抗薬テルミサルタンの メタボリックシンドロームに対する効果の検討 指導教員門脇孝教授 東京大学大学院医学系研究科 平成 19 年 4 月入学 医学博士課程 内科学専攻 氏名廣瀬理沙 要旨 背景 目的 わが国の死因の第二位と第三位を占める心筋梗塞や脳梗塞などの心血管疾患を引き起こす基盤となる病態として 過剰なエネルギー摂取と運動不足などの生活習慣により内臓脂肪が蓄積する内臓脂肪型肥満を中心に
論文の内容の要旨 論文題目アンジオテンシン受容体拮抗薬テルミサルタンの メタボリックシンドロームに対する効果の検討 指導教員門脇孝教授 東京大学大学院医学系研究科 平成 19 年 4 月入学 医学博士課程 内科学専攻 氏名廣瀬理沙 要旨 背景 目的 わが国の死因の第二位と第三位を占める心筋梗塞や脳梗塞などの心血管疾患を引き起こす基盤となる病態として 過剰なエネルギー摂取と運動不足などの生活習慣により内臓脂肪が蓄積する内臓脂肪型肥満を中心に
木村の有機化学小ネタ 糖の構造 単糖類の鎖状構造と環状構造 1.D と L について D-グルコースとか L-アラニンの D,L の意味について説明する 1953 年右旋性 ( 偏光面を右に曲げる ) をもつグリセルアルデヒドの立体配置が
 糖の構造 単糖類の鎖状構造と環状構造.D と L について D-グルコースとか L-アラニンの D,L の意味について説明する 9 年右旋性 ( 偏光面を右に曲げる ) をもつグリセルアルデヒドの立体配置が X 線回折実験により決定され, 次の約束に従い, 構造式が示された 最も酸化された基を上端にする 上下の原子または原子団は中心原子より紙面奥に位置する 左右の原子または原子団は中心原子より紙面手前に位置する
糖の構造 単糖類の鎖状構造と環状構造.D と L について D-グルコースとか L-アラニンの D,L の意味について説明する 9 年右旋性 ( 偏光面を右に曲げる ) をもつグリセルアルデヒドの立体配置が X 線回折実験により決定され, 次の約束に従い, 構造式が示された 最も酸化された基を上端にする 上下の原子または原子団は中心原子より紙面奥に位置する 左右の原子または原子団は中心原子より紙面手前に位置する
スライド 1
 各論 (6) 物質代謝 異化と同化 物質代謝 異化と同化膵島ホルモン ( インスリン グルカゴン ) 糖尿病メタボリックシンドローム Presented by 岡本 飛永 松本 物質代謝とは エネルギーを消費して物質を合成 エネルギーを産生 同化を促進するホルモン : インスリン IGF-1 GH アンドロゲン 異化を促進するホルモン : グルカゴン 甲状腺ホルモン アドレナリン 膵島ホルモン 膵島とは
各論 (6) 物質代謝 異化と同化 物質代謝 異化と同化膵島ホルモン ( インスリン グルカゴン ) 糖尿病メタボリックシンドローム Presented by 岡本 飛永 松本 物質代謝とは エネルギーを消費して物質を合成 エネルギーを産生 同化を促進するホルモン : インスリン IGF-1 GH アンドロゲン 異化を促進するホルモン : グルカゴン 甲状腺ホルモン アドレナリン 膵島ホルモン 膵島とは
大学院博士課程共通科目ベーシックプログラム
 平成 30 年度医科学専攻共通科目 共通基礎科目実習 ( 旧コア実習 ) 概要 1 ). 大学院生が所属する教育研究分野における実習により単位認定可能な実習項目 ( コア実習項目 ) 1. 組換え DNA 技術実習 2. 生体物質の調製と解析実習 3. 薬理学実習 4. ウイルス学実習 5. 免疫学実習 6. 顕微鏡試料作成法実習 7. ゲノム医学実習 8. 共焦点レーザー顕微鏡実習 2 ). 実習を担当する教育研究分野においてのみ単位認定可能な実習項目
平成 30 年度医科学専攻共通科目 共通基礎科目実習 ( 旧コア実習 ) 概要 1 ). 大学院生が所属する教育研究分野における実習により単位認定可能な実習項目 ( コア実習項目 ) 1. 組換え DNA 技術実習 2. 生体物質の調製と解析実習 3. 薬理学実習 4. ウイルス学実習 5. 免疫学実習 6. 顕微鏡試料作成法実習 7. ゲノム医学実習 8. 共焦点レーザー顕微鏡実習 2 ). 実習を担当する教育研究分野においてのみ単位認定可能な実習項目
酵素阻害剤
 阻害剤の反応速度論福岡大学理学部化学科寺田成之. はじめに 阻害剤 (inhibitors) は酵素と相互に作用し, その反応効率を低下させる合成物または天然に存在する化合物 である ) それらは代謝反応速度をコントロールするための医薬品として用いられたり, 酵素反応機構を理解 するための道具としても用いられる 多くの有毒な化合物は酵素阻害剤で, 生体に大きな影響を与えるため, 抗生物質, 農薬,
阻害剤の反応速度論福岡大学理学部化学科寺田成之. はじめに 阻害剤 (inhibitors) は酵素と相互に作用し, その反応効率を低下させる合成物または天然に存在する化合物 である ) それらは代謝反応速度をコントロールするための医薬品として用いられたり, 酵素反応機構を理解 するための道具としても用いられる 多くの有毒な化合物は酵素阻害剤で, 生体に大きな影響を与えるため, 抗生物質, 農薬,
解糖系でへ 解糖系でへ - リン酸 - リン酸 1,-2 リン酸 ジヒドロキシアセトンリン酸 - リン酸 - リン酸 1,-2 リン酸 ジヒドロキシアセトンリン酸 AT AT リン酸化で細胞外に AT 出られなくなる 異性化して炭素数 AT の分子に分解される AT 2 ホスホエノール AT 2 1
 糖質の代謝 消化管 デンプン 小腸 肝門脈 AT 中性脂肪コレステロール アミノ酸 血管 各組織 筋肉 ムコ多糖プリンヌクレオチド AT 糖質の代謝 糖質からの AT 合成 の分解 : 解糖系 と酸化的リン酸化嫌気条件下の糖質の分解 : 発酵の合成 : 糖新生 糖質からの物質の合成 の合成プリンヌクレオチドの合成 : ペントースリン酸回路グルクロン酸の合成 : ウロン酸回路 糖質の代謝 体内のエネルギー源
糖質の代謝 消化管 デンプン 小腸 肝門脈 AT 中性脂肪コレステロール アミノ酸 血管 各組織 筋肉 ムコ多糖プリンヌクレオチド AT 糖質の代謝 糖質からの AT 合成 の分解 : 解糖系 と酸化的リン酸化嫌気条件下の糖質の分解 : 発酵の合成 : 糖新生 糖質からの物質の合成 の合成プリンヌクレオチドの合成 : ペントースリン酸回路グルクロン酸の合成 : ウロン酸回路 糖質の代謝 体内のエネルギー源
の感染が阻止されるという いわゆる 二度なし現象 の原理であり 予防接種 ( ワクチン ) を行う根拠でもあります 特定の抗原を認識する記憶 B 細胞は体内を循環していますがその数は非常に少なく その中で抗原に遭遇した僅かな記憶 B 細胞が著しく増殖し 効率良く形質細胞に分化することが 大量の抗体産
 TOKYO UNIVERSITY OF SCIENCE 1-3 KAGURAZAKA, SHINJUKU-KU, TOKYO 162-8601, JAPAN Phone: +81-3-5228-8107 報道関係各位 2018 年 8 月 6 日 免疫細胞が記憶した病原体を効果的に排除する機構の解明 ~ 記憶 B 細胞の二次抗体産生応答は IL-9 シグナルによって促進される ~ 東京理科大学 研究の要旨東京理科大学生命医科学研究所
TOKYO UNIVERSITY OF SCIENCE 1-3 KAGURAZAKA, SHINJUKU-KU, TOKYO 162-8601, JAPAN Phone: +81-3-5228-8107 報道関係各位 2018 年 8 月 6 日 免疫細胞が記憶した病原体を効果的に排除する機構の解明 ~ 記憶 B 細胞の二次抗体産生応答は IL-9 シグナルによって促進される ~ 東京理科大学 研究の要旨東京理科大学生命医科学研究所
共同研究チーム 個人情報につき 削除しております 1
 2016 年 12 月 19 日 17 時 ~ 記者レクチャー @ 文部科学省 細胞死を司る カルシウム動態の制御機構を解明 - アービット (IRBIT) が小胞体ーミトコンドリア間の Ca 2+ の移動を制御 - 共同研究チーム 個人情報につき 削除しております 1 アポトーシス : プログラムされた細胞死多細胞生物にみられる細胞の死に方の一つ 不要になった細胞や損傷を受けた細胞が積極的に自滅して個体を健全な状態に保つメカニズム
2016 年 12 月 19 日 17 時 ~ 記者レクチャー @ 文部科学省 細胞死を司る カルシウム動態の制御機構を解明 - アービット (IRBIT) が小胞体ーミトコンドリア間の Ca 2+ の移動を制御 - 共同研究チーム 個人情報につき 削除しております 1 アポトーシス : プログラムされた細胞死多細胞生物にみられる細胞の死に方の一つ 不要になった細胞や損傷を受けた細胞が積極的に自滅して個体を健全な状態に保つメカニズム
フォルハルト法 NH SCN の標準液または KSCN の標準液を用い,Ag または Hg を直接沈殿滴定する方法 および Cl, Br, I, CN, 試料溶液に Fe SCN, S 2 を指示薬として加える 例 : Cl の逆滴定による定量 などを逆滴定する方法をいう Fe を加えた試料液に硝酸
 沈殿滴定とモール法 沈殿滴定沈殿とは溶液に試薬を加えたり加熱や冷却をしたとき, 溶液から不溶性固体が分離する現象, またはその不溶性固体を沈殿という 不溶性固体は, 液底に沈んでいいても微粒子 ( コロイド ) として液中を浮遊していても沈殿と呼ばれる 沈殿滴定とは沈殿が生成あるいは消失する反応を利用した滴定のことをいう 沈殿が生成し始めた点, 沈殿の生成が完了した点, または沈殿が消失した点が滴定の終点となる
沈殿滴定とモール法 沈殿滴定沈殿とは溶液に試薬を加えたり加熱や冷却をしたとき, 溶液から不溶性固体が分離する現象, またはその不溶性固体を沈殿という 不溶性固体は, 液底に沈んでいいても微粒子 ( コロイド ) として液中を浮遊していても沈殿と呼ばれる 沈殿滴定とは沈殿が生成あるいは消失する反応を利用した滴定のことをいう 沈殿が生成し始めた点, 沈殿の生成が完了した点, または沈殿が消失した点が滴定の終点となる
RNA Poly IC D-IPS-1 概要 自然免疫による病原体成分の認識は炎症反応の誘導や 獲得免疫の成立に重要な役割を果たす生体防御機構です 今回 私達はウイルス RNA を模倣する合成二本鎖 RNA アナログの Poly I:C を用いて 自然免疫応答メカニズムの解析を行いました その結果
 RNA Poly IC D-IPS-1 概要 自然免疫による病原体成分の認識は炎症反応の誘導や 獲得免疫の成立に重要な役割を果たす生体防御機構です 今回 私達はウイルス RNA を模倣する合成二本鎖 RNA アナログの Poly I:C を用いて 自然免疫応答メカニズムの解析を行いました その結果 Poly I:C により一部の樹状細胞にネクローシス様の細胞死が誘導されること さらにこの細胞死がシグナル伝達経路の活性化により制御されていることが分かりました
RNA Poly IC D-IPS-1 概要 自然免疫による病原体成分の認識は炎症反応の誘導や 獲得免疫の成立に重要な役割を果たす生体防御機構です 今回 私達はウイルス RNA を模倣する合成二本鎖 RNA アナログの Poly I:C を用いて 自然免疫応答メカニズムの解析を行いました その結果 Poly I:C により一部の樹状細胞にネクローシス様の細胞死が誘導されること さらにこの細胞死がシグナル伝達経路の活性化により制御されていることが分かりました
練習問題
 生物有機化学 練習問題 ( はじめに ) 1 以下の各問題中で 反応機構を書け ということは 電子の流れを曲がった矢印を用いて説明せよ ということである 単純に生成物を書くだけでは正答とはならない 2 で表される結合は 立体異性体の混合物であることを表す 3 反応式を表す矢印 ( ) に書かれている試薬に番号が付いている場合 1. の試薬 を十分に反応させた後に 2. の試薬を加えることを表す 例えば
生物有機化学 練習問題 ( はじめに ) 1 以下の各問題中で 反応機構を書け ということは 電子の流れを曲がった矢印を用いて説明せよ ということである 単純に生成物を書くだけでは正答とはならない 2 で表される結合は 立体異性体の混合物であることを表す 3 反応式を表す矢印 ( ) に書かれている試薬に番号が付いている場合 1. の試薬 を十分に反応させた後に 2. の試薬を加えることを表す 例えば
脳組織傷害時におけるミクログリア形態変化および機能 Title変化に関する培養脳組織切片を用いた研究 ( Abstract_ 要旨 ) Author(s) 岡村, 敏行 Citation Kyoto University ( 京都大学 ) Issue Date URL http
 脳組織傷害時におけるミクログリア形態変化および機能 Title変化に関する培養脳組織切片を用いた研究 ( Abstract_ 要旨 ) Author(s) 岡村, 敏行 Citation Kyoto University ( 京都大学 ) Issue Date 2009-03-23 URL http://hdl.handle.net/2433/124054 Right Type Thesis or
脳組織傷害時におけるミクログリア形態変化および機能 Title変化に関する培養脳組織切片を用いた研究 ( Abstract_ 要旨 ) Author(s) 岡村, 敏行 Citation Kyoto University ( 京都大学 ) Issue Date 2009-03-23 URL http://hdl.handle.net/2433/124054 Right Type Thesis or
化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イ
 化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イオンと陰イオンの静電気的な引力による結合を 1 1 という ⑵ 2 個の水素原子は, それぞれ1 個の価電子を出し合い,
化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イオンと陰イオンの静電気的な引力による結合を 1 1 という ⑵ 2 個の水素原子は, それぞれ1 個の価電子を出し合い,
<4D F736F F F696E74202D2093AE95A88DD C88A77824F DD CC91E38ED3205B8CDD8AB B83685D>
 第 2 回細胞の代謝 教科書 4 章 &16 章 代謝 (Metabolism) 教科書 p46 好気的条件下で生きている細胞は 細胞外から摂取した栄養素を呼吸により酸化し 細胞活動エネルギーを獲得し 細胞内の様々な物質を分解 作り替える 細胞内の物質変換の過程を代謝と呼ぶ 酵素 代謝 物質変換 + エネルギー取入れ 生物 物質 & エネルギー 代謝 ATP 体構築 & 運動その他の活動 生物現象は
第 2 回細胞の代謝 教科書 4 章 &16 章 代謝 (Metabolism) 教科書 p46 好気的条件下で生きている細胞は 細胞外から摂取した栄養素を呼吸により酸化し 細胞活動エネルギーを獲得し 細胞内の様々な物質を分解 作り替える 細胞内の物質変換の過程を代謝と呼ぶ 酵素 代謝 物質変換 + エネルギー取入れ 生物 物質 & エネルギー 代謝 ATP 体構築 & 運動その他の活動 生物現象は
<4D F736F F D208DC58F498F4390B D4C95F189DB8A6D A A838A815B C8EAE814095CA8E86325F616B5F54492E646F63>
 インフルエンザウイルス感染によって起こる炎症反応のメカニズムを解明 1. 発表者 : 一戸猛志東京大学医科学研究所附属感染症国際研究センター感染制御系ウイルス学分野准教授 2. 発表のポイント : ウイルス感染によって起こる炎症反応の分子メカニズムを明らかにした注 炎症反応にはミトコンドリア外膜の mitofusin 2(Mfn2) 1 タンパク質が必要であった ウイルス感染後の過剰な炎症反応を抑えるような治療薬の開発
インフルエンザウイルス感染によって起こる炎症反応のメカニズムを解明 1. 発表者 : 一戸猛志東京大学医科学研究所附属感染症国際研究センター感染制御系ウイルス学分野准教授 2. 発表のポイント : ウイルス感染によって起こる炎症反応の分子メカニズムを明らかにした注 炎症反応にはミトコンドリア外膜の mitofusin 2(Mfn2) 1 タンパク質が必要であった ウイルス感染後の過剰な炎症反応を抑えるような治療薬の開発
リアルタイムPCRの基礎知識
 1. リアルタイム PCR の用途リアルタイム PCR 法は 遺伝子発現解析の他に SNPs タイピング 遺伝子組み換え食品の検査 ウイルスや病原菌の検出 導入遺伝子のコピー数の解析などさまざまな用途に応用されている 遺伝子発現解析のような定量解析は まさにリアルタイム PCR の得意とするところであるが プラス / マイナス判定だけの定性的な解析にもその威力を発揮する これは リアルタイム PCR
1. リアルタイム PCR の用途リアルタイム PCR 法は 遺伝子発現解析の他に SNPs タイピング 遺伝子組み換え食品の検査 ウイルスや病原菌の検出 導入遺伝子のコピー数の解析などさまざまな用途に応用されている 遺伝子発現解析のような定量解析は まさにリアルタイム PCR の得意とするところであるが プラス / マイナス判定だけの定性的な解析にもその威力を発揮する これは リアルタイム PCR
第4回 炭水化物の消化吸収と代謝(1)
 第 4 回炭水化物の消化吸収と 代謝 (1) 日紫喜光良 基礎生化学 2014.05.20 1 テーマ (1) 炭水化物の消化吸収 肝細胞などによる血糖の取り込み 細胞内での代謝の第一段階 - 解糖系 - (2) 解糖系に接続したグリコーゲン合成系 - エネルギー貯蔵形態のひとつ - について 2 項目 1 炭水化物の消化 2 吸収と肝臓への輸送 3 血糖の細胞への取り込み 4 解糖系とその調節 5グリコーゲン合成
第 4 回炭水化物の消化吸収と 代謝 (1) 日紫喜光良 基礎生化学 2014.05.20 1 テーマ (1) 炭水化物の消化吸収 肝細胞などによる血糖の取り込み 細胞内での代謝の第一段階 - 解糖系 - (2) 解糖系に接続したグリコーゲン合成系 - エネルギー貯蔵形態のひとつ - について 2 項目 1 炭水化物の消化 2 吸収と肝臓への輸送 3 血糖の細胞への取り込み 4 解糖系とその調節 5グリコーゲン合成
(Microsoft Word - \230a\225\266IChO46-Preparatory_Q36_\211\374\202Q_.doc)
 問題 36. 鉄 (Ⅲ) イオンとサリチルサリチル酸の錯形成 (20140304 修正 : ピンク色の部分 ) 1. 序論この簡単な実験では 水溶液中での鉄 (Ⅲ) イオンとサリチル酸の錯形成を検討する その錯体の実験式が求められ その安定度定数を見積もることができる 鉄 (Ⅲ) イオンとサリチル酸 H 2 Sal からなる安定な錯体はいくつか知られている それらの構造と組成はpHにより異なる 酸性溶液では紫色の錯体が生成する
問題 36. 鉄 (Ⅲ) イオンとサリチルサリチル酸の錯形成 (20140304 修正 : ピンク色の部分 ) 1. 序論この簡単な実験では 水溶液中での鉄 (Ⅲ) イオンとサリチル酸の錯形成を検討する その錯体の実験式が求められ その安定度定数を見積もることができる 鉄 (Ⅲ) イオンとサリチル酸 H 2 Sal からなる安定な錯体はいくつか知られている それらの構造と組成はpHにより異なる 酸性溶液では紫色の錯体が生成する
木村の有機化学小ネタ セルロース系再生繊維 再生繊維セルロースなど天然高分子物質を化学的処理により溶解後, 細孔から押し出し ( 紡糸 という), 再凝固させて繊維としたもの セルロース系の再生繊維には, ビスコースレーヨン, 銅アンモニア
 セルロース系再生繊維 再生繊維セルロースなど天然高分子物質を化学的処理により溶解後, 細孔から押し出し ( 紡糸 という), 再凝固させて繊維としたもの セルロース系の再生繊維には, ビスコースレーヨン, 銅アンモニアレーヨンがあり, タンパク質系では, カゼイン, 大豆タンパク質, 絹の糸くず, くず繭などからの再生繊維がある これに対し, セルロースなど天然の高分子物質の誘導体を紡糸して繊維としたものを半合成繊維と呼び,
セルロース系再生繊維 再生繊維セルロースなど天然高分子物質を化学的処理により溶解後, 細孔から押し出し ( 紡糸 という), 再凝固させて繊維としたもの セルロース系の再生繊維には, ビスコースレーヨン, 銅アンモニアレーヨンがあり, タンパク質系では, カゼイン, 大豆タンパク質, 絹の糸くず, くず繭などからの再生繊維がある これに対し, セルロースなど天然の高分子物質の誘導体を紡糸して繊維としたものを半合成繊維と呼び,
