本日の内容 1. PMDA の業務 2. 薬事戦略相談の事業内容 3. 薬事戦略相談の活用 2
|
|
|
- たみじろう たにしき
- 5 years ago
- Views:
Transcription
1 PMDA 薬事戦略相談の現状と課題 独立行政法人医薬品医療機器総合機構 Pharmaceuticals and Medical Devices Agency (PMDA) 審査マネジメント部長中山智紀 1
2 本日の内容 1. PMDA の業務 2. 薬事戦略相談の事業内容 3. 薬事戦略相談の活用 2
3 本日の内容 1. PMDA の業務 2. 薬事戦略相談の事業内容 3. 薬事戦略相談の活用 3
4 PMDA とは PMDA( 独立行政法人医薬品医療機器総合機構 ) は 国民の健康 安全の向上に積極的に貢献することを目指して 医薬品医療機器法に基づく医薬品 医療機器等の承認審査及び安全対策 並びに健康被害救済の3つの業務を行う厚生労働省所管の独立行政法人 このような業務を行う組織は日本 * ではPMDAだけ *PMDA と同様の組織は 米国では FDA( 米国食品医薬品局 ) 欧州では EMA( 欧州医薬品庁 ) がある 国民の安全を守る 審査リスクの抑制 世界に誇る薬事システム 安全継続的リスクの最小化 国民 救済発生した被害の救済 日本独自のセイフティ トライアングル ~3 つの業務による総合的なリスクマネジメント ~ 4
5 PMDA の 3 大業務 健康被害救済 医薬品の副作用や生物由来製品を介した感染等による健康被害に対して, 迅速な救済を実施 承認審査 医薬品や医療機器等の品質 有効性 安全性について, 治験前から承認まで一貫した体制で開発への助言 審査を実施 安全対策 市販後における安全性に関する情報の収集, 分析, 提供を実施 5
6 本日の内容 1. PMDA の業務 2. 薬事戦略相談の事業内容 3. 薬事戦略相談の活用 6
7 治験相談(医薬品)薬事戦略相談主に製薬企業向け主にアカデミア ベンチャー向け非臨床試験前シーズ候補確定PMDA が行う対面助言 ( 各種相談 ) 非臨床試験調査臨床試験審査市販後 ( 創薬 合成 ) ( 薬理 ) ( 毒性 ) 第 Ⅰ 相 第 Ⅱ 相 第 Ⅲ 相 第 Ⅳ 相 手続相談 薬事戦略開発計画等相談 第 Ⅰ 相試験開始前相談 安全性相談 30 日 第 Ⅱ 相試験開始前相談 申請前相談 品質相談生物学的同等性試験等相談信頼性基準適合性相談 医薬品 / 医療機器 / 再生医療等製品戦略相談 再生医療等製品等の品質及び安全性に係る相談 第 Ⅱ 相試験終了後相談 追加相談 優先審査品目該当性相談 要件 に該当 製造販売後臨床試験等計画相談 製造販売後臨床試験等終了時相談 要件 : 未承認薬適応外薬検討会議の検討又は選定品目であって 治験費用を公的研究資金で賄うもの ( 詳しくは実施要綱を確認してください )
8 死の谷 (Death Valley) への PMDA の取組 薬事戦略相談日本発の革新的な医薬品 医療機器の創出に向け 有望なシーズを持つ大学 研究機関 ベンチャー企業を主な対象として 開発初期から必要な試験 治験に関する指導 助言を実施するものとして H23 年 7 月 1 日より開始 基礎研究から実用化に向けては様々な課題があり 課題解決に向けた審査当局との早期相談が重要である 例えば 品質や毒性データ等を適切に収集しておらず 臨床試験が実施できないというケース 革新的な医薬品 医療機器で 品質 安全性 有効性の評価方法が確立しておらず 開発者等で検討した独自の評価方法を用いて臨床試験等を実施しても 品質 安全性 有効性が十分に確保ができたか 評価ができないことから 承認審査が迅速に行えないケースなどがある 基礎研究日本発の創薬 機器シーズ 品質試験 非臨床試験 臨床試験 実用化 革新的医薬品 医療機器 疑問点の例 再生医療等に用いる細胞 組織やバイオ医薬品に関する品質 毒性試験法に関する疑問 初期段階での評価項目の決定や必要な被験者数に疑問 着実な開発に向けては このような疑問を放置せずできるだけ早い段階から PMDA と相談し 確認しておくことが重要 設置当初から 臨床試験は主に臨床開発初期 (POC(Proof of Concept) 試験 ( 前期第 Ⅱ 相試験程度 ) まで ) を対象
9 開発ラグ解消支援に向けて ( 最近の動き ) 以下のとおり薬事戦略相談の相談区分の拡充 見直しを行い 平成 26 年 11 月から実施 検証的試験プロトコルへの助言として 一定の要件を満たす医療上の必要性の高い品目の場合には アカデミアが主導する第 Ⅱ/Ⅲ 相 第 Ⅲ 相の検証的試験も 試行的に薬事戦略相談の対象とする ロードマップへの助言として モノの特性に応じた開発計画のロードマップ等 試験計画の一般的な考え方や進め方に関する助言のみを対象とする 薬事開発計画等戦略相談 を試行的に創設する 再生医療等製品の相談区分を 医薬品 医療機器から独立して設定 基礎研究 有望なシーズ アカデミアベンチャー企業 企業 薬事戦略相談の拡充各試験のプロトコルへの助言品質非臨床臨床試験探索的試試験試験験 ロードマップへの助言 検証的試験 実用化 革新的医薬品医療機器再生医療等製品 青 : 現行の範囲赤 : 拡充の範囲 検証的試験のプロトコルへの助言も実施 試験プロトコルだけでなく 開発全体のロードマップへの助言も実施 開発全体のロードマップへの助言も実施 18
10 薬事戦略相談のプロセスとその関係 1 大学 研究機関ベンチャー企業 自分のシーズが薬事戦略相談に馴染むのか確認したい シーズの実用化の道筋について相談したい 個別面談 ( 無料 ) 論点整理 事前面談 ( 無料 ) 相談内容の整理のためテクニカルエキスパートが主として対応 必要に応じて審査チームも同席します 必要な資料が整ってからの面談申込みをお願いします また 面談申込みから面談実施までは 2~3 週間程度の準備期間が通常 必要となります 科学的議論 ( 記録は 1 ヶ月目処に確定 ) 対面助言 ( 有料 ) 主として審査チームと テクニカルエキスパートが相談に対応 必要に応じて当該分野の外部専門家が同席します 事前面談に向けて 薬事戦略相談課のテクニカルエキスパートが 薬事戦略相談事業の手続きや事業の内容を説明します
11 個別面談と事前面談 個別面談 ( 手数料不要 ) 薬事戦略相談事業の理解を深めてもらうため 薬事戦略相談の詳細や 研究内容やシーズ等を踏まえた承認取得に向けての懸念点等の相互理解に関する面談 相談 1 回当たり 20 分程度とする 相談記録は作成しない 事前面談 ( 手数料不要 ) 薬事戦略相談については あらかじめ 相談範囲 論点の整理 データ等の確認 承認申請等に係る一般的なアドバイス等に関して事前に面談を行う 相談 1 回当たり 30 分程度とする 相談記録は作成しない 11
12 対面助言と薬事開発計画等戦略相談 対面助言 ( 手数料必要 ) 事前面談に引き続き 一定の要件を満たすものについては 提出された資料に基づき 現在得られているデータをもとに 今後の治験の実施 承認申請に向けての課題の整理や 具体的な指導 助言を行う 相談 1 回当たり 2 時間程度とする 相談記録を作成する 薬事開発計画等戦略相談 ( 手数料必要 ) 開発計画のロードマップ等 試験計画の一般的な考え方や進め方に関して 個別品目に対する事前調査を必須としない案件の相談を行う 相談 1 回当たり 30 分程度とする 相談記録を作成する 12
13 対面助言の相談手数料 医薬品戦略相談 1 医療機器戦略相談 1 3 相談区分 再生医療等製品戦略相談 1 再生医療等製品等の品質及び安全性に係る相談 1 4 薬事開発計画等戦略相談 5 1 申込当たりの相談手数料 1,541,600 円 (154,100 円 ) 2 874,000 円 (87,400 円 ) 2 874,000 円 (87,400 円 ) 2 1,541,600 円 (154,100 円 ) 2 73,600 円 1:1 回当たりの相談時間は 2 時間程度 2: 別に定める要件を満たす大学 研究機関 ベンチャー企業の場合 3: 体外診断用医薬品は 医療機器戦略相談にて対応 4:1 申込で複数回の対面助言が可能 5:1 回当たりの相談時間は 30 分程度 13
14 薬事戦略相談のプロセスとその関係 2 1~2 か月を目安 日程調整依頼の受付 1~3: 実施希望月の 2 か月前の月初め 4 5: 随時 対面助言の種類 1 医薬品戦略相談 2 医療機器戦略相談 3 再生医療等製品戦略相談 4 再生医療等製品等の品質及び安全性に係る相談 5 薬事開発計画等戦略相談 個別面談 事前面談 日程調整結果の連絡 対面助言の日程調整依頼 手数料振込 申込書提出 対面助言の資料提出 対面助言の実施 相談記録の確定 必要に応じて 原則 15 勤務日以内 原則 は 5 週間前 2 は 3 週間前 30 勤務日以内を目処 実際の日程調整依頼の受付日 対面助言の資料搬入日は ホームページで確認してください 対面助言の日程調整依頼書の提出に関しては 対面助言資料の準備状況も考慮してください
15 薬事戦略相談の実施状況 個別面談 / 事前面談 平成 23 年度 ( 注 1) 平成 24 年度平成 25 年度平成 26 年度 平成 27 年度 (9 月末 ) 合計 個別面談 ( うち関西支部実施 ( 注 2) ) (20) 271 (63) 80(30) 1,008 (113) 事前面談 ( うち関西支部実施 ( 注 2) ) (26) 325 (57) 171(26) 1,249 (109) 対面助言 平成 23 年度 ( 注 1) 平成 24 年度平成 25 年度平成 26 年度 平成 27 年度 (9 月末 ) 合計 医薬品戦略相談 医療機器戦略相談 ( 注 3) 再生医療等製品戦略相談 再生医療等製品等の品質及び安 ( 注 4) 5 [7] 7 [13] 19 [32] 18 [44] 8 [16] 57 [112] 全性に係る相談 ( 注 5) 薬事開発計画等戦略相談 合計 31 [33] 40 [46] 123 [136] 85 [111] 34 [42] 313 [368] 注 1: 薬事戦略相談事業は H23.7.1から実施 注 2:H から実施 注 3:H から実施 ( それまでは医薬品戦略相談又は医療機器戦略相談として実施 ) 注 4:H まで医薬品戦略相談として受付けたものを含む また [ ] 内の数値は 再生医療等製品等に係る治験計画の届出を行う前に 当該製品の品質及び安全性に係る十分な確認を行うために必要な範囲で 複数日に渡って相談を行ったものを 個別に計上した場合の延べ件数 15 注 5:H から実施
16 本日の内容 1. PMDA の業務 2. 薬事戦略相談の事業内容 3. 薬事戦略相談の活用 16
17 相談項目の立て方のイメージ 例えば 革新的製品で 有効性や安全性の評価方法について 既存の評価方法がない場合 このような有効性の評価方法を開発したが この方法で証明できれば 有効性があると考えてよいか? 現時点では適切な指標はないので 最終的には 対象疾患の標準治療法との比較をすることを予定している この考え方で問題ないか? 17
18 相談者に対するお願い 相談対象となる製品の内容 これまでに得られているデータ 今後得る予定のデータ それらデータの利用方法 予定している効能 効果や用法 用量を明確にして 相談資料を作成してください 相談の際には 相談者が懸念する課題と対応方法を具体的に示し 相談者としてその方法が適当と考える理由を明確にしてください 以上の相談内容を論理的な文章にまとめて 相談資料を作成し 必要に応じて図表を用いてください また 数値や結果の根拠資料については 添付資料としてください 18
19 相談者に対するお願い ( 続き ) 相談内容は漠然とした内容 例えば 相談者が作成した治験実施計画全般について懸念される点を意見してほしいといった相談事項は対応できませんので ご注意ください 課題や懸念点 それらへの対応方法が明確になっていない場合には 内容確認に時間を要し 有意義な議論 意見交換ができない場合があります 特に 開発初期段階の相談では 承認申請にあたって新たな毒性試験は不要などといった確定的な意見を述べることが難しい場合があることをご理解ください 19
20 AMED ー PMDA の連携強化について平成 27 年 8 月 19 日連携協定締結 革新的な医薬品 医療機器 再生医療等製品の創出を効率的に進めるためには 規制方針を踏まえた研究開発戦略の構築 最新の研究開発の動向を踏まえた合理的な規制の実現が必要である このため 本邦発の革新的医薬品 医療機器等の創出に向けて AMED による医療分野の研究開発の推進業務等 PMDA による審査 相談業務等についてそれぞれの使命や責務を果たしつつ それぞれが持つ知識や経験を相互に活用する AMED による委託研究課題 研究者シーズ 基礎 応用研究 非臨床試験 治験承認申請 審査承認 実用化 課題採択 進捗管理 評価 AMED 出口戦略を見据えた研究の増加 採択の条件 相談記録の共有 評価時の助言 実用化の視点からの研究評価の強化 最新研究動向のインプット AMED 情報 医療分野の研究開発動向 (RS 研究含む ) 創薬支援事業の実施状況 医療機器開発支援 ( 伴走コンサル ) の実施状況 情報共有 PMDA 承認申請に向けた効率的かつ円滑な研究推進 実用化促進 研修講師派遣 AMEDによる助言 指導のための協力 ( 例 : 信頼性調査方法に関するSOP 等の共有 AMED 職員勉強会への講師派遣 ) 臨床研究 治験研修事業の実施 助言 指導環境の整備 治験関連スタッフ お互いの業務に活用 薬事戦略相談 革新的医療技術創出拠点等 PMDA 情報 医薬品 医療機器等の規制動向 薬事戦略相談の実施状況 治験の実施状況 (FIH 医師主導治験 ) 11
21 AMED ー PMDA 連携協定の内容 (H 締結 ) 1. 薬事戦略相談の活用 AMED が採択した研究のうち 実用化段階に移行するものについては 薬事戦略相談を受けることを採択の条件とする 出口戦略を見据えた研究の実施増 2.AMED の研究評価への協力 AMED が採択した研究の中間評価等において PMDA は薬事戦略相談の結果を踏まえて AME D が求める内容についてコメントを出す 実用化の観点からの研究評価の質の向上 3. 臨床研究 治験環境整備に関する相互協力 臨床研究の質向上及び治験環境整備を目指し AMED が各研究代表者や革新的医療技術創出拠点等に対して行う助言 指導が適切に行われるよう PMDA の助言ノウハウ等を適宜情報共有するなど 適切に連携する 4. 情報の共有 AMED が持つ医療分野の研究開発動向や PMDA が持つ医薬品 医療機器等の規制動向など お互いが持つ情報を共有し それぞれの業務に活用する 21
22 先駆け審査指定制度と PMDA におけるアクション 2. 審査パートナー制 6 か月 薬事戦略相談 非臨床試験臨床研究 1. 先駆け指定 3. 事前評価 4. 優先審査 治験 I/II / 探索的治験 3. 優先治験相談 1 か月 第 Ⅲ 相試験 / 検証的治験 場合によっては第 Ⅲ 相試験の結果の承認申請後の提出を認める 承認 先駆け審査指定制度の運用にあたり PMDA における具体的アクションは以下のとおり 1. 先駆け指定に際し 厚労省からの依頼を受け 新薬 医療機器等審査各部が 先駆け指定基準のうち 画期性 対象疾患の重篤性 対象疾患に係る極めて高い有効性への該当性の評価を行う ( 具体的手続き タイムフレーム 書類等については医薬品は平成 27 年 4 月 医療機器 体外診断用医薬品 再生医療等製品は平成 27 年 7 月に厚生労働省が通知発出 ) 医薬品について 厚生労働省において平成 27 年 5 月に指定希望品目を公募したところ 56 品目の登録申込があり 予備的審査を経て 50 品目が正式に指定申請され PMDA において評価を行った後 平成 27 年 10 月 27 日付けをもって 6 品目が指定された ( 次スライド参照 ) 指定品目は PMDA の HP に掲載 医療機器等については 平成 27 年 9 月 14 日 ~10 月 7 日に指定希望品目を公募し 現在 予備的審査を実施中 2. 審査パートナー制 ( コンシェルジュ ) に関し コンシェルジュ業務等を行う部長クラスの職員 ( 先駆け審査業務調整役 ) 及び担当職員を配置した 3. 治験相談 事前評価に関し 1 優先相談の見直し : 先駆け審査指定品目は 優先対面助言品目として取扱う 2 事前評価の充実 : 先駆け総合評価相談を新設し 申請予定資料の事前の評価等を行う ( 医薬品は平成 27 年 5 月 15 日 医療機器 体外診断用医薬品 再生医療等製品は平成 27 年 9 月 14 日に相談枠を設置 ) 4. 優先審査に関し コンシェルジュによる管理のもと 適切に優先審査 ( 調査 ) を実施 22
23 医薬品の先駆け審査指定制度の対象品目一覧 指定を受けた医薬品の名称 指定を受けた申請者 指定を受けた予定される効能又は効果 シロリムス (NPC-12G) ノーベルファーマ株式会社結節性硬化症に伴う血管線維腫 NS-065/NCNP-01 日本新薬株式会社デュシェンヌ型筋ジストロフィー (DMD) S 塩野義製薬株式会社 A 型又は B 型インフルエンザウイルス感染症 BCX7353 ASP2215 ペムブロリズマブ ( 遺伝子組換え ) 株式会社 Integrated Development Associates アステラス製薬株式会社 MSD 株式会社 遺伝性血管浮腫 (HAE) の患者を対象とした血管性浮腫の発作の管理 初回再発又は治療抵抗性の FLT3 遺伝子変異陽性急性骨髄性白血病 治癒切除不能な進行 再発の胃癌 指定医薬品の使用に際して体外診断用医薬品等が必要とされる場合には併せて対応を行う 23
24 詳しい内容は PMDA ホームページでご確認ください ご静聴ありがとうございました 24
ともに 申請者が承認審査のスケジュールに沿って法令上求められる製造体制を整備することや承認後円滑に医療現場に提供するための対応が十分になされることで 更なる迅速な実用化を促すものである この制度では 原則として新規原理 新規作用機序等により 生命に重大な影響がある重篤な疾患等に対して 極めて高い有効
 ともに 申請者が承認審査のスケジュールに沿って法令上求められる製造体制を整備することや承認後円滑に医療現場に提供するための対応が十分になされることで 更なる迅速な実用化を促すものである この制度では 原則として新規原理 新規作用機序等により 生命に重大な影響がある重篤な疾患等に対して 極めて高い有効性が期待される医療機器 体外診断用医薬品 再生医療等製品を指定することとする また 本制度では PMDA
ともに 申請者が承認審査のスケジュールに沿って法令上求められる製造体制を整備することや承認後円滑に医療現場に提供するための対応が十分になされることで 更なる迅速な実用化を促すものである この制度では 原則として新規原理 新規作用機序等により 生命に重大な影響がある重篤な疾患等に対して 極めて高い有効性が期待される医療機器 体外診断用医薬品 再生医療等製品を指定することとする また 本制度では PMDA
希少疾病用医薬品 希少疾病用医療機器 希少疾病用再生医療等製品に係る優先的な対面助言 優先審査及び手数料の減免と RS 戦略相談 / 総合相談について 独立行政法人医薬品医療機器総合機構 大阪会場 : ワクチン等審査部仲井友子東京会場 : 新薬審査第五部河野紘隆 1
 希少疾病用医薬品 希少疾病用医療機器 希少疾病用再生医療等製品に係る優先的な対面助言 優先審査及び手数料の減免と RS 戦略相談 / 総合相談について 独立行政法人医薬品医療機器総合機構 大阪会場 : ワクチン等審査部仲井友子東京会場 : 新薬審査第五部河野紘隆 1 希少疾病用医薬品 医療機器 再生医療等製品の指定制度における PMDA の役割 2 開発企業 ( 指定申請企業 ) 厚生労働省医薬品医療機器総合機構医薬基盤
希少疾病用医薬品 希少疾病用医療機器 希少疾病用再生医療等製品に係る優先的な対面助言 優先審査及び手数料の減免と RS 戦略相談 / 総合相談について 独立行政法人医薬品医療機器総合機構 大阪会場 : ワクチン等審査部仲井友子東京会場 : 新薬審査第五部河野紘隆 1 希少疾病用医薬品 医療機器 再生医療等製品の指定制度における PMDA の役割 2 開発企業 ( 指定申請企業 ) 厚生労働省医薬品医療機器総合機構医薬基盤
医薬品 医療機器の開発ステージと PMDA 審査関連業務 研究開発 非臨床試験 臨床試験 ( 治験 ) 承認申請 承認 市販 相談業務 薬事戦略相談対面助言 ( 治験相談 ) 審査 承認審査業務 再審査 再評価 GLP 調査 GCP 調査 信頼性保証業務 GPSP 調査 GMP/QMS 調査業務 基
 ~ 薬事戦略相談の活用について ~ 2014 年 11 月 5 日 PMDA 関西支部開設 1 周年記念シンポジウム 薬事戦略相談等の活用による革新的医療技術の実用化促進に向けて ( 独 ) 医薬品医療機器総合機構 ( PMDA ) 関西支部相談課長平田雅一 0 医薬品 医療機器の開発ステージと PMDA 審査関連業務 研究開発 非臨床試験 臨床試験 ( 治験 ) 承認申請 承認 市販 相談業務 薬事戦略相談対面助言
~ 薬事戦略相談の活用について ~ 2014 年 11 月 5 日 PMDA 関西支部開設 1 周年記念シンポジウム 薬事戦略相談等の活用による革新的医療技術の実用化促進に向けて ( 独 ) 医薬品医療機器総合機構 ( PMDA ) 関西支部相談課長平田雅一 0 医薬品 医療機器の開発ステージと PMDA 審査関連業務 研究開発 非臨床試験 臨床試験 ( 治験 ) 承認申請 承認 市販 相談業務 薬事戦略相談対面助言
審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果
![審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果 審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果](/thumbs/92/108604766.jpg) 審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
(3) 事前面談の日程等の連絡申込書を受け付けた後に 機構担当者より 電話で日程等を連絡します なお 事前面談の質問内容に応じて 電話による回答を行う場合があります (4) (5)( 略 ) (3) 事前面談の日程等の連絡申込書を受付けた後に 機構担当者より 電話で日程等を連絡します なお 事前面談
 レギュラトリーサイエンス戦略相談に関する実施要綱新旧対照表 改正後 3. 相談の種類 RS 戦略相談の申込みに際しては 予め 事前面談を申し込みいただき 機構の担当者と上に示した事項について面談を行ってください 事前面談の結果を踏まえた上で 対面助言の申込みをしていただくことになります 対面助言の対象については 原則として 優先分野 ( 下記 ) に該当し かつ 有望性が期待できるものとします (
レギュラトリーサイエンス戦略相談に関する実施要綱新旧対照表 改正後 3. 相談の種類 RS 戦略相談の申込みに際しては 予め 事前面談を申し込みいただき 機構の担当者と上に示した事項について面談を行ってください 事前面談の結果を踏まえた上で 対面助言の申込みをしていただくことになります 対面助言の対象については 原則として 優先分野 ( 下記 ) に該当し かつ 有望性が期待できるものとします (
再生医療の制度的な対応の検討について 薬事法等制度改正についてのとりまとめ平成 24 年 1 月 24 日厚生科学審議会医薬品制度改正部会 1 再生医療製品については 今後も 臓器機能の再生等を通じて 重篤で生命を脅かす疾患等の治療等に ますます重要な役割を果たすことが期待される 特に ips 細胞
 薬事戦略相談について ( 事業の概要等 ) 日本発の革新的な医薬品 医療機器の創出に向け 有望なシーズを持つ大学 研究機関 ベンチャー企業を主な対象として 開発初期から必要な試験 治験に関する指導 助言を実施するものとして 平成 23 年 7 月 1 日より開始した 基礎研究から実用化に向けては様々な課題があり 課題解決に向けた審査当局との早期相談が重要である 例えば 品質のデータや毒性データ等を適切に実施していない場合
薬事戦略相談について ( 事業の概要等 ) 日本発の革新的な医薬品 医療機器の創出に向け 有望なシーズを持つ大学 研究機関 ベンチャー企業を主な対象として 開発初期から必要な試験 治験に関する指導 助言を実施するものとして 平成 23 年 7 月 1 日より開始した 基礎研究から実用化に向けては様々な課題があり 課題解決に向けた審査当局との早期相談が重要である 例えば 品質のデータや毒性データ等を適切に実施していない場合
医療機器開発マネジメントにおけるチェック項目
 2018 年 11 月作成 医療機器開発マネジメントにおけるチェック項目 1. 各ステージゲートにおけるチェック項目 (1) チェック項目作成の目的従来個々の事業において実施されていた 事前 中間 事後の各ゲートにおける評価項目 Go/no-go の判断を 医療機器開発全期間を通して整理し 共通認識化する 技術的観点及び事業化の観点の双方を意識し 医療機器開発の特性を考慮したチェック項目を設定する
2018 年 11 月作成 医療機器開発マネジメントにおけるチェック項目 1. 各ステージゲートにおけるチェック項目 (1) チェック項目作成の目的従来個々の事業において実施されていた 事前 中間 事後の各ゲートにおける評価項目 Go/no-go の判断を 医療機器開発全期間を通して整理し 共通認識化する 技術的観点及び事業化の観点の双方を意識し 医療機器開発の特性を考慮したチェック項目を設定する
本日のトピック 人道的見地から実施される治験について 最近の新医薬品審査の状況について 最近の治験の動向について 2
 平成 27 年度治験推進地域連絡会議 人道的見地から実施される治験と 医薬品等の審査及び治験に関する 最近の動向について 厚生労働省医薬 生活衛生局審査管理課 1 本日のトピック 人道的見地から実施される治験について 最近の新医薬品審査の状況について 最近の治験の動向について 2 本日のトピック 人道的見地から実施される治験について 最近の新医薬品審査の状況について 最近の治験の動向について 3 欧米での人道的見地から実施される未承認薬アクセス制度
平成 27 年度治験推進地域連絡会議 人道的見地から実施される治験と 医薬品等の審査及び治験に関する 最近の動向について 厚生労働省医薬 生活衛生局審査管理課 1 本日のトピック 人道的見地から実施される治験について 最近の新医薬品審査の状況について 最近の治験の動向について 2 本日のトピック 人道的見地から実施される治験について 最近の新医薬品審査の状況について 最近の治験の動向について 3 欧米での人道的見地から実施される未承認薬アクセス制度
ドラッグラグの現状 日本においては平均して世界初上市から約 4 年遅れて上市されており 最も遅れの少ない米国と比較しておよそ 2.5 年の開きがある * 1,417 (= 約 4 年 ) 約 2.5 年 日本 フランス デン マーク ドイツ ス
 今後の機構の体制について 平成 19 年 6 月 8 日医薬品医療機器総合機構 ドラッグラグの現状 日本においては平均して世界初上市から約 4 年遅れて上市されており 最も遅れの少ない米国と比較しておよそ 2.5 年の開きがある * 1,417 (= 約 4 年 ) 915 757 約 2.5 年 620 583 538 512 505 日本 フランス デン マーク ドイツ スウェーデン スイス英国米国
今後の機構の体制について 平成 19 年 6 月 8 日医薬品医療機器総合機構 ドラッグラグの現状 日本においては平均して世界初上市から約 4 年遅れて上市されており 最も遅れの少ない米国と比較しておよそ 2.5 年の開きがある * 1,417 (= 約 4 年 ) 915 757 約 2.5 年 620 583 538 512 505 日本 フランス デン マーク ドイツ スウェーデン スイス英国米国
本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シ
 医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 医薬品の再審査に係る関連法規 2. 医薬品の再審査申請資料の適合性調査 2.1. GPSP 実地調査における調査の視点 2.2. 適合性書面調査における調査の視点 2.3. ( 参考 ) 医薬品再審査適合性調査相談の現況 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの任意提出と事前提出資料 ( 実施手続き通知の改正 )
MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1
 MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1 MDSAP 報告書の受入れの概要 (1/2) 日本は 平成 27 年 6 月にMDSAPに参加する旨を発表 関係者との意見交換を行い MDSAP 報告書の受け入れについて 以下の通知を発出した 平成 28 年 6 月 22 日薬生監麻発 0622 第 3 号 薬生機審発 0622
MDSAP の調査結果の 試行的受入れについて ( 独 ) 医薬品医療機器総合機構 品質管理部 登録認証機関監督課 1 MDSAP 報告書の受入れの概要 (1/2) 日本は 平成 27 年 6 月にMDSAPに参加する旨を発表 関係者との意見交換を行い MDSAP 報告書の受け入れについて 以下の通知を発出した 平成 28 年 6 月 22 日薬生監麻発 0622 第 3 号 薬生機審発 0622
別添 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について < 半年ごとの定期報告の受け付け> Q1 平成 26 年 6 月 30 日までの間は 治験依頼者 ( 自ら治験を実施する者を除く ) が提出する副作用等症例の定期報告は なお従前の例によることができる とあるが 平成 26 年
 事務連絡 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局審査管理課 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 第 273 条第 3 項に基づく治験副作用等定期報告については 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について ( 平成 24 年
事務連絡 平成 25 年 7 月 1 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬食品局審査管理課 治験副作用等症例の定期報告に関する質疑応答集 (Q&A) について 薬事法施行規則 ( 昭和 36 年厚生省令第 1 号 ) 第 273 条第 3 項に基づく治験副作用等定期報告については 薬事法施行規則等の一部を改正する省令の施行に関する留意事項について ( 平成 24 年
医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など ) 医薬品候補物質のスクリーニン
 特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
JCROA自主ガイドライン第4版案 GCP監査WG改訂案及び意見
 受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
受託業務の適正な実施に関する日本 CRO 協会の自主ガイドライン ( 第 4 版 ) 目 次 1. 本ガイドライン制定の背景 2. 目的 3. 関連法規の遵守 4. 受託業務の範囲 5. 受託の検討 6. 受託業務の品質管理及び品質保証 7. 健康被害補償と損害賠償 8. 教育 9. モニタリング 10. 情報セキュリティ 11. 本会員の重大事態への対応 1/5 1. 本ガイドライン制定の背景日本
審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ]
![審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ] 審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ]](/thumbs/91/105024304.jpg) 審査報告書 平成 26 年 2 月 7 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所
審査報告書 平成 26 年 2 月 7 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所
PMDA の概要 セイフティトライアングル 3 つの業務による総合的なリスクマネジメント 3 つの役割を一体として行う世界で唯一の公的機関として レギュラトリーサイエンスに基づき より安全でより品質のよい製品をより早く医療現場に届け 医療水準の向上に貢献する 2
 PMDA の中期計画と臨床研究中核病院等との 人材交流について 独立行政法人医薬品医療機器総合機構 Pharmaceuticals and Medical Devices Agency ( PMDA ) 理事 ( 技監 ) 北條泰輔 2015 年 3 月 4 日革新的医療技術創出拠点プロジェクト合同会議 PMDA の概要 セイフティトライアングル 3 つの業務による総合的なリスクマネジメント 3 つの役割を一体として行う世界で唯一の公的機関として
PMDA の中期計画と臨床研究中核病院等との 人材交流について 独立行政法人医薬品医療機器総合機構 Pharmaceuticals and Medical Devices Agency ( PMDA ) 理事 ( 技監 ) 北條泰輔 2015 年 3 月 4 日革新的医療技術創出拠点プロジェクト合同会議 PMDA の概要 セイフティトライアングル 3 つの業務による総合的なリスクマネジメント 3 つの役割を一体として行う世界で唯一の公的機関として
る として 平成 20 年 12 月に公表された 規制改革推進のための第 3 次答申 において 医療機器開発の円滑化の観点から 薬事法の適用範囲の明確化を図るためのガイドラインを作成すべきであると提言したところである 今般 薬事法の適用に関する判断の透明性 予見可能性の向上を図るため 臨床研究におい
 都道府県知事 各保健所設置市長殿 特別区長 薬食発 0331 第 7 号 平成 22 年 3 月 31 日 厚生労働省医薬食品局長 臨床研究において用いられる未承認医療機器の提供等に係る 薬事法の適用について 薬事法 ( 昭和 35 年法律第 145 号 ) は 医療機器について品質 有効性及び安全性の確保がなされた製品のみが流通するよう種々の規制を設けているが 薬事法第 14 条第 1 項の承認を受けていない医療機器
都道府県知事 各保健所設置市長殿 特別区長 薬食発 0331 第 7 号 平成 22 年 3 月 31 日 厚生労働省医薬食品局長 臨床研究において用いられる未承認医療機器の提供等に係る 薬事法の適用について 薬事法 ( 昭和 35 年法律第 145 号 ) は 医療機器について品質 有効性及び安全性の確保がなされた製品のみが流通するよう種々の規制を設けているが 薬事法第 14 条第 1 項の承認を受けていない医療機器
員長及び医薬品医療機器等法登録認証機関協議会代表幹事宛て送付するこ ととしていることを申し添えます 記 1. 基本要件基準第 13 条第 5 項及び第 6 項への適合性確認の基本的な考え方について (1)2023 年 ( 平成 35 年 )2 月 28 日 ( 以下 経過措置期間終了日 という )
 薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
薬生機審発 0301 第 1 号 平成 30 年 3 月 1 日 各都道府県薬務主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医療機器審査管理課長 ( 公印省略 ) 医療機器の電磁両立性に関する日本工業規格の改正の取扱いについて すべての能動型医療機器は 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第四十一条第三項の規定により厚生労働大臣が定める医療機器の基準 ( 平成 17
本の医薬品 医療機器産業の国際競争 強化と い経済成 を実現 基本的考え 現状の課題 本で われる臨床研究に対する 援や制度上の制約が障壁となり 本発のシーズが 新的な医薬品 医療機器の開発につながっていない 企業の治験着 の遅れ 治験の実施や承認審査に時間がかかる等により欧 との間にドラッグ ラグ
 資料 2 医療イノベーションに関する資料 平成 23 年 5 月 19 日厚生労働省 本の医薬品 医療機器産業の国際競争 強化と い経済成 を実現 基本的考え 現状の課題 本で われる臨床研究に対する 援や制度上の制約が障壁となり 本発のシーズが 新的な医薬品 医療機器の開発につながっていない 企業の治験着 の遅れ 治験の実施や承認審査に時間がかかる等により欧 との間にドラッグ ラグ デバイス ラグが
資料 2 医療イノベーションに関する資料 平成 23 年 5 月 19 日厚生労働省 本の医薬品 医療機器産業の国際競争 強化と い経済成 を実現 基本的考え 現状の課題 本で われる臨床研究に対する 援や制度上の制約が障壁となり 本発のシーズが 新的な医薬品 医療機器の開発につながっていない 企業の治験着 の遅れ 治験の実施や承認審査に時間がかかる等により欧 との間にドラッグ ラグ デバイス ラグが
中医協総 医薬品及び医療機器の費用対効果評価に関する取扱いについて 1 既収載品に係る費用対効果評価の手続き (1) 対象品目の指定中央社会保険医療協議会の定める以下の選定基準に基づき 費用対効果評価専門部会において指定 公表されたものとする 次の全ての要件を満たす品
 中医協総 - 5 2 8. 2. 1 0 医薬品及び医療機器の費用対効果評価に関する取扱いについて 1 既収載品に係る費用対効果評価の手続き (1) 対象品目の指定中央社会保険医療協議会の定める以下の選定基準に基づき 費用対効果評価専門部会において指定 公表されたものとする 次の全ての要件を満たす品目を対象とする なお 2においてイのⅰ イのⅱ ロのⅰ 及びロのⅱは それぞれ1 品目が該当するものとし
中医協総 - 5 2 8. 2. 1 0 医薬品及び医療機器の費用対効果評価に関する取扱いについて 1 既収載品に係る費用対効果評価の手続き (1) 対象品目の指定中央社会保険医療協議会の定める以下の選定基準に基づき 費用対効果評価専門部会において指定 公表されたものとする 次の全ての要件を満たす品目を対象とする なお 2においてイのⅰ イのⅱ ロのⅰ 及びロのⅱは それぞれ1 品目が該当するものとし
次 Ⅰ. 総論 2 Ⅱ. 重点分野 3 Ⅲ. 人材育成 確保 6 Ⅳ. 情報管理 8 Ⅴ. その他 9 1
 平成 27 年 5 月 27 日第 9 回健康 医療戦略専門調査会提出資料 資料 12-2 医療分野研究開発推進計画 の実行状況に係る助言と今後の対応について 平成 27 年 5 月 27 日内閣官房健康 医療戦略室文部科学省厚生労働省経済産業省 次 Ⅰ. 総論 2 Ⅱ. 重点分野 3 Ⅲ. 人材育成 確保 6 Ⅳ. 情報管理 8 Ⅴ. その他 9 1 Ⅰ. 総論 1. 平成 26 年度の取組状況に関する主な評価
平成 27 年 5 月 27 日第 9 回健康 医療戦略専門調査会提出資料 資料 12-2 医療分野研究開発推進計画 の実行状況に係る助言と今後の対応について 平成 27 年 5 月 27 日内閣官房健康 医療戦略室文部科学省厚生労働省経済産業省 次 Ⅰ. 総論 2 Ⅱ. 重点分野 3 Ⅲ. 人材育成 確保 6 Ⅳ. 情報管理 8 Ⅴ. その他 9 1 Ⅰ. 総論 1. 平成 26 年度の取組状況に関する主な評価
国立病院機構大阪医療センター受託研究取扱細則
 国立病院機構大阪医療センター 受託研究取扱細則 ( 主旨 ) 第 1 条国立病院機構大阪医療センターにおける受託研究の取扱いに関しては 国立病院機構大阪医療センター受託研究取扱規程 ( 以下 規程 という ) 及び他に定めるもののほか 規程第 1 条第 2 項に規定するこの細則の定めるところによる ( 総則 ) 第 2 条研究責任者は 原則として医長職相当以上とする ただし 副作用報告及び感染症報告を受託研究として実施する場合
国立病院機構大阪医療センター 受託研究取扱細則 ( 主旨 ) 第 1 条国立病院機構大阪医療センターにおける受託研究の取扱いに関しては 国立病院機構大阪医療センター受託研究取扱規程 ( 以下 規程 という ) 及び他に定めるもののほか 規程第 1 条第 2 項に規定するこの細則の定めるところによる ( 総則 ) 第 2 条研究責任者は 原則として医長職相当以上とする ただし 副作用報告及び感染症報告を受託研究として実施する場合
北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下
 北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下 モニタリング という ) 監査の受け入れ 並びに試験審査委員会( 治験審査委員会が兼ねる 以下 治験審査委員会
北里大学病院モニタリング 監査 調査の受け入れ標準業務手順 ( 製造販売後臨床試験 ) 第 1 条 ( 目的 ) 本手順書は 北里大学病院において製造販売後臨床試験 ( 以下 試験とする ) 依頼者 ( 試験依頼者が業務を委託した者を含む 以下同じ ) が実施する直接閲覧を伴うモニタリング ( 以下 モニタリング という ) 監査の受け入れ 並びに試験審査委員会( 治験審査委員会が兼ねる 以下 治験審査委員会
写 薬生発 0131 第 1 号 平成 30 年 1 月 31 日 都道府県知事 殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 関係手数料令の一部を改正する政令の公布について この度 医薬品 医療機器等の品質 有効性及び安全性の確
 薬生発 0131 第 3 号 平成 30 年 1 月 31 日 独立行政法人医薬品医療機器総合機構理事長殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 関係手数料令の一部を改正する政令の公布について 標記につきまして 別添写しのとおり都道府県知事宛てに通知しましたので お 知らせいたします 写 薬生発 0131 第 1 号 平成 30
薬生発 0131 第 3 号 平成 30 年 1 月 31 日 独立行政法人医薬品医療機器総合機構理事長殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 関係手数料令の一部を改正する政令の公布について 標記につきまして 別添写しのとおり都道府県知事宛てに通知しましたので お 知らせいたします 写 薬生発 0131 第 1 号 平成 30
( 別紙 ) 承認申請時の電子データ提出に関する基本的考え方について ( 平成 26 年 6 月 20 日付け薬食審査発 0620 第 6 号厚生労働省医薬食品局審査管理課長通知 ) 新旧対照表 ( 別添 ) 改正後 承認申請時の電子データ提出に関する基本的考え方 1. 承認申請時に電子データ提出を
 ( 別紙 ) 承認申請時の電子データ提出に関する基本的考え方について ( 平成 26 年 6 月 20 日付け薬食審査発 0620 第 6 号厚生労働省医薬食品局審査管理課長通知 ) 新旧対照表 ( 別添 ) 改正後 承認申請時の電子データ提出に関する基本的考え方 1. 承認申請時に電子データ提出を求める背景 2. 電子データの提出対象となる品目と資料の範囲 (1) 対象となる品目 原則として 医薬品の承認申請について
( 別紙 ) 承認申請時の電子データ提出に関する基本的考え方について ( 平成 26 年 6 月 20 日付け薬食審査発 0620 第 6 号厚生労働省医薬食品局審査管理課長通知 ) 新旧対照表 ( 別添 ) 改正後 承認申請時の電子データ提出に関する基本的考え方 1. 承認申請時に電子データ提出を求める背景 2. 電子データの提出対象となる品目と資料の範囲 (1) 対象となる品目 原則として 医薬品の承認申請について
< F2D8E9197BF A836F815B2E6A7464>
 ( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
審査結果 平成 25 年 9 月 27 日 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 審査結果 ] 平成 25 年 4 月 26 日開
![審査結果 平成 25 年 9 月 27 日 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 審査結果 ] 平成 25 年 4 月 26 日開 審査結果 平成 25 年 9 月 27 日 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 審査結果 ] 平成 25 年 4 月 26 日開](/thumbs/53/31072016.jpg) 審査報告書 平成 25 年 9 月 27 日独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 剤形 含量 ]
審査報告書 平成 25 年 9 月 27 日独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 剤形 含量 ]
2. 検討 ~ 医療に関する事故の特殊性など (1) 医師等による医療行為における事故 医師等が患者に対してどのような医療行為を施すべきかという判断は 医師等の医学的な専門知識 技能に加え 医師等の経験 患者の体質 その時の患者の容態 使用可能な医療機器等の設備等に基づきなされるものである ( 個別
 資料 1 消費者安全調査委員会による事故等原因調査等の進め方について ( 議論のたたき台 ) ~ 医療に関する事故の考え方 ~ 1. 前提 消費者安全調査委員会の調査対象医療に関する事故については 消費者安全法に規定する生命又は身体の被害に係る消費者事故等に当たり得ることから その場合は 消費者安全調査委員会が行う事故等原因調査等の対象になる 消費者安全調査委員会の役割生命又は身体の被害に係る消費者事故等の原因を究明し
資料 1 消費者安全調査委員会による事故等原因調査等の進め方について ( 議論のたたき台 ) ~ 医療に関する事故の考え方 ~ 1. 前提 消費者安全調査委員会の調査対象医療に関する事故については 消費者安全法に規定する生命又は身体の被害に係る消費者事故等に当たり得ることから その場合は 消費者安全調査委員会が行う事故等原因調査等の対象になる 消費者安全調査委員会の役割生命又は身体の被害に係る消費者事故等の原因を究明し
<4D F736F F D E598BC68BA CD89EF8B638E9197BF2E646F6378>
 平成 25 年 4 月 23 日 規制改革会議議長 岡 素之 規制改革会議の活動報告 (4 月 -2) 4/17 第 6 回産業競争力会議に報告の内容のうち 以下 2 項目に関し追加 補足する 1. 国際先端テスト 国際先端テストの導入 定着を図るため 本会議の最優先案件 4つのWGの検討項目の中から国際比較をすることが効果的な項目を選定し 個別具体的に実施中 4/17 規制改革会議にて決定された14
平成 25 年 4 月 23 日 規制改革会議議長 岡 素之 規制改革会議の活動報告 (4 月 -2) 4/17 第 6 回産業競争力会議に報告の内容のうち 以下 2 項目に関し追加 補足する 1. 国際先端テスト 国際先端テストの導入 定着を図るため 本会議の最優先案件 4つのWGの検討項目の中から国際比較をすることが効果的な項目を選定し 個別具体的に実施中 4/17 規制改革会議にて決定された14
Microsoft PowerPoint - ⑨140925,30日薬連講習会(後発RMP)930.ppt [互換モード]
![Microsoft PowerPoint - ⑨140925,30日薬連講習会(後発RMP)930.ppt [互換モード] Microsoft PowerPoint - ⑨140925,30日薬連講習会(後発RMP)930.ppt [互換モード]](/thumbs/101/151698947.jpg) 後発医薬品 RMP について 厚生労働省医薬食品局安全対策課磯﨑正季子 1 後発医薬品への RMP の適用 平成 24 年 4 月 11 日薬食安発 0411 第 1 号 薬食審査発 0411 第 2 号安全対策課長 審査管理課長連名通知 医薬品リスク管理計画指針について 適用範囲医療用医薬品 ( 新医薬品 バイオ後続品 後発医薬品 ) 策定検討の時点 承認申請時 新医薬品 バイオ後続品後発医薬品
後発医薬品 RMP について 厚生労働省医薬食品局安全対策課磯﨑正季子 1 後発医薬品への RMP の適用 平成 24 年 4 月 11 日薬食安発 0411 第 1 号 薬食審査発 0411 第 2 号安全対策課長 審査管理課長連名通知 医薬品リスク管理計画指針について 適用範囲医療用医薬品 ( 新医薬品 バイオ後続品 後発医薬品 ) 策定検討の時点 承認申請時 新医薬品 バイオ後続品後発医薬品
【押印あり】日本医学会宛
 別紙 再生医療等製品患者登録システムへの参加協力のお願い 患者登録システムの目的 患者登録システムは 再生医療等製品の市販後の使用状況や患者予後等のデータを収集し 迅速な安全対策や新たな製品開発等を通じて 医療の向上に役立てることを目的としています 患者登録システムは 製品毎に構築 運用されます この患者登録システムは 一般的には レジストリ と呼ばれることもあります 構築形態例 患者登録システムの対象
別紙 再生医療等製品患者登録システムへの参加協力のお願い 患者登録システムの目的 患者登録システムは 再生医療等製品の市販後の使用状況や患者予後等のデータを収集し 迅速な安全対策や新たな製品開発等を通じて 医療の向上に役立てることを目的としています 患者登録システムは 製品毎に構築 運用されます この患者登録システムは 一般的には レジストリ と呼ばれることもあります 構築形態例 患者登録システムの対象
Microsoft Word - 【発送版】製造所の登録通知
 薬食機参発 1003 第 1 号 平成 26 年 10 月 3 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いについて 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業は登録制に移行され
薬食機参発 1003 第 1 号 平成 26 年 10 月 3 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 医療機器及び体外診断用医薬品の製造業の取扱いについて 薬事法等の一部を改正する法律 ( 平成 25 年法律第 84 号 以下 改正法 という ) により 医療機器及び体外診断用医薬品の製造業は登録制に移行され
臨床評価とは何か ( 独 ) 医薬品医療機器総合機構医療機器審査第一部方眞美
 臨床評価とは何か ( 独 ) 医薬品医療機器総合機構医療機器審査第一部方眞美 本日の Agenda 1. 臨床評価とは 2. 医療機器の特性を踏まえた有効性 安全性評価 3. 各国の規制の違い 4. 臨床評価報告書について 5. 臨床評価報告書の概念 6. 臨床研究と治験の違いは? 7. 文献評価の問題点 8. 治験活性化にむけて 臨床評価 とは そのものの有効性と安全性をヒトで評価すること 自己認証の欧州から出てきた概念
臨床評価とは何か ( 独 ) 医薬品医療機器総合機構医療機器審査第一部方眞美 本日の Agenda 1. 臨床評価とは 2. 医療機器の特性を踏まえた有効性 安全性評価 3. 各国の規制の違い 4. 臨床評価報告書について 5. 臨床評価報告書の概念 6. 臨床研究と治験の違いは? 7. 文献評価の問題点 8. 治験活性化にむけて 臨床評価 とは そのものの有効性と安全性をヒトで評価すること 自己認証の欧州から出てきた概念
資料 2-4 イソプロピルアンチピリン製剤の安全対策について 平成 23 年 6 月 23 日平成 23 年度薬事 食品衛生審議会医薬品等安全対策部会安全対策調査会 ( 第 2 回 ) 1. イソプロピルアンチピリン製剤の安全性に係る調査結果報告書 ( 別紙 ) 1 ページ
 資料 2-4 イソプロピルアンチピリン製剤の安全対策について 平成 23 年 6 月 23 日平成 23 年度薬事 食品衛生審議会医薬品等安全対策部会安全対策調査会 ( 第 2 回 ) 1. イソプロピルアンチピリン製剤の安全性に係る調査結果報告書 ( 別紙 ) 1 ページ 別紙 調査結果報告書 平成 23 年 6 月 13 日 独立行政法人医薬品医療機器総合機構 I. 品目の概要 [ 販売名 ]
資料 2-4 イソプロピルアンチピリン製剤の安全対策について 平成 23 年 6 月 23 日平成 23 年度薬事 食品衛生審議会医薬品等安全対策部会安全対策調査会 ( 第 2 回 ) 1. イソプロピルアンチピリン製剤の安全性に係る調査結果報告書 ( 別紙 ) 1 ページ 別紙 調査結果報告書 平成 23 年 6 月 13 日 独立行政法人医薬品医療機器総合機構 I. 品目の概要 [ 販売名 ]
Microsoft Word - H _概要_.doc
 平成 25 年 2 月独立行政法人国立病院機構西新潟中央病院倫理審査委員会 ( 受託研究 ) 議事要旨 開催日時 開催場所 出席委員名は別紙のとおり 治験及び製造販売後臨床試験に関する調査審議事項 審議事項 治験等の実施に関する研究 継続 ME2080 の Dravet 症候群患者を対象とした一般臨床試験 ( 第 Ⅲ 相 ) (Protocol No:STP-1) 被験薬 :ME2080(Stiripentol)
平成 25 年 2 月独立行政法人国立病院機構西新潟中央病院倫理審査委員会 ( 受託研究 ) 議事要旨 開催日時 開催場所 出席委員名は別紙のとおり 治験及び製造販売後臨床試験に関する調査審議事項 審議事項 治験等の実施に関する研究 継続 ME2080 の Dravet 症候群患者を対象とした一般臨床試験 ( 第 Ⅲ 相 ) (Protocol No:STP-1) 被験薬 :ME2080(Stiripentol)
Microsoft PowerPoint - 資料4 医療機器の薬事承認について
 資料 4 医療機器の薬事承認等について 厚生労働省医薬食品局審査管理課医療機器審査管理室 医療行為と医療機器 薬事法における一般的名称 4000 種類以上 ( 品目数 30 万品目以上 ) 予防 ( 検査 ) 診断 治療 リハビリ 心電計 内視鏡 自動牽引装置 レントゲン装置 ペースメーカ 血圧計 レーザメス 人工心臓 ステント マイクロ波治療器 人工心肺装置 血液検査装置 超音波診断装置 X 線
資料 4 医療機器の薬事承認等について 厚生労働省医薬食品局審査管理課医療機器審査管理室 医療行為と医療機器 薬事法における一般的名称 4000 種類以上 ( 品目数 30 万品目以上 ) 予防 ( 検査 ) 診断 治療 リハビリ 心電計 内視鏡 自動牽引装置 レントゲン装置 ペースメーカ 血圧計 レーザメス 人工心臓 ステント マイクロ波治療器 人工心肺装置 血液検査装置 超音波診断装置 X 線
医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年
![医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年 医薬品たるコンビネーション製品の不具合報告等に関する Q&A [ 用いた略語 ] 法 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律 ( 昭和 35 年法律第 145 号 ) 施行規則 : 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則 ( 昭和 36 年](/thumbs/91/107149459.jpg) 事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
事務連絡 平成 29 年 6 月 9 日 各都道府県衛生主管部 ( 局 ) 薬務主管課御中 厚生労働省医薬 生活衛生局安全対策課 コンビネーション製品の副作用等報告に関する Q&A について の改訂について コンビネーション製品の副作用等報告に関するQ&Aについては コンビネーション製品の副作用等報告に関するQ&Aについて ( 平成 26 年 10 月 31 日付け厚生労働省医薬食品局安全対策課事務連絡
管下関係業者に周知いただくとともに 適切な指導を行い その実施に遺漏な きようお願いいたします 記 第 1 体外診断用医薬品の製造販売業又は製造業を行う旨の届出等について 1. 届出対象者旧薬事法に基づき 体外診断用医薬品を取り扱う以下の者 (1) 旧薬事法第 12 条第 1 項の第二種医薬品製造販
 薬食機参発 0 8 2 1 第 1 号 薬食安発 0 8 2 1 第 1 号 平成 2 6 年 8 月 2 1 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 厚生労働省医薬食品局安全対策課長 ( 公印省略 ) 体外診断用医薬品の製造販売業又は製造業を行う旨の届出等について 薬事法等の一部を改正する法律 ( 平成
薬食機参発 0 8 2 1 第 1 号 薬食安発 0 8 2 1 第 1 号 平成 2 6 年 8 月 2 1 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 厚生労働省医薬食品局安全対策課長 ( 公印省略 ) 体外診断用医薬品の製造販売業又は製造業を行う旨の届出等について 薬事法等の一部を改正する法律 ( 平成
Microsoft Word - H _概要_.doc
 平成 25 年 5 月独立行政法人国立病院機構西新潟中央病院倫理審査委員会 ( 受託研究 ) 議事要旨 開催日時 開催場所 出席委員名は別紙のとおり 治験及び製造販売後臨床試験に関する調査審議事項 審議事項 治験等の実施に関する研究 継続 部分発作を有する小児てんかん患者を対象とした TRI476(Oxcarbazepine) 第 Ⅱ/Ⅲ 相試験被験薬 :TRI476(Oxcarbazepine)
平成 25 年 5 月独立行政法人国立病院機構西新潟中央病院倫理審査委員会 ( 受託研究 ) 議事要旨 開催日時 開催場所 出席委員名は別紙のとおり 治験及び製造販売後臨床試験に関する調査審議事項 審議事項 治験等の実施に関する研究 継続 部分発作を有する小児てんかん患者を対象とした TRI476(Oxcarbazepine) 第 Ⅱ/Ⅲ 相試験被験薬 :TRI476(Oxcarbazepine)
審査報告 (1) 別紙 平成 29 年 4 月 3 日 本申請において 申請者が提出した資料及び医薬品医療機器総合機構における審査の概略等は 以下 のとおりである 申請品目 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノ
![審査報告 (1) 別紙 平成 29 年 4 月 3 日 本申請において 申請者が提出した資料及び医薬品医療機器総合機構における審査の概略等は 以下 のとおりである 申請品目 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノ 審査報告 (1) 別紙 平成 29 年 4 月 3 日 本申請において 申請者が提出した資料及び医薬品医療機器総合機構における審査の概略等は 以下 のとおりである 申請品目 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノ](/thumbs/92/110667825.jpg) 審査報告書 平成 29 年 5 月 17 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノバルティスファーマ株式会社 [ 申請年月日 ] 平成 28 年 7 月 28 日 [ 剤形 含量
審査報告書 平成 29 年 5 月 17 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノバルティスファーマ株式会社 [ 申請年月日 ] 平成 28 年 7 月 28 日 [ 剤形 含量
査を実施し 必要に応じ適切な措置を講ずること (2) 本品の警告 効能 効果 性能 用法 用量及び使用方法は以下のとお りであるので 特段の留意をお願いすること なお その他の使用上の注意については 添付文書を参照されたいこと 警告 1 本品投与後に重篤な有害事象の発現が認められていること 及び本品
 薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
対象疾患の重篤性など 一定の要件を満たす画期的な新薬などについて 開発の早期段階から対象品目に指定し 薬事承認に関する相談 審査で優先的な取扱いをすることで 承認審査の期間を短縮することを目的としたものだ 通常の新医薬品の場合 12 カ月を目標に審査を行っているが この制度を活用することで 審査期間
 第 163 号平成 27 年 10 月 30 日 ( 金曜日 ) 有馬公認会計士 税理士事務所 136-0071 東京都江東区亀戸 2-24-3 グランズ亀戸 3F TEL(03)5875-0315 http://www.care-advice.net 厚労省 先駆け審査指定制度 の対象 6 品目を初めて指定新制度は 目標審査期間を通常の半分の 6 か月に短縮 薬局に健康サポート機能 高度薬学管理機能求める厚労省
第 163 号平成 27 年 10 月 30 日 ( 金曜日 ) 有馬公認会計士 税理士事務所 136-0071 東京都江東区亀戸 2-24-3 グランズ亀戸 3F TEL(03)5875-0315 http://www.care-advice.net 厚労省 先駆け審査指定制度 の対象 6 品目を初めて指定新制度は 目標審査期間を通常の半分の 6 か月に短縮 薬局に健康サポート機能 高度薬学管理機能求める厚労省
薬-1 長期収載品と後発品
 中医協薬 - 1 2 5. 1 1. 2 0 長期収載品と後発品 ~ 後発品への置換えによる財政効果並びに長期収載品及び新薬創出 適応外薬解消等促進加算 ~ 中間とりまとめ ( 抜粋 ) 中間とりまとめの閾値について 中医協薬 -1 25.11.13 2. 長期収載品 ( 先発医薬品 ) の薬価及び後発品への置き換えについてイ ) 長期収載品の薬価については 市場実勢価格を反映することを原則とするが
中医協薬 - 1 2 5. 1 1. 2 0 長期収載品と後発品 ~ 後発品への置換えによる財政効果並びに長期収載品及び新薬創出 適応外薬解消等促進加算 ~ 中間とりまとめ ( 抜粋 ) 中間とりまとめの閾値について 中医協薬 -1 25.11.13 2. 長期収載品 ( 先発医薬品 ) の薬価及び後発品への置き換えについてイ ) 長期収載品の薬価については 市場実勢価格を反映することを原則とするが
標準業務手順 目次
 浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
浜松医科大学医学部附属病院治験審査委員会標準的業務手順書 第 1 章治験審査委員会 ( 目的と適用範囲 ) 第 1 条本手順書は GCP 省令等に基づいて 浜松医科大学医学部附属病院治験審査委員会の運営に関する手続及び記録の保存方法を定めるものである 2 本手順書は 医薬品及び医療機器の製造販売承認申請又は承認事項一部変更承認申請 ( 以下 承認申請 という ) の際に提出すべき資料の収集のために行う治験に対して適用する
本日の講演内容 1. PMDA コンパニオン診断薬 WG 2. 本邦におけるコンパニオン診断薬の規制 3. 遺伝子パネルを用いた NGS コンパニオン診断システム 1 2 規制上の取扱い 評価の考え方 2
 わが国での NGS 診断パネル承認の考え方 独立行政法人医薬品医療機器総合機構上席審議役 ( 機器審査等担当 ) 佐藤岳幸 本日の講演内容 1. PMDA コンパニオン診断薬 WG 2. 本邦におけるコンパニオン診断薬の規制 3. 遺伝子パネルを用いた NGS コンパニオン診断システム 1 2 規制上の取扱い 評価の考え方 2 本日の講演内容 1. PMDA コンパニオン診断薬 WG 2. 本邦におけるコンパニオン診断薬の規制
わが国での NGS 診断パネル承認の考え方 独立行政法人医薬品医療機器総合機構上席審議役 ( 機器審査等担当 ) 佐藤岳幸 本日の講演内容 1. PMDA コンパニオン診断薬 WG 2. 本邦におけるコンパニオン診断薬の規制 3. 遺伝子パネルを用いた NGS コンパニオン診断システム 1 2 規制上の取扱い 評価の考え方 2 本日の講演内容 1. PMDA コンパニオン診断薬 WG 2. 本邦におけるコンパニオン診断薬の規制
4. 独立行政法人医薬品医療機器総合機構 (PMDA) との連携創薬シーズの実用化に向けて 独立行政法人医薬品医療機器総合機構 (PMDA) が実施する RS 総合相談 RS 戦略相談を利用することが想定される場合 相談者からの同意を得た上で 独立行政法人医薬品医療機器総合機構 (PMDA) に対し
 創薬ナビに関する実施要領 平成 27 年 4 月 1 日平成 27 年 7 月 1 日改定平成 27 年 12 月 25 日改定平成 29 年 11 月 10 日改定 1. 事業の目的創薬ナビは 我が国の大学や公的研究機関で生み出された優れた研究成果 ( 創薬シーズ ) を確実に実用化につなげるため 創薬研究に取り組む大学等の研究者からの様々な相談に応じることでアカデミア発創薬を支援することを目的としています
創薬ナビに関する実施要領 平成 27 年 4 月 1 日平成 27 年 7 月 1 日改定平成 27 年 12 月 25 日改定平成 29 年 11 月 10 日改定 1. 事業の目的創薬ナビは 我が国の大学や公的研究機関で生み出された優れた研究成果 ( 創薬シーズ ) を確実に実用化につなげるため 創薬研究に取り組む大学等の研究者からの様々な相談に応じることでアカデミア発創薬を支援することを目的としています
最近の薬務行政について
 平成 25 年 7 月 26 日現在 薬事法改正について 厚生労働省医薬食品局審査管理課 医療機器審査管理室 これらの内容には現段階で検討中の内容が含まれており 今後変更する可能性があります 薬事法改正法案及び再生医療等安全性確保法案の概要について 現在 国民が受ける医療の質の向上を図るため 革新的な医薬品 医療機器の創出や再生医療の研究開発及び実用化を促進していくことが喫緊の課題となっている 併せて
平成 25 年 7 月 26 日現在 薬事法改正について 厚生労働省医薬食品局審査管理課 医療機器審査管理室 これらの内容には現段階で検討中の内容が含まれており 今後変更する可能性があります 薬事法改正法案及び再生医療等安全性確保法案の概要について 現在 国民が受ける医療の質の向上を図るため 革新的な医薬品 医療機器の創出や再生医療の研究開発及び実用化を促進していくことが喫緊の課題となっている 併せて
目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2
 免疫アレルギー疾患等実用化研究事業 ( 移植医療技術開発研究分野 ) 2019 年度 1 次公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 戦略推進部 難病研究課 2018 年 11 月 1 目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2 1. はじめに
免疫アレルギー疾患等実用化研究事業 ( 移植医療技術開発研究分野 ) 2019 年度 1 次公募に係る府省共通研究開発管理システム (e-rad) への入力方法について 戦略推進部 難病研究課 2018 年 11 月 1 目次 1. はじめに 2. 実際の応募手続き 2-a. 手続きを始める前に 2-b. 研究開発提案書様式の取得 2-c. 応募の新規登録 2-d. 応募情報の入力 2 1. はじめに
本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2. 書面調査 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの見直し 3.2. 医薬品再審査適合性調査相談 ( 新設 ) 2
 医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2. 書面調査 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの見直し 3.2. 医薬品再審査適合性調査相談 ( 新設 ) 2 本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2.
医薬品の製造販売後調査の 現状と留意点 1 本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2. 書面調査 3. 適合性調査の効率化に向けて 3.1. 安全性情報管理シートの見直し 3.2. 医薬品再審査適合性調査相談 ( 新設 ) 2 本日の内容 1. 再審査申請と関連法規 2. 医薬品の再審査申請資料適合性調査 2.1. 実地調査 2.2.
2. 各検討課題に関する論点 (1) 費用対効果評価の活用方法 費用対効果評価の活用方法について これまでの保険給付の考え方等の観点も含め どう考 えるか (2) 対象品目の選定基準 1 費用対効果評価の対象とする品目の範囲 選択基準 医療保険財政への影響度等の観点から 対象となる品目の要件をどう設
 中医協費薬材 - 3 3 0. 1 2. 5 費用対効果評価に関する検討状況について ( 報告 ) 1. 概要 費用対効果評価については これまで以下の課題につき 中医協において協議及び論点の整 理を行ってきたところ 今後 関係業界からのヒアリングを行い とりまとめを行う予定 (1) 費用対効果評価の活用方法 (2) 対象品目の選択基準 1 費用対効果評価の対象とする品目の範囲 選択基準 3 品目選定のタイミング
中医協費薬材 - 3 3 0. 1 2. 5 費用対効果評価に関する検討状況について ( 報告 ) 1. 概要 費用対効果評価については これまで以下の課題につき 中医協において協議及び論点の整 理を行ってきたところ 今後 関係業界からのヒアリングを行い とりまとめを行う予定 (1) 費用対効果評価の活用方法 (2) 対象品目の選択基準 1 費用対効果評価の対象とする品目の範囲 選択基準 3 品目選定のタイミング
添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示され
 添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示されます 検索条件設定時の注意 検索はテキスト文章 (SGML 又は XML) が対象となっており 画像及び
添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示されます 検索条件設定時の注意 検索はテキスト文章 (SGML 又は XML) が対象となっており 画像及び
薬事法等の一部改正に伴う特許法施行令改正に係る事前評価書
 薬事法等の一部改正に伴う特許法施行令改正に係る事前評価書 1. 政策の名称 薬事法改正に伴い新たに定義される再生医療等製品に係る製造販売の承認を特許権 の存続期間の延長登録の理由となる処分に追加するべく措置を講じる政策 2. 担当部局 経済産業省特許庁審査第一部調整課審査基準室長滝口尚良 電話番号 : 03-3501-0046 e-mail: PA2A10@jpo.go.jp 3. 評価実施時期 平成
薬事法等の一部改正に伴う特許法施行令改正に係る事前評価書 1. 政策の名称 薬事法改正に伴い新たに定義される再生医療等製品に係る製造販売の承認を特許権 の存続期間の延長登録の理由となる処分に追加するべく措置を講じる政策 2. 担当部局 経済産業省特許庁審査第一部調整課審査基準室長滝口尚良 電話番号 : 03-3501-0046 e-mail: PA2A10@jpo.go.jp 3. 評価実施時期 平成
バイオ医薬品は生物を用いて製造されます 通常 細菌や動物細胞などの生体の中で目的とするタンパク質を産生させます バイオ医薬品の特性は製造プロセスの状態に依存するところが大きく しばしば プロセスが製品 と喩えられます 事実 製造プロセスにおける小さな変更でも 最終製品の違いにつながる可能性があります
 バイオ医薬品とバイオシミラー ( バイオ後続品 ) に関する Q&A 1. バイオテクノロジーとは そしてバイオ医薬品の役割とはどのようなものでしょうか? バイオテクノロジーとは 製品やサービスを生み出するために生物やその一部による修飾を用いた一連の方法やプロセスです 1970 年代のいわゆる 組換えDNA 技術 の発展 展開により 分子レベル でのバイオテクノロジーという新たな時代が幕を開け 様々な分野で知識革命を引き起こしました
バイオ医薬品とバイオシミラー ( バイオ後続品 ) に関する Q&A 1. バイオテクノロジーとは そしてバイオ医薬品の役割とはどのようなものでしょうか? バイオテクノロジーとは 製品やサービスを生み出するために生物やその一部による修飾を用いた一連の方法やプロセスです 1970 年代のいわゆる 組換えDNA 技術 の発展 展開により 分子レベル でのバイオテクノロジーという新たな時代が幕を開け 様々な分野で知識革命を引き起こしました
Microsoft Word - (発出)マル製通知案
 薬食機参発 1119 第 7 号 薬食監麻発 1119 第 12 号 平成 26 年 11 月 19 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 厚生労働省医薬食品局監視指導 麻薬対策課長 ( 公印省略 ) 医療機器及び体外診断用医薬品の製造所の変更又は追加に係る手続 の迅速化について 医療機器及び体外診断用医薬品の製造所の変更に係る手続きの迅速化については
薬食機参発 1119 第 7 号 薬食監麻発 1119 第 12 号 平成 26 年 11 月 19 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) ( 公印省略 ) 厚生労働省医薬食品局監視指導 麻薬対策課長 ( 公印省略 ) 医療機器及び体外診断用医薬品の製造所の変更又は追加に係る手続 の迅速化について 医療機器及び体外診断用医薬品の製造所の変更に係る手続きの迅速化については
Microsoft Word - (発番)医療機器の製造販売承認申請について
 薬食発 1120 第 5 号 平成 26 年 11 月 20 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医療機器の製造販売承認申請について 医療機器の製造販売承認申請の取扱いについては 医療機器の製造販売承認申請について ( 平成 17 年 2 月 16 日付け薬食発第 0216002 号厚生労働省医薬食品局長通知 以下 旧通知 という ) 等により実施してきたところです 先般
薬食発 1120 第 5 号 平成 26 年 11 月 20 日 各都道府県知事殿 厚生労働省医薬食品局長 ( 公印省略 ) 医療機器の製造販売承認申請について 医療機器の製造販売承認申請の取扱いについては 医療機器の製造販売承認申請について ( 平成 17 年 2 月 16 日付け薬食発第 0216002 号厚生労働省医薬食品局長通知 以下 旧通知 という ) 等により実施してきたところです 先般
PowerPoint プレゼンテーション
 2018 年 3 月 31 日第 24 回抗悪性腫瘍薬開発フォーラム ( 於 : がん研究会がん研究所 ) 将来の承認審査の視点 独立行政法人医薬品医療機器総合機構 (PMDA) 新薬審査第五部 清原宏眞 本日のお話 国等の動き 審査の視点 本講演は 講演者の個人的見解に基づくものであり ( 独 ) 医薬品医療機器総合機構 (PMDA) の公式見解を示すものではありません 先駆け審査指定制度 世界に先駆けて
2018 年 3 月 31 日第 24 回抗悪性腫瘍薬開発フォーラム ( 於 : がん研究会がん研究所 ) 将来の承認審査の視点 独立行政法人医薬品医療機器総合機構 (PMDA) 新薬審査第五部 清原宏眞 本日のお話 国等の動き 審査の視点 本講演は 講演者の個人的見解に基づくものであり ( 独 ) 医薬品医療機器総合機構 (PMDA) の公式見解を示すものではありません 先駆け審査指定制度 世界に先駆けて
胚乳細胞中のタンパク質顆粒 I(PB-I) に改変型 Cry j 1タンパク質 及びCry j 2タンパク質を蓄積させたものです 2 スギ花粉ペプチド含有米( キタアケ ) スギ花粉が有する主要アレルゲンタンパク質 2 種 (Cry j 1 Cry j 2) の7 種類の主要 T 細胞エピトープを連
 別紙 1 平成 30 年 4 月 10 日 スギ花粉米 の外部機関への提供に関する応募要領 1. 趣旨国立研究開発法人農業 食品産業技術総合研究機構 ( 農研機構 ) は 遺伝子組換え (GM) イネにより 農研機構の隔離ほ場で生産した スギ花粉米 ( スギ花粉ポリペプチド含有米 及び スギ花粉ペプチド含有米 ) を活用した用途開発等の実用化を加速するため 一定の条件の下で これらの生物材料を民間企業や大学
別紙 1 平成 30 年 4 月 10 日 スギ花粉米 の外部機関への提供に関する応募要領 1. 趣旨国立研究開発法人農業 食品産業技術総合研究機構 ( 農研機構 ) は 遺伝子組換え (GM) イネにより 農研機構の隔離ほ場で生産した スギ花粉米 ( スギ花粉ポリペプチド含有米 及び スギ花粉ペプチド含有米 ) を活用した用途開発等の実用化を加速するため 一定の条件の下で これらの生物材料を民間企業や大学
医師主導治験取扱要覧
 15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
 医学会発第 49 号 平成 29 年 3 月 23 日 日本医学会分科会 理事長 会長殿 日本医学会長 髙久史麿 公印省略 薬事戦略相談に関する実施要綱の一部改正等について ( 周知依頼 ) 平素より, 本会の事業推進にご協力を賜りまして, 誠にありがとうございます. このほど, 医薬品医療機器総合機構 (PMDA) から本職宛に, 標記の依頼が参りました.PMDA では平成 23 年 6 月 30
医学会発第 49 号 平成 29 年 3 月 23 日 日本医学会分科会 理事長 会長殿 日本医学会長 髙久史麿 公印省略 薬事戦略相談に関する実施要綱の一部改正等について ( 周知依頼 ) 平素より, 本会の事業推進にご協力を賜りまして, 誠にありがとうございます. このほど, 医薬品医療機器総合機構 (PMDA) から本職宛に, 標記の依頼が参りました.PMDA では平成 23 年 6 月 30
ことを通じて (1) 国民が 世界最先端の医薬品 医療機器 再生医療等製品の恩恵を受けることができるよう これらをより早く安全に医療現場に届けるための審査等業務 (2) 世界最先端の医薬品等が海外での使用経験なく我が国の医療現場で使用される状況を想定し 保健衛生上の危害発生の防止 発生時の的確かつ迅
 資料 6 平成 30 年 10 月 17 日 ( 独 ) 医薬品医療機器総合機構 第 4 期中期計画の方向性について ( 案 ) Ⅰ. 第 4 期中期計画の基本的考え方 当機構は 医薬品の副作用による健康被害を迅速に救済するとともに 医薬品 医療機器等の品質 有効性及び安全性を確保するための審査及び安全対策の体制を拡充強化することを目的として 平成 16 年 4 月に発足した 平成 20 年度には
資料 6 平成 30 年 10 月 17 日 ( 独 ) 医薬品医療機器総合機構 第 4 期中期計画の方向性について ( 案 ) Ⅰ. 第 4 期中期計画の基本的考え方 当機構は 医薬品の副作用による健康被害を迅速に救済するとともに 医薬品 医療機器等の品質 有効性及び安全性を確保するための審査及び安全対策の体制を拡充強化することを目的として 平成 16 年 4 月に発足した 平成 20 年度には
2 改善命令 1への対応 TIB 審査会は ファーマコビジランス部門が委員長および事務局を務め 営業部門から独立した組織として運営しており 更に 2014 年 4 月より 審査体制の強化を目指し 法的観点から法務部員を メディカルサイエンスの立場からメディカルアフェアーズ部員 ( 医師 ) を委員に
 2015 年 7 月 10 日 武田薬品工業株式会社 厚生労働省発薬食 0612 第 7 号に係る改善命令に対する改善計画 弊社は 2014 年 3 月以降 医療関係者向けの広告資材に関する審査 管理体制を強化してまいりましたが 今般の改善命令を受け 再発防止のため 下記のとおり新たな改善策を実施いたします なお 改善策の実施状況につきましては 今後 定期的に厚生労働省医薬食品局監視指導 麻薬対策課までご報告いたしますとともに
2015 年 7 月 10 日 武田薬品工業株式会社 厚生労働省発薬食 0612 第 7 号に係る改善命令に対する改善計画 弊社は 2014 年 3 月以降 医療関係者向けの広告資材に関する審査 管理体制を強化してまいりましたが 今般の改善命令を受け 再発防止のため 下記のとおり新たな改善策を実施いたします なお 改善策の実施状況につきましては 今後 定期的に厚生労働省医薬食品局監視指導 麻薬対策課までご報告いたしますとともに
医療イノベーションに向けて 日本学術会議からの提言
 日本製薬工業協会医薬品評価委員会 薬事委員会合同総会 2012 年 4 月 25 日 PMDA における 相談 審査業務の現状と今後 ( 独 ) 医薬品医療機器総合機構 (PMDA) 内海英雄 審査等業務の充実 承認審査体制の拡充強化等 新医薬品の承認までの期間を 2.5 年 ( 開発期間と審査期間をそれぞれ 1.5 年 1.0 年 ) 短縮することを目指す ( 平成 19 年度から 5 年間 )
日本製薬工業協会医薬品評価委員会 薬事委員会合同総会 2012 年 4 月 25 日 PMDA における 相談 審査業務の現状と今後 ( 独 ) 医薬品医療機器総合機構 (PMDA) 内海英雄 審査等業務の充実 承認審査体制の拡充強化等 新医薬品の承認までの期間を 2.5 年 ( 開発期間と審査期間をそれぞれ 1.5 年 1.0 年 ) 短縮することを目指す ( 平成 19 年度から 5 年間 )
前項に規定する事項のうち当該被験薬の治験薬概要書から予測できないもの に改め 同項を同条第三項とし 同条第一項の次に次の一項を加える 2治験依頼者は 被験薬について法第八十条の二第六項に規定する事項を知ったときは その発現症例一覧等を当該被験薬ごとに 当該被験薬について初めて治験の計画を届け出た日等
 厚生労働省令第二十四号薬事法(昭和三十五年法律第百四十五号)第十四条第三項(同条第九項及び同法第十九条の二第五項において準用する場合を含む ) 第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む ) 第八十条の二第一項 第四項及び第五項並びに第八十二条の規定に基づき 医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十年二月二十九日厚生労働大臣舛添要一医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令医薬品の臨床試験の実施の基準に関する省令(平成九年厚生省令第二十八号)の一部を次のように改正する
厚生労働省令第二十四号薬事法(昭和三十五年法律第百四十五号)第十四条第三項(同条第九項及び同法第十九条の二第五項において準用する場合を含む ) 第十四条の四第四項及び第十四条の六第四項(これらの規定を同法第十九条の四において準用する場合を含む ) 第八十条の二第一項 第四項及び第五項並びに第八十二条の規定に基づき 医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令を次のように定める 平成二十年二月二十九日厚生労働大臣舛添要一医薬品の臨床試験の実施の基準に関する省令の一部を改正する省令医薬品の臨床試験の実施の基準に関する省令(平成九年厚生省令第二十八号)の一部を次のように改正する
「ヒトES細胞の樹立に関する指針」(案)及び「ヒトES細胞の分配及び使用に関する指針」(案)に関するパブリック・コメント(意見公募手続)の結果について
 平成 26 年 11 月 2 5 日 文部科学省研究振興局ライフサイエンス課生命倫理 安全対策室 厚生労働省医政局研究開発振興課再生医療研究推進室 厚 生 労 働 省 医 薬 食 品 局 医療機器 再生医療等製品担当参事官室 ヒト ES 細胞の樹立に関する指針 ( 案 ) 及び ヒト ES 細胞の分配及び使用に関する指針 ( 案 ) に関するパブリックコメント ( 意見公募手続 ) の結果について
平成 26 年 11 月 2 5 日 文部科学省研究振興局ライフサイエンス課生命倫理 安全対策室 厚生労働省医政局研究開発振興課再生医療研究推進室 厚 生 労 働 省 医 薬 食 品 局 医療機器 再生医療等製品担当参事官室 ヒト ES 細胞の樹立に関する指針 ( 案 ) 及び ヒト ES 細胞の分配及び使用に関する指針 ( 案 ) に関するパブリックコメント ( 意見公募手続 ) の結果について
3 治験実施計画書目的 当該治験について 治験実施計画書が手順書に従い適切に作成及び改訂されていることを確認する 次の事項を調べる (1) 治験実施計画書の記載項目 ( 再生医療等製品 GCP 省令第 7 条第 1 項に規定する項目 ) (2) 治験実施計画書の作成 改訂の手順と日付 (3) 治験計
 別添 10 再生医療等製品 GCP 省令チェックリスト Ⅰ 治験依頼者 ( 受託機関を含む ) 用 1 組織及び体制目的 治験の依頼及び管理に当たって 再生医療等製品 GCP 省令に沿った業務を行うために適切にして十分な人材を有し かつ 組織及び体制が確立していることを確認する 1 治験依頼者の組織 ( 当該被験機器の開発組織を含む ) と再生医療等製品 G CP 省令に係わる組織との関係 2 治験の依頼及び管理の業務に従事する者の氏名
別添 10 再生医療等製品 GCP 省令チェックリスト Ⅰ 治験依頼者 ( 受託機関を含む ) 用 1 組織及び体制目的 治験の依頼及び管理に当たって 再生医療等製品 GCP 省令に沿った業務を行うために適切にして十分な人材を有し かつ 組織及び体制が確立していることを確認する 1 治験依頼者の組織 ( 当該被験機器の開発組織を含む ) と再生医療等製品 G CP 省令に係わる組織との関係 2 治験の依頼及び管理の業務に従事する者の氏名
料 情報の提供に関する記録 を作成する方法 ( 作成する時期 記録の媒体 作成する研究者等の氏名 別に作成する書類による代用の有無等 ) 及び保管する方法 ( 場所 第 12 の1⑴の解説 5に規定する提供元の機関における義務 8 個人情報等の取扱い ( 匿名化する場合にはその方法等を含む ) 9
 北里研究所病院研究倫理委員会研究申請時確認シート ( 補助資料 ) 20170425 Ver.2.0 < 研究計画書の確認 > 記載項目 1 研究の名称 2 研究の実施体制 ( 研究機関の名称及び研究者等の氏名を含む ) 3 研究の目的及び意義 4 研究の方法及び期間 5 研究対象者の選定方針 6 研究の科学的合理性の根拠 7インフォームド コンセントを受ける手続等 ( インフォームド コンセントを受ける場合には
北里研究所病院研究倫理委員会研究申請時確認シート ( 補助資料 ) 20170425 Ver.2.0 < 研究計画書の確認 > 記載項目 1 研究の名称 2 研究の実施体制 ( 研究機関の名称及び研究者等の氏名を含む ) 3 研究の目的及び意義 4 研究の方法及び期間 5 研究対象者の選定方針 6 研究の科学的合理性の根拠 7インフォームド コンセントを受ける手続等 ( インフォームド コンセントを受ける場合には
(Microsoft Word -
 事務連絡 平成 30 年 2 月 28 日 医薬品 医療機器等製造販売業者殿 奈良県医療政策部薬務課薬物監視係長 医薬品 医療機器等の回収の取扱いについて 医薬品 医薬部外品 化粧品及び医療機器等の回収については 医薬品 医療機器等の回収について ( 平成 26 年 12 月 21 日付け薬食発 1121 第 10 号厚生労働省医薬食品局長通知 ) 及び 医薬品 医療機器等の回収の取扱いについて (
事務連絡 平成 30 年 2 月 28 日 医薬品 医療機器等製造販売業者殿 奈良県医療政策部薬務課薬物監視係長 医薬品 医療機器等の回収の取扱いについて 医薬品 医薬部外品 化粧品及び医療機器等の回収については 医薬品 医療機器等の回収について ( 平成 26 年 12 月 21 日付け薬食発 1121 第 10 号厚生労働省医薬食品局長通知 ) 及び 医薬品 医療機器等の回収の取扱いについて (
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社
 オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7
![審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7 審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7](/thumbs/92/110490968.jpg) 審査報告書 平成 26 年 1 月 6 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [
審査報告書 平成 26 年 1 月 6 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [
平成 23 年 7 月 5 日 米国医療機器 IVD 工業会 (AMDD) 会長デイビット W. パウエル 欧州ビジネス協会 (EBC) 医療機器委員会 委員長ダニー リスバーグ 医療機器 ( 体外診断用検査機器を含む ) の薬事法改正に係る提言 はじめに 医薬品は新しい有効成分を探しあるいは創り
 医療機器の薬事法改正に係る米国医療機器 IVD 工業会 (AMDD) 欧州ビジネス協会 (EBC) 共同提言書 平成 23 年 7 月 5 日 米国医療機器 IVD 工業会 (AMDD) 会長デイビット W. パウエル 欧州ビジネス協会 (EBC) 医療機器委員会 委員長ダニー リスバーグ 医療機器 ( 体外診断用検査機器を含む ) の薬事法改正に係る提言 はじめに 医薬品は新しい有効成分を探しあるいは創り
医療機器の薬事法改正に係る米国医療機器 IVD 工業会 (AMDD) 欧州ビジネス協会 (EBC) 共同提言書 平成 23 年 7 月 5 日 米国医療機器 IVD 工業会 (AMDD) 会長デイビット W. パウエル 欧州ビジネス協会 (EBC) 医療機器委員会 委員長ダニー リスバーグ 医療機器 ( 体外診断用検査機器を含む ) の薬事法改正に係る提言 はじめに 医薬品は新しい有効成分を探しあるいは創り
はじめに 本演題発表に関連して 開示すべき利益相反関係にある企業等はありません これまでの臨床や研究 PMDAの新薬承認審査 ワーキンググループ業務の経験に基づき 個人の考えとして発表するものです 公開情報をもとに説明しますが 職務上の守秘義務により ご説明出来ない場合もあります 質問 議論は大歓迎
 第 41 回日本臨床免疫学会特別講演 2 11 月 27 日 ( 水 )15:50~16:20 第 2 会場 ( 海峡メッセ下関 10 階 国際会議場 ) オーファンドラッグの開発に向けて 医薬品医療機器総合機構 (PMDA) 新薬審査第 3 部審査役代理オーファン医薬品ワーキンググループ ( 神経内科専門医 ) 中村治雅 はじめに 本演題発表に関連して 開示すべき利益相反関係にある企業等はありません
第 41 回日本臨床免疫学会特別講演 2 11 月 27 日 ( 水 )15:50~16:20 第 2 会場 ( 海峡メッセ下関 10 階 国際会議場 ) オーファンドラッグの開発に向けて 医薬品医療機器総合機構 (PMDA) 新薬審査第 3 部審査役代理オーファン医薬品ワーキンググループ ( 神経内科専門医 ) 中村治雅 はじめに 本演題発表に関連して 開示すべき利益相反関係にある企業等はありません
本日の内容 1. 未承認対照薬等の取り扱い別添の 4.(3) ウ.( ア ) 2. 対象疾患の悪化等を評価項目にする試験別添の 7.(3) イ.( ア ) 3. 承認取得者以外の治験国内管理人が治験 依頼者となる場合別添の7.(3) オ. 4. 医師主導治験との情報共有別添の7.(3) カ. 5.
 治験の安全性対応シンポジウム 安全性二課長通知の改訂点平成 25 年 5 月 15 日付二課長通知 ( 薬食審査発 0515 第 1 号 薬食安発 0515 第 1 号 ) 2013 年 12 月 16 日 日本製薬工業協会医薬品評価委員会臨床評価部会五十嵐元 山城恭子 1 本日の内容 1. 未承認対照薬等の取り扱い別添の 4.(3) ウ.( ア ) 2. 対象疾患の悪化等を評価項目にする試験別添の
治験の安全性対応シンポジウム 安全性二課長通知の改訂点平成 25 年 5 月 15 日付二課長通知 ( 薬食審査発 0515 第 1 号 薬食安発 0515 第 1 号 ) 2013 年 12 月 16 日 日本製薬工業協会医薬品評価委員会臨床評価部会五十嵐元 山城恭子 1 本日の内容 1. 未承認対照薬等の取り扱い別添の 4.(3) ウ.( ア ) 2. 対象疾患の悪化等を評価項目にする試験別添の
QbDを用いた新薬申請の審査とGMP適合性調査 -現状及び課題-
 QbD を用いた新薬申請の 審査と GMP 適合性調査 - 現状及び課題 - 医薬品医療機器総合機構 新薬審査第五部 松田嘉弘 品質管理部 森末政利 審査の視点から 本日の内容 ICH Q8 Q9 Q10 Q11について QbD 申請の状況 審査の事例 審査における課題 調査の視点から GMP 調査とQbD 調査のポイント 調査の事例 QbDが実現すること ICH Q8 Q9 Q10 Q11 について
QbD を用いた新薬申請の 審査と GMP 適合性調査 - 現状及び課題 - 医薬品医療機器総合機構 新薬審査第五部 松田嘉弘 品質管理部 森末政利 審査の視点から 本日の内容 ICH Q8 Q9 Q10 Q11について QbD 申請の状況 審査の事例 審査における課題 調査の視点から GMP 調査とQbD 調査のポイント 調査の事例 QbDが実現すること ICH Q8 Q9 Q10 Q11 について
Microsoft Word - 【案1】登録認証機関立入要領改正通知(Ver )
 薬食機参発 1121 第 38 号平成 26 年 11 月 21 日 各登録認証機関の長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) 登録認証機関等に対する立入検査の実施要領の改正について 薬事法 ( 昭和 35 年法律第 145 号 ) の規定による登録認証機関等に対する立入 検査の実施要領については 登録認証機関等に対する立入検査の実施要領について ( 平成 18
薬食機参発 1121 第 38 号平成 26 年 11 月 21 日 各登録認証機関の長殿 厚生労働省大臣官房参事官 ( 医療機器 再生医療等製品審査管理担当 ) 登録認証機関等に対する立入検査の実施要領の改正について 薬事法 ( 昭和 35 年法律第 145 号 ) の規定による登録認証機関等に対する立入 検査の実施要領については 登録認証機関等に対する立入検査の実施要領について ( 平成 18
子宮頸がん予防措置の実施の推進に関する法律案要綱
 第一総則 子宮頸がん予防措置の実施の推進に関する法律案要綱 一目的 けいりこの法律は 子宮頸がんの罹患が女性の生活の質に多大な影響を与えるものであり 近年の子宮頸が んの罹患の若年化の進行が当該影響を一層深刻なものとしている状況及びその罹患による死亡率が高い 状況にあること並びに大部分の子宮頸がんにヒトパピローマウイルスが関与しており 予防ワクチンの 接種及び子宮頸部の前がん病変 ( 子宮頸がんに係る子宮頸部の異形成その他の子宮頸がんの発症前にお
第一総則 子宮頸がん予防措置の実施の推進に関する法律案要綱 一目的 けいりこの法律は 子宮頸がんの罹患が女性の生活の質に多大な影響を与えるものであり 近年の子宮頸が んの罹患の若年化の進行が当該影響を一層深刻なものとしている状況及びその罹患による死亡率が高い 状況にあること並びに大部分の子宮頸がんにヒトパピローマウイルスが関与しており 予防ワクチンの 接種及び子宮頸部の前がん病変 ( 子宮頸がんに係る子宮頸部の異形成その他の子宮頸がんの発症前にお
鑑-H リンゼス錠他 留意事項通知の一部改正等について
 日医発第 617 号 ( 保 154) 平成 30 年 8 月 29 日 都道府県医師会長殿 日本医師会長横倉義武 医薬品医療機器等法上の効能 効果等の変更に伴う留意事項の一部改正等について 平成 30 年 8 月 21 日付け保医発 0821 第 1 号厚生労働省保険局医療課長通知により 添付資料の通り保険適用上の取扱いに関する留意事項が一部改正されましたのでお知らせ申し上げます 今回の改正は 同日付けで添付資料の医薬品の効能
日医発第 617 号 ( 保 154) 平成 30 年 8 月 29 日 都道府県医師会長殿 日本医師会長横倉義武 医薬品医療機器等法上の効能 効果等の変更に伴う留意事項の一部改正等について 平成 30 年 8 月 21 日付け保医発 0821 第 1 号厚生労働省保険局医療課長通知により 添付資料の通り保険適用上の取扱いに関する留意事項が一部改正されましたのでお知らせ申し上げます 今回の改正は 同日付けで添付資料の医薬品の効能
なお,PMDA メディナビでパスワードを設定済の方は, 共通のパスワードとなります (4) 登録完了 ( 図 2 ステップ 3) なお, 登録後, ログイン時は (1) で表示される画面で, ログイン画面へ をクリックし, メー ルアドレス及びパスワードを入力してください 図 1 PMDA メディナ
 2 マイ医薬品集作成サービス について 独立行政法人医薬品医療機器総合機構 (PMDA) では,PMDAメディナビ( 医薬品医療機器情報配信サービス ) にご登録いただいている方がご利用いただける登録 利用無料の追加機能として, マイ医薬品作成サービス を提供しています あらかじめ情報が必要な医薬品を登録しておけば, 添付文書情報等の最新情報を一覧で管理 閲覧することができる大変便利なサービスです
2 マイ医薬品集作成サービス について 独立行政法人医薬品医療機器総合機構 (PMDA) では,PMDAメディナビ( 医薬品医療機器情報配信サービス ) にご登録いただいている方がご利用いただける登録 利用無料の追加機能として, マイ医薬品作成サービス を提供しています あらかじめ情報が必要な医薬品を登録しておけば, 添付文書情報等の最新情報を一覧で管理 閲覧することができる大変便利なサービスです
生殖発生毒性試験の実施時期について
 S5(R3) Informal 医薬品の生殖発生毒性試験法 ( 改訂 ) 日本製薬工業協会 ICH プロジェクト委員会 S5(R3) Informal WG トピックリーダー藤原道夫 1 本日の内容 1. リスボンInformal WG 対面会議開催に至る経緯 2. ミネアポリス会議以後の活動 3. S5(R3) コンセプトペーパーの変遷 4. S5(R3) に向けて検討されるべき事項 5. S5(R3)
S5(R3) Informal 医薬品の生殖発生毒性試験法 ( 改訂 ) 日本製薬工業協会 ICH プロジェクト委員会 S5(R3) Informal WG トピックリーダー藤原道夫 1 本日の内容 1. リスボンInformal WG 対面会議開催に至る経緯 2. ミネアポリス会議以後の活動 3. S5(R3) コンセプトペーパーの変遷 4. S5(R3) に向けて検討されるべき事項 5. S5(R3)
の連携による明確な出口戦略を持って NCを含む臨床研究中核病院などの 拠点 及びそのネットワークが中心となり 拠点外シーズ 拠点外施設も含め all Japan 体制で効率的に研究開発が進められる環境作り ( 1~3) を目指す 1 このような環境が整うことのメリットとしては 我が国における医薬品等
 AMED による橋渡し研究 臨床研究 治験の推進について ( 別紙 ) 臨床研究 治験基盤事業部 1. 基本的考え方 方向性 ( 別添イメージ図参照 ) 〇 AMEDが設立されたことを受け 有望シーズの治験や臨床研究については AMEDとして同一組織となった創薬支援戦略部 戦略推進部 産学連携部 知的財産部と連携しつつ また PMDAともよく連携しながら 橋渡し研究から研究者主導治験等の実施 仲介
AMED による橋渡し研究 臨床研究 治験の推進について ( 別紙 ) 臨床研究 治験基盤事業部 1. 基本的考え方 方向性 ( 別添イメージ図参照 ) 〇 AMEDが設立されたことを受け 有望シーズの治験や臨床研究については AMEDとして同一組織となった創薬支援戦略部 戦略推進部 産学連携部 知的財産部と連携しつつ また PMDAともよく連携しながら 橋渡し研究から研究者主導治験等の実施 仲介
抗悪フォーラム 永井最終版.ppt
 コンパニオン診断薬を用いた抗がん剤の 開発及び評価における留意点 永井純正 Sumimasa NAGAI, M.D., Ph.D. 医薬品医療機器総合機構専門委員 ( 前職新薬審査第五部審査専門員 ) 東京大学医科学研究所先端医療研究センター はじめに 本発表は 個人の見解に基づくものであり PMDA の公式見解を示すものではありません コンパニオン診断薬プロジェクト 横断的基準作成プロジェクトの一つ医薬品
コンパニオン診断薬を用いた抗がん剤の 開発及び評価における留意点 永井純正 Sumimasa NAGAI, M.D., Ph.D. 医薬品医療機器総合機構専門委員 ( 前職新薬審査第五部審査専門員 ) 東京大学医科学研究所先端医療研究センター はじめに 本発表は 個人の見解に基づくものであり PMDA の公式見解を示すものではありません コンパニオン診断薬プロジェクト 横断的基準作成プロジェクトの一つ医薬品
PSP 省令 と それぞれ略称する 記 1. 改正施行規則について希少疾病用医療機器その他の医療上特にその必要性が高いと認められる医療機器であり かつ 当該医療機器についての臨床試験の実施に特に長期間を要すると認められるものに係る承認申請をする場合においては 改正 GVP 省令第 9 条の3 第 1
 薬生発 07 31 第 4 号 平成 29 年 7 月 31 日 各都道府県知事殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則の一部を改正する省令 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令の一部を改正する省令 及び 医療機器の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令
薬生発 07 31 第 4 号 平成 29 年 7 月 31 日 各都道府県知事殿 厚生労働省医薬 生活衛生局長 ( 公印省略 ) 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律施行規則の一部を改正する省令 医薬品 医薬部外品 化粧品 医療機器及び再生医療等製品の製造販売後安全管理の基準に関する省令の一部を改正する省令 及び 医療機器の製造販売後の調査及び試験の実施の基準に関する省令の一部を改正する省令
本日の内容 1. はじめに 2. PMDA について 3. 医療機器の審査 相談体制について 4. おわりに
 初めての医療機器開発 ( 初級編 ) ~ 審査のしくみ ~ 独立行政法人医薬品医療機器総合機構 (PMDA) 医療機器審査第二部穴原玲子 本日の内容 1. はじめに 2. PMDA について 3. 医療機器の審査 相談体制について 4. おわりに 1. はじめに 医療機器を開発するにあたって どのようなものを医療機器と呼ぶのか? 医療機器を開発するとはどういうことか? 医療機器を上市するためにはどうしたらいいか?
初めての医療機器開発 ( 初級編 ) ~ 審査のしくみ ~ 独立行政法人医薬品医療機器総合機構 (PMDA) 医療機器審査第二部穴原玲子 本日の内容 1. はじめに 2. PMDA について 3. 医療機器の審査 相談体制について 4. おわりに 1. はじめに 医療機器を開発するにあたって どのようなものを医療機器と呼ぶのか? 医療機器を開発するとはどういうことか? 医療機器を上市するためにはどうしたらいいか?
3. 実施時期平成 29 年 4 月 3 日より本件改修後のQMS 調査申請書の作成及び機構受付が可能となります 4. その他 本改修により承認申請書とQMS 調査申請書の同時申請が可能となるのは 両申請書をDW APで作成した場合に限ります (FD 申請ソフトによる申請の場合は同時申請できません
 事務連絡平成 29 年 3 月 17 日 一般社団法人日本医療機器産業連合会御中 独立行政法人医薬品医療機器総合機構審査業務部 承認申請書及び QMS 調査申請書の同時申請にかかる DWAP の改修について 今般 医療機器 WEB 申請プラットフォーム ( 以下 DWAP という ) を活用した医療機器製造販売承認申請書又は外国製造医療機器製造販売承認申請書 ( 一部変更承認申請書を含む 以下 承認申請書
事務連絡平成 29 年 3 月 17 日 一般社団法人日本医療機器産業連合会御中 独立行政法人医薬品医療機器総合機構審査業務部 承認申請書及び QMS 調査申請書の同時申請にかかる DWAP の改修について 今般 医療機器 WEB 申請プラットフォーム ( 以下 DWAP という ) を活用した医療機器製造販売承認申請書又は外国製造医療機器製造販売承認申請書 ( 一部変更承認申請書を含む 以下 承認申請書
製造販売後調査事務手続き等 について
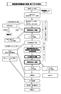 製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
製造販売後調査の実施 終了までの流れ 調査申し込み希望 調査面談シートをご提出下さい 事前予約後臨床研究センターへの訪問 不 研究的要素を含む場合 倫理委員会 実施不可 不 : 実施不可 1 年毎に実施状況報告書提出 場合によっては途中精算可能 契約期間が 1 年以上の場 臨床研究センター訪問ヒアリング資料の提出 手続きの説明 薬事委員会にて審議 契約書締結後 実施 実施要綱等変更の発生登録期間 契約期間延長希望症例追加希望
(2) 開発戦略に係る相談以下の留意点を踏まえた上で 本相談を申し込んでください 開発戦略に係る相談は より効率的かつ効果的な再生医療等製品の開発戦略を練ることを目的として 機構と相談者がその時点で得られている試験成績 科学的見地に基づき 予想される開発の結果を想定した上で 当該再生医療等製品の開発
 ( 別添 8) 対面助言のうち 再生医療等製品の治験相談 ( 再生医療等製品の先駆け総合評価相談 事前評価相談 対面助言事後相談及び信頼性基準適合性調査相談を除く ) に関する実施要綱 1. 対面助言の区分及び内容本実施要綱の対象とする対面助言の区分及び内容については 本通知の別紙 5 のとおりです なお 拡大治験の実施が予想される再生医療等製品の開発においては 可能な限り 主たる治験に関する臨床試験デザインの相談を利用することを勧めます
( 別添 8) 対面助言のうち 再生医療等製品の治験相談 ( 再生医療等製品の先駆け総合評価相談 事前評価相談 対面助言事後相談及び信頼性基準適合性調査相談を除く ) に関する実施要綱 1. 対面助言の区分及び内容本実施要綱の対象とする対面助言の区分及び内容については 本通知の別紙 5 のとおりです なお 拡大治験の実施が予想される再生医療等製品の開発においては 可能な限り 主たる治験に関する臨床試験デザインの相談を利用することを勧めます
PowerPoint プレゼンテーション
 第 1 5 回地域医療構想に関する W G 平成 3 0 年 7 月 2 0 日 資料 2-1 1. 地域医療構想調整会議の活性化に向けた方策 ( その 3) 1 公立 公的病院等を中心とした機能分化 連携の推進について 2 地元に密着した 地域医療構想アドバイザー について 1 経済財政運営と改革の基本方針 2018 ( 平成 30 年 6 月 15 日閣議決定 )[ 抜粋 ] 4. 主要分野ごとの計画の基本方針と重要課題
第 1 5 回地域医療構想に関する W G 平成 3 0 年 7 月 2 0 日 資料 2-1 1. 地域医療構想調整会議の活性化に向けた方策 ( その 3) 1 公立 公的病院等を中心とした機能分化 連携の推進について 2 地元に密着した 地域医療構想アドバイザー について 1 経済財政運営と改革の基本方針 2018 ( 平成 30 年 6 月 15 日閣議決定 )[ 抜粋 ] 4. 主要分野ごとの計画の基本方針と重要課題
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠 50mg 医薬品リスク管理計画書 (RMP) の概要 有効成分 タペンタ 錠 100mg 製造販売業者 ヤンセンファーマ株式会社 薬効分類 821 提出年月 平成 30 年
 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
概要 PMDAにおける次世代審査 相談体制の構築 データ標準の利用 承認申請時の電子データ提出に関する基本的考え方 ( 案 ) について パイロット実施について CDISC 利用に関する今後の検討と展望 2014/05/16 CDISC 概説コース 2
 CDISC 概説コース PMDA の取り組みと 日本における CDISC の利用について 独立行政法人医薬品医療機器総合機構次世代審査等推進室 / スペシャリスト ( 生物統計担当 ) 安藤友紀 CDISC 2012 1 概要 PMDAにおける次世代審査 相談体制の構築 データ標準の利用 承認申請時の電子データ提出に関する基本的考え方 ( 案 ) について パイロット実施について CDISC 利用に関する今後の検討と展望
CDISC 概説コース PMDA の取り組みと 日本における CDISC の利用について 独立行政法人医薬品医療機器総合機構次世代審査等推進室 / スペシャリスト ( 生物統計担当 ) 安藤友紀 CDISC 2012 1 概要 PMDAにおける次世代審査 相談体制の構築 データ標準の利用 承認申請時の電子データ提出に関する基本的考え方 ( 案 ) について パイロット実施について CDISC 利用に関する今後の検討と展望
薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リ
 薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リスク管理計画の実施状況及び得られた結果の評価に関する報告の様式 提出等の取扱いについては 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について
薬生安発 0302 第 1 号 平成 30 年 3 月 2 日 各都道府県衛生主管部 ( 局 ) 長殿 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について の一部改正について 再審査期間中の新医薬品以外の医薬品の医薬品リスク管理計画の実施状況及び得られた結果の評価に関する報告の様式 提出等の取扱いについては 医薬品リスク管理計画の実施に基づく再審査期間終了後の評価報告について
Microsoft Word (発出版)適正使用通知案(冷凍アブレーション)
 医政経発 0219 第 1 号薬食審査発 0219 第 1 号薬食安発 0219 第 1 号 平成 26 年 2 月 19 日 特定非営利活動法人日本小児循環器学会理事長殿 厚生労働省医政局経済課長 厚生労働省医薬食品局審査管理課長 厚生労働省医薬食品局安全対策課長 医療機器 Arctic Front Advance 冷凍アブレーションカテーテル 等の適正使用について 平素より厚生労働行政に御理解と御協力を賜り誠にありがとうございます
医政経発 0219 第 1 号薬食審査発 0219 第 1 号薬食安発 0219 第 1 号 平成 26 年 2 月 19 日 特定非営利活動法人日本小児循環器学会理事長殿 厚生労働省医政局経済課長 厚生労働省医薬食品局審査管理課長 厚生労働省医薬食品局安全対策課長 医療機器 Arctic Front Advance 冷凍アブレーションカテーテル 等の適正使用について 平素より厚生労働行政に御理解と御協力を賜り誠にありがとうございます
4.7.4 プロセスのインプットおよびアウトプット (1) プロセスへのインプット情報 インプット情報 作成者 承認者 備 考 1 開発に関するお客様から お客様 - の提示資料 2 開発に関する当社収集資 リーダ - 料 3 プロジェクト計画 完了報 リーダ マネージャ 告書 ( 暫定計画 ) 4
 サンプル : プロジェクト管理規定 4.7 プロジェクト立ち上げ 4.7.1 目的 本プロセスはリーダ主導で プロジェクト体制の確立とプロジェクト内容 分担 業務指示 プロジェクト目標 担当者別プロジェクト目標を開発メンバに周知徹底することによって 組織としての意識統一を図るとともに開発プロセスをスムーズに立ち上げることを目的とする 4.7.2 このプロセスにかかわる人物の役割と責務 部門 略記 参加
サンプル : プロジェクト管理規定 4.7 プロジェクト立ち上げ 4.7.1 目的 本プロセスはリーダ主導で プロジェクト体制の確立とプロジェクト内容 分担 業務指示 プロジェクト目標 担当者別プロジェクト目標を開発メンバに周知徹底することによって 組織としての意識統一を図るとともに開発プロセスをスムーズに立ち上げることを目的とする 4.7.2 このプロセスにかかわる人物の役割と責務 部門 略記 参加
P00041
 P14004 エネルギー 環境新技術先導プログラム 基本計画 イノベーション推進部 1. 制度の目的 目標 内容 (1) 制度の目的 1 政策的な重要性平成 25 年 9 月 総合科学技術会議において 攻めの温暖化外交戦略を組み立てるべく 環境エネルギー技術革新計画 が改定され この中で 新たな革新技術のシーズを発掘していくことの重要性 や ハイリスクだがコストの大幅な引下げや飛躍的なエネルギー効率の向上を達成する創造的な技術を創出する
P14004 エネルギー 環境新技術先導プログラム 基本計画 イノベーション推進部 1. 制度の目的 目標 内容 (1) 制度の目的 1 政策的な重要性平成 25 年 9 月 総合科学技術会議において 攻めの温暖化外交戦略を組み立てるべく 環境エネルギー技術革新計画 が改定され この中で 新たな革新技術のシーズを発掘していくことの重要性 や ハイリスクだがコストの大幅な引下げや飛躍的なエネルギー効率の向上を達成する創造的な技術を創出する
PowerPoint プレゼンテーション
 地域医療構想調整会議について 資料 1-2 医療法の規定 第 30 条の 14 都道府県は 構想区域その他の当該都道府県の知事が適当と認める区域ごとに 診療に関する学識経験者の団体その他の医療関係者 医療保険者その他の関係者との協議の場を設け 関係者との連携を図りつつ 医療計画において定める将来の病床数の必要量を達成するための方策その他の地域医療構想の達成を推進するために必要な事項について協議を行うものとする
地域医療構想調整会議について 資料 1-2 医療法の規定 第 30 条の 14 都道府県は 構想区域その他の当該都道府県の知事が適当と認める区域ごとに 診療に関する学識経験者の団体その他の医療関係者 医療保険者その他の関係者との協議の場を設け 関係者との連携を図りつつ 医療計画において定める将来の病床数の必要量を達成するための方策その他の地域医療構想の達成を推進するために必要な事項について協議を行うものとする
(別添様式)
 未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名 要望された医薬品 ユーシービージャパン株式会社要望番号 Ⅱ-254.2 成分名 Lacosamide ( 一般名 ) Vimpat 販売名 未承認薬 適応 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) 未承認薬 適応外薬 他の抗てんかん薬で十分な効果が認められないてんかん患者の部分発作
未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名 要望された医薬品 ユーシービージャパン株式会社要望番号 Ⅱ-254.2 成分名 Lacosamide ( 一般名 ) Vimpat 販売名 未承認薬 適応 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) 未承認薬 適応外薬 他の抗てんかん薬で十分な効果が認められないてんかん患者の部分発作
がんのウイルス療法とは がんのウイルス療法とは がん細胞のみで増えることができるウイルスを感染させ ウイルスが直接がん細胞を破壊する治療法です ウイルス療法では 遺伝子工学技術を用いてウイルスゲノムを 設計 して がん細胞ではよく増えても正常細胞では全く増えないウイルスを人工的に造って臨床に応用しま
 [PRESS RELEASE] 2018 年 8 月 2 日 東京大学医科学研究所附属病院 悪性胸膜中皮腫のウイルス療法を開始 ~ 抗がんウイルス G47Δ を用いた初の胸腔内投与 ~ 東京大学医科学研究所附属病院では 脳腫瘍外科教授藤堂具紀を総括責任者として 悪性胸膜中皮腫に対するウイルス療法の臨床試験を開始します ウイルス療法とは がん細胞だけで増殖するように人工的に改変したウイルスを使う新しいがん治療法で
[PRESS RELEASE] 2018 年 8 月 2 日 東京大学医科学研究所附属病院 悪性胸膜中皮腫のウイルス療法を開始 ~ 抗がんウイルス G47Δ を用いた初の胸腔内投与 ~ 東京大学医科学研究所附属病院では 脳腫瘍外科教授藤堂具紀を総括責任者として 悪性胸膜中皮腫に対するウイルス療法の臨床試験を開始します ウイルス療法とは がん細胞だけで増殖するように人工的に改変したウイルスを使う新しいがん治療法で
<4D F736F F F696E74202D2097D58FB08E8E8CB1838F815B834E F197D58FB E96D8816A66696E616C CF68A4A2E >
 再生医療等製品の非臨床安全性評価の考え方 ex vivo 遺伝子治療を中心に 独立行政法人医薬品医療機器総合機構 (PMDA) 再生医療製品等審査部 真木一茂 様式 1-B 第 24 回日本遺伝子細胞治療学会学術集会 CO I 開示 発表者名 : 真木一茂 演題発表に関連し 開示すべき CO I 関係にある企業などはありません 2 1 本日の話 1.Ex vivo 遺伝子治療について 2. 治験開始に必要な非臨床試験
再生医療等製品の非臨床安全性評価の考え方 ex vivo 遺伝子治療を中心に 独立行政法人医薬品医療機器総合機構 (PMDA) 再生医療製品等審査部 真木一茂 様式 1-B 第 24 回日本遺伝子細胞治療学会学術集会 CO I 開示 発表者名 : 真木一茂 演題発表に関連し 開示すべき CO I 関係にある企業などはありません 2 1 本日の話 1.Ex vivo 遺伝子治療について 2. 治験開始に必要な非臨床試験
Microsoft PowerPoint - 【e-Rad設定】研究者用(H30年度)二次新システム未対応
 厚生労働科学研究費補助金の応募に係る 府省共通研究開発管理システム (e-rad) への 入力方法について < 注意事項 > e-radは平成 30 年 2 月 28 日 ( 水 ) から 新システムに移行しました ユーザビリティ改善の観点から 画面デザイン メニュー構成等が全面的に刷新されました 新システムのマニュアルは e-radポータルサイトに掲載しています 主な変更点についても記載しておりますので
厚生労働科学研究費補助金の応募に係る 府省共通研究開発管理システム (e-rad) への 入力方法について < 注意事項 > e-radは平成 30 年 2 月 28 日 ( 水 ) から 新システムに移行しました ユーザビリティ改善の観点から 画面デザイン メニュー構成等が全面的に刷新されました 新システムのマニュアルは e-radポータルサイトに掲載しています 主な変更点についても記載しておりますので
(1) 書面による助言書面による助言は 上記 2. の対面助言の日程調整により対面助言を受けることが決定した品目のうち相談者の事前の了解が得られた場合に行います 書面による助言を希望する場合には 対面助言日程調整依頼書及び日程調整結果を受けて提出する 医薬品対面助言申込書 ( 業務方法書実施細則の様
 ( 別添 1) 対面助言のうち 新医薬品及び生物学的製剤等 1) の治験相談 ( 新医薬品の先駆け総合評価相談 新医薬品の事前評価相談 新医薬品の優先審査品目該当性相談 ファーマコゲノミクス バイオマーカー相談 新医薬品の対面助言事後相談 新医薬品の申請電子データ提出確認相談 医薬品 GCP/GLP/GPSP 相談及び医薬品信頼性基準適合性調査相談を除く ) に関する実施要綱 1. 対面助言の区分及び内容本実施要綱の対象とする対面助言の区分及び内容については
( 別添 1) 対面助言のうち 新医薬品及び生物学的製剤等 1) の治験相談 ( 新医薬品の先駆け総合評価相談 新医薬品の事前評価相談 新医薬品の優先審査品目該当性相談 ファーマコゲノミクス バイオマーカー相談 新医薬品の対面助言事後相談 新医薬品の申請電子データ提出確認相談 医薬品 GCP/GLP/GPSP 相談及び医薬品信頼性基準適合性調査相談を除く ) に関する実施要綱 1. 対面助言の区分及び内容本実施要綱の対象とする対面助言の区分及び内容については
別紙様式 (Ⅴ)-1-3で補足説明している 掲載雑誌は 著者等との間に利益相反による問題が否定できる 最終製品に関する研究レビュー 機能性関与成分に関する研究レビュー ( サプリメント形状の加工食品の場合 ) 摂取量を踏まえた臨床試験で肯定的な結果が得られている ( その他加工食品及び生鮮食品の場合
 別紙様式 (Ⅴ)-1 機能性の科学的根拠に関する点検表 1. 製品概要商品名アサヒ凹茶 ( ぼこちゃ ) 機能性関与成分名りんごポリフェノール ( りんご由来プロシアニジンとして ) 表示しようとする本品には りんごポリフェノール ( りんご由来プロシア機能性ニジンとして ) が含まれるので 体脂肪が気になる方のお腹の脂肪を減らす機能があります 2. 科学的根拠 臨床試験及び研究レビュー共通事項 (
別紙様式 (Ⅴ)-1 機能性の科学的根拠に関する点検表 1. 製品概要商品名アサヒ凹茶 ( ぼこちゃ ) 機能性関与成分名りんごポリフェノール ( りんご由来プロシアニジンとして ) 表示しようとする本品には りんごポリフェノール ( りんご由来プロシア機能性ニジンとして ) が含まれるので 体脂肪が気になる方のお腹の脂肪を減らす機能があります 2. 科学的根拠 臨床試験及び研究レビュー共通事項 (
国立仙台病院受託研究取扱規程
 独立行政法人国立病院機構仙台医療センター受託研究取扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構仙台医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程の定めるところによる 2 契約 経理及び書式等については 原則として独立行政法人国立病院機構
独立行政法人国立病院機構仙台医療センター受託研究取扱規程 ( 通則 ) 第 1 条独立行政法人国立病院機構仙台医療センター ( 以下 当院 という ) における国及びそれに準じる機関以外の者 ( 以下 依頼者 という ) から委託を受けて行う研究 ( 以下 受託研究 という ) の取扱いについては この規程の定めるところによる 2 契約 経理及び書式等については 原則として独立行政法人国立病院機構
