|
|
|
- あきお つねざき
- 5 years ago
- Views:
Transcription
1
2 非臨床試験の概括評価の目次 頁 2.4. 非臨床試験の概括評価... ~xr1i 非臨床試験概略... ~xr2i 薬理試験... ~xr3i 効力を裏付ける薬理試験... ~xr4i 副次的薬理試験... ~xr5i 安全性薬理試験... ~xr6i 薬物動態試験... ~xr7i 吸収... ~xr8i 分布... ~xr9i 代謝... ~xr10i 排泄... ~xr11i 薬物動態学的薬物相互作用... ~xr12i 毒性試験... ~xr13i 単回投与毒性試験... ~xr14i 反復投与毒性試験... ~xr15i 遺伝毒性試験... ~xr16i がん原性試験... ~xr17i 生殖発生毒性試験... ~xr18i 代謝物および不純物の毒性... ~xr19i 総括および結論... ~xr20i 参考文献一覧... ~xr21i 12
3 2.4 の略号等一覧 略語 ( 略称 ) 定義 省略されていない名称 5AR 5α-reductase(5α 還元酵素 ) AUC Area under the concentration-time curve( 血清中濃度 - 時間曲線下面積 ) 3β-HSD 3β-hydroxy- 5 -steroid dehydrogenase/3-keto- 5 -steroid isomerase C 27 -HSD 3β-hydroxy- 5 -C 27 -steroid oxido-reductase CYP Cytochrome P450( チトクローム P450) C 24 Concentration at 24 hours after dosing( 投与 24 時間後の血清中濃度 ) C max Maximum observed drug concentration in blood( 最高血清中濃度 ) C ss Concentration at steady state( 定常状態における血清中濃度 ) DHT Dihydrotestosterone( ジヒドロテストステロン ) ED 30 前立腺重量を 30% 低下させる用量 GLP Good Laboratory Practice( 医薬品の安全性に関する非臨床試験の実施の基準に関す る省令 ) HPLC High Performance Liquid Chromatography( 高速液体クロマトグラフィー ) HPLC/MS 高速液体クロマトグラフ- 質量分析法 IC 50 50% inhibitory concentration( 酵素活性を 50% 阻害する薬物濃度 ) k 3 /Ki 見かけの二次反応速度定数 Ki 5AR と被験物質の結合反応の第 1 ステップの阻害定数 LH Luteinising Hormone( 黄体形成ホルモン ) t 1/2 Apparent half life on terminal phase ( 消失半減期 ) t max Time to maximum observed drug concentrations in blood( 最高血清中濃度到達時間 )
4 2.4. 非臨床試験の概括評価 非臨床試験概略デュタステリドは 5α 還元酵素 (5α-reductase 以下 5AR) 阻害を作用機序とする新規の前立腺肥大症治療薬である 非臨床試験ではデュタステリドの薬理 薬物動態および毒性評価を行った なお 安全性薬理試験の一部および毒性試験は GLP に準拠して実施した 効力を裏付ける薬理試験として in vitro 試験および in vivo 試験における 5AR 阻害作用 前立腺におけるジヒドロテストステロン (DHT) 濃度の低下作用 および前立腺重量の低下作用に関する試験を実施した また in vitro 試験における代謝物の 5AR 阻害作用に関する試験 ならびに副次的薬理試験として 各種受容体 酵素 イオンチャネルなどに対する親和性に関する試験を実施した さらに 安全性薬理試験として 中枢神経系 心血管系および呼吸系に及ぼす影響を検討する試験を実施した 薬物動態試験としてデュタステリドの吸収 分布 代謝および排泄を毒性試験で用いたマウス ラット イヌ ウサギおよびサルにより検討した 試験はおもに臨床投与経路である経口投与で 一部の試験では静脈内および経皮投与も実施した なお 本申請の適応症は前立腺肥大症であり 男性のみの適用で女性に対しては禁忌であることから 動物での胎盤通過性試験および乳汁移行試験は実施しなかった 毒性試験として 単回および反復経口投与毒性 遺伝毒性 がん原性 生殖発生毒性ならびに代謝物および不純物の毒性について検討した 薬理試験効力を裏付ける薬理試験として 5AR 阻害作用のプロファイルを明らかにするため 組換えヒト 5AR を含む各種動物由来の 5AR に対する阻害作用を in vitro 試験において検討し in vivo での 5AR 阻害作用を確認するため 去勢ラットにおけるテストステロン投与後の前立腺組織中 DHT 濃度に及ぼす影響を検討した また 前立腺肥大症治療薬としての効力を確認するため 前立腺重量に及ぼす影響を検討し 前立腺重量の低下作用が DHT 濃度の低下を伴うものであることを確認するため 前立腺組織中および血清中の DHT およびテストステロン濃度を測定した さらに デュタステリドのヒト血清中代謝物に薬理活性があるか否かを検討するため 5AR 阻害作用を in vitro 試験により検討した 副次的薬理試験として 5AR 阻害作用以外の薬理活性を示すか否かを確認するために ステロイド代謝酵素および胆汁酸合成系酵素に対する影響を検討し さらに 各種受容体 イオンチャネル モノアミン再取り込み部位および細胞内情報伝達系に関与する酵素あるいは受容体への親和性を in vitro 試験により検討した 安全性薬理試験として 中枢神経系 心血管系および呼吸系に及ぼす影響を検討した 効力を裏付ける薬理試験デュタステリドは in vitro 試験においてヒト 1 型および 2 型 5AR に対して時間依存的な阻害作用を有し その阻害作用の指標である k 3 /Ki 値はフィナステリドのそれぞれ約 45 倍および約 2.5 倍であった また デュタステリドのヒト 2 型 5AR に対する阻害作用はヒト 1 型 p. 1
5 5AR に対する作用の約 4 倍であった ( 参照 ) このことから デュタステリドは 1 型および 2 型 5AR を阻害し いずれのアイソザイムに対する阻害作用もフィナステリドより強力であることが示唆された また デュタステリドは経口投与により 外因性に投与されたテストステロンの DHT への変換を前立腺組織において阻害し デュタステリドの 5AR 阻害作用はフィナステリドよりも長時間持続したことから ( 参照 ) in vivo においてもデュタステリドは 5AR を阻害することが示された ラットにデュタステリド 2mg/kg を経口投与すると 7.49 時間で t max となり 15.8 時間の t 1/2 で消失するのに対し ( 参照 ) フィナステリド 5mg/kg を経口投与した場合には 2.0 時間で t max となり 0.72 時間の t 1/2 で消失することが報告されており [ 石井, 1994] in vivo 試験におけるデュタステリドの 5AR 阻害作用がフィナステリドより長く持続したことは 血中濃度推移の違いに起因する可能性が示唆された デュタステリドはラットに反復経口投与することにより前立腺重量を低下させ その作用の強さは ED 30 値 ( 前立腺重量を 30% 低下させる用量 ) の比較によりフィナステリドの約 20 倍であることが示された ( 参照 ) In vitro 試験におけるラット 1 型および 2 型 5AR に対するデュタステリドの阻害活性は フィナステリドのそれぞれ約 20 倍および約 10 倍強力であり ( 参照 ) in vivo 試験における前立腺重量低下作用の違いは in vitro 試験での 5AR 阻害活性の差に起因すると考えられた また 前立腺には 1 型および 2 型 5AR の両アイソザイムの存在が報告されており [Normington, 1992; Torres, 2003] デュタステリドはフィナステリドと異なり両アイソザイムに対して同程度の阻害作用を示すことから より強力な前立腺重量低下作用を発現した可能性も考えられた さらに デュタステリド投与ラットの前立腺組織中 DHT 濃度は低下しており ( 参照 ) 前立腺重量の低下は前立腺組織における DHT 濃度の低下に起因する可能性が示唆された なお 前立腺重量の低下作用を示したものの 精巣 肝臓および副腎重量に対しては影響を示さなかった ( 参照 ) また デュタステリドは去勢ラットにおけるテストステロン誘発前立腺重量増加も抑制した ( 参照 ) これらのことから デュタステリドは 1 型および 2 型 5AR を阻害し 前立腺中の DHT 濃度を低下させることにより 前立腺重量を低下させると考えられた In vitro 試験において デュタステリドのヒト血清中主代謝物である 4 - 水酸化体 6- 水酸化体および 1,2- 二水素化体 ( 参照 ) は 5AR 阻害作用を示した 4 - 水酸化体の活性はデュタステリドの約 1/10 の活性であり 6- 水酸化体の活性はデュタステリドと同程度であった これらの代謝物はデュタステリド同様 時間依存的な 5AR 阻害作用を示した また 1,2- 二水素化体は 5AR に対して時間依存的な阻害作用を示さなかったものの デュタステリドと同程度の IC 50 値で抑制した ( 参照 ) 副次的薬理試験デュタステリドは ステロイド代謝酵素である 3β-hydroxy- 5 -steroid dehydrogenase/3-keto- 5 -steroid isomerase(3β-hsd) および胆汁酸合成系酵素の一つである 3β-hydroxy- 5 -C 27 - steroid oxido-reductase(c 27 -HSD) に対して ほとんど阻害作用を示さなかった ( 参照 ) また デュタステリドはアンドロゲン エストロゲンおよびプロゲステロンの 3 種 p. 2
6 の性ホルモン受容体への親和性を示さず 37 種の各種受容体 イオンチャネル モノアミ ン再取り込み部位および細胞内情報伝達系に関与する酵素あるいは受容体に対しても親和性を示さなかった ( および 参照 ) 安全性薬理試験デュタステリドは中枢神経系 心血管系および呼吸系に対して in vivo 試験では影響を示さなかった イヌのプルキンエ線維を用いた検討で 3.3µg/mL で活動電位持続時間の短縮および最大脱分極速度の低下が認められた ( 参照 ) 薬物動態試験デュタステリドの薬物動態試験を毒性試験に用いたマウス ラット イヌ ウサギおよびサルで実施した 試験はおもに臨床投与経路である経口投与で 一部の試験は静脈内および経皮投与で実施した 血清中デュタステリド濃度は UV 検出器または MS 検出器を装備した HPLC 法で測定した 代謝物の分析はおもに HPLC/MS/MS 法で 一部の試験では radio- HPLC 法で行った また 動物での代謝物をヒトと比較する試験では 19 F-NMR 1 H-NMR HPLC/MS 法および HPLC/MS/MS 法を用いた ( 参照 ) 吸収マウスに本薬の 1~500mg/kg ラットに 2~500mg/kg およびイヌに 0.5~50mg/kg を単回経口投与したときの血清中未変化体の t max はマウスで 8~12 時間 ラットで 7.49~31.2 時間 イヌで 4.0~8.7 時間であり t 1/2 はマウスで 42.5~62.6 時間 ラットで 15.8~35.9 時間 イヌで 52.3~151 時間であったことから 本薬の吸収および消失は緩やかであると考えられた ラットに 2mg/kg イヌに 0.5mg/kg を経口投与したときのバイオアベイラビリティはそれぞれ 58 および 2.38% であったが ラットに 500mg/kg イヌに 50mg/kg を経口投与したときのバイオアベイラビリティはそれぞれ 7 および 0.80% と投与量増加に伴い低下した また ラットに 1mg/kg イヌに 0.1mg/kg を単回静脈内投与したときの血清クリアランスはそれぞれ 348 および 5.00mL/hr/kg 分布容積はそれぞれ 6055 および 639mL/kg であった マウスに 1 ~500mg/kg/ 日を 82 日間 ラットに 0.5~500mg/kg/ 日を 30~90 日間 イヌに 0.5~50mg/kg/ 日を 26 週間経口投与したときの血清中未変化体濃度は投与量増加の割合を下回って増加し 薬物動態の非線型が確認されたが 本薬が難水溶性化合物 (2.3.S.1.3 参照 ) であり 高用量群では消化管内で完全に溶解しなかったことに起因すると考えられた いずれの動物種でも低いクリアランスおよび長い半減期に起因した蓄積性が確認された 雌ラットの曝露量は雄よりも高く 性差がみられたが マウスおよびイヌで性差は確認されなかった また ウサギに 0.1~40mg/kg を単回経皮投与したときの血清中には未変化体が検出されたことから 本薬はヒトでも皮膚を介して体内に吸収されると考えられた ( 参照 ) 分布有色マウスに 14 C-デュタステリドの 3.3mg/kg/ 日を単回および 7 日間経口投与したときの放射能は広く組織に分布した 単回経口投与後の放射能は大部分の組織で投与 8 時間後に最 p. 3
7 大となり その後 緩やかに体内から消失した 反復経口投与後の組織内放射能は副腎髄質および消化管内容物などで単回投与よりも低くなり ほとんどの組織で単回投与の約 4 倍以内であったが 精巣 骨 水晶体およびブドウ膜の一部の時点では 6 倍以上であった ラットに 3 H-デュタステリドの 2mg/kg を単回経口投与したときの放射能はマウスと同様に広く組織に分布したが 投与 14 日後にはいずれの組織においても放射能は検出されなかった ( 参照 ) また ラット イヌおよびヒトでの血漿蛋白結合率はいずれも 99.5% 超であり 雄ラットを除いて 本薬は血球中よりも血漿中に分布した ( 参照 ) 代謝ラットおよびイヌに単回経口投与したときの血清および糞中にはおもに未変化体が検出された 反復投与後のヒト糞中にはおもに 4 種類の代謝物が確認されたことから 動物でも反復投与後の代謝物を検討した その結果 ラットでもヒト糞中に検出された 4 種類の代謝物が確認された マウス ラットおよびイヌの血清中にはヒト血清中と同様にアニリン環の 4 位が水酸化された 4 - 水酸化体がおもに検出され ラット血清中ではステロイド環の 6 位が水酸化された 6- 水酸化体 マウス ラットおよびイヌの血清中にはステロイド環の 1,2 位が水素化された 1,2- 二水素化体 アニリン環の 4 位およびステロイド環の 6 位が水酸化された 6,4 - 二水酸化体 もわずかに検出されたことから 本薬の代謝に種差はないものと考えられた ( 参照 ) 雌ラットに 30mg/kg/ 日 雄ラットに 500mg/kg/ 日 雌雄イヌに 50mg/kg/ 日まで 26 週間経口投与したときの肝薬物代謝酵素に誘導はみられなかった ( 参照 ) 排泄ラットに 14 C-デュタステリドの 10mg/kg および 3 H-デュタステリドの 13mg/kg イヌに 14 C-デュタステリドの 0.5 および 50mg/kg を単回経口投与したときの放射能は大部分 ( それぞれ約 75 および 79~86%) が糞中に排泄され 放射能の主排泄経路は糞であることが示された また 胆管カニュレーション処置したラットに 14 C-デュタステリドの 1mg/kg イヌに 0.1mg/kg を単回静脈内投与したときの放射能は胆汁中にそれぞれ 32.2 および 24.2% 排泄された また 胆管カニュレーション処置したラットおよびイヌに静脈内投与したときの糞中にそれぞれ 28.0 および 65.6% の放射能が検出されたことから 放射能は消化管分泌すると考えられた ( 参照 ) 薬物動態学的薬物相互作用イヌにデュタステリドとカルシウムチャネル遮断薬であるベラパミルを併用投与した際にデュタステリドの薬物動態は併用による影響を受けなかった ( 参照 ) 毒性試験単回および反復投与毒性 in vivo 遺伝毒性 がん原性 生殖発生毒性試験はマウス ラット ウサギまたはイヌを用い 臨床適用経路である経口投与により実施した また ヒト精 p. 4
8 液を介して妊婦が曝露された際の胚 胎児発生に対する影響を検討するため サルを用いて静脈内投与により試験を実施した 単回投与毒性試験マウス ( 参照 ) およびラット ( 参照 ) における単回経口投与時の概略の致死量はそれぞれ 2000 および 1500mg/kg 超であった イヌに 8 日間反復経口投与した際の本薬の急性毒性を評価した結果 ( 参照 ) 概略の致死量は 100mg/kg/ 日超であった 反復投与毒性試験本薬をラットに 26 週間まで ( および 参照 ) イヌに 53 週間まで反復経口投与した結果 ( および 参照 ) 投与 2 週以降よりラット ( 雄 500mg/kg/ 日 雌 100mg/kg/ 日 ) およびイヌ ( 10mg/kg/ 日 ) ともに自発運動低下 協調運動性失調 振戦あるいは痙攣などの中枢神経系の症状が観察され 切迫屠殺例も散見された これら中枢神経系の症状は可逆的であり 関連する器官 組織の病理組織学的変化を伴わず 高曝露時に ( ラット :17000ng/mL 以上 イヌ :12600ng/mL 以上 ) 観察されたことから 非特異的反応と考えられた 本薬の薬理作用による DHT 低下に起因すると考えられる雄性副生殖器の変化が 雄ラットの受胎能試験 ( 参照 ) を含むすべての反復投与試験で観察され ( 表 ) ラットの 0.05mg/kg/ 日以上およびイヌの 0.5mg/kg/ 日以上で前立腺および精巣上体の萎縮がみられ ラットでは精嚢萎縮も認められた ラットおよびイヌの前立腺ならびにイヌの精巣上体 (50mg/kg/ 日 ) の変化以外については 休薬により回復性あるいは回復傾向を示した ラットおよびイヌともに 精巣には特記すべき変化は認められなかった 雌では ラットの 2.5mg/kg/ 日以上で子宮重量の低値傾向または低値 10mg/kg/ 日以上で卵巣の重量低値および萎縮 卵胞嚢胞数および発情間期動物数の増加がみられ イヌでは 0.5mg/kg/ 日以上で黄体期への移行動物数の増加ならびに乳腺発達および分泌物増加 3mg/kg/ 日以上で子宮粘膜上皮空胞化 内膜過形成および嚢胞形成が認められた また イヌでは 0.5mg/kg/ 日以上で可逆的な下垂体 ( 前葉色素嫌性細胞肥大 ) 甲状腺 ( 重量増加 C 細胞過形成あるいは濾胞上皮細胞空胞化 ) および副腎 ( 皮質細胞肥大およびリポフスチン様色素沈着 ) の変化が認められた ( 表 ) 内分泌器官に対する影響は 4,5,3-oxo 構造を有する糖質 鉱質コルチコイド プロゲステロンおよびアンドロゲンなどのステロイドホルモンも 5AR の基質となることから [Russell, 1994] 高濃度の本薬の長期曝露によるステロイド合成組織に対する影響および視床下部 - 下垂体 - 性腺 / 副腎軸に対する影響による生理的変動に適応した二次的変化と考えられた 薬理作用に起因する生殖器の変化および軽度で可逆的な内分泌器官の変化以外に特記すべき所見が認められなかった用量を無毒性量とすると 長期反復投与毒性試験における雄ラットおよび雄イヌの無毒性量はそれぞれ 50 および 3mg/kg/ 日と推定された p. 5
9 表 雄ラットおよび雄イヌに認められた薬理作用による直接的および二次変化と その発現用量 動物種 ラット イヌ 投与期間 5 週間 26 週間 31 週間 26 週間 53 週間 ( 雄受胎能試験 ) 投与量 (mg/kg/ 日 ) 2, 10, , 50, , 10, 50, , 5, , 3, 50 a 前立腺萎縮 精嚢萎縮 該当せず 該当せず 精巣上体萎縮 下垂体色素嫌性 - - ND 細胞肥大 甲状腺重量増加 - - ND C 細胞過形成等 副腎細胞肥大等 - - ND a: 投与 43 日より 10mg/kg/ 日に減量 ND: 検討せず -: 対照群との間に有意な差なし萎縮 : 重量低値 小型化 上皮萎縮および分泌物減少含む ラットおよびイヌともに 反復経口投与により曝露量は概して投与量増加の割合を下回って増加し ラットでは雌の方が高い曝露量を示したが イヌでは明らかな性差は認められなかった また 本薬は反復投与により血清中未変化体は蓄積性を示すが 投与 4 週までには定常状態に達することから ラットについては定常状態における血清中未変化体濃度 (C ss ) イヌについては 370 日投与後 24 時間の血清中未変化体濃度 (C 24 ) と 臨床用量 (0.5mg/ 日 ) をヒト ( 日本人前立腺肥大症患者 ) に反復投与した際の血清中濃度 (C ss : 約 45ng/mL) を比較した その結果 ( 表 ) 長期反復投与における雄ラットおよび雄イヌの無毒性量での曝露量は 臨床曝露量のそれぞれ約 16 および 104 倍に相当した 表 長期反復経口投与試験における動物の曝露量とヒト曝露量の比較 動物種 性別 投与量 (mg/kg/ 日 ) C 24 (ng/ml) a ヒト C ss 比 # ラット (26 週間 ) # # イヌ 50/10 b (53 週間 ) # /10 b ヒト 0.01 (0.5mg/ 日 ) 45 #: 無毒性量 a: 最終測定時の値 ラットおよびヒト ( 参照 ) は C ss b: 一般状態悪化のため 投与 43 日目より 10mg/kg/ 日に減量 p. 6
10 遺伝毒性試験細菌を用いた復帰突然変異試験 哺乳類培養細胞を用いた in vitro 染色体異常試験およびラットを用いた骨髄小核試験により遺伝毒性を検討した結果 ( 参照 ) いずれの試験においても陰性を示したことから 本薬は遺伝毒性を有していないと考えられた がん原性試験マウスおよびラットの 2 年間経口投与によるがん原性試験を実施した ( 参照 ) マウスでは 500mg/kg/ 日まで本薬に起因すると考えられる腫瘍および過形成の発現頻度の増加は認められなかった ラットでは 7.5mg/kg/ 日まで有意な発現頻度の増加はみられなかったが 53mg/kg/ 日で精巣間細胞腫の発現頻度の増加が認められた しかしながら 本薬は遺伝毒性を有しておらず 精巣間細胞腫の発現は 視床下部 - 下垂体 - 精巣軸を介した循環黄体形成ホルモン (LH) 量の上昇に起因した二次的影響によると考えられた [Prahalada, 1994] 生殖発生毒性試験本薬の薬理作用に起因する影響が 雄受胎能および胎児発生 ( 雄性次世代の雌性化 ) に認められた 雄ラットの受胎能試験 ( 交配 または 24 週前より最長 31 週間経口投与 ) では ( 参照 ) 0.05mg/kg/ 日以上のすべての本薬投与群に用量および投与期間に応じた受胎率の低下がみられ 副生殖器の萎縮を伴ったが いずれの変化も回復性または回復傾向を示した また 10mg/kg/ 日以上の投与群では交尾率の低下が投与 24 週の交配時に認められた 精巣および精子濃度 運動性に本薬投与による影響は認められなかった 本薬投与雄と交配させた無処置雌の血清中に低濃度ではあるが未変化体が検出され 本薬が精液を介して雌に移行した可能性が考えられた 雄親動物に対する無毒性量は 0.05mg/kg/ 日未満であった 受胎率の低下は膣栓数の減少を伴ったことから 前立腺および精嚢液分泌減少による膣栓形成不全に起因する変化と考えられ この影響は 膣栓の形成が受胎率に関係するげっ歯類に特異的な影響 [Cukierski, 1991; Sofikitis, 1992; Carballada, 1992] と考えられた 雌受胎能および着床までの初期胚発生に関する試験では ( 参照 ) 2.5mg/kg/ 日以上の投与群で雌親動物の体重増加量の低値および雄胎児の雌性化 ( 肛門生殖結節間距離の短縮 ) がみられ 0.05mg/kg/ 日以上の投与群では胎児体重の低値が認められた 雌親動物に対する無毒性量は 0.05mg/kg/ 日 胚 胎児に対する無毒性量は 0.05mg/kg/ 日未満であった ラットの胚 胎児発生に関する試験では ( 参照 ) 母動物の体重増加量の低値が 2.5mg/kg/ 日以上の投与群に 摂餌量の低値および妊娠期間の延長が 12.5mg/kg/ 日以上の投与群に認められた また 妊娠期間の延長がみられたが 1 型 5AR 欠損マウスで妊娠末期子宮頸におけるプロゲステロン代謝阻害によると考えられる分娩障害がみられていることから [Mahendroo, 1999] 本薬の 1 型 5AR 阻害作用に起因した影響と考えられた 次世代では 0.05mg/kg/ 日以上の投与群で雄胎児 出生児の外生殖器の雌性化 ( 肛門生殖結節間距離の短縮 尿道下裂あるいは包皮腺拡張 ) および乳頭発達がみられたが DHT は尿生殖洞および生殖結節の雄性化に必要なアンドロゲンであり [McPhaul, 1998; George, 1994] 乳頭発達抑制にも寄与していることが示唆されている [Imperato-McGinley, 1986] ことから 予測された影響 p. 7
11 であった また 2.5mg/kg/ 日以上の投与群では胎児体重の低値 母動物の体重増加抑制に起因した骨化遅延が認められた 母動物に対する無毒性量は 0.05mg/kg/ 日 次世代に対する無毒性量は 0.05mg/kg/ 日未満であった 一方 ウサギの胚 胎児発生に関する試験では ( および 参照 ) 200mg/kg/ 日においても母動物に本薬投与に起因すると考える影響は認められなかった 胎児では 頬骨癒合が 30mg/kg/ 日以上の高用量群でみられた 0.05mg/kg/ 日以上の投与群では 雄胎児に尿道会陰側拡張 偏在および腺包皮層板腹側部開口を特徴とした外生殖器の雌性化が観察され 数例では雌性化のより重度な変化として尿道下裂が認められた 母動物に対する無毒性量は 200mg/kg/ 日 胎児に対する無毒性量は 0.05mg/kg/ 日未満であった しかしながら サルの胚 胎児発生に関する静脈内投与試験では ( 参照 ) 2010ng/ 匹 / 日においても母動物および胎児毒性は発現しなかった ラットの出生前および出生後発生ならびに母体の機能に関する試験では ( 参照 ) F 0 母動物の体重増加量の低値および妊娠期間の延長が 2.5mg/kg/ 日以上の投与群で認められた F 1 出生児では 0.05mg/kg/ 日以上の雄に外生殖器の雌性化 ( 肛門生殖結節間距離短縮 ) がみられ 2.5mg/kg/ 日以上では尿道下裂の増加 尿道下裂が原因と考えられる交尾率および受胎率の低下 ならびに精嚢および前立腺の慢性炎症の発現率増加が認められた また 2.5mg/kg/ 日以上では 乳頭発達 精嚢および前立腺の小型化 重量低値も観察され DHT に依存した前立腺の分化と精嚢の生後発育が抑制されたため [Imperato-McGinley, 1992; Shima, 1990] と考えられた 母動物および F 1 雌出生児に対する無毒性量は 0.05mg/kg/ 日 F 1 雄出生児に対する無毒性量は 0.05mg/kg/ 日未満であった 代謝物および不純物の毒性本薬のヒト血清中主代謝物である 4 - 水酸化体および 1,2- 二水素化体について細菌を用いた復帰突然変異試験を実施した結果 ( 参照 ) 代謝活性化の有無にかかわらず復帰突然変異誘発能を示さなかった また 定常状態における 4 - 水酸化体の血清中濃度は ラットの 15mg/kg/ 日 ( 雌 ) および 53mg/kg/ 日 ( 雄 ) ではヒトを上回り ラットの 53mg/kg/ 日 ( 雄 ) での血清中主代謝物 (1,2- 二水素化体および 6- 水酸化体 ) 濃度は いずれもヒトでの血清中濃度よりも高いと推察された さらに ラット 26 週間投与毒性試験の雄の 50mg/kg/ 日群にみられた変化は 本薬の薬理作用に起因した生殖器の変化のみであったことから いずれの代謝物の安全性も評価されており 主代謝物による新たな毒性変化はないと考えられた 原薬に安全性の確認が必要となる閾値 (0.15%) を超えて含まれる 9 種類の不純物 (2.3.S.4.1 参照 ) の安全性について イヌの長期反復投与毒性試験 マウスがん原性試験および遺伝毒性 ( 小核 ) 試験に使用されたバッチに含まれている不純物含量を基に各不純物の安全性を評価した結果 ( 参照 ) イヌの 53 週間反復投与毒性試験の無毒性量における各不純物の推定曝露量は 最大臨床用量 (0.5mg/ 日 =0.01mg/kg/ 日 ) における各不純物の推定最大曝露量 ( それぞれの規格値の上限が含まれていると仮定した場合 ) の少なくとも 15 倍以上であり マウスがん原試験および小核試験における陰性用量での各不純物の推定曝露量は 最大臨床用量での推定最大曝露量の 3000 倍以上となることから いずれの不純物についても安全性が確認されていると判断した p. 8
12 総括および結論非臨床試験成績により デュタステリドの薬理 薬物動態および毒性評価を行った In vitro 試験において デュタステリドはヒト 1 型および 2 型 5AR を時間依存的に阻害し ラット 1 型および 2 型 5AR ならびにサル前立腺 5AR を阻害した In vivo 試験において デュタステリドは外因性に投与したテストステロンの前立腺における DHT への変換を阻害した デュタステリドは経口投与によりラットの前立腺組織中 DHT 濃度を低下させ 前立腺重量を低下させた また ラットの前立腺重量を低下させた用量で 精嚢重量を低下させたものの 精巣 肝臓および副腎重量には影響を示さなかった さらに デュタステリドは去勢ラットにおけるテストステロン誘発前立腺重量増加を抑制した これらのことから デュタステリドは経口投与により 1 型および 2 型 5AR を阻害し 前立腺中の DHT 濃度を低下させることにより 前立腺重量を低下させると考えられた また デュタステリドは類薬であるフィナステリドに比べて in vitro 試験においてより強い 5AR 阻害活性を示し in vivo 試験においてより持続的な 5AR 阻害作用を示した さらに ラットにおけるデュタステリドの前立腺重量低下作用の強さは ED 30 値で比較すると フィナステリドの約 20 倍であった 臨床用量 (0.5mg/ 日 ) をヒト ( 日本人前立腺肥大症患者 ) に反復投与した際の未変化体の C ss ( 臨床曝露量 ) は 約 45ng/mL であることが示されている ( 参照 ) ヒトの 5AR に対するデュタステリドの阻害定数 (Ki 値 ) は 1 型 5AR に対しては 3.2ng/mL(6nM) 2 型 5AR に対しては 3.7ng/mL(7nM) であった この Ki 値は臨床曝露量よりもはるかに低いことから ヒトに臨床用量を投与した際に 1 型および 2 型 5AR を十分に阻害する可能性が示された さらに デュタステリドは不可逆的な時間依存的酵素阻害作用を有するため Ki 値から予想されるよりも より強い阻害作用を示す可能性があると考えられる また デュタステリドの 5AR 阻害活性はヒトとラットで異なっており ラットの 5AR に対してヒトよりも約 25 倍 (1 型 5AR に対しては約 20 倍 (Ki 値 ) 2 型 5AR に対しては約 30 倍 (k 3 /Ki 値 )) 高い阻害活性を有することが示されている この阻害活性の違いを考慮すると 臨床曝露量に相当するラットにおける血中濃度は 1.8ng/mL(45 25ng/mL) と考えられる ラットにデュタステリドの 0.05mg/kg/ 日を 21 日間反復経口投与した際の C 24 は 1.78ng/mL であることから ( 参照 ) ヒトとラットに対する阻害活性の違いを考慮すると 臨床曝露量に相当する血中濃度となるようなラットでの用量は 0.05mg/kg に近い値であることが推定された デュタステリドは 0.01~1mg/kg/ 日をラットに 14 日間反復経口投与することにより前立腺重量を低下させ その ED 30 値は 0.19mg/kg/ 日であることが示されており 臨床曝露量に相当するラットでの用量において前立腺重量を低下させる可能性が示唆された 一方 デュタステリドのヒト血清中主代謝物である 4 - 水酸化体 6- 水酸化体および 1,2- 二水素化体は 5AR 阻害作用を示した 4 - 水酸化体および 6- 水酸化体は時間依存的な 5AR 阻害作用を示し その活性はそれぞれデュタステリドの約 1/10 および同程度であった また 1,2- 二水素化体は 5AR に対して時間依存的な阻害作用を示さなかったものの その IC 50 値はデュタステリドと同程度であった しかしながら ヒトにおける 4 - 水酸化体 6- 水酸化体および 1,2- 二水素化体の曝露量 (C ss ) は 血清中デュタステリド濃度の約 1/10 であったこ p. 9
13 とから ( 参照 ) デュタステリドの臨床効果に寄与する割合は低いと考えられた 副次的薬理試験において デュタステリドは 10µM の濃度においても ステロイド代謝系酵素 胆汁酸合成系酵素および性ホルモン受容体を含む各種受容体 酵素などに対してほとんど作用を示さず 5AR を選択的に阻害することが示唆された デュタステリドの 10µM は臨床曝露量の 200 倍以上であり デュタステリドは臨床使用において 5AR 阻害作用以外の作用に起因する重篤な副作用を発現する可能性は低いものと考えられた 安全性薬理試験の結果 中枢神経系 心血管系および呼吸系に対して in vivo では影響が認められず in vitro において 3.3µg/mL でイヌのプルキンエ線維の活動電位に影響が認められたものの この薬物濃度は臨床曝露量の約 70 倍であることから 臨床上 重篤な有害事象が発現する可能性は低いと考えられた 以上をまとめると デュタステリドは 5AR を選択的に阻害することにより前立腺重量を低下させ その作用は類薬であるフィナステリドより強く また 安全性薬理試験においても臨床上問題となるような影響を示さなかったことから 前立腺肥大症の治療薬としての高い有用性が期待される マウス ラットおよびイヌに本薬を経口投与したときの吸収および消失は緩やかであった 本薬の分布容積はラットでは総体液量よりも大きく イヌでは総体液量と同程度であったことから 本薬は広く組織に分布すると考えられた いずれの動物種においても 低いクリアランスおよび長い半減期に起因した蓄積性が確認された また マウスおよびイヌでの血清中未変化体濃度は雌雄で同程度であったが 雌ラットでの血清中未変化体濃度は雄よりも高く 性差が確認された また ウサギに本薬を経皮投与したときの血清中に未変化体が検出されたことから 本薬はヒトでも皮膚を介して体内に吸収されると考えられた マウスおよびラットで本薬は広く組織に分布し マウスに反復投与したときの組織内放射能の分布特性は単回投与と類似しており ほとんどの組織で単回投与の約 4 倍以内であった ラット イヌおよびヒトでの本薬の血漿蛋白結合率はいずれも 99.5% 超であった 本薬は雌ラット 雄イヌおよびヒト ( 男性 ) では血球中よりも血漿中に分布したが 雄ラットでは血漿中よりも血球中に分布した なお 本申請の適応症は前立腺肥大症であり 男性のみの適用で女性に対しては禁忌であることから 動物での胎盤通過性試験および乳汁移行試験は実施しなかった ヒト肝ミクロソームを用いた in vitro 代謝試験では 本薬はほとんど代謝されなかった ( 参照 ) ラットおよびイヌでの単回経口投与後の血清および糞中にはおもに未変化体が検出されたが 代謝物の存在もわずかに確認された 反復経口投与後のヒト糞中には 4 種類の主代謝物 ( このうちの 2 種類は 4 - 水酸化体および 6- 水酸化体 ) その他に 6 種類の代謝物 ( 未同定 ) が少量検出されたこと ( 参照 ) から マウス ラットおよびイヌの定常状態における代謝物を分析した その結果 動物およびヒトでの血清中主代謝物は 4 - 水酸化体であり ラットでは 6- 水酸化体 マウス ラットおよびイヌでは 6,4 - 二水酸化体および 1,2- 二水素化体もわずかに検出された ヒトで検出された代謝物はいずれも動物で存在が確認されたことから 本薬の代謝に種差はないと考えられた また ラットお p. 10
14 よびイヌに高用量のデュタステリドを 26 週間経口投与したときの肝薬物代謝酵素に誘導がみられなかったことから 本薬が臨床で肝薬物代謝酵素を誘導する可能性は低いと考えられた ラットおよびイヌに本薬を単回経口投与したときの主排泄経路は糞であることが示され 胆汁排泄および消化管分泌も確認された イヌにデュタステリドと CYP3A および P 糖蛋白質の基質であるベラパミルを併用した際の本薬の薬物動態に変化は認められなかったことから 本薬を CYP3A および P 糖蛋白質の基質と併用投与した際に薬物動態学的薬物相互作用が起こる可能性は低いと考えられた 以上のことから デュタステリドの動物における吸収 分布 代謝および排泄はヒトと類似していると考えられた 反復経口投与により 臨床曝露量のラットで約 378 倍以上 イヌで約 280 倍以上の曝露で中枢神経系に対する可逆的な影響がみられたが 高濃度曝露による非特異的反応と考えられ 臨床用量で発現する可能性は低いと考える ラット イヌともに雄性副生殖器 ( 前立腺 精嚢および精巣上体 ) に薬理作用に起因した変化がみられ ラットではげっ歯類に特異的である前立腺および精嚢液分泌減少による膣栓形成不全に起因すると考えられる可逆的な受胎率の低下が認められた 受胎率の低下は精子形成および運動性の影響を伴っておらず 健康成人男性に本剤 0.5mg/ 日を 1 年間投与した海外臨床試験 (ARIA1009 試験 ) においても いずれの精液パラメータの平均値も基準範囲内であり 試験開始前に設定した臨床的に重要な変動は認められなかったことから ( 参照 ) 臨床用量でヒトの精子形成能および受胎能に影響する可能性は低いと考える イヌでは 下垂体 甲状腺および副腎において軽度な組織学的変化を伴う影響がみられたが これらの影響は 高濃度 ( 臨床曝露量の約 49 倍以上 ) での長期曝露によるステロイド合成組織に対する影響および視床下部 - 下垂体 - 性腺 / 副腎軸を介したホルモン状態の生理的変動に適応した変化であると考えられ 臨床用量でヒトの内分泌器官に影響を及ぼす可能性は低いと考える なお 健康成人男性に本剤 20mg を 7 日間投与した時 (ARIA1001 試験 ) のコルチゾール濃度 ( 参照 ) ならびに本剤 0.5mg/ 日を 1 年間投与した時 (ARIA1009 試験 ) のサイロキシン 甲状腺刺激ホルモン 卵胞刺激ホルモン ( 参照 ) および LH( 参照 ) 濃度に臨床的に意義のある影響は認められていない 長期反復投与毒性試験における雄ラットおよび雄イヌの無毒性量はそれぞれ 50 および 3mg/kg/ 日であり それぞれの曝露量は臨床曝露量の約 16 および 104 倍に相当する 雌性生殖器においても 5AR 阻害に起因すると考えられる影響がみられたが 本申請の適応症は前立腺肥大症で 男性のみの適応であり 女性に対しては禁忌であることから 臨床使用において危惧される所見ではないと考えられた マウスのがん原性試験においては 臨床曝露量の約 261 倍まで本薬に関連すると考えられる腫瘍の発現は認められなかった ラットのがん原性試験では 臨床曝露量の約 69 倍まで本薬に関連すると考えられる腫瘍の発現はみられなかったが 臨床曝露量の約 141 倍で精巣間細胞腫の発現頻度の増加が認められた しかしながら 本薬は遺伝毒性を有しておらず 視床下部 - 下垂体 - 精巣軸に対する影響を介した循環 LH 量の上昇に起因した二次的影響に p. 11
15 よると考えられること また この影響はヒトへの外挿性が低いと判断されていることから [Capen, 2001; Alison, 1994; Clegg, 1997; Cook, 1999] ヒトに精巣間細胞腫を発現させる可能性は低いと考える ラットおよびウサギにおいて 雄胎児の外生殖器の雌性化が試験したすべての用量 ( 0.05mg/kg/ 日 ) で認められた 本薬は女性に適応される薬物ではないが ウサギで経皮吸収することが確認されていること 臨床用量でヒト精液中に最高 14ng/mL の濃度で検出されていることから (ARIA1009 試験 参照 ) 妊娠初期あるいは妊娠している可能性のある女性が カプセルから漏れた本薬に接触あるいは精液を介して単発 偶発的に曝露された場合 男児外生殖器の発達が阻害される可能性がある しかしながら 精液を介した曝露に関しては 精液中 ( 精液量 :5mL) の未変化体が子宮および膣粘膜より 100% 吸収されると仮定した際の女性 (50kg) における曝露量 (1.4ng/kg) の約 186 倍 (260ng/kg/ 日 : 2010ng/ 匹 / 日を体重 ( 妊娠 97 日の平均体重 7.73kg) で換算 ) を 5AR のアミノ酸配列および生化学的特性がヒトと類似しているアカゲザル [Ellsworth, 1998] の器官形成期に静脈内投与しても 雄胎児の雌性化は認められなかった また 本薬はヒト血漿中および精液中蛋白との結合率が高く (>96% 参照 ) 子宮 膣からの吸収量が低下することが考えられることから 精液を介した子宮曝露によりヒト男児外生殖器の発達に影響を及ぼす可能性は低いと考える ヒトにおける血清中主代謝物が新たな毒性変化を引き起こす可能性は低いと考えられ 不純物についても安全性が確認されていると判断した 以上の非臨床試験成績から 臨床用量の 0.5mg/ 日を投与することにより前立腺肥大症患者の前立腺を縮小させることが期待され 長期にわたり投与しても重篤な有害事象が生じる可能性は低いと考えられた ただし 本薬は経皮吸収され 消失半減期が長いことから 小児および妊娠初期あるいは妊娠している可能性のある女性 ( 男子胎児の外生殖器の発達に対する影響を避けるため ) は カプセルから漏れた本薬に直接触れないよう注意する必要があると考えられた 参考文献一覧 Alison RH, Capen CC, Prentice DE. Neoplastic lesions of questionable significance to humans. Toxicol Pathol. 1994;22: Capen CC. Toxic responses of the endocrine system. In: Klaassen CD, editor. Casarett and Doull s Toxicology: The basic science of poison, 6th edition. New York:The McGraw-Hill Companies, Inc., 2001: Carballada R, Esponda P. Role of fluid from seminal vesicles and coagulating glands in sperm transport into the uterus and fertility in rats. J Reprod Fertil. 1992;95: p. 12
16 Clegg ED, Cook JC, Chapin RE, et al. Leydig cell hyperplasia and adenoma formation: mechanisms and relevance to humans. Reprod Toxicol. 1997;11: Cook JC, Klinefelter GR, Hardisty JF, et al. Rodent Leydig cell tumorigenesis: a review of the physiology, pathology, mechanisms, and relevance to humans. Crit Rev Toxicol. 1999;29: Cukierski MA, Sina JL, Prahalada S, et al. Effects of seminal vesicle and coagulating gland ablation on fertility in rats. Reprod Toxicol. 1991;5: Ellsworth KP, Azzolina BA, Cimis G, et al. Cloning, expression and characterization of rhesus macaque types 1 and 2 5alpha-reductase: evidence for mechanism-based inhibition by finasteride. J Steroid Biochem Mol Biol. 1998;66: George FW, Wilson JD. In: Knobil E and Neill JD, editor. Sex determination and differentiation. The physiology and reproduction, 2nd edition. New York:Raven Press, Ltd, 1994:3-28. Imperato-McGinley J, Binienda Z, Gedney J, et al. Nipple differentiation in fetal male rats treated with an inhibitor of the enzyme 5α-reductase: definition of a selective role for dihydrotestosterone. Endocrinology. 1986;118: Imperato-McGinley J, Sanchez RS, Spencer JR, et al. Comparison of the effects of the 5α-reductase inhibitor finasteride and the antiandrogen flutamide on prostate and genital differentiation: doseresponse studies. Endocrinology. 1992;131: Mahendroo MS, Russell DW. Male and female isoenzymes of steroid 5α-reductase. Rev Reprod. 1999;4: McPhaul MJ. The biology of the male reproductive tract. In: Korach KS, editor. Reproductive and developmental toxicology. New York:Marcel Dekker, Inc, 1998: Normington K, Russell DW. Tissue distribution and kinetic characteristics of rat steroid 5α-reductase isozymes. Evidence for distinct physiological functions. J Biol Chem. 1992;267: Prahalada S, Majka JA, Soper KA, et al. Leydig cell hyperplasia and adenomas in mice treated with finasteride, a 5α-reductase inhibitor: a possible mechanism. Fundam Appl Toxicol. 1994;22: Russell DW, Wilson JD. Steroid 5α-reductase: two genes/two enzymes. Annu Rev Biochem. 1994;63: Shima H, Tsuji M, Young P, et al. Postnatal growth of mouse seminal vesicle is dependent on 5αdihydrotestosterone. Endocrinology. 1990;127: Sofikitis N, Takahashi C, Kadowaki H, et al. The role of the seminal vesicles and coagulating glands in fertilization in the rat. Int J Androl. 1992;15: p. 13
17 Torres JM, Ruiz E, Ortega E. Development of a quantitative RT-PCR method to study 5α-reductase mrna isozymes in rat prostate in different androgen status. Prostate. 2003;56:74-9. 石井康行, 石井美樹夫, 向山裕子ら. フィナステリドの体内動態 (I): ラットにおける単回投与後の吸収 分布および排泄. 薬物動態. 1994;9: p. 14
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社
 オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
オクノベル錠 150 mg オクノベル錠 300 mg オクノベル内用懸濁液 6% 2.1 第 2 部目次 ノーベルファーマ株式会社 Page 2 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 第 2 部 :CTD の概要 ( サマリー ) 2.1 CTD の目次 ( 第 2 部から第 5 部 ) 2.2 諸言 2.3 品質に関する概括資料 2.3.I 諸言 2.3.S 原薬 ( オクスカルバゼピン,
 非臨床概要薬理試験の目次 項目 頁 2.6.1. 緒言... 2.6.1 ~xr1i - p. 1 2.6.2. 薬理試験の概要文... 2.6.2 ~xr2i - p. 1 2.6.2.1. まとめ... 2.6.2 ~xr3i - p. 1 2.6.2.2. 効力を裏付ける試験... 2.6.2 ~xr4i - p. 6 2.6.2.2.1. 5AR 阻害作用... 2.6.2 ~xr5i -
非臨床概要薬理試験の目次 項目 頁 2.6.1. 緒言... 2.6.1 ~xr1i - p. 1 2.6.2. 薬理試験の概要文... 2.6.2 ~xr2i - p. 1 2.6.2.1. まとめ... 2.6.2 ~xr3i - p. 1 2.6.2.2. 効力を裏付ける試験... 2.6.2 ~xr4i - p. 6 2.6.2.2.1. 5AR 阻害作用... 2.6.2 ~xr5i -
一般薬理試験及び毒性試験 2. 毒性試験 (1) 単回投与毒性試験 ( マウス イヌ サル ) 33) 動物種 投与経路 投与量 (mg/kg) 概略の致死量 (mg/kg) マウス 経口 2000 雌雄 :>2000 腹腔内 300 雌雄 :300 経口 750 雌雄 :>750 腹腔内 500
 枢神経系影響なし心血管系一般薬理試験及び毒性試験 1. 一般薬理試験 32) 試験項目 動物種 ( 性 動物数 ) 投与経路投与量主な結果 評価中一般状態 体温及び自発運動量に及ぼす作用 (Irwin 法 ) ( 雄 4 ) 30 100 300mg/kg herg 電流に及ぼす作用 ( ホールセルパッチクランプ法 ) herg 発現ヒト胎児腎細胞株 HEK293 in vitro 4 20 100μmol/L
枢神経系影響なし心血管系一般薬理試験及び毒性試験 1. 一般薬理試験 32) 試験項目 動物種 ( 性 動物数 ) 投与経路投与量主な結果 評価中一般状態 体温及び自発運動量に及ぼす作用 (Irwin 法 ) ( 雄 4 ) 30 100 300mg/kg herg 電流に及ぼす作用 ( ホールセルパッチクランプ法 ) herg 発現ヒト胎児腎細胞株 HEK293 in vitro 4 20 100μmol/L
薬物動態試験の概要文
 アマージ錠 2.5mg 製造販売承認申請 CTD 第 2 部 2.6 非臨床試験の概要文及び概要表 2.6.4 薬物動態試験の概要文 2.6.5 薬物動態試験概要表 グラクソ スミスクライン株式会社 目次 頁 2.6.4. 薬物動態試験の概要文 1 2.6.4.1. まとめ 1 2.6.4.2. 分析法 4 2.6.4.2.1. 被験物質 4 2.6.4.2.2. 分析方法 4 2.6.4.3. 吸収
アマージ錠 2.5mg 製造販売承認申請 CTD 第 2 部 2.6 非臨床試験の概要文及び概要表 2.6.4 薬物動態試験の概要文 2.6.5 薬物動態試験概要表 グラクソ スミスクライン株式会社 目次 頁 2.6.4. 薬物動態試験の概要文 1 2.6.4.1. まとめ 1 2.6.4.2. 分析法 4 2.6.4.2.1. 被験物質 4 2.6.4.2.2. 分析方法 4 2.6.4.3. 吸収
平成14年度研究報告
 平成 14 年度研究報告 研究テーマ 多嚢胞性卵巣発症に関する遺伝性素因の解析 - PCO の解析 - 北海道大学大学院医学研究科 助手菅原照夫 現所属 : 北海道大学大学院医学研究科 医学部連携研究センター サマリー 多嚢胞性卵巣 (PCO) は生殖可能年齢の婦人の 5 10% に発症する内分泌疾患である 臨床症状は 月経不順 多毛 肥満 排卵障害が主な特徴であり 難治性の不妊症の主な原因である
平成 14 年度研究報告 研究テーマ 多嚢胞性卵巣発症に関する遺伝性素因の解析 - PCO の解析 - 北海道大学大学院医学研究科 助手菅原照夫 現所属 : 北海道大学大学院医学研究科 医学部連携研究センター サマリー 多嚢胞性卵巣 (PCO) は生殖可能年齢の婦人の 5 10% に発症する内分泌疾患である 臨床症状は 月経不順 多毛 肥満 排卵障害が主な特徴であり 難治性の不妊症の主な原因である
Microsoft PowerPoint
 ニコチン受容体を介するステロイド産生幹細胞の分化制御 矢澤隆志 ( 旭川医科大学生化学講座細胞制御科学分野 ) コレステロール StAR コレステロール CYP11A1 プレグネノロン CYP17A1 17α-OH pregnenolone CYP17A1 DHEA 生殖腺 3β-HSD CYP19A1 プロゲステロン 17α-OH progesterone Androstenedione Estrone
ニコチン受容体を介するステロイド産生幹細胞の分化制御 矢澤隆志 ( 旭川医科大学生化学講座細胞制御科学分野 ) コレステロール StAR コレステロール CYP11A1 プレグネノロン CYP17A1 17α-OH pregnenolone CYP17A1 DHEA 生殖腺 3β-HSD CYP19A1 プロゲステロン 17α-OH progesterone Androstenedione Estrone
グルコースは膵 β 細胞内に糖輸送担体を介して取り込まれて代謝され A T P が産生される その結果 A T P 感受性 K チャンネルの閉鎖 細胞膜の脱分極 電位依存性 Caチャンネルの開口 細胞内 Ca 2+ 濃度の上昇が起こり インスリンが分泌される これをインスリン分泌の惹起経路と呼ぶ イ
 薬効薬理 1. 作用機序 アナグリプチンはジペプチジルペプチダーゼ -4(DPP-4) の競合的かつ可逆的な選択的阻害剤である インクレチンであるグルカゴン様ペプチド-1(GL P-1) 及びグルコース依存性インスリン分泌刺激ポリペプチド (GI P) は グルコース依存的なインスリン分泌促進作用やグルカゴン分泌抑制作用等 ( 主にGLP-1の作用 ) を有するが 24) DPP-4により分解されて活性を失う
薬効薬理 1. 作用機序 アナグリプチンはジペプチジルペプチダーゼ -4(DPP-4) の競合的かつ可逆的な選択的阻害剤である インクレチンであるグルカゴン様ペプチド-1(GL P-1) 及びグルコース依存性インスリン分泌刺激ポリペプチド (GI P) は グルコース依存的なインスリン分泌促進作用やグルカゴン分泌抑制作用等 ( 主にGLP-1の作用 ) を有するが 24) DPP-4により分解されて活性を失う
2.6.4 薬物動態試験の概要文 目次 略語 略号一覧 薬物動態試験の概要文 まとめ 吸収 分布 代謝 ( 動物種間の比較 ) 排泄
 タリオン 錠 5mg, タリオン 錠 10mg タリオン OD 錠 5mg, タリオン OD 錠 10mg 製造販売承認事項一部変更承認申請書 添付資料 第 2 部 ( モジュール 2) 2.6 非臨床試験の概要文及び概要表 2.6.4 薬物動態試験の概要文 田辺三菱製薬株式会社 1 2.6.4 薬物動態試験の概要文 目次 略語 略号一覧... 3 2.6.4 薬物動態試験の概要文... 5 2.6.4.1
タリオン 錠 5mg, タリオン 錠 10mg タリオン OD 錠 5mg, タリオン OD 錠 10mg 製造販売承認事項一部変更承認申請書 添付資料 第 2 部 ( モジュール 2) 2.6 非臨床試験の概要文及び概要表 2.6.4 薬物動態試験の概要文 田辺三菱製薬株式会社 1 2.6.4 薬物動態試験の概要文 目次 略語 略号一覧... 3 2.6.4 薬物動態試験の概要文... 5 2.6.4.1
(2) 健康成人の血漿中濃度 ( 反復経口投与 ) 9) 健康成人男子にスイニー 200mgを1 日 2 回 ( 朝夕食直前 ) 7 日間反復経口投与したとき 血漿中アナグリプチン濃度は投与 2 日目には定常状態に達した 投与 7 日目における C max 及びAUC 0-72hの累積係数はそれぞれ
 1. 血漿中濃度 (1) 健康成人の血漿中濃度 ( 単回経口投与 ) 8) 健康成人男子にスイニー 100mg 又は200mgを空腹時に単回経口投与したときの血漿中アナグリプチン濃度は 投与後約 1~ 2 時間で C maxに達した後 二相性の消失を示し t 1/2αは約 2 時間 t 1/2βは約 6 時間であった C max 及びAUC0- は投与量の増加に伴って増加した 血漿中アナグリプチン濃度推移
1. 血漿中濃度 (1) 健康成人の血漿中濃度 ( 単回経口投与 ) 8) 健康成人男子にスイニー 100mg 又は200mgを空腹時に単回経口投与したときの血漿中アナグリプチン濃度は 投与後約 1~ 2 時間で C maxに達した後 二相性の消失を示し t 1/2αは約 2 時間 t 1/2βは約 6 時間であった C max 及びAUC0- は投与量の増加に伴って増加した 血漿中アナグリプチン濃度推移
トリアムシノロンアセトニド マキュエイド硝子体内注用 40mg 医薬品製造販売承認事項一部変更承認申請書 添付資料 CTD 第 2 部 ( 資料概要 ) 2.6 非臨床試験の概要文及び概要表 薬物動態試験の概要文 わかもと製薬株式会社 1
 トリアムシノロンアセトニド マキュエイド硝子体内注用 40mg 医薬品製造販売承認事項一部変更承認申請書 添付資料 CTD 第 2 部 ( 資料概要 ) 2.6 非臨床試験の概要文及び概要表 2.6.4 薬物動態試験の概要文 わかもと製薬株式会社 1 2.6.4 薬物動態試験の概要文マキュエイド硝子体内注用 目次 2.6.4 薬物動態試験の概要文... 4 2.6.4.1 まとめ... 4 2.6.4.2
トリアムシノロンアセトニド マキュエイド硝子体内注用 40mg 医薬品製造販売承認事項一部変更承認申請書 添付資料 CTD 第 2 部 ( 資料概要 ) 2.6 非臨床試験の概要文及び概要表 2.6.4 薬物動態試験の概要文 わかもと製薬株式会社 1 2.6.4 薬物動態試験の概要文マキュエイド硝子体内注用 目次 2.6.4 薬物動態試験の概要文... 4 2.6.4.1 まとめ... 4 2.6.4.2
ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル
 ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル 1mg は 1 カプセル中ロペラミド塩酸塩 1 mg を含有し消化管から吸収されて作用を発現する このことから
ロペラミド塩酸塩カプセル 1mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロペラミド塩酸塩は 腸管に選択的に作用して 腸管蠕動運動を抑制し また腸管内の水分 電解質の分泌を抑制して吸収を促進することにより下痢症に効果を示す止瀉剤である ロペミン カプセル 1mg は 1 カプセル中ロペラミド塩酸塩 1 mg を含有し消化管から吸収されて作用を発現する このことから
<4D F736F F F696E74202D2097D58FB08E8E8CB1838F815B834E F197D58FB E96D8816A66696E616C CF68A4A2E >
 再生医療等製品の非臨床安全性評価の考え方 ex vivo 遺伝子治療を中心に 独立行政法人医薬品医療機器総合機構 (PMDA) 再生医療製品等審査部 真木一茂 様式 1-B 第 24 回日本遺伝子細胞治療学会学術集会 CO I 開示 発表者名 : 真木一茂 演題発表に関連し 開示すべき CO I 関係にある企業などはありません 2 1 本日の話 1.Ex vivo 遺伝子治療について 2. 治験開始に必要な非臨床試験
再生医療等製品の非臨床安全性評価の考え方 ex vivo 遺伝子治療を中心に 独立行政法人医薬品医療機器総合機構 (PMDA) 再生医療製品等審査部 真木一茂 様式 1-B 第 24 回日本遺伝子細胞治療学会学術集会 CO I 開示 発表者名 : 真木一茂 演題発表に関連し 開示すべき CO I 関係にある企業などはありません 2 1 本日の話 1.Ex vivo 遺伝子治療について 2. 治験開始に必要な非臨床試験
抗菌薬の殺菌作用抗菌薬の殺菌作用には濃度依存性と時間依存性の 2 種類があり 抗菌薬の効果および用法 用量の設定に大きな影響を与えます 濃度依存性タイプでは 濃度を高めると濃度依存的に殺菌作用を示します 濃度依存性タイプの抗菌薬としては キノロン系薬やアミノ配糖体系薬が挙げられます 一方 時間依存性
 2012 年 1 月 4 日放送 抗菌薬の PK-PD 愛知医科大学大学院感染制御学教授三鴨廣繁抗菌薬の PK-PD とは薬物動態を解析することにより抗菌薬の有効性と安全性を評価する考え方は アミノ配糖体系薬などの副作用を回避するための薬物血中濃度モニタリング (TDM) の分野で発達してきました 近年では 耐性菌の増加 コンプロマイズド ホストの増加 新規抗菌薬の開発の停滞などもあり 現存の抗菌薬をいかに科学的に使用するかが重要な課題となっており
2012 年 1 月 4 日放送 抗菌薬の PK-PD 愛知医科大学大学院感染制御学教授三鴨廣繁抗菌薬の PK-PD とは薬物動態を解析することにより抗菌薬の有効性と安全性を評価する考え方は アミノ配糖体系薬などの副作用を回避するための薬物血中濃度モニタリング (TDM) の分野で発達してきました 近年では 耐性菌の増加 コンプロマイズド ホストの増加 新規抗菌薬の開発の停滞などもあり 現存の抗菌薬をいかに科学的に使用するかが重要な課題となっており
新規 P2X4 受容体アンタゴニスト NCP-916 の鎮痛作用と薬物動態に関する検討 ( 分野名 : ライフイノベーション分野 ) ( 学籍番号 )3PS1333S ( 氏名 ) 小川亨 序論 神経障害性疼痛とは, 体性感覚神経系の損傷や疾患によって引き起こされる痛みと定義され, 自発痛やアロディ
 九州大学学術情報リポジトリ Kyushu University Institutional Repository 新規 P2X4 受容体アンタゴニスト NCP-916 の鎮痛作用と薬物動態に関する検討 小川, 亨 http://hdl.handle.net/2324/178378 出版情報 : 九州大学, 216, 博士 ( 創薬科学 ), 課程博士バージョン : 権利関係 : やむを得ない事由により本文ファイル非公開
九州大学学術情報リポジトリ Kyushu University Institutional Repository 新規 P2X4 受容体アンタゴニスト NCP-916 の鎮痛作用と薬物動態に関する検討 小川, 亨 http://hdl.handle.net/2324/178378 出版情報 : 九州大学, 216, 博士 ( 創薬科学 ), 課程博士バージョン : 権利関係 : やむを得ない事由により本文ファイル非公開
非臨床概要薬物動態試験の目次 項目 - 頁 薬物動態試験の概要文 p まとめ p 分析方法 p 被験物質 p
 非臨床概要薬物動態試験の目次 項目 - 頁 2.6.4. 薬物動態試験の概要文... 2.6.4 - p. 1 2.6.4.1. まとめ... 2.6.4 - p. 1 2.6.4.2. 分析方法... 2.6.4 - p. 4 2.6.4.2.1. 被験物質... 2.6.4 - p. 4 2.6.4.2.2. 分析法... 2.6.4 - p. 4 2.6.4.3. 吸収... 2.6.4 -
非臨床概要薬物動態試験の目次 項目 - 頁 2.6.4. 薬物動態試験の概要文... 2.6.4 - p. 1 2.6.4.1. まとめ... 2.6.4 - p. 1 2.6.4.2. 分析方法... 2.6.4 - p. 4 2.6.4.2.1. 被験物質... 2.6.4 - p. 4 2.6.4.2.2. 分析法... 2.6.4 - p. 4 2.6.4.3. 吸収... 2.6.4 -
1)~ 2) 3) 近位筋脱力 CK(CPK) 高値 炎症を伴わない筋線維の壊死 抗 HMG-CoA 還元酵素 (HMGCR) 抗体陽性等を特徴とする免疫性壊死性ミオパチーがあらわれ 投与中止後も持続する例が報告されているので 患者の状態を十分に観察すること なお 免疫抑制剤投与により改善がみられた
 適正使用に欠かせない情報です 必ずお読みください 使用上の注意 改訂のお知らせ 注 1) 処方箋医薬品 ATORVASTATIN TABLETS AMALUET COMBINATION TABLETS 注 1) 処方箋医薬品 PRAVASTATIN SODIUM TABLETS 注 1) 注意 - 医師等の処方箋により使用すること PITAVASTATIN CALCIUM TABLETS 2016
適正使用に欠かせない情報です 必ずお読みください 使用上の注意 改訂のお知らせ 注 1) 処方箋医薬品 ATORVASTATIN TABLETS AMALUET COMBINATION TABLETS 注 1) 処方箋医薬品 PRAVASTATIN SODIUM TABLETS 注 1) 注意 - 医師等の処方箋により使用すること PITAVASTATIN CALCIUM TABLETS 2016
ルグリセロールと脂肪酸に分解され吸収される それらは腸上皮細胞に吸収されたのちに再び中性脂肪へと生合成されカイロミクロンとなる DGAT1 は腸管で脂質の再合成 吸収に関与していることから DGAT1 KO マウスで認められているフェノタイプが腸 DGAT1 欠如に由来していることが考えられる 実際
 学位論文の内容の要旨 論文提出者氏名 津田直人 論文審査担当者 主査下門顕太郎副査吉田雅幸横関博雄 論文題目 Intestine-Targeted DGAT1 Inhibition Improves Obesity and Insulin Resistance without Skin Aberrations in Mice ( 論文内容の要旨 ) < 要旨 > Diacylglycerol O-acyltransferase
学位論文の内容の要旨 論文提出者氏名 津田直人 論文審査担当者 主査下門顕太郎副査吉田雅幸横関博雄 論文題目 Intestine-Targeted DGAT1 Inhibition Improves Obesity and Insulin Resistance without Skin Aberrations in Mice ( 論文内容の要旨 ) < 要旨 > Diacylglycerol O-acyltransferase
トピロリック錠 インタビューフォーム
 Ⅸ. 非臨床試験に関する項目 1. 薬理試験 (1) 薬効薬理試験 ( Ⅵ. 薬効薬理に関する項目 参照 ) (2) 副次的薬理試験 該当資料なし 42) (3) 安全性薬理試験 試験項目 動物種 / 系統投与経路 ( 例数 ) 投与量 特記すべき所見 中枢神経系 一般状態 体温及び自発運動量に及ぼす作用 (Irwin 法 ) ラット / Wistar( 雄 4) herg 電流に及ぼす作用 herg
Ⅸ. 非臨床試験に関する項目 1. 薬理試験 (1) 薬効薬理試験 ( Ⅵ. 薬効薬理に関する項目 参照 ) (2) 副次的薬理試験 該当資料なし 42) (3) 安全性薬理試験 試験項目 動物種 / 系統投与経路 ( 例数 ) 投与量 特記すべき所見 中枢神経系 一般状態 体温及び自発運動量に及ぼす作用 (Irwin 法 ) ラット / Wistar( 雄 4) herg 電流に及ぼす作用 herg
薬物動態試験 : 単回投与後の組織分布 ( その3) 薬物動態試験 : 反復投与後の組織分布 薬物動態試験 : 反復投与後の組織分布 ( 続き ) 薬物動態試験 : 反復投与後の組織分布 ( 続き )...
 2.6.5 目次 2.6.5...4 2.6.5.1 薬物動態試験 : 一覧表 ( その1)...4 2.6.5.1 薬物動態試験 : 一覧表 ( その2)...5 2.6.5.1 薬物動態試験 : 一覧表 ( その3)...6 2.6.5.1 薬物動態試験 : 一覧表 ( その4)...7 2.6.5.1 薬物動態試験 : 一覧表 ( その5)...8 2.6.5.2 薬物動態試験 : 分析方法及びバリデーション試験
2.6.5 目次 2.6.5...4 2.6.5.1 薬物動態試験 : 一覧表 ( その1)...4 2.6.5.1 薬物動態試験 : 一覧表 ( その2)...5 2.6.5.1 薬物動態試験 : 一覧表 ( その3)...6 2.6.5.1 薬物動態試験 : 一覧表 ( その4)...7 2.6.5.1 薬物動態試験 : 一覧表 ( その5)...8 2.6.5.2 薬物動態試験 : 分析方法及びバリデーション試験
氏名 ( 本籍 ) 鈴木桂子 学位の種類薬 A 子 博士 学位記番号用 下 E コ王 学位授与の日付昭和 54 年 3 月 6 日 学位授与の要件学位規則第 5 条第 2 項該当 学位論文題目 ラット卵巣におけるステロイドホルモン合成に関する研究 ( 主査 ) ー論文審査委員教授近, f~i 雅日
 Title Author(s) ラット卵巣におけるステロイドホルモン合成に関する研究 鈴木, 桂子 Citation Issue Date Text Version none URL http://hdl.handle.net/11094/32337 DOI rights 氏名 ( 本籍 ) 鈴木桂子 学位の種類薬 A 子 博士 学位記番号用 下 E コ王 学位授与の日付昭和 54 年 3 月 6
Title Author(s) ラット卵巣におけるステロイドホルモン合成に関する研究 鈴木, 桂子 Citation Issue Date Text Version none URL http://hdl.handle.net/11094/32337 DOI rights 氏名 ( 本籍 ) 鈴木桂子 学位の種類薬 A 子 博士 学位記番号用 下 E コ王 学位授与の日付昭和 54 年 3 月 6
使用上の注意 1. 慎重投与 ( 次の患者には慎重に投与すること ) 1 2X X 重要な基本的注意 1TNF 2TNF TNF 3 X - CT X 4TNFB HBsHBcHBs B B B B 5 6TNF 7 8dsDNA d
 2015 5 7 201410 28 TNF 阻害薬 TNFFab シムジア 皮下注 200mg シリンジ Cimzia 200mg Syringe for S.C. Injection セルトリズマブペゴル ( 遺伝子組換え ) 製剤 873999 22400AMX01488000 20132 20133 20155 20079 警告 1. 2. 1 2 X - CT 3. TNF 4. 1 禁忌
2015 5 7 201410 28 TNF 阻害薬 TNFFab シムジア 皮下注 200mg シリンジ Cimzia 200mg Syringe for S.C. Injection セルトリズマブペゴル ( 遺伝子組換え ) 製剤 873999 22400AMX01488000 20132 20133 20155 20079 警告 1. 2. 1 2 X - CT 3. TNF 4. 1 禁忌
薬物動態開発の経緯 特性製品概要臨床成績副作用 mgを空腹時に単回経口投与副作用また 日本人及び白人健康成人男性において アピキサバン 薬物動態薬物動態非臨床試験に関する事項非臨床試験に関する事項1. 血中濃度 (1) 単回投与 (CV185013) 11) 日本人健康成人男性
 薬物動態開発の経緯 特性製品概要臨床成績副作用2.5 1 25 5mgを空腹時に単回経口投与副作用また 日本人及び白人健康成人男性において アピキサバン 薬物動態薬物動態非臨床試験に関する事項非臨床試験に関する事項1. 血中濃度 (1) 単回投与 (CV18513) 11) 日本人健康成人男性 12 例に アピキサバン 2.5 1mg を空腹時に単回経口投与 したとき 投与後 3 3.5 時間で最高血漿中濃度に達し
薬物動態開発の経緯 特性製品概要臨床成績副作用2.5 1 25 5mgを空腹時に単回経口投与副作用また 日本人及び白人健康成人男性において アピキサバン 薬物動態薬物動態非臨床試験に関する事項非臨床試験に関する事項1. 血中濃度 (1) 単回投与 (CV18513) 11) 日本人健康成人男性 12 例に アピキサバン 2.5 1mg を空腹時に単回経口投与 したとき 投与後 3 3.5 時間で最高血漿中濃度に達し
抑制することが知られている 今回はヒト子宮内膜におけるコレステロール硫酸のプロテ アーゼ活性に対する効果を検討することとした コレステロール硫酸の着床期特異的な発現の機序を解明するために 合成酵素であるコ レステロール硫酸基転移酵素 (SULT2B1b) に着目した ヒト子宮内膜は排卵後 脱落膜 化
 論文の内容の要旨 論文題目 着床期ヒト子宮内膜におけるコレステロール硫酸の発現調節機序及び機能の解析 指導教員武谷雄二教授 東京大学大学院医学系研究科 平成 15 年 4 月入学 医学博士課程 生殖 発達 加齢医学専攻 清末美奈子 緒言 着床とは 受精卵が分割し形成された胚盤胞が子宮内膜上皮へ接着 貫通し 子 宮内膜間質を浸潤して絨毛構造を形成するまでの一連の現象をいう 胚盤胞から分化した トロフォブラストが浸潤していく過程で
論文の内容の要旨 論文題目 着床期ヒト子宮内膜におけるコレステロール硫酸の発現調節機序及び機能の解析 指導教員武谷雄二教授 東京大学大学院医学系研究科 平成 15 年 4 月入学 医学博士課程 生殖 発達 加齢医学専攻 清末美奈子 緒言 着床とは 受精卵が分割し形成された胚盤胞が子宮内膜上皮へ接着 貫通し 子 宮内膜間質を浸潤して絨毛構造を形成するまでの一連の現象をいう 胚盤胞から分化した トロフォブラストが浸潤していく過程で
ピルシカイニド塩酸塩カプセル 50mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにピルジカイニド塩酸塩水和物は Vaughan Williams らの分類のクラスⅠCに属し 心筋の Na チャンネル抑制作用により抗不整脈作用を示す また 消化管から速やかに
 ピルシカイニド塩酸塩カプセル 50mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにピルジカイニド塩酸塩水和物は Vaughan Williams らの分類のクラスⅠCに属し 心筋の Na チャンネル抑制作用により抗不整脈作用を示す また 消化管から速やかに吸収され 体内でもほとんど代謝を受けない頻脈性不整脈 ( 心室性 ) に優れた有効性をもつ不整脈治療剤である
ピルシカイニド塩酸塩カプセル 50mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにピルジカイニド塩酸塩水和物は Vaughan Williams らの分類のクラスⅠCに属し 心筋の Na チャンネル抑制作用により抗不整脈作用を示す また 消化管から速やかに吸収され 体内でもほとんど代謝を受けない頻脈性不整脈 ( 心室性 ) に優れた有効性をもつ不整脈治療剤である
検査項目情報 トータルHCG-β ( インタクトHCG+ フリー HCG-βサブユニット ) ( 緊急検査室 ) chorionic gonadotropin 連絡先 : 基本情報 ( 標準コード (JLAC10) ) 基本情報 ( 診療報酬 ) 標準コード (JLAC10)
 chorionic gonadotropin 連絡先 : 3479 2-2908 基本情報 ( 標準コード (JLAC10) ) 基本情報 ( 診療報酬 ) 標準コード (JLAC10) 診療報酬 分析物 9186 4. 内分泌学的検査 >> 4F. 性腺 胎盤ホルモンおよび結合蛋白 >> 4F090. Ver.2 4F090 HCGβ サブユニット (β-hcg) 特掲診療料 >> 検査 >> 検体検査料
chorionic gonadotropin 連絡先 : 3479 2-2908 基本情報 ( 標準コード (JLAC10) ) 基本情報 ( 診療報酬 ) 標準コード (JLAC10) 診療報酬 分析物 9186 4. 内分泌学的検査 >> 4F. 性腺 胎盤ホルモンおよび結合蛋白 >> 4F090. Ver.2 4F090 HCGβ サブユニット (β-hcg) 特掲診療料 >> 検査 >> 検体検査料
シプロフロキサシン錠 100mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを
 シプロフロキサシン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを有し 上気道感染症 尿路感染症 皮膚感染症などに有効なニューキノロン系の合成抗菌剤である シプロキサン 錠
シプロフロキサシン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにシプロフロキサシン塩酸塩は グラム陽性菌 ( ブドウ球菌 レンサ球菌など ) や緑膿菌を含むグラム陰性菌 ( 大腸菌 肺炎球菌など ) に強い抗菌力を示すように広い抗菌スペクトルを有し 上気道感染症 尿路感染症 皮膚感染症などに有効なニューキノロン系の合成抗菌剤である シプロキサン 錠
3. 安全性本治験において治験薬が投与された 48 例中 1 例 (14 件 ) に有害事象が認められた いずれの有害事象も治験薬との関連性は あり と判定されたが いずれも軽度 で処置の必要はなく 追跡検査で回復を確認した また 死亡 その他の重篤な有害事象が認められなか ったことから 安全性に問
 フェキソフェナジン塩酸塩錠 6mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにフェキソフェナジン塩酸塩は 第二世代抗ヒスタミン薬の一つであり 抗原抗体反応に伴って起こる肥満細胞からのヒスタミンなどのケミカルメディエーターの遊離を抑制すると共に ヒスタミンの H1 作用に拮抗することにより アレルギー症状を緩和する 今回 フェキソフェナジン塩酸塩錠 6mg
フェキソフェナジン塩酸塩錠 6mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにフェキソフェナジン塩酸塩は 第二世代抗ヒスタミン薬の一つであり 抗原抗体反応に伴って起こる肥満細胞からのヒスタミンなどのケミカルメディエーターの遊離を抑制すると共に ヒスタミンの H1 作用に拮抗することにより アレルギー症状を緩和する 今回 フェキソフェナジン塩酸塩錠 6mg
生殖発生毒性試験の実施時期について
 S5(R3) Informal 医薬品の生殖発生毒性試験法 ( 改訂 ) 日本製薬工業協会 ICH プロジェクト委員会 S5(R3) Informal WG トピックリーダー藤原道夫 1 本日の内容 1. リスボンInformal WG 対面会議開催に至る経緯 2. ミネアポリス会議以後の活動 3. S5(R3) コンセプトペーパーの変遷 4. S5(R3) に向けて検討されるべき事項 5. S5(R3)
S5(R3) Informal 医薬品の生殖発生毒性試験法 ( 改訂 ) 日本製薬工業協会 ICH プロジェクト委員会 S5(R3) Informal WG トピックリーダー藤原道夫 1 本日の内容 1. リスボンInformal WG 対面会議開催に至る経緯 2. ミネアポリス会議以後の活動 3. S5(R3) コンセプトペーパーの変遷 4. S5(R3) に向けて検討されるべき事項 5. S5(R3)
ータについては Table 3 に示した 両製剤とも投与後血漿中ロスバスタチン濃度が上昇し 試験製剤で 4.7±.7 時間 標準製剤で 4.6±1. 時間に Tmaxに達した また Cmaxは試験製剤で 6.3±3.13 標準製剤で 6.8±2.49 であった AUCt は試験製剤で 62.24±2
 ロスバスタチン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロスバスタチンは HMG-CoA 還元酵素を競合的に阻害することにより HMG-CoA のメバロン酸への変更を減少させ コレステロール生合成における早期の律速段階を抑制する高コレステロール血症治療剤である 今回 ロスバスタチン錠 mg TCK とクレストール 錠 mg の生物学的同等性を検討するため
ロスバスタチン錠 mg TCK の生物学的同等性試験 バイオアベイラビリティの比較 辰巳化学株式会社 はじめにロスバスタチンは HMG-CoA 還元酵素を競合的に阻害することにより HMG-CoA のメバロン酸への変更を減少させ コレステロール生合成における早期の律速段階を抑制する高コレステロール血症治療剤である 今回 ロスバスタチン錠 mg TCK とクレストール 錠 mg の生物学的同等性を検討するため
資料4-4 木酢液の検討状況について
 資料 4-4 木酢液の検討状況について 木酢液の薬効 薬害 安全性等に係る検討に関し 第 6 回及び第 8 回合同 会合において 以下のとおり整理された 安全性 薬効 薬害に係る試験の実施 ( 論点 ) 第 6 回合同会合において検討した結果 変異原性試験 ( 復帰突然変異原性試験 ) の結果について指摘があった また 1) 木酢液 に含まれるホルムアルデヒドについては IARC( 国際ガン研究機関
資料 4-4 木酢液の検討状況について 木酢液の薬効 薬害 安全性等に係る検討に関し 第 6 回及び第 8 回合同 会合において 以下のとおり整理された 安全性 薬効 薬害に係る試験の実施 ( 論点 ) 第 6 回合同会合において検討した結果 変異原性試験 ( 復帰突然変異原性試験 ) の結果について指摘があった また 1) 木酢液 に含まれるホルムアルデヒドについては IARC( 国際ガン研究機関
あった AUCtはで ± ng hr/ml で ± ng hr/ml であった 2. バイオアベイラビリティの比較およびの薬物動態パラメータにおける分散分析の結果を Table 4 に示した また 得られた AUCtおよび Cmaxについてとの対数値
 モンテルカストチュアブル錠 5mg TCK の生物学的同等性試験 ( 口中溶解後 水なし投与 ) バイオアベイラビリティの比較 辰巳化学株式会社 はじめにモンテルカストナトリウムは アレルギーのメディエーターの 1 つであるロイコトリエン (LT) の受容体の内 cyslt1 受容体を遮断する抗アレルギー薬である 今回 モンテルカストチュアブル錠 5mg TCK とキプレス チュアブル錠 5mg の生物学的同等性を検討するため
モンテルカストチュアブル錠 5mg TCK の生物学的同等性試験 ( 口中溶解後 水なし投与 ) バイオアベイラビリティの比較 辰巳化学株式会社 はじめにモンテルカストナトリウムは アレルギーのメディエーターの 1 つであるロイコトリエン (LT) の受容体の内 cyslt1 受容体を遮断する抗アレルギー薬である 今回 モンテルカストチュアブル錠 5mg TCK とキプレス チュアブル錠 5mg の生物学的同等性を検討するため
( 問 ) 日本の現代の食生活等において 健康への影響に気をつけなければならないと考える項目はどれですか? その必要が大きい順に 10 個選んでください 1. 病原性微生物 2. ふぐ毒 キノコの毒等の自然毒 3. 農薬の残留 4. 食品添加物 5. 動物用医薬品の畜産物への残留 6. アクリルアミ
 資料 4 食品安全委員会における農薬の食品健康影響評価について 内閣府食品安全委員会事務局 ( 問 ) 日本の現代の食生活等において 健康への影響に気をつけなければならないと考える項目はどれですか? その必要が大きい順に 10 個選んでください 1. 病原性微生物 2. ふぐ毒 キノコの毒等の自然毒 3. 農薬の残留 4. 食品添加物 5. 動物用医薬品の畜産物への残留 6. アクリルアミド クロロプロパノール等
資料 4 食品安全委員会における農薬の食品健康影響評価について 内閣府食品安全委員会事務局 ( 問 ) 日本の現代の食生活等において 健康への影響に気をつけなければならないと考える項目はどれですか? その必要が大きい順に 10 個選んでください 1. 病原性微生物 2. ふぐ毒 キノコの毒等の自然毒 3. 農薬の残留 4. 食品添加物 5. 動物用医薬品の畜産物への残留 6. アクリルアミド クロロプロパノール等
( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 教授 花房俊昭 宮村昌利 副査副査 教授教授 朝 日 通 雄 勝 間 田 敬 弘 副査 教授 森田大 主論文題名 Effects of Acarbose on the Acceleration of Postprandial
 ( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 花房俊昭 宮村昌利 副査副査 朝 日 通 雄 勝 間 田 敬 弘 副査 森田大 主論文題名 Effects of Acarbose on the Acceleration of Postprandial Hyperglycemia-Induced Pathological Changes Induced by Intermittent
( 様式甲 5) 学位論文内容の要旨 論文提出者氏名 論文審査担当者 主査 花房俊昭 宮村昌利 副査副査 朝 日 通 雄 勝 間 田 敬 弘 副査 森田大 主論文題名 Effects of Acarbose on the Acceleration of Postprandial Hyperglycemia-Induced Pathological Changes Induced by Intermittent
前立腺癌は男性特有の癌で 米国においては癌死亡者数の第 2 位 ( 約 20%) を占めてい ます 日本でも前立腺癌の罹患率 死亡者数は急激に上昇しており 現在は重篤な男性悪性腫瘍疾患の1つとなって図 1 います 図 1 初期段階の前立腺癌は男性ホルモン ( アンドロゲン ) に反応し増殖します そ
 再発した前立腺癌の増殖を制御する新たな分子メカニズムの発見乳癌治療薬が効果的 発表者筑波大学先端領域学際研究センター教授柳澤純 (junny@agbi.tsukuba.ac.jp TEL: 029-853-7320) ポイント 女性ホルモンが制御する新たな前立腺癌の増殖 細胞死メカニズムを発見 女性ホルモン及び女性ホルモン抑制剤は ERβ 及び KLF5 を通じ FOXO1 の発現量を変化することで前立腺癌の増殖
再発した前立腺癌の増殖を制御する新たな分子メカニズムの発見乳癌治療薬が効果的 発表者筑波大学先端領域学際研究センター教授柳澤純 (junny@agbi.tsukuba.ac.jp TEL: 029-853-7320) ポイント 女性ホルモンが制御する新たな前立腺癌の増殖 細胞死メカニズムを発見 女性ホルモン及び女性ホルモン抑制剤は ERβ 及び KLF5 を通じ FOXO1 の発現量を変化することで前立腺癌の増殖
略語一覧 略語 略していない表現 ( 英 ) 略していない表現 ( 日 ) HPLC high performance liquid chromatography 高速液体クロマトグラフィー LMB Leucomethylene blue ロイコメチレンブルー MAO monoamine oxida
 目次 1. 非臨床試験計画概略...4 2. 薬理試験...5 3. 薬物動態試験...7 4. 毒性試験...8 5. 総括及び結論...10 6. 参考文献一覧...12 1 略語一覧 略語 略していない表現 ( 英 ) 略していない表現 ( 日 ) HPLC high performance liquid chromatography 高速液体クロマトグラフィー LMB Leucomethylene
目次 1. 非臨床試験計画概略...4 2. 薬理試験...5 3. 薬物動態試験...7 4. 毒性試験...8 5. 総括及び結論...10 6. 参考文献一覧...12 1 略語一覧 略語 略していない表現 ( 英 ) 略していない表現 ( 日 ) HPLC high performance liquid chromatography 高速液体クロマトグラフィー LMB Leucomethylene
CTD 第 2 部 2.6 非臨床試験の概要文及び概要表 毒性試験の概要文 MSD 株式会社
 CTD 第 2 部 MSD 株式会社 目次 頁 表一覧... 2 略号及び用語の定義... 3 2.6.6.1 まとめ... 4 2.6.6.2 単回投与毒性試験... 9 2.6.6.3 反復投与毒性試験... 10 2.6.6.4 遺伝毒性試験... 24 2.6.6.5 がん原性試験... 26 2.6.6.6 生殖発生毒性試験... 29 2.6.6.7 局所刺激性試験... 37 2.6.6.8
CTD 第 2 部 MSD 株式会社 目次 頁 表一覧... 2 略号及び用語の定義... 3 2.6.6.1 まとめ... 4 2.6.6.2 単回投与毒性試験... 9 2.6.6.3 反復投与毒性試験... 10 2.6.6.4 遺伝毒性試験... 24 2.6.6.5 がん原性試験... 26 2.6.6.6 生殖発生毒性試験... 29 2.6.6.7 局所刺激性試験... 37 2.6.6.8
Untitled
 上原記念生命科学財団研究報告集, 25 (2011) 86. 線虫 C. elegans およびマウスをモデル動物とした体細胞レベルで生じる性差の解析 井上英樹 Key words: 性差, ストレス応答,DMRT 立命館大学生命科学部生命医科学科 緒言性差は雌雄の性に分かれた動物にみられ, 生殖能力の違いだけでなく形態, 行動などそれぞれの性の間でみられる様々な差異と定義される. 性差は, 形態や行動だけでなく疾患の発症リスクの男女差といった生理的なレベルの差異も含まれる.
上原記念生命科学財団研究報告集, 25 (2011) 86. 線虫 C. elegans およびマウスをモデル動物とした体細胞レベルで生じる性差の解析 井上英樹 Key words: 性差, ストレス応答,DMRT 立命館大学生命科学部生命医科学科 緒言性差は雌雄の性に分かれた動物にみられ, 生殖能力の違いだけでなく形態, 行動などそれぞれの性の間でみられる様々な差異と定義される. 性差は, 形態や行動だけでなく疾患の発症リスクの男女差といった生理的なレベルの差異も含まれる.
別紙様式 (Ⅱ)-1 添付ファイル用 商品名 : イチョウ葉脳内 α( アルファ ) 安全性評価シート 食経験の評価 1 喫食実績による食経験の評価 ( 喫食実績が あり の場合 : 実績に基づく安全性の評価を記載 ) 弊社では当該製品 イチョウ葉脳内 α( アルファ ) と同一処方の製品を 200
 商品名 : イチョウ葉脳内 α( アルファ ) 安全性評価シート 食経験の評価 1 喫食実績による食経験の評価 ( 喫食実績が あり の場合 : 実績に基づく安全性の評価を記載 ) 弊社では当該製品 イチョウ葉脳内 α( アルファ ) と同一処方の製品を 2003 年 1 月より全国で販売しており これまでに累計 350 万袋以上の販売実績がある 健康被害情報について お客様より健康食品相談室に申告があった内容を解析したところ
商品名 : イチョウ葉脳内 α( アルファ ) 安全性評価シート 食経験の評価 1 喫食実績による食経験の評価 ( 喫食実績が あり の場合 : 実績に基づく安全性の評価を記載 ) 弊社では当該製品 イチョウ葉脳内 α( アルファ ) と同一処方の製品を 2003 年 1 月より全国で販売しており これまでに累計 350 万袋以上の販売実績がある 健康被害情報について お客様より健康食品相談室に申告があった内容を解析したところ
アミヴィッド静注 CTD 第 2 部 2.1 第 2 部から第 5 部の目次 富士フイルム RI ファーマ株式会社
 CTD 第 2 部 富士フイルム RI ファーマ株式会社 ( 空白ページ ) 2 第 2 部 ( モジュール 2): CTD の概要 ( サマリー ) ---------------------------------------------- 第 2 巻 2.2 緒言 2.3 品質に関する概括資料緒言 2.3.S 原薬 (AV-105, ) 2.3.S 原薬 ( フロルベタピル ( 18 F),
CTD 第 2 部 富士フイルム RI ファーマ株式会社 ( 空白ページ ) 2 第 2 部 ( モジュール 2): CTD の概要 ( サマリー ) ---------------------------------------------- 第 2 巻 2.2 緒言 2.3 品質に関する概括資料緒言 2.3.S 原薬 (AV-105, ) 2.3.S 原薬 ( フロルベタピル ( 18 F),
2. 改訂内容および改訂理由 2.1. その他の注意 [ 厚生労働省医薬食品局安全対策課事務連絡に基づく改訂 ] 改訂後 ( 下線部 : 改訂部分 ) 10. その他の注意 (1)~(3) 省略 (4) 主に 50 歳以上を対象に実施された海外の疫学調査において 選択的セロトニン再取り込み阻害剤及び
![2. 改訂内容および改訂理由 2.1. その他の注意 [ 厚生労働省医薬食品局安全対策課事務連絡に基づく改訂 ] 改訂後 ( 下線部 : 改訂部分 ) 10. その他の注意 (1)~(3) 省略 (4) 主に 50 歳以上を対象に実施された海外の疫学調査において 選択的セロトニン再取り込み阻害剤及び 2. 改訂内容および改訂理由 2.1. その他の注意 [ 厚生労働省医薬食品局安全対策課事務連絡に基づく改訂 ] 改訂後 ( 下線部 : 改訂部分 ) 10. その他の注意 (1)~(3) 省略 (4) 主に 50 歳以上を対象に実施された海外の疫学調査において 選択的セロトニン再取り込み阻害剤及び](/thumbs/91/105459093.jpg) - 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 使用上の注意改訂のお知らせ 2010 年 8 月 製造販売元 選択的セロトニン再取り込み阻害剤 ( 一般名 : パロキセチン塩酸塩水和物 ) 謹啓時下益々ご清栄のこととお慶び申し上げます 平素は 弊社医薬品につきまして格別のご高配を賜り 厚く御礼申し上げます さて この度 の 使用上の注意 を改訂致しましたのでお知らせ申し上げます なお
- 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 使用上の注意改訂のお知らせ 2010 年 8 月 製造販売元 選択的セロトニン再取り込み阻害剤 ( 一般名 : パロキセチン塩酸塩水和物 ) 謹啓時下益々ご清栄のこととお慶び申し上げます 平素は 弊社医薬品につきまして格別のご高配を賜り 厚く御礼申し上げます さて この度 の 使用上の注意 を改訂致しましたのでお知らせ申し上げます なお
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 <その他分野 ( 消化器官用薬 解毒剤 その他 )> 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号
 資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
有害性総合評価
 別冊 6 初期リスク評価書 No.55( 初期 ) ニトロメタン (Nitromethane) 目次 本文 1 別添 1 有害性総合評価表 6 別添 2 有害性評価書 9 別添 3 ばく露作業報告集計表 20 別添 4 測定分析法 21 2011 年 7 月 厚生労働省 化学物質のリスク評価検討会 1 物理的性状等 (1) 化学物質の基本情報名称 : ニトロメタン別名 :Nitrocarbol 化学式
別冊 6 初期リスク評価書 No.55( 初期 ) ニトロメタン (Nitromethane) 目次 本文 1 別添 1 有害性総合評価表 6 別添 2 有害性評価書 9 別添 3 ばく露作業報告集計表 20 別添 4 測定分析法 21 2011 年 7 月 厚生労働省 化学物質のリスク評価検討会 1 物理的性状等 (1) 化学物質の基本情報名称 : ニトロメタン別名 :Nitrocarbol 化学式
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠 50mg 医薬品リスク管理計画書 (RMP) の概要 有効成分 タペンタ 錠 100mg 製造販売業者 ヤンセンファーマ株式会社 薬効分類 821 提出年月 平成 30 年
 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
第 2 部 CTD の概要 一般名 : バンデタニブ 版番号 : 薬物動態試験の概要文 カプレルサ 錠 100 mg 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています
 第 2 部 CTD の概要 一般名 : バンデタニブ 版番号 : 2.6.4 薬物動態試験の概要文 カプレルサ 錠 100 mg 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています 2.6.4 薬物動態試験の概要文一般名 : バンデタニブ 目次 頁 目次...2 略語及び専門用語一覧表...6 1 まとめ...
第 2 部 CTD の概要 一般名 : バンデタニブ 版番号 : 2.6.4 薬物動態試験の概要文 カプレルサ 錠 100 mg 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています 2.6.4 薬物動態試験の概要文一般名 : バンデタニブ 目次 頁 目次...2 略語及び専門用語一覧表...6 1 まとめ...
ザガーロ使用上の注意の解説
 市販直後調査平成 28 年 6 月 ~ 平成 28 年 12 月 2016 年 6 月作成 - 医薬品の適正使用に欠かせない情報です 必ずお読みください - 新医薬品の 使用上の注意 の解説 男性型脱毛症治療薬 処方箋医薬品 ( 注意 - 医師等の処方箋により使用すること ) デュタステリドカプセル 禁忌 ( 次の患者には投与しないこと ) (1) 本剤の成分及び他の 5α 還元酵素阻害薬に対し過敏症の既往歴のある患者
市販直後調査平成 28 年 6 月 ~ 平成 28 年 12 月 2016 年 6 月作成 - 医薬品の適正使用に欠かせない情報です 必ずお読みください - 新医薬品の 使用上の注意 の解説 男性型脱毛症治療薬 処方箋医薬品 ( 注意 - 医師等の処方箋により使用すること ) デュタステリドカプセル 禁忌 ( 次の患者には投与しないこと ) (1) 本剤の成分及び他の 5α 還元酵素阻害薬に対し過敏症の既往歴のある患者
資料 6 rash2 マウス ( 短期発がんモデル ) の特性と品質管理 財団法人実験動物中央研究所 浦野浩司 2018/3/7 1
 資料 6 rash2 マウス ( 短期発がんモデル ) の特性と品質管理 財団法人実験動物中央研究所 浦野浩司 2018/3/7 1 本日の話題 1. rash2 マウスとは? 2. 開発経緯と現状 3. 実質的標準動物としての品質管理 2 本日の話題 1. rash2 マウスとは? 2. 開発経緯と現状 3. 実質的標準動物としての品質管理 3 短期発がん性試験モデルの概要 Tg マウスにがん原物質
資料 6 rash2 マウス ( 短期発がんモデル ) の特性と品質管理 財団法人実験動物中央研究所 浦野浩司 2018/3/7 1 本日の話題 1. rash2 マウスとは? 2. 開発経緯と現状 3. 実質的標準動物としての品質管理 2 本日の話題 1. rash2 マウスとは? 2. 開発経緯と現状 3. 実質的標準動物としての品質管理 3 短期発がん性試験モデルの概要 Tg マウスにがん原物質
2.4 非臨床試験の概括評価 乾燥組織培養不活化狂犬病ワクチン ラビピュール筋注用 第 2 部 ( モジュール 2): CTD の概要 ( サマリー ) 2.4 非臨床試験の概括評価 1
 乾燥組織培養不活化狂犬病ワクチン ラビピュール筋注用 第 2 部 ( モジュール 2): CTD の概要 ( サマリー ) 1 目次 目次... 2 略号表... 3 用語の説明... 3... 4 2.4.1 非臨床試験計画概略... 4 2.4.2 薬理試験... 7 2.4.2.1 効力を裏付ける試験... 7 2.4.2.2 副次的薬理試験... 8 2.4.2.3 安全性薬理試験... 8
乾燥組織培養不活化狂犬病ワクチン ラビピュール筋注用 第 2 部 ( モジュール 2): CTD の概要 ( サマリー ) 1 目次 目次... 2 略号表... 3 用語の説明... 3... 4 2.4.1 非臨床試験計画概略... 4 2.4.2 薬理試験... 7 2.4.2.1 効力を裏付ける試験... 7 2.4.2.2 副次的薬理試験... 8 2.4.2.3 安全性薬理試験... 8
加工デンプン(栄養学的観点からの検討)
 加工デンプン ( 栄養学的観点からの検討 ) 加工デンプンは 未加工デンプンが有する物理化学的性状を変化させ 利便性の拡大を図るために加工処理を施したものであり 通常 未加工デンプンに代わるものとして用いられる デンプンは三大栄養素の一つである炭水化物の摂取源であることから 炭水化物の摂取量 加工デンプンの摂取量 加工デンプンの体内動態 ( 消化酵素分解率 ) から 加工デンプンの食品への使用について栄養学的観点からの検討を行う
加工デンプン ( 栄養学的観点からの検討 ) 加工デンプンは 未加工デンプンが有する物理化学的性状を変化させ 利便性の拡大を図るために加工処理を施したものであり 通常 未加工デンプンに代わるものとして用いられる デンプンは三大栄養素の一つである炭水化物の摂取源であることから 炭水化物の摂取量 加工デンプンの摂取量 加工デンプンの体内動態 ( 消化酵素分解率 ) から 加工デンプンの食品への使用について栄養学的観点からの検討を行う
Ⅰ. 改訂内容 ( 部変更 ) ペルサンチン 錠 12.5 改 訂 後 改 訂 前 (1) 本剤投与中の患者に本薬の注射剤を追加投与した場合, 本剤の作用が増強され, 副作用が発現するおそれがあるので, 併用しないこと ( 過量投与 の項参照) 本剤投与中の患者に本薬の注射剤を追加投与した場合, 本
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意 改訂のお知らせ 2006 年 1 月日本ベーリンガーインゲルハイム株式会社 注 ) 処方せん医薬品 ( ジピリダモール製剤 ) = 登録商標注 ) 注意 - 医師等の処方せんにより使用すること 謹啓時下ますますご清祥のこととお慶び申し上げます 平素は弊社製品につきましてご愛顧を賜り厚く御礼申し上げます さて, この度, 自主改訂によりペルサンチン
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 使用上の注意 改訂のお知らせ 2006 年 1 月日本ベーリンガーインゲルハイム株式会社 注 ) 処方せん医薬品 ( ジピリダモール製剤 ) = 登録商標注 ) 注意 - 医師等の処方せんにより使用すること 謹啓時下ますますご清祥のこととお慶び申し上げます 平素は弊社製品につきましてご愛顧を賜り厚く御礼申し上げます さて, この度, 自主改訂によりペルサンチン
審査結果 平成 23 年 4 月 5 日 [ 販 売 名 ] ゴナールエフ皮下注用 150 [ 一 般 名 ] ホリトロピンアルファ ( 遺伝子組換え ) [ 申請者名 ] メルクセローノ株式会社 [ 申請年月日 ] 平成 22 年 7 月 21 日 [ 審査結果 ] 提出された資料から 本剤の視床
![審査結果 平成 23 年 4 月 5 日 [ 販 売 名 ] ゴナールエフ皮下注用 150 [ 一 般 名 ] ホリトロピンアルファ ( 遺伝子組換え ) [ 申請者名 ] メルクセローノ株式会社 [ 申請年月日 ] 平成 22 年 7 月 21 日 [ 審査結果 ] 提出された資料から 本剤の視床 審査結果 平成 23 年 4 月 5 日 [ 販 売 名 ] ゴナールエフ皮下注用 150 [ 一 般 名 ] ホリトロピンアルファ ( 遺伝子組換え ) [ 申請者名 ] メルクセローノ株式会社 [ 申請年月日 ] 平成 22 年 7 月 21 日 [ 審査結果 ] 提出された資料から 本剤の視床](/thumbs/92/108897527.jpg) 審査報告書 平成 23 年 4 月 5 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販 売 名 ] ゴナールエフ皮下注用 150 [ 一 般 名 ] ホリトロピンアルファ ( 遺伝子組換え ) [ 申請者名 ] メルクセローノ株式会社 [ 申請年月日 ] 平成 22 年 7 月 21 日 [ 剤形 含量
審査報告書 平成 23 年 4 月 5 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販 売 名 ] ゴナールエフ皮下注用 150 [ 一 般 名 ] ホリトロピンアルファ ( 遺伝子組換え ) [ 申請者名 ] メルクセローノ株式会社 [ 申請年月日 ] 平成 22 年 7 月 21 日 [ 剤形 含量
アスナプレビル 毒性試験の概要文 Page 2 用語及び略語一覧 8-MOP 8-methoxypsoralen 8- メトキシソラレン ALP alkaline phosphatase アルカリホスファターゼ ALT alanine aminotransferase アラニンアミノトラ
 アスナプレビル 2.6.6 毒性試験の概要文 Page 1 CTD 第 2 部 2.6 非臨床試験の概要文及び概要表 2.6.6 毒性試験の概要文 ブリストル マイヤーズ株式会社 アスナプレビル 2.6.6 毒性試験の概要文 Page 2 用語及び略語一覧 8-MOP 8-methoxypsoralen 8- メトキシソラレン ALP alkaline phosphatase アルカリホスファターゼ
アスナプレビル 2.6.6 毒性試験の概要文 Page 1 CTD 第 2 部 2.6 非臨床試験の概要文及び概要表 2.6.6 毒性試験の概要文 ブリストル マイヤーズ株式会社 アスナプレビル 2.6.6 毒性試験の概要文 Page 2 用語及び略語一覧 8-MOP 8-methoxypsoralen 8- メトキシソラレン ALP alkaline phosphatase アルカリホスファターゼ
DCHP
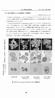
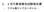 2. 2 1. 1) 2) 2 Crj:CD(SD)IGS SPF 0 240 1200 6000 ppm 2 F0 10 F0 10 F1 21 F1 3 10 F1 3 10 F2 21 0 240 1200 6000 ppm 1 F0 0 15.88 79.57 401.8 mg/kg/day F0 0 20.80 104.19 510.7 mg/kg/day F1 0 17.84 89.89
2. 2 1. 1) 2) 2 Crj:CD(SD)IGS SPF 0 240 1200 6000 ppm 2 F0 10 F0 10 F1 21 F1 3 10 F1 3 10 F2 21 0 240 1200 6000 ppm 1 F0 0 15.88 79.57 401.8 mg/kg/day F0 0 20.80 104.19 510.7 mg/kg/day F1 0 17.84 89.89
られる 糖尿病を合併した高血圧の治療の薬物治療の第一選択薬はアンジオテンシン変換酵素 (ACE) 阻害薬とアンジオテンシン II 受容体拮抗薬 (ARB) である このクラスの薬剤は単なる降圧効果のみならず 様々な臓器保護作用を有しているが ACE 阻害薬や ARB のプラセボ比較試験で糖尿病の新規
 論文の内容の要旨 論文題目アンジオテンシン受容体拮抗薬テルミサルタンの メタボリックシンドロームに対する効果の検討 指導教員門脇孝教授 東京大学大学院医学系研究科 平成 19 年 4 月入学 医学博士課程 内科学専攻 氏名廣瀬理沙 要旨 背景 目的 わが国の死因の第二位と第三位を占める心筋梗塞や脳梗塞などの心血管疾患を引き起こす基盤となる病態として 過剰なエネルギー摂取と運動不足などの生活習慣により内臓脂肪が蓄積する内臓脂肪型肥満を中心に
論文の内容の要旨 論文題目アンジオテンシン受容体拮抗薬テルミサルタンの メタボリックシンドロームに対する効果の検討 指導教員門脇孝教授 東京大学大学院医学系研究科 平成 19 年 4 月入学 医学博士課程 内科学専攻 氏名廣瀬理沙 要旨 背景 目的 わが国の死因の第二位と第三位を占める心筋梗塞や脳梗塞などの心血管疾患を引き起こす基盤となる病態として 過剰なエネルギー摂取と運動不足などの生活習慣により内臓脂肪が蓄積する内臓脂肪型肥満を中心に
PowerPoint プレゼンテーション
 北海道大学病院市民公開講座前立腺癌について知ろう! 前立腺がんの薬物治療 北海道大学大学院医学研究院腎泌尿器外科学分野 大澤崇宏 前立腺癌の治療 限局性がん局所進行がん転移がん 前立腺癌の治療 限局性がん局所進行がん転移がん PSA
北海道大学病院市民公開講座前立腺癌について知ろう! 前立腺がんの薬物治療 北海道大学大学院医学研究院腎泌尿器外科学分野 大澤崇宏 前立腺癌の治療 限局性がん局所進行がん転移がん 前立腺癌の治療 限局性がん局所進行がん転移がん PSA
アスナプレビル 2.4 非臨床試験の概括評価 Page 2 用語及び略語一覧 ADME absorption, distribution, metabolism and excretion 吸収 分布 代謝及び排泄 ALP alkaline phosphatase アルカリフォスファターゼ ALT
 アスナプレビル 2.4 非臨床試験の概括評価 Page 1 CTD 第 2 部 2.4 非臨床試験の概括評価 ブリストル マイヤーズ株式会社 アスナプレビル 2.4 非臨床試験の概括評価 Page 2 用語及び略語一覧 ADME absorption, distribution, metabolism and excretion 吸収 分布 代謝及び排泄 ALP alkaline phosphatase
アスナプレビル 2.4 非臨床試験の概括評価 Page 1 CTD 第 2 部 2.4 非臨床試験の概括評価 ブリストル マイヤーズ株式会社 アスナプレビル 2.4 非臨床試験の概括評価 Page 2 用語及び略語一覧 ADME absorption, distribution, metabolism and excretion 吸収 分布 代謝及び排泄 ALP alkaline phosphatase
PowerPoint プレゼンテーション
 第 2 回サラシア属植物シンポジウム講演要旨平成 21 年 8 月 25 日近畿大学において サラシア属植物エキス含有飲料の食後血糖上昇抑制効果と長期摂取および過剰摂取の安全性の検討 平成 21 年 8 月 25 日 企画室北林広巳 1 サラシアエキスの有効性と安全性 サラシア属植物含有飲料について 有効性試験 安全性試験の結果をご報告いたします 注 ) TB0018 コタラノール L はサラシア属植物エキス含有飲料を指します
第 2 回サラシア属植物シンポジウム講演要旨平成 21 年 8 月 25 日近畿大学において サラシア属植物エキス含有飲料の食後血糖上昇抑制効果と長期摂取および過剰摂取の安全性の検討 平成 21 年 8 月 25 日 企画室北林広巳 1 サラシアエキスの有効性と安全性 サラシア属植物含有飲料について 有効性試験 安全性試験の結果をご報告いたします 注 ) TB0018 コタラノール L はサラシア属植物エキス含有飲料を指します
Microsoft Word - m2-6-4-pharmacokinetics-written-summary_ver 1.9_類縁物質おきかえ-1…
 1 目次...8 2.6.4.1 まとめ...8 2.6.4.1.1 Org 25969 の薬物動態...8 2.6.4.1.2 Org 25969 がロクロニウムの薬物動態特性に及ぼす影響... 11 2.6.4.1.3 Org 48302 の薬物動態...12 2.6.4.2 分析法...16 2.6.4.2.1 ラット血漿中の Org 25969 を測定する液体クロマトグラフィー -タンデム質量分析法のバリデーション
1 目次...8 2.6.4.1 まとめ...8 2.6.4.1.1 Org 25969 の薬物動態...8 2.6.4.1.2 Org 25969 がロクロニウムの薬物動態特性に及ぼす影響... 11 2.6.4.1.3 Org 48302 の薬物動態...12 2.6.4.2 分析法...16 2.6.4.2.1 ラット血漿中の Org 25969 を測定する液体クロマトグラフィー -タンデム質量分析法のバリデーション
 ,...~,.'~ 表 2.6.2.2-26 試験管内 PAE 菌株薬剤 MIC (µg/ml) PAE (h) 1 MIC 4 MIC STFX 0.025 0.92 2.35 S. aureus FDA 209-P LVFX 0.20 0.68 2.68 CPFX 0.20 1.05 1.59 SPFX 0.10 0.35 1.07 STFX 0.025 2.33 1.14 E. coli KL-16
,...~,.'~ 表 2.6.2.2-26 試験管内 PAE 菌株薬剤 MIC (µg/ml) PAE (h) 1 MIC 4 MIC STFX 0.025 0.92 2.35 S. aureus FDA 209-P LVFX 0.20 0.68 2.68 CPFX 0.20 1.05 1.59 SPFX 0.10 0.35 1.07 STFX 0.025 2.33 1.14 E. coli KL-16
審査報告 (1) 別紙 平成 29 年 4 月 3 日 本申請において 申請者が提出した資料及び医薬品医療機器総合機構における審査の概略等は 以下 のとおりである 申請品目 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノ
![審査報告 (1) 別紙 平成 29 年 4 月 3 日 本申請において 申請者が提出した資料及び医薬品医療機器総合機構における審査の概略等は 以下 のとおりである 申請品目 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノ 審査報告 (1) 別紙 平成 29 年 4 月 3 日 本申請において 申請者が提出した資料及び医薬品医療機器総合機構における審査の概略等は 以下 のとおりである 申請品目 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノ](/thumbs/92/110667825.jpg) 審査報告書 平成 29 年 5 月 17 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノバルティスファーマ株式会社 [ 申請年月日 ] 平成 28 年 7 月 28 日 [ 剤形 含量
審査報告書 平成 29 年 5 月 17 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販売名 ] ジャドニュ顆粒分包 90 mg 同顆粒分包 360 mg [ 一般名 ] デフェラシロクス [ 申請者 ] ノバルティスファーマ株式会社 [ 申請年月日 ] 平成 28 年 7 月 28 日 [ 剤形 含量
PEGIFNα2b 目次 (1 of 2) 略語一覧表 毒性試験の概要文
 ペグインターフェロンアルファ 2b( 遺伝子組換え ) 第 2 部 CTD の概要 (6) 非臨床試験の概要文及び概要表 6 毒性試験の概要文 シェリング プラウ株式会社 PEGIFNα2b 目次 (1 of 2) 略語一覧表........................................................................... 1 2.6.6 毒性試験の概要文...............................................................
ペグインターフェロンアルファ 2b( 遺伝子組換え ) 第 2 部 CTD の概要 (6) 非臨床試験の概要文及び概要表 6 毒性試験の概要文 シェリング プラウ株式会社 PEGIFNα2b 目次 (1 of 2) 略語一覧表........................................................................... 1 2.6.6 毒性試験の概要文...............................................................
緒言
 CERA 2.2 緒言 Page 1 ミルセラ注シリンジ25 μg ミルセラ注シリンジ50 μg ミルセラ注シリンジ75 μg ミルセラ注シリンジ100 μg ミルセラ注シリンジ150 μg ミルセラ注シリンジ200 μg ミルセラ注シリンジ250 μg [ 腎性貧血 ] 第 2 部 CTD の概要 ( サマリー ) 2.2 緒言 中外製薬株式会社 CERA 2.2 緒言 Page 2 目次頁 2.2
CERA 2.2 緒言 Page 1 ミルセラ注シリンジ25 μg ミルセラ注シリンジ50 μg ミルセラ注シリンジ75 μg ミルセラ注シリンジ100 μg ミルセラ注シリンジ150 μg ミルセラ注シリンジ200 μg ミルセラ注シリンジ250 μg [ 腎性貧血 ] 第 2 部 CTD の概要 ( サマリー ) 2.2 緒言 中外製薬株式会社 CERA 2.2 緒言 Page 2 目次頁 2.2
目次 頁 表一覧...3 図一覧...4 略号及び用語の定義 まとめ 単回投与 ( 急性 ) 毒性 反復投与毒性 遺伝毒性 がん原性
 カンサイダス点滴静注用 50mg カンサイダス点滴静注用 70mg 第 2 部 ( モジュール 2) CTD の概要 ( サマリー ) - 毒性 - MSD 株式会社 目次 頁 表一覧...3 図一覧...4 略号及び用語の定義...5 2.6.6.1 まとめ...6 2.6.6.1.1 単回投与 ( 急性 ) 毒性...6 2.6.6.1.2 反復投与毒性...7 2.6.6.1.3 遺伝毒性...10
カンサイダス点滴静注用 50mg カンサイダス点滴静注用 70mg 第 2 部 ( モジュール 2) CTD の概要 ( サマリー ) - 毒性 - MSD 株式会社 目次 頁 表一覧...3 図一覧...4 略号及び用語の定義...5 2.6.6.1 まとめ...6 2.6.6.1.1 単回投与 ( 急性 ) 毒性...6 2.6.6.1.2 反復投与毒性...7 2.6.6.1.3 遺伝毒性...10
名称未設定-4
 Page 1 沈降インフルエンザワクチン H5N1 生研 1mL 第 2 部 ( モジュール 2):CTD の概要 ( サマリー ) 2.6 非臨床試験の概要文及び概要表 2.6.6 毒性試験の概要文 デンカ生研株式会社 沈降インフルエンザワクチン H5N1 生研 2.6.6 毒性試験の概要文 Page 2 沈降インフルエンザワクチン H5N1 生研 2.6.6 毒性試験の概要文 Page 3 目
Page 1 沈降インフルエンザワクチン H5N1 生研 1mL 第 2 部 ( モジュール 2):CTD の概要 ( サマリー ) 2.6 非臨床試験の概要文及び概要表 2.6.6 毒性試験の概要文 デンカ生研株式会社 沈降インフルエンザワクチン H5N1 生研 2.6.6 毒性試験の概要文 Page 2 沈降インフルエンザワクチン H5N1 生研 2.6.6 毒性試験の概要文 Page 3 目
ボンビバ錠 2.4 非臨床試験の概括評価 Page 1 ボンビバ錠 100mg ( イバンドロン酸ナトリウム水和物 ) [ 骨粗鬆症 ] 第 2 部 ( モジュール 2) CTD の概要 ( サマリー ) 2.4 非臨床試験の概括評価 中外製薬株式会社
![ボンビバ錠 2.4 非臨床試験の概括評価 Page 1 ボンビバ錠 100mg ( イバンドロン酸ナトリウム水和物 ) [ 骨粗鬆症 ] 第 2 部 ( モジュール 2) CTD の概要 ( サマリー ) 2.4 非臨床試験の概括評価 中外製薬株式会社 ボンビバ錠 2.4 非臨床試験の概括評価 Page 1 ボンビバ錠 100mg ( イバンドロン酸ナトリウム水和物 ) [ 骨粗鬆症 ] 第 2 部 ( モジュール 2) CTD の概要 ( サマリー ) 2.4 非臨床試験の概括評価 中外製薬株式会社](/thumbs/104/163593291.jpg) ボンビバ錠 2.4 非臨床試験の概括評価 Page 1 ボンビバ錠 100mg ( イバンドロン酸ナトリウム水和物 ) [ 骨粗鬆症 ] 第 2 部 ( モジュール 2) CTD の概要 ( サマリー ) 2.4 非臨床試験の概括評価 中外製薬株式会社 ボンビバ錠 2.4 非臨床試験の概括評価 Page 2 略語一覧略語 英名 和名 ALN Alendronate sodium hydrate アレンドロン酸ナトリウム水和物
ボンビバ錠 2.4 非臨床試験の概括評価 Page 1 ボンビバ錠 100mg ( イバンドロン酸ナトリウム水和物 ) [ 骨粗鬆症 ] 第 2 部 ( モジュール 2) CTD の概要 ( サマリー ) 2.4 非臨床試験の概括評価 中外製薬株式会社 ボンビバ錠 2.4 非臨床試験の概括評価 Page 2 略語一覧略語 英名 和名 ALN Alendronate sodium hydrate アレンドロン酸ナトリウム水和物
添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示され
 添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示されます 検索条件設定時の注意 検索はテキスト文章 (SGML 又は XML) が対象となっており 画像及び
添付文書情報 の検索方法 1. 検索条件を設定の上 検索実行 ボタンをクリックすると検索します 検索結果として 右フレームに該当する医療用医薬品の販売名の一覧が 販売名の昇順で表示されます 2. 右のフレームで参照したい販売名をクリックすると 新しいタブで該当する医療用医薬品の添付文書情報が表示されます 検索条件設定時の注意 検索はテキスト文章 (SGML 又は XML) が対象となっており 画像及び
葉酸とビタミンQ&A_201607改訂_ indd
 L FO AT E VI TAMI NB12 医療関係者用 葉酸 とビタミンB ビタミンB12 アリムタ投与に際して 警告 1 本剤を含むがん化学療法に際しては 緊急時に十分対応できる医療施設において がん化学療 法に十分な知識 経験を持つ医師のもとで 本剤の投与が適切と判断される症例についてのみ投 与すること 適応患者の選択にあたっては 各併用薬剤の添付文書を参照して十分注意すること また 治療開始に先立ち
L FO AT E VI TAMI NB12 医療関係者用 葉酸 とビタミンB ビタミンB12 アリムタ投与に際して 警告 1 本剤を含むがん化学療法に際しては 緊急時に十分対応できる医療施設において がん化学療 法に十分な知識 経験を持つ医師のもとで 本剤の投与が適切と判断される症例についてのみ投 与すること 適応患者の選択にあたっては 各併用薬剤の添付文書を参照して十分注意すること また 治療開始に先立ち
目次 生物薬剤学試験及び関連する分析法 背景及び概観 製剤開発過程 バイオアベイラビリティ メマンチン塩酸塩の絶対バイオアベイラビリティ メマン
 メマリー錠 5 mg メマリー錠 10 mg メマリー錠 20 mg ( メマンチン塩酸塩 ) CTD 第 2 部 CTD の概要 2.7 臨床概要 2.7.1 生物薬剤学試験及び関連する分析法 第一三共株式会社 1 M2-GD-4-9912 目次 2.7.1 生物薬剤学試験及び関連する分析法...6 2.7.1.1 背景及び概観...6 2.7.1.1.1 製剤開発過程...6 2.7.1.1.2
メマリー錠 5 mg メマリー錠 10 mg メマリー錠 20 mg ( メマンチン塩酸塩 ) CTD 第 2 部 CTD の概要 2.7 臨床概要 2.7.1 生物薬剤学試験及び関連する分析法 第一三共株式会社 1 M2-GD-4-9912 目次 2.7.1 生物薬剤学試験及び関連する分析法...6 2.7.1.1 背景及び概観...6 2.7.1.1.1 製剤開発過程...6 2.7.1.1.2
資料3 農薬の気中濃度評価値の設定について(案)
 資料 3 農薬の気中濃度評価値の設定について ( 案 ) 1. 気中濃度評価値の定義及び算出方法 1.1. 本事業における定義気中濃度評価値とは 人の健康を保護する観点から 街路樹や公園などで使用される農薬による人の健康への影響を評価する際の目安として 吸入毒性試験成績を基に適切な安全幅を見込んで設定する 一般に 気中濃度評価値以下の濃度であれば 人の健康に好ましくない影響が起きることはないと考えられる
資料 3 農薬の気中濃度評価値の設定について ( 案 ) 1. 気中濃度評価値の定義及び算出方法 1.1. 本事業における定義気中濃度評価値とは 人の健康を保護する観点から 街路樹や公園などで使用される農薬による人の健康への影響を評価する際の目安として 吸入毒性試験成績を基に適切な安全幅を見込んで設定する 一般に 気中濃度評価値以下の濃度であれば 人の健康に好ましくない影響が起きることはないと考えられる
添付文書の薬物動態情報 ~基本となる3つの薬物動態パラメータを理解する~
 SAJP.SA.18.02.0496(2) 添付文書の薬物動態情報 基本となる 3 つの 薬物動態パラメータを理解する 城西国際大学薬学部 臨床統計学研究室山村重雄 医療用医薬品添付文書とは 目的 : 患者の安全を確保し 適正使用を図るために必要な情報を医師 歯科医師および薬剤師などの医療関係者に提供する 法的規制 : 医薬品医療機器等法第 52 条で記載内容が定められ 医薬品の製造販売業者は医薬品には情報を付与することが義務
SAJP.SA.18.02.0496(2) 添付文書の薬物動態情報 基本となる 3 つの 薬物動態パラメータを理解する 城西国際大学薬学部 臨床統計学研究室山村重雄 医療用医薬品添付文書とは 目的 : 患者の安全を確保し 適正使用を図るために必要な情報を医師 歯科医師および薬剤師などの医療関係者に提供する 法的規制 : 医薬品医療機器等法第 52 条で記載内容が定められ 医薬品の製造販売業者は医薬品には情報を付与することが義務
スライド 1
 3 年次後期専門科目群 Ⅰ ( 必修科目 ) 2 単位 臨床薬理学 5 回目 生物薬剤学講座児玉庸夫 1 臨床薬理学は薬物治療学を支える 基礎として機能する 薬物治療学 臨床薬理学 治療薬や用量などの薬物治療の個別化 臨床薬物動態学 例えば TDM や薬物相互作用 医療薬学 例えば 調剤 製剤 服薬指導 在宅医療における訪問薬剤管理指導 2 臨薬 臨床薬理学は医薬品開発や臨床薬効評価などを行う学問である
3 年次後期専門科目群 Ⅰ ( 必修科目 ) 2 単位 臨床薬理学 5 回目 生物薬剤学講座児玉庸夫 1 臨床薬理学は薬物治療学を支える 基礎として機能する 薬物治療学 臨床薬理学 治療薬や用量などの薬物治療の個別化 臨床薬物動態学 例えば TDM や薬物相互作用 医療薬学 例えば 調剤 製剤 服薬指導 在宅医療における訪問薬剤管理指導 2 臨薬 臨床薬理学は医薬品開発や臨床薬効評価などを行う学問である
本書の読み方 使い方 ~ 各項目の基本構成 ~ * 本書は主に外来の日常診療で頻用される治療薬を取り上げています ❶ 特徴 01 HMG-CoA 代表的薬剤ピタバスタチン同種同効薬アトルバスタチン, ロスバスタチン HMG-CoA 還元酵素阻害薬は主に高 LDL コレステロール血症の治療目的で使 用
 本書の読み方 使い方 ~ 各項目の基本構成 ~ * 本書は主に外来の日常診療で頻用される治療薬を取り上げています ❶ 特徴 01 HMG-CoA 代表的薬剤ピタバスタチン同種同効薬アトルバスタチン, ロスバスタチン HMG-CoA 還元酵素阻害薬は主に高 LDL コレステロール血症の治療目的で使 用される その強力なコレステロール低下作用と, コレステロール低下作用を 介さない作用 ( 血管内皮機能改善作用,
本書の読み方 使い方 ~ 各項目の基本構成 ~ * 本書は主に外来の日常診療で頻用される治療薬を取り上げています ❶ 特徴 01 HMG-CoA 代表的薬剤ピタバスタチン同種同効薬アトルバスタチン, ロスバスタチン HMG-CoA 還元酵素阻害薬は主に高 LDL コレステロール血症の治療目的で使 用される その強力なコレステロール低下作用と, コレステロール低下作用を 介さない作用 ( 血管内皮機能改善作用,
添付文書がちゃんと読める 薬物動態学 著 山村重雄竹平理恵子城西国際大学薬学部臨床統計学
 添付文書がちゃんと読める 薬物動態学 著 山村重雄竹平理恵子城西国際大学薬学部臨床統計学 1 序章 吸収された薬物は, 体の中で ( distribution) します 分布 とは, 体の中で薬物がどのように存在しているかを示しています 体の中の薬物の 分布 には大きく 2 つの要素が関わっています 1 つは, 薬物の, もう 1 つは薬物のです 血液中では, 薬物の一部分は血液中のタンパク ( たとえばアルブミンや
添付文書がちゃんと読める 薬物動態学 著 山村重雄竹平理恵子城西国際大学薬学部臨床統計学 1 序章 吸収された薬物は, 体の中で ( distribution) します 分布 とは, 体の中で薬物がどのように存在しているかを示しています 体の中の薬物の 分布 には大きく 2 つの要素が関わっています 1 つは, 薬物の, もう 1 つは薬物のです 血液中では, 薬物の一部分は血液中のタンパク ( たとえばアルブミンや
2.6.4 薬物動態試験の概要文
 ポプスカイン 0.75% 注 75mg/10mL ポプスカイン 0.75% 注 150mg/20mL ポプスカイン 0.25% 注 25mg/10mL ポプスカイン 0.25% 注バッグ 250mg/100mL ポプスカイン 0.75% 注シリンジ 75mg/10mL ポプスカイン 0.25% 注シリンジ 25mg/10mL に関する資料 第 2 部 丸石製薬株式会社 薬物動態試験の化学構造式一覧表
ポプスカイン 0.75% 注 75mg/10mL ポプスカイン 0.75% 注 150mg/20mL ポプスカイン 0.25% 注 25mg/10mL ポプスカイン 0.25% 注バッグ 250mg/100mL ポプスカイン 0.75% 注シリンジ 75mg/10mL ポプスカイン 0.25% 注シリンジ 25mg/10mL に関する資料 第 2 部 丸石製薬株式会社 薬物動態試験の化学構造式一覧表
目次頁略号一覧表 まとめ 反復投与毒性試験 ラット ラット 7 日間経口投与試験及び 4 週間回復性試験 ( 試験番号 TX CTD ) 考察及び結論
 ソホスブビル 第 2 部 CTD の概要 2.6 非臨床試験の概要文及び概要表 2.6.6 毒性試験の概要文 ギリアド サイエンシズ株式会社 1 目次頁略号一覧表... 4 1 まとめ... 6 2 反復投与毒性試験... 7 2.1 ラット... 7 2.1.1 ラット 7 日間経口投与試験及び 4 週間回復性試験 ( 試験番号 TX-334-2012 CTD 4.2.3.2.1)... 7 3
ソホスブビル 第 2 部 CTD の概要 2.6 非臨床試験の概要文及び概要表 2.6.6 毒性試験の概要文 ギリアド サイエンシズ株式会社 1 目次頁略号一覧表... 4 1 まとめ... 6 2 反復投与毒性試験... 7 2.1 ラット... 7 2.1.1 ラット 7 日間経口投与試験及び 4 週間回復性試験 ( 試験番号 TX-334-2012 CTD 4.2.3.2.1)... 7 3
薬物動態開発の経緯 特性製品情報(3) 薬物動態に対する食事の影響 ( 外国人データ )(B66119)12) 品情報臨床成績臨床成績薬物動態薬物動態薬効薬理薬効薬理一般薬理 毒性一般薬理 毒性(2) 反復投与 (CV18546) 11) 日本人健康成人男性 6 例に アピキサバン 1 回 2.5
 薬物動態開発の経緯 特性製品情報2.5 1 25 5mgを空腹時に単回経口投与品情報また 日本人及び白人健康成人男性において アピキサバン 臨床成績臨床成績薬物動態薬物動態薬効薬理薬効薬理一般薬理 毒性一般薬理 毒性1. 血中濃度 (1) 単回投与 (CV18513) 1) 日本人健康成人男性 12 例に アピキサバン2.5 1mgを空腹時に単回経口投与 したとき 投与後 3 3.5 時間で最高血漿中濃度に達し
薬物動態開発の経緯 特性製品情報2.5 1 25 5mgを空腹時に単回経口投与品情報また 日本人及び白人健康成人男性において アピキサバン 臨床成績臨床成績薬物動態薬物動態薬効薬理薬効薬理一般薬理 毒性一般薬理 毒性1. 血中濃度 (1) 単回投与 (CV18513) 1) 日本人健康成人男性 12 例に アピキサバン2.5 1mgを空腹時に単回経口投与 したとき 投与後 3 3.5 時間で最高血漿中濃度に達し
スライド 1
 薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
薬生審査発 0328 第 1 号薬生安発 0328 第 2 号平成 28 年 3 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局安全対策課長 ( 公印省略 ) ビガバトリン製剤の使用に当たっての留意事項について ビガバトリン製剤 ( 販売名 : サブリル散分包 500mg 以下 本剤 という
ハーボニー 配合錠 第 2 部 ( モジュール 2):CTD の概要 ( サマリー ) 2.4 非臨床試験の概括評価 ギリアド サイエンシズ株式会社
 ハーボニー 配合錠 第 2 部 ( モジュール 2):CTD の概要 ( サマリー ) 2.4 非臨床試験の概括評価 ギリアド サイエンシズ株式会社 目次 1. 非臨床試験の概括評価... 10 1.1 非臨床試験計画概要... 10 1.1.1 レジパスビル... 10 1.1.2 レジパスビル / ソホスブビル... 11 2. 薬理試験... 13 2.1 効力を裏付ける試験... 13 2.1.1
ハーボニー 配合錠 第 2 部 ( モジュール 2):CTD の概要 ( サマリー ) 2.4 非臨床試験の概括評価 ギリアド サイエンシズ株式会社 目次 1. 非臨床試験の概括評価... 10 1.1 非臨床試験計画概要... 10 1.1.1 レジパスビル... 10 1.1.2 レジパスビル / ソホスブビル... 11 2. 薬理試験... 13 2.1 効力を裏付ける試験... 13 2.1.1
検査項目情報 1171 一次サンプル採取マニュアル 4. 内分泌学的検査 >> 4F. 性腺 胎盤ホルモンおよび結合蛋白 >> 4F090. トータル HCG-β ( インタクト HCG+ フリー HCG-β サブユニット ) トータル HCG-β ( インタクト HCG+ フリー HCG-β サブ
 chorionic gonadotropin 連絡先 : 3483 基本情報 4F090 HCGβサブユニット (β-hcg) 分析物 JLAC10 診療報酬 識別 材料 023 血清 測定法 結果識別 第 2 章 特掲診療料 D008 第 3 部 検査 第 1 節 検体検査料 第 1 款 検体検査実施料 ( 生化学的検査 (Ⅱ) ) 18 ヒト絨毛性ゴナドトロピン -β サブユニット (HCG-β)
chorionic gonadotropin 連絡先 : 3483 基本情報 4F090 HCGβサブユニット (β-hcg) 分析物 JLAC10 診療報酬 識別 材料 023 血清 測定法 結果識別 第 2 章 特掲診療料 D008 第 3 部 検査 第 1 節 検体検査料 第 1 款 検体検査実施料 ( 生化学的検査 (Ⅱ) ) 18 ヒト絨毛性ゴナドトロピン -β サブユニット (HCG-β)
Microsoft Word - 資料1【決定(差し替え)】調査結果報告書 調査会後修正
 資料 1 調査結果報告書 平成 25 年 12 月 2 日 独立行政法人医薬品医療機器総合機構 システアミン塩酸塩を配合した洗い流すヘアセット料の安全性に関する調査 I. 品目の概要 [ 対象 ] システアミン塩酸塩を配合した洗い流すヘアセット料 [ 効能の範囲 ] 髪型を整え 保持する等 [ 用法 ] 頭髪に塗布し 髪型を整える操作を行い その後洗浄する等 [ 備考 ] 特になし [ 調査担当部
資料 1 調査結果報告書 平成 25 年 12 月 2 日 独立行政法人医薬品医療機器総合機構 システアミン塩酸塩を配合した洗い流すヘアセット料の安全性に関する調査 I. 品目の概要 [ 対象 ] システアミン塩酸塩を配合した洗い流すヘアセット料 [ 効能の範囲 ] 髪型を整え 保持する等 [ 用法 ] 頭髪に塗布し 髪型を整える操作を行い その後洗浄する等 [ 備考 ] 特になし [ 調査担当部
スライド 1
 3 年次前期専門科目群 Ⅰ ( 必修科目 ) 2 単位 医療薬剤学 Ⅰ 8 回目 生物薬剤学講座児玉庸夫 1 医療薬剤学 Ⅰ は医薬品の有効性と 安全性を基礎から理解するための学問 医薬品 有効性 安全性 2 講義の内容 (1) 第 1 回薬物の生体内運命 第 2 回薬物の副作用 ( 薬物有害反応 )( 小テスト ) 第 3 回薬物の循環系移行と排泄 ( 小テスト ) 第 4 回薬物の投与方法と経口投与製剤
3 年次前期専門科目群 Ⅰ ( 必修科目 ) 2 単位 医療薬剤学 Ⅰ 8 回目 生物薬剤学講座児玉庸夫 1 医療薬剤学 Ⅰ は医薬品の有効性と 安全性を基礎から理解するための学問 医薬品 有効性 安全性 2 講義の内容 (1) 第 1 回薬物の生体内運命 第 2 回薬物の副作用 ( 薬物有害反応 )( 小テスト ) 第 3 回薬物の循環系移行と排泄 ( 小テスト ) 第 4 回薬物の投与方法と経口投与製剤
妊娠認識および胎盤形成時のウシ子宮におけるI型IFNシグナル調節機構に関する研究 [全文の要約]
![妊娠認識および胎盤形成時のウシ子宮におけるI型IFNシグナル調節機構に関する研究 [全文の要約] 妊娠認識および胎盤形成時のウシ子宮におけるI型IFNシグナル調節機構に関する研究 [全文の要約]](/thumbs/93/111654027.jpg) Title 妊娠認識および胎盤形成時のウシ子宮における I 型 IFN シグナル調節機構に関する研究 [ 全文の要約 ] Author(s) 白水, 貴大 Issue Date 2017-03-23 Doc URL http://hdl.handle.net/2115/65952 Type theses (doctoral - abstract of entire text) Note この博士論文全文の閲覧方法については
Title 妊娠認識および胎盤形成時のウシ子宮における I 型 IFN シグナル調節機構に関する研究 [ 全文の要約 ] Author(s) 白水, 貴大 Issue Date 2017-03-23 Doc URL http://hdl.handle.net/2115/65952 Type theses (doctoral - abstract of entire text) Note この博士論文全文の閲覧方法については
博第265号
 氏名 ( 本籍 ) くさま草間 かずや和哉 ( 埼玉県 ) 学位の種類博士 ( 薬学 ) 学位記番号 学位授与の日付 学位授与の要件 博第 265 号 平成 26 年 3 月 20 日 学位規則第 4 条第 1 項該当 学位論文題目妊娠成立に向けた子宮内膜間質細胞の脱落膜化と腺の成熟過程における Exchange protein directly activated by camp(epac) の役割
氏名 ( 本籍 ) くさま草間 かずや和哉 ( 埼玉県 ) 学位の種類博士 ( 薬学 ) 学位記番号 学位授与の日付 学位授与の要件 博第 265 号 平成 26 年 3 月 20 日 学位規則第 4 条第 1 項該当 学位論文題目妊娠成立に向けた子宮内膜間質細胞の脱落膜化と腺の成熟過程における Exchange protein directly activated by camp(epac) の役割
研究成果報告書
 様式 C-19 F-19 Z-19( 共通 ) 1. 研究開始当初の背景これまでバソプレッシンやオキシトシンは雌性生殖器 すなわち子宮や卵巣への作用が注目され臨床薬物の開発も行われてきたが 雄性生殖器への作用については依然として不明な点が多い そこで本研究では雄性生殖機能に注目してバソプレッシン受容体の機能解明を目的とする バソプレッシンは 9 つのアミノ酸から構成されるペプチドホルモンで 脳下垂体後葉から血液中に分泌された後
様式 C-19 F-19 Z-19( 共通 ) 1. 研究開始当初の背景これまでバソプレッシンやオキシトシンは雌性生殖器 すなわち子宮や卵巣への作用が注目され臨床薬物の開発も行われてきたが 雄性生殖器への作用については依然として不明な点が多い そこで本研究では雄性生殖機能に注目してバソプレッシン受容体の機能解明を目的とする バソプレッシンは 9 つのアミノ酸から構成されるペプチドホルモンで 脳下垂体後葉から血液中に分泌された後
児に対する母体の甲状腺機能低下症の影響を小さくするためにも 甲状腺機能低下症を甲状腺ホル モン薬の補充でしっかりとコントロールしておくのが無難と考えられます 3) 胎児 新生児の甲状腺機能低下症 胎児の甲状腺が生まれながらに ( 先天的に ) 欠損してしまう病気があります 通常 妊娠 8-10 週頃
 甲状腺機能低下症の妊娠に対する影響 1) 甲状腺機能低下症が母体に与える影響 甲状腺機能低下症があると流産 早産 胎盤早期剥離 産後甲状腺炎の頻度が増えると考えられています ただし流産や早産に関しては甲状腺機能低下症とはほとんど関連がなく甲状腺抗体陽性 ( 橋本病 ) と関連が深いとの考え方もあります 子癇前症や妊娠性高血圧 ( 妊娠中毒症 ) 児の出生時体重の異常 周産期死亡率は甲状腺機能低下症で頻度が上がるという報告とそうでない報告があり
甲状腺機能低下症の妊娠に対する影響 1) 甲状腺機能低下症が母体に与える影響 甲状腺機能低下症があると流産 早産 胎盤早期剥離 産後甲状腺炎の頻度が増えると考えられています ただし流産や早産に関しては甲状腺機能低下症とはほとんど関連がなく甲状腺抗体陽性 ( 橋本病 ) と関連が深いとの考え方もあります 子癇前症や妊娠性高血圧 ( 妊娠中毒症 ) 児の出生時体重の異常 周産期死亡率は甲状腺機能低下症で頻度が上がるという報告とそうでない報告があり
( 続紙 1 ) 京都大学 博士 ( 薬学 ) 氏名 大西正俊 論文題目 出血性脳障害におけるミクログリアおよびMAPキナーゼ経路の役割に関する研究 ( 論文内容の要旨 ) 脳内出血は 高血圧などの原因により脳血管が破綻し 脳実質へ出血した病態をいう 漏出する血液中の種々の因子の中でも 血液凝固に関
 Title 出血性脳障害におけるミクログリアおよびMAPキナーゼ経路の役割に関する研究 ( Abstract_ 要旨 ) Author(s) 大西, 正俊 Citation Kyoto University ( 京都大学 ) Issue Date 2010-03-23 URL http://hdl.handle.net/2433/120523 Right Type Thesis or Dissertation
Title 出血性脳障害におけるミクログリアおよびMAPキナーゼ経路の役割に関する研究 ( Abstract_ 要旨 ) Author(s) 大西, 正俊 Citation Kyoto University ( 京都大学 ) Issue Date 2010-03-23 URL http://hdl.handle.net/2433/120523 Right Type Thesis or Dissertation
ルリコナゾールルコナック爪外用液 5% CTD 第 2 部 ( モジュール2): CTDの概要 ( サマリー ) 2.4 非臨床試験の概括評価 佐藤製薬株式会社
 ルコナック爪外用液 5% CTD 第 2 部 ( モジュール2): CTDの概要 ( サマリー ) 佐藤製薬株式会社 略号一覧表 略号 英語 日本語 AUC area under the plasma concentration-time curve 血漿中濃度 - 時間曲線下面積 C. albicans Candida albicans - DMBA 7,12-dimethylbenz[a]anthracene
ルコナック爪外用液 5% CTD 第 2 部 ( モジュール2): CTDの概要 ( サマリー ) 佐藤製薬株式会社 略号一覧表 略号 英語 日本語 AUC area under the plasma concentration-time curve 血漿中濃度 - 時間曲線下面積 C. albicans Candida albicans - DMBA 7,12-dimethylbenz[a]anthracene
審議結果報告書 平成 30 年 1 1 月 2 0 日医薬 生活衛生局医薬品審査管理課 [ 販 売 名 ] セリンクロ錠 10mg [ 一 般 名 ] ナルメフェン塩酸塩水和物 [ 申請者名 ] 大塚製薬株式会社 [ 申請年月日 ] 平成 29 年 10 月 17 日 [ 審議結果 ] 平成 30
![審議結果報告書 平成 30 年 1 1 月 2 0 日医薬 生活衛生局医薬品審査管理課 [ 販 売 名 ] セリンクロ錠 10mg [ 一 般 名 ] ナルメフェン塩酸塩水和物 [ 申請者名 ] 大塚製薬株式会社 [ 申請年月日 ] 平成 29 年 10 月 17 日 [ 審議結果 ] 平成 30 審議結果報告書 平成 30 年 1 1 月 2 0 日医薬 生活衛生局医薬品審査管理課 [ 販 売 名 ] セリンクロ錠 10mg [ 一 般 名 ] ナルメフェン塩酸塩水和物 [ 申請者名 ] 大塚製薬株式会社 [ 申請年月日 ] 平成 29 年 10 月 17 日 [ 審議結果 ] 平成 30](/thumbs/103/158056963.jpg) 審議結果報告書 平成 30 年 1 1 月 2 0 日医薬 生活衛生局医薬品審査管理課 [ 販 売 名 ] セリンクロ錠 10mg [ 一 般 名 ] ナルメフェン塩酸塩水和物 [ 申請者名 ] 大塚製薬株式会社 [ 申請年月日 ] 平成 29 年 10 月 17 日 [ 審議結果 ] 平成 30 年 11 月 9 日に開催された医薬品第一部会において 本品目を承認して差し支えないとされ 薬事 食品衛生審議会薬事分科会に報告することとされた
審議結果報告書 平成 30 年 1 1 月 2 0 日医薬 生活衛生局医薬品審査管理課 [ 販 売 名 ] セリンクロ錠 10mg [ 一 般 名 ] ナルメフェン塩酸塩水和物 [ 申請者名 ] 大塚製薬株式会社 [ 申請年月日 ] 平成 29 年 10 月 17 日 [ 審議結果 ] 平成 30 年 11 月 9 日に開催された医薬品第一部会において 本品目を承認して差し支えないとされ 薬事 食品衛生審議会薬事分科会に報告することとされた
検査項目情報 1174 一次サンプル採取マニュアル 4. 内分泌学的検査 >> 4F. 性腺 胎盤ホルモンおよび結合蛋白 >> 4F090.HCGβ サブユニット (β-hcg) ( 遊離 ) HCGβ サブユニット (β-hcg) ( 遊離 ) Department of Clinical Lab
 chorionic gonadotropin beta-subunit (free) 連絡先 : 3495 基本情報 4F090 HCGβサブユニット (β-hcg) 分析物 JLAC10 診療報酬 識別 材料 023 血清 測定法 006 ラジオイムノアッセイ (RIA) (IRMA 法 ) 結果識別 第 2 章 特掲診療料 D008 18 ヒト絨毛性ゴナドトロピン-βサブユニット (HCG-β)
chorionic gonadotropin beta-subunit (free) 連絡先 : 3495 基本情報 4F090 HCGβサブユニット (β-hcg) 分析物 JLAC10 診療報酬 識別 材料 023 血清 測定法 006 ラジオイムノアッセイ (RIA) (IRMA 法 ) 結果識別 第 2 章 特掲診療料 D008 18 ヒト絨毛性ゴナドトロピン-βサブユニット (HCG-β)
ザガーロカプセル
 2015 年 10 月改訂 ( 第 2 版 )( : 改訂箇所 ) 2015 年 9 月作成 ( 第 1 版 ) 規制区分 : ( 注意 - 医師等の処方箋により使用すること ) 日本標準商品分類番号 8 7 2 4 9 貯法 : 室温保存 ( 光及び湿気を避けるため PTP 包装のまま保存すること ) 使用期限 : 包装に表示 承認番号 22700AMX01012 22700AMX01013 薬価収載
2015 年 10 月改訂 ( 第 2 版 )( : 改訂箇所 ) 2015 年 9 月作成 ( 第 1 版 ) 規制区分 : ( 注意 - 医師等の処方箋により使用すること ) 日本標準商品分類番号 8 7 2 4 9 貯法 : 室温保存 ( 光及び湿気を避けるため PTP 包装のまま保存すること ) 使用期限 : 包装に表示 承認番号 22700AMX01012 22700AMX01013 薬価収載
Microsoft Word - Ⅲ-11. VE-1 修正後 3.14.doc
 平成 18 年度厚生労働科学研究費補助金 ( 循環器疾患等生活習慣病対策総合研究事業 ) 日本人の食事摂取基準 ( 栄養所要量 ) の策定に関する研究 主任研究者柴田克己滋賀県立大学教授 Ⅲ. 分担研究者の報告書 11. 高 α- トコフェロールあるいは高 γ- トコフェロール摂取に伴うビタミン E の 血中濃度変化と運動トレーニングの影響 分担研究者森口覚 山口県立大学教授 研究要旨ビタミン E
平成 18 年度厚生労働科学研究費補助金 ( 循環器疾患等生活習慣病対策総合研究事業 ) 日本人の食事摂取基準 ( 栄養所要量 ) の策定に関する研究 主任研究者柴田克己滋賀県立大学教授 Ⅲ. 分担研究者の報告書 11. 高 α- トコフェロールあるいは高 γ- トコフェロール摂取に伴うビタミン E の 血中濃度変化と運動トレーニングの影響 分担研究者森口覚 山口県立大学教授 研究要旨ビタミン E
ダクラタスビル塩酸塩 薬物動態試験の概要文 Page 2 用語及び略語一覧 ATP adenosine triphosphate アデノシン三リン酸 AUC area under the concentration-time curve 血中濃度曲線下面積 AUC(INF) area u
 ダクラタスビル塩酸塩 2.6.4 薬物動態試験の概要文 Page 1 CTD 第 2 部 2.6 非臨床試験の概要文及び概要表 2.6.4 薬物動態試験の概要文 ブリストル マイヤーズ株式会社 ダクラタスビル塩酸塩 2.6.4 薬物動態試験の概要文 Page 2 用語及び略語一覧 ATP adenosine triphosphate アデノシン三リン酸 AUC area under the concentration-time
ダクラタスビル塩酸塩 2.6.4 薬物動態試験の概要文 Page 1 CTD 第 2 部 2.6 非臨床試験の概要文及び概要表 2.6.4 薬物動態試験の概要文 ブリストル マイヤーズ株式会社 ダクラタスビル塩酸塩 2.6.4 薬物動態試験の概要文 Page 2 用語及び略語一覧 ATP adenosine triphosphate アデノシン三リン酸 AUC area under the concentration-time
Epilepsy2015
 Key Concepts 1. 患者個々の治療のゴールをできるだけ早く設定 てんかんの薬物治療 薬物治療学 小川竜一 か または他の抗てんかん薬へ切り替える 第一 選択薬とは異なる作用機序の薬物 3. 年齢や合併症 服薬コンプライアンスなどの基本 情報も抗てんかん薬の選択に影響 2. 抗てんかん薬の投与が中止できる患者も存在する 決定する必要がある 50%~70%は単剤で管理でき る 2 慢性の脳の病気
Key Concepts 1. 患者個々の治療のゴールをできるだけ早く設定 てんかんの薬物治療 薬物治療学 小川竜一 か または他の抗てんかん薬へ切り替える 第一 選択薬とは異なる作用機序の薬物 3. 年齢や合併症 服薬コンプライアンスなどの基本 情報も抗てんかん薬の選択に影響 2. 抗てんかん薬の投与が中止できる患者も存在する 決定する必要がある 50%~70%は単剤で管理でき る 2 慢性の脳の病気
日本標準商品分類番号 カリジノゲナーゼの血管新生抑制作用 カリジノゲナーゼは強力な血管拡張物質であるキニンを遊離することにより 高血圧や末梢循環障害の治療に広く用いられてきた 最近では 糖尿病モデルラットにおいて増加する眼内液中 VEGF 濃度を低下させることにより 血管透過性を抑制す
 日本標準商品分類番号 872491 カリジノゲナーゼの血管新生抑制作用 カリジノゲナーゼは強力な血管拡張物質であるキニンを遊離することにより 高血圧や末梢循環障害の治療に広く用いられてきた 最近では 糖尿病モデルラットにおいて増加する眼内液中 VEGF 濃度を低下させることにより 血管透過性を抑制することが示されたが 血管新生に対するカリジノゲナーゼの影響を評価した報告はない そこで今回 網膜血管新生に対するカリジノゲナーゼの役割を同定するため
日本標準商品分類番号 872491 カリジノゲナーゼの血管新生抑制作用 カリジノゲナーゼは強力な血管拡張物質であるキニンを遊離することにより 高血圧や末梢循環障害の治療に広く用いられてきた 最近では 糖尿病モデルラットにおいて増加する眼内液中 VEGF 濃度を低下させることにより 血管透過性を抑制することが示されたが 血管新生に対するカリジノゲナーゼの影響を評価した報告はない そこで今回 網膜血管新生に対するカリジノゲナーゼの役割を同定するため
創薬 創剤における探索動態研究の役割と課題 布施英一協和発酵工業株式会社医薬研究センター薬物動態研究所 1. はじめに弊社では 1990 年代初期より探索ステージにおける動態研究の体制を整備してきた 特に 1996 年から探索動態専門のグループを立ち上げ 欧州の製薬会社での経験を有するコンサルタント
 創薬 創剤における探索動態研究の役割と課題 布施英一協和発酵工業株式会社医薬研究センター薬物動態研究所 1. はじめに弊社では 1990 年代初期より探索ステージにおける動態研究の体制を整備してきた 特に 1996 年から探索動態専門のグループを立ち上げ 欧州の製薬会社での経験を有するコンサルタントと契約し 1 年に 1-2 回のコンサルティングを実施し 欧米の製薬会社の探索動態の方法論を取り入れてきた
創薬 創剤における探索動態研究の役割と課題 布施英一協和発酵工業株式会社医薬研究センター薬物動態研究所 1. はじめに弊社では 1990 年代初期より探索ステージにおける動態研究の体制を整備してきた 特に 1996 年から探索動態専門のグループを立ち上げ 欧州の製薬会社での経験を有するコンサルタントと契約し 1 年に 1-2 回のコンサルティングを実施し 欧米の製薬会社の探索動態の方法論を取り入れてきた
研究成果報告書
 様式 C-19 科学研究費補助金研究成果報告書 平成 21 年 5 月 20 日現在 研究種目 : 基盤研究 (C) 研究期間 :2007~2008 課題番号 :19592419 研究課題名 ( 和文 ) 漢方薬による歯周疾患治療への応用とその作用機序解明 研究課題名 ( 英文 ) Application of Kampo medicine to periodontal disease treatment
様式 C-19 科学研究費補助金研究成果報告書 平成 21 年 5 月 20 日現在 研究種目 : 基盤研究 (C) 研究期間 :2007~2008 課題番号 :19592419 研究課題名 ( 和文 ) 漢方薬による歯周疾患治療への応用とその作用機序解明 研究課題名 ( 英文 ) Application of Kampo medicine to periodontal disease treatment
2008年10月2日
 2008 年 10 月 16 日 日本小児内分泌学会 成長ホルモン委員会 SGA 性低身長症における GH 治療の実施上の注意 SGA 性低身長症における成長ホルモン (GH) 治療が 2008 年 10 月 16 日に承認されました 詳細については 改訂されたジェノトロピン ( ファイザー株式会社 ) の添付文書により確認して下さい 日本小児内分泌学会では SGA 性低身長症におけるGH 治療に関するガイドライン
2008 年 10 月 16 日 日本小児内分泌学会 成長ホルモン委員会 SGA 性低身長症における GH 治療の実施上の注意 SGA 性低身長症における成長ホルモン (GH) 治療が 2008 年 10 月 16 日に承認されました 詳細については 改訂されたジェノトロピン ( ファイザー株式会社 ) の添付文書により確認して下さい 日本小児内分泌学会では SGA 性低身長症におけるGH 治療に関するガイドライン
テイカ製薬株式会社 社内資料
 テイカ製薬株式会社社内資料 アレルギー性結膜炎治療剤トラニラスト点眼液.5% TS TRANILAST Ophthalmic Solution.5% TS 生物学的同等性に関する資料 発売元 : 興和株式会社 製造販売元 : テイカ製薬株式会社 9 年 月作成 TSTR5BE9 ラット及びモルモットアレルギー性結膜炎モデルにおける生物学的同等性試験 Ⅰ. 試験の目的トラニラスト点眼液.5% TS および標準製剤の生物学的同等性をラット受動感作アレルギー性結膜炎モデル及びモルモット能動感作アレルギー性結膜炎モデルを用い薬力学的に検討した
テイカ製薬株式会社社内資料 アレルギー性結膜炎治療剤トラニラスト点眼液.5% TS TRANILAST Ophthalmic Solution.5% TS 生物学的同等性に関する資料 発売元 : 興和株式会社 製造販売元 : テイカ製薬株式会社 9 年 月作成 TSTR5BE9 ラット及びモルモットアレルギー性結膜炎モデルにおける生物学的同等性試験 Ⅰ. 試験の目的トラニラスト点眼液.5% TS および標準製剤の生物学的同等性をラット受動感作アレルギー性結膜炎モデル及びモルモット能動感作アレルギー性結膜炎モデルを用い薬力学的に検討した
第 2 部 CTD の概要 一般名 : ダパグリフロジンプロピレングリコール水和物 版番号 : 2.4 非臨床試験の概括評価 フォシーガ 本書は ブリストル マイヤーズ株式会社及びアストラゼネカ株式会社の機密文書です 機密保持を求める条件で本書を公開する場合があることを除いては 本書の受領により 本
 第 2 部 CTD の概要 一般名 : ダパグリフロジンプロピレングリコール水和物 版番号 : 2.4 非臨床試験の概括評価 フォシーガ 本書は ブリストル マイヤーズ株式会社及びアストラゼネカ株式会社の機密文書です 機密保持を求める条件で本書を公開する場合があることを除いては 本書の受領により 本書に記載された非公開の情報は ブリストル マイヤーズ株式会社又はアストラゼネカ株式会社の書面による事前の承認なく公開又は開示しないことに同意したものとします
第 2 部 CTD の概要 一般名 : ダパグリフロジンプロピレングリコール水和物 版番号 : 2.4 非臨床試験の概括評価 フォシーガ 本書は ブリストル マイヤーズ株式会社及びアストラゼネカ株式会社の機密文書です 機密保持を求める条件で本書を公開する場合があることを除いては 本書の受領により 本書に記載された非公開の情報は ブリストル マイヤーズ株式会社又はアストラゼネカ株式会社の書面による事前の承認なく公開又は開示しないことに同意したものとします
日本内科学会雑誌第98巻第12号
 表 1. 喘息の長期管理における重症度対応段階的薬物療法 重症度 長期管理薬 : 連用 : 考慮 発作時 ステップ 1 軽症間欠型 喘息症状がやや多い時 ( 例えば 1 月に 1 ~2 回 ), 血中 喀痰中に好酸球増加のある時は下記のいずれか 1 つの投与を考慮 吸入ステロイド薬 ( 最低用量 ) テオフィリン徐放製剤 ロイコトリエン拮抗薬 抗アレルギー薬 短時間作用性吸入 β2 刺激薬または短時間作用性経口
表 1. 喘息の長期管理における重症度対応段階的薬物療法 重症度 長期管理薬 : 連用 : 考慮 発作時 ステップ 1 軽症間欠型 喘息症状がやや多い時 ( 例えば 1 月に 1 ~2 回 ), 血中 喀痰中に好酸球増加のある時は下記のいずれか 1 つの投与を考慮 吸入ステロイド薬 ( 最低用量 ) テオフィリン徐放製剤 ロイコトリエン拮抗薬 抗アレルギー薬 短時間作用性吸入 β2 刺激薬または短時間作用性経口

 測定した また Scrは酵素法にて測定し その参考基 r =0.575 p
測定した また Scrは酵素法にて測定し その参考基 r =0.575 p