目次
|
|
|
- きゅういち たもん
- 4 years ago
- Views:
Transcription
1 FactSage 無料体験セミナー 2011 抜粋資料 1
2 まえがき FactSage 無料体験セミナーにご参加いただきありがとうございます セミナーでは 本資料の例題を使いながら 講師と一緒に FactSage を操作することで FactSage の基本的な使い方を体験していただきます 計算結果の正しさを実感していただくために イメージや確認が比較的容易な例題を用意しました FactSage は 化学反応式についての平衡定数や活量を調べる伝統的な解析 (3 章 ) から 現代的な熱力学平衡計算 (4 章 ) そして計算状態図の作成 (5,6 章 ) までを お手伝いしてくれます セミナー終了後は オフィス 研究所にお戻りになり 現在かかえている問題に適用してみて下さい FactSage による解析が問題解決の糸口になればうれしく思います そして また皆様にお会いできれば幸いです RCCM FactSage サポートチーム 2
3 目次 1 章はじめに 章 FactSage メイン画面 章化学反応式と平衡定数 章熱力学平衡計算 章計算状態図 章計算状態図 2( 電位 -ph 図 )
4 はじめに 4
5 FactSage とは 熱力学平衡計算ソフトウェア & データベース 1. 熱力学平衡計算 2. 計算状態図作成 3. 熱力学データベースの管理と編集 5
6 熱力学平衡計算とは 容器に多種類の物質を入れて 温度一定 圧力一定の条件で 長時間放置しておくと 化学反応がおこり 体積 組成などの巨視的な性質が時間的に変化しない状態 ( 平衡状態 ) に達する Fe, C, S, SiO 2,... 平衡状態 1650,1atm ( 温度 圧力一定 ) 長時間放置 組成の時間変化の解析は不可? 気体? 液体? どのような組成? 注 ) 平衡計算は容器の形状は考慮しない 熱力学平衡計算 6
7 熱力学平衡計算の例 (H 2 O の平衡計算 ) 1 mol H 2 O FactSage 計算結果画面 50,1 atm 入力内容 水が安定 系の熱力学量 7
8 熱力学平衡計算の例 (H 2 O の熱解離 ) 1 mol H 2 O 100 ~ atm 8
9 熱力学平衡計算の例 ( アルミニウム合金 ) 50 Al + 25 Ca + 25 Si (gram) 300 ~ atm 9
10 熱力学平衡計算の例 ( 溶鋼の脱硫処理 ) 溶鋼中の硫黄分をスラグを使って取り除く 溶鋼 :Fe, C, Si, Mn, S, Al, Ar スラグ :CaO, SiO 2, Al 2 O 3, MnO, FeO 温度 :1650 圧力 :1 atm 気体 スラグ 溶鋼中の硫黄 溶鋼 スラグ中の硫黄 添加するスラグの量 ( 100gram) 10
11 熱力学平衡計算の例 ( メタンの断熱燃焼温度 ) 25 CH O 2 (mole) 燃焼過程の間に外部への熱損失がないときの 燃焼ガスの最終温度 断熱燃焼温度 : ΔH = 0 1 atm 11
12 計算状態図 状態図 : 系の平衡状態となる相を 組成や温度などに対して示した図 12
13 水溶液の計算状態図 13
14 平衡状態における系の組成を求めるには 閉鎖系 ( 外界とエネルギーの交換はできるが 物質の交換はできない系 ) において 系の組成は 等温等圧の条件下では 系のギブズエネルギーが減少する方向に自発的に変化する 平衡状態における系の組成は 系のギブズエネルギーが最小になっている組成である 14
15 FactSage の平衡計算 例 : 25, 1atm で以下の系の平衡組成は? Mg + 3 Cu 2 O + 2 Fe 3 C + Ar? 質量保存則をみたす組み合わせはいろいろある 1 MgO + 6 Cu Fe + 2 C Fe 3 O 4 + Ar 2 MgO + 6 Cu Fe + 2 C Fe 2 O 3 + Ar 3 MgCO Cu + 6 Fe + 1 C +Ar 4 6 Cu Fe + 2 C MgFe 2 O MgO + Ar etc FactSage は 各物質のギブズエネルギーの和が最小となる組み合わせを探索する 1, kJ, 2: kJ, 3: kJ, 4: kJ,... 平衡状態は 1 の組成 十分に評価 ( アセスメント ) された ギブズエネルギーのデータベース (FACT, SGTE が有名 ) が必要 15
16 純物質データベースと溶体データベース 熱力学データベースには ギブズエネルギー エンタルピー エントロピーなどの熱力学データが含まれている FactSage の熱力学データベースには 純物質データベースと溶体データベースの 2 種類がある 純物質 (Compound, Pure substance) 元素物質である単体 希薄水溶液中のイオン 化学量論化合物 ( 元素の比が一定の化合物 ) 例 :Au, Cu 2+, Cu 5 FeS 4, Mg 3 Si 4 O 10 (OH) 2 溶体 (Solution) 純物質が原子あるいは分子の尺度で混合したもの 液体のものを溶液 固体のものを固溶体とよぶ 例 : 合金 溶融スラグ 溶鋼 16
17 純物質と溶体のギブズエネルギーの式 純物質 G a bt ct ln T dt 2 et G : ギブズエネルギー, T: 温度 3 f T G X G X G RT X ln X X ln X ) G E 溶体 ( 例 :2 成分系 Redlich - Kister モデル ) 2 ( E G X1X 2L12 X1X 2( X1 X 2) L12 X1X 2( X1 X 2) L12... L12 a b T c T ln T G 1,G2 : 純物質 1, 2 のギブズエネルギー X 1, X 2 : 純物質 1, 2 のモル分率 測定値を再現するようにパラメーター a,b,... と a ν,b ν,... を最適化 溶体データベースは 純物質データベースとカップルになっている 17
18 FactSage で使用可能なデータベース 純物質データベース カップルになっている純物質 & 溶体データベース 18
19 FactSage メイン画面 19
20 FactSage メイン画面 ボタンメニューをクリックして作業目的に応じたモジュールを起動する熱力学平衡計算をしたい Equilib をクリック計算状態図を作成したい Phase Diagram をクリック 熱力学平衡計算 計算状態図の作成 20
21 FactSage メイン画面 説明書の表示 データベースの説明書 熱力学データの検索と表示熱力学データファイルの管理 純物質データの編集 溶体データベースの編集 21
22 FactSage メイン画面 化学反応式を設定して状態量の変化量 平衡定数を計算 ガス分圧に対する安定領域を計算 電位 -ph 図 ( プールべ図 ) の作成熱力学平衡計算計算状態図の作成モデルパラメーターの最適化 22
23 FactSage メイン画面 Equilib の計算結果ファイルからグラフを作成 ミクスチャー ストリームの編集 平衡計算結果の高度な処理グラフの編集スラグの粘度計算 FactSage の終了 23
24 化学反応式と平衡定数 Reaction モジュール 24
25 Reaction モジュール 化学反応式を設定して状態量の変化量 平衡定数などを計算複数の純物質の G, H, C p などの状態量の和を表示溶体データベースは使用しない Reaction の起動 25
26 銅の酸化反応 4 Cu + O 2 = 2 Cu 2 O の標準状態における等温反応 1. 新規設定 2. データベースの設定 3. 単位の設定 4. + をクリックして入力場所を作成 5. 化学反応式を入力 非標準状態を扱うときにチェックを入れる 6. Next をクリック 26
27 銅の酸化反応 7. 温度を設定して Calculate をクリック 平衡定数 K eq = exp( -DG 0 /RT ) 標準状態で計算しているので DG 0 は表中の Delta G(J) 27
28 銅の酸化反応 4 Cu + O 2 = 2 Cu 2 O の平衡状態の計算 1. 新規設定 2. データベースの設定 3. 単位の設定 4. + をクリックして入力場所を作成 6. 化学反応式を入力圧力の変数は P 5. 非標準状態を扱う 7. Next をクリック 28
29 銅の酸化反応 標準状態における反応 P O2 (g) = 1.0 atm, a Cu(s) = 1.0 前例の 1000K の結果と一致することを確認してください 標準状態で計算しているので Delta_G(J) は DG 0 の意味である 前例より 1000 K では K eq = 温度を設定して Calculate をクリック 29
30 銅の酸化反応 平衡状態で T = 1000K, a Cu(s) = 1.0, a Cu2 O(s) = 1.0 のとき P O2 (g) は? DG DG 0 2 acu 2O RT ln 4 acu P O 2 DG = 0 のとき DG 12. 次式が成り立つことを確認 P O2 (g) = 1/K eq = 1/ = RT ln K eq, K eq a a 4 Cu 2 Cu O 2 P 標準状態なので DG 0 O 2 標準状態ではないので DG 11. Calculate をクリック 9. 温度と銅の活量を設定 酸素分圧は未知なので空白 10. 平衡状態なので DG = 0 30
31 銅の酸化反応 平衡状態で T = 1000K, P O2 (g) = 1atm, a Cu2 O(s) = 1.0 のとき a Cu(s) は? 温度を未知にすると必ず T 印が表示される 平衡状態で P O2 (g) = atm, a Cu(s) = 1.0, a Cu2 O(s) = 1.0 のとき温度は? 31
32 メタンの断熱燃焼温度 メタンの断熱燃焼温度の計算 1. 新規設定 2. データベースの設定 3. 単位の設定 4. + をクリックして入力場所を作成 変数 <Alpha> 5. 化学反応式を入力 6. Next をクリック 32
33 メタンの断熱燃焼温度 ΔH < 0 は発熱反応 化学量論的反応 (A = 2) CH O 2 = CO H 2 O 酸素過剰での反応 (A > 2) CH 4 + (2 + 過剰 ) O 2 = CO H 2 O + ( 過剰 )O 2 7. <A> および温度を設定して Calculate をクリック 33
34 メタンの断熱燃焼温度 断熱燃焼温度 <A> が増加するにつれて断熱燃焼温度は低下する 注意 : 燃焼温度を正確に求めるには Equilib で平衡断熱燃焼温度を計算する 高温では生成物の熱解離を考慮しなくてはならない 77~79 ページを参照のこと 8. 断熱変化 ΔH = 0 の計算 34
35 水溶液中における銅イオンの還元 標準還元電位の計算 1. 新規設定 2. データベースの設定 3. 単位の設定 4. + をクリックして入力場所を作成 Cu[2+], Cu[++], H[+] のように入力 5. 化学反応式を入力 6. Next をクリック 35
36 水溶液中における銅イオンの還元 イオンを含む計算では G の列が標準還元電位となる 標準還元電位 Eº= -ΔGº/nF n: 反応に関与する電子の数 F(=96485 C/mol): ファラデー定数 n の変更 36
37 水溶液中における銅イオンの還元 標準還元電位 7. 温度等を設定して Calculate 37
38 水溶液中における銅イオンの還元 平衡状態において H 2 の分圧を変化させたときの Cu 2+ の活量の変化 7. 温度等を設定して Calculate 38
39 熱力学平衡計算 Equilib モジュール 39
40 Equilib モジュールの起動 熱力学平衡計算純物質データベースと溶体データベースを使用 Equilib の起動 40
41 Equilib モジュールの起動 Equilib を起動すると 直前の設定を読み込むか尋ねられる 新規設定のときは いいえを選択する Equilib には 4 つのウィンドウがある (1) Menu (2) Reactants (3) List (4) Results 41
42 データベースの選択 Data Search をクリック Fact53 を選択 少なくとも 1 つ純物質データベースを選択する必要がある データを含めるかどうか選択 プラズマ 水溶液 25 のデータしかない純物質 有機化合物 CxHy... の X の上限 溶体相の最小成分の数 SGTE, SGsold, SGnucl, TDnucl, FSlite, FTlite を使うとき 1 にする場合がある 成分数 1 の溶体相は純物質である 42
43 単位の設定 Units または T(C) P(atm)... Vol(litre) をクリックして Units 画面で設定 43
44 H 2 O の平衡計算 最初に H 2 O の平衡計算を練習して Equilib の基本的な操作を学ぼう 1. 新規設定 2. Fact53 を選択 3. 単位の設定 4. 反応種を入力 1mol の H2O ストリームは同じ温度 圧力の物質の集まり 1 でよい 初期条件の設定 反応前後の熱力学量の変化を計算するときチェックを入れる 設定しない場合は 反応種の元素の量のみが結果に依存する この問題では H2O の代わりに H O2 としても全く同じ結果になる 5. Next をクリック 44
45 H 2 O の平衡計算 6. 平衡状態で存在しそうな相や物質を選択考えている温度では 氷は存在しないので 液相と気相のみ 気相は理想気体のデータを使用 Menu Window ( メニュー画面 ) 溶体相の表示 この例では溶体相は無い 気相の成分を選択する場合は gas を右クリック 次ページ 7. 温度が 25 と 150 の場合を一度に計算 圧力は 1 atm に設定 45
46 H 2 O の平衡計算 gas を右クリック O3(g) を平衡計算に考慮しない 平衡計算に考慮しない場合の例 物質のデータの有効温度範囲外の温度で 平衡計算するとき 考慮しないほうが適切なときがある 準安定な物質を考慮したい場合 物質数が Equilib の上限 (1500) を超える場合 46
47 H 2 O の平衡計算 8. normal を選択して Calculate をクリック 9. 出力フォーマットを選択通常 ChemSage フォーマットがおすすめ 47
48 H 2 O の平衡計算 25 の場合 圧力を平衡状態で気体が生成される値まで下げたときの気相成分のフガシティー ( 理想気体なので分圧 ) 圧力を atm に設定して再計算して確認 気相は存在しない Results Window ( 結果画面 ) 安定相の活量は 1 25 では水 気相の体積 25 では気相は存在しないので体積は 0 系の熱力学量 48
49 H 2 O の平衡計算 150 の場合 理想気体で計算しているので 分圧 = モル分率 全圧 (1 atm) 気相の組成水蒸気以外はほとんど では水は存在しない 気相の元素のモル分率 全圧の意味ではない 安定相の活量は 1 49
50 H 2 O の平衡計算 気相の単位をモルからグラムに変更 10. List Window をクリック 13. gram を選択 の結果を表示 12. 気相と液相を表示 14. Refresh をクリック 50
51 H 2 O の平衡計算 相転移温度の計算 15. Menu Window をクリック 16. normal + transitions を選択 17. Calculate をクリック 51
52 H 2 O の平衡計算 で相転移 気相と水の活量は より高温では気相が存在 52
53 H 2 O の平衡計算 実在気体のデータで計算 18. Menu Window をクリック 19. real を選択 20. Calculate をクリック 53
54 H 2 O の平衡計算 100 で相転移 実在気体のデータは高圧の計算で主に利用される SGPS で計算した場合は 実在気体のデータがないため理想気体と同じ結果になる 54
55 H 2 O の平衡計算 固相 ( 氷 ) を入れて計算 21. Menu Window をクリック 22. ideal を選択 23. pure solids を選択 24. normal を選択して Calculate をクリック 55
56 H 2 O の平衡計算 25 の氷のデータは有効温度範囲外なので T 印が表示される 今回の計算では 氷の量は 0 になり結果は間違っていない 一般に T 印が表示されていて 物質量が 0 でない物質は 選択しないで再計算を行ったほうがよい場合がある 56
57 H 2 O の平衡計算 ( 計算結果のグラフ ) ガス分圧の温度変化 1. 平衡状態で存在しそうな相を選択 2. 温度を入力 150 から 2000 まで 50 刻みで計算するという意味 3. Calculate をクリック 57
58 H 2 O の平衡計算 ( 計算結果のグラフ ) 計算結果 ページ以降を表示 58
59 H 2 O の平衡計算 ( 計算結果のグラフ ) 5. Plot Results を起動 6. Axes をクリック 59
60 H 2 O の平衡計算 ( 計算結果のグラフ ) 7. X 軸 Y 軸を設定して OK をクリック 60
61 H 2 O の平衡計算 ( 計算結果のグラフ ) 8. Select をクリックしてグラフに表示する物質を選択 10. グラフに表示する物質を選択して OK をクリック 9. 見やすくするために 大きい順に並び変える mass(max) を選択して Refresh をクリック 61
62 H 2 O の平衡計算 ( 計算結果のグラフ ) 11. ラベルの大きさや数 12. グラフ画面の設定 13. Plot をクリック 62
63 H 2 O の平衡計算 ( 計算結果を Excel 形式で保存 ) ガス分圧の変化を Excel 形式で保存 1. 結果画面 (Results Window) で Save or Print As をクリック 2. Excel Spreadsheet を選択し Spreadsheet setup... をクリック 63
64 H 2 O の平衡計算 ( 計算結果を Excel 形式で保存 ) 4. 右クリックで項目一覧を表示 T(C) を選択 3. 表示項目数を設定 ( 系に関する量 ) 5. 表示項目数を設定 ( 化学種の量 ) 6. 右クリックで項目一覧を表示 log(a) を選択 7. Select... をクリックして化学種の選択 ( 次ページ ) 64
65 H 2 O の平衡計算 ( 計算結果を Excel 形式で保存 ) 選択した化学種の数 9. OK をクリック 8. 化学種を選択して OK をクリック 10. OK をクリック 65
66 H 2 O の平衡計算 ( 計算結果を Excel 形式で保存 ) 11. 保存先を入力して Save をクリック 注意 (1) 上書き保存はしないこと (2) 保存先のフォルダー名とファイル名は英数字にすること 12. 保存したファイルを Excel 2007 で開くと下のメッセージが表示されるが気にせず はい をクリック 66
67 H 2 O の平衡計算 ( 水の加熱 ) 25, 1 g の水に 1 cal の熱量を与えたときの系の組成と温度を求める 1. 反応種を入力 2. Fact53 を選択 3. 単位を設定 4. Initial Conditions にチェックを入れて初期条件を設定 5. Next をクリック 67
68 H 2 O の平衡計算 ( 水の加熱 ) 6. 平衡状態で存在しそうな相や物質を選択 8. 与える熱量 (Delta H) の設定 7. 圧力の設定 9. 予想される系の温度を入力 10. Calculate をクリック 68
69 H 2 O の平衡計算 ( 水の加熱 ) 系の温度 気相は存在しない 設定した熱量 69
70 H 2 O の平衡計算 ( 水の加熱 ) 練習 : 25, 1 g の水に与える熱量を変化させたとき 系の温度が下のように変化することを確認してください 70
71 硫化鉄の酸化 硫化鉄の酸化を計算 酸素と硫化鉄のモル分率を変化させる 1. 新規設定 2. Fact53 を選択 3. 単位を設定 4. + をクリックして 入力場所を作成 5. 反応種を入力物質量を変数 <A> で設定 6. Next をクリック 71
72 硫化鉄の酸化 7. 平衡状態で存在しそうな物質を選択 8. 温度 圧力を入力 9. normal + transitions を選択して Calculate をクリック 10. 酸素の量を 0.6 mol から 0.65 mol まで mol 刻みで変化させる 72
73 硫化鉄の酸化 酸素を 0.6 mol から 0.65 mol まで mol 刻みで変化させたときの平衡計算結果 normal + transitions を選択したので物質が変化する酸素の量も表示されている 73
74 硫化鉄の酸化 ( 計算結果のグラフ ) 1. Plot Results... を選択 2. X 軸,Y 軸を選択 74
75 硫化鉄の酸化 ( 計算結果のグラフ ) 3. グラフに表示する物質を選択 75
76 硫化鉄の酸化 ( 計算結果のグラフ ) 4. ラベルとグラフ画面の設定をして Plot をクリック 76
77 平衡断熱燃焼温度 メタンの平衡断熱燃焼温度の計算 1. 新規設定 2. Fact53 を選択 3. 単位を設定 4. + をクリックして 入力場所を作成 5. Initial Conditions にチェックを入れて 反応種を入力 6. Next をクリック 77
78 平衡断熱燃焼温度 7. 平衡状態で存在しそうな物質を選択 8. 圧力 エンタルピー変化 ( 断熱反応なので 0) を入力 温度は未知なので空白 10. Calculate をクリック 9. 予想される温度 78
79 平衡断熱燃焼温度 生成物の温度 : ( 平衡断熱燃焼温度 ) Reaction を使った計算と比較してください (32~34 ページ ) 79
80 希薄水溶液 (FACT53) 希薄な水溶液 (~0.001molal) は FACT53 の水溶液相を使って計算できる 1. 新規設定 2. Fact53 を選択 水溶液を含める ( 次ページ ) 4. + をクリックして 入力場所を作成 3. 単位を設定 銅鉱石の成分 5. 反応種を入力 6. Next をクリック 溶解剤 80
81 希薄水溶液 (FACT53) 水溶液相化学種を含める データベース選択画面より Include aqueous species にチェック 81
82 希薄水溶液 (FACT53) 7. 平衡状態で存在しそうな物質を選択 pure liquids は含めない 8. 温度と圧力を入力水溶液データの有効温度範囲の上限は 550K(277 ) 9. Calculate をクリック 82
83 希薄水溶液 (FACT53) 水溶液相 FACT53 以外の水溶液のデータベースには FTmisc-PITZ FThelg がある 固相 水溶液相の特性 83
84 酸化物の溶融 SiO 2 - B 2 O 3 -CaO-Al 2 O 3 系の平衡計算 まず用いるデータベースを検索する 1. Database Documentation を起動して SiO 2 - B 2 O 3 -CaO-Al 2 O 3 系を検索 FToxid が適切なことがわかる 4 成分のうち各 2 成分系 (SiO 2 -B 2 O 3, SiO 2 - CaO, SiO 2 -Al 2 O 3, B 2 O 3 -CaO, B 2 O 3 -Al 2 O 3, CaO-Al 2 O 3 ) の最適化されたデータがあれば 正確度の高い予測結果が期待できる この系では 各 2 成分系のデータに加えて CaO-Al 2 O 3 -SiO 2 の 3 成分系のデータもありよい状況である 84
85 酸化物の溶融 2. 新規設定 3. FToxid 選択 ( 次ページ ) 5. + をクリックして 入力場所を作成 4. 単位を設定 6. 反応種を入力 7. Next をクリック 85
86 酸化物の溶融 溶体相の情報を確認 Menu 画面から Database Documentation にアクセス 8. 溶体相の Full Name をクリック基本情報が表示される 9. Information をクリックして詳細情報を表示 86
87 酸化物の溶融 FToxid-SLAGA の情報が表示される 入力物質の全てが成分に含まれている また B 2 O 3 が存在しているので J オプションを使用する 87
88 酸化物の溶融 10. FToxid-SLAGA の + 印を右クリック J オプションを選択 11. 同様に他の相も Information を調べながら選択する FToxid-Mel_ と FToxid-Gehl は同時に選択してはいけない B が含まれているので FToxid-Gehl を使うことにする 88
89 酸化物の溶融 12. 平衡状態で存在しそうな物質を選択 溶融スラグ相を選択したので pure liquids は選択しない 14. normal + transitions を選択して Calculate をクリック 13. 温度と圧力を入力 89
90 酸化物の溶融 で融け始める 90
91 酸化物の溶融 1300 では溶融スラグ相は 2 相分離している 91
92 酸化物の溶融 ( 計算結果のグラフ ) 1. Plot Results... を選択 3. 表示する物質の選択 ( 次ページ ) 2. X 軸,Y 軸を選択 92
93 酸化物の溶融 ( 計算結果のグラフ ) 4. 単位を gram にして Refresh をクリック 選択した物質をクリアするときクリック 5. Show をクリックして pure solids と SOLUTIONS を選択 93
94 酸化物の溶融 ( 計算結果のグラフ ) 6. Gram(max) をダブルクリックして大きい順にソート 7. プロットする物質を選択 8. OK をクリック 94
95 酸化物の溶融 ( 計算結果のグラフ ) 9. ラベルとグラフ画面の設定をして Plot をクリック 95
96 酸化物の溶融 ( 計算結果のグラフ ) 溶融開始温度 96
97 Al-Ca-Si 系の平衡計算 Al-Ca-Si 系の平衡計算 まず用いるデータベースを検索する 1. Database Documentation を起動して Al-Ca-Si が含まれる系を検索 3 成分のうち各 2 成分系 (Al-Ca, Al-Si, Ca-Si) の最適化されたデータがあれば 正確度の高い予測結果が期待できる SGTE2004, SGTE2007, FTlite, FSstel, TDnucl が適切であることがわかる 97
98 Al-Ca-Si 系の平衡計算 2. SGTE 2007 の list of optimized... を調べてパラメーターが最適化されている相を確認 ここに掲載されている相のみを選択する 青字は 3 成分の相互作用パラメーターが最適化されている相 黒色は 3 成分の相互作用パラメーターは最適化されていないが 各 2 成分は最適化されている相 (ST) は化学量論化合物で SGTE 純物質データベース または SGTE 溶体データベースにデータがある 98
99 Al-Ca-Si 系の平衡計算 3. Documentation で SGTE 2007 の general description を調べて データベースの使い方を確認 LIQUID, FCC, BCC, HCP は I(J) オプションが必要な場合がある B2_BCC, L12_FCC は必ず I オプションを設定する 1 成分の溶体 ( すなわち化学量論化合物 ) を選べるようにする 例 : In-Sb 系の ZINCBLENDE_B3 相 (InSb) InSb は SGTE 純物質データベースに存在しない 99
100 Al-Ca-Si 系の平衡計算 4. 新規設定 5. SGTE を選択 ( 次ページ ) 7. + をクリックして 入力場所を作成 6. 単位を設定 8. 反応種を入力 9. Next をクリック 100
101 Al-Ca-Si 系の平衡計算 5-1 SGTE を選択 5-2 ここでは 2 を選択 In-Sb 系など 1 成分溶体相 ( 化学量論化合物 ) が含まれる系では 1 を選択 5-3 OK をクリック 101
102 Al-Ca-Si 系の平衡計算 10. pure solids を右クリック 平衡状態で存在しそうな純物質を Documentation を参考に選択 102
103 Al-Ca-Si 系の平衡計算 11. 平衡状態で存在する相を Documentation を参考に選択 12. 温度と圧力を入力 13. transitions を選択して Calculate をクリック 103
104 Al-Ca-Si 系の平衡計算 625 では液相と化学量論化合物が平衡している 104
105 Al-Ca-Si 系の平衡計算 ( 計算結果のグラフ ) 14. グラフの作成 溶融開始温度 105
106 計算状態図 1 Phase Diagram モジュール 106
107 Phase Diagram モジュール 計算状態図の作成純物質データベースと溶体データベースを利用 Phase Diagram の起動 107
108 Phase Diagram モジュールの起動 Phase Diagram を起動すると 直前の設定を読み込むか尋ねられる 新規設定のときは いいえを選択する Phase Diagram には 4 つのウィンドウがある (1) Menu (2) Components (3) List (4) Results 108
109 データベースの選択 Data Search をクリック Fact53 の選択 データを含めるかどうか選択 プラズマ 水溶液 25 のデータしかない純物質 有機化合物 CxHy... の X の上限 溶体相の最小成分の数 SGTE, SGsold, SGnucl, TDnucl, FSlite, FTlite を使うとき 1 にする場合がある 成分数 1 の溶体相は純物質である 109
110 単位の設定 Units または T(C) P(atm)... Vol(litre) をクリックして Units 画面で設定 110
111 CaO-SiO 2 2 成分系状態図 CaO-SiO 2 2 成分系状態図を作成する まず使用するデータベースを検索する 1. Database Documentation を起動して CaO-SiO 2 系を検索する FToxid が適切なことがわかる CaO-Al 2 O 3 -SiO 2 は 3 成分系で最適化されたデータがあることを意味している 3 成分系で最適化されていることは 各 2 成分系でも最適化されているので CaO-SiO 2 系は最適化されたデータがある 111
112 CaO-SiO 2 2 成分系状態図 2. Phase Diagram を起動 Components Window 3. 新規設定 4. 単位を設定 6. + をクリックして入力場所を作成 5. データベースの選択 ( 次ページ参照 ) 7. 物質を入力 8. Next をクリック 112
113 CaO-SiO 2 2 成分系状態図 Data Search 5-1. Data Search をクリック 5-2. FToxid を選択 5-3. OK をクリック 113
114 CaO-SiO 2 2 成分系状態図 12. Variables をクリック ( 次ページ参照 ) Menu Window 10. 平衡状態で存在しそうな溶体相を選択 9. Show をチェック 11. 平衡状態で存在しそうな純物質を選択 溶融スラグ相を選択するので pure liquids は選択しない ASlag-liq を選択すると自動的に I オプション (2 相分離する可能性がある場合は必須 ) が設定される 114
115 CaO-SiO 2 2 成分系状態図 Variables 温度を Y 軸に設定 ( 範囲 :600~2600K) X-Y 2 元座標のグラフを選択 Next ボタンをクリック 圧力を 1atm に設定 SiO2 のモル分率を X 軸に設定 ( 範囲 :0~1) OK をクリック 115
116 CaO-SiO 2 2 成分系状態図 13. Parameters をクリック Parameters 14. ラベルの大きさ 色等の設定 15. 計算に時間がかかるときは yes を選択 16. OK をクリック 116
117 CaO-SiO 2 2 成分系状態図 17. Calculate をクリック 計算結果 左クリックしてラベルを貼り付けることができる CaSiO3(s2) + Ca3Si2O7(s) 117
118 CaO-SiO 2 2 成分系状態図 Phase Equilibrium モード Phase Equilibrium モードで平衡計算したい場所をクリック クリックした点で平衡計算が実行される ChemSage フォーマットは中ほどから 118
119 CaO-Al 2 O 3 -SiO 2 3 成分系状態図 CaO-Al 2 O 3 -SiO 2 3 成分系状態図を作成する 1. Database Documentation を起動して CaO-Al 2 O 3 -SiO 2 系を検索する FToxid を使用する 119
120 CaO-Al 2 O 3 -SiO 2 3 成分系状態図 2. Phase Diagram を起動 Components Window 3. 新規設定 4. 単位を設定 6. + をクリックして入力場所を作成 5. FToxid を選択 7. 物質を入力 8. Next をクリック 120
121 CaO-Al 2 O 3 -SiO 2 3 成分系状態図 Menu Window 9. 平衡状態で存在しそうな溶体相を選択 11. Variables をクリック ( 次ページ参照 ) 10. 平衡状態で存在しそうな純物質を選択 121
122 CaO-Al 2 O 3 -SiO 2 3 成分系状態図 Variables 三角形の状態図 温度と圧力を設定 Next をクリック つの角 A, B, C にそれぞれ対応する物質を選択 A: SiO 2, B: CaO, C: Al 2 O OK をクリック 順番に注意 #1:A-Corner #2:C-Corner #3:B-Corner 122
123 CaO-Al 2 O 3 -SiO 2 3 成分系状態図 12. Calculate をクリック 計算結果 123
124 CaO-Al 2 O 3 -SiO 2 3 成分系状態図 タイラインモード タイラインモード 表示したい場所でクリック 124
125 サンプルの表示 1. メニューバー File Directories FToxid phase diagrams を選択 3. サンプルの表示シングルクリックでプレビュー ダブルクリックで設定と状態図の読込み 125
126 CaCl 2 -LiCl-KCl 3 成分系液相面図 CaCl 2 -LiCl-KCl 3 成分系液相面図を作成する 1. Database Documentation を起動して CaCl 2 -LiCl-KCl 系を検索する FTsalt を使用する 126
127 CaCl 2 -LiCl-KCl 3 成分系液相面図 2. FTsalt は ( 熱力学データのパラメーターが ) 最適化されている系のリストが Database Documentation に掲載されている FTsalt list of optimized systems and calculated phase diagrams を選択して CaCl2-KCl-LiCl を確認 Phase Diagram や Equilib では ここに掲載されている相とオプションを選択する それ以外の相を選択すると間違った結果になることがある 127
128 CaCl 2 -LiCl-KCl 3 成分系液相面図 Components Window 3. 新規設定 4. 単位を設定 6. + をクリックして入力場所を作成 8. Next をクリック 5. FTsalt を選択 7. 物質を入力 128
129 CaCl 2 -LiCl-KCl 3 成分系液相面図 Menu Window 9. 溶体相を選択 (I オプション, O オプション ) 10. 純物質を選択 11. Variables を設定 O オプション : 液相のみ表示 129
130 CaCl 2 -LiCl-KCl 3 成分系液相面図 Variables 三角形の状態図 ( 投影図 ) 温度の設定温度 :projection 範囲 :default Step: 圧力 : 一定 Next をクリック つの角 A, B, C にそれぞれ対応する物質を選択 A: CaCl 2, B: KCl, C: LiCl OK をクリック 130
131 CaCl 2 -LiCl-KCl 3 成分系液相面図 12. Parameters をクリック Parameters 13. 温度スケール 液相面図の設定 131
132 CaCl 2 -LiCl-KCl 3 成分系液相面図 14. チェックを入れる univariants: 共融線 isotherms: 等温線 計算結果 15. Calculate をクリック 132
133 Cr-Fe-Ni 3 成分系状態図 Cr-Fe-Ni 3 成分系状態図を作成する 1. Database Documentation を起動して Cr-Fe-Ni 系を検索する SGTE 2007 などで 各 2 成分部分系 (Cr-Fe, Cr-Ni, Fe-Ni) のデータがある 3 成分系で正確な状態図を計算できる可能性が高い 133
134 Cr-Fe-Ni 3 成分系状態図 2. SGTE 2007 の list of optimized... を調べてパラメーターが最適化されている相を確認 青色の相は最適化されている 黒色の相は最適化されていないが各 2 成分の相互作用パラメーターは最適化されている 134
135 Cr-Fe-Ni 3 成分系状態図 3. Phase Diagram を起動 Components Window 4. 新規設定 5. 単位を設定 7. + をクリックして入力場所を作成 6. SGTE を選択 8. 物質を入力 9. Next をクリック 135
136 Cr-Fe-Ni 3 成分系状態図 Menu Window 10. 平衡状態で存在しそうな溶体相を選択 11. Variables をクリック ( 次ページ参照 ) 純物質は選択しない 136
137 Cr-Fe-Ni 3 成分系状態図 Variables 三角形の状態図 温度と圧力を設定 Next をクリック つの角 A, B, C にそれぞれ対応する物質を選択 A: Cr, B: Ni, C: Fe OK をクリック 順番に注意 #1:A-Corner #2:C-Corner #3:B-Corner 137
138 Cr-Fe-Ni 3 成分系状態図 12. Calculate をクリック 計算結果 138
139 Cr-Fe-Ni 3 成分系状態図 タイラインモード タイラインモード 表示したい場所でクリック 139
140 計算状態図 2 EpH モジュール 140
141 EpH モジュールの起動 電位 -ph 図 ( プールべ図 ) の作成純物質データのみが使われる 溶体データは使用できないため非理想水溶液や固溶体を扱うことはできない EpH の起動 141
142 Cu-H 2 O 系の電位 -ph 図 Cu の電位 -ph 図の作成 Cu の電位 -ph 図のサンプル同じ図を EpH モジュールで作成する «Atlas of Electrochemical Equilibriain Aqueous Solution» (M. Pourbaix, PergammonPress, 1966) Cu(OH) 2 は準安定物質で考慮されていない 142
143 Cu-H 2 O 系の電位 -ph 図 データベースの選択 1. Data Search をクリック 2. Fact53 純物質データベースを選択 143
144 Cu-H 2 O 系の電位 -ph 図 3. 1-Metal を選択 Metals に Cu を入力 5. 等圧線をひくときは gas にチェックを入れる 6. 温度 4. Next をクリック 7. X 軸 Y 軸 8. ラベル 144
145 Cu-H 2 O 系の電位 -ph 図 9. 計算に含める物質の選択物質の活量 分圧 質量モル濃度の設定 11. ボタンをクリック 10. 準安定物質 Cu(OH) 2 (s) を考慮しない 298K のデータしかない 145
146 Cu-H 2 O 系の電位 -ph 図 12. 各イオンの活量 ( 希薄なので質量モル濃度とみなせる ) を共通の値に設定 この値は 腐食域 不動態域 不感域の境界線に関係する 13. Calculate をクリック 146
147 Cu-H 2 O 系の電位 -ph 図 計算結果 プールべが作成した図と比較 147
148 FactSage 無料体験セミナー 2011 抜粋資料 2012 年 2 月 14 日 著者 : 深山大元 Research Center of Computational Mechanics, Inc. 株式会社計算力学研究センター 東京都品川区戸越 戸越 NI ビル TEL: FAX
鉄 (Fe) の酸化に関するポテンシャル図 Keyword: ポテンシャル図計算 自由エネルギー表示 酸化反応 酸素分圧の計算 はじめに鉄 (Fe) は 酸化することにより酸化鉄と総称される 酸化数に応じて 酸化第一鉄 ( ウスタイト :FeO) 赤鉄鋼( ヘマタイト :Fe 2O 3) 磁鉄鉱(
 鉄 (Fe) の酸化に関するポテンシャル図 Keyword: ポテンシャル図計算 自由エネルギー表示 酸化反応 酸素分圧の計算 はじめに鉄 (Fe) は 酸化することにより酸化鉄と総称される 酸化数に応じて 酸化第一鉄 ( ウスタイト :FeO) 赤鉄鋼( ヘマタイト :Fe 2O ) 磁鉄鉱( マグネタイト :Fe O) と呼称されている ヘマタイトは 工業的用途の一つとしてベンガラという顔料に使用されている
鉄 (Fe) の酸化に関するポテンシャル図 Keyword: ポテンシャル図計算 自由エネルギー表示 酸化反応 酸素分圧の計算 はじめに鉄 (Fe) は 酸化することにより酸化鉄と総称される 酸化数に応じて 酸化第一鉄 ( ウスタイト :FeO) 赤鉄鋼( ヘマタイト :Fe 2O ) 磁鉄鉱( マグネタイト :Fe O) と呼称されている ヘマタイトは 工業的用途の一つとしてベンガラという顔料に使用されている
スライド 0
 熱 学 Ⅲ 講義資料 化学反応のエクセルギー解析 京都 芸繊維 学 学院 芸科学研究科機械システム 学部 耕介准教授 2014/5/13 2014/5/9 1/23 なぜ, 化学反応を伴うエクセルギーを学ぶのか?? 従来までに学んだ熱 学 エンジンやガスタービンの反応器は, 外部加熱過程 ( 外部から熱を加える過程 ) に置き換えていた. 実際には化学反応を伴うため, 現実的. 化学反応 を伴う熱
熱 学 Ⅲ 講義資料 化学反応のエクセルギー解析 京都 芸繊維 学 学院 芸科学研究科機械システム 学部 耕介准教授 2014/5/13 2014/5/9 1/23 なぜ, 化学反応を伴うエクセルギーを学ぶのか?? 従来までに学んだ熱 学 エンジンやガスタービンの反応器は, 外部加熱過程 ( 外部から熱を加える過程 ) に置き換えていた. 実際には化学反応を伴うため, 現実的. 化学反応 を伴う熱
(Microsoft PowerPoint _4_25.ppt [\214\335\212\267\203\202\201[\203h])
![(Microsoft PowerPoint _4_25.ppt [\214\335\212\267\203\202\201[\203h]) (Microsoft PowerPoint _4_25.ppt [\214\335\212\267\203\202\201[\203h])](/thumbs/88/115555943.jpg) 平成 25 年度化学入門講義スライド 第 3 回テーマ : 熱力学第一法則 平成 25 年 4 月 25 日 奥野恒久 よく出てくる用語 1 熱力学 (thermodynamcs) 系 (system) 我々が注意を集中したい世界の特定の一部分外界 (surroundngs) 系以外の部分 系 外界 系に比べてはるかに大きい温度 体積 圧力一定系の変化の影響を受けない よく出てくる用語 2 外界との間で開放系
平成 25 年度化学入門講義スライド 第 3 回テーマ : 熱力学第一法則 平成 25 年 4 月 25 日 奥野恒久 よく出てくる用語 1 熱力学 (thermodynamcs) 系 (system) 我々が注意を集中したい世界の特定の一部分外界 (surroundngs) 系以外の部分 系 外界 系に比べてはるかに大きい温度 体積 圧力一定系の変化の影響を受けない よく出てくる用語 2 外界との間で開放系
Microsoft PowerPoint - 熱力学Ⅱ2FreeEnergy2012HP.ppt [互換モード]
![Microsoft PowerPoint - 熱力学Ⅱ2FreeEnergy2012HP.ppt [互換モード] Microsoft PowerPoint - 熱力学Ⅱ2FreeEnergy2012HP.ppt [互換モード]](/thumbs/79/80168709.jpg) 熱力学 Ⅱ 第 章自由エネルギー システム情報工学研究科 構造エネルギー工学専攻 金子暁子 問題 ( 解答 ). 熱量 Q をある系に与えたところ, 系の体積は膨張し, 温度は上昇した. () 熱量 Q は何に変化したか. () またこのとき系の体積がV よりV に変化した.( 圧力は変化無し.) 内部エネルギーはどのように表されるか. また, このときのp-V 線図を示しなさい.. 不可逆過程の例を
熱力学 Ⅱ 第 章自由エネルギー システム情報工学研究科 構造エネルギー工学専攻 金子暁子 問題 ( 解答 ). 熱量 Q をある系に与えたところ, 系の体積は膨張し, 温度は上昇した. () 熱量 Q は何に変化したか. () またこのとき系の体積がV よりV に変化した.( 圧力は変化無し.) 内部エネルギーはどのように表されるか. また, このときのp-V 線図を示しなさい.. 不可逆過程の例を
木村の理論化学小ネタ 液体と液体の混合物 ( 二成分系 ) の気液平衡 はじめに 純物質 A( 液体 ) と純物質 B( 液体 ) が存在し, 分子 A の間に働く力 分子 B の間に働く力 分子 A と分子 B の間に働く力 のとき, A
 との混合物 ( 二成分系 ) の気液平衡 はじめに 純物質 ( ) と純物質 ( ) が存在し, 分子 の間に働く力 分子 の間に働く力 分子 と分子 の間に働く力 のとき, と の混合物は任意の組成 ( モル分率 ) においてラウールの法則が成り立つ ラウールの法則 ある温度で純物質 が気液平衡状態にあるときの の蒸気圧 ( 飽和蒸気圧 ) を, 同温の を含む溶液が気液平衡状態にあるときの溶液中の
との混合物 ( 二成分系 ) の気液平衡 はじめに 純物質 ( ) と純物質 ( ) が存在し, 分子 の間に働く力 分子 の間に働く力 分子 と分子 の間に働く力 のとき, と の混合物は任意の組成 ( モル分率 ) においてラウールの法則が成り立つ ラウールの法則 ある温度で純物質 が気液平衡状態にあるときの の蒸気圧 ( 飽和蒸気圧 ) を, 同温の を含む溶液が気液平衡状態にあるときの溶液中の
平成27年度 前期日程 化学 解答例
 受験番号 平成 27 年度前期日程 化学 ( その 1) 解答用紙 工学部 応用化学科 志願者は第 1 問 ~ 第 4 問を解答せよ 農学部 生物資源科学科, 森林科学科 志願者は第 1 問と第 2 問を解答せよ 第 1 問 [ 二酸化炭素が発生する反応の化学反応式 ] 点 NaHCO 3 + HCl NaCl + H 2 O + CO 2 CO 2 の物質量を x mol とすると, 気体の状態方程式より,
受験番号 平成 27 年度前期日程 化学 ( その 1) 解答用紙 工学部 応用化学科 志願者は第 1 問 ~ 第 4 問を解答せよ 農学部 生物資源科学科, 森林科学科 志願者は第 1 問と第 2 問を解答せよ 第 1 問 [ 二酸化炭素が発生する反応の化学反応式 ] 点 NaHCO 3 + HCl NaCl + H 2 O + CO 2 CO 2 の物質量を x mol とすると, 気体の状態方程式より,
木村の理論化学小ネタ 熱化学方程式と反応熱の分類発熱反応と吸熱反応化学反応は, 反応の前後の物質のエネルギーが異なるため, エネルギーの出入りを伴い, それが, 熱 光 電気などのエネルギーの形で現れる とくに, 化学変化と熱エネルギーの関
 熱化学方程式と反応熱の分類発熱反応と吸熱反応化学反応は, 反応の前後の物質のエネルギーが異なるため, エネルギーの出入りを伴い, それが, 熱 光 電気などのエネルギーの形で現れる とくに, 化学変化と熱エネルギーの関係を扱う化学の一部門を熱化学という 発熱反応反応前の物質のエネルギー 大ネルギ熱エネルギーー小エ反応後の物質のエネルギー 吸熱反応 反応後の物質のエネルギー 大ネルギー熱エネルギー小エ反応前の物質のエネルギー
熱化学方程式と反応熱の分類発熱反応と吸熱反応化学反応は, 反応の前後の物質のエネルギーが異なるため, エネルギーの出入りを伴い, それが, 熱 光 電気などのエネルギーの形で現れる とくに, 化学変化と熱エネルギーの関係を扱う化学の一部門を熱化学という 発熱反応反応前の物質のエネルギー 大ネルギ熱エネルギーー小エ反応後の物質のエネルギー 吸熱反応 反応後の物質のエネルギー 大ネルギー熱エネルギー小エ反応前の物質のエネルギー
例題 1 表は, 分圧 Pa, 温度 0 および 20 において, 水 1.00L に溶解する二酸化炭素と 窒素の物質量を表している 二酸化炭素窒素 mol mol mol mol 温度, 圧力, 体積を変えられる容器を用意し,
 ヘンリーの法則問題の解き方 A. ヘンリーの法則とは溶解度が小さいある気体 ( 溶媒分子との結合力が無視できる気体 ) が, 同温 同体積の溶媒に溶けるとき, 溶解可能な気体の物質量または標準状態換算体積はその気体の分圧に比例する つまり, 気体の分圧が P のとき, ある温度 ある体積の溶媒に n mol または標準状態に換算してV L 溶けるとすると, 分圧が kp のとき, その溶媒に kn
ヘンリーの法則問題の解き方 A. ヘンリーの法則とは溶解度が小さいある気体 ( 溶媒分子との結合力が無視できる気体 ) が, 同温 同体積の溶媒に溶けるとき, 溶解可能な気体の物質量または標準状態換算体積はその気体の分圧に比例する つまり, 気体の分圧が P のとき, ある温度 ある体積の溶媒に n mol または標準状態に換算してV L 溶けるとすると, 分圧が kp のとき, その溶媒に kn
<4D F736F F F696E74202D A E90B6979D89C8816B91E63195AA96EC816C82DC82C682DF8D758DC03189BB8A7795CF89BB82C68CB48E AA8E E9197BF2E >
 中学 2 年理科まとめ講座 第 1 分野 1. 化学変化と原子 分子 物質の成り立ち 化学変化 化学変化と物質の質量 基本の解説と問題 講師 : 仲谷のぼる 1 物質の成り立ち 物質のつくり 物質をつくる それ以上分けることができない粒を原子という いくつかの原子が結びついてできたものを分子という いろいろな物質のうち 1 種類の原子からできている物質を単体 2 種類以上の原子からできている物質を化合物という
中学 2 年理科まとめ講座 第 1 分野 1. 化学変化と原子 分子 物質の成り立ち 化学変化 化学変化と物質の質量 基本の解説と問題 講師 : 仲谷のぼる 1 物質の成り立ち 物質のつくり 物質をつくる それ以上分けることができない粒を原子という いくつかの原子が結びついてできたものを分子という いろいろな物質のうち 1 種類の原子からできている物質を単体 2 種類以上の原子からできている物質を化合物という
高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ
![高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ 高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ](/thumbs/94/118405200.jpg) 高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ溶質の20% 溶液 100gと30% 溶液 200gを混ぜると質量 % はいくらになるか ( 有効数字
高 1 化学冬期課題試験 1 月 11 日 ( 水 ) 実施 [1] 以下の問題に答えよ 1)200g 溶液中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 整数 ) 2)200g 溶媒中に溶質が20g 溶けている この溶液の質量 % はいくらか ( 有効数字 2 桁 ) 3) 同じ溶質の20% 溶液 100gと30% 溶液 200gを混ぜると質量 % はいくらになるか ( 有効数字
第 11 回化学概論 酸化と還元 P63 酸化還元反応 酸化数 酸化剤 還元剤 金属のイオン化傾向 酸化される = 酸素と化合する = 水素を奪われる = 電子を失う = 酸化数が増加する 還元される = 水素と化合する = 酸素を奪われる = 電子を得る = 酸化数が減少する 銅の酸化酸化銅の還元
 第 11 回化学概論 酸化と還元 P63 酸化還元反応 酸化数 酸化剤 還元剤 金属のイオン化傾向 酸化される = 酸素と化合する = 水素を奪われる = 電子を失う = 酸化数が増加する 還元される = 水素と化合する = 酸素を奪われる = 電子を得る = 酸化数が減少する 銅の酸化酸化銅の還元 2Cu + O 2 2CuO CuO + H 2 Cu + H 2 O Cu Cu 2+ + 2e
第 11 回化学概論 酸化と還元 P63 酸化還元反応 酸化数 酸化剤 還元剤 金属のイオン化傾向 酸化される = 酸素と化合する = 水素を奪われる = 電子を失う = 酸化数が増加する 還元される = 水素と化合する = 酸素を奪われる = 電子を得る = 酸化数が減少する 銅の酸化酸化銅の還元 2Cu + O 2 2CuO CuO + H 2 Cu + H 2 O Cu Cu 2+ + 2e
CERT化学2013前期_問題
 [1] から [6] のうち 5 問を選んで解答用紙に解答せよ. いずれも 20 点の配点である.5 問を超えて解答した場合, 正答していれば成績評価に加算する. 有効数字を適切に処理せよ. 断りのない限り大気圧は 1013 hpa とする. 0 C = 273 K,1 cal = 4.184 J,1 atm = 1013 hpa = 760 mmhg, 重力加速度は 9.806 m s 2, 気体
[1] から [6] のうち 5 問を選んで解答用紙に解答せよ. いずれも 20 点の配点である.5 問を超えて解答した場合, 正答していれば成績評価に加算する. 有効数字を適切に処理せよ. 断りのない限り大気圧は 1013 hpa とする. 0 C = 273 K,1 cal = 4.184 J,1 atm = 1013 hpa = 760 mmhg, 重力加速度は 9.806 m s 2, 気体
気体の性質-理想気体と状態方程式
 自由エネルギー 熱力学関数 202 5/3 第 3セメスター化学 B 第 7 回講義担当奥西みさき前回の復習 : エントロピー今回の主題 : 自由エネルギー 講義資料は研究室のWebに掲載 htt://www.tagen.tohoku.ac.j/labo/ueda/index-j.html クラウジウスの式 サイクルに流れ込む熱量を正とする 不可逆サイクル 2 可逆サイクル η 熱機関 C η 熱機関
自由エネルギー 熱力学関数 202 5/3 第 3セメスター化学 B 第 7 回講義担当奥西みさき前回の復習 : エントロピー今回の主題 : 自由エネルギー 講義資料は研究室のWebに掲載 htt://www.tagen.tohoku.ac.j/labo/ueda/index-j.html クラウジウスの式 サイクルに流れ込む熱量を正とする 不可逆サイクル 2 可逆サイクル η 熱機関 C η 熱機関
<4D F736F F D2089BB8A778AEE E631358D E5F89BB8AD28CB3>
 第 15 講 酸化と還元 酸化 還元とは切ったリンゴをそのまま放置すると, 時間が経つにつれて断面が変色します これはリンゴの断面が酸化した現象を示しています ピカピカの10 円玉も, しばらくすると黒く, くすんでいきます これも酸化です この10 円玉を水素ガスのなかに入れると, 元のきれいな10 円玉に戻ります これが還元です 1 酸化還元の定義 2 酸化数とは? 3 酸化剤 還元剤についての理解
第 15 講 酸化と還元 酸化 還元とは切ったリンゴをそのまま放置すると, 時間が経つにつれて断面が変色します これはリンゴの断面が酸化した現象を示しています ピカピカの10 円玉も, しばらくすると黒く, くすんでいきます これも酸化です この10 円玉を水素ガスのなかに入れると, 元のきれいな10 円玉に戻ります これが還元です 1 酸化還元の定義 2 酸化数とは? 3 酸化剤 還元剤についての理解
PowerPoint プレゼンテーション
 熱力学第一法則 1 物体が他の物体に与える影響 動かす / 止める ふくらませる / しぼませる 温める / 冷やす 明るくする / 暗くする 結合させる / 分解させる 電気を流す / 電気を消費する 機械的エネルギー ( 仕事 ) 熱エネルギー ( 熱量 ) 光エネルギー 化学エネルギー電気的エネルギー 系の内部エネルギーの変化量 ΔU = ( 仕事 )+( 化学エネルギー )+( 電気的エネルギー
熱力学第一法則 1 物体が他の物体に与える影響 動かす / 止める ふくらませる / しぼませる 温める / 冷やす 明るくする / 暗くする 結合させる / 分解させる 電気を流す / 電気を消費する 機械的エネルギー ( 仕事 ) 熱エネルギー ( 熱量 ) 光エネルギー 化学エネルギー電気的エネルギー 系の内部エネルギーの変化量 ΔU = ( 仕事 )+( 化学エネルギー )+( 電気的エネルギー
Slide 1
 3. 溶解 沈殿反応 天然水の化学組成 大陸地殻表層 (mg kg ) 河川水 (mg kg ) Al 77.4.5 Fe 3.9.4 Ca 9.4 3.4 Na 5.7 5. 8.6.3 Mg 3.5 3.4 Andrews et al. (3) An introduction to Environmental Chemistry 天然水の特徴 天然水の金属イオンは主に岩石の風化により生じる ただし
3. 溶解 沈殿反応 天然水の化学組成 大陸地殻表層 (mg kg ) 河川水 (mg kg ) Al 77.4.5 Fe 3.9.4 Ca 9.4 3.4 Na 5.7 5. 8.6.3 Mg 3.5 3.4 Andrews et al. (3) An introduction to Environmental Chemistry 天然水の特徴 天然水の金属イオンは主に岩石の風化により生じる ただし
Microsoft PowerPoint - ‚æ4‘Í
 第 4 章平衡状態 目的物質の平衡状態と自由エネルギーの関係を理解するとともに, 平衡状態図の基礎的な知識を習得する. 4.1 自由エネルギー 4.1.1 平衡状態 4.1.2 熱力学第 1 法則 4.1.3 熱力学第 2 法則 4.1.4 自由エネルギー 4.2 平衡状態と自由エネルギー 4.2.1 レバールール 4.2.2 平衡状態と自由エネルギー 4.3 平衡状態図 4.3.1 全率固溶型 4.3.2
第 4 章平衡状態 目的物質の平衡状態と自由エネルギーの関係を理解するとともに, 平衡状態図の基礎的な知識を習得する. 4.1 自由エネルギー 4.1.1 平衡状態 4.1.2 熱力学第 1 法則 4.1.3 熱力学第 2 法則 4.1.4 自由エネルギー 4.2 平衡状態と自由エネルギー 4.2.1 レバールール 4.2.2 平衡状態と自由エネルギー 4.3 平衡状態図 4.3.1 全率固溶型 4.3.2
目次 I. 孤立系 ( 気相 ) II. 単成分液体 III. 混合液体 1 希薄水溶液 2 任意の濃度の溶液 IV. タンパク質 1 リガンドなし 2 リガンドあり V. ポリマー VI. 固液界面補足 Acpypeによる電荷の割り当て補足 RESP 電荷の割り当て 2017/10/01 Copy
 Winmostar チュートリアルシミュレーションセルの作成 V8.000 株式会社クロスアビリティ question@winmostar.com 2017/10/01 目次 I. 孤立系 ( 気相 ) II. 単成分液体 III. 混合液体 1 希薄水溶液 2 任意の濃度の溶液 IV. タンパク質 1 リガンドなし 2 リガンドあり V. ポリマー VI. 固液界面補足 Acpypeによる電荷の割り当て補足
Winmostar チュートリアルシミュレーションセルの作成 V8.000 株式会社クロスアビリティ question@winmostar.com 2017/10/01 目次 I. 孤立系 ( 気相 ) II. 単成分液体 III. 混合液体 1 希薄水溶液 2 任意の濃度の溶液 IV. タンパク質 1 リガンドなし 2 リガンドあり V. ポリマー VI. 固液界面補足 Acpypeによる電荷の割り当て補足
MM1_02_ThermodynamicsAndPhaseDiagram
 2.9 三元系の平衡 現実に用いられている実用合金の多くは 3 つ以上の成分からなる多元系合金であ る 従って 三元系状態図を理解することは 非常に重要である 前節までの二元系 状態図の場合の考え方は 基本的に三元以上の系にも適用できる Fig.2.46 Gibbs の三角形 三元合金の組成は Fig.2.46 に示す正三角形 (Gibbs の三角形 ) 上に示すことができる 三角形の各頂点は それぞれ
2.9 三元系の平衡 現実に用いられている実用合金の多くは 3 つ以上の成分からなる多元系合金であ る 従って 三元系状態図を理解することは 非常に重要である 前節までの二元系 状態図の場合の考え方は 基本的に三元以上の系にも適用できる Fig.2.46 Gibbs の三角形 三元合金の組成は Fig.2.46 に示す正三角形 (Gibbs の三角形 ) 上に示すことができる 三角形の各頂点は それぞれ
2 Zn Zn + MnO 2 () 2 O 2 2 H2 O + O 2 O 2 MnO 2 2 KClO 3 2 KCl + 3 O 2 O 3 or 3 O 2 2 O 3 N 2 () NH 4 NO 2 2 O + N 2 ( ) MnO HCl Mn O + CaCl(ClO
 1 [1]. Zn + 2 H + Zn 2+,. K Ca Na Mg Al Zn Fe Ni Sn Pb H Cu Hg Ag Pt Au H (H + ),,. [2] ( ) ( ) CO 2, S, SO 2, NH 3 () + () () + () FeS Fe S ( ) + ( ) ( ) + ( ) 2 NH 4 Cl + Ca(OH) 2 Ca O + 2 NH 3,.,,.,,.,.
1 [1]. Zn + 2 H + Zn 2+,. K Ca Na Mg Al Zn Fe Ni Sn Pb H Cu Hg Ag Pt Au H (H + ),,. [2] ( ) ( ) CO 2, S, SO 2, NH 3 () + () () + () FeS Fe S ( ) + ( ) ( ) + ( ) 2 NH 4 Cl + Ca(OH) 2 Ca O + 2 NH 3,.,,.,,.,.
Microsoft PowerPoint - 多成分系の熱力学.pptx
 /7/ 目次 第 3 回講義資料 I. 一成分系の熱力学の復習 II. III. 化学ポテンシャルの導入 相平衡 I. 成分溶液の混合. 化学平衡多成分系の熱力学への拡張と幾つかの基本的な熱力学の問題への応用 I. 一成分系の熱力学の復習. 熱力学の第一法則と第二法則. カルノーサイクル 3. エントロピー 4. 自由エネルギー 5. 熱力学ポテンシャルとマクスウェルの関係式 熱力学の応用にとって最も重要な役割を果たすのが熱力学ポテンシャルであり
/7/ 目次 第 3 回講義資料 I. 一成分系の熱力学の復習 II. III. 化学ポテンシャルの導入 相平衡 I. 成分溶液の混合. 化学平衡多成分系の熱力学への拡張と幾つかの基本的な熱力学の問題への応用 I. 一成分系の熱力学の復習. 熱力学の第一法則と第二法則. カルノーサイクル 3. エントロピー 4. 自由エネルギー 5. 熱力学ポテンシャルとマクスウェルの関係式 熱力学の応用にとって最も重要な役割を果たすのが熱力学ポテンシャルであり
MM1_02_ThermodynamicsAndPhaseDiagram
 2.4 2 成分系 3 回生 材料組織学 1 緒言 次に 2 成分系 ( 例えば元素 A と元素 B から成る A-B 二元系合金 ) の熱力学を取 り扱う 2.4.1 二元固溶体のギブス自由エネルギーいま 純金属 A と純金属 B が同じ結晶構造を持ち これらはどのような組成でも完全に混じり合って 同一の結晶構造の固溶体 (solid solution) を形成すると仮定する いま 1 モルの均一な
2.4 2 成分系 3 回生 材料組織学 1 緒言 次に 2 成分系 ( 例えば元素 A と元素 B から成る A-B 二元系合金 ) の熱力学を取 り扱う 2.4.1 二元固溶体のギブス自由エネルギーいま 純金属 A と純金属 B が同じ結晶構造を持ち これらはどのような組成でも完全に混じり合って 同一の結晶構造の固溶体 (solid solution) を形成すると仮定する いま 1 モルの均一な
PowerPoint プレゼンテーション
 1.2 熱力学の法則 1 エネルギーが移るとき 一部は熱で逃げる ( 熱も含めれば 全エネルギーは保存される ) 自然の法則 なにかが起こる前の物体のエネルギー なにかが起こった後の物体のエネルギー = 他の物体に与える影響 + 熱 これまでに実験的 理論的な反例がない 熱力学第一法則 2 物体が他の物体に与える影響 動かす / 止める ふくらませる / しぼませる 温める / 冷やす 明るくする
1.2 熱力学の法則 1 エネルギーが移るとき 一部は熱で逃げる ( 熱も含めれば 全エネルギーは保存される ) 自然の法則 なにかが起こる前の物体のエネルギー なにかが起こった後の物体のエネルギー = 他の物体に与える影響 + 熱 これまでに実験的 理論的な反例がない 熱力学第一法則 2 物体が他の物体に与える影響 動かす / 止める ふくらませる / しぼませる 温める / 冷やす 明るくする
2014 年度大学入試センター試験解説 化学 Ⅰ 第 1 問物質の構成 1 問 1 a 1 g に含まれる分子 ( 分子量 M) の数は, アボガドロ定数を N A /mol とすると M N A 個 と表すことができる よって, 分子量 M が最も小さい分子の分子数が最も多い 分 子量は, 1 H
 01 年度大学入試センター試験解説 化学 Ⅰ 第 1 問物質の構成 1 問 1 a 1 g に含まれる分子 ( 分子量 M) の数は, アボガドロ定数を N A /mol とすると M N A 個 と表すことができる よって, 分子量 M が最も小さい分子の分子数が最も多い 分 子量は, 1 = 18 N = 8 3 6 = 30 Ne = 0 5 = 3 6 l = 71 となり,1 が解答 (
01 年度大学入試センター試験解説 化学 Ⅰ 第 1 問物質の構成 1 問 1 a 1 g に含まれる分子 ( 分子量 M) の数は, アボガドロ定数を N A /mol とすると M N A 個 と表すことができる よって, 分子量 M が最も小さい分子の分子数が最も多い 分 子量は, 1 = 18 N = 8 3 6 = 30 Ne = 0 5 = 3 6 l = 71 となり,1 が解答 (
A solution to Problems(物理化学II)Problem5
 A solution to roblems( 物理化学 II)roblem 5 ) Q 0, W 0, Δ 0, ΔU0, nr dg - Sd d より, G - 8.345 298 2.303log(6/) - 4440(J/mol) da - Sd d A - 8.345 298 2.303log(6/) - 4440(J/mol) 2) da - Sd d A ΔA da d, ΔG d R
A solution to roblems( 物理化学 II)roblem 5 ) Q 0, W 0, Δ 0, ΔU0, nr dg - Sd d より, G - 8.345 298 2.303log(6/) - 4440(J/mol) da - Sd d A - 8.345 298 2.303log(6/) - 4440(J/mol) 2) da - Sd d A ΔA da d, ΔG d R
(Microsoft Word - \230a\225\266IChO46-Preparatory_Q36_\211\374\202Q_.doc)
 問題 36. 鉄 (Ⅲ) イオンとサリチルサリチル酸の錯形成 (20140304 修正 : ピンク色の部分 ) 1. 序論この簡単な実験では 水溶液中での鉄 (Ⅲ) イオンとサリチル酸の錯形成を検討する その錯体の実験式が求められ その安定度定数を見積もることができる 鉄 (Ⅲ) イオンとサリチル酸 H 2 Sal からなる安定な錯体はいくつか知られている それらの構造と組成はpHにより異なる 酸性溶液では紫色の錯体が生成する
問題 36. 鉄 (Ⅲ) イオンとサリチルサリチル酸の錯形成 (20140304 修正 : ピンク色の部分 ) 1. 序論この簡単な実験では 水溶液中での鉄 (Ⅲ) イオンとサリチル酸の錯形成を検討する その錯体の実験式が求められ その安定度定数を見積もることができる 鉄 (Ⅲ) イオンとサリチル酸 H 2 Sal からなる安定な錯体はいくつか知られている それらの構造と組成はpHにより異なる 酸性溶液では紫色の錯体が生成する
Xamテスト作成用テンプレート
 気体の性質 1 1990 年度本試験化学第 2 問 問 1 次の問い (a b) に答えよ a 一定質量の理想気体の温度を T 1 [K] または T 2 [K] に保ったまま, 圧力 P を変える このときの気体の体積 V[L] と圧力 P[atm] との関係を表すグラフとして, 最も適当なものを, 次の1~6のうちから一つ選べ ただし,T 1 >T 2 とする b 理想気体 1mol がある 圧力を
気体の性質 1 1990 年度本試験化学第 2 問 問 1 次の問い (a b) に答えよ a 一定質量の理想気体の温度を T 1 [K] または T 2 [K] に保ったまま, 圧力 P を変える このときの気体の体積 V[L] と圧力 P[atm] との関係を表すグラフとして, 最も適当なものを, 次の1~6のうちから一つ選べ ただし,T 1 >T 2 とする b 理想気体 1mol がある 圧力を
暔棟壔妛墘廗栤戣
 化学 III 演習問題 1 L = 1dm 3,1 cal = 4.184 J,R = 8.314 J K -1 mol -1 I. 物質の存在状態 1. 原子, 分子の構造について説明せよ キーワード電子, 原子核, 陽子, 中性子, 共有結合, 水分子などの具体的分子 2. 物質の三態について, それぞれの特徴およびそれらの間の違いを説明せよ キーワード固体, 液体, 気体, 構造, 分子の運動状態
化学 III 演習問題 1 L = 1dm 3,1 cal = 4.184 J,R = 8.314 J K -1 mol -1 I. 物質の存在状態 1. 原子, 分子の構造について説明せよ キーワード電子, 原子核, 陽子, 中性子, 共有結合, 水分子などの具体的分子 2. 物質の三態について, それぞれの特徴およびそれらの間の違いを説明せよ キーワード固体, 液体, 気体, 構造, 分子の運動状態
物理学 II( 熱力学 ) 期末試験問題 (2) 問 (2) : 以下のカルノーサイクルの p V 線図に関して以下の問題に答えなさい. (a) "! (a) p V 線図の各過程 ( ) の名称とそのと (& きの仕事 W の面積を図示せよ. # " %&! (' $! #! " $ %'!!!
 物理学 II( 熱力学 ) 期末試験問題 & 解答 (1) 問 (1): 以下の文章の空欄に相応しい用語あるいは文字式を記入しなさい. 温度とは物体の熱さ冷たさを表す概念である. 物体は外部の影響を受けなければ, 十分な時間が経過すると全体が一様な温度の定常的な熱平衡状態となる. 物体 と物体 が熱平衡にあり, 物体 と物体 が熱平衡にあるならば, 物体 と物体 も熱平衡にある. これを熱力学第 0
物理学 II( 熱力学 ) 期末試験問題 & 解答 (1) 問 (1): 以下の文章の空欄に相応しい用語あるいは文字式を記入しなさい. 温度とは物体の熱さ冷たさを表す概念である. 物体は外部の影響を受けなければ, 十分な時間が経過すると全体が一様な温度の定常的な熱平衡状態となる. 物体 と物体 が熱平衡にあり, 物体 と物体 が熱平衡にあるならば, 物体 と物体 も熱平衡にある. これを熱力学第 0
偏微分の定義より が非常に小さい時には 与式に上の関係を代入すれば z f f f ) f f f dz { f } f f f f f 非常に小さい = 0 f f z z dz d d opright: A.Asano 7 まとめ z = f (, 偏微分 独立変数が 個以上 ( 今は つだけ考
 opright: A.Asano 微分 偏微分 Δ の使い分け 微分の定義 従属変数 = f () という関数の微分を考える は独立変数 熱力学のための数学基礎 U du d Δ: ある状態と他の状態の差を表しています U d : 微分記号 Δ の差が極微小 極限的に 0 の関係を表します : 偏微分記号 変数が つ以上で成り立っている関数で d f ( ) f ( ) lim lim d 0 0
opright: A.Asano 微分 偏微分 Δ の使い分け 微分の定義 従属変数 = f () という関数の微分を考える は独立変数 熱力学のための数学基礎 U du d Δ: ある状態と他の状態の差を表しています U d : 微分記号 Δ の差が極微小 極限的に 0 の関係を表します : 偏微分記号 変数が つ以上で成り立っている関数で d f ( ) f ( ) lim lim d 0 0
505_切削オーバーレイ
 切削オーバーレイ [ 測量計算 ] の [ 切削オーバーレイ ] について 簡単な操作例で解説します 解説内容がオプションプログラムの説明である場合があります ご了承ください 目次 切削オーバーレイ. 作業設定 - [ 建設 CAD] を起動する - [ 切削オーバーレイ ] を起動する - 設計層を設定する. 現地盤の入力 - 入力条件を確認する - 測点を自動入力する - 地盤高を入力する 6
切削オーバーレイ [ 測量計算 ] の [ 切削オーバーレイ ] について 簡単な操作例で解説します 解説内容がオプションプログラムの説明である場合があります ご了承ください 目次 切削オーバーレイ. 作業設定 - [ 建設 CAD] を起動する - [ 切削オーバーレイ ] を起動する - 設計層を設定する. 現地盤の入力 - 入力条件を確認する - 測点を自動入力する - 地盤高を入力する 6
等温可逆膨張最大仕事 : 外界と力学的平衡を保って膨張するとき 系は最大の仕事をする完全気体を i から まで膨張させるときの仕事は dw d dw nr d, w nr ln i nr 1 dw d nr d i i nr (ln lni ) nr ln これは右図 ( テキスト p.45, 図
 物理化学 Ⅱ 講義資料 ( 第 章熱力学第一法則 ) エネルギーの保存 1 系と外界系 : 注目している空間 下記の つに分類される 開放系 : 外界との間でエネルギーの交換ができ さらに物資の移動も可能閉鎖系 : 外界との間でエネルギーの交換はできるが 物質の移動はできない孤立系 : 外界との間でエネルギーも物質も移動できない外界 : 系と接触している巨大な世界 例えば エネルギーの出入りがあっても
物理化学 Ⅱ 講義資料 ( 第 章熱力学第一法則 ) エネルギーの保存 1 系と外界系 : 注目している空間 下記の つに分類される 開放系 : 外界との間でエネルギーの交換ができ さらに物資の移動も可能閉鎖系 : 外界との間でエネルギーの交換はできるが 物質の移動はできない孤立系 : 外界との間でエネルギーも物質も移動できない外界 : 系と接触している巨大な世界 例えば エネルギーの出入りがあっても
HSC Chemistry for Windows
 HSC 8 の新機能 HSC メインメニュー HSC 8 のおもな新機能 最新の Microsoft.NET 4.5 環境を使って HSC 7 の計算モジュールの大部分が書き直されました これは最新のウィンドウズの下で HSC の開発を続行できることになります アップデートされた HSC モジュールに多くの新機能が付け加えられました 計算ルーチンの精度が改良されました データベースは 25,000
HSC 8 の新機能 HSC メインメニュー HSC 8 のおもな新機能 最新の Microsoft.NET 4.5 環境を使って HSC 7 の計算モジュールの大部分が書き直されました これは最新のウィンドウズの下で HSC の開発を続行できることになります アップデートされた HSC モジュールに多くの新機能が付け加えられました 計算ルーチンの精度が改良されました データベースは 25,000
<576F F202D F94BD899E8EAE82CC8DEC82E895FB5F31325F352E6C7770>
 1 ( 問 ) 金属が溶けて H 2 を発生する場合 ( 例 ) 1. 金属と H で考える Na H 2O H 2 Fe H 2 H 2 2Na 2H 2Na H 2 Fe 2H Fe 2 H 2 2. 水の場合は OH を両辺に加える 2'. 酸の場合は 酸の陰イオンを両辺に加える 3. たし算をする Na H 2O K H 2O Ca H 2O Mg H 2O Zn H 2 Fe H 2 Al
1 ( 問 ) 金属が溶けて H 2 を発生する場合 ( 例 ) 1. 金属と H で考える Na H 2O H 2 Fe H 2 H 2 2Na 2H 2Na H 2 Fe 2H Fe 2 H 2 2. 水の場合は OH を両辺に加える 2'. 酸の場合は 酸の陰イオンを両辺に加える 3. たし算をする Na H 2O K H 2O Ca H 2O Mg H 2O Zn H 2 Fe H 2 Al
Microsoft PowerPoint - siryo7
 . 化学反応と溶液 - 遷移状態理論と溶液論 -.. 遷移状態理論 と溶液論 7 年 5 月 5 日 衝突論と遷移状態理論の比較 + 生成物 原子どうしの反応 活性錯体 ( 遷移状態 ) は 3つの並進 つの回転の自由度をもつ (1つの振動モードは分解に相当 ) 3/ [ ( m m) T] 8 IT q q π + π tansqot 3 h h との並進分配関数 [ πmt] 3/ [ ] 3/
. 化学反応と溶液 - 遷移状態理論と溶液論 -.. 遷移状態理論 と溶液論 7 年 5 月 5 日 衝突論と遷移状態理論の比較 + 生成物 原子どうしの反応 活性錯体 ( 遷移状態 ) は 3つの並進 つの回転の自由度をもつ (1つの振動モードは分解に相当 ) 3/ [ ( m m) T] 8 IT q q π + π tansqot 3 h h との並進分配関数 [ πmt] 3/ [ ] 3/
AutoTune 機能 1.AutoTune 機能 AutoTune 機能を使用して 測定化合物のモニターイオン (m/z) コーン電圧 及び (MS/ MS システムの場合 ) コリジョンエネルギーの最適化を行い MS メソッドを自動作成する方法についてご紹介します 同時にレポートを印刷することも
 1. を使用して 測定化合物のモニターイオン (m/z) コーン電圧 及び (MS/ MS システムの場合 ) コリジョンエネルギーの最適化を行い MS メソッドを自動作成する方法についてご紹介します 同時にレポートを印刷することも可能です 1.1 測定化合物のイオン化確認 シリンジに 測定化合物 ( 濃度 0.1 ~ 1 μg/ml 前後 ) を準備します ( 最初から高濃度のものを MS に導入しますと
1. を使用して 測定化合物のモニターイオン (m/z) コーン電圧 及び (MS/ MS システムの場合 ) コリジョンエネルギーの最適化を行い MS メソッドを自動作成する方法についてご紹介します 同時にレポートを印刷することも可能です 1.1 測定化合物のイオン化確認 シリンジに 測定化合物 ( 濃度 0.1 ~ 1 μg/ml 前後 ) を準備します ( 最初から高濃度のものを MS に導入しますと
物理化学I-第12回(13).ppt
 I- 12-1 11 11.1 2Mg(s) + O 2 (g) 2MgO(s) [Mg 2+ O 2 ] Zn(s) + Cu 2+ (aq) Zn 2+ (aq) + Cu(s) - 2Mg(s) 2Mg 2+ (s) + 4e +) O 2 (g) + 4e 2O 2 (s) 2Mg(s) + O 2 (g) 2MgO(s) Zn(s) Zn 2+ (aq) + 2e +) Cu 2+ (aq)
I- 12-1 11 11.1 2Mg(s) + O 2 (g) 2MgO(s) [Mg 2+ O 2 ] Zn(s) + Cu 2+ (aq) Zn 2+ (aq) + Cu(s) - 2Mg(s) 2Mg 2+ (s) + 4e +) O 2 (g) + 4e 2O 2 (s) 2Mg(s) + O 2 (g) 2MgO(s) Zn(s) Zn 2+ (aq) + 2e +) Cu 2+ (aq)
イオン化傾向 イオン化傾向 1 金属の単体はいずれも酸化されて陽イオンになりうる 金属のイオンのなりやすさを表したものをイオン化傾向という イオン化傾向 K Ca Na Mg Al Zn Fe Ni Sn Pb (H) Cu Hg Ag Pt Au e- を出してイオンになりやすい酸化されやすい イ
 イオン化傾向 イオン化傾向 金属の単体はいずれも酸化されて陽イオンになりうる 金属のイオンのなりやすさを表したものをイオン化傾向という イオン化傾向 K Ca Na Mg Al Zn Fe Ni Sn Pb (H) Cu Hg Ag Pt Au e- を出してイオンになりやすい酸化されやすい イオンになりにくい酸化されにくい イオン化傾向の覚え方 K かそう Ca か Na な Mg ま Al あ
イオン化傾向 イオン化傾向 金属の単体はいずれも酸化されて陽イオンになりうる 金属のイオンのなりやすさを表したものをイオン化傾向という イオン化傾向 K Ca Na Mg Al Zn Fe Ni Sn Pb (H) Cu Hg Ag Pt Au e- を出してイオンになりやすい酸化されやすい イオンになりにくい酸化されにくい イオン化傾向の覚え方 K かそう Ca か Na な Mg ま Al あ
化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イ
 化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イオンと陰イオンの静電気的な引力による結合を 1 1 という ⑵ 2 個の水素原子は, それぞれ1 個の価電子を出し合い,
化学 1( 応用生物 生命健康科 現代教育学部 ) ( 解答番号 1 ~ 29 ) Ⅰ 化学結合に関する ⑴~⑶ の文章を読み, 下の問い ( 問 1~5) に答えよ ⑴ 塩化ナトリウム中では, ナトリウムイオン Na + と塩化物イオン Cl - が静電気的な引力で結び ついている このような陽イオンと陰イオンの静電気的な引力による結合を 1 1 という ⑵ 2 個の水素原子は, それぞれ1 個の価電子を出し合い,
フォルハルト法 NH SCN の標準液または KSCN の標準液を用い,Ag または Hg を直接沈殿滴定する方法 および Cl, Br, I, CN, 試料溶液に Fe SCN, S 2 を指示薬として加える 例 : Cl の逆滴定による定量 などを逆滴定する方法をいう Fe を加えた試料液に硝酸
 沈殿滴定とモール法 沈殿滴定沈殿とは溶液に試薬を加えたり加熱や冷却をしたとき, 溶液から不溶性固体が分離する現象, またはその不溶性固体を沈殿という 不溶性固体は, 液底に沈んでいいても微粒子 ( コロイド ) として液中を浮遊していても沈殿と呼ばれる 沈殿滴定とは沈殿が生成あるいは消失する反応を利用した滴定のことをいう 沈殿が生成し始めた点, 沈殿の生成が完了した点, または沈殿が消失した点が滴定の終点となる
沈殿滴定とモール法 沈殿滴定沈殿とは溶液に試薬を加えたり加熱や冷却をしたとき, 溶液から不溶性固体が分離する現象, またはその不溶性固体を沈殿という 不溶性固体は, 液底に沈んでいいても微粒子 ( コロイド ) として液中を浮遊していても沈殿と呼ばれる 沈殿滴定とは沈殿が生成あるいは消失する反応を利用した滴定のことをいう 沈殿が生成し始めた点, 沈殿の生成が完了した点, または沈殿が消失した点が滴定の終点となる
B. モル濃度 速度定数と化学反応の速さ 1.1 段階反応 ( 単純反応 ): + I HI を例に H ヨウ化水素 HI が生成する速さ は,H と I のモル濃度をそれぞれ [ ], [ I ] [ H ] [ I ] に比例することが, 実験により, わかっている したがって, 比例定数を k
![B. モル濃度 速度定数と化学反応の速さ 1.1 段階反応 ( 単純反応 ): + I HI を例に H ヨウ化水素 HI が生成する速さ は,H と I のモル濃度をそれぞれ [ ], [ I ] [ H ] [ I ] に比例することが, 実験により, わかっている したがって, 比例定数を k B. モル濃度 速度定数と化学反応の速さ 1.1 段階反応 ( 単純反応 ): + I HI を例に H ヨウ化水素 HI が生成する速さ は,H と I のモル濃度をそれぞれ [ ], [ I ] [ H ] [ I ] に比例することが, 実験により, わかっている したがって, 比例定数を k](/thumbs/81/83835231.jpg) 反応速度 触媒 速度定数 反応次数について. 化学反応の速さの表し方 速さとは単位時間あたりの変化の大きさである 大きさの値は 0 以上ですから, 速さは 0 以上の値をとる 化学反応の速さは単位時間あたりの物質のモル濃度変化の大きさで表すのが一般的 たとえば, a + bb c (, B, は物質, a, b, c は係数 ) という反応において,, B, それぞれの反応の速さを, B, とし,
反応速度 触媒 速度定数 反応次数について. 化学反応の速さの表し方 速さとは単位時間あたりの変化の大きさである 大きさの値は 0 以上ですから, 速さは 0 以上の値をとる 化学反応の速さは単位時間あたりの物質のモル濃度変化の大きさで表すのが一般的 たとえば, a + bb c (, B, は物質, a, b, c は係数 ) という反応において,, B, それぞれの反応の速さを, B, とし,
Microsoft PowerPoint - anachem2018PPT
 分析化学 II 分担 : 竹原, 恩田 講義分担竹原 :/( 水 ),( 金 ),9,6,/,9,6,( 木 ) 恩田 :/3( 金 ),/7,,,/,5,/,8 竹原の分担内容 クリスチャン分析化学 I 第 7 版, 第 ~5 章 電気分析化学 試験 ( 竹原 ): 中間試験 回 + 最終試験 回 http://www.scc.kyushuu.ac.jp/reac/index_j.html 電気化学的セルアノード
分析化学 II 分担 : 竹原, 恩田 講義分担竹原 :/( 水 ),( 金 ),9,6,/,9,6,( 木 ) 恩田 :/3( 金 ),/7,,,/,5,/,8 竹原の分担内容 クリスチャン分析化学 I 第 7 版, 第 ~5 章 電気分析化学 試験 ( 竹原 ): 中間試験 回 + 最終試験 回 http://www.scc.kyushuu.ac.jp/reac/index_j.html 電気化学的セルアノード
木村の化学重要問題集 01 解答編解説補充 H S H HS ( 第 1 電離平衡 ) HS H S ( 第 電離平衡 ) そこで溶液を中性または塩基性にすることにより, つまり [ H ] を小さくすることにより, 上の電離平衡を右に片寄らせ,[ S ] を大きくする 193. 陽イオン分析 配位
![木村の化学重要問題集 01 解答編解説補充 H S H HS ( 第 1 電離平衡 ) HS H S ( 第 電離平衡 ) そこで溶液を中性または塩基性にすることにより, つまり [ H ] を小さくすることにより, 上の電離平衡を右に片寄らせ,[ S ] を大きくする 193. 陽イオン分析 配位 木村の化学重要問題集 01 解答編解説補充 H S H HS ( 第 1 電離平衡 ) HS H S ( 第 電離平衡 ) そこで溶液を中性または塩基性にすることにより, つまり [ H ] を小さくすることにより, 上の電離平衡を右に片寄らせ,[ S ] を大きくする 193. 陽イオン分析 配位](/thumbs/91/107310906.jpg) 木村の化学重要問題集 01 解答編解説補充 1. 無機物質の性質 反応 187. 気体の製法と性質補足ネスラー試薬とアンモニアの反応 1.. ネスラー試薬 [ HgI ] の調製 KI KI Hg ¾¾ HgI ¾¾ [ HgI ] 赤色沈殿. ネスラー試薬とアンモニアの反応 [ HgI ] ( NH ) [ ] NH HgI ( 微量 : 黄色, 多量 : 赤褐色 ) 190. 陽イオンの分離と性質
木村の化学重要問題集 01 解答編解説補充 1. 無機物質の性質 反応 187. 気体の製法と性質補足ネスラー試薬とアンモニアの反応 1.. ネスラー試薬 [ HgI ] の調製 KI KI Hg ¾¾ HgI ¾¾ [ HgI ] 赤色沈殿. ネスラー試薬とアンモニアの反応 [ HgI ] ( NH ) [ ] NH HgI ( 微量 : 黄色, 多量 : 赤褐色 ) 190. 陽イオンの分離と性質
intra-mart Accel Platform — ViewCreator ユーザ操作ガイド 第6版
 Copyright 2012 NTT DATA INTRAMART CORPORATION 1 Top 目次 intra-mart Accel Platform ViewCreator ユーザ操作ガイド第 6 版 2016-04-01 改訂情報 ViewCreator について基本的な設定データ参照一覧リスト集計クロス集計とグラフ集計データ参照へのショートカットスマートフォンからの参照 2 改訂情報
Copyright 2012 NTT DATA INTRAMART CORPORATION 1 Top 目次 intra-mart Accel Platform ViewCreator ユーザ操作ガイド第 6 版 2016-04-01 改訂情報 ViewCreator について基本的な設定データ参照一覧リスト集計クロス集計とグラフ集計データ参照へのショートカットスマートフォンからの参照 2 改訂情報
Winmostar- Gromacs Tutorial 2 タンパク系 (pdb2gmx を使用 ) V6.005 株式会社クロスアビリティ 2016/1/15
 Winmostar- Gromacs Tutorial 2 タンパク系 (pdb2gmx を使用 ) V6.005 株式会社クロスアビリティ question@winmostar.com 2016/1/15 修正履歴 2015/7/16 版 ( スライド 2) 修正履歴を追加 ( スライド 7) 部分削除の操作修正 ( スライド 9) MDP Run parameters 画面の差し替え (refcoord-scaling
Winmostar- Gromacs Tutorial 2 タンパク系 (pdb2gmx を使用 ) V6.005 株式会社クロスアビリティ question@winmostar.com 2016/1/15 修正履歴 2015/7/16 版 ( スライド 2) 修正履歴を追加 ( スライド 7) 部分削除の操作修正 ( スライド 9) MDP Run parameters 画面の差し替え (refcoord-scaling
Microsoft Word - 第7回講義資料 .docx
 7. 展伸用アルミニウム合金 - 多元系合金 - 今回の講義では, 展伸用アルミニウム合金である Al-Mg 合金 (5000 系 ),Al-Mg-Si 合金 (6000 系 ) 及び Al-Mg-Zn(-Cu) 合金 (7000 系 ) について学習する ( 表 6.1).4000 系に属する Al-Si 合金は主に鋳造用として用いられるため, 鋳造アルミニウム合金の回に詳細を説明する. 7.1
7. 展伸用アルミニウム合金 - 多元系合金 - 今回の講義では, 展伸用アルミニウム合金である Al-Mg 合金 (5000 系 ),Al-Mg-Si 合金 (6000 系 ) 及び Al-Mg-Zn(-Cu) 合金 (7000 系 ) について学習する ( 表 6.1).4000 系に属する Al-Si 合金は主に鋳造用として用いられるため, 鋳造アルミニウム合金の回に詳細を説明する. 7.1
2004 年度センター化学 ⅠB p1 第 1 問問 1 a 水素結合 X HLY X,Y= F,O,N ( ) この形をもつ分子は 5 NH 3 である 1 5 b 昇華性の物質 ドライアイス CO 2, ヨウ素 I 2, ナフタレン 2 3 c 総電子数 = ( 原子番号 ) d CH 4 :6
 004 年度センター化学 ⅠB p 第 問問 a 水素結合 X HLY X,Y= F,O,N ( ) この形をもつ分子は 5 NH である 5 b 昇華性の物質 ドライアイス CO, ヨウ素 I, ナフタレン c 総電子数 = ( 原子番号 ) d CH 4 :6+ 4 = 0個 6+ 8= 4個 7+ 8= 5個 + 7= 8個 4 + 8= 0個 5 8= 6個 4 構造式からアプローチして電子式を書くと次のようになる
004 年度センター化学 ⅠB p 第 問問 a 水素結合 X HLY X,Y= F,O,N ( ) この形をもつ分子は 5 NH である 5 b 昇華性の物質 ドライアイス CO, ヨウ素 I, ナフタレン c 総電子数 = ( 原子番号 ) d CH 4 :6+ 4 = 0個 6+ 8= 4個 7+ 8= 5個 + 7= 8個 4 + 8= 0個 5 8= 6個 4 構造式からアプローチして電子式を書くと次のようになる
Microsoft Word - t30_西_修正__ doc
 反応速度と化学平衡 金沢工業大学基礎教育部西誠 ねらい 化学反応とは分子を構成している原子が組み換り 新しい分子構造を持つことといえます この化学反応がどのように起こるのか どのような速さでどの程度の分子が組み換るのかは 反応の種類や 濃度 温度などの条件で決まってきます そして このような反応の進行方向や速度を正確に予測するために いろいろな数学 物理的な考え方を取り入れて化学反応の理論体系が作られています
反応速度と化学平衡 金沢工業大学基礎教育部西誠 ねらい 化学反応とは分子を構成している原子が組み換り 新しい分子構造を持つことといえます この化学反応がどのように起こるのか どのような速さでどの程度の分子が組み換るのかは 反応の種類や 濃度 温度などの条件で決まってきます そして このような反応の進行方向や速度を正確に予測するために いろいろな数学 物理的な考え方を取り入れて化学反応の理論体系が作られています
1. 報告依頼業務 報告書集計システムを利用して 本部の報告依頼者が 売上実績見通しを各支社から収集し 報告書を作成します 依頼側の業務 1
 つかってみようガイド 報告書集計システム 1. 報告依頼業務 報告書集計システムを利用して 本部の報告依頼者が 売上実績見通しを各支社から収集し 報告書を作成します 依頼側の業務 1 1-1 報告書依頼側のシステム起動 ようこそ ページから 報告書を依頼する方はこちら をクリックします 2 1-1 報告書依頼側のシステム起動 ログインします 本書ではサンプルで登録されている下記ユーザーを利用してご説明します
つかってみようガイド 報告書集計システム 1. 報告依頼業務 報告書集計システムを利用して 本部の報告依頼者が 売上実績見通しを各支社から収集し 報告書を作成します 依頼側の業務 1 1-1 報告書依頼側のシステム起動 ようこそ ページから 報告書を依頼する方はこちら をクリックします 2 1-1 報告書依頼側のシステム起動 ログインします 本書ではサンプルで登録されている下記ユーザーを利用してご説明します
目次 1. 回答作成手順 2 2. ツールの起動 3 3. 一般情報の入力 6 4. 成分表の入力 9 5. 依頼者情報の入力 エラーチェック XMLファイルの作成 動作設定 ( 任意 ) ( ご参考 ) 各種シートのボタン機能 ( ご参
 JAMP MSDSplus 作成マニュアル (Ver.4.0 対応 ) 第 1.00 版 2012.4.2 富士通株式会社 お願い 本資料は富士通グループのお取引先内でのみ 且つ当社グループ向けの調査回答品にのみ利用可能です 目次 1. 回答作成手順 2 2. ツールの起動 3 3. 一般情報の入力 6 4. 成分表の入力 9 5. 依頼者情報の入力 13 6. エラーチェック 14 7. XMLファイルの作成
JAMP MSDSplus 作成マニュアル (Ver.4.0 対応 ) 第 1.00 版 2012.4.2 富士通株式会社 お願い 本資料は富士通グループのお取引先内でのみ 且つ当社グループ向けの調査回答品にのみ利用可能です 目次 1. 回答作成手順 2 2. ツールの起動 3 3. 一般情報の入力 6 4. 成分表の入力 9 5. 依頼者情報の入力 13 6. エラーチェック 14 7. XMLファイルの作成
Microsoft PowerPoint - presentation2007_06_RedoxOxidation.ppt
 酸化還元反応 : xidatinreductin reactin (redx reactin) 酸化還元電位 : redx ptential 化学反応 電池 ( 電気化学セル ): electr chemical cell 硫酸銅 (II) SO SO に変化なし SO SO 電気エネルギー 青色が薄くなる 粒表面に が析出する イオン反応式 ボルタ電池 (Vlta cell) SO H e H H
酸化還元反応 : xidatinreductin reactin (redx reactin) 酸化還元電位 : redx ptential 化学反応 電池 ( 電気化学セル ): electr chemical cell 硫酸銅 (II) SO SO に変化なし SO SO 電気エネルギー 青色が薄くなる 粒表面に が析出する イオン反応式 ボルタ電池 (Vlta cell) SO H e H H
基礎化学 Ⅰ 第 5 講原子量とモル数 第 5 講原子量とモル数 1 原子量 (1) 相対質量 まず, 大きさの復習から 原子 ピンポン玉 原子の直径は, 約 1 億分の 1cm ( 第 1 講 ) 原子とピンポン玉の関係は, ピンポン玉と地球の関係と同じくらいの大きさです 地球 では, 原子 1
 第 5 講原子量とモル数 1 原子量 (1) 相対質量 まず, 大きさの復習から 原子 ピンポン玉 原子の直径は, 約 1 億分の 1cm ( 第 1 講 ) 原子とピンポン玉の関係は, ピンポン玉と地球の関係と同じくらいの大きさです 地球 では, 原子 1 つの質量は? 水素原子は,0.167 10-23 g 酸素原子は,2.656 10-23 g 炭素原子は,1.993 10-23 g 原子の質量は,
第 5 講原子量とモル数 1 原子量 (1) 相対質量 まず, 大きさの復習から 原子 ピンポン玉 原子の直径は, 約 1 億分の 1cm ( 第 1 講 ) 原子とピンポン玉の関係は, ピンポン玉と地球の関係と同じくらいの大きさです 地球 では, 原子 1 つの質量は? 水素原子は,0.167 10-23 g 酸素原子は,2.656 10-23 g 炭素原子は,1.993 10-23 g 原子の質量は,
<979D89F E B E786C7378>
 電気化学 (F2027&F2077) 第 1 回講義平成 22 年 4 月 13 日 ( 火 ) 電気化学の概説 1. カリキュラムの中での本講義の位置づけの理解 2. 電気化学の発展 3. 電気化学の学問領域, 主な分野 4. 電気化学が支える先端技術分野と持続的社会 はじめに の部分 電気化学の歴史, 体系, エネルギー変換電気化学が深く関係する学問領域と先端技術の例を挙げよ電気化学が関係する先端技術の例を挙げよ
電気化学 (F2027&F2077) 第 1 回講義平成 22 年 4 月 13 日 ( 火 ) 電気化学の概説 1. カリキュラムの中での本講義の位置づけの理解 2. 電気化学の発展 3. 電気化学の学問領域, 主な分野 4. 電気化学が支える先端技術分野と持続的社会 はじめに の部分 電気化学の歴史, 体系, エネルギー変換電気化学が深く関係する学問領域と先端技術の例を挙げよ電気化学が関係する先端技術の例を挙げよ
<4D F736F F F696E74202D20352D335F8D5C90AC CF909482CC90B690AC82C695D28F572E707074>
 RD_301 構成要素一覧と検索 から構成要素の編集辞書 ( 削除 ) を作る 作成 ( 編集 ) する削除辞書を開きます 構成要素を検索します ドラック & ドロップでも OK 範囲を選択して右クリック 右クリック 削除辞書に登録 ( 追加 ) したい構成要素を選択しコピーします 削除辞書に追加 ( 貼りつけ ) ます Step5. 削除辞書に構成要素が登録 ( 追加 ) されます 構成要素一覧と検索
RD_301 構成要素一覧と検索 から構成要素の編集辞書 ( 削除 ) を作る 作成 ( 編集 ) する削除辞書を開きます 構成要素を検索します ドラック & ドロップでも OK 範囲を選択して右クリック 右クリック 削除辞書に登録 ( 追加 ) したい構成要素を選択しコピーします 削除辞書に追加 ( 貼りつけ ) ます Step5. 削除辞書に構成要素が登録 ( 追加 ) されます 構成要素一覧と検索
【バーコード作成】マニュアル 第1版
 日本 JC 入場管理システム 2012 バーコードバーコード作成作成マニュアルマニュアル 第 1 版 平成 23 年 1 月 6 日 本書概要本書は JC 入場管理システムにおける バーコード作成機能 操作方法について 説明したものです 改版履歴 更新日版数修正概要 2011/1/6 初版リリース 2 /14 目次 1. バーコードの作成 ( 簡略版 )... 4 2. バーコードの作成 ( ヒサゴ工房工房を利用利用したした場合
日本 JC 入場管理システム 2012 バーコードバーコード作成作成マニュアルマニュアル 第 1 版 平成 23 年 1 月 6 日 本書概要本書は JC 入場管理システムにおける バーコード作成機能 操作方法について 説明したものです 改版履歴 更新日版数修正概要 2011/1/6 初版リリース 2 /14 目次 1. バーコードの作成 ( 簡略版 )... 4 2. バーコードの作成 ( ヒサゴ工房工房を利用利用したした場合
PrimerArray® Analysis Tool Ver.2.2
 研究用 PrimerArray Analysis Tool Ver.2.2 説明書 v201801 PrimerArray Analysis Tool Ver.2.2 は PrimerArray( 製品コード PH001 ~ PH007 PH009 ~ PH015 PN001 ~ PN015) で得られたデータを解析するためのツールで コントロールサンプルと 1 種類の未知サンプル間の比較が可能です
研究用 PrimerArray Analysis Tool Ver.2.2 説明書 v201801 PrimerArray Analysis Tool Ver.2.2 は PrimerArray( 製品コード PH001 ~ PH007 PH009 ~ PH015 PN001 ~ PN015) で得られたデータを解析するためのツールで コントロールサンプルと 1 種類の未知サンプル間の比較が可能です
目次 1. HLA Fusion 3.0 がインストール可能な環境 HLA Fusion 3.0 のインストール HLA Fusion 3.4 のインストール 初期設定用データベース接続 ( 初めての方のみ ) 既存データベースのUpg
 目次 1. HLA Fusion 3.0 がインストール可能な環境... 1 2. HLA Fusion 3.0 のインストール... 2 3. HLA Fusion 3.4 のインストール... 4 4. 初期設定用データベース接続 ( 初めての方のみ )... 5 5. 既存データベースのUpgrade 方法 (HLA Fusion 3~3.3 を既に使用の方 )... 7 6. インストールが成功したかの確認...
目次 1. HLA Fusion 3.0 がインストール可能な環境... 1 2. HLA Fusion 3.0 のインストール... 2 3. HLA Fusion 3.4 のインストール... 4 4. 初期設定用データベース接続 ( 初めての方のみ )... 5 5. 既存データベースのUpgrade 方法 (HLA Fusion 3~3.3 を既に使用の方 )... 7 6. インストールが成功したかの確認...
2017 年度一般入試前期 A 日程 ( 1 月 23 日実施 ) 化学問題 (63 ページ 74 ページ ) 問題は大問 Ⅰ Ⅳ までありますが 一部 他科目との共通問題となっています 大問 Ⅰ は 化学基礎 + 生物基礎 の大問 Ⅰ と共通の問題です 大問 Ⅱ は 化学基礎 + 生物基礎 の大問
 2017 年度一般入試前期 A 日程 ( 1 月 23 日実施 ) 化学問題 (63 ページ 74 ページ ) 問題は大問 Ⅰ Ⅳ までありますが 一部 他科目との共通問題となっています 大問 Ⅰ は 化学基礎 + 生物基礎 の大問 Ⅰ と共通の問題です 大問 Ⅱ は 化学基礎 + 生物基礎 の大問 Ⅱ と共通の問題です 63 必要があれば, 次の数値を使いなさい 原子量 H=1. 0,C=12,O=16,S=32
2017 年度一般入試前期 A 日程 ( 1 月 23 日実施 ) 化学問題 (63 ページ 74 ページ ) 問題は大問 Ⅰ Ⅳ までありますが 一部 他科目との共通問題となっています 大問 Ⅰ は 化学基礎 + 生物基礎 の大問 Ⅰ と共通の問題です 大問 Ⅱ は 化学基礎 + 生物基礎 の大問 Ⅱ と共通の問題です 63 必要があれば, 次の数値を使いなさい 原子量 H=1. 0,C=12,O=16,S=32
法政大学情報メディア教育研究センター研究報告 Vol 年 69 完全液体と完全固体の相転移計算法 Phase Transition in Perfect Liquid and Perfect Solid 片岡洋右山田祐
 法政大学情報メディア教育研究センター研究報告 Vol.6 年 69 http://hdl.handle.net/4/795 完全液体と完全固体の相転移計算法 Phase Transition in Perfect and Perfect 片岡洋右山田祐理 Yosuke Kataoka and Yuri Yamada 法政大学生命科学部環境応用化学科 Equations of state on perfect
法政大学情報メディア教育研究センター研究報告 Vol.6 年 69 http://hdl.handle.net/4/795 完全液体と完全固体の相転移計算法 Phase Transition in Perfect and Perfect 片岡洋右山田祐理 Yosuke Kataoka and Yuri Yamada 法政大学生命科学部環境応用化学科 Equations of state on perfect
電話機のファイル形式
 この章では テキスト エディタを使用して作成する CSV データ ファイルのファイル形式を設定 する方法について説明します 電話機 CSV データ ファイルを作成するためのテキスト エディタ, 1 ページ の検索, 2 ページ CSV データ ファイルの電話機ファイル形式の設定, 3 ページ テキストベースのファイル形式と CSV データ ファイルの関連付け, 7 ページ 電話機 CSV データ ファイルを作成するためのテキスト
この章では テキスト エディタを使用して作成する CSV データ ファイルのファイル形式を設定 する方法について説明します 電話機 CSV データ ファイルを作成するためのテキスト エディタ, 1 ページ の検索, 2 ページ CSV データ ファイルの電話機ファイル形式の設定, 3 ページ テキストベースのファイル形式と CSV データ ファイルの関連付け, 7 ページ 電話機 CSV データ ファイルを作成するためのテキスト
Winmostar - LAMMPS Tutorial 4 界面ビルダ V5.012 株式会社クロスアビリティ 2015/6/18
 Winmostar - LAMMPS Tutorial 界面ビルダ V5.012 株式会社クロスアビリティ question@winmostar.com 2015/6/18 界面ビルダ概要 界面ビルダ は分子動力学計算を行うための初期配置作成ツールの一つである 本チュートリアルではポリマーを題材としているが対象となる系は分子から成る液体や無機 / 金属結晶界面 固固界面 固液界面 液液界面などであってもよい
Winmostar - LAMMPS Tutorial 界面ビルダ V5.012 株式会社クロスアビリティ question@winmostar.com 2015/6/18 界面ビルダ概要 界面ビルダ は分子動力学計算を行うための初期配置作成ツールの一つである 本チュートリアルではポリマーを題材としているが対象となる系は分子から成る液体や無機 / 金属結晶界面 固固界面 固液界面 液液界面などであってもよい
ゲートウェイ ファイル形式
 ゲートウェイ ファイル形式 この章では Cisco Unified Communications Manager 一括管理 BAT を使用して Cisco Unified Communications Manager データベース内の Cisco ゲートウェイのファイル形式を一括して設定す る方法について説明します ゲートウェイ ファイル形式の検索, 1 ページ ゲートウェイ ファイル形式の設定,
ゲートウェイ ファイル形式 この章では Cisco Unified Communications Manager 一括管理 BAT を使用して Cisco Unified Communications Manager データベース内の Cisco ゲートウェイのファイル形式を一括して設定す る方法について説明します ゲートウェイ ファイル形式の検索, 1 ページ ゲートウェイ ファイル形式の設定,
木村の理論化学小ネタ 理想気体と実在気体 A. 標準状態における気体 1mol の体積 標準状態における気体 1mol の体積は気体の種類に関係なく 22.4L のはずである しかし, 実際には, その体積が 22.4L より明らかに小さい
 理想気体と実在気体 A. 標準状態における気体 1mol の体積 標準状態における気体 1mol の体積は気体の種類に関係なく.4L のはずである しかし, 実際には, その体積が.4L より明らかに小さい気体も存在する このような気体には, 気体分子に, 分子量が大きい, 極性が大きいなどの特徴がある そのため, 分子間力が大きく, 体積が.4L より小さくなる.4L とみなせる実在気体 H :.449
理想気体と実在気体 A. 標準状態における気体 1mol の体積 標準状態における気体 1mol の体積は気体の種類に関係なく.4L のはずである しかし, 実際には, その体積が.4L より明らかに小さい気体も存在する このような気体には, 気体分子に, 分子量が大きい, 極性が大きいなどの特徴がある そのため, 分子間力が大きく, 体積が.4L より小さくなる.4L とみなせる実在気体 H :.449
生存確認調査ツール
 Hos-CanR.0 独自項目運用マニュアル FileMaker pro を使用 登録作業者用 Ver. バージョン改訂日付改訂内容 Ver. 00//5 初版 Ver. 0// FileMaker Pro の動作確認の追加 はじめに 本マニュアルについて Hos-CanR.0 院内がん登録システム ( 以降は Hos-CanR.0 と記述します ) では 独自項目の作成 登録 サポートはなくなり
Hos-CanR.0 独自項目運用マニュアル FileMaker pro を使用 登録作業者用 Ver. バージョン改訂日付改訂内容 Ver. 00//5 初版 Ver. 0// FileMaker Pro の動作確認の追加 はじめに 本マニュアルについて Hos-CanR.0 院内がん登録システム ( 以降は Hos-CanR.0 と記述します ) では 独自項目の作成 登録 サポートはなくなり
データの作成方法のイメージ ( キーワードで結合の場合 ) 地図太郎 キーワードの値は文字列です キーワードの値は重複しないようにします 同じ値にする Excel データ (CSV) 注意キーワードの値は文字列です キーワードの値は重複しないようにします 1 ツールバーの 編集レイヤの選択 から 編
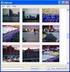 手順 4 Excel データを活用する ( リスト / グラフ 色分け ) 外部の表データ (CSV 形式 ) を読み込み リスト表示やカード表示 その値によって簡単なグラフ ( 円 正方形 棒の 3 種類 ) や色分け表示することができます この機能を使って地図太郎の属性情報に無い項目も Excel で作成し CSV 形式で保存することにより 自由に作成することができます (Excel でデータを保存するとき
手順 4 Excel データを活用する ( リスト / グラフ 色分け ) 外部の表データ (CSV 形式 ) を読み込み リスト表示やカード表示 その値によって簡単なグラフ ( 円 正方形 棒の 3 種類 ) や色分け表示することができます この機能を使って地図太郎の属性情報に無い項目も Excel で作成し CSV 形式で保存することにより 自由に作成することができます (Excel でデータを保存するとき
図 1 アドインに登録する メニューバーに [BAYONET] が追加されます 登録 : Excel 2007, 2010, 2013 の場合 1 Excel ブックを開きます Excel2007 の場合 左上の Office マークをクリックします 図 2 Office マーク (Excel 20
![図 1 アドインに登録する メニューバーに [BAYONET] が追加されます 登録 : Excel 2007, 2010, 2013 の場合 1 Excel ブックを開きます Excel2007 の場合 左上の Office マークをクリックします 図 2 Office マーク (Excel 20 図 1 アドインに登録する メニューバーに [BAYONET] が追加されます 登録 : Excel 2007, 2010, 2013 の場合 1 Excel ブックを開きます Excel2007 の場合 左上の Office マークをクリックします 図 2 Office マーク (Excel 20](/thumbs/92/109963601.jpg) BayoLink Excel アドイン使用方法 1. はじめに BayoLink Excel アドインは MS Office Excel のアドインツールです BayoLink Excel アドインは Excel から API を利用して BayoLink と通信し モデルのインポートや推論の実行を行います BayoLink 本体ではできない 複数のデータを一度に推論することができます なお現状ではソフトエビデンスを指定して推論を行うことはできません
BayoLink Excel アドイン使用方法 1. はじめに BayoLink Excel アドインは MS Office Excel のアドインツールです BayoLink Excel アドインは Excel から API を利用して BayoLink と通信し モデルのインポートや推論の実行を行います BayoLink 本体ではできない 複数のデータを一度に推論することができます なお現状ではソフトエビデンスを指定して推論を行うことはできません
Microsoft Word - ラベルマイティStep1.doc
 ラベルマイティ STEP 1 はじめに 1 レッスン 1 ラベルマイティでできること 3 1 ラベルマイティでできること 3 レッスン2 ラベルマイティの概要 4 1 ラベルマイティの起動 4 2 ガイドメニュー 7 3 画面構成 11 4 ラベルマイティの終了 14 第 1 章プリントアイテムを作ってみよう 1 レッスン1 テンプレートを選ぼう 3 1 のし紙 3 レッスン1のまとめ 4 レッスン2
ラベルマイティ STEP 1 はじめに 1 レッスン 1 ラベルマイティでできること 3 1 ラベルマイティでできること 3 レッスン2 ラベルマイティの概要 4 1 ラベルマイティの起動 4 2 ガイドメニュー 7 3 画面構成 11 4 ラベルマイティの終了 14 第 1 章プリントアイテムを作ってみよう 1 レッスン1 テンプレートを選ぼう 3 1 のし紙 3 レッスン1のまとめ 4 レッスン2
Microsoft PowerPoint - qchem3-11
 8 年度冬学期 量子化学 Ⅲ 章量子化学の応用.6. 溶液反応 9 年 1 月 6 日 担当 : 常田貴夫准教授 溶液中の反応 溶液反応の特徴は 反応する分子の周囲に常に溶媒分子が存在していること 反応過程が遅い 反応自体の化学的効果が重要 遷移状態理論の熱力学表示が適用できる反応過程が速い 反応物が相互に接近したり 生成物が離れていく拡散過程が律速 溶媒効果は拡散現象 溶液中の反応では 分子は周囲の溶媒分子のケージ内で衝突を繰り返す可能性が高い
8 年度冬学期 量子化学 Ⅲ 章量子化学の応用.6. 溶液反応 9 年 1 月 6 日 担当 : 常田貴夫准教授 溶液中の反応 溶液反応の特徴は 反応する分子の周囲に常に溶媒分子が存在していること 反応過程が遅い 反応自体の化学的効果が重要 遷移状態理論の熱力学表示が適用できる反応過程が速い 反応物が相互に接近したり 生成物が離れていく拡散過程が律速 溶媒効果は拡散現象 溶液中の反応では 分子は周囲の溶媒分子のケージ内で衝突を繰り返す可能性が高い
P 和佐田.indd
 Gaussian 03 Q Gaussian 03 [1,2] Q U S 1 2 k B 1.38054 10 23 JK 1 T 1 2 Q el Q trans Q rot Q vib 3 Q Q el Q trans Q rot Q vib 1 24 5 U E el E trans E rot E vib S S el S trans S rot S vib 6 3 4 5 6 R R 1.987
Gaussian 03 Q Gaussian 03 [1,2] Q U S 1 2 k B 1.38054 10 23 JK 1 T 1 2 Q el Q trans Q rot Q vib 3 Q Q el Q trans Q rot Q vib 1 24 5 U E el E trans E rot E vib S S el S trans S rot S vib 6 3 4 5 6 R R 1.987
PowerPoint プレゼンテーション
 薬品分析化学第 8 回 HendersonHasselbalch の式 ( 復習 ) ph 緩衝液 (p 55 ~) 溶液中に共役酸 塩基対が存在しているとき ph p 共役酸 塩基の濃度関係を表す 8 弱酸 HA の平衡式 O H O A において HA H A = mol/l, [A= mol/l とすると O [A より O A A [A となり ph p が導かれる 〇弱酸 HA ( mol/l)
薬品分析化学第 8 回 HendersonHasselbalch の式 ( 復習 ) ph 緩衝液 (p 55 ~) 溶液中に共役酸 塩基対が存在しているとき ph p 共役酸 塩基の濃度関係を表す 8 弱酸 HA の平衡式 O H O A において HA H A = mol/l, [A= mol/l とすると O [A より O A A [A となり ph p が導かれる 〇弱酸 HA ( mol/l)
CPT2L1Z1J154.indd
 要点学習化学変化と原子分子 1 1 30 分分解, 物質のしくみ CPT2L1-Z1J1-01 要点 要点を読んで重要なポイントを確認しましょう 分解 1 分解 物質そのものが 性質が異なる別の物質に変わる変化を() といいます 1 種類の物質が2 種類以上の別の物質に分かれる化学変化をといいます 加熱により起こる分解をとくにといい 電流を流すことにより起こる分解をとくに といいます 2 炭酸水素ナトリウムを熱分解する実験
要点学習化学変化と原子分子 1 1 30 分分解, 物質のしくみ CPT2L1-Z1J1-01 要点 要点を読んで重要なポイントを確認しましょう 分解 1 分解 物質そのものが 性質が異なる別の物質に変わる変化を() といいます 1 種類の物質が2 種類以上の別の物質に分かれる化学変化をといいます 加熱により起こる分解をとくにといい 電流を流すことにより起こる分解をとくに といいます 2 炭酸水素ナトリウムを熱分解する実験
平成20年度 神戸大学 大学院理学研究科 化学専攻 入学試験問題
 化学 Ⅰ- 表紙 平成 31 年度神戸大学大学院理学研究科化学専攻入学試験 化学 Ⅰ 試験時間 10:30-11:30(60 分 ) 表紙を除いて 7 ページあります 問題 [Ⅰ]~ 問題 [Ⅵ] の中から 4 題を選択して 解答しなさい 各ページ下端にある 選択する 選択しない のうち 該当する方を丸で囲みなさい 各ページに ( 用紙上端 ) と ( 用紙下端 ) を記入しなさい を誤って記入すると採点の対象とならないことがあります
化学 Ⅰ- 表紙 平成 31 年度神戸大学大学院理学研究科化学専攻入学試験 化学 Ⅰ 試験時間 10:30-11:30(60 分 ) 表紙を除いて 7 ページあります 問題 [Ⅰ]~ 問題 [Ⅵ] の中から 4 題を選択して 解答しなさい 各ページ下端にある 選択する 選択しない のうち 該当する方を丸で囲みなさい 各ページに ( 用紙上端 ) と ( 用紙下端 ) を記入しなさい を誤って記入すると採点の対象とならないことがあります
Taro-化学3 酸塩基 最新版
 11 酸 塩基の反応 P oint.29 酸 塩基 ブレンステッドの酸 塩基 酸 水素イオンを 物質 塩基 水素イオンを 物質 NH3 + H2O NH4 + + OH - 酸 塩基の性質 1 リトマス紙 2 フェノールフタレイン溶液 3BTB 液 4 メチルオレンジ 5 金属と反応 6 味 7 水溶液中に存在するイオン 酸 塩基 酸 塩基の分類 1 価数による分類 1 価 2 価 3 価 酸 塩基
11 酸 塩基の反応 P oint.29 酸 塩基 ブレンステッドの酸 塩基 酸 水素イオンを 物質 塩基 水素イオンを 物質 NH3 + H2O NH4 + + OH - 酸 塩基の性質 1 リトマス紙 2 フェノールフタレイン溶液 3BTB 液 4 メチルオレンジ 5 金属と反応 6 味 7 水溶液中に存在するイオン 酸 塩基 酸 塩基の分類 1 価数による分類 1 価 2 価 3 価 酸 塩基
3Dプリンタ用CADソフト Autodesk Meshmixer入門編[日本語版]
![3Dプリンタ用CADソフト Autodesk Meshmixer入門編[日本語版] 3Dプリンタ用CADソフト Autodesk Meshmixer入門編[日本語版]](/thumbs/101/150216105.jpg) ご購入はこちら. http://shop.cqpub.co.jp/hanbai 第 1 章操作メニュー ソフトウェアの立ち上げ時に表示されるトップ メニューと, 各メニューの役割について紹介します. ソフトウェアを使うにあたり, どこからスタートさせるのか確認しましょう. 最初に, 操作メニューから確認していきましょう. ソフトウェアを立ち上げると, 図 1-1 が現れます. この画面で, 大きく三つの操作メニュー
ご購入はこちら. http://shop.cqpub.co.jp/hanbai 第 1 章操作メニュー ソフトウェアの立ち上げ時に表示されるトップ メニューと, 各メニューの役割について紹介します. ソフトウェアを使うにあたり, どこからスタートさせるのか確認しましょう. 最初に, 操作メニューから確認していきましょう. ソフトウェアを立ち上げると, 図 1-1 が現れます. この画面で, 大きく三つの操作メニュー
<8B9E93738CF092CA904D94CC814090BF8B818F B D836A B B B816A2E786C73>
 京都交通信販 請求書 Web サービス操作マニュアル 第 9 版 (2011 年 2 月 1 日改訂 ) 京都交通信販株式会社 http://www.kyokoshin.co.jp TEL075-314-6251 FX075-314-6255 目次 STEP 1 >> ログイン画面 請求書 Web サービスログイン画面を確認します P.1 STEP 2 >> ログイン 請求書 Web サービスにログインします
京都交通信販 請求書 Web サービス操作マニュアル 第 9 版 (2011 年 2 月 1 日改訂 ) 京都交通信販株式会社 http://www.kyokoshin.co.jp TEL075-314-6251 FX075-314-6255 目次 STEP 1 >> ログイン画面 請求書 Web サービスログイン画面を確認します P.1 STEP 2 >> ログイン 請求書 Web サービスにログインします
Microsoft Word - basic_15.doc
 分析の原理 15 電位差測定装置の原理と応用 概要 電位差測定法は 溶液内の目的成分の濃度 ( 活量 ) を作用電極と参照電極の起電力差から測定し 溶液中のイオン濃度や酸化還元電位の測定に利用されています また 滴定と組み合わせて当量点の決定を電極電位変化より行う電位差滴定法もあり 電気化学測定法の一つとして古くから研究 応用されています 本編では 電位差測定装置の原理を解説し その応用装置である
分析の原理 15 電位差測定装置の原理と応用 概要 電位差測定法は 溶液内の目的成分の濃度 ( 活量 ) を作用電極と参照電極の起電力差から測定し 溶液中のイオン濃度や酸化還元電位の測定に利用されています また 滴定と組み合わせて当量点の決定を電極電位変化より行う電位差滴定法もあり 電気化学測定法の一つとして古くから研究 応用されています 本編では 電位差測定装置の原理を解説し その応用装置である
Microsoft Word - HOBO雨量専用説明書_v1.1.doc
 HOBOevent による雨量データの 回収と変換の方法 Rev 1.1 HOBO ペンダントシリーズ パルス入力 ベースステーション (USB) 雨量各種 HobowareLite 2007 年 9 月 http://www.weather.co.jp/ 目次 目次...1 はじめに...2 HOBOWARELITE の開始...2 ケーブル接続...2 HOBOwareLite の開始...2
HOBOevent による雨量データの 回収と変換の方法 Rev 1.1 HOBO ペンダントシリーズ パルス入力 ベースステーション (USB) 雨量各種 HobowareLite 2007 年 9 月 http://www.weather.co.jp/ 目次 目次...1 はじめに...2 HOBOWARELITE の開始...2 ケーブル接続...2 HOBOwareLite の開始...2
PowerPoint プレゼンテーション
 高圧ガス管理支援システム (IASO G3) について 2018 年 5 月 TOHOKU UNIVERSITY 目次 1. 高圧ガス管理システムの起動とログイン 2 2. 高圧ガス管理支援システムの概要及び管理の流れ 3 3. 高圧ガス管理支援システムのメイン画面 4 4. 高圧ガスボンベの登録 ( 購入 借用のボンベの登録 ) 5 5. 高圧ガスボンベの返却 ( 複数のボンベを一括返却する場合
高圧ガス管理支援システム (IASO G3) について 2018 年 5 月 TOHOKU UNIVERSITY 目次 1. 高圧ガス管理システムの起動とログイン 2 2. 高圧ガス管理支援システムの概要及び管理の流れ 3 3. 高圧ガス管理支援システムのメイン画面 4 4. 高圧ガスボンベの登録 ( 購入 借用のボンベの登録 ) 5 5. 高圧ガスボンベの返却 ( 複数のボンベを一括返却する場合
1 第 6 章演習問題解 第 6 章演習問題解答本文 146 ページ 問 1 以下の水の状態図に基づいて, 次の文章の空欄に適当な語句を入れよ. 解答 3 本の実線で区切られた 3 つの領域 I,II,III において安定な状態はそれぞれ 氷, 水, 水蒸気 であり, 曲線 ab 上では 氷 と水が
 第 6 章演習問題解 第 6 章演習問題本文 46 ページ 問 以下の水の状態図に基づいて, 次の文章の空欄に適当な語句を入れよ. 3 本の実線で区切られた 3 つの領域 I,II,III において安定な状態はそれぞれ 氷, 水, 水蒸気 であり, 曲線 ab 上では 氷 と水が共存し, 曲線 ac 上では水と 水蒸気 が共存する. 氷, 水, 水蒸気全てが共存できる領域は図の a であり, 三重点
第 6 章演習問題解 第 6 章演習問題本文 46 ページ 問 以下の水の状態図に基づいて, 次の文章の空欄に適当な語句を入れよ. 3 本の実線で区切られた 3 つの領域 I,II,III において安定な状態はそれぞれ 氷, 水, 水蒸気 であり, 曲線 ab 上では 氷 と水が共存し, 曲線 ac 上では水と 水蒸気 が共存する. 氷, 水, 水蒸気全てが共存できる領域は図の a であり, 三重点
1. 画面説明 ここでは普通にアプリケーションを開いた場合に表示される対話型画面の説明をしています パスワード ( 再入力 ) パスワード登録 パスワード消去 事前チェックの処理の際に必要になるパスワードを
 使い方ガイド 1. 画面説明... 2 2. 使用方法 ( 対話型画面編 )... 5 3. 使用方法 ( 右クリックメニュー編 )... 9 4. 使用方法 ( デスクトップショートカット編 )... 11 5. 注意事項... 13 1 1. 画面説明 ここでは普通にアプリケーションを開いた場合に表示される対話型画面の説明をしています 1 2 3 4 5 6 7 8 9 10 11 12 13
使い方ガイド 1. 画面説明... 2 2. 使用方法 ( 対話型画面編 )... 5 3. 使用方法 ( 右クリックメニュー編 )... 9 4. 使用方法 ( デスクトップショートカット編 )... 11 5. 注意事項... 13 1 1. 画面説明 ここでは普通にアプリケーションを開いた場合に表示される対話型画面の説明をしています 1 2 3 4 5 6 7 8 9 10 11 12 13
基本設計書
 Dahua アプリかんたん手順 (2) SmartPlayer 操作手順書 (1.00 版 ) 2017 年 09 月 05 日 三星ダイヤモンド工業株式会社 it 事業部 文書番号 :MDI-it-MAN-076 変更履歴 版数 変更日 区分 変更箇所頁項番 変更内容 1.00 2017/09/05 新規 新規作成 1 /13 目次 1. 本手順書について... 3 2. インストール / アンインストール...
Dahua アプリかんたん手順 (2) SmartPlayer 操作手順書 (1.00 版 ) 2017 年 09 月 05 日 三星ダイヤモンド工業株式会社 it 事業部 文書番号 :MDI-it-MAN-076 変更履歴 版数 変更日 区分 変更箇所頁項番 変更内容 1.00 2017/09/05 新規 新規作成 1 /13 目次 1. 本手順書について... 3 2. インストール / アンインストール...
ゲートウェイのファイル形式
 CHAPTER 47 Cisco Unified Communications Manager 一括管理 (BAT) を使用すると シスコのを Cisco Unified Communications Manager データベースに一括して設定できます 次のトピックでは これらのタスクの情報とについて説明します の検索 の設定 の検索 を検索するは 次のとおりです ステップ 1 [ 一括管理 ]>[
CHAPTER 47 Cisco Unified Communications Manager 一括管理 (BAT) を使用すると シスコのを Cisco Unified Communications Manager データベースに一括して設定できます 次のトピックでは これらのタスクの情報とについて説明します の検索 の設定 の検索 を検索するは 次のとおりです ステップ 1 [ 一括管理 ]>[
スライド 1
 ラベル屋さん HOME かんたんマニュアル リンクコース 目次 STEP 1-2 : ( 基礎編 ) 用紙の選択と文字の入力 STEP 3 : ( 基礎編 ) リンクの設定 STEP 4 : ( 基礎編 ) リンクデータの入力と印刷 STEP 5 : ( 応用編 ) リンクデータの入力 1 STEP 6 : ( 応用編 ) リンクデータの入力 2 STEP 7-8 : ( 応用編 ) リンク機能で使ったデータをコピーしたい場合
ラベル屋さん HOME かんたんマニュアル リンクコース 目次 STEP 1-2 : ( 基礎編 ) 用紙の選択と文字の入力 STEP 3 : ( 基礎編 ) リンクの設定 STEP 4 : ( 基礎編 ) リンクデータの入力と印刷 STEP 5 : ( 応用編 ) リンクデータの入力 1 STEP 6 : ( 応用編 ) リンクデータの入力 2 STEP 7-8 : ( 応用編 ) リンク機能で使ったデータをコピーしたい場合
数学 -1 以下の問に答えよ. ただし i = 1 である. 問 1 複素数 z = e iθ (0 θ 2π) のとき, 1 6cos θ+10 を z で表せ. 問 2 複素関数 f(z) = i 3z 2 +10z+3 を, 複素平面上の任意の単一閉曲線 C に沿って 積分せよ. 問 3 実積
 数学 -1 以下の問に答えよ. ただし i = 1 である. 問 1 複素数 z = e iθ (0 θ 2π) のとき, 1 6cos θ+10 を z で表せ. 問 2 複素関数 f(z) = i 3z 2 +10z+3 を, 複素平面上の任意の単一閉曲線 C に沿って 積分せよ. 問 3 実積分 0 2π dθ 6cos θ+10 を求めよ. 数学 -2 以下の問に答えよ. 問 1 xy 正規直交座標系上で全微分可能な関数
数学 -1 以下の問に答えよ. ただし i = 1 である. 問 1 複素数 z = e iθ (0 θ 2π) のとき, 1 6cos θ+10 を z で表せ. 問 2 複素関数 f(z) = i 3z 2 +10z+3 を, 複素平面上の任意の単一閉曲線 C に沿って 積分せよ. 問 3 実積分 0 2π dθ 6cos θ+10 を求めよ. 数学 -2 以下の問に答えよ. 問 1 xy 正規直交座標系上で全微分可能な関数
The world leader in serving science OMNIC ユーザーライブラリベーシックマニュアル サーモフィッシャーサイエンティフィック株式会社
 The world leader in serving science OMNIC ユーザーライブラリベーシックマニュアル サーモフィッシャーサイエンティフィック株式会社 目次 1. 概要 3 2. ユーザーライブラリ作成手順 4 3. スペクトルの追加 11 OMNIC User Library Basic Manual rev.1-1 - 1. 概要 このマニュアルは FT-IR( フーリエ変換赤外分光装置
The world leader in serving science OMNIC ユーザーライブラリベーシックマニュアル サーモフィッシャーサイエンティフィック株式会社 目次 1. 概要 3 2. ユーザーライブラリ作成手順 4 3. スペクトルの追加 11 OMNIC User Library Basic Manual rev.1-1 - 1. 概要 このマニュアルは FT-IR( フーリエ変換赤外分光装置
ゲートウェイのファイル形式
 この章では Cisco Unified Communications Manager 一括管理 BAT を使用して シスコのゲー トウェイのファイル形式を Cisco Unified Communications Manager データベースに一括して設定す る方法について説明します の検索, 1 ページ の設定, 2 ページ ファイル形式と CSV データ ファイルの関連付け, 5 ページ の検索
この章では Cisco Unified Communications Manager 一括管理 BAT を使用して シスコのゲー トウェイのファイル形式を Cisco Unified Communications Manager データベースに一括して設定す る方法について説明します の検索, 1 ページ の設定, 2 ページ ファイル形式と CSV データ ファイルの関連付け, 5 ページ の検索
1. 画面説明 ここでは普通にアプリケーションを開いた場合に表示される対話型画面の説明をしています パスワード ( 再入力 ) パスワード登録 パスワード消去 事前チェックの処理の際に必要になるパスワ
 使い方ガイド 1. 画面説明... 2 2. 使用方法 ( 対話型画面編 )... 5 3. 使用方法 ( 右クリックメニュー編 )... 10 4. 使用方法 ( フォルダ単位編 )... 12 5. 注意事項... 15 1 1. 画面説明 ここでは普通にアプリケーションを開いた場合に表示される対話型画面の説明をしています 1 2 3 4 5 6 7 8 9 10 11 14 12 13 15
使い方ガイド 1. 画面説明... 2 2. 使用方法 ( 対話型画面編 )... 5 3. 使用方法 ( 右クリックメニュー編 )... 10 4. 使用方法 ( フォルダ単位編 )... 12 5. 注意事項... 15 1 1. 画面説明 ここでは普通にアプリケーションを開いた場合に表示される対話型画面の説明をしています 1 2 3 4 5 6 7 8 9 10 11 14 12 13 15
ユーザ デバイス プロファイルの ファイル形式
 CHAPTER 34 CSV データファイルの作成にテキストエディタを使用する場合 デバイスフィールドと回線フィールドを CSV データファイル内で識別するファイル形式を使用する必要があります このファイル形式には次のオプションがあります Default User Device Profile: ユーザデバイスプロファイルのデバイスフィールドと回線フィールドの事前決定済みの組み合せを含む Simple
CHAPTER 34 CSV データファイルの作成にテキストエディタを使用する場合 デバイスフィールドと回線フィールドを CSV データファイル内で識別するファイル形式を使用する必要があります このファイル形式には次のオプションがあります Default User Device Profile: ユーザデバイスプロファイルのデバイスフィールドと回線フィールドの事前決定済みの組み合せを含む Simple
温泉の化学 1
 H O 1,003 516 149 124 2,237 1974 90 110 1km 2,400 ( 100 Mg 200 (98 ) 43,665 mg 38,695 mg 19,000 mg 2000 2000 Na-Ca-Cl 806 1970 1989 10 1991 4 ph 1 981 10,000 1993... (^^; (SO_4^{2-}) " " 1973-1987 1970
H O 1,003 516 149 124 2,237 1974 90 110 1km 2,400 ( 100 Mg 200 (98 ) 43,665 mg 38,695 mg 19,000 mg 2000 2000 Na-Ca-Cl 806 1970 1989 10 1991 4 ph 1 981 10,000 1993... (^^; (SO_4^{2-}) " " 1973-1987 1970
14551 フェノール ( チアゾール誘導体法 ) 測定範囲 : 0.10~2.50 mg/l C 6H 5OH 結果は mmol/l 単位でも表示できます 1. 試料の ph が ph 2~11 であるかチェックします 必要な場合 水酸化ナトリウム水溶液または硫酸を 1 滴ずつ加えて ph を調整
 14551 フェノール ( チアゾール誘導体法 ) 0.10~2.50 mg/l C 6H 5OH 結果は mmol/l 単位でも表示できます 2. ピペットで 10 ml の試料を反応セルに取り ねじぶたで閉じて攪拌します 3. グレーのミクロスプーンで 1 回分の試薬 Ph-1K を加えて ねじぶたでセルを閉じます 4. セルをよく振とうして 固体物を溶かします 5. 緑のミクロスプーンで 1
14551 フェノール ( チアゾール誘導体法 ) 0.10~2.50 mg/l C 6H 5OH 結果は mmol/l 単位でも表示できます 2. ピペットで 10 ml の試料を反応セルに取り ねじぶたで閉じて攪拌します 3. グレーのミクロスプーンで 1 回分の試薬 Ph-1K を加えて ねじぶたでセルを閉じます 4. セルをよく振とうして 固体物を溶かします 5. 緑のミクロスプーンで 1
Moodleアンケートの質問一括変換ツール
 Moodle アンケートの質問一括変換ツール Visual Basic 版 1 ツールの概要 1.1 ツールの配布と利用について 1 1.2 動作環境について 1 1.3 ツールの機能について 1 1.4 入力ファイルについて 2 1.5 ツールの起動 3 1.6 XML ファイルへの変換 4 1.7 XML ファイルからの逆変換 4 2 入力ファイルの書式 2.1 2 行モードと 1 行モード 6
Moodle アンケートの質問一括変換ツール Visual Basic 版 1 ツールの概要 1.1 ツールの配布と利用について 1 1.2 動作環境について 1 1.3 ツールの機能について 1 1.4 入力ファイルについて 2 1.5 ツールの起動 3 1.6 XML ファイルへの変換 4 1.7 XML ファイルからの逆変換 4 2 入力ファイルの書式 2.1 2 行モードと 1 行モード 6
e.Typist v.9.0 表原稿編
 操作マニュアル 表原稿編 e.typist エントリー基本操作 目次 1. はじめに 2. 認識範囲の設定 2-1. 自動で設定 2-2. 手動で設定 3. 認識 4. データ転送 ページ 2 3 3 3 4 5 作業例 1. 罫線 画像の表示 作業例 2. 罫線の入っていない表の認識 作業例 3. 少し複雑な表の認識 6 8 12 本マニュアルでは 表原稿の認識についての説明のみとなっています 本マニュアル以外の
操作マニュアル 表原稿編 e.typist エントリー基本操作 目次 1. はじめに 2. 認識範囲の設定 2-1. 自動で設定 2-2. 手動で設定 3. 認識 4. データ転送 ページ 2 3 3 3 4 5 作業例 1. 罫線 画像の表示 作業例 2. 罫線の入っていない表の認識 作業例 3. 少し複雑な表の認識 6 8 12 本マニュアルでは 表原稿の認識についての説明のみとなっています 本マニュアル以外の
2019 年度大学入試センター試験解説 化学 第 1 問問 1 a 塩化カリウムは, カリウムイオン K + と塩化物イオン Cl - のイオン結合のみを含む物質であり, 共有結合を含まない ( 答 ) 1 1 b 黒鉛の結晶中では, 各炭素原子の 4 つの価電子のうち 3 つが隣り合う他の原子との
 219 年度大学入試センター試験解説 化学 第 1 問問 1 a 塩化カリウムは, カリウムイオン K + と塩化物イオン Cl - のイオン結合のみを含む物質であり, 共有結合を含まない ( 答 ) 1 1 b 黒鉛の結晶中では, 各炭素原子の 4 つの価電子のうち 3 つが隣り合う他の原子との共有結合に使われ, 残りの 1 つは結晶を構成する層上を自由に移動している そのため, 黒鉛は固体の状態で電気をよく通す
219 年度大学入試センター試験解説 化学 第 1 問問 1 a 塩化カリウムは, カリウムイオン K + と塩化物イオン Cl - のイオン結合のみを含む物質であり, 共有結合を含まない ( 答 ) 1 1 b 黒鉛の結晶中では, 各炭素原子の 4 つの価電子のうち 3 つが隣り合う他の原子との共有結合に使われ, 残りの 1 つは結晶を構成する層上を自由に移動している そのため, 黒鉛は固体の状態で電気をよく通す
untitled
 NPO 2006( ) 11 14 ( ) (2006/12/3) 1 50% % - - (CO+H2) ( ) 6 44 1) --- 2) ( CO H2 ) 2 3 3 90 3 3 2 3 2004 ( ) 1 1 4 1 20% 5 ( ) ( ) 2 6 MAWERA ) MAWERA ( ) ( ) 7 6MW -- 175kW 8 ( ) 900 10 2 2 2 9 -- - 10
NPO 2006( ) 11 14 ( ) (2006/12/3) 1 50% % - - (CO+H2) ( ) 6 44 1) --- 2) ( CO H2 ) 2 3 3 90 3 3 2 3 2004 ( ) 1 1 4 1 20% 5 ( ) ( ) 2 6 MAWERA ) MAWERA ( ) ( ) 7 6MW -- 175kW 8 ( ) 900 10 2 2 2 9 -- - 10
i ( 23 ) ) SPP Science Partnership Project ( (1) (2) 2010 SSH
 i 1982 2012 ( 23 ) 30 1998 ) 2002 2006 2009 1999 2009 10 2004 SPP Science Partnership Project 2004 2005 2009 ( 29 2010 (1) (2) 2010 SSH ii ph 21 2006 10 B5 A5 2014 2 2014 2 iii 21 1962 1969 1987 1992 2005
i 1982 2012 ( 23 ) 30 1998 ) 2002 2006 2009 1999 2009 10 2004 SPP Science Partnership Project 2004 2005 2009 ( 29 2010 (1) (2) 2010 SSH ii ph 21 2006 10 B5 A5 2014 2 2014 2 iii 21 1962 1969 1987 1992 2005
Microsoft Word _Chap_4_Text_1.DOC
 第 4 章ポテンシャルダイヤグラム 東京大学岡部徹関西大学大石敏雄 4.1 はじめに 金属の製錬をはじめとして 材料の溶解 乾式精製 熱間加工といった高温工程では材料は必ず空気 SO 2 H 2 O CO などのガスと接触している 真空といえども我々が現場で作り出せる程度の真空度では濃度に違いはあってもこのことに変わりはない これらの雰囲気ガスは我々が必要に応じて導入するものと 材料自体が発生するものとがあるが
第 4 章ポテンシャルダイヤグラム 東京大学岡部徹関西大学大石敏雄 4.1 はじめに 金属の製錬をはじめとして 材料の溶解 乾式精製 熱間加工といった高温工程では材料は必ず空気 SO 2 H 2 O CO などのガスと接触している 真空といえども我々が現場で作り出せる程度の真空度では濃度に違いはあってもこのことに変わりはない これらの雰囲気ガスは我々が必要に応じて導入するものと 材料自体が発生するものとがあるが
PRONETA
 PRONETA 操作概要 PROFINET IO デバイスの無償診断ツール シーメンス株式会社デジタルファクトリー事業本部ファクトリーオートメーション部 2015 年 12 月 22 日 目次 ここで紹介している操作は PRONETA バージョン 2.2 を基にしています PRONETA 概要 3 動作環境と起動方法 4 ホーム画面 5 ネットワーク解析画面 6 IOチェック画面 9 設定画面 13
PRONETA 操作概要 PROFINET IO デバイスの無償診断ツール シーメンス株式会社デジタルファクトリー事業本部ファクトリーオートメーション部 2015 年 12 月 22 日 目次 ここで紹介している操作は PRONETA バージョン 2.2 を基にしています PRONETA 概要 3 動作環境と起動方法 4 ホーム画面 5 ネットワーク解析画面 6 IOチェック画面 9 設定画面 13
写真の閲覧方法 1. 閲覧する納品データの種類の選択 ( 写真 ) P3 写真の閲覧写真の閲覧写真の閲覧 2. 写真を一覧から選択 表示 3. 写真をサムネイル一覧から選択 表示 4. 写真をアルバム形式で表示 P5~ P7~ P9~ 5. 写真の便利な表示方法 拡大 / 縮小 回転 明るさ補正 6
 新潟県 CALS システム 電子検査システム 簡易検査ビューワ ( 工事用 ) 操作マニュアル別冊 ~ 写真の閲覧 ~ 平成 25 年 7 月 1 写真の閲覧方法 1. 閲覧する納品データの種類の選択 ( 写真 ) P3 写真の閲覧写真の閲覧写真の閲覧 2. 写真を一覧から選択 表示 3. 写真をサムネイル一覧から選択 表示 4. 写真をアルバム形式で表示 P5~ P7~ P9~ 5. 写真の便利な表示方法
新潟県 CALS システム 電子検査システム 簡易検査ビューワ ( 工事用 ) 操作マニュアル別冊 ~ 写真の閲覧 ~ 平成 25 年 7 月 1 写真の閲覧方法 1. 閲覧する納品データの種類の選択 ( 写真 ) P3 写真の閲覧写真の閲覧写真の閲覧 2. 写真を一覧から選択 表示 3. 写真をサムネイル一覧から選択 表示 4. 写真をアルバム形式で表示 P5~ P7~ P9~ 5. 写真の便利な表示方法
Microsoft PowerPoint - kougi2.ppt
 C プログラミング演習 第 2 回 Microsoft Visual Studio.NET を使ってみよう 説明 例題 1. プログラム実行の体験 コンピュータを役に立つ道具として実感する 次ページのプログラムを使って, Microsoft Visual Studio.NETでの C++ ソースファイル編集, ビルド, テスト実行の一連の過程を体験する 例題 1 のプログラムの機能 計算の繰り返し
C プログラミング演習 第 2 回 Microsoft Visual Studio.NET を使ってみよう 説明 例題 1. プログラム実行の体験 コンピュータを役に立つ道具として実感する 次ページのプログラムを使って, Microsoft Visual Studio.NETでの C++ ソースファイル編集, ビルド, テスト実行の一連の過程を体験する 例題 1 のプログラムの機能 計算の繰り返し
 1 1....4 2....4 3....4 4....5 5....13 6....14 2 Ver 0.0 1.0 2.0 RoHS JGP 3 1. URL 2. 3. 4 4. 5 6 7 8 9 10 11 12 5. 13 6. 14 15 LODE JGP JGP DUNS 21 DUNS 22 g kg kg = g 23 入力例 4 化学物質含有の有無を入力して下さい 別紙 1 調査対象化学物質リスト
1 1....4 2....4 3....4 4....5 5....13 6....14 2 Ver 0.0 1.0 2.0 RoHS JGP 3 1. URL 2. 3. 4 4. 5 6 7 8 9 10 11 12 5. 13 6. 14 15 LODE JGP JGP DUNS 21 DUNS 22 g kg kg = g 23 入力例 4 化学物質含有の有無を入力して下さい 別紙 1 調査対象化学物質リスト
