定整理番号 内 -1 薬効分類 117 精神神経用剤 ( 内用薬 ) 成分名ブレクスピプラゾール新薬収載希望者大塚製薬 ( 株 ) 新医薬品の薬価算定について 販売名 ( 規格単位 ) レキサルティ錠 1mg(1mg1 錠 ) レキサルティ錠 2mg(2mg1 錠 ) 効能 効果統合失
|
|
|
- としみ むらかわ
- 5 years ago
- Views:
Transcription
1 新医薬品一覧表 ( 平成 30 年 4 月 18 日収載予定 ) 中医協総 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等薬効分類ページ 1 レキサルティ錠 1mg レキサルティ錠 2mg 1mg1 錠 2mg1 錠 大塚製薬 ブレクスピプラゾール 新有効成分含有医薬品 円類似薬効比較方式 (Ⅰ) 円 精神神経用剤 ( 統合失調症用薬 ) 内 アトーゼット配合錠 LD アトーゼット配合錠 HD 1 錠 1 錠 MSD エゼチミブ / アトルバスタチンカルシウム水和物 新医療用配合剤 円新医療用配合剤の特例 円 内 218 高脂血症用剤 ( 高コレステロール血症 家族性高コレステロール血症用薬 ) 4 3 ネキシウム懸濁用顆粒分包 10mg ネキシウム懸濁用顆粒分包 20mg 10mg1 包 20mg1 包 アストラゼネカ エソメプラゾールマグネシウム水和物 新用量 新剤形医薬品 円類似薬効比較方式 (Ⅰ) 小児加算 (A=5%) 円 内 232 消化性潰瘍用剤 ( 胃潰瘍 十二指腸潰瘍等用薬 ) 6 4 グーフィス錠 5mg 5mg1 錠 EA ファーマエロビキシバット水和物新有効成分含有医薬品 円類似薬効比較方式 (Ⅰ) 下痢 浣腸剤 ( 慢性便秘症 ( 器質的疾患によ内 235 る便秘を除く ) 用薬 ) 8 5 リムパーザ錠 100mg リムパーザ錠 150mg 100mg1 錠 150mg1 錠 アストラゼネカ オラパリブ 新有効成分含有医薬品 3, 円原価計算方式 5, 円 有用性加算 (Ⅱ)(A=5%) その他の腫瘍用薬 ( 白金系抗悪性腫瘍剤感 加算係数 0.2 内 429 受性の再発卵巣癌における維持療法用薬 ) 10 6 シダキュアスギ花粉舌下錠 2,000JAU シダキュアスギ花粉舌下錠 5,000JAU 2,000JAU1 錠 5,000JAU1 錠 鳥居薬品スギ花粉エキス原末新有効成分含有医薬品 円類似薬効比較方式 (Ⅰ) 有用性加算 (Ⅱ)(A=5%) 円小児加算 (A=5%) 内 449 その他のアレルギー用薬 ( スギ花粉症 ( 減感作療法 ) 用薬 ) 12 7 サチュロ錠 100mg 100mg1 錠ヤンセンファーマベダキリンフマル酸塩新有効成分含有医薬品 21, 円類似薬効比較方式 (Ⅰ) 8 イブリーフ静注 20mg 20mg2mL1 瓶千寿製薬イブプロフェン L- リシン新有効成分含有医薬品 13,012 円原価計算方式 抗結核剤 ( 多剤耐性肺結核用薬 ) 内 622 注 219 その他の循環器官用薬 ( 未熟児動脈管開存症で保存療法 ( 水分制限 利尿剤投与等 ) が無効の場合用薬 ) ファセンラ皮下注 30mgシリンジ 30mg1mL1 筒 アストラゼネカ ベンラリズマブ ( 遺伝子組 換え ) 10 ベスポンサ点滴静注用 1mg 1mg1 瓶 ファイザー イノツズマブオゾガマイシ ン ( 遺伝子組換え ) 新有効成分含有医薬品 351,535 円類似薬効比較方式 (Ⅰ) 新有効成分含有医薬品 1,307,092 円原価計算方式 有用性加算 (Ⅱ)(A=10%) 市場性加算 (Ⅰ)(A=10%) 加算係数 0.2 注 423 その他の呼吸器官用薬 ( 気管支喘息 ( 既存注 229 治療によっても喘息症状をコントロールできない難治の患者に限る ) 用薬 ) 抗腫瘍性抗生物質製剤 ( 再発又は難治性の CD22 陽性の急性リンパ性白血病用薬 ) イストダックス点滴静注用 10mg 10mg1 瓶 ( 溶解液付 ) セルジーンロミデプシン新有効成分含有医薬品 109,753 円類似薬効比較方式 (Ⅰ) 注 429 その他の腫瘍用薬 ( 再発又は難治性の末梢性 T 細胞リンパ腫用薬 ) テセントリク点滴静注 1200mg 1,200mg20mL1 瓶 中外製薬 アテゾリズマブ ( 遺伝子組 換え ) 新有効成分含有医薬品 625,567 円類似薬効比較方式 (Ⅰ) その他の腫瘍用薬 ( 切除不能な進行 再発注 429 の非小細胞肺癌用薬 ) デュピクセント皮下注 300mgシリンジ 300mg2mL1 筒 サノフィ デュピルマブ ( 遺伝子組換 え ) 新有効成分含有医薬品 81,640 円原価計算方式有用性加算 (Ⅰ)(A=45%) その他のアレルギー用薬 ( 既存治療で効果加算係数 0.2 注 449 不十分なアトピー性皮膚炎用薬 ) ナルベイン注 2mg ナルベイン注 20mg 2mg1mL1 管 20mg2mL1 管 第一三共プロファーマ ヒドロモルフォン塩酸塩 新投与経路医薬品 725 円類似薬効比較方式 (Ⅰ) 6,340 円 あへんアルカロイド系麻薬 ( 中等度から高度注 811 の疼痛を伴う各種癌における鎮痛用薬 ) アレサガテープ 4mg アレサガテープ 8mg 4mg1 枚 8mg1 枚 久光製薬 エメダスチンフマル酸塩 新投与経路医薬品 円類似薬効比較方式 (Ⅰ) 円 その他のアレルギー用薬 ( アレルギー性鼻外 449 炎用薬 ) 30 品目数 成分数 内用薬 12 7 注射薬 8 7 外用薬 2 1 計
2 定整理番号 内 -1 薬効分類 117 精神神経用剤 ( 内用薬 ) 成分名ブレクスピプラゾール新薬収載希望者大塚製薬 ( 株 ) 新医薬品の薬価算定について 販売名 ( 規格単位 ) レキサルティ錠 1mg(1mg1 錠 ) レキサルティ錠 2mg(2mg1 錠 ) 効能 効果統合失調症 主な用法 用量 通常 成人にはブレクスピプラゾールとして 1 日 1 回 1mg から投与を開始した 後 4 日以上の間隔をあけて増量し 1 日 1 回 2mg を経口投与する 算算定方式類似薬効比較方式 (Ⅰ) 成分名 : アリピプラゾール会社名 : 大塚製薬 ( 株 ) 比較薬 販売名 ( 規格単位 ) 薬価 (1 日薬価 ) エビリファイ錠 6mg 円 (6mg1 錠 ) ( 円 ) 規格間比エビリファイ錠 6mg とエビリファイ錠 12mg の規格間比 : 補正加算 外国平均価格調整 算定薬価 1mg1 錠 円 2mg1 錠 円 (1 日薬価 : 円 ) 外国価格 1mg 1 錠米国 (NADAC)32.27 ト ル 3, 円 2mg 1 錠米国 (NADAC)32.29 ト ル 3, 円 予測年度 新薬収載希望者による市場規模予測 予測本剤投与患者数予測販売金額 ( ピーク時 ) 10 年度 12 万人 128 億円 ( 参考 ) 1mg 1 錠米国 (AWP)40.38 ト ル 4, 円 2mg 1 錠米国 (AWP)40.38 ト ル 4, 円 ( 注 1) 為替レートは平成 29 年 2 月 ~ 平成 30 年 1 月の平均 ( 注 2) 米国 (AWP) は従来参照していた RED BOOK の価格 最初に承認された国 ( 年月 ): 米国 (2015 年 7 月 ) 製造販売承認日平成 30 年 1 月 19 日 薬価基準収載予定日平成 30 年 4 月 18 日 2
3 算定方式類似薬効比較方式 (Ⅰ) 第一回算定組織平成 30 年 3 月 15 日最類似薬選定の妥当性薬価算定組織における検討結果のまとめ 新薬 最類似薬 成分名ブレクスピプラゾールアリピプラゾール イ. 効能 効果 ロ. 薬理作用 ハ. 組成及び化学構造 統合失調症 ドパミン D2 受容体部分アゴニスト作用 統合失調症 双極性障害における躁症状の改善 うつ病 うつ状態 ( 既存治療で十分な効果が認められない場合に限る ) 小児期の自閉スペクトラム症に伴う易刺激性 左に同じ ニ. 投与形態剤形用法 内用錠剤 1 日 1 回 左に同じ左に同じ 1 日 1 回又は 2 回補正加算画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 有用性加算 (Ⅱ) (5~30%) 市場性加算 (Ⅰ) 市場性加算 (Ⅱ) (5%) 小児加算 (5~20%) 先駆け審査指定制度加算 当初算定案に対する新薬収載希望者の不服意見の要点 第二回算定組織 平成年月日 上記不服意見に対する見解 3
4 新医薬品の薬価算定について 整理番号 内 -2 薬効分類 218 高脂血症用剤 ( 内用薬 ) 成分名エゼチミブ / アトルバスタチンカルシウム水和物新薬収載希望者 MSD( 株 ) 販売名 ( 規格単位 ) アトーゼット配合錠 LD(1 錠 ) (1 錠中 エゼチミブ / アトルバスタチンとして 10mg/10mg を含有 ) アトーゼット配合錠 HD(1 錠 ) (1 錠中 エゼチミブ / アトルバスタチンとして 10mg/20mg を含有 ) 効能 効果高コレステロール血症 家族性高コレステロール血症 主な用法 用量通常 成人には 1 日 1 回 1 錠を食後に経口投与する 新医療用配合剤の特例 算 定 算定方式 比較薬 自社品の薬価の 0.8 倍 + 他社の後発品の最低薬価 により算定 (1 のみ自社品がある ) したところ エゼチミブ 10mg 錠単剤 ( ゼチーア錠 10mg) の薬価を下回ったため 本剤の薬価はゼチーア錠 10mg の薬価と同額とした 成分名 :1エゼチミブ 2アトルバスタチンカルシウム水和物 会社名 :1MSD( 株 ) 2 日医工 ( 株 ) 他 2 社 販売名 ( 規格単位 ) 薬価 (1 日薬価 ) 1ゼチーア錠 10mg 円 (10mg1 錠 ) ( 円 ) 2アトルバスタチン錠 10mg 日医工 他 2 品目 円 (10mg1 錠 ) (24.40 円 ) 補正加算 外国平均価格調整 算定薬価アトーゼット配合錠 LD 1 錠 円 (1 日薬価 円 ) アトーゼット配合錠 HD 1 錠 円 ( 参考 : アトーゼット配合錠 LD に対応する先発医薬品単剤 2 剤 ( ゼチーア錠 10 mg リピトール錠 10mg) の合計 1 日薬価 円 ) 外国価格 LD 1 錠 HD 1 錠独国 ユーロ 円仏国 ユーロ 円外国平均価格 円 新薬収載希望者による市場規模予測 予測年度予測本剤投与患者数予測販売金額 ( ピーク時 ) 3 年度 64 万人 277 億円 ( 注 1) 為替レートは平成 29 年 2 月 ~ 平成 30 年 1 月の平均 ( 注 2) 米国 (AWP) は従来参照していた RED BOOK の価格 最初に承認された国 ( 年月 ): 米国 (2013 年 5 月 ) 製造販売承認日平成 29 年 9 月 27 日薬価基準収載予定日平成 30 年 4 月 18 日 4
5 薬価算定組織における検討結果のまとめ 算定方式新医療用配合剤の特例第一回算定組織平成 30 年 3 月 15 日 最類似薬選定の妥当性 成分名 イ. 効能 効果 ロ. 薬理作用 ハ. 組成及び化学構造 新薬エゼチミブ / アトルバスタチンカルシウム水和物 高コレステロール血症 家族性高コレステロール血症 コレステロール吸収抑制作用 / コレステロール生合成阻害作用エゼチミブ アトルバスタチン 最類似薬 1エゼチミブ 2アトルバスタチンカルシウム水和物 1 高コレステロール血症 家族性高コレステロール血症 ホモ接合体性シトステロール血症 2 左に同じ 1コレステロール吸収抑制作用 2コレステロール生合成阻害作用 1エゼチミブ 2アトルバスタチン ニ. 投与形態剤形用法 内用錠剤 1 日 1 回 1 左に同じ左に同じ 2 左に同じ左に同じ 左に同じ左に同じ画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 補有用性加算 (Ⅱ) 正(5~30%) 市場性加算 (Ⅰ) 加 算市場性加算 (Ⅱ) (5%) 小児加算 (5~20%) 先駆け審査指定制度加算 当初算定案に対する新薬収載希望者の不服意見の要点 上記不服意見に対する見解 第二回算定組織 平成年月日 5
6 整理番号 内 -3 新医薬品の薬価算定について 薬効分類 232 消化性潰瘍用剤 ( 内用薬 ) 成分名 エソメプラゾールマグネシム水和物 新薬収載希望者アストラゼネカ ( 株 ) 販売名 ( 規格単位 ) 効能 効果 ネキシウム懸濁用顆粒分包 10mg(10mg1 包 ) ネキシウム懸濁用顆粒分包 20mg(20mg1 包 ) 胃潰瘍 十二指腸潰瘍 吻合部潰瘍 逆流性食道炎 非びらん性胃食道逆流症 ( 本剤 10mg 包のみ ) Zollinger-Ellison 症候群 非ステロイド性抗炎症薬投与時における胃潰瘍又は十二指腸潰瘍の再発抑制 低用量アスピリン投与時における胃潰瘍又は十二指腸潰瘍の再発抑制下記におけるヘリコバクター ピロリの除菌の補助胃潰瘍 十二指腸潰瘍 胃 MALT リンパ腫 特発性血小板減少性紫斑病 早期胃癌に対する内視鏡的治療後胃 ヘリコバクター ピロリ感染胃炎 主な用法 用量 < ヘリコバクター ピロリの除菌の補助以外 > 成人 :1 回 20mg を用時水で懸濁して 1 日 1 回経口投与 ( 非びらん性胃食道逆流症は 1 回 1 0mg) 小児 :1 歳以上の幼児及び小児には 体重 20kg 未満では 1 回 10mg 体重 20kg 以上では症状に応じて 1 回 10~20mg を用時水で懸濁して 1 日 1 回経口投与 ( 非びらん性胃食道逆流症は 1 回 10mg) < ヘリコバクター ピロリの除菌の補助 > 成人には 1 回 20mg を用時水で懸濁して アモキシシリン水和物として 1 回 750mg( 力価 ) 及びクラリスロマイシンとして 1 回 200mg( 力価 ) の 3 剤を同時に 1 日 2 回 7 日間経 口投与 算定方式類似薬効比較方式 (Ⅰ) 成分名 : エソメプラゾールマグネシム水和物会社名 : アストラゼネカ ( 株 ) 比較薬算販売名 ( 規格単位 ) 薬価 (1 日薬価 ) ネキシウムカプセル 20mg 円 (20mg1カプセル) ( 円 ) 剤形間比セルセプトカプセル 250mgと同内用懸濁散 31.8% の剤形間比 : 定規格間比ネキシウムカプセル 20mgと同カプセル 10mgの規格間比 : 補正加算 外国平均価格調整 小児加算 (A=5%) ( 加算前 ) ( 加算後 ) 20mg1 包 円 円 算定薬価 10mg1 包 円 20mg1 包 円 (1 日薬価 : 円 ) 外国価格 新薬収載希望者による市場規模予測 10mg1 包 米国 (NADAC)( ドル 円 ) 英国 ポンド 円 独国 ユーロ 円 仏国 ユーロ 円 外国平均価格 円 20mg1 包 米国 (NADAC) ドル 円 外国平均価格 円 ( 参考 ) 米国 (AWP) 10mg1 包 20mg1 包 ドル 1, 円 製造販売承認日平成 30 年 1 月 19 日 予測年度 予測本剤投与患者 予測販売金額 ( ピーク時 ) 7 年度 8.6 万人 11 億円 ( 注 1) 為替レートは平成 29 年 2 月 ~ 平成 30 年 1 月の平均 ( 注 2) 外国の価格に大きな開きがあるので 調整した外国平均価格を用いている ( は最低価格の 2.5 倍を上回るため対象から除いた ) ( 注 3) 米国 (AWP) は従来参照していた RED BOOK の価格 最初に承認された国 ( 年月 ): 米国 (2006 年 10 月 ) 薬価基準収載予定日平成 30 年 4 月 18 日 6
7 算定方式類似薬効比較方式 (Ⅰ) 第一回算定組織平成 30 年 3 月 15 日最類似薬選定の妥当性薬価算定組織における検討結果のまとめ 新薬 最類似薬 成分名エソメプラゾールマグネシウム水和物左に同じ イ. 効能 効果 胃潰瘍 十二指腸潰瘍 吻合部潰瘍 左に同じ逆流性食道炎 非びらん性胃食道逆流症 (10mg 規格のみ ) Zolli nger-ellison 症候群 非ステロイド性抗炎症薬投与時における胃潰瘍又は十二指腸潰瘍の再発抑制 低用量アスピリン投与時における胃潰瘍又は十二指腸潰瘍の再発抑制下記におけるヘリコバクター ピロリの除菌の補助胃潰瘍 十二指腸潰瘍 胃 MALT リンパ腫 特発性血小板減少性紫斑病 早期胃癌に対する内視鏡的治療後胃 ヘリコバクター ピロリ感染胃炎 ロ. 薬理作用 ハ. 組成及び化学構造 胃酸分泌抑制作用 / プロトンポンプ阻害作用 左に同じ 左に同じ ニ. 投与形態剤形用法 画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 有用性加算 (Ⅱ) (5~30%) 市場性加算 (Ⅰ) 市場性加算 (Ⅱ) (5%) 小児加算 (5~20%) 先駆け審査指定制度加算 内用顆粒剤 1 日 1~2 回 該当する (A=5(%)) 左に同じカプセル剤左に同じ補正加算本剤は 小児に係る用法 用量が含まれていること 比較薬は小児加算を受けていないことから 加算の要件に該当する 加算率については 国内小児試験における症例数が限られていること等から 5% が妥当であると判断した 当初算定案に対する新薬収載希望者の不服意見の要点 上記不服意見に対する見解 第二回算定組織 平成年月日 7
8 整理番号 内 -4 新医薬品の薬価算定について 薬効分類 235 下痢 浣腸剤 ( 内用薬 ) 成分名エロビキシバット水和物 新薬収載希望者 EA ファーマ ( 株 ) 販売名 ( 規格単位 ) グーフィス錠 5mg(5mg1 錠 ) 効能 効果慢性便秘症 ( 器質的疾患による便秘を除く ) 主な用法 用量 通常 成人にはエロビキシバットとして 10mg を 1 日 1 回食前に経口投与する 算定方式類似薬効比較方式 (Ⅰ) なお 症状により適宜増減するが 最高用量は1 日 15mgとする 算比較薬定成分名 : ルビプロストン会社名 : マイラン EPD 合同会社 販売名 ( 規格単位 ) 薬価 (1 日薬価 ) アミティーザカプセル24μg 円 (24μg1カプセル) ( 円 ) 比較薬の 1 日薬価は 実使用量の平均値 ( 安全性定期報告書より ) を基に算出している 補正加算 外国平均価格調整 算定薬価 5mg1 錠 円 (1 日薬価 : 円 ) 算定に当たっては 本剤の国内長期投与試験での平均投与量に基づく 1 日薬価を合わせた 外国価格 新薬収載希望者による市場規模予測 予測年度予測本剤投与患者数予測販売金額 最初に承認された国 : 日本 ( ピーク時 ) 9 年度 63 万人 120 億円 製造販売承認日平成 30 年 1 月 19 日 薬価基準収載予定日平成 30 年 4 月 18 日 8
9 算定方式類似薬効比較方式 (Ⅰ) 第一回算定組織平成 30 年 3 月 15 日最類似薬選定の妥当性薬価算定組織における検討結果のまとめ 新薬 最類似薬 成分名エロビキシバット水和物ルビプロストン イ. 効能 効果 慢性便秘症 ( 器質的疾患による便秘を除く ) 左に同じ ロ. 薬理作用胆汁酸再吸収抑制作用腸液分泌促進作用 ハ. 組成及び化学構造 ニ. 投与形態剤形用法 内用錠剤 1 日 1 回 適宜増減 画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 有用性加算 (Ⅱ) (5~30%) 市場性加算 (Ⅰ) 市場性加算 (Ⅱ) (5%) 小児加算 (5~20%) 先駆け審査指定制度加算 左に同じカプセル剤 1 日 2 回 適宜減量補正加算当初算定案に対する新薬収載希望者の不服意見の要点 上記不服意見に対する見解 第二回算定組織 平成年月日 9
10 整理番号 内 -5 新医薬品の薬価算定について 薬効分類 429 その他の腫瘍用薬 ( 内用薬 ) 成分名 オラパリブ 新薬収載希望者アストラゼネカ ( 株 ) 販売名 ( 規格単位 ) 効能 効果 主な用法 用量状態により適宜減量する 算定方式原価計算方式原価算計算定リムパーザ錠 100mg(100mg1 錠 ) リムパーザ錠 150mg(150mg1 錠 ) 白金系抗悪性腫瘍剤感受性の再発卵巣癌における維持療法 通常 成人にはオラパリブとして 300mg を 1 日 2 回 経口投与する なお 患者の 製品総原価 2, 円 4, 円 営業利益 流通経費 円 ( 流通経費を除く価格の 14.7%) 円 ( 消費税を除く価格の 7.3%) 出典 : 医薬品産業実態調査報告書 ( 厚生労働省医政局経済課 ) 円 ( 流通経費を除く価格の 14.7%) 円 ( 消費税を除く価格の 7.3%) 出典 : 医薬品産業実態調査報告書 ( 厚生労働省医政局経済課 ) 100mg1 錠 150mg1 錠 消費税 円 円 補正加算 外国平均価格調整 算定薬価 有用性加算 (Ⅱ)(A=5%) 加算係数 =0.2 ( 加算前 ) ( 加算後 ) 100mg1 錠 3, 円 3, 円 150mg1 錠 5, 円 5, 円 100mg1 錠 3, 円 150mg1 錠 5, 円 外国価格 ( 参考 ) 100mg 1 錠米国 (AWP) ト ル 15, 円 150mg 1 錠米国 (AWP) ト ル 15, 円 予測年度 新薬収載希望者による市場規模予測 予測本剤投与患者数予測販売金額 ( ピーク時 ) 9 年度 1.2 千人 69 億円 ( 注 1) 為替レートは平成 29 年 2 月 ~ 平成 30 年 1 月の平均 ( 注 2) 米国 (AWP) は従来参照していた RED BOOK の価格 最初に承認された国 ( 年月 ): 米国 (2017 年 8 月 ) 製造販売承認日平成 30 年 1 月 19 日薬価基準収載予定日平成 30 年 4 月 18 日 10
11 算定方式原価計算方式第一回算定組織平成 30 年 3 月 15 日原価計算方式を採用する妥当性正加算薬価算定組織における検討結果のまとめ 新薬 類似薬がない根拠 成分名オラパリブ既存の化学療法剤又は分子標的治療薬とは 臨床的位置付けや薬イ. 効能 効果白金系抗悪性腫瘍剤感受性の再発卵巣癌にお理作用が異なるなど 総合的に ける維持療法類似の効能 効果 薬理作用等をロ. 薬理作用 PARP( ポリ (ADP-リボース) ポリメラーゼ ) 持つ新薬算定最類似薬はないと判阻害作用断した ハ. 組成及び化学構造 ニ. 投与形態剤形用法 画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 内用錠剤 1 日 2 回補有用性加算 (Ⅱ) (5~30%) 市場性加算 (Ⅰ) 市場性加算 (Ⅱ) (5%) 小児加算 (5~20%) 先駆け審査指定制度加算 該当する (A=5%) [ イ. 臨床上有用な新規作用機序 :1-b=1p] 本剤は DNA 修復に関わる PARP( ポリ (ADP- リボース ) ポリメラーゼ ) を阻害することにより DNA 損傷を蓄積させ 細胞死が誘導されることで腫瘍増殖抑制作用を示すと考えられている新規作用機序医薬品である 白金系抗悪性腫瘍剤感受性の再発卵巣癌患者に対する維持療法として単独投与した臨床試験において 無増悪生存期間の統計学的に有意な延長が認められ 承認審査において臨床的意義があると評価されていることから 有用性加算 (Ⅱ)(A=5%) とすることが適当と判断した 当初算定案に対する新薬収載希望者の不服意見の要点 上記不服意見に対する見解 第二回算定組織 平成年月日 11
12 整理番号 内 -6 新医薬品の薬価算定について 薬効分類 449 その他のアレルギー用剤 ( 内用薬 ) 成分名 スギ花粉エキス 新薬収載希望者鳥居薬品 ( 株 ) 販売名 ( 規格単位 ) シダキュアスギ花粉舌下錠 2,000JAU(2,000JAU1 錠 ) シダキュアスギ花粉舌下錠 5,000JAU(5,000JAU1 錠 ) 効能 効果スギ花粉症 ( 減感作療法 ) 主な用法 用量 通常 投与開始後 1 週間は シダキュアスギ花粉舌下錠 2,000JAU を 1 日 1 回 1 錠 投与 2 週目以降は シダキュアスギ花粉舌下錠 5,000JAU を 1 日 1 回 1 錠 舌下にて 1 分間保持した後 飲み込む その後 5 分間は うがいや飲食を 算定方式類似薬効比較方式 (Ⅰ) 控える 比較薬算定成分名 : 標準化スギ花粉エキス会社名 : 鳥居薬品 ( 株 ) 販売名 ( 規格単位 ) 薬価 (1 日薬価 ) シダトレンスギ花粉舌下液 2,000JAU/mLパック 円 (1mL1 包 ) ( 円 ) 規格間比シダトレンスギ花粉舌下液 2,000JAU/mL パック ( 汎用 ) とシダトレンスギ花粉舌下液 2,000JAU/mL ボトル ( 準汎用 ) の規格間比 : 補正加算 有用性加算 (Ⅱ)(A=5%) 小児加算(A=5%) ( 加算前 ) ( 加算後 ) 5,000JAU1 錠 円 円 外国平均価格調整 算定薬価 2,000JAU1 錠 円 5,000JAU1 錠 円 (1 日薬価 : 円 ) 外国価格 最初に承認された国 : 日本 新薬収載希望者による市場規模予測 予測年度予測本剤投与患者予測販売金額 ( ピーク時 ) 3 年度 3.8 万人 16 億円 製造販売承認日平成 29 年 9 月 27 日 薬価基準収載予定日平成 30 年 4 月 18 日 12
13 算定方式類似薬効比較方式 (Ⅰ) 第一回算定組織平成 30 年 3 月 15 日最類似薬選定の妥当性薬価算定組織における検討結果のまとめ 新薬 成分名スギ花粉エキス左に同じ イ. 効能 効果スギ花粉症 ( 減感作療法 ) 左に同じ ロ. 薬理作用特異的減感作作用左に同じ ハ. 組成及び化学構造 ニ. 投与形態剤形用法 画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 有用性加算 (Ⅱ) (5~30%) 市場性加算 (Ⅰ) 市場性加算 (Ⅱ) (5%) 小児加算 (5~20%) 先駆け審査指定制度加算 スギの花粉を原料とし 抽出して得たスギアレルゲン 内用舌下錠 1 日 1 回 左に同じ 左に同じ舌下液左に同じ補正加算該当する (A=5(%)) [ 高い有効性等 : 内容 ( 高い有効性 ):2-1 a(1p) 示し方 ( その他 ):2-2 b(1p)= 1 1=1p] 最類似薬 本剤は 既に承認されているシダトレン舌下液より高力価での減感作療法を可能とすること等を目的として開発され 5 歳以上のスギ花粉症患者を対象とした国内第 Ⅱ/Ⅲ 相臨床試験等の結果 本剤 5,000JAU の有効性は シダトレン舌下液 2,000JAU と比較してより高い傾向が認められていることを踏まえ 有用性加算 (Ⅱ)(A=5%) を適用することが妥当と判断した 該当する (A=5(%)) 本剤は 5 歳以上の小児を対象に国内で臨床試験が実施され 小児に係る用法 用量が含まれていること 比較薬は小児加算を受けていないことから加算の要件に該当する 加算率については 日本人小児患者における本剤の安全性及び有効性のデータが限られていること等から 5% が妥当であると判断した 当初算定案に対する新薬収載希望者の不服意見の要点 上記不服意見に対する見解 第二回算定組織 平成年月日 13
14 整理番号 内 -7 薬効分類 622 抗結核剤 ( 内用薬 ) 成分名ベダキリンフマル酸塩新薬収載希望者ヤンセンファーマ ( 株 ) 新医薬品の薬価算定について 販売名 ( 規格単位 ) 効能 効果 主な用法 用量 サチュロ錠 100mg(100mg1 錠 ) < 適応菌種 > 本剤に感性の結核菌 < 適応症 > 多剤耐性肺結核 通常 成人には投与開始から 2 週間は 1 日 1 回 400mg を食直後に経口投与する その後 3 週以降は 1 回 200mg を週 3 回 48 時間以上の間隔をあけて 算定方式類似薬効比較方式 (Ⅰ) 食直後に経口投与する 投与に際しては 必ず他の抗結核薬と併用する 算比較薬定成分名 : デラマニド会社名 : 大塚製薬 ( 株 ) 販売名 ( 規格単位 ) 薬価 (1 日薬価 ) デルティバ錠 50mg 6, 円 (50mg1 錠 ) (24, 円 ) 補正加算 外国平均価格調整 算定薬価 100mg1 錠 21, 円 (1 日薬価 :24, 円 ) 外国価格 100mg1 錠英国 99.47ポンド 14, 円独国 ユーロ 22, 円外国平均価格 18, 円 新薬収載希望者による市場規模予測 予測年度予測本剤投与患者数予測販売金額 ( ピーク時 ) 10 年度 22 人 9.0 千万円 ( 参考 ) 米国 (AWP) ドル 21, 円 ( 注 1) 為替レートは平成 29 年 2 月 ~ 平成 30 年 1 月の平均 ( 注 2) 米国 (AWP) は従来参照していた RED BOOK の価格 最初に承認された国 ( 年月 ): 米国 (2012 年 12 月 ) 製造販売承認日平成 30 年 1 月 19 日 薬価基準収載予定日平成 30 年 4 月 18 日 14
15 算定方式類似薬効比較方式 (Ⅰ) 第一回算定組織平成 30 年 3 月 15 日最類似薬選定の妥当性薬価算定組織における検討結果のまとめ 新薬 最類似薬 成分名ベダキリンフマル酸塩デラマニド イ. 効能 効果 ロ. 薬理作用 ハ. 組成及び化学構造 < 適応菌種 > 本剤に感性の結核菌 < 適応症 > 多剤耐性肺結核 アデノシン 5 - 三リン酸 (AT P) 合成酵素阻害作用 左に同じ ミコール酸合成阻害作用 ニ. 投与形態剤形用法 内用錠剤開始 2 週間は 1 日 1 回 3 週以降は週 3 回 画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 有用性加算 (Ⅱ) (5~30%) 市場性加算 (Ⅰ) 市場性加算 (Ⅱ) (5%) 小児加算 (5~20%) 先駆け審査指定制度加算 左に同じ左に同じ 1 日 2 回補正加算当初算定案に対する新薬収載希望者の不服意見の要点 上記不服意見に対する見解 第二回算定組織 平成年月日 15
16 整理番号 注 -1 新医薬品の薬価算定について 薬効分類 219 その他の循環器官用薬 ( 注射薬 ) 成分名 イブプロフェン L- リシン 新薬収載希望者千寿製薬 ( 株 ) 販売名 ( 規格単位 ) 効能 効果 主な用法 用量 イブリーフ静注 20mg(20mg2mL1 瓶 ) 注 ) 医療上の必要性の高い未承認薬 適応外薬検討会議の評価に基づく開発公募品目 下記疾患で保存療法 ( 水分制限 利尿剤投与等 ) が無効の場合未熟児動脈管開存症 通常 3 回 イブプロフェンとして初回は 10mg/kg 2 回目及び 3 回目は 5mg/ kgを15 分以上かけて24 時間間隔で静脈内投与する 算定方式原価計算方式原価算計算定製品総原価 営業利益 流通経費 9,526 円 1,642 円 ( 流通経費を除く価格の 14.7%) 880 円 ( 消費税を除く価格の 7.3%) 出典 : 医薬品産業実態調査報告書 ( 厚生労働省医政局経済課 ) 消費税 964 円 補正加算 外国平均価格調整 算定薬価 20mg2mL1 瓶 13,012 円 外国価格 参考 20mg2mL1 瓶米国 (AWP) ドル 82,082 円 予測年度 新薬収載希望者による市場規模予測 予測本剤投与患者数予測販売金額 ( ピーク時 ) 5 年度 1.2 千人 4.7 千万円 ( 注 1) 為替レートは平成 29 年 2 月 ~ 平成 30 年 1 月の平均 ( 注 2) 米国 (AWP) は従来参照していた RED BOOK の価格 最初に承認された国 ( 年月 ): 米国 (2006 年 4 月 ) 製造販売承認日平成 30 年 1 月 19 日薬価基準収載予定日平成 30 年 4 月 18 日 16
17 算定方式原価計算方式第一回算定組織平成 30 年 3 月 15 日原価計算方式を採用する妥当性補正加算薬価算定組織における検討結果のまとめ 新薬 類似薬がない根拠 成分名 イブプロフェン L-リシン 類似の効能 効果を有するイン ドメタシンナトリウム ( インダシイ. 効能 効果下記疾患で保存療法 ( 水分制限 利尿剤投与ン静注用 ) は 薬価収載後 10 年等 ) が無効の場合以上 ( 平成 6 年 12 月収載 ) であ未熟児動脈管開存症ること等から 総合的に類似の効 ロ. 薬理作用 動脈管閉鎖作用 能 効果 薬理作用をもつ新薬算 定最類似薬はないと判断した ハ. 組成及び化学構造 ニ. 投与形態剤形用法 画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 有用性加算 (Ⅱ) (5~30%) 市場性加算 (Ⅰ) 市場性加算 (Ⅱ) (5%) 小児加算 (5~20%) 先駆け審査指定制度加算 注射注射剤静脈内投与 当初算定案に対する新薬収載希望者の不服意見の要点 第二回算定組織 平成年月日 上記不服意見に対する見解 17
18 新医薬品の薬価算定について 整理番号 注 -2 薬効分類 229 その他の呼吸器官用薬 ( 注射薬 ) 成分名ベンラリズマブ ( 遺伝子組換え ) 新薬収載希望者アストラゼネカ ( 株 ) 販売名 ( 規格単位 ) 効能 効果 ファセンラ皮下注 30mg シリンジ (30mg1mL1 筒 ) 気管支喘息 ( 既存治療によっても喘息症状をコントロールできない難治の患者に限る ) 主な用法 用量 通常 成人にはベンラリズマブ ( 遺伝子組換え ) として 1 回 30mg を 初回 4 週後 8 週後に皮下に注射し 以降 8 週間隔で皮下に注射する 算定算定方式類似薬効比較方式 (Ⅰ) 成分名 : メポリズマブ ( 遺伝子組換え ) 会社名 : グラクソ スミスクライン ( 株 ) 比較薬 販売名 ( 規格単位 ) 薬価 (1 日薬価 ) ヌーカラ皮下注用 100mg 175,684 円 (100mg1 瓶 ) (6,274 円 ) 補正加算 キット特徴部分の原材料費 外国平均価格調整 30mg1mL1 筒 351,368 円 351,535 円 算定薬価 30mg1mL1 筒 351,535 円 (1 日薬価 :6,277 円 ) 外国価格 ( 参考 ) 米国 (AWP)5, ト ル 638,683 円 ( 注 1) 為替レートは平成 29 年 2 月 ~ 平成 30 年 1 月の平均 ( 注 2) 米国 (AWP) は従来参照していた RED BOOK の価格 予測年度 新薬収載希望者による市場規模予測 予測本剤投与患者数予測販売金額 ( ピーク時 ) 9 年度 7.9 千人 153 億円 最初に承認された国 ( 年月 ): 米国 (2017 年 11 月 ) 製造販売承認日平成 30 年 1 月 19 日薬価基準収載予定日平成 30 年 4 月 18 日 18
19 算定方式類似薬効比較方式 (Ⅰ) 第一回算定組織平成 30 年 3 月 15 日最類似薬選定の妥当性薬価算定組織における検討結果のまとめ 新薬 最類似薬 成分名ベンラリズマブ ( 遺伝子組換え ) メポリズマブ ( 遺伝子組換え ) イ. 効能 効果 気管支喘息 ( 既存治療によっても喘息症状をコントロールできない難治の患者に限る ) 左に同じ ロ. 薬理作用抗 IL-5 受容体作用抗 IL-5 作用 ハ. 組成及び化学構造 451 個のアミノ酸残基からなる H 鎖 (γ1 鎖 )2 本及び 214 個のアミノ酸残基からなる L 鎖 (κ 鎖 )2 本で構成される糖タンパク質であり ヒト IL-5 受容体 α に対する遺伝子組換えヒト化モノクローナル抗体 ( 分子量 : 約 148,000) 449 個のアミノ酸残基からなる H 鎖 (γ1 鎖 )2 本及び 220 個のアミノ酸残基からなる L 鎖 (κ 鎖 )2 本で構成される糖タンパク質であり ヒト IL-5 に対する遺伝子組換えヒト化モノクローナル抗体 ( 分子量 : 約 149,000) ニ. 投与形態剤形用法 注射注射剤 ( キット製品 ) 8 週に 1 回 皮下投与 左に同じ注射剤 4 週に 1 回 皮下投与補正加算画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 有用性加算 (Ⅱ) (5~30%) 市場性加算 (Ⅰ) 市場性加算 (Ⅱ) (5%) 小児加算 (5~20%) 先駆け審査指定制度加算 当初算定案に対する新薬収載希望者の不服意見の要点 第二回算定組織 平成年月日 上記不服意見に対する見解 19
20 整理番号 注 -3 新医薬品の薬価算定について 薬効分類 423 抗腫瘍性抗生物質製剤 ( 注射薬 ) 成分名イノツズマブオゾガマイシン ( 遺伝子組換え ) 新薬収載希望者ファイザー ( 株 ) 販売名 ( 規格単位 ) 効能 効果 主な用法 用量 ベスポンサ点滴静注用 1mg(1mg1 瓶 ) 再発又は難治性の CD22 陽性の急性リンパ性白血病 通常 成人にはイノツズマブオゾガマイシン ( 遺伝子組換え ) として 1 日目は 0.8m g/m 2 ( 体表面積 ) 8 及び 15 日目は 0.5mg/m 2 ( 体表面積 ) を 1 日 1 回 1 時間以上かけて点滴静脈内投与した後 休薬する 1 サイクル目は 21~28 日間 2サイクル目以降は28 日間を1サイクルとし 投与を繰り返す 算定方式原価計算方式原価算計算定製品総原価 営業利益 流通経費 消費税 補正加算 外国平均価格調整 920,190 円 158,579 円 ( 流通経費を除く価格の 14.7%) 84,952 円 ( 消費税を除く価格の 7.3%) 出典 : 医薬品産業実態調査報告書 ( 厚生労働省医政局経済課 ) 93,098 円 有用性加算 (Ⅱ)(A=10%) 市場性加算 (Ⅰ)(A=10%) 加算係数 =0.2 1mg1 瓶 ( 加算前 ) ( 加算後 ) 1,256,819 円 1,307,092 円 算定薬価 1mg1 瓶 1,307,092 円 外国価格 1mg1 瓶英国 8, ポンド 1,158,912 円独国 16, ユーロ 2,083,027 円外国平均価格 1,620,969 円 ( 参考 ) 米国 (AWP)22, ト ル 2,513,280 円 ( 注 1) 為替レートは平成 29 年 2 月 ~ 平成 30 年 1 月の平均 ( 注 2) 米国 (AWP) は従来参照していた RED BOOK の価格 予測年度 新薬収載希望者による市場規模予測 予測本剤投与患者数予測販売金額 ( ピーク時 ) 3 年度 263 人 24 億円 最初に承認された国 ( 年月 ): 欧州 (2017 年 6 月 ) 製造販売承認日平成 30 年 1 月 19 日薬価基準収載予定日平成 30 年 4 月 18 日 20
21 算定方式原価計算方式第一回算定組織平成 30 年 3 月 15 日原価計算方式を採用する妥当性補正加算薬価算定組織における検討結果のまとめ 成分名 イ. 効能 効果 ロ. 薬理作用 ハ. 組成及び化学構造 ニ. 投与形態剤形用法 画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 新薬 イノツズマブオゾガマイシン ( 遺伝子組換え ) 再発又は難治性の CD22 陽性の急性リンパ性白血病 二本鎖 DNA 切断作用 (CD22 に選択的に結合 ) 抗生物質結合ヒト化抗 CD22 モノクローナル抗体 注射注射剤週 1 回 3 回投与後休薬 (21~28 日サイクル ) 類似薬がない根拠 類似の薬理作用 化学構造等を有する既収載品がなく 新薬算定最類似薬はないと判断した 有用性加算 (Ⅱ) (5~30%) 市場性加算 (Ⅰ) 市場性加算 (Ⅱ) (5%) 小児加算 (5~20%) 先駆け審査指定制度加算 該当する (A=10%) [ イ. 新規作用機序 ( 異なる標的分子 重篤疾患 ):1-b=1p 1-c=1p] 本剤は 抗腫瘍性抗生物質と抗 CD22 抗体の複合体であり CD22 抗原を介して細胞内に取り込まれ DNA 二本鎖を切断するという新規作用機序を有する 再発又は難治性の CD22 陽性の急性リンパ性白血病患者を対象とした国際共同第 Ⅲ 相試験において 主要評価項目である血液学的完全寛解率について 既存化学療法に対する本剤の優越性が検証されていること等から 有用性加算 (Ⅱ)(A=10%) が妥当と考える 該当する (A=10%) 本剤は希少疾病用医薬品として指定を受けていることから 加算の要件に該当する ただし 作用機序は異なるが 類似の効能 効果を有する化学療法剤が既に薬価収載されていること等から 限定的な評価とした 当初算定案に対する新薬収載希望者の不服意見の要点 上記不服意見に対する見解 第二回算定組織 平成年月日 21
22 新医薬品の薬価算定について 整理番号 注 -4 薬効分類 429 その他の腫瘍用薬 ( 注射薬 ) 成分名ロミデプシン新薬収載希望者セルジーン ( 株 ) 販売名 ( 規格単位 ) イストダックス点滴静注用 10mg(10mg1 瓶 ( 溶解液付 )) 効能 効果再発又は難治性の末梢性 T 細胞リンパ腫 主な用法 用量 通常 成人にはロミデプシンとして 14mg/m 2 ( 体表面積 ) を 日目に 4 時間かけて点滴静注した後 休薬 (16~28 日目 ) する この 28 日間を 算定方式類似薬効比較方式 (Ⅰ) 1サイクルとして投与を繰り返す なお 患者の状態により適宜減量する 算比較薬定成分名 : プララトレキサート会社名 : ムンディファーマ ( 株 ) 販売名 ( 規格単位 ) 薬価 (1 日薬価 ) ジフォルタ注射液 20mg 89,632 円 (20mg1mL1 瓶 ) (24,695 円 ) 補正加算 外国平均価格調整 算定薬価 10mg1 瓶 109,753 円 (1 日薬価 :24,694 円 ) 外国価格 10mg1 瓶米国 (ASP) 3, ドル 368,292 円外国平均価格 368,292 円 ( 参考 ) 米国 (AWP) 3, ドル 429,899 円 新薬収載希望者による市場規模予測 予測年度予測本剤投与患者数予測販売金額 ( ピーク時 ) 10 年度 466 人 7.9 億円 ( 注 1) 為替レートは平成 29 年 2 月 ~ 平成 30 年 1 月の平均 ( 注 2) 米国 (AWP) は従来参照していた RED BOOK の価格 最初に承認された国 ( 年月 ): 米国 (2009 年 11 月 ) 製造販売承認日平成 29 年 7 月 3 日 薬価基準収載予定日平成 30 年 4 月 18 日 22
23 算定方式類似薬効比較方式 (Ⅰ) 第一回算定組織平成 30 年 3 月 15 日最類似薬選定の妥当性薬価算定組織における検討結果のまとめ 新薬 最類似薬 成分名ロミデプシンプララトレキサート イ. 効能 効果 ロ. 薬理作用 ハ. 組成及び化学構造 再発又は難治性の末梢性 T 細胞リンパ腫 ヒストン脱アセチル化酵素 (HDA C) 阻害作用 左に同じ ジヒドロ葉酸還元酵素阻害作用 ニ. 投与形態剤形用法 画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 有用性加算 (Ⅱ) (5~30%) 市場性加算 (Ⅰ) 市場性加算 (Ⅱ) (5%) 小児加算 (5~20%) 先駆け審査指定制度加算 注射注射剤週 1 回 3 週間投与後 1 週間休薬 注射注射剤週 1 回 6 週間投与後 1 週間休薬補正加算当初算定案に対する新薬収載希望者の不服意見の要点 上記不服意見に対する見解 第二回算定組織 23
24 整理番号 注 -5 新医薬品の薬価算定について 薬効分類 429 その他の腫瘍用薬 ( 注射薬 ) 成分名アテゾリズマブ ( 遺伝子組換え ) 新薬収載希望者中外製薬 ( 株 ) 販売名 ( 規格単位 ) 効能 効果 テセントリク点滴静注 1200mg(1,200mg20mL1 瓶 ) 切除不能な進行 再発の非小細胞肺癌 主な用法 用量 通常 成人にはアテゾリズマブ ( 遺伝子組換え ) として 1 回 1200mg を 60 分 算定方式類似薬効比較方式 (Ⅰ) かけて3 週間間隔で点滴静注する 算比較薬定成分名 : ニボルマブ ( 遺伝子組換え ) 会社名 : 小野薬品工業 ( 株 ) 販売名 ( 規格単位 ) 薬価 (1 日薬価 ) オプジーボ点滴静注 100mg 278,029 円 (100mg10mL1 瓶 ) (29,789 円 ) 補正加算 外国平均価格調整 算定薬価 1,200mg20mL1 瓶 625,567 円 (1 日薬価 :29,789 円 ) 外国価格 1,200mg20mL1 瓶米国 (ASP)9,095.04ドル 1,018,644 円英国 3,807.69ポンド 548,307 円独国 6,350.52ユーロ 800,166 円外国平均価格 789,039 円 ( 参考 ) 1,200mg20mL1 瓶米国 (AWP)10,344.00ドル 1,158,528 円 新薬収載希望者による市場規模予測 予測年度 予測本剤投与患者予測販売金額 ( ピーク時 ) 8 年度 6.3 千人 285 億円 ( 注 1) 為替レートは平成 29 年 2 月 ~ 平成 30 年 1 月の平均 ( 注 2) 米国 (AWP) は従来参照していた RED BOOK の価格 最初に承認された国 ( 年月 ): 米国 (2016 年 5 月 ) 製造販売承認日平成 30 年 1 月 19 日 薬価基準収載予定日平成 30 年 4 月 18 日 24
25 算定方式類似薬効比較方式 (Ⅰ) 第一回算定組織平成 30 年 3 月 15 日最類似薬選定の妥当性薬価算定組織における検討結果のまとめ 新薬 最類似薬 成分名アテゾリズマブ ( 遺伝子組換え ) ニボルマブ ( 遺伝子組換え ) イ. 効能 効果 ロ. 薬理作用 ハ. 組成及び化学構造 ニ. 投与形態剤形用法 画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 有用性加算 (Ⅱ) (5~30%) 市場性加算 (Ⅰ) 市場性加算 (Ⅱ) (5%) 切除不能な進行 再発の非小細胞肺癌 PD-1/PD-1 リガンド結合阻害作用 ヒト PD-L1 に対する遺伝子組換えヒト化 IgG 1 モノクローナル抗体 ( アミノ酸 214 個の L 鎖 2 本とアミノ酸 448 個の H 鎖 2 本からなるタンパク質 ) 分子量 :145,000 注射注射剤 3 週間間隔 根治切除不能な悪性黒色腫切除不能な進行 再発の非小細胞肺癌根治切除不能又は転移性の腎細胞癌再発又は難治性の古典的ホジキンリンパ腫再発又は遠隔転移を有する頭頸部癌がん化学療法後に増悪した治癒切除不能な進行 再発の胃癌 左に同じ ヒト PD-1 に対する遺伝子組換えヒト IgG 4 モノクローナル抗体 (440 個のアミノ酸残基からなる重鎖 2 本及び 214 個のアミノ酸残基からなる軽鎖 2 本で構成される糖タンパク質 ) 分子量 : 約 145,000 左に同じ左に同じ 2 週間間隔補正加算小児加算 (5~20%) 先駆け審査指定制度加算 当初算定案に対する新薬収載希望者の不服意見の要点 上記不服意見に対する見解 第二回算定組織 平成年月日 25
26 整理番号 注 -6 新医薬品の薬価算定について 薬効分類 449 その他のアレルギー用薬 ( 注射薬 ) 成分名デュピルマブ ( 遺伝子組換え ) 新薬収載希望者サノフィ ( 株 ) 販売名 ( 規格単位 ) 効能 効果 主な用法 用量 デュピクセント皮下注 300mg シリンジ (300mg2mL1 筒 ) 既存治療で効果不十分なアトピー性皮膚炎 通常 成人には初回に 600mg を皮下投与し その後は 1 回 300mg を 2 週間隔で 皮下投与する 算定方式原価計算方式原価算計算定製品総原価 営業利益 流通経費 消費税 補正加算 外国平均価格調整 54,838 円 9,450 円 ( 流通経費を除く価格の 14.7%) 5,063 円 ( 消費税を除く価格の 7.3%) 出典 : 医薬品産業実態調査報告書 ( 厚生労働省医政局経済課 ) 5,548 円 有用性加算 (Ⅰ)(A=45%) 加算係数 = mg2mL1 筒 ( 加算前 ) ( 加算後 ) 74,899 円 81,640 円 算定薬価 300mg2mL1 筒 81,640 円 外国価格 300mg2mL1 筒英国 ポンド 91,072 円独国 ユーロ 112,312 円外国平均価格 101,692 円 ( 参考 ) 米国 (AWP)1, ドル 191,262 円 予測年度 新薬収載希望者による市場規模予測 予測本剤投与患者数予測販売金額 ( ピーク時 ) 10 年度 2.0 万人 329 億円 ( 注 1) 為替レートは平成 29 年 2 月 ~ 平成 30 年 1 月の平均 ( 注 2) 米国 (AWP) は従来参照していた RED BOOK の価格 最初に承認された国 ( 年月 ): 米国 (2017 年 3 月 ) 製造販売承認日平成 30 年 1 月 19 日薬価基準収載予定日平成 30 年 4 月 18 日 26
27 算定方式原価計算方式第一回算定組織平成 30 年 3 月 15 日原価計算方式を採用する妥当性補正加算薬価算定組織における検討結果のまとめ 新薬 類似薬がない根拠 成分名 デュピルマブ ( 遺伝子組換え ) 類似の薬理作用 組成 化学構 イ. 効能 効果 既存治療で効果不十分なアトピー性皮膚炎 造等を有する既収載品はない ロ. 薬理作用 ハ. 組成及び化学構造 ニ. 投与形態剤形用法 IL-4/IL-13 シグナル伝達阻害作用 インターロイキン -4 受容体の α サブユニットに対するヒト型モノクローナル抗体で 452 個のアミノ酸残基からなる H 鎖 2 本及び 21 9 個のアミノ酸残基からなる L 鎖 2 本で構成される糖タンパク質 ( 分子量 : 約 152,00 0) 注射注射剤皮下投与 画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 有用性加算 (Ⅱ) (5~30%) 市場性加算 (Ⅰ) 市場性加算 (Ⅱ) (5%) 小児加算 (5~20%) 先駆け審査指定制度加算 該当する (A=45%) イ. 新規作用機序 ( 大きく異なる作用点 ):1-a=2p ハ. 治療方法の改善 ( 不十分例での効果 ) ( 効果の増強 ):3-a,d=2p 合計 :5p( 有用性加算 (I))+2p+2p=9p 本剤は アトピー性皮膚炎の病態において重要な役割を担う IL-4 及び I L-13 のシグナル伝達を阻害する臨床上有用な新規の作用機序を有すると認められる 既存の外用薬が使用できなかった中等症から重症のアトピー性皮膚炎患者又は既存の外用薬で効果不十分な中等症から重症のアトピー性皮膚炎患者の皮膚病変の有意な改善が示されていること等から 治療方法の改善が客観的に示されていると認められる 以上を踏まえ 有用性加算 (Ⅰ)A=45% が妥当と判断した 当初算定案に対する新薬収載希望者の不服意見の要点 上記不服意見に対する見解 第二回算定組織 平成年月日 27
28 整理番号 注 -7 新医薬品の薬価算定について 薬効分類 811 あへんアルカロイド系麻薬 ( 注射薬 ) 成分名 ヒドロモルフォン塩酸塩 新薬収載希望者第一三共プロファーマ ( 株 ) 販売名 ( 規格単位 ) 効能 効果 主な用法 用量 ナルベイン注 2mg(2mg1mL1 管 ) ナルベイン注 20mg(20mg2mL1 管 ) 注 ) 医療上の必要性の高い未承認薬 適応外薬検討会議の評価に基づく開発公募品目 中等度から高度の疼痛を伴う各種癌における鎮痛 通常 成人にはヒドロモルフォンとして 1 日 0.5~25mg を持続静脈内又は持 算定方式類似薬効比較方式 (Ⅰ) 続皮下投与する なお 症状に応じて適宜増減する 算比較薬定成分名 : オキシコドン塩酸塩水和物会社名 : 塩野義製薬 ( 株 ) 販売名 ( 規格単位 ) 薬価 (1 日薬価 ) オキファスト注 50mg 1,585 円 (1%5mL1 管 ) (7,925 円 ) 規格間比オキファスト注 50mg 及びオキファスト注 10mg の規格間比 : 補正加算 外国平均価格調整 算定薬価 2mg1mL1 管 725 円 20mg2mL1 管 6,340 円 (1 日薬価 :7,925 円 ) ) 切換え換算比に基づく薬価算定であることから 1 日薬価は 通常最大用量の比較薬が投与されている患者において 比較薬から本剤に切り替えたときの一日当たりの薬価を記載 外国価格 2mg1mL1 管英国 1.598ポンド 230 円独国 4.487ユーロ 565 円外国平均価格 398 円 新薬収載希望者による市場規模予測 予測年度予測本剤投与患者予測販売金額 ( ピーク時 ) 10 年度 4.2 万人 13 億円 20mg1mL1 管 英国 ポンド 3,744 円 独国 ユーロ 3,295 円 外国平均価格 3,520 円 ( 注 1) 為替レートは平成 29 年 2 月 ~ 平成 30 年 1 月の平均 ( 注 2) 米国 (AWP) は従来参照していた RED BOOK の価格 最初に承認された国 ( 年月 ): 米国 (1984 年 1 月 ) 製造販売承認日平成 30 年 1 月 19 日 薬価基準収載予定日平成 30 年 4 月 18 日 28
29 算定方式類似薬効比較方式 (Ⅰ) 第一回算定組織平成 30 年 3 月 15 日最類似薬選定の妥当性薬価算定組織における検討結果のまとめ 新薬 最類似薬 成分名ヒドロモルフォン塩酸塩オキシコドン塩酸塩水和物 イ. 効能 効果 ロ. 薬理作用 ハ. 組成及び化学構造 中等度から高度の疼痛を伴う各種癌における鎮痛 求心性痛覚伝導路抑制作用 / 下行性痛覚抑制系賦活による鎮痛作用 左に同じ 左に同じ ニ. 投与形態剤形用法 画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 有用性加算 (Ⅱ) (5~30%) 市場性加算 (Ⅰ) 市場性加算 (Ⅱ) (5%) 小児加算 (5~20%) 先駆け審査指定制度加算 当初算定案に対する新薬収載希望者の不服意見の要点 上記不服意見に対する見解 注射注射剤静脈内又は皮下投与 第二回算定組織 左に同じ左に同じ左に同じ補正加算平成年月日 29
30 整理番号 外 -1 新医薬品の薬価算定について 薬効分類 449 その他のアレルギー用薬 ( 外用薬 ) 成分名 エメダスチンフマル酸塩 新薬収載希望者久光製薬 ( 株 ) 販売名 ( 規格単位 ) 効能 効果 主な用法 用量 アレサガテープ 4mg(4mg1 枚 ) アレサガテープ 8mg(8mg1 枚 ) アレルギー性鼻炎 通常 成人にはエメダスチンフマル酸塩として 1 回 4mg を胸部 上腕部 背部又は腹部のいずれかに貼付し 24 時間毎に貼り替える なお 症状に応じて 1 算定方式類似薬効比較方式 (Ⅰ) 回 8mgに増量できる 算比較薬定成分名 : ルパタジンフマル酸塩会社名 : 帝國製薬 ( 株 ) 販売名 ( 規格単位 ) 薬価 (1 日薬価 ) ルパフィン錠 10mg 円 (10mg1 錠 ) (67.50 円 ) 剤形間比類似薬に適当な剤形間比がない :1 規格間比ビソノテープ 4mg と同 8mg の規格間比 : 補正加算 外国平均価格調整 算定薬価 4mg1 枚 円 (1 日薬価 :67.50 円 ) 8mg1 枚 円 外国価格 新薬収載希望者による市場規模予測 予測年度予測本剤投与患者予測販売金額 最初に承認された国 : 日本 ( ピーク時 ) 6 年度 45 万人 26 億円 製造販売承認日平成 30 年 1 月 19 日 薬価基準収載予定日平成 30 年 4 月 18 日 30
31 算定方式類似薬効比較方式 (Ⅰ) 第一回算定組織平成 30 年 3 月 15 日最類似薬選定の妥当性薬価算定組織における検討結果のまとめ 新薬 最類似薬 成分名エメダスチンフマル酸塩ルパタジンフマル酸塩 イ. 効能 効果 アレルギー性鼻炎 アレルギー性鼻炎 蕁麻疹 皮膚疾 患 ( 湿疹 皮膚炎 皮膚そう痒症 ) に伴うそう痒 ロ. 薬理作用 ハ. 組成及び化学構造 ケミカルメディエータ受容体拮抗作用 / 抗ヒスタミン作用 左に同じ ニ. 投与形態剤形用法 画期性加算 (70~120%) 有用性加算 (Ⅰ) (35~60%) 有用性加算 (Ⅱ) (5~30%) 市場性加算 (Ⅰ) 市場性加算 (Ⅱ) (5%) 小児加算 (5~20%) 先駆け審査指定制度加算 当初算定案に対する新薬収載希望者の不服意見の要点 上記不服意見に対する見解 外用貼付剤 1 日 1 回 第二回算定組織 内用錠剤左に同じ補正加算平成年月日 31
分類
 高脂血症用剤 MSD= バイエル薬品 アトーゼット配合錠 LD 872189 2189101F1020 アトーゼット配合錠 HD 872189 2189101F2026 エゼチミブ / アトルバスタチンカルシウム水和物 1 錠 177.00 小腸コレステロールトランスポーター阻害剤 / HMG-CoA 還元酵素阻害剤配合剤 1 日 1 回 1 錠を食後に経口投与 1 錠 177.00 高コレステロール血症
高脂血症用剤 MSD= バイエル薬品 アトーゼット配合錠 LD 872189 2189101F1020 アトーゼット配合錠 HD 872189 2189101F2026 エゼチミブ / アトルバスタチンカルシウム水和物 1 錠 177.00 小腸コレステロールトランスポーター阻害剤 / HMG-CoA 還元酵素阻害剤配合剤 1 日 1 回 1 錠を食後に経口投与 1 錠 177.00 高コレステロール血症
厚生労働省告示024号/平成22年1月22日告示/平成22年1月22日施行
 厚生労働省告示第 206 号 / 平成 30 年 4 月 17 日告示 / 平成 30 年 4 月 18 日施行 区分商品名規格単位会社名成分名効能 効果用法 用量規制等備考 内用薬レキサルティ 1mg1 錠大塚製薬ブレクスピプ統合失調症 通常 にはブレクスピプラゾールとして 1 日 1 回 1mg から投与を開始した後 劇 錠 1mg ラゾール 4 日以上の間隔をあけて増量し 1 日 1 回 2mg
厚生労働省告示第 206 号 / 平成 30 年 4 月 17 日告示 / 平成 30 年 4 月 18 日施行 区分商品名規格単位会社名成分名効能 効果用法 用量規制等備考 内用薬レキサルティ 1mg1 錠大塚製薬ブレクスピプ統合失調症 通常 にはブレクスピプラゾールとして 1 日 1 回 1mg から投与を開始した後 劇 錠 1mg ラゾール 4 日以上の間隔をあけて増量し 1 日 1 回 2mg
Microsoft Word - 新薬123(2018.4).doc
 新薬情報 平成 30 年 4 月 18 日付内用薬 12 品目 外用薬 2 品目 注射薬 8 品目が薬価収載されました [ 内用薬 ] は最小包装単位 [ 新医薬品情報 ] 2018.5.1 薬効分類番号 商品名 ( 社名 ) 薬価 成分 含量 ホンタイ識別コード * 効能 効果 / 用法 用量 117 レキサルティ錠 1mg 268.90 ブレクスピプラゾール1mg/ 錠 BRX1 レキサルティ錠
新薬情報 平成 30 年 4 月 18 日付内用薬 12 品目 外用薬 2 品目 注射薬 8 品目が薬価収載されました [ 内用薬 ] は最小包装単位 [ 新医薬品情報 ] 2018.5.1 薬効分類番号 商品名 ( 社名 ) 薬価 成分 含量 ホンタイ識別コード * 効能 効果 / 用法 用量 117 レキサルティ錠 1mg 268.90 ブレクスピプラゾール1mg/ 錠 BRX1 レキサルティ錠
発 再燃を繰り返す逆流性食道炎の維持療法を除く ) においては 通常 8 週間まで 十二指腸潰瘍においては 通常 6 週間まで 非びらん性胃食道逆流症においては 通常 4 週間までと限定されていることから 使用にあたっては十分留意すること 2 本製剤は 既に薬価収載後 1 年以上を経過している ネキ
 日医発第 145 号 ( 保 27) 平成 30 年 4 月 27 日 都道府県医師会長殿 日本医師会長横倉義武 使用薬剤の薬価 ( 薬価基準 ) の一部改正等について 平成 30 年 4 月 17 日付け厚生労働省告示第 206 号をもって薬価基準の一部が改正され 同年 4 月 18 日から適用されました 今回の改正は 医薬品医療機器法の規定に基づき承認を得た新医薬品 (15 成分 22 品目 )
日医発第 145 号 ( 保 27) 平成 30 年 4 月 27 日 都道府県医師会長殿 日本医師会長横倉義武 使用薬剤の薬価 ( 薬価基準 ) の一部改正等について 平成 30 年 4 月 17 日付け厚生労働省告示第 206 号をもって薬価基準の一部が改正され 同年 4 月 18 日から適用されました 今回の改正は 医薬品医療機器法の規定に基づき承認を得た新医薬品 (15 成分 22 品目 )
SKMBT_C552D
 を繰り返す逆流性食道炎の維持療法を除く ) においては 通常 8 週間まで 十二指腸潰瘍においては 通常 6 週間まで 非びらん性胃食道逆流症においては 通常 4 週間までと限定されていることから 使用にあたっては十分留意すること 2 本製剤は 既に薬価収載後 1 年以上を経過している ネキシウムカプセル 10mg 及び同カプセル 20mg ( 以下 既収載品 という ) と有効成分が同一であり 今般
を繰り返す逆流性食道炎の維持療法を除く ) においては 通常 8 週間まで 十二指腸潰瘍においては 通常 6 週間まで 非びらん性胃食道逆流症においては 通常 4 週間までと限定されていることから 使用にあたっては十分留意すること 2 本製剤は 既に薬価収載後 1 年以上を経過している ネキシウムカプセル 10mg 及び同カプセル 20mg ( 以下 既収載品 という ) と有効成分が同一であり 今般
D961H は AstraZeneca R&D Mӧlndal( スウェーデン ) において開発された オメプラゾールの一方の光学異性体 (S- 体 ) のみを含有するプロトンポンプ阻害剤である ネキシウム (D961H の日本における販売名 ) 錠 20 mg 及び 40 mg は を対象として
 第 2 部 CTD の概要 一般名 : エソメプラゾールマグネシウム水和物 版番号 : 2.2 緒言 ネキシウム カプセル ネキシウム 懸濁用顆粒分包 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています D961H は AstraZeneca R&D Mӧlndal( スウェーデン ) において開発された オメプラゾールの一方の光学異性体
第 2 部 CTD の概要 一般名 : エソメプラゾールマグネシウム水和物 版番号 : 2.2 緒言 ネキシウム カプセル ネキシウム 懸濁用顆粒分包 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています D961H は AstraZeneca R&D Mӧlndal( スウェーデン ) において開発された オメプラゾールの一方の光学異性体
区分商品名規格単位薬価 ( 円 ) 包装単位製造販売成分名効能 効果用法 用量規制等承認年月日備考 胃潰瘍 十二指腸潰瘍 吻合部潰瘍 Zollinger-Ellison 症候群ネキシウム懸濁用顆粒分包 10mg1 包 円 28 包アストラゼネエソメプラ 胃潰瘍 十二指腸潰処方 新用量 剤
 新医薬品が薬価収載されましたのでお知らせいたします 区分 商品名 規格単位 薬価 ( 円 ) 包装単位 製造販売 成分名 効能 効果 用法 用量 規制等 承認年月日 備考 レキサルティ錠 1mg 1mg1 錠 268.90 円 [PTP]100 錠 10) 500 錠 50) [ プラスチックボトル ] 500 錠 1,000 錠 大塚製薬 ブレクスピプラゾール 統合失調症 通常 成人にはブレクスピプラゾールとして1
新医薬品が薬価収載されましたのでお知らせいたします 区分 商品名 規格単位 薬価 ( 円 ) 包装単位 製造販売 成分名 効能 効果 用法 用量 規制等 承認年月日 備考 レキサルティ錠 1mg 1mg1 錠 268.90 円 [PTP]100 錠 10) 500 錠 50) [ プラスチックボトル ] 500 錠 1,000 錠 大塚製薬 ブレクスピプラゾール 統合失調症 通常 成人にはブレクスピプラゾールとして1
中医協薬 -1 参考 薬価制度の抜本改革について ( その4) 2 薬価算定方式の正確性 透明性について類似薬効比較方式 ( 参考資料 ) 1 類似薬効比較方式 (Ⅰ) 同じ効果を持つ類似薬がある場合には 市場での公正な競争を確保する観点から 新薬の 1 日薬価を既存類似
 中医協薬 -1 参考 1 2 9. 2. 2 2 薬価制度の抜本改革について ( その4) 2 薬価算定方式の正確性 透明性について類似薬効比較方式 ( 参考資料 ) 1 類似薬効比較方式 (Ⅰ) 同じ効果を持つ類似薬がある場合には 市場での公正な競争を確保する観点から 新薬の 1 日薬価を既存類似薬の 1 日薬価に合わせる 類似薬効比較方式 (Ⅰ) 1 錠 =50 円 1 日 3 錠 = 1 錠
中医協薬 -1 参考 1 2 9. 2. 2 2 薬価制度の抜本改革について ( その4) 2 薬価算定方式の正確性 透明性について類似薬効比較方式 ( 参考資料 ) 1 類似薬効比較方式 (Ⅰ) 同じ効果を持つ類似薬がある場合には 市場での公正な競争を確保する観点から 新薬の 1 日薬価を既存類似薬の 1 日薬価に合わせる 類似薬効比較方式 (Ⅰ) 1 錠 =50 円 1 日 3 錠 = 1 錠
整理番号 内 -1 新医薬品の薬価算定について 薬効分類 248 混合ホルモン剤 ( 内用薬 ) 成分名レボノルゲストレル / エチニルエストラジオール 新薬収載希望者ノーベルファーマ ( 株 ) 販売名 ( 規格単位 ) ジェミーナ配合錠 (1 錠 ) (1 錠中 レボノルゲストレル
 新医薬品一覧表 ( 平成 30 年 8 月 29 日収載予定 ) 中医協総 -2-1 30.8.22 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等薬効分類ページ 1 ジェミーナ配合錠 1 錠 ノーベルファーマ レボノルゲストレル / エチニ新医療用配合剤 ルエストラジオール 2 ダフクリア錠 200mg 200mg1 錠 アステラス製薬 フィダキソマイシン 新有効成分含有医
新医薬品一覧表 ( 平成 30 年 8 月 29 日収載予定 ) 中医協総 -2-1 30.8.22 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等薬効分類ページ 1 ジェミーナ配合錠 1 錠 ノーベルファーマ レボノルゲストレル / エチニ新医療用配合剤 ルエストラジオール 2 ダフクリア錠 200mg 200mg1 錠 アステラス製薬 フィダキソマイシン 新有効成分含有医
使用薬剤の薬価(薬価基準)の一部改正等について(厚生労働省保険局医療課:H )
 事務連絡 平成 30 年 4 月 17 日 別記関係団体御中 厚生労働省保険局医療課 使用薬剤の薬価 ( 薬価基準 ) の一部改正等について 標記について 別添のとおり地方厚生 ( 支 ) 局医療課長 都道府県民生主管部 ( 局 ) 国 民健康保険主管課 ( 部 ) 長及び都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管 課 ( 部 ) 長あて通知しましたのでお知らせいたします [ 別記
事務連絡 平成 30 年 4 月 17 日 別記関係団体御中 厚生労働省保険局医療課 使用薬剤の薬価 ( 薬価基準 ) の一部改正等について 標記について 別添のとおり地方厚生 ( 支 ) 局医療課長 都道府県民生主管部 ( 局 ) 国 民健康保険主管課 ( 部 ) 長及び都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管 課 ( 部 ) 長あて通知しましたのでお知らせいたします [ 別記
新医薬品の薬価算定について 整理番号 内 -1 薬効分類 119 その他の中枢神経系用薬 ( 内用薬 ) 成分名フマル酸ジメチル新薬収載希望者バイオジェン ジャパン ( 株 ) 販売名 ( 規格単位 ) テクフィデラカプセル 120mg(120mg1 カプセル ) テクフィデラカプセル
 新医薬品一覧表 ( 平成 29 年 2 月 15 日収載予定 ) 中医協総 -1-1 29.2.8 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等薬効分類ページ 1 テクフィデラカプセル 120mg テクフィデラカプセル 240mg 120mg1 カプセル 240mg1 カプセル バイオジェン ジャパンフマル酸ジメチル 新有効成分含有医薬品 2 リンゼス錠 0.25mg 0.25mg1
新医薬品一覧表 ( 平成 29 年 2 月 15 日収載予定 ) 中医協総 -1-1 29.2.8 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等薬効分類ページ 1 テクフィデラカプセル 120mg テクフィデラカプセル 240mg 120mg1 カプセル 240mg1 カプセル バイオジェン ジャパンフマル酸ジメチル 新有効成分含有医薬品 2 リンゼス錠 0.25mg 0.25mg1
(表紙)【中医協用】平成27年2月収載予定新薬0202
 新医薬品等一覧表 ( 平成 27 年 2 月 24 日収載予定 ) 中医協総 -2 27.2.18 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等薬効分類ページ 1 タケキャブ錠 10mg タケキャブ錠 20mg 10mg1 錠 20mg1 錠 武田薬品工業 ボノプラザンフマル酸塩 新有効成分含 有医薬品 2 パリエット錠 5mg 5mg1 錠 エーザイ ラベプラゾールナトリウム
新医薬品等一覧表 ( 平成 27 年 2 月 24 日収載予定 ) 中医協総 -2 27.2.18 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等薬効分類ページ 1 タケキャブ錠 10mg タケキャブ錠 20mg 10mg1 錠 20mg1 錠 武田薬品工業 ボノプラザンフマル酸塩 新有効成分含 有医薬品 2 パリエット錠 5mg 5mg1 錠 エーザイ ラベプラゾールナトリウム
新医薬品の薬価算定について 整理番号 内 -1 薬効分類 235 下剤 浣腸剤 ( 内用薬 ) 成分名 マクロゴール4000/ 塩化ナトリウム / 炭酸水素ナトリウム / 塩化カリウム 新薬収載希望者 EAファーマ ( 株 ) 販売名 ( 規格単位 ) モビコール配合内用剤 (6.85
 新医薬品一覧表 ( 平成 30 年 11 月 20 日収載予定 ) 中医協総 -2-1 30.11.14 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等薬効分類ページ 1 モビコール配合内用剤 6.8523g1 包 EAファーマ マクロゴール4000/ 塩化ナ新医療用配合剤 トリウム / 炭酸水素ナトリウ ム / 塩化カリウム 83.90 円類似薬効比較方式 (Ⅰ) 小児加算
新医薬品一覧表 ( 平成 30 年 11 月 20 日収載予定 ) 中医協総 -2-1 30.11.14 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等薬効分類ページ 1 モビコール配合内用剤 6.8523g1 包 EAファーマ マクロゴール4000/ 塩化ナ新医療用配合剤 トリウム / 炭酸水素ナトリウ ム / 塩化カリウム 83.90 円類似薬効比較方式 (Ⅰ) 小児加算
新医薬品一覧表 ( 平成 31 年 2 月 26 日収載予定 ) 中医協総 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等薬効分類ページ 1 ビムパットドライシロップ10% 10%1g ユーシービージャパン ラコサミド 新用量 新剤形医 薬品 386.
 新医薬品一覧表 ( 平成 31 年 2 月 26 日収載予定 ) 中医協総 -1-1 31.2.20 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等薬効分類ページ 1 ビムパットドライシロップ10% 10%1g ユーシービージャパン ラコサミド 新用量 新剤形医 薬品 386.20 円類似薬効比較方式 (Ⅰ) 新薬創出等加算 内 113 抗てんかん剤 ( てんかん患者の部分発作
新医薬品一覧表 ( 平成 31 年 2 月 26 日収載予定 ) 中医協総 -1-1 31.2.20 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等薬効分類ページ 1 ビムパットドライシロップ10% 10%1g ユーシービージャパン ラコサミド 新用量 新剤形医 薬品 386.20 円類似薬効比較方式 (Ⅰ) 新薬創出等加算 内 113 抗てんかん剤 ( てんかん患者の部分発作
<4D F736F F F696E74202D F2817C CBB8D7382CC96F289BF8AEE8F8090A C982C282A282C42E B8CDD8AB
 参考資料 中医協薬 -1 24.6.6 現行の薬価基準制度について 平成 24 年 4 月 ( 赤字は 平成 24 年度薬価制度改革による導入 修正箇所 ) 1 現行薬価基準制度の概要 1. 薬価基準は 医療保険から保険医療機関や保険薬局 ( 保険医療機関等 ) に支払われる際の医薬品の価格を 定めたもの 2. 薬価基準は 平成 24 年 2 月 10 日に中医協がとりまとめ た 薬価算定の基準について
参考資料 中医協薬 -1 24.6.6 現行の薬価基準制度について 平成 24 年 4 月 ( 赤字は 平成 24 年度薬価制度改革による導入 修正箇所 ) 1 現行薬価基準制度の概要 1. 薬価基準は 医療保険から保険医療機関や保険薬局 ( 保険医療機関等 ) に支払われる際の医薬品の価格を 定めたもの 2. 薬価基準は 平成 24 年 2 月 10 日に中医協がとりまとめ た 薬価算定の基準について
<4D F736F F D208BA38D DA81458BA38D878AE98BC6838A E646F6378>
 平成 26 年 10 月 14 日 ジャディアンス錠 平成 25 年 10 月 8 日 ( 錠 25mg) 日本ベーリンガー 品目 10mg, 同錠 25mg 年月日 平成 25 年 12 月 13 日 ( 錠 10mg) 者名 インゲルハイム株式会社 薬事分科会審議参加規程における, 上記品目に係る競合品目, 競合企業及びその選定理由は以下のとおりです 競合品目 1 競合品目 2 競合品目 3 スーグラ錠
平成 26 年 10 月 14 日 ジャディアンス錠 平成 25 年 10 月 8 日 ( 錠 25mg) 日本ベーリンガー 品目 10mg, 同錠 25mg 年月日 平成 25 年 12 月 13 日 ( 錠 10mg) 者名 インゲルハイム株式会社 薬事分科会審議参加規程における, 上記品目に係る競合品目, 競合企業及びその選定理由は以下のとおりです 競合品目 1 競合品目 2 競合品目 3 スーグラ錠
先発品とのの相違の一覧 エダラボン点滴静注 30mg 杏林 エダラボン点滴静注 30mg 杏林 脳梗塞急性期に伴う神経症候 日常生活動作障害 機能障害の改善 通常 成人に 1 回 1 管 ( エダラボンとして 30mg) を適当量の生理食塩液等で用時希釈し 30 分かけて 1 日朝夕 2 回の点滴静
 先発品とのの相違の一覧 ( ご注意 ) 赤字は 先発品と異なる です この一覧に掲載している項目は 主に です その他使用上の注意などにつきましては 各製品の添付文書をご参照下さい 用語や文面など 一部異なる場合があります 詳細は各製品の添付文書ご参照ください 2018 年 4 月 4 日 アリピプラゾール OD 錠 3mg/6mg/12mg 杏林 アリピプラゾール OD 錠 3mg 杏林 アリピプラゾール
先発品とのの相違の一覧 ( ご注意 ) 赤字は 先発品と異なる です この一覧に掲載している項目は 主に です その他使用上の注意などにつきましては 各製品の添付文書をご参照下さい 用語や文面など 一部異なる場合があります 詳細は各製品の添付文書ご参照ください 2018 年 4 月 4 日 アリピプラゾール OD 錠 3mg/6mg/12mg 杏林 アリピプラゾール OD 錠 3mg 杏林 アリピプラゾール
No. 銘柄名 規格単位 会社名 成分名 承認区分 算定薬価 算定方式 補正加算等 1 イーケプラドライシロップ50% 50%1g ユーシービージャパン レベチラセタム 新用量医薬品 円類似薬効比較方式 (Ⅰ) 小児加算 (A=10(%)) 2 イルトラ配合錠 LD イルトラ配合錠 H
 No. 銘柄名 規格単位 会社名 成分名 承認区分 定薬価 定方式 補正加等 1 イーケプラドライシロップ50% 50%1g ユーシービージャパン レベチラセタム 新用量医薬品 253.90 円類似薬効比較方式 (Ⅰ) 小児加 (A=10(%)) 2 イルトラ配合錠 LD イルトラ配合錠 HD 1 錠 1 錠 塩野義製薬 3 ルナベル配合錠 ULD 1 錠 ノーベルファーマ ノルエチステロン / エチニルエストラジ
No. 銘柄名 規格単位 会社名 成分名 承認区分 定薬価 定方式 補正加等 1 イーケプラドライシロップ50% 50%1g ユーシービージャパン レベチラセタム 新用量医薬品 253.90 円類似薬効比較方式 (Ⅰ) 小児加 (A=10(%)) 2 イルトラ配合錠 LD イルトラ配合錠 HD 1 錠 1 錠 塩野義製薬 3 ルナベル配合錠 ULD 1 錠 ノーベルファーマ ノルエチステロン / エチニルエストラジ
 瘙 整理番号 11-09- 内 -1 薬効分類 113 抗てんかん剤 ( 内用薬 ) 成分名ガバペンチン新薬収載希望者ファイザー ( 株 ) 新医薬品の薬価定について 販売名 ( 規格単位 ) ガバペンシロップ 5%(5%1mL) 効能 効果 他の抗てんかん薬で十分な効果が認められないてんかん患者の部分発作 ( 二次性全般化発作を含む ) に対する抗てんかん薬との併用療法 主な用法 用量 通常 成人及び
瘙 整理番号 11-09- 内 -1 薬効分類 113 抗てんかん剤 ( 内用薬 ) 成分名ガバペンチン新薬収載希望者ファイザー ( 株 ) 新医薬品の薬価定について 販売名 ( 規格単位 ) ガバペンシロップ 5%(5%1mL) 効能 効果 他の抗てんかん薬で十分な効果が認められないてんかん患者の部分発作 ( 二次性全般化発作を含む ) に対する抗てんかん薬との併用療法 主な用法 用量 通常 成人及び
用法・用量DB
 データベース データベースの概要 医療用医薬品の添付文書に記載されているに関するデータベースです 処方薬の適正な投与量 ( 上限 下限 ) や投与日数 ( 上限 下限 ) などのチェック および患者さんへの服薬指導にご利用いただくことが可能です 本データベースは 医療用医薬品の添付文書に記載されているの情報を網羅しています データベースの特徴 年齢や体重 体表面積 適応病名 投与経路 療法毎にデータを作成しているため
データベース データベースの概要 医療用医薬品の添付文書に記載されているに関するデータベースです 処方薬の適正な投与量 ( 上限 下限 ) や投与日数 ( 上限 下限 ) などのチェック および患者さんへの服薬指導にご利用いただくことが可能です 本データベースは 医療用医薬品の添付文書に記載されているの情報を網羅しています データベースの特徴 年齢や体重 体表面積 適応病名 投与経路 療法毎にデータを作成しているため
相談品目の薬価基準追補収載のお知らせ
 薬価基準追補収載 ( 新薬 ) のお知らせ 平成 30 年 4 月 17 日公益社団法人福岡県薬剤師会薬事情報センター厚労省は新医薬品の薬価基準追補収載を平成 30 年 4 月 17 日に告示した 4 月 18 日から適用する 内用薬 毒 : 毒薬, 劇 : 劇薬, 処 : 処方箋医薬品, 麻 : 麻薬, 生 : 生物由来製品分類医薬品名 ( 会社名 ) 規格 単位薬価 ( 円 ) 規制備考 ( 成分,
薬価基準追補収載 ( 新薬 ) のお知らせ 平成 30 年 4 月 17 日公益社団法人福岡県薬剤師会薬事情報センター厚労省は新医薬品の薬価基準追補収載を平成 30 年 4 月 17 日に告示した 4 月 18 日から適用する 内用薬 毒 : 毒薬, 劇 : 劇薬, 処 : 処方箋医薬品, 麻 : 麻薬, 生 : 生物由来製品分類医薬品名 ( 会社名 ) 規格 単位薬価 ( 円 ) 規制備考 ( 成分,
(表紙)【中医協用】平成28年11月収載予定新薬1018
 新医薬品一覧表 ( 平成 28 年 11 月 18 日収載予定 ) 中医協総 -1-1 28.11.9 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等薬効分類ページ 1 エビリファイ錠 1mg 1mg1 錠 大塚製薬 アリピプラゾール 新効能 新用 量 新剤型医 薬品 2 ミカトリオ配合錠 1 錠 日本ベーリンガー インゲルハイム テルミサルタン / アムロジピンベシル酸塩 /
新医薬品一覧表 ( 平成 28 年 11 月 18 日収載予定 ) 中医協総 -1-1 28.11.9 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等薬効分類ページ 1 エビリファイ錠 1mg 1mg1 錠 大塚製薬 アリピプラゾール 新効能 新用 量 新剤型医 薬品 2 ミカトリオ配合錠 1 錠 日本ベーリンガー インゲルハイム テルミサルタン / アムロジピンベシル酸塩 /
医科_第20次(追加)審査情報提供(広報用)
 第 20 次審査情報提供事例 ( 医科 ) 追加 平成 31 年 4 月 22 日提供分 社会保険診療報酬支払基金 審査情報提供事例について 審査支払機関における診療報酬請求に関する審査は 健康保険法 療養担当規則 診療報酬点数表及び関係諸通知等を踏まえ各審査委員会の医学的 歯科医学的見解に基づいて行われています 一方 審査の公平 公正性に対する関係方面からの信頼を確保するため 審査における一般的な取扱いについて広く関係者に情報提供を行い
第 20 次審査情報提供事例 ( 医科 ) 追加 平成 31 年 4 月 22 日提供分 社会保険診療報酬支払基金 審査情報提供事例について 審査支払機関における診療報酬請求に関する審査は 健康保険法 療養担当規則 診療報酬点数表及び関係諸通知等を踏まえ各審査委員会の医学的 歯科医学的見解に基づいて行われています 一方 審査の公平 公正性に対する関係方面からの信頼を確保するため 審査における一般的な取扱いについて広く関係者に情報提供を行い
分類
 用そ薬の他の腫瘍 糖尿病用剤 アステラス製薬 日本ベーリンガーインゲルハイム ゾスパタ錠 40 mg 4291053F1021 トラディアンス配合錠 AP 3969108F1027 トラディアンス配合錠 BP 3969108F2023 ギルテリチニブフマル酸塩 エンパグリフロジン / リナグリプチン 40 mg 1 錠 19,409.10 抗悪性腫瘍剤 (FLT3 阻害剤 ) 再発又は難治性の FLT3
用そ薬の他の腫瘍 糖尿病用剤 アステラス製薬 日本ベーリンガーインゲルハイム ゾスパタ錠 40 mg 4291053F1021 トラディアンス配合錠 AP 3969108F1027 トラディアンス配合錠 BP 3969108F2023 ギルテリチニブフマル酸塩 エンパグリフロジン / リナグリプチン 40 mg 1 錠 19,409.10 抗悪性腫瘍剤 (FLT3 阻害剤 ) 再発又は難治性の FLT3
< F2D F289BF8AEE8F808D908EA CA926D>
 保医発 0912 第 1 号平成 23 年 9 月 12 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 使用薬剤の薬価 ( 薬価基準 ) 等の一部改正について 使用薬剤の薬価( 薬価基準 ) ( 平成 20 年厚生労働省告示第 60 号
保医発 0912 第 1 号平成 23 年 9 月 12 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 使用薬剤の薬価 ( 薬価基準 ) 等の一部改正について 使用薬剤の薬価( 薬価基準 ) ( 平成 20 年厚生労働省告示第 60 号
<4D F736F F D2082A8926D82E782B995B68F C D815B838B43505F4F E31302E646F63>
 医薬品の適正使用に欠かせない情報です 必ずお読みください 効能 効果 用法 用量 追加に伴う 使用上の注意 改訂のお知らせ 2010 年 11 月 東和薬品株式会社 このたび 平成 22 年 6 月に承認事項一部変更承認申請をしていました弊社製品のランソプラゾールカプセル15mg/30mg トーワ ランソプラゾールOD 錠 15mg/30mg トーワ の 効能 効果 用法 用量 追加が平成 22 年
医薬品の適正使用に欠かせない情報です 必ずお読みください 効能 効果 用法 用量 追加に伴う 使用上の注意 改訂のお知らせ 2010 年 11 月 東和薬品株式会社 このたび 平成 22 年 6 月に承認事項一部変更承認申請をしていました弊社製品のランソプラゾールカプセル15mg/30mg トーワ ランソプラゾールOD 錠 15mg/30mg トーワ の 効能 効果 用法 用量 追加が平成 22 年
(事務連絡)公知申請に係る前倒し保険適用通知
 保医発 0425 第 1 号 平成 30 年 4 月 25 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 ( 公印省略 ) 公知申請に係る事前評価が終了した医薬品の保険上の取扱いについて 本日開催の薬事 食品衛生審議会医薬品第二部会において
保医発 0425 第 1 号 平成 30 年 4 月 25 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 ( 公印省略 ) 公知申請に係る事前評価が終了した医薬品の保険上の取扱いについて 本日開催の薬事 食品衛生審議会医薬品第二部会において
新医薬品の薬価定について 整理番号 内 -1 薬効分類 114 解熱鎮痛消炎剤 ( 内用薬 配合剤 ) 成分名トラマドール塩酸塩 アセトアミノフェン新薬収載希望者ヤンセンファーマ ( 株 ) 販売名 ( 規格単位 ) 効能 効果 主な用法 用量 トラムセット配合錠 (1 錠 ) (1
 No. 銘柄名規格単位会社名成分名承認区分定薬価定方式補正加等 1 トラムセット配合錠 1 錠 ヤンセンファー マ 新医薬品一覧表 ( 平成 23 年 7 月 19 日収載予定 ) トラマドール塩酸塩 アセトアミノフェン 新医療用配合剤 68.20 円類似薬効比較方式 (Ⅰ) 有用性加 (Ⅱ) (A=10(%)) 内 114 中医協総 2-1 23. 7. 13 薬効分類解熱鎮痛消炎剤 ( 非オピオイド鎮痛剤で治療困難な非がん性慢性疼痛又は抜歯後の疼痛における鎮痛用薬
No. 銘柄名規格単位会社名成分名承認区分定薬価定方式補正加等 1 トラムセット配合錠 1 錠 ヤンセンファー マ 新医薬品一覧表 ( 平成 23 年 7 月 19 日収載予定 ) トラマドール塩酸塩 アセトアミノフェン 新医療用配合剤 68.20 円類似薬効比較方式 (Ⅰ) 有用性加 (Ⅱ) (A=10(%)) 内 114 中医協総 2-1 23. 7. 13 薬効分類解熱鎮痛消炎剤 ( 非オピオイド鎮痛剤で治療困難な非がん性慢性疼痛又は抜歯後の疼痛における鎮痛用薬
No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等 1 ロゼレム錠 8mg 8mg1 錠 武田薬品工業 ラメルテオン 新有効成分 円類似薬効比較方式 (Ⅰ) 2 リリカカプセル 25mg リリカカプセル 75mg リリカカプセル 150mg 25mg1 カプセル 75m
 o. 銘柄名規格単位会社名成分名承認区分定薬価定方式補正加等 1 ロゼレム錠 8mg 8mg1 錠 武田薬品工業 ラメルテオン 新有効成分 82.60 円類似薬効比較方式 (Ⅰ) 2 リリカカプセル 25mg リリカカプセル 75mg リリカカプセル 150mg 25mg1 カプセル 75mg1 カプセル 150mg1 カプセル 新医薬品一覧表 ( 平成 22 年 6 月 11 日収載予定 ) ファイザー
o. 銘柄名規格単位会社名成分名承認区分定薬価定方式補正加等 1 ロゼレム錠 8mg 8mg1 錠 武田薬品工業 ラメルテオン 新有効成分 82.60 円類似薬効比較方式 (Ⅰ) 2 リリカカプセル 25mg リリカカプセル 75mg リリカカプセル 150mg 25mg1 カプセル 75mg1 カプセル 150mg1 カプセル 新医薬品一覧表 ( 平成 22 年 6 月 11 日収載予定 ) ファイザー
<817989DB92B790E096BE A338C8E8EFB8DDA975C92E F28E5A92E F2E786C73>
 新医薬品一覧表 ( 平成 23 年 3 月 11 日収載予定 ) No. 銘柄名 規格単位 会社名 成分名 承認区分 定薬価 定方式 補正加等 1 メマリー錠 5mg メマリー錠 10mg メマリー錠 20mg 5mg1 錠 10mg1 錠 20mg1 錠 第一三共 メマンチン塩酸塩 新有効成分医薬品 133.90 円類似薬効比較方式 239.20 円 (Ⅰ) 427.50 円 内 119 中医協総
新医薬品一覧表 ( 平成 23 年 3 月 11 日収載予定 ) No. 銘柄名 規格単位 会社名 成分名 承認区分 定薬価 定方式 補正加等 1 メマリー錠 5mg メマリー錠 10mg メマリー錠 20mg 5mg1 錠 10mg1 錠 20mg1 錠 第一三共 メマンチン塩酸塩 新有効成分医薬品 133.90 円類似薬効比較方式 239.20 円 (Ⅰ) 427.50 円 内 119 中医協総
審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7
![審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7 審査結果 平成 26 年 1 月 6 日 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [ 審査結果 ] 平成 25 年 7](/thumbs/92/110490968.jpg) 審査報告書 平成 26 年 1 月 6 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [
審査報告書 平成 26 年 1 月 6 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販 売 名 ] ダラシン S 注射液 300mg 同注射液 600mg [ 一 般 名 ] クリンダマイシンリン酸エステル [ 申請者名 ] ファイザー株式会社 [ 申請年月日 ] 平成 25 年 8 月 21 日 [
鑑-H リンゼス錠他 留意事項通知の一部改正等について
 日医発第 617 号 ( 保 154) 平成 30 年 8 月 29 日 都道府県医師会長殿 日本医師会長横倉義武 医薬品医療機器等法上の効能 効果等の変更に伴う留意事項の一部改正等について 平成 30 年 8 月 21 日付け保医発 0821 第 1 号厚生労働省保険局医療課長通知により 添付資料の通り保険適用上の取扱いに関する留意事項が一部改正されましたのでお知らせ申し上げます 今回の改正は 同日付けで添付資料の医薬品の効能
日医発第 617 号 ( 保 154) 平成 30 年 8 月 29 日 都道府県医師会長殿 日本医師会長横倉義武 医薬品医療機器等法上の効能 効果等の変更に伴う留意事項の一部改正等について 平成 30 年 8 月 21 日付け保医発 0821 第 1 号厚生労働省保険局医療課長通知により 添付資料の通り保険適用上の取扱いに関する留意事項が一部改正されましたのでお知らせ申し上げます 今回の改正は 同日付けで添付資料の医薬品の効能
中医協総 医薬品及び医療機器の費用対効果評価に関する取扱いについて 1 既収載品に係る費用対効果評価の手続き (1) 対象品目の指定中央社会保険医療協議会の定める以下の選定基準に基づき 費用対効果評価専門部会において指定 公表されたものとする 次の全ての要件を満たす品
 中医協総 - 5 2 8. 2. 1 0 医薬品及び医療機器の費用対効果評価に関する取扱いについて 1 既収載品に係る費用対効果評価の手続き (1) 対象品目の指定中央社会保険医療協議会の定める以下の選定基準に基づき 費用対効果評価専門部会において指定 公表されたものとする 次の全ての要件を満たす品目を対象とする なお 2においてイのⅰ イのⅱ ロのⅰ 及びロのⅱは それぞれ1 品目が該当するものとし
中医協総 - 5 2 8. 2. 1 0 医薬品及び医療機器の費用対効果評価に関する取扱いについて 1 既収載品に係る費用対効果評価の手続き (1) 対象品目の指定中央社会保険医療協議会の定める以下の選定基準に基づき 費用対効果評価専門部会において指定 公表されたものとする 次の全ての要件を満たす品目を対象とする なお 2においてイのⅰ イのⅱ ロのⅰ 及びロのⅱは それぞれ1 品目が該当するものとし
1 新規採用医薬品 薬事委員会の決定による医薬品採用の開始 一般名 薬効等 開始日 オキシコンチン TR 錠 5mg オキシコドン塩酸塩水和物持続性癌疼痛治療剤 平成 0 年 7 月 19 日 ( 木 ) 取扱い中止医薬品 取扱い中止予定薬品の詳細については 随時 医療情報端末に掲載しています 掲載
 平成 0 年 7 月 5 日 DI ニュース Drug Information News 本情報は以下の URL でも参照できます http://www.med.osaka-cu.ac.jp/pharmacy/ 薬剤部 DI 室 (74) No.77 掲載内容 ( 目次 ) 1 新規採用医薬品 薬事委員会の決定による医薬品採用の開始 取扱い中止医薬品 -1 薬事委員会の決定による取扱い中止 - 販売中止による取扱い中止
平成 0 年 7 月 5 日 DI ニュース Drug Information News 本情報は以下の URL でも参照できます http://www.med.osaka-cu.ac.jp/pharmacy/ 薬剤部 DI 室 (74) No.77 掲載内容 ( 目次 ) 1 新規採用医薬品 薬事委員会の決定による医薬品採用の開始 取扱い中止医薬品 -1 薬事委員会の決定による取扱い中止 - 販売中止による取扱い中止
< F2D CF6926D905C90BF82C98C5782E992CA926D88C4>
 保医発 1031 第 1 号平成 24 年 10 月 31 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 公知申請に係る事前評価が終了した医薬品の保険上の取扱いについて 本日開催の薬事 食品衛生審議会医薬品第二部会において 別添 1の7
保医発 1031 第 1 号平成 24 年 10 月 31 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 公知申請に係る事前評価が終了した医薬品の保険上の取扱いについて 本日開催の薬事 食品衛生審議会医薬品第二部会において 別添 1の7
モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム 製造販売業者 EA ファーマ株式会社 薬効分類 提出年月 平成 30 年 10 月 1.1. 安全
 モビコール配合内用剤 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はEAファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません EA ファーマ株式会社 モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム
モビコール配合内用剤 に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はEAファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません EA ファーマ株式会社 モビコール 配合内用剤に係る 医薬品リスク管理計画書 (RMP) の概要 販売名 モビコール 配合内用剤 有効成分 マクロゴール4000 塩化ナトリウム 炭酸水素ナトリウム 塩化カリウム
改訂の理由及び調査の結果直近 3 年度の国内副作用症例の集積状況 転帰死亡症例 アモキシシリン水和物及びクラブラン酸カリウム アモキシシリン水和物の国内症例が集積したことから 専門委員の意見も踏まえた調査の結果 改訂することが適切と判断した 血小板減少関連症例 1 アモキシシリン水和物 3 例 (
 アモキシシリン水和物含有製剤の 使用上の注意 の改訂について 成分名該当商品名効能 効果改訂の概要 成分名該当商品名 ( 承認取得者 ) 1 アモキシシリン水和物 1 サワシリンカプセル 125 同カプセ 2 クラブラン酸カリウル 250 同細粒 10% 同錠 250( アム アモキシシリン水ステラス製薬株式会社 ) パセト和物シンカプセル 125 同カプセル 3 ランソプラゾール ア 250 同細粒
アモキシシリン水和物含有製剤の 使用上の注意 の改訂について 成分名該当商品名効能 効果改訂の概要 成分名該当商品名 ( 承認取得者 ) 1 アモキシシリン水和物 1 サワシリンカプセル 125 同カプセ 2 クラブラン酸カリウル 250 同細粒 10% 同錠 250( アム アモキシシリン水ステラス製薬株式会社 ) パセト和物シンカプセル 125 同カプセル 3 ランソプラゾール ア 250 同細粒
審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果
![審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果 審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果](/thumbs/92/108604766.jpg) 審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
< F2D C D838A8BDB92CA926D2E6A7464>
 保医発 0221 第 31 号平成 25 年 2 月 21 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 ヘリコバクター ピロリ感染の診断及び治療に関する取扱いについて の一部改正について 今般 ヘリコバクター ピロリ感染の診断及び治療に使用する医薬品の効能
保医発 0221 第 31 号平成 25 年 2 月 21 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 ヘリコバクター ピロリ感染の診断及び治療に関する取扱いについて の一部改正について 今般 ヘリコバクター ピロリ感染の診断及び治療に使用する医薬品の効能
DRAFT#9 2011
 報道関係各位 2019 年 1 月 8 日 ユーシービージャパン株式会社 抗てんかん剤 ビムパット ドライシロップ 10% 及び ビムパット 点滴静注 200mg 製造販売承認のお知らせ ユーシービージャパン株式会社 ( 本社 : 東京都新宿区 代表取締役社長 : 菊池加奈子 以下 ユーシービージャパン また ユーシービーグループを総称して以下 ユーシービー ) は本日 抗てんかん剤 ビムパット ドライシロップ
報道関係各位 2019 年 1 月 8 日 ユーシービージャパン株式会社 抗てんかん剤 ビムパット ドライシロップ 10% 及び ビムパット 点滴静注 200mg 製造販売承認のお知らせ ユーシービージャパン株式会社 ( 本社 : 東京都新宿区 代表取締役社長 : 菊池加奈子 以下 ユーシービージャパン また ユーシービーグループを総称して以下 ユーシービー ) は本日 抗てんかん剤 ビムパット ドライシロップ
<4D F736F F F696E74202D2095E288E25F8CBB8D7382CC96F289BF8AEE8F8090A C982C282A282C BD90AC E A5F93FA967B8CEA94C5>
 中医協薬 -1 参考 7 28.11.30 現行の薬価基準制度について 厚生労働省保険局医療課 ( 下線部は 平成 28 年度薬価制度改革による導入 修正箇所 ) 1 現行薬価基準制度の概要 1. 薬価基準は 医療保険から保険医療機関や保険薬局 ( 保険医療機関等 ) に支払われる際の医薬品の価格を定めたもの 2. 薬価基準は 平成 28 年 2 月 10 日に中医協がとりまとめた 薬価算定の基準について
中医協薬 -1 参考 7 28.11.30 現行の薬価基準制度について 厚生労働省保険局医療課 ( 下線部は 平成 28 年度薬価制度改革による導入 修正箇所 ) 1 現行薬価基準制度の概要 1. 薬価基準は 医療保険から保険医療機関や保険薬局 ( 保険医療機関等 ) に支払われる際の医薬品の価格を定めたもの 2. 薬価基準は 平成 28 年 2 月 10 日に中医協がとりまとめた 薬価算定の基準について
301128_課_薬生薬審発1128第1号_ニボルマブ(遺伝子組換え)製剤の最適使用推進ガイドラインの一部改正について
 薬生薬審発 1128 第 1 号平成 30 年 1 1 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) ニボルマブ ( 遺伝子組換え ) 製剤の最適使用推進ガイドライン ( 非小細胞肺癌 悪性黒色腫 頭頸部癌 腎細胞癌 古典的ホ ジキンリンパ腫 胃癌及び悪性胸膜中皮腫 ) の一部改正について 経済財政運営と改革の基本方針
薬生薬審発 1128 第 1 号平成 30 年 1 1 月 28 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) ニボルマブ ( 遺伝子組換え ) 製剤の最適使用推進ガイドライン ( 非小細胞肺癌 悪性黒色腫 頭頸部癌 腎細胞癌 古典的ホ ジキンリンパ腫 胃癌及び悪性胸膜中皮腫 ) の一部改正について 経済財政運営と改革の基本方針
< E38BA695F18D A956996DA88EA C816995BD90AC E82588C8E8EFB8DDA975C92E8816A2E786C73>
 中医協総 - 1 1 9. 9. 1 9 No. 銘柄名 規格単位 会社名 成分名 承認区分 算定薬価 算定方式 補正加算等 1 トピナ錠 50mg トピナ錠 100mg 50mg1 錠 100mg1 錠 協和醱酵工業 トピラマート 新有効成分 104.80 円類似薬効比較方式 (Ⅰ) 171.60 円外国平均価格調整 ( 引上げ ) 2 セララ錠 25mg セララ錠 50mg セララ錠 100mg
中医協総 - 1 1 9. 9. 1 9 No. 銘柄名 規格単位 会社名 成分名 承認区分 算定薬価 算定方式 補正加算等 1 トピナ錠 50mg トピナ錠 100mg 50mg1 錠 100mg1 錠 協和醱酵工業 トピラマート 新有効成分 104.80 円類似薬効比較方式 (Ⅰ) 171.60 円外国平均価格調整 ( 引上げ ) 2 セララ錠 25mg セララ錠 50mg セララ錠 100mg
中医協総 新医薬品一覧表 ( 平成 21 年 3 月 13 日収載予定 ) No. 銘柄名 規格単位 会社名 成分名 承認区分 算定薬価 算定方式 補正加算等 1 トレリーフ錠 25mg 25mg1 錠 大日本住友製薬ゾニサミド 新効能 新用量 1, 円類似薬効比
 中医協総 - 1 21.2.25 新医薬品一覧表 ( 平成 21 年 3 月 13 日収載予 ) No. 銘柄名 規格単位 会社名 成分名 承認区分 算薬価 算方式 補正加算等 1 トレリーフ錠 25mg 25mg1 錠 大日本住友製薬ゾニサミド 新効能 新用量 1,084.90 円類似薬効比較方式 (Ⅰ) 有用性加算 (Ⅱ) (A=5%) 薬効分類内 116 抗パーキンソン剤 ( レボドパ含有製剤に他の抗パーキンソン病薬を使用しても十分に効果が得られなかった場合のパーキンソン病用薬
中医協総 - 1 21.2.25 新医薬品一覧表 ( 平成 21 年 3 月 13 日収載予 ) No. 銘柄名 規格単位 会社名 成分名 承認区分 算薬価 算方式 補正加算等 1 トレリーフ錠 25mg 25mg1 錠 大日本住友製薬ゾニサミド 新効能 新用量 1,084.90 円類似薬効比較方式 (Ⅰ) 有用性加算 (Ⅱ) (A=5%) 薬効分類内 116 抗パーキンソン剤 ( レボドパ含有製剤に他の抗パーキンソン病薬を使用しても十分に効果が得られなかった場合のパーキンソン病用薬
未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名要望された医薬品要望内容 CSL ベーリング株式会社要望番号 Ⅱ-175 成分名 (10%) 人免疫グロブリン G ( 一般名 ) プリビジェン (Privigen) 販売名 未承認薬 適応 外薬の分類
 未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名要望された医薬品要望内容 CSL ベーリング株式会社要望番号 Ⅱ-175 成分名 (10%) 人免疫グロブリン G ( 一般名 ) プリビジェン (Privigen) 販売名 未承認薬 適応 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) ( 要望されたについて記載する
未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名要望された医薬品要望内容 CSL ベーリング株式会社要望番号 Ⅱ-175 成分名 (10%) 人免疫グロブリン G ( 一般名 ) プリビジェン (Privigen) 販売名 未承認薬 適応 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) ( 要望されたについて記載する
Microsoft Word - 鑑
 日医発第 133 号 ( 保 33) 平成 2 8 年 4 月 2 5 日 都道府県医師会長 殿 日本医師会長横倉義武 使用薬剤の薬価 ( 薬価基準 ) の一部改正等について 平成 28 年 4 月 19 日付け厚生労働省告示第 209 号をもって薬価基準の一部が改正され 平成 28 年 4 月 20 日から適用されました 今回の改正は 医薬品医療機器等法の規定に基づき承認を得た新医薬品等 (7 成分
日医発第 133 号 ( 保 33) 平成 2 8 年 4 月 2 5 日 都道府県医師会長 殿 日本医師会長横倉義武 使用薬剤の薬価 ( 薬価基準 ) の一部改正等について 平成 28 年 4 月 19 日付け厚生労働省告示第 209 号をもって薬価基準の一部が改正され 平成 28 年 4 月 20 日から適用されました 今回の改正は 医薬品医療機器等法の規定に基づき承認を得た新医薬品等 (7 成分
整理番号 内 -1 新医薬品の薬価定について 薬効分類 399 他に分類されない代謝性医薬品 ( 内用薬 ) 成分名フィンゴリモド塩酸塩 新薬収載希望者 販売名 ( 規格単位 ) 効能 効果 田辺三菱製薬 ( 株 ) ノバルティスファーマ ( 株 ) イムセラカプセル 0.5mg(0.
 No. 銘柄名規格単位会社名成分名承認区分定薬価定方式補正加等 1 イムセラカプセル 0.5mg ジレニアカプセル 0.5mg 0.5mg1 カプセル 0.5mg1 カプセル 田辺三菱製薬ノバルティスファーマ 新医薬品一覧表 ( 平成 23 年 11 月 25 日収載予定 ) フィンゴリモド塩酸塩新有効成分 8,172.00 円類似薬効比較方式 (Ⅰ) 有用性加 (Ⅰ) 8,172.00 円 (A=40(%))
No. 銘柄名規格単位会社名成分名承認区分定薬価定方式補正加等 1 イムセラカプセル 0.5mg ジレニアカプセル 0.5mg 0.5mg1 カプセル 0.5mg1 カプセル 田辺三菱製薬ノバルティスファーマ 新医薬品一覧表 ( 平成 23 年 11 月 25 日収載予定 ) フィンゴリモド塩酸塩新有効成分 8,172.00 円類似薬効比較方式 (Ⅰ) 有用性加 (Ⅰ) 8,172.00 円 (A=40(%))
<4D F736F F D2082A8926D82E782B995B68F D815B838B8FF E31312E646F63>
 医薬品の適正使用に欠かせない情報です 必ずお読みください 効能 効果 用法 用量 追加に伴う 使用上の注意 改訂のお知らせ 2010 年 11 月 東和薬品株式会社 このたび 平成 22 年 6 月に承認事項一部変更承認申請をしていました弊社製品のオメプラゾール錠 トーワ 10mg/20mgの 効能 効果 用法 用量 追加が平成 22 年 11 月 15 日付にて 下記の内容で承認されました また承認に伴い
医薬品の適正使用に欠かせない情報です 必ずお読みください 効能 効果 用法 用量 追加に伴う 使用上の注意 改訂のお知らせ 2010 年 11 月 東和薬品株式会社 このたび 平成 22 年 6 月に承認事項一部変更承認申請をしていました弊社製品のオメプラゾール錠 トーワ 10mg/20mgの 効能 効果 用法 用量 追加が平成 22 年 11 月 15 日付にて 下記の内容で承認されました また承認に伴い
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 <その他分野 ( 消化器官用薬 解毒剤 その他 )> 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号
 資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠 50mg 医薬品リスク管理計画書 (RMP) の概要 有効成分 タペンタ 錠 100mg 製造販売業者 ヤンセンファーマ株式会社 薬効分類 821 提出年月 平成 30 年
 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任はヤンセンファーマ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ヤンセンファーマ株式会社 タペンタ 錠 25mg タペンタ 錠 50mg タペンタ 錠 100mg に係る 販売名 タペンタ 錠 25mg タペンタ 錠
第 2 部 CTD の概要 一般名 : エソメプラゾールマグネシウム水和物 版番号 : 緒言 ネキシウム カプセル ネキシウム 懸濁用顆粒分包 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています
 第 2 部 CTD の概要 一般名 : エソメプラゾールマグネシウム水和物 版番号 : 2.6.1 緒言 ネキシウム カプセル ネキシウム 懸濁用顆粒分包 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています 2.6.1 緒言一般名 : エソメプラゾールマグネシウム水和物 目次 頁 目次... 2 略語及び専門用語一覧表...
第 2 部 CTD の概要 一般名 : エソメプラゾールマグネシウム水和物 版番号 : 2.6.1 緒言 ネキシウム カプセル ネキシウム 懸濁用顆粒分包 本資料に記載された情報に係る権利はアストラゼネカ株式会社に帰属します 弊社の事前の承諾なく本資料の内容を他に開示することは禁じられています 2.6.1 緒言一般名 : エソメプラゾールマグネシウム水和物 目次 頁 目次... 2 略語及び専門用語一覧表...
タケキャブ錠 10 mg 他に係る医薬品リスク管理計画書 (RMP) の概要 ( 別紙様式 ) 販売名 タケキャブ錠 10 mg 同 20 mg 有効成分 ボノプラザンフマル酸塩 製造販売業者 武田薬品工業株式会社 薬効分類 提出年月 2018 年 4 月 1.1. 安全性検討事項 重要
 タケキャブ錠 10 mg タケキャブ錠 20 mg に係る 医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任は 武田薬品工業株式会社に帰属するものであり 当該情報を適正使用以外の営利目的に利用することはできません 武田薬品工業株式会社 タケキャブ錠 10 mg 他に係る医薬品リスク管理計画書 (RMP) の概要 ( 別紙様式 ) 販売名 タケキャブ錠 10 mg 同 20 mg
タケキャブ錠 10 mg タケキャブ錠 20 mg に係る 医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容の責任は 武田薬品工業株式会社に帰属するものであり 当該情報を適正使用以外の営利目的に利用することはできません 武田薬品工業株式会社 タケキャブ錠 10 mg 他に係る医薬品リスク管理計画書 (RMP) の概要 ( 別紙様式 ) 販売名 タケキャブ錠 10 mg 同 20 mg
中医協総 再生医療等製品の医療保険上の取扱いについて 再生医療等製品の保険適用に係る取扱いについては 平成 26 年 11 月 5 日の中医協総会において 以下のとおり了承されたところ < 平成 26 年 11 月 5 日中医協総 -2-1( 抜粋 )> 1. 保険適
 中医協総 - 3 3 1. 3. 2 7 再生医療等製品の医療保険上の取扱いについて 再生医療等製品の保険適用に係る取扱いについては 平成 26 年 11 月 5 日の中医協総会において 以下のとおり了承されたところ < 平成 26 年 11 月 5 日中医協総 -2-1( 抜粋 )> 1. 保険適用に係る今後の対応について 再生医療等製品の保険適用に関する当面の間の対応 薬事法改正後に承認 ( 条件
中医協総 - 3 3 1. 3. 2 7 再生医療等製品の医療保険上の取扱いについて 再生医療等製品の保険適用に係る取扱いについては 平成 26 年 11 月 5 日の中医協総会において 以下のとおり了承されたところ < 平成 26 年 11 月 5 日中医協総 -2-1( 抜粋 )> 1. 保険適用に係る今後の対応について 再生医療等製品の保険適用に関する当面の間の対応 薬事法改正後に承認 ( 条件
No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等 1 トラムセット配合錠 1 錠 ヤンセンファー マ 新医薬品一覧表 ( 平成 23 年 7 月 19 日収載予定 ) トラマドール塩酸塩 アセトアミノフェン 新医療用配合剤 円類似薬効比較方式 (Ⅰ) 有用性加算 (Ⅱ
 No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等 1 トラムセット配合錠 1 錠 ヤンセンファー マ 新医薬品一覧表 ( 平成 23 年 7 月 19 日収載予定 ) トラマドール塩酸塩 アセトアミノフェン 新医療用配合剤 68.20 円類似薬効比較方式 (Ⅰ) 有用性加算 (Ⅱ) (A=10(%)) 内 114 中医協総 2-1 23. 7. 13 薬効分類解熱鎮痛消炎剤 (
No. 銘柄名規格単位会社名成分名承認区分算定薬価算定方式補正加算等 1 トラムセット配合錠 1 錠 ヤンセンファー マ 新医薬品一覧表 ( 平成 23 年 7 月 19 日収載予定 ) トラマドール塩酸塩 アセトアミノフェン 新医療用配合剤 68.20 円類似薬効比較方式 (Ⅰ) 有用性加算 (Ⅱ) (A=10(%)) 内 114 中医協総 2-1 23. 7. 13 薬効分類解熱鎮痛消炎剤 (
< E38BA A95BD90AC E328C8E8EFB8DDA975C92E F22E786C7378>
 No. 銘柄名 規格単位 会社名 成分名 承認区分 定薬価 定方式 補正加等 薬効分類 1 コレアジン錠 12.5 mg 12.5mg1 錠 アルフレッサファーマ テトラベナジン 新有効成分含有医薬品 385.40 円原価計方式 内 119 その他の中枢神経系用薬 ( ハンチントン病に伴う舞踏運動用薬 ) 2 ミニリンメルトOD 錠 60μg 60μg1 錠 フェリング デスモプレシン酢酸塩 新効能
No. 銘柄名 規格単位 会社名 成分名 承認区分 定薬価 定方式 補正加等 薬効分類 1 コレアジン錠 12.5 mg 12.5mg1 錠 アルフレッサファーマ テトラベナジン 新有効成分含有医薬品 385.40 円原価計方式 内 119 その他の中枢神経系用薬 ( ハンチントン病に伴う舞踏運動用薬 ) 2 ミニリンメルトOD 錠 60μg 60μg1 錠 フェリング デスモプレシン酢酸塩 新効能
1. 医薬品リスク管理計画を策定の上 適切に実施すること 2. 国内での治験症例が極めて限られていることから 製造販売後 一定数の症例に係るデータが集積されるまでの間は 全 症例を対象に使用成績調査を実施することにより 本剤使用患者の背景情報を把握するとともに 本剤の安全性及び有効性に関するデータを
 薬生薬審発 0525 第 3 号薬生安発 0525 第 1 号平成 30 年 5 月 25 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) トファシチニブクエン酸塩製剤の使用に当たっての留意事項について トファシチニブクエン酸塩製剤 ( 販売名 : ゼルヤンツ錠
薬生薬審発 0525 第 3 号薬生安発 0525 第 1 号平成 30 年 5 月 25 日 都道府県各保健所設置市衛生主管部 ( 局 ) 長殿特別区 厚生労働省医薬 生活衛生局医薬品審査管理課長 ( 公印省略 ) 厚生労働省医薬 生活衛生局医薬安全対策課長 ( 公印省略 ) トファシチニブクエン酸塩製剤の使用に当たっての留意事項について トファシチニブクエン酸塩製剤 ( 販売名 : ゼルヤンツ錠
150800247.indd
 ヘリコバクター ピロリ ピロリ菌 感染症について 消化器内科 藤澤 聖 1983 年に胃の粘膜からピロリ菌が発見されて以来様々な研究がなされ ピロリ菌と胃の関係や 種々の病気との関連について明らかになってきました ピロリ菌が胃に感染すると長い年月をかけて 萎縮性胃炎 腸上皮化生という状態を惹き起こし そこから大部分の胃癌が発生すると言われてい ます また胃潰瘍 十二指腸潰瘍や胃 MALT リンパ腫など胃腸疾患のみならず
ヘリコバクター ピロリ ピロリ菌 感染症について 消化器内科 藤澤 聖 1983 年に胃の粘膜からピロリ菌が発見されて以来様々な研究がなされ ピロリ菌と胃の関係や 種々の病気との関連について明らかになってきました ピロリ菌が胃に感染すると長い年月をかけて 萎縮性胃炎 腸上皮化生という状態を惹き起こし そこから大部分の胃癌が発生すると言われてい ます また胃潰瘍 十二指腸潰瘍や胃 MALT リンパ腫など胃腸疾患のみならず
審査結果 平成 25 年 9 月 27 日 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 審査結果 ] 平成 25 年 4 月 26 日開
![審査結果 平成 25 年 9 月 27 日 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 審査結果 ] 平成 25 年 4 月 26 日開 審査結果 平成 25 年 9 月 27 日 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 審査結果 ] 平成 25 年 4 月 26 日開](/thumbs/53/31072016.jpg) 審査報告書 平成 25 年 9 月 27 日独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 剤形 含量 ]
審査報告書 平成 25 年 9 月 27 日独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] アナフラニール錠 10 mg 同錠 25 mg [ 一般名 ] クロミプラミン塩酸塩 [ 申請者名 ] アルフレッサファーマ株式会社 [ 申請年月日 ] 平成 25 年 5 月 17 日 [ 剤形 含量 ]
DRAFT#9 2011
 報道関係各位 2019 年 3 月 25 日 ユーシービージャパン株式会社 第一三共株式会社 抗てんかん剤 ビムパット 点滴静注 200mg 新発売のお知らせ ユーシービージャパン株式会社 ( 本社 : 東京都新宿区 代表取締役社長 : 菊池加奈子 以下 ユーシービージャパン ユーシービーグループを総称して以下 ユーシービー ) と第一三共株式会社 ( 本社 : 東京都中央区 代表取締役社長 : 眞鍋淳
報道関係各位 2019 年 3 月 25 日 ユーシービージャパン株式会社 第一三共株式会社 抗てんかん剤 ビムパット 点滴静注 200mg 新発売のお知らせ ユーシービージャパン株式会社 ( 本社 : 東京都新宿区 代表取締役社長 : 菊池加奈子 以下 ユーシービージャパン ユーシービーグループを総称して以下 ユーシービー ) と第一三共株式会社 ( 本社 : 東京都中央区 代表取締役社長 : 眞鍋淳
平成 30 年 8 月 10 日 リポバス錠 5, 10, 20 アトーゼット配合錠 LD, MSD 株式会社 HD 競合品目 1 クレストール錠 クレストールOD 錠 アストラゼネカ 競合品目 2 リピトール錠 アステラス製薬 競合品目 3 リバロ錠 リバロOD 錠 興和 自社製品を除いた同効品で
 平成 30 年 8 月 7 日 リピトール錠 5mg リピトール錠 10mg アステラス製薬株式会社 競合品目 1 クレストール錠 2.5mg クレストール錠 5mg クレストールOD 錠 2.5mg クレストールOD 錠 5mg( ロスバスタチンカルシウム ) 競合品目 2 リバロ錠 1mg リバロ錠 2mg リバロ錠 4mg ( ピタバスタチンカルシウム ) 競合品目 3 メバロチン錠 5 メバロチン錠
平成 30 年 8 月 7 日 リピトール錠 5mg リピトール錠 10mg アステラス製薬株式会社 競合品目 1 クレストール錠 2.5mg クレストール錠 5mg クレストールOD 錠 2.5mg クレストールOD 錠 5mg( ロスバスタチンカルシウム ) 競合品目 2 リバロ錠 1mg リバロ錠 2mg リバロ錠 4mg ( ピタバスタチンカルシウム ) 競合品目 3 メバロチン錠 5 メバロチン錠
したことによると考えられています 4. ピロリ菌の検査法ピロリ菌の検査法にはいくつかの種類があり 内視鏡を使うものとそうでないものに大きく分けられます 前者は 内視鏡を使って胃の組織を採取し それを材料にしてピロリ菌の有無を調べます 胃粘膜組織を顕微鏡で見てピロリ菌を探す方法 ( 鏡検法 ) 先に述
 ピロリ菌のはなし ( 上 ) 大阪掖済会病院部長 消化器内科佐藤博之 1. はじめにピロリ菌という言葉を聞いたことがある方も多いと思います ピロリ菌はヒトの胃の中に住む細菌で 胃潰瘍や十二指腸潰瘍に深く関わっていることが明らかにされています 22 年前に発見されてから研究が精力的に進められ 以後 胃潰瘍や十二指腸潰瘍の治療法が大きく様変わりすることになりました 我が国では 2000 年 11 月に胃潰瘍
ピロリ菌のはなし ( 上 ) 大阪掖済会病院部長 消化器内科佐藤博之 1. はじめにピロリ菌という言葉を聞いたことがある方も多いと思います ピロリ菌はヒトの胃の中に住む細菌で 胃潰瘍や十二指腸潰瘍に深く関わっていることが明らかにされています 22 年前に発見されてから研究が精力的に進められ 以後 胃潰瘍や十二指腸潰瘍の治療法が大きく様変わりすることになりました 我が国では 2000 年 11 月に胃潰瘍
Microsoft PowerPoint - __________________________ ppt
 日本ヘリコバクター学会のガイドラインについて教えて下さい ピロリ菌を除菌すると胃癌の予防になるのですか? 2009 年 1 月 日本ヘリコバクター学会よりピロリ菌除菌に関するガイドラインが発表されました それによるとピロリ菌に感染している人はすべて除菌を受けることを強く勧められています (%) 12 8 内視鏡治療後の別の胃癌の発生率 除菌しない場合 : 4.1 %/ 年 除菌できた場合 :1.4
日本ヘリコバクター学会のガイドラインについて教えて下さい ピロリ菌を除菌すると胃癌の予防になるのですか? 2009 年 1 月 日本ヘリコバクター学会よりピロリ菌除菌に関するガイドラインが発表されました それによるとピロリ菌に感染している人はすべて除菌を受けることを強く勧められています (%) 12 8 内視鏡治療後の別の胃癌の発生率 除菌しない場合 : 4.1 %/ 年 除菌できた場合 :1.4
厚生労働省医薬 生活衛生局 情報の概要 355 No. 医薬品等対策情報の概要頁 1 免疫抑制剤の妊婦等に関する禁忌の見直しについて 厚生労働省では, 平成 17 年 10 月から国立成育医療研究センターに 妊娠と薬情報センター を設置し, 相談業務及び調査業務を実施しており, 平成 28 年から集
 355 1. 免疫抑制剤の妊婦等に関する禁忌の見直しについて 3 2. 市販直後調査の対象品目一覧 7 ( 参考資料 )GPSP 省令の改正と製造販売後調査等について 9 この医薬品 医療機器等安全性情報は, 厚生労働省において収集された副作用等の情報を基に, 医薬品 医療機器等のより安全な使用に役立てていただくために, 医療関係者に対して情報提供されるものです 医薬品 医療機器等安全性情報は, 独立行政法人医薬品医療機器総合機構ホームページ
355 1. 免疫抑制剤の妊婦等に関する禁忌の見直しについて 3 2. 市販直後調査の対象品目一覧 7 ( 参考資料 )GPSP 省令の改正と製造販売後調査等について 9 この医薬品 医療機器等安全性情報は, 厚生労働省において収集された副作用等の情報を基に, 医薬品 医療機器等のより安全な使用に役立てていただくために, 医療関係者に対して情報提供されるものです 医薬品 医療機器等安全性情報は, 独立行政法人医薬品医療機器総合機構ホームページ
(別添様式)
 未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会協和発酵キリン株式会社 要要望番号望成分名さ ( 一般名 ) れ販売名た未承認薬 適応医薬品 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) II-23 アモキシシリン水和物パセトシン細粒 10% 未承認薬適応外薬胃潰瘍又は十二指腸潰瘍におけるヘリコバクター
未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会協和発酵キリン株式会社 要要望番号望成分名さ ( 一般名 ) れ販売名た未承認薬 適応医薬品 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) II-23 アモキシシリン水和物パセトシン細粒 10% 未承認薬適応外薬胃潰瘍又は十二指腸潰瘍におけるヘリコバクター
ポプスカイン0.75% 注シリンジ 75mg /10 院 Popscaine 75mg /10 院 / 筒 丸石 薬価 円 / 筒 効 硬膜外麻酔 用 ( 注 )1 回 150mg ( 本剤として20 院 ) までを硬膜外腔に投与 禁 大量出血やショック状態, 注射部位またはその周辺に
 神経系に作用する薬剤 局所麻酔薬 ( エステル型 ) ( プロカイン塩酸塩 ) プロカニン注 0.5% Procanine 25mg /5 院 / 管 光 薬価 92.00 円 /A 効 浸潤麻酔 用 ( 注 )1 回 1000mgの範囲内で使用 ( 基準最高用量 :1 回 1000mg ). 必要に応じアドレナリン ( 濃度 1:10 万 ~ 20 万 ) を添加 禁 メトヘモグロビン血症, 本剤の成分又は安息香酸エステル
神経系に作用する薬剤 局所麻酔薬 ( エステル型 ) ( プロカイン塩酸塩 ) プロカニン注 0.5% Procanine 25mg /5 院 / 管 光 薬価 92.00 円 /A 効 浸潤麻酔 用 ( 注 )1 回 1000mgの範囲内で使用 ( 基準最高用量 :1 回 1000mg ). 必要に応じアドレナリン ( 濃度 1:10 万 ~ 20 万 ) を添加 禁 メトヘモグロビン血症, 本剤の成分又は安息香酸エステル
Microsoft PowerPoint 臨床薬理学会ポスターKFK.ppt [互換モード]
![Microsoft PowerPoint 臨床薬理学会ポスターKFK.ppt [互換モード] Microsoft PowerPoint 臨床薬理学会ポスターKFK.ppt [互換モード]](/thumbs/48/24461773.jpg) 日本人と外国人の薬物動態の違いが日本における承認用量に与える影響 福永悟史, Frank Arnold, 草間真紀子, 小野俊介, 杉山雄一 東京大学大学院薬学系研究科 背景 日本で承認申請される医薬品の申請資料に 海外臨床試験データが含まれることは多い 海外臨床試験データを利用する場合 開発企業またはPMDAの審査では 民族的要因の影響が慎重に検討される 内因性民族的要因を検討する重要な指標として薬物動態がある
日本人と外国人の薬物動態の違いが日本における承認用量に与える影響 福永悟史, Frank Arnold, 草間真紀子, 小野俊介, 杉山雄一 東京大学大学院薬学系研究科 背景 日本で承認申請される医薬品の申請資料に 海外臨床試験データが含まれることは多い 海外臨床試験データを利用する場合 開発企業またはPMDAの審査では 民族的要因の影響が慎重に検討される 内因性民族的要因を検討する重要な指標として薬物動態がある
(Microsoft PowerPoint - \201iweb\214\374\201j2009_11 \222\307\225\342\225i\224\255\224\204\210\304\223\340.PPT)
 平成 21 年 11 月 13 日 Drug Information 平成 21 年 11 月度追補品販売のごのご案内 謹啓時下ますますご清栄のこととお慶び申し上げます 平素は 格別のご高配を賜り 厚く御礼申し上げます さて この度平成 21 年 11 月 13 日付官報にて アムロジピン OD 錠 2.5mg 5mg KRM サルポグレラートサルポグレラート塩酸塩錠 50mg 100mg KRM
平成 21 年 11 月 13 日 Drug Information 平成 21 年 11 月度追補品販売のごのご案内 謹啓時下ますますご清栄のこととお慶び申し上げます 平素は 格別のご高配を賜り 厚く御礼申し上げます さて この度平成 21 年 11 月 13 日付官報にて アムロジピン OD 錠 2.5mg 5mg KRM サルポグレラートサルポグレラート塩酸塩錠 50mg 100mg KRM
緒言
 CERA 2.2 緒言 Page 1 ミルセラ注シリンジ25 μg ミルセラ注シリンジ50 μg ミルセラ注シリンジ75 μg ミルセラ注シリンジ100 μg ミルセラ注シリンジ150 μg ミルセラ注シリンジ200 μg ミルセラ注シリンジ250 μg [ 腎性貧血 ] 第 2 部 CTD の概要 ( サマリー ) 2.2 緒言 中外製薬株式会社 CERA 2.2 緒言 Page 2 目次頁 2.2
CERA 2.2 緒言 Page 1 ミルセラ注シリンジ25 μg ミルセラ注シリンジ50 μg ミルセラ注シリンジ75 μg ミルセラ注シリンジ100 μg ミルセラ注シリンジ150 μg ミルセラ注シリンジ200 μg ミルセラ注シリンジ250 μg [ 腎性貧血 ] 第 2 部 CTD の概要 ( サマリー ) 2.2 緒言 中外製薬株式会社 CERA 2.2 緒言 Page 2 目次頁 2.2
スライド 1
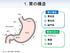 1. 胃の構造 胃の構造 胃底部 胃底部 胃体部 幽門部 胃液の成分ペプシン胃酸粘液 1. 胃の構造 胃の構造と役割 噴門胃底部胃体部幽門部 粘液を分泌胃酸 ( 塩酸 ) ペプシンを分泌胃酸 ( 塩酸 ) ペプシンを分泌ガストリンを血液中に分泌 ペプシン 胃酸 粘液 タンパク質を分解 病原菌の殺菌やペプシノーゲンの活性化 ペプシンや胃酸から胃粘膜を保護 1. 復習 胃の構造と役割 噴門 胃底部 胃体部
1. 胃の構造 胃の構造 胃底部 胃底部 胃体部 幽門部 胃液の成分ペプシン胃酸粘液 1. 胃の構造 胃の構造と役割 噴門胃底部胃体部幽門部 粘液を分泌胃酸 ( 塩酸 ) ペプシンを分泌胃酸 ( 塩酸 ) ペプシンを分泌ガストリンを血液中に分泌 ペプシン 胃酸 粘液 タンパク質を分解 病原菌の殺菌やペプシノーゲンの活性化 ペプシンや胃酸から胃粘膜を保護 1. 復習 胃の構造と役割 噴門 胃底部 胃体部
(別添様式)
 未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名 要望された医薬品 ユーシービージャパン株式会社要望番号 Ⅱ-254.2 成分名 Lacosamide ( 一般名 ) Vimpat 販売名 未承認薬 適応 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) 未承認薬 適応外薬 他の抗てんかん薬で十分な効果が認められないてんかん患者の部分発作
未承認薬 適応外薬の要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項 会社名 要望された医薬品 ユーシービージャパン株式会社要望番号 Ⅱ-254.2 成分名 Lacosamide ( 一般名 ) Vimpat 販売名 未承認薬 適応 外薬の分類 ( 該当するものにチェックする ) 効能 効果 ( 要望された効能 効果について記載する ) 未承認薬 適応外薬 他の抗てんかん薬で十分な効果が認められないてんかん患者の部分発作
<4D F736F F D B A814089FC92F982CC82A8926D82E782B95F E31328C8E5F5F E646F63>
 - 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ 抗悪性腫瘍剤 ( ブルトン型チロシンキナーゼ阻害剤 ) ( 一般名 : イブルチニブ ) 2016 年 12 月 この度 抗悪性腫瘍剤 イムブルビカ カプセル 140 mg ( 以下標記製品 ) につきまして 再発又は難治性のマントル細胞リンパ腫 の効能追加承認を取得したことに伴い
- 医薬品の適正使用に欠かせない情報です 必ずお読み下さい - 効能 効果 用法 用量 使用上の注意 等改訂のお知らせ 抗悪性腫瘍剤 ( ブルトン型チロシンキナーゼ阻害剤 ) ( 一般名 : イブルチニブ ) 2016 年 12 月 この度 抗悪性腫瘍剤 イムブルビカ カプセル 140 mg ( 以下標記製品 ) につきまして 再発又は難治性のマントル細胞リンパ腫 の効能追加承認を取得したことに伴い
(2) レパーサ皮下注 140mgシリンジ及び同 140mgペン 1 本製剤については 最適使用推進ガイドラインに従い 有効性及び安全性に関する情報が十分蓄積するまでの間 本製剤の恩恵を強く受けることが期待される患者に対して使用するとともに 副作用が発現した際に必要な対応をとることが可能な一定の要件
 保医発 0331 第 9 号 平成 29 年 3 月 31 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 ( 公印省略 ) 抗 PCSK9 抗体製剤に係る最適使用推進ガイドラインの策定に伴う留意事項の 一部改正について 抗 PCSK9
保医発 0331 第 9 号 平成 29 年 3 月 31 日 地方厚生 ( 支 ) 局医療課長都道府県民生主管部 ( 局 ) 国民健康保険主管課 ( 部 ) 長都道府県後期高齢者医療主管部 ( 局 ) 後期高齢者医療主管課 ( 部 ) 長 殿 厚生労働省保険局医療課長 ( 公印省略 ) 抗 PCSK9 抗体製剤に係る最適使用推進ガイドラインの策定に伴う留意事項の 一部改正について 抗 PCSK9
日医発第147号(保27)
 日医発第 618 号 ( 保 151) 平成 23 年 9 月 30 日 都道府県医師会長殿 日本医師会長 原中勝征 使用薬剤の薬価 ( 薬価基準 ) 等の一部改正について 平成 23 年 9 月 12 日付け厚生労働省告示第 319 号をもって薬価基準の一部が改正され 告示の日から適用されました 今回の改正は 薬事法の規定に基づき承認を得た新医薬品で 薬価基準への収載希望のあった14 成分 18
日医発第 618 号 ( 保 151) 平成 23 年 9 月 30 日 都道府県医師会長殿 日本医師会長 原中勝征 使用薬剤の薬価 ( 薬価基準 ) 等の一部改正について 平成 23 年 9 月 12 日付け厚生労働省告示第 319 号をもって薬価基準の一部が改正され 告示の日から適用されました 今回の改正は 薬事法の規定に基づき承認を得た新医薬品で 薬価基準への収載希望のあった14 成分 18
 WIC-1 WIC-2 医療機器の保険適用について ( 平成 23 年 10 月収載予定 ) 区分 C1( 新機能 ) 販売名 企業名 保険償還価格 算定方式 補正加算等 外国平均価格との比 8 月 24 日日本メディカルマテリアル外国における 1 Aquala ライナー 77,500 円類似機能区分比較方式補正加算なし了承株式会社販売実績なし コンプリヘンシブ 8 月 24 日バイオメット ジャパン
WIC-1 WIC-2 医療機器の保険適用について ( 平成 23 年 10 月収載予定 ) 区分 C1( 新機能 ) 販売名 企業名 保険償還価格 算定方式 補正加算等 外国平均価格との比 8 月 24 日日本メディカルマテリアル外国における 1 Aquala ライナー 77,500 円類似機能区分比較方式補正加算なし了承株式会社販売実績なし コンプリヘンシブ 8 月 24 日バイオメット ジャパン
審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ]
![審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ] 審査結果 平成 26 年 2 月 7 日 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所 [ 申請年月日 ]](/thumbs/91/105024304.jpg) 審査報告書 平成 26 年 2 月 7 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所
審査報告書 平成 26 年 2 月 7 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりである 記 [ 販売名 ] 1 ヘプタバックス-Ⅱ 2 ビームゲン 同注 0.25mL 同注 0.5mL [ 一般名 ] 組換え沈降 B 型肝炎ワクチン ( 酵母由来 ) [ 申請者名 ] 1 MSD 株式会社 2 一般財団法人化学及血清療法研究所
患者 ID: 氏名 : ピロリ菌外来説明文書 1. ピロリ菌はいつ誰によって発見されたのでしょうかピロリ菌はオーストラリアのウォレンとマーシャルによって 1983 年ヒトの胃の中から発見されました その後 ピロリ菌がヒトの胃に与える様々な影響が解明
 ピロリ菌外来 についてのお知らせ ( 平成 21 年 11 月開設 ) 平成 21 年 11 月より当院消化器内科外来において 保険適応のない方についてピロリ菌の判定 除菌を目的とする ピロリ菌外来を実施してきましたが 平成 26 年 4 月からは 内視鏡検査を 6 ヶ月以内に行った方については 原則すべての患者において保険診療でピロリ菌の除菌ができるようになりました しかしながら 保険診療では除菌治療は
ピロリ菌外来 についてのお知らせ ( 平成 21 年 11 月開設 ) 平成 21 年 11 月より当院消化器内科外来において 保険適応のない方についてピロリ菌の判定 除菌を目的とする ピロリ菌外来を実施してきましたが 平成 26 年 4 月からは 内視鏡検査を 6 ヶ月以内に行った方については 原則すべての患者において保険診療でピロリ菌の除菌ができるようになりました しかしながら 保険診療では除菌治療は
<4D F736F F D DC58F4994C5817A53544C2094E789BA928D5F8AB38ED28CFC834B F94CC94848CB392C78B4C C5292E646F63>
 ステラーラ皮下注 45mg シリンジ 患者向医薬品ガイド 2018 年 7 月更新 この薬は? 販売名 一般名 含有量 (1 シリンジ中 ) ステラーラ皮下注 45mg シリンジ Stelara Subcutaneous Injection 45mg syringe ウステキヌマブ ( 遺伝子組換え ) Ustekinumab(Genetical Recombination) 45mg 患者向医薬品ガイドについて
ステラーラ皮下注 45mg シリンジ 患者向医薬品ガイド 2018 年 7 月更新 この薬は? 販売名 一般名 含有量 (1 シリンジ中 ) ステラーラ皮下注 45mg シリンジ Stelara Subcutaneous Injection 45mg syringe ウステキヌマブ ( 遺伝子組換え ) Ustekinumab(Genetical Recombination) 45mg 患者向医薬品ガイドについて
WIC-2
 WIC-1 WIC-2 No. 銘柄名規格単位会社名成分名承認区分定薬価定方式補正加等 1 イムセラカプセル 0.5mg ジレニアカプセル 0.5mg 0.5mg1 カプセル 0.5mg1 カプセル 田辺三菱製薬ノバルティスファーマ 新医薬品一覧表 ( 平成 23 年 11 月 25 日収載予定 ) フィンゴリモド塩酸塩新有効成分 8,172.00 円類似薬効比較方式 (Ⅰ) 有用性加 (Ⅰ) 8,172.00
WIC-1 WIC-2 No. 銘柄名規格単位会社名成分名承認区分定薬価定方式補正加等 1 イムセラカプセル 0.5mg ジレニアカプセル 0.5mg 0.5mg1 カプセル 0.5mg1 カプセル 田辺三菱製薬ノバルティスファーマ 新医薬品一覧表 ( 平成 23 年 11 月 25 日収載予定 ) フィンゴリモド塩酸塩新有効成分 8,172.00 円類似薬効比較方式 (Ⅰ) 有用性加 (Ⅰ) 8,172.00
要望番号 ;Ⅱ-286 未承認薬 適応外薬の要望 ( 別添様式 ) 1. 要望内容に関連する事項 要望者 ( 該当するものにチェックする ) 学会 ( 学会名 ; 特定非営利活動法人日本臨床腫瘍学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 優先順位 33 位 ( 全 33 要望
 未承認薬 適応外薬の要望 ( 別添様式 ) 1. 要望内容に関連する事項 要望者 ( 該当するものにチェックする ) 学会 ( 学会名 ; 特定非営利活動法人日本臨床腫瘍学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 優先順位 33 位 ( 全 33 要望中 ) 要望する医薬品 成 分 名 ( 一般名 ) 販 売 名 会 社 名 国内関連学会 ロペラミドロペミンヤンセンファーマ株式会社
未承認薬 適応外薬の要望 ( 別添様式 ) 1. 要望内容に関連する事項 要望者 ( 該当するものにチェックする ) 学会 ( 学会名 ; 特定非営利活動法人日本臨床腫瘍学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 優先順位 33 位 ( 全 33 要望中 ) 要望する医薬品 成 分 名 ( 一般名 ) 販 売 名 会 社 名 国内関連学会 ロペラミドロペミンヤンセンファーマ株式会社
肛門用薬2.5mg 1 錠 PTP 100T その他の泌尿生殖器官及び新薬価基準収載品目 ほくやく DI 室平成 26 年 4 月 17 日官報告示 011(611)1099 の他の循環器官用薬分類そメーカー 商品名 成分名 規格 薬価 ( 円 ) 効能 効果 用法 用量 包装 発売日
 精神神経用剤新薬価基準収載品目 ほくやく DI 室平成 26 年 4 月 17 日官報告示 011(611)1099 分類メーカー商品名成分名規格薬価 ( 円 ) 効能 効果用法 用量包装発売日 抗てんかん剤協和発酵キリン トピナ細粒 10% 871139 1139008C1020 トピラマート 10% 1g 191.90 抗てんかん剤 他の抗てんかん薬で十分な効果が認められないてんかん患者の部分発作
精神神経用剤新薬価基準収載品目 ほくやく DI 室平成 26 年 4 月 17 日官報告示 011(611)1099 分類メーカー商品名成分名規格薬価 ( 円 ) 効能 効果用法 用量包装発売日 抗てんかん剤協和発酵キリン トピナ細粒 10% 871139 1139008C1020 トピラマート 10% 1g 191.90 抗てんかん剤 他の抗てんかん薬で十分な効果が認められないてんかん患者の部分発作
要望番号 ;Ⅱ 未承認薬 適応外薬の要望 ( 別添様式 1) 1. 要望内容に関連する事項 要望 者 ( 該当するものにチェックする ) 優先順位 学会 ( 学会名 ; 日本ペインクリニック学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 2 位 ( 全 4 要望中 )
 未承認薬 適応外薬の要望 ( 別添様式 1) 1. 要望内容に関連する事項 要望 者 ( 該当するものにチェックする ) 優先順位 学会 ( 学会名 ; 日本ペインクリニック学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 2 位 ( 全 4 要望中 ) 成分名 ( 一般名 ) 塩酸リドカイン 販売名 0.5%/1%/2% キシロカイン 要望する医薬品要望内容 会社名 国内関連学会
未承認薬 適応外薬の要望 ( 別添様式 1) 1. 要望内容に関連する事項 要望 者 ( 該当するものにチェックする ) 優先順位 学会 ( 学会名 ; 日本ペインクリニック学会 ) 患者団体 ( 患者団体名 ; ) 個人 ( 氏名 ; ) 2 位 ( 全 4 要望中 ) 成分名 ( 一般名 ) 塩酸リドカイン 販売名 0.5%/1%/2% キシロカイン 要望する医薬品要望内容 会社名 国内関連学会
使用上の注意 1. 慎重投与 ( 次の患者には慎重に投与すること ) 1 2X X 重要な基本的注意 1TNF 2TNF TNF 3 X - CT X 4TNFB HBsHBcHBs B B B B 5 6TNF 7 8dsDNA d
 2015 5 7 201410 28 TNF 阻害薬 TNFFab シムジア 皮下注 200mg シリンジ Cimzia 200mg Syringe for S.C. Injection セルトリズマブペゴル ( 遺伝子組換え ) 製剤 873999 22400AMX01488000 20132 20133 20155 20079 警告 1. 2. 1 2 X - CT 3. TNF 4. 1 禁忌
2015 5 7 201410 28 TNF 阻害薬 TNFFab シムジア 皮下注 200mg シリンジ Cimzia 200mg Syringe for S.C. Injection セルトリズマブペゴル ( 遺伝子組換え ) 製剤 873999 22400AMX01488000 20132 20133 20155 20079 警告 1. 2. 1 2 X - CT 3. TNF 4. 1 禁忌
<4D F736F F D2082A8926D82E782B995B68F E834E838D838A E3132>
 医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能 効果 用法 用量 使用上の注意 改訂のお知らせ 2013 年 12 月 東和薬品株式会社 このたび 平成 25 年 8 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 25 年 11 月 29 日付にて 下記の内容で承認されました また 使用上の注意 を改訂致しましたので 併せてお知らせ申し上げます
医薬品の適正使用に欠かせない情報です 必ずお読み下さい 効能 効果 用法 用量 使用上の注意 改訂のお知らせ 2013 年 12 月 東和薬品株式会社 このたび 平成 25 年 8 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 25 年 11 月 29 日付にて 下記の内容で承認されました また 使用上の注意 を改訂致しましたので 併せてお知らせ申し上げます
PT51_p69_77.indd
 臨床講座 特発性血小板減少性紫斑病 ITP の登場によりその危険性は下がりました また これまで 1 ヘリコバクター ピロリの除菌療法 治療の中心はステロイドであり 糖尿病 不眠症 胃炎 ヘリコバクター ピロリ ピロリ菌 は 胃炎や胃 十二指 満月様顔貌と肥満などに悩む患者が多かったのですが 腸潰瘍に深く関わっています ピロリ菌除菌療法により約 受容体作動薬によりステロイドの減量 6 割の患者で 血小板数が
臨床講座 特発性血小板減少性紫斑病 ITP の登場によりその危険性は下がりました また これまで 1 ヘリコバクター ピロリの除菌療法 治療の中心はステロイドであり 糖尿病 不眠症 胃炎 ヘリコバクター ピロリ ピロリ菌 は 胃炎や胃 十二指 満月様顔貌と肥満などに悩む患者が多かったのですが 腸潰瘍に深く関わっています ピロリ菌除菌療法により約 受容体作動薬によりステロイドの減量 6 割の患者で 血小板数が
<4D F736F F D2082A8926D82E782B995B68F D815B838B4E618FF931306D E3131>
 医薬品の適正使用に欠かせない情報です 必ずお読みください 効能 効果 用法 用量 追加及び 使用上の注意 改訂のお知らせ 2012 年 11 月 東和薬品株式会社 このたび 平成 24 年 5 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 24 年 11 月 19 日付にて 下記の内容で承認されました また 使用上の注意 の項も改訂致しましたので 併せてお知らせ申し上げます
医薬品の適正使用に欠かせない情報です 必ずお読みください 効能 効果 用法 用量 追加及び 使用上の注意 改訂のお知らせ 2012 年 11 月 東和薬品株式会社 このたび 平成 24 年 5 月に承認事項一部変更承認申請をしていました弊社上記製品の 効能 効果 用法 用量 追加が平成 24 年 11 月 19 日付にて 下記の内容で承認されました また 使用上の注意 の項も改訂致しましたので 併せてお知らせ申し上げます
医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など ) 医薬品候補物質のスクリーニン
 特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
特定保健用食品の表示許可制度専門調査会 (H23.2.28) 資料 5 再審査制度 再評価制度について 厚生労働省医薬食品局審査管理課 医薬品の基礎研究から承認審査 市販後までの主なプロセス 基礎研究 非臨床試験 動物試験等 品質の評価安全性の評価有効性の評価 候補物質の合成方法等を確立 最適な剤型の設計 一定の品質を確保するための規格及び試験方法などの確立 有効期間等の設定 ( 長期安定性試験など
日本内科学会雑誌第98巻第12号
 表 1. 喘息の長期管理における重症度対応段階的薬物療法 重症度 長期管理薬 : 連用 : 考慮 発作時 ステップ 1 軽症間欠型 喘息症状がやや多い時 ( 例えば 1 月に 1 ~2 回 ), 血中 喀痰中に好酸球増加のある時は下記のいずれか 1 つの投与を考慮 吸入ステロイド薬 ( 最低用量 ) テオフィリン徐放製剤 ロイコトリエン拮抗薬 抗アレルギー薬 短時間作用性吸入 β2 刺激薬または短時間作用性経口
表 1. 喘息の長期管理における重症度対応段階的薬物療法 重症度 長期管理薬 : 連用 : 考慮 発作時 ステップ 1 軽症間欠型 喘息症状がやや多い時 ( 例えば 1 月に 1 ~2 回 ), 血中 喀痰中に好酸球増加のある時は下記のいずれか 1 つの投与を考慮 吸入ステロイド薬 ( 最低用量 ) テオフィリン徐放製剤 ロイコトリエン拮抗薬 抗アレルギー薬 短時間作用性吸入 β2 刺激薬または短時間作用性経口
<4D F736F F D DC58F4994C5817A54524D5F8AB38ED28CFC88E396F B CF8945C8CF889CA92C789C1816A5F3294C52E646
 患者向医薬品ガイド トレムフィア皮下注 100mg シリンジ 2018 年 11 月更新 この薬は? 販売名 一般名 含有量 (1 シリンジ中 ) トレムフィア皮下注 100mgシリンジ Tremfya Subcutaneous Injection 100mg syringe グセルクマブ ( 遺伝子組換え ) Guselkumab(Genetical Recombination) 100mg 患者向医薬品ガイドについて
患者向医薬品ガイド トレムフィア皮下注 100mg シリンジ 2018 年 11 月更新 この薬は? 販売名 一般名 含有量 (1 シリンジ中 ) トレムフィア皮下注 100mgシリンジ Tremfya Subcutaneous Injection 100mg syringe グセルクマブ ( 遺伝子組換え ) Guselkumab(Genetical Recombination) 100mg 患者向医薬品ガイドについて
スイッチ OTC 医薬品の候補となる成分についての要望 に対する見解 1. 要望内容に関連する事項 組織名日本消化器病学会 要望番号 H28-11 H28-12 H28-16 成分名 ( 一般名 ) オメプラゾール ランソプラゾール ラベプラゾールオメプラゾール : 胸やけ ( 胃酸の逆流 ) 胃痛
 スイッチ OTC 医薬品の候補となる成分についての要望 に対する見解 1. 要望内容に関連する事項 組織名日本消化器病学会 要望番号 H28-11 H28-12 H28-16 成分名 ( 一般名 ) オメプラゾール ランソプラゾール ラベプラゾールオメプラゾール : 胸やけ ( 胃酸の逆流 ) 胃痛 もたれ むかつき 要望内容 効能 効果 ランソプラゾール : 繰り返しおこる胸やけ ( 食道への胃酸の逆流
スイッチ OTC 医薬品の候補となる成分についての要望 に対する見解 1. 要望内容に関連する事項 組織名日本消化器病学会 要望番号 H28-11 H28-12 H28-16 成分名 ( 一般名 ) オメプラゾール ランソプラゾール ラベプラゾールオメプラゾール : 胸やけ ( 胃酸の逆流 ) 胃痛 もたれ むかつき 要望内容 効能 効果 ランソプラゾール : 繰り返しおこる胸やけ ( 食道への胃酸の逆流
議題 3. ファイザー の依頼による白血病患者を対象とした SKI-606 の第 Ⅲ 相試験 ( 整理番号 :476) 議題 4. 武田バイオ開発センター の依頼による第 Ⅰ 相試験 ( 整理番号 : 487) 議題 5. ノバルティスファーマ の依頼による肺動脈性肺高血圧症患者を対象とした QTI
 平成 25 年度第 7 回浜松医科大学医学部附属病院治験審査委員会 会議の記録の概要 開催日時平成 25 年 10 月 3 日 ( 木 )17:00~19:00 開催場所浜松医科大学サテライトオフィス ( プレスタワー 11 階 ) 管理棟第一会議室 ( 会場を web 会議システムで中継して実施 ) 出席委員名主会場 : 梅村和夫 白井直人 山崎勝康 鈴木理久 杉田豊 可知茂男 副会場 : 大橋知世
平成 25 年度第 7 回浜松医科大学医学部附属病院治験審査委員会 会議の記録の概要 開催日時平成 25 年 10 月 3 日 ( 木 )17:00~19:00 開催場所浜松医科大学サテライトオフィス ( プレスタワー 11 階 ) 管理棟第一会議室 ( 会場を web 会議システムで中継して実施 ) 出席委員名主会場 : 梅村和夫 白井直人 山崎勝康 鈴木理久 杉田豊 可知茂男 副会場 : 大橋知世
451) 議題 3. ファイザー の依頼による白血病患者を対象とした SKI-606 の第 Ⅲ 相試験 ( 整理番号 :476) 議題 4. 武田バイオ開発センター の依頼による第 Ⅰ 相試験 ( 整理番号 : 487) 議題 5. ノバルティスファーマ の依頼による肺動脈性肺高血圧症患者を対象とし
 平成 25 年度第 6 回浜松医科大学医学部附属病院治験審査委員会 会議の記録の概要 開催日時平成 25 年 9 月 5 日 ( 木 )17:00~19:00 開催場所浜松医科大学サテライトオフィス ( プレスタワー 11 階 ) 管理棟第一会議室 ( 会場を web 会議システムで中継して実施 ) 出席委員名主会場 : 白井直人 鈴木理久 杉田豊 鈴木敏弘 可知茂男 副会場 : 平川聡史 坂口孝宣
平成 25 年度第 6 回浜松医科大学医学部附属病院治験審査委員会 会議の記録の概要 開催日時平成 25 年 9 月 5 日 ( 木 )17:00~19:00 開催場所浜松医科大学サテライトオフィス ( プレスタワー 11 階 ) 管理棟第一会議室 ( 会場を web 会議システムで中継して実施 ) 出席委員名主会場 : 白井直人 鈴木理久 杉田豊 鈴木敏弘 可知茂男 副会場 : 平川聡史 坂口孝宣
査を実施し 必要に応じ適切な措置を講ずること (2) 本品の警告 効能 効果 性能 用法 用量及び使用方法は以下のとお りであるので 特段の留意をお願いすること なお その他の使用上の注意については 添付文書を参照されたいこと 警告 1 本品投与後に重篤な有害事象の発現が認められていること 及び本品
 薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
薬食機参発 0918 第 4 号薬食安発 0918 第 1 号 ( 別記 ) 殿 テムセル HS 注については 本日 造血幹細胞移植後の急性移植片対宿主病 を効能 効果又は性能として承認したところですが 本品については 治験症例が限られていること 重篤な不具合が発現するリスクがあることから その 使用に当たっての留意事項について 御了知いただくとともに 貴会会員への周知方よろしくお願いします なお
減量・コース投与期間短縮の基準
 用法 用量 通常 成人には初回投与量 (1 回量 ) を体表面積に合せて次の基準量とし 朝食後および夕食後の 1 日 2 回 28 日間連日経口投与し その後 14 日間休薬する これを 1 クールとして投与を繰り返す ただし 本剤の投与によると判断される臨床検査値異常 ( 血液検査 肝 腎機能検査 ) および消化器症状が発現せず 安全性に問題がない場合には休薬を短縮できるが その場合でも少なくとも
用法 用量 通常 成人には初回投与量 (1 回量 ) を体表面積に合せて次の基準量とし 朝食後および夕食後の 1 日 2 回 28 日間連日経口投与し その後 14 日間休薬する これを 1 クールとして投与を繰り返す ただし 本剤の投与によると判断される臨床検査値異常 ( 血液検査 肝 腎機能検査 ) および消化器症状が発現せず 安全性に問題がない場合には休薬を短縮できるが その場合でも少なくとも
スライド 1
 1/5 PMDA からの医薬品適正使用のお願い ( 独 ) 医薬品医療機器総合機構 No.6 2012 年 1 月 ラミクタール錠 ( ラモトリギン ) の重篤皮膚障害と用法 用量遵守 早期発見について ラミクタール錠は 用法 用量 を遵守せず投与した場合に皮膚障害の発現率が高くなることが示されている ( 表 1 参照 ) ため 用法 用量 を遵守することが平成 20 年 10 月の承認時より注意喚起されています
1/5 PMDA からの医薬品適正使用のお願い ( 独 ) 医薬品医療機器総合機構 No.6 2012 年 1 月 ラミクタール錠 ( ラモトリギン ) の重篤皮膚障害と用法 用量遵守 早期発見について ラミクタール錠は 用法 用量 を遵守せず投与した場合に皮膚障害の発現率が高くなることが示されている ( 表 1 参照 ) ため 用法 用量 を遵守することが平成 20 年 10 月の承認時より注意喚起されています
Microsoft Word - 医薬品情報_ コピー
 2018 年 6 月号 医薬品情報 2018 年 5 月 25 日発行 1. 採用医薬品 5 月薬事委員会における採用 2018 年 5 月 30 日 ( 水 ) より処方して下さい 1 テセントリク点滴静注 1200mg --------------------------------------- 1 2 ネキシウム懸濁用顆粒分包 10mg 20mg --------------------------
2018 年 6 月号 医薬品情報 2018 年 5 月 25 日発行 1. 採用医薬品 5 月薬事委員会における採用 2018 年 5 月 30 日 ( 水 ) より処方して下さい 1 テセントリク点滴静注 1200mg --------------------------------------- 1 2 ネキシウム懸濁用顆粒分包 10mg 20mg --------------------------
( 別添 ) 御意見 該当箇所 一般用医薬品のリスク区分 ( 案 ) のうち イブプロフェン ( 高用量 )(No.4) について 意見内容 <イブプロフェン ( 高用量 )> 本剤は 低用量製剤 ( 最大 400mg/ 日 ) と比べても製造販売後調査では重篤な副作用の報告等はない 一方で 今まで
 医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第三十六条の七第一項第一号及び第二号の規定に基づき厚生労働大臣が指定する第一類医薬品及び第二類医薬品 の一部改正に係る意見の募集について に対して寄せられた御意見について 厚生労働省医薬 生活衛生局安全対策課 1. 意見募集期間 : 平成 28 年 6 月 3 日 ( 金 ) から平成 28 年 7 月 2 日 ( 土 ) まで 2. 提出意見数
医薬品 医療機器等の品質 有効性及び安全性の確保等に関する法律第三十六条の七第一項第一号及び第二号の規定に基づき厚生労働大臣が指定する第一類医薬品及び第二類医薬品 の一部改正に係る意見の募集について に対して寄せられた御意見について 厚生労働省医薬 生活衛生局安全対策課 1. 意見募集期間 : 平成 28 年 6 月 3 日 ( 金 ) から平成 28 年 7 月 2 日 ( 土 ) まで 2. 提出意見数
シダキュアスギ舌下錠 2,000JAU 5,000JAU に係る医薬品リスク管理計画書 (RMP) の概要 販売名 シダキュアスギ舌下錠 2,000JAU,5,000JAU 有効成分 スギ花粉エキス原末 承認取得者名 鳥居薬品株式会社 薬効分類 提出年月 平成 30 年 8 月 1.1.
 シダキュアスギ舌下錠 2,000JAU シダキュアスギ舌下錠 5,000JAU に係る医薬品リスク管理計画書 本資料に記載された情報に関する権利及び内容についての責任は 鳥居薬品株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません 鳥居薬品株式会社 1 シダキュアスギ舌下錠 2,000JAU 5,000JAU に係る医薬品リスク管理計画書 (RMP) の概要 販売名 シダキュアスギ舌下錠
シダキュアスギ舌下錠 2,000JAU シダキュアスギ舌下錠 5,000JAU に係る医薬品リスク管理計画書 本資料に記載された情報に関する権利及び内容についての責任は 鳥居薬品株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません 鳥居薬品株式会社 1 シダキュアスギ舌下錠 2,000JAU 5,000JAU に係る医薬品リスク管理計画書 (RMP) の概要 販売名 シダキュアスギ舌下錠
 エムプリシティ点滴静注用 300 mg エムプリシティ点滴静注用 400 mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はブリストル マイヤーズスクイブ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ブリストル マイヤーズスクイブ株式会社 医薬品リスク管理計画書 平成 29 年 10 月 16 日 独立行政法人医薬品医療機器総合機構理事長殿
エムプリシティ点滴静注用 300 mg エムプリシティ点滴静注用 400 mg に係る医薬品リスク管理計画書 本資料に記載された情報に係る権利及び内容についての責任はブリストル マイヤーズスクイブ株式会社にあります 当該情報を適正使用以外の営利目的に利用することはできません ブリストル マイヤーズスクイブ株式会社 医薬品リスク管理計画書 平成 29 年 10 月 16 日 独立行政法人医薬品医療機器総合機構理事長殿
審査報告書 平成 29 年 10 月 13 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販売名 ] 1ネキシウムカプセル 10 mg 2 同カプセル 20 mg 3ネキシウム懸濁用顆粒分包 10 mg
![審査報告書 平成 29 年 10 月 13 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販売名 ] 1ネキシウムカプセル 10 mg 2 同カプセル 20 mg 3ネキシウム懸濁用顆粒分包 10 mg 審査報告書 平成 29 年 10 月 13 日 独立行政法人医薬品医療機器総合機構 る 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりであ 記 [ 販売名 ] 1ネキシウムカプセル 10 mg 2 同カプセル 20 mg 3ネキシウム懸濁用顆粒分包 10 mg](/thumbs/91/105640160.jpg) 審議結果報告書 平成 29 年 11 月 16 日医薬 生活衛生局医薬品審査管理課 [ 販 売 名 ] ネキシウムカプセル10mg 同カプセル20mg 同懸濁用顆粒分包 10mg 同懸濁用顆粒分包 20mg [ 一 般 名 ] エソメプラゾールマグネシウム水和物 [ 申請者名 ] アストラゼネカ株式会社 [ 申請年月日 ] 平成 28 年 12 月 20 日 [ 審議結果 ] 平成 29 年 11
審議結果報告書 平成 29 年 11 月 16 日医薬 生活衛生局医薬品審査管理課 [ 販 売 名 ] ネキシウムカプセル10mg 同カプセル20mg 同懸濁用顆粒分包 10mg 同懸濁用顆粒分包 20mg [ 一 般 名 ] エソメプラゾールマグネシウム水和物 [ 申請者名 ] アストラゼネカ株式会社 [ 申請年月日 ] 平成 28 年 12 月 20 日 [ 審議結果 ] 平成 29 年 11
(別添様式)
 未承認薬 適応外薬要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項会サノフィ株式会社社 名 要望番号 Ⅲ-3-19 成分名 ( 一般名 ) フルダラビンリン酸エステル 販売名フルダラ静注用 50mg 要望された医薬品 未承認薬 適 応外薬分類 ( 該当するもにチェックする ) 未承認薬 2009 年 4 月以降に FDA 又は EMA で承認されたが 国内で承認されていない医薬品
未承認薬 適応外薬要望に対する企業見解 ( 別添様式 ) 1. 要望内容に関連する事項会サノフィ株式会社社 名 要望番号 Ⅲ-3-19 成分名 ( 一般名 ) フルダラビンリン酸エステル 販売名フルダラ静注用 50mg 要望された医薬品 未承認薬 適 応外薬分類 ( 該当するもにチェックする ) 未承認薬 2009 年 4 月以降に FDA 又は EMA で承認されたが 国内で承認されていない医薬品
