2017 年 9 月 20 日 13:00~17:00 平成 29 年度第 1 回 ( 第 11 回 ) 臨床研究 治験活性化協議会独立行政法人国立病院機構東京医療センター 3 階大会議室 疾患登録システム ( 患者レジストリ ) について 国立研究開発法人国立がん研究センター東病院岡本渉 大津敦
|
|
|
- もえり つちかね
- 7 years ago
- Views:
Transcription
1 2017 年 9 月 20 日 13:00~17:00 平成 29 年度第 1 回 ( 第 11 回 ) 臨床研究 治験活性化協議会独立行政法人国立病院機構東京医療センター 3 階大会議室 疾患登録システム ( 患者レジストリ ) について 国立研究開発法人国立がん研究センター東病院岡本渉 大津敦
2
3 日本再興戦略改訂 2015( 平成 27 年 6 月 30 日閣議決定 ) 抜粋 (3) 新たに講ずべき具体的な施策 8 クリニカル イノベーション ネットワークの構築 ( 疾患登録情報を活用した臨床開発インフラの整備 ) 国立高度専門医療研究センター (NC) が構築する疾患登録システムなど各種疾患登録情報を活用して NC 臨床研究中核病院 独立行政法人医薬品医療機器総合機 (PMDA) 国立研究開発法人日本医療研究開発機構などを中核とするネットワークを構築し 産学連携による治験コンソーシアムを形成 日本再興戦略 2016( 平成 28 年 6 月 2 日閣議決定 ) 抜粋 第 2 具体的施策 2. 世界最先端の健康立国へ Ⅳ) 日本発の優れた医薬品 医療機器等の開発 事業化 グローバル市場獲得 国際貢献 2 クリニカル イノベーション ネットワークの構築等によるイノベーション推進
4
5
6
7
8 CIN の推進に向けての特別研究班からの提言 国立高度専門医療研究センター (NC) 等において構築する疾患登録システム ( 患者レジストリ ) を基盤とした 新たな治験 臨床研究の推進方策に関する研究 (H27- 特別 - 指定 -018) CIN 推進の仕組み 疾患登録情報の活用を進めるために NC 以外も含め広く患者レジストリ情報の収集 分析 倫理的課題 個人情報保護への対応 Good Registry Practice 登録項目の標準化 医療情報の治験 臨床研究への利活用の仕組み 産学の連携 企業の参加しやすいコンソーシアムのあり方 ワンストップ サービスを実現する中央支援センター ( 仮称 ) の構築 具体的な解決方策 課題解決に向けたレジストリ 登録システムの構築 CIN-WG 等により実施 必要な疾患領域を考慮して 以下の課題抽出とシステム構築 治験対照群としての活用に資するレジストリ 製造販売後調査 安全性対策に資するレジストリ
9 クリニカル イノベーション ネットワーク (CIN) の進捗 がん環CIN-WG循器CIN-WG精CIN-WG の設置 神 神際経CIN-WG国CIN-WG成育寿CIN-WG長病CIN-WG難CIN-WG 治験 臨床研究における患者レジストリのあり方 倫理面 個人情報保護への対応 情報登録システムのあり方 自然暦調査 治験対照群として患者登録システム 製薬企業の要望 各 WG の進捗管理 助言 論点整理の結果を提供 CIN 特別研究班 (H27 ー特別ー指定ー 018) 6NC 医薬基盤 健康 栄養研より参画 外メーカーの国内開国内開発の活性化海発呼び込みクリニカル イノベーション ネットワーク (CIN) 疾患登録情報を活用した臨床開発インフラの整備 ( 2020 ジャパンチャレンジ プロジェクト 10 日本再興戦略改訂 2015 日本再興戦略 2016 ) 特別研究班からの提言CIN 推進の仕組み疾患登録情報の活用を進めるために NC 以外も含め広く患者レジストリ情報の収集 分析 倫理的課題 個人情報保護への対応 Good Registry Practice 登録項目の標準化 医療情報の治験 臨床研究への利活用の仕組み産学の連携 企業の参加しやすいコンソーシアムのあり方ワンストップ サービスを実現する中央支援センター ( 仮称 ) の構築具体的な登録システムの構築課題解決に向けたレジストリ 登録システムの構築 治験対照群としての活用に資するレジストリ 製造販売後調査 安全性対策に資するレジストリ 国立研究開発法人日本医療研究開発機構による事業 ( 平成 28 年度 ) 臨床研究 治験推進研究事業 1 2. 疾患登録システム ( 患者レジストリ ) を活用した臨床研究 医師主導治験の推進 (1 課題 5,000 万円 NCC2 件 NCNP1 件 九州大学 1 件 岐阜大学 1 件 ) 1 3. 医薬品開発に利活用する疾患登録システム ( 患者レジストリ ) の研究開発 (1 課題 10,000 万円 NCC1 件 NCNP1 件 名古屋大学 1 件 ) 2 1. 疾患登録システム及び治験ネットワークの連携等に関する研究 (1 課題 1,000 万円 NCNP1 件 ) 医療機器開発推進研究事業 1. 医療機器開発に利活用する疾患登録システム ( 患者レジストリ ) の研究開発 (1 課題 10,000 万円脳神経外科学会 1 件 ) 医薬品等規制調和 評価研究事業 患者レジストリーデータを用い 臨床開発の効率化を目指すレギュラトリーサイエンス研究 (1 課題 2,000 万円群馬大学 1 件 ) ほか疾患レジストリ研究多数あり
10 中央支援部門 ( 仮称 ) 構想 CIN に基づく治験 臨床研究を迅速に実施することを支援する部門 疾患レジストリの利活用促進のため臨床開発 疾患レジストリーに関する知識 経験 人材を集約し レジストリー運営のあり方 手続きの簡素化 迅速化 企業利活用の促進等 CIN を推進する 開発者に対して コーディネート機能を有するワンストップサービスの提供を行う 国 事務局運営 共通基盤構築に係る費用拠出 中央支援部門 ( 仮称 ) 製薬企業等コンソーシアム ニーズの反映 中枢機能 ワンストップ サービスの提供 企業ニーズ把握 開発戦略等受付 疾患等の情報提供 広報治療法開発成果による還元 PMDA 製薬企業等 レギュラトリーサイエンス研究 情報提供依頼 対価支払 治験実施可能性調査 治験リクルーティング 治験対照群検討 情報提供 審査支援 (CDISC 規格等でのデータ提供等 ) 疾患登録情報の可視化 リスト化 疾患レジストリの運営調整 情報提供 構築支援 ( 法的対応 SOP 整備 ヘ ストフ ラクティス提示等 ) 治験ネットワーク 疾患レジストリ共通基盤のあり方検討 構築 コーディネート業務 ニーズ把握 ( 国民の声 ) 構成する要員 ( 案 ) 医師 薬剤師 治験事務局 治験コーディネーター 臨床統計家 レギュラトリー サイエンス データサイエンス 医療情報 ICT 倫理 知的財産権等の法律関連 国民 A B NC 中核病院 X 学会 X がん登録難病登録 臨床研究中核病院等 一般病院等 診療所 患者 将来的にゲノム医療 バイオリソース IRUDとの連携 Precision medicineへ向けたコホート研究
11 製薬協医機連 FIRM 厚生労働省 AMED PMDA CIN-WG レジストリ構築 中村班神経 筋疾患 ( 筋ジス ) 祖父江班 ALS 大津班がん領域 クリニカル イノベーション ネットワーク推進支援事業 CIN 構想の加速 推進を目指したレジストリ情報統合拠点の構築研究開発代表者 : 國土典宏 (NCGM) AMED CIN 研究班 ( レジストリ関連 ) 嘉山班脳神経外科医療機器 医薬品等規制調和 評価研究事業患者レジストリーデータを活用した臨床開発効率化のための新たな臨床研究デザインの開発研究開発代表者 : 林邦彦 ( 群馬大学 ) 臨床研究 治験推進研究事業疾患登録システムの有効活用によるクリニカルイノベーションネットワーク構想の推進方策に関する研究研究開発代表者 : 武田伸一 (NCNP) CIN 推進拠点 新たな試験デザイン信頼性基準 難治性疾患実用化研究事業希少難治性疾患克服のための 生きた難病レジストリ の設計と構築研究開発代表者 : 松田文彦 ( 京都大学 ) CIN 推進の仕組み横断的課題
12 製薬協医機連 FIRM 厚生労働省 AMED PMDA CIN-WG レジストリ構築 中村班神経 筋疾患 ( 筋ジス ) 祖父江班 ALS 大津班がん領域 クリニカル イノベーション ネットワーク推進支援事業 CIN 構想の加速 推進を目指したレジストリ情報統合拠点の構築研究開発代表者 : 國土典宏 (NCGM) AMED CIN 研究班 ( レジストリ関連 ) 嘉山班脳神経外科医療機器 医薬品等規制調和 評価研究事業患者レジストリーデータを活用した臨床開発効率化のための新たな臨床研究デザインの開発研究開発代表者 : 林邦彦 ( 群馬大学 ) 臨床研究 治験推進研究事業疾患登録システムの有効活用によるクリニカルイノベーションネットワーク構想の推進方策に関する研究研究開発代表者 : 武田伸一 (NCNP) CIN 推進拠点 新たな試験デザイン信頼性基準 難治性疾患実用化研究事業希少難治性疾患克服のための 生きた難病レジストリ の設計と構築研究開発代表者 : 松田文彦 ( 京都大学 ) CIN 推進の仕組み横断的課題
13 AMED 武田班における検討課題 既存及び構築中の疾患登録システムに係る情報収集及び情報公開に向けた検討 疾患登録システムにかかる情報を収集し ウェブサイトなどで情報が一元的に収集 可視化 ワンストップ機能としての レジストリのリスト化提案 疾患登録システム及び治験ネットワークの連携等に関する検討 治験 臨床研究実施基盤との連携を進める上での課題を抽出 問題解決 CIN における臨床研究中核病院等の役割について疾患登録システムの活用等 レジストリとネットワークのアンケート実施 個人情報保護法に対応した企業等における疾患登録システムの活用に関する検討 個人情報保護法の実施も踏まえて 患者への説明 同意の方策について検討 国民自身 ( 健常者 患者等 ) のレジストリ情報の提供に関する意識調査 統合指針改正案へのパブコメ 課題の抽出 疾患登録システムの活用に係る費用負担のあり方に関する検討 疾患登録システムや中央支援部門 ( 仮 ) などの運営の継続性踏まえ 利活用者による費用負担のあり方 運営に対する開発者の関わり方 利益相反に関する課題の整理 製薬工業協会へのアンケート実施中
14 製薬協医機連 FIRM 厚生労働省 AMED PMDA CIN-WG レジストリ構築 中村班神経 筋疾患 ( 筋ジス ) 祖父江班 ALS 大津班がん領域 クリニカル イノベーション ネットワーク推進支援事業 CIN 構想の加速 推進を目指したレジストリ情報統合拠点の構築研究開発代表者 : 國土典宏 (NCGM) 医薬品等規制調和 評価研究事業患者レジストリーデータを活用した臨床開発効率化のための新たな臨床研究デザインの開発研究開発代表者 : 林邦彦 ( 群馬大学 ) AMED CIN 研究班 ( レジストリ関連 ) 嘉山班脳神経外科医療機器 CIN 推進拠点 臨床研究 治験推進研究事業疾患登録システムの有効活用によるクリニカルイノベーションネットワーク構想の推進方策に関する研究研究開発代表者 : 武田伸一 (NCNP) 新たな試験デザイン信頼性基準 CIN 推進の仕組み横断的課題 難治性疾患実用化研究事業希少難治性疾患克服のための 生きた難病レジストリ の設計と構築研究開発代表者 : 松田文彦 ( 京都大学 )
15 患者レジストリを利用した臨床開発の促進と効率化 臨床開発の促進と効率化のため 患者レジストリ利用による 臨床研究デザインと解析法 患者レジストリ利用に対する 信頼性基準の考え方 難病 希少疾患 医療機器 手術など 通常のランダム化比較試験実施困難 1-arm 試験では結果解釈が困難 事後的外部対照データは収集困難で比較可能性が低い 患者登録データを利用した臨床開発の海外動向 2016 年 11 月 15 日 患者レジストリーデータを活用した臨床開発効率化のための新たな臨床研究デザインの開発 研究班会議資料一部改変
16 レジストリーデータの信頼性保証に関する分担班 患者レジストリデータを医薬品等の承認申請資料等として活用する場合におけるデータの信頼性担保に関する基本的考え方 ( 案 ) 構成国立がん研究センター 柴田大朗 ( 分担班責任者 ) 国立循環器病研究センター 山本晴子群馬大学ビッグデータ統合解析センター 浅尾高行医薬品医療機器総合機構 中村悟医薬品利活用研究班からの協力者名古屋大学 ( 祖父江班 ) 国立精神 神経医療研究センター ( 中村班 ) 国立がん研究センター東病院 ( 大津班 ) 医療機器利活用研究班からの協力者日本脳神経外科学会
17 製薬協医機連 FIRM 厚生労働省 AMED PMDA CIN-WG レジストリ構築 中村班神経 筋疾患 ( 筋ジス ) 祖父江班 ALS 大津班がん領域 クリニカル イノベーション ネットワーク推進支援事業 CIN 構想の加速 推進を目指したレジストリ情報統合拠点の構築研究開発代表者 : 國土典宏 (NCGM) AMED CIN 研究班 ( レジストリ関連 ) 嘉山班脳神経外科医療機器 医薬品等規制調和 評価研究事業患者レジストリーデータを活用した臨床開発効率化のための新たな臨床研究デザインの開発研究開発代表者 : 林邦彦 ( 群馬大学 ) 臨床研究 治験推進研究事業疾患登録システムの有効活用によるクリニカルイノベーションネットワーク構想の推進方策に関する研究研究開発代表者 : 武田伸一 (NCNP) CIN 推進拠点 新たな試験デザイン信頼性基準 CIN 推進の仕組み横断的課題 難治性疾患実用化研究事業希少難治性疾患克服のための 生きた難病レジストリ の設計と構築研究開発代表者 : 松田文彦 ( 京都大学 )
18
19 中央支援部門 ( 仮称 ) CIN に基づく治験 臨床研究を迅速に実施することを支援する部門 疾患レジストリの利活用促進のため臨床開発 疾患レジストリーに関する知識 経験 人材を集約し レジストリー運営のあり方 手続きの簡素化 迅速化 企業利活用の促進等 CIN を推進する 開発者に対して コーディネート機能を有するワンストップサービスの提供を行う 国 事務局運営 共通基盤構築に係る費用拠出 中央支援部門 ( 仮称 ) 製薬企業等コンソーシアム PMDA 製薬企業等 ニーズの反映 レギュラトリーサイエンス研究 情報提供依頼 対価支払 治験実施可能性調査 治験リクルーティング 治験対照群検討 情報提供 審査支援 (CDISC 規格等でのデータ提供等 ) 中枢機能 ワンストップ サービスの提供 企業ニーズ把握 開発戦略等受付 疾患登録情報の可視化 リスト化 疾患レジストリの運営調整 情報提供 構築支援 ( 法的対応 SOP 整備 ヘ ストフ ラクティス提示等 ) 治験ネットワーク 疾患レジストリ共通基盤のあり方検討 構築 コーディネート業務 A B NC 中核病院 X 学会 X がん登録難病登録 臨床研究中核病院等 一般病院等 診療所 患者 疾患等の情報提供 広報治療法開発成果による還元 ニーズ把握 ( 国民の声 ) 構成する要員 ( 案 ) 医師 薬剤師 治験事務局 治験コーディネーター 臨床統計家 レギュラトリー サイエンス データサイエンス 医療情報 ICT 倫理 知的財産権等の法律関連 国民 将来的にゲノム医療 バイオリソース IRUDとの連携 Precision medicineへ向けたコホート研究
20 中央支援部門の提供するワンストップとは 20 ワンストップサービス(システム構築 保守運用業務の一本化)レジストリレジストリレジストリレジストリ 患者データの購入治験対照群の検討製造販売後調査製薬企業 / アカデミアワンストップサービス(問い合わせ 受発注業務の一本化)中央支援部門アカデミア
21 製薬協医機連 FIRM 厚生労働省 AMED PMDA CIN-WG レジストリ構築 中村班神経 筋疾患 ( 筋ジス ) 祖父江班 ALS 大津班がん領域 クリニカル イノベーション ネットワーク推進支援事業 CIN 構想の加速 推進を目指したレジストリ情報統合拠点の構築研究開発代表者 : 國土典宏 (NCGM) AMED CIN 研究班 ( レジストリ関連 ) 嘉山班脳神経外科医療機器 医薬品等規制調和 評価研究事業患者レジストリーデータを活用した臨床開発効率化のための新たな臨床研究デザインの開発研究開発代表者 : 林邦彦 ( 群馬大学 ) 臨床研究 治験推進研究事業疾患登録システムの有効活用によるクリニカルイノベーションネットワーク構想の推進方策に関する研究研究開発代表者 : 武田伸一 (NCNP) CIN 推進拠点 新たな試験デザイン信頼性基準 CIN 推進の仕組み横断的課題 難治性疾患実用化研究事業希少難治性疾患克服のための 生きた難病レジストリ の設計と構築研究開発代表者 : 松田文彦 ( 京都大学 )
22 産学連携全国がんゲノムスクリーニング (SCRUM-Japan) (n= 5,127: 2015/ /06) No. of pts enrolled 検体収集遺伝子スクリーニング企業 医師主導治験への登録
23 ゲノム診断技術開発の進歩によるがんの希少フラクション化 肺がん ( 非小細胞非扁平上皮 ) 消化器がん ( 大腸 ) Next Generation Sequencing 肺がん ( 扁平上皮 ) 消化器がん ( 胃 ) 消化器がん ( 食道 ) 希少フラクション化により医薬品開発を行う上での問題が生じている
24 Different outcomes in the same molecular alteration Efficacy of vemurafenib in BRAF V600E mutant melanoma and CRC Efficacy of T-DM1 in HER2 positive BC and GC HER2 breast cancer :positive results melanoma:rr = 86% Chapman PB, et al. NEJM Jun 5. Verma S et al. N Engl J Med 2012;367: CRC:RR= 5% HER2 gastric cancer:negative results Kopetz S, et al.: J Clin Oncol. 2010; 28 (suppl; abstr 3534) Kang YK, et al.:gi cancer symposium 2016 同じ分子異常であっても がん種によって治療薬の効果が異なる場合がある
25 ゲノム診断技術開発の進歩によるがんの希少フラクション化 患者数が少ない疾患 集団において医薬品開発を行う場合の問題点 1. 無作為化比較臨床試験の実施にあたり 統計学的仮説から導き出した有効性を検証するために必要な症例数を集めるまでに 時間やコストがかかる 又は必要症例数を集めること自体が不可能 2. 対象となる患者の比較対照患者における臨床経過の実態把握が不十分 ( 薬を使用しなかった時に比べ 本当に効果があるのか分からない ) 全国規模でのゲノムスクリーニングによる治験適格患者の集積ゲノム異常毎のナチュラルヒストリーの把握 SCRUM-Japan を活用したレジストリ構築による希少フラクションに対する新薬開発の促進
26 SCRUM-Japan を活用した産官学連携がん治療開発とレジストリの構築の概要 患者レジストリの構築 ( 本研究班 ) 疾患ごとの遺伝子異常頻度および患者分布 取得データに関する協議 前向きレジストリデータ取得 ( 登録開始 ) 肺 消化器領域での希少がん フラクションの臨床ゲノム情報から治験比較対照群のデータ構築 X 遺伝子異常陽性かつ治験非登録例での臨床情報 ( 他治療での奏効率 予後など ) オンラインでの臨床ゲノムデータ共有 ( 構築済み ) CDISC など国際標準に対応した臨床ゲノム DB 構築 ( 構築中 ) 治験デザインの提案 承認審査時の重要参考データ供出 国際連携 参加製薬企業 アカデミアによる新たな創薬 標的探索 ゲノムデータ利用 検体二次利用 SCRUM-Japan における世界最大規模臨床ゲノム情報 ( 製薬 16 社と全国 245 医療機関との共同 ) 治験結果による新薬承認申請 製造販売承認取得 教育 啓蒙 教育 人材育成 (e-learning/ トレーニング開始 ) 新たな治験薬の提供 Precision medicine の実現 新たなバイオマーカー候補 Liquid biopsy 免疫ゲノムパネル 年間 2,500 例を超える症例集積と新薬開発治験 40 試験 ( 現時点 ) への効率的な登録
27 SCRUM-Japan 臨床ゲノム情報統合データベース患者レジストリとしての活用 疾患登録システムの活用例 レジストリの分類 ( 企業の活用方法として 主に 下記の 4 つを想定 ) A) 市場性調査 : 患者数 地域分布などから 日本での医薬品開発可能性を検討 B) 患者リクルート : 登録された患者を 治験 臨床研究に効率的に組入れ C) 治験対照群 : 患者自然歴を把握し 治験の対照群として利用 (Single Arm 試験 ) D) 市販後安全性調査 : 市販後 副作用の発生状況などを把握 SCRUM-Japan レジストリでカバーする範囲 1 A) 及び B) の目的での運用は既に始まっている 2 今後 C) 又は D) の目的での運用を目指し 医薬品 医療機器の開発環境整備に向け 規制当局 ( 医薬局 PMDA) 製薬協等の企業関係者も交え 新たなレジストリを構築 検証を行い 疾患登録システムに関するガイドラインを策定する予定 医薬品開発の時間軸とレジストリ 非臨床 Ph1 Ph2 Ph3 承認申請 製造販売後 再審査 A) 市場性調査 B) 治験リクルート C) 治験対照群として承認申請に活用 D) 市販後安全性調査
28 製造販売承認申請資料として活用される比較対照データ作成のために必要な事項についての協議 PMDA 新薬第 5 部との協議 データ収集項目 遺伝子異常 : 各がん種で治療開発対象となることが見込まれる遺伝子 ( 各がん種 2~3 遺伝子 ) 治療効果 : 腫瘍縮小効果 (RECIST) 治療期間 (TTF) 奏効期間 (PFS) 全生存期間 (OS) データ収集範囲 GI-SCREEN(20 施設 ): 全 20 施設 LC-SCRUM( 約 200 施設 ): 上位 50 施設を選定 PMDA 信頼性保証部 AMED 林班との協議 データの質担保 セントラルモニタリング SDV( サンプリング ) データセットの標準化 収集項目の標準コード化 CDISC 標準化への対応 患者レジストリデータを申請資料として活用する場合におけるデータの信頼性担保に関する基本的な考え方 PMDA 安全部 AMED 武田班との協議 データベースを情報源とする安全性情報の取扱いについて 改正医学系指針への対応 倫理面 登録医療機関との契約
29 SCRUM-Japan 疾患レジストリを活用した新薬承認審査時の治験対照群データ作成のための前向き多施設共同研究 (SCRUM-Japan Registry) 目的 産学連携全国がんゲノムスクリーニング事業 (SCRUM-Japan) に登録された症例の中で 対象となる遺伝子異常に対する新薬開発試験が実施されており 近い将来その新薬承認申請が見込まれる遺伝子異常陽性例での治療効果データなどを前向きに集積し 当該新薬の承認審査時に比較可能な治験対照群のデータを作成する 承認審査時の 評価資料 とすることを目指す質保証 ( 信頼性保証 ) されたデータの収集 マネジメント=施設数を限定 GI-SCREEN: 全 20 施設 LC-SCRUM: 登録上位約 50 施設
30 SCRUM-Japan 疾患レジストリを活用した新薬承認審査時の治験対照群データ作成のための前向き多施設共同研究 (SCRUM-Japan Registry) 本研究の対象とする遺伝子異常等 がん腫 対象とする遺伝子異常等 大腸癌 BRAF 遺伝子変異 ERBB2 遺伝子増幅 MET 遺伝子増幅 NTRK 融合遺伝子 RSPO2/3 融合遺伝子 RNF43 遺伝子変異 HER2 陽性 (IHC, ISH 等 ) BRAF 陽性 (PCR 等 ) 胃癌 食道癌 非扁平上皮非小細胞肺癌 扁平上皮非小細胞肺癌 胆道癌 膵臓癌 FGFR2 遺伝子増幅 MET 遺伝子増幅 ERBB2 遺伝子増幅 PIK3CA 遺伝子変異及び増幅 RET 融合遺伝子 MET ex14skip 及び遺伝子増幅 ERBB2 遺伝子変異及び遺伝子増幅 FGFR1/2/3 遺伝子増幅及び融合遺伝子 PIK3CA 遺伝子変異及び遺伝子増幅 FGFR2 融合遺伝子 ERBB2 遺伝子増幅 IDH1 遺伝子変異 BRCA2 遺伝子変異 ATM 遺伝子変異 PALB2 遺伝子変異 HER2 陽性 (IHC, ISH 等 ) 各領域の KOL 製薬企業等と協議の上 対象とする遺伝子異常等を選定
31 評価項目 SCRUM-Japan 疾患レジストリを活用した新薬承認審査時の治験対照群データ作成のための前向き多施設共同研究 (SCRUM-Japan Registry) 対象とする各遺伝子異常陽性集団ごとに 以下の項目を収集及び算出する 1 各治療ラインにおける以下の項目 奏効率 (RR: Response Rate)( 最良総合効果 ) 無増悪生存期間 (PFS: Progression Free Survival) 奏効持続期間 (DoR: Duration of Response) 治療成功期間 (TTF: Time to Treatment Failure) 病勢制御率 (DCR: Disease Control Rate) 2 全生存期間 (OS: Overall Survival) 目標登録数約 630 例 目標症例数の設定根拠 : 本研究の対象とする遺伝子異常等 ( 別紙 1, p21) 参照 なお 本研究の対象が追加された場合 その対象の頻度に応じて 目標症例数を変更する 研究期間登録期間 : 研究許可日 ~2019 年 3 月 31 日研究期間 : 研究許可日 ~2022 年 3 月 31 日 各遺伝子異常陽性症例における標準治療の治療効果に注目 レジストリ登録後効果判定画像評価 6-10 週に 1 回 本研究では 各遺伝子異常の頻度により集積ペースが異なるため 解析が可能な数に達したと判断された時点で 各遺伝子異常陽性集団ごとにデータ解析を行なう 詳細は 別途 解析計画書に定める
32 SCRUM-Japan Registry 患者レジストリを外部の治験対照群として活用した医師主導治験の概要 ゲノム等の検査委託機関 腫瘍組織検査 リキッドバイオプシー 産学連携全国がんゲノムスクリーニング SCRUM-Japan 検体の提出 結果の返却 医師主導治験実施施設 医師主導治験不参加施設 HER2 陽性 BRAF 陽性 紹介 治験に同意適格規準を満たす その他 医師主導治験 治験治療 HER2( 岡本班 ) BRAF( 吉野班 ) 疾患レジストリ外部の治験対照群ナチュラルヒストリーデータの収集 ( 大津班 ) 相談事項 : 自然歴データを利用することについて相談事項に対する機構の意見自然歴データの信頼性を適切に担保可能であることを前提として 自然歴データと比較する本試験を評価資料とすることは可能と考える RS 戦略相談等 対象患者 主要評価項目 症例数 治験対照群の設定 コンパニオン診断薬など 製造販売承認申請の評価資料
33 SCRUM-Japan レジストリデータ収集の効率化と質担保 AMED 林班による信頼性担保に関する基本的考え方 ( 案 ) に準拠した SOP 作成 セントラルモニタリング及び SDV( サンプリング ) の実施を予定 CRC 派遣によるデータ入力補助
34 実施医療機関 3 Laboratory 電子カルテ CDASH 収集項目データ 3 臨床研究用データ入出力機能 xlsx or ODM SCRUM-Japan Registry SCRUM-Japan レジストリデータ収集システムおよび CDISC 標準化対応 3 テンプレート作成データ入出力機能 (H29 年 9 月完成予定 ) 電子カルテテンプレート 4 派遣 CRC による入力システム ( 構築済み ) 臨床研究 DB(EDC) Data 症例データ収集用データベース (EDC) CRF 仕様 2 3 電子カルテテンプレートは国立がん研究センター東病院で整合性と実施可能性を検証した後に多施設での実装を図る予定 (H30 年度 ) 収集項目等の配信 メタデータ管理 Report file (QC file) Data Center 1SDTM (SOP 仕様書作成済 H29 年 12 月完成予定 ) SDTM 仕様 2 メタデータ管理 ( 構築済み ) 1 CRF 仕様 SDTM Data Set ADaM Analysis CDISC SHARE Define -XML SCRUM-J Registry Secure Data Storage SCRUM-J 臨床ゲノム統合 DB VCF BAM Raw data Validation 規制当局 Data share Approval AI, DL etc.. 製薬企業 Drug Development Basic Research Academia
35 Acknowledgement SCRUM-Japan Participating Institutes and Companies Atsushi Ohtsu, Koichi Goto (LC-SCRUM-Japan), Takayuki Yoshino (GI-SCREEN-Japan), Katsuya Tsuchihara (SCRUM-Japan Data Center), Genta Ohno (SCRUM-Japan Office) National Cancer Center Hospital East Kiyotaka Yoh, Shigeki Umemura, Eri Sugiyama, Hibiki Udagawa (LC-SCRUM-Japan) Kohei Shitara, Chigusa Morizane, Takatsugu Kojima (GI-SCREEN-Japan) NCCHE Office of Biobank Translational Research Tomohisa Sudo, Izumi Miki, Akiko Nakayama, Junko Kuramochi, Yuri Murata, Yuko Tagami, Yumiko Shimanishi NCCHE Office of Clinical Research Yoshihiro Aoyagi, Nozomu Fuse Division of TR, NCC-EPOC Shingo Matsumoto, Sachiyo Mimaki, Ayako Suzuki, Hideki Makinoshima, Koutatsu Matsushima, Sayuri Todoroki, Motoki Kasahara, Satoshi Tada (Dynacom Co. Ltd), Tomohiro Sakamoto (Tottori Univ), Hiroyasu Esumi (Tokyo Univ. Sci.), Takashi Kohno
36 御清聴ありがとうございました All Activities for Cancer Patients
PowerPoint プレゼンテーション
 第 4 回臨床開発環境整備推進会議資料 2-1 SCRUM-Japan 疾患レジストリの進捗報告 国立がん研究センター東病院大津敦 2018 年 3 月 15 日厚労省 産学連携全国がんゲノムスクリーニング事業 (SCRUM-Japan ) (n= 7,553: 2015/02-2017/12) 全国 250 施設の参加 ゲノム解析結果に基づく企業 医師主導治験 : Umbrella type 25
第 4 回臨床開発環境整備推進会議資料 2-1 SCRUM-Japan 疾患レジストリの進捗報告 国立がん研究センター東病院大津敦 2018 年 3 月 15 日厚労省 産学連携全国がんゲノムスクリーニング事業 (SCRUM-Japan ) (n= 7,553: 2015/02-2017/12) 全国 250 施設の参加 ゲノム解析結果に基づく企業 医師主導治験 : Umbrella type 25
PowerPoint プレゼンテーション
 第 5 回臨床開発環境整備推進会議 平成 31 年 3 月 13 日 資料 1-1 臨床研究 治験推進研究事業 疾患登録システムの有効活用によるクリニカルイノベーションネットワーク構想の推進方策に関する研究 国立研究開発法人 研究開発代表者 国立精神 神経医療研究センター 理事 武田伸一 資料内容 関連研究班の位置付け 検討課題 既存及ひ 構築中の患者レジストリのリスト化について CIN-WG 個人情報保護法への対応
第 5 回臨床開発環境整備推進会議 平成 31 年 3 月 13 日 資料 1-1 臨床研究 治験推進研究事業 疾患登録システムの有効活用によるクリニカルイノベーションネットワーク構想の推進方策に関する研究 国立研究開発法人 研究開発代表者 国立精神 神経医療研究センター 理事 武田伸一 資料内容 関連研究班の位置付け 検討課題 既存及ひ 構築中の患者レジストリのリスト化について CIN-WG 個人情報保護法への対応
PowerPoint プレゼンテーション
 研究開発課題名難病 希少疾患の医薬品開発におけるクリニカルイノベーションネットワーク構想の推進を目指した疾患登録システム ( 患者レジストリ ) の構築 研究開発代表者 国立研究開発法人国立精神 神経医療研究センター 資料 2-3 トランスレーショナルメディカルセンター 臨床研究支援室長 発表内容 本研究の目標 実施体制 Remudy の実績と課題 目指すもの 疾患登録システム レジストリの信頼性について
研究開発課題名難病 希少疾患の医薬品開発におけるクリニカルイノベーションネットワーク構想の推進を目指した疾患登録システム ( 患者レジストリ ) の構築 研究開発代表者 国立研究開発法人国立精神 神経医療研究センター 資料 2-3 トランスレーショナルメディカルセンター 臨床研究支援室長 発表内容 本研究の目標 実施体制 Remudy の実績と課題 目指すもの 疾患登録システム レジストリの信頼性について
2015_JBCRG
 5 2015.11.13 II Precision medicine SCRUM-Japan EPOC SCRUM-Japan 20152 20173 2250 186 20 20159 IRB NGS ; Oncomine Cancer Research Panel143 CLIA 2TAT 14 Central Testing at CLIA Labs Oncomine Cancer Research
5 2015.11.13 II Precision medicine SCRUM-Japan EPOC SCRUM-Japan 20152 20173 2250 186 20 20159 IRB NGS ; Oncomine Cancer Research Panel143 CLIA 2TAT 14 Central Testing at CLIA Labs Oncomine Cancer Research
PowerPoint プレゼンテーション
 背景 クリニカル イノベーション ネットワーク (CIN) の背景と概要 資料 3 新しい医薬品 医療機器等の開発に当たっては 世界的にコストが高騰している 特に 医薬品にあっては タフツ大学の試算によると 1 新薬当たり $2,558 million( 約 3,000 億円 ) 要するといわれている (Nov. 18, 2014, Tufts Center for the Study of Drug
背景 クリニカル イノベーション ネットワーク (CIN) の背景と概要 資料 3 新しい医薬品 医療機器等の開発に当たっては 世界的にコストが高騰している 特に 医薬品にあっては タフツ大学の試算によると 1 新薬当たり $2,558 million( 約 3,000 億円 ) 要するといわれている (Nov. 18, 2014, Tufts Center for the Study of Drug
1-5
 第 8 回がん新薬開発合同シンポジウム アカデミアの立場から :SCRUM-Japan レジストリでの新しい取り組み 国立がん研究センター東病院大津敦 岡本渉 布施望 青柳吉博吉野孝之 後藤功一 土原一哉 2018 年 10 月 5 日東京 産学連携全国がんゲノムスクリーニング事業 (SCRUM-Japan ) の概要 (n= 9,630: 2015/02-2018/06) 全国 260 施設の参加
第 8 回がん新薬開発合同シンポジウム アカデミアの立場から :SCRUM-Japan レジストリでの新しい取り組み 国立がん研究センター東病院大津敦 岡本渉 布施望 青柳吉博吉野孝之 後藤功一 土原一哉 2018 年 10 月 5 日東京 産学連携全国がんゲノムスクリーニング事業 (SCRUM-Japan ) の概要 (n= 9,630: 2015/02-2018/06) 全国 260 施設の参加
AMED CIN 推進支援公開シンポジウム SCRUM-Japan を利用したがん新薬開発に資する疾患登録システムの構築 国立がん研究センター東病院大津敦 2018 年 7 月 12 日東京
 AMED CIN 推進支援公開シンポジウム SCRUM-Japan を利用したがん新薬開発に資する疾患登録システムの構築 国立がん研究センター東病院大津敦 2018 年 7 月 12 日東京 産学連携全国がんゲノムスクリーニング事業 (SCRUM-Japan ) (n= 9,590: 2015/02-2018/05) 全国 250 施設の参加 ゲノム解析結果に基づく企業 医師主導治験 : Umbrella
AMED CIN 推進支援公開シンポジウム SCRUM-Japan を利用したがん新薬開発に資する疾患登録システムの構築 国立がん研究センター東病院大津敦 2018 年 7 月 12 日東京 産学連携全国がんゲノムスクリーニング事業 (SCRUM-Japan ) (n= 9,590: 2015/02-2018/05) 全国 250 施設の参加 ゲノム解析結果に基づく企業 医師主導治験 : Umbrella
PowerPoint プレゼンテーション
 第 5 回臨床開発環境整備推進会議 平成 31 年 3 月 13 日 資料 1-3 患者レジストリーデータを用い 臨床開発の効率化を目指すレギュラトリーサイエンス研究 - 新たな臨床研究デザインの開発 平成 30 年度 医薬品等規制調和 評価研究事業 - 研究者所属機関 - 群馬大学 国立精神 神経医療研究センター 国立国際医療研究センター 国立成育医療研究センター 国立循環器病研究センター 国立長寿医療研究センター
第 5 回臨床開発環境整備推進会議 平成 31 年 3 月 13 日 資料 1-3 患者レジストリーデータを用い 臨床開発の効率化を目指すレギュラトリーサイエンス研究 - 新たな臨床研究デザインの開発 平成 30 年度 医薬品等規制調和 評価研究事業 - 研究者所属機関 - 群馬大学 国立精神 神経医療研究センター 国立国際医療研究センター 国立成育医療研究センター 国立循環器病研究センター 国立長寿医療研究センター
PowerPoint プレゼンテーション
 コンパニオン診断の現状 ~ 肺がんを例に ~ 2017 年 7 月 29 日 個別化医療に必要なコンパニオン診断薬 コンパニオン診断薬 ~ 肺癌治療を例に ~ NGS によるコンパニオン診断システム 個別化医療の概念 効果と安全性の両面で優れた治療法として世界的に関心が高まっており 特にがん治療などにおいて 今後の中心的役割を担うものと考えられています 薬剤投与前にバイオマーカーと呼ばれる特定の分子や遺伝子を診断し
コンパニオン診断の現状 ~ 肺がんを例に ~ 2017 年 7 月 29 日 個別化医療に必要なコンパニオン診断薬 コンパニオン診断薬 ~ 肺癌治療を例に ~ NGS によるコンパニオン診断システム 個別化医療の概念 効果と安全性の両面で優れた治療法として世界的に関心が高まっており 特にがん治療などにおいて 今後の中心的役割を担うものと考えられています 薬剤投与前にバイオマーカーと呼ばれる特定の分子や遺伝子を診断し
臨床研究 治験推進研究事業疾患登録システムの有効活用によるクリニカルイノベーションネットワーク構想の推進方策に関する研究 (16lk h0001) 研究開発代表者 資料 2-1 国立研究開発法人国立精神 神経医療研究センター 神経研究所長 武田伸一 資料内容 クリニカル イノベーション
 臨床研究 治験推進研究事業疾患登録システムの有効活用によるクリニカルイノベーションネットワーク構想の推進方策に関する研究 (16lk0201059h0001) 研究開発代表者 資料 2-1 国立研究開発法人国立精神 神経医療研究センター 神経研究所長 武田伸一 資料内容 クリニカル イノベーション ネットワーク (CIN) の進捗 関連研究班の位置付け 検討課題 既存及ひ 構築中の患者レジストリのリスト化について
臨床研究 治験推進研究事業疾患登録システムの有効活用によるクリニカルイノベーションネットワーク構想の推進方策に関する研究 (16lk0201059h0001) 研究開発代表者 資料 2-1 国立研究開発法人国立精神 神経医療研究センター 神経研究所長 武田伸一 資料内容 クリニカル イノベーション ネットワーク (CIN) の進捗 関連研究班の位置付け 検討課題 既存及ひ 構築中の患者レジストリのリスト化について
Microsoft PowerPoint - 3. 資料2 がんゲノム情報管理センターの進捗状況
 第 1 回がんゲノム医療推進コンソーシアム運営会議平成 30 年 8 月 1 日 資料 2 がんゲノム情報管理センターの進捗状況 間野博行がんゲノム情報管理センター長 1 がんゲノム情報管理センターの設置 厚生労働省の がんゲノム医療推進コンソーシアム懇談会報告書 ( 平成 29 年 6 月 27 日とりまとめ ) には がんゲノム医療実用化に向けた工程として がんゲノム医療 研究のマスターデータベースである
第 1 回がんゲノム医療推進コンソーシアム運営会議平成 30 年 8 月 1 日 資料 2 がんゲノム情報管理センターの進捗状況 間野博行がんゲノム情報管理センター長 1 がんゲノム情報管理センターの設置 厚生労働省の がんゲノム医療推進コンソーシアム懇談会報告書 ( 平成 29 年 6 月 27 日とりまとめ ) には がんゲノム医療実用化に向けた工程として がんゲノム医療 研究のマスターデータベースである
本日の講演内容 1. PMDA コンパニオン診断薬 WG 2. 本邦におけるコンパニオン診断薬の規制 3. 遺伝子パネルを用いた NGS コンパニオン診断システム 1 2 規制上の取扱い 評価の考え方 2
 わが国での NGS 診断パネル承認の考え方 独立行政法人医薬品医療機器総合機構上席審議役 ( 機器審査等担当 ) 佐藤岳幸 本日の講演内容 1. PMDA コンパニオン診断薬 WG 2. 本邦におけるコンパニオン診断薬の規制 3. 遺伝子パネルを用いた NGS コンパニオン診断システム 1 2 規制上の取扱い 評価の考え方 2 本日の講演内容 1. PMDA コンパニオン診断薬 WG 2. 本邦におけるコンパニオン診断薬の規制
わが国での NGS 診断パネル承認の考え方 独立行政法人医薬品医療機器総合機構上席審議役 ( 機器審査等担当 ) 佐藤岳幸 本日の講演内容 1. PMDA コンパニオン診断薬 WG 2. 本邦におけるコンパニオン診断薬の規制 3. 遺伝子パネルを用いた NGS コンパニオン診断システム 1 2 規制上の取扱い 評価の考え方 2 本日の講演内容 1. PMDA コンパニオン診断薬 WG 2. 本邦におけるコンパニオン診断薬の規制
Microsoft PowerPoint - 01CDISC概要短縮版.ppt
 CDISC 標準の概要 東京大学医学部附属病院大学病院医療情報ネットワーク研究センター木内貴弘 目次 1.CDISC 標準について 2. 医療の世界のデータ交換標準と臨床研究の世界のデータ交換標準 3.CDISC 標準を活用した効率的な臨床研究 1.CDISC 標準について CDISC とは? Clinical Data Interchange Standards Consortium の略 ( 非営利の臨床データ標準化団体
CDISC 標準の概要 東京大学医学部附属病院大学病院医療情報ネットワーク研究センター木内貴弘 目次 1.CDISC 標準について 2. 医療の世界のデータ交換標準と臨床研究の世界のデータ交換標準 3.CDISC 標準を活用した効率的な臨床研究 1.CDISC 標準について CDISC とは? Clinical Data Interchange Standards Consortium の略 ( 非営利の臨床データ標準化団体
研究から医療へ より医療への実利用が近いもの ゲノム医療研究推進ワーキンググループ報告書 (AMED) 臨床ゲノム情報統合データベース公募 対象疾患の考え方の方向性 第 1 グループ ( 主に を目指す ) 医療への実利用が近い疾患 領域の着実な推進 単一遺伝子疾患 希少疾患 難病 ( 生殖細胞系列
 ゲノム医療実現に向けた対象疾患の考え方 ( 案 ) 資料 3-1 1. これまでの整理について において 比較的エビデンスが蓄積されており 医療への実利用が近い疾患 領域であり 着実に推進する必要がある 第 1 グループと ( 医療への実利用は近くないが ) 多くの国民が罹患する一般的な疾患への対応にゲノム情報等を応用する 第 2 グループに整理された なお 医療分野研究開発推進計画 ( 健康 医療戦略推進本部決定
ゲノム医療実現に向けた対象疾患の考え方 ( 案 ) 資料 3-1 1. これまでの整理について において 比較的エビデンスが蓄積されており 医療への実利用が近い疾患 領域であり 着実に推進する必要がある 第 1 グループと ( 医療への実利用は近くないが ) 多くの国民が罹患する一般的な疾患への対応にゲノム情報等を応用する 第 2 グループに整理された なお 医療分野研究開発推進計画 ( 健康 医療戦略推進本部決定
PowerPoint プレゼンテーション
 2018 年 3 月 31 日第 24 回抗悪性腫瘍薬開発フォーラム ( 於 : がん研究会がん研究所 ) 将来の承認審査の視点 独立行政法人医薬品医療機器総合機構 (PMDA) 新薬審査第五部 清原宏眞 本日のお話 国等の動き 審査の視点 本講演は 講演者の個人的見解に基づくものであり ( 独 ) 医薬品医療機器総合機構 (PMDA) の公式見解を示すものではありません 先駆け審査指定制度 世界に先駆けて
2018 年 3 月 31 日第 24 回抗悪性腫瘍薬開発フォーラム ( 於 : がん研究会がん研究所 ) 将来の承認審査の視点 独立行政法人医薬品医療機器総合機構 (PMDA) 新薬審査第五部 清原宏眞 本日のお話 国等の動き 審査の視点 本講演は 講演者の個人的見解に基づくものであり ( 独 ) 医薬品医療機器総合機構 (PMDA) の公式見解を示すものではありません 先駆け審査指定制度 世界に先駆けて
抗悪フォーラム 永井最終版.ppt
 コンパニオン診断薬を用いた抗がん剤の 開発及び評価における留意点 永井純正 Sumimasa NAGAI, M.D., Ph.D. 医薬品医療機器総合機構専門委員 ( 前職新薬審査第五部審査専門員 ) 東京大学医科学研究所先端医療研究センター はじめに 本発表は 個人の見解に基づくものであり PMDA の公式見解を示すものではありません コンパニオン診断薬プロジェクト 横断的基準作成プロジェクトの一つ医薬品
コンパニオン診断薬を用いた抗がん剤の 開発及び評価における留意点 永井純正 Sumimasa NAGAI, M.D., Ph.D. 医薬品医療機器総合機構専門委員 ( 前職新薬審査第五部審査専門員 ) 東京大学医科学研究所先端医療研究センター はじめに 本発表は 個人の見解に基づくものであり PMDA の公式見解を示すものではありません コンパニオン診断薬プロジェクト 横断的基準作成プロジェクトの一つ医薬品
UMIN INDICE Lower level data communication protocol for CDISC ODM規約
 UMIN INDICE Lower level data communication protocol for CDISC ODM 規約 API Ver2.7 用 UMIN INDICE システムに臨床研究データを CDISC ODM 形式で電子的に送付する場合の ODM 下層レベルのデータ交換規約 UMIN センター 2013/05/16 目次 1 概要...- 2-1.1 UMIN センター...-
UMIN INDICE Lower level data communication protocol for CDISC ODM 規約 API Ver2.7 用 UMIN INDICE システムに臨床研究データを CDISC ODM 形式で電子的に送付する場合の ODM 下層レベルのデータ交換規約 UMIN センター 2013/05/16 目次 1 概要...- 2-1.1 UMIN センター...-
医師主導治験取扱要覧
 15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
15. 監査の実施に関する手順書 1. 目的と適用範囲本手順書は 当該治験において 及び監査担当者が 監査を適切に実施するための手順その他必要な事項を定めるものである なお が 本手順に係る業務を 治験調整委員会への業務委嘱に関する手順書 によって治験調整委員会に委嘱する場合 当該業務については 本手順書中の を 治験調整委員会 と読み替える 2. 実施体制及び責務 2.1. の責務 (1) は 当該治験の品質保証のため
医療機器開発マネジメントにおけるチェック項目
 2018 年 11 月作成 医療機器開発マネジメントにおけるチェック項目 1. 各ステージゲートにおけるチェック項目 (1) チェック項目作成の目的従来個々の事業において実施されていた 事前 中間 事後の各ゲートにおける評価項目 Go/no-go の判断を 医療機器開発全期間を通して整理し 共通認識化する 技術的観点及び事業化の観点の双方を意識し 医療機器開発の特性を考慮したチェック項目を設定する
2018 年 11 月作成 医療機器開発マネジメントにおけるチェック項目 1. 各ステージゲートにおけるチェック項目 (1) チェック項目作成の目的従来個々の事業において実施されていた 事前 中間 事後の各ゲートにおける評価項目 Go/no-go の判断を 医療機器開発全期間を通して整理し 共通認識化する 技術的観点及び事業化の観点の双方を意識し 医療機器開発の特性を考慮したチェック項目を設定する
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 <その他分野 ( 消化器官用薬 解毒剤 その他 )> 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号
 資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
資料 3 1 医療上の必要性に係る基準 への該当性に関する専門作業班 (WG) の評価 < 代謝 その他 WG> 目次 小児分野 医療上の必要性の基準に該当すると考えられた品目 との関係本邦における適応外薬ミコフェノール酸モフェチル ( 要望番号 ;II-231) 1 医療上の必要性の基準に該当しないと考えられた品目 本邦における適応外薬ミコフェノール酸モフェチル
北里大学グローバル臨床研究拠点
 日本主導型グローバル臨床研究 体制整備 : 北里大学の取り組み 1 1. 事業概要 目的 1. グローバル臨床研究の立案から実施 結果の公表まで グローバル開発の入り口から出口まで を多角的に支援できる体制を強化する 2. 法人内外のネットワークを活用し 日本発の創薬 医療機器シーズを育成する キャッチフレーズ 実学の精神 のもと オール北里体制で日本主導型グローバル臨床研究推進の中核を担う 2 学校法人北里研究所
日本主導型グローバル臨床研究 体制整備 : 北里大学の取り組み 1 1. 事業概要 目的 1. グローバル臨床研究の立案から実施 結果の公表まで グローバル開発の入り口から出口まで を多角的に支援できる体制を強化する 2. 法人内外のネットワークを活用し 日本発の創薬 医療機器シーズを育成する キャッチフレーズ 実学の精神 のもと オール北里体制で日本主導型グローバル臨床研究推進の中核を担う 2 学校法人北里研究所
PowerPoint プレゼンテーション
 資料 5 平成 28 年度採択課題及び平成 29 年度予算案報告 クリニカル イノベーション ネットワークの構築 ( 疾患登録情報を活用した臨床開発インフラの整備 ) 平成 29 年度予算案 ( 平成 28 年度予算額 ) コア事業 20.7 億円 (7.6 億円 ) 疾患登録情報を活用した治験 臨床研究等 課題 背景 医薬品等の開発費用は 世界的に高騰し 特に我が国は諸外国と比べて開発コストが高い
資料 5 平成 28 年度採択課題及び平成 29 年度予算案報告 クリニカル イノベーション ネットワークの構築 ( 疾患登録情報を活用した臨床開発インフラの整備 ) 平成 29 年度予算案 ( 平成 28 年度予算額 ) コア事業 20.7 億円 (7.6 億円 ) 疾患登録情報を活用した治験 臨床研究等 課題 背景 医薬品等の開発費用は 世界的に高騰し 特に我が国は諸外国と比べて開発コストが高い
本日の内容 1. 本邦におけるコンパニオン診断システムの規制 2. NGSを用いたコンパニオン診断システム 1 規制上の取扱い 2 評価の考え方と検討課題 3. NGSを用いた遺伝子検査システムに関連した課題 2
 次世代シークエンサーを用いたコンパニオン診断システムの開発における課題と今後の方向性について 独立行政法人医薬品医療機器総合機構体外診断薬審査室柳原玲子 本日の内容 1. 本邦におけるコンパニオン診断システムの規制 2. NGSを用いたコンパニオン診断システム 1 規制上の取扱い 2 評価の考え方と検討課題 3. NGSを用いた遺伝子検査システムに関連した課題 2 PMDA 横断的基準作成等プロジェクトチーム
次世代シークエンサーを用いたコンパニオン診断システムの開発における課題と今後の方向性について 独立行政法人医薬品医療機器総合機構体外診断薬審査室柳原玲子 本日の内容 1. 本邦におけるコンパニオン診断システムの規制 2. NGSを用いたコンパニオン診断システム 1 規制上の取扱い 2 評価の考え方と検討課題 3. NGSを用いた遺伝子検査システムに関連した課題 2 PMDA 横断的基準作成等プロジェクトチーム
法医学問題「想定問答」(記者会見後:平成15年 月 日)
 平成 28 年 5 月 26 日 肺がんに対する新たな分子標的治療を発見! 本研究成果のポイント 肺がんのうち 5% 程度を占める KRAS( 1) 遺伝子変異肺がんは, 上皮間葉移行 ( 2) 状態により上皮系と間葉系の 2 種類に分類される KRAS 遺伝子変異を有する肺がんに対し現在臨床試験中の MEK 阻害薬は, 投与後に細胞表面受容体を活性化することにより効果が減弱され, 活性化される細胞表面受容体は上皮間葉移行状態により異なる
平成 28 年 5 月 26 日 肺がんに対する新たな分子標的治療を発見! 本研究成果のポイント 肺がんのうち 5% 程度を占める KRAS( 1) 遺伝子変異肺がんは, 上皮間葉移行 ( 2) 状態により上皮系と間葉系の 2 種類に分類される KRAS 遺伝子変異を有する肺がんに対し現在臨床試験中の MEK 阻害薬は, 投与後に細胞表面受容体を活性化することにより効果が減弱され, 活性化される細胞表面受容体は上皮間葉移行状態により異なる
審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果
![審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果 審査結果 平成 23 年 4 月 11 日 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年 11 月 11 日 [ 審査結果](/thumbs/92/108604766.jpg) 審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
審査報告書 平成 23 年 4 月 11 日 独立行政法人医薬品医療機器総合機構 承認申請のあった下記の医薬品にかかる医薬品医療機器総合機構での審査結果は 以下のとおりで ある 記 [ 販 売 名 ] ミオ MIBG-I123 注射液 [ 一 般 名 ] 3-ヨードベンジルグアニジン ( 123 I) 注射液 [ 申請者名 ] 富士フイルム RI ファーマ株式会社 [ 申請年月日 ] 平成 22 年
平成28年度第11回治験審査委員会開催記録の概要
 平成 30 年度第 7 回治験審査委員会開催記録の概要 開催年月日 開催場所 出席者 平成 30 年 10 月 10 日 ( 水 )17:43~19:45 2 階応接室富永副院長 小野管理局長 松本総務部長 村山検査部長 津田消化器内科部長 松本薬剤部長 芳賀検査技師長 中尾薬剤部次長 辻野放射線部長 長澤看護部次長 根来医師 ( 外部委員 ) 前田弁護士( 外部委員 ) 審議案件 新規 変更 その他
平成 30 年度第 7 回治験審査委員会開催記録の概要 開催年月日 開催場所 出席者 平成 30 年 10 月 10 日 ( 水 )17:43~19:45 2 階応接室富永副院長 小野管理局長 松本総務部長 村山検査部長 津田消化器内科部長 松本薬剤部長 芳賀検査技師長 中尾薬剤部次長 辻野放射線部長 長澤看護部次長 根来医師 ( 外部委員 ) 前田弁護士( 外部委員 ) 審議案件 新規 変更 その他
1. はじめに ステージティーエスワンこの文書は Stage Ⅲ 治癒切除胃癌症例における TS-1 術後補助化学療法の予後 予測因子および副作用発現の危険因子についての探索的研究 (JACCRO GC-07AR) という臨床研究について説明したものです この文書と私の説明のな かで わかりにくいと
 StageⅢ 治癒切除胃癌症例における TS-1 術後補助化学療法の 予後予測因子および副作用発現の危険因子についての 探索的研究 (JACCRO GC-07AR) についてのご説明 説明 同意文書 作成日 :2014 年 5 月 27 日 施設名 : 東京医科大学八王子医療センター 1. はじめに ステージティーエスワンこの文書は Stage Ⅲ 治癒切除胃癌症例における TS-1 術後補助化学療法の予後
StageⅢ 治癒切除胃癌症例における TS-1 術後補助化学療法の 予後予測因子および副作用発現の危険因子についての 探索的研究 (JACCRO GC-07AR) についてのご説明 説明 同意文書 作成日 :2014 年 5 月 27 日 施設名 : 東京医科大学八王子医療センター 1. はじめに ステージティーエスワンこの文書は Stage Ⅲ 治癒切除胃癌症例における TS-1 術後補助化学療法の予後
PowerPoint プレゼンテーション
 電子データ申請時代における Biostatistician のあるべき姿 第一三共株式会社 奥田恭行 1 Disclaimer 本発表内容は発表者の経験に基づいた個人的見解であり 所属する組織を代表した意見ではないことにご留意下さい 2 背景 拡大する生物統計担当者の業務とその弊害 近年では 社内で生物統計担当者が関与を求められる業務範囲は広がりつつあり その中でも CDISC 標準実装 電子データ申請対応に関する業務増が大きい
電子データ申請時代における Biostatistician のあるべき姿 第一三共株式会社 奥田恭行 1 Disclaimer 本発表内容は発表者の経験に基づいた個人的見解であり 所属する組織を代表した意見ではないことにご留意下さい 2 背景 拡大する生物統計担当者の業務とその弊害 近年では 社内で生物統計担当者が関与を求められる業務範囲は広がりつつあり その中でも CDISC 標準実装 電子データ申請対応に関する業務増が大きい
<4D F736F F F696E74202D208EA18CB B90B389BB8DEC8BC694C F E B93C782DD8EE682E890EA97705D205B8CDD8AB
 治験等適正化作業班における 検討 独立行政法人国立病院機構本部伊藤澄信 第 6 回治験中核病院 拠点医療機関等協議会 本日の内容 設置の経緯等について 主な検討内容について 今後の課題について その他 1 設置の経緯 (1) 1. 設置の背景 新たな治験活性化 5 カ年計画の中間見直しに関する検討会 報告の 重点的取組事項 ( アクションプラン ) の進捗 において 今後 取組みをより加速かつ強化すべき課題
治験等適正化作業班における 検討 独立行政法人国立病院機構本部伊藤澄信 第 6 回治験中核病院 拠点医療機関等協議会 本日の内容 設置の経緯等について 主な検討内容について 今後の課題について その他 1 設置の経緯 (1) 1. 設置の背景 新たな治験活性化 5 カ年計画の中間見直しに関する検討会 報告の 重点的取組事項 ( アクションプラン ) の進捗 において 今後 取組みをより加速かつ強化すべき課題
サマリー記載について
 第 64 回 HL7 セミナー HL7 標準規格 退院時サマリー のご紹介 退院時サマリー標準規格 開発検討の経緯 平成 30 年 3 月 豊田建日本 HL7 協会 ( 株式会社 HCI) HL7 CDA について HL7 Clinical Document Architecture (CDA) 文書構造を有する診療情報を記述するためのXMLによる言語 2009 年 11 月 ISO 規格 ISO/HL7
第 64 回 HL7 セミナー HL7 標準規格 退院時サマリー のご紹介 退院時サマリー標準規格 開発検討の経緯 平成 30 年 3 月 豊田建日本 HL7 協会 ( 株式会社 HCI) HL7 CDA について HL7 Clinical Document Architecture (CDA) 文書構造を有する診療情報を記述するためのXMLによる言語 2009 年 11 月 ISO 規格 ISO/HL7
一次サンプル採取マニュアル PM 共通 0001 Department of Clinical Laboratory, Kyoto University Hospital その他の検体検査 >> 8C. 遺伝子関連検査受託終了項目 23th May EGFR 遺伝子変異検
 Department of Clinical Laboratory, Kyoto University Hospital 6459 8. その他の検体検査 >> 8C. 遺伝子関連検査受託終了項目 23th May. 2017 EGFR 遺伝子変異検査 ( 院内測定 ) c-erbb/egfr [tissues] 基本情報 8C051 c-erbb/egfr JLAC10 診療報酬 分析物 識別材料測定法
Department of Clinical Laboratory, Kyoto University Hospital 6459 8. その他の検体検査 >> 8C. 遺伝子関連検査受託終了項目 23th May. 2017 EGFR 遺伝子変異検査 ( 院内測定 ) c-erbb/egfr [tissues] 基本情報 8C051 c-erbb/egfr JLAC10 診療報酬 分析物 識別材料測定法
ごあいさつ バイオシミラーの課題 バイオ医薬品は 20 世紀後半に開発されて以来 癌や血液疾患 自己免疫疾患等多くの難治性疾患に卓抜した治療効果を示し また一般にベネフィット リスク評価が高いと言われています しかしその一方で しばしば高額となる薬剤費用が 患者の経済的負担や社会保障費の増大に繋がる
 ごあいさつ バイオシミラーの課題 バイオ医薬品は 20 世紀後半に開発されて以来 癌や血液疾患 自己免疫疾患等多くの難治性疾患に卓抜した治療効果を示し また一般にベネフィット リスク評価が高いと言われています しかしその一方で しばしば高額となる薬剤費用が 患者の経済的負担や社会保障費の増大に繋がると指摘されています こうした中 バイオシミラーの普及は 拡大する医療費の抑制に貢献するとともに 経済的な理由でバイオ医薬品による治療を躊躇されている患者に対する治療アクセスの改善を約束します
ごあいさつ バイオシミラーの課題 バイオ医薬品は 20 世紀後半に開発されて以来 癌や血液疾患 自己免疫疾患等多くの難治性疾患に卓抜した治療効果を示し また一般にベネフィット リスク評価が高いと言われています しかしその一方で しばしば高額となる薬剤費用が 患者の経済的負担や社会保障費の増大に繋がると指摘されています こうした中 バイオシミラーの普及は 拡大する医療費の抑制に貢献するとともに 経済的な理由でバイオ医薬品による治療を躊躇されている患者に対する治療アクセスの改善を約束します
資料2 ゲノム医療をめぐる現状と課題(確定版)
 第 1 回ゲノム医療等実用化推進 TF 平成 27 年 11 月 17 日 資料 2 ゲノム医療等をめぐる現状と課題 ゲノム情報の特性 日本医学会の指摘する 遺伝学的検査 診断を実施する際に考慮すべき遺伝情報の特性 遺伝情報には次のような特性があり 遺伝学的検査およびその結果に基づいてなされる診断を行う際にはこれらの特性を十分考慮する必要がある 生涯変化しないこと 血縁者間で一部共有されていること
第 1 回ゲノム医療等実用化推進 TF 平成 27 年 11 月 17 日 資料 2 ゲノム医療等をめぐる現状と課題 ゲノム情報の特性 日本医学会の指摘する 遺伝学的検査 診断を実施する際に考慮すべき遺伝情報の特性 遺伝情報には次のような特性があり 遺伝学的検査およびその結果に基づいてなされる診断を行う際にはこれらの特性を十分考慮する必要がある 生涯変化しないこと 血縁者間で一部共有されていること
PowerPoint プレゼンテーション
 CDISC を利用した相互運用性について (Interoperability using CDISC) National Center for Global Health and Medicine, Center for Clinical Sciences, Dep. of Data Science Clinical Epidemiology/ JCRAC Data Center 大津洋 ( Hiroshi
CDISC を利用した相互運用性について (Interoperability using CDISC) National Center for Global Health and Medicine, Center for Clinical Sciences, Dep. of Data Science Clinical Epidemiology/ JCRAC Data Center 大津洋 ( Hiroshi
< F2D8E9197BF A836F815B2E6A7464>
 ( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
( 第 1 回検討会の資料 3 の P.16) 治験薬 GMP の概要 治験薬の品質を保証することで 不良な治験薬から被験者を保護する 均一な品質の治験薬を用いることで 治験の信頼性を確保する 治験薬と市販後製品とで同一の品質を保証することで 市販後製品の有効性と安全性を確保する 根拠 医薬品の臨床試験の実施の基準に関する省令(GCP 省令 ) に基づく通知 治験薬の製造管理及び品質管理基準及び治験薬の製造施設の構造設備基準
1. ストーマ外来 の問い合わせ窓口 1 ストーマ外来が設定されている ( はい / ) 上記外来の名称 対象となるストーマの種類 7 ストーマ外来の説明が掲載されているページのと は 手入力せずにホームページからコピーしてください 他施設でがんの診療を受けている または 診療を受けていた患者さんを
 がんの診療に関連した専門外来の問い合わせ窓口 記載の有無 あり とするとデータ抽出の対象となります 記載する内容がない場合は なし としてください なし の場合は以下について記入の必要はありません 病院名 : 公立大学法人横浜市立大学附属病院 平成 9 年 9 月 1 日現在 あり がん診療に関連した専門外来の の項目は 以下の表の疾患名を用いて記載してください 表の中に 該当する病名がない場合は
がんの診療に関連した専門外来の問い合わせ窓口 記載の有無 あり とするとデータ抽出の対象となります 記載する内容がない場合は なし としてください なし の場合は以下について記入の必要はありません 病院名 : 公立大学法人横浜市立大学附属病院 平成 9 年 9 月 1 日現在 あり がん診療に関連した専門外来の の項目は 以下の表の疾患名を用いて記載してください 表の中に 該当する病名がない場合は
CROCO について
 CROCO について CROCO とは コース 正式名称 Clinical Research Online Professional Certification Program at Osaka University といい 大阪大学医学部附属病院が提供する 臨床研究に関する教育の e-learning サイトです 臨床研究を実施する研究者 専門職の方 倫理審査委員会の委員 事務局の方を対象に 臨床研究に必要な情報
CROCO について CROCO とは コース 正式名称 Clinical Research Online Professional Certification Program at Osaka University といい 大阪大学医学部附属病院が提供する 臨床研究に関する教育の e-learning サイトです 臨床研究を実施する研究者 専門職の方 倫理審査委員会の委員 事務局の方を対象に 臨床研究に必要な情報
学位論文の内容の要旨 論文提出者氏名 佐藤雄哉 論文審査担当者 主査田中真二 副査三宅智 明石巧 論文題目 Relationship between expression of IGFBP7 and clinicopathological variables in gastric cancer (
 学位論文の内容の要旨 論文提出者氏名 佐藤雄哉 論文審査担当者 主査田中真二 副査三宅智 明石巧 論文題目 Relationship between expression of IGFBP7 and clinicopathological variables in gastric cancer ( 論文内容の要旨 ) < 要旨 > Insulin-like growth factor ( 以下 IGF)
学位論文の内容の要旨 論文提出者氏名 佐藤雄哉 論文審査担当者 主査田中真二 副査三宅智 明石巧 論文題目 Relationship between expression of IGFBP7 and clinicopathological variables in gastric cancer ( 論文内容の要旨 ) < 要旨 > Insulin-like growth factor ( 以下 IGF)
がん登録実務について
 平成 28 年度東京都がん登録説明会資料 2-1 がん登録届出実務について (1) 1. 届出対象 2. 届出候補見つけ出し 3. 診断日 4. 届出票の作成例示 東京都地域がん登録室 1 1. 届出対象 1 原発部位で届出 2 入院 外来を問わず 当該腫瘍に対して 自施設を初診し 診断あるいは治療の対象 ( 経過観察を含む ) となった腫瘍を届出 3 届出対象となった腫瘍を 1 腫瘍 1 届出の形で届出
平成 28 年度東京都がん登録説明会資料 2-1 がん登録届出実務について (1) 1. 届出対象 2. 届出候補見つけ出し 3. 診断日 4. 届出票の作成例示 東京都地域がん登録室 1 1. 届出対象 1 原発部位で届出 2 入院 外来を問わず 当該腫瘍に対して 自施設を初診し 診断あるいは治療の対象 ( 経過観察を含む ) となった腫瘍を届出 3 届出対象となった腫瘍を 1 腫瘍 1 届出の形で届出
Microsoft Word - H _概要_.doc
 平成 25 年 2 月独立行政法人国立病院機構西新潟中央病院倫理審査委員会 ( 受託研究 ) 議事要旨 開催日時 開催場所 出席委員名は別紙のとおり 治験及び製造販売後臨床試験に関する調査審議事項 審議事項 治験等の実施に関する研究 継続 ME2080 の Dravet 症候群患者を対象とした一般臨床試験 ( 第 Ⅲ 相 ) (Protocol No:STP-1) 被験薬 :ME2080(Stiripentol)
平成 25 年 2 月独立行政法人国立病院機構西新潟中央病院倫理審査委員会 ( 受託研究 ) 議事要旨 開催日時 開催場所 出席委員名は別紙のとおり 治験及び製造販売後臨床試験に関する調査審議事項 審議事項 治験等の実施に関する研究 継続 ME2080 の Dravet 症候群患者を対象とした一般臨床試験 ( 第 Ⅲ 相 ) (Protocol No:STP-1) 被験薬 :ME2080(Stiripentol)
JICA 事業評価ガイドライン ( 第 2 版 ) 独立行政法人国際協力機構 評価部 2014 年 5 月 1
 JICA 事業評価ガイドライン ( 第 2 版 ) 独立行政法人国際協力機構 評価部 2014 年 5 月 1 JICA 事業評価ガイドライン ( 第 2 版 ) ( 事業評価の目的 ) 1. JICA は 主に 1PDCA(Plan; 事前 Do; 実施 Check; 事後 Action; フィードバック ) サイクルを通じた事業のさらなる改善 及び 2 日本国民及び相手国を含むその他ステークホルダーへの説明責任
JICA 事業評価ガイドライン ( 第 2 版 ) 独立行政法人国際協力機構 評価部 2014 年 5 月 1 JICA 事業評価ガイドライン ( 第 2 版 ) ( 事業評価の目的 ) 1. JICA は 主に 1PDCA(Plan; 事前 Do; 実施 Check; 事後 Action; フィードバック ) サイクルを通じた事業のさらなる改善 及び 2 日本国民及び相手国を含むその他ステークホルダーへの説明責任
Microsoft PowerPoint _tech_siryo4.pptx
 資料 4-4 平成 26 年度第 3 回技術委員会資料 次年度アクションアイテム案 2015.03.26 事務局 前回の委員会にて設定されたテーマ 1. オープンデータガイド ( 活 編 ) の作成 2. オープンデータガイド ( 提供編 ) のメンテナンス 3. ツール集の作成 4. 講習会 テキスト作成 5. 国際標準化活動 をつけたテーマについては ワーキンググループを発 させて 作業を う
資料 4-4 平成 26 年度第 3 回技術委員会資料 次年度アクションアイテム案 2015.03.26 事務局 前回の委員会にて設定されたテーマ 1. オープンデータガイド ( 活 編 ) の作成 2. オープンデータガイド ( 提供編 ) のメンテナンス 3. ツール集の作成 4. 講習会 テキスト作成 5. 国際標準化活動 をつけたテーマについては ワーキンググループを発 させて 作業を う
公益社団法人日本医師会治験促進センターの事業は 国立研究開発法人日本医療研究開発機構 (AMED) の委託研究であり本日はその成果の一部を発表します カット ドゥ スクエアが 実現する電磁化と etmf 対応について 電磁化推進シンポジウム医療機関の治験関連文書の電磁化に係る課題解決に向けて < 東
 公益社団法人日本医師会治験促進センターの事業は 国立研究開発法人日本医療研究開発機構 (AMED) の委託研究であり本日はその成果の一部を発表します カット ドゥ スクエアが 実現する電磁化と etmf 対応について 電磁化推進シンポジウム医療機関の治験関連文書の電磁化に係る課題解決に向けて < 東京会場 >2017 年 10 月 25 日 ( 水 ) 日本医師会館 < 福岡会場 >2017 年 11
公益社団法人日本医師会治験促進センターの事業は 国立研究開発法人日本医療研究開発機構 (AMED) の委託研究であり本日はその成果の一部を発表します カット ドゥ スクエアが 実現する電磁化と etmf 対応について 電磁化推進シンポジウム医療機関の治験関連文書の電磁化に係る課題解決に向けて < 東京会場 >2017 年 10 月 25 日 ( 水 ) 日本医師会館 < 福岡会場 >2017 年 11
PowerPoint プレゼンテーション
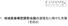 第 1 5 回地域医療構想に関する W G 平成 3 0 年 7 月 2 0 日 資料 2-1 1. 地域医療構想調整会議の活性化に向けた方策 ( その 3) 1 公立 公的病院等を中心とした機能分化 連携の推進について 2 地元に密着した 地域医療構想アドバイザー について 1 経済財政運営と改革の基本方針 2018 ( 平成 30 年 6 月 15 日閣議決定 )[ 抜粋 ] 4. 主要分野ごとの計画の基本方針と重要課題
第 1 5 回地域医療構想に関する W G 平成 3 0 年 7 月 2 0 日 資料 2-1 1. 地域医療構想調整会議の活性化に向けた方策 ( その 3) 1 公立 公的病院等を中心とした機能分化 連携の推進について 2 地元に密着した 地域医療構想アドバイザー について 1 経済財政運営と改革の基本方針 2018 ( 平成 30 年 6 月 15 日閣議決定 )[ 抜粋 ] 4. 主要分野ごとの計画の基本方針と重要課題
過去の医薬品等の健康被害から学ぶもの
 新薬による薬害事件を如何に防ぐか - ソリブジン事件とイレッサ事件から学ぶ - 土井脩 ( 医薬品医療機器レギュラトリーサイエンス財団 ) Pharmaceutical and Medical Device Regulatory Science Society of Japan 2019.01.01 ( レギュラトリーサイエンスエキスパート研修会 薬害教育 ) 研修用教材としてまとめたものであり 公式見解などをまとめたものではありません
新薬による薬害事件を如何に防ぐか - ソリブジン事件とイレッサ事件から学ぶ - 土井脩 ( 医薬品医療機器レギュラトリーサイエンス財団 ) Pharmaceutical and Medical Device Regulatory Science Society of Japan 2019.01.01 ( レギュラトリーサイエンスエキスパート研修会 薬害教育 ) 研修用教材としてまとめたものであり 公式見解などをまとめたものではありません
1. ストーマ外来 の問い合わせ窓口 1 ストーマ外来が設定されている ( / ) 上記外来の名称 ストマ外来 対象となるストーマの種類 コロストーマとウロストーマ 4 大腸がん 腎がん 膀胱がん ストーマ管理 ( 腎ろう, 膀胱ろう含む ) ろう孔管理 (PEG 含む ) 尿失禁の管理 ストーマ外
 がんの診療に関連した専門外来の問い合わせ窓口 記載の有無 あり とするとデータ抽出の対象となります 記載する内容がない場合は なし としてください なし の場合は以下について記入の必要はありません 病院名 : 岐阜大学医学部附属病院 平成 9 年 9 月 1 日現在 あり がん診療に関連した専門外来の の項目は 以下の表の疾患名を用いて記載してください 表の中に 該当する病名がない場合は その病名を直接記載してください
がんの診療に関連した専門外来の問い合わせ窓口 記載の有無 あり とするとデータ抽出の対象となります 記載する内容がない場合は なし としてください なし の場合は以下について記入の必要はありません 病院名 : 岐阜大学医学部附属病院 平成 9 年 9 月 1 日現在 あり がん診療に関連した専門外来の の項目は 以下の表の疾患名を用いて記載してください 表の中に 該当する病名がない場合は その病名を直接記載してください
2018/9/29 ICPM 2018 セッション3 医薬品安全性 国内と海外のデータベースの特徴と医薬品安全性モニタリングへの応用 - 異なる視点からのデータベースの理解 - 医療情報データベースを活用した 医薬品の製造販売後調査について 独立行政法人医薬品医療機器総合機構医療情報活用部疫学課梶山
 2018/9/29 ICPM 2018 セッション3 医薬品安全性 国内と海外のデータベースの特徴と医薬品安全性モニタリングへの応用 - 異なる視点からのデータベースの理解 - 医療情報データベースを活用した 医薬品の製造販売後調査について 独立行政法人医薬品医療機器総合機構医療情報活用部疫学課梶山和浩 2018/9/29 2 Disclosure of Conflict of Interest (COI)
2018/9/29 ICPM 2018 セッション3 医薬品安全性 国内と海外のデータベースの特徴と医薬品安全性モニタリングへの応用 - 異なる視点からのデータベースの理解 - 医療情報データベースを活用した 医薬品の製造販売後調査について 独立行政法人医薬品医療機器総合機構医療情報活用部疫学課梶山和浩 2018/9/29 2 Disclosure of Conflict of Interest (COI)
は関連する学会 専門医制度と連携しており, 今後さらに拡大していきます. 日本外科学会 ( 外科専門医 ) 日本消化器外科学会 ( 消化器外科専門医 ) 消化器外科領域については, 以下の学会が 消化器外科データベース関連学会協議会 を組織して,NCD と連携する : 日本消化器外科学会, 日本肝胆
 資料 1 事業実施計画書 ( 事業実施計画書第 3.2 版平成 30 年 3 月 26 日更新 ) 事業実施計画書 平成 30 年 3 月 26 日 一般社団法人 National Clinical Database 100-0005 東京都千代田区丸の内 1-8-3 丸の内トラストタワー本館 20 階 1. 事業の名称 一般社団法人 National Clinical Database における手術
資料 1 事業実施計画書 ( 事業実施計画書第 3.2 版平成 30 年 3 月 26 日更新 ) 事業実施計画書 平成 30 年 3 月 26 日 一般社団法人 National Clinical Database 100-0005 東京都千代田区丸の内 1-8-3 丸の内トラストタワー本館 20 階 1. 事業の名称 一般社団法人 National Clinical Database における手術
医薬品説明会資料 ジェネリック (後発医薬品)
 17 2 12 13 GMP 14 GVP 2 日医工MPS2010 基本的なジェネリック発売までの流れ 製造販売元A社 管理 開発部門 製造部門 A社 管理 開発 販売部門 A社工場 製造指示 出荷 製造業者 Z 製造委託 承認 製造販売承認の申請 A社 営業部門 医療機関 卸売業者 厚生労働大臣 医薬品医療機器総合機構 9 Z社工場 基本的には 各社で製剤に関する研究 開発を行い 製造に関する申請書の提出
17 2 12 13 GMP 14 GVP 2 日医工MPS2010 基本的なジェネリック発売までの流れ 製造販売元A社 管理 開発部門 製造部門 A社 管理 開発 販売部門 A社工場 製造指示 出荷 製造業者 Z 製造委託 承認 製造販売承認の申請 A社 営業部門 医療機関 卸売業者 厚生労働大臣 医薬品医療機器総合機構 9 Z社工場 基本的には 各社で製剤に関する研究 開発を行い 製造に関する申請書の提出
概要 PMDAにおける次世代審査 相談体制の構築 データ標準の利用 承認申請時の電子データ提出に関する基本的考え方 ( 案 ) について パイロット実施について CDISC 利用に関する今後の検討と展望 2014/05/16 CDISC 概説コース 2
 CDISC 概説コース PMDA の取り組みと 日本における CDISC の利用について 独立行政法人医薬品医療機器総合機構次世代審査等推進室 / スペシャリスト ( 生物統計担当 ) 安藤友紀 CDISC 2012 1 概要 PMDAにおける次世代審査 相談体制の構築 データ標準の利用 承認申請時の電子データ提出に関する基本的考え方 ( 案 ) について パイロット実施について CDISC 利用に関する今後の検討と展望
CDISC 概説コース PMDA の取り組みと 日本における CDISC の利用について 独立行政法人医薬品医療機器総合機構次世代審査等推進室 / スペシャリスト ( 生物統計担当 ) 安藤友紀 CDISC 2012 1 概要 PMDAにおける次世代審査 相談体制の構築 データ標準の利用 承認申請時の電子データ提出に関する基本的考え方 ( 案 ) について パイロット実施について CDISC 利用に関する今後の検討と展望
スライド 1
 CDISC 標準対応で SAS プログラマーが 抱える問題点と解決策 片山雅仁小山卓己山本松雄イーピーエス株式会社 CRO 事業本部 DS センター Problems and solutions that SAS programmers faced with CDISC Standards. Masahito Katayama, Takumi Koyama, Matsuo Yamamoto Data
CDISC 標準対応で SAS プログラマーが 抱える問題点と解決策 片山雅仁小山卓己山本松雄イーピーエス株式会社 CRO 事業本部 DS センター Problems and solutions that SAS programmers faced with CDISC Standards. Masahito Katayama, Takumi Koyama, Matsuo Yamamoto Data
皮的肺生検 ) で遺伝子変異が特定できる可能性がある場合に 血液検査後に 気管支鏡検査 ( または経皮的肺生検 ) を受けたい と回答したのは 130 名 (87.8%) でした 確定診断の検査時にて辛い思いをされた 92 名の方においても 82 名 (89.2%) が再度その辛い思いをした検査を受
 報道関係各位 2016 年 12 月 14 日アストラゼネカ株式会社認定 NPO 法人キャンサーネットジャパン株式会社クリニカル トライアル 非小細胞肺がん患者の 94% が新たな治療の可能性を求め遺伝子検査の受診を希望 ~ 進行 再発非小細胞肺がん患者への組織採取や遺伝子検査に関する意識調査 ~ アストラゼネカ株式会社 ( 本社 : 大阪市北区 代表取締役社長 : デイヴィド フレドリクソン 以下
報道関係各位 2016 年 12 月 14 日アストラゼネカ株式会社認定 NPO 法人キャンサーネットジャパン株式会社クリニカル トライアル 非小細胞肺がん患者の 94% が新たな治療の可能性を求め遺伝子検査の受診を希望 ~ 進行 再発非小細胞肺がん患者への組織採取や遺伝子検査に関する意識調査 ~ アストラゼネカ株式会社 ( 本社 : 大阪市北区 代表取締役社長 : デイヴィド フレドリクソン 以下
13 (参考資料4-5)松下参考人資料(三菱総研)
 参考資料 4-5 第 3 回医療 介護データ等の解析基盤に関する有識者会議資料 2-1 医療 介護データ等の解析における民間シンクタンクの役割と課題 2018 年 6 月 14 日 ヘルスケア ウェルネス事業本部ヘルスケアデータ戦略グループ松下知己 Copyright (C) Mitsubishi Research Institute, Inc. 1. 当社における医療 介護データ等の解析業務の実績について
参考資料 4-5 第 3 回医療 介護データ等の解析基盤に関する有識者会議資料 2-1 医療 介護データ等の解析における民間シンクタンクの役割と課題 2018 年 6 月 14 日 ヘルスケア ウェルネス事業本部ヘルスケアデータ戦略グループ松下知己 Copyright (C) Mitsubishi Research Institute, Inc. 1. 当社における医療 介護データ等の解析業務の実績について
国立がん研究センター東病院臨床開発センター臨床試験支援室 / 早期 探索臨床研究センター支援ユニット佐藤暁洋
 国立がん研究センター東病院臨床開発センター臨床試験支援室 / 早期 探索臨床研究センター支援ユニット佐藤暁洋 TR 臨床研究拠点 ( 厚労省 文科省 ) 橋渡し拠点 早期探索拠点 臨床研究中核拠 点 札幌医大 北大 旭川医大 東北大学 国立がん研究センター ( がん ) 国立循環器病研究センター ( 脳心血管 ) 北海道大学 千葉大学 東京大学大阪大学 ( 脳心血管 ) 名古屋大学 京都大学東京大学
国立がん研究センター東病院臨床開発センター臨床試験支援室 / 早期 探索臨床研究センター支援ユニット佐藤暁洋 TR 臨床研究拠点 ( 厚労省 文科省 ) 橋渡し拠点 早期探索拠点 臨床研究中核拠 点 札幌医大 北大 旭川医大 東北大学 国立がん研究センター ( がん ) 国立循環器病研究センター ( 脳心血管 ) 北海道大学 千葉大学 東京大学大阪大学 ( 脳心血管 ) 名古屋大学 京都大学東京大学
